Солевой диатез — повод для беспокойства или беспроблемное состояние | Здоровая жизнь | Здоровье
Мочесолевой диатез – это преддверие образования песка и камней в почках. Причина его может быть врожденной, вызванной нарушениями обмена веществ, пороками анатомического развития мочевыводящих путей.
Но до сих пор единой теории патогенеза мочекаменной болезни нет. Сама расшифровка слова «диатез» означает «пороговые изменения» – это еще и не болезнь, но в организме уже есть изменения, которые могут повлечь за собой заболевание – при изменениях иммунитета, травмах, переохлаждениях. И тогда может начаться образование камней. Часто люди, имеющие мочесолевой диатез, об этом могут и не подозревать. Интересно, что когда врачи-урологи делают анализ мочи членам своей семьи, часто выясняется, что, например, из шести человек (бабушка, дедушка, двое детей и родители) – у двух человек точно будет диагностировано это состояние.
Больше всего от солевого диатеза страдают женщины вследствие частых воспалительных заболеваний – в основном восходящего характера.
Если в роду, особенно по женской линии, есть стойкая мочекаменная болезнь, если образовывались камни (не обязательно, чтобы они были оперированы), и если при этом женщина за собой неадекватно следит, есть возможность запуска полного каскада биохимических изменений.
Соли не обязательно превращаются в камни. Если нет постоянного хронического воспалительного процесса, нет анатомических особенностей развития мочеполовой системы, если человек пьет достаточное количество воды – значит, благоприятных условий для откладывания камней нет. Например, из десяти больных солевым диатезом, лечение необходимо одному-двум.
Однако при постановке диагноза не нужно вымывать соли большим количеством воды, это может навредить. Если есть какие-то предвестники проблем, тогда рекомендуется диета, исключающая жареное, копченое, соленое. Пища должна быть вареной и пареной – не раздражающей. При правильном водном режиме почки очищаются, хороший эффект имеет арбуз, почечные чаи.
Если есть какие-то предвестники проблем, тогда рекомендуется диета, исключающая жареное, копченое, соленое. Пища должна быть вареной и пареной – не раздражающей. При правильном водном режиме почки очищаются, хороший эффект имеет арбуз, почечные чаи.Врожденное нарушение обмена веществ никуда не исчезает. Но сам по себе мочесолевой диатез большой проблемы для общества не создает. Раз в год обязательно делает УЗИ. Если его настораживает появление солей, он может посидеть на диете, попить почечные травы, поехать в санаторий — на воды.
Считается, что 60-80% мочевых камней – это соединения кальция. Когда соли начинают образовываться в камни, есть смысл узнать, какие это соли: оксалаты, фосфаты, ураты, соединения кальция? Например, фосфаты легко ломаются, быстрее выводятся из организма, но в тоже время они чаще сочетаются с инфекцией. Ураты и оксалаты — шиповатой поверхности, довольно плотные. Кальциевые – самые плотные, но с ними связано меньше инфекций.
Особо беспокоиться по поводу солевого диатеза не стоит. Человеческий организм — «универсальный компьютер»: он чувствует, что от лишнего надо избавляться. И при нормальном водном режиме ненужное вымывается.
Человеческий организм — «универсальный компьютер»: он чувствует, что от лишнего надо избавляться. И при нормальном водном режиме ненужное вымывается.
Но если в анализе мочи определяется высокое содержание солей – человеку надо задуматься, как минимум, о характере питания и водного режима, потому что при кислой или лужной моче будут выпадать соли. Характер питания является важным фактором риска в развитии мочекаменной болезни, в связи с чем немаловажную роль приобретают диетотерапия, адекватное поддержание водного баланса. При уратах предусматривают исключение мясных продуктов, бобовых, кофе, шоколада. При кальций-оксалатных солях ограничивают молоко, сыр, зеленые овощи, клубнику, крепкий чай, какао. При кальций-фосфатных солях не рекомендуют часто есть рыбу и молочные продукты.
Смотрите также:
Природа против заболеваний почек! | Еженедельник АПТЕКА
Весенняя пора — как капризная девушка с изменчивым настроением. В течение дня теплая солнечная погода может быстро смениться холодным ветром и проливным дождем. Соскучившись по легкой одежде, многие из нас ходят по улице в коротких куртках и открытой обуви, что не всегда соответствует погоде и может привести к переохлаждению. А ведь именно этот фактор играет немаловажную роль в развитии патологии почек и мочевого пузыря. Также он способен стать причиной обострения цистита (Коркан И.П., 2011). Какое лекарственное средство выбрать для профилактики и лечения данных заболеваний этой весной?
Соскучившись по легкой одежде, многие из нас ходят по улице в коротких куртках и открытой обуви, что не всегда соответствует погоде и может привести к переохлаждению. А ведь именно этот фактор играет немаловажную роль в развитии патологии почек и мочевого пузыря. Также он способен стать причиной обострения цистита (Коркан И.П., 2011). Какое лекарственное средство выбрать для профилактики и лечения данных заболеваний этой весной?
Для того, чтобы избавить свой бюджет от лишних растрат, стоит обратить внимание на лекарственные средства, предназначенные как для профилактики, так и для лечения патологии мочевыводящих путей. В этом отношении особое внимание привлекает комбинированный препарат на растительной основе — УРОХОЛУМ от Житомирской фармацевтической компании Vishpha Эфирные масла, являющиеся компонентами УРОХОЛУМА, способствуют улучшению кровоснабжения почечного эпителия, фенолкарбоновые кислоты помогают усилить диурез, а флавоноиды обладают спазмолитическим свойством. Противовоспалительное действие препарата обусловлено органическими кислотами (Сохин С.А., Мельник В.В., 2012). УРОХОЛУМ также проявляет антиазотемический эффект, выводит из организма мочевину, мочевую кислоту и хлориды, способствует выведению песка и конкрементов из почек, мочевого и желчного пузырей.
Эфирные масла, являющиеся компонентами УРОХОЛУМА, способствуют улучшению кровоснабжения почечного эпителия, фенолкарбоновые кислоты помогают усилить диурез, а флавоноиды обладают спазмолитическим свойством. Противовоспалительное действие препарата обусловлено органическими кислотами (Сохин С.А., Мельник В.В., 2012). УРОХОЛУМ также проявляет антиазотемический эффект, выводит из организма мочевину, мочевую кислоту и хлориды, способствует выведению песка и конкрементов из почек, мочевого и желчного пузырей.
Применение УРОХОЛУМА будет актуально в составе комплексной терапии острых и хронических заболеваний мочевыводящих путей (цистит, уретрит) и почек (пиелонефрит). Кроме того, УРОХОЛУМ показан при моче- и почечнокаменной болезнях, солевом диатезе, хроническом холецистите, дискинезии желчевыводящих путей. Стоит отметить, что включение фитопрепаратов в схему терапии острых воспалительных заболеваний почек и мочевыводящих путей может повысить эффективность лечения, а также предотвратить хронизацию процесса (Денисенко В. П. и соавт., 2013).
П. и соавт., 2013).
УРОХОЛУМ — сила природы для ваших почек!
Дополнительную информацию об этом препарате можно узнать на сайте http://www.uroholum.com.uа.
Пресс-служба «Еженедельника АПТЕКА»
Цікава інформація для Вас:
Солевой диатез — симптомы, диагностика, лечение заболевания
Геморрагические диатезы – целая группа патологий, различающихся причиной возникновения, течением заболевания и его тяжестью, основным симптомом которых является повышенная кровоточивость. Болезни встречаются как у детей (чаще врожденные), так и у взрослых (обычно приобретенные).
Поставить нозологический диагноз, определить причину заболевания, стадию течения и прогноз, назначить соответствующее лечение способен только врач после тщательного обследования пациента при помощи лабораторных и инструментальных методов.
Геморрагические диатезы
Понятие «геморрагический диатез » не является конкретной нозологической единицей, то есть диагнозом. Это собирательное название геморрагических и тромбогеморрагических заболеваний и синдромов, возникающих при:
Это собирательное название геморрагических и тромбогеморрагических заболеваний и синдромов, возникающих при:
При всех типах геморрагических диатезов наблюдается выраженная склонность к рецидивирующим кровотечениям и кровоизлияниям в окружающие ткани, возникающим как самопроизвольно, то есть без воздействия повреждающего фактора, так и в результате незначительных травм.
Они могут быть основным клиническим проявлением заболевания (гемофилия) и осложнением какой-либо хронически протекающей патологии (апластическая анемия, лейкозы и др.).
- Патогенез геморрагических диатезов связан с повреждающим действием на определенное звено гемостаза.
- Гемостаз — биологическая система, чье функционирование направлено на сохранение циркулирующей в русле крови в жидком состоянии и профилактику и борьбу с возникшим кровотечением.
- Она включает в себя следующие элементы:
| Элемент | Описание |
| Эндотелий | Клетки, выстилающие внутреннюю поверхность кровеносных и лимфатических сосудов, полости сердца |
| Тромбоциты | Кровяные клетки, играющие одну из важнейших ролей в свертывании крови |
| Плазменные факторы свертывания | Специальные белки, содержащиеся в плазме крови и тромбоцитах. Обеспечивают формирование сгустка фибрина, тем самым принимая участие в свертывании крови Обеспечивают формирование сгустка фибрина, тем самым принимая участие в свертывании крови |
Дефицит и нарушение работы любого из факторов свертывания системы крови способны привести к возникновению кровотечений, кровоизлияний и тромбоза – прижизненного формирования сгустков внутри сосудов.
Классификация
Классификация геморрагических диатезов основана на проблемах системы гемостаза. В соответствии с патогенетическим механизмом формирования кровотечений выделяют следующие типы:
| Заболевания | Описание |
| Тромбоцитопатии | Группа заболеваний, связанные с дисфункцией тромбоцитарного звена системы свертывания крови |
| Тробоцитопении | При патологиях этой группы наблюдается снижение числа циркулирующих в крови тромбоцитов по той или иной причине |
| Тромбоцитастении | Заболевания, возникающие в результате «травмы» тромбоцитов вследствие генетического дефекта, иммунных и токсических повреждений |
| Коагулопатии (гемофилии) | Группа наследственных или приобретенных патологий, характеризующихся нарушениями в системе плазменных факторов свертывания. Заболевания возникают из-за недостаточного содержания в крови факторов свертывания, при их слабой активности, при наличии ингибиторов – веществ, замедляющих их деятельность Заболевания возникают из-за недостаточного содержания в крови факторов свертывания, при их слабой активности, при наличии ингибиторов – веществ, замедляющих их деятельность |
| Патологии с высокой фибринолитической активностью | Фибринолиз – важная часть системы гемостаза. Действие этого процесса направлено на растворение тромбов и сгустков крови. Реакция фибринолиза является важнейшим защитным фактором, предотвращающим обтурацию (закупорку) кровеносных сосудов сформированными сгустками фибрина. Другой неотъемлемой функцией процесса является возобновление проходимости после устранения угрозы кровотечения |
| Ангиопатии |
|
| ДВС -синдром (синдром диссеминированного внутрисосудистого свертывания ) | Жизнеугрожающее состояние, возникающее вследствие тотального тромбообразования во всех кровеносных сосудах |
Этиология
К причинам, влияющим на развитие и течение геморрагических диатезов, относят следующие факторы:
К возникновению одной из форм геморрагического диатеза способна привести любая комбинация факторов.
Клиническая картина
В зависимости от типа заболевания, его тяжести и течения, в клинике геморрагического диатеза могут преобладать как анемические (неспецифические), так и геморрагические (специфические) симптомы:
| Симптомы | Описание |
| Неспецифические | Пациенты предъявляют жалобы на: |
| Специфические | Выявляются при проведении дополнительных методов обследования пациента. Визуально лечащий врач может обнаружить наличие множественных кровоизлияний в мягкие ткани различного размера и пр. |
Клиническая картина геморрагических диатезов зависит от вида кровотечений:
| Тип кровоточивости | Описание |
| Гематомный | ГематомаХарактеризуется образованием полостей, заполненных кровью – гематом, а также обильными наружными кровотечениями из поврежденных сосудов кожных покровов и слизистых. Является компонентом гемофилий Является компонентом гемофилий |
| Петехиально-пятнистый (микроциркуляторный) | Наблюдаются поверхностные кровоизлияния в кожных покровах и слизистых оболочках, имеющие вид пятен, не выступающих над поверхностью ткани. Петехии бывают различного размера и цвета, при пальпации безболезненны. Их появление связано с кровоточивостью десен, маточными, носовыми и другими кровотечениями. Этот тип обнаруживается при различных тромбоцитопатиях |
| Петехиально-гематомный (смешанный) |
|
| Васкулитно-пурпурный | Кровоизлияния, сопровождающиеся отложением гемосидерина в толще кожных покрововНад поверхностью кожных покровов и слизистых оболочек выступают небольшие уплотнения пурпурного цвета, являющиеся сгустками свернувшейся крови. При исчезновении кровоизлияний длительное время остаются небольшие бурые пятна – гемосидерин (пигмент, образующийся при распаде гемоглобина). Этот признак является патогномоничным – при других типах его отложений не наблюдается. Возникает при воспалении стенки мелких сосудов микроциркуляторного русла – геморрагическом и идиопатическом васкулитах При исчезновении кровоизлияний длительное время остаются небольшие бурые пятна – гемосидерин (пигмент, образующийся при распаде гемоглобина). Этот признак является патогномоничным – при других типах его отложений не наблюдается. Возникает при воспалении стенки мелких сосудов микроциркуляторного русла – геморрагическом и идиопатическом васкулитах |
| Ангиоматозный | Сосудистая звездочка — телеангиоэктазияНа кожных покровах, слизистых оболочках и многих внутренних органах (особенно легких, печени, почках) возникают патологически деформированные сосуды, принимающие вид пурпурных звездочек или ниточек – телеангиоэктазий. При надавливании пальцем кровоизлияния бледнеют, но вскоре снова приобретают привычную для них окраску. Телеангиоэктазии способны возникать даже при незначительных микротравмах различных участков тела человека и являются причиной кровотечений: носовых, легочных, печеночных, почечных и др. Этот тип свойствен заболеваниям, сопровождающимся патологическими изменениями в кровеносных сосудах невоспалительного характера, что приводит к повышенному повреждению стенки – например, наследственная болезнь Рандю-Ослера |
У новорожденных и детей младшего возраста признаки геморрагического диатеза способны возникнуть даже вследствие незначительной травмы. Ведущими симптомами при этой группе заболеваний являются кровотечения и кровоизлияния.
Ведущими симптомами при этой группе заболеваний являются кровотечения и кровоизлияния.
Диагностика
Для постановки диагноза лечащему врачу необходимо собрать анамнез жизни и заболевания пациента: уточнить, с какого времени он почувствовал ухудшение состояния, с чем связывает возникшее явление, не наблюдались ли подобные признаки у близких родственников. Важным диагностическим моментом будет оценка питания больного. Также проводится анализ данных клинических и лабораторных методов обследования.
Окончательный диагноз может быть вынесен коллегиально – после совещания между специалистами различных областей (врача-инфекциониста, генетика, акушера, педиатра и др.).
Для назначения адекватного лечения и эффективной программы реабилитации необходимо установить патогенез нарушения работы системы гемостаза для каждой конкретной формы заболевания. С этой целью проводится целый ряд клинических и лабораторных методов диагностики:
| Метод | Описание |
| Определение времени кровотечения | Нормальные значения колеблются в районе 2-5 минут, в зависимости от конституциональных (возраст, пол, и др. ) и индивидуальных особенностей. Исследование проводится с целью оценки участия тромбоцитарного звена в процессе свертывания крови. Если кровотечение не останавливается после 5 минут, следует говорить о недостаточности функции тромбоцитов ) и индивидуальных особенностей. Исследование проводится с целью оценки участия тромбоцитарного звена в процессе свертывания крови. Если кровотечение не останавливается после 5 минут, следует говорить о недостаточности функции тромбоцитов |
| Определение протромбинового (ПВ) и тромбопластинового (АЧТВ) времени | Исследование проводится для того, чтобы уточнить характер нарушений плазменных факторов свертывания. Различная комбинация удлинения и укорочения показателей протромбинового (ПВ) и тромбопластинового (АЧТВ) времени позволяют судить об их дефицитах |
| Тест с оценкой растворения сгустков эуглобулина | Этот тест проводится, когда изменений тромбоцитарного и плазматического звеньев системы гемостаза не наблюдается. Отсюда следует, что нарушена работа системы фибринолиза. Нормальное время расщепления сгустка составляет около 2-4 часов, укорочение интервала свидетельствует о нарушении фибринолитической активности как о возможной причине геморрагического синдрома |
| Пробы «жгута» и «щипка» | Пробы проводятся с целью диагностики патологических изменений в стенках кровеносных сосудов. Лечащий врач устанавливает манжету («жгут») на плечо или бедро, затем накачивает ее до максимально допустимых значений, при которых пальпируется пульс на лучевой или артерии тыла стопы. При наличии патологических изменений стенки сосуда на кожных покровах предплечья или голени возникают точечные кровоизлияния. Их образование во время пальцевого сдавления («щипок») кожной складки также является положительным симптомом васкулита Лечащий врач устанавливает манжету («жгут») на плечо или бедро, затем накачивает ее до максимально допустимых значений, при которых пальпируется пульс на лучевой или артерии тыла стопы. При наличии патологических изменений стенки сосуда на кожных покровах предплечья или голени возникают точечные кровоизлияния. Их образование во время пальцевого сдавления («щипок») кожной складки также является положительным симптомом васкулита |
Основы лечения и профилактики
Лечение любой формы геморрагического диатеза – трудная задача как для врача, так и для пациента. Комплексная терапия состоит из следующих этапов:
| Методы | Описание |
| Медикаментозное лечение | Направлено на увеличение концентрации тромбоцитов в кровеносном русле, коррекцию уровня факторов свертывания крови, «укрепление» стенок сосудов посредством витаминотерапии |
| Остановка кровотечения |
|
| Хирургическое вмешательство | |
| Инфузионная терапия | Направлена на замещение объема циркулирующей крови и кровяных клеток. Используется цельная биологическая жидкость, прошедшая тщательный контроль, свежезамороженная плазма, тромбо- и эритромассы Используется цельная биологическая жидкость, прошедшая тщательный контроль, свежезамороженная плазма, тромбо- и эритромассы |
| Физиотерапия | Назначается лечебная физкультура, гимнастика и др. Они необходимы для скорейшего выздоровления и эффективного периода реабилитации |
Для профилактики геморрагических диатезов пациенту следует:
- 1. Проходить плановую диспансеризацию и весь спектр анализов крови.
- 2. При подозрении на наличие одной из форм геморрагического диатеза проводить анализ на наследственную предрасположенность к развитию этой группы патологии.
- 3. Тщательное планировать беременность. Для этих целей были созданы специализированные медико-генетические центры.
- 4. Отказаться от злоупотребления алкоголем, курения табака и психоактивных веществ.
- 5. Придерживаться правильного питания с дозированным содержанием всех необходимых нутриентов, витаминов и микроэлементов.
- 6. Под контролем лечащего врача принимать лекарственные препараты, негативно сказывающиеся на тромбоцитарной функции, например, ацетилсалициловую кислоту (аспирин).

- 7. Избегать пункции глубоких вен, внутримышечных инъекций, длительной иммобилизации.
- 8. Максимально ограничить действие повреждающего фактора, особенно черепно-мозговых травм.
Солевой диатез
Солевым диатезом принято называть конституциональные или приобретенные особенности организма человека, вследствие которых возникает предрасположенность к повышению концентрации в моче органических солей кальция, что со временем может привести к развитию патологии мочевыделительной системы.
Обращаем внимание, что диатез почек — не патологическое состояние и не болезнь, а всего лишь приобретенная или врожденная особенность конституции, которая при неблагоприятном стечении обстоятельств может привести к развитию заболевания почек. На стадии диатеза клиницисты сталкиваются лишь с повышением в моче уровня органических солей (ураты, фосфаты и оксалаты) кальция и появлением в почках эхо-позитивных включений.
Причины и предрасполагающие факторы
Почему происходит повышение уровня солей в моче? Группа причин связана с нарушением транспорта органических веществ и электролитов в почечных канальцах.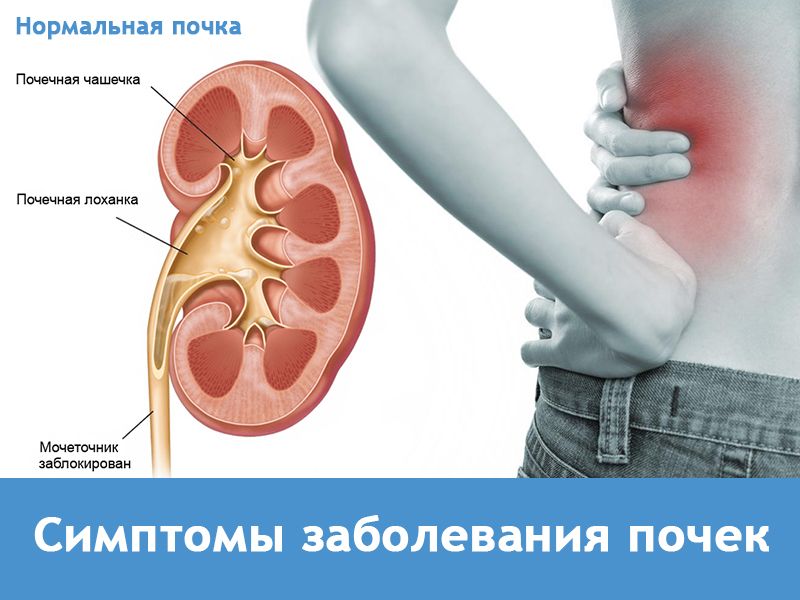 Причиной нарушения транспорта оных может быть генетический дефицит определенного фермента (энзимопатия) в клетках почечных канальцев — в этом случае мы говорим о наследственной тубулопатии, которая вызывает диатез почек.
Причиной нарушения транспорта оных может быть генетический дефицит определенного фермента (энзимопатия) в клетках почечных канальцев — в этом случае мы говорим о наследственной тубулопатии, которая вызывает диатез почек.
Зачастую нарушения транспорта в почках возникают вследствие перенесенных ранее заболеваний почечной паренхимы (гломерулонефрит, пиелонефрит, интерстициальный нефрит). Подобные дефекты составляют группу приобретенных тубулопатий, и именно они чаще всего являются причиной солевого диатеза у взрослых.
Однако, одного лишь наличия врожденной или приобретенной тубулопатии недостаточно для развития диатеза почек.
Для появления клинических и лабораторных признаков необходимо, чтобы на дефекты канальцевого транспорта наслоилось действие определенных внешних факторов.
Наиболее значимыми являются особенности питания и водного режима в сочетании с климатическими условиями, что следует учитывать при определении стратегии лечения солевого диатеза.
Появлению клинико-лабораторных признаков способствует нарушение водного режима, при котором человек регулярно выпивает меньше воды, чем ему необходимо.
Дефицит воды сопровождается уменьшением экскреции жидкости в почках и повышением плотности мочи, а это естественным путем повышает концентрацию солей кальция (уратов, оксалатов) и создает условия для их кристаллизации.
Особенно неблагоприятно сказывается дефицит жидкости на людях, проживающих в жарком климате.
Второй механизм развития солевого диатеза — увеличение поступления органических кислот (и их предшественников) с пищей, и этот момент мы будем учитывать при составлении диеты при солевом диатезе.
Рацион, богатый мясными блюдами и субпродуктами, шоколадом и какао, рыбными консервами и бобовыми способствует усилению пуринового обмена и повышению уровня уратов, а меню, в котором присутствуют овощи, богатые щавелевой кислотой, чревато образованием оксалатов.
Солевой диатез: симптомы и критерии диагностики
Диагноз мы можем поставить на основании данных лабораторного обследования. Повышение в анализе мочи уровня органических кислот (кристаллурия, уратурия) позволяет заподозрить у пациента диатез почек. Подтверждают диагноз данные ультразвукового обследования, в процессе которого в почечных лоханках определяются эхо-позитивные элементы, которые являются кристаллами солей кальция.
Повышение в анализе мочи уровня органических кислот (кристаллурия, уратурия) позволяет заподозрить у пациента диатез почек. Подтверждают диагноз данные ультразвукового обследования, в процессе которого в почечных лоханках определяются эхо-позитивные элементы, которые являются кристаллами солей кальция.
Субъективные симптомы солевого диатеза появляются уже на стадии трансформации данной особенности конституции в патологический процесс. Больной предъявляет жалобы на боли в области поясницы, к которым нередко присоединяются боли внизу живота и рези при мочеиспускании.
Эти жалобы и вынуждают пациента обратиться за медицинской помощью. Появление подобных симптомов солевого диатеза, как правило, сопровождается наличием в почечных лоханках (и в мочевыводящих путях) конкрементов, что говорит о развитии уролитиаза. Спутниками мочекаменной болезни нередко становится пиелонефрит и гидронефроз почек. Возможно присоединение цистита и воспаления мочеточника.
Солевой диатез: лечение
Поскольку мы говорим не о заболевании, а об определенной особенности метаболических процессов, более уместно будет называть комплекс мероприятий, о которых пойдет речь ниже, мерами профилактики и предупреждения развития патологии.
Мы недаром посвятили значительную часть материала причинам диатеза почек. Вдумчивый читатель на основании одного лишь этого раздела может составить план терапии, мы лишь поможем правильно расставить приоритеты.
Генетическая тубулопатия, равно как и приобретенный дефект работы почечных канальцев, коррекции не поддается. Посему, при солевом диатезе диета и водный режим имеют первостепенное значение.
Каждый человек, у которого обнаружены изменения в анализе мочи и включения в почечных лоханках, должен позаботиться о том, чтобы ежедневно выпивать как минимум 2 — 2,5 литра.
В условиях жаркого климата эту цифру нужно увеличивать исходя из актуальных потребностей организма.
Дальнейшие рекомендации зависят от типа солей, которые обнаружены в моче и заставили клинициста поставить диагноз солевой диатез. Диета при наличии оксалатов требует элиминации из рациона продуктов, богатых щавелевой кислотой (ревень, инжир, щавель, томаты, шпинат), а повышение уровня уратов предполагает уменьшение потребления мяса, субпродуктов, а также бобовых, шоколада, кофе и какао.
Следует учесть, что некоторое количество органических солей через гепатобилиарную систему выделяется в просвет кишечника, после чего вновь всасывается в кровь.
Дабы разорвать этот круг, при лечении солевого диатеза назначаются энтеросорбенты, которые абсорбируют токсические компоненты и выводят их из организма. Препаратом выбора признан Энтеросгель, обладающий сорбционными и детоксикационными свойствами.
Энтеросгель избирательно абсорбирует на своей поверхности токсины, также препарат снижает проницаемость стенки кишечника для патогенных агентов.
В схеме лечения солевого диатеза найдется место фитотерапии (назначаются фитопрепараты, обладающие мягким мочегонным действием) и диуретиками, однако, и травяные сборы, и лекарственные препараты с диуретическим эффектом должны приниматься только по назначению врача.
Солевой диатез
Почки – жизненно важный орган, являющийся компонентом мочевыделительной системы, и участвующий во многих процессах жизнедеятельности организма, нарушение которых чревато пагубными последствиями.
Благодаря слаженной работе этого парного органа происходит выведение конечных продуктов распада и ядовитых веществ, обеспечение кислотно-щелочного баланса крови, ее фильтрация, выработка гормонов, полноценный белковый и углеводный обмен.
Особо важной функцией почек является удаление неизрасходованного остатка поступающих в организм солей, излишек которых увеличивает нагрузку на данный орган, нанося существенный урон всему организму.
Скопление избыточной массы солей провоцирует довольно серьезное нарушение – солевой диатез, считающийся первым шагом к мочекаменной болезни и к почечной недостаточности, активное прогрессирование которых грозит организму непоправимыми последствиями.
Солевой диатез представляет собою накопление различных солей и их соединений в почечных лоханках, запускающее процесс поражения почек. Этот недуг способен довольно длительный период протекать без каких-либо проявлений до тех пор, пока прогрессирование патологии не достигнет критической отметки.
Причины
К основным факторам, оказывающим стимулирующее влияние на развитие солевого диатеза, относятся наследственная предрасположенность, заключающаяся в неполноценном функционировании органов мочевыделительной системы, наличие хронических заболеваний, поражающих почки воспалительных процессов.
Солевой диатез может стать результатом допущения погрешностей в рационе питания. Так, чрезмерное увлечение копченостями, соленой, острой и жирной пищей провоцирует огромную нагрузку на мочевиделительную систему, вследствие чего происходит нарушение ее функционирования.
Провоцирующим активизацию солевого диатеза фактором является недостаточное поступление в организм воды, что влечет за собой замедление метаболизма и, как результат, задержку и отложение веществ, которые в норме должны быть расщеплены. Запустить поражение почек может также употребление некачественной воды, содержащей большое количество солей либо наоборот лишенной важных микроэлементов, например, из-за пропускания через фильтр.
Существенную роль в прогрессировании недуга играет дефективное функционирование эндокринной системы, проявляющееся в гормональных нарушениях и неполноценном обмене веществ. Довольно часто патология зарождается на фоне беременности.
Способствует формированию солевого диатеза дефицит в организме витаминов и важных микроэлементов. Кроме того, нарушение работы почек из-за которого развивается солевой диатез может быть вызвано травмами.
Симптомы
Поскольку клинические признаки солевого диатеза проявляются, как правило, когда патологический процесс приобретает уже достаточно агрессивную форму, высока вероятность возникновения симптомов пиелонефрита, мочекаменной болезни, гидронефроза почек, часто сопутствующих протеканию данного заболевания.
Прогрессирование солевого диатеза может сопровождаться жжением и резью после мочеиспускания, возникающим в связи с раздражением слизистой оболочки из-за резкого повышения в моче уровня кислотности.
Также возможно ощущение болей в пояснице, иногда внизу живота. Помимо этого, при солевом диатезе могут наблюдаться частые позывы к мочеиспусканию, темный окрас мочи и наличие в ней кровянистых примесей.
К симптомам, провоцируемым острой формой нарушения процесса выведения жидкости из организма, относятся также проблемы с артериальным давлением, тошнота, отечность, рвотные позывы.
Лечение
Ключевую роль в разработке стратегии терапии солевого диатеза играет особенность клинической картины недуга, сообщает клиника Viva Киев.
После проведения УЗИ-диагностики определяется необходимость хирургического вмешательства, показанием к которому считается обнаружение в почках крупных конкрементов.
Высокоэффективной альтернативой классическому оперативному лечению являются малоинвазивные методы, в частности лазерные технологии, радиоволновая терапия, эндоскопические техники.
На начальных стадиях развития солевого диатеза, когда еще не запущен процесс формирования камней, практикуется применение консервативной методики лечения.
Основой медикаментозной терапии этого недуга является назначение лечебных средств, благотворно влияющих на работу почек, и мочегонных препаратов, способствующих вымыванию солей из мочевыделительной системы.
В дополнение вводятся также противовоспалительные средства нестероидного типа, помогающие снизить раздражение слизистых оболочек, спровоцированное высокой концентрацией солей в моче.
Для устранения сформированных в почках камней небольшого размера практикуют проведение медикаментозного лечения посредством назначения препаратов, действие которых направлено на самостоятельное отхождение или растворение конкремента. После определения причины, вызвавшей активизацию солевого диатеза, применяются меры для восполнения водного баланса в организме и коррекции питания с помощью ограничений в употреблении определенных продуктов.
При необходимости восстановления витаминного запаса в курс терапии включается назначение витаминных комплексов.
Осложнения
Солевой диатез – первая ступень к развитию нефролитиаза, или почечнокаменной болезни.
Запущенная форма патологии может послужить причиной к образованию почечной недостаточности, при прогрессировании которой есть высокий риск нарушений в функционировании всех систем организма.
К осложнениям, возникновение которых достаточно высоковероятно при солевом диатезе, причисляются также разнообразные патологии воспалительного характера, проявляющиеся посредством дисфункции органов мочевыделительной системы.
Дабы не усугубить ситуацию, при проявлении симптомов, указывающих на нарушение функционирования почек, не стоит медлить с обращением к квалифицированному специалисту.
Отсутствие в случае прогрессирования патологии должной медицинской помощи может спровоцировать не только перетекание острой формы недуга в хроническую, но и развитие более опасных заболеваний, которые на запущенных стадиях способны привести к летальному исходу.
Солевой диатез — повод для беспокойства или беспроблемное состояние
Мочесолевой диатез – это преддверие образования песка и камней в почках. Причина его может быть врожденной, вызванной нарушениями обмена веществ, пороками анатомического развития мочевыводящих путей.
Но до сих пор единой теории патогенеза мочекаменной болезни нет. Сама расшифровка слова «диатез» означает «пороговые изменения» – это еще и не болезнь, но в организме уже есть изменения, которые могут повлечь за собой заболевание – при изменениях иммунитета, травмах, переохлаждениях.
И тогда может начаться образование камней. Часто люди, имеющие мочесолевой диатез, об этом могут и не подозревать.
Интересно, что когда врачи-урологи делают анализ мочи членам своей семьи, часто выясняется, что, например, из шести человек (бабушка, дедушка, двое детей и родители) – у двух человек точно будет диагностировано это состояние.
Больше всего от солевого диатеза страдают женщины вследствие частых воспалительных заболеваний – в основном восходящего характера. За счет короткой и широкой уретры у женщин очень часто возникают циститы.
Если лечить заболевание самостоятельно и неправильно, то в итоге инфекция внедрится в подслизистый слой, откуда проникнет в почки.
Там, где есть воспаление, при благоприятных условиях формируется так называемая «матрица» камнеобразования.
Если в роду, особенно по женской линии, есть стойкая мочекаменная болезнь, если образовывались камни (не обязательно, чтобы они были оперированы), и если при этом женщина за собой неадекватно следит, есть возможность запуска полного каскада биохимических изменений.
Соли не обязательно превращаются в камни. Если нет постоянного хронического воспалительного процесса, нет анатомических особенностей развития мочеполовой системы, если человек пьет достаточное количество воды – значит, благоприятных условий для откладывания камней нет. Например, из десяти больных солевым диатезом, лечение необходимо одному-двум.
Однако при постановке диагноза не нужно вымывать соли большим количеством воды, это может навредить. Если есть какие-то предвестники проблем, тогда рекомендуется диета, исключающая жареное, копченое, соленое. Пища должна быть вареной и пареной – не раздражающей. При правильном водном режиме почки очищаются, хороший эффект имеет арбуз, почечные чаи.
Врожденное нарушение обмена веществ никуда не исчезает. Но сам по себе мочесолевой диатез большой проблемы для общества не создает. Раз в год обязательно делает УЗИ. Если его настораживает появление солей, он может посидеть на диете, попить почечные травы, поехать в санаторий — на воды.
Считается, что 60-80% мочевых камней – это соединения кальция.
Когда соли начинают образовываться в камни, есть смысл узнать, какие это соли: оксалаты, фосфаты, ураты, соединения кальция? Например, фосфаты легко ломаются, быстрее выводятся из организма, но в тоже время они чаще сочетаются с инфекцией. Ураты и оксалаты — шиповатой поверхности, довольно плотные. Кальциевые – самые плотные, но с ними связано меньше инфекций.
Особо беспокоиться по поводу солевого диатеза не стоит. Человеческий организм — «универсальный компьютер»: он чувствует, что от лишнего надо избавляться. И при нормальном водном режиме ненужное вымывается.
Но если в анализе мочи определяется высокое содержание солей – человеку надо задуматься, как минимум, о характере питания и водного режима, потому что при кислой или лужной моче будут выпадать соли.
Характер питания является важным фактором риска в развитии мочекаменной болезни, в связи с чем немаловажную роль приобретают диетотерапия, адекватное поддержание водного баланса. При уратах предусматривают исключение мясных продуктов, бобовых, кофе, шоколада.
При кальций-оксалатных солях ограничивают молоко, сыр, зеленые овощи, клубнику, крепкий чай, какао. При кальций-фосфатных солях не рекомендуют часто есть рыбу и молочные продукты.
Симптомы диатеза у детей. Виды диатеза, как его избежать — клиника «Добробут»
Распространенный термин «диатез» – это не диагноз, как многие почему-то считают. Это врожденная аномалия конституции – пограничное состояние, характеризующееся повышенным риском возникновения ряда заболеваний.
Причина диатеза у грудных детей – наследственная предрасположенность организма, проявляющаяся патологической реакцией (гиперреактивностью) на определенные раздражители.
Склонность к диатезу можно считать результатом своеобразного накопления предыдущими поколениями особенностей от воздействия неблагоприятных условий среды.
Механизм появления диатеза связан с особенностями работы иммунной системы (избыточная продукция Ig E) ,нарушениями обмена веществ, повышенной проницаемостью капилляров. При определенных условиях снижается приспосабливаемость организма, изменяется его реактивность, вследствие чего возникает предрасположенность к определенным болезням.
Симптомы диатеза у детей
Симптоматика зависит от возраста малыша. Диатез у ребенка на щеках, сыпь, опрелости в складках кожи, покраснение, боль в животе, плохой аппетит, частый стул – такие симптомы характерны для грудничков.
Реакция может возникнуть при употреблении в пищу коровьего молока, сока или пюре из оранжевых/красных плодов, а в случае исключительно грудного вскармливания – при погрешностях в питании матери.
Поэтому профилактика диатеза у новорожденных заключается в выявлении продуктов, после употребления которых мамой ребенка «обсыпает», и исключении их из рациона матери.
Соблюдение гипоаллергенной диеты женщинами из группы риска по рождению ребенка с аллергической предрасположенностью может снизить вероятность развития диатеза. Чаще всего малыши реагируют на цитрусовые, шоколад, яйца, морепродукты.
Основные симптомы диатеза у детей старше одного года – сыпь и зуд.Такая реакция может быть на следующие продукты:
- цитрусовые;
- клубнику, малину;
- шоколад, какао;
- арахис, мед;
- рыбу;
- крабы, креветки, раки.
У детей с экссудативно-катаральным диатезом уже на первом месяце жизни появляются стойкие опрелости в кожных складках, себорейные корочки на голове, а чуть позже – покраснение кожи щек, эритематозные пятна на разных частях тела, зудящая узелковая сыпь на конечностях, сухость и шелушение кожи, участки мокнутия.
На сгибах рук/ног появляются высыпания, причиняющие нестерпимый зуд. При расчесываниях ребенок может занести инфекцию. Вид «географической карты» приобретает язык, наблюдаются аллергические высыпания по всему телу. Дети могут страдать затяжными конъюнктивитами, отитами, ринитами.
У девочек с экссудативным диатезом может развиться вульвовагинит.
Геморрагический диатез
Для этого расстройства характерна склонность к кровоизлияниям или кровоточивости, что является следствием нарушений свертываемости крови. Отмечают несколько форм состояния: от легкой до крайне тяжелой.
Диагноз «геморрагический диатез» объединяет ряд врожденных и приобретенных патологий, при которых наблюдается склонность к повторным кровотечениям и кровоизлияниям. Как выглядит диатез? У детей, страдающих этим видом диатеза, синяки на теле появляются спонтанно без видимых причин или вследствие легких прикосновений.
При этом количество и размеры кровоподтеков абсолютно не соответствуют повреждениям. Механизм развития такого состояния связан с патологией тромбоцитов, нарушением свертываемости крови или поражением стенок сосудов.
Геморрагический диатез у детей может быть следствием генетических нарушений, например, при гемофилии или болезни фон Виллебранда.
Симптоматика зависит от причины заболевания. При нарушении проницаемости стенок сосудов появляется мелкая сыпь по всему телу, включая слизистые оболочки, может присутствовать кровь в моче. Боль в животе, суставах, отеки также могут свидетельствовать о геморрагическом диатезе.
При нарушении свертываемости крови у детей обычно выявляют анемию. У маленьких пациентов, страдающих геморрагическим диатезом, часто наблюдаются носовые кровотечения, внезапные подкожные кровоизлияния и кровоизлияния в суставную полость.
У девочек в половозрелом возрасте отмечаются меноррагии (менструальные кровопотери, превышающие норму).
Другие виды диатеза
Мочекислый диатез не рассматривают как патологию. Он является одним из вариантов аномалии конституции. Для состояния характерна повышенная интенсивность пуринового обмена, конечный продукт которого – мочевая кислота.
При этом виде диатеза наблюдается склонность к дискинезиям ЖКТ с возникновением ацетонемической рвоты, часто встречаются заболевания сердечно-сосудистой, нервной систем, мочекаменная и желчекаменная болезни, артриты, сахарный диабет.
«Солевой диатез» – диагноз, не имеющий отношения к детям. Патология диагностируется у людей старше 25 лет. При этом заболевании происходит избыточное накопление в почечных лоханках солей, которые периодически выделяются с мочой. Соли способствуют образованию камней в почках и/или мочевом пузыре.
Профилактика и терапия эксудативно-катарального диатеза
Прежде всего, необходимо соблюдать гигиену. Показаны ежедневные ванны с отваром лаврового листа, специальными смягчающими средствами . Ванны оказывают успокаивающее, дезинфицирующее, увлажняющее действие.
Не купайте ребенка слишком долго, не используйте мочалки! Не растирайте мокрую кожу – высушите ее, промокая мягким полотенцем. Желательно использовать дехлорированную воду (можно отстаивать воду в ванне в течение 1-2 часов, а затем нагревать, можно использовать фильтры или смягчители для воды).
В течение 3-5 минут после купания нанесите на кожу смягчающее средство – это позволит сохранить в коже влагу.
Чем лечить диатез на лице у грудничка? Самый простой способ – соблюдение гипоаллергенной диеты кормящей мамой. Исключив аллергены из пищи, по максимуму ограничив синтетические моющие средства, можно обойтись без лекарств. Также следует убрать ковры, проводить ежедневную влажную уборку, выбирать для ребенка только хлопчатобумажную одежду и качественные игрушки.
Медикаментозное лечение диатеза у детей:
- антигистаминные средства оказывают двойное действие: противоаллергическое и седативное, исключение – препараты третьего поколения (эриус в сиропе, ксизал в каплях), которые не вызывают сонливость;
- энтеросорбенты;
- при наличии дисбактериоза назначают пробиотики;
- гормональные мази применяют с осторожностью и только по назначению врача.
Подробнее о видах диатеза и способах лечения читайте на нашем сайте https://www.dobrobut.com/
Связанные услуги: Консультация педиатра
ᐈ Диатез ~ 【Симптомы, лечение, профилактика в Киеве】
???? Диатез: симптомы, лечение
Меню
Диатез – это комплекс симптомов, сигнализирующих о возникновении у пациента нарушений работы организма или предрасположенности к хроническим патологиям. Под термином «диатез» скрываются изменения в регулировании нервных и гормональных процессов, которые и служат причиной патологических реакций. Патологию не следует считать заболеванием, а врачебные мероприятия направлены на избавление от симптомов.
Виды диатеза:
- экссудативно-катаральная форма характеризуется кожными высыпаниями, поражениями слизистых оболочек, нестабильной прибавкой массы тела;
- лимфатико-гипопластическая форма – страдают лимфатические узлы, вследствие чего снижается иммунитет;
- нервно-артритическая форма характеризуется повышенной возбудимостью и кожными высыпаниями;
- желудочно-кишечная форма – объектом поражения становятся органы пищеварения;
- при геморрагической форме часто возникают кровотечения.
К другим видам диатеза относят мочесолевой, солевой, мочевой и мочекаменный диатез.
Причины диатеза:
- наличие хронических аллергических патологий у родителей;
- постоянные стрессовые ситуации;
- хронические заболевания внутренних органов;
- злоупотребление нездоровой пищей с пряностями и большим количеством жира;
- дисбаланс гормонов в организме;
- вредные привычки пациента.
Провоцировать состояние может и нарушение работы коры надпочечников.
До конца объяснить механизм возникновения патологии не удалось. Каждый отдельный случай имеют свою причину и, как следствие, меры борьбы с ним. При диатезе симптомы возникают внезапно, но могут пройти к определенному периоду. Большое значение имеет не только лечение диатеза, но и соблюдение профилактических мероприятий.
- Признаки диатеза отличаются разнообразием в зависимости от формы.
- Классическое проявление – высыпания, постоянно сопровождающие патологию.
- К характерным симптомам диатеза относят:
- процесс шелушения кожи;
- на пораженном участке отмечается зуд и болезненность;
- возникающий конъюнктивит сопровождается слезотечением и чувством жжения глаз;
- эпидермис становится отечным.
Как правило, симптомы проходят после начала лечения или удаления раздражителя. В противном случае возникает хроническая форма заболевания.
Первые симптомы диатеза начинают проявляться в младенческом возрасте. В это время ребенок зависит от грудного кормления, поэтому провоцирующим фактором становятся вещества, попадающие в детский организм с молоком матери.
К причинам диатеза у детей относят:
- неполноценное питание матери в период вынашивания ребенка;
- постоянные инфекционные заболевания в детском возрасте, сопровождающиеся приемом многочисленных препаратов;
- нарушение в структуре питания младенца.
При этом существуют общие симптомы диатеза:
- ребенок быстро утомляется и не может приспособиться к новым условиям жизни;
- возникают трудности в коммуникации с другими детьми;
- инфекционные заболевания происходят чаще, чем у сверстников;
- миндалины увеличены;
- нарушения, связанные с обменом веществ, приводят к минимальной массе тела и небольшому росту;
- появление кожной сыпи по всему телу.
После обследования у педиатра дополнительно потребуется консультация детского врача-дерматолога и аллерголога, которые помогут с назначением комплексного лечения.
При вынашивании ребенка у женщины может возникнуть аллергическая, мочекислая или геморрагическая форма патологии. Заболевание возникает на фоне нарушений свертываемости крови, появления аллергических реакций и действия щавелевой кислоты в организме. Лечение заключается в сбалансированной диете и удалении провоцирующего фактора. Отказ от лечения может привести к передаче патологии ребенку.
Последствия диатеза негативно влияют на организм. Часто возникает экзема или бактериальные поражения кожи. Патология провоцирует развитие аллергического дерматита, бронхиальной астмы, поллиноза. Проявление симптомов дисбактериоза тоже один из элементов диатеза.
Семейный врач или педиатр смогут диагностировать заболевание по ярко выраженным клиническим признакам. Но диагностика диатеза должна сопровождаться выявлением факторов, способствующих возникновению патологии. Поэтому врач проводит беседу для сбора подробного анамнеза.
Диагностика диатеза базируется и на лабораторных методах. Обязательно сдать кровь и мочу на общий и биохимический анализы. Необходимо проведение иммунологического тестирования. Дисбактериоз подтверждается анализом кала.
Дополнительные способы диагностики:
- рентген грудной клетки;
- УЗИ внутренних органов.
Лечение диатеза требует комплексного подхода. Первоочередная задача – ликвидация факторов, провоцирующих диатез. Пациенту требуется специализированная диета. Чтобы кожные симптомы не доставляли проблем, пораженные дерматологические участки обрабатываются мазями.
В лечении диатеза не обойтись без медикаментозной терапии:
- антигистаминные назначения – это основа нивелирования симптомов аллергических реакций;
- абсорбенты эффективно выводят аллергены;
- в случае нарушений работы желудочно-кишечного тракта врач назначает пробиотики;
- иммуномодуляторы.
Исчезновение симптомов зависит от формы заболевания. Чтобы предупредить появление рецидивов, необходимо периодически показываться врачу. Проведение повторных лабораторных методов исследования, соблюдение диеты, отказ от запрещенных продуктов и профилактика диатеза помогут побороть патологию.
К профилактике диатеза относят определенные мероприятия:
- необходимо сбалансировать рацион;
- важным фактором является эмоциональный покой;
- ребенка необходимо как можно раньше приложить к груди;
- при склонности к аллергии в одежде должны преобладать хлопчатобумажные ткани, а стирать нужно детским мылом;
- обязательны гимнастические упражнения, закаливание и массаж.
Основным фактором избавления от патологии является соблюдение диеты. Гипоаллергенная диета при диатезе необходима еще на стадии обострения.
То есть пациент не должен употреблять острые и жирные блюда, а также пряности. Рацион требует ограничения жирной пищи, гороха, фасоли, рыбных продуктов и специй.
Полностью исключить в диете при диатезе нужно морепродукты, шоколад, цитрусовые плоды и яйца.
Важным фактором в борьбе с диатезом остается четкое соблюдение назначений врача. В комплексе можно применять проверенные народные средства. Среди местных препаратов – мазь с пихтовым маслом или облепиха, разбавленная зеленкой. Устраняют симптомы диатеза отвар девясила с горчавкой и ежедневный прием сока черной редьки.
Специалисты клиники МЕДИКОМ обеспечат комплексный подход в лечении диатеза, который включает консультации педиатра, врача-дерматолога, аллерголога и нефролога. Лечение диатеза в Киеве пациентов различного возраста возможно в подразделениях клиники на Оболони и Печерске. Обращайтесь к нам при первых симптомах, чтобы патология не переросла в длительное и мучительное заболевание.
все специалисты
Отличный Сайт. Не первый раз нахожу здесь, ответ на вопросы.
Спасибо за информацию, все методы работают.
Информативная статья, узнала много нового. Спасибо.
Спасибо за действенный совет.
Очень, часто обращаюсь к этому сайту, но сейчас не нашел своих симптомов.
Спасибо за статью очень помогла.
Солевой диатез | Энтеросгель
Солевым диатезом принято называть конституциональные или приобретенные особенности организма человека, вследствие которых возникает предрасположенность к повышению концентрации в моче органических солей кальция, что со временем может привести к развитию патологии мочевыделительной системы.
Обращаем внимание, что диатез почек — не патологическое состояние и не болезнь, а всего лишь приобретенная или врожденная особенность конституции, которая при неблагоприятном стечении обстоятельств может привести к развитию заболевания почек. На стадии диатеза клиницисты сталкиваются лишь с повышением в моче уровня органических солей (ураты, фосфаты и оксалаты) кальция и появлением в почках эхо-позитивных включений.
Причины и предрасполагающие факторы
Почему происходит повышение уровня солей в моче? Группа причин связана с нарушением транспорта органических веществ и электролитов в почечных канальцах. Причиной нарушения транспорта оных может быть генетический дефицит определенного фермента (энзимопатия) в клетках почечных канальцев — в этом случае мы говорим о наследственной тубулопатии, которая вызывает диатез почек.
Зачастую нарушения транспорта в почках возникают вследствие перенесенных ранее заболеваний почечной паренхимы (гломерулонефрит, пиелонефрит, интерстициальный нефрит). Подобные дефекты составляют группу приобретенных тубулопатий, и именно они чаще всего являются причиной солевого диатеза у взрослых.
Однако, одного лишь наличия врожденной или приобретенной тубулопатии недостаточно для развития диатеза почек. Для появления клинических и лабораторных признаков необходимо, чтобы на дефекты канальцевого транспорта наслоилось действие определенных внешних факторов. Наиболее значимыми являются особенности питания и водного режима в сочетании с климатическими условиями, что следует учитывать при определении стратегии лечения солевого диатеза.
Появлению клинико-лабораторных признаков способствует нарушение водного режима, при котором человек регулярно выпивает меньше воды, чем ему необходимо. Дефицит воды сопровождается уменьшением экскреции жидкости в почках и повышением плотности мочи, а это естественным путем повышает концентрацию солей кальция (уратов, оксалатов) и создает условия для их кристаллизации. Особенно неблагоприятно сказывается дефицит жидкости на людях, проживающих в жарком климате.
Второй механизм развития солевого диатеза — увеличение поступления органических кислот (и их предшественников) с пищей, и этот момент мы будем учитывать при составлении диеты при солевом диатезе. Рацион, богатый мясными блюдами и субпродуктами, шоколадом и какао, рыбными консервами и бобовыми способствует усилению пуринового обмена и повышению уровня уратов, а меню, в котором присутствуют овощи, богатые щавелевой кислотой, чревато образованием оксалатов.
Солевой диатез: симптомы и критерии диагностики
Диагноз мы можем поставить на основании данных лабораторного обследования. Повышение в анализе мочи уровня органических кислот (кристаллурия, уратурия) позволяет заподозрить у пациента диатез почек. Подтверждают диагноз данные ультразвукового обследования, в процессе которого в почечных лоханках определяются эхо-позитивные элементы, которые являются кристаллами солей кальция.
Субъективные симптомы солевого диатеза появляются уже на стадии трансформации данной особенности конституции в патологический процесс. Больной предъявляет жалобы на боли в области поясницы, к которым нередко присоединяются боли внизу живота и рези при мочеиспускании.
Эти жалобы и вынуждают пациента обратиться за медицинской помощью. Появление подобных симптомов солевого диатеза, как правило, сопровождается наличием в почечных лоханках (и в мочевыводящих путях) конкрементов, что говорит о развитии уролитиаза. Спутниками мочекаменной болезни нередко становится пиелонефрит и гидронефроз почек. Возможно присоединение цистита и воспаления мочеточника.
Солевой диатез: лечение
Поскольку мы говорим не о заболевании, а об определенной особенности метаболических процессов, более уместно будет называть комплекс мероприятий, о которых пойдет речь ниже, мерами профилактики и предупреждения развития патологии.
Мы недаром посвятили значительную часть материала причинам диатеза почек. Вдумчивый читатель на основании одного лишь этого раздела может составить план терапии, мы лишь поможем правильно расставить приоритеты.
Генетическая тубулопатия, равно как и приобретенный дефект работы почечных канальцев, коррекции не поддается. Посему, при солевом диатезе диета и водный режим имеют первостепенное значение. Каждый человек, у которого обнаружены изменения в анализе мочи и включения в почечных лоханках, должен позаботиться о том, чтобы ежедневно выпивать как минимум 2 — 2,5 литра. В условиях жаркого климата эту цифру нужно увеличивать исходя из актуальных потребностей организма.
Дальнейшие рекомендации зависят от типа солей, которые обнаружены в моче и заставили клинициста поставить диагноз солевой диатез. Диета при наличии оксалатов требует элиминации из рациона продуктов, богатых щавелевой кислотой (ревень, инжир, щавель, томаты, шпинат), а повышение уровня уратов предполагает уменьшение потребления мяса, субпродуктов, а также бобовых, шоколада, кофе и какао.
Следует учесть, что некоторое количество органических солей через гепатобилиарную систему выделяется в просвет кишечника, после чего вновь всасывается в кровь. Дабы разорвать этот круг, при лечении солевого диатеза назначаются энтеросорбенты, которые абсорбируют токсические компоненты и выводят их из организма. Препаратом выбора признан Энтеросгель, обладающий сорбционными и детоксикационными свойствами. Энтеросгель избирательно абсорбирует на своей поверхности токсины, также препарат снижает проницаемость стенки кишечника для патогенных агентов.
В схеме лечения солевого диатеза найдется место фитотерапии (назначаются фитопрепараты, обладающие мягким мочегонным действием) и диуретиками, однако, и травяные сборы, и лекарственные препараты с диуретическим эффектом должны приниматься только по назначению врача.
Солевой диатез почек: причины, симптоматика, лечение заболевания
Почки выполняют несколько важных функций организма, но главная задача – регуляция и вывод жидкости. Редко какой человек внимательно следит за тем, чтобы организм получал жидкость в необходимом объеме. Обычно мы употребляем воду лишь по мере развития жажды. Однако такое отношение к здоровью может привести к серьезным заболеваниям, таким как пиелонефрит и солевой диатез.
Солевой диатез почек
В течении всей жизни почечные лоханки выводят вместе с жидкостью множество солей, фосфатов и их производных соединений. Если функции почек не имеют патологических нарушений, с организма выводятся все вредные шлаки. Но стоит произойти небольшому воспалению, возникает пиелонефрит. Его следствием часто становится солевой диатез.
Принято считать, что вовремя обратившись к урологу, больной пиелонефритом полностью излечивается. В действительности почки после любого воспаления попадают в разряд больных органов, за состоянием которых необходимо следить до конца жизни. Солевой диатез редко появляется как самостоятельное заболевание, чаще он относится к остаточному и хроническому явлению. Заболевание остро проявляется в тот момент, когда в почках появляются ураты, соли мочевой кислоты, оксалаты.
Обострение болезни может спровоцировать возникновение цистита, простатита, уретрита. Иногда симптоматика этих заболеваний может помешать сразу определить первоисточник недомогания. Поэтому диагностика любого заболевания, связанного с почками, должна начинаться с клинической картины анализов. Больной может самостоятельно оценить целесообразность обращения к специалисту по результатам анализа мочи. В норме у здорового человека не должно быть в моче белка, солей или камней. Если же в исследовании указано их присутствие, то это означает наличие воспалительного процесса, так или иначе связанного с почками, в таких случаях обращение к урологу/гинекологу необходимо.
Симптомы мочекислого диатеза и способы его лечения.
Симптомы и признаки пищевой аллергия у грудничков читайте по этому адресу.
Причины солевого диатеза
Заболевание может развиваться на фоне беременности, поскольку в это время на организм идет повышенная нагрузка. Особенно в первые месяцы, когда формируется малыш, организм перестраивается и в итоге может возникнуть проблема с почечной функцией.
Часто причиной заболевания становится стремление пить очищенную воду. Такая вода, по ложному убеждению многих, очищена от вредных примесей. Однако она очищена не только от вредностей, но и от всех полезных элементов. Если такую воду употреблять регулярно, организм быстро приходит в запущенное состояние. Нарушаются обменные процессы, истощается уровень важных ферментов, которые должны поступать с водой. Также важно следить, чтобы организм каждый день получал достаточное количество воды, особенно в жаркую погоду, когда вместе с потом испаряется слишком много влаги. В противном случае возрастает плотность мочи, создавая тем самым идеальные условия для кристаллизации солей и песка. При недостаточном количестве жидкости в почечных лоханках скапливаются шлаки, которые в итоге приводят к быстрому прогрессированию солевого диатеза.
Другой, более частой, причиной становится питание. Вредная еда оставляет в организме множество примесей разрушающего характера. Почки, если они здоровы, активно избавляются от них. Но если злоупотреблять таким питанием, функция почек снижается от чрезмерной перенагрузке. В итоге почки не успевают выводить вредные элементы и они копятся в организме, пока не наступит серьезная интоксикация.
Но почки, как и любой орган, могут иметь патологии врожденного характера. Например, наследственная почечная недостаточность может служить стабильным провокатором солевого диатеза и его последствий. Однако генетическая предрасположенность и врожденность к развитию таких болезней встречается намного реже.
Симптомы солевого диатеза
Заболевание может длительный срок протекать почти незаметно. Больной не чувствует болей, дискомфорта, ложное благополучие приводит к тому, что обращение к врачу происходит несвоевременно. Но со временем появляются боли в пояснице, рези при позывах к моче, может быть температура. Если сразу не принять мер, в моче может появиться кровь. Это уже говорит о том, что в почках есть кристаллизация. Камни, образуясь из кристаллов солей, травмируют стенки мочевого канала, итогом и становится появление крови в моче.
Важно обратиться за помощью до того момента, как появится кровь. Самолечение солевого диатеза исключено, поскольку только специалист может определить степень заболевания, тип солей и причину обострения. Часто первым симптомом становится более общий признак расстройства функции почек: частое мочеиспускание и постоянные позывы. Этот признак появляется обычно намного раньше, чем возникает боль. Первый сигнал того, что нарушены почечные функции. Но может быть и обратная картина: больной почти не ходит в туалет, моча выделяется крайне скудно, низ живота тянет.
Какой бы из признаков не дал о себе знать, необходимо обратиться к урологу/гинекологу.
Инструкция по применению цитрин. Побочные эффекты и противопоказания.
Инструкции по применению средства от аллергии Эриус читайте по этому адресу.
Симптомы и диагностику себорейной экземы узнайте здесь: http://allermed.ru/allergicheskie-zabolevaniya/ekzema/seborejnaya-ekzema.html.
Лечение солевого диатеза
Схема лечения солевого диатеза полностью зависит от клинической картины заболевания. Диагностирование проводиться при помощи УЗИ, результатов исследования анализов крови и мочи. Если в почках уже обнаружены крупные камни, то потребуется хирургическое вмешательство. Операция по дроблению камней проводится в стационере, потом требуется курс восстановительной терапии.
При наличии солей назначаются препараты из группы мочегонных с целью освободить орган от вредоносных отложений. Концентрат мочи быстро выводится, тем самым минимизируя риск образования камней. Кроме того, такая моча, проходя через организм, может спровоцировать воспаления других органов. Поэтому крайне важно избавиться от нее быстрее.
Нужно отметить, что отложения в почках могут быть разного вида, поэтому самолечение может усугубить положение и привести к неизлечимости. Часто попытки вылечиться при помощи советов интернета или знакомых, делают невозможным достижение ремиссии заболевания. Схема лечения, равно как и диета, назначается лечащим специалистом только на основании всех исследований.
Солевой диатез может легко определяться на самых ранних стадиях. Для этого вполне достаточно проходить обследование раз в полгода. Важно понимать, что почки – внутренний орган, ответственный за многие процессы в организме, их невозможно диагностировать только пальпацией или визуально. Если заболевание будет развиваться, оно легко станет хроническим состоянием и будет регулярно провоцировать обострение более сложных болезней.
Солевой диатез у детей симптомы Внутренние заболевания Клиники и врачи
Лечение болезней Озонатор GL-3188 Секреты долголетия Лечебная косметика Шокирующие статьи             Контакты
Болезни по категориям:
Глисты, Гельминты
Урогенитальные инфекции
Кожные болезни
Солевой диатез: лечение и симптомы, солевой диатез у детей
Солевой диатез почек может вызывать жуткие боли!
Что такое Солевой диатез почек? Давайте разберемся.
Солевой диатез почек – это накопление в лоханках почек песка, периодическое выделение с мочой уратов, оксалатов кальция, солей мочевой кислоты, фосфатов, карбонатов а также их сочетаний. Как правили солевому диатезу уже сопутствует воспалительный процесс в почках различной интенсивности в виде хронического пиелонефрита. А при выделении солей с мочой появляются явления острого или хронического цистопиелита, цистита, уретрита, простатита. Более того, наличие песка или эхо-позитивных включений в лоханках почек – это первый шаг к появлению в лоханках почек камней (конкрементов) с развитием мочекаменной болезни. И повышается вероятность смерти от почечной недостаточности. Чтобы избежать столь грозные осложнения солевого диатеза почек необходимо своевременно применить рациональное лечение.
Солевой диатез почек на разных стадиях:
О степени несоответствия возможностей Ваших собственных почек и Вашего индивидуального рациона питания, образа жизни. При этом в лоханках почек определяются включения разнообразной формы и размеров. А в анализе мочи определяются ураты, оксалаты кальция, солей мочевой кислоты, фосфаты, карбонаты и их многочисленные комбинации. И времени, на протяжении которого это несоответствие наблюдается (в лоханках почек пока только песок или уже камни).
Солевой диатез у детей:
Солевой диатез может определяться даже у маленьких детей. Однако чаще всего солевой диатез возникает не от рождения, а на определенном этапе жизни. Т.е. при снижении возможностей почек до определенной величины. И фактически, отражает степень почечной недостаточности. Хотя диагноз «почечная недостаточность» вместе с диагнозом «солевой диатез» и не выставляется.
Солевой диатез — симптомы и причины болезни:
Солевой диатез почек — это состояние, при котором на УЗИ в лоханках почек определяются так называемые эхо-позитивные включения. Учитывая, что у большинства людей признаки солевого диатеза с помощью УЗИ можно выявить примерно с 20-ти лет, на эти результаты исследования не обращают активного внимания. И за такую беспечность многие расплачиваются более существенными заболеваниями. Ранее диагноз «солевой диатез почек» ставился после появления таких симптомов как периодически возникающее частое мочеиспускание, наличие рези внизу живота, по специфическому болевому синдрому, связанному с собственно мочеиспусканием. Сегодня благодаря УЗИ появилась возможность выявлять признаки солевого диатеза до его явных клинических проявлений. Многие считают, что солевой диатез касается лишь патологии почек. И очень ошибаются. Причины образования определяемых с помощью УЗИ включений в лоханках почек разнообразны. Солевой диатез – следствие цепи нарушений в организме. С далеко идущими последствиями.
Солевой диатез — первая причина: Качество употребляемой жидкости. Многие делают упор на употребление преимущественно чистой воды. И совершают грубейшую ошибку! Чтобы вода всосалась из пищеварительной системы в кровь, для обеспечения ее циркуляции по организму и удаления через кожу, органы дыхания и почки необходимо иметь запас витаминов, микроэлементов, белков, источник энергии. Т.к. чистая вода (а тем более – очищенная) всего этого лишена – при регулярном ее употреблении неизменно возникнет дефицит тех самых витаминов, микроэлементов, белков. И соответствующие заболевания. Для обеспечения нормальной циркуляции жидкости по организму лучше употреблять в качестве источника жидкости сок, компот, чай, овощной суп, отвар либо настой из лекарственных растений, собственно овощи и фрукты.
Солевой диатез — вторая причина: Состояние собственно почек. Неспособность почек эффективно выводить все продукты жизнедеятельности имеет значение в появлении солевого диатеза. Но врачебный опыт свидетельствует, что значение важное, но не основное. Значительно чаще солевой диатез почек появляется вследствие действия других причин.
Солевой диатез — третья причина: Количество жидкости, употребляемое ежедневно. Чаще всего солевой диатез появляется на фоне недостаточного употребления жидкости. Суточная потребность в жидкости – от 3 до 5% от массы тела. Или 3-5мл жидкости на каждый килограмм массы тела. Если регулярно употребляемое количество жидкости меньше нормы – концентрирование продуктов жизнедеятельности приводит к их удалению через почки также в концентрированном виде. И способствует выпадению в лоханках почек осадка из концентрированной мочи, что после УЗИ проявляется двумя новыми словами в диагнозе: «солевой диатез».
Солевой диатез — четвертая причина: Это рацион питания человека. Каждый продукт питания оставляет после себя в организме след в виде различных соединений. А почки – это один из основных органов очищения крови и организма в целом. И если определенные продукты поступают в чрезмерных количествах либо неблагоприятных сочетаниях – признаки солевого диатеза неизменно со временем проявятся. Диета при солевом диатезе почек будет зависеть от состава солей, которые выделяются из организма с мочой.
Солевой диатез — пятая причина: Относительный дефицит жидкости из-за ее потерь другими путями – путем испарения через кожу, органы дыхания. При этом не хватает воды для работы почек, и вновь происходит концентрирование продуктов жизнедеятельности в моче, их оседание в виде осадка в лоханках почек. И прогрессирование солевого диатеза.
Солевой диатез — лечение (как лечить солевой диатез):
Первое направление лечения солевого диатеза — это коррекция рациона питания, применение индивидуальной диеты в соответствии с составом выделяющихся с мочой солей. Это самый внешне простой, и вместе с тем самый сложный путь в рациональном лечении солевого диатеза. Т.к. для этого целенаправленные действия должны совершать именно Вы. Причем регулярно.
Второе направление лечения солевого диатеза — от выбора лечебных средств для улучшения способности почек очищать кровь, проводить очищение организма, выводить с мочой разнообразные соли. Здесь во многом определяющим моментом является цена, которую Вы готовы заплатить за те или иные средства.
Эффективная помощь в лечении солевого диатеза и многое другое находится в разделах ниже.
Озонатор GL-3188. Уникальная система обеззараживания продуктов питания, воды, воздуха от грибков, паразитов, плесени. яиц глистов, бактерий и ядохимикатов.
Солевой диатез: лечение, симптомы, признаки, диета
Солевой диатез говорит о генетической предрасположенности к мочекаменной болезни и к заболеваниям суставов.
Соль, видимая при УЗИ исследовании, не является каким-либо нарушением: это вполне нормальное состояние организма.
Солевой диатез почек является накоплением песка в почечных лоханках, когда вместе с мочой выделяются:
Часто этому состоянию сопутствует воспаление почек – хронический пиелонефрит.
При выведении с мочой солей возникает:
Кроме того, наличие эхо-позитивных включений или песок в почечных лоханках является солевым диатезом, говорящем о развитии мочекаменной болезни.
Почечный песок говорит о слабой работе почек.
Солевой диатез у беременных зависит от:
При солевом диатезе у беременных камни еще не успели образоваться, но для их появления уже созданы все предпосылки.
Солевой диатез у детей можно обнаружить на самых ранних этапах жизни ребенка, однако, наиболее часто это заболевание образуется при определенной стадии почечной недостаточности.
Фактически, солевой диатез отражает различные степени почечной недостаточности.
Симптомы солевого диатеза
Если не принять своевременных мер, возникнут осложнения в виде:
Лечение диатеза народными средствами
Некоторые детишки едят все подряд, нюхают цветочки, и у них все в порядке. А другим стоит съесть лишнюю конфетку, так сразу начинается диатез. Почему же так происходит? Дело в том, что многие дети рождаются с расположенностью к аллергии. Это называется атопией. С этой атопией ребенку придется прожить всю жизнь. Когда малыш маленький, атопия проявляется через аллергии, или дерматиты. Атопический дерматит — это и есть диатез.
Диатез может начать появляться у малыша с первых месяцев жизни . Он бывает трех стадий. Первая — младенческая, вторая- детская, и последняя — подростковая или ее еще называют взрослой. Все эти диатезы протекают с паузами. Бывает, что ребенок вырастает, и болезнь проходит сама по себе.
На первых месяцах жизни малыша проявляется младенческий диатез. Он бывает сухой и мокнущий. Симптомы мокнущего диатеза — покраснение кожи, сильный зуд, возвышение, появление пузырьков на коже. Эти пузырьки лопаются, и на коже остаются мокрые участки. Многие участки покрываются корочкой. Появляться диатез может на любых участках тела. Бывает, что из-за открытых ранок в кровь попадает инфекция. Если так случается, то на коже еще появляются гнойнички. Бывает, что сухой и мокнущий диатезы сочетаются вместе. Или же из одного вида младенческого диатеза превращаются в другой.
С двух и примерно до двенадцати лет может протекать подростковая форма диатеза. Эта форма характеризуется повышенной потливостью и покраснением в кожных складках, зудом, сыпью или даже появлением чешуек.
К пятнадцати годам обычно диатез проходит сам. Если же он не прошел, то он перерастает во взрослую стадию, которая также называется нейродермитом. При этом заболевании, кожа в некоторых участках (чаще всего на локтях, промежности, бедрах и так далее) становится сухой и жесткой. Появляются зуд и борозды.
Все лечение должно проходить под строгим наблюдением врача. Купать малыша надо как можно чаще. Только вода должна отстояться перед купанием часа два, это поможет ее дехлорировать. Не желательно использовать мочалку. Все средства гигиены должны быть нейтральны pH (5,5). После того, как малыш принял ванну, не трите его полотенцем, а просто промокните. Натрите ребенка специальным кремом для детей с дерматитом.
При соблюдении рекомендации вы сможете избавить свое чадо от диатеза. Так же для борьбы с диатезом можно использовать народные средства.
Лечение солевого диатеза почек
Заболевание солевой диатез представляет собой накопление в лоханках почек избыточного количества солей, которые временами выделяются вместе с мочой под видом уратов, оксалатов, фосфатов, карбонатов, а также других скоплений.
Кроме этого соли приводят к образованию в почках и мочевом пузыре камней. Поэтому лечение солевого диатеза почек должно быть своевременным и качественным, иначе тяжелых осложнений не избежать.
Лечения солевого диатеза народными средствами
В народной медицине, возможно, найти рецепты от любого недуга, в том числе и от солевого диатеза почек. Чтобы вывести соли и камни из почек и мочевыделительной системы выпивайте несколько раз на протяжении дня сок лимона, разбавленный с одной второй стакана горячей воды.
Параллельно с этим принимайте в таком же количестве соков смеси свекольного, огуречного, морковного по три – четыре раза за день в течение двух дней или недель до полного исчезновения недуга.
Вопрос: нужна помощь. У ребенка 3 мес.очень сильный диатез. Помогите если кто сталкивался с такой проблемой.?
Чем Вы его кормите Если на искуственном вскармливании, может быть смесь не подходит. У моего ребенка был диатез на Тутелли
А чем кормите Если смесью, то может быть стоит сменить смесь. Не кажадая подходит ребенку. Поищите смеси на основе козьего молока — они не вызывают аллергию. А если ребенок на грудном вскармливании, то маме надо следить за своим питанием — не употреблять продукты, вызывающие аллергию — шоколад, цитрусовые, копчености, мед и т.д. Для адекватного лечения обратитесь к аллергологу или дерматологу. Нам назначали капли Зодак и крем Афлодерм. Нам помогло. Сходите к специалисту — не тяните.
У моей знакомой оба ребенка были диатезниками. Ей посоветовали в еду яичную скорлупу подмешивать, мелко-мелко размельченную. Она в кофемолке молола, потому что если ребенок почувствует ее, больше есть уже не будет. Еще через день купала в крепком отваре череды, можно просто обтирать. Мальчишки уже выросли, диатеза у них никогда больше не было.
последите за своим питанием, если кормите грудью, если нет то внимательно следите за питанием ребенка и обязательно сдайте анализы на флору. Вообще сходите к врачу он вам даст направление на все анализы какие нужно сдать. а по результатам даст рекомендации.
Пока сдаете анализы, попробуйте вот что: скорлупа от вареных яиц(лучше домашних), убираете с нее пленочку, толчете в ступке до порошка, берете на кончик ножа, высыпаете в ложечку и капаете туда сок лимона, даете ребенку. Месяц, два, пока не пройдет диатез. Я всем это советую, потому что вылечила так своего сына, когда ему было 8 мес. Тоже долго мучились, пока не увидела рецепт по телевизору.
Перейдите временно на соевое питание, пока диатез не пройдет!!А проблемные места специальным кремом смазывайте.
Начните вести дневник ( есоли ГВ что вы едите) если смесь то что еще даете. так же вопрос атмосферы в квартире( животные, бабушка которая вяжет, дедушка который пилит.) Вопрос косметики которой вы пользуетесь, духи кремы, шампуни. Так же средства уборки, стиральные порошки и прочее, в чем стираете детское белье( детским порошком в машине после того как постирали взрослым порошком папины джинсы.) какую одежду носит ребенок нет ли пуховых кофточек и синтетики. В чем купаете и чем мажете. А дальше алерголог, сдача крови на алергены, сдача микрофлоры, проверка зубов и горла У ВСЕХ взрослых кто общается с ребенком. ( паппа, мама бабушки тетушки. ) я в свое время сказала нет справки нет приходов к нам. здоровье ребенка мне дороже вашей боязни сходить к лору и к стоматологу.
Для начала подумайте и вспомните, что сами ели (если на ГВ). Если в голову ничего не приходит, убирайте из своего рациона большинство продуктов, переходите на минимально аллергенные и потом постепенно добавляйте новые и наблюдайте, не появится ли диатез снова.
да я вам сочувствую у моего ребенка был сильный диатез в 2 месяца. Подавайте ему фенистил, купайте в отваре ромашки или лаврового листа, а еще купите в аптеке мазь синафлана и разводите его с детским кремом и мажте, вот увитеде через несколько часов кожа побереет и не будет так сильно чисаться
Солевой диатез
Почки выполняют несколько важных функций организма, но главная задача — регуляция и вывод жидкости. Редко какой человек внимательно следит за тем, чтобы организм получал жидкость в необходимом объеме. Обычно мы употребляем воду лишь по мере развития жажды. Однако такое отношение к здоровью может привести к серьезным заболеваниям, таким как пиелонефрит и солевой диатез.
Солевой диатез почек
В течении всей жизни почечные лоханки выводят вместе с жидкостью множество солей, фосфатов и их производных соединений. Если функции почек не имеют патологических нарушений, с организма выводятся все вредные шлаки. Но стоит произойти небольшому воспалению, возникает пиелонефрит. Его следствием часто становится солевой диатез.
Принято считать, что вовремя обратившись к урологу, больной пиелонефритом полностью излечивается. В действительности почки после любого воспаления попадают в разряд больных органов, за состоянием которых необходимо следить до конца жизни. Солевой диатез редко появляется как самостоятельное заболевание, чаще он относится к остаточному и хроническому явлению. Заболевание остро проявляется в тот момент, когда в почках появляются ураты, соли мочевой кислоты, оксалаты.
Обострение болезни может спровоцировать возникновение цистита, простатита, уретрита. Иногда симптоматика этих заболеваний может помешать сразу определить первоисточник недомогания. Поэтому диагностика любого заболевания, связанного с почками, должна начинаться с клинической картины анализов. Больной может самостоятельно оценить целесообразность обращения к специалисту по результатам анализа мочи. В норме у здорового человека не должно быть в моче белка, солей или камней. Если же в исследовании указано их присутствие, то это означает наличие воспалительного процесса, так или иначе связанного с почками, в таких случаях обращение к урологу/гинекологу необходимо.
Симптомы и признаки пищевой аллергия у грудничков читайте по этому адресу .
Причины солевого диатеза
Заболевание может развиваться на фоне беременности, поскольку в это время на организм идет повышенная нагрузка. Особенно в первые месяцы, когда формируется малыш, организм перестраивается и в итоге может возникнуть проблема с почечной функцией.
Часто причиной заболевания становится стремление пить очищенную воду. Такая вода, по ложному убеждению многих, очищена от вредных примесей. Однако она очищена не только от вредностей, но и от всех полезных элементов. Если такую воду употреблять регулярно, организм быстро приходит в запущенное состояние. Нарушаются обменные процессы, истощается уровень важных ферментов, которые должны поступать с водой. Также важно следить, чтобы организм каждый день получал достаточное количество воды, особенно в жаркую погоду, когда вместе с потом испаряется слишком много влаги. В противном случае возрастает плотность мочи, создавая тем самым идеальные условия для кристаллизации солей и песка. При недостаточном количестве жидкости в почечных лоханках скапливаются шлаки, которые в итоге приводят к быстрому прогрессированию солевого диатеза.
Другой, более частой, причиной становится питание. Вредная еда оставляет в организме множество примесей разрушающего характера. Почки, если они здоровы, активно избавляются от них. Но если злоупотреблять таким питанием, функция почек снижается от чрезмерной перенагрузке. В итоге почки не успевают выводить вредные элементы и они копятся в организме, пока не наступит серьезная интоксикация.
Но почки, как и любой орган, могут иметь патологии врожденного характера. Например, наследственная почечная недостаточность может служить стабильным провокатором солевого диатеза и его последствий. Однако генетическая предрасположенность и врожденность к развитию таких болезней встречается намного реже.
Симптомы солевого диатеза
Заболевание может длительный срок протекать почти незаметно. Больной не чувствует болей, дискомфорта, ложное благополучие приводит к тому, что обращение к врачу происходит несвоевременно. Но со временем появляются боли в пояснице, рези при позывах к моче, может быть температура. Если сразу не принять мер, в моче может появиться кровь. Это уже говорит о том, что в почках есть кристаллизация. Камни, образуясь из кристаллов солей, травмируют стенки мочевого канала, итогом и становится появление крови в моче.
Важно обратиться за помощью до того момента, как появится кровь. Самолечение солевого диатеза исключено, поскольку только специалист может определить степень заболевания, тип солей и причину обострения. Часто первым симптомом становится более общий признак расстройства функции почек: частое мочеиспускание и постоянные позывы. Этот признак появляется обычно намного раньше, чем возникает боль. Первый сигнал того, что нарушены почечные функции. Но может быть и обратная картина: больной почти не ходит в туалет, моча выделяется крайне скудно, низ живота тянет.
Какой бы из признаков не дал о себе знать, необходимо обратиться к урологу/гинекологу.
Инструкции по применению средства от аллергии Эриус читайте по этому адресу .
Лечение солевого диатеза
Схема лечения солевого диатеза полностью зависит от клинической картины заболевания. Диагностирование проводиться при помощи УЗИ, результатов исследования анализов крови и мочи. Если в почках уже обнаружены крупные камни, то потребуется хирургическое вмешательство. Операция по дроблению камней проводится в стационере, потом требуется курс восстановительной терапии.
Солевой диатез может легко определяться на самых ранних стадиях. Для этого вполне достаточно проходить обследование раз в полгода. Важно понимать, что почки — внутренний орган, ответственный за многие процессы в организме, их невозможно диагностировать только пальпацией или визуально. Если заболевание будет развиваться, оно легко станет хроническим состоянием и будет регулярно провоцировать обострение более сложных болезней.
Источники:
zdorovie.kiev.ua, hvatit-bolet.ru, helpboss.ru, allermed.ru
Следующие статьи:
СОЛЕВОЙ ДИАТЕЗ отражает состояние почек, суставов, других внутренних органов.
Лечение солевого диатеза по методу доктора Скачко
Солевой диатез отражает состояние почек, суставов, других внутренних органов.Врач, фитотерапевт, диетолог Борис Скачко
Что такое солевой диатез? Это состояние, при котором на УЗИ в лоханках почек определяются так называемые эхо-позитивные включения. Учитывая, что у большинства людей признаки солевого диатеза с помощью УЗИ можно выявить примерно с 20-ти лет, на эти результаты исследования не обращают активного внимания. И за такую беспечность многие расплачиваются более существенными заболеваниями.Ранее диагноз «солевой диатез» ставился после появления таких симптомов как периодически возникающее частое мочеиспускание, наличие рези внизу живота, по специфическому болевому синдрому, связанному с собственно мочеиспусканием. Сегодня благодаря УЗИ появилась возможность выявлять признаки солевого диатеза до его явных клинических проявлений.
Многие считают, что солевой диатез касается лишь патологии почек. И очень ошибаются. Причины образования определяемых с помощью УЗИ включений в лоханках почек разнообразны. Солевой диатез – следствие цепи нарушений в организме. С далеко идущими последствиями.
Первая причина. Это рацион питания человека. Каждый продукт питания оставляет после себя в организме след в виде различных соединений. А почки – это один из основных органов очищения крови и организма в целом. И если определенные продукты поступают в чрезмерных количествах либо неблагоприятных сочетаниях – признаки солевого диатеза неизменно со временем проявятся. ДИЕТА ПРИ СОЛЕВОМ ДИАТЕЗЕ будет зависеть от состава солей, которые выделяются из организма с мочой. Т.е. от наличия в моче УРАТОВ, СОЛЕЙ МОЧЕВОЙ КИСЛОТЫ, ОКСАЛАТОВ, ФОСФАТОВ, КАРБОНАТОВ и их КОМБИНАЦИЙ.
Вторая причина. Состояние собственно почек. Неспособность почек эффективно выводить все продукты жизнедеятельности имеет значение в появлении солевого диатеза. Но врачебный опыт свидетельствует, что значение важное, но не основное. Значительно чаще солевой диатез появляется вследствие действия других причин.
Третья причина. Количество жидкости, употребляемое ежедневно. Чаще всего солевой диатез появляется на фоне недостаточного употребления жидкости. Суточная потребность в жидкости – от 3 до 5% от массы тела. Или 3-5мл жидкости на каждый килограмм массы тела. Если регулярно употребляемое количество жидкости меньше нормы – концентрирование продуктов жизнедеятельности приводит к их удалению через почки также в концентрированном виде. И способствует выпадению в лоханках почек осадка из концентрированной мочи, что после УЗИ проявляется двумя новыми словами в диагнозе: «солевой диатез».
Четвертая причина. Качество употребляемой жидкости. Многие делают упор на употребление преимущественно чистой воды. И совершают грубейшую ошибку! Чтобы вода всосалась из пищеварительной системы в кровь, для обеспечения ее циркуляции по организму и удаления через кожу, органы дыхания и почки необходимо иметь запас витаминов, микроэлементов, белков, источник энергии. Т.к. чистая вода (а тем более – очищенная) всего этого лишена – при регулярном ее употреблении неизменно возникнет дефицит тех самых витаминов, микроэлементов, белков. И соответствующие заболевания. Для обеспечения нормальной циркуляции жидкости по организму лучше употреблять в качестве источника жидкости сок, компот, чай, овощной суп, отвар либо настой из лекарственных растений, собственно овощи и фрукты.
Пятая причина. Относительный дефицит жидкости из-за ее потерь другими путями – путем испарения через кожу, органы дыхания. При этом не хватает воды для работы почек, и вновь происходит концентрирование продуктов жизнедеятельности в моче, их оседание в виде осадка в лоханках почек. И прогрессирование солевого диатеза.
В каких еще органах можно найти отражение солевого диатеза. Продукты жизнедеятельности, которые не получилось удалить из организма через почки, накапливаются в околосуставных тканях с появлением не только специфического артрита, но и артроза. Также такое состояние приводит к гормональным нарушениям и отражается на состоянии щитовидной железы, молочных желез (мастопатия), матки (эрозия шейки матки, фибромиома). А выделение из организма концентрированной мочи часто служит раздражителем для простаты и обострением не только цистита, уретрита, но и простатита. А на фоне гормональных нарушений появляется призрак аденомы простаты.Как ведут борьбу с солевым диатезом? Чаще всего стремятся устранить не причины, а следствие. И дают мочегонные пусть и растительного происхождения. Что как минимум обостряет хронический цистопиелит, цистит, уретрит, простатит. Как максимум — постепенно истощает возможности почек.
Крепкого Вам здоровья. И разумного к нему отношения.
Доктор Скачко, натуропат, фитотерапевт, реабилитолог, диетолог, автор 22 опубликованных книг и брошюр, более 40 научных, более 400 популярных статей по темам: фитотерапия, валеология, правильное, здоровое питание, здоровый образ жизни.
Другие статьи на тему «СОЛЕВОЙ ДИАТЕЗ»:
«Формула здоровья доктора Скачко №8» — проверенный временем и в клинических условиях рецепт народной медицины. Он позволяет активировать кровообращение в почках, чем и обеспечивает очищение крови от разнообразных солей (ураты, оксалаты, соли мочевой кислоты, фосфаты, карбонаты и их сочетаний), других продуктов жизнедеятельности. Благодаря этому способствует не только уменьшению симптомов солевого диатеза, но и предупреждает развитие воспалительного процесса в почках (хронический пиелонефрит, цистопиелит), уменьшает степень выраженности и отдаляет проявления почечной недостаточности. Благодаря рациональному сочетанию лекарственных растений позволяет проводить эффективное лечение разнообразных нарушений работы почек. Формула №8 — №1 в лечении почек. Попробуйте и убедитесь сами!
Статьи доктора Бориса Скачко на сайте:
Запись на индивидуальную консультацию по тел.:
+38-094-927-89-20
+38-067-992-40-62
+38-044-383-19-20
Гиперурикозурия и подагрический диатез: основы практики, патофизиология, этиология
Автор
Биджан Шекарриз, доктор медицины Директор отделения лапароскопии и минимально инвазивной хирургии, доцент урологии, кафедра урологии, Медицинский университет штата Нью-Йорк, Государственный университет штата Нью-Йорк
Биджан Шекарриз, доктор медицины, является членом следующих медицинских обществ: Американской ассоциации урологов , Endourological Society
Раскрытие информации: не подлежит разглашению.
Соавтор (ы)
Маршалл Столлер, доктор медицины Профессор и заместитель председателя, медицинский директор Центра мочевых камней, отделение урологии, Калифорнийский университет, Сан-Франциско, медицинский факультет
Маршалл Столлер, доктор медицины, является членом следующих медицинских обществ: Американская урологическая ассоциация
Раскрытие информации: нечего раскрывать.
Брайан Эйснер, доктор медицины Инструктор по хирургии, отделение урологии, Массачусетская больница общего профиля — Гарвардская медицинская школа; Научный сотрудник по эндоурологии, отделение урологии, Калифорнийский университет
Брайан Эйснер, доктор медицинских наук, является членом следующих медицинских обществ: Американская урологическая ассоциация, Эндоурологическое общество
Раскрытие информации: не подлежит разглашению.
Специальная редакционная коллегия
Франсиско Талавера, фармацевт, доктор философии Адъюнкт-профессор, Фармацевтический колледж Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие информации: Получил зарплату от Medscape за работу. для: Medscape.
Главный редактор
Брэдли Филдс Шварц, DO, FACS Профессор урологии, директор Центра лапароскопии и эндоурологии, Департамент хирургии, Медицинский факультет Университета Южного Иллинойса
Брэдли Филдс Шварц, DO, FACS является членом следующих медицинских обществ: Американский колледж хирургов, Американская урологическая ассоциация, Ассоциация военных остеопатических врачей и хирургов, Эндоурологическое общество, Общество лапароэндоскопических хирургов, Общество университетских урологов
Раскрытие информации: Служить (d) в качестве директора, офицера, партнера, сотрудника, советника, консультанта или попечитель: Совет директоров Общества эндоурологов; Избранный президент Северо-Центральная секция Американской ассоциации урологов
Служить (d) в качестве докладчика или члена бюро докладчиков для: Cook Medical.
Дополнительные участники
Аллен Дональд Сефтел, доктор медицины Профессор урологии Университета медицины и стоматологии Нью-Джерси — Медицинская школа Роберта Вуда Джонсона; Заведующий отделением урологии, директор Урологической ординатуры, Университетская больница Купера
Аллен Дональд Сефтел, доктор медицины, является членом следующих медицинских обществ: Американская урологическая ассоциация
Раскрытие информации: Получил гонорар от lilly за консультацию; Получен гонорар от компании abbott за консультацию; Получено консультационное вознаграждение от вспомогательного учреждения за консультацию; Получено консультационное вознаграждение от агента за консультацию; Получал гонорары от урологического журнала за членство в совете директоров; Получил гонорар от эндо за консультацию.
Солевой диатез почек, что это такое, симптомы и лечение
Солевой диатез почек — патологический процесс, сопровождающийся накоплением различных солей в почечной лоханке. В почках могут накапливаться и выводиться с мочой: оксалаты, фосфаты, ураты, карбонаты, соли мочевой кислоты.
В основе патогенеза этого заболевания лежат следующие механизмы:
- Нарушение процессов клубочковой и канальцевой фильтрации.
- Снижение всасывания веществ и выведение продуктов распада.
- Нарушение регуляции обмена веществ на уровне нервной системы.
Причины патологии
Чаще всего заболевание развивается на фоне уже имеющегося воспалительного процесса в почках. Это может быть пиелонефрит, гломерулонефрит и др. Иногда солевой диатез, наоборот, становится причиной пиелонефрита.
Это связано с тем, что повышенное содержание солей в моче отрицательно влияет на слизистую оболочку мочевого пузыря — она изъязвляет и разрушает ее локально.В результате в мочевом пузыре образуются очаги воспаления, к которым может присоединиться инфекция и пойти восходящим путем к почкам.
Однако, помимо острого или хронического воспаления, можно выделить ряд причин, вызывающих накопление солей.
К ним относятся:
- Беременность — увеличивается нагрузка на почки, которые не справляются со своими функциями.
- Получение только очищенной воды, лишенной не только вредных, но и полезных микро- и макроэлементов.
- Недостаточное потребление жидкости — приводит к увеличению вязкости мочи и способствует более интенсивной кристаллизации и осаждению солей.
- Частое употребление «нездоровой» пищи, при переработке которой в организм попадает много консервантов, красителей и генно-модифицированных компонентов. В результате организм может перестать справляться с переработкой такой пищи, а вредные продукты обмена будут откладываться в почках, вызывая интоксикацию.
- Генетически обусловленная почечная недостаточность.Редкая, но все же частая причина.
Помимо основных причин, вызывающих данный патологический процесс, существует ряд факторов, способствующих его возникновению. К ним относятся: врожденные пороки развития почек, регулярное использование фильтра для воды, постоянное употребление минеральной воды, гипо- или авитаминоз.
Клиническая картина
Солевой диатез почек длительное время протекает бессимптомно, и больной даже не подозревает, что у него проблемы со здоровьем.Заболевание начинает проявляться тогда, когда количество солей, накопленных в тазу, оказывается достаточным, чтобы нарушить работу органа.
Клиническая картина прогрессирующего заболевания основана на таких признаках как:
- Болезненные ощущения в поясничной области разной степени выраженности: боли могут быть тупыми, ноющими по своему характеру, реже — острыми, колющими. Боль может распространяться в правую и левую сторону, а также в задний проход. Некоторые пациенты жалуются на болезненные тянущие ощущения внизу живота — в области проекции мочевого пузыря.
- Режущие боли при мочеиспускании и позывы к мочеиспусканию.
- Частые позывы к мочеиспусканию.
- Гематурия — это появление крови в моче.
- Иногда олигурия или анурия — это небольшое выделение с мочой, в запущенных случаях моча практически не выводится.
- Падение артериального давления. На начальных этапах отмечается появление артериальной гипертензии с последующим падением давления.
- Диспептические симптомы: тошнота, вздутие живота, иногда рвота.
- Повышение температуры тела, свидетельствующее об активном воспалительном процессе.При сильном воспалении температура тела может достигать 40 и более градусов, прогрессирует интоксикация.
Алгоритм диагностики
Диагностический поиск проблемы включает такие исследования, как:
- Общий анализ мочи.
- Тест с тремя стеклами.
- Оценка суточного сбора мочи.
- Общий анализ крови.
- УЗИ брюшной полости, малого таза и забрюшинного пространства.
- Рентгенологическое исследование органов малого таза.
- При необходимости КТ или МРТ.
Приведенные выше методы инструментального исследования позволяют точно оценить площадь локализации, размер и форму камней.
Лечение солевого диатеза
В первую очередь лечебное воздействие на солевой диатез — это диета, специально подобранная для каждого пациента. Диета составляется в зависимости от того, какие соли содержатся в моче пациента, но для всех них существует одно общее правило — избегать употребления продуктов, богатых фосфором, калием и кальцием.Питьевой режим также должен быть достаточно интенсивным.
Человек с этим заболеванием должен выпивать не менее 2 литров жидкости (а именно воды) в день.
Схема лечения подбирается строго индивидуально для каждого пациента. Если количество соли и песка незначительно и по результатам УЗИ нет крупных камней в почках, проводится консервативное лечение.
При обнаружении достаточно крупных камней и камней с острыми или неровными краями встает вопрос об их хирургическом удалении.
Консервативное лечение почечного солевого диатеза основано на применении таких групп лекарственных средств, как:
- Антибиотики широкого спектра действия после выявления микроорганизма, вызвавшего первичное воспаление. Чаще всего используются: Амоксициллин, Цефалоспорин, Кларитромицин.
- Спазмолитики: Дротаверин, Спазмалгон.
- Нестероидные противовоспалительные средства: Кеторол, Нимесулид, Ибупрофен.
- диуретики, действие которых направлено на скорейшее выведение солей из почек: Спиронолактон, Фуросемид, Тригрим.
- Уросептики: Канефрон, Цистон.
Если диатез перерос в полноценный мочекаменную болезнь, показано хирургическое лечение. Мелкие камни удаляются дистанционной литотрипсией — они дробятся электромагнитными волнами. А более крупные удаляются хирургическим путем.
Профилактика
Основой профилактики почечного солевого диатеза является лечение хронических заболеваний мочевыделительной системы, сбалансированное сбалансированное питание и соблюдение питьевого режима.
Detonic — уникальное лекарство, помогающее бороться с гипертонией на всех этапах ее развития.
Комплексное действие растительных компонентов препарата Детоник на стенки сосудов и вегетативную нервную систему способствует быстрому снижению артериального давления. Кроме того, этот препарат предотвращает развитие атеросклероза благодаря уникальным компонентам, которые участвуют в синтезе лецитина — аминокислоты, регулирующей метаболизм холестерина и предотвращающей образование атеросклеротических бляшек.
Детоник не вызывает привыкания и абстинентного синдрома, так как все компоненты продукта натуральные.
Подробная информация о Detonic находится на странице производителя www.detonicnd.com.
Чрескожная нефростомия — обзор
ЧРЕЗМЕРНАЯ НЕФРОСТОМИЯ
Чрескожная нефростомия (ПКН) — это процедура, которая устанавливает связь между кожей и почечной собирательной системой. Годвин и его коллеги были первыми, кто описал эту процедуру в 1955 году. 24 С тех пор PCN вытеснила хирургическое вмешательство в качестве основной процедуры временного дренирования закупоренной собирательной системы. Он обеспечивает дренаж под низким давлением из верхних отделов мочевыводящей системы, что позволяет лечить уросепсис и улучшать функцию почек перед окончательной терапией основного обструктивного состояния.
PCN — это фундаментальный метод доступа к мочевыводящим путям. 25, 26 Это может быть окончательная процедура или первый шаг перед более сложными процедурами.Наиболее частым показанием является быстрое облегчение гидронефротической собирательной системы из-за обструкции лоханочно-мочеточникового перехода (рис. 69-7), обструкции верхнечелюстного сустава с единственной функционирующей почкой, обструкции уретеровезикального перехода (UVJ), обструкции после пиелопластики, обструкции после литотрипсии задние уретральные клапаны (PUV), первичный блокирующий мегауретер или внешнее сжатие мочеточников (например, солидные опухоли, лимфома). 27 К другим важным показаниям относятся следующие:
- •
Дренирование инфицированной собирательной системы (пионефроз), снижающее риск сепсиса.
- •
PCN также выполняется для отвода мочи из почечной собирающей системы с целью заживления дистальных свищей, урином или утечек (рис. 69-8).
- •
Для отведения мочи при геморрагическом цистите.
- •
Для создания чрескожного тракта для дальнейшего вмешательства в почку и собирательную систему (нефролитотомия, антеградная установка стента мочеточника, дилатация мочеточника, извлечение инородных тел, эндопиелотомия при обструкции верхнечелюстного сустава, уротелиальная кистевая биопсия).
- •
Для введения лекарств (например, противогрибковых, антибактериальных, противоопухолевых) непосредственно в собирательную систему, снижая системные эффекты лекарств.
- •
Для оценки потенциала восстановления при хронической обструкции почки (значительное увеличение почечного плазменного потока в течение 10 дней после декомпрессии пораженной почки является надежным предиктором восстановления функции почек). 28
Единственными противопоказаниями являются неизлечимый кровоточащий диатез, недостаточность свертываемости крови и неблагоприятная анатомия.Однако, если коагулопатия вызвана уросепсисом, может потребоваться дренаж мочи до того, как будет исправлено нарушение кровотечения. Тяжелые электролитные изменения (гиперкалиемия, метаболический ацидоз) также являются относительным противопоказанием и должны лечиться до ПЯН и могут даже потребовать срочного гемодиализа.
Размещение нефростомии в расширенных коллекторах имеет высокий уровень успеха, от 98% до 100%. 29–38 Показатели успешности в недилатированных системах сбора немного ниже, в диапазоне от 85% до 90%. 39 Пациенты с расширенными собирательными системами, осложненными уросепсисом или азотемией, имеют почти немедленную реакцию после дренирования PCN. Боль и жар обычно проходят через 24–48 часов. 40 Кроме того, после дренирования смертность от грамотрицательной септицемии у пациентов с обструкцией мочевыводящих путей снижается в пять раз. 41 Пациенты с надвигающейся почечной недостаточностью могут вернуться к нормальной или почти нормальной функции почек в среднем в течение недели после дренирования. 42
Предварительная оценка включает в себя клинический анамнез для выявления потенциальной тенденции к кровотечению, общий анализ крови, количество тромбоцитов, ЧТВ и МНО для оценки риска кровотечения. 43–45 Использование рутинных анализов крови противоречиво, и некоторые авторы считают, что для выполнения процедуры достаточно тщательного анамнеза нарушений свертываемости крови, почечной недостаточности, заболеваний печени и использования антитромбоцитарных препаратов и антикоагулянтов. 32 В нашей практике мы регулярно используем лабораторные анализы крови для оценки риска кровотечения. Принятые значения включают МНО <1,3, нормальное ЧТВ для возраста и минимальное количество тромбоцитов> 50,000 × 10 9 / л в экстренных ситуациях. 46
Аномальные параметры свертывания крови могут потребовать коррекции свежезамороженной плазмой, витамином К или тромбоцитами. Если пациент находится на инфузии гепарина, рекомендуется прекратить прием как минимум на 2 часа. Если пациент принимает низкомолекулярный гепарин, необходимо отменить его на 12 часов. Если пациент принимает аспирин или другие препараты, влияющие на функцию тромбоцитов (нестероидные противовоспалительные средства, бета-лактамные антибиотики), а PCN является плановым, процедура откладывается на 5-7 дней.
Анализируются мочевина, креатинин, результаты анализа мочи, посев мочи и чувствительность, а также любые предыдущие визуальные исследования [сонография, КТ, магнитно-резонансная томография (МРТ), ядерная медицина]. У детей со сложной аномальной анатомией (сколиоз, врожденный порок развития) и в ситуациях плохой визуализации почки перед PCN рекомендуется делать снимки поперечного сечения, чтобы определить связь почки с толстой кишкой, тонкой кишкой, селезенкой, печенью, желчным пузырем и т. Д. и плевра.
Антибиотикопрофилактика проводится всем пациентам. Общие патогенные микроорганизмы в моче включают E. coli, Proteus, Klebsiella и энтерококк. Поэтому антибиотик широкого спектра действия вводится менее чем за 2 часа до процедуры. Выбор времени приема очень важен, потому что риск инфекционных осложнений увеличивается в пять раз, если антибиотики вводятся более чем за 3 часа до процедуры. 47 Некоторые авторы предлагают продолжать прием антибиотиков в течение 24-48 часов у пациентов с низким риском развития сепсиса и в течение 48-72 часов в группах высокого риска (диабетики, струвитные камни, непроходимость мочевыводящих путей, инструменты для мочевыводящих путей, постоянное лечение). катетеры). 45 Пациентам с высоким риском сердечных заболеваний требуется специальная профилактика эндокардита.
В нашей практике большинство процедур нефростомии проводится под общим наркозом. Тем не менее, в других центрах для успешного выполнения нефростомии применяли седативные препараты и местную анестезию. 26, 27, 48 Пациента помещают в положение лежа или наклонно-наклонное положение с подъемом ипсилатеральной стороны на 20–30 градусов, а место доступа отображается с помощью сонографии.Заднебоковой доступ (игла под углом от 30 до 45 градусов по отношению к поверхности стола) предпочтительнее, чтобы избежать жизненно важных структур, таких как толстая кишка, печень или селезенка. 25 Кожа стерильно обработана и обработана драпировкой.
В подкожные ткани вводят местный анестетик, чтобы минимизировать дискомфорт после процедуры, и делают небольшой разрез кожи (5 мм) для облегчения доступа. Плоскость наименьшей васкуляризации по Броделю (разделение почечной артерии на большую переднюю и заднюю ветви на стыке передних 2/3 и задней 1/3 осевого изображения почки) определяется с помощью цветной допплерографии и в режиме реального времени. под сонографическим контролем чашечку прокалывают через почечную паренхиму.Следует избегать прямой пункции почечной лоханки или инфундибулума, чтобы свести к минимуму вероятность повреждения междолевых и основных почечных сосудов. 49 Это также снижает вероятность утечки мочи или потери доступа из-за отсутствия поддерживающей паренхимы. 4, 26
В качестве альтернативы, только рентгеноскопическое наблюдение или КТ и рентгеноскопия могут использоваться в качестве методов визуализации, когда присутствует рентгеноконтрастный камень чашечки или когда тазово-лоханочная система затемняется контрастом (внутривенные или ретроградные инъекции) .Следует соблюдать осторожность в отношении радиационного облучения и контрастной нефропатии, особенно у детей, при использовании КТ и рентгеноскопии.
Доступ осуществляется с помощью иглы малого калибра (обычно зажигалки Chiba Hi-lighter 22-го калибра). В недилатированных системах может быть полезным использование внутривенного болюса жидкости или мочегонных средств 50 для расширения собирательной системы и облегчения почечного доступа. Стилет иглы удаляется, и небольшой образец мочи отправляется на посев и определение чувствительности.Следует проявлять осторожность, чтобы полностью не распаковать собирающую систему, поскольку почечный доступ может быть случайно потерян. Затем вводится минимальное количество контраста, чтобы подтвердить положение иглы в почечной лоханке. Затем 0,018-дюймовую проволоку из нержавеющей стали Mandril или нитиноловую проволоку продвигают под рентгеноскопическим контролем в мочеточник или оставляют свернутой в почечной лоханке. 26 Затем используется набор Neff или система введения Accustick для увеличения размера тракта, и проводник 0,035 или 0,038 дюйма (Benston, Amplatz, superstiff Amplatz, Glidewire) помещается в мочеточник или почечную лоханку.
В качестве альтернативы, начальный доступ осуществляется непосредственно с помощью иглы BSDN 19 размера или ангиокатетера 16 размера, а проводник 0,035 дюйма (Benston, Amplatz, Glidewire) продвигается в почечную лоханку. Этот подход имеет преимущество в том, что сводит к минимуму количество манипуляций на трактах, что снижает риск потери почечного доступа или образования перинефрических урином. Основным недостатком является то, что требуется более крупная игла для доступа, что увеличивает риск кровотечений. Корал и его коллеги 27 защищают эту технику у новорожденных и маленьких детей с расширенными собирательными системами из-за риска быстрой декомпрессии или расслоения почечной лоханки во время серийных расширений трактов.Важно помнить, что ПКН у новорожденных и младенцев более сложная, чем у детей старшего возраста.
Затем тракт постепенно расширяют фасциальными расширителями (например, расширителями Кунса) до подходящего французского размера, и, наконец, продвигают нефростомическую трубку и помещают в почечную лоханку. Как только трубка окажется в сборной системе, внутренний троакар и проволочный направитель можно будет удалить, а удерживающий механизм отремонтировать. Затем вводится небольшое количество контраста, чтобы подтвердить положение трубки (рис. 69-9).
Доступны несколько конструкций нефростомической трубки, различающиеся в основном типом удерживающего механизма. Две основные формы — это Malecot (кончик тюльпана) и фиксирующийся кончик косички (Рисунок 69-10). Катетеры Malecot слегка втягиваются после введения, позволяя боковым сторонам расширяться за пределы внешнего диаметра катетера. Катетеры с фиксацией косичек имеют дистальную петлю, которая восстанавливается путем натягивания веревки после введения трубки в почечную лоханку. Размер трубки выбирается на усмотрение интервенционного радиолога.Новорожденных обычно дренируют с помощью французского дренажа № 5 или 6. Детей старшего возраста сливают с помощью французских дренажных труб от 8 до 12, в зависимости от характеристик сливаемой жидкости.
В дополнение к проверке трубки может быть показана диагностическая нефростограмма. При выполнении нефростограммы не следует чрезмерно растягивать систему, чтобы снизить риск разрыва почек (т. Е. Рис. 69-11). Если есть какие-либо признаки инфекции, нефростограмма не проводится, чтобы снизить вероятность бактериемии и сепсиса.Нефростомическую трубку оставляют открытой для дренирования, пациента лечат антибиотиками, а нефростограмму откладывают на 48-72 часа.
Основные показатели жизнедеятельности обычно проверяются в течение 6-8 часов, а затем в соответствии с клиническим статусом пациента. Больных держат на постельном режиме в течение 6 часов. Допускается диета, если она переносится, всегда начиная с прозрачных жидкостей, потому что у некоторых пациентов возникает тошнота и рвота после анестезии или седативных средств. Боль и лихорадка лечатся симптоматически, и лечение антибиотиками продолжается в течение 24-72 часов после процедуры.Контролируется вход и выход из нефростомы. После снятия обструкции может развиться постобструктивный диурез (и этого следует ожидать). В нашей практике пробирка промывается 5 мл физиологического раствора каждые 8 часов для поддержания проходимости пробирки.
Если у пациента развивается макрогематурия или дренаж крови через PCN, выполняется нефростограмма, чтобы оценить связь между трубкой и основным сосудом (артерией или веной). Большинство ППН — это стационарные процедуры. Однако в избранной группе детей и подростков они могут выполняться амбулаторно.Кандидаты не должны иметь признаков инфекции, сопутствующих заболеваний и иметь адекватную функцию почек до процедуры. Кроме того, родители должны уметь ухаживать за трубкой PCN и иметь легкий доступ к медицинскому обслуживанию рядом с домом. 48
В целом у 10% пациентов после ПЯН разовьются незначительные или серьезные осложнения. 38 Сообщаемый уровень смертности от PCN составляет примерно 0,2%. 39 Кровоизлияние, требующее переливания, сообщается в 1% к 2.4% случаев, 29, 30 в основном из-за псевдоаневризмы почечной артерии 51 или артериовенозных свищей. 52 Большинство кровотечений проходят самостоятельно и не требуют вмешательства. Некоторым пациентам потребуется переливание крови или продуктов крови (свежезамороженная плазма [СЗП], тромбоциты), чтобы остановить кровотечение. У пациентов с уремией десмопрессин может использоваться для улучшения функции тромбоцитов. Если через нефростомию проходит крупный кровоток или на нефростограмме видны большие сгустки, необходимо промыть PCN холодным физиологическим раствором.Катетер для нефростомии, возможно, потребуется увеличить (по крайней мере, на 2 французских размера), чтобы попытаться тампонировать источник кровотечения. У пациентов с постоянным или рецидивирующим кровотечением через 3-5 дней после введения PCN следует рассмотреть возможность проведения ангиографии и эмболизации. Наконец, если гематокрит падает без макрогематурии, для оценки забрюшинного кровотечения рекомендуется поперечное сечение (УЗИ, КТ). 53 О сепсисе после ПЯН сообщается от 0,5% до 3,5% всех случаев. 29, 30, 33, 41 Однако, если пионефроз рассматривается отдельно как показание, у 7% пациентов разовьется сепсис, несмотря на соответствующую профилактику антибиотиками. 40, 54, 55 Другие серьезные осложнения включают пневмоторакс (1%), 29 плевральный выпот, пневмонию, воздушную эмболию, 56 непреднамеренное повреждение соседних органов (толстой кишки, 57 двенадцатиперстной кишки, селезенки) , и перитонит.
Незначительные осложнения не редкость, в том числе микроскопическая гематурия (которая обычно проходит в течение 48 часов), боль, лихорадка, периренальная гематома, самоограничение экстравазации мочи и проблемы, связанные с катетером. Частота смещения катетера колеблется от 1% до 30%, 29, 30 в зависимости от продолжительности времени, в течение которого требуется PCN.Закупорка может возникнуть у 1% пациентов. Регулярная промывка трубки и обильное потребление жидкости могут помочь предотвратить это осложнение.
Метаболические факторы , которые увеличиваются
Риск повторных камней включает:
Меламин нефролитиаз 2009.pdf Оценочные и диагностические тесты:
| Лечение
Камни в почках: Неотложное лечение 1. Обезболивание Rx 2. Удаление камня для устранения непроходимости мочевыводящих путей.
3. Инфекция Rx антибиотиками как указано REF: ACP PIER 2009 Ввести в / в жидкости пациентам с острым нефролитиазом только для лечения истощения объема .
Обоснование:
Рассмотрите возможность планового урологического лечения любого бессимптомного внутрикалицериновые камни после прохождения урологического вмешательства по поводу симптоматического камень.
Медикаментозная терапия почечных камней
Обезболивание: В рандомизированном контролируемом исследовании 130 пациентов с почечной коликой и умеренной боль, пациенты получали либо морфин, 5 мг, а затем 5 мг через 20 минут; кеторолак, 15 мг, а затем 15 мг через 20 минут; или их комбинация.Комбинация морфина и кеторолака превосходила оба препарата. для облегчения боли и требуется меньше «спасательной анальгезии» (48). Комментарии: Среди опиатов меперидин вызывает большую тошноту. и рвота у некоторых пациентов и противопоказана при наличии почечной недостаточности. недостаточность. Для расширения и расслабления мочеточника: Обоснование: стероиды могут уменьшить отек мочеточника, облегчая отхождение камней. тогда как нифедипин, блокатор кальциевых каналов, предположительно вызывает мочеточниковый дилатация и расслабление. Тамсулозин, антагонист α1-адренорецепторов, также может действовать как спазмолитик, увеличение дистального изгнания камня мочеточника, но было исследовано только в одно пилотное исследование. Свидетельство:
REF: Неотложная медицина Розена: концепции и клиническая практика, 6-е изд.2006 Самый важный фактор, связанный с прохождением исчисления через
мочеполовой тракт — это его размер. Камни мочеточника возникают в почках с гравитацией и перистальтикой. способствуя их прохождению по мочеточнику. Почечные камни редко вызывают полная непроходимость. Вдоль мочеточника имеется пять участков, где камни могут быть затронуты. Во-первых, камень может застрять в чашечке почки или переходят в почечную лоханку и застревают в лоханке мочеточника соединение.Относительно большая почечная лоханка (1 см) резко сужается на своем дистальной части, где он равен диаметру прилегающего к нему мочеточника (от 2 до 3 мм). Третья область — около края таза, где дуги мочеточника перегибаются. подвздошные сосуды кзади в истинный таз. Самый ограниченный область вдоль мочеточника и обычное место защемления — это мочеточниково-пузырный переход. Это место входа мочеточника. мышечная оболочка мочевого пузыря (интрамуральный мочеточник).На момент постановки диагноза до 75% камней располагаются в дистальной трети мочеточника. Ну наконец то, камни могут застрять в пузырном отверстии. Профилактика или хроническое лечение
Две трети камней мочеточника, которые проходят самопроизвольно, проходят в течение четырех недели после появления симптомов.Среднее время прохождения камня также увеличивается. по мере увеличения размера камня. Камень мочеточника, который не прошел в течение одного-двух месяцев вряд ли пройдет самопроизвольно при продолжении наблюдение. Кроме того, камни мочеточника, которые все еще имеют симптомы через четыре недели частота осложнений составляет 20% (включая ухудшение функции почек, сепсис и стриктура мочеточника). Таким образом, наблюдение до четырех недель. обычно разумно, если можно обеспечить последующее наблюдение. |
Визуализация гемодиализа: почечные и внепочечные данные | Insights into Imaging
Костно-мышечная система
У пациентов с хроническим заболеванием почек и находящихся на гемодиализе может развиться множество различных скелетно-мышечных аномалий, включая вторичный гиперпаратиреоз, остеомаляцию, остеосклероз, остеопороз, амилоидоз и различные болезни отложения кристаллов [23].
Другие аномалии, связанные с биохимическим нарушением хронической почечной недостаточности, включают кальцификаты мягких тканей / сосудов и кристаллические артропатии.
Костно-мышечные последствия, преимущественно связанные с диализом, включают токсичность алюминия, проявляющуюся в виде остеомаляции в результате приема солей алюминия в составе фосфатсвязывающих антацидных кислот, используемых для контроля гиперфосфатемии, амилоидоза и деструктивной спондилоартропатии.
Амилоидоз, связанный с диализом, является частым и серьезным осложнением у пациентов, длительно находящихся на диализе, и проявляется синдромом запястного канала, кистозными поражениями костей, деструктивной спондилоартропатией, артритом, периартритом и поражением системных органов [24].
Деструктивная спондилоартропатия характеризуется быстро прогрессирующими рентгенологическими аномалиями, включая потерю межпозвонкового дискового пространства, эрозию субхондральной кости в прилегающих телах позвонков и образование новой кости (рис. 7). У некоторых пациентов деструктивные изменения могут быть серьезными, имитирующими инфекционный спондилит: сохранение низкой интенсивности сигнала на Т2-взвешенных изображениях обычно позволяет исключить инфекции [23].
Рис. 7Рентгеновский снимок позвоночника.Диффузный остеосклероз позвоночника у пациента, находящегося на хроническом гемодиализе. Распространение плотности субконцевых пластин на нескольких смежных уровнях ( стрелки ), узор, известный как «позвоночник из джерси из шерстяного трикотажа»
Аваскулярный некроз, остеомиелит (рис. 8a, b), септический артрит, тендиноз / разрыв сухожилия и бурсит / синовит вызываются сочетанием хронической почечной недостаточности, стероидных / иммунодепрессантов и диализа [25].
Фиг.8a , b : аксиальная КТ без анализа ( a ), сагиттальная плоскость.Остеомиелит предплюсны у мужчины 72 лет с хронической почечной недостаточностью на диализе. Обширные костные изменения, вовлекающие все кости предплюсны с важными участками остеолиза, связанными с участками остеосклероза. Инфекция широко поражает пяточную кость с внутрикостной жидкостью и газовыми компонентами. На боковой стороне пяточной кости виден свищ с подкожной мягкой тканью ( стрелка )
Почечная остеодистрофия
Нарушения со стороны костно-мышечной системы многочисленны и часты у пациентов с хронической почечной недостаточностью.Хроническая почечная недостаточность, гемодиализ, перитонеальный диализ, трансплантация почки и прием различных лекарственных препаратов провоцируют сложные биохимические нарушения кальций-фосфатного обмена с широким спектром патологий костей и мягких тканей, называемых почечной остеодистрофией [26]. Почечная остеодистрофия — это общий термин, применяемый ко всем патологическим особенностям костей у пациентов с хронической почечной недостаточностью, и он включает остеомаляцию или рахит в зависимости от возраста пациента, вторичный гиперпаратиреоз с резорбцией кости, периостальную реакцию, коричневые опухоли, остеосклероз, остеопороз, мягкие ткани. кальцификации тканей и сосудов.
Множественные факторы играют роль в возникновении остеодистрофии почек, включая дефицит активной формы витамина D из-за нарушения почечного метаболизма и увеличение секреции паратгормона из-за гиперфосфатемии, вызывающей гипокальциемию за счет осаждения кальция [5].
Рентгенография по-прежнему является наиболее важным и широко применяемым методом [27] для выявления изменений почечной остеодистрофии. Радионуклидная визуализация, компьютерная томография и магнитно-резонансная томография показаны реже и в основном используются для более чувствительной и точной идентификации (асептический некроз кости, инфекция, зоны Лузера), морфологических проявлений (инфекция позвоночника с нервным поражением) и дифференциальной диагностики осложнений ( деструктивная спондилоартропатия в сравнении с инфекцией позвоночника).
Остеокластическая резорбция кости затрагивает поверхности кости и может быть поднадкостничной, интракортикальной, эндостальной, трабекулярной, субхондральной, подсвязочной и субсухожильной. Ранние рентгенологические изменения резорбции поднадкостничной кости могут быть продемонстрированы на пучках фаланг и лучевых сторонах средних фаланг пальцев второго и третьего пальцев руки (рис. 9a, b) [26]. Ранняя поднадкостничная резорбция приводит к потере четкости кортикальной кости с характерным кружевным внешним видом, который позже прогрессирует до полного исчезновения кортикального слоя.Усиленная резорбция костей концевых фаланг может привести к акроостеолизу с разделением пучка и основания фаланги. Поднадкостничная резорбция часто сочетается с внутрикортикальным туннелированием и эндостальной резорбцией, что вызывает зубчатые дефекты внутреннего кортикального контура. При запущенном заболевании может наблюдаться широко распространенная резорбция трабекул внутри костного мозга с потерей четкости и исчезновением трабекул. Наиболее типичное проявление резорбции губчатой кости возникает на своде черепа и называется череп «соль и перец» [26].
Фиг.9a , b : a Рентгенологическое изображение левой руки пациента, находящегося на хроническом гемодиализе. b Увеличение. Вторичный гиперпаратиреоз с резорбцией костной ткани по радиальным сторонам средних фаланг пальцев ( стрелки )
Резорбция субхондральной кости может поражать различные суставы, чаще всего крестцово-подвздошные, грудинно-ключичные и акромиально-ключичные суставы, межпозвоночные диски и лобковый симфиз.Рентгенологические изменения в крестцово-подвздошных суставах аналогичны изменениям, наблюдаемым при анкилозирующем спондилите, и включают расширение суставной щели и эрозии субхондральной кости, окруженные остеосклерозом [26].
Подсвязочная и субсухожильная резорбция кости происходит во многих местах, особенно в седалищных буграх, вертлугах бедра и местах прикрепления клювовидно-ключичных связок.
Образование новой кости в надкостнице может наблюдаться у пациентов с развитым гиперпаратиреозом, поражающим плюсневые кости, бедренную кость, таз, плечевую кость, лучевую кость, локтевую кость, пястные кости и фаланги.
Остеосклероз часто встречается у пациентов с почечной остеодистрофией и вторичным гиперпаратиреозом (рис. 10a, b). Костный склероз при почечной остеодистрофии может поражать различные элементы скелета, но обычно он преобладает в осевом скелете. Одна из типичных находок включает широкий остеосклероз, локализованный ниже замыкательных пластинок тел позвонков с нормальной плотностью средних частей (внешний вид «майки рэггер») [26].
Фиг.10a , b : неулучшенный CT.Крестцовая область, аксиальная плоскость ( a ) и коронковая реформация ( b ). Почечная остеодистрофия левого крыла подвздошной кости с диффузным склерозом костей и некоторыми участками резорбции ( стрелки ) вследствие вторичного гиперпаратиреоза у пациента, находящегося на хроническом гемодиализе
Рентгенологические признаки остеомаляции — снижение плотности костной ткани с потерей четкости кортикального слоя кости и укрупнение трабекулярного рисунка. Зоны ослабления (например, переломы Молочника, псевдопереломы) — редкие, но патогномические признаки, которые наиболее часто встречаются в медиальной части шейки бедра, лобковых ветвях, подвздошной кости, лопатках, ребрах и акромионе.Зоны Looser представляют собой неминерализованный остеоид и представляют собой прозрачные линии, перпендикулярные коре головного мозга, часто симметричные по расположению.
Рахитоподобные изменения могут возникать в незрелом скелете и отражать аномальную эндохондральную оссификацию. Рентгенологические признаки включают остеопению с размягчением и сгибанием костей, расширение пластинки роста, а также купирование, расширение, деминерализацию и дезорганизацию метафиза [26].
Остеопоротическая кость характеризуется истончением кортикального слоя и трабекул.Эти особенности наиболее очевидны в элементах скелета, богатых губчатым веществом (позвоночник, проксимальный отдел бедра и предплечье). При запущенном остеопорозе может произойти потеря трабекул с патологическими переломами. В позвоночном столбе исчезновение поперечных трабекул с сохранением трабекул вертикального сжатия приводит к появлению характерных вертикальных штрихов. Конечными результатами являются патологические переломы с клиновидными, двояковогнутыми (у рыбных позвонков) или уплощенными телами позвонков и деформациями позвоночника.Переломы позвонков можно оценить субъективно или с помощью количественных методов. В целом чувствительность рентгенографии оставляет желать лучшего; Прежде чем остеопороз можно будет обнаружить на обычных рентгенограммах, необходимо потерять от 30% до 50% костной ткани [26].
Коричневые опухоли
Коричневые опухоли — это форма кистозно-фиброзного остита, конечная стадия ремоделирования кости при первичном или вторичном гиперпаратиреозе [28]. У пациентов с хронической почечной недостаточностью коричневые опухоли представляют собой крайнее и серьезное осложнение почечной остеодистрофии [28–31].Коричневые опухоли возникают в результате локального замещения кости васкуляризированной фиброзной тканью (кистозный остеит фиброза) в результате стимулируемой паратироидным гормоном остеокластической активности [5]. Пациенты с почечной остеодистрофией с коричневыми опухолями фактически имеют автономно функционирующие паращитовидные железы или третичный гиперпаратиреоз [5]. Фиброзная ткань содержит гигантские клетки, и поражения могут стать кистозными в результате некроза и разжижения [5]. Эти поражения представляют собой репаративный клеточный процесс, а не опухолевый процесс, и расположены в областях интенсивной резорбции кости (рис.11а, б) [5, 32].
Фиг.11a , b : неулучшенная КТ, коронарные ( a ) и сагиттальные ( b ) реформации. Коричневая опухоль у пациента, находящегося на хроническом гемодиализе с третичным гиперпаратиреозом. Коричневая опухоль выглядит как литическое поражение подвздошной кости ( стрелка )
Коричневые опухоли возникают как одиночные или множественные рентгенопрозрачные поражения и могут обнаруживаться как внутри кости, так и в прилегающих мягких тканях.При отсутствии лечения они могут подвергнуться центральному некрозу и образованию кист [5]. Рентгенологически коричневые опухоли представляют собой четко выраженные литические поражения, часто эксцентрические или кортикальные, которые могут вызывать образование гребешков и расширение кости.
Метастатическая кальцификация мягких тканей и сосудов
Биохимическое нарушение хронической почечной недостаточности включает метастатические кальцификации сосудов и мягких тканей и кристаллические артропатии. Сосудистые кальцификации проявляются как медиальные, так и интимальные кальцификации артерий и являются отличительным признаком ускоренного атеросклероза, наблюдаемого при уремии [33].
Кальцифицирующая уремическая артериолопатия — редкое, но опасное для жизни осложнение, которое, по оценкам, встречается у 1% пациентов с хроническим заболеванием почек и у 4,1% пациентов, находящихся на поддерживающем гемодиализе [34]. Суставной кальциноз характеризуется отложением большого количества кальция вокруг околосуставных областей и обычно наблюдается в плечевых, локтевых и тазобедренных суставах [35]. У пациентов, находящихся на гемодиализе, могут наблюдаться даже висцеральные (миокардиальные и перикардиальные) кальцификации.
Сосудистые кальцификации очень часто встречаются при терминальной стадии почечной недостаточности, особенно у пациентов, находящихся на гемодиализе (рис. 12а, б) [36, 37]. Механизмами кальцификации сосудов являются гиперфосфатемия и повышенное содержание продуктов кальция (Ca) и фосфата (P) [38, 39].
Фиг.12a , b : Рентгенологические изображения нескольких сегментов скелета разных пациентов (все из которых проходят длительный гемодиализ) показывают диффузные кальцификации периферических артерий ( стрелки, ).Сосудистые кальцификации проявляются как медиальные, так и интимальные кальцификаты артерий
Сосудистая кальцификация вызывает жесткость стенки сосуда и снижает эластичность сосудов [40]. Иваса и др. показали гораздо более высокий уровень кальцификации внутричерепных артерий у пациентов, находящихся на гемодиализе, чем в общей популяции, и это открытие, как сообщается, является независимым фактором риска ишемического инсульта. Наиболее частыми участками кальцификации у пациентов, находящихся на гемодиализе, были внутренняя сонная артерия и позвоночные артерии [41].
Сердечно-сосудистые осложнения
Сердечно-сосудистые осложнения часто встречаются у пациентов с хронической почечной недостаточностью и связаны с атеросклерозом и гиперлипидемией, гипертонией из-за задержки натрия и изменениями в ренин-ангиотензиновой оси, дисфункцией миокарда и перикардитом. Более 50% пациентов с терминальной стадией почечной недостаточности, получающих хронический гемодиализ, умирают от сердечно-сосудистых заболеваний, включая застойную сердечную недостаточность из-за увеличения постнагрузки левого желудочка: перегрузки объемом между диализами, гипертония, повышенная жесткость артерий, анемия, кровоток (артериовенозный свищ) и симпатическая активация.Пациенты, находящиеся на диализе, имеют более высокий риск развития атеросклероза, а также основного сахарного диабета и / или гипертонии как причин терминальной стадии почечной недостаточности [4]. Атеросклероз поражает основные и все периферические артерии, включая внутрипочечные артерии. Кальцификации миокарда, коронарных артерий и сердечных клапанов часто наблюдаются у пациентов с терминальной стадией почечной недостаточности [40, 42].
Поражения кальцификации сердечно-сосудистой системы могут привести к развитию ряда клинически значимых осложнений, включая ишемию миокарда, инфаркт миокарда, нарушение функции миокарда, застойную сердечную недостаточность, недостаточность сердечного клапана и сердечные аритмии [43, 44].Было продемонстрировано, что отложения амилоида B2-микроглобулина широко локализованы в сердцах пациентов с длительным гемодиализом [45], в частности, на уровне эндокарда, миокарда и стенки мелких сосудов [24].
Осложнения со стороны грудной клетки
Пациенты с хронической почечной недостаточностью могут иметь несколько отклонений от нормы, видимых на рентгенограмме грудной клетки из-за изменений метаболизма фосфора и кальция, изменений гемостаза, артериальной гипертензии, задержки жидкости или из-за диализа.
Грудные осложнения гемодиализа можно разделить на две основные категории: сердечно-сосудистые и легочные [46].
Сердечно-сосудистые заболевания включают кальцификацию аорты, кардиомегалию, кальцификаты коронарных артерий, перикардиальный выпот, легочную тромбоэмболию и внутрипредсердный тромб [46].
Наиболее частые легочные аномалии включают интерстициальный и альвеолярный отек из-за застойной сердечной недостаточности, плеврального выпота, ателектаза легких, метастатических кальцификатов в легкие и кальцификатов стенок бронхов, плевры и сосудов грудной стенки.Паренхиматозные аномалии легких, видимые на КТ, включают участки матового стекла, утолщение межлобулярной перегородки, рубцы паренхиматозного фиброза, буллую эмфизему, перибронховаскулярное интерстициальное утолщение, увеличенный калибр сосудов, бронхоэктазы и утолщение плевры и трещин [46].
Частота легочных инфекций у пациентов с уремией выше по сравнению с населением в целом, с признаками уплотнения паренхимы и / или плеврального выпота [46].
Золотистый стафилококк продолжает оставаться наиболее распространенным (20.8%) причиной бактериальной инфекции у пациентов, находящихся на длительном гемодиализе [46]. Пациенты, находящиеся на гемодиализе, подвергаются повышенному риску развития активного туберкулеза после первичного инфицирования, активации тихой болезни или реактивации ранее существовавшей туберкулезной инфекции [46].
Неврологические осложнения
Пациенты с терминальной стадией почечной недостаточности часто имеют аномалии центральной нервной системы, некоторые из которых связаны с самой терминальной стадией почечной недостаточности, а другие связаны с проблемами, вторичными после гемодиализа [47].
Наиболее частые неврологические осложнения в этой группе пациентов включают очаговые поражения белого вещества, церебральную атрофию, диализную энцефалопатию, гипертоническую энцефалопатию, церебральный инфаркт, внутримозговое кровоизлияние, синдром задней обратимой энцефалопатии, синдром осмотической демиелизной синусовой инфекции и диализный тромбоэмболический синдром. синдром. Периферическая нейропатия также часто встречается у пациентов с хронической почечной недостаточностью [5].
Острое цереброваскулярное заболевание — одна из наиболее частых причин заболеваемости и смертности пациентов, находящихся на длительном лечении гемодиализом.Церебральная ишемия и инфаркт являются важными факторами риска инсульта и вызваны окклюзией мелких глубоко проникающих церебральных артерий. Пациенты, находящиеся на гемодиализе, подвергаются большему риску кровоизлияния в мозг из-за терапии антикоагулянтами (например, гепарин и низкомолекулярные гепарины), дефектов адгезии тромбоцитов, анемии и недостаточного контроля артериальной гипертензии. Кровоизлияние в мозг может быть внутрипаренхиматозным, субдуральным, эпидуральным или субарахноидальным. Пациенты с терминальной стадией почечной недостаточности также имеют предрасполагающие факторы, которые приводят к тромбозу синусовой вены.
Гематологические отклонения
Гематологические отклонения являются одними из наиболее частых проявлений уремии [4]. Эти нарушения включают анемию, кровотечение и дисфункцию гранулоцитов и тромбоцитов. Основными причинами анемии при хронической почечной недостаточности являются дефицит эритропоэтина, гликопротеина, который обычно вырабатывается почками, и дефицит железа из-за пониженного потребления железа и частого забора крови. Терапия эритропоэтином улучшила общее состояние пациентов с хронической почечной недостаточностью.У пациентов с уремическим синдромом жировой костный мозг постепенно замещается кроветворным содержимым костного мозга с гипоинтенсивным видом на Т1-взвешенных МРТ-изображениях в различных анатомических областях (особенно в позвоночнике и костях верхних и нижних конечностей). Геморрагический диатез часто встречается у пациентов с хронической почечной недостаточностью. Самопроизвольное нетравматическое кровотечение может повлиять на околопочечное и субкапсулярное пространства, почечную паренхиму или собирательную систему. У пациентов с уремией часто встречается желудочно-кишечное кровотечение [5].
Инкапсуляция перитонеального склероза
Хотя медицинские соображения могут диктовать выбор для некоторых пациентов непрерывного амбулаторного перитонеального диализа (CAPD) или гемодиализа, в большинстве случаев почечная недостаточность поддается лечению любым из этих методов.
Следовательно, важно распознать некоторые потенциально смертельные осложнения CAPD, которые должны быть обнаружены на ранней стадии, чтобы позволить быстрое прерывание CAPD и направить пациента только на лечение гемодиализом.
Инкапсулирующий перитонеальный склероз — нечастое серьезное осложнение CAPD [48], связанное со значительной заболеваемостью и смертностью.
В большом исследовании, проведенном Rigby и Hawley [49], общая распространенность инкапсулирующего перитонеального склероза составляет 0,7%; тем не менее, распространенность увеличивается до 19,4% у пациентов, получавших CAPD [49] более 8 лет.
Инкапсулирующий склероз брюшины — это состояние, характеризующееся фиброзным утолщением брюшины, которое может прогрессировать до инкапсуляции петель тонкой кишки с последующей непроходимостью кишечника.Утолщение брюшины может быть гладким, нерегулярным и узловатым, а легкое утолщение брюшины обычно прогрессирует до диффузного, сильного утолщения брюшины и, в конечном итоге, кальцификации брюшины.
Утолщение брюшины прогрессирует до перитонеальной инкапсуляции вовлеченных петель тонкой кишки, процесса, который был описан как «коконирование» тонкой кишки оболочкой из фиброзной склерозированной брюшины.
Петли тонкой кишки часто собираются в центре, инкапсулируя фиброзную брюшину.Фиброзный процесс может проявляться в виде скопления связанных вместе петель тонкой кишки. В конечном итоге может возникнуть некроз тонкой кишки с перфорацией.
При инкапсулировании склероза брюшины утолщенные фиброзные мембраны брюшины могут привести к локализованному асциту. Поскольку тонкая кишка становится вовлеченной, связанной и похожей на массу, привязанная тонкая кишка также может производить локализованные скопления жидкости.
Было описано множество других осложнений, связанных с перитонеальным диализом, включая дисфункцию катетера, гематому, утечку диализата и гидроторакс [50].
Осложнения доступа к диализу
Повторный доступ к кровообращению важен для проведения адекватного поддерживающего гемодиализа. Пациенты с терминальной почечной недостаточностью, которым требуется длительный гемодиализ, нуждаются в прочном сосудистом доступе, и поддержание приемлемого сосудистого доступа является важной проблемой для пациентов с почечной недостаточностью. Гемодиализ обычно выполняется с использованием трансплантата из внутреннего артериовенозного свища (AVF) или политетрафторэтилена (PTFE, тефлон), также известного как протезный мостовидный протез (PBG).Хирургически сконструированные артериовенозные (AV) фистулы (радио- или брахиоцефальные), синтетические AV-трансплантаты или венозный катетер, расположенный в центральной вене, являются обычными средствами создания сосудистого доступа для длительного гемодиализа.
Стеноз сосудов — основная причина нарушения доступа. Было показано, что лечение стеноза с помощью чрескожных вмешательств, ангиопластики, внутрипросветных сосудистых стентов или томболизиса в качестве альтернативы хирургическому вмешательству увеличивает шансы на выживание пациентов с диализом AVF и PBG [51].Для быстрого выявления развития стеноза доступа можно использовать несколько методов наблюдения. Цветное доплеровское ультразвуковое исследование [52] и цифровая субтракционная ангиография [53] наиболее часто используются для обнаружения стеноза доступа, в то время как недавно были внедрены мультидетекторная КТ с контрастным усилением [54] и МР-ангиография шунтов [55]. Ангиографическая оценка через пункцию плечевой артерии показана при планировании интервенционной процедуры.
Артериовенозные свищи
Атриовентрикулярная фистула считается лучшим долговременным сосудистым доступом для гемодиализа, поскольку она обеспечивает адекватный кровоток, является продолжительной и имеет меньшую частоту осложнений, чем другие типы доступа.Нефролог или хирург создает атриовентрикулярную фистулу. В результате вена становится больше и сильнее, что упрощает повторное введение иглы при гемодиализе. Атриовентрикулярные свищи также имеют некоторые недостатки, включая неполное созревание вены, и может потребоваться период в 1–4 месяца, прежде чем можно будет использовать атриовентрикулярную фистулу. Дисфункция свища — наиболее частая причина повторного вмешательства и повторной госпитализации. Частота осложнений АВФ увеличивается с возрастом и дозой эритропоэтина, а также среди пациентов с ранее неудачным шунтированием в анамнезе [56].Клинические симптомы включают слабый кровоток с потерей дрожания в трансплантате, увеличивающуюся псевдоаневризму или ипсилатеральный отек конечностей.
Основные осложнения атриовентрикулярной фистулы включают тромбоз с окклюзией или стенозом венозного оттока (рис. 13а, в), а также аневризму или псевдоаневризму венозного тракта (рис. 14а, в) вблизи или дистальнее анастомоза с лучевая артерия [57]. В частности, обструкция венозного оттока является наиболее частой причиной тромбоза АВФ и плохого диализа.Чаще всего псевдоаневризмы обнаруживаются в местах повторной пункции или хирургического анастомоза.
Фиг.13a — c : 80-летний пациент мужского пола с хронической почечной недостаточностью, находящийся на гемодиализе. Стеноз (длиной около 5 см) оттока АВФ руки ( стрелка ) ( а ), леченный ангиопластикой ( b ) с восстановлением нормальной проходимости ( c )
Фиг.14a — c : АВФ предплечья на уровне метафиза лучевой кости у 70-летнего пациента с хронической почечной недостаточностью на диализе. Отток перианастомотических псевдоаневризм ( стрелки, ). В месте пункции располагаются аневризмы или псевдоаневризмы вен
Осложнения артериального тракта при АВФ встречаются редко. Поражение проксимальных артерий, окклюзия или стеноз артериального анастомоза легко выявляются с помощью цифровой субтракционной ангиографии.Артериальный стеноз выглядит как суженная область, прилегающая к участкам эктазии трансплантата или между ними. Разрыв лучевой артерии может определять гематому со сдавлением нервных структур в запястном канале.
Артериовенозные трансплантаты
AV-фистула с большой проходимостью и низким профилем осложнений обычно является первым выбором для создания сосудистого доступа. Однако, когда поверхностные вены не подходят для образования AV-фистулы или все они были истощены в результате повторных процедур AV-фистулы, альтернативой являются артериовенозные трансплантаты с использованием расширенного политетрафторэтилена (PTFE) [58].Трансплантат из ПТФЭ — протезный мостовидный протез (PBG) — состоит из синтетического катетера, вставленного и ушитого в артерию, обычно лучевую артерию, и вены, обычно головную или базиликовую.
В отличие от артериовенозной фистулы, используемой для хронического гемодиализа, AV-трансплантат можно использовать немедленно. Как и при естественной АВФ, в первую очередь следует использовать недоминантную руку [58]. По сравнению с правильно сформированными свищами, трансплантаты имеют больше проблем со свертыванием и инфекциями и требуют более ранней замены.Однако ухоженный трансплантат может прослужить несколько лет.
Общая частота осложнений для AV-трансплантатов в два раза выше, чем для AV-свищей. Наиболее частым осложнением, связанным с атриовентрикулярным трансплантатом, является обструкция венозного оттока с тромбозом трансплантата, что составляет от 85 до 90% проблем с гемодиализом. ПБГ имеют более короткую среднюю проходимость, чем нативные АВФ. Наиболее частые причины неудач включают хирургическое перекручивание или перегиб трансплантата во время имплантации, артериальные пробки, стеноз венозного анастомоза или неожиданный венозный стеноз.Венозный стеноз приводит к проблемам, которые в конечном итоге вызывают неадекватный диализ. Чаще всего стеноз затрагивает венозный анастомоз, но он может возникать в любом месте системы, состоящей из трансплантата, анастомоза и дренирующих вен. Полный тромбоз легко идентифицируется, если он затрагивает трансплантат или всю венозную конечность. Более того, АВ трансплантаты могут вызывать осложнения, связанные со стенозом артериального притока, стенозом артериального анастомоза, стенозом внутри трансплантата, псевдоаневризмой трансплантата и дегенерацией трансплантата.Варианты лечения — хирургическая ревизия или эндоваскулярная установка стент-графта.
Идентификация нового дисфункционального варианта рецептора P2Y12 тромбоцитов, ассоциированного с кровоточащим диатезом | Кровь
Чтобы предсказать последствия замены p.His187Gln на молекулярном уровне, мы провели исследования молекулярного моделирования P2Y 12 R. Две недавно опубликованные кристаллографические структуры человеческого P2Y 12 R, 12,13 в комплексе как с агонистом, так и с антагонистом, оказались очень полезными для этого исследования.Более того, модели варианта P2Y 12 R p.His187Gln были построены с использованием связанной с агонистом кристаллической структуры P2Y 12 R для анализа возможных структурных различий из-за этой вариации последовательности.
TM5 в обеих кристаллических структурах P2Y 12 R необычно прямая и наклонная из-за отсутствия пролина (например, позиция 5.50 в системе нумерации Баллестероса-Вайнштейна) 25 или остатков глицина в этой спирали в другом G-белке -связанные рецепторы, дестабилизирующие его прямую α-спиральную конформацию.Предыдущие попытки моделирования P2Y 12 R на основе имеющихся кристаллографических шаблонов были неточными из-за этой разницы.
В обеих структурах точка мутации расположена в верхней части TM5, обращенной внутрь к сайту связывания, рядом с лигандом. Сравнение двух различных кристаллографических структур, связанных с агонистом и антагонистом, выявило большие конформационные изменения, происходящие в TM6 и TM7, но также немного отличающуюся ориентацию TM5.Следовательно, конформации остатков в этой спирали, включая His187 (5.36), различаются в двух структурах. В структуре P2Y 12 R, связанной с антагонистом WT, боковая цепь His187 более ориентирована на TM4 и ограничивает сайт связывания, обеспечивая гидрофобные взаимодействия с лигандом AZD1283. В структуре P2Y 12 R, связанной с агонистом WT, боковая цепь His187 (5.36) напрямую взаимодействует через Н-связь с 2′-гидроксильной группой 2MeSADP (рис. 5). Более того, ароматическое кольцо этого гистидина перпендикулярно адениновому ядру и может стабилизировать его за счет гидрофобных взаимодействий.Стыковка PSB-0413 в этой структуре WT P2Y 12 R очень напоминает режим связывания 2MeSADP (Рисунок 5). Фактически, адениновые основания двух лигандов занимают общий ароматический сайт связывания, образуя π-π взаимодействие с Tyr105 (3,33) и Н-связи с Asn191 (5,40). 2-пропилтиогруппа PSB-0413 простирается глубже в тот же гидрофобный карман, занятый 2-метилтиогруппой кристаллизованного агониста и ограниченный Phe106 (3,34), Met152 (4,53), Leu155 (4,56), Ser156 (4,57), Val190 (5.39) и Cys194 (5,43). 2′- и 3′-гидроксильные группы рибозы образуют H-связывающие взаимодействия с Lys179 (EL2) и His187 (5,36) и с Lys179 (EL2) и карбонилом основной цепи Cys97 (3,25) соответственно. Нерасщепляемая трифосфатоподобная цепь PSB-0413 направлена к TM2 и образует многочисленные гидрофильные и ионные взаимодействия с Lys80 (2,60), Arg93 (3,21), Arg256 (6,55), Tyr259 (6,58) и Lys280 (7,35).
При стыковке с P2Y 12 R p.Модели вариантов His187Gln, PSB-0413 показали ту же ориентацию в сайте связывания и аналогичные взаимодействия, что и в рецепторе WT (данные не показаны). Однако в зависимости от ротамера боковой цепи Gln187 сеть водородных связей, включающая 2′-гидроксильную группу, может различаться. Фактически, в некоторых ротамерах Gln187 не образует водородной связи с лигандом, в то время как в других он может действовать как акцептор водородной связи или донор водородной связи.
границ | Почечная лимфатическая система: анатомия, физиология и клиническое значение
Введение
Лимфатические сосуды по всему телу начинаются как слепые капилляры в интерстициальном пространстве.Они сливаются, образуя более крупные сборные сосуды, которые в конечном итоге стекают в вены. Таким образом, они выполняют жизненно важную функцию по всему телу, включая почки, отводя жидкость и макромолекулы из межклеточного пространства и возвращая их в системный кровоток. Это предотвращает накопление интерстициальной жидкости, которая может ухудшить доставку кислорода к тканям. Почка обильно снабжена лимфатическими сосудами, что свидетельствует о ключевой роли почечной лимфатической системы в нормальных и стрессовых физиологических состояниях (Kaiserling, 1940).Однако роль почечных лимфатических сосудов в заболевании, а также анатомия и физиология почечных лимфатических сосудов в целом в последние десятилетия в значительной степени игнорировались.
Лимфатическая дисфункция определяется как неспособность адекватно дренировать интерстициальную жидкость и может иметь множество причин (например, недостаточность клапана, обструкция лимфатических сосудов, потеря градиентов давления или потеря сократимости гладких мышц). Клинически это проявляется как периферический отек с ямками на конечностях, но менее очевиден в почках.Однако из-за жесткости почечной капсулы нарушение лимфодренажа может привести к повышению внутрипочечного давления и способствовать нарушению функции почек. Мы подозреваем, что этот упускаемый из виду механизм присутствует в различных клинических сценариях, таких как застойная сердечная недостаточность (ЗСН), ОПП на фоне ССВО, хроническая почечная недостаточность, почечная недостаточность трансплантата и другие.
Это составляет множество клинических сценариев, в которых почечные лимфатические узлы могут играть важную роль, однако в недавней литературе имеется удивительно мало информации по этой важной теме.Здесь мы стремимся всесторонне изучить состояние почечной лимфатической системы. Начнем с обзора сравнительной анатомии человека и животных. Затем следует обсуждение физиологии почечной лимфатической системы в нормальных и стрессовых условиях, а затем краткое изложение последствий почечной лимфатической дисфункции при различных болезненных состояниях.
Анатомия лимфатических сосудов почек
Методы изучения анатомии лимфатических сосудов почек
Считается, что Паоло Масканьи сделал первое описание почечных лимфатических сосудов в 1787 году после введения ртути в почки трупов (Mascagni, 1787).С тех пор в большинстве исследований для микроскопического исследования почечной ткани использовались красители (например, триптановый синий, тушь, краситель Эванс синий), вводимые внутривенно или в паренхиму почек. Однако в последние десятилетия изучение анатомии почечной лимфатической системы значительно продвинулось благодаря усовершенствованию методов визуализации и разработке маркеров LEC.
Маркеры лимфатических эндотелиальных клеток
Хотя маркеры LEC не специфичны для LEC, они могут отличать их от эндотелиальных клеток кровеносных сосудов.Наиболее широко используемыми маркерами являются подпланин, LYVE-1, рецептор фактора роста эндотелия сосудов 3 (VEGFR-3) и связанный с просперо фактор транскрипции гомео-бокса 1 (Prox1) (Seeger et al., 2012). Из них подпланин, трансмембранный белок муцинового типа, является наиболее надежным в почках человека и может быть локализован в залитой парафином ткани с помощью антител к подпланину (Kalof and Cooper, 2009).
Визуализация почечной лимфатической системы
in vivoПочечно-лимфатические анатомические исследования, будь то микроскопические или микрорентгенографические исследования, ранее требовали удаления почки.Однако методы визуализации больших лимфатических сосудов in vivo были разработаны и используются в настоящее время (например, педальная лимфангиография, лимфангиография и лимфосцинтиграфия) (Itkin and Nadolski, 2018), хотя существующие методы не позволяют визуализировать почечные лимфатические узлы. Однако возможно визуализировать центральную лимфатическую систему путем инъекции контраста в паховые лимфатические узлы (интранодальная лимфангиография) и прямой трансабдоминальной катетеризации цистерны хили (Itkin and Nadolski, 2018).Также описаны малоинвазивные лимфатические процедуры. Введение материала для эмболизации, такого как клей N-бутилцианоакрилат (N-BCA) (TRUFILL, Codman Neuro, Rayhnam, MA, США), в интерстиций лимфатических узлов может привести к их распространению и эмболизации ниже по течению (Itkin and Nadolski, 2018 ). Лимфатические сосуды печени можно визуализировать путем введения контрастного вещества в перипортальное пространство (Itkin et al., 2017). В совокупности это указывает на то, что в будущем может быть осуществима интерстициальная инъекция контрастного вещества (или зонда) для визуализации почечных лимфатических узлов.
Эмбриологическая анатомия
Sabin (1909) впервые предположил, что LECs возникают путем прорастания из эмбриональных вен, что теперь подтверждено исследованиями по отслеживанию клонов с использованием маркеров LEC (Tammela and Alitalo, 2010). Используя экспрессию LYVE-1, Lee et al. (2011) изучали развитие почечных лимфатических сосудов у эмбрионов мышей. Внутрипочечные лимфатические сосуды, связанные с внепочечными лимфатическими сплетениями, были впервые обнаружены у 13-дневного эмбриона. Эти лимфатические сосуды образовали хорошо организованные сети, которые следовали за развивающимися дугообразными и междольковыми сосудами в течение следующих нескольких дней.В мозговом веществе почек ни на одной стадии развития не наблюдалось.
Ли и др. (2011) отметили, что разбросанные клетки LYVE-1 + наблюдались в развивающихся дугообразных венах, главным образом в ветвящихся зачатках, и что лимфатические сосуды в основном располагались вокруг развивающихся вен до 4-го дня постнатального развития. Незрелые макрофаги и дендритные клетки также экспрессировал LYVE-1 и появлялся раньше LYVE-1 + лимфатических сосудов. Эти клетки были замечены тесно переплетенными или даже составляющими часть стенки лимфатического сосуда.Они пришли к выводу, что клетки LYVE-1 + первоначально отрываются от вен, но что макрофаги и дендритные клетки LYVE-1 + имеют решающее значение в организации процесса ветвления, который соединяет эти клетки с экстрапочечными лимфатическими сосудами. VEGF-C, по-видимому, также играет важную регулирующую роль в этом процессе ветвления (Lee et al., 2011; Mohamed and Sequeira-Lopez, 2018). Tanabe et al. (2012) аналогичным образом обнаружили, что почечные лимфатические сосуды у крыс первоначально развиваются из ранее существовавших внепочечных лимфатических сосудов и простираются к коре головного мозга по сосудистой сети почек.Внутрипочечные лимфатические сосуды впервые были обнаружены на 20-й день эмбриона. До сих пор неясно, обладают ли почки млекопитающих внутренними лимфатическими предшественниками, которые способствуют развитию внутрипочечных лимфатических сосудов (Mohamed and Sequeira-Lopez, 2018).
Анатомия сосудов почек
Почечные лимфатические узлы следуют топографии почечной сосудистой сети (O’Morchoe and O’Morchoe, 1988), поэтому уместен краткий обзор артериального кровоснабжения почек. Обычно имеется одна почечная артерия, снабжающая каждую почку.В почечном синусе он делится на пять сегментарных артерий (заднюю, верхнюю, передне-верхнюю, передне-нижнюю и нижнюю) (Bhimji and Leslie, 2018). Каждый сегмент почки состоит из долей (состоящих из почечной пирамиды, перекрытой частью почечной коры), которая затем делится на почечные долей (состоящие из нефронов, окружающих один костномозговой луч и стекающих в одинарный коллекторный канал). Артерии, отходящие от сегментарной артерии, следуют этому дольчатому образцу (рис. 1).Между долями отделяется междолевая артерия, дающая начало дугообразным артериям, которые пересекают кортико-мозговое соединение. От каждой дугообразной артерии отходит междольковая артерия, которая расходится между долками в направлении капсулы. Они выделяют афферентные артериолы, ведущие к клубочку. Венозная система такая же, как и артериальная, за исключением того, что имеется сообщение между венами из разных сегментов, тогда как сегментарные артерии являются концевыми артериями.
Рисунок 1. Строение лимфатической системы почек человека. (A) Лимфа проходит от 4–5 почечных лимфатических узлов корней на каждой почке к различным группам лимфатических узлов аорты. Большая часть лимфы, оттекающей из почки, собирается в хиловой цистерне и выводится через грудной проток в центральную венозную систему шеи. (B) Схематическое изображение доли почек человека. Слепые лимфатические капилляры начинаются в веществе почечной дольки в виде внутрилобулярных лимфатических сосудов, которые, в свою очередь, становятся межлобулярными лимфатическими сосудами.Отсюда лимфа может течь либо к капсуле, либо к воротам. Клапаны присутствуют на уровне капсулы и дугообразных сосудов, чтобы предотвратить обратный ток. Внутрипочечные артерии показаны красным цветом, а внутрипочечные вены — синим. Вставка показывает детали сообщающихся и перфорирующих лимфатических сосудов, пронизывающих почечную капсулу. (C) Схема, показывающая морфологию почечных лимфатических сосудов. Лимфатические сосуды морфологически различаются между начальными капиллярами (без базальной мембраны или гладкой мускулатуры), пре-коллекторами (некоторые гладкие мышцы и случайные клапаны) и коллекторами (непрерывная базальная мембрана и слой гладких мышц, клапаны присутствуют).Рисунок основан на информации из O’Morchoe and O’Morchoe (1988) и Seeger et al. (2012).
Сравнительная почечная лимфатическая анатомия
Почечные лимфатические узлы у позвоночных, не являющихся млекопитающими
Лимфатическая система, вероятно, эволюционировала примерно в то время, когда водные организмы переселились на сушу, поскольку у рыб нет хорошо развитой лимфатической системы, но есть у земноводных (Brown, 2005). У рептилий, многих земноводных и эмбрионов птиц есть лимфатические «сердца», которые помогают движению лимфы. Это пульсирующие камеры, расположенные в точках входа лимфатических сосудов в вены.Они сильно различаются по толщине стенок, содержат клапан и бьются независимо от сердечного ритма (Satoh and Nitatori, 1980). Почки рыб и бесхвостых амфибий играют вспомогательную роль в качестве лимфоидного органа, тогда как почки амниотов становятся менее важными (Manning, 1979). В целом, отчеты о почечной анатомии рептилий (например, Davis et al., 1976) и птиц (например, Morild et al., 1985) не упоминают почечную лимфатическую систему.
Почечная лимфатическая анатомия млекопитающих
Большинство исследований по анатомии лимфатической системы почек проводилось на млекопитающих, особенно на собаках.В плодотворном исследовании Пирс (1944) вводил в почки собак, кроликов и морских свинок тушь, а также вводил внутривенно триптановый синий, чтобы очертить почечные лимфатические сосуды под микроскопом. Он обнаружил, что почечные лимфатические сосуды начинаются в коре головного мозга как внутрилобулярных лимфатических узлов , которые представляют собой разреженные трубки с слепым концом в непосредственной близости от почечных канальцев. Они проходят близко к почечному тельцу, но не входят в него, прежде чем присоединиться к межлобулярным лимфатическим сосудам , которые соединяются с более крупными дугообразными лимфатическими сосудами и междолевыми лимфатическими сосудами .Затем они стекают в прикорневую лимфатическую систему (рис. 1). Из почечной капсулы у собаки выходят 6–8 внутригрудных лимфатических и 4–6 лимфатических каналов (Cockett, 1977). Капсульные лимфатические сосуды после выхода из капсулы, по-видимому, соединяются с внутригрудными лимфатическими сосудами в почечном синусе и воротах (Yazdani et al., 2014). Общий объем корковой лимфы в почках собаки приблизительно эквивалентен только 1% объема крови в кортикальных перитубулярных капиллярах (O’Morchoe and Albertine, 1980).
Анатомия у разных видов очень похожа, за некоторыми исключениями; в почках кролика отсутствует внутрилобулярная лимфатическая система (O’Morchoe and O’Morchoe, 1988), а в почках овцы отсутствует капсульная система (McIntosh and Morris, 1971) (Таблица 1).Виды с наименее развитой внутрикортикальной лимфатической системой (кролик) имеют самую низкую концентрирующую способность мочи, а виды с самой обширной системой (золотой хомяк) имеют самую высокую концентрирующую способность (Niiro et al., 1986).
Таблица 1. Сравнение почечной лимфатической анатомии между видами.
Почечная лимфатическая анатомия человека
Базовая анатомия почечной лимфатической системы млекопитающих, описанная выше, аналогична анатомии человека (рис. 1).Это было показано с помощью микроскопии при вскрытии (Rawson, 1949) или рентгенографических исследований (Cuttino et al., 1989) и подтверждено с помощью маркеров LEC. Ishikawa et al. (2006), используя антитело к подопланину (рис. 2), изучили нормальную ткань почек человека, полученную при вскрытии, и подтвердили, что лимфатические сосуды наиболее многочисленны в интерстиции, окружающей междольковые, дугообразные и междолевые артерии и вены.
Рисунок 2. D2-40 Иммуноокрашивание лимфатических сосудов нормальной почки. (a) Лимфатические капилляры в интерстиции вокруг клубочка, (b) лимфатические сосуды, имеющие щелевидную структуру, распределены вокруг междольковой артерии и вены в коре головного мозга, (c) множественные лимфатические капилляры в интерстиции вокруг расширенная междольковая вена, несколько лимфатических капилляров присутствуют сразу под венозным эндотелием, (d) лимфатический капилляр виден в центре рисунка, показывая нормальный мозговой слой.Воспроизведено с разрешения Ishikawa et al. (2006).
Из левой почки лимфатические сосуды входят в преаортальные, парааортальные и ретроаортальные лимфатические узлы, а из правой почки — в паракавальные, прекавальные, ретрокавальные и межортокавальные лимфатические узлы (Karmali et al., 2014). Обе почки также отправляют лимфатические сосуды кзади от аорты, которые могут перемещаться непосредственно в грудной проток (Assouad et al., 2006). Поверхность верхнего полюса может также стекать через диафрагму в лимфатические узлы заднего средостения.Почечные лимфатические сосуды могут достигать очень отдаленных узлов, но всегда в конечном итоге соединяются с источником грудного протока, обычно через хилую цистерну (Assouad et al., 2006) (Рисунок 1).
Конечный грудной проток по-разному отводится в левую внутреннюю или внешнюю яремную вену, левую подключичную вену или венозный угол (Ratnayake et al., 2018). В этом месте находится устьевой клапан, который предотвращает обратный ток венозной крови (Ratnayake et al., 2018).
Подробные характеристики почечной лимфатической анатомии человека и млекопитающих
Связь между внутрипочечными и капсульными лимфатическими узлами
Пирс (1944) обнаружил связь между кортикальными и капсульными / периренальными лимфатическими сосудами у собак, предполагая, что лимфа может покидать почку альтернативным путем, а не через почечные ворота.Синий краситель Эванса, введенный в паренхиму почек, появляется в внутригрудных или капсульных лимфатических сосудах, или в обоих (Sugarman et al., 1942). Эта лимфатическая связь была подтверждена у других видов (Bell et al., 1968; O’Morchoe, 1985), включая людей (Rawson, 1949), и недавно с использованием маркеров LEC (Seeger et al., 2012), но Kaiserling (1940) ) не удалось обнаружить эту коммуникацию у кроликов.
Holmes et al. (1977a) описали два набора соединительных лимфатических сосудов у собак, которые различаются в зависимости от того, где они проникают в капсулу (рис. 1).Первые — это перфорирующих лимфатических узлов, , которых большинство. Они проникают в капсулу в любой точке самостоятельно или с помощью небольшой вены из субкапсулярного сплетения. Они образуют первичный путь для лимфы из самых поверхностных частей коры, в отличие от внутригрудного пути (внутригрудный путь является основным путем для большей части почечной лимфы). Вторые — это сообщающиеся лимфатические сосуды , которые образуют основное связующее звено между внутригрудной и капсульной системами. Они являются продолжением межлобулярных лимфатических сосудов и тесно связаны с редкими межлобулярными артериями и венами, которые проникают в капсулу.Было обнаружено, что каждая почка содержит только 5–10 междольковых артерий, которые проникают в капсулу таким образом, и из них 60% сопровождаются сообщающейся лимфатической. Там, где он пробивал капсулу, лимфатический сосуд был единичным, но с обеих сторон капсулы он быстро разветвлялся, образуя либо межлобулярное лимфатическое сплетение, либо капсульное сплетение. Отличные гистологические срезы сообщающихся и перфорирующих лимфатических сосудов у собаки см. В Holmes et al. (1977a).
Медуллярная лимфатическая система
Пирс (1944) не обнаружил доказательств наличия мозговых лимфатических сосудов у собак, что согласуется с отсутствием артериального кровоснабжения в мозговом веществе, и пришел к выводу, что их не существует.Начиная с Пирса, в большинстве исследований на животных не удалось обнаружить мозговые лимфатические сосуды. Макинтош и Моррис (1971), используя световую и электронную микроскопию, а также физиологические исследования, не обнаружили никаких доказательств наличия медуллярной лимфатической системы у овец. Bell et al. (1968), Альбертина и О’Морхо (1980) и Элиска (1984) не смогли обнаружить медуллярную лимфатическую систему у собак. В отличие от этих результатов, Cuttino et al. (1985) сообщили о медуллярной лимфатической системе у свиней, Cockett (1977) у собак и Ruszniják et al. (1960) на кроликах.Исследования на животных, изучающие содержание почечной лимфы, показали, что мозговая интерстициальная жидкость должна вносить вклад в внутрикорпусную лимфу (Keyl et al., 1972), предполагая наличие мозговых лимфатических сосудов. Однако движение жидкости внутри мозгового интерстиция к юкстамедуллярным лимфатическим сосудам (в коре) также может вызвать этот результат (Albertine и O’Morchoe, 1980; O’Morchoe and O’Morchoe, 1988).
Rawson (1949) картировал лимфатическое распределение в образце вскрытия почек человека. Образец взят от пациента с карциномой желудка, которая ретроградно метастазировала в почечные лимфатические сосуды.Это расширило лимфатические сосуды и сделало их видимыми под микроскопом. Он пришел к выводу, что почечная лимфатическая система начинается вслепую в двух областях; рядом с капсулой Боумена в коре головного мозга и под слизистой оболочкой сосочка в мозговом веществе. Те, что находятся в коре, стекают вниз к дугообразным сосудам, а те, что в мозговом веществе, стекают, чтобы встретить их. Выводы Роусона были противоречивыми из-за наличия рака в почечных лимфатических сосудах, и недавние обзорные статьи не основывались на его работе, а вместо этого предполагали, основываясь на исследованиях на животных, что лимфатические сосуды отсутствуют в нормальном мозговом веществе почек человека (Lee et al. al., 2011; Seeger et al., 2012). Однако Ishikawa et al. (2006) обнаружили мозговые лимфатические сосуды в нормальной почечной ткани человека в четырех из десяти случаев (рис. 2), но только вблизи коры головного мозга, при этом ничего не было обнаружено в центральной области продолговатого мозга.
Клубочковые и тубулярные лимфатические узлы
Bell et al. (1968) обнаружили многочисленные мелкие лимфатические сосуды, тесно связанные с клубочками, но ни один из них не проникал в клубочки. Эти суда либо полностью (лошадь), либо частично (собака) окружали капсулу Боумена.Элиска (1984) смогла обнаружить редкие и очень маленькие лимфатические сосуды рядом с канальцами между междольковыми артериями и отметила, что лимфатические сосуды, окружающие клубочки, становятся более редкими по мере удаления от междольковой артерии. Ishikawa et al. (2006) подтвердили, что лимфатические капилляры спорадически окружают клубочки у людей, но не проникают в них (рис. 2).
Клапаны
Двустворчатые клапаны видны в преколлекторных (дугообразных и междолевых лимфатических сосудах) и собирающих (прикорневых) лимфатических сосудах и способствуют однонаправленному потоку к воротам ворот и лимфатическим узлам аорты (Seeger et al., 2012) (рисунок 1). Для сообщающихся и перфорирующих лимфатических сосудов часто присутствует единственный клапан, когда они пересекают капсулу, ориентированные таким образом, чтобы предотвратить обратный поток с поверхности в почечную паренхиму (Holmes et al., 1977a). Эти клапаны переходят в капсульные лимфатические сосуды и там многочисленны. В межлобулярных лимфатических сосудах клапаны отсутствуют (Holmes et al., 1977a). Таким образом, лимфа, образующаяся в коре головного мозга, может выходить из почки в любом направлении.
Почечный интерстиций
Почечный интерстиций определяется как межтрубное, экстрагломерулярное, внесосудистое пространство почки (Zeisberg and Kalluri, 2015).Он со всех сторон связан трубчатой и базальной мембранами сосудов. Кортикальный почечный интерстиций делится на (а) перитубулярный интерстиций, (б) периартериальный интерстиций и (в) клубочковый и внегломерулярный мезангиум (Lemley and Kriz, 1991). Лимфатические сосуды находятся в периартериальном интерстиции, который представляет собой богатую жидкостью рыхлую соединительнотканную оболочку. Он виден вокруг афферентных артериол и более крупных артерий, но менее выражен в эфферентных артериолах и трубчатых капиллярах.
Морфология почечных лимфатических сосудов
Почечные лимфатические капилляры считаются частью интерстиция, поскольку у них отсутствует базальная мембрана.Они отличаются от кровеносных сосудов тем, что имеют слепые окончания и не имеют перицитов. LEC капилляров представляют собой однослойные, частично перекрывающиеся клетки в форме «дубового листа», соединенные между собой посредством прерывисто расположенных «пуговичных» соединений, которые приводят к межперепадным промежуткам (Seeger et al., 2012). Эти соединения состоят из сосудистого эндотелиального кадгерина (VE-cadherin) и различных белков, связанных с плотными контактами (например, окклюдина, zonula occludens-1) (Baluk et al., 2007). LEC связаны с периваскулярным матриксом нитями.Такое расположение приводит к увеличению диаметра просвета сосуда и ширине межклеточных промежутков при наличии отека тканей, что облегчает поступление жидкости (Seeger et al., 2012). Преколлекторы (дугообразные и междолевые лимфатические сосуды) демонстрируют некоторые периваскулярные гладкомышечные клетки, а коллекторы (внутригрудные лимфатические сосуды) содержат непрерывные эндотелиальные соединения, базальную мембрану и слой гладкомышечных клеток (рис. 1). Лимфатические сосуды обычно транспортируют лимфу посредством как внешней перекачки, вторичной по отношению к силам окружающих тканей, так и внутренней перекачки через эти гладкомышечные клетки, причем последняя, вероятно, преобладает в почечных лимфатических сосудах (Zawieja, 2009).
Связь с артериями и венами
Ishikawa et al. (2006) показали, что у людей лимфатические сосуды вокруг междольковых вен были более развиты, чем лимфатические сосуды вокруг междольковых артерий. Они увидели обильное количество лимфатических сосудов в интерстиции вокруг междолевых артерий, но отметили, что лимфатические сосуды, окружающие междолевые вены, были распределены не только в интерстиции, но и в самой стенке, как в средах, так и в интиме непосредственно под эндотелием. Хотя лимфатические сосуды проходят близко к почечным сосудам, Элиска (1984) и другие не смогли обнаружить какие-либо анатомические внутрипочечные лимфо-венозные шунты.Однако лимфовенозные коммуникации наблюдались на уровне почечной вены у крыс и приматов, но не в исследованиях аутопсии человека (Karmali et al., 2014).
Краткое изложение лимфатической анатомии почек человека
Почечно-лимфатическая анатомия человека имеет ту же общую структуру, что и другие млекопитающие. Лимфатические капилляры с слепым концом начинаются около почечных канальцев, проходят рядом с клубочком и затем следуют по почечным артериям в виде междольковых, дугообразных и междолевых лимфатических сосудов. В коре межлобулярные лимфатические сосуды не имеют клапанов, поэтому лимфа может перемещаться по основному маршруту к воротам или к капсульному лимфатическому сплетению, проникая в капсулу.Таким образом, лимфа может выходить из почки двумя разными путями. Лимфатические капилляры относительно многочисленны в коре головного мозга, но очень редко в мозговом веществе. Они привязаны к окружающему интерстицию, лишены базальной мембраны и имеют межпозиционные промежутки между эндотелиальными клетками. Более крупные дугообразные, междолевые и прикорневые лимфатические узлы имеют клапаны для однонаправленного потока и гладкую мускулатуру для перекачивания лимфы.
Физиология почечной лимфатической системы в нормальных условиях
Методы изучения физиологии лимфатических сосудов почек
Подобно опубликованным исследованиям лимфатической анатомии почек, физиологические исследования в значительной степени полагались на животных.Экспериментально in vivo Образцы почечной лимфы были получены у собак (LeBrie and Mayerson, 1960) и крыс (Hargens et al., 1977), но не у людей. Измерение скорости почечного лимфатического кровотока у животных оказалось трудным из-за анатомического расположения лимфатических сосудов в почках, но было достигнуто и будет обсуждаться в соответствующих разделах ниже.
Формирование почечной лимфы
Лимфатические сосуды удаляют жидкость и макромолекулы из интерстициального пространства между канальцами и капиллярами.Лимфа попадает в лимфатические капилляры в соответствии с балансом между гидростатическим и онкотическим давлением в соответствии с уравнением Старлинга (Staub and Taylor, 1984). Все кровеносные капилляры пропускают белки в интерстиций, особенно если присутствуют эндотелиальные фенестрации. В почках фенестрации чаще встречаются на той стороне стенки капилляра, которая обращена к почечному канальцу, поскольку капилляр и канальец лежат близко друг к другу (Pinter, 1988). Следовательно, поскольку повторный захват белков капилляром не завершен, белки плазмы, вероятно, будут накапливаться в узком интерстициальном пространстве между капилляром и канальцем (рис. 3).Если белки, попадающие в интерстиций, не удаляются, важный градиент онкотического давления исчезнет, что приведет к уменьшению потока жидкости и электролитов из канальцев в перитубулярные капилляры (Cockett, 1977; Pinter, 1988). Почки уникальны среди органов тем, что имеют большой внесосудистый пул альбумина, который быстро удаляется и пополняется. Слоткофф и Лилиенфилд (1967) продемонстрировали это путем внутривенного введения собакам радиоактивно меченых эритроцитов и альбумина. Затем они перфузировали почки декстраном (молекулярная масса 75 000) и измерили оставшуюся радиоактивность тканей.Они обнаружили, что большая часть меченого альбумина остается в почках по сравнению с мечеными эритроцитами, и пришли к выводу, что существует значительный внесосудистый пул альбумина. Эта разница была наибольшей в мозговом веществе, где меньше лимфатических сосудов для удаления альбумина. Интерстициальный альбумин в мозговом веществе необходим для способности почек концентрировать мочу. В коре головного мозга удаление интерстициального альбумина является основной функцией лимфатических сосудов, где, как упоминалось выше, градиенты онкотического давления необходимы для канальцевой реабсорбции.
Рис. 3. Схема потоков реабсорбента из почечных канальцев в капилляр и белка из капилляров в лимфу в почечной коре. Фенестрации на стенке капилляра группируются рядом с узкими интерстициальными пространствами между капилляром и канальцем. Лимфа образуется в интерстициальном пространстве и попадает в лимфатические капилляры. Этот механизм не применяется в мозговом веществе, где лимфатические сосуды разрежены, а интерстициальная жидкость и макромолекулы попадают в прямую вазу.Рисунок основан на информации Пинтера (1988).
Интерстициальная жидкость и белки свободно поступают в конечные лимфатические сосуды по градиентам гидростатического и онкотического давления. Давление в интерстициальной жидкости почек положительное, в отличие от давления подкожной ткани или мышц, что приводит к относительно высокому нормальному лимфотоку (Ott and Knox, 1976). Проникновение в лимфатические сосуды происходит в основном через межпозиционные промежутки между LEC, но эти эндотелиальные клетки обладают высокой эндоцитарной способностью и также участвуют в трансклеточном поглощении жидкости и макромолекул (Seeger et al., 2012). Проникновение также облегчается связующими нитями и отсутствием базальной мембраны. Нити соединяют LEC с окружающим периваскулярным матриксом и, следовательно, увеличивают размер межэндотелиальных промежутков, когда ткань отечна. Состав лимфы в конечных лимфатических сосудах почти такой же, как и в интерстициальной жидкости, из которой она получена.
Формирование и поток капсулярной лимфы по сравнению с лимфой внутрикрудного канала
Лимфа из самой внешней части коры головного мозга в основном отводится через капсульные лимфатические сосуды, в отличие от лимфы из продолговатого мозга и остальной части коры, которая в основном отводится через прикорневые лимфатические сосуды (O’Morchoe et al., 1975). Хотя большая часть почечной лимфы образуется в коре головного мозга, скорость оттока из лимфатической системы коры головного мозга была измерена в 4-8 раз больше, чем лимфатическая система в капсулах (Keyl et al., 1965), что позволяет предположить, что большая часть лимфы из коры головного мозга отводится через внутрикорпусные, а не капсульные лимфатические сосуды. . Об этом также свидетельствует тот факт, что электролитный состав внутригрудной лимфы очень похож на плазму, потому что электролитный состав кортикального интерстиция (где образуется большая часть внутригрудной лимфы) также очень похож на плазму.Эти растворенные вещества обнаруживаются в высоких концентрациях в интерстиции мозгового вещества (из-за требований противоточного механизма для концентрирования мочи), и почечная внутрикорпусная лимфа отражала бы эти концентрации, если бы она главным образом дренировала мозговое вещество (Keyl et al., 1965).
Состав почечной лимфы в нормальных условиях
Почечная лимфа образуется из капиллярного фильтрата и реабсорбата канальцев
Исследования подтвердили, что почечная лимфа образуется как из капиллярного фильтрата, так и из реабсорбата канальцев (Bell and Lowsitisukdi, 1983; Bell, 1984).Каплан и др. (1942) вводили собакам инулин внутривенно и обнаружили соотношение почечного инулина, лимфа / артериальная плазма, равное 0,68. Если почечная лимфа получена исключительно из реабсорбции почечных канальцев, содержание инулина в лимфатической системе будет близко к нулю, поскольку инулин не реабсорбируется. В других исследованиях было обнаружено, что соотношение лимфа / плазма составляет 0,80 для инулина (Keyl et al., 1965), 0,78 для креатинина (Cockett et al., 1969) и 0,58 для пара-аминогиппурата (PAH) (Keyl et al., 1965). . Смешанный источник почечной лимфы также можно показать, измерив соотношение меченой глюкозы (реабсорбированной проксимальным канальцем) и маннита (не реабсорбированной) в почечной лимфе по сравнению с плазмой (Cook et al., 1982). Меченая глюкоза появляется в почечной лимфе в большей пропорции по сравнению с маннитом после реабсорбции из проксимальных канальцев, что указывает на то, что реабсорбция канальцев способствует образованию почечной лимфы.
Если почечная лимфа была получена исключительно из капиллярного фильтрата, то ее электролитный состав был бы идентичен плазме (Cockett, 1977), и хотя биохимия почечной лимфы действительно похожа на плазму, она не идентична. ЛеБри и Майерсон (1959) обнаружили, что капсульная лимфа имеет 11.На 3 и 26,9% выше концентрации Na + и Cl — соответственно по сравнению с плазмой. Они пришли к выводу, что дистальный каналец способен реабсорбировать растворенное вещество независимо от воды, и этот концентрированный раствор Na + и Cl — смешивается с капиллярным фильтратом для образования почечной лимфы. Это не было подтверждено Майерсоном (1963), который предположил, что содержание натрия было ошибочно высоким и незначительным. В других исследованиях были обнаружены аналогичные концентрации Na + , K + , Mg 2+ , осмоляльность и pH в плазме и почечной лимфе (Swann et al., 1958; ЛеБри и Майерсон, 1959; Кейл и др., 1965). Концентрация мочевины в почечной лимфе варьируется между исследованиями, с соотношением лимфа / плазма 1,4 (Swann et al., 1958), 1,3 (Sugarman et al., 1942) и 0,89 (Keyl et al., 1965), и это расхождение может представлять различие в методологиях. Кейл и др. (1965) предположили, что повышенное соотношение лимфа / плазма мочевины происходит из-за пережатия капсульных лимфатических сосудов с целью их набухания для канюляции. Это нарушает нормальный почечный лимфодренаж, что приводит к изменению содержания интерстициальной мочевины.Все эти исследования предполагают, что капиллярный фильтрат, а не реабсорбция канальцев, является основным источником почечной лимфы.
Почечные лимфатические белки
Концентрация белка в почечной лимфе сильно различается и составляет 20% (крыса) (Hargens et al., 1977), 34% (собака) (Keyl et al., 1965), 49% (собака) (Atkins et al. ., 1988), 50% (собака) (ЛеБри и Майерсон, 1960), 60% (собака) (ЛеБри и Майерсон, 1959) и 66% (собака) (Генри и др., 1969) системных уровней в плазме, и 70% уровней лимфы грудного протока (LeBrie and Mayerson, 1959).Содержание белка в почечной лимфе зависит от скорости потока (Sugarman et al., 1942; LeBrie and Mayerson, 1960; Bell, 1985), при этом более низкая концентрация белка связана с увеличением скорости лимфотока. Это также зависит от того, анестезировано животное или нет, с более высокой концентрацией белка при анестезии, хотя механизм этого неизвестен (Henry et al., 1969).
ЛеБри и Майерсон (1959, 1960) не обнаружили различий в относительных пропорциях различных белков (альбумин, альфа-1, альфа-2, бета и гамма-глобулины) между почечной лимфой и плазмой, но другие обнаружили большую долю альбумина и альфа-глобулинов. в лимфе (Swann et al., 1958; Кейл и др., 1965; Hargens et al., 1977). Почечный лимфатический клиренс альбумина был рассчитан как довольно высокий (0,16 см 3 / мин / 100 г почки), что согласуется с относительно высокой проницаемостью почечных капилляров (Atkins et al., 1988) и высокими уровнями интерстициальный альбумин (Slotkoff, Lilienfield, 1967).
Почечная лимфа содержит относительно высокую концентрацию ренина, который не обнаруживается в лимфе из других органов или в крови почечной вены (Lever and Peart, 1962; Moffat, 1981).Это можно объяснить тем, что лимфатические сосуды расположены в непосредственной близости от юкстагломерулярного аппарата, где ренин синтезируется и действует паракринным образом (Moffat, 1981). Аналогичным образом было обнаружено, что уровни ангиотензина II в почечной лимфе выше, чем в почечных артериальных или венозных пробах у собак (Bailie et al., 1971). Было отмечено, что частичная окклюзия почечной артерии (стеноз почечной артерии) вызывает повышение концентрации ренина в почечной лимфе (Lever and Peart, 1962). Аполипопротеины (в частности, ARP и A-IV), которые предположительно выполняют роль транспорта липидов в почечном интерстиции, также присутствуют в почечной лимфе в относительно высоких концентрациях (Roheim et al., 1976).
Скорость почечного лимфотока в нормальных условиях
Общий почечный лимфоток трудно измерить, потому что почечные лимфатические узлы не сливаются перед входом в периаортальную цепь (Atkins et al., 1988). Различия в экспериментальных измерениях почечного лимфотока отражают эту трудность. Считается, что в нормальных условиях лимфоток представляет собой небольшую часть жидкости, покидающей почку (Goodwin and Kaufman, 1956), но в некоторых сообщениях предполагается, что лимфоток равен потоку мочи в нормальных условиях (Stolarczyk and Carone, 1975).Sugarman et al. (1942) подсчитали, что лимфоток составляет около 2% от реабсорбции жидкости в почках (что примерно соответствует потоку мочи). Cockett (1977) оценивает лимфоток примерно в половину объема потока мочи у собак в исходных условиях. Аткинс и др. (1988) рассчитали средний общий почечный лимфоток 0,36 мл / мин на 100 г почки, при этом каждая почка обеспечивает 21% оттока грудного протока у голодных собак. Авторы приписывают такую высокую ценность тому факту, что животные голодали и, как ожидается, у них будет низкий поток хиловых цистерн (Аткинс и др., 1988).
Дренаж интерстициальной жидкости и белка в продолговатом мозге
В отличие от коры, рециркуляция интерстициальной жидкости и белков из мозгового вещества происходит не через лимфатические сосуды. Вместо распространения в кортико-медуллярные лимфатические сосуды они в основном удаляются через прямую вазу. Tenstad et al. (2001) показали это путем введения меченого альбумина во внутренний мозг почек крысы и обнаружили, что он сначала появился в плазме, а не в лимфе. Напротив, альбумин, введенный в кору головного мозга, сначала был замечен в лимфе грудного протока.Перенос в прямую вазу, вероятно, происходит из-за конвективного потока, где белки перемещаются вместе с жидкостью. Медуллярная жидкость движется вниз по градиенту концентрации из собирательных каналов в интерстиций, а затем в прямую вазу. Этот процесс можно объяснить с помощью математических моделей (Wang, Michel, 2000). Tenstad et al. (2001) пришли к выводу, что, подобно мозгу, роговице и костному мозгу, «лимфатические сосуды во внутреннем мозговом веществе просто не нужны».
Физиология почечной лимфатической системы при патологических состояниях
Состав почечной лимфы при патологических состояниях
Электролиты
LeBrie и Mayerson (1960) изучали состав почечной лимфы после частичной окклюзии нижней полой вены (имитирующей правожелудочковую недостаточность).Они не обнаружили изменений в концентрации Na + и Cl —, хотя общий лимфатический поток (и, следовательно, общее содержание Na + и Cl —) увеличился. Обильный диурез вызывает снижение концентраций Na + и Cl — в почечной лимфе, изменение, на которое не влияют исходные концентрации электролитов в плазме (O’Morchoe et al., 1970; O’Morchoe et al., 1978).
Белки
Повышенное венозное давление (с 22 до 30–35 см вод. Ст. 2 O у собак) вызывает заметно непропорциональное повышение содержания лимфатического белка в почках (LeBrie and Mayerson, 1960).Считается, что это происходит из-за увеличения потери капиллярного белка при повышении венозного давления до этого уровня (LeBrie and Mayerson, 1960). Содержание белка в почечной лимфе снижается во время диуреза, что является прямым результатом увеличения скорости лимфатического потока (LeBrie, 1968).
Роль лимфатических сосудов в жидкостной экономике почек
Функция «предохранительного клапана» лимфатических сосудов почек
Три пути, по которым жидкость может покидать почки, — это венозный, мочеточниковый и лимфатический. Эти три системы связаны друг с другом и действуют взаимно (Katz and Cockett, 1959).Обструкция как верхнего мочеточника, так и почечной вены приводит к увеличению давления и потока лимфы в почках, а перевязка лимфатических сосудов приводит к увеличению оттока мочи (Cockett, 1977). Лимфатическая система действует как механизм «предохранительного клапана», защищающий почки от высокого внутрипочечного давления, например, при повышенном IRVP или гидронефрозе (Goodwin and Kaufman, 1956).
Почечный лимфоток во время диуреза
Шмидт и Хейман (1929) обнаружили, что несоответствие между почечным артериальным и венозным током во время обильного диуреза у собак не полностью объясняется производством мочи, и пришли к выводу, что оставшаяся часть покидает почки через лимфатические сосуды.Они показали, что почка во время диуреза была способна производить значительное количество лимфы. O’Morchoe et al. (1970) обнаружили усиление лимфотока при диурезе маннитом, но не мерсалилом или фуросемидом. Они пришли к выводу, что влияние маннита на лимфоток было связано с общим увеличением интерстициальной жидкости, а не с какими-либо специфическими внутрипочечными последствиями самого диуреза.
Почечный лимфоток при повышенном венозном давлении
Повышение системного венозного давления вызывает уменьшение потока мочи и концентрации натрия в моче, однако это, вероятно, связано с изменениями почечного кровотока, что приводит к снижению скорости клубочковой фильтрации (СКФ), а не прямым следствием венозного давления ( ЛеБри и Майерсон, 1960).
Повышенное системное венозное давление вызывает увеличение почечного лимфотока. Кац (1958) измерял давление капсульных лимфатических сосудов у собак во время окклюзии почечной вены или мочеточника. Лимфатическое давление начало резко повышаться через 5 с после окклюзии почечной вены и снизилось через 7 с после его сброса (рис. 4). Повышению интерстициального давления предшествовало повышение лимфатического давления. Эти изменения также произошли при частичной окклюзии почечной вены, — ситуации, напоминающей повышенное венозное давление, наблюдаемое при сердечной недостаточности.LeBrie и Mayerson (1960) подсчитали, что почечный лимфоток увеличивался до 2400 мл / 24 ч от обеих почек в условиях частичной окклюзии нижней полой вены (НПВ). Это составляет объем в 3–4 раза больше, чем объем плазмы у собаки весом 15 кг.
Рис. 4. (вверху) Влияние компрессии почечной вены на лимфатическое давление в капсуле почек у собаки. Обратите внимание, что повышение давления происходит через 5 с после сдавления почечной вены. (внизу) Влияние окклюзии мочеточника на капсульное лимфатическое давление у собаки.Мочеточник оставался зажатым на протяжении всего периода времени, указанного на графике. Внезапное падение давления примерно через 33 минуты наблюдалось, когда почка была очень напряжена и, вероятно, из-за закупорки лимфатических сосудов в месте их выхода из почки. Адаптировано с разрешения Каца (1958).
IRVP и объем интерстициальной жидкости являются основными движущими силами образования почечной лимфы (Bell et al., 1972, 1974; Keyl et al., 1972). Зажатие почечной артерии вызывает снижение капсулярного лимфатического давления, что отражает снижение IRVP и тканевого давления (Рисунок 5) (Bell et al., 1972). IRVP быстро восстанавливается, когда артерия не пережата; однако давление тканей и лимфатическое давление восстанавливаются медленнее. Bell et al. (1972) предположили, что давление ткани было результатом объема интерстициальной жидкости, который необходимо было восполнить после того, как артерия была разжата. Эти эксперименты актуальны для пациентов с тяжелым острым заболеванием, у которых плохая почечная перфузия (например, сердечно-сосудистый шок). Однако почечное лимфатическое и тканевое давление сохраняется даже при сниженном почечном кровотоке до тех пор, пока не снижается венозное давление, что показывает, что IRVP является основным фактором производства почечной лимфы (Bell et al., 1974).
Рисунок 5. Изменения капсулярного лимфатического давления (LcP), внутрипочечного венозного давления (IRVP) и тканевого давления (TP) до, во время и после 60-секундной окклюзии почечной артерии. Адаптировано с разрешения Bell et al. (1972).
Почечный лимфоток при гидронефрозе
Гидронефроз также вызывает увеличение почечного лимфатического потока (Goodwin and Kaufman, 1956). Однако повышение лимфатического давления происходит более постепенно после окклюзии мочеточника по сравнению с окклюзией почечной вены (Katz, 1958) (рис. 4).Bell et al. (1974) отметили, что давление в лоханке почек относительно неэффективно для увеличения лимфатического давления и кровотока в условиях пониженного почечного кровотока. Следовательно, увеличение лимфатического давления и потока, наблюдаемое при повышении тазового давления, вероятно, на самом деле связано с внутрипочечной венозной обструкцией, вторичной по отношению к повышенному тазовому давлению. Было обнаружено, что повышенное тазовое давление препятствует венозному оттоку из почки из-за интимной внутрипочечной анатомической взаимосвязи между почечными венами и лоханкой (Keyl et al., 1972; Holmes et al., 1977b). У собак обструкция мочеточника приводит к отведению внутригрудной лимфы в капсульную лимфу в течение 3 дней из-за сдавления прикорневых лимфатических сосудов в почечном синусе растянутой почечной лоханкой (Holmes et al., 1977b).
На рис. 4 показано внезапное снижение капсулярного лимфатического давления, когда почка была заметно напряжена. Автор пришел к выводу, что это произошло из-за окклюзии капсульных лимфатических сосудов на выходе из почки. Это демонстрирует способ, которым капсульные почечные лимфатические сосуды могут не работать при отечной почке.Предположительно, это могло бы привести к ухудшению отека почек и почечной функции, хотя авторы не исследовали это дальше (Katz, 1958).
Пиелолимфатический противоток
Еще одним объяснением увеличенного почечного лимфотока, наблюдаемого при гидронефрозе, является пиелолимфатический обратный ток. Это было показано экспериментально на свиньях и кроликах и наблюдениями на людях (Morrison, 1929; Narath, 1951; Cuttino et al., 1978; Bidgood et al., 1981). Было замечено, что ретроградная мочеточниковая инъекция контраста под давлением разрывает своды, заполняет интерстиций и дренирует через кортикальные и кортико-медуллярные лимфатические сосуды (Cuttino et al., 1978). Это было изображено как еще одно свидетельство механизма «предохранительного клапана» почечной лимфы (Goodwin and Kaufman, 1956). В отличие от лимфатико-венозных коммуникаций, это не прямая анатомическая связь (если нет патологического свища, например паразитарная хилурия), а, скорее, двухэтапный процесс, при котором жидкость сначала перемещается в интерстиций, а затем в лимфатические сосуды (Goodwin и Кауфман, 1956; Трифут и др., 1987). Важность лимфатического оттока при гидронефрозе также можно увидеть там, где метастатическая обструкция как мочеточника, так и оттока лимфатических сосудов почек приводит к разрыву мочеточника (Fergusson, 1943).О’Морхо и О’Морхо (1988) возражали против действия пиелолимфатического обратного потока, действующего как «предохранительный клапан» при гидронефрозе, ссылаясь на тот факт, что почечная внутрикорпусная лимфа и закупоренная тазовая моча имеют очень разный состав (Holmes et al., 1977b), и разница в составе увеличивается при длительной закупорке, что противоположно тому, что можно было бы предсказать, если бы имел место эффект «предохранительного клапана».
Почечный интерстициальный отек
Сводка различных факторов, которые могут привести к интерстициальному отеку почек, представлена на рисунке 6.Выделение и лигирование лимфатических сосудов почек вызывает интерстициальный отек почек, увеличение размера почек, повышение тканевого давления, диурез и натурез (Kaiserling and Soostmeyer, 1939; Goodwin and Kaufman, 1956; Stolarczyk and Carone, 1975; Wilcox et al. , 1984). Wilcox et al. (1984) показали, что наблюдаемые изменения не были вызваны случайной перевязкой почечного нерва, изменениями почечной гемодинамики (например, СКФ) или изменениями осмолярности.
Рис. 6. Схема, представляющая четыре основных механизма (A – D) , которые способствуют возникновению почечного интерстициального отека. (A) Дисфункция лимфатического оттока. (1) Сжатие капсулы: сообщающиеся и перфорирующие лимфатические сосуды дренируют поверхностную кору при нормальных обстоятельствах, но могут дренировать большую часть почки, если внутригрудной путь затруднен. Эти лимфатические сосуды могут быть заблокированы механическим сдавливанием напряженной почечной капсулой из-за почечного интерстициального отека (см. Почечный лимфоток во время гидронефроза и рисунок 4). (2) Обструкция лимфатического оттока: лимфатические сосуды, дренирующие почку в воротах, могут быть заблокированы экспериментально или клинически из-за метастатического заболевания, или могут быть удалены во время трансплантации почки, что вызывает эффективную обструкцию оттока (см. Интерстициальный отек почек и Постпочечная трансплантация). .(3) Центральная венозная гипертензия: повышенное давление в подключичной вене может препятствовать эффективному дренажу из грудного протока, что приводит к увеличению почечного лимфатического оттока (см. Застойная сердечная недостаточность). Центральная венозная гипертензия также увеличивает внутрипочечное венозное давление (см. B5 ). (4) Обструкция верхнего мочеточника вызывает растяжение почечной лоханки, которое сдавливает прикорневые вены и лимфатические сосуды, и может вызывать пиелолимфатический отток (см. Почечный лимфоток во время гидронефроза и пиелолимфатический отток). (B) Дисфункция лимфатического притока (лимфатическая перегрузка). (5) Повышенное внутрипочечное венозное давление вызывает увеличение интерстициальной жидкости и лимфатического потока (см. Почечный лимфоток при повышенном венозном давлении). (6) Другие причины лимфатической перегрузки: начальные лимфатические капилляры могут быть переполнены из-за чрезмерного количества интерстициальной жидкости по другим причинам, например, гипопротеинемии (см. Почечный интерстициальный отек). (7) Диурез вызывает усиление лимфатического потока, потому что избыток жидкости в почечных канальцах приводит к тому, что больше жидкости реабсорбируется в интерстициальное пространство (см. Почечный лимфоток во время диуреза). (C) Механическое сжатие внутрипочечных собирающих лимфатических сосудов: они могут быть сдавлены интерстициальным отеком почек из-за нерастяжимости почечной капсулы (см. Связь внутрипочечного давления с почечной лимфатической функцией). (D) Другие причины внутрипочечной лимфатической дисфункции, такие как несостоятельность клапанов (например, первичные лимфатические нарушения) или функциональное сужение (например, лимфангиоспазм) (см. Почечный интерстициальный отек и Первичная почечная лимфатическая дисфункция).Артерии — красным, вены — синим, лимфатические — зеленым.
Goodwin и Kaufman (1956) утверждали, что почечный интерстициальный отек является результатом того, что почечные лимфатические сосуды достигают своей способности уносить интерстициальную жидкость. Они перечисляют факторы, которые могут привести к этому, как (i) механическая обструкция лимфатических сосудов (например, опухоль), (ii) функциональное лимфатическое сужение (например, лимфангиоспазм), (iii) чрезмерный лимфоток (например, гипопротеинемия), или (iv) патологические изменения самих лимфатических сосудов (e.g., первичные лимфатические клапанные нарушения или перерезанные лимфатические сосуды после трансплантации).
Взаимосвязь между почечной лимфатической дисфункцией и функцией почек
Почечная лимфатическая дисфункция, определяемая как нарушение адекватного дренажа, ведущее к почечному интерстициальному отеку, может привести к снижению функции почек из-за изменений давления в инкапсулированной почке (Mullens et al., 2017). Действительно, повышенное давление внутри почечной капсулы приводит к снижению СКФ и почечной перфузии (Jaffee et al., 2018). Федер и Макдональд (1967) измерили функцию почек после обструкции всех лимфатических узлов корня и капсулы у собак. Как и ожидалось, почка стала опухшей и напряженной, а диурез и уровень натрия в моче увеличились. К удивлению, они также обнаружили немного увеличенный клиренс креатинина и п-аминогиппурата в почках с обструкцией. Они предположили, что это происходит из-за ауторегуляции почечного кровотока, когда повышенное тканевое давление вызывает сжатие почечного сосудистого русла и последующую рефлекторную гиперемию.
О’Морхо и О’Морхо (1988) предположили, что не было никаких конкретных доказательств, указывающих на особую взаимозависимую связь между функцией почек и почечной лимфатической системой. Они указали на практическую проблему перекрытия почечных лимфатических узлов без повреждения почечных нервов. Они также подчеркнули тот факт, что в большинстве предыдущих исследований просто изучались поток и состав почечной лимфы в различных условиях (например, диурез, обструкция мочеточника, повышенное почечное венозное давление), и предположили, что все изменения могут быть просто связаны с измененными гемодинамическими эффектами.Они пришли к выводу, что лимфатическая система функционирует в почках, как и в других частях тела, для удаления накопленного белка и жидкости из интерстициальных пространств, но остается неизвестным, какой эффект удаление лимфатической системы оказывает на функцию почек.
Белл и Парри (1974) также не считают, что почечная лимфатическая система оказывает специфическое влияние на функцию почек. В почках собак они лигировали все наблюдаемые внутригрудные лимфатические узлы, а также жировую ткань на обоих полюсах почек, чтобы заблокировать капсульные лимфатические сосуды.В отличие от экспериментов, описанных ранее, ни субкапсулярное давление, ни IRVP не увеличивались после лимфатической перевязки. Кроме того, они повторили эксперимент после частичной обструкции почечной вены и не отметили разницы между лимфатической перевязкой и контролем при повышении IRVP. Они пришли к выводу, что почечные лимфатические сосуды не участвуют в первую очередь в регуляции внутрипочечного давления. Они признали, что перевязка лимфатических сосудов приводит к интерстициальному отеку, но предположили, что это может быть более выражено у кроликов (где отсутствует капсулярная лимфатическая связь), чем у собак.Они предполагают, что гистологические изменения, наблюдаемые при лимфатической перевязке, связаны с накоплением токсических продуктов метаболизма в тканях, а не с изменениями, связанными с давлением. Выводы Белла и Парри, похоже, противоречат другим исследованиям (например, Wilcox et al., 1984), и, возможно, им не удалось перевязать все лимфатические сосуды. Федер и Макдональд (1967) обнаружили, что многие дополнительные лимфатические каналы, которые ранее не распознавались, открылись после лигирования всех наблюдаемых внутригрудных и капсульных лимфатических сосудов у собак.
Связь внутрипочечного давления с почечной лимфатической функцией
Изучая взаимосвязь между почечным венозным давлением, интерстициальным давлением и лимфотоком, Rohn et al. (1996) разработали простую экспериментальную модель на собаках, в которой лимфоток (Q L ) измерялся при различных давлениях оттока (P O ). Исходя из этого, они смогли рассчитать единый источник давления (P L ), проталкивающий почечную лимфу через единичное сопротивление (R L ).Как и ожидалось, они обнаружили более высокий P L при повышении почечного венозного давления. Важно отметить, что они обнаружили плато в соотношении Q L и P O , где не было изменений в потоке лимфы при снижении давления на выходе с 5 до -5 см вод. Ст. 2 О. Это плато расширялось при повышении венозного давления ( до 27,2 см вод. ст. 2 O), так что не было изменений в потоке лимфы при снижении давления на выходе с 20 до -5 см вод. ст. 2 О. Из-за этого расширения в Q L vs.P L , они пришли к выводу, что почечное интерстициальное давление может частично коллапсировать внутрипочечный сбор лимфатических сосудов (не начальных капилляров, лимфатических сосудов, которые привязаны посредством прикрепления нитей к интерстиции), что, в свою очередь, может нарушить лимфоток. Это имеет важное значение, предполагая, что за пределами критической точки интерстициального отека лимфоток не будет увеличиваться, а отек и функция почек значительно ухудшатся. Интересно, что такое же плато наблюдалось в лимфатическом потоке легких у собаки (Drake et al., 1982) и овец (Drake et al., 1985), но эффект был менее заметным. Это может быть отражением менее растяжимой почечной капсулы. Другой важный вывод их статьи заключается в том, что повышенное давление на выходе из почечных лимфатических сосудов (имитирующее повышенное системное венозное давление) значительно снижает почечный лимфоток, что может иметь последствия для пациентов с острым и критическим заболеванием, у которых повышенное центральное венозное давление .
Лимфатическая функция почек при различных болезненных состояниях
Застойная сердечная недостаточность
Застойная сердечная недостаточность (ЗСН) вызывает повышение системного венозного давления, что оказывает множественное воздействие на почечную лимфу.Повышенное венозное давление ложится двойной нагрузкой на почечные лимфатические сосуды, увеличивая постгломерулярную капиллярную фильтрацию и препятствуя оттоку торакальных лимфатических сосудов в шее, что может вызывать эффекты противодавления, уменьшающие отток лимфатических сосудов почек (Drake et al., 1998). Как указывалось ранее, увеличение IRVP приводит к увеличению почечного лимфатического давления и кровотока из-за повышенной капиллярной фильтрации (Dumont et al., 1963). Возможно, нарушение лимфодренажа в шее происходит из-за того, что центральный венозный застой вызывает функциональную обструкцию устьевого клапана грудного протока, хотя в настоящее время это не доказано (Ratnayake et al., 2018). Чрезмерная нагрузка на лимфатические сосуды может привести к нарушению адекватного лимфодренажа (лимфатическая дисфункция). Каттино и др. (1989), изучая анатомию почечной лимфатической системы, обнаружили, что им приходилось использовать образцы вскрытия от пациентов с ХСН, потому что лимфатические сосуды расширились, а клапаны стали некомпетентными. Это был единственный способ ретроградной инъекции внутригрудной лимфатической системы с контрастным веществом и изучение анатомии лимфатических сосудов с использованием методов микрорадиографии. В целом это говорит о том, что почечный лимфодренаж может быть нарушен при ХСН из-за нарушения оттока и недостаточности клапанов.
Почечные лимфатические сосуды также способствуют задержке натрия и ухудшению генерализованного отека при ХСН. Частичная окклюзия НПВ (напоминающая ЗСН) увеличивает почечный лимфоток и содержание Na + , а также снижает уровень Na + в моче и обратный поток (Katz and Cockett, 1959). Считается, что этот механизм способствует задержке натрия и жидкости при ЗСН за счет рециркуляции Na + и жидкости, а не выведения их с мочой. Повышенный почечный лимфатический поток также вымывает интерстициальные белки, что снижает осмотическое давление коллоидов в почечном интерстиции и дополнительно способствует реабсорбции натрия (Mullens et al., 2017).
Было показано, что внешний отток лимфы при повышенном центральном венозном давлении снижает образование отеков без снижения венозного давления в кишечнике (Drake et al., 1998). Это говорит о том, что дренаж наружного грудного протока может иметь терапевтическое воздействие на почки (а также другие органы) при ХСН (Dumont et al., 1963).
Острая травма почек
Клинические проявления ОПН и почечного интерстициального отека тесно и взаимно связаны (Prowle et al., 2010). Почечный интерстициальный отек может быть результатом многих факторов, но особенно связан с почечной лимфатической дисфункцией (рис. 6). Интерстициальный отек почек не только является следствием ОПП (из-за воспаления почек и повышенной проницаемости капилляров), но и сам по себе может привести к ОПП. Поскольку почка инкапсулирована, избыток интерстициальной жидкости приводит к непропорциональному повышению внутрипочечного давления и последующему снижению почечного кровотока и СКФ (Firth et al., 1988). Было показано, что декапсуляция почек снижает частоту ОПП у пациентов с геморрагическим шоком, требующих массивной реанимации (Stone and Fulenwider, 1977).Почечный интерстициальный отек также ухудшает диффузию кислорода и метаболитов за счет увеличения расстояния диффузии (Prowle et al., 2010). Кроме того, в инкапсулированной почке он может сжимать лимфатический дренаж, начиная вязкий цикл, который приводит к ухудшению отека и почечной функции (см. Связь внутрипочечного давления с почечной лимфатической функцией). Все это подчеркивает ключевую роль почечных лимфатических узлов в профилактике как ОПП, так и почечного интерстициального отека.
Многие исследования показали, что почечный венозный застой также является важным фактором развития ОПП и, возможно, даже более важным, чем артериальная недостаточность (Li et al., 2011; Jaffee et al., 2018). Обычно венозный застой приводит к повреждению почек ишемического типа (Jaffee et al., 2018). Почечный венозный застой увеличивает интерстициальную жидкость и почечный лимфатический поток (см. Почечный лимфоток при повышенном венозном давлении). Следовательно, почечная лимфатическая дисфункция, при которой лимфодренаж не удовлетворяет потребности по какой-либо причине, может ухудшить ОПП в условиях венозного застоя (например, сердечная недостаточность, агрессивная жидкостная реанимация, внутрибрюшная гипертензия) (Prowle et al., 2010).
Хроническая почечная недостаточность
Как и в случае ОПН, лимфатические сосуды почек имеют сложное отношение к профилактике, патогенезу и разрешению хронических заболеваний почек (ХБП). Большинство, если не все, ХЗП характеризуются тубулоинтерстициальным воспалением и расширением интерстициального пространства за счет отложения внеклеточного матрикса, что, в свою очередь, приводит к фиброзу (Seeger et al., 2012). Считается, что почечные лимфатические сосуды способствуют развитию самого фиброза (Yazdani et al., 2014). CCL21 конститутивно экспрессируется LEC почек и может привлекать CCR7-положительные фиброциты. Было показано, что блокирование этого пути снижает фиброз почек (Sakai et al., 2006), что позволяет предположить причинную роль почечных лимфатических сосудов в развитии ХЗП.
Почечный интерстициальный отек наблюдается почти при всех ХБП, обычно связанных с тубулоинтерстициальным повреждением и гипопротеинемией, вторичной по отношению к протеинурии (Yazdani et al., 2014). Подобно ОПП, это можно рассматривать как следствие ХБП и один из факторов, способствующих ей.Это происходит из-за нарушения архитектуры ткани, повышенной гидравлической проводимости и ремоделирования интерстициального матрикса (Yazdani et al., 2014). Следовательно, лимфатическая дисфункция может способствовать развитию ХБП по этому механизму. Следовательно, лимфангиогенез активируется при ХБП как попытка разрешения (см. Лимфангиогенез). Необходимы дальнейшие исследования для полного выяснения роли почечных лимфатических сосудов как при ОПП, так и при ХБП.
Постпочечный трансплантат
После трансплантации почки, когда лимфатические сосуды неизбежно разделяются, почка увеличивается в размерах из-за интерстициального отека (Goodwin and Kaufman, 1956).Педерсен и Моррис (1970) изучали этот феномен у овец. Они заметили увеличение производства лимфы в почке после трансплантации, особенно при отторжении трансплантата, и увеличения размера почки можно было бы избежать, если бы почечную лимфу дренировали искусственно. Пересаженные почки демонстрируют активный лимфангиогенез у людей и крыс, а также LEC, которые активно организуют воспалительные узелки посредством экспрессии хемокина CCL21 (Yazdani et al., 2014). В настоящее время неизвестно, является ли лимфангиогенез вредным или полезным для пересаженной почки, и в этой области необходимы дальнейшие исследования (Yazdani et al., 2014).
Лимфангиогенез
Новообразованные лимфатические сосуды (лимфангиогенез) обычно действуют как защита, помогая устранить отек тканей и воспалительные инфильтраты. Почечный лимфангиогенез связан с почечным фиброзом, воспалением и отторжением трансплантата (Kerjaschki et al., 2004; Seeger et al., 2012; Yazdani et al., 2014). При ХБП, таких как диабетическая нефропатия, степень лимфангиогенеза, по-видимому, больше коррелирует с фиброзом, чем с воспалением (Sakamoto et al., 2009). В модели протеинурии крыс лимфангиогенез происходил до притока макрофагов, отложения коллагена и интерстициального фиброза, что указывает на возможную причинную роль в фиброзе (Yazdani et al., 2014). Лимфангиогенез также наблюдается в моделях гидронефроза и гипертензии на крысах (Suzuki et al., 2012; Kneedler et al., 2017). У людей это наблюдается при терминальной стадии почечной недостаточности и почечно-клеточной карциноме (в ткани, окружающей опухоль) (Ishikawa et al., 2006). Это также признак гидронефроза у людей вокруг междолевых и дугообразных сосудов, но не вокруг междольковых сосудов (Ishikawa et al., 2006). Он не обнаруживается в образцах старого или нового инфаркта почек или острого канальцевого некроза (Ishikawa et al., 2006). Терапия, направленная на стимуляцию лимфангиогенеза (например, 9- цис- ретиноевой кислоты), улучшила набухание тканей на животных моделях лимфедемы и также может играть роль в лечении интерстициального отека почек (Choi et al., 2012; Yazdani et al. , 2014). Однако эти методы лечения потенциально могут быть вредными, поскольку лимфатические сосуды транспортируют антигенпрезентирующие клетки к лимфатическим узлам, а LEC могут инициировать иммунные ответы сами по себе (например,г., после трансплантации) (Yazdani et al., 2014).
Долгосрочные эффекты почечной лимфатической перевязки
Долгосрочные эффекты лигирования прикорневых лимфатических сосудов у людей можно увидеть при трансплантации почек, когда лимфатические сосуды донорской почки лигируются (Ranghino et al., 2015). Эти эффекты также наблюдаются после лимфатической перевязки для лечения тяжелой хилурии (Zhuo et al., 2013). Было показано, что человеческая почка может долгое время выжить после лимфатической перевязки, предположительно за счет новых лимфатических связей.Однако истинные последствия этого неизвестны. Zhang et al. (2007a, b) изучали влияние почечной лимфатической перевязки у крыс в течение 8 недель. Они лигировали как внутригрудные, так и капсульные лимфатические сосуды и включали животных, у которых одна почка была перевязана, а другая удалена, чтобы напоминать одну трансплантированную почку. Они обнаружили тяжелую протеинурию через 1 неделю после перевязки, а через 2 недели функция почек начала ухудшаться из-за повышения уровня креатинина в сыворотке и снижения клиренса креатинина. Гистологически почки показали повреждение канальцев, тубулоинтерстициальный фиброз и расширение мезангиума, возможно, из-за усиленной активации сигнального пути TGF-β1 / Smad.Эти изменения ухудшились за 8-недельный период исследования. Лимфатическая перевязка почек также вызывает усиленный апоптоз почечных клеток (Zhang et al., 2009; Cheng et al., 2013). Склероз почечной паренхимы также наблюдался у крыс через 3 месяца после перевязки грудного протока (Умбетов, 1989), хотя в этой ситуации трудно объяснить причину и следствие. Почечный интерстициальный фиброз был замечен и предположительно развивается как следствие неабсорбированного почечного интерстициального отека в ретроспективном долгосрочном исследовании на людях (Wehrmann et al., 1989).
Первичная почечная лимфатическая дисфункция
Первичные лимфатические расстройства разнообразны, и в большинстве зарегистрированных случаев механизм не установлен. При большинстве заболеваний дефекты лимфатических клапанов являются причиной лимфатической дисфункции (Ballard et al., 2018). У этих пациентов обычно наблюдается двусторонняя лимфедема нижних конечностей (например, лимфедема Нонне-Милроя, ранняя лимфедема). В литературе очень мало информации о почечных эффектах этих различных синдромов, но известно, что некоторые из них со временем вызывают почечную недостаточность и структурные дефекты (Northup et al., 2003).
Заключение
Почечной лимфатической системе, несмотря на ее обилие, в последние годы уделялось мало внимания или вообще не уделялось никакого внимания. Начальные лимфатические капилляры (внутрилобулярные лимфатические сосуды) лежат в коре головного мозга, в непосредственной близости от почечных канальцев и клубочков, и дренируют избыток межклеточной жидкости и макромолекул, которые накапливаются в межклеточном пространстве. Они присоединяются к межлобулярным лимфатическим сосудам, которые не имеют клапанов, и оттуда лимфа может следовать по дугообразным и междолевым лимфатическим сосудам к воротам или проникать в капсулу, чтобы присоединиться к капсулярным лимфатическим сосудам.Этот двойной выход из почки может быть полезен при лимфатической обструкции.
Почечная лимфа в основном состоит из капиллярного фильтрата и поэтому образуется в избытке при повышении IRVP, например, при сердечной недостаточности или агрессивной жидкостной реанимации. Другой основной движущей силой образования почечной лимфы является объем интерстициального пространства (и давление), которое может увеличиваться с увеличением проницаемости капилляров (например, воспалением почек или ССВО). Неспособность почечных лимфатических сосудов адекватно отводить интерстициальную жидкость (лимфатическая дисфункция) приводит к почечному интерстициальному отеку.Отек может усугубиться, если почечная капсула становится настолько напряженной, что препятствует проникновению и обмену лимфатических сосудов, когда они выходят из почки через капсулу. Точно так же внутрипочечный лимфатический путь может стать функционально заблокированным, поскольку внутрипочечный отек, и последующие изменения давления вызывают коллапс дугообразных и междолевых лимфатических сосудов. Отсутствие лимфодренажа, таким образом, усугубляет почечный интерстициальный отек в этом инкапсулированном органе, и мы предполагаем, что это может привести к повышению внутрипочечного давления и способствовать нарушению функции почек.Эта относительно неизученная патологическая ось в настоящее время ожидает дальнейшего клинического исследования.
Вклад авторов
JW, AP и MI разработали концепцию рукописи. PR проверил литературу и подготовил рукопись. JH, JW, MI и AP рассмотрели рукопись, отредактировали критически и внесли интеллектуальный вклад.
Финансирование
PR был профинансирован г-жой Лайлой Хэддон через Фонд Медицинской школы Оклендского университета. JH финансировался благотворительным фондом Hugo Charitable Trust.
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Благодарности
Авторы выражают признательность г-же Вивьен Уорд, которая помогла с иллюстрацией фигур.
Сокращения
ОПП, острая травма почек; IRVP — внутрипочечное венозное давление; LEC, лимфатическая эндотелиальная клетка; LYVE-1, рецептор гиалуроновой кислоты 1 лимфатических сосудов; SIRS, синдром системной воспалительной реакции.
Ссылки
Альбертина, К. Х., и О’Морчо, К. К. (1980). Комплексное световое и электронно-микроскопическое исследование существования интрамедуллярных лимфатических сосудов в почках собаки. Лимфология 13, 100–106.
PubMed Аннотация | Google Scholar
Ассуад, Дж., Рике, М., Фуко, К., Хидден, Г., и Дельмас, В. (2006). Почечный лимфатический дренаж и соединения грудных протоков: последствия для распространения рака. Лимфология 39, 26–32.
PubMed Аннотация | Google Scholar
Аткинс, Дж. Л., О’Морчо, К. С. С. и Пинтер, Г. Г. (1988). Общий лимфатический клиренс белка из почечного интерстиция. Contr. Нефрол. 68, 238–244. DOI: 10.1159 / 000416520
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бейли, М. Д., Ректор, Ф. К., и Селдин, Д. У. (1971). Ангиотензин II в плазме артериальных и почечных вен и почечной лимфе у собак. J. Clin. Вкладывать деньги. 50, 119–126.DOI: 10.1172 / JCI106465
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Баллард М., Вольф К. Т., Непящих З., Диксон Дж. Б., Алексеев А. (2018). Исследование влияния морфологии на динамическую функцию лимфатического клапана. Biomech. Модель. Мех. 17, 1343–1356. DOI: 10.1007 / s10237-018-1030-y
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Балук П., Фьюкс Дж., Хашизуме Х., Романо Т., Лашниц Э., Бутц С. и др.(2007). Функционально специализированные соединения между эндотелиальными клетками лимфатических сосудов. J. Exp. Med. 204, 2349–2362. DOI: 10.1084 / jem.20062596
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Белл, Р. Д. (1984). Почечный лимфоток и состав во время диуреза ацетазоламидом и фуросемидом. Лимфология 17, 10–14.
PubMed Аннотация | Google Scholar
Белл, Р. Д. (1985). Изменения постгломерулярной гемодинамики изменяют состав почечной лимфы собак. Microcirc. Лимфатический эндотелий 2, 477–485.
PubMed Аннотация | Google Scholar
Белл, Р. Д., Кейл, М. Дж., Шрейдер, Ф. Р., Джонс, Э. У. и Генри, Л. П. (1968). Почечные лимфатические узлы: внутреннее распределение. Нефрон 5, 454–463. DOI: 10.1159 / 000179655
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Белл Р. Д., Лоуситисукди А. (1983). Почечное лимфообразование у собак при остром расширении ЭКФ. Лимфология 16, 228–232.
PubMed Аннотация | Google Scholar
Белл Р. Д., Синклер Р. Дж. И Кейл М. Дж. (1972). Взаимосвязь почечной гемодинамики, внутрипочечного давления и почечного лимфообразования. Proc. Soc. Exp. Биол. Med. 139, 109–112. DOI: 10.3181 / 00379727-139-36089
CrossRef Полный текст | Google Scholar
Белл Р. Д., Синклер Р. Дж. И Парри В. Л. (1974). Влияние динамики почечной жидкости на давление, поток и состав почечной лимфы. Лимфология 3, 143–148.
PubMed Аннотация | Google Scholar
Бхимджи, С.С., Лесли, С.В. (2018). Анатомия, брюшная полость и таз, почки. Остров сокровищ, Флорида: StatPearls Publishing.
Бидгуд, В. Д., Каттино, Дж. Т., Кларк, Р. Л. и Волберг, Ф. М. (1981). Пиеловенозный и пиелолимфатический обратный ток при ретроградной пиелографии при тромбозе почечных вен. Инвест. Радиол. 16, 13–19. DOI: 10.1097 / 00004424-198101000-00003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ченг, Дж., Wang, J., Liu, Y. T., Zhang, T., Sun, A., Wang, W., et al. (2013). Лимфатическая перевязка почек усугубляет почечную дисфункцию из-за индукции апоптоза эпителиальных клеток канальцев у мононефрэктомированных крыс. Clin. Нефрол. 79, 124–131. DOI: 10.5414 / CN107627
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Чой, И., Ли, С., Чанг, Х. К., Ли, Ю. С., Ким, К. Э., Чой, Д., и др. (2012). 9-цис-ретиноевая кислота способствует лимфангиогенезу и ускоряет регенерацию лимфатических сосудов: терапевтическое значение 9-цис-ретиноевой кислоты при вторичной лимфедеме. Тираж 125, 872–882. DOI: 10.1161 / CIRCULATIONAHA.111.030296
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Кокетт, А.Т.К., Робертс, А.П., и Мур, Р.С. (1969). Доказательства наличия двух внутрипочечных лимфатических сетей. Инвест. Урол. 7, 266–270.
Каттино, Дж. Т., Кларк, Р. Л., Фрид, Ф. А., и Стивенс, П. С. (1978). Микрорадиографическая демонстрация пиелолимфатического обратного тока в почке свиньи. Am. J. Roentgenol. 131, 501–505. DOI: 10.2214 / ajr.131.3.501
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Каттино, Дж. Т., Кларк, Р. Л., и Дженнетт, Дж. К. (1989). Микрорадиографическая демонстрация внутрипочечных микролимфатических путей человека. Урол. Радиол. 11, 83–87. DOI: 10.1007 / BF02926482
CrossRef Полный текст | Google Scholar
Каттино, Дж. Т., Дженнетт, Дж. К., Кларк, Р. Л. и Квок, Л. (1985). Медуллярная лимфатическая система почек: исследования свиней с помощью микрорадиографии, световой и электронной микроскопии. Лимфология 18, 24–30.
PubMed Аннотация | Google Scholar
Дэвис, Л. Э., Шмидт-Нильсен, Б., Столте, Х. и Букман, Л. М. (1976). Анатомия и ультраструктура выделительной системы ящерицы, Sceloporus cyanogenys . J. Morphol. 149, 279–326. DOI: 10.1002 / jmor.10514
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Дрейк Р. Э., Адкок Д. К., Скотт Р. Л. и Гэйбл Дж. К. (1982). Влияние давления оттока на лимфоток из легких собаки. Circ. Res. 50, 865–869. DOI: 10.1161 / 01.RES.50.6.865
CrossRef Полный текст | Google Scholar
Дрейк, Р. Э., Гислер, М., Лайне, Г., Габель, Дж. К., и Хансен, Т. (1985). Влияние давления оттока на лимфоток в легких у неканетизированных овец. J. Appl. Physiol. 58, 70–76. DOI: 10.1152 / jappl.1985.58.1.70
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Дрейк Р. Э., Тиг Р. А. и Гэйбл Дж. К. (1998). Лимфодренаж уменьшает отек кишечника и потерю жидкости. Лимфология 31, 68–73.
PubMed Аннотация | Google Scholar
Дюмон А. Э., Клаусс Р. Х., Рид Г. Э. и Тайс Д. А. (1963). Лимфодренаж у пациентов с застойной сердечной недостаточностью: сравнение с данными при циррозе печени. N. Eng. J. Med. 269, 949–952. DOI: 10.1056 / NEJM1963103126
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Элиска О. (1984). Топография внутрипочечных лимфатических сосудов. Лимфология 17, 135–141.
Google Scholar
Федер, Ф. П., и Макдональд, Д. Ф. (1967). Изменения функции почек, вызванные обструкцией лимфатических узлов. J. Urol. 97, 432–438. DOI: 10.1016 / S0022-5347 (17) 63053-2
CrossRef Полный текст | Google Scholar
Фергюссон, Дж. Д. (1943). Стриктура мочеточника с перинефральной экстравазацией мочи, вызванная метастазами молчащей карциномы желудка. Brit. J. Surg. 31, 283–286. DOI: 10.1002 / bjs.18003112315
CrossRef Полный текст | Google Scholar
Ферт, Дж.Д., Рейн А. Э. и Ледингем Дж. Г. (1988). Повышенное венозное давление: прямая причина задержки натрия почками при отеках? Ланцет 331, 1033–1035.
Google Scholar
Гудвин, У. Э. и Кауфман, Дж. Дж. (1956). Почечные лимфатические узлы I: обзор некоторой соответствующей литературы. Урол. Surv. 6, 305–329.
Google Scholar
Генри, Л. П., Кейл, М. Дж., И Белл, Р. Д. (1969). Поток и концентрация белка капсульной почечной лимфы у собаки в сознании. Am. J. Physiol. 217, 411–413. DOI: 10.1152 / ajplegacy.1969.217.2.411
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Холмс, М. Дж., О’Морчо, П. Дж., И О’Морчо, К. К. (1977a). Морфология внутрипочечной лимфатической системы. Капсульные и внутрикорпоративные коммуникации. Am. J. Anat. 149, 333–352.
PubMed Аннотация | Google Scholar
Холмс, М. Дж., О’Морчо, П. Дж., И О’Морчо, К. К. (1977b). Роль почечной лимфы при гидронефрозе. Инвест. Урол. 15, 215–219.
Google Scholar
Исикава Ю., Акасака Ю., Кигучи Х., Акишима-Фукасава Ю., Хасегава Т., Ито К. и др. (2006). Лимфатическая система почек человека в норме и при патологии. Гистопатология 49, 265–273. DOI: 10.1111 / j.1365-2559.2006.02478.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Иткин М., Надольски Г. Дж. (2018). Современные методы лимфангиографии и вмешательств: текущее состояние и перспективы развития. Cardiovasc. Intervent. Радиол. 41, 366–376. DOI: 10.1007 / s00270-017-1863-2
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Иткин М., Пикколи Д. А., Надольски Г., Рычик Дж., ДеВитт А., Пинто Э. и др. (2017). Белковая энтеропатия у больных с врожденными пороками сердца. J. Am. Coll. Кардиол. 69, 2929–2937. DOI: 10.1016 / j.jacc.2017.04.023
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Джаффи, В., Ходгинс, С., Макги, У. Т. (2018). Отек тканей, баланс жидкости и исходы пациентов при тяжелом сепсисе: обзор систем органов. J. Intens. Care Med. 33, 502–509. DOI: 10.1177 / 0885066617742832
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Кайзерлинг, Х. (1940). Лимфатики и лимфангит почек. Арка Вирхова. F. Путь. Анат. 306, 322–359. DOI: 10.1007 / BF02595100
CrossRef Полный текст
Кайзерлинг, Х., и Соостмейер, Т. (1939). Важность лимфатической системы почек для функции почек. Wiener Kiln. Wochenschr. 52, 1113–1116.
Google Scholar
Каплан А., Фридман М. и Крюгер Х. Э. (1942). Наблюдения за происхождением почечной лимфы. Am. J. Physiol. 138, 553–556. DOI: 10.1152 / ajplegacy.1943.138.3.553
CrossRef Полный текст | Google Scholar
Керьяшки Д., Регеле Х. М., Моосбергер И., Надь-Боярски К., Watschinger, B., Soleiman, A., et al. (2004). Лимфатический неоангиогенез при трансплантации почек человека связан с иммунологически активными лимфоцитарными инфильтратами. J. Am. Soc. Нефрол. 15, 603–612. DOI: 10.1097 / 01.ASN.0000113316.52371.2E
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Кейл М. Дж., Белл Р. Д. и Парри В. Л. (1972). Резюме почечно-лимфатических исследований. Пер. Являюсь. Доц. Генерал Урин. Surg. 64, 140–144.
Google Scholar
Кейл, М.Дж., Скотт, Дж. Б., Дабни, Дж. М., Хэдди, Ф. Дж., Харви, Р. Б., Белл, Р. Д. и др. (1965). Состав почечной прикорневой лимфы собак. Am. J. Physiol. 209, 1031–1033. DOI: 10.1152 / ajplegacy.1965.209.5.1031
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Книдлер, С. К., Филлипс, Л. Е., Хадсон, К. Р., Бекман, К. М., Лопес Гельстон, К. А., Рутковски, Дж. М. и др. (2017). Воспаление и повреждение почек связаны с лимфангиогенезом при гипертонии. Am. J. Physiol. Почечный. Physiol. 312, F861 – F869. DOI: 10.1152 / ajprenal.00679.2016
PubMed Аннотация | CrossRef Полный текст | Google Scholar
ЛеБри, С. Дж., И Майерсон, Х. С. (1959). Состав почечной лимфы и его значение. Proc. Soc. Exp. Биол. Med. 100, 378–380. DOI: 10.3181 / 00379727-100-24633
CrossRef Полный текст | Google Scholar
ЛеБри, С. Дж., И Майерсон, Х. С. (1960). Влияние повышенного венозного давления на поток и состав почечной лимфы. Am. J. Physiol. 198, 1037–1040. DOI: 10.1152 / ajplegacy.1960.198.5.1037
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ли, Х. В., Цинь, Ю. X., Ким, Ю. М., Пак, Э. Ю., Хван, Дж. С., Хо, Г. Х. и др. (2011). Экспрессия лимфатического эндотелия-специфического рецептора гиалуроновой кислоты LYVE-1 в развивающейся почке мыши. Cell Tissue Res. 343, 429–444. DOI: 10.1007 / s00441-010-1098-x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ли, Х., Лю, М., Беджа, Д., Тобурн, К., Габриельсон, К., Ракузен, Л. и др. (2011). Острая почечная венозная обструкция более вредна для почек, чем артериальная окклюзия: значение для мышиных моделей острого повреждения почек. Am. J. Physiol. Renal Physiol. 302, F519 – F525. DOI: 10.1152 / ajprenal.00011.2011
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Масканьи, П. (1787). Vasorum Lymphaticorum Corporis Humani Historic et Ichnographia. Сиена: Паццини Карли.
Майерсон, Х.С. (1963). «Физиологическое значение лимфы» в Справочнике по физиологии № . Тираж 2 , ред. У. Ф. Гамильтон и П. Доу (Балтимор, Мэриленд: Waverly Press), 1035–1073.
Google Scholar
Макинтош, Г. Х., и Моррис, Б. (1971). Лимфатические сосуды почек и образование почечной лимфы. J. Physiol. 214, 365–376. DOI: 10.1113 / jphysiol.1971.sp009438
CrossRef Полный текст | Google Scholar
Моррисон, Д.М. (1929). Пути абсорбции при гидронефрозе; эксперименты с красителями в полностью закупоренном мочеточнике. Br. J. Urol. 1, 30–45. DOI: 10.1111 / j.1464-410X.1929.tb06853.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Mullens, W., Verbrugge, F.H., Nijst, P., and Tang, W.H.W. (2017). Почечная авидность натрия при сердечной недостаточности: от патофизиологии к стратегиям лечения. Eur. Харт J. 38, 1872–1882. DOI: 10.1093 / eurheartj / ehx035
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Нарат, П.А. (1951). Почечный таз и мочеточник. Нью-Йорк, Нью-Йорк: Грун и Страттон.
Google Scholar
Нииро, Г. К., Ярош, Х. М., О’Морчо, П. Дж., И О’Морчо, К. С. С. (1986). Почечная корковая лимфатическая система у крыс, хомяков и кроликов. Am. J. Anat. 177, 21–34. DOI: 10.1002 / aja.1001770104
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Нортап, К. А., Витте, М. Х., и Витте, К. Л. (2003). Синдромная классификация наследственной лимфедемы. Лимфология 36, 162–189.
PubMed Аннотация | Google Scholar
О’Морчо, К.С.С. (1985). «Лимфодренаж почки», в Experimental Biology of the Lymphatic Circulation , ed. М. Дж. Джонстон (Нью-Йорк, Нью-Йорк: Elsevier Biomedical), 261–304.
Google Scholar
О’Морчо, К.С.С., и Альбертина, К.Х. (1980). Почечная корковая лимфатическая система у собак с беспрепятственным оттоком лимфы и мочи. Анат. Рек. 198, 427–438.DOI: 10.1002 / ar.1091980305
PubMed Аннотация | CrossRef Полный текст | Google Scholar
О’Морчо, К.С.С., и О’Морчо, П.Дж. (1988). Почечная лимфатическая система: краткий обзор. Contr. Нефрол. 68, 230–237. DOI: 10.1159 / 000416519
CrossRef Полный текст | Google Scholar
О’Морчо, К.С.С., О’Морчо, П.Дж. и Донати, Э.Дж. (1975). Сравнение внутригрудной и капсульной почечной лимфы. Am. J. Physiol. 229, 416–421. DOI: 10.1152 / ajplegacy.1975.229.2.416
PubMed Аннотация | CrossRef Полный текст | Google Scholar
О’Морчо, К.С.С., О’Морчо, П.Дж. и Хини, Н.М. (1970). Почечная внутрикорпусная лимфа: влияние диуреза на кровоток и состав у собак. Circ. Res. 26, 469–479. DOI: 10.1161 / 01.RES.26.4.469
PubMed Аннотация | CrossRef Полный текст | Google Scholar
О’Морчо, К.С.С., О’Морчо, П.Дж., Холмс, М.Дж. и Ярош, Х.М. (1978). Поток и состав почечной прикорневой лимфы во время увеличения объема и диуреза солевым раствором. Лимфология 11, 27–31.
PubMed Аннотация | Google Scholar
Отт, К. Э., и Нокс, Ф. Г. (1976). Тканевое давление и динамика жидкости в почках. Fed. Proc. 35, 1872–1875.
Google Scholar
Педерсен, Н.С., и Моррис, Б. (1970). Роль лимфатической системы в отторжении гомотрансплантатов: исследование лимфы из почечных трансплантатов. J. Exp. Med. 131, 936–969. DOI: 10.1084 / jem.131.5.936
CrossRef Полный текст | Google Scholar
Пинтер, Г.Г. (1988). Почечная лимфа: жизненно важна для почек и ценна для физиолога. Physiol. 3, 189–193. DOI: 10.1152 / Physiologyonline.1988.3.5.189
CrossRef Полный текст | Google Scholar
Проул, Дж. Р., Эчеверри, Дж. Э., Лигабо, В., Ронко, К., и Белломо, Р. (2010). Баланс жидкости и острое повреждение почек. Nat. Преподобный Нефрол. 6, 107–115. DOI: 10.1038 / nrneph.2009.213
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Рангино, А., Сеголони, Г. П., Ласапонара, Ф., и Бьянконе, Л. (2015). Лимфатические расстройства после трансплантации почки: новые взгляды на старые осложнения. Clin. Почки J. 8, 615–622. DOI: 10.1093 / ckj / sfv064
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ратнаяке, К. Б. Б., Эскотт, А. Б. Дж., Филлипс, А. Р. Дж., И Виндзор, Дж. А. (2018). Анатомия и физиология терминального грудного протока и устьевого клапана в состоянии здоровья и болезни: потенциальные последствия для вмешательства. J. Anat. 233, 1–14. DOI: 10.1111 / joa.12811
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Роусон, А. Дж. (1949). Распределение лимфатических сосудов почек человека, как показано в случае карциноматозного проникновения. Arch. Дорожка. 47, 283–292.
PubMed Аннотация | Google Scholar
Рон, Д. А., Стюарт, Р. Х., Элк, Дж. Р., Лейн, Г. А., и Дрейк, Р. Э. (1996). Почечная лимфатическая функция после повышения венозного давления. Лимфология 29, 67–75.
PubMed Аннотация | Google Scholar
Ruszniják, I., Földi, M., and Szabó, G. (1960). «Лимфатическая система и лимфообращение», в Physiology and Patology , 2nd Edn, ed. Л. Юлтен (Нью-Йорк, Нью-Йорк: Пергамон).
Google Scholar
Сабин, Ф. Р. (1909). Лимфатическая система эмбрионов человека с учетом морфологии системы в целом. Am. J. Anat. 9, 43–91. DOI: 10.1002 / aja.10000
CrossRef Полный текст | Google Scholar
Сакаи Н., Вада Т., Йокояма Х., Липп М., Уэха С., Мацусима К. и др. (2006). Передача сигналов хемокина вторичной лимфоидной ткани (SLC / CCL21) / CCR7 регулирует фиброциты при почечном фиброзе. PNAS 103, 14098–14103. DOI: 10.1073 / pnas.0511200103
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Сакамото И., Ито Ю., Мизуно М., Судзуки Ю., Савай А., Танака А. и др. (2009). Лимфатические сосуды развиваются при тубулоинтерстициальном фиброзе. Kidney Int. 75, 828–838. DOI: 10.1038 / ki.2008.661
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Сато Ю. и Нитатори Т. (1980). «О тонком строении лимфатических сердец у земноводных и рептилий», в Hearts and Heart-like Organs. Том 1: Сравнительная анатомия и развитие , изд. Г. Х. Борн (Кембридж, Массачусетс: Academic Press), 149–169. DOI: 10.1016 / B978-0-12-119401-7.50011-6
CrossRef Полный текст | Google Scholar
Шмидт, К.Ф. и Хейман Дж. М. (1929). Примечание об образовании лимфы в почках собаки и влиянии на нее некоторых диуретиков. Am. J. Physiol. 91, 157–160. DOI: 10.1152 / ajplegacy.1929.91.1.157
CrossRef Полный текст | Google Scholar
Staub, N.C., и Taylor, A.E. (1984). Отек. Нью-Йорк, Нью-Йорк: Raven Press.
Google Scholar
Столарчик Дж. И Кароне Ф. А. (1975). Влияние почечной лимфатической окклюзии и венозного сужения на функцию почек. Am. J. Pathol. 78, 285–296.
PubMed Аннотация | Google Scholar
Шугарман, Дж., Фридман, М., Барретт, Э. и Аддис, Т. (1942). Распределение, поток, содержание белка и мочевины в почечной лимфе. Am. J. Physiol. 138, 108–112. DOI: 10.1152 / ajplegacy.1942.138.1.108
CrossRef Полный текст | Google Scholar
Судзуки Ю., Ито Ю., Мизуно М., Кинаши Х., Савай А., Нода Ю. и др. (2012). Трансформирующий фактор роста-бета индуцирует экспрессию сосудистого эндотелиального фактора роста-С, что приводит к лимфангиогенезу при односторонней обструкции мочеточника у крыс. Kidney Int. 81, 865–879. DOI: 10.1038 / ki.2011.464
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Суонн, Х. Г., Ормсби, А. А., Делашоу, Дж. Б., и Тарп, В. У. (1958). Связь лимфы с увеличивающейся жидкостью почек. Proc. Soc. Exp. Биол. Med. 97, 517–522. DOI: 10.3181 / 00379727-97-23792
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Танабэ, М., Симидзу, А., Масуда, Ю., Катаока, М., Исикава, А., Wakamatsu, K., et al. (2012). Развитие лимфатической сосудистой сети и морфологическая характеристика почки крысы. Clin. Exp. Нефрол. 16, 833–842. DOI: 10.1007 / s10157-012-0637-z
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Тенстад, О., Хейераас, К. Дж., Уиг, Х. и Окленд, К. (2001). Дренаж белков плазмы из интерстиция мозгового вещества почек у крыс. J. Physiol. 536, 533–539. DOI: 10.1111 / j.1469-7793.2001.0533c.xd
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Трифут, С.А., Коссовер, М. Ф., и Айкен, Д. В. (1987). Радиоизотопное обнаружение лимфатико-венозных коммуникаций у живых животных. J. Lab. Clin. Med. 65, 688–697.
Умбетов Т. З. (1989). Морфофункциональная перестройка почек при нарушении лимфатического оттока. Арх. Анат. Гистол. Эмбриол. 96, 72–78.
PubMed Аннотация | Google Scholar
Ван В. и Мишель К. С. (2000). Моделирование обмена белков плазмы между микроциркуляцией и интерстицией мозгового вещества почек. Am. J. Physiol. Renal Physiol. 279, F334 – F344. DOI: 10.1152 / ajprenal.2000.279.2.F334
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Wehrmann, M., Bohle, A., Bogenschutz, O., Eissele, R., Freislederer, A., Ohlschlegel, C., et al. (1989). Долгосрочный прогноз хронического идиопатического перепончатого гломерулонефрита. Анализ 334 случаев с особым вниманием к канальцево-интерстициальным изменениям. Clin. Нефрол. 31, 67–76.
PubMed Аннотация | Google Scholar
Уилкокс, К.S., Sterzel, R.B., Dunckel, P.T., Mohrmann, M., and Perfetto, M. (1984). Почечное интерстициальное давление и экскреция натрия во время перевязки внутригрудной лимфатической системы. Am. J. Physiol. 247, F344 – F351. DOI: 10.1152 / ajprenal.1984.247.2.F344
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Яздани, С., Навис, Г., Хиллебрандс, Дж. Л., ван Гур, Х. и ван дер Борн, Дж. (2014). Лимфангиогенез при почечных заболеваниях: пассивный наблюдатель или активный участник? Expert Rev.Мол. Med. 16: e15. DOI: 10.1017 / erm.2014.18
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Чжан, Т., Гуань, Г., Чен, Б., Лю, Г., Ли, X., и Хоу, X. (2007a). Роль нарушения почечного лимфообращения на функцию и структуру почек у крыс. J. Shandong Univ. 5, 482–485.
Zhang, T., Guan, G., Liu, G., Sun, J., Chen, B., Li, X., et al. (2007b). Нарушение циркуляции лимфы приводит к развитию фиброза почек у крыс после или без контралатеральной нефрэктомии. Нефрология 13, 128–138. DOI: 10.1111 / j.1440-1797.2007.00851.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Чжан, Т., Лю, Г., Сунь, М., Гуань, Г., Чен, Б., и Ли, X. (2009). Функциональные, гистологические и биохимические последствия почечной лимфатической недостаточности у мононефрэктомированных крыс. J. Nephrol. 22, 109–116.
Google Scholar
Чжо, В., Чай, Дж., Сюй, Т., Ву, В., Ян, С., и Тан, Дж. (2013). Ретроперитонеоскопическое лимфатическое отключение почечной ножки на одном участке для лечения серьезной филяриальной хилурии. Банка. J. Urol. 20, 6726–6729.
PubMed Аннотация | Google Scholar
.
