ОСОБЕННОСТИ ПОРАЖЕНИЯ СЕРДЦА ПРИ МЕТАБОЛИЧЕСКОМ СИНДРОМЕ У ПАЦИЕНТОВ МОЛОДОГО И СРЕДНЕГО ВОЗРАСТА | Громнацкий
1. Аронов Д.М., Лупанов В.П. Функциональные пробы в кардиологии. Москва: МЕДпресс-информ. 2002. 296 с.
2. Баевский P.M., Иванов Г.Г. Вариабельность сердечного ритма: теоретические аспекты и возможности клинического применения. М.: Медицина, 2000. 295 с.
3. А. Дабровски, Б. Дабровски, Р. Пиотрович. Суточное мониторирование ЭКГ. М.: Медпрактика, 1998. 208 с.
4. Громнацкий Н.И. Руководство по внутренним болезням. М.: МИА, 2006. С. 439-444.
5. Митьков В.В., Сандриков В.А. Клиническое руководство по ультразвуковой диагностике. М.: Видар, 1998. Т. V. 360 c.
7. Профилактика, диагностика и лечение артериальной гипертензии. Российские рекомендации (второй пересмотр)//Кардиоваскулярная терапия и профилактика. М., 2004 (приложение). С. 5-16.
8. Чазова И.Е., Мычка В.Б. Метаболический синдром. М.: Media Medica, 2004. С. 47-49.
9. Чеботарев Д.Ф. Руководство по гериатрии. М.: Медицина, 1982. 544 с.
10. Reaven G. Role of insulin resistance in human disease//Diabetes 1988; 37: 1595-1607.
11. Third Report of the National Cholesterol Education Program (NCEP) Expert Panel on detection evaluation and treatment of high blood cholesterol in adults (Adult Treatment Panel III)//JAMA. 2001; 285: 2486-249.
|
В основе ишемической болезни сердца лежит недостаточное снабжение сердечной мышцы кислородом. То есть это несоответствие между потребностью и доставкой. Чаще всего причиной ИБС является атеросклероз коронарных артерий. Внутри коронарной артерии образуется атеросклеротическая бляшка, которая закрывает её просвет. При повышенной нагрузке (физическая, психологическая нагрузка) сердцу требуется больше кислорода, однако доставка его ограничена из-за частичного стеноза (закупорки) коронарной артерии. Поэтому основной симптом при Инфаркт миокарда — некроз (омертвление) участка сердечной мышцы. Причины инфаркта миокарда те же, что и стенокардии. Основной симптом — длительная загрудинная боль (более 30 мин), не снимающаяся нитратами. В результате перенесенного инфаркта миокарда, или вследствие других заболеваний (миокардит) мышечная ткань сердца замещается соединительной, то есть образуется рубец. Рубцовые изменения миокарда называются кардиосклерозом. | Вступить в РМОАГ |
Автоматический анализ функции левого желудочка (АФЛЖ) в Ижевске, цены, описание, врачи
Автоматический анализ функции левого желудочка (АФЛЖ) – это принципиально новый, объективный метод исследования сердца, не имеющий альтернативы (ни ЭКГ, ни холтеровское мониторирование, ни привычное эхо, ни коронарография не дают той информации, которую мы можем получить с помощью эхокардиографии с автоматическим анализом функции левого желудочка (АФЛЖ). Широко применяется в клиниках Европы и Америки.
Уникальность процедуры
Одной из самых больших и порой неразрешимых проблем врача-диагноста является точное (во всех смыслах) определение функции левого желудочка сердца и ее нарушений при и после инфаркта миокарда, при патологии (сужении, тромбозе) коронарных артерий, при заболеваниях, вызывающих диффузные поражения миокарда – при инфекциях; гипертонической болезни, метаболических и эндокринных заболеваниях, оценка эффективности оперативного лечения (АКШ, стент). АФЛЖ дает эту возможность на самых ранних стадиях заболевания или осложнения, что порой определяет судьбу пациента.
Объем получаемой информации настолько велик и достоверен, что сфера применения уникальной суперкомпьютерной технологии постоянно расширяется.
Без АФЛЖ оценка ситуации, определение тактики и выбор адекватного лечения – непростой и долгий и не всегда правильный процесс. По сути, автоматический анализ функции левого желудочка — единственная возможность на доклинической стадии увидеть и количественно оценить степень поражения миокарда, выявить диффузные изменения миокарда при кардиомиопатиях различной этиологии (метаболических, дисгормональных, эндокринных), при бактериальных и вирусных инфекциях, миокардитах, гипертонической болезни).
С результатами АФЛЖ «на руках» врач быстро определит для Вас самый верный путь на поправку и выздоровление.
АФЛЖ в клинике Медсервис
В клинике Медсервис используется оборудование экспертного класса, обеспечивающее беспрецедентную скорость сбора и обработки информации. Благодаря этому, изображение сердца формируется в течение одного сердечного сокращения, исключая геометрические искажения и обеспечивая высокую четкость отображения всех анатомических структур на одном изображении. Благодаря точной визуализации, врач получает подробную информацию о состоянии исследуемого органа.
Метод безболезнен, безопасен и выполняется, как обычное ЭХО-КГ и может быть сделан столько раз, сколько необходимо в ходе лечения сложных случаев. Аналогичные методики – отсутствуют.
Показания
При любом заболевании миокарда, изменении или нарушении его функций вследствие заболеваний, травм или хирургических операций методом выбора диагностики является АФЛЖ.
Особо отмечаем, что вследствие высокоточной и автоматической компьютерной обработки информации – получается абсолютно достоверная картина состояния миокарда, воспроизводимая и понятная в любой приличной клинике России и всего мира.
АФЛЖ показана даже здоровым людям – тем, кто ценит свое здоровье и хочет жить долго и комфортно, т.к. АФЛЖ в этом случае является точнейшим паспортом здорового сердца.
Противопоказания
Противопоказаний для проведения АФЛЖ — нет
Подготовка к процедуре АФЛЖ
Специальная подготовка не требуется
Результат исследования
После проведения АФЛЖ пациенту выдается соответствующее заключение, которое необходимо предоставить своему лечащему врачу. На основании этого заключения лечащий врач определит, есть ли нарушения в работе сердца, требуются ли дополнительные методы диагностики, нужно ли лечение.
Современный алгоритм диагностики ИБС: варианты нагрузочного тестирования.
Аксельрод А.С. – д.м.н профессор кафедры профилактической и неотложной кардиологии,
Зав. отделением функциональной диагностики Клиники кардиологии
ИПО ФГБОУ ВО Первого МГМУ им. И.М. Сеченова
Ранняя диагностика ИБС по-прежнему является одной из наиболее актуальных проблем практической кардиологии, поскольку именно первичная профилактика осложнений приводит к снижению сердечно-сосудистой смертности и случаев нефатальных осложнений. На сегодняшний день «золотым стандартом» диагностики ИБС по-прежнему остается коронароангиография. Это исследование является инвазивным и сопряжено со всеми возможными рисками инвазивных осложнений.
Априорно высокая претестовая вероятность стенозирующего коронарного атеросклероза у мужчин старше 40 лет при наличии типичных ангинозных болей показана в одной из известных таблиц Diamod GA еще в 1979
Рисунок 1. Претестовая вероятность ИБС у мужчин и женщин в зависимости от возраста и клинических проявлений (Diamond GA, 1979)
По сути мужчина старше 40 лет с факторами риска ИБС (гиперхолестеринемия, артериальная гипертензия, отягощенный семейный анамнез) может быть направлен на коронароангиографию для исключения стенозирующего коронарного атеросклероза без предварительного проведения нагрузочного теста. Однако эта таблица становится практически бесполезной при наличии у пациента с множественными факторами риска ИБС немой ишемии миокарда.
Однако эта таблица становится практически бесполезной при наличии у пациента с множественными факторами риска ИБС немой ишемии миокарда.
Алгоритм диагностики ИБС с использованием визуализирующих методик.
Использование так называемых «визуализирующих методик» позволяет решить вопрос о необходимости проведения коронароангиографии, то есть позволяет учесть такие качества скринингового ЭКГ-теста, как чувствительность, специфичность и воспроизводимость.
В самом начале этого алгоритма
Рисунок 2. Алгоритм диагностики ИБС
в зависимости от клинических проявлений ИБС мы имеем возможность выбора одного из трех вариантов нагрузочного теста:
- нагрузочный тредмил-тест;
- велоэргометрия;
- спироэргометрия.
Нагрузочный тредмил-тест по сути является универсальным скрининговым исследованием и подходит для любого пациента, независимо от возраста и физических возможностей, так как ходьба — наиболее физиологический вид физической активности.
В отличие от этого варианта стресс-системы,велоэргометр занимает гораздо меньше места, но не пригоден для тестирования пожилых людей с выраженной патологией суставов.
В том случае, когда мы подозреваем одышку как эквивалент стенокардии, мы используем особый метод скринингового стресс-теста – спироэргометрию.
К визуализирующим методикам относят три варианта инструментальной диагностики, которые при сомнительном результате нагрузочного теста могут быть доводом в пользу проведения коронароангиографии:
- мультиспиральная компьютерная томография коронарных артерий с контрастированием;
- перфузионная сцинтиграфия миокарда с нагрузкой;
- стресс-эхокардиография миокарда (с нагрузочной стресс-системой или с использованием добутамина).
Стоит вернуться к вопросу о том, какую динамику ЭКГ на сегодняшний день принято считать достоверным критерием ишемии миокарда, а какие электрокардиографические изменения могут косвенно свидетельствовать в пользу значимого стенозирующего коронарного атеросклероза.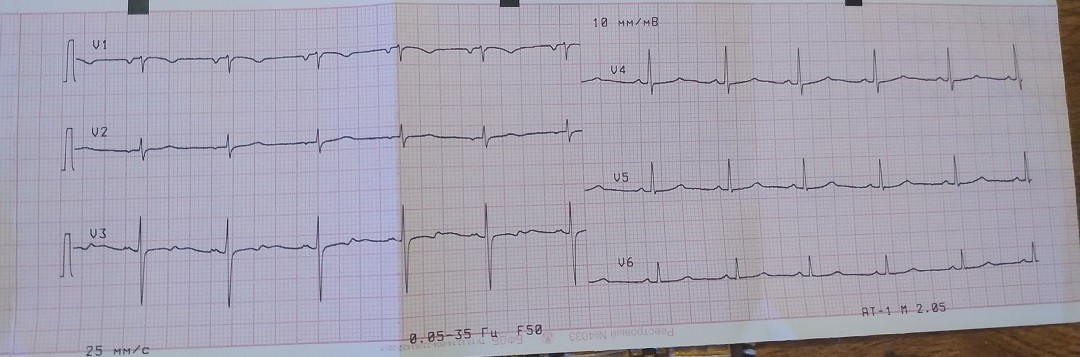
В соответствии с критериями Darrow M, 2000
Рисунок 3. Наиболее специфичные ЭКГ-критерии ишемии миокарда
и современными пересмотрами, представленными в различных рекомендациях, наиболее достоверными критериями ишемии миокарда в настоящее время являются следующие ЭКГ-критерии:
и современными пересмотрами, представленными в различных рекомендациях, наиболее достоверными критериями ишемии миокарда в настоящее время являются следующие ЭКГ-критерии:
- горизонтальная депрессия сегмента ST не менее 1 мм;
- косонисходящая депрессия сегмента ST не менее 1 мм;
- медленная косовосходящая депрессия сегмента ST не менее 1.5 мм;
- элевация сегмента ST.
Следует также отметить, что в связи с низкой специфичностью депрессии сегмента ST у женщин диагностически значимой является значение депрессии 2 мм. Сомнительный результат нагрузочного теста у женщин нередко можно увидеть в виде заключения «проба сомнительная (“женский” ложноположительный тест? немая ишемия миокарда?)». На сегодняшний день можно также видеть обсуждения о высокой чувствительности и не столь высокой специфичности медленной косовосхоящей депрессии сегмента ST cо спорами относительно достаточности ее значения 1.5 мм.
Использование визуализирующих методик возможно в ситуации, когда получен отрицательный результат нагрузочного теста, однако имеющиеся клинические данные и особенности анамнеза позволяют усомниться в высокой воспроизводимости и высокой чувствительности теста у данного больного. Особенностями нагрузочного тестирования, которые должны насторожить лечащего врача в вопросе достаточной воспроизводимости теста могут быть следующие результаты нагрузочного теста при нормальной динамике сегмента ST:
- снижение АД на пике нагрузки и в восстановительном периоде или выраженный симпатико-астенический тип реакции на нагрузку;
- индукция желудочковых нарушений сердечного ритма на пике нагрузки или в восстановительном периоде (стресс-индуцированные желудочковые нарушения сердечного ритма), особенно в сочетании с низкой толерантностью к физической нагрузке.

Возможности спироэргометрии как скринингового стресс-теста у пациентов с ИБС.
Для пациентов, предъявляющих жалобу на одышку, которая может быть расценена как эквивалент стенокардии, наиболее оптимальным вариантом скринингового нагрузочного теста является спироэргометрия. Это исследование является одномоментной оценкой функционального состояния сердечно-сосудистой системы, дыхательной системы и клеточного метаболизма. Полученные параметры позволяют оценить степень и место нарушений, а также определить прогноз дальнейшего течения имеющейся патологии.
По сути данный инструментальный метод исследования позволяет провести дифференциальный диагноз одышки по значению пикового потребления кислорода (VO2 peak) и является «золотым стандартом» оценки толерантности к физической нагрузке
Рисунок 4. Спироэргометрия
На самом деле, помимо скринингового исследования этот инструментальный метод является диагностическим методом с широким спектром возможностей
Рисунок 5. Показания к эргоспирометрии
который позволяет его использовать в различных областях медицины. В частности, такой показатель, как пиковое потребление кислорода (VO2 peak), позволяет уточнить риск периоперационных осложнений
Рисунок 6. Прогностическое значение пикового потребления кислорода (VO2 peak).
При этом методика позволяет достоверно оценить тяжесть хронической сердечной недостаточности у пациентов с ИБС
Рисунок 7. Тяжесть хронической сердечной недостаточности у пациентов с ИБС.
На сегодняшний день считается доказанным, что увеличение переносимости нагрузок на 1% приводит к снижению сердечно-сосудистой смертности на 2%, а VO2 peak является независимым предиктором смертности.
Используя систематические индивидуальные физические тренировки, врач-реабилитолог достигает «перехода» пациентов из класса в класс.
Вероятно, в практике любого врача-кардиолога имеются истории, демонстрирующие значимость визуализирующих методик в диагностическом алгоритме некоторых пациентов.
Показательной является история пациента К., 53 лет, который обратился в клинику кардиологии УКБ №1 в октябре 2016 года в связи с регистрацией парной желудочковой экстрасистолии на ЭКГ покоя. Из анамнеза было известно, что с 1996 года в анализе липидного спектра крови регистрировалась гиперхолестеринемия 9-12 ммоль/л. От приема статинов пациент отказывался. Ежедневно посещал фитнесс-клуб, и лишь при активном расспросе отмечал появление одышки в течение последнего года при длительной интенсивной ходьбе. Обращал также на себя внимание отягощенный семейный анамнез (у отца пациента имеется мультифокальный атеросклероз, клинически – немая ишемия миокарда).
При проведении трансторакальной эхокардиографии не было выявлено нарушений локальной и глобальной сократимости, ФВ составила 68%, лоцировалось уплотнение аорты, створок аортального и митрального клапана без признаков формирования порока. Пациенту было предложено проведение коронароангиографии, от которой он отказался. При проведении суточного мониторирования ЭКГ была зарегистрирована одиночная и парная желудочковая экстрасистолия
Рисунок 8. Результаты холтеровского мониторирования пациента К., 53 лет (одиночная и парная желудочковая экстрасистолия).
Перед проведением нагрузочного тредмил-теста обращала на себя внимание частая одиночная мономорфная желудочковая экстрасистолия с резким учащением на пике нагрузки
Рисунок 9. Стресс-индуцированная мономорфная желудочковая экстрасистолия у пациента К. во время нагрузочного тредмил-теста.
Кроме того, на этой же ступени теста была зарегистрирована устойчивая горизонтальная депрессия сегмента ST в отведениях II, III, aVF, V3-6 до 2. 5 мм. Пациент предъявлял жалобы на одышку.
5 мм. Пациент предъявлял жалобы на одышку.
Рисунок 10. Ишемическая динамика сегмента ST у пациента К., 53 лет. А – ЭКГ на пике нагрузки; Б – появление косонисходящей депрессии сегмента ST в восстановительном периоде.
А.
Б
Поскольку от предложенной коронароангиографии пациент вновь отказался, была проведена мультиспиральная компьютерная томография коронарных артерий с контрастированием, которая продемонстрировала протяженный стеноз передней межжелудочковой артерии и окклюзию правой коронарной артерии
Рисунок 11. Стенозирующий атеросклероз коронарных артерий у больного К., 53 лет.
ПМЖВ в проксимальном сегменте имеет кальцинированную протяженную бляшку со стенозированием 50-75% (Указано стрелкой
ПКА в проксимальном сегменте окклюзирована (указано стрелкой), дистальный отдел и ЗМЖВ заполняются контрастным веществом.
Предложенный случай демонстрирует полное соответствие скринингового тредмил-теста и результатов одной из визуализирующих методик, однако в практической кардиологии нередко имеются случаи рассогласования результатов этих методов исследования.
Довольно показательным в этом смысле является случай пациентки М., 63 лет, которая обратилась в клинику кардиологии УКБ №1 ПМГМУ им. И.М. Сеченова по поводу давящих болей в области сердца, возникающих при подъёме в гору в течение последних 6 месяцев. В анамнезе также обращал на себя внимание затяжной эпизод давящих болей в области сердца, возникший около 2 месяцев назад. При стационарном обследовании была выявлена умеренная гиперхолестеринемия (6.8 ммоль/л), лоцирована уплотненная аорта при проведении трансторакальной эхокардиографии. С учетом эпизода затяжных болей в области сердца пациентке была проведена перфузионная сцинтиграфия миокарда с нагрузкой, где выявлен дефект перфузии боковой стенки в покое с переходом на заднюю стенку при нагрузке
Рисунок 12. Результаты перфузионной сцинтиграфии пациентки М., 63 лет: дефект перфузии боковой стенки в покое с переходом на заднюю стенку при нагрузке.
Результаты перфузионной сцинтиграфии пациентки М., 63 лет: дефект перфузии боковой стенки в покое с переходом на заднюю стенку при нагрузке.
На представленных иллюстрациях видно, что значимой динамики ЭКГ на фоне нагрузки не зарегистрировано.
Также демонстративным является случай пациента Л., 54 лет, госпитализированного в стационар в декабре 2016 года с жалобами на давящий дискомфорт в области сердца, возникающий при ходьбе на 200 м с августа 2016 года и усилившийся в холодную погоду в декабре. При проведении трансторакальной эхокардиографии и нагрузочного тредмил-теста значимой патологии выявлено не было. Однако, с учетом наличия множественных факторов риска (мужской пол, возраст старше 40 лет, курение, гиперхолестеринемия 9 ммоль/л, отягощенный семейный анамнез, артериальная гипертензия) пациенту была проведена коронароангиография. Выявлен 90% стеноз передней межжелудочковой артерии (ПМЖА) и 70% стеноз диагональной артерии (ДА). После проведения стентирования ПМЖА на фоне терапии бисопрололом 5 мг/сут, клопидогрелем 75 мг/сут и аторвастатином 20 мг/сут в январе при ходьбе в холодную погоду пациент отметил возобновление болей в области сердца. Проведена перфузионная сцинтиграфия миокарда с нагрузкой
Рисунок 13. Результаты перфузионной сцинтиграфии миокарда пациента Л., 54 лет: стресс-индуцированный передне-боковой дефект перфузии на пике нагрузки при отсутствии значимой динамики сегмента ST.
где выявлены симптомы стресс-индуцированной ишемии миокарда. После стентирования 70% стеноза ДА была получена положительная динамика контрольной перфузионной сцинтиграфии миокарда. Пациент также отметил полное отсутствие болей при ходьбе.
Довольно типичной является история пациента Д, 62 лет, который обратился на амбулаторную консультацию с жалобами на боли в икроножных мышцах при ходьбе. При проведении дуплексного сканирования артерий ног были выявлены множественные значимые стенозы артерий нижних конечностей, что позволяло расценить жалобы как проявление облитерирующего атеросклероза артерий нижних конечностей. У такого пациента, безусловно, было необходимо исключение гемодинамически значимого стенозирующего атеросклероза коронарных артерий и немой ишемии миокарда, однако при попытке проведения тредмил-теста проба была неинформативной: боли в ногах возникли при достижении 60% возрастной нормы. При проведении трансторакальной эхокардиографии была выявлена гипокинезия нижней стенки левого желудочка.
У такого пациента, безусловно, было необходимо исключение гемодинамически значимого стенозирующего атеросклероза коронарных артерий и немой ишемии миокарда, однако при попытке проведения тредмил-теста проба была неинформативной: боли в ногах возникли при достижении 60% возрастной нормы. При проведении трансторакальной эхокардиографии была выявлена гипокинезия нижней стенки левого желудочка.
Для решения вопроса о мультифокальности и необходимости проведения коронароангиографии пациенту был проведен добутаминовый тест как вариант стресс-эхокардиографии. Появление двухфазной реакции сократимости (двухфазный добутаминовый ответ) для этого пациента позволило бы не только решить вопрос необходимости проведения коронароангиографии, но и оценить необходимость реваскуляризации миокарда.
Как известно, подтверждением наличия жизнеспособного миокарда является увеличение сократимости сегментов с исходной сниженной сократимостью в ответ на введение низких (5-10 мкг/кг/мин) доз добутамина с последующим ухудшением сократимости в тех же сегментах на фоне введения высоких (20 мкг/кг/мин) доз.
У пациента Д. проба была положительной: как видно из представленной иллюстрации
Рисунок 14. Положительный результат добутаминового теста у пациента Д., 62 лет
имеется сужение полости левого желудочка с последующим ее расширением, что является признаком последовательного улучшения, а затем ухудшения сократимости. При проведении коронароангиографии у пациента было выявлено гемодинамически значимое многососудистое поражение коронарных артерий, а в дальнейшем успешно проведено аорто-коронарное шунтирование.
Таким образом, на сегодняшний день можно сказать, что неинвазивная диагностика ИБС представляет собой отлаженный, но не всегда очевидный алгоритм. Чаще всего мы используем визуализирующие методики диагностики ИБС (перфузионную сцинтиграфию миокарда с нагрузкой, стресс-эхокардиографию, мультиспиральную компьютерную томографию) при сомнительном результате скринингового нагрузочного теста или при невозможности его проведения (пациенты с облитерирующим атеросклерозом артерий нижних конечностей). Однако отсутствие типичной ишемической динамики сегмента ST у пациента с несколькими факторами риска ИБС оправданно позволяет использовать визуализирующие методики диагностики, несмотря на отрицательный результат первичного теста, поскольку именно клинический статус пациента в сочетании с данными его анамнеза позволяют определить единственно верный для каждого конкретного пациента алгоритм диагностики.
Однако отсутствие типичной ишемической динамики сегмента ST у пациента с несколькими факторами риска ИБС оправданно позволяет использовать визуализирующие методики диагностики, несмотря на отрицательный результат первичного теста, поскольку именно клинический статус пациента в сочетании с данными его анамнеза позволяют определить единственно верный для каждого конкретного пациента алгоритм диагностики.
Что такое метаболический синдром?
В настоящее время сердечно-сосудистые заболевания (инфаркт миокарда, инсульт и т. д.) и сахарный диабет 2 типа лидируют среди причин смертности, поэтому профилактика этих заболеваний — важная проблема современности. В основе профилактики любого заболевания лежит борьба с факторами риска. Термин метаболический синдром применяется в медицине именно с целью раннего выявления и устранения факторов риска сердечно-сосудистых заболеваний и диабета.
Нарушения, входящие в рамки метаболического синдрома, длительно остаются незамеченными, часто начинают формироваться в детском и юношеском возрасте, неизбежно приводя к атеросклеротическим заболеваниям, диабету, артериальной гипертонии. Зачастую пациентам с ожирением, «немного» повышенным уровнем глюкозы, артериальным давлением на верхней границе нормы не уделяется должного внимания. Только когда эти факторы риска перейдут в серьезное заболевание, пациент удостаивается внимания здравоохранения.
Важно, чтобы факторы риска выявлялись и корригировались как можно раньше, до того, как они приведут к сердечно-сосудистым катастрофам. В этом огромную роль играет введение и применение такого понятия как метаболический синдром.
Метаболический синдром — это комплекс изменений, связанный с нарушением обмена веществ. Гормон инсулин перестает восприниматься клетками и не выполняет свои функции. В таком случае развивается инсулинорезистентность или нечувствительность к инсулину, что приводит к нарушению усвоения клетками глюкозы, а также патологическим изменениям всех систем и тканей. На сегодняшний день, согласно 10-му международному классификатору болезней, метаболический синдром не считается отдельным заболеванием. Это состояние, когда организм одновременно страдает от четырех болезней (нарушений):
На сегодняшний день, согласно 10-му международному классификатору болезней, метаболический синдром не считается отдельным заболеванием. Это состояние, когда организм одновременно страдает от четырех болезней (нарушений):
- гипертонии
- ожирения
- ишемической болезни сердца
- сахарного диабета 2 типа
В развитых странах, где большинство населения ведет малоподвижный образ жизни, 10–25% людей старше 30 лет страдают от данных нарушений. В старшей возрастной группе показатели возрастают до 40%. Так в Европе количество больных превысило 50 млн человек. За ближайшие четверть века заболеваемость повысится на 50%. За последние два десятилетия количество больных среди детей и подростков увеличилось до 6,5%. Эту тревожную статистику связывают с пристрастием к углеводной диете.
Метаболический синдром поражает преимущественно мужчин. Женщинам эта болезнь грозит во время и после менопаузы. У представительниц слабого пола после 50-ти лет риск развития метаболического синдрома возрастает в 5 раз. К сожалению, современная медицина не в состоянии вылечить метаболический синдром. Однако есть и хорошие новости. Большинство изменений, развившихся в результате метаболического синдрома, обратимы. Грамотное лечение, правильное питание и здоровый образ жизни помогают надолго стабилизировать состояние.
Причины метаболического синдрома
Инсулин в организме выполняет множество функций. Но его основная задача — связаться в инсулиночувствительными рецепторами, которые есть в оболочке каждой клетки. После этого запускается механизм транспортировки глюкозы из межклеточного пространства внутрь клетки. Таким образом, инсулин «открывает двери» в клетку для глюкозы. Если рецепторы не реагируют на инсулин, то и сам гормон и глюкоза накапливаются в крови. В основе развития метаболического синдрома лежит нечувствительность к инсулину — инсулинорезистентность. Это явление может вызываться рядом причин.
1. Генетическая предрасположенность. У некоторых людей нечувствительность к инсулину заложена на генетическом уровне. Ген, который несет ответственность за развитие метаболического синдрома, находится в 19 хромосоме. Его мутации могут привести к тому, что
У некоторых людей нечувствительность к инсулину заложена на генетическом уровне. Ген, который несет ответственность за развитие метаболического синдрома, находится в 19 хромосоме. Его мутации могут привести к тому, что
- у клеток недостаточно рецепторов, отвечающих за связывание инсулина;
- рецепторы не чувствительны к инсулину;
- иммунная система вырабатывает антитела, которые блокируют инсулиночувствительные рецепторы;
- поджелудочная железа вырабатывает аномальный инсулин.
2. Диета с высоким содержанием жиров и углеводов — самый важный фактор развития метаболического синдрома. Насыщенные жирные кислоты, поступающие с животными жирами в большом количестве, способствуют развитию ожирения. Кроме того жирные кислоты вызывают изменения в оболочках клеток, делая их нечувствительными к действию инсулина. Чрезмерно калорийное питание приводит к тому, что в кровь поступает много глюкозы и жирных кислот. Их избыток откладывается в жировых клетках в подкожной жировой клетчатке, а также в других тканях. Это приводит к снижению их чувствительности к инсулину.
3. Малоподвижный образ жизни. Уменьшение физической активности влечет за собой снижение скорости всех обменных процессов, в том, числе и расщепления и усвоения жиров. Жирные кислоты блокируют транспорт глюкозы в клетку и снижают чувствительность ее мембраны к инсулину.
4. Длительная не леченная артериальная гипертония. Вызывает нарушение периферического кровообращения, которое сопровождается снижением чувствительности тканей к инсулину.
5. Пристрастие к низкокалорийным диетам. Если калорийность суточного рациона составляет менее 300 ккал, это приводит к необратимым нарушениям обмена веществ. Организм «экономит» и наращивает запасы, что приводит к усиленному жироотложению.
6. Длительные психические нагрузки и стресс нарушают нервную регуляцию органов и тканей. В результате нарушается производство гормонов, в том числе инсулина, и реакция клеток на них.
В результате нарушается производство гормонов, в том числе инсулина, и реакция клеток на них.
7. Приём препаратов-антагонистов инсулина:
- глюкагон;
- кортикостероиды;
- пероральные контрацептивы;
- тиреоидные гормоны.
Эти лекарственные препараты уменьшают поглощение тканями глюкозы, что сопровождается снижением чувствительности к инсулину.
8. Передозировка инсулина при лечении сахарного диабета. Неправильно подобранное лечение приводит к тому, что в крови находится большое количество инсулина. Это вызывает привыкание рецепторов. Инсулинорезистентность в этом случае является своеобразной защитной реакцией организма от высокой концентрации инсулина.
9. Гормональные нарушения. Жировая ткань является эндокринным органом и выделяет гормоны, которые снижают чувствительность к инсулину. Причем, чем более выражено ожирение, тем ниже чувствительность. У женщин при повышенной выработке тестостерона и сниженной эстрогена жиры накапливаются по «мужскому» типу, нарушается работа сосудов и развивается артериальная гипертензия. Снижение уровня гормонов щитовидной железы также способно вызвать повышение уровня липидов (жиров) в крови и развитие инсулинорезистентности.
10. Возрастные изменения у мужчин. С возрастом снижается выработка тестостерона, что приводит к инсулинорезистентности, ожирению и гипертонии.
11. Апное во сне. Задержка дыхания во сне вызывает кислородное голодание мозга и усиленную выработку соматотропного гормона. Это вещество способствуют развитию нечувствительности к инсулину.
Симптомы метаболического синдрома
Рассмотрим все критерии метаболического синдрома.
1. Главный и обязательный критерий — абдоминальное ожирение, т. е. ожирение, при котором жировая ткань откладывается преимущественно в области живота. Иногда такое ожирение называют ожирением «по типу яблока» или «андроидным». Жировая клетчатка скапливается не только под кожей, но и вокруг внутренних органов. Она не только сдавливает их, затрудняя их работу, но и играет роль эндокринного органа. Жир выделяет вещества, способствующие появлению воспаления, повышению уровня фибрина в крови, что повышает риск развития тромбов. Отложение жира преимущественно в области бедер и ягодиц («по типу груши», «гиноидное») не имеет столь неблагоприятных последствий и в качестве критерия метаболического синдрома не рассматривается. Определить абдоминальное ожирение очень просто, достаточно измерить объем талии на уровне середины расстояния между краями реберных дуг и подвздошных костей. Для европеоидной нации показателями абдоминального ожирения являются объем талии у мужчин более 94–102 см, у женщин — более 80–88 см. Для азиатской популяции показатель ожирения у мужчин более строгий — объем талии более 90 см, а для женщин также — более 80 см.
Жировая клетчатка скапливается не только под кожей, но и вокруг внутренних органов. Она не только сдавливает их, затрудняя их работу, но и играет роль эндокринного органа. Жир выделяет вещества, способствующие появлению воспаления, повышению уровня фибрина в крови, что повышает риск развития тромбов. Отложение жира преимущественно в области бедер и ягодиц («по типу груши», «гиноидное») не имеет столь неблагоприятных последствий и в качестве критерия метаболического синдрома не рассматривается. Определить абдоминальное ожирение очень просто, достаточно измерить объем талии на уровне середины расстояния между краями реберных дуг и подвздошных костей. Для европеоидной нации показателями абдоминального ожирения являются объем талии у мужчин более 94–102 см, у женщин — более 80–88 см. Для азиатской популяции показатель ожирения у мужчин более строгий — объем талии более 90 см, а для женщин также — более 80 см.
2. Артериальная гипертензия диагностируется, если систолическое артериальное давление более или равно 130 мм. рт. ст., диастолическое более или равно 85 мм. рт. ст. Красные пятна на груди и шее. Это признаки повышения давления связанного со спазмом сосудов, который вызван избытком инсулина.
3. Нарушения липидного спектра. Для диагностики потребуется бихимический анализ крови: определение уровня триацилглицеридов и холестерина липопротеинов высокой плотности.
4. Нарушением углеводного обмена считается уровень глюкозы крови натощак более 5,6 ммоль/л, или лечение сахароснижающими препаратами.
Диагностика метаболического синдрома
При необходимости лечащий врач назначит дополнительное обследование:
— суточный мониторинг артериального давления, ЭКГ-исследование, ультразвуковое исследование сердца и сосудов, определение биохимических показателей уровня липидов крови, исследования функции печени и почек, определение глюкозы крови через 2 часа после еды или после проведения орального глюкозтолерантного теста.
Лечение метаболического синдрома
Лечение метаболического синдрома заключается в ведении здорового образа жизни и медикаментозной терапии. Изменение образа жизни означает изменение питания, режима физических нагрузок и отказ от вредных привычек. Фармакотерапия (назначение лекарственных препаратов) не будет иметь эффекта, если пациент не соблюдает правила питания и режима физической активности.
Рекомендации по питанию при метаболическом синдроме
— Крайне не рекомендуются чрезмерно строгие диеты и голодание. Снижение массы тела должно быть постепенным (на 5–10% за первый год). При быстрых темпах снижения массы тела пациенту трудно удержать полученный результат, практически всегда потерянные килограммы также быстро возвращаются.
— Более полезным и эффективным будет изменение состава питания: снижение употребления животных жиров, замена животных жиров растительными, увеличение потребления растительной клетчатки, волокон и снижение потребления поваренной соли.
— Следует практически полностью исключить сладкие газированные напитки, кондитерские изделия, фаст-фуд.
— Употребление хлеба лучше ограничить до 150–200 граммов в день.
— Супы должны быть преимущественно овощные.
— Из мясных продуктов лучше выбрать нежирные сорта говядины, птицы или рыбу в отварном или заливном виде.
— Из круп лучше использовать гречневую и овсяную, возможны также рисовая, пшённая, перловая, крупы, манную лучше максимально ограничить.
— Картофель, морковь, свёклу, рекомендуется употреблять не более 200 граммов в день. Овощи, богатые клетчаткой (помидоры, огурцы, болгарский перец, капусту, салат, редис, кабачки) и зелень возможно употреблять практически без ограничений в сыром и варёном или печёном виде.
— Яйца рекомендуется использовать не более 1–2 штуки в день.
— Фрукты и ягоды можно употреблять до 200–300 граммов в день.
— Молоко минимальной жирности, нежирные кисломолочные продукты и творог — 1–2 стакана в день. Сливки, жирные сорта сыров, сметану рекомендуется употреблять изредка.
Сливки, жирные сорта сыров, сметану рекомендуется употреблять изредка.
— Из напитков разрешены чай, некрепкий кофе в умеренных количествах, томатный сок, компоты и соки из ягод и фруктов кислых сортов, лучше домашнего приготовления без сахара.
Борьба с вредными привычками: ограничение алкоголя, отказ от курения.
Список рекомендованных продуктов:
- нежирные сорта мяса животных (телятина, кролик, курица без шкурки) и птицы 150–200 г в сутки;
- рыба и морепродукты 150 г;
- яйца — 1–2 в день в виде омлета или сваренные вкрутую;
- нежирные молочные продукты;
- творог 100–200 г;
- нежирные и неострые сорта твердого сыра — ограниченно до 30 г;
- нежирные говяжьи сосиски или вареная колбаса 2 раза в неделю;
- овощи 25% в сыром виде, остальные в тушеном, вареном, запеченном, приготовленном на пару (не менее 400 г).
Рекомендованы зеленые овощи;
- фрукты и ягоды несладкие сорта до 400 г. Свежие, замороженные или консервированные без сахара.
- квашеная капуста, промытая водой;
- каши из перловой, гречневой, ячной крупы, бурый рис. 150–200 г на порцию с условием ограничения хлеба;
- первые блюда (250–300 г) на слабом обезжиренном мясном, рыбном или грибном бульоне, вегетарианские супы;
- хлеб из муки грубого помола, изделия с отрубями до 200 г;
- чаи, фруктовые и овощные соки без сахара;
- полоска черного шоколада, желе и муссы заменителях сахара;
- потребление жидкости ограничивают до 1,5 л. Это вызывает усиленный распад жиров в организме.
Необходимо отказаться от таких продуктов:
- кондитерские изделия: конфеты, печенье, изделия с кремом;
- выпечка, особенно вредна сдобная и слоеная;
- жирные сорта мяса: свинина, баранина, утка;
- консервы, копченое мясо и рыба, колбаса, ветчина;
- рис, манная и овсяная крупы, макароны;
- сливки, сладкий йогурт, жирный творог и изделия из него;
- маргарин, кулинарный жир;
- изюм, бананы, виноград, финики и другие сладкие фрукты;
- майонез, жирные острые соусы, пряности;
- сладкие газированные напитки, соки и нектары с сахаром.

1 раз в 1–2 недели можно делать выходной и умеренно употреблять «нежелательные» продукты.
Рекомендации по режиму физических нагрузок при метаболическом синдроме
Рекомендуется постепенное увеличение физической активности. Следует предпочесть такие виды спорта как ходьба, бег, гимнастика, плавание. Главное, чтобы физические нагрузки были регулярными и соответствовали вашим возможностям.
Медикаментозное лечение метаболического синдрома
Фармакотерапия метаболического синдрома направлена на лечение ожирения, нарушений углеводного обмена, артериальной гипертонии и дислипидемии.
Лечением метаболического синдрома занимаются врачи-эндокринологи. Но учитывая, что в организме больного происходят разнообразные патологические изменения, может потребоваться консультация: терапевта, кардиолога, диетолога.
Профилактика метаболического синдрома
Что нужно делать?
- Питайтесь правильно. Ешьте 5–6 раз в день небольшими порциями. У вас не должно возникать чувство голода. В противном случае, организм, получая питательные вещества, откладывает их про запас, что способствует развитию ожирения.
- Больше двигайтесь. Это помогает сжигать калории и нормализует обмен веществ. Используйте каждую возможность проявить физическую активность: ходите на работу пешком, поднимайтесь по ступенькам, мойте пол руками, а не шваброй.
- Купите абонемент в тренажерный зал или бассейн. Потраченные деньги будут вас стимулировать посещать занятия.
- Массаж и самомассаж. Эта процедура нормализует кровообращение в тканях, особенно в нижних конечностях, что делает клетки более чувствительными к воздействию инсулина.
- Пройдите курс физиотерапии: барокамера, миостимуляция, криотерапия, грязелечение прекрасно ускоряют обмен веществ. Направление в физкабинет можно получить у вашего лечащего врача.

- Гирудотерапия. Лечение пиявками улучшает все характеристики крови и нормализует кровоток, что важно для поддержания метаболизма в организме.
- Следите за уровнем холестерина. После 40 лет не реже чем раз в год проверяйте уровень «хорошего» и «плохого» холестеринов, чтобы при необходимости своевременно начать лечение.
Вам выполнили экг и обнаружили синусовую тахикардию…что это значит? — Наука на TJ
{«id»:114168,»url»:»https:\/\/tjournal.ru\/science\/114168-vam-vypolnili-ekg-i-obnaruzhili-sinusovuyu-tahikardiyu-chto-eto-znachit»,»title»:»\u0412\u0430\u043c \u0432\u044b\u043f\u043e\u043b\u043d\u0438\u043b\u0438 \u044d\u043a\u0433 \u0438 \u043e\u0431\u043d\u0430\u0440\u0443\u0436\u0438\u043b\u0438 \u0441\u0438\u043d\u0443\u0441\u043e\u0432\u0443\u044e \u0442\u0430\u0445\u0438\u043a\u0430\u0440\u0434\u0438\u044e…\u0447\u0442\u043e \u044d\u0442\u043e \u0437\u043d\u0430\u0447\u0438\u0442?»,»services»:{«vkontakte»:{«url»:»https:\/\/vk.com\/share.php?url=https:\/\/tjournal.ru\/science\/114168-vam-vypolnili-ekg-i-obnaruzhili-sinusovuyu-tahikardiyu-chto-eto-znachit&title=\u0412\u0430\u043c \u0432\u044b\u043f\u043e\u043b\u043d\u0438\u043b\u0438 \u044d\u043a\u0433 \u0438 \u043e\u0431\u043d\u0430\u0440\u0443\u0436\u0438\u043b\u0438 \u0441\u0438\u043d\u0443\u0441\u043e\u0432\u0443\u044e \u0442\u0430\u0445\u0438\u043a\u0430\u0440\u0434\u0438\u044e…\u0447\u0442\u043e \u044d\u0442\u043e \u0437\u043d\u0430\u0447\u0438\u0442?»,»short_name»:»VK»,»title»:»\u0412\u041a\u043e\u043d\u0442\u0430\u043a\u0442\u0435″,»width»:600,»height»:450},»facebook»:{«url»:»https:\/\/www.facebook.com\/sharer\/sharer.php?u=https:\/\/tjournal.ru\/science\/114168-vam-vypolnili-ekg-i-obnaruzhili-sinusovuyu-tahikardiyu-chto-eto-znachit»,»short_name»:»FB»,»title»:»Facebook»,»width»:600,»height»:450},»twitter»:{«url»:»https:\/\/twitter.com\/intent\/tweet?url=https:\/\/tjournal. ru\/science\/114168-vam-vypolnili-ekg-i-obnaruzhili-sinusovuyu-tahikardiyu-chto-eto-znachit&text=\u0412\u0430\u043c \u0432\u044b\u043f\u043e\u043b\u043d\u0438\u043b\u0438 \u044d\u043a\u0433 \u0438 \u043e\u0431\u043d\u0430\u0440\u0443\u0436\u0438\u043b\u0438 \u0441\u0438\u043d\u0443\u0441\u043e\u0432\u0443\u044e \u0442\u0430\u0445\u0438\u043a\u0430\u0440\u0434\u0438\u044e…\u0447\u0442\u043e \u044d\u0442\u043e \u0437\u043d\u0430\u0447\u0438\u0442?»,»short_name»:»TW»,»title»:»Twitter»,»width»:600,»height»:450},»telegram»:{«url»:»tg:\/\/msg_url?url=https:\/\/tjournal.ru\/science\/114168-vam-vypolnili-ekg-i-obnaruzhili-sinusovuyu-tahikardiyu-chto-eto-znachit&text=\u0412\u0430\u043c \u0432\u044b\u043f\u043e\u043b\u043d\u0438\u043b\u0438 \u044d\u043a\u0433 \u0438 \u043e\u0431\u043d\u0430\u0440\u0443\u0436\u0438\u043b\u0438 \u0441\u0438\u043d\u0443\u0441\u043e\u0432\u0443\u044e \u0442\u0430\u0445\u0438\u043a\u0430\u0440\u0434\u0438\u044e…\u0447\u0442\u043e \u044d\u0442\u043e \u0437\u043d\u0430\u0447\u0438\u0442?»,»short_name»:»TG»,»title»:»Telegram»,»width»:600,»height»:450},»odnoklassniki»:{«url»:»http:\/\/connect.ok.ru\/dk?st.cmd=WidgetSharePreview&service=odnoklassniki&st.shareUrl=https:\/\/tjournal.ru\/science\/114168-vam-vypolnili-ekg-i-obnaruzhili-sinusovuyu-tahikardiyu-chto-eto-znachit»,»short_name»:»OK»,»title»:»\u041e\u0434\u043d\u043e\u043a\u043b\u0430\u0441\u0441\u043d\u0438\u043a\u0438″,»width»:600,»height»:450},»email»:{«url»:»mailto:?subject=\u0412\u0430\u043c \u0432\u044b\u043f\u043e\u043b\u043d\u0438\u043b\u0438 \u044d\u043a\u0433 \u0438 \u043e\u0431\u043d\u0430\u0440\u0443\u0436\u0438\u043b\u0438 \u0441\u0438\u043d\u0443\u0441\u043e\u0432\u0443\u044e \u0442\u0430\u0445\u0438\u043a\u0430\u0440\u0434\u0438\u044e…\u0447\u0442\u043e \u044d\u0442\u043e \u0437\u043d\u0430\u0447\u0438\u0442?&body=https:\/\/tjournal.ru\/science\/114168-vam-vypolnili-ekg-i-obnaruzhili-sinusovuyu-tahikardiyu-chto-eto-znachit»,»short_name»:»Email»,»title»:»\u041e\u0442\u043f\u0440\u0430\u0432\u0438\u0442\u044c \u043d\u0430 \u043f\u043e\u0447\u0442\u0443″,»width»:600,»height»:450}},»isFavorited»:false}
ru\/science\/114168-vam-vypolnili-ekg-i-obnaruzhili-sinusovuyu-tahikardiyu-chto-eto-znachit&text=\u0412\u0430\u043c \u0432\u044b\u043f\u043e\u043b\u043d\u0438\u043b\u0438 \u044d\u043a\u0433 \u0438 \u043e\u0431\u043d\u0430\u0440\u0443\u0436\u0438\u043b\u0438 \u0441\u0438\u043d\u0443\u0441\u043e\u0432\u0443\u044e \u0442\u0430\u0445\u0438\u043a\u0430\u0440\u0434\u0438\u044e…\u0447\u0442\u043e \u044d\u0442\u043e \u0437\u043d\u0430\u0447\u0438\u0442?»,»short_name»:»TW»,»title»:»Twitter»,»width»:600,»height»:450},»telegram»:{«url»:»tg:\/\/msg_url?url=https:\/\/tjournal.ru\/science\/114168-vam-vypolnili-ekg-i-obnaruzhili-sinusovuyu-tahikardiyu-chto-eto-znachit&text=\u0412\u0430\u043c \u0432\u044b\u043f\u043e\u043b\u043d\u0438\u043b\u0438 \u044d\u043a\u0433 \u0438 \u043e\u0431\u043d\u0430\u0440\u0443\u0436\u0438\u043b\u0438 \u0441\u0438\u043d\u0443\u0441\u043e\u0432\u0443\u044e \u0442\u0430\u0445\u0438\u043a\u0430\u0440\u0434\u0438\u044e…\u0447\u0442\u043e \u044d\u0442\u043e \u0437\u043d\u0430\u0447\u0438\u0442?»,»short_name»:»TG»,»title»:»Telegram»,»width»:600,»height»:450},»odnoklassniki»:{«url»:»http:\/\/connect.ok.ru\/dk?st.cmd=WidgetSharePreview&service=odnoklassniki&st.shareUrl=https:\/\/tjournal.ru\/science\/114168-vam-vypolnili-ekg-i-obnaruzhili-sinusovuyu-tahikardiyu-chto-eto-znachit»,»short_name»:»OK»,»title»:»\u041e\u0434\u043d\u043e\u043a\u043b\u0430\u0441\u0441\u043d\u0438\u043a\u0438″,»width»:600,»height»:450},»email»:{«url»:»mailto:?subject=\u0412\u0430\u043c \u0432\u044b\u043f\u043e\u043b\u043d\u0438\u043b\u0438 \u044d\u043a\u0433 \u0438 \u043e\u0431\u043d\u0430\u0440\u0443\u0436\u0438\u043b\u0438 \u0441\u0438\u043d\u0443\u0441\u043e\u0432\u0443\u044e \u0442\u0430\u0445\u0438\u043a\u0430\u0440\u0434\u0438\u044e…\u0447\u0442\u043e \u044d\u0442\u043e \u0437\u043d\u0430\u0447\u0438\u0442?&body=https:\/\/tjournal.ru\/science\/114168-vam-vypolnili-ekg-i-obnaruzhili-sinusovuyu-tahikardiyu-chto-eto-znachit»,»short_name»:»Email»,»title»:»\u041e\u0442\u043f\u0440\u0430\u0432\u0438\u0442\u044c \u043d\u0430 \u043f\u043e\u0447\u0442\u0443″,»width»:600,»height»:450}},»isFavorited»:false}
51 856 просмотров
Изменение метаболизма миокарда при сердечной недостаточности, обусловленной некоронар.
 ..ными заболеваниями, под влнянием рефрак… и энергостима
..ными заболеваниями, под влнянием рефрак… и энергостимал.
(«л
-Ъ На правах рукописи
о
САНИНА Наталья Петровна
УДК 615-45; 616.127-002
Изменение метаболизма миокарда при сер ччной недостаточности, обусловленной некоронаг’ ными заболеваниями, под влиянием рефракт н энергостима
14.00.06 — Кардиология
АВТОРЕФЕРАТ диссертации на соискание ученой степени кандидата медицинских наук
Москва 1997
Работа выполнена в Московском областном научн исследовательском клиническом институте им. М.Ф.Владимирского.
Научные руководители:
Засл. деятель науки РФ, академик РАМН,
профессор, доктор медицинских наук Н.Р. Палеев
Засл. деятель науки РГ, академик АМН РГ, член-корр. РАМ
профессор, доктор медицинских наук Н.В.Карсанов
Официальные оппоненты:
Профессор, доктор медицинских наук
В.П.Померанцев
Профессор, доктор медицинских наук
П.Х.Джанашия
Ведущая организация: Медицинская академия им. Н.И.Сеченова.
Защита состоится «_»_ 1997 года в_час. на заседай]
диссертационного Совета Д.084.08.01 в Московском медицинском стомат логическом институте (ул. Долгоруковская, д.4.).
С диссертацией можно ознакомиться в библиотеке институ (ул.Вучетича, 10-а).
Автореферат разослан «_»_ 1997 г.
Ученый секретарь диссертационного Совета
доктор медицинских наук,
профессор
Л.Л.Кириченко
АКТУАЛЬНОСТЬ ПРОБЛЕМЫ. В последние годы отмечается неуклонный рост некоронарогенных заболеваний миокарда (НЗМ), в связи с чем они продолжают оставаться одной из основных проблем в клинике внутренних болезней. По распространенности и тяжести ведущее место сре-ци НЗМ занимают миокардиты. На них приходится 9,2% общего числа кардиологических больных (Н.Р.Палеев и соавт., 1982) и 10-11% среди НЗМ ‘М.И.Теодори, 1972, М.О.Янковская, М.А.Гуревич, 1979). Дилатационная кардиомиопатия (ДКМП) диагностируется в 6,5% случаев НЗМ (Sotos и :оавт., 1992; Macral, 1994), из них в 20-25% случаев она носит семейный характер (Hogye, 1994). И наконец, 25% НЗМ приходится на хроническое шкогольное поражение сердца (АПС) (ВОЗ, 1959). Перечисленные формы татологии очень часто осложняются сердечной недостаточностью (СН). Например, при ДКМП она развивается у 26% больных.
В 1994 году в России число больных хронической СН составило 3,5 ллн. (Е.И.Чазов, 1994 г.), а в США — более 3 млн. (Deedwania, 1995).
Сегодняшняя терапия СН, основанная на применении сердечных гли-;озидов (СГ), мочегонных препаратов, бета-блокаторов и ингибиторов АПФ Weber, 1995; Cohn, 1996) ориентирована, в основном, на создание благо-фиятных условий для работы сердца путем уменьшения пред- и пост-гагрузки. Ни одна из традиционных методик лечения не предусматривает армоничного воздействия на внутриклеточные процессы, приводящие к развитию дисфункции левого желудочка (ЛЖ) миокарда. И это несмотря [а то, что установлена связь СН с нарушением метаболизма и энергетиче-кого обеспечения миокарда (Н.Р.Палеев и соавт., 1982, 1996 а,б, 1997; íraunwald и соавт., 1992; Katz, 1990; М.А.Гуревич и соат., 1994; Г.В.Карсанов и соавт., 1984,1990,1995 а,б, 1996).
Попытки коррекции этих нарушений с помощью таких метаболиче-ких препаратов, как компоненты адениловой системы — АТФ, АМФ
(фосфаден), фосфокреатин (неотон), продукты деградации адениловых нук-леотидов (инозин или рибоксин, аденозин), субстраты цикла Кребса (сукцинат и малат натрия), фермент цепи переноса электронов — цитохром С, ключевой фермент гликолиза — фруктозо-1,6-дифосфат, оротовая кислота и ее соли, а также другие соединения (В.В.Гацура и соавт., 1993), не дали желаемого результата.
Новые препараты, рефрактерны и энергостим, обладающие способностью активно влиять на функционирование всех трех систем кардиомиоци-та, ответственных за акт сокращение-расслабление, улучшают ультраструктуру кардиомиоцита, повышают его функциональную активность и тем самым существенно уменьшают тяжесть СН.
Необходимость разработки надежных критериев оценки тяжести метаболических расстройств в кардиомиоците и эффективности коррекции биохимических сдвигов в крови и миокарде при лечении СН кардиотроп-ным средством рефрактерином и антигипоксантом энергостимом определили актуальность поставленных в работе задач.
ЦЕЛЬ ИССЛЕДОВАНИЯ. Изучить нарушения метаболических процессов в миокарде и иммунологических показателей при НЗМ и разработать принципы терапии СН, в основе которой лежит коррекция метаболических сдвигов с помощью двух новых препаратов — рефрактерина и энерго-стима.
ЗАДАЧИ: 1. Изучить особенности клинико-функционального состояния больных с СН, обусловленной НЗМ, и их связь с метаболическими нарушениями в миокарде при различной степени тяжести СН.
2. Изучить особенности ряда иммунологических показателей у больных с СН различной степени тяжести и возможность коррекции выявленных нарушений с помощью пептидного морфогена гидры (ПМГ).
3. Оценить эффективность рефрактерина и энергостима как средств коррекции метаболических нарушений в кардиомиоците и крови при НЗМ.
4. Выявить взаимосвязь между достигнутым улучшением показателей метаболизма миокарда, клинико-функциональным состоянием сердечно-:осудистой системы и качеством жизни больных НЗМ при лечении рефрак-герином и энергостимом в сравнении с традиционной терапией.
НАУЧНАЯ НОВИЗНА. Впервые в процессе лечения рефрактери-ном и энергостимом проведен комплексный анализ метаболических отклонений, отражающих эффективность образования энергии в миокарде, и кли-нико-функционального состояния больных с СН, обусловленной НЗМ. Разработана терапия рефрактерином и энергостимом, позволяющая достичь гакой степени коррекции метаболических нарушений, которая обеспечивает восстановление процесса образования энергии в кардиомиоците, что, в звою очередь, ведет к существенному улучшению центральной гемодинамики, устранению дисфункции миокарда и тем самым, в отличие от традиционной терапии, преодолению рефрактерное™ миокарда к медикаментозному воздействию и предотвращению развития гликозидной интоксикации.
Впервые получены сравнительные данные о влиянии терапии рефрактерином и энергостимом и традиционной терапии на показатели качества жизни и клинико-функциональное состояние больных СН, обусловленной НЗМ, в зависимости от степени тяжести СН. Выявлен выраженный антиаритмический эффект рефрактерина и энергостима и их способность снимать и предотвращать развитие гликозидной интоксикации при СН незави-:имо от степени ее тяжести.
Впервые изучены особенности субпопуляционного состава лимфоцитов периферической крови больных с СН, обусловленной НЗМ, и возможность коррекции выявленных нарушений с помощью ПМГ.
Энергостим и рефрактерны могут быть также рекомендованы в качестве препаратов для лечения различных форм нарушений ритма и профилактики их возникновения на всех стадиях развития СН.
ПРАКТИЧЕСКАЯ ЗНАЧИМОСТЬ. Впервые показана эффективность применения рефрактерина и энергостима в терапевтическом стационаре для коррекции метаболических нарушений в миокарде у больных с СН, обусловленной НЗМ. Установлена корреляция биохимических и иммунологических показателей со степенью тяжести СН. Это позволило предложить новые критерии для диагностики, прогноза и коррекции СН при НЗМ. Выявлена корреляция биохимических показателей биоптатов и крови из коронарного синуса с аналогичными показателями периферической крови. Тем самым открыта возможность использовать методики определения содержания НАД, НАД-Н, цитохрома С, инозина, гликолитической активности, лак-тата и пирувата в периферической крови в сочетании с иммунологическими тестами определения экспрессии на мембранах Т-лимфоцитов гликопроте-идных молекул СД+-3, СД+-4, СД+-8 антигенов в качестве диагностических лабораторных тестов тяжести СН.
ВНЕДРЕНИЕ В ПРАКТИКУ. Методики определения содержания никотинамидадениндинуклеотида (НАД), его восстановленной формы (НАД-Н), цитохрома С, инозина, гликолитической активности, микрометоды контроля концентрации лактата и пирувата в периферической крови, а также иммунологические тесты определения экспрессии на мембранах Т-лимфоцитов гликопротеидных молекул СД-3, СД-4, СД-8 антигенов внедрены в практику работы кардиопульмонологического отделения МОНИКИ.
Разработанные способы лечения СН рефрактерином и энергостимом внедрены в терапевтическую практику в кардиопульмонологического отделении МОНИКИ, отделения кардиологии областного кардиологического
центра в г.Жуковский и кардиологического отделения Клинской районной больницы.
Материалы диссертационной работы легли в основу методических рекомендаций «Применение кардиотропного средства рефрактерина и анти-гипоксанта энергостима в лечении НЗМ».
АПРОБАЦИЯ РАБОТЫ. Основные положения диссертации представлены на II (Москва, 1996) и III (Москва, 1997) Всероссийском съезде «Человек и Лекарство», Всероссийской конференции «Прикладные аспекты исследований скелетных, сердечных и гладких мышц» (Пущино, 1996), московской областной конференции «Ишемия миокарда» (Жуковский, 1996), I Российском конгрессе по патфизиологии (Москва, 1996).
ОБЪЕМ И СТРУКТУРА ДИССЕРТАЦИИ. Диссертация состоит из введения, обзора литературы, глав, посвященных описанию материалов, методов и результатов исследований, их обсуждению, выводов, а также списка литературы, включающего _ работ отечественных и_- иностранных авторов.
Диссертационная работа состоит из _ печатных страниц, включая
_таблиц и _рисунков.
ОСНОВНЫЕ ПОЛОЖЕНИЯ, ВЫНОСИМЫЕ НА ЗАЩИТУ
1. Комплексная оценка клинико-функционального состояния больного с СН, обусловленной НЗМ, значений и соотношений биохимических показателей, характеризующих нарушение метаболических процессов в крови, миокарде, а также иммунологических сдвигов в крови является необходимым этапом при определении рациональной терапевтической тактики. При этом контроль биохимических показателей миокарда (биоптатов) может осуществляться путем оценки соответствующих показателей крови.
2. В качестве базовой терапии СН II-IV функционального класса (ФК) по классификации NYHA, обусловленной НЗМ, может быть использо-
ван трехнедельный курс рефрактерина в дозе 200 мг внутривенно капельно в 100 мл 5% раствора глюкозы (в случае противопоказаний к использованию глюкозы — в 100 мл физиологического раствора).
3. Применение энергостима и рефрактерина позволяет эффективно корректировать нарушения метаболизма в миокарде и крови. Тем самым получена возможность влиять на основной патогенетический механизм возникновения, развития и прогрессирования СН.
Достигнутая нормализация биохимических показателей определяет существенное повышение качества жизни больного, которое коррелирует с улучшением клинико-функционального состояния и показателей центральной гемодинамики при I-IV ФК СН.
4. Терапевтический эффект рефрактерина характеризуется отсутствием гликозидной интоксикации и способностью преодолевать рефрактер-ность миокарда к медикаментозному воздействию, а также выраженным антиаритмическим действием.
5. Энергостим при СН I-IV ФК по NYHA проявляет выраженный антигипоксический эффект, существенно снижает выраженность нарушений ритма и проводимости, улучшает центральную гемодинамику, повышает толерантность сердца к физической нагрузке и может быть рекомендован как средство для профилактики гликозидной интоксикации.
ОБЩАЯ ХАРАКТЕРИСТИКА МАТЕРИАЛА И МЕТОДЫ ИССЛЕДОВАНИЯ
В исследование включен 121 больной с различной степенью СН, обусловленной НЗМ (миокардит, миокардитический кардиосклероз (МК), ДКМП, АПС), в том числе 57 женщин и 64 мужчины в возрасте от 18 до 54 лет (средний возраст составил 39,3±8,2 лет) (Табл 1). С миокардитом было 44, с МК — 34, с ДКМП — 24, с АПС -19 больных (Табл 2).
ДЕМОГРАФИЧЕСКИЕ ПОКАЗАТЕЛИ ОБСЛЕДОВАННЫХ БОЛЬНЫХ
Все контрольная группа го основная группа <6 контрольная группа ункциональ I основная группа ный класс II контрольная группа сердечной основная группа 15 недостаточ» контрольная группа 24 ности III основная группа 25 контрольная группа 15 IV основная группа 16
Количество больных Средний возраст 60 38,5 ±8,5 61 40,1 ± 7,9 5 29,5 ± 3,4 29,7 ± 4,6 36,9 ± 8,2 33,1±6,8 40,5±9,6 38,9±692 39,8±7,5 38,6±6,6
Распоеделе- МУЖЧИН ние по полу: женщин Индекс массы 32 28 24,5 ± 2,3 32 29 24,5 ±1,8 3 2 23,8 ± 3,5 2 3 23,4 ± 4,3 10 6 24,5 ± 1,9 9 6 23,8 ± 2,9 13 11 26,8 ± 2,0 13 12 25,1 ±2,6 6 9 24,8 ± 2,9 8 8 24,6 ± 2,9
ПРИМЕЧАНИЕ: [индекс массы] = [масса, кг] / [рост, м]2
РАСПРЕДЕЛЕНИЕ БОЛЬНЫХ ПО ГРУППАМ С УЧЕТОМ НОЗОЛОГИИ, ТЯЖЕСТИ СН И ПРОДОЛЖИТЕЛЬНОСТИ ЗАБОЛЕВАНИЯ
Таблица 2.
Функциональным класс и длительность заболевания I ФК СН II ФК сн III ФК СН IV ФК СН Итого
Всего В тч с Д [мт. аяболеватя Всего В тч. с дпп. заболев»«* Всего В тч сдгмт мболеватя Всего В т.ч. с дшт. мболемтя
до 6 м- 6-1.5 г. 1,5-4 г > 4 лет до 6 м. 6-1,5 г. 1,5-4 г. > 4 лет до 6 м 6-1,5 г 1,5-4 г > 4 лет до 6 м 6-1,5 г 1,5-» г. > 4 лет
Группа НОЗОЛОГИЯ 5 о d Е 2 5 о f о Ж X О О i 2 X о О t О * Г О 1 2 X о О г о X О Контр. X и О Q. fX О У 5 о ё-х о V 5 о | Контр. X и о f S 5 О о. Е 2 X о О Контр. | 5 о Контр. | X о о Контр. X и О е- X О Ж X и О f 2 X о о 1 2 X и о f 2 X о О f 2 5 о 1 2
Миокардит 3 3 2 1 1 2 7 7 3 3 2 2 2 2 9 9 1 2 3 2 3 4 2 1 3 3 2 2 1 1 22 22
МК 2 2 1 1 1 1 8 7 3 1 3 2 2 4 5 4 1 1 2 2 3 3 3 1 1 2 2 18 16
ДКМП 0 2 2 7 7 1 2 2 1 1 1 3 3 4 4 1 1 1 2 2 1 11 13
АПС 0 0 4 4 1 1 3 3 6 5 1 1 3 3 2 1 10 9
Итого: 5 5 2 2 2 3 1 •f 5 16 5 6 3 5 4 4 4 25 24 2 5 6 5 9 10 8 4 16 15 2 3 3 3 6 6 5 3 61 60
Все обследованные больные рандомизированы в две группы: контрольную (60 больных со средним возрастом 38,5±8,5 лет) и основную (61 больной со средним возрастом 40,1±7,9 лет). В контрольной группе лечение проводили традиционной терапией, а в основной — рефрактерином и энерго-стимом.
В контрольной группе у 22 больных СН развилась на фоне миокардита, у 16 — МК, у 13 — ДКМП и у 9 — АПС. В основной группе у 22 больных СН обусловлена миокардитом, у 18 — МК, у 11 — ДКМП и у 10 — АПС). Клинические признаки СН I ФК по классификации Нью-Йоркской ассоциации сердца (NYHA) наблюдали у 8,1% больных основной и 8,4% контрольной группы, II ФК-у 25,2 и 26,3%, III ФК — у И0 и 39,4%, IV ФК — у 26,4 и 27,3%, соответственно.
При постановке диагноза миокардит использовали классификацию Н.Р.Палеева и соавт. (1982), а также рекомендации NYHA, дополненные Take и соавт. (1981) и Ю.И.Новиковым (1988). Диагностика основывалась и на морфологических критериях эндомиокардиальных биоптатов Higuchi и соавт. (1990), заключающихся в появлении двух и более лимфоцитов, окруженных миофибриллами, в одном поле зрения при увеличении в 400 раз.
Признаком МК считали сохранение в течение 12 и более месяцев после перенесенного миокардита патологических изменений ЭКГ, органический характер которых подтверждался функциональными пробами и эндо-миокардиальной биопсией. Исключение ИБС проводили по критериям, рекомендованным ВОЗ, на основе клинико-функционального исследования
Диагноз ДКМП ставили на основе клинических и гемодинамических признаков воспаления и клинического и инструментального исключения других возможных причин быстрого развития кардиомегалии.
Диагноз АПС ставили с учетом наличия II стадии хронического алкоголизма по классификации А.А.Портнова и Н.И.Пятницкой (1973).
Больные обеих групп с учетом ЭхоКГ показателей (фракция выброса (ФВ) и размеры ЛЖ) разделены на три подгруппы. Первую составили 10 больных с I ФК СН и 21 больной со II ФК СН, у которых сократительнная способность ЛЖ не была снижена. Во вторую подгруппу вошли 10 больных со II ФК СН и 26 больных с III ФК СН, у которых ФВ была менее 45%, а конечно-диастолический размер (КДР) ЛЖ не превышал 6,0 см. В третью подгруппу вошли 11 больных с III ФК СН и 20 больных с IV ФК СН, у которых ФВ не превышала 30%, а КДР ЛЖ был более 6,0 см..
В работе использовали следующие функциональные методы исследования: клинический, электрокардиографический, холтеровское мониториро-вание ЭКГ, рентгеноконтрастный, эндомиокардиальная биопсия.
ЭхоКГ исследования проводили на аппарате VINGMED/CFM-75 фирмы «Diasonics» с датчиком 2,5-3,5 МГц методами двухмерной и доп-плер-эхокардиографии с регистрацией в М- и В-импульсно-волновом и непрерывно-волновом режимах и синхронной записью ЭКГ. Доплер цветное картирование проводили по общепринятой методике (В.В.Зарецкий, 1979).
У всех больных определяли содержание пиридиновых нуклеотидов (Bessho и соавт., 1989; Katsumi и соавт., 1986), цитохрома С (С.Р.Мардашев и соавт., 1969; Chance, 1957; Rosenthal и соавт., 1943) и инозина (Bakken и соавт., 1982), гликолитическую активность (Klein и соавт., 1976), а также содержание лактата и пирувата энзиматическим методом с использованием наборов фирмы «Boehringer Mannheim» (Австрия).
Изучение механизма участия иммунокомпетентных клеток в патогенезе инфекционно-аллергического миокардита и влияния на него ПМГ про-зедено по методике Г.В.Порядина и соавт. (1996) на лимфоцитах 31 здоро-зого донора и 18 больных миокардитом со II-IV ФК СН.
Для ориентировочной оценки качества жизни больных использовали зопросник, разработанный Миннесотстким университетом (1986), со стра-
тификацией по ФК СН (Rector и соавт., 1987). Он содержит 21 вопрос и адаптирован для больных с тяжелой CH. Для более полной оценки качества жизни больных использовали вопросник психологического статуса больного (Testa и соавт., 1993).
Статистическую обработку и корреляционный анализ полученных данных проводили по общепринятым методикам (Г.Ф.Лакин, 1990). Различия принимали как существенные при Р<0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
ДЕЙСТВИЕ ЭНЕРГОСТИМА ПРИ ЛЕЧЕНИИ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ I-П ФК ПО NYHA У БОЛЬНЫХ С НЗМ.
Данная группа включает в себя 31 больного: 16 мужчин (7 в основной подгруппе и 9 в контрольной) и 15 женщин (6 и 9 соответственно). Средний возраст больных в основной подгруппе — 29,1 ±3,4 года, в контрольной -35,9±5,1 года. В ходе предварительного обследования с использованием указанных выше функциональных методов для уточнения ФК СН всем больным сделана ЭхоКГ с физической нагрузкой, которая и позволила выявить изменения фаз сердечного цикла, неадекватные нагрузке изменения ФВ, снижение толерантности к физической нагрузке (ЧСС не выше 120 уд./мин. при максимальной нагрузке не более 450 Вт).
При лечении больных контрольной группы использовали традиционную терапию нестероидными противовоспалительными препаратами: индо-метацин в суточной дозе 200 мг или ортафен 100мг, рибоксин по две таблетки (200 мг) три раза в сутки.
В основной подгруппе на фоне той же противовоспалительной терапии применяли энергостим в дозе 100-200 мг внутривенно капельно в 100 мл 5% глюкозы в течение 14 дней.
Применение энергостима ведет к повышению толерантности к физической нагрузке, что проявляется в исчезновении такого симптома СН, как быстрая утомляемость, улучшении эмоционального статуса пациентов, нормализации ЧСС, изменении индекса Опье в сторону уменьшения потребления миокардом кислорода, снижении ФК СН (Табл 3). Весьма заметные изменения происходят в данных ЭКГ и холтеровского мониторирования. Во время предварительного обследования и в основной и контрольной группе синусовая тахикардия наблюдалась у 71-72% больных, экстра и па-расистолия — 55%, миграция водителя ритма — 32%, метаболические изменения миокарда — 70% и АУ-блокада I степени у 75% больных. После лечения энергостимом произошло снижение частоты синусовой тахикардии до 40%, экстра и парасистолии — до 39,5%, миграции водителя ритма — до 18%, метаболических нарушений — до 42% У больных контрольной группы после проведения противовоспалительной и метаболической терапии уменьшение частоты нарушений ритма и проводимости происходит в значительно меньшей степени (Табл 4).
В отличие от традиционной терапии, при лечении энергостимом, происходит увеличение ФВ на 11%, — на 10%, улучшается диастоличе-ская функция ЛЖ: отношение УЕ/Уд уменьшается на 10,6% (с 1,77 до 1,60).
Наряду с улучшением внутрисердечной гемодинамики в крови нормализуется отношение лактат/пируват (уменьшается с 85,4 до 36,5), увеличивается отношение НАД/НАД-Н (с 0,6 до 0,9) и быстро снижается содержание инозина (с 1,5 до 0,5 нмоль/мл, Табл 5). Следует подчеркнуть, что в группе больных с 1-Н ФК СН стойкие положительные биохимические сдвиги происходят уже на седьмой день лечения энергостимом. В контрольной группе также наблюдается нормализация биохимических показателей, коррелирующая с улучшением качества жизни больных, но лишь на 13-й день лечения.
СРЕДНИЙ ФК И ТЯЖЕСТЬ СИМПТОМОВ СН, ОБУСЛОВЛЕННОЙ МИОКАРДИТОМ И МИОКАРДИТИЧЕСКИМ КАРДИОСКЛЕРОЗОМ, ДО И ПОСЛЕ ЛЕЧЕНИЯ ЭНЕРГОСТИМОМ. Таблица 3.
Показатель Контрольная группа (п=18) Основная группа (п-13)
До лечения После лечения До лечения После лечения
Средний ФК СН 1,94 ±0,15 1,61 ±0,11* 1,85 ±0,08 1,08 ±0,18**
Симптомы СН Одышка — ортопноэ — учащенное дыхание (5-1 балл) 2,16 ±0,12 0,20 ±0,14* 2,08 ± 0,25 0,15 ± 0,11*
Хрипы влажные по всем полям — единичные в нижних отделах (3-1 балл) 1,00 ±0,14 0,05 ± 0,07* 0,62 ±0,15 Отсутствуют
Отеки ног с асцитом и/или плевр, выпотом — пастозность голени (3 -1 балл) 0,61 ±0,12 0,05 ± 0,07* 0,46 ±0,19 Отсутствуют
Увеличение размеров печени (+1 см — 1 балл) 1,94 ±0,36 0,44 ±0,17* 1,85 ±0,28 Отсутствуют
ЧСС: -(91-110 уд/мин) — 1 балл: — (более 110 уд/мин) -2 балла. 0,60 ±0,19 0,20 ±0,10* 9,92 ± 0,08 Отсутствуют
ПРИМЕЧАНИЕ: *- при сравнении средних величин до и после лечения внутри групп достоверность различий Р< 0,001 -0,05.
** — при сравнении с соответствующими значениями контрольной группы достоверность различий Р < 0,001 — 0,05.
ы
Содержание лактата и пирувата, НАД, НАД-Н, инозина, цитохрома С в крови больных НЗМ
до и после лечения энергостимом
ФК СН по ЫУНА НАД нмоль/мл НАД-Н нмоль/мл НАД + НАД-Н нмоль/мл НАД / НАД-Н Лактат мкмоль/мл Пируват мкмоль/мл Лактат / пируват Цитохром С нмоль/мл Инозин нмоль/мл
до лечении после лечения 11,8±2,9 17,1±2,2* 20,0±2,9 18,3±3,3 30,1±2,6 36,6±3,1* 0,60±0,08 0,92±0,16* 2,2±0,8 1,4±0,3* 35,3±9,1 43,3±11,4 65±6 36,7±13,8* 1,26±0,32 2,00±0,10* 1,50±0,20 0,98±0,32*
до лечения после лечения 8,99±2,19 12,30±1,25* 17,8±2,7 16,3±3,8 21,2±3,6 26,2±3,2 0,46±0,15 0,78±0,13* 5,6±0,9 2,3±0,6* 23,9±6,8 37,6±5,7 275±62 61±25* 0,95±0,27 1,63±0,35* 1,8±0,5 1,2±0,3
ПРИМЕЧАНИЕ: *- достоверность различий средних до и после лечения в каждой группе 0,001 < Р < 0,05.
ДЕЙСТВИЕ ЭНЕРГОСТИМА НА НАРУШЕНИЯ РИТМА И ПРОВОДИМОСТИ У БОЛЬНЫХ С СН 1-11 ФК ПО МУНА _Таблица 4.
ПРИЗНАКИ В контрольной группе (п=16) В основной группе (п-15)
до лечения после лечения до лечения после лечения
Тахикардия 11 7 11 6
Очаговая дистрофия миокарда 12 9 10 6
Экстрасистолия: предсердная желудочковая 5 4 6 3
3 2 2 1
Парасистолия 1 1 1 1
Параксизмальная тахикардия 9 7 8 2
Параксизм фибрилляции предсердий 1 0 1 0
АУ блокада 1 степени II степени 12 0 11 0
2 0 2 0
Эктопический ритм и миграция водителя ритма 4 4 4 2
Блокады ножек пучка Гиса: БПНПГ БПВЛНПГ 4 4 3 3
3 3 2 2
Гипокалиемия 3 2 3 1
Слабость синусового узла 0 0 0 0
ДЕЙСТВИЕ ЭНЕРГОСТИМА ПРИ ЛЕЧЕНИИ СЕРДЕЧНОЙ
НЕДОСТАТОЧНОСТИ Ш-1У ФК ПО ГЧУНА У БОЛЬНЫХ С ЮМ.
В этом разделе описаны результаты исследования действия энерго-стима, полученные на группе из 23 больных (15 мужчин, 8 женщин, средний возраст 40,5±4,5 лет), у которых СН развилась на фоне АПС (17 случаев) и ДКМП (6 случаев). Контрольную группу составили 13 больных, основную -10.
Больные контрольной группы получали лечение комбинацией диуретика (фуросемид в дозе 40 мг в сутки), вазодилататора (нитросорбид 80 мг или оликард по одной капсуле в сутки) и рибоксина (внутривенно 200 мг или по две таблетки три раза в день).
В основной подгруппе на фоне применения диуретика (в случае приступов одышки и снижения диуреза) и вазодилататора проводили лечение антигипоксическим препаратом энергостимом в дозе 200 мг в сутки внутривенно капельно в 100 мл 5% раствора глюкозы.
В контрольной группе выраженность симптомов СН на протяжении 21-24 дней лечения уменьшается на 58,6%, а средний ФК- на 12,0% (Табл 6).
Однако улучшение клинических симптомов СН в этой группе не сопровождается улучшением центральной гемодинамики: не изменяются КСР и КДР ЛЖ и ПЖ, а также УсГ, отсутствуют достоверные изменения ФВ и минутного объема (МО), нет существенного снижения давления в легочной артерии (ЛА). Таким образом, под воздействием терапии комбинацией диуретика, вазодилататора и рибоксина происходит диссоциация между симптомами ХСН, развившейся в связи с НЗМ, и показателями центральной гемодинамики, структурно-функциональным состоянием сердца.
Терапия энергостимом приводит к более выраженному ослаблению симптомов СН. Средний ФК СН уменьшается на 34% (с 3,15±0,15 до 2,1±0,2 Р<0,001) (Табл 6). Важно, что, в отличие от стандартной терапии, при лечении энергостимом происходит не только более существенное изменение клинических проявлений СН в сторону улучшения, но и значительно уменьшается КДР, КСР ЛЖ и КДР ПЖ (на 18%, 19% и 15% соответственно), возрастает на 24% скорость циркулярного укорочения волокон (Усг), на 26% ФВ и на 32% МО. При этом среднее давление в ЛА уменьшается с 26 до 16 мм рт.ст.
Системное артериальное давление (АД), как и в контрольной группе, достоверно не изменяется. Судя по изменению индекса Опье, только при лечении энергостимом снижается потребность миокарда в кислороде.
Если до курса энергостима фибрилляция и трепетание предсердий имели место у 41,2% больных основной группы, то после лечения эти нарушения ритма сохраняются только у 17,6% больных. Улучшение энергетических процессов в миокарде, по-видимому, лежит в основе нормализации БТ-Т, положительной динамики очаговой дистрофии.
Также отмечено улучшение метаболических процессов и электролитного дисбаланса (гипокалиемии), но в значительно меньшей степени, чем в основной группе.
Следует подчеркнуть, что на фоне терапии энергостимом в трех слу-[аях брадисистолической формы мерцательной аритмии наблюдалось уча-цение ритма до нормосистолии, а у двух больных произошло восстановле-ше синусового ритма.
В результате трехнедельного курса лечения энергостимом содержа-ше лактата в крови уменьшается в 2,9 раза. Так как содержание пирувата 1ри этом не изменяется, то отношение лактат/пируват резко снижается (в 3,5 1аза) и достигает уровня нормы. Содержание НАД возрастает в 1,85 раза, а 1АД-Н, наоборот, уменьшается в 1,6 раза. Это ведет к нормализации соот-гошения пиридиновых нуклеотидов и, как следствие, восстановлению регуляции этим соотношением соответствующих биоэнергетических процессов, частности, гликолитической активности эритроцитов, которая возрастает в ,5 раза по сравнению с уровнем, зафиксированным в контрольной группе Табл 5). Содержание основного фермента электронтранспортирующей ;епи митохондрий, цитохрома С, повышается в 1,6 раза.
Описанные биохимические сдвиги в крови при АПС и ДКМП оказа-ись аналогичными биохимическим сдвигом, зафиксированным в миокарде помощью эндокардиальной биопсии. Это означает, что при ДКМП и АПС крови, так же, как и в миокарде, развивается энергетический дефицит, а нергостим устраняет это энергодефицитное состояние. Следовательно, в словиях клиники по картине биохимических показателей крови с опреде-енной степенью вероятности можно судить о процессах, происходящих в :иокарде, и контролировать эффективность лечения энергостимом, рефрак-ерином и другими лекарственными средствами.
В контрольной группе, несмотря на применение рибоксина (инозина), зменения ни одного из перечисленных выше показателей не документиру->тся, за исключением некоторого снижения содержания лактата и тенден-ии к снижению инозина.
Применение энергостима сопровождается существенным повышением качества жизни больных (Табл 6).
ДЕЙСТВИЕ РЕФРАКТЕРИНА ПРИ ЛЕЧЕНИИ БОЛЬНЫХ С ХРОНИЧЕСКОЙ СН П-Ш ФК ПО NYHA.
В эту группу вошли больные с СН II ФК (10) и III (26) с ФВ от 45%
до 30% и КДР ЛЖ не более 6,0 см. Средний возраст — 37,5±5,3 лет. В контрольной группе лечение проводили традиционным способом комбинацией СГ (строфантин К 0,05% 1,0 внутривенно, затем дигоксин в суточной дозе 0,25 мг) диуретика и вазодилататора, усиленной рибоксином. Средний ФК СН в этой группе больных до начала лечения составлял 2,69±0,23 или по балльной оценке выраженности симптомов СН — 10,24+0,85 балла (Табл 7).
В основной подгруппе лечение больных проводили рефрактери-ном в дозе 200 мг в 100 мл 5% раствора глюкозы, а при низком диурезе и выраженной одышке усиливали диуретиком (лазикс внутривенно или фурасемид в дозе 40 мг в сутки per os). Средний ФК в этой подгруппе до начала лечения был 2,63+0,08 при общей сумме баллов тяжести симптомов СН равной 10,1+0,75 (Табл 7).
Применение рефрактерина приводит к быстрому и выраженному улучшению состояния больных (Табл 7). В результате ни один из них не остается в исходном ФК СН и к двадцатому дню лечения средний ФК снижается до 1,7±0,1 (в контрольной группе до 2,22±0,18).
Урежение ритма на 15% у больных контрольной группы в шести случаях осложнилось гликозидной интоксикацией, появлением желудочковой экстрасистолии, что требовало уменьшить дозы или вовсе отменить СГ. В основной группе ЧСС уменьшается на 25%, и ни в одном случае интоксикация не отмечена.
Данные ЭхоКГ исследований свидетельствуют, что под влиянием рефрактерина КДР и КСР ЛЖ уменьшаются на 23,0% и 15,0%, соответственно, а аналогичные характеристики ПЖ-на 12,0% и 15,0%, Vcf увеличи-
Таблица 6.
ДЕЙСТВИЕ ЭНЕРГОСТИМА НА ФК, СТЕПЕНЬ ВЫРАЖЕННОСТИ СИМПТОМОВ И КАЧЕСТВО ЖИЗНИ БОЛЬНЫХ ХСН МНУ ФК ПО ИУНА
Функциональный класс и оценка тяжести симтомов в баллах Контрольная группа (п-13) Основная группа (п=10)
До лечения После лечения До лечения После лечения
Средний функциональный класс сердечной недостаточности 3.16 ±0,25 2,79 ±0,18 3,15 ± 0,15 2,10 ±0.21
Симптомы сн Одышка — ортопноэ — учащенное дыхание (5-1 балл ) 3,81 ±0,15 2,77 ± 0,25 3,91 ±0,18 1,38 ±0,22
Хрипы влажные по всем полям — единичные в нижних отделах (3-1 1.69 ±0,20 0,33 ±0,13 1,68 ±0,15 0,25 ±0,12
Отеки ног с асцитом и/или плевр, выпотом — пастоэность голени (3 -1 2,36 ±0,15 0,48 ±0,15 1,75 ±0,21 0,23 ±0,15
Увеличение размеров печени (+1 см — 1 балл) 3,15 ± 0,15 1,15 ±0,35 3,45 ± 0,21 0,45 ±0,16
ЧСС: — ( 91 -110) -1 балл; — (более 110) -2 балла. 3,15 ±0,15 1,15 ±0,35 3,45 ±0,21 0,45 ±0,16
Обшая сумма 17,35 ±0,20 8,65 ± 0,30 17,40 ±0,20 4,85 ± 0,20
Качество жизни Тяжесть ХСН по Миннесотовскому опроснику 3,15 ±0,17 2,75 ±0,18 3,20 ± 0,20 1.20 ±0,15
Психологически хорошее самочувствие 2,41 ±0,15 2,85 ± 0,20 2,35 ±0,13 3,37 ± 0,37
Нарушение сна 2,89 ±0.14 1,65 ±0,15 2,84 ±0,13 0,75 ±0,15
Психологическое самочувствие 2,60 ± 0,15 2,01 ±0,18 2,54 ±0,15 1,21 ±0,23
[Хорошее самочувствие 2,58 ±0,15 2,65 ±0,13 2,62 ± 0,21 2,95 ± 0,05
Таблица 7. ДЕЙСТВИЕ РЕФРАКТЕРИНА НА СРЕДНИЙ ФК. СТЕПЕНЬ ВЫРАЖЕННОСТИ СИМПТОМОВ И КАЧЕСТВО ЖИЗНИ БОЛЬНЫХ ХСН Н-Ш ФК ПО МГНА
Функциональный класс и оценка тяжести симтомов в баллах Контрольная группа (п=18) Основная группа (п=18)
До лечения После лечения До лечения После лечения
Средний ФК СН 2,69 ± 0,23 2,22 ±0,18 2,63 ± 0,08 1,70 ±0,10
Симптомы СН Одышка — ортопноэ — учащенное дыхание (5-1 балл ) 3,31 ±0,21 1,94 ±0,06 3,25 ± 0,24 0,40 ±0,19
Хрипы влажные по всем полям — единичные в нижних отделах (3-1 балг ) 1,20 ±0,25 0,18 ±0,01 1,42 ±0,24 0,10 ±0,08
Отеки ног с асцитом и/или плевр, выпотом — пастозн. голени (3 -1 балл) 1,65 ±0,21 0,29 ±0,16 1,48 ±0,20 отсутствуют
Увеличение размеров печени (+1 см — 1 балл) 2,98 ± 0,58 0,82 ± 0,33 3,01 ±0,31 0,40 ± 0,20
ЧСС: — (91-110)-1 балл; — (более 110) — 2 балла. 1,10 ±0,36 0,41 ±0,13 0,94 ± 0,22 отсутствуют
Общая сумма 10,24 ±0,85 3,84 ±0,15 10,10 ±0,75 0,90 ± 0,20
Качество жизни Тяжесть ХСН по Миннесотовскому опроснику 3,53 ±0,21 2,85± 0,23 3,62± 0,24 1,85± 0,23
Психологически хорошее самочувствие 2,14 ± 0,17 2,05 ±0,17 2,25 ± 0,37 3,21 ±0,18
Нарушение сна 2,19± 0,23 1,82 ±0,19 2,17 ±0,23 0,92 ± 0,09
Психологическое самочувствие 2,38 ±0,17 2,05 ±0,16 2.41 ±0,31 1.52 ±0,15
Хорошее самочувствие 2,00 ±0,15 2,23 ±0,10 1,90 ± 0,15 2,75 ± 0,09
вается на 28%, а ФВ — на 12%, происходит существенное снижение общего периферического сопротивления (ОПС) и давления в JIA. Улучшение систолической функции сердца под влиянием рефрактерина сопровождается выраженным улучшением его диастолической функции (Рис 1).
Стандартная терапия, усиленная рибоксином, при продолжительности 35-40 дней не ведет к достоверному изменению всех названных выше показателей.
Нормализация показателей центральной гемодинамики под влиянием рефрактерина коррелирует с изменением отношения лактат/пируват (падает более, чем в 3 раза), отношения НАД/НАД-Н (увеличивается в 1,37 раза), а также со снижением содержания инозина (в 1,5 раза) (Рис 2). В ту же сторону изменяются соответствующие показатели биоптатов миокарда.
В случае стандартной терапии имеет место, хотя и в существенно меньшей степени, чем под влиянием рефрактерина, снижение отношения лактат/пируват и проявляется тенденция к снижению содержания инозина в плазме крови.
Исходные значения показателей качества жизни больных обеих групп существенно не различаются. В результате применения рефрактерина динамика показателей качества жизни достоверно улучшается, тогда как в контрольной группе заметного влияния не отмечается (Табл. 7). Это дает основание говорить о более благоприятном прогностическом значении монотерапии рефрактерином.
ДЕЙСТВИЕ РЕФРАКТЕРИНА ПРИ ЛЕЧЕНИИ БОЛЬНЫХ С НЗМ, ОСЛОЖНЕННЫМИ СН Ш-IV ФК ПО NYHA.
Контрольную группу составили 10 больных НЗМ с СН IV ФК и 5 с Ш
ФК с резко сниженной сократительной функцией миокарда (ФВ менее 30%, КДР более 6,0 см). В основную группу, получавшую терапию рефрактерином, вошли 10 больных с СН IV ФК и 6 с III ФК и соответствующими значениями ФВ и КДР.
Изменения показателей относительно исходного уровна (до лечения) в процентах
100 п
||
Лактат/пирумт НШ
I
МП
Инозин Н
Цитохроы С НАД ЯЯ НАД/НАД-Н 99 Гликолитмческая
активность
НАД-Н
Рае. 2. Д
После применения традиционной терапии комбинацией строфантина К 0,05% 1 мл или корглюкона 0,06% 1мл внутривенно, вазодилататора (оликард-40 по одной капсуле один раз в сутки или изокет 40 мг внутривенно капельно) и диуретика (лазикс в дозе 40-60 мг, а затем фурасемид в дозе 40-80 мг per os), усиленной введением метаболического препарата (рибоксиин 200 мг внутривенно или per os 6 таблеток по 200 мг в сутки) в течение одного месяца происходит уменьшение среднего ФК СН на 8% (с 3,7±0,2 до 3,3+0,1 при Р< 0,01).— до лечения
— после традиционном терапии достоверность различий Р < 0,01
** — достоверность различий Р< 0,001
Следует отметить, что уменьшение перечисленных симптомов СН и показателей центральной гемодинамики в группе больных, леченных реф-рактерином, сопровождается уменьшением индекса Опье (Рис 4Б), тогда как у больных в контрольной подгруппе, получавших стандартную терапию, потребность миокарда в кислороде остается высокой.
Таким образом, лечение рефрактерином ведет к уменьшению симптомов СН, что коррелирует с улучшением показателей центральной гемодинамики, а также снижением постнагрузки (уменьшением ОПС) и предна-грузки, тогда как при стандартной терапии уменьшение симптомов СН не сопровождается существенным улучшением центральной гемодинамики.
В контрольной группе, несмотря на применение в комбинации рибоксина, нет существенного снижения соотношения лактат/пируват, степень повышения которого отражает тяжесть СН. Не повышается уровень глико-литической активности эритроцитов и плазмы крови. Отсутствие уловимых изменений в указанных показателях, по-видимому, является следствием того, что стандартная терапия, усиленная рибоксином, не приводит к повышению содержания НАД, и соответствующему снижению содержания НАД-Н, отношение которых, также как и их абсолютное содержание, является важным фактором в регуляции процесса гликолиза и цикла трикарбоновых кислот.
Указанные изменения в периферической крови достоверно отражают изменения в биоптатах и крови из коронарного синуса.
Adam и соавт. (1983) высказано предположение, что существует зависимость между отношением НАД/НАД-Н и механическим резервом сердечной мышцы. Методом поверхностной флуориметрии установлено влияние НАД на микроциркуляцию в миокарде (Kedem и соавт., 1981 и Костин и соавт., 1989).
Отношение НАД/НАД-Н отражает состояние ключевых звеньев цикла Кребса, гликолиза и переноса протонов в цепь окислительного фосфори-лирования, тогда как отношение лактат/пируват, которое традиционно используется для оценки тяжести ишемических и гипоксических процессов в миокарде, характеризует лишь зависимость процесса гликолиза от уровня кислорода в клетке. Более того, показана взаимосвязь между повышением содержания НАД-Н и степенью повышения ЧСС.
Многофакторный корреляционный анализ выявил взаимосвязь отношения НАД/НАДН не только с ФК СН, но и с Усс, диастолическим показателем Уе / Уа, что позволяет сделать вывод о значении биохимического теста НАД/НАД-Н в прогнозе течения НЗМ (Рис 5).
Рис. 5. Взаимосвязь суммы и отношения пиридиновых нуклеотидов с ФК СН
Суммарное содержание НАД и НАД-Н, нмоль/мл
ИЗМЕНЕНИЕ ИММУНОЛОГИЧЕСКИХ ПОКАЗАТЕЛЕЙ В ЗАВИСИМОСТИ ОТ ФК СН И ВЛИЯНИЕ ПМГ НА НИХ
При миокардитах наблюдается повышение количества СБ8+ — клеток в периферической крови по сравнению со здоровыми людьми, мало зависящее от ФК СН. У больных с Ш-ГУ ФК СН наблюдается существенное повышение СБ4+-клеток, а у пациентов с II ФК СН их количество снижается.
ПМГ (0,1 — 10 нМ) не влияет на фетогемаглютинин (ФГА)-индуцированную пролиферацию лимфоцитов здоровых доноров и в 2-3 раза усиливает включение 3Н-тимидина лимфоцитами больных миокардитом с II-
III ФК СН. Лимфоциты больных с IV ФК СН демонстрируют ослабленный ответ на ПМГ. Кратковременная (1 час) инкубация лимфоцитов больных миокардитом с ПМГ (1 нМ) вызывает повышение числа С04+-клеток, выделенных из крови пациентов с II-III ФК и не влияет на поверхностный фенотип лимфоцитов больных с IV ФК СН. Продолжительная (16 часов) инкубация с ПМГ (1 нМ) лимфоцитов больных миокардитом с П-ШФК СН вызывает повышение числа С04+-клеток и снижение доли С08+-лимфоцитов.
Полученные результаты, с одной стороны, демонстрируют выраженный иммуномодулирующий эффект ПМГ при миокардитах, а с другой — косвенно указывают на нарушение рецепции и, возможно, продукции ПМГ у больных с тяжелым течением заболевания. Последнее наблюдение может иметь определенную диагностическую ценность, а также создает предпосылки для изучения возможностей клинического использования ПМГ.
ВЫВОДЫ: 1. У больных некоронарогенными заболеваниями миокарда усиление тяжести сердечной недостаточности сопровождается снижением содержания никотинамидадениндинуклеотида, цитохрома С и глико-литической активности, повышением содержания инозина и отношения лактат/пируват.
2. Биохимические сдвиги в крови коррелируют с аналогичными показателями биоптатов миокарда.
3. Применение рефрактерина и энергостима обусловило восстановление нормального содержания и соотношения пиридиновых нуклеотидов, цитохрома С, лактата и пирувата, повышение гликолитической активности крови, улучшение функциональной способности кардиомиоцита и миокарда в целом.
4. На фоне терапии рефрактерином и энергостимом улучшается клиническое состояние больных, снижается функциональный класс сердечной недостаточности, уменьшаются объемы камер сердца, повышается фракция
выброса и диастолическая функция миокарда, что приводит к улучшению качества жизни больных. При применении рефрактерина не наблюдается гликозидной интоксикации.
5. In vitro установлена способность пептидного морфогена гидры корректировать иммунологические сдвиги в лимфоцитах периферической крови. Это создает возможность использовать его как иммуномодулирую-щее средство в лечении миокардита.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ. 1. Так как достоверно установлена корреляция между биохимическими показателями биоптатов миокарда, крови из коронарного синуса и периферической крови, рекомендовать в качестве лабораторного теста тяжести СИ при НЗМ и контроля эффективности действия лекарственных средств определение содержания НАД, НАД-Н и их отношения, цитохрома С, инозина, лактата и пирувата, а также гликолитической активности в периферической крови.
2. Рекомендовать больным с НЗМ, осложненными СН II ФК, применение кардиотропного средства рефрактерина в дозе 200 мг в сутки внутривенно капельно в 100 мл глюкозы или физиологического раствора в течение 14 дней, а больным с III-IV ФК СН и существенно сниженной ФВ-курс рефрактерина в дозе 300 мг в сутки внутривенно капельно в течение 21-30 дней.
3. Применять антигипоксическое средство энергостим больным с I-IV ФК СН, развившейся при НЗМ и особенно при АПС, в дозе 200 мг внутривенно капельно в 100 мл физиологического раствора на протяжении 10-25 дней в зависимости от тяжести СН.
4. Рекомендовать использование определения экспрессии гликопроте-идных молекул CD+-3, CD+-4, CD+-8 — антигенов на мембранах Т-пимфоцитов в качестве лабораторного теста тяжести иммуно-зоспалительного процесса.
ПУБЛИКАЦИИ ПО ТЕМЕ ДИССЕРТАЦИИ
1. Лечение рефрактерином хронической сердечной недостаточности, обусловленной некоронарогенными заболеваниями миокарда. Кардиология. -1997,- № 3.- С.51-55. (соавт.: Палеев Н.Р., Пронина В.П., Сукоян Г.В., Кар-санов Н.В.).
2. Применение энергостима при лечении тяжелой хронической сердечной недостаточности, обусловленной алкогольным поражением сердца. Клим. мед.. -1997,- № 4. — С.35-41. (соавт.: Палеев Н.Р., Пронина В.П., Кар-санов В.Н., Сукоян Г.В., Карсанов Н.В.).
3. Действие нового кардиотропного препарата рефрактерина и антиги-поксического, антиишемического средства энергостима на некоторые биохимические показатели крови и биоптатов в процессе лечения сердечной недостаточности. Матер. Всероссийской конференции «Прикладные аспекты исследований скелетных, сердечных и гладких мышц». — Пущино. 1996,-С.125-126. (соавт. Палеев Н.Р., Сукоян Г.В., Карсанов Н.В.).
4. Применение рефрактерина при сердечной недостаточности у больных с некоронарогенными заболеваниями миокарда. Матер. III Российского национального конгресса «Человек и лекарство». — Москва. 1996. — С. 18. (соавт. Палеев Н.Р., Сукоян Г.В., Карсанов Н.В.).
5. Оценка методом допплер-эхокардиографии эффективности лечения сердечной недостаточности рефрактерином. Матер. III Российского национального конгресса «Человек и лекарство». — Москва. 1996. — С.181. (соавт.: Палеев Н.Р., Пронина В.П., Сукоян Г.В., Карсанов Н.В.).
6. Иммуномодулирующий эффект пептидного морфогена гидры у больных иефекционно-аллергическим миокардитом in vitro. — Доклад на I Российском конгрессе по патфизиологии, — Москва, 17-19 октября 1996. -С.68-71. (соавт.: Казимирский А.Н., Салмаси Ж.М., Макарков А.И., Шуга-нов Е.Г., Порядин Г.В.).
7. Применение рефрактерина при сердечной недостаточности у больных с некоронарогенными заболеваниями миокарда. Матер, научно-практической кардиологической конференции «Актуальные вопросы лечения хронических форм ИБС».- Жуковский. 1996. — С.52-53 (соавт.: Палеев Н.Р., Сукоян Г.В., Карсанов Н.В.).
8. Оценка методом доплер-эхокардиографии эффективности лечения сердечной недостаточности рефрактерином. Матер, научно-практической кардиологической конференции «Актуальные вопросы лечения хронических форм ИБС». — Жуковский. 1996. — С.53-54 (соавт.: Палеев Н.Р., Пронина В.П., Сукоян Г.В., Карсанов Н.В.).
Физиология, потребность миокарда в кислороде — StatPearls
Введение
Сердечно-сосудистая система представляет собой сложную сосудистую сеть, которая обеспечивает кровью и кислородом все тело. Потребность миокарда в кислороде — это количество кислорода, которое требуется сердцу для поддержания оптимальной функции, а снабжение миокарда кислородом — это количество кислорода, поступающего в сердце кровью, которое контролируется коронарными артериями. Когда организм работает в оптимальном физиологическом состоянии, снабжение миокарда кислородом не превышает потребности миокарда в кислороде [1].
Функция
Поскольку сердце работает исключительно в рамках аэробного метаболизма, митохондрии миокарда должны поддерживать изобилие кислорода для продолжения окислительного фосфорилирования. Частота сердечных сокращений, сократимость и напряжение стенки желудочка — три фактора, определяющие потребность миокарда в кислороде. Увеличение любой из этих переменных требует от организма адаптации, чтобы поддерживать адекватное поступление кислорода к сердцу.
Считается, что частота сердечных сокращений является наиболее важным фактором, влияющим на потребность миокарда в кислороде.При учащении пульса миокард должен работать тяжелее, чтобы завершить сердечный цикл более эффективно. При сокращении сердечного цикла время диастолы сокращается. Поскольку диастола заканчивается преждевременно, количество крови, которая обычно заполняет желудочки, уменьшается, и насыщенный кислородом гемоглобин не может достигать субэндокарда. В оптимальных условиях потребность миокарда в кислороде будет равна поставке кислорода миокарду; однако, когда есть структурное повреждение от бляшки, которая препятствует потоку, может быть несоответствие между спросом и предложением, что приводит к ишемии.
Сократимость или инотропизм — это скорость увеличения внутрижелудочкового давления во время сокращения при данной длине мышечного волокна. Интересно, что миоциты обладают врожденной способностью сокращать мышцы любой длины. Эта сила измеряется после закрытия митрального клапана и до открытия аортального клапана, в течение которого внутрижелудочковый объем остается постоянным.
На сократимость влияют различные внутренние и внешние силы, включая концентрацию кальция.Кальций высвобождается саркоплазматической сетью сердечной мышцы и связывается с тропонином C. Эта связь стимулирует конформационные изменения тропомиозина, которые высвобождают его из участков связывания на актиновой нити. При высвобождении тропомиозина активные центры актина могут свободно связывать миозин, который вызывает расщепление аденозинтрифосфата (АТФ) на аденозиндифосфат (АДФ) и неорганический фосфат (P). Затем происходит силовой удар миозиновой головки, который заставляет актиновую нить по центру к саркомеру, и АДФ и Р отделяются от миозиновой головки, что приводит к сокращению.Как только АТФ снова присоединяется к миозину, актин высвобождается. Этот цикл продолжается до тех пор, пока внутриклеточные запасы кальция не истощатся, не прекратится связывание тропонина С и кальция, и тропомиозин может вернуться к своему первоначальному подтверждению, чтобы покрыть сайты связывания на актине. Следовательно, внутриклеточная концентрация кальция прямо пропорциональна силе сокращения [2].
Натяжение стенки желудочка зависит от толщины миокарда желудочка. Закон Лапласа гласит, что натяжение стенки желудочка пропорционально радиусу желудочка и внутрижелудочковому давлению.У пациентов с ишемической болезнью сердца снижается снабжение миокарда кровью и кислородом. В этом случае сократимость снизится. Поскольку желудочек больше не может адекватно сокращаться, конечный систолический объем увеличится. Избыток крови, остающийся в желудочке, вызовет расширение радиуса желудочка и внутрижелудочковое давление, что приведет к более высокому натяжению стенки.
Механизм
Способность крови переносить кислород и поток через коронарные артерии регулируют снабжение миокардом кислородом.Переносимость кислорода может быть уменьшена при нескольких состояниях, которые включают либо снижение концентрации эритроцитов, либо снижение насыщения гемоглобина кислородом. Например, при анемии количество здоровых эритроцитов ниже среднего. Несмотря на то, что красные кровяные тельца могут быть полностью насыщены кислородом, их недостаточно для снабжения мышц достаточным количеством кислорода. Обычно это вызвано недостатком в питании железа, витамина B12 или фолиевой кислоты, который легко исправить.Однако могут быть более разрушительные причины, такие как талассемия, серповидно-клеточная анемия и различные врожденные дефициты ферментов, которые труднее лечить [1] [3].
Гемоглобин — это часть эритроцита, переносящая кислород, и он полностью насыщается, когда связывает четыре молекулы кислорода. С каждой молекулой кислорода, которую гемоглобин выделяет в ткани, он связывает оставшиеся молекулы кислорода с большим сродством. Обычно гемоглобин рассеивает только одну молекулу кислорода, прежде чем он вернется в легкие и снова станет полностью насыщенным.Окись углерода связывается с гемоглобином с гораздо большим сродством, чем кислород. Когда гемоглобин возвращается в легкие для повторной оксигенации, он обычно имеет одно или два из четырех доступных пространств связывания [1] [3].
Так как окись углерода связывается с гемоглобином с более высоким сродством, чем кислород, он защищает пустые места связывания гемоглобина быстрее, чем поступающий кислород. К этому моменту гемоглобин насыщен кислородом на пятьдесят — семьдесят пять процентов, а оксидом углерода — на двадцать пять — пятьдесят процентов.Несмотря на то, что к гемоглобину прикреплены молекулы кислорода, он не выделяет их в тканях. Это происходит потому, что сродство гемоглобина к кислороду обратно пропорционально его насыщению кислородом. Следовательно, возникающая гипоксия возникает не из-за недостатка кислорода, а скорее из-за более высокого сродства гемоглобина к кислороду, когда он лишь частично насыщен им [1] [3].
Несмотря на то, что способность переносить кислород может влиять на снабжение миокарда кислородом, коронарный кровоток является основным определяющим фактором снабжения кислородом.Кровоток в коронарной артерии зависит от давления, деленного на сопротивление. Потребление кислорода миокардом равно коронарному кровотоку, умноженному на разницу артериально-венозного кислорода. Во время диастолы желудочки получают кровь до систолического сокращения. Эта фаза наполнения сердечного цикла позволяет коронарным артериям обеспечивать максимальный приток крови к сердцу. Кроме того, это единственная фаза сердечного цикла, которая позволяет крови достигать субэндокарда, который является наиболее дистальной частью [1] [3].
Патофизиология
Повышение потребности миокарда в кислороде может стать клинически значимым, если оно превышает поступление кислорода в миокард. Это может произойти на более поздних стадиях ишемической болезни сердца (ИБС). За годы плохо контролируемой гиперлипидемии у пациента могут развиться атеросклеротические бляшки в основных артериях, кровоснабжающих сердце. Как только целостность сосудистой сети нарушена, могут развиваться бляшки, которые начинают сокращать диаметр коронарных артерий [1].
Клиническая значимость
Как только сосуд окклюзируется более чем на семьдесят процентов, у пациента обычно появляются симптомы. Обычно эти симптомы, такие как боль в груди, одышка при нагрузке и потоотделение, проявляются во время активности или стресса, когда сердцу требуется больше кислорода. Это классифицируется как стабильная стенокардия. Однако, как только симптомы начинают проявляться после меньшей физической активности или в состоянии покоя, болезнь прогрессирует до восьмидесятипроцентной окклюзии, и может быть поставлен диагноз нестабильная стенокардия [4] [5].
Лицо, поступившее в отделение неотложной помощи со стенокардией, должно быть обследовано на предмет несоответствия предложения и потребности миокарда в кислороде. Первый тест для определения этого — электрокардиограмма (ЭКГ) в 12 отведениях, которая измеряет электрическую активность сердца. Сегмент ST представляет собой время между деполяризацией желудочков и реполяризацией желудочков. Если сегмент ST повышен по прибытии, это может указывать на острый инфаркт миокарда; однако, если имеется депрессивный сегмент ST, это может быть признаком острой ишемии [2] [4].
Если ЭКГ ничем не примечательна, кардиологи могут провести тест с физической нагрузкой. В контролируемой среде кардиологи могут контролировать кровяное давление пациента, сатурацию кислорода и электрическую активность сердца. Выполняя упражнения, пациент заставляет сердце увеличивать частоту и сократимость, тем самым повышая потребность миокарда в кислороде. Если сосуды атеросклеротические, сердце не сможет адаптироваться к изменениям спроса, поэтому будет несоответствие между спросом и предложением, которое будет соответственно представлено на ЭКГ [6] [4].
Кроме того, если у пациентов есть противопоказания к ЭКГ с физической нагрузкой, они могут пройти визуализацию перфузии миокарда (MPI). Визуализацию перфузии миокарда можно использовать для исследования миокарда на предмет дефицита кислородного снабжения миокарда из-за атеросклеротических бляшек от ишемической болезни сердца. Сначала пациентам вводят аналог аденозина и ядерный изотоп, которые вводятся через внутривенный катетер. Аналог аденозина нагружает сердце и увеличивает потребность миокарда в кислороде.За пациентом наблюдают за изменениями сатурации кислорода, артериального давления, частоты сердечных сокращений и ритма [4].
Теперь можно приступить ко второй части ядерного стресс-теста. Накопление ядерного изотопа в сосудах позволяет получить четкие изображения коронарных артерий и окружающей сосудистой сети. В настоящее время стандартная модель включает сбор изображений из семнадцати сегментов: 16 видов по короткой оси и вид по длинной оси апикального сегмента. Кардиологи оценивают каждое изображение по шкале от нуля до четырех; 0 = нормально, 1 = слегка ненормально, 2 = умеренно ненормально, 3 = сильно ненормально, 4 = отсутствует.Суммарная оценка перфузии (SPS) — это общая оценка, включающая изображения в состоянии покоя и стресса, суммарная оценка в состоянии покоя (SRS) представляет тяжесть инфаркта миокарда, а суммарная оценка стресса (SSS) отражает степень ишемии и инфаркта миокарда. Для определения только тяжести ишемии необходимо рассчитать суммарную разницу в баллах (SDS) путем вычитания SRS из SSS [6] [4].
Несоответствие между поставкой и потребностью миокарда кислорода может привести к ишемии миокарда или инфаркту.К сожалению, инфаркт приводит к необратимому повреждению миокарда. Однако ишемию и потенциальные причины несоответствия можно контролировать с помощью различных фармацевтических агентов, включая нитраты, блокаторы бета-адренорецепторов и блокаторы кальциевых каналов. Каждый из этих классов препаратов увеличивает снабжение миокарда кислородом и снижает потребность миокарда в кислороде в разной степени [1] [7].
Нитраты вызывают расслабление гладких мышц сосудов, что вызывает расширение коронарных артерий и системного венозного кровообращения.Когда сосуды, по которым кровь, не содержащая оксигенацию, возвращается к сердцу, расширяются, вызывая увеличение венозной емкости, происходит соответствующее уменьшение преднагрузки сердца, объема желудочка и напряжения стенки желудочка во время систолы. Из-за смещения нагрузки сердца в сторону уменьшения потребность миокарда в кислороде снижается. Кроме того, за счет расширения коронарных артерий нитраты также увеличивают поступление кислорода в миокард. Увеличенный радиус сосудистой сети, снабжающей сердце, позволяет крови обходить потенциальные бляшки, обеспечивая непрерывный приток крови [8] [9].
Блокаторы бета-адренорецепторов подавляют действие катехоламинов на бета-рецепторы. Обычно симпатическая нервная система стимулирует высвобождение катехоламинов для связывания с бета-рецепторами, вызывая увеличение частоты сердечных сокращений, сократимости и артериального давления за счет сужения сосудов. Поскольку бета-блокаторы предотвращают взаимодействие катехоламинов с бета-адренорецепторами, происходит снижение частоты сердечных сокращений и сократимости, что снижает потребность миокарда в кислороде. Кроме того, более медленное сердце позволяет увеличить диастолическую часть сердечного цикла.Из-за этого во время фазы наполнения в сердце может поступать больше крови [1].
Блокаторы кальциевых каналов предотвращают проникновение кальция через потенциалзависимые каналы. Поскольку сократимость зависит от высвобождения кальция из саркоплазматического ретикулума, уменьшение поступления кальция по своей природе вызывает снижение сократимости. Это падение сократимости вызывает снижение потребности миокарда в кислороде. Кроме того, сосудорасширяющее действие блокаторов кальциевых каналов на гладкие мышцы сосудов приводит к увеличению поступления кислорода в миокард [10].
Метаболические изменения при острой ишемии, реперфузии и некрозе миокарда с использованием МР-спектроскопии гиперполяризованного [1-13 C] пирувата in vivo
Этика
Это исследование было одобрено Комитетом по уходу и использованию животных при Национальном университете Чоннам. Все эксперименты проводились в соответствии с соответствующими инструкциями и правилами.
Модель животного
Восемнадцать свободных от патогенов 7-недельных самцов крыс Sprague-Dawley были получены от Orient Co.(Иксан, Корея). Крыс содержали в среде с автоматическим контролем температуры с 12-часовым циклом свет-темнота. Во время операции крыс анестезировали 2,5–3,0% изофлураном, интубировали и подвергали механической вентиляции со скоростью 60 вдохов в минуту с помощью аппарата ИВЛ для мелких животных (Harvard Rodent Ventilator; Harvard Apparatus, Саут-Натик, Массачусетс, США) 18, 19 . Восемнадцать крыс, перенесших левую торакотомию без окклюзии левой передней нисходящей (LAD) коронарной артерии, использовали в качестве контроля с имитацией операции.Затем этим крысам был проведен тот же протокол, но с окклюзией коронарной артерии ПМЖВ в миокарде с использованием изогнутой иглы и шелка 5-0, в соответствии с руководящими принципами для экспериментальных моделей ишемии и инфаркта миокарда 20,21 . Чтобы облегчить снятие шва, в шелковую нить под узлом вставляли небольшое силиконовое кольцо. Затем сундук был закрыт. Через 20 минут для 8 крыс и 90 минут для 8 крыс была инициирована реперфузия путем повторного открытия грудной клетки и разрезания лигатуры вокруг коронарной артерии ПМЖВ.В гистопатологическом анализе использовали двух крыс с ложной операцией. В конце экспериментов все животные были умерщвлены в соответствии с рекомендациями Ветеринарной медицинской ассоциации животных.
Подготовка животных
Как описано ранее 18,19 , крыс анестезировали 2,5–3% изофлураном, смешанным с кислородом (1 л / мин). Катетер размера 24 вводили в хвостовую вену каждой крысы для внутривенного (IV) введения гиперполяризованного раствора [1- 13 C] Pyr.Во время МРТ и измерений 13 C MRS частота дыхания крысы контролировалась датчиком давления модели 1025 (SA Instruments Inc., Стони-Брук, Нью-Йорк, США) и поддерживалась между 60 и 70 вдохами в минуту. Температуру тела также контролировали с помощью немагнитного ректального температурного датчика (FISO Technologies, Квебек, Квебек, Канада) и поддерживали приблизительно 36 ° C.
Поляризация и гиперполяризация
13 C МР-спектроскопияПротокол был описан ранее в наших опубликованных статьях 18,19 .[1- 13 C] пировиноградную кислоту (23-24 мг; Isotec, Майамисбург, Огайо), содержащую 15 мМ тритильного радикала (OX063; Oxford Instruments, Абингдон, Великобритания), переносили в чашку для образца из политетрафторэтилена и замораживали с использованием жидкого гелия. 18,19 . Образец пировиноградной кислоты был гиперполяризован с использованием поляризатора Hypersense DNP (Oxford Instruments) при 3,35 Тл и 1,4 К при микроволновом облучении 94,1 ГГц в течение 1–1,5 ч, затем растворен в 4,2–4,3 мл перегретого щелочного буфера, содержащего 40 мМ Trizma Pre-Set. Кристаллы pH 7.6, 80 мМ NaOH, 50 мМ NaCl и 2,69 мМ динатрия ЭДТА 18,19 . Гиперполяризованный раствор [1- 13 C] Pyr (80 мМ) вводили внутривенно через катетер, помещенный в хвостовую вену крысы 18,19 . Аликвоту раствора использовали для измерения процента поляризации (17–20%) с помощью спектрометра MQC (Oxford Instruments), а pH (7,0–7,5) измеряли с помощью электронных весов AUW-220D (Shimadzu, Tokyo, Japan). 18,19 .
Гиперполяризованный 13 C MRS выполняли на сканере GE MR750 3 T (GE Healthcare, Милуоки, Висконсин, США) с использованием специальной поверхностной катушки с внутренним диаметром 37 мм. 18,19 .Для динамического исследования спектры 13 C регистрировались каждые 2 с в течение 120 с сразу после инъекции Pyr из 10-мм среза с полем зрения 70 × 70 мм на сердце через 15 мин реперфузии. после 20 и 90 мин окклюзии коронарной артерии. Перед исследованием гиперполяризованного 13 C усиление пропускания было откалибровано с использованием термополяризованного фантома 13 C-обогащенной мочевины (8 M, легированный Magnevist 1% по объему), помещенного рядом с центром катушки. Данные динамического MRS были получены с использованием последовательности импульсов визуализации с химическим сдвигом со свободной индукционной задержкой (FIDCSI) (GE Healthcare) с полосой сбора данных 5000 Гц, 4096 точками и срезов-селективным радиочастотным импульсом с углом поворота 10 ° 18,19 .В течение периода предварительного сканирования перед получением спектров 13 C линейное регулирование шиммирования выполнялось по сердечной ткани. Крысам проводили МРТ продолжительностью примерно 10 мин, затем 2 мин гиперполяризованного MRS 13 C с [1- 13 C] Pyr. 13 C динамические спектры были получены от 8 крыс с ложной операцией в контрольной группе и 8 крыс с травмой AMI / R, а также у 8 крыс с ложной операцией в контрольной группе и 8 крыс с некрозом, индуцированным AMI.
Обработка данных и статистический анализ
СпектрыMR были обработаны и проанализированы с использованием программного обеспечения SAGE (GE Healthcare), как описано ранее Moon et al . 18,19,22 . Динамические данные MRS были аподизированы с помощью гауссовского фильтра 9 Гц во временной области и заполнены нулями до 16 384 точек данных с последующим преобразованием Фурье. Динамические спектры в режиме поглощения корректировались по базовой линии с последующей коррекцией фазы в нулевом и первом порядках 18,19,22 . Высоты пиков сигналов метаболитов использовали для количественного определения [1- 13 C] Lac (185 частей на миллион), [1- 13 C] пиргидрата (181 частей на миллион), [1-9 13 C] Ala (177 частей на миллион), [1- 13 C] Pyr (172 частей на миллион), 13 C бикарбонат (162 частей на миллион) и 13 CO 2 (126 частей на миллион) 14,18,19,22 .Отдельные метаболиты были нормализованы по сигналам общего углерода (tC), которые являются суммой [1- 13 C] Lac, [1- 13 C] пиргидрата, [1- 13 C] Ala , [1- 13 C] Pyr, 13 C Bicar и 13 CO 2 сигналов. Кроме того, метаболит 13 C Bicar был нормализован по сигналам [1- 13 C] Lac + Ala, а метаболит [1- 13 C] Lac был нормализован до сигнала 13 C Bicar 7,17 .Для количественной оценки обменных курсов используют соотношение площади под кривой (AUC) гиперполяризованного [1- 13 C] Lac к [1- 13 C] Pyr (Lac / Pyr) и [1- 13 C] ] Бикарбонат к [1- 13 C] Pyr (бикарбонат / Pyr) рассчитывали в трех группах: 23 . Дифференциальные соотношения метаболитов между двумя группами анализировали с помощью критерия знаковых рангов Уилкоксона и U-критерия Манна-Уитни при P <0,05 (двусторонний тест) с использованием SPSS 19.0 (Чикаго, Иллинойс, США) 19 . Процентные изменения (%) уровня метаболитов в результате повреждения и некроза AMI / R рассчитывались по следующему уравнению: 19 :
$$ {\ rm {Metabolite}} \, {\ rm {change}} \, ({\ rm {MC}}) \, (\%) = {({\ rm {MC}}} _ {{\ rm {after}} {\ rm {AMI}} / {\ rm {R}} {\ rm {или}} {\ rm {некроз}}} \ mbox {-} {{\ rm {MC}}} _ {{\ rm {sham}}}) / {{\ rm {MC}}} _ { {\ rm {sham}}} \ times 100 $$
Величину внутриклеточного pH in vivo регулировали с помощью буферной системы Bicar.Расчет pH с помощью уравнения Хендерсона-Хассельбаха допускается при химическом равновесии, зависящем от pH: 13 C Bicar и 13 CO 2 16 . В качестве константы диссоциации предполагается, что pKa составляет 6,17 in vivo 16 . Поскольку высоты пиков максимальной интенсивности сигнала гиперполяризованного 13 C-меченного Bicar и образованного CO 2 пропорциональны молекулярным концентрациям, pH рассчитывали по соотношению этих сигналов.Кроме того, тест корреляции Спирмена использовался для анализа корреляций между уровнями метаболитов [1- 13 C] и значениями pH с доверительным интервалом 95%. Кроме того, была проанализирована кривая рабочих характеристик приемника (ROC) для оценки диагностической эффективности гиперполяризованного [1- 13 C] пирувата MRS в имитационной контрольной группе, группе AMI / R и некрозе.
Биохимический анализ сыворотки
После гиперполяризации 13 C Исследование MRS, образцы крови 0.У всех крыс собирали 5–1 мл. Образцы сыворотки собирали центрифугированием при 3000 об / мин в течение 15 минут и хранили при -80 ° C до использования для биохимических анализов, как описано в предыдущих исследованиях 18,19 . Креатинкиназу (CK), аспартатаминотрансферазу (AST) и лактатдегидрогеназу (LDH) измеряли с помощью автоанализатора с коммерчески доступным набором для тестирования (VET TEST 8008; IDEXX Laboratories, Westbrook, ME, USA) 18,19 .
Гистопатологический анализ и окрашивание трифенилтетразолием
Фрагменты ткани миокарда примерно 1.4 × 1,2 × 0,3 см. 3 были извлечены из контрольных крыс с ложной операцией и крыс, индуцированных AMI / R, и зафиксированы в 10% формальдегиде. После 24-часовой фиксации фрагменты были обезвожены, очищены и заключены в парафин 18,19 . Затем парафиновые блоки разрезали на срезы толщиной 2 мкм и окрашивали гематоксилином и эозином (H&E) для оценки повреждения сердца 18,19 . Цифровая камера (FO124SC; FOculus, Финнинг, Германия) использовалась для получения изображений срезов для оценки гистопатологии.
Кроме того, после того, как сердца были разрезаны на 2-миллиметровые поперечные срезы, срезы тканей инкубировали в 2% хлориде 2,3,5-трифенилтетразолия (ТТС) в течение 10 минут при 37 ° C, чтобы обеспечить демаркацию области инфаркта.
Подъем сегмента ST на электрокардиограмме: признак ишемии миокарда | Сердечно-сосудистые исследования
Аннотация
В 1972 году Kjekshus et al. опубликовал основополагающую статью «Распространение повреждения миокарда и его связь с эпикардиальными изменениями сегмента ST после коронарной окклюзии у собак» в журнале Cardiovascular Research . В этой статье было показано, что подъем сегмента ST, происходящий на в начале после окклюзии левой нисходящей коронарной артерии, был тесно связан с истощением некротических клеток креатинкиназой и снижением кровотока на более поздней стадии (24 ч. ).Эта корреляция была особенно заметной, если инфаркт был трансмуральным. Исходя из этих феноменологических взаимосвязей, эта статья кратко описывает и суммирует экспериментальные исследования, которые были выполнены в других лабораториях после публикации Kjekshus et al. Особое внимание уделяется обсуждению основных основных механизмов, лежащих в основе клинически наблюдаемого подъема сегмента ST и его эволюции после острой стадии ишемии, то есть изменений трансмембранного потенциала действия и изменения электрического межклеточного взаимодействия. .
1 Введение
В 1972 году Kjekshus et al. [1] опубликовал статью, озаглавленную «Распространение повреждения миокарда и его связь с эпикардиальными изменениями сегмента ST после коронарной окклюзии у собак» в Cardiovascular Research . Эта и другие родственные публикации [1–5] были направлены на определение ранних маркеров размера инфаркта. В то время подъем сегмента ST уже использовался в клинической электрокардиографии как прямой индикатор острой ишемии.Тем не менее, статьи, опубликованные этими авторами, считаются основополагающими, поскольку они ознаменовали начало периода, который внес значительный вклад в понимание электрофизиологических изменений при ишемии миокарда и механизмов формирования инфаркта. В разделе 2 этого краткого обзора, посвященного публикации Kjekshus et al., Будут обсуждаться ранние исследования изменений сегмента ST как признака ишемии миокарда. Раздел 3 будет посвящен взаимосвязи между изменениями сегмента ST на электрокардиограмме, лежащими в основе ранними изменениями метаболизма и распространением некроза.В разделе 4 будут обсуждаться клеточные электрофизиологические механизмы, приводящие к изменениям внутрисердечного внеклеточного электрического поля и электрокардиограммы. Наконец, дополнительные сложности, присущие интерпретации подъема сегмента ST in vivo, будут описаны в Разделе 5.
2 Повышение сегмента ST как маркер острой ишемии миокарда
Термин ишемическое повреждение был первоначально получен из наблюдения, что механическое повреждение сердца вызывает изменения внеклеточной электрограммы, очень похожие на ишемию.В 1879 году Бердон-Сандерсон и Пейдж [6] уже описали эффекты механического повреждения поверхности сердца лягушки и отметили, что во время активности поврежденный участок заряжается положительно по отношению к неповрежденной поверхности. За последние четыре десятилетия многие исследователи изучали влияние механического или ишемического повреждения на локальные внеклеточные электрограммы в сердце. Таким образом, постепенно было установлено, что элевация ST, описанная на поверхностной электрокардиограмме, в действительности соответствует комбинации изменения сегмента TQ и реального изменения сегмента ST на .Samson и Scher [7] представили первые доказательства того, что депрессия исходного диастолического уровня на внеклеточной электрограмме была связана с изменением мембранного потенциала покоя ишемических клеток, открытие, которое было подтверждено Prinzmetal et al. [8]. Samson и Scher [7] постулировали, что реальная элевация сегмента ST в основном была вызвана сокращением потенциала ишемического действия, эта точка зрения позже была частично оспорена. На момент публикации работы Maroko, Kjekshus, Sobel, Ross, Braunwald и других было общепризнанным, что подъем сегмента ST является индикатором ишемического повреждения.Однако большинство основных клеточных механизмов, лежащих в основе изменений ишемической электрокардиограммы, до сих пор не были должным образом описаны, как обсуждается ниже.
3 Подъем сегмента ST, изменения ишемического метаболизма и размер инфаркта
Основная цель статей Maroko, Kjekshus, Sobel, Ross и Braunwald состояла в том, чтобы определить маркеры ишемии и ранние предикторы размера инфаркта. Таким образом, было показано, что истощение миокарда креатинфосфокиназы (КФК) является показателем ишемического повреждения клеток и размера инфаркта [3].Кроме того, было продемонстрировано, что степень истощения КФК тесно коррелировала со степенью снижения кровотока в миокарде после коронарной окклюзии [3] и со степенью некроза миокарда, оцененной гистологически [5]. Результаты, представленные в статье Kjekshus et al. проиллюстрированы и обобщены на рис. 1. В этой статье была поставлена цель сопоставить изменения в кровотоке миокарда и истощение КФК с изменениями сегмента ST на электрокардиограмме. Соответственно на рис.1 внеклеточные электрограммы, записанные с помощью неполяризуемых электродов до и после окклюзии передней межжелудочковой коронарной артерии сердца собаки in situ, сравнивались с соответствующими локальными уровнями КФК, взятыми из субэпи- («наружного») и субэндокардиального (« внутренний ‘) мышечные слои. Из этой статьи стала очевидной тесная корреляция между изменениями сегмента ST, зарегистрированными в начале (15 минут после коронарной окклюзии), более поздним признаком некроза клеток (содержание КФК после через 24 часа ) и остаточным кононарным кровотоком. .Более того, наблюдался постоянный градиент между более тяжелым субэндокардиальным истощением CPK и субэпикардиальным истощением CPK, и корреляция между эпикардиальными изменениями сегмента ST была ближе к изменениям CPK в субэпикарде, чем в субэндокарде. Эти трансмуральные градиенты между электрическими, метаболическими изменениями и изменениями потока после коронарной окклюзии, как позже выяснилось, были специфичными для сердца собаки. В сердцах собак переменная коллатеральная циркуляция препятствует уменьшению кровотока из первоначально закупоренного сосуда [9].В сердце свиньи коллатеральный кровоток отсутствует, а пограничная зона ишемии, в которой коронарный кровоток изменяется с нормального на очень низкий, простирается всего на несколько миллиметров [10]. Сама пограничная зона состоит из пересекающихся между собой здоровых и некротических тканей с резким разделением между некротической и выжившей тканью [10]. Таким образом, постепенное изменение средней концентрации ишемических метаболитов и креатинфосфата в этой пограничной зоне связано с изменением соотношения некротических и выживших клеток. Аналогично наблюдениям Kjekshus et al., эксперименты на свином сердце подтвердили, что корреляция между изменениями сегмента ST во время ранней ишемии с более поздними показателями некроза действительна только в том случае, если изменения сегмента ST измеряются до первых 15–20 минут острой ишемии. На более поздних стадиях метаболиты продолжают изменяться, в то время как изменения в сегментах ST снижаются [11] из-за разобщения клеток (см. Ниже).
Рис. 1
Изменения эпикардиального сегмента ST через 15 минут после коронарной окклюзии и активность CPK через 24 часа в соответствующих субэпикардиальных и субэндокардиальных образцах из репрезентативного сердца собаки.LVP = давление в левом желудочке. Расположение пронумерованных участков для отбора проб и окклюзионной коронарной перемычки показано на центральной диаграмме (воспроизведено из [1] с разрешения).
Рис. 1
Изменения эпикардиального сегмента ST через 15 минут после коронарной окклюзии и активность CPK через 24 часа в соответствующих субэпикардиальных и субэндокардиальных образцах репрезентативного сердца собаки. LVP = давление в левом желудочке. Расположение пронумерованных участков для отбора проб и окклюзионной коронарной перемычки показано на центральной диаграмме (воспроизведено из Ref.[1] с разрешения).
4 Электрофизиологические и ионные изменения клеток, объясняющие подъем сегмента ST
Регистрация трансмембранных потенциалов действия с поверхности всего сердца с артериальной перфузией позволила установить основную взаимосвязь между изменениями внеклеточных униполярных электрограмм и клеточными электрическими изменениями. В основополагающей статье Downar et al. [12] показали, что региональная ишемия связана с быстрыми изменениями трансмембранных потенциалов действия.Быстрая потеря поляризации мембраны во время фазы покоя (сдвиг потенциала покоя к более положительным значениям) сопровождалась потерей амплитуды, укорочением и уменьшением скорости восходящего движения трансмембранного потенциала действия, пока ишемическая ткань не стала совершенно неуправляемой. примерно через 10 мин ишемии (рис. 2). В дополнение к характеристике основных изменений потенциала действия, эта работа показала основные клеточные электрофизиологические особенности острой ишемической ткани, которые позже стали важными для нашего понимания злокачественных желудочковых аритмий: (1) электрические альтернативы, которые были описаны как предвестник желудочковой тахикардии и фибрилляции, и (2) длительное восстановление потенциала действия вверх, называемое постреполяризационной рефрактерностью, феномен, обусловленный зависящим от времени восстановлением каналов Na + и Ca ++ после инактивации [ 13].Это первоначальное исследование изменений трансмембранного потенциала действия ишемической ткани стимулировало ряд дальнейших экспериментальных исследований, направленных на: (1) более точное определение природы клеточных электрических изменений; или (2) взаимосвязь между внеклеточным и трансмембранным потенциалами. Чтобы отделить реальное изменение сегмента ST от изменения сегмента TQ, электрограммы постоянного тока, записанные неполяризуемыми электродами, регистрировали с нескольких интрамуральных и эпикардиальных участков в целых сердцах [11].Как показано на фиг. 3A и B, региональная ишемия вызывает заметный сдвиг как сегмента ST, так и сегмента TQ. В случае сердца свиньи, где ишемические зоны являются трансмуральными, изменения были относительно однородными по всей стенке желудочка. Следовательно, градиент внеклеточного потенциала во время ST- и TQ-сегмента можно отнести к протеканию тока повреждения между внеклеточными и внутриклеточными компартментами нормальной и ишемической ткани. Было установлено, что ток ишемического повреждения имеет силу, которая теоретически может оказывать стимулирующее действие [14].Поскольку стимулирующий эффект диастолического тока может происходить только в тех местах, где ток течет наружу (из внутриклеточного во внеклеточный отсек), особая аритмогенная роль приписывается току повреждения в ситуации электрических альтернаций [14].
Рис. 3
Распределение эпикардиального потенциала в диастоле (вверху) и систоле (внизу) через 15–25 мин окклюзии левой передней нисходящей артерии. Звездочки на самой нижней электрограмме указывают моменты цикла, в которых измерялись потенциалы.Сигналы регистрировались из затененной области под передней частью сердца, показанной на вставке, в местах на расстоянии 3 мм друг от друга. Показанные внеклеточные комплексы были записаны с участков вдоль указанной линии крутых градиентов потенциала. Прямоугольный импульс указывает на калибровку 30 мВ. Изопотенциальные линии на обеих картах представляют собой шаги 4 мВ (изменено из [11] с разрешения).
Рис. 3
Распределение эпикардиального потенциала в диастоле (вверху) и систоле (внизу) через 15–25 мин окклюзии левой передней нисходящей артерии.Звездочки на самой нижней электрограмме указывают моменты цикла, в которых измерялись потенциалы. Сигналы регистрировались из затененной области под передней частью сердца, показанной на вставке, в местах на расстоянии 3 мм друг от друга. Показанные внеклеточные комплексы были записаны с участков вдоль указанной линии крутых градиентов потенциала. Прямоугольный импульс указывает на калибровку 30 мВ. Изопотенциальные линии на обеих картах представляют собой шаги 4 мВ (изменено из [11] с разрешения).
Рис.2
Трансмембранные потенциалы действия, зарегистрированные в субэпикарде левого желудочка сердца свиньи in situ до и после окклюзии левой передней нисходящей коронарной артерии (изменено из [12] с разрешения).
Рис. 2
Трансмембранные потенциалы действия, зарегистрированные из субэпикарда левого желудочка сердца свиньи in situ до и после окклюзии левой передней нисходящей коронарной артерии (изменено из [12] с разрешения).
Работа над клеточной электрофизиологической основой подъема сегмента ST и депрессии сегмента TQ также выявила еще одно важное изменение электрического поведения, связанное с ишемией, а именно электрическое разъединение сердечных клеток [11]. В работе Kjekshus et al., Подъем сегмента ST был постулирован как достоверный маркер ишемии миокарда только в течение нескольких минут сразу после коронарной окклюзии. Оценка реального подъема сегмента ST и депрессии сегмента TQ показала, что оба значения достигли максимума примерно через 10–15 минут коронарной окклюзии и затем снизились до тех пор, пока они почти не исчезли в центре ишемической зоны после 2 часов поддерживаемой коронарной окклюзии [11]. .Это общее снижение травмирующего тока лучше всего объяснялось увеличением сопротивления внутри токовой петли, очевидными кандидатами на это изменение были щелевые переходы. Расцепление при ишемии также было предложено путем прямых измерений изменений резистентности тканей целого сердца [15].
Более подробное определение двух основных процессов, определяющих электрокардиографические изменения при ишемии: (1) изменение трансмембранного потенциала действия; и (2) изменение электрического сцепления между клетками стало возможным с развитием более сложных методов определения изменений активности ионов во внеклеточном и внутриклеточном пространствах и межклеточного сопротивления.В работе Харриса [16] было продемонстрировано, что ишемическая ткань сердца теряет ионы K из своего внутриклеточного пространства, изменение, которое было связано с аритмогенезом. Введение ионно-чувствительных электродов в целое сердце [17,18] позволило непосредственно контролировать внеклеточные [H + ], [K + ] и [Na + ] в ишемической области и коррелировать эти значения с изменением трансмембранного потенциала действия. Очень похоже на подъем сегмента ST, депрессию сегмента TQ и связанные с ним изменения трансмембранного потенциала, [K + ] быстро увеличивался в ишемической зоне до уровня плато и демонстрировал вторичное повышение через 15-20 мин.Изменение потенциала покоя близко следовало за изменением внеклеточного [K + ], и оценки изменения равновесного потенциала [K + ] предполагали полный баланс между деполяризованным потенциалом покоя и распределением [K + ] ионы [19]. Механизмы, управляющие изменением потенциала покоя и клеточной потерей калия, стали предметом длительных споров между несколькими группами, частично предлагающими расходящиеся экспериментальные данные и / или интерпретации.Основная проблема была связана с тем фактом, что изменения потенциала покоя и изменения внеклеточного [K + ], [K +] o , могут быть взаимно интерактивными, то есть увеличение [K +] o может объяснить изменение мембранного потенциала и, наоборот, изменение мембранного потенциала может объяснить потерю внутриклеточного [K + ]. Наблюдение за тем, что гипоксические и ишемические клетки теряют калий [20] и что сокращение потенциала действия во время гипоксии в значительной степени связано с открытием АТФ-чувствительных каналов K + [21, 22], было принято в качестве аргумента в пользу открытия [K + ] каналов как первичный механизм [23].В качестве второй гипотезы утверждалось, что увеличение [K + ] o просто отражает ингибирование зависящей от энергии накачки K + / Na + . Эта гипотеза была, по крайней мере, частично подтверждена тем фактом, что насос K + / Na + был показан при ранней ишемии, чтобы реагировать на нагрузку Na + [19, 24], и что методы определения внутриклеточного Na + при ишемии показал противоречивые результаты. Третья гипотеза связывает клеточную потерю K + с анаэробным гликолизом, внутриклеточным и метаболическим подкислением.Было высказано предположение, что K + может перераспределяться вследствие движения электрогенных анионов (например, лактата), теория, которая, по-видимому, объясняет потерю K + из скелетных мышц во время усталости и напряженных анаэробных упражнений [19]. Дальнейшие гипотезы включали сдвиги концентраций ионов, связанные с осмотическим набуханием [25]. Основная трудность с определением механизма потери клеточного K + во время ишемии связана с тем фактом, что K + накапливается в узких межклеточных щелях.Следовательно, большое изменение [K + ] o отражает очень незначительный дисбаланс однонаправленных трансмембранных потоков [26]. В отличие от механизмов, ответственных за сдвиг мембранного потенциала покоя, изменения трансмембранного потенциала действия, по-видимому, относительно хорошо изучены. Таким образом, положительный сдвиг мембранного потенциала и увеличенный [K + ] o приводят к прогрессирующей инактивации каналов Na + с уменьшением скорости движения вверх и амплитуды потенциала действия.Сравнение различных компонентов ишемии, закисления, повышенного [K + ] o и гипоксии показало, что закисление и гипоксия усиливают эффект повышенного [K + ] o для изменения потенциала действия [ 27], при этом АТФ-чувствительный ток K + может играть дополнительную роль [28].
Поразительной особенностью электрических изменений при ишемии миокарда является диссоциация между очень ранними изменениями трансмембранных потенциалов действия и более отсроченным электрическим разобщением между клетками.Как упоминалось выше, только эта диссоциация позволяет протеканию тока травмы и возникновению ранних изменений сегмента ST на электрокардиограмме: изменения трансмембранного потенциала создают движущую силу для протекания тока травмы, протекания тока сам по себе требует путей с низким сопротивлением между ишемической и неишемической областями, то есть интактной межклеточной связью. Анализ кабеля в специально разработанной сосочковой мышце кролика с артериальной перфузией показал, что электрическое разобщение клеток между клетками быстро развивается примерно через 12-15 минут после коронарной окклюзии и завершается примерно через 30-40 минут [29].Это быстрое начало может быть изменено предварительным кондиционированием [30], подкислением [31] и мерами, влияющими на энергетический метаболизм [32]. Его точный механизм до конца не выяснен, потому что ряд изменений, которые, как известно, сами по себе влияют на сопротивление щелевых соединений in vivo, происходят почти одновременно с ишемическим межклеточным разобщением: закисление [33,34], увеличение внутриклеточного [Ca ++ ], [33,34] и накопление липидных метаболитов [35]. Наблюдение, что увеличение внутриклеточного [Ca ++ ] немного предшествует началу ишемического межклеточного разобщения [36], привело к гипотезе о том, что [Ca ++ ] может быть инициатором электрического разобщения и что все другие вышеупомянутые изменения происходят как следствие быстро развивающегося энергетического дисбаланса и нарушения ионного гомеостаза.Несколько наблюдений показывают, что уменьшение цитозольной термодинамической движущей силы, так называемое изменение свободной энергии при гидролизе АТФ [37], приводит к истощению [Ca ++ ] из саркоплазматического ретикулума, как первичному событию этого последующего самовоспроизводящиеся ионные и метаболические изменения [38].
Еще один уровень сложности, описывающий детерминанты ишемической элевации ST на электрокардиограмме, связан с наблюдением, что во всем сердце, даже при полностью развитой (без кровотока) ишемии, электрические изменения неоднородны.Распределение изопотенциальных линий сегментов ST и TQ на рис. 3 показывает: (1) непрерывное уменьшение от центра ишемической зоны к ишемической границе; и (2) локально нерегулярные изопотенциальные линии, указывающие на электрическую неоднородность [11]. Эти градиенты были тщательно изучены и сопоставлены с изменениями внеклеточных K + и H + в интактных сердцах свиней [39–41]. Интересно, что градиенты были обнаружены в полностью ишемизированной ткани, то есть в отсутствие местного кислорода (рис.4). Поскольку эти градиенты быстро развивались на несколько миллиметров, диффузия K + и H + из ишемизированного миокарда в неишемический миокард не могла полностью объяснить электрическую неоднородность. Еще одно диффундирующее и летучее вещество, которое может объяснить эту неоднородность в относительно большом масштабе, — это диоксид углерода, который накапливается до> 300 мм рт. Ст. В центре ишемической зоны. На изолированной ишемизированной папиллярной мышце кролика было продемонстрировано, что накопление и диффузия углекислого газа оказывают большое влияние на клеточную потерю и сопутствующее накопление внеклеточного K + , и что диффузия углекислого газа может объяснить центробежное снижение внеклеточного K + и H + в ишемической области [42].
Рис. 4
Нижняя панель: схематическое изображение изменений [K + ] o , pH и PO 2 в ишемической зоне от центра к границе. Верхняя панель: схематическое изображение потенциалов действия, типичных для различных ишемических зон, показанных на нижней панели. Воспроизведено из исх. [39] с разрешения.
Рис. 4
Нижняя панель: схематическое изображение изменений [K + ] o , pH и PO 2 в ишемической зоне от центра к границе.Верхняя панель: схематическое изображение потенциалов действия, типичных для различных ишемических зон, показанных на нижней панели. Воспроизведено из исх. [39] с разрешения.
5 Подъем сегмента ST: количественный маркер регионарной ишемии?
Механизмы, лежащие в основе острых изменений сегмента ST на электрокардиограмме, как кратко обсуждалось в предыдущих разделах, указывают на высокий уровень сложности. Кроме того, существует определенная степень неопределенности в интерпретации экспериментальных результатов, которая в основном связана с методологическими трудностями в оценке клеточных и молекулярных механизмов в цельной сердечной ткани с закупоренными сосудами.Несмотря на сложность, описанные выше механизмы были исследованы на относительно простых и частично редукционистских экспериментальных моделях. Существует множество других переменных, которые могут быть важны для объяснения ишемического подъема сегмента ST. Во-первых, клиническая ишемия часто может быть связана с ограниченным, но не полностью прерванным кровоснабжением сердца. Несоответствие между четко разграниченной зоной некроза при инфаркте свиней и наличием электропроводящей ткани при инфаркте человека предполагает, что картина потока в зонах инфаркта человека может быть сложной.Ишемию с низким потоком нельзя рассматривать как патофизиологически эквивалентную полной ишемии без потока. Например, важные ионные изменения, такие как накопление внеклеточного калия, наблюдаются только при коронарном кровотоке <30% от нормы [43]. Более того, бескислородная перфузия связана со значительно большей потерей клеточного K + , чем ишемия без кровотока [44]. Таким образом, относительно небольшие изменения в уменьшении потока, вероятно, повлияют на ионные и связанные с ними электрические изменения.Во-вторых, клиническое повышение сегмента ST после инфаркта миокарда часто сохраняется после острой фазы ишемии, особенно в случае аневризмы желудочков. Стойкое ишемическое повреждение в пограничной зоне инфаркта миокарда в сочетании с низким электрическим сопротивлением рубцовой ткани в центре инфаркта может частично объяснить это явление [45,46]. В качестве третьего фактора, влияющего на подъем сегмента ST, следует упомянуть влияние автономной нервной системы. Повышенный симпатический тонус влияет на величину подъема сегмента ST, наблюдаемого на ранней стадии ишемии [47], а связанное с метаболизмом истощение запасов норадреналина в ишемизированном миокарде играет важную роль в электрофизиологических изменениях, наблюдаемых после коронарной окклюзии [48,49].Таким образом, работа Kjekshus et al. продемонстрировал важную взаимосвязь между подъемом сегмента ST при острой ишемии миокарда и степенью более позднего некроза и снижения коронарного кровотока. Однако подъем сегмента ST как количественный маркер острой ишемии следует использовать с осторожностью из-за множества переменных, способствующих этому электрокардиографическому изменению.
Список литературы
[1]Распространение повреждения миокарда и его связь с эпикардиальными изменениями сегмента ST после окклюзии коронарной артерии у собак
Cardiovasc Res.
1972
6
490
499
[2]Благоприятные эффекты стимуляции блуждающего нерва на ишемический миокард во время блокады бета-рецепторов
Scand J Clin Lab Invest.
1981
41
383
389
[3]Снижение активности креатинфосфокиназы миокарда после экспериментального инфаркта миокарда у кролика
Circ Res.
1970
27
403
414
[4]Уменьшение размера инфаркта путем вдыхания кислорода после острой коронарной окклюзии
Тираж
1975
52
360
368
[5]и другие.
Влияние инфузии глюкозы, инсулина и калия на инфаркт миокарда после экспериментальной окклюзии коронарной артерии
Тираж
1972
45
1160
1175
[6]О временной зависимости возбудительного процесса в желудочке сердца лягушки
J. Physiol. (Лондон)
1879
2
384
429
[7]Механизм изменения сегмента ST при остром повреждении миокарда
Circ.Res.
1960
8
780
787
[8]Ишемия миокарда. Характер ишемических электрокардиографических паттернов в желудочках млекопитающих, определяемых внутриклеточными электрографическими и метаболическими изменениями
г. Дж Кардиол
1961
8
493
503
[9]Модели сердечных аритмий на животных
Cardiovasc Res.
1998
39
165
177
[10]и другие.
«Пограничная зона» при ишемии миокарда. Электрофизиологическая, метаболическая и гистохимическая корреляция в сердце свиньи
Circ Res.
1979
44
576
588
[11]Механизм и динамика изменений сегментов S-T и T-Q во время острой регионарной ишемии миокарда в сердце свиньи, определяемые внеклеточными и внутриклеточными записями
Circ Res.
1978
42
603
613
[12]Влияние острой окклюзии коронарной артерии на субэпикардиальные трансмембранные потенциалы в интактном сердце свиньи
Circ.
1977
56
217
224
[13]Медленное восстановление после инактивации входящих токов в миокардиальных волокнах млекопитающих
J Physiol (Лондон)
1974
240
703
724
[14]и другие.
Поток «травмирующего» тока и характер возбуждения во время ранних желудочковых аритмий при острой регионарной ишемии миокарда в изолированном сердце свиней и собак.Доказательства двух различных аритмогенных механизмов
Circ Res.
1980
47
151
165
[15]Распределение сердечного потенциала
Медицинская физика и экспериментальная кардиология
1976
Амстердамский университет
Амстердам
[16]Факторы возбуждения желудочковой тахикардии, возникающие в результате ишемии миокарда. Калий — главный возбудитель
Наука
1954
119
200
203
[17]Влияние острой окклюзии коронарной артерии на локальную внеклеточную активность миокарда K + у свиней
Тираж
1980
61
768
778
[18]Увеличение внеклеточных K + и H + миокарда и высвобождение норадреналина как возможная причина ранних аритмий после острой окклюзии коронарной артерии у свиней
J Mol Cell Cardiol.
1980
12
579
593
[19]Мембранный потенциал покоя, внеклеточная активность калия и внутриклеточная активность натрия во время острой глобальной ишемии в изолированном перфузируемом сердце морской свинки
Circ Res.
1983
52
442
450
[20]Гипоксия увеличивает отток калия из миокарда млекопитающих
Experientia
1976
32
483
484
[21]сульфонилмочевины, АТФ-чувствительные каналы K + и потеря клеточного K + во время гипоксии, ишемии и метаболического ингибирования в желудочке млекопитающих
Circ Res.
1991
69
623
637
[22]и другие.
Накопление калия в глобально ишемизированном сердце млекопитающих
Circ Res.
1990
67
835
843
[23]АТФ-регулируемые K-каналы в сердечной мышце
Природа
1983
305
147
148
[24]Накопление внеклеточного K + во время ишемии миокарда в изолированном сердце кролика
Am J Physiol.
1982
242
H619
H628
[25]Вклад сокращения внеклеточного пространства во внеклеточное накопление K + при ишемии миокарда кролика
J Physiol (Лондон)
1996
490
215
228
[26]Первый электрокардиографический признак ишемии миокарда: электрофизиологическое предположение
Тираж
1976
53
Доп.Я
82
84
[27]и другие.
Сравнение эффектов регионарной ишемии, гипоксии, гиперкалиемии и ацидоза на внутриклеточные и внеклеточные потенциалы и метаболизм в изолированном сердце свиньи
Circ Res.
1980
46
634
646
[28]Электрофизиологические эффекты острой ишемии миокарда: теоретическое исследование измененной возбудимости клеток и продолжительности потенциала действия
Cardiovasc Res.
1997
35
256
272
[29]Электрическое разъединение и увеличение внеклеточного сопротивления после индукции ишемии изолированной папиллярной мышцы кролика с артериальной перфузией
Circ Res.
1987
61
271
279
[30]и другие.
Ишемическое прекондиционирование задерживает вызванное ишемией электрическое разобщение клеток в миокарде кролика за счет активации АТФ-чувствительных калиевых каналов [опубликованная ошибка появляется в Cardiovasc Res 1993 Jul; 27 (7): 1385]
Cardiovasc Res.
1993
27
644
651
[31]Изменения внеклеточного и внутриклеточного pH в ишемической папиллярной мышце кролика
Circ Res.
1992
71
460
470
[32]Пассивные электрические свойства, механическая активность и внеклеточный калий в желудочковой мышце кролика с артериальной перфузией и ишемией. Эффект блокады поступления кальция или гипокальциемии
Circ Res.
1990
66
1461
1473
[33]Зависимость контактной проводимости от протонов, ионов кальция и магния в парных клетках сердца морской свинки
J. Physiol.
1987
382
193
211
[34]Модификация проводимости щелевого соединения двухвалентными катионами и протонами в клетках сердца новорожденных крыс
J Mol Cell Cardiol.
1995
27
1633
1643
[35]Ингибирование проводимости щелевого соединения длинноцепочечными ацилкарнитинами и их преимущественное накопление в сарколемме соединения во время гипоксии
Circ Res.
1993
72
879
889
[36]и другие.
Внутриклеточный Ca 2+ , межклеточная электрическая связь и механическая активность в ишемической папиллярной мышце кролика. Эффекты прекондиционирования и метаболической блокады
,00Circ Res.
1996
79
237
246
[37]Изменение свободной энергии гидролиза АТФ во время глобальной ишемии и аноксии в сердце крысы.Его возможная роль в регуляции транссарколеммальных градиентов натрия и калия
J Mol Cell Cardiol.
1984
16
1023
1036
[38]Клеточные аспекты ранней сократительной недостаточности при ишемии
Сердце и сердечно-сосудистая система
1991
Raven Press
Нью-Йорк
1975
1996
[39]Коронел Р. Распределение внеклеточного калия во время ишемии миокарда.Диссертация, Амстердамский университет, Нидерланды, 1988 г.
[40]и другие.
Распределение внеклеточного калия и его связь с электрофизиологическими изменениями при острой ишемии миокарда в изолированном перфузируемом сердце свиньи
Тираж
1988
77
1125
1138
[41]и другие.
Распределение внеклеточного калия и электрофизиологические изменения во время двухэтапной коронарной перевязки в изолированном перфузируемом сердце собаки
Тираж
1989
80
165
177
[42]Ранние изменения внеклеточного калия в ишемизированном миокарде кролика.Роль внеклеточного накопления и диффузии углекислого газа
Circ Res.
1992
70
409
422
[43]Влияние постепенного снижения коронарного кровотока на ионные, электрические и механические показатели ишемии у свиньи
Тираж
1987
76
1127
1134
[44]Диссоциация между потерей клеточного K + , сокращением времени реполяризации и тканевыми уровнями АТФ во время гипоксии и ишемии миокарда
Circ Res.
1993
72
560
570
[45]и другие.
Пассивная передача ишемических изменений сегмента ST в рубце инфаркта миокарда с низким электрическим сопротивлением у свиньи
Cardiovasc Res.
1998
40
103
112
[46]и другие.
Подъем сегмента ST на поверхности излеченного трансмурального инфаркта миокарда у свиней.Условия пассивной передачи из ишемической периинфарктной зоны
Тираж
1995
91
1552
1559
[47]и другие.
Влияние регионарной денервации на электрограммы постоянного тока эпикарда при коронарной окклюзии у свиней
Am J Physiol.
1987
253
х238
146
[48] Высвобождение катехоламинов и накопление калия в изолированном глобально ишемизированном сердце кролика
J Mol Cell Cardiol.
1988
20
887
896
[49]Нексоцитотическое высвобождение эндогенного норадреналина в ишемическом и аноксическом сердце крысы: механизм и метаболические потребности
Circ Res.
1987
60
194
205
Авторские права © 2000, Европейское общество кардиологов
реакций, изменений и симптомов ЭКГ — ЭКГ и ЭХО
Как и все другие клетки человеческого тела, сердечные миоциты используют АТФ (аденозинтрифосфат) в качестве основного источника энергии.АТФ производится путем метаболизма углеводов (глюкозы), жиров или белков, в зависимости от того, что доступно. АТФ поддерживает все клеточные функции, такие как сокращение и расслабление. Увеличение нагрузки на сердце за счет увеличения частоты сердечных сокращений и сократительной способности (т. Е. Сократительной силы) приводит к усилению метаболизма. Сердечные клетки обладают высокой способностью обеспечивать соответствие спроса и предложения АТФ; увеличение сердечной нагрузки приводит к увеличению производства АТФ, а наоборот . Важно отметить, что сердечным миоцитам требуется аэробный метаболизм (кислород) для производства достаточного количества АТФ.Это означает, что сердцу необходим непрерывный кровоток для поддержания клеточной функции.
Ишемия миокарда возникает при недостатке кислорода. Недостаточное поступление кислорода приводит к снижению выработки АТФ и, как следствие, нарушению клеточного метаболизма. В случае ишемии сердечные миоциты защищаются, переключаясь на анаэробный метаболизм. Это возможно, потому что сердечные миоциты хранят гликоген (форма хранения глюкозы), который можно использовать для производства АТФ в отсутствие кислорода.К сожалению, гликоген производит лишь небольшое количество АТФ, а запасы гликогена ограничены. Чтобы снизить потребность в кислороде, сердечные миоциты перестают сокращаться в анаэробных условиях (то есть во время ишемии). Эти две меры — то есть переход на анаэробный метаболизм и прекращение сокращений — позволяют миокарду выдержать 20-30 минут тяжелой ишемии. Если перфузия миокарда (кровоток) в зоне ишемии не восстановится до этого срока, клетка погибнет.
Фигура 1.Клеткам миокарда требуется постоянная подача кислорода для поддержания нормального метаболизма. Если поступление кислорода меньше потребности в кислороде, развивается ишемия. Клетки миокарда могут переключаться на анаэробный метаболизм и прекращать сокращения, чтобы облегчить ишемию. Это позволяет клетке выдерживать до 30 минут тяжелой ишемии. Если кровоток не восстановится до 30 минут, клетка погибнет. Гибель клеток миокарда называется инфарктом миокарда.Ишемия миокарда в клинической практике: ишемическая болезнь сердца
В клинической практике ишемия миокарда встречается во многих ситуациях.При стабильной стенокардии появляются атеросклеротические бляшки, которые ограничивают коронарный кровоток и вызывают симптомы при повышенной нагрузке на миокард (физическая нагрузка). Чем тяжелее стеноз, тем более выражены симптомы. Стабильная стенокардия диагностируется с помощью теста с физической нагрузкой (ЭКГ с нагрузкой). Цель стресс-теста — увеличить рабочую нагрузку миокарда (и, следовательно, потребность в кислороде), чтобы спровоцировать ишемию в миокарде, снабжаемую атеросклеротическими артериями. Это также вызывает типичные изменения ЭКГ.Однако при острых коронарных синдромах симптомы и изменения ЭКГ проявляются в покое из-за сильного снижения коронарного кровотока, вызванного острым атеротромбозом.
Таблица 1: Реакция миокарда и ЭКГ в различных условиях с ишемией или повышенной нагрузкой
| СОСТОЯНИЕ КОРОНАРНОЙ АРТЕРИИ | НАСТРОЙКА | ЭФФЕКТ | РЕАКЦИЯ ЭКГ |
| атеросклероз | Нормальная коронарная артерия ишемия возникнуть не может. | На ЭКГ покоя изменений нет. | |
| Повышенная нагрузка на миокард (упражнения) | Обеспечение кислородом увеличивается параллельно с повышенным потреблением кислорода во время физических упражнений. Таким образом, спрос и предложение сбалансированы, и ишемии не происходит. (У некоторых людей наблюдается доброкачественная форма ишемии, локализованная в субэндокарде во время упражнений; это проявляется депрессиями сегмента ST с подъемом сегмента ST во время упражнений, но у человека нет симптомов). | На ЭКГ покоя изменений нет. Доброкачественная депрессия сегмента ST имеет восходящий сегмент ST во время нагрузочного тестирования. | |
| Стабильная ишемическая болезнь сердца (атеросклеротическая бляшка, вызывающая стеноз 70% и более) | В состоянии покоя | Без симптомов. | На ЭКГ покоя изменений нет. |
| Повышенная нагрузка на миокард (упражнения) | Потребность в кислороде увеличивается с рабочей нагрузкой, но стеноз (атеросклеротическая бляшка) ограничивает необходимое увеличение кровотока, что приводит к ишемии миокарда.Ишемия проявляется болью в груди. Этот тип ишемии (вызванный повышенной нагрузкой) локализуется в субэндокардиальном мышечном слое. Это обратимо и разрешится после прекращения упражнения. Только в редких случаях (если ишемия тяжелая и продолжительная) это приводит к утечке тропонина (т. Е. К гибели клеток). | Тест с физической нагрузкой используется, чтобы спровоцировать тот же ишемический процесс, и он может выявить депрессию сегмента ST, уменьшение амплитуды зубца T и, в редких случаях, подъем сегмента ST. | |
| Стабильная, но тяжелая болезнь коронарных артерий (атеросклеротическая бляшка, вызывающая стеноз 90% или более) | В состоянии покоя | Тяжелый атеросклероз может вызывать ишемию уже в состоянии покоя. Это серьезное заболевание, которое находится между стабильным атеросклерозом и острым коронарным синдромом. | ЭКГ в состоянии покоя может показать отклонение ST и / или изменения зубца T. |
| Разрыв / эрозия бляшки с последующим острым коронарным синдромом | В любое время | Трансмуральная ишемия вызывает подъем сегмента ST.Субэндокардиальная ишемия вызывает депрессию сегмента ST. Симптомы выражены (особенно при трансмуральной ишемии) и не облегчаются отдыхом или введением нитроглицерина. | ЭКГ покоя показывает отклонение ST, изменения зубца Т и иногда изменения QRS |
| Любой статус коронарной артерии | Вазоспазм коронарной артерии | Спазм коронарной артерии может вызвать полную обструкцию кровотока. Это практически всегда временно, и спазм сосудов прекращается до развития инфаркта.Таким образом, практически во всех случаях происходит полное восстановление функции клеток после того, как спазм сосудов рассосался. | ЭКГ покоя обычно показывает подъем сегмента ST, что указывает на трансмуральную ишемию |
Время — мышцы: 30 минут от ишемии миокарда до инфаркта
Продолжительность ишемии имеет решающее значение, когда произошла окклюзия. Миокард, снабжаемый закупоренной артерией, немедленно становится ишемическим и перестает сокращаться. Как упоминалось выше, клетки возвращаются к анаэробному метаболизму, чтобы сохранить жизнеспособность.Это позволяет клетке выдержать 20–30 минут ишемии. Если коронарный кровоток восстановится в течение этого периода времени, весь ишемизированный миокард выздоровеет (после короткого периода сократительной дисфункции [называемого оглушенным миокардом ] ). Если коронарный кровоток не восстанавливается, начнется инфаркт, и некроз будет распространяться как волна в воде, начиная с наиболее ишемизированной области, то есть в субэндокарде. Оттуда инфаркт будет распространяться по направлению к эпикарду. См. Рисунок 2 .
Рисунок 2. Естественное течение тотальных окклюзий (трансмуральная ишемия).Время, необходимое для того, чтобы весь ишемический миокард стал инфарктом, представляет большой интерес. В литературе традиционно предполагается, что инфаркт завершается в течение 4-6 часов, но это ставится под сомнение в более новых исследованиях, которые предполагают более длительную. Недавние исследования фактически предполагают, что инфаркт может быть завершен через 2–12 часов после появления симптомов. Такой широкий временной диапазон обусловлен факторами, изменяющими естественный ход.Одним из таких факторов является наличие коллатерального коронарного кровообращения.
Тотальные окклюзии (приводящие к острому ИМпST) обычно сохраняются до тех пор, пока практически весь ишемический миокард не подвергнется инфаркту (если реперфузионная терапия не успешна). Треть всех окклюзий реканализируется спонтанно в течение 12–24 часов (коронарные артерии имеют тромболитическую систему, которая, хотя и слишком поздно, обрабатывает тромб). Однако следует отметить, что, хотя подавляющая часть пораженного миокарда будет некротизирована к моменту реканализации артерии, восстановление кровотока может фактически улучшить сократительную функцию и прогноз.Это связано с тем, что в зоне поражения или рядом с ней может находиться миокард , находящийся в спячке, . Спящий миокард сильно ишемизирован, но жизнеспособен и может полностью восстановиться, если восстановится кровоток. Более того, восстановление кровотока улучшает заживление области инфаркта (что приводит к более сильному рубцу) и замедляет ремоделирование желудочков (что приводит к сердечной недостаточности).
Рисунок 3 (вверху) показывает, как инфаркт распространяется от субэндокарда к эпикарду.Причина, по которой инфаркт начинается в субэндокарде, просто потому, что он имеет самые плохие предпосылки в случае ишемии. Субэндокард расположен слишком далеко от полости желудочка, чтобы получать кислород из полости. Более того, он получает кровь, которая уже извлечена из большей части кислорода, поскольку она прошла через большую часть стенки желудочка (коронарный кровоток направлен от эпикарда к эндокарду ( Рисунок 3 ).
Электрокардиограммы (ЭКГ, ЭКГ) и другие специализированные тесты ЭКГ
Электрокардиограмма (также называемая ЭКГ или ЭКГ) — это тест, который регистрирует электрическую активность вашего сердца через небольшие электроды, прикрепленные к коже груди, рук и ног. .ЭКГ может быть частью обычного медицинского осмотра или использоваться в качестве теста на сердечные заболевания. ЭКГ можно использовать для дальнейшего исследования симптомов, связанных с проблемами сердца.
ЭКГ — это быстрые, безопасные, безболезненные и недорогие тесты, которые обычно выполняются при подозрении на сердечное заболевание.
Ваш врач использует ЭКГ, чтобы:
- Оценить ваш сердечный ритм
- Диагностировать плохой кровоток в сердечной мышце (ишемию)
- Диагностировать сердечный приступ
- Оценить определенные аномалии вашего сердца, например, увеличенное сердце
Как мне подготовиться к ЭКГ?
Чтобы подготовиться к ЭКГ:
- Не используйте кремы и лосьоны для жирной или жирной кожи в день обследования.Они мешают контакту электрода с кожей.
- Избегайте чулочно-носочных изделий во всю длину, потому что электроды необходимо размещать непосредственно на ногах.
- Наденьте рубашку, которую можно легко снять, чтобы повесить провода на груди.
Что происходит во время ЭКГ
Во время ЭКГ техник прикрепит 10 электродов с липкими подушечками к коже груди, рук и ног. Мужчины могут сбрить волосы на груди, чтобы улучшить связь. Вы будете лежать ровно, пока компьютер рисует на миллиметровой бумаге электрические импульсы, проходящие через ваше сердце.Это называется ЭКГ в состоянии покоя. Этот же тест можно использовать для контроля вашего сердца во время упражнений.
Присоединение электродов и завершение теста занимает около 10 минут, но фактическая запись занимает всего несколько секунд.
Ваши шаблоны ЭКГ будут храниться в файле для последующего сравнения с будущими записями ЭКГ.
Если у вас есть вопросы, обязательно спросите своего врача.
Что такое холтеровский монитор?
В дополнение к стандартной ЭКГ ваш врач может порекомендовать другие специализированные тесты ЭКГ, включая холтеровское мониторирование или электрокардиограмму с усредненным сигналом.
Холтеровское мониторирование — это портативная ЭКГ, которая контролирует электрическую активность сердца человека, как правило, в течение одного-двух дней, 24 часа в сутки. Его чаще всего используют, когда врач подозревает нарушение сердечного ритма или ишемию (недостаточный приток крови к сердечной мышце).
Это безболезненный тест; электроды от монитора приклеиваются к коже липкой лентой. Как только монитор будет на месте, вы можете пойти домой и заняться всеми своими обычными делами (кроме душа). Вас попросят вести дневник вашей деятельности и любых симптомов, которые вы испытываете, и когда они возникают.
Что такое монитор событий?
Если симптомы возникают нечасто, врач может порекомендовать монитор событий. Это устройство, которое при нажатии кнопки записывает и сохраняет электрическую активность сердца в течение нескольких минут. Каждый раз, когда у вас появляются симптомы, вы должны пытаться получить показания на мониторе. Мониторы событий обычно используются в течение одного месяца. Эта информация может быть позже передана по телефону врачу для интерпретации.
Что такое электрокардиограмма с усредненным сигналом?
Это безболезненный тест, используемый для оценки того, подвержен ли человек высокому риску развития потенциально смертельной сердечной аритмии.Он выполняется аналогично ЭКГ, но с использованием сложных технологий для выявления риска сердечных аритмий.
Электролитные аномалии
Автор: Шэрон Борд, доктор медицины, FACEP
Редактор: Кенни Бан, доктор медицины
Введение
У пациентов часто бывает электрокардиограмма (ЭКГ). отделение неотложной помощи. Эту ЭКГ можно использовать для оценки ишемических изменений, но также она может дать врачу возможность заблаговременно оценить уровень электролитов у пациента.Сочетание истории болезни в сочетании с результатами ЭКГ, соответствующими повышенному уровню калия, должно побудить к неотложному лечению для стабилизации сердечной оболочки.
Цели
- Выявить изменения ЭКГ, связанные с гипер- и гипокалиемией
- Выявить изменения ЭКГ, связанные с гипер- и гипокальциемией
- Обсудить общую этиологию и клиническую картину каждой из вышеперечисленных электролитных аномалий
Гиперкалиемия
Повышенный уровень калия — распространенное и опасное для жизни состояние, которое наблюдается в отделении неотложной помощи.Гиперкалиемия определяется как сывороточный К, превышающий 5,5. Для снижения заболеваемости и смертности, связанных с этим заболеванием, ключевым моментом является раннее выявление и лечение. Важно помнить, что калий — это прежде всего внутриклеточный катион. Когда наблюдается избыток внеклеточного калия из-за сдвигов или невозможности его выделения, пациенты могут испытывать аритмию и, возможно, остановку сердца.
Обратите внимание на пиковые зубцы T у этого пациента с калием 7,0Выполнение ранней ЭКГ, особенно у пациентов с высоким риском, с уделением особого внимания изменениям, связанным с гиперкалиемией, может спасти жизнь.Пациенты с высоким риском включают пациентов, получающих заместительную почечную терапию (перитонеальный или гемодиализ), пациентов с подозрением на диабетический кетоацидоз или пациентов с острой почечной недостаточностью. ЭКГ изменяет прогресс от пиковых зубцов T до расширенных QRS и, в конечном итоге, до желудочковой тахикардии, фибрилляции или остановки электрической активности без пульса. Эти прогрессирующие изменения могут коррелировать с повышением уровня калия. Например, пиковые зубцы T могут соответствовать уровню калия примерно 6, тогда как остановка сердца обычно происходит при более высоких уровнях.
Обратите внимание, как PR и QRS удлиняются при гиперкалиемии, пока у пациента не разовьется «синусоидальная» картина ЭКГ. Наиболее важным начальным лечением, которое следует назначить при обнаружении изменений на ЭКГ, является введение глюконата кальция или хлорида кальция. Некоторые практикующие врачи экстренной медицины рекомендуют вводить кальций только с пиковыми зубцами T. Другие будут лечить, только если будут обнаружены дополнительные результаты. Кальций стабилизирует сердечные оболочки и, в свою очередь, предотвратит дальнейшее развитие аритмий.После определения уровня калия дополнительное лечение, чтобы помочь в перемещении калия внутриклеточно и способствовать полному выведению из организма.
Гипокалиемия
ЭКГ также может дать раннее указание на низкий уровень калия. Гипокалиемия определяется как уровень калия ниже 3,5, но изменения на ЭКГ обычно не происходят, пока уровень не опустится ниже 2,7. Как и повышенный уровень калия, низкий уровень калия может вызвать аритмию миокарда и значительную эктопию.Изменения ЭКГ могут включать увеличение амплитуды и ширины зубца P, сглаживание и инверсию зубца T, заметные зубцы U и кажущиеся длинные интервалы QT из-за слияния зубцов T и U. Зубец U — это отклонение после зубца T. Гипокалиемия вызывает увеличенные и заметные зубцы Т на ЭКГ. Критически низкий уровень калия (<1,7) может привести к torsades de pointes.
Пациент с калием 1,7. Гипокалиемия может возникать вторично на фоне приема лекарств (наиболее частые причины включают гидрохлоротиазид и фуросемид), желудочно-кишечной недостаточности, чрезмерного лечения гиперкалиемии или переноса калия в клетки.Гипомагниемия часто бывает связана с гипокалиемией; поэтому важно проверять уровень магния у любого пациента с аритмией. Тяжелую гипокалиемию с изменениями ЭКГ следует лечить в срочном порядке с помощью внутривенного введения хлорида калия до K 4-4,5. Уровень магния также должен быть восполнен до уровня, превышающего 2.
Гиперкальциемия
Повышенный уровень кальция определяется как уровень более 2,7 ммоль / л, при тяжелой гиперкальциемии более 3.4 ммоль / л. Наиболее частая находка на ЭКГ, связанная с гиперкальциемией, — это укорочение интервала QT. В тяжелых случаях могут наблюдаться зубцы Осборна или J или может развиться фибрилляция желудочков. Распознавание этих результатов ЭКГ может потребовать неотложного лечения.
ЭКГ у пациента с гиперкальциемией, QT укорачивается. Гомеостаз кальция — это баланс костной абсорбции и реабсорбции, паратироидного гормона и, прежде всего, почечной экскреции. Причины гиперкальциемии включают гиперпаратиреоз, миелому, костные метастазы, синдром молочной щелочи, саркоидоз или избыточное потребление витамина D.Неотложное лечение для снижения уровня кальция включает внутривенную регидратацию, введение петлевых диуретиков или бисфосфонатов. Дальнейшее лечение после исчезновения изменений ЭКГ должно быть направлено на исправление или лечение основной причины.
Гипокальциемия
Основные жалобы пациентов с гипокальциемией включают карпопедальный спазм, нервно-мышечную возбудимость и возможное развитие тяжелых судорог. Помимо получения ранней ЭКГ для подтверждения диагноза, также могут быть проверены признаки Хвостека и Труссо.Признак Хвостека положительный, если лицевой нерв постукивать под углом челюсти, будут отмечены подергивания лицевых мышц с той же стороны. Симптом Труссо проявляется накачиванием манжеты для измерения кровяного давления выше систолического АД в течение трех минут. У пациентов с гипокальциемией наблюдается сокращение и спазм мышц кисти, запястья и пальцев.
Пациент с гипокальциемией, обратите внимание на длинный интервал QT.Наиболее частой находкой на ЭКГ у пациентов с гипокальциемией является удлинение интервала QT без каких-либо дальнейших изменений.Гипокальциемия редко вызывает более серьезные сердечные аритмии, хотя может быть обнаружена фибрилляция предсердий. Причины низкого уровня кальция включают гипопаратиреоид, низкий уровень витамина D, острый панкреатит и прием фуросемида.
Учебный центр ЭКГ — Введение в клиническую электрокардиографию
Извините, но этот сайт поддерживается только браузером, строго совместимым с HTML. Сайт может продолжать работать, но может отображаться некорректно.
Если вы используете Internet Explorer 6 или более раннюю версию, мы рекомендуем вам обновить ваш браузер до Intenet Explorer 8+ или попробовать совместимый браузер, например Firefox или Google Chrome.
Темы для изучения:
- Общие сведения о нарушениях ST-T и U-волны
- Высота сегмента ST
- Депрессия сегмента ST
Общее введение в аномалии зубцов ST, T и U
Базовая концепция: Специфичность аномалий ST-T и зубца U в большей степени обеспечивается клиническими обстоятельствами в которой обнаруживаются изменения ЭКГ, чем по самим частным изменениям.Таким образом, термин неспецифический ST-T abnormalities , часто используется, когда клинические данные недоступны для корреляции с результатами ЭКГ. Этот не значит, что изменения ЭКГ неважны! Ответственность за лечение пациенту, чтобы убедиться в важности результатов ЭКГ.
Факторы, влияющие на конфигурацию зубцов ST-T и U, включают:
- Собственное заболевание миокарда (например,, миокардит, ишемия, инфаркт, инфильтративные или миопатические процессы)
- Лекарственные средства (например, дигоксин, хинидин, трициклические препараты и многие другие)
- Электролитные нарушения калия, магния, кальция
- Нейрогенные факторы (например, инсульт, кровотечение, травма, опухоль и т. Д.)
- Метаболические факторы (например, гипогликемия, гипервентиляция)
- Реполяризация предсердий (например, при высокой частоте сердечных сокращений зубец T предсердий может опускать начало сегмента ST)
- Нарушения желудочковой проводимости и ритмы, возникающие в желудочках
«Вторичные» изменения ST-T (это нормальных ST-T изменений исключительно из-за изменений в последовательности желудочковой активации):
- Изменения ST-T, наблюдаемые при блокаде ножек пучка Гиса (обычно полярность ST-T противоположна главному или терминальному отклонению QRS)
- Изменения ST-T в пучковой блокаде
- Изменения ST-T при неспецифической IVCD
- Изменения ST-T, обнаруженные в предварительном возбуждении WPW
- Изменения ST-T при ЖЭ, желудочковых аритмиях и желудочковых ритмах
«Первичные» аномалии ST-T (изменения ST-T, которые не зависят от изменений желудочковой активации и могут быть результатом глобальных или сегментарных патологических процессов, влияющих на реполяризацию желудочков):
- Действие лекарств (e.г., дигоксин, хинидин и др.)
- Электролитные нарушения (например, гипокалиемия)
- Ишемия, инфаркт, воспаление и т. Д.
- Нейрогенные эффекты (например, субаррахноидальное кровоизлияние, вызывающее удлинение интервала QT)
Дифференциальная диагностика подъема сегмента ST
Нормальный вариант «Ранняя реполяризация» (обычно вогнутый вверх, заканчивающийся симметричными большими вертикальными зубцами T)
Пример №1: «Ранняя реполяризация»: обратите внимание на высокий отрыв сегмента ST в отведениях V4-6; подъем ST в V2-3 обычно наблюдается на большинстве нормальных ЭКГ; элевация ST в V2-6 вогнута вверх, что является еще одной характеристикой этого нормального варианта.
Ишемическая болезнь сердца (обычно выпуклая вверх или выпрямленная)
- Острая трансмуральная травма — как при этом остром переднем ИМ
- Устойчивое повышение сегмента ST после острого ИМ предполагает аневризму желудочков
- Элевация ST также может рассматриваться как проявление (вариантной) стенокардии Принцметала (спазма коронарной артерии)
- Элевация сегмента ST во время тестирования с физической нагрузкой свидетельствует о чрезвычайно сильном стенозе или спазме коронарной артерии (трансмуральной ишемии)
Острый перикардит
- Вогнутая элевация сегмента ST вверх в большинстве отведений, кроме aVR
- Нет реципрокной депрессии сегмента ST (кроме aVR)
- В отличие от «ранней реполяризации», зубцы T обычно имеют низкую амплитуду, а частота сердечных сокращений обычно увеличивается.
- Может наблюдаться депрессия сегмента PR, проявление травмы предсердий
Другие причины:
- Гипертрофия левого желудочка (в правом прекардиальных отведениях с большими S-зубцами)
- Блокада левой ножки пучка Гиса (в правом прекардиальных отведениях с большими S-зубцами)
- Гиперкалиемия тяжелой степени
- Гипотермия (заметные зубцы J или волны Осборна)
Дифференциальная диагностика депрессии сегмента ST
Обычные варианты или артефакты:
- Псевдо-депрессия ST (блуждающая базовая линия из-за плохого контакта кожи с электродом)
- Физиологическая депрессия J-соединения с синусовой тахикардией (скорее всего, из-за реполяризации предсердий)
- Депрессия сегмента ST, вызванная гипервентиляцией
- Ишемическая болезнь сердца
- Субэндокардиальная ишемия (вызванная физической нагрузкой или во время приступа стенокардии — как показано ниже)
- Депрессия сегмента ST часто характеризуется как «горизонтальная», «восходящая» или «нисходящая»
- MI без зубца Q
- Реципрокные изменения при остром инфаркте миокарда с зубцом Q (e.
- Субэндокардиальная ишемия (вызванная физической нагрузкой или во время приступа стенокардии — как показано ниже)




