Профилактика и лечение основных бактериальных болезней птицы — avisvet.ru
Опубликованно от 13.10.2015
Профилактика и лечение основных бактериальных болезней птицы (сальмонеллез, колибактериоз, орнитобактериоз, клостридиоз, кампилобактериоз, псевдомоноз, стафилококкоз)ПРОФИЛАКТИКА И ЛЕЧЕНИЕ ОСНОВНЫХ
БАКТЕРИАЛЬНЫХ БОЛЕЗНЕЙ ПТИЦЫ
(сальмонеллез, колибактериоз, орнитобактериоз, клостридиоз, кампилобактериоз, псевдомоноз, стафилококкоз)
Читать статью в формате PDF.
В последние 20-30 лет многие представления о микрофлоре птиц, её составе и роли в поддержании здоровья и возникновении заболеваний существенно изменились и обогатились. С современных позиций микрофлору птиц следует рассматривать как совокупность множества биоценозов, занимающих многочисленные экологические ниши на коже, слизистых всех открытых внешней среде полостей организма. О чрезвычайной сложности, населяющей организм человека, животных и птицу микрофлоры указывает тот факт, что в 1 грамме содержимого слепой кишки микробиологами определяется более 2-х биллионов микроорганизмов — представителей 17 различных семейств, 45 родов и свыше 400 видов. В любом организме всегда имеются постоянно обитающие виды бактерий и транзиторные условно-патогенные микроорганизмы. Микрофлора, присутствующая в организме птицы, находится между собой в разнообразных взаимоотношениях, и при недостатке или избытке того или иного субстрата, а также изменении окружающей среды, происходит быстрое нарушение микробной экологической системы.
Исследователями становлено, что наиболее распространёнными и приводящими к значительным потерям в бройлерном птицеводстве являются сальмонеллез (пуллорозтиф, паратифозные инфекции), колибактериоз, орнитобактериоз, кампилобактериоз, стафилококкоз, псевдомоноз, клостридиоз. Менее распространенные, но могут быть выделены у птиц при септическом процессе, такие микробы как гемофилы, пастереллы, клебсиеллы, листерелы, цитробактер, стрептококки и др.
По сообщениям печати, в странах Евросоюза медики и ветеринары обеспокоены распростране
симптомы, диагностика, лечение, меры профилактики, препараты
нет комментариев
0
Время на чтение: 7 минут


Название болезни: некротический энтерит (анаэробная энтеротоксемия, клостридиозный энтерит)
Токсико-инфекционная болезнь
Симптомы острой формы: истощение, диарея, полный отказ от еды, жажда, угнетение, малоподвижность, запрокидывание головы
Препараты для лечения: энрофлоксацин 10%, триэн 10%, энроксил 10%, байтрил 10%, 5% и 2,5%
Требуется вакцинация противококцидными препаратами
Болезнь смертельна для птицы
В целях борьбы с заболеванием проводится дезинфекция
Некротический энтерит является клинической формой последней стадии дисбактериоза. Часто предшественником или сопутствующим заболеванием энтерита является кокцидиоз. Инфекция проявляется в виде некроза кишечника, вызванного бактерией Clostridium perfringens, которая нарушает микрофлору ЖКТ и вызывает его воспаление.
Симптомы
Некротический энтерит существует в двух формах: острая клиническая форма и субклиническая. Острая форма преимущественно поражает цыплят в возрасте от 2 до 6 недель, в меньшей степени молодняк и взрослых особей.
Острая форма энтерита имеет следующие симптомы:
- резкое снижение аппетита;
- угнетенность и депрессия птицы;
- диарея с пометом темного цвета;
- молодняк по-разному набирает вес;
- закрытые глаза;
- взъерошенность перьев;
- судороги;
- смертность в течение 1-2 часов после начала судорог. Падеж до 1% в день от всего поголовья.
Субклиническое течение заболевания:
- задержка в росте молодняка;
- светлый липкий помет с непереваренным кормом;
- увеличение расхода кормов.
Чихание и хрипы у домашних кур: диагностика заболеваний верхних дыхательных путей, лечение, профилактика
ЧитатьПонос у цыплят: основные причины возникновения, распространенные заболевания, связанные с ним, способы профилактики и лечения
ЧитатьПотеря перьев и облысение у кур: при каких болезнях возможен этот симптом? Препараты для лечения самых распространенных заболеваний
ЧитатьЧтобы распознать заболевание на начальной стадии, следует регулярно отслеживать состояние помета кур и цыплят и следить за их общим состоянием.
Патологоанатомические изменения
Наблюдаются:
- некротические очаги на стенках тонкого кишечника, подвздошной впадины, двенадцатиперстной кишки;
- вздутый рыхлый кишечник;
- наличие в кишечнике темной, плохо пахнущей жидкости.
У вашей птицы похожие симптомы?
ДаНет
Патогенез
Некротический энтерит – инфекция, вызванная анаэробной грамположительной, споро- и токсинообразующей палочкой клостридией. Споры бактерии длительное время сохраняются в почве, в донном иле, разлагающихся растениях, воде и корме.
Попадая в организм птицы, сама по себе бактерия опасности не несет. Но при дисбалансе микрофлоры кишечника, вызванном плохим несбалансированным кормлением и болезнями, бактерии размножаются с большой скоростью и вызывают образование токсинов, которые, в свою очередь, разрушают слизистую стенок кишечника и эритроциты в крови.В отдельных случаях препятствуют передаче нервных импульсов к легким и сердцу, вследствие чего птица гибнет.
Диагностика
На начальной стадии развития болезнь диагностируют на основании характерных патологических изменений и бактериологического анализа соскоба слизистой кишечника. При микроскопическом исследовании обнаруживают грамположительные неподвижные палочки клостридий. Гистологические исследования показывают наличие очагов некроза.


Проводят лабораторные анализы помета птицы, подстилки, воды и почвы вокруг птичника, выделяя возбудителя инфекции. Диагноз подтверждают после выращивания бактерии на дифференциальной среде.
Лечение
Лечение в острой стадии неэффективно.
Лечение перманентной (субклинической) формы заболевания проводится антибиотиками. Дозировка рассчитывается, согласно содержанию действующего вещество в препарате.
Энрофлоксацин 10% , триэн 10%, байтрил 10%, энроксин 10% (содержание активного антибиотика 100 мг/1 мл раствора):
- взрослым курам, бройлерам с 2-х месяцев назначают по 10 мг на 1 кг массы особи в сутки, что эквивалентно 10 мл препарата на 10 л воды. Дают вместо питья в течение 5 дней. Расчет дозы производят, согласно массе особей:
- молодняку бройлеров, цыплятам 5 мл суспензии разводят в 10 л воды (5 мг антибиотика на 1 кг веса). Поят птицу от 3 до 5 суток. Дают только воду с антибиотиком. Количество готового раствора зависит от массы поголовья.
Мнение эксперта
Садчиков Николай Алексеевич
Ветеринар орнитолог
Задать вопросКурам-несушкам препараты, содержащие энрофлоксацин, противопоказаны ввиду накопления в яйцах активного вещества.
Байтрил 5% и 2,5 % (содержание энрофлоксацина 50 мг, 25 мг/1 мл раствора) готовят аналогично с байтрил 10%, высчитывая дозировку в соответствии с содержанием антибиотика на 1 мл жидкости.
Борьба с распространением
Для предотвращения распространения некротического энтерита принимаются следующие меры:
- из рациона птиц исключают рыбную и мясокостную муку;
- животные жиры заменяют растительными;
- пшеницу, ячмень и рожь заменяют на кукурузу;
- в корм и воду добавляют карбоновые кислоты;
- используют глубокую подстилку с хорошей вентиляцией;
- подстилку обрабатывают органическими кислотами для контроля в ней бактерий.
Ракушка как минеральная добавка для кур. В чем польза, с какого возраста и в каком виде можно давать?
СмотретьМел как кормовая добавка для кур – зачем он нужен?
ЧитатьКормление кур ячменем: можно ли давать его бройлерам?
ПодробнееИспользование молочной сыворотки в качестве источника белка животного происхождения
ЧитатьЯичная скорлупа в рационе кур и цыплят. Как правильно давать?
ПодробнееКак давать рыбий жир цыплятам, несушкам и бройлерам?
СмотретьТрикальцийфосфат кормовой для взрослых кур, цыплят и бройлеров
ДалееМеры профилактики
Лучшим способом борьбы с появлением дисбактериоза, а в дальнейшем и некротического энтерита служит своевременная профилактика и создание необходимых условий для содержания птицы:
- полнорационное кормление;
- правильная вакцинация молодняка кокцидиостатиками;
- поддержание правильной микрофлоры кишечника с помощью пробиотиков и пребиотиков;
- введение витаминных комплексов во избежание авитаминоза;
- наличие чистой питьевой воды;
- сухая свежая подстилка, хорошая вентиляция помещений;
- исключение стрессовых ситуаций для птицы;
- при использовании инкубатора полное обеззараживание последнего перед закладкой яиц;
- регулярная дезинфекция помещений и инвентаря.
По назначению ветеринарного врача для нормализации кишечной микрофлоры могут назначаться пробиотики (бифидобактерии и лактобациллы) и пребиотики (инулин, лактулоза).
Содержание птицы
Рейтинг курятников для зимнего и летнего содержания
Топ – 9Обзор лучших клеток для кур
Топ – 9Какую поилку выбрать для кур
Топ – 15Кормушки в курятник: бункерные, навесные, лотковые
Топ — 15Правильное кормление
- Корма
- Рецепты
- Добавки
Описание корма для яичных пород. Инструкция по кормлению кур несушек
Минеральный и витаминный составы, нормы кормления
Используется для кормления кур-несушек в возрасте 15-17 недель
Состав и инструкция по кормлению цыплят бройлеров
Важные отличия от предыдущей линейки, схемы применения Старт, Рост, Финиш
Проращивание и запаривание ячменя и пшеницы для кур: как правильно это сделать и как давать несушкам
Правила кормления бройлерных кур пшеницей. Дозировка для цыплят со второго дня жизни и взрослых птиц
Приготовление мешанки для бройлеров в домашних условиях
Как и в каком виде можно использовать рис и гречку для кормления кур. Нормы для взрослых птиц и цыплят
Каким хлебом можно кормить кур и как правильно это делать
Продукт дают в ограниченных количествах: переизбыток в кормлении может нанести серьезный вред птице Содержание
Мел как пищевая добавка для куриного корма. Нормы кормления для цыплят, молодняка и кур-несушек
Мясокостная мука – обязательная добавка для кормления кур, содержащая белок и жиры животного происхождения
Как давать рыбий жир цыплятам, несушкам и бройлерам. В чём польза препарата и существуют ли противопоказания
Известняковая (доломитовая) мука в рационе кур. Преимущество перед мелом и кормовой ракушкой
Суточная дозировка соли для взрослых птиц и молодняка и случаи нежелательного употребления
Препараты, которые используют при лечении
Для снижения риска заболеваемости кур и цыплят, а также для лечения используют антибиотики, пробиотики и пребиотики.
| Название | Описание препарата |
| Энрофлоксацин, байтрил, триэн, энроксил | Антибиотики широкого спектра действия группы фторхинолонов, активны в отношении грамположительных и грамотрицательных бактерий |
| Пробиотики (бифидобактерии и лактобациллы) | Добавка предназначена для восстановления микрофлоры кишечника, лечения дисбактериозов различной этиологии и инфекционных заболеваний |
| Пребиотики (инулин, лактулоза) | Пребиотические вещества способствуют стимуляции бифидобактерий, оказывают положительное влияние на микрофлору кишечника |
Для увеличения продуктивности и снижения общей заболеваемости достаточно поддерживать чистоту в курятнике и местах выгула птиц, а также следить за тем, чтобы куры получали все необходимые питательные вещества с кормом.
Автор статьи
Ветеринар орнитолог
Клостридиоз птиц — Паразиты человека
Опубликованно от 13.10.2015
Содержание статьи:
ПРОФИЛАКТИКА И ЛЕЧЕНИЕ ОСНОВНЫХ
БАКТЕРИАЛЬНЫХ БОЛЕЗНЕЙ ПТИЦЫ
(сальмонеллез, колибактериоз, орнитобактериоз, клостридиоз, кампилобактериоз, псевдомоноз, стафилококкоз)
Читать статью в формате PDF.
В последние 20-30 лет многие представления о микрофлоре птиц, её составе и роли в поддержании здоровья и возникновении заболеваний существенно изменились и обогатились. С современных позиций микрофлору птиц следует рассматривать как совокупность множества биоценозов, занимающих многочисленные экологические ниши на коже, слизистых всех открытых внешней среде полостей организма. О чрезвычайной сложности, населяющей организм человека, животных и птицу микрофлоры указывает тот факт, что в 1 грамме содержимого слепой кишки микробиологами определяется более 2-х биллионов микроорганизмов — представителей 17 различных семейств, 45 родов и свыше 400 видов. В любом организме всегда имеются постоянно обитающие виды бактерий и транзиторные условно-патогенные микроорганизмы. Микрофлора, присутствующая в организме птицы, находится между собой в разнообразных взаимоотношениях, и при недостатке или избытке того или иного субстрата, а также изменении окружающей среды, происходит быстрое нарушение микробной экологической системы.
Исследователями становлено, что наиболее распространёнными и приводящими к значительным потерям в бройлерном птицеводстве являются сальмонеллез (пуллорозтиф, паратифозные инфекции), колибактериоз, орнитобактериоз, кампилобактериоз, стафилококкоз, псевдомоноз, клостридиоз. Менее распространенные, но могут быть выделены у птиц при септическом процессе, такие микробы как гемофилы, пастереллы, клебсиеллы, листерелы, цитробактер, стрептококки и др.
По сообщениям печати, в странах Евросоюза медики и ветеринары обеспокоены распространением с продуктами питания таких зоонозов как кампилобактериоз, листериоз, которые вызывают у человека диарею.
Для профилактики инфицирования птицы возбудителями бактериальных болезней во всех птицеводческих хозяйствах, особенно на репродукторах первого и второго порядка мясных кроссов птиц, выполняют технологические, зоогигиенические, ветеринарные и санитарные требования, определенные ветеринарно-санитарными правилами для птицеводческих хозяйств и руководствами по выращиванию и содержанию птицы, а также программой биобезопасности.
Сальмонеллез
Распространение сальмонелл в птицеводческих хозяйствах значительно шире, чем об этом принято считать. Её находят практически везде (почва, растения, насекомые, домашние и дикие животные и птица, грызуны и т.д.). Мониторинг 5200 образцов кормового сырья, проведенный в Нидерландах в 1996 году, показал, что 13,5% рыбной муки, 2% соевого шрота, 17.2% рапсового шрота, 6.2% мясной муки инфицированы сальмонеллами. По сообщению ГУ переработки сальмонеллы были выделены в 148 случаях, что составляет 16.7%. Выделены 9 серотипов, но наиболее часто выделяемым является С.энтеритидис, тифимуриум, галинарум-пуллорум.
Существует две главные группы инфицирования организма кур сальмонеллой. К первой отнесены хозяин специфические неподвижные С. пуллорум-галинарум, которые вызывают пуллорозтиф. Эти сальмонеллы в 1970-1985 годы причиняли бройлерному птицеводству серьёзный экономический ущерб, но в результате проведения обширных программ серологических исследований и уничтожения птиц-бактерионосителей были искоренены. Ко второй группе относятся подвижные серотипы сальмонелл, т.н. паратифозные, в частности С. энтеритидис и тифимуриум, которые связаны с пищевыми токсикоинфекциями человека. С этими возбудителями предстоит длительная и напряженная борьба.
Болезнь у птицы проявляется поражением желудочнокишечного тракта и септицемией, пневмонией и артритами (род сальмонелл имеет более 2320 серотипов). Источником возбудителя инфекции является больная и переболевшая домашняя и дикая птица, животные, а также грызуны. Факторами передачи — инфицированные корма, вода, подстилка, предметы ухода, оборудование, одежда и обувь, инкубационное яйцо.
Симптомы: тифозное состояние и диарея у кур, а у цыплят — угнетение, белый понос, респираторные признаки и смертность в течение первых 1 -2 недель жизни. Патологические изменения у кур — воспаление яичников и кишечника, у цыплят — поражение слепой кишки, некротические очаги на сердце, легких, кишечнике, мышцах.
Диагностика: клиническая, серологическая, бактериологическая.
Лечение: антибиотикотерапия с применением ампицилина, тетрациклина, гентамицина, левомицетина, канамицина цыплятам 3-4 г на 1000 голов, взрослой птице — 40-45 мг/кг живой массы с кормом или водой в течение 6 дней. Для взрослой птицы применяют фуразолидон в дозе 400 г/тонну корма в течение 7-10 дней, а цыплятам — препараты на основе энрофлоксацина.
Ввиду того, что очень часто появляются штаммы сальмонелл, устойчивые к антибиотикам и химиотерапевтическим средствам, лечение необходимо проводить на основании антибиотикограммы и определении чувствительности сальмонелл к лекарственным средствам.
Наиболее радикальным решением проблемы является изоляция и ликвидация больных и подозрительных в заболевании птиц в прародительских и рапрародительских стадах племенной птицы, очистку и дезинфекцию помещений и скармливание птице гранулированных термическим способом комбикормов. Для предотвращения появления болезни на птицефабрике необходимо соблюдать ветеринарно-санитарные правила и проводить специфическую профилактику в родительских стадах с помощью живых и инактивированных вакцин. Было показано, что убитые или живые вакцины снижают восприимчивость кур к паратифозным инфекциям, а вырабатываемые антитела накапливаются в яйцах и обеспечивают цыплят достаточно сильной защитой. Израильская компания «Абик» разработала и предлагает для промышленного птицеводства России инактивированную вакцину «Сальмабик» для профилактики сальмонеллеза, вызванного С.энтеритидис и тифимуриум. У провакцинированных птиц иммунитет формируется через 21-28 суток и сохраняется 18 месяцев, при этом передаётся пассивный иммунитет потомству. Вакцина вводится двукратно, в нижнюю треть шеи в возрасте 9-12 недель и через 3-4 недели после первой вакцинации (не позднее 3 недель до начала яйцекладки). Применение этой вакцины в ряде птицеводческих хозяйств страны позволило стабилизировать Немецкая фирма «Ломанн Анималь» разработала живую вакцину против С.энтеритидис под названием «АвиПро Сальмонеллавак Е». Вакцина содержит метаболически мутировавший штамм с низкой вирулентностью и стимулирует развитие у цыплят клеточного и гуморального иммунитета, который наступает через несколько дней после оральной вакцинации и сохраняется на протяжении всего производственного цикла (60 недель).
Борьба с сальмонеллезом может быть эффективной, если она основана на 4-х классических принципах: получение суточных цыплят от здоровых племенных стад; скармливание птице чистых кормов; защита от распространения сальмонелл другими животными и человеком; хорошие условия содержания птиц в хозяйстве.
Колибактериоз
Болезнь представляет собой очень серьезную опасность для бройлерного производства во всем мире и приводит к огромным экономическим потерям из-за браковки, снижения сортности при убое бройлеров, привесов и ухудшения конверсии корма. В структуре падежа птиц от заразных болезней удельный вес колибактериоза в последние годы стабильно держится на уровне 75-80%.
Огромный научный материал, накопленный в нашей стране и за рубежом, показывает, что основную роль в развитии колибактериозной инфекции играют следующие факторы:
- Недостаточное и физиологически необоснованное кормление родительского стада, в результате которого из неполноценных инкубационных яиц выводятся недоразвитые цыплята.
- Нарушение зоогигиенических правил содержания родителей, в результате чего на инкубацию направляются яйца с загрязненной и инфицированной скорлупой, которые плохо поддаются эффективной дезинфекции.
- Антисанитарные условия инкубации и высокий уровень инфицированное™ цыплят на выводе.
- Недостаточный воздухообмен в птичниках в период интенсивного роста бройлеров.
- Бактериальная загрязненность комбикормов и наличие в стадах возбудителей вирусных болезней.
К настоящему времени известно более 9000 серологических вариантов кишечных палочек (эшерихий) по 0-,К- и Н-антигенам, но у птиц наиболее часто вызывают заболевания штаммы эшерихий следующих серогрупп: 078, 0115, 01, 02, 0111, 018, 026. Мониторинг патологического материала из 50 птицеводческих хозяйств, проведенный Государственным научным центром прикладной микробиологии в 2000-2003 годах, показал, что 99.8% выделенных культур относятся к Э.коли, а в ряде случаев выделена культура эшерихий с антигеном 0157:Н7, которая ответственна за возникновение геморрагического колита у людей.
Болезнь имеет самые различные симптомы, ассоциируемые чаще всего с другими заболеваниями: воспаление воздухоносных мешков (аэросаккулит), воспаление пуповины (омфалит), миокардит и перикардит, сальпингит, перитонит.синовит, панофтальмит, синдром «вздутой головы», целлюлит, энтерит.
Колибактерии — представители кишечной микрофлоры млекопитающих и птиц, и при хороших условиях содержания и кормления у птац не вызывают большого вреда. Болезнь получает развитие, когда иммунные механизмы у цыплят повреждены и снижена резистентность организма в условиях плохого воздухообмена, загрязнения бактериями воды и кормов, при нарушении кожного покрова и раздражении слизистой респираторного тракта аммиаком и пылью, воздействии токсинов и при недостатке питательных веществ. Большинство вспышек колибактериоза (омфалита) у бройлеров наблюдается в первые пять дней, и в возрасте 25 дней и старше. При наличии в стаде вирусов ньюкаслской болезни, инфекционного бронхита и ларинготрахеита заболевание протекает тяжело с высоким отходом птицы — 0.5-1.5% в сутки. Проявляется колибактериоз у бройлеров как респираторное заболевание в виде геморрагического трахеита, аэросаккулита, перигепатита и перикардита. Заболевшие бройлеры малоподвижны, хрипят, плохо едят.
Патологические поражения, которые наблюдаются при колибактериозе, характерны для многих заболеваний. Выделение и идентификация возбудителя, определение вирулентности и чувствительности кишечной палочки к лекарственным препаратам являются важными предпосылками успешной борьбы с инфекцией.
Возбудитель чувствителен к многим лекарствам: хлортетрациклину, левомицетину, ампицилину, гентамицину, сульфаниламидным и нитрофурановым препаратам, энрофоксацину, ципрофлоксацину и другим. Однако этот возбудитель может быть устойчивым к препаратам, особенно к тем, которые на протяжении долгого времени используются в хозяйстве. Поэтому определять чувствительность препарата к выделенному возбудителю необходимо в обязательном порядке, чтобы избежать использования неэффективных лекарственных средств и не усугублять ситуацию.
Эффективная профилактика заболевания может быть достигнута при соблюдении следующих условий:
- Проведение надлежащей очистки и дезинфекции помещений, кормового и вентиляционного оборудования при смене птицепоголовья.
- Использование кормов и воды, свободных от энтеропатогенных кишечных палочек, введение в корма и воду различных органических кислот для создания неблагоприятной среды для размножения микробов.
- Сокращение до минимума количества вакцинаций бройлеров живыми вакцинами против вирусных болезней мелкодисперсными аэрозолями.
- Регулярное истребление грызунов, фекалии которых источник патогенных кишечных палочек и сальмонелл.
- Полноценное витаминное, минеральное и аминокислотное питание племенной птицы и получение чистых, с крепкой скорлупой инкубационных яиц, соблюдение самого высокого уровня гигиены при инкубации яиц и выводе цыплят.
- Поддержание оптимального микроклимата в помещениях, исключение сквозняков и холода.
Орнитобактериоз
Заболевание в отечественном птицеводстве практически не известное и плохо изученное, хотя в странах Европы, Азии и Америке оно широко распространено и причиняет ощутимый экономический ущерб. Установлен факт циркуляции высоковирулентного штамма орнитобактериоза в птицеводческих хозяйствах Нидерландов, Германии — основных поставщиков племенной продукции в наши хозяйства. Трудности выделения и типизации возбудителя существенно осложняют его идентификацию и создают проблемы при организации мер борьбы и профилактики.
Болезнь у бройлеров проявляется в возрасте 3-4 недели. Наблюдают респираторные симптомы разной тяжести (ринит, коньюнктивит, «опухание головы»), а наиболее характерный патологоанатомический признак у бройлеров — воспаление воздухоносных мешков и скопление фибрина, наличие пенистого или йогуртоподобного экссудата, пневмония, перикардит.
По литературным данным известно, что американские изоляты орнитобактерий оказались устойчивыми к тетрациклину и апрамицину, но чувствительны к пенициллину; европейские — устойчивы к гентамицину, ампицилину, неомицину и триметаприму, но чувствительны к хлорамфениколу, амоксицилину. Сообщается, что для предотвращения орнитобактериоза оказалась эффективна комбинация болгарского препарата родотиума с тетрациклином, но были не эффективны энрофлоксацин и доксициклин.
Поэтому лечение орнитобактериоза затруднено из-за нестабильной чувствительности возбудителя к лекарственным препаратам.
Клостридиоз
Вспышки клостридиоза (некротического энтерита) отмечаются у бройлеров довольно часто в возрасте от двух недель при скармливании высоких доз некачественного соевого шрота и рыбной муки, которые плохо перевариваются, и характеризуется депрессией, снижением аппетита, диареей и взъерошенностью оперения. Клиническая форма заболевания характеризуется высокой смертностью. Предрасполагающим фактором является повреждение слизистой оболочки кишечника грубой клетчаткой и семенами сорных трав, а также различными штаммами кокцидий. Патолого-анатомические изменения обычно встречаются в двенадцатиперстной, тощей и подвздошной кишках. Слизистая оболочка утолщена и покрыта свободно или плотно прилегающей фибринознодифтеритической мембраной. Кишечник наполнен газами и имеет «вареный вид», часто увеличена печень.
Для лечения и профилактики болезни эффективно используются различные лекарственные средства: ампицилин, энрофлоксацин, бацитрацин, линкомицин, окситатграциклин, фуразолидон с кормом или с водой. Компания «ИНВЕ Нутри-Ад Балтия» рекомендует применять препарат Адимикс-натриевая соль масляной кислоты в сочетании с подкислителем кормов и воды Сальмо-Нил, а также адсорбент токсинов Токси-Нил. Однако, некротический энтерит — это сложное многофакторное заболевание, поэтому введение любой альтернативной кормовой и лечебной добавки с целью поддержания продуктивности бройлеров и контроля возникновения заболевания должно сопровождаться жёсткими гигиеническими и санитарно-ветеринарными мерами.
Псевдомоноз
Заболевание вызывается синегнойной палочкой, протекает по типу острой или хронической токсикосептикоинфекции и поражает в основном куриные эмбрионы и цыплят 1 — 10 дневного возраста, т.е. в первые дни жизни. Разрывы скорлупы яиц в любой период инкубации ведут к массовому заражению цыплят на выводе, повышенному отходу бройлеров при выращивании. При вскрытии трупов наблюдают одно или двухстороннюю пневмонию и перерождение печени, увеличение желчного пузыря, иногда — отложение мочекислых солей в почках и мочеточниках. В лечебно-профилактических целях применяются антибактериальные препараты согласно результатам постановки чувствительности. Очень часто культура чувствительна к гентамицину, амикацину и стрептомицину, но не чувствительна к энрофлоксацину, тетерациклину, ампицилину и фуразолидону.
Появление псевломоноза на бройлерной птицефабрике — признак низкой ветеринарно-санитарной культуры ведения производства, особенно в инкубатории, и использования некачественных кормов.
Стафилококкоз (стафилококк овый артрит)
У взрослой птицы (кур и петухов) и бройлеров, особенно при содержании их на сетчатых и планчатых полах и клетках, это заболевание стало одной из важных проблем. Потери от болезни (выбраковка племенной птицы по причине артритов, тендовагинитов, снижение выводимости и оплодотворяемости) очень велики, например, в Нидерландах они оценивались примерно в 30 млн. франков в год. Исследования показали, что связки у птиц тяжелых пород менее прочны и устойчивы к натяжению, чем у яичных. Показано, что заражение связок и суставных капсул происходит стафилококком, который фильтруется через кровь и необходим какой-то стресс для проявления заболевания.
Стафилококк может вызвать:
- Флегмону на голове взрослых кур после ранения их петухами в период спаривания, при этом голова опухает, и кожа на ней окрашивается в сине-зеленый цвет. Число пораженных кур может достигать 5%.
- Опухание подошв на ногах (абсцесс) среди молодняка и кур, чаще петухов, особенно при плохой (твердой, влажной) подстилке и в клетках.
- Некротический геморрагический дерматит сережек и мочек у взрослой птицы.
- Опухание суставов конечностей — инфекционный синовит.
- Воспаление пуповины (омфалит) — у вылупившихся цыплят при открытой пуповине.
Ранними клиническими признаками являются: взъерошенное оперение, прихрамывание, угнетение, диарея.
При опухании суставов птица плохо двигается и больше сидит, опираясь на грудную кость, вследствие чего развиваются намины. Для стафилококкоза характерен низкий процент заболеваемости и смертности, однако выбраковка птиц всегда увеличивается.
Патолого-анатомические изменения проявляются разнообразно. Опухшие суставы наполнены серозным, фибринозным или казеозным экссудатом, суставной хрящ эрозирован, наблюдается некроз головки бедренной кости. При септицемии — катаральный энтерит, пневмония, перикардит, некротические участки на печени и гиперемия печени, селезенки и почек.
Диагноз ставится на основании патолого-анатомических изменений и бактериологических исследований.
Профилактика болезни основана на устранении предрасполагающих причин и строгом соблюдении зоогигиенических и технологических требований. Лечение лекарственными средствами эффективно, но обязательно необходимо проводить тесты на чувствительность возбудителя, т.к. для стафилококков характерна устойчивость к антибиотикам. Применяют сульфаниламиды, линкомицин, гентамицин, хлортетрациклин, хлорамфеникол, биовит-80 и сочетания, например, препарат леновит — синергидное действие левомицетина, норсульфазола и хлортетрациклина в дозе 2.5 кг/т корма в течение 10-12 дней.
Кампилобактериоз
Европейское агентство по безопасности продуктов питания и европейский центр по профилактике и контролю за заболеваниями в отчете за 2007 год указывают, что кампилобактериоз является самым распространенным зоонозным заболеванием среди людей (200507 случаев — рост по сравнению с 2006 г составил 14.2%). Кампилобактерии обнаруживаются в сыром птичьем мясе в 26% случаев.
Изучение встречаемости видов кампилобактерий у птицы показало, что она колебается от 6% в Швеции и 10% в Финляндии и Норвегии до 100% в Италии. Несмотря на предпринятые многочисленные исследования, источники заражения птицы Кампилобактериозом остаются неизвестными. Согласно действующей инструкции в нашей стране, хозяйство считается благополучным по кампилобактериозу, если при исследовании патологического материала (15-20 проб) уровень инфицированности не превышает 50%.
Мероприятия по профилактике и борьбе с кампилобактериозом птиц проводятся на основе действующих ветеринарно-санитарных правил для птицеводческих хозяйств и инструкции «Профилактика и борьба с заразными болезнями, общими для человека и животных», раздел 4 (СП 3.1.087-96 и ВП 13.4.1307-96). Особое внимание следует обращать на очистку и дезинфекцию бункеров для кормов и кормовозов с постоянным микробиологическим контролем; соблюдать режим очистки, дезинфекции тары и грузовиков для перевозки бройлеров; в ванну для шпарки добавлять 40 мл/л соляной кислоты; обрабатывать тушки аэрозолем воды в течение 15 сек. или 1-2% раствором молочной кислоты при pH 2.0, а их охлаждение в воде с содержанием активного хлора 10-20 мг/л; соблюдать правила личной гигиены работниками цехов убоя и переработки птицы.
Большинство штаммов кампилобактерий полирезистентны и обладают устойчивостью ко многим антибиотикам. Эффективны гентамицин, левомицетин, фуразолидон, ципрофлоксацин, ампицилин, линкомицин. Препараты следует применять только после определения чувствительности к ним выделенных кампилобактерий.
Читать статью в формате PDF.
Николай Васильевич Кожемяка —
заслуженный ветеринарный врач Российской Федерации, специалист по промышленному птицеводству. Годы жизни 1937-2010. В этом году исполняется 5 лет как Николай Васильевич ушел из жизни.
Николай Васильевич Кожемяка – в 1965 году окончил Московскую Ветеринарную Академию и был направлен для работы во Всесоюзный научно-исследовательский и технологический институт птицеводства ВНИИТИП на Загорскую экспериментальную базу, где с 1965 по 1966 год работал в должности ветеринарного врача, а затем в 1966 году переведен на должность главного ветврача. С 1969 года работал в должности старшего экономиста в отделе ветеринарии в Птицепроме МСХ СССР, откуда был откомандирован в рамках правительственной программы помощи дружественным странам на Кубу главным ветеринарным врачом-эпизоотологом по птицеводству. Вернувшись на родину в 1972 году, продолжил научные изыскания в Московской ветеринарной академии и свою работу в Птицепроме СССР в должности главного специалиста отдела ветеринарии.
Продолжая свою профессиональную деятельность Николай Васильевич работал в должности начальника отдела ветеринарии, а затем в должности начальника отдела ветеринарной защиты и санитарного контроля. С 1991 по 2001 год при Российской академии сельскохозяйственных наук был экономистом I категории, а также главным ветврачом – руководителем группы спецпроектов по ветеринарии. Н.В.Кожемякой опубликовано более 70 статей, посвященных патологиям птицы и решению ветеринарных проблем, он соавтор 7 методических рекомендаций по выращиванию бройлеров и производству мяса яиц, автор книги «Справочник ветеринарного врача птицеводческого предприятия». Соавтор нескольких отечественных яичных кроссов. С 2001 по 2010 годы Николай Васильевич Кожемяка руководил консультационно-аналитическим отделом в ветеринарной компании «АВИС». По материалам публикации “Справочник ветеринарного врача бройлерного предприятия”, с разрешений ГК “АВИС”.
Фото Наталии Бауэр
Source: avisvet.ru
Почитайте еще:
Дифференциальная диагностика клостридиозов с использованием ПЦР
к.б.н. Афонюшкин В.Н., Черепушкина В.С., Киревичева А.С. Дударева Е.В., к.б.н.Филипенко М.Л., ФГБНУ Институт экспериментальной ветеринарии Сибири и Дальнего Востока, Новосибирская обл. п. Краснообск, ФГБУН Институт химической биологии и фундаментальной медицины, Новосибирск
Клостридиозы кур вызываемые Clostridium. perfringens наносят существенный экономический ущерб экономики птицефабрик и могут являться причиной заражения и отравления людей потребляющих птицеводческую продукцию с неблагополучных по клостридиозам птицефабрик. С использованием ПЦР анализа, гистологических и микробиологических методов оценили инфицированность кишечника кур и цыплят-бройлеров различных возрастов. Обнаруженный неравномерный характер распределения процента инфицированных цыплят (0-80%), свидетельствует или о наличии неучтенных факторов влияющих на восприимчивость к заражению (например, структура микробиоценоза кишечника), либо эффективность санитарных мероприятий, достаточна для предотвращения заноса С. perfringens в отдельные птичники
Ключевые слова: Clostridium perfringens, клостридиозы, полимеразная цепная реакция, куры, цыплята-бройлеры
Clostridium. perfringens — грамположительная, анаэробная спорообразующая палочковидная бактерия рода Clostridium. Подобно другим клостридиям, C. perfringens широко распространены во внешней среде, особенно в окультуренных (унавоженных) почвах. Они сохраняются здесь не только в виде спор, но и активно вегетируют, особенно при повышенной (45 ° C) температуре. Вместе с тем представители этого вида, пожалуй, больше, чем другие клостридии, экологически связаны с кишечником человека и животных [2-4]. По спектру продуцируемых токсинов различают пять типов C. perfringens — А, B, C, D, E. Заболевания человека чаще связаны с типом А (газовая гангрена, пищевое отравление) и изредка — С (некротизирующий энтероколит). В целом понятие «токсин» у C. perfringens довольно расплывчато, объединяя не менее 14 факторов с летальной и гистолитической активностью. Главными являются альфа (α) — , бета (β) — , эпсилон (ε) — и йота (ι) — токсины. [3]. Существуют различные методы для идентификации бактерий, многие из них являются трудоемкими, дорогими, а также обладают низкой чувствительностью и специфичностью [2.]. Актуальность работы также связана с широкой распространенностью на птицефабриках токсикозов и инфекций ассоциируемых с C.perfringens, наличием рисков заражения людей и рисками возникновения как спорадических, так и массовых случаев токсикоинфекций. Для диагностики пищевых и кормовых токсикоинфекций, вызванных C.perfringens, применяют методы микробиологического анализа, предпочтительно с оценкой содержания спор на 1 гр. кишечного содержимого (диагностически значимым критерием является наличие более 10 5 спор/гр) [5, 6]. Также используют серологическую диагностику [7, 8]. Важное значение имеет определение типа токсина, продуцируемого микроорганизмом [9-12].
Клостридиозы у птицы возникают скорее не вследствие самого факта заражения клостридиями, а вследствие создания их высокой концентрации в организме за счет размножения или поступления извне в высокой концентрации [13-15]. Поэтому сложной задачей является дифференциальная диагностика клостридиозов. Одним из путей решения проблемы является анализ инцидентности на основе массовых скрининговых исследований у птицы с различными уровнями манифестации клостридиозов (а также с отсутствием оных).
Цель исследования заключается в усовершенствовании критериев дифференциальной диагностики клостридиальных поражений печени и кишечника у кур и цыплят-бройлеров
Материалы и методы
Исследования проводились в секторе молекулярной биологии птиц ФГБНУ ИЭВСиДВ и лаборатории фармакогеномики ФГБУН ИХБФМ
Для изучения уровня инфицированности кур C.perfringens исследовали 1052 пробы клоакальных смывов, более 50 проб патологического материала отобранных на 7 птицефабриках РФ.
Клостридий культивировали на бульоне Шедлера. Выделение ДНК из культур осуществляли методом с FAST, силико-сорбционным и фенол-хлороформным методами. Выявление геномной ДНК C.perfringens в биоматериале птицы проводили с использованием двух методических подходов: 1- Прямое детектирование геномной ДНК, выделенной из патологического материала (печень, кишечное содержимое) силико-сорбционным методом. 2- Предварительное обогащение проб биоматериала путем культивирования в анаэробных условиях в пробирках с бульоном Шедлера. В последующем проводили выделение геномной ДНК силико-сорбционным методом и методом с FAST. Для гистологических исследований, материал фиксировали 10% раствором забуференного формалина, кусочки тканей пропитывали парафином, после предварительного обезвоживания в возрастающих концентрациях спиртов. Срезы окрашивали метиленовым синим по Леффлеру и гематоксилин-эозином по Вейгерту.
ПЦР в режиме реального времени с Taqman зондом проводили на реалтайм-амплификаторе «MiniOpticon» (BioRad) и LightCicler (Roche). Праймеры для детектирования C.perfringens. имели следующую структуру: CPF1 acatgttcagctgaccgatact (Tm=61.33), CPF2 cacgtgctctaccgactga ( Tm=61.49), Taqman зонд имел структуру Fam- catcggcttctaaaggcttaaccgtc –BHQ. ПЦР проводили в конечном объеме 25 мкл, содержащем 67 мМ трис. -HCl (рН 8,9), 16 мМ сульфат аммония; 2,4 мМ MgCl2; 0,01% Твин 20; 0,2 mM дНТФ; 0,5 mкM растворы олигонуклеотидных праймеров, Taq-ДНК полимераза 1-2ед.
Результаты собственных исследований и обсуждение
Дифференциальную диагностику гепатитов проводили с использованием комплекса методов: эпизоотологического, патологоанатомического, гистологического и ПЦР.
При патологоанатомических исследованиях обращали внимание на наличие некротических изменений в слизистой желудочно-кишечного тракта толстого и тонкого отдела кишечника, некроза печени. Также, по мнению специалистов птицефабрик, признаком клостридиоза являлось газообразование в толстом отделе кишечника. Однако массовое проявление газообразования у трупов птицы род. стада одной из птицефабрик в августе 2014 г. не сопровождалось наличием клостридий, по данным ПЦР. Микробиологические исследования позволили выделить дрожжеподобные грибы рода Candida, наличие которых в кишечнике также сопровождается бродильными процессами. Вышеупомянутые изменения в печени и кишечнике встречались преимущественно у птицы родительского стада т.е. взрослой птицы, несушки и бройлеров предубойного возраста. Тем не менее, положительные пробы ПЦР у птицы с такой пораженной печенью встречались в 12-37% случаев. Наличие положительных, на наличие ДНК C. perfringens проб печени, тем не менее, также не может свидетельствовать о первичной этиологической роли клостридий в поражении печени и кишечника.
Так, при гистологическом исследовании, в очагах некротических поражений печени и кишечника встречались клостридии (Рис. № 1).
Рис. 1 Наличие клостридий в очагах поражения слизистой кишечника птиц
На птицефабрике бройлерного направления в 2014 г, мы отмечали рост смертности цыплят-бройлеров, нарастающей к убою, начиная с 30 дневного возраста, за 2 месяца, к октябрю сохранность, в среднем, снизилась с 96 до 93%. Более значительный ущерб понесло родительское стадо, где на 1 птичник с 20 тысячным поголовьем, в среднем, смертность достигала 20-25 голов в день, что превышало нормативы в 4-5 раз. При этом также отмечались некротические поражения в печени и только одна проба печени из восьми, содержал ДНК C.perfringens, по данным ПЦР. Данный факт косвенно указывал об отсутствии значимой роли С. perfringens в возникновении некротических поражений печени. Комплекс патологоанатомических, эпизоотологических и гистологических исследований, показал отсутствие ассоциации клостридий с поражениями печени и позволил установить наличие гепатоспленомегалии.
Обращаемость ветеринарных специалистов по поводу клостридиозов носила, преимущественно, сезонный характер и затрагивала осенний и весенний периоды как в 2014 г. так и 2010—2013 гг. (срок наблюдения). Следует отметить, что в эти же периоды, на неблагополучных птицефабриках, встречался синдром массовых коагулопатий ассоциированных с «белой» стенкой кишечника. Особенностью коагулопатий являлось быстрое свертывание крови при контакте с воздухом, а в стенке кишечника встречались аномально удлиненные энтероциты (рис. 3) (данный синдром был описан нами ранее [16]).
Рисунок 3. Аномальная «вытянутость» энтероцитов при синдроме белая стенка кишечника – коагулопатия.
Можно предположить, что факторы предрасполагающие к возникновению синдрома коагулопатии – белой стенки кишечника и росту встречаемости некротических энтеритов-гепатитов, являются общими. Однако данное предположение требует дополнительного накопления статистических данных.
Для изучения уровня инфицированности кур C.perfringens исследовали 1052 пробы клоакальных смывов. Протокол исследований был следующий:
- Тампоны стерильными ножницами отрезали и помещали в пробирку эппендорфа с 800 мкл бульона Шедлера под вазелиновым маслом
- Пробы инкубировали при 37оС в течение суток
- Удаляли питательную среду, тампон и минеральное масло и к осадку бактерий добавляли 300 мкл. FAST
- Пробы прогревали при 95оС 10 минут
- Выделенную ДНК использовали для проведения ПЦР.
Как следует из таблиц №№1, 2, во-первых, птичники неравномерно распределяются по инфицированности цыплят-бройлеров на основании анализа клоакальных смывов методом ПЦР с предварительным подращиванием образцов.
Первые положительные пробы появляются у цыплят, начиная с возраста 19-20 суток, что можно объяснить появлением протяженных анаэробных зон желудочно-кишечного тракта и повышением вероятности заражения клостридиями с увеличением возраста.
Таблица -1. Инфицированность С. perfringens клоакальных смывов цыплят — бройлеров и птицы род. стада клоакальных смывов в августе 2014 года
| возраст | Процент положительных проб в неблагополучных птичниках | Средний процент положительных проб в неблагополучных птичниках | n | Кол-во птичников | Кол-во птичников не имеющих зараженной птицы |
| 5-8 | 0 | 0 | 80 | 4 | 4 |
| 10-12 | 0 | 0 | 80 | 4 | 4 |
| 19-21 | 8,3-25 | 13,04 | 112 | 5 | 2 |
| 30 | 80-45 | 62,5 | 120 | 6 | 4 |
| 35-36 | 15-35 | 23,3 | 120 | 6 | 0 |
| 39-40 | 35-45 | 39,16 | 120 | 6 | 0 |
| Взрослые (род стадо) | 0 | 0 | 100 | 5 | 5 |
Таблица — 2. Инфицированность С. perfringens клоакальных смывов цыплят — бройлеров и птицы род. стада клоакальных смывов в октябре 2014 года
| Возраст, дн. | Процент положительных проб в неблагополучных птичниках | Средний процент положительных проб в неблагополучных птичниках | n | Кол-во птичников | Кол-во птичников не имеющих зараженной птицы |
| 30 | 20-15 | 17,5 | 80 | 4 | 2 |
| 35-36 | 10 | 10 | 80 | 4 | 3 |
| 39-40 | 0 | 0 | 80 | 4 | 4 |
| взрослые | 5 | 5 | 80 | 4 | 3 |
Неравномерный характер распределения процента инфицированных цыплят, свидетельствует или о наличии неучтенных факторов влияющих на восприимчивость к заражению (например, структура микробиоценоза кишечника), либо эффективность санитарных мероприятий, достаточна для предотвращения заноса С. perfringens в отдельные птичники. Неравномерность благополучия разных птичников в отношении C.perfringens позволяет считать метод оценки инфицированности цыплят, данным инфекционным агентом, достаточно информативным в качестве оценки рисков возникновения клостридиозов.
Заключение: В структуре дифференциальной диагностики некротических энтероколитов – гепатитов, вызванных токсикоинфекцией С. perfringens ПЦР — диагностика позволяет верифицировать результаты гистологических и патологоанатомических исследований, инфицированность цыплят-бройлеров, по данным анализа клоакальных смывов, в возрасте 19-35 дн. (в неблагополучных, по наличию клостридий, птичниках) варьирует от 8,3-80%.
- Список использованных источников
- В.Н. Афонюшкин, М.Л. Филипенко, Ю.И. Хрипко, Е.В.Дударева Вопросы разработки и оптимизации ПЦР в режиме реального времени для выявления труднокультивируемых и некультивируемых бактериальных патогенов на примере Ornithobacterium rhinotracheale/Сборник трудов всероссийской научно-практической конференции с международным участием «Молекулярная диагностика -2010» Москва, 2010 Том II, -C. 52-55
- Canard, B., Saint-Joanis, B. & Cole, S. T. Genomic diversity and organization of virulence genes in the pathogenic anaerobe Clostridium perfringens. Mol Microbiol 6, (1992). 1421—1429.
- Granum, P. E. & Stewart, G. Molecular biology of Clostridium perfringens/ In Genetics and Molecular Biology of Anaerobic Bacteria, (1993). pp. 235-247. Edited by M. Sebald. New York: Springer.
- A. Fimlaid, J. P. Bond, K. C. Schutz1, E. E. Putnam1, J. M. Leung,
- D. Lawley, A. Shen Global Analysis of the Sporulation Pathway of Clostridium difficile //PLOS Genetics, 2013, Vol. 9 (8), e1003660, doi:10.1371/journal.pgen.1003660
- Nowell V.J., Kropinski A.M., Songer J.G., MacInnes J.I, Parreira V.R, Prescott J.F. Genome sequencing and analysis of a type A Clostridium perfringens isolate from a case of bovine clostridial abomasitis.// PLoS One. 2012;7 (3):e32271. doi: 10.1371/journal.pone.0032271. Epub 2012 Mar 8.
- Parreira V.R., Costa M., Eikmeyer F., Blom J., Prescott J.F. Sequence of two plasmids from Clostridium perfringens chicken necrotic enteritis isolates and comparison with C. perfringens conjugative plasmids.// PLoS One. 2012;7 (11):e49753. doi: 10.1371/journal.pone.0049753. Epub 2012 Nov 26.
- Miyamoto K., Yumine N., Mimura K., Nagahama M., Li J., McClane B.A., Akimoto S. Identification of novel Clostridium perfringens type E strains that carry an iota toxin plasmid with a functional enterotoxin gene.// PLoS One. 2011;6 (5):e20376. doi: 10.1371/journal.pone.0020376. Epub 2011 May 31.
- Rood, & Cole T. Molecular genetics and pathogenesis of Clostridium perfringens. Microbiol Rev 55, (1991). pp.621-648.
- Hauschild, A. H. W. 1975. Criteria and procedures for implicating Clostridium perfringens in foodborne outbreaks. Can. J. Public Health 66:388-392.2.
- Hatheway, C. L., D. N. Whaley, and V. R. Dowell, Jr. 1980. Epidemiological aspects of Clostridium perfringens foodborne illness. Food Technol. 34:77-79;90.
- Harmon, S. M., and D. A. Kautter. 1986. Evaluation of a reversed passive latex agglutination test kit for Clostridium perfringens J. Food Prot. 49:523-525.
- Berry, P. R., J. C. Rodhouse, S. Hughes, B. A. Bartholomew,and R. J. Gilbert. 1988. Evaluation of ELISA, RPLA, and Vero cell assays for detecting Clostridiun perfringens enterotoxin in faecal specimens. J. Clin. Pathol. 41:458-461.
- Berry, P. R., A. A. Wieneke, J. C. Rodhouse, and R. J. Gilbert. 1987. Immunological techniques in microbiology. Soc. Appl. Bacteriol. Tech. Ser. 24:245-254.
- Stringer, M. F. 1985. Clostridium perfringens type A food poisoning, p. 117- In S. P. Borriello (ed.), Clostridia in gastrointestinal disease. CRC Press, Boca Raton, Fla.
- В. Н. Афонюшкин, С. В. Леонов, Л. И. Сулимова, Н. А. Сигарева, Изучение массовой коагулопатии и сопутствующие патологии сельскохозяйственной птицы в Сибирском регионе в 2007–2008 гг.// БИО №8 (107), август 2009 г., -С. 4-6
Клостридиоз КРС: симптомы и лечение, вакцина
Каждый фермер сталкивается с различными заболеваниями крупного рогатого скота. Одни диагностировать легко, другие, наоборот, поддаются диагностике сложно. Болезни могут протекать начиная с лёгкого недомогания и могут заканчиваться летальным исходом. Сегодня речь пойдёт о клостридиозе, которому долго не уделяли должного внимания.
ПоказатьСкрытьЧто такое клостридиоз
 Клостридиоз является инфекционным заболеванием крупного рогатого скота. Кроме этой группы домашних животных, его вспышки фиксируют у птиц и свиней. Его вызывает анаэробная бактерия Clostridium. Она устойчива ко многим факторам внешней среды и дезинфекторам. Так, бактерия может выживать при минусовой температуре, отсутствии кислорода, нагреве. Особенно хороша для её размножения влажная бескислородная среда при температуре около тридцати пяти градусов тепла. Споры клостридий покрыты оболочкой, которая и защищает их от воздействия внешних факторов.
Клостридиоз является инфекционным заболеванием крупного рогатого скота. Кроме этой группы домашних животных, его вспышки фиксируют у птиц и свиней. Его вызывает анаэробная бактерия Clostridium. Она устойчива ко многим факторам внешней среды и дезинфекторам. Так, бактерия может выживать при минусовой температуре, отсутствии кислорода, нагреве. Особенно хороша для её размножения влажная бескислородная среда при температуре около тридцати пяти градусов тепла. Споры клостридий покрыты оболочкой, которая и защищает их от воздействия внешних факторов.
Попадая в организм животного, эта оболочка разрушается и бактерии начинают выделять очень сильные токсины. Они поражают желудок и кишечник, вызывая некротический энтерит, а также печень, почки, нервную, мышечную системы. Клостридии вызывают животные заболевания, а именно энтеротоксемию, столбняк, отёк в злокачественной форме, эмкар, ботулизм. В организм скота они могут попасть орально и через раны на теле. Основным механизмом передачи считается орально-фекальный. После инфицирования через короткий промежуток времени возможен летальный исход.
Важно! Клостридиозу особо подвержены молодые телята до четырёхмесячного возраста. У них болезнь протекает очень быстро и велик процент падежа. Фермерам следует обратить особое внимание на эту категорию животных.
Причины появления
Клостридиоз может поразить организм крупного рогатого скота по следующим причинам:
- кормление животных некачественным кормом и таким, который содержит антибиотики. Последнее сильно разрушает иммунную систему коровы и они более подвержены различным заболеваниям;
- заражённая бактерией почва, вода;
- грязный хлев, антисанитарные условия содержания поголовья.

Клинические признаки
Симптомы болезни разнятся в зависимости от того, как он проник в организм и какую болезнь вызвала бактерия. Если бактерия попадает орально-фекальным путём, то сначала наблюдается общее недомогание скота, а после – токсины начинают разрушать желудочно-кишечный тракт, нервную систему и другие органы. При злокачественном отёке может поражаться подкожная клетчатка, образовываются холодные припухлости с пенистым экссудатом, ощущается хруст при прощупывании, повышается сердечный ритм. Симптомы похожи при эмкаре.
Если животное заразилось ботулизмом, то может наблюдаться нарушение акта глотания, вода выделяется через ноздри, имеет место диарея, слюноотделение.
При энтеротоксемии повышается температура тела, нарушается координация движений, животное плохо передвигается, наблюдаются спазмы мышц, ухудшается дыхательный рефлекс, стул становится жидким, иногда с примесями крови.
 При столбняке могут иметь место паралич, судороги, обильное выделение пота, твёрдость мышц.
При столбняке могут иметь место паралич, судороги, обильное выделение пота, твёрдость мышц.
Знаете ли вы? Учёные доказали, что коровы чувствуют магнитное поле земли и поэтому во время еды и отдыха располагаются вдоль его линий.
Диагностика
Окончательно диагностировать клостридиоз можно только в лабораторных условиях. Для этого на исследование отправляют необходимый биоматериал. В разных случаях таким могут быть кровь, кусочки поражённых тканей, содержимое кишечника, раны.
Патологоанатомические изменения
В зависимости от типа вызванной клостридой болезни фиксируют различные изменения органов и тканей. Может иметь место вздутие, воспаление в подкожной клетчатке и мышцах, ощущается треск при нажатии, из тканей выделяется пенистый экссудат.
 При энтеротоксемии, в частности поражаются внутренние органы, а именно водянистая жидкость скапливается в брюшной полости, утолщаются стенки кишечника, увеличиваются лимфатические узлы, видны кровоизлияния в печени, почках, слизистых. При ботулизме и столбняке кровь густая и тёмная, а мышцы по цвету напоминают отварное мясо.
При энтеротоксемии, в частности поражаются внутренние органы, а именно водянистая жидкость скапливается в брюшной полости, утолщаются стенки кишечника, увеличиваются лимфатические узлы, видны кровоизлияния в печени, почках, слизистых. При ботулизме и столбняке кровь густая и тёмная, а мышцы по цвету напоминают отварное мясо.
Лечение
Если организм крупного рогатого скота поражён клостридой, то после диагностики необходима комплексная терапия, которая зависит от приобретённой болезни.
Важно! При любом, особенно массовом, недомогании скота, нужно незамедлительно вызвать ветеринара и после провести необходимые исследования. Раннее обращение значительно снижает развитие болезней в острых формах и падёж.
Общие рекомендации
В самом начале заболевшее животное необходимо изолировать от остального поголовья. Его нужно разместить в отдельном стойле и создать максимально комфортные условия содержания. Животное ничего не должно раздражать, должна быть приемлемая температура помещения, чистая, сухая подстилка и специфическое питание хорошего качества. В первое время, а именно до сорока восьми часов, еду давать не нужно, а после маленькими порциями вводить легкоусвояемый корм. Вода должна быть всегда в достаточном количестве.
Нужно промывать животному желудок при помощи клизм, давать вяжущие препараты, пробиотики.  Обязательна дезинфекция помещения при помощи средств, которые активны в отношении клостридий. Это, как правило, препараты, которые содержат хлор, бром, йод и называются галеновыми.
Обязательна дезинфекция помещения при помощи средств, которые активны в отношении клостридий. Это, как правило, препараты, которые содержат хлор, бром, йод и называются галеновыми.
Антибиотики
Без антибиотиков при лечении клостридиоза не обойтись. Наиболее эффективной считается пенициллиновая группа, метронидазол и его производные. В целом антимикробная терапия может включать такие препараты, как ампициллин, амоксициллин, хлортетрациклин, биомицин, бициллин 5, сульфадиметоксин.
Вакцина против клостридиоза
Также разработаны несколько вакцин, что формируют резистентность организма животного к заболеваниям, которые вызывают клостриды. Через двадцать один день после вакцинации у животных формируется иммунный ответ к заболеванию. Вакцины выпускаются разными производителями и, как правило, содержат антигены нескольких наиболее значимых возбудителей клостридиоза.
 Рекомендовано вакцинировать весь скот, кроме тёлок на последнем месяце беременности и других животных стразу после операции кастрации. Одноразовая доза вакцины вводится по инструкции согласно возрасту и массе животного, а через десять дней рекомендуется сделать ревакцинацию.
Рекомендовано вакцинировать весь скот, кроме тёлок на последнем месяце беременности и других животных стразу после операции кастрации. Одноразовая доза вакцины вводится по инструкции согласно возрасту и массе животного, а через десять дней рекомендуется сделать ревакцинацию.
Знаете ли вы? Грамм рубца коровьего желудка содержит около десяти миллиардов бактерий и миллион инфузорий.
Другие меры профилактики
Болезнь легче предупредить, чем лечить, поэтому во избежание клостридиоза следует проводить ряд мероприятий, а именно:
- соблюдать санитарные и гигиенические нормы содержания животных;
- регулярно чистить копыта;
- не выпасать скот вблизи скотомогильников и мест гибели животных;
- проводить регулярную дезинфекцию хлевов;
- не использовать некачественные корма;
- при проведении любых ветеринарных мероприятий соблюдать правила асептики.
 При содержании коров и другого крупного рогатого скота необходимо следить за их здоровьем. Нужно соблюдать элементарную гигиену в хлеву и на прилегающих к нему территориях. Это снизит вероятность инфекционных и иных заболеваний. Также важна правильная и своевременная диагностика животных, если у вас возникли сомнения относительно их здоровья.
При содержании коров и другого крупного рогатого скота необходимо следить за их здоровьем. Нужно соблюдать элементарную гигиену в хлеву и на прилегающих к нему территориях. Это снизит вероятность инфекционных и иных заболеваний. Также важна правильная и своевременная диагностика животных, если у вас возникли сомнения относительно их здоровья.
Ветеринария, Некротический энтерит кур. Современное представление
Кишечник взрослой птицы населяют более 400 видов различных бактерий.
Бесконтрольное размножение патогенной микрофлоры существенно сказывается на усвоении корма, поскольку в кишечнике возникают конкурентные отношения между микро и макроорганизмом за питательные компоненты.
Высокий микробный фон провоцирует иммунную систему организма, вызывая острый иммунный ответ. Такая ответная реакция «стоит» организму птицы больших энергетических затрат, что в свою очередь снижает аппетит и может привести к развитию метаболических нарушений.
Некоторые из бактерий, такие как энтерококки, лактобациллы и бактероиды, способны деконъюгировать желчные соли (соединения желчных кислот с жирами). Это сказывается на переваримости липидов, особенно когда в кормах имеется высокий уровень насыщенных жиров.
Именно поэтому поддержание здорового баланса микрофлоры (нормофлоры) кишечника является залогом контроля и фактором сдерживания активного размножения патогенных анаэробов (Clostridia, Escherichia coli).
Для поддержания такого баланса необходимо глубокое понимание принципов взаимодействия между элементами желудочно-кишечного тракта, компонентами кормов и микрофлорой.
Функции микрофлоры кишечника
Эндогенные бактерии, населяющие желудочно-кишечный тракт организма любого животного и птицы в следствие огромного размера их популяций (биомассы) имеют существенное воздействие на организм своего хозяина (макроорганизм).
Наиболее наглядно взаимоотношения микрофлоры и макроорганизма прослеживаются на моделях с использованием SPF-животных (Specific Pathogen Free) со «стерильным» желудочно-кишечным трактом.
В результате таких исследований был выявлен целый ряд преимуществ, которые имеют обычные животные, обладающие «нормофлорой», по сравнению с SPF-организмами:
• Нормофлора кишечника синтезирует и выделяет витамины сверх своих собственных нужд. Эти витамины легко утилизируются организмом хозяина. Так, например, некоторые бактерии синтезируют витамины К и В12, лактобактерии — витамины группы В. В тоже время SPF-животные испытывают сильнейший дефицит витамина К и нуждаются в дополнительном вводе его в рацион.
• Нормофлора предупреждает колонизацию патогенных микроорганизмов через конкуренцию за места ее прикрепления и незаменимые питательные элементы. Этот эффект считается наиболее «полезным» для макроорганизма. Он был продемонстрирован как на поверхности кожи, в кишечнике, так и на различных слизистых оболочках экспериментальных животных. Так, например, spf-животное можно заразить 10-ю бактериями салмонелл в то время как для обычного животного инфекционная доза того же патогена — порядка 106 клеток.
• Нормофлора находится в антагонистических отношениях с другими бактериями, продуцируя субстанции, подавляющие или убивающие экзогенную микрофлору. Кишечная микрофлора продуцирует целый ряд разнообразных веществ – от неспецифических жирных кислот и перекисей до высокоспецифических «бактериоцинов», летально воздействующих на жизнедеятельность инородных бактерий.
• Нормофлора стимулирует развитие определенных тканей, например, слепой кишки и некоторых лимфатических образований (Пейеровы бляшки) желудочно-кишечного тракта. Так, слепая кишка spf-животных, в сравнении с нормальными, увеличена в размерах, стенки ее утоньшены, заполнена жидким содержимым. Лимфатические образования кишечника – также недоразвиты по причине отсутствия бактериальной стимуляции.
• Нормофлора стимулирует продукцию перекрестных антител. Низкие уровни антител, вырабатываемые в организме на антигены нормофлоры кишечника, имеют свойство перекрестной защиты от различных экзогенных микроорганизмов, тем самым предупреждая инфекции и инвазии. Антитела, вырабатываемые против антигенов эндогенной микрофлоры иногда называются «естественными» и отсутствуют в организме spf-животных.
К сожалению, микробный баланс в организме, особенно в желудочно-кишечном тракте, довольно хрупок и легко нарушается под воздействием ряда факторов.
Факторы, нарушающие нормальное взаимодействие кишечной стенки и микрофлоры, можно условно разделить на 2 категории:
• Биологические факторы, воздействующие непосредственно на кишечную стенку: кокцидии, некоторые вирусы (Parvo, REO и др), бактерии (Cl. Perfringens, E.coli, Salmonella).
Для контроля этих факторов принципиальное значение имеет соблюдение правил неспецифической (биозащита и санитарно-гигиенические обработки), а также специфической профилактики (вакцинация, медикация).
• Кормовые факторы: сырьевой и гранулометрический состав, питательность и сбалансированность кормов.
Так, содержание некрахмалистых полисахаридов (НПС) в зерновом сырье – важнейший фактор в развитии расстройств пищеварения. В течение последних лет во всем мире проводится огромная исследовательская работа по изучению воздействия водорастворимых НПС на пищеварение.β-глюканы, пектин и карбоксиме-тилцеллюлоза – яркие примеры НПС, присутствующие в больших количествах в пшенице, ячмене, ржи и т.п.. Высокое содержание такого сырья в кормах способствует повышению вязкости химуса, замедлению его продвижения по кишечной трубке, ферментации НПС и бурному размножению анаэробной микрофлоры, потерей баланса нормофлоры (дисбактериоз), нарушением пищеварения и всасывания в кишечнике.
— Структура (гранулометрический состав) кормов – также играет существенную роль в развитии дисбактериозов. Так, при мелком помоле зернового сырья функция мышечного отдела желудка постепенно утрачивается и он превращается в «транзитный» орган. В такой ситуации нарушается перистальтика и антиперистальтика кишечной стенки, что приводит к ускоренному прохождению непереваренных кормовых масс в кишечнике. Непереваренный корм не может быть усвоен кишечными ворсинками и подвергается ферментации в дистальном отделе тонкого кишечника под воздействием доминирующей там анаэробной микрофлоры. Далее ситуация складывается по уже описанному сценарию.
Этиология и патогенез
Возбудителем НЭ кур является преимущественно Clostridium Perfringens типа С, который вызывает аналогичную патологию у индеек. Реже возбудителем выступает C. perfringens типов А, В или Е.
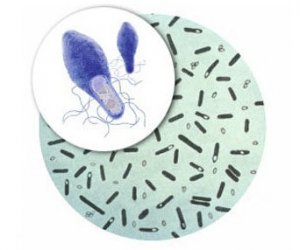
C. perfringens (ранее C. welchii) – грам-положительная, анаэробная, споро-образующая палочка рода Clostridium (Фото 1). Этот убиквитарный микроорганизм можно обнаружить в составе разлагающегося растительного субстрата, донных отложений водоемов, кишечном тракте человека и других позвоночных, насекомых и в любом типе почв. Известны как минимум 8 антигенных типов токсинов C. perfringens — А-G (включая С-. и С-.).
Род Clostridium включает как свободно-живущие бактерии, так и важнейшие патогены – возбудители различных клостридиозов. Некоторые виды имеют важное промышленное значение (Таблица 1).
Табл. 1. Наиболее важные представители Рода Clostridium и их значение.
НЭ регистрируется по всему миру в районах ведения интенсивного птицеводства.
К возбудителю восприимчивы цыплята в возрасте 2-24 недель. Чаще всего заболевание развивается у 2-5 недельных бройлеров напольного выращивания, а также индеек в возрасте 7-12 недель.
Возможны вспышки на 12-24-недельных несушках напольного содержания, а также в сочетании с кокцидиозом в возрасте 12-16 недель у ремонтной молодки клеточного выращивания.
C.perfringens является неотъемлемой частью облигатной нормофлоры кишечника – преимущественно дистального участка тонкого кишечника (подвздошной кишки и слепых отростков). Размер популяции возбудителя в значительной степени зависит от сырьевого состава и структуры комбикорма.
Предрасполагающие факторы к развитию или обострению заболевания:
• Высокое содержание в кормах пшеницы, ячменя или ржи с повышенным содержанием некрахмалистых поли- и олигосахаридов, а также некачественной рыбной муки.
• Смена сырьевого и гранулометрического состава комбикорма — чрезмерное мелкий помол зернового сырья, ускоряющий прохождение непереваренного корма и его дальнейшую ферментацию микрофлорой кишечника.
• Повреждение слизистой кишечной стенки паразитами (субклинический кокцидиоз), при РЕО-вирусной инфекции (синдром мальадсорбции) или воздействием микотоксинов.
• Низкий ветеринарно-санитарный статус птицеводческих помещений – недостаточно качественная подготовка корпусов во время санитарного разрыва между партиями птицы (споры клостридий высокоустойчивы в окружающей среде, особенно при некачественной механической чистке помещения и его дезинфекции).
• Стрессовые факторы: неоптимальный микроклимат, высокая плотность посадки, выход на пик продуктивности для племенной птицы и т.п.
• Иммуносупрессорные инфекции: БМ, ИББ, ВАЦ и др.
Клинические проявления и патологоанатомическая картина
Чаще всего признаком вспышки НЭ в стаде является внезапный всплеск падежа. Однако на ранних стадиях заболевания можно наблюдать птицу в состоянии депрессии, со взъерошенным оперением, диареей. Отмечается высокая неоднородность поголовья по живой массе.
Субклинически НЭ протекает у бройлеров с признаками задержки роста и развития на фоне плохой переваримости кормов – дисбактериоз.
На подстилке четко различим липкий, светлоокрашенный помет с остатками непереваренного корма в следствие снижения переваримости жира из-за разрушения солей желчных кислот (Фото 1)
Зачастую, при распространении проблемы наблюдается ухудшение качества подстилки вследствие ее намокания.
Патологические изменения локализованы преимущественно в тонком отделе кишечника (12-перстная кишка) в виде вздутия, рыхлости, с содержанием зловонной жидкости.
Характерные поражения слизистой оболочки кишечной стенки обусловлены воздействием экзотоксинов: α (альфа) – у Сl. Perfringens тип А и С, и β (бета) – Сl. Perfringens тип С.
Слизистая оболочка обычно покрыта псевдомембранозным налетом желто-коричневого цвета, часто ассоциируемым с фактурой «турецкого полотенца» (Фото 2). Это поражение может носить как генерализованный (вдоль всего кишечника), так и локальный (отдельный участок) характер.
Иногда степень непереваримости кормов настолько высока, что на вскрытии содержимое мышечного желудка по своей структуре практически не отличается от содержимого прямой кишки (Фото 3).
Болезнь персистирует в стаде в течение 5-10 дней. Отход птицы за этот период варьирует в пределах 2-50%.
Диагностика
Постановка диагноза осуществляется на основании характерных клинических признаков, патолого-анатомических изменений и выделения возбудителя из патматериала с последующей микроскопией.
Предварительный диагноз базируется на характерных патизменениях и микроскопии мазка из соскоба слизистой кишечника.
При окраске по грамму и микроскопии легко обнаруживаются крупные грам-положительные палочки (Фото 4).
Гистологическое исследование демонстрирует очаги коагулятивного некроза, погруженные в стенку кишечника на 1/3-1/2 его толщины, а так же наличие большого количества коротких толстых палочек C.perfringens в фибринозно-некротических очагах.
Лабораторное подтверждение диагноза – путем выделения возбудителя из содержимого кишечника, соскобов слизистой оболочки или из цекальных лимфоидных бляшек (анаэробная инкубация на чашках с кровяным агаром 12 часов при 370С) (Фото 5).
Выделить возбудителя можно из содержимого кишечника, помета, корма, пыли и подстилки, а также в большом количестве – из почвы вокруг птичников.
Классически колонии окружены двойной зоной гемолиза: внутренней — полного гемолиза и внешней — обесцвечивания и частичного гемолиза (Фото 3). Однако этот критерий не может быть определяющим, поскольку не все штаммы выделяют оба токсина, отвечающие за гемолиз.
Колония состоит из грам-положительных палочек без спор. Подтверждается диагноз после культивации возбудителя на дифференциальной среде.
Большинство штаммов C.perfringens ферментируют глюкозу, мальтозу, лактозу, сахарозу; не ферментирует маннитол; по-разному ферментируют салицин.
Дифференциальная диагностика
Поражения же при НЭ локализуются преимущественно в 12-перстной и тощей кишке с очень редким вовлечением слепых отростков и печени.
Зачастую НЭ и кокцидиоз протекают параллельно, поэтому вероятность выделения обоих возбудителей из патматериала очень высока.
Профилактика и лечение
Прежде всего для эффективного мониторинга состояния желудочно-кишечного тракта необходим постоянный контроль качества помета. Для этого рекомендуется установить в птичниках напольного выращивая бройлеров перевернутые пластиковые ящики с сетчатым дном и выстеленной под ними бумагой (Фото 6) . Если диаметр влажной зоны вокруг помета на бумаге превышает 2см (Фото 7), это свидетельствует о нарушении соотношения корм / вода и является индикатором прогрессирующего дисбактериоза.
В связи с убиквитарностью C.perfringens необходимо исключить первоначальные факторы, воздействующие на нормофлору кишечника и провоцирующие активный рост популяции возбудителя НЭ.
Возможны несколько путей:
• При выборе сырья использовать компоненты с низкой вязкостью и небольшой фракцией НПС.
• Уменьшение % ввода в комбикорм рыбной муки.
• Улучшение структуры комбикормов – более грубый помол зернового сырья.
• Дача части зерна в цельном виде, начиная со второй недели откорма.
• Использование солей желчных кислот или повышение уровня ненасыщенных жирных кислот в рационе.
• Использование ферментов, позволяющих расщеплять и лучше усваивать НПС.
• Использование поливитаминных препаратов для предупреждения авитаминозов.
• Добавление в питьевую воду и корма органических кислот (фумаровая, бутыровая, уксусная, пропионовая, Selko pH) с целью снижения рН и достижения бактериостатического эффекта.
• Использование кокцидиостатиков, преимущественно ионофорного ряда — предупреждает повреждение кишечной стенки, следствием которого часто выступает НЭ.
• Использование пребиотиков (фруктоолигосахариды – инулин, лактулоза и др.)
• Использование кормовых антибиотиков (бацитрацин, линкомицин, авопарцин, нитровин), а также выпойной (окситетрациклин, пенициллин, эритромицин, амоксициллин, метронидазол, тилозин).
Заключение
Дисбактериозы и клостридиозы широко распространены в птицеводстве и, безусловно, наносят существенный урон экономике любого предприятия — как за счет снижения привесов, так и повышения расхода корма (при неэффективной утилизации питательных веществ), а так же повышенного падежа птицы от энтеритов и кокцидиоза на финальной стадии откорма.
Однако, борьба с данной патологии должна базироваться прежде всего на профилактике путем контроля качества используемого в кормопроизводстве сырья, физической структуры кормов (качество дробления зерновых), на снижении стрессовых факторов, и только в последнюю очередь – на грамотном применении кокцидиостатиков, а также кормовых и лечебных антибиотиков.
Библиография
• Diseases of Poultry. 11th Edition. Y.M Saif, 2003.
• Langhout, D.J.. The role of the intestinal flora as affected by non-starch polysaccharides in broiler chicks. Wageningen University.1998
• North, M.O. and D.D. Bell. Commercial Chicken production Manual, 4th Edition
• Kenneth Todar. The Pathogenic Clostridia.University of Wisconsin-Madison Department of Bacteriology. 2005
• Poultry Diseases, 5th Edition, Jonathan Gregory, Frank Jordan et al. 2001.
Авторы: Эдуард С. Маилян. Кандидат ветеринарных наук. Ведущий специалист по птицеводству, ООО «ТехКoрм»; C. perfringens (welchii) ; Eimeria brunetti. ; C.colinum; Eimeria brunetti ; Lactobacillus acidophilus, Streptococcus
Причины, виды, симптомы, лечение, профилактика
Клостридии (Clostridium) – спорообразующие микроорганизмы, развивающиеся при полном отсутствии кислорода, питающиеся мертвой органикой и превращающие органические вещества в неорганические.
Что такое клостридии?
Клостридии широко распространены в почве и воде. Некоторые виды являются болезнетворными и вызывают кишечные инфекции и множество других заболеваний таких как столбняк, газовая гангрена, несколько видов колита, ботулизм и др. Если условия для развития клостридии неблагоприятны, то она образует споры, которые могут сохраняться и при наличии кислорода, в воздухе, пыли, на поверхностях предметов, на руках.
При попадании в организм клостридии способны разрушать ткани, что при отсутствии лечения может привести к тяжелым осложнениям и даже к смерти.
Учеными установлено, что яды клостридии оказывают влияние на психику человека: например, предполагается, что имеется связь между клостридиями и аутизмом. Это подтверждает опасность клостридий. Положительным моментом является то, что исцеление от клостридий приводит к исчезновению психических симптомов.
За пищевые отравления (диарею) ответственна Clostridium perfringens (клостридия перфрингенс).
Clostridium difficile начинает активно развиваться в кишечнике при нарушении микрофлоры, особенно часто на фоне приема антибиотиков.
Что делать, если обнаружены клостридии в кале?
Clostridium difficile может в норме содержаться в кишечнике. По статистике она содержится в микрофлоре у 3 % здоровых людей и у 20-40 % пациентов госпитальных клиник. В анализе кала в норме она не должна превышать 105 кое/г. Однако если нарушается «здоровье» микрофлоры кишечника, что особенно часто происходит при приеме антибиотиков, то клостридии начинают усиленно размножаться, выделяя сильнодействующий яд (токсин), что приводит как минимум к диарее, но может вызвать и более серьезные заболевания.
Если клостридия обнаружена в кале в допустимых количествах, и отсутствуют другие настораживающие симптомы (диарея, тошнота, боли в животе),то не следует прибегать к медикаментозной терапии. В этом случае необходимо уделять особое внимание формированию здоровой микрофлоры кишечника.
Клостридия Clostridium perfringens
Эти клостридии вырабатывают токсин (яд). Токсин очень стойкий и сохраняется даже при температуре 100 градусов Цельсия. Clostridium perfringens вызывают тяжелое отравление (гастроэнтерит).
Как передаются Clostridium perfringens?
Инфекцию чаще всего обнаруживают в мясе и домашней птице. Заражение людей чаще всего происходит из-за несоблюдения технологии приготовления и хранения больших количеств пищи.
Штаммы клостридий, загрязняющие мясо, могут сохраняться при первичной обработке. Во время повторной обработки образуются их споры. При вспышке острой инфекции могут заболеть до 70 % лиц, контактировавших с инфекцией.
Симптомы
Симптомы пищевого отравления появляются через 12-24 часа после того, как был съеден зараженный продукт.
Различают клостридии перфрингенс типа А и С.
При заражении Clostridium perfringens типа А развивается умеренно выраженный гастроэнтерит со следующими симптомами:
- боли в животе,
- водянистая диарея.
При заражении Clostridium perfringens типа С может развиться некротический энтерит с тяжелыми симптомами:
- острые боли в животе,
- кровавая диарея,
- тошнота,
- шок,
- перитонит.

Диагностика
Диагноз устанавливается по результатам анализа на высевание культуры Clostridium perfringens в кале.
Лечение
При заболевании типа А лечение проводится антибиотиками.
В случае развития некротического гастроэнтерита необходимо срочное хирургическое вмешательство.
Профилактика
Профилактикой заболевания является соблюдение санитарных требований при хранении мяса, особенно на предприятиях общественного питания.
Можно ли вылечить Clostridium perfringens?
В большинстве случаев заболевание вылечивается полностью. Важно как можно раньше начать лечение, чтобы не допустить развития некроза.
Клостридия Clostridium difficile
Желудочно-кишечный дискомфорт во время приема антибиотиков встречается часто, но при прекращении приема препарата все симптомы исчезают. Если же эти симптомы вызваны клостридиями, то они не только не прекращаются при отмене антибиотиков, но могут продолжаться еще несколько недель после отмены или даже появиться только через несколько недель после окончания приема препарата.
Возбудитель Clostridium difficile передается при прямом контакте с инфицированным человеком, например, через руки или через предметы общего пользования, такие как дверные ручки, перила или туалеты. Особенно часто страдают клостридиальной инфекцией пациенты больниц.
Главным симптомом является диарея. Как правило, она появляется через 4-9 дней после начала приема антибиотиков.
Исследования показали, что у пациентов, которые находятся в медицинском госпитале 1-2 недели, процент инфицированности составляет 13%. Если же пациенты находятся в клинике больше 4 недель, то Clostridium difficile обнаруживается у 50% обследованных людей.
Последнее время эта проблема стала особенно острой, так как заболеваемость этой патологией возросла в несколько раз с увеличением и смертности от нее. В 2009 году Европейское общество клинических микробиологов и инфекционистов опубликовало свои рекомендации по лечению, по критериям оценки тяжести и оценки эффективности лечения этой инфекции.
Чем опасна Clostridium difficile?
Clostridium difficile относится к облигатным анаэробам, является грамположительной спорообразующей бациллой с фекально-оральным путем передачи.
Эта бацилла продуцирует два цитотоксина: А и В.
Токсин А ослабляет связь между клетками эпителия толстой кишки, что позволяет токсину В проникать между ними и запускать целый ряд воспалительных реакций, включающих продукцию деструктивных агентов и приводящих к тяжелому повреждению тканей.
Лишь в 1978 году было установлено, что именно Clostridium difficile приводит к развитию псевдомембранозного колита, возникающего при приеме антибиотиков.
При приеме антибиотиков нарушается микрофлора кишечника. Споры Clostridium difficile устойчивы к воздействию кислоты. Попадая в желудок, они проникают в кишечник, где нарушенная микрофлора не подавляет их. Они переходят в вегетативную форму и начинают продуцировать токсины.
Микробиологами был описан новый штамм Clostridium difficile, который вырабатывает А и В токсины в 16-23 раза больше по сравнению с прежними штаммами. При заражении этим штаммом развиваются более тяжелые виды заболевания.
Симптомы диареи и колита, вызванных Clostridium difficile
Симптомы обычно проявляются на 5-10 день от начала лечения антибиотиками, хотя встречаются случаи возникновения признаков на 2 день терапии. Но возможно появление симптомов и через 10 недель после прекращения приема антибиотиков.
Типичными симптомами диареи и колита, развивающихся от воздействия Clostridium difficile являются:
- профузная зловонная диарея
- слизь в кале
- схваткообразные боли в животе
- тенезмы (ложные схватки)
- скрытая кровь в анализе кала (иногда кровь в кале)
- лейкоциты в кале.
Живот мягкий, но болезненный при пальпации в области ободочной кишки.
Для заболевания характерны такие общие симптомы как:
- тошнота
- рвота
- дегидратация
- умеренная лихорадка.
Колит, ограниченный правой половиной толстой кишки, проявляется локальной болью в животе, лейкоцитозом, лихорадкой при умеренной или небольшой диарее.
Наиболее тяжелым вариантом развития заболевания является токсический мегаколон. Это состояние может возникнуть на фоне урежениея стула, что иногда расценивается как положительная динамика лечения.
Однако такие симптомы как задержка газов, раздувание ободочной кишки, высокий лейкоцитоз, уменьшение объема циркулирующей крови, скопление жидкости в брюшной полости являются типичными проявлениями этого состояния.
Лечение токсического мегаколона должно быть хирургическим.
Тяжесть течения заболевания зависит от штамма Clostridium difficile и состояния иммунитета пациента.
Довольно часто встречается бессимптомное носительство Clostridium difficile.
Легкая форма диареи, вызванной Clostridium difficile
Легкая форма диареи характеризуется следующими признаками:
- умеренные боли в животе
- понос 4 раза в сутки
- отсутствие общих симптомов (тошнота, рвота, лихорадка).
Такой вид диареи, вызванной Clostridium difficile, не требует медикаментозного лечения. Необходимо отменить антибиотики, назначить препараты, восстанавливающие микрофлору кишечника.
Колит, вызванный Clostridium difficile
Более тяжелой формой является колит, вызванный Clostridium difficile. Колит может протекать в форме колита без псевдомембран и в форме псевдомембранозного колита.
Колит без псевдомембран протекает со всеми системными признаками этого заболевания: с лихорадкой, дегидратацией, болями в животе, рвотой, жидким водянистым стулом до 20 раз в день, но без отклонений в анализах.
Псевдомембранозный энтероколит вызывает те же симптомы, но при колоноскопии выявляются псевдомембраны и может быть подтвержден отклонениями в анализах.
Степени тяжести заболеваний, вызванных Clostridium difficile
В рекомендациях по диагностике и лечению Clostridium difficile-ассоциированной диареи или колита приведены конкретные критерии для оценки тяжести этого состояния.
Для простоты восприятия они сведены в таблицу.
| Степень тяжести | Симптомы |
|---|---|
| Легкое течение | диарея до 5-7 раз в сутки умеренная боль в животе отсутствие лихорадки отсутствие лейкоцитоза |
| Средне-тяжелое течение | диарея 10-15 раз в сутки боль в животе температура умеренное обезвоживание умеренный лейкоцитоз |
| Тяжелое течение | гектическая лихорадка > 38,5 С тяжелая интоксикация нарушения кровообращения признаки перитонита признаки кишечной непроходимости лейкоцитоз со сдвигом влево наличие псевдомембран признаки токсического мегаколона признаки асцита сильное обезвоживание электролитное нарушение |
Пациенты со среднетяжелой и тяжелой формами ААД (антибиотикоассоциированная диарея) подлежат обязательной госпитализации.
Лечение Clostridium difficile
Современные рекомендации по лечению четко определяют тактику ведения больных с ААД (диареей) и ААК (колитом).
У значительного числа пациентов диарея, вызванная Clostridium difficile, протекает в легкой форме. Она проходит сама после отмены антибиотиков и не требует специального лечения. Иногда, в случае обезвоживания организма, необходимо восполнение жидкости и солей (электролитов).
Для восполнения жидкости и солей рекомендуется обильное питье не газированной минеральной воды, несладких травяных настоев или специальных аптечных растворов.
В случаях, когда заболевание протекает с явными признаками колита, возникает необходимость в проведении антибактериальной терапии, активной в отношении Clostridium difficile.
Определены критерии оценки эффективности антибактериальной терапии:
- уменьшение частоты стула,
- улучшение консистенции стула,
- улучшение общего состояния пациента,
- положительная динамика клинических и лабораторных показателей,
- отсутствие новых признаков прогрессирования болезни.
Если эти критерии не выполняются, то необходима корректировка препарата.
Хирургическое лечение колита, вызванного Clostridium difficile
Показаниями к хирургическому лечению псевдомембранозного колита следующие:
- перфорация ободочной кишки,
- прогрессирование системного воспаления с развитием токсического мегаколона и кишечной непроходимости при адекватной антибактериальной терапии.
Профилактика
- Поскольку главной причиной развития Clostridium difficile являются антибиотики, то главной рекомендацией является рациональное применение антибактериальных препаратов.
- Соблюдение санитарно-гигиенических норм.
- Изоляция пациента с диареей.
- Быстрая постановка диагноза.
- Мытье рук с мылом для удаления спор с поверхности кожи.
- Обработка рук спиртом бесполезна, так как не обеспечивает удаление спор.
Можно ли вылечить Clostridium difficile?
Прогноз зависит от степени тяжести диареи или колита, вызванных клостридией Clostridium difficile, характера течения, наличия осложнений.
При легком и среднетяжелом течении заболевание вылечивается полностью. Лихорадка проходит через 1-2 суток, а понос прекращается через 5-7 дней.
В последнее время появился новый эффективный метод лечения даже тяжелых случаев заболевания с помощью пересадки кала.
Неблагоприятными факторами являются непроходимость кишечника, псевдомембранозный колит, почечная недостаточность.
