Анемия при беременности
Под анемией понимают снижение уровня гемоглобина в крови.
Во время беременности в организме женщины увеличивается количество жидкости, а значит, и объем циркулирующей крови. За счет этого кровь «разжижается» и доля гемоглобина в ее общем объеме падает. Это считается нормальным явлением, в связи с чем нижняя граница количества гемоглобина при беременности установлена на уровне 110 г/л (при норме для небеременной женщины в 120–140 г/л). Но дальнейшее падение уровня гемоглобина является опасным для здоровья и даже жизни будущей матери.
В зависимости от значений этого показателя анемия при беременности может быть:
- легкой степени тяжести — 110–90 г/л;
- умеренно выраженной — 89–70 г/л;
- тяжелой — 69–40 г/л.
Наиболее частыми осложнениями при анемии во время беременности считаются:
- угроза прерывания беременности;
- гестоз;
- пониженное артериальное давление;
- преждевременная отслойка плаценты;
- задержка развития плода;
- преждевременные роды;
- анемия в первый год жизни ребенка.

Так что анемия при беременности — отнюдь не безобидное состояние. Оно имеет серьезные последствия и для матери, и для плода.
Во время беременности железо расходуется не только на кроветворение матери, но и на нужды плода. Особенно активно этот расход возрастает на 16–20-й неделях, когда запускается процесс кроветворения у плода. К концу беременности запасы железа истощаются у любой женщины и для их полного восстановления необходимо 2–3 года.
Другими причинами анемии при беременности являются:
- дефицит железа в пище главным образом из-за недостаточного количества мяса в рационе;
- дефицит витаминов группы B и C, необходимых для нормального усвоения железа;
- болезни, при которых возникает недостаток белков, участвующих в обмене железа, включая тяжелый гестоз;
- ранний гестоз (токсикоз), мешающий полноценно питаться;
- частые роды с небольшим интервалом.
Если же говорить о группах риска развитии анемии во время беременности, то к ним можно причислить женщин: с многоплодной беременностью и многорожавших; имевших до наступления беременности менструации длительностью более 5 дней; у которых были симптомы анемии во время предыдущей беременности; с гестозом; с хроническими заболеваниями желудочно-кишечного тракта, печени, хроническими инфекциями; вегетарианок. Все, попавшие в группу риска, должны особенно тщательно следить за своим состоянием и по возможности позаботиться о профилактике анемии во время беременности.
Все, попавшие в группу риска, должны особенно тщательно следить за своим состоянием и по возможности позаботиться о профилактике анемии во время беременности.
Учитывая, что во время беременности потребность организма женщины в микроэлементе возрастает на 15–33%, на передний план обычно выходят симптомы, указывающие на гипоксию: слабость, быстрая утомляемость; нарушение сна: днем — сонливость, ночью — бессонница; головные боли; головокружения, шум в ушах; одышка; сердцебиение; обмороки.
Переносимость симптомов анемии индивидуальна: кто-то падает в обморок при относительно высоких значениях гемоглобина, кто-то отказывается от госпитализации с гемоглобином на уровне около 70 г/л, искренне не понимая всей тяжести анемии и ее опасности при беременности. Именно поэтому клинический анализ крови во время беременности проводится обязательно и несколько раз. Имеет значение и падение значений железа в сыворотке крови и сывороточного ферритина. Снижение количества последнего до 12 мкг/л говорит о дефиците железа, даже если гемоглобин еще в норме.
Лечение анемии в период ожидания малыша включат в себя диетотерапию. Одна из основ как профилактики, так и лечения анемии при беременности — правильное питание. Питание для профилактики анемии при беременности должно содержать в достаточном количестве вещества, необходимые для нормального кроветворения, — это мясо, рыба. В этих продуктах железо изначально двухвалентное, поэтому легко всасывается. Но одной диеты может быть недостаточно даже для профилактики.
Для лечения анемии назначаются препараты железа. Обычно ограничиваются средствами для перорального приема (т.е. внутрь) — препараты железа в инъекциях рекомендуют только в тяжелых случаях и только в условиях стационара.
Как российские, так и зарубежные эксперты отмечают, что профилактика анемии у беременных эффективней, чем ее лечение, и чем выше уровень гемоглобина, тем проще привести его к норме. Впрочем, о том же говорит и здравый смысл. Поэтому, планируя беременность и тем более уже ожидая ребенка, лучше заняться профилактикой анемии не дожидаясь, пока недостаток железа станет заметен.
Врач-гематолог (заведующий),
консультационным отделением Рачкова Т.А.
Городская клиническая больница №31 — Пациентам в помощь. Гематологические заболевания. Часть III. Миелодиспластические синдромы
Страница 1 из 7
Когда ставят диагноз «миелодиспластический синдром», то всегда помнят о том, что существует множество других болезней, способных ухудшить кровь и изменить костный мозг: это хронические инфекции (туберкулез, токсоплазмоз…), аутоиммунные заболевания (системная красная волчанка, ревматоидный артрит…), разнообразные опухоли. Вот почему пациента нужно всесторонне обследовать, а МДС является, скорее, диагнозом исключения, то есть его ставят тогда, когда все другие причины изменения крови исключены. МДС – болезнь пожилых, средний возраст пациентов составляет 70 лет.
Всем клеткам крови человека дает начало стволовая клетка. По мере взросления ее потомков выделяются 3 основных ветви, или ростка: красный росток (эритроидный), белый росток (лейкоцитарный) и тромбоцитный (тромбоцитарный).
Термин «миелодиспластический» состоит из трех частей: «миело-» – греческая приставка, обозначающая связь с костным мозгом, «дис-» – приставка, обозначающая «нарушение», и «-плазия» – конечная часть сложных слов, обозначающая «развитие». Термином «синдром» называют совокупность связанных между собой признаков. Таким образом, из самого названия следует, что в организме произошла какая-то поломка, которая привела к тому, что нарушено созревание (развитие) клеток костного мозга. Причины ученым еще предстоит выяснить, но из-за нарушения на тех или иных этапах взросления клеток кровь начинает меняться. Вначале страдает один росток крови, чаще всего эритроидный. У человека постепенно в крови снижается гемоглобин, больной начинает чувствовать слабость, нарастающее недомогание, привычная работа оказывается не по силам, а отдых не приносит облегчения.
Диагноз «миелодиспластический синдром» (МДС) поставить довольно сложно. Здесь лечащий врач, как никогда, нуждается в помощи врачей-лаборантов: цитолога и цитогенетика с хорошей лабораторией. Врач-цитолог, глядя в микроскоп, тщательно анализирует костный мозг, капелька которого нанесена на специальное маленькое стекло и делает заключение о том, есть ли внешние признаки нарушения работы костного мозга. Этот метод относится к одному из самых технически простых, однако специалистов-цитологов, способных выявить и оценить «неправильные» клетки, в городе очень мало. Врач-цитогенетик с помощью сложной аппаратуры анализирует делящиеся клетки костного мозга и ищет типичные изменения в генах, которые очень важны для диагноза, прогноза, выбора лечения и контроля за ним.
Когда ставят диагноз МДС, то всегда помнят о том, что существует множество других болезней, способных ухудшить кровь и изменить костный мозг: это хронические инфекции (туберкулез, токсоплазмоз…), аутоиммунные заболевания (системная красная волчанка, ревматоидный артрит…), разнообразные опухоли. Вот почему пациента нужно всесторонне обследовать, а МДС является, скорее, диагнозом исключения, то есть его ставят тогда, когда все другие причины изменения крови исключены. МДС – болезнь пожилых, средний возраст пациентов составляет 70 лет.
Чем же опасен миелодиспластический синдром, кроме низкого гемоглобина? Одним из самых неприятных и опасных следствий является постепенное накапливание поломок в кроветворении, поскольку первая поломка в зрелых клетках «тянет» за собой другие поломки и уже в более молодых клетках. Со временем заболевают все более и более активные клетки, и возникает болезнь «острый лейкоз». Наблюдая за пациентами, а также анализируя картину их болезни, врачи научились примерно предсказывать его появление. Риск перехода МДС в острый лейкоз записывают специальными прогностическими индексами (IPSS, WPSS и другими), которые обычно указывают в диагнозе.
Риск перехода МДС в острый лейкоз записывают специальными прогностическими индексами (IPSS, WPSS и другими), которые обычно указывают в диагнозе.
Миелодисплатический синдром существует в нескольких видах:
Мировая статистика показывает, что в зависимости от разных факторов пациенты с МДС живут от одного-двух месяцев до нескольких лет.
Продукты, которые помогут повысить уровень гемоглобина
Дефицит гемоглобина в крови в большинстве случаев легко восполнить, включив в свой рацион полезные продукты.
Гемоглобин – один из важнейших белков в организме человека. Его недостаток чреват постоянной слабостью, сухостью кожи, выпадением волос и даже частыми обмороками. Чтобы не доводить до крайних случаев, каждому человеку следует регулярно проверять уровень гемоглобина.
Но даже если анализ показал явную нехватку, не стоит впадать в панику и бежать в аптеку. Помогут и обычные продукты, которые недорого стоят, и многими искренне любимы.
Помогут и обычные продукты, которые недорого стоят, и многими искренне любимы.
Прежде всего, советуем увеличить долю фруктов и овощей в ежедневном рационе. Позаботьтесь, чтобы вы регулярно ели
-
яблоки,
-
гранат,
-
капусту всех видов,
-
-
финики,
-
свеклу,
-
тыкву,
-
арбуз.
Это все — источники полезного для здоровья железа.
Кроме того в меню следует обязательно включить рыбу, мясо, сыр, молочные продукты, говяжью печень, фасоль, гречку, сухофрукты. Эти продукты также помогут наладить здоровье и поддерживать уровень гемоглобина на должном уровне.
Однако, стоит также помнить, что эффект будет гораздо выше, если одновременно есть больше продуктов, богатых витамином С (он помогает организму усваивать железо). В связи с этим нужно есть больше лимонов, апельсинов, мандаринов и других цитрусовых.
Кстати, зимой лучшим помощником в поднятии уровня гемоглобина в крови станет обычная квашенная капуста. Как установили ученые, витамина С в ней больше, чем в аскорбинке.
А вот кофе, крепкий чай и какао на время «вкусного лечения» лучше отменить. Ведь они, в отличие от цитрусовых, серьезно мешают усвоению железа.
Анемия у пожилых людей, причины, лечение, питание при недостатке железа
После 60 лет очень важно контролировать показатели гемоглобина, так как железодефицитная анемия у пожилых людей может стать причиной серьезного ухудшения самочувствия. Слабость, быстрая утомляемость, частые головокружения нередко воспринимаются как неизбежный признак старости, однако, эти симптомы могут просто свидетельствовать о снижении уровня гемоглобина. Правильное, своевременное лечение способно помочь восстановить силы и вернуть бодрость духа.
Правильное, своевременное лечение способно помочь восстановить силы и вернуть бодрость духа.
Причины анемии в пожилом возрасте
Согласно статистике, около 40% людей преклонного возраста страдают от пониженного гемоглобина. Специалисты выделяют следующие причины анемии у пожилого человека:
- Недостаток железа в организме. Это самый распространенный фактор, вызывающий анемию. Часто наблюдается при кровопотерях или скудном, недостаточном питании.
- Малокровие, вызванное хроническими болезнями. Онкологические, инфекционные, аутоиммунные заболевания нередко сопровождаются низким гемоглобином. Этот вид анемии принято лечить параллельно с основным диагнозом.
- Дефицит фолиевой кислоты. Возникает из-за того, что в пищу употребляется мало продуктов, богатых этим микроэлементом. Лечится приемом соответствующих препаратов.
- Нехватка витамина В12. Болезнь диагностируется сложнее всего, так как симптомы анемии у пожилого человека в этом случае похожи на признаки инфаркта.
 Точную картину можно получить только после анализа крови.
Точную картину можно получить только после анализа крови.
Анемия опасна тем, что нарушается транспорт кислорода в крови. Важно периодически проходить обследования, чтобы не упустить развитие болезни. При показателях гемоглобина ниже 110 г/л врач должен назначить дополнительные анализы, чтобы выявить основную причину недомогания и назначить эффективное лечение. Некоторые легкомысленно относятся к низкому гемоглобину, не считая это опасным заболеванием. Однако, если игнорировать анемию, она может вызвать серьезные когнитивные нарушения. Постепенно снижается физическая активность и работоспособность, повышается риск травм и переломов, ухудшается работа сосудов и сердца. При анемии любая болезнь лечится намного дольше, чем обычно. Низкий гемоглобин является причиной затяжного заживления ран. Кроме того, показатели анализа крови, не соответствующие норме, часто являются признаком развития злокачественных опухолей.
Симптомы анемии у пожилых людей
Симптомы заболевания достаточно размытые, их часто путают с другими, характерными для пожилого возраста болезнями. В основном, поражаются волосы и кожа, кишечник и желудок, нервная система и сердечная мышца. Если расположить симптомы низкого гемоглобина от самых распространенных к более редким, получится следующий список:
В основном, поражаются волосы и кожа, кишечник и желудок, нервная система и сердечная мышца. Если расположить симптомы низкого гемоглобина от самых распространенных к более редким, получится следующий список:
- Бледность кожных покровов;
- Головокружения;
- Хроническая усталость, мышечная слабость;
- Ломкие слоящиеся ногти;
- Сухость кожи;
- Замедленный рост волос, секущиеся кончики;
- Ранки и “заеды” в области губ.
Так же пациентов часто беспокоит шум в ушах и учащенное сердцебиение. Все перечисленные симптомы вызывают серьезный дискомфорт. Если на начальных стадиях пожилой человек может не обратить внимание на ухудшение самочувствия, то со временем неприятные ощущения становятся постоянными спутниками. Важно не терять время и начать лечение на ранних стадиях, когда терапия наиболее эффективна.
Диагностика анемии и особенности лечения
В пожилом возрасте нижняя граница нормы уровня гемоглобина — 110 г/л. Снижение показателей говорит о легкой степени анемии. Если гемоглобин падает до 70-89 г/л, речь уже идет о средней степени тяжести болезни. При тяжелой патологии показатели ниже 70 г/л. Диагностировать заболевание можно с помощью обыкновенного анализа крови.
Снижение показателей говорит о легкой степени анемии. Если гемоглобин падает до 70-89 г/л, речь уже идет о средней степени тяжести болезни. При тяжелой патологии показатели ниже 70 г/л. Диагностировать заболевание можно с помощью обыкновенного анализа крови.
При назначении лечения врач учитывает не только данные исследований, но и возраст пациента, его состояние, наличие хронических болезней и другие особенности. На начальной стадии, когда показатели не критические, можно скорректировать дефицит железа специальной диетой. Витамины, БАДы, сбалансированное питание при анемии в пожилом возрасте способны предотвратить нехватку полезных микроэлементов и помочь улучшить состояние больного.
Когда речь идет о средней и тяжелой стадии анемии, диетой уже не обойтись. Необходимы специализированные препараты, способствующие активному образованию в клетках гемоглобина и эритроцитов. Лекарства принимают по схеме, назначенной врачом. Как правило, во время еды: так полезные вещества лучше усваиваются организмом. У некоторых препаратов имеются побочные эффекты: тошнота, запоры, боли в животе. Средняя продолжительность лечения — 3-5 месяцев. При необходимости, кроме таблеток, назначаются внутримышечные или внутривенные уколы.
У некоторых препаратов имеются побочные эффекты: тошнота, запоры, боли в животе. Средняя продолжительность лечения — 3-5 месяцев. При необходимости, кроме таблеток, назначаются внутримышечные или внутривенные уколы.
Если показатели гемоглобина критические, может встать вопрос о переливании крови. Это решение обычно принимается консилиумом врачей.
Диета при анемии у пожилых людей
Правильное, сбалансированное питание — лучшая профилактика анемии. Кроме того, диета может помочь при начальной стадии заболевания, когда гемоглобин находится на уровне нижней границы нормы. Приветствуется употребление продуктов, богатых белками: белок способствует синтезу гемоглобина. Рекомендуется добавить в рацион блюда из телятины и говяжьей печени. При анемии полезны гранаты, яблоки, абрикосы. Кроме того, большое количество необходимых микроэлементов и витаминов содержится в отваре шиповника.
Примерный список обязательных к употреблению продуктов выглядит следующим образом:
- Животные белки (мясо, яйца, морепродукты).

- Продукты, улучшающие состав крови (свиная печень, орехи, свежая зелень).
- Овощи, фрукты, ягоды желтого и оранжевого цвета (сладкий перец, цитрусы, томаты, облепиха).
- Натуральный темный мед (если нет аллергии).
- Гречка, сваренная на воде.
Нужно быть осторожными с молочными продуктами и употреблять их отдельно от препаратов, содержащих железо. Любителям крепкого чая придется отказаться от своих привычек: чай мешает всасыванию железа в кровь.
Режим питания должен быть отлаженным. Принимать пищу желательно в одно и то же время, не допуская сильного чувства голода. Нужно исключить переедание: количество — не значит, качество. Из рациона рекомендуется исключить сдобу, конфеты, другие сладости, для которых характерно содержание так называемых быстрых углеводов. Запрещен прием алкоголя, так как этиловый спирт ухудшает процесс усваивания полезных микроэлементов. Единственное исключение — красное сухое вино. Разрешается пить не более 1-2 бокалов в неделю.
Очень полезны при анемии богатые витаминами свежевыжатые соки: морковный, свекольный, гранатовый. Главное, соблюдать меру, чтобы не повысить кислотность желудка. Грамотный подход к организации питания способен помочь в борьбе с анемией. В сочетании с терапией, назначенной врачом, достигается хороший эффект, и уровень гемоглобина обычно возвращается к нормальным показателям.
Важно! Информация, представленная в статье, носит исключительно ознакомительный характер. Опубликованные материалы не призывают к самостоятельному лечению. Поставить диагноз и назначить адекватное лечение может только врач. Посещение и консультация квалифицированного специалиста строго обязательны!
Железодефицитные состояния у подростков: принципы коррекции | #09/14
Одним из важных направлений в педиатрии является подростковая медицина, или гебиатрия, — раздел медицины, изучающий процессы полового созревания, взросления, роста и развития организма подростка, а также специфические заболевания, характерные для подросткового периода жизни.
Пубертатный период имеет свои уникальные особенности, обусловленные мощной вегетативной, эндокринной и иммунной перестройкой организма на фоне физиологического ростового скачка, а также нарушениями психосоциальной адаптации. Именно в это время формируются многочисленные транзиторные функциональные расстройства и проявляются ранее скрытые органические дефекты: гипоталамическая дисфункция, с широким спектром клинических проявлений (вегетососудистая дистония, метаболический синдром и пр.), врожденная неполноценность соединительной ткани (висцероптозы, суставная гипермобильность, остеохондроз и пр.), что способствует снижению адаптации к воздействию внешней среды. Следует отметить, что нозологические формы в этот возрастной период имеют существенные отличия. Так, у подростков доминируют заболевания эндокринной, нервной и костно-мышечной систем, тогда как инфекционные и простудные заболевания чаще регистрируются у детей младшего возраста, у взрослых возрастает частота новообразований и болезней системы кровообращения. Для этого возраста характерна полисистемность (полиморбидность) заболеваний. Например, у девушки, считающей себя практически здоровой, при тщательном обследовании диагностируются дисменорея, железодефицитное состояние, нарушение осанки, плоскостопие, нефроптоз, нестабильность шейного отдела позвоночника, хронический тонзиллит, миопия, синдром раздраженного кишечника с запором, дисфункция билиарного тракта, кристаллурия.
Для этого возраста характерна полисистемность (полиморбидность) заболеваний. Например, у девушки, считающей себя практически здоровой, при тщательном обследовании диагностируются дисменорея, железодефицитное состояние, нарушение осанки, плоскостопие, нефроптоз, нестабильность шейного отдела позвоночника, хронический тонзиллит, миопия, синдром раздраженного кишечника с запором, дисфункция билиарного тракта, кристаллурия.
Железодефицитное состояние относится к одной из актуальных проблем подросткового возраста. Уменьшение количества железа в организме приводит к нарушению образования гемоглобина и снижению темпов его синтеза, накоплению свободного протопорфирина в эритроцитах, развитию гипохромной анемии и трофических расстройств в органах и тканях.
В настоящее время не вызывает сомнения, что главным фактором, способствующим развитию железодефицитной анемии у подростков, является несоответствие между запасами железа в организме и потребностями в нем.
Дефицит железа в подростковом возрасте значительно чаще наблюдается у девушек, что может быть обусловлено обильными менструациями. Однако в тех случаях, когда потребности в железе намного превышают его поступление, железодефицитная анемия может развиться и у юношей. Наиболее частыми причинами в данном случае являются интенсивный рост подростка, занятия тяжелыми видами спорта, исходный низкий уровень железа на фоне несбалансированного питания, вегетарианства. Следует помнить, что железодефицитная анемия часто наблюдается при таких состояниях, как нервная анорексия, идиопатический гемосидероз легких, синдром Гудпасчера, атрансферринемия, коллагенозы, заболевания желудка и 12-перстной кишки, в том числе ассоциированные с Н. pylori, повторные кишечные инфекции, лямблиоз, глистные инвазии, воспалительные заболевания кишечника, инфекционные заболевания (туберкулез, бруцеллез, микоз и пр.), а также при хронической почечной недостаточности и в процессе диализного лечения [1, 2].
Однако в тех случаях, когда потребности в железе намного превышают его поступление, железодефицитная анемия может развиться и у юношей. Наиболее частыми причинами в данном случае являются интенсивный рост подростка, занятия тяжелыми видами спорта, исходный низкий уровень железа на фоне несбалансированного питания, вегетарианства. Следует помнить, что железодефицитная анемия часто наблюдается при таких состояниях, как нервная анорексия, идиопатический гемосидероз легких, синдром Гудпасчера, атрансферринемия, коллагенозы, заболевания желудка и 12-перстной кишки, в том числе ассоциированные с Н. pylori, повторные кишечные инфекции, лямблиоз, глистные инвазии, воспалительные заболевания кишечника, инфекционные заболевания (туберкулез, бруцеллез, микоз и пр.), а также при хронической почечной недостаточности и в процессе диализного лечения [1, 2].
Выделяют прелатентный дефицит железа (опустошаются запасы железа только из депо при сохранении транспортного и гемоглобинового фондов железа), латентный дефицит железа (составляет 70% от всех железодефицитных анемий) и железодефицитная анемия (составляет 30% от всех железодефицитных состояний) (табл. ).
).
Клиническая картина железодефицитной анемии состоит из двух ведущих синдромов: анемического и сидеропенического. Для последнего характерны дистрофические изменения кожи и ее придатков; извращение вкуса и обоняния, мышечные боли (ввиду дефицита миоглобина), мышечная гипотония, изменения нервной регуляции.
Следует отметить, что клинические проявления заболевания в подростковом возрасте отличаются от проявлений у детей раннего возраста. Так, для них более характерны койлонихии, синева склер (через истонченную склеру просвечивает сосудистая оболочка), вкусовые и обонятельные нарушения, дисфагия, диспепсия.
Диагностика железодефицитных состояний основывается на определении представленных выше лабораторных показателей. Основным критерием является содержание ферритина в сыворотке крови [3]. Однако при невозможности определения данного показателя можно ориентироваться на уровень гемоглобина, определение которого доступно в любом медицинском учреждении.
Целесообразно ежегодное определение уровня гемоглобина у девушек, имеющих обильные кровопотери при менструации или иной природы, низкое потребление железа с пищей (пищевые ограничения для снижения веса, вегетарианство и пр.), железодефицитную анемию различной природы в анамнезе. Юноши нуждаются в контроле уровня гемоглобина, если интенсивно занимаются тяжелыми видами спорта (анемия атлетов).
Во всех случаях железодефицитного состояния необходимо установить непосредственную причину его возникновения и по возможности ее ликвидировать (устранить источник кровопотери, провести терапию основного заболевания, осложнившегося сидеропенией). Лечение должно быть комплексным и нацеленным не только на устранение анемии как симптома, но и на ликвидацию дефицита железа и восполнение его запасов в организме.
Необходимо обогатить рацион подростка продуктами — основными источниками железа, при этом имеет значение не только количество железа в конкретном продукте, но и степень его всасывания и возможность усвоения организмом.
Мясо, особенно красное (телятина, говядина, баранина), является лучшим источником гемового железа, из него усваивается 20–25% железа. Железо из курицы и свинины усваиваются в меньшей степени. А в печени и рыбе железо содержится в виде ферритина и гемосидерина, поэтому усваивается еще хуже.
Негемовое железо (овощи, фрукты, орехи) усваивается плохо (1–5%), причем на его усвоение влияет много факторов, которые могут как улучшать, так и ухудшать его всасывание. Так, усиливают всасывание железа: витамин С (особенно много в цитрусовых), соляная кислота (содержится в желудочном соке), фруктоза (фрукты, мед). Ухудшают всасывание железа: препараты, снижающие кислотность желудочного сока (антисекреторные препараты, антациды), кальций (много в молочных продуктах), оксалаты (шпинат, капуста, свекла, орехи, шоколад, чай и пр.), полифенолы (какао, кофе, черный и некоторые виды травяного чая), фитиновая кислота (грецкие орехи, миндаль, бобовые, отруби) [4].
Однако когда анемия уже развилась, ее нельзя вылечить только диетой: железодефицитная анемия лечится препаратами железа. Питание помогает поддерживать нормальный баланс железа в организме после лечения.
Питание помогает поддерживать нормальный баланс железа в организме после лечения.
К наиболее часто применяемым соединениям железа в педиатрической практике относятся препараты железа трехвалентного гидроксид полимальтозат и соли двухвалентного железа — сульфат, фумарат, хлорид и глюконат. Для улучшения всасывания соли двухвалентного железа комбинируют с органическими кислотами, аминокислотами и другими соединениями. Предпочтение отдается пероральным формам, так как по сравнению с парентеральным введением скорость восстановления уровня гемоглобина почти не отличается, а количество побочных эффектов резко снижено. Прием препаратов железа рекомендуется за 1 час до еды, предпочтительно в вечернее время, так как процесс абсорбции железа увеличивается во второй половине суток.
Терапевтический эффект при пероральном приеме железа появляется постепенно. Первым положительным клиническим признаком является исчезновение или уменьшение мышечной слабости. На 8–12 день от начала лечения повышается содержание ретикулоцитов в периферической крови. Нормализация гемоглобина происходит к 4–5 неделе от начала терапии.
Нормализация гемоглобина происходит к 4–5 неделе от начала терапии.
В последние годы в терапии железодефицитных состояний у подростков активно применяют железосодержащие препараты нового поколения на основе полимальтазного комплекса гидроокиси трехвалентного железа — Мальтофер и Мальтофер Фол, который кроме железа содержит фолиевую кислоту, принимающую участие в выработке нуклеиновых кислот, пуринов, аминокислот, стимулирущих эритропоэз.
Результаты применения Мальтофера различными авторами оцениваются положительно [5]. Одной из привлекательных характеристик этого препарата является его низкая токсичность. Препарат хорошо переносится, имеет приятный вкус и форму жевательных таблеток, что, несомненно, повышает приверженность к терапии. При железодефицитной анемии детям и подросткам в возрасте от года до 12 лет Мальтофер назначается в дозе 50–100 мг в сутки, при латентном дефиците и для профилактики дефицита железа — по 25–50 мг в сутки. Детям и подросткам старше 12 лет — по 100–300 мг в сутки, а при латентном дефиците железа и в профилактических целей — по 50–100 мг в сутки. Длительность терапии, как правило, составляет не менее 2 мес, что обусловлено степенью дефицита железа в организме и истощения его запасов, скоростью кроветворения, всасываемостью. В случае клинически выраженного дефицита железа нормализация гемоглобина достигается лишь через 2–3 мес после начала лечения. Для восстановления внутренних резервов железа прием в профилактических дозах должен быть продолжен в течение нескольких месяцев. При продолжающихся кровопотерях необходимо проводить профилактические курсы лечения препаратом железа (по 1 мес 2–4 раза в год).
Длительность терапии, как правило, составляет не менее 2 мес, что обусловлено степенью дефицита железа в организме и истощения его запасов, скоростью кроветворения, всасываемостью. В случае клинически выраженного дефицита железа нормализация гемоглобина достигается лишь через 2–3 мес после начала лечения. Для восстановления внутренних резервов железа прием в профилактических дозах должен быть продолжен в течение нескольких месяцев. При продолжающихся кровопотерях необходимо проводить профилактические курсы лечения препаратом железа (по 1 мес 2–4 раза в год).
Литература
- Коровина Н. А., Заплатников А. Л., Захарова И. Н. Железодефицитные анемии у детей (руководство для врачей). М., 1999. С. 64.
- Финогенова Н. А., Чернов В. М., Морщакова Е. Ф. и др. Анемии у детей: диагностика и лечение. М., 2000. С. 9–17.
- Финогенова Н. А., Чернов В. М., Морщакова Е. Ф. и др. Анемии у детей. Диагностика, дифференциальная диагностика, лечение.
 М., 2004. С. 20–64.
М., 2004. С. 20–64. - Городецкий В. В., Годулян О. В. Железодефицитные состояния и железодефицитная анемия: лечение и диагностика (метод. рекомендации). М., 2006. С. 25.
- Соболева М. К. Опыт применения препаратов Мальтофер и Мальтофер Фол при лечении железодефицитной анемии у детей и подростков // Сибирский консилиум. 2003, № 1, с. 79–82.
Т. А. Бокова1, кандидат медицинских наук
Г. В. Масликова, кандидат медицинских наук
ГБУЗ МО МОНИКИ им. М. Ф. Владимирского, Москва
1 Контактная информация: [email protected]
Кислород падает — значит, ковид? Какой уровень считается опасным и почему дело может быть не в лёгких
Даже если человек не болеет пневмонией и не ощущает одышки, коронавирус способен незаметно морить его внутренние органы кислородным голодом.

Кислорода в крови должно быть минимум 95%, а лучше 98%. Если меньше — это уже повод обратиться к врачу. Давайте разберёмся, почему это так важно, особенно во время пандемии.
Для этого нужно прояснить, что именно происходит, когда мы дышим. Без этого невозможно понять невероятное коварство «короны». Итак, мы вдыхаем воздух, который пока ещё содержит вполне достаточно кислорода. Его ловят специальные крошечные пузырьки, которыми выстлана вся внутренняя поверхность лёгких, — альвеолы. У каждого человека их 600–700 миллионов. И каждый такой пузырёк опутан целой сетью микроскопических кровеносных сосудов — капилляров. В них поступает уже «отработанная» венозная кровь, которой срочно нужна кислородная заправка. У капилляров тонкие стенки, да и у альвеол тоже, так что кислород из воздуха в пузырьке свободно проходит сквозь препятствия внутрь капилляров по естественному закону диффузии — «перемешивания» молекул разных веществ.
Фото © Shutterstock
Но это только начало процесса. Дальше молекулы кислорода нужно доставить через кровь в органы и ткани организма. Этим занимаются специальные молекулы в эритроцитах — гемоглобин. Конструкция гемоглобина состоит из белка глобина и ещё одной структуры под названием гем. В этом геме находится железо, которое отлично взаимодействует с кислородом. Только сам по себе гем моментально окисляется, то есть забирает себе кислород навсегда и никому его больше не отдаёт. А вот в сочетании с глобином он временно захватывает несколько молекул и несёт к месту назначения — в мозг, печень и все прочие органы и ткани. Там кислород «сходит с трамвая», то есть высвобождается, чтобы вступить в другие химические реакции, обеспечивающие нашу жизнедеятельность.
Дальше молекулы кислорода нужно доставить через кровь в органы и ткани организма. Этим занимаются специальные молекулы в эритроцитах — гемоглобин. Конструкция гемоглобина состоит из белка глобина и ещё одной структуры под названием гем. В этом геме находится железо, которое отлично взаимодействует с кислородом. Только сам по себе гем моментально окисляется, то есть забирает себе кислород навсегда и никому его больше не отдаёт. А вот в сочетании с глобином он временно захватывает несколько молекул и несёт к месту назначения — в мозг, печень и все прочие органы и ткани. Там кислород «сходит с трамвая», то есть высвобождается, чтобы вступить в другие химические реакции, обеспечивающие нашу жизнедеятельность.
Что происходит при ковиде?
Самое, пожалуй, очевидное — это поражение альвеол. Дело в том, что у их клеток, как и положено, есть оболочки — мембраны. А в эти мембраны в довольно большом количестве встроены особые белки, обозначенные в микробиологии как АПФ2 (в англоязычном варианте — ACE2). Не будем расшифровывать, потому что это не так важно. Тут самое интересное, что эти АПФ2 служат в качестве клеточных рецепторов — отвечают за взаимодействие клеток с окружающей средой. Так вот, эти самые рецепторы оказались максимально удобной мишенью для SARS-CoV-2. Как мы уже усвоили, «корона» ковидной частицы (шипы, которые из неё торчат) — это Spyke-белки. Именно этими «крючками» коронавирусный элемент легко цепляется за АПФ2, крепко жмёт его руку и уверяет, что он — вкусное и полезное угощение. И наивная клетка радостно это дело проглатывает.
Не будем расшифровывать, потому что это не так важно. Тут самое интересное, что эти АПФ2 служат в качестве клеточных рецепторов — отвечают за взаимодействие клеток с окружающей средой. Так вот, эти самые рецепторы оказались максимально удобной мишенью для SARS-CoV-2. Как мы уже усвоили, «корона» ковидной частицы (шипы, которые из неё торчат) — это Spyke-белки. Именно этими «крючками» коронавирусный элемент легко цепляется за АПФ2, крепко жмёт его руку и уверяет, что он — вкусное и полезное угощение. И наивная клетка радостно это дело проглатывает.
Как следствие, по сигналу тревоги капилляры начинают выделять жидкое содержимое крови — экссудат. В этой жидкости есть иммуноглобулины для борьбы с интервентами, а ещё это замедляет кровоток, чтобы вирус не разносило по всему организму. Беда в том, что экссудат заполняет пузырьки и снижает, так сказать, полезную площадь, предназначенную для воздуха.
В то же время, по мнению директора НИИ фтизиопульмонологии Петра Яблонского, кислород при ковиде перестаёт поступать в капилляры, потому что нарушается контакт между стенками кровеносных сосудов и альвеол, которые в нормальном состоянии практически единое целое.
Альвеоло-капиллярная мембрана — это самый тонкий механизм внутреннего дыхания, именно в этой мембране происходит этот интимный процесс обогащения кислородом крови, эритроциты именно там насыщаются. И когда эти две среды разобщены, то получается такой момент шунтирования — кровь пробегает через лёгкие, но уходит, не нагруженная кислородом
Пётр Яблонский
Директор Санкт-Петербургского НИИ фтизиопульмонологии, доктор медицинских наук
Но это далеко не все способы кислородной блокады в ковидном арсенале. Есть ещё кое-что. Этот вирус с таким же успехом оккупирует эритроциты. Об этом заявили в том числе учёные из Дальневосточного федерального университета. Более того, по их мнению, красные кровяные тельца — ключевая мишень ковида. К похожим, если не аналогичным, выводам пришли, к примеру, китайские исследователи. По их данным, коронавирус разрушает гемоглобин — отрывает от него гем и использует как «запчасть» для своего будущего репликанта, а ненужное железо просто выбрасывает.
А при таком раскладе, как мы теперь понимаем, кислород никуда не переносится. Транспорт не работает. Именно поэтому российские учёные (опять же из ДФУ) призвали обратить самое пристальное внимание на своё здоровье, если во рту ощущается привкус железа. Это могут быть останки разорванного гемоглобина, которые выделяются со слюной. Исследователи подчеркнули, что подобные ощущения — первичная реакция на коронавирус, то есть это происходит на самых ранних этапах вероломной атаки. А значит, никаких намёков на заболевание (да и вообще никаких признаков недомогания) может ещё не быть. А меж тем организм уже приближается к критической нехватке кислорода, от которой страдают все органы без исключения. Это грозит полиорганной недостаточностью и смертью. Учёные считают, что в такой ситуации аппарат ИВЛ совершенно бесполезен: сколько ни старайся обеспечить лёгкие кислородом, развозить его по организму некому. По мнению исследователей, стоит вместо искусственной вентиляции ввести больному дозу эритроцитов и обеспечить его витамином В12, потому что он отвечает за кроветворение.
Однако директор Санкт-Петербургского НИИ фтизиопульмонологии Пётр Яблонский предупредил и о возможной опасности подобных мер.
Введение эритроцитной массы мало и даже контрпродуктивно, потому что мы тем самым усиливаем тромбогенный потенциал крови. Я не видел больных ковидом с анемией
Пётр Яблонский
Директор Санкт-Петербургского НИИ фтизиопульмонологии, доктор медицинских наук
А вот дыхательную маску доктор медицинских наук однозначно одобряет.
С точки зрения прогноза и недопущения до искусственной вентиляции — это, безусловно, хороший метод
Пётр Яблонский
Директор Санкт-Петербургского НИИ фтизиопульмонологии, доктор медицинских наук
Как следить за уровнем кислорода в крови?
Учёный пояснил, что продающиеся в аптеках бытовые измерительные приборы — оксиметры, пульсоксиметры — показывают не самые точные данные, но для отслеживания состояния организма их вполне достаточно. При этом он посоветовал прикладывать не один палец, а по очереди несколько пальцев обеих рук. А действительно качественный анализ можно провести только с помощью газоанализаторов, которые есть, к примеру, в скорой и в отделениях реанимации.
А действительно качественный анализ можно провести только с помощью газоанализаторов, которые есть, к примеру, в скорой и в отделениях реанимации.
Вот только очень хотелось бы как-то обойтись без этого.
Хронический лейкоз
Вам поставили диагноз: Хронический лейкоз?Наверняка Вы задаётесь вопросом: что же теперь делать?
Подобный диагноз всегда делит жизнь на «до» и «после». Все эмоциональные ресурсы пациента и его родных брошены на переживания и страх. Но именно в этот момент необходимо изменить вектор «за что» на вектор «что можно сделать». Очень часто пациенты чувствуют себя безгранично одинокими вначале пути. Но вы должны понимать — вы не одни.
Мы поможем вам справиться с болезнью и будем идти с вами рука об руку через все этапы вашего лечения.
Предлагаем вашему вниманию краткий, но очень подробный обзор хронического лейкоза.
Его подготовили высоко квалифицированные специалисты Отдела лекарственного лечения злокачественных новообразований МРНЦ имени А. Ф. Цыба и Отдела лекарственного лечения опухолей МНИОИ имени П.А. Герцена – филиалов ФГБУ «НМИЦ радиологии» Минздрава России под редакцией заведующих отделами, д.м.н. ФАЛАЛЕЕВОЙ Н.А. и д.м.н. ФЕДЕНКО А.А.
Ф. Цыба и Отдела лекарственного лечения опухолей МНИОИ имени П.А. Герцена – филиалов ФГБУ «НМИЦ радиологии» Минздрава России под редакцией заведующих отделами, д.м.н. ФАЛАЛЕЕВОЙ Н.А. и д.м.н. ФЕДЕНКО А.А.
МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Хронический лимфолейкоз (ХЛЛ)— Опухолевое заболевание, морфологическим субстратом которого являются малого размера зрелые В-лимфоциты, обнаруживающиеся преимущественно в крови, костном мозге, лимфатических узлах, селезёнке и печени.
Для установления диагноза ХЛЛ, согласно современным критериям, необходимо наличие трех признаков: абсолютное число лимфоцитов крови не менее 5 х10 9 /л, более 30% лимфоцитов в костном мозге, иммунологическое подтверждение наличия опухолевых лимфоцитов со строго определенными характеристиками, без которого диагноз ХЛЛ не может считаться доказанным, поскольку дифференциальный диагноз с похожими заболеваниями проводится на основании именно иммунофенотипирования .
ХЛЛ — наиболее распространенный вид лейкоза в странах Европы и Северной Америки, где на его долю приходится до 30% всех лейкозов. Ежегодная заболеваемость ХЛЛ в этих странах составляет 3-3,5 случая на 100000 населения в год, при этом среди лиц старше 65 лет – до 20 случаев и старше 70 лет – до 50 на 100000.
Средний возраст заболевших — 65 лет, почти 70% заболевают между 50 и 70 годами, только около 10% — до 40 лет. Мужчины заболевают в 2 раза чаще женщин.
В большинстве случаев на ранних этапах ХЛЛ характеризуется медленным течением с постепенно нарастающим лейкоцитозом, который без лечения может достигать 500-1000 х109/л и более, лимфоцитозом, обычно коррелирующим с уровнем лейкоцитоза и составляющим 70-85-99%. Уровни гемоглобина, числа тромбоцитов на ранних этапах болезни обычно нормальные. При высоком лейкоцитозе и лимфоцитозе — уровни гемоглобина и числа тромбоцитов часто сниженные за счет вытеснения нормального кроветворения лейкозным клоном или присоединения нередких для ХЛЛ аутоиммунных осложнений – аутоиммунной гемолитической анемии и/или тромбоцитопении.
Уровни гемоглобина, числа тромбоцитов на ранних этапах болезни обычно нормальные. При высоком лейкоцитозе и лимфоцитозе — уровни гемоглобина и числа тромбоцитов часто сниженные за счет вытеснения нормального кроветворения лейкозным клоном или присоединения нередких для ХЛЛ аутоиммунных осложнений – аутоиммунной гемолитической анемии и/или тромбоцитопении.
Темпы течения болезни и продолжительность жизни при ХЛЛ колеблются в широких пределах – от 2-3 до 20-30 лет. Медленное развитие в начале болезни – причина того, что у 70% пациентов с ХЛЛ диагностируется при анализе крови, сделанном в связи с другими заболеваниями. Примерно у 15-20% больных клинические и гематологические признаки заболевания остаются стабильными и минимально выраженными без лечения на протяжении многих лет и не влияют на продолжительность жизни.
При медленном прогрессировании ХЛЛ больной остается под наблюдением (выжидательная тактика), сигналом к началу лечения служат:
• Массивная инфильтрация костного мозга лимфоцитами (более 80% лимфоцитов в миелограмме), особенно если при этом имеется снижение уровня эритроцитов и тромбоцитов.
• Быстрое нарастание лимфоцитоза – удвоении абсолютного числа лимфоцитов в крови менее чем за 12 мес.
Химиотерапия хронического лейкоза:В настоящее время препаратом выбора при ХЛЛ являются флударабин и флударабинсодержащие режимы. Схема FCR (флударабин, циклофосфамид, ритуксимаб) является стандартом терапии 1-й линии у молодых пациентов без тяжелой сопутствующей патологии. Хлорамбуцил (лейкеран), в настоящее время остаются стандартом стартовой терапии у пациентов преклонного возраста. Увеличение показателей выживаемости без прогрессирования может быть достигнуто путем добавления к хлорамбуцилу ритуксимаба.
Препарат Бендамустин, вследствие своей низкой токсичности иногда является единственной возможностью терапии у пожилых пациентов, а также больных с сопутствующей патологией.
Таргетная (избирательная, точечная) терапия ХЛЛ: Важным шагом в разработке новых методов терапии при ХЛЛ стало добавление к флударабин-содержащим режимам моноклональных антител к антигену CD20 (ритуксимаб, обинотузумаб). В настоящее время лечение большинства пациентов проводится с использованием моноклональных анти-CD-20-антител.
В настоящее время лечение большинства пациентов проводится с использованием моноклональных анти-CD-20-антител.
Спектр таргетных препаратов при ХЛЛ расширяется с каждым годом. В настоящее время в России зарегистрирован препарат ибрутиниб (ингибитор тирозинкиназы Брутона) для лечения крайне неблагоприятной группы пациентов ХЛЛ с делецией хромосомы 17р или мутацией ТР53. Список таргетных препаратов постоянно обновляется.
Филиалы и отделения Центра, в которых лечат хронический лейкозФГБУ «НМИЦ радиологии» Минздрава России обладает всеми необходимыми технологиями лучевого, химиотерапевтического и хирургического лечения, включая расширенные и комбинированные операции. Все это позволяет выполнить необходимые этапы лечения в рамках одного Центра, что исключительно удобно для пациентов.
Отдел лекарственного лечения злокачественных новообразований МРНЦ имени А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России
Заведующая отделом, д. м.н. ФАЛАЛЕЕВА Наталья Александровна
м.н. ФАЛАЛЕЕВА Наталья Александровна
8 (484) 399 – 31-30, г. Обнинск, Калужской области
Отдел лекарственного лечения опухолей МНИОИ имени П.А. Герцена –филиал ФГБУ «НМИЦ радиологии» Минздрава России
Заведующий отделом, д.м.н. ФЕДЕНКО Александр Александрович
8 (494) 150 11 22
10 распространенных причин и что спросить
Вам когда-нибудь говорили, что у кого-то из старших родственников анемия?
Или, возможно, вы заметили, что количество эритроцитов в отчете о крови помечено как «низкое»? Или заметили «низкий гемоглобин» в заключении врача?
Анемия означает, что количество эритроцитов ниже нормы, и она очень часто встречается у пожилых людей. Около 10% самостоятельно живущих людей старше 65 лет страдают анемией. А с возрастом анемия становится еще более распространенным явлением.
Но многие пожилые люди и семьи с трудом понимают анемию.
В этом нет ничего удивительного: анемия связана с головокружительным набором основных заболеваний и может представлять собой что угодно, от опасной для жизни чрезвычайной ситуации до легкой хронической проблемы, которая едва заставляет врача моргать.
И все же меня беспокоит, что пожилые люди и семьи не знают больше о анемии. Если вы или ваш родственник страдаете этим заболеванием, важно понимать, что происходит, и каков план последующих действий.(Я так часто обнаруживал, что пациент не знал, что у него была анемия!) Непонимание анемии также может привести к ненужному беспокойству или, возможно, даже к неподходящему лечению препаратами железа.
Рекомендуемая загрузка: Что спросить у медицинских работников об анемии. Используйте этот бесплатный PDF-файл, чтобы задать ключевые вопросы о своем состоянии анемии, в том числе о том, что было сделано для диагностики причины и каков план лечения. Нажмите здесь, чтобы загрузить. А поскольку анемия часто вызывается какой-либо другой проблемой в организме, непонимание анемии часто означает, что люди не понимают чего-то еще, что важно для их здоровья.
К счастью, вам не нужно быть врачом, чтобы хорошо разбираться в основах анемии.
Этот пост поможет вам понять:
- Как выявляется и диагностируется анемия у пожилых людей.
- Симптомы анемии.
- Наиболее частые причины анемии и тесты, которые часто используются для их выявления.
- Что спросить у врача.
- Как улучшить наблюдение, если у вас или вашего родственника диагностирована анемия.
Анемия означает более низкое, чем обычно, количество эритроцитов, циркулирующих в крови.
Эритроциты всегда подсчитываются как часть теста «Полный анализ крови» (CBC), который является очень часто заказываемым анализом крови.
Тест CBC обычно включает следующие результаты:
- Количество лейкоцитов (WBCs): количество лейкоцитов на микролитр крови
- Количество красных кровяных телец (RBCs): количество красных кровяных телец на микролитр крови
- Гемоглобин (Hgb): сколько граммов этого переносящего кислород белка на децилитр крови
- Гематокрит (Hct): фракция крови, состоящая из эритроцитов
- Средний корпускулярный объем (MCV): средний размер эритроцитов
- Количество тромбоцитов (Plts): сколько тромбоцитов (меньших клеток, участвующих в свертывании крови) на микролитр крови
(Для получения дополнительной информации о тесте CBC см. Эту страницу Medline.Дополнительные сведения об общих анализах крови см. В разделе Общие сведения о лабораторных анализах: 10 часто используемых анализов крови для пожилых людей.)
Эту страницу Medline.Дополнительные сведения об общих анализах крови см. В разделе Общие сведения о лабораторных анализах: 10 часто используемых анализов крови для пожилых людей.)
Обычно при обнаружении анемии врачи полагаются на уровень гемоглобина и гематокрит, а не на количество эритроцитов.
«Нормальный» уровень гемоглобина обычно находится в диапазоне 14-17 г / дл для мужчин и 12-15 г / дл для женщин. Однако разные лаборатории могут определять нормальный диапазон по-разному.
Низкий уровень гемоглобина — то есть ниже нормы — можно использовать для выявления анемии.Клиницисты часто подтверждают более низкий уровень гемоглобина, повторяя общий анализ крови.
Если врачи обнаруживают анемию, они обычно пересматривают измерение среднего корпускулярного объема (включенного в общий анализ крови), чтобы увидеть, являются ли эритроциты меньше или больше, чем обычно. Мы делаем это, потому что размер красных кровяных телец может помочь врачам определить первопричину анемии.
Следовательно, анемию часто описывают как:
- Микроцитарные: эритроциты меньше нормы
- Нормоцитарные: эритроциты нормального размера
- Макроцитарные: красные тельца крупнее нормальных
Красные кровяные тельца в крови используют гемоглобин для переноса кислорода из легких в каждую клетку вашего тела.Поэтому, когда человеку не хватает правильно функционирующих красных кровяных телец, в организме начинают проявляться симптомы, связанные с недостатком кислорода.
Общие симптомы анемии:
- усталость
- слабость
- одышка
- высокий пульс
- головные боли
- становится бледнее, что часто сначала можно увидеть, заглянув внутрь нижних век
- понизить артериальное давление (особенно если анемия вызвана кровотечением)
Тем не менее, у людей очень часто бывает легкая анемия, то есть уровень гемоглобина, который не намного ниже нормы, и в этом случае симптомы могут быть едва заметными или вовсе отсутствовать.
Это потому, что тяжесть симптомов зависит от двух решающих факторов:
- Насколько ниже нормы уровень гемоглобина?
- Как быстро гемоглобин упал до этого уровня?
Этот второй фактор очень важно иметь в виду. Человеческое тело в некоторой степени адаптируется к более низкому уровню гемоглобина, но только если на это отводятся недели или месяцы.
Таким образом, это означает, что если чей-то гемоглобин упадет с 12,5 г / дл до 10 г / дл (что мы обычно считаем умеренным уровнем анемии), они, вероятно, будут чувствовать себя довольно неприятно, если это падение произойдет в течение двух дней, но гораздо меньше. так, если он медленно развивался в течение двух месяцев
Иногда люди хотят знать, насколько низким должен быть гемоглобин, чтобы анемия была «тяжелой». Это действительно зависит от истории болезни человека и от того, насколько быстро упал гемоглобин, но обычно гемоглобин от 6,5 до 7,9 г / дл часто считается «тяжелой» анемией.
Иногда люди хотят знать, насколько низким может упасть гемоглобин перед смертью. Как правило, уровень гемоглобина ниже 6,5 г / дл считается опасным для жизни. Но опять же, как долго организм может переносить низкий уровень гемоглобина, зависит от многих факторов, в том числе от того, продолжает ли гемоглобин быстро падать (например, из-за внутреннего кровотечения) или медленно падает.Исследование Свидетелей Иеговы, умерших после отказа от переливания крови, показало, что люди с гемоглобином от 4,1 до 5 г / дл умирали в среднем примерно через 11 дней.
Наиболее частые причины анемии у пожилых людейВсякий раз, когда обнаруживается анемия, важно выяснить , что такое , вызывающее пониженное количество эритроцитов.
По сравнению с большинством клеток в организме нормальные эритроциты имеют короткую продолжительность жизни: около 100–120 дней.Таким образом, здоровое тело всегда должно производить красные кровяные тельца. Это делается в костном мозге и занимает около семи дней, затем новые эритроциты работают в крови в течение 3-4 месяцев. Как только эритроцит умирает, организм восстанавливает железо и повторно использует его для создания новых красных кровяных телец.
Это делается в костном мозге и занимает около семи дней, затем новые эритроциты работают в крови в течение 3-4 месяцев. Как только эритроцит умирает, организм восстанавливает железо и повторно использует его для создания новых красных кровяных телец.
Анемия возникает, когда что-то идет не так с этими нормальными процессами. У детей и молодых людей причина анемии обычно одна. Но у пожилых людей довольно часто бывает несколько сосуществующих причин анемии.
Полезно думать об анемии, рассматривая две категории причин:
- Проблема , производящая эритроцитов и / или
- Проблема потеря эритроцитов
Вот наиболее частые причины низкого гемоглобина для каждой категории:
Проблемы с производством красных кровяных телец . К ним относятся проблемы, связанные с костным мозгом (где образуются красные кровяные тельца), а также дефицит витаминов и других веществ, используемых для производства красных кровяных телец. Общие конкретные причины включают:
Общие конкретные причины включают:
- Химиотерапия или другие лекарства , влияющие на клетки костного мозга, ответственные за выработку красных кровяных телец.
- Недостаток железа . Это иногда случается с вегетарианцами и другими людьми, которые не едят много мяса. Но чаще это происходит из-за хронической кровопотери, например обильных менструаций у молодых женщин, или медленно кровоточащей язвы желудка или тонкой кишки, или даже из-за хронического кровотечения в толстой кишке.
- Недостаток витаминов, необходимых для эритроцитов .Витамин B12 и фолиевая кислота необходимы для образования красных кровяных телец.
- Низкий уровень эритропоэтина . Эритропоэтин обычно вырабатывается почками и помогает стимулировать костный мозг вырабатывать красные кровяные тельца. (Это «эпо» вещество, используемое неэтичными спортсменами в «кровяном допинге».) Люди с заболеванием почек часто имеют низкий уровень эритропоэтина, что может вызвать анемию.

- Хроническое воспаление . Многие хронические заболевания связаны с хроническим воспалением слабой или средней степени.Рак и хронические инфекции также могут вызывать воспаление. Воспаление, похоже, мешает выработке красных кровяных телец, явление, известное как «анемия хронического заболевания».
- Заболевания костного мозга. Любое заболевание, поражающее костный мозг или клетки крови, может мешать выработке красных кровяных телец и, следовательно, вызывать анемию.
Проблемы с потерей эритроцитов. Кровопотеря вызывает анемию, потому что красные кровяные тельца покидают кровоток. Это может происходить быстро и очевидно, но также может происходить медленно и незаметно.Как отмечалось выше, медленное кровотечение может усугубить анемию, вызывая дефицит железа. Вот некоторые примеры того, как люди теряют кровь:
- Травмы и травмы . Это может вызвать явно очевидное кровотечение, но также иногда вызывает у людей кровотечение в пространство внутри тела, которое бывает труднее обнаружить.

- Хроническое кровотечение в желудке, тонкой или толстой кишке . Это может быть связано со многими причинами, среди которых наиболее частые:
- Частые заборы крови .Это в основном проблема для людей, которые госпитализированы и ежедневно берут кровь на анализ.
- Менструальное кровотечение . Обычно это проблема молодых женщин, но иногда встречается у женщин старшего возраста.
Существует также третья категория анемий, связанных с аномальным разрушением красных кровяных телец в организме до того, как они доживут до своей обычной продолжительности жизни. Это называется гемолитической анемией, и она встречается гораздо реже.
В крупном исследовании причин анемии у пожилых американцев, не проживающих в специализированных учреждениях, было обнаружено следующее:
- Одна треть анемий была вызвана дефицитом железа, витамина B12 и / или фолиевой кислоты.
- Одна треть была вызвана хроническим заболеванием почек или анемией хронического заболевания.

- Одна треть анемий была «необъяснимой».
После обнаружения анемии медицинским работникам важно провести дополнительную оценку и наблюдение, чтобы выяснить, что может быть причиной анемии.
Понимание хронологии анемии — быстро или медленно? Стабильно ли показатель эритроцитов или продолжает снижаться со временем? — помогает врачам разобраться в том, что происходит и насколько острая ситуация.
Общие контрольные тесты включают:
- Проверка стула на признаки микроскопической кровопотери
- Проверка уровня ферритина (который отражает запасы железа в организме)
- Проверка уровня витамина B12 и фолиевой кислоты
- Проверка функции почек, которая первоначально выполняется путем анализа расчетной скорости клубочковой фильтрации (включается в большинство основных результатов анализа крови)
- Проверка количества ретикулоцитов, которое показывает, пытается ли костный мозг производить дополнительные эритроциты для компенсации анемии
- Проверка уровня «маркера воспаления» в крови, например скорости оседания эритроцитов (СОЭ) или С-реактивного белка (СРБ)
- Оценка мазка периферической крови, что означает исследование клеток крови под микроскопом.

- Анализы мочи для проверки белков, связанных с определенными заболеваниями клеток крови
Если анемия достаточно сильна или у человека серьезные симптомы, врачи могут также рассмотреть возможность переливания крови.Однако, хотя даже легкая анемия связана с худшими результатами для здоровья, исследования показывают, что переливание крови от легкой до умеренной анемии, как правило, не приносит пользы. (Этот вопрос особенно актуален, когда люди госпитализированы или находятся в острой форме.)
Что спросить у врача при анемии Рекомендуемая загрузка: Что спросить у медицинских работников об анемии. Используйте этот бесплатный PDF-файл, чтобы задать ключевые вопросы о своем состоянии анемии, в том числе о том, что было сделано для диагностики причины и каков план лечения.Нажмите здесь, чтобы загрузить. Если вам сказали, что у вас или у вашего старшего родственника анемия, убедитесь, что вы понимаете, насколько серьезной она кажется, и , что, по мнению врачей, может быть ее причиной. . Это поможет вам понять план последующего наблюдения и лечения.
. Это поможет вам понять план последующего наблюдения и лечения.
Некоторые конкретные вопросы, которые могут быть полезны, включают:
- Насколько серьезна анемия? Кажется ли он легким, умеренным или тяжелым?
- Как вы думаете, что вызывает это? Могло ли быть задействовано несколько причин или факторов?
- Как вы думаете, сколько времени у меня была анемия? Вроде стабильно или становится хуже?
- Это причина моих симптомов или вы думаете, что что-то еще вызывает мои симптомы?
- Могут ли быть задействованы какие-либо из моих лекарств?
- Каковы наши планы на дальнейшую оценку?
- Каков наш план лечения этой анемии?
- Когда вы рекомендуете еще раз проверить CBC? Каков наш план по мониторингу анемии?
Не забудьте запросить и сохранить копии результатов лабораторных исследований.Это поможет вам и вашим врачам в будущем иметь возможность просматривать ваши прошлые лаборатории, связанные с анемией и любыми связанными с этим тестами.
Очень распространенный диагноз у пожилых людей — железодефицитная анемия. Если вам поставили диагноз этого типа анемии, убедитесь, что врачи проверили уровень ферритина или иным образом подтвердили, что у вас низкий уровень железа.
Я действительно просмотрел медицинские карты, в которых пациенту прописывали железо от анемии, но не было зарегистрировано фактического низкого уровня железа.Это говорит о том, что врач мог предположить, что анемия возникла из-за низкого содержания железа.
Однако, хотя дефицит железа является обычным явлением, важно, чтобы клиницисты и пациенты подтвердили, что это причина, прежде чем переходить к лечению добавками железа. Врачи также должны оценить другие причины анемии, поскольку пожилые люди очень часто одновременно испытывают несколько причин анемии (например, дефицит железа и дефицит витамина В12 ).
Если дефицит железа подтвержден, убедитесь, что врачи попытались проверить любые причины медленной кровопотери.
У пожилых людей часто возникают микроскопические кровотечения в желудке или толстой кишке, особенно если они ежедневно принимают аспирин или нестероидные противовоспалительные препараты (НПВП), такие как ибупрофен. (По этой и другим причинам НПВП включены в список медикаментов Пива, которые пожилые люди должны использовать с осторожностью.)
Имейте в виду, что добавки железа часто вызывают у пожилых людей запор. Таким образом, вы хотите принимать их только в том случае, если подтверждена железодефицитная анемия, и вы хотите убедиться, что все причины продолжающейся кровопотери (которая вызывает потерю железа) устранены.
Наиболее важные выводы по анемии у пожилых людейВот то, что, я надеюсь, вы вынесете из этой статьи:
1. Анемия — очень распространенное заболевание у пожилых людей и часто имеет несколько основных причин.
2. Анемия часто бывает хронической от легкой до средней степени тяжести; не позволяйте последующей деятельности проваливаться сквозь трещины.
3. Если у вас диагностирована анемия или вы заметили в лабораторном отчете уровень гемоглобина ниже нормы, не забудьте задать вопросы, чтобы понять вашу анемию.Вы хотите знать:
- Анемия хроническая или новая?
- Это легкая, умеренная или тяжелая форма?
- Что считается причиной? Проверялись ли вы на наличие распространенных проблем, таких как низкий уровень железа или витамина B12?
4. Если у вас низкий уровень железа: может ли это быть из-за небольшого внутреннего кровотечения и может ли это быть связано с аспирином, нестероидным противовоспалительным препаратом, таким как ибупрофен, или другим лекарством?
5. Сохраняйте копии лабораторных отчетов.
6. Убедитесь, что вы знаете, каков план, чтобы следить за анализом крови и определять причину анемии.
У вас есть вопросы по поводу анемии у пожилых людей? Пожалуйста, разместите их ниже!
Примечание. Мы получили более 200 комментариев к этому сообщению, поэтому комментарии будут закрыты. Если у вас есть вопрос, скорее всего, его уже задали и ответили. Спасибо!
Если у вас есть вопрос, скорее всего, его уже задали и ответили. Спасибо!
Вам также может быть полезно прочитать следующие статьи:
Общие сведения о лабораторных исследованиях: 10 часто используемых анализов крови для пожилых людей
Как избежать вреда от дефицита витамина B12
Эта статья была впервые опубликована в 2016 году, а незначительные обновления были внесены в ноябре 2020 года. (Основные принципы анемии у пожилых людей не сильно меняются со временем.)
Когда следует делать переливание госпитализированному пациенту?
Случай
65-летний житель дома престарелых направлен в отделение неотложной помощи с продуктивным кашлем, лихорадкой и низким кровяным давлением, и ему поставлен диагноз внебольничная пневмония. В анамнезе он злоупотреблял табаком, имел гипертонию и инсульт правой средней мозговой артерии. Его приемные лаборатории показали уровень гемоглобина 9,0 г / дл. На следующий день после госпитализации его гипотония исчезла, и он сообщает, что чувствует себя намного лучше после двух литров внутривенной жидкости и антибиотиков. Однако у него уровень гемоглобина 7,9 г / дл. Признаков кровотечения нет. Следует ли этому госпитализированному пациенту делать переливание крови?
В анамнезе он злоупотреблял табаком, имел гипертонию и инсульт правой средней мозговой артерии. Его приемные лаборатории показали уровень гемоглобина 9,0 г / дл. На следующий день после госпитализации его гипотония исчезла, и он сообщает, что чувствует себя намного лучше после двух литров внутривенной жидкости и антибиотиков. Однако у него уровень гемоглобина 7,9 г / дл. Признаков кровотечения нет. Следует ли этому госпитализированному пациенту делать переливание крови?
Обзор
Когда делать переливание эритроцитов — клинический вопрос, с которым часто сталкиваются госпиталисты.Людям с острой кровопотерей, хронической кровопотерей, анемией хронического заболевания и гемолитической анемией часто делают переливания. Госпиталистов, работающих в качестве консультантов, могут спросить, когда следует переливать крови пациентам в периоперационном периоде.
По оценкам, до 25% эритроцитов, переливаемых в США, являются неприемлемыми.1-4 Многие врачи переливают кровь, основываясь на количестве, а не на объективных результатах. Чрезмерное употребление является обычным явлением из-за широкой доступности эритроцитов, нечасто предполагаемых осложнений и необоснованного опасения неблагоприятных исходов, если пациенту не будет проведено переливание крови.
Чрезмерное употребление является обычным явлением из-за широкой доступности эритроцитов, нечасто предполагаемых осложнений и необоснованного опасения неблагоприятных исходов, если пациенту не будет проведено переливание крови.
Тахикардия, низкое кровяное давление и снижение сатурации кислорода — признаки, которые врачи могут использовать при принятии решения о переливании крови. Электрокардиографические изменения, связанные с тканевой гипоксией, могут возникать при уровне гемоглобина <5 г / дл у здоровых взрослых. Исследования показывают, что смертность и заболеваемость быстро возрастают при уровнях от <5,0 до 6,0 г / дл5. В настоящее время не существует диагностических серологических тестов для определения гипоксии тканей, которая является физиологической причиной выявления красных кровяных телец.
Переливание эритроцитов может быть терапией, спасающей жизнь; однако это не безобидное вмешательство.По оценкам, 10% трансфузионных реакций будут иметь какие-либо побочные эффекты. 6 Использование эритроцитов подвергает пациентов гемолитическим трансфузионным реакциям, инфекциям и острым травмам легких, связанным с переливанием крови.7,8 Кроме того, возникают ненужные экономические расходы и ограничиваются ресурсы. отвлечены от других пациентов.
6 Использование эритроцитов подвергает пациентов гемолитическим трансфузионным реакциям, инфекциям и острым травмам легких, связанным с переливанием крови.7,8 Кроме того, возникают ненужные экономические расходы и ограничиваются ресурсы. отвлечены от других пациентов.
Госпиталисты должны уметь описывать показания к переливанию эритроцитов и понимать доказательства за и против его использования. Врачи, которые осознают риски и преимущества использования эритроцитов, как правило, переливают меньше крови, чем менее информированные.9, 10
Обзор данных
Общие результаты: несмотря на долгую историю переливания эритроцитов, которая восходит к 1818 году, когда Джеймс Бланделл успешно спас женщину, истекающую кровью от послеродового кровотечения, накоплено мало доказательств этого. надлежащее использование. В 1980-х годах открытие вируса иммунодефицита человека вызвало опасения по поводу безопасности продуктов крови. Это стимулировало исследования и дискуссии о методах переливания эритроцитов, с растущим объемом литературы, не поддерживающей переливание для произвольного триггера, например, «правило 10/30», которое относилось к гемоглобину 10 г / дл или гематокриту 30%. .9
.9
Наблюдательные исследования вызвали озабоченность, связав заболеваемость и смертность с использованием эритроцитов. Среди 1958 хирургических пациентов, которые отказались от переливания крови по религиозным мотивам, смертность увеличилась при уровне гемоглобина <6,0 г / дл. Уровни гемоглобина выше 7,0 г / дл не показали увеличения смертности.11 Недавний всеобъемлющий обзор включал 272 596 пациентов с хирургическими вмешательствами, травмами и ОИТ в 45 обсервационных исследованиях. Обзор включал исследования с конечными точками, включая смертность, инфекции, синдром полиорганной дисфункции и синдром острого респираторного дистресса, и пришел к выводу, что переливание крови связано с более высоким риском заболеваемости и смертности.12 (см. Рис. 1, стр. 20)
Более высокая частота инфекций, связанных с переливаниями крови, наблюдалась у пациентов с послеоперационной травмой, острыми травмами, раком желудочно-кишечного тракта, перенесшими операцию, операцией коронарного шунтирования, хирургическим вмешательством на бедре, ожогами, критическими заболеваниями и пациентами. требующие вентиляции. (см. рис. 2, стр. 21) 12 Повышенный риск инфицирования, вероятно, связан с временным угнетением иммунной системы, вызванным переливанием эритроцитов. Длительное пребывание в больнице пациентов после операции колоректальной хирургии и пациентов интенсивной терапии было связано с переливаниями.13
требующие вентиляции. (см. рис. 2, стр. 21) 12 Повышенный риск инфицирования, вероятно, связан с временным угнетением иммунной системы, вызванным переливанием эритроцитов. Длительное пребывание в больнице пациентов после операции колоректальной хирургии и пациентов интенсивной терапии было связано с переливаниями.13
Метаанализ нескольких рандомизированных контролируемых исследований свидетельствует в пользу ограниченного использования эритроцитов. Преобладающее количество доказательств получено в исследовании «Требования к переливанию крови в критических состояниях» (TRICC) 14. Это рандомизированное контрольное испытание с участием критически больных терапевтических и хирургических пациентов продемонстрировало ограничительную стратегию (триггер переливания <7,0 г / дл) и было столь же эффективным, как и либеральная стратегия переливания (триггер переливания <10,0 г / дл). (см. рис. 3, стр. 22). Действительно, пациенты в ограничительной группе исследования, которые были менее больны и моложе 55 лет, имели более низкий уровень смертности, чем те, кому переливали обильно. 15 На сегодняшний день не существует рандомизированных контрольных исследований на базе больниц, оценивающих исходы у пациентов с анемией, не получающих ОИТ.
15 На сегодняшний день не существует рандомизированных контрольных исследований на базе больниц, оценивающих исходы у пациентов с анемией, не получающих ОИТ.
Эти данные привели к растущему консенсусу в отношении того, что ограниченное использование крови приводит к улучшению результатов лечения пациентов. У пациентов без сердечно-сосудистых заболеваний данные свидетельствуют о том, что большинство пациентов переносят уровень гемоглобина 7,0 г / дл 5
Кардиологические пациенты
Экспериментальные и клинические данные свидетельствуют о том, что пациенты с сердечно-сосудистыми заболеваниями менее терпимы к анемии.Пациенты с ишемической болезнью сердца с большей вероятностью будут иметь неблагоприятные исходы, чем пациенты без коронарной болезни, если им не будет проведено переливание эритроцитов.11,16
Миокард имеет более высокий коэффициент экстракции кислорода по сравнению с коэффициентом экстракции кислорода тканями, что делает он более чувствителен к анемии. 17,18 При наличии сердечного заболевания может потребоваться более высокий порог для переливания крови; однако точный рекомендуемый порог остается спорным. Ограничительная стратегия переливания эритроцитов (поддержание гемоглобина в пределах 7.0 г / дл и 9,0 г / дл) оказались безопасными для большинства тяжелобольных пациентов с сердечно-сосудистыми заболеваниями.14
17,18 При наличии сердечного заболевания может потребоваться более высокий порог для переливания крови; однако точный рекомендуемый порог остается спорным. Ограничительная стратегия переливания эритроцитов (поддержание гемоглобина в пределах 7.0 г / дл и 9,0 г / дл) оказались безопасными для большинства тяжелобольных пациентов с сердечно-сосудистыми заболеваниями.14
Данные более противоречивы для пациентов с острым коронарным синдромом (ОКС). В некоторых исследованиях была обнаружена повышенная смертность, а в другом — снижение ОКС при использовании эритроцитов.19–21. Необходимы дальнейшие исследования, чтобы определить, когда следует давать эритроциты пациентам с коронарной болезнью.
Желудочно-кишечное кровотечение
Решение о переливании крови при желудочно-кишечном кровотечении принимает во внимание место и этиологию кровотечения, доступность лечения и риск продолжения кровотечения.После того, как кровопотеря будет контролироваться, необходимо принять решение о том, как лечить анемию. В настоящее время нет исследований, посвященных изучению исходов для пациентов, которые получали и не получали кровь при остром или хроническом желудочно-кишечном кровотечении.
В настоящее время нет исследований, посвященных изучению исходов для пациентов, которые получали и не получали кровь при остром или хроническом желудочно-кишечном кровотечении.
Кроме того, не проводилось исследований, чтобы определить, когда следует переливать кровь пациентам с хронической кровопотерей ЖКТ. Исследования пациентов с острым желудочно-кишечным кровотечением и сердечно-сосудистыми заболеваниями показали увеличение смертности, но неизвестно, влияет ли использование конкретных триггеров переливания крови на исходы в этой группе.
Эксперты считают, что при использовании эритроцитов у пациентов с желудочно-кишечным кровотечением следует руководствоваться имеющимися данными. Пациентам без сердечных заболеваний переливание эритроцитов требуется редко после окончательного лечения и прекращения кровопотери, за исключением случаев, когда гемоглобин <7,0 г / дл 22
Назад к случаю
Пациенту, описанному в нашем случае, переливать нельзя если у него нет клинических признаков или симптомов тканевой гипоксемии. Следует начать соответствующее обследование его анемии и, если выявлена этиология, применить окончательное лечение или вмешательство.
Следует начать соответствующее обследование его анемии и, если выявлена этиология, применить окончательное лечение или вмешательство.
Bottom Line
Если нет клинических признаков тканевой гипоксии, симптоматической анемии или гемоглобина <7,0 г / дл, переливание эритроцитов не рекомендуется, если у пациента нет активного ОКС или серьезного основного коронарного заболевания. TH
Д-р Дресслер — заместитель директора программы, доцент медицины, Отделение общей внутренней медицины, Университетская больница Эмори, Атланта. Д-р ВандерЭнде — доцент медицины отделения общей внутренней медицины больницы Университета Эмори, Атланта.
Ссылки
1. Велч Х.Г., Михан К.Р., Гудноу ЛТ. Разумные стратегии планового переливания эритроцитов. Ann Intern Med. 1992; 116 (5): 393-402.
2. Тарттер П.И., Бэррон Д.М. Ненужные переливания крови при плановой хирургии колоректального рака. Переливание. 1985; 25 (2): 113-115.
3. Саксена С., Вайнер Дж. М., Рабинович А., Фрайди Дж., Шульман И. А., Кармель Р. Практика переливания крови у медицинских пациентов. Arch Int Med. 1993; 153 (22): 2575-80.
М., Рабинович А., Фрайди Дж., Шульман И. А., Кармель Р. Практика переливания крови у медицинских пациентов. Arch Int Med. 1993; 153 (22): 2575-80.
4.Палермо Дж., Бове Дж., Кац А. Дж.. Образцы использования крови в Коннектикуте. Переливание. 1980; 20 (6): 704-710.
5. Карсон Дж. Л., Рейнольдс Р. К.. В поисках порога переливания. Гематология. 2005; 10 (Приложение 1): 86-88.
6. Уокер РХ. Специальный отчет: риски переливания крови. Am J Clin Pathol. 1987; 88 (3): 374-378.
7. Блайхман М.А., Вамвакас ЕС. Сохраняющийся риск инфекций, передаваемых при переливании крови. N Engl J Med. 2006; 355 (13): 1303-1305.
8. Spiess BD. Риски переливания: нацеленность на результат.Переливание. 2004; 44 (Дополнение 12): 4С-14С.
9. Салем-Шац С.Р., Аворн Дж., Сумераи С.Б. Влияние клинических знаний, организационного контекста и стиля практики на принятие решения о переливании крови. ДЖАМА. 1990; 264 (4): 476-483.
10. Уилсон К., МакДугалл Л., Фергюссон Д. , Грэм И., Тинмут А., Хеберт П.С. Эффективность вмешательств, направленных на снижение количества случаев несоответствующего переливания крови врачом: что можно узнать из систематического обзора литературы. Переливание. 2002; 42 (9): 1224-1229.
, Грэм И., Тинмут А., Хеберт П.С. Эффективность вмешательств, направленных на снижение количества случаев несоответствующего переливания крови врачом: что можно узнать из систематического обзора литературы. Переливание. 2002; 42 (9): 1224-1229.
11. Карсон Дж. Л., Дафф А., Позес Р. М. и др. Влияние анемии и сердечно-сосудистых заболеваний на хирургическую смертность и заболеваемость. Ланцет. 1996; 348 (9034): 1055-1060.
12. Marik PE, Corwin HL. Эффективность переливания эритроцитов в критических состояниях: систематический обзор литературы. Crit Care Med. 2008; 36 (9): 2667-2674.
13. Рагхаван М, Марик ЧП. Анемия, переливание аллогенной крови и иммуномодуляция у тяжелобольных. Грудь. 2005; 127 (1): 295-307.
14.Hebert PC, Wells G, Blajchman MA и др. Многоцентровое рандомизированное контролируемое клиническое исследование требований к переливанию крови в отделениях интенсивной терапии. Требования к переливанию крови у исследователей интенсивной терапии, канадская группа исследований в области интенсивной терапии. N Engl J Med. 1999; 340 (6): 409-417.
N Engl J Med. 1999; 340 (6): 409-417.
15. Карсон Дж. Л., Хилл С., Карлесс П., Хеберт П., Генри Д. Триггеры для переливания крови: систематический обзор литературы. Transfus Med Rev.2002; 16 (3): 187-199.
16. Сабатин М.С., Морроу Д.А., Джульяно Р.П. и др. Связь уровня гемоглобина с клиническими исходами при острых коронарных синдромах.Тираж. 2005; 111 (16): 2042-2049.
17. Ян К.М., Чиен С. Влияние вариаций гематокрита на коронарную гемодинамику и использование кислорода. Am J Physiol. 1977; 233 (1): h206-h213.
18. Вилдерсон Д.К. РАСЛ, Гулд С.А., Сегал Х.Л., Мосс Г.С. Пределы сердечной компенсации у анемичных павианов. Операция. 1988; 103 (6): 665-670.
19. Рао С.В., Джоллис Дж. Г., Харрингтон Р.А. и др. Взаимосвязь переливания крови и клинических исходов у пациентов с острыми коронарными синдромами. ДЖАМА. 2004; 292 (13): 1555-1562.
20. Wu WC, Rathore SS, Wang Y, Radford MJ, Krumholz HM. Переливание крови пациентам пожилого возраста с острым инфарктом миокарда. N Engl J Med. 2001; 345 (17): 1230-1236.
N Engl J Med. 2001; 345 (17): 1230-1236.
21. Hebert PC, Fergusson DA. Доходит ли до сути дела переливание крови? ДЖАМА. 2004; 292 (13): 1610-1612.
22. Херншоу С., Трэвис С., Мерфи М. Роль переливания крови в лечении кровотечений из верхних и нижних отделов кишечника. Лучшая практика Res Clin Gastroenterology. 2008; 22 (2): 355-371.
Анемия у пожилых людей — AgingCare.com
Анемия у пожилых людей может быть вызвана множеством факторов, например хроническими заболеваниями, дефицитом железа, дефицитом витамина B12 и кровотечениями. Хотя это может показаться не серьезной проблемой для здоровья, исследования показали, что пожилые люди с анемией с большей вероятностью потеряют физические способности, испытают функциональное снижение, будут госпитализированы и помещены в дома престарелых по сравнению с пожилыми людьми без этого заболевания. Даже пограничная анемия может способствовать этим результатам для здоровья, поэтому для лиц, осуществляющих уход, важно знать признаки и симптомы, чтобы обеспечить ее своевременное обнаружение и лечение.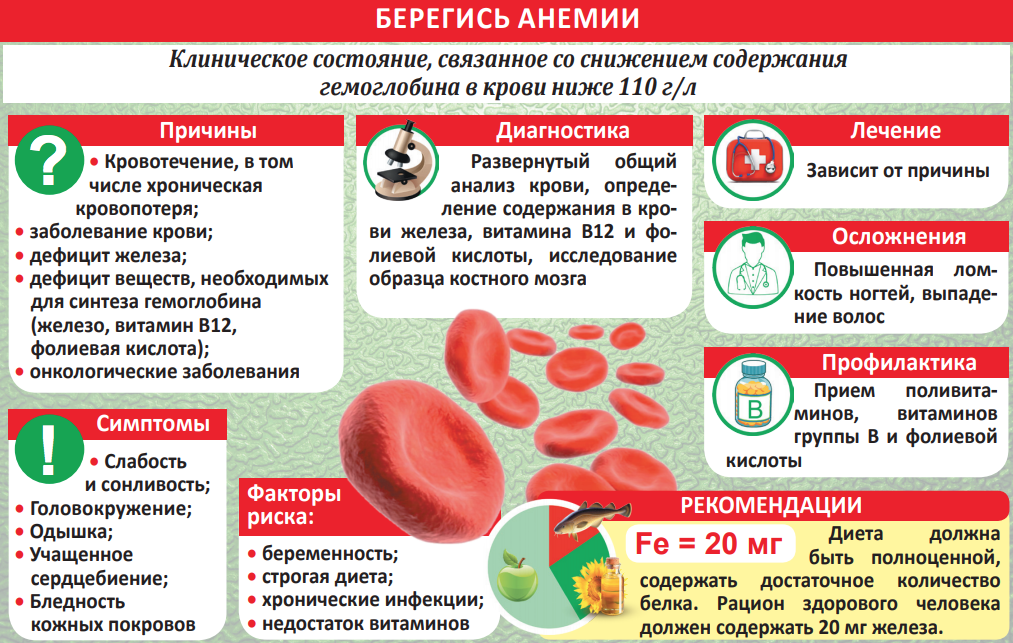
Что такое анемия?
Когда человек страдает анемией, количество эритроцитов в крови или количество гемоглобина в этих клетках ниже, чем должно быть. Анемия может возникнуть из-за потери крови, недостаточного или неправильного производства эритроцитов (эритроцитов) или разрушения этих клеток. Это состояние диагностируется путем измерения количества каждого из них с помощью простого анализа крови.
«Гемоглобин — это белок в эритроцитах, который переносит кислород во все ткани тела, что делает его важным компонентом здоровья и жизни», — объясняет Кэрол Элдридж, DNP, RN, CNE, NEA-BC, вице-президент Post- Лицензирование и программы последипломного образования в Медицинском колледже Чемберлена.«Если уровень гемоглобина ниже 12 граммов на децилитр крови у женщины или 13,5 граммов на децилитр у мужчины, этот человек может быть назван страдающим анемией».
Признаки анемии
Когда пожилые люди замечают, что они устали или становятся немного слабее, чем раньше, они часто связывают это с общим старением. Элдридж говорит, что это предположение иногда верно, но общие симптомы «старости», такие как усталость, слабость, головокружение, раздражительность, бледность кожи и одышка, часто указывают на более серьезные (и поддающиеся лечению) заболевания.«Эти признаки всегда должны указывать на то, что близкий человек должен пройти обследование у поставщика медицинских услуг», — утверждает она.
Элдридж говорит, что это предположение иногда верно, но общие симптомы «старости», такие как усталость, слабость, головокружение, раздражительность, бледность кожи и одышка, часто указывают на более серьезные (и поддающиеся лечению) заболевания.«Эти признаки всегда должны указывать на то, что близкий человек должен пройти обследование у поставщика медицинских услуг», — утверждает она.
Причины анемии
Анемия может быть острой с внезапным и тяжелым началом или хронической, медленно развивающейся в течение длительного периода времени. Разница в начале болезни может пролить свет на причину анемии, а также помогает определить, какой курс лечения будет наиболее эффективным. В некоторых случаях явную причину невозможно найти, но даже в этом случае анемию можно вылечить с хорошими результатами.
По данным Американского общества гематологов, примерно 10 процентов американцев старше 65 лет страдают анемией. Двумя наиболее частыми причинами являются хронические заболевания (такие как язвы, заболевание печени или почек, гипотиреоз, воспаление желудка или кишечника и рак) и дефицит железа. Дефицит витамина B12 или фолиевой кислоты встречается не так часто.
Дефицит витамина B12 или фолиевой кислоты встречается не так часто.
Некоторые лекарства также могут способствовать развитию анемии. Это особенно верно для пожилых людей, которые обычно принимают несколько рецептов.«Многие лекарства могут иметь синергетический эффект и вызывать побочные эффекты, которые сильнее влияют на организм», — говорит Элдридж. Примеры этих лекарств включают ингибиторы АПФ, блокаторы рецепторов ангиотензина (БРА), а также некоторые антибиотики и противосудорожные средства. Лечение рака, такое как лучевая терапия и химиотерапия, также может повредить костный мозг, где образуются эритроциты. «Полезно рассматривать анемию как симптом другого основного заболевания, а не как основную проблему», — советует Элдридж.
Просмотрите наши бесплатные
Руководства по уходу за пожилыми людьми
Железодефицитная анемия
Хотя они являются менее распространенными причинами анемии у пожилых людей, дефицит железа, витамина B12 и фолиевой кислоты можно легко выявить и лечить. «Решение проблем с питанием может существенно повлиять на самочувствие и функционирование пожилых людей и может предотвратить потерю физических способностей, которая может привести к госпитализации или помещению в дом престарелых», — считает Элдридж.Для диагностики этих недостатков используются простые анализы крови, а затем обычно назначаются диетические добавки.
«Решение проблем с питанием может существенно повлиять на самочувствие и функционирование пожилых людей и может предотвратить потерю физических способностей, которая может привести к госпитализации или помещению в дом престарелых», — считает Элдридж.Для диагностики этих недостатков используются простые анализы крови, а затем обычно назначаются диетические добавки.
Низкое содержание железа — наиболее известная причина анемии, но обычно она поражает людей более молодого возраста. Элдридж утверждает, что когда это происходит у пожилых людей, это обычно связано с ограниченным всасыванием железа в кишечнике или желудочно-кишечным кровотечением. «Кому-то с железодефицитной анемией могут быть прописаны добавки железа, и очень важно следовать инструкциям врача относительно добавок», — призывает она.Чрезмерное потребление железа может вызвать рвоту, диарею, головную боль, раздражительность, усталость и даже повреждение сердца и суставов. Даже в правильных дозах добавки железа могут вызывать запор, тошноту, диарею и боль в желудке.
Эти побочные эффекты можно уменьшить, если принимать таблетки во время еды. Добавки железа и кальция не следует принимать вместе, так как кальций мешает усвоению железа. Добавки железа с замедленным высвобождением обычно не рекомендуются, потому что лучше всего всасывается в верхних отделах пищеварительного тракта.Прием этих таблеток с небольшим количеством апельсинового сока или в сочетании с добавкой витамина С также может способствовать усвоению. Еще одно простое решение — добавить в рацион любимого человека больше продуктов, богатых железом. Красное мясо, яичные желтки, орехи, морепродукты, бобы и цельнозерновые продукты — все это здоровые источники этого минерала.
Пожилые люди иногда теряют способность усваивать витамин B12 из пищи. Недостаток витамина B12 можно лечить пероральными добавками, но Элдридж говорит, что инъекции обычно являются наиболее эффективным лечением.Чтобы увеличить количество этого витамина в рационе, пожилые люди должны есть говядину, птицу, рыбу, печень, устриц, моллюсков, молоко, сыр и яйца.
С дефицитом фолиевой кислоты можно справиться с помощью диеты, включающей большое количество сырых или слегка приготовленных зеленых, листовых овощей, крестоцветных овощей (брокколи, брюссельская капуста и цветная капуста), свежих фруктов, молочных продуктов и цельнозерновых продуктов. Врач может прописать добавку фолиевой кислоты, которая представляет собой одну из форм фолиевой кислоты.
Лечение анемии, вызванной хроническими заболеваниями
Если анемия вызвана хроническим заболеванием, естественно, лучше всего лечить основное заболевание.Это также известно как «анемия хронического заболевания» или ACD. Пациенты с ACD часто имеют в организме достаточное количество железа и питательных веществ, но они не используются эффективно для образования новых красных кровяных телец. «Хотя причина этого нарушения способности использовать железо неизвестна, некоторые эксперты считают, что оно является частью иммунного ответа организма, направленного на предотвращение роста бактерий и дальнейшего вреда», — предполагает Элдридж. «Это одна из причин, почему добавки железа не являются эффективным средством лечения ACD».
«Это одна из причин, почему добавки железа не являются эффективным средством лечения ACD».
Инфекции, воспаления, гормональный дисбаланс и злокачественные новообразования — это несколько основных причин ACD.Другие условия также могут быть виноваты. «Хроническая болезнь почек — один из конкретных примеров, и существуют полезные лекарства, которые стимулируют костный мозг производить больше красных кровяных телец», — предполагает Элдридж. Конкретные методы лечения полностью зависят от общего состояния здоровья человека и сопутствующих заболеваний.
Существуют и другие формы анемии, которые встречаются реже и требуют серьезного медицинского вмешательства. Лечение может включать стероиды, переливание крови или даже операцию по удалению увеличенной селезенки или восстановлению аномальных кровеносных сосудов, опухолей или сердечных клапанов.
«Ключом к борьбе с анемией всегда является обнаружение первопричины, когда это возможно, а затем работа с поставщиком медицинских услуг для лечения как причины, так и симптомов», — рекомендует Элдридж.
При каком уровне гемоглобина запускается переливание крови?
Бхананкер С.М., Рамайя Р. Тенденции переливания травм. Инт Дж. Крит. Илл. Ин. Науч. . 2011 января 1 (1): 51-6. [Медлайн]. [Полный текст].
Поповский М.С., Мур С.Б. Диагностические и патогенетические аспекты острого повреждения легких, связанного с переливанием крови. Переливание крови . 1985 ноябрь-декабрь. 25: 573-577. [Медлайн].
[Рекомендации] Carson JL, Guyatt G, Heddle NM, Grossman BJ, Cohn CS, Fung MK, et al. Рекомендации по клинической практике от AABB: Пороги переливания эритроцитов и их хранение. ЯМА . 2016 15 ноября. 316 (19): 2025-2035. [Медлайн].
Shander A, Goodnough LT. Цели и ограничения бескровной медицинской помощи. Curr Opin Hematol . 2006 ноябрь 13: 462-470.[Медлайн].
2006 ноябрь 13: 462-470.[Медлайн].
Carson JL, Noveck H, Berlin JA, Gould SA. Смертность и заболеваемость у пациентов с очень низким послеоперационным уровнем гемоглобина, которым отказывают в переливании крови. Переливание крови . 2002 июл.42 (7): 812-8. [Медлайн].
Целевая группа Американского общества анестезиологов по периоперационному контролю крови. Практические рекомендации по периоперационному контролю крови: обновленный отчет Целевой группы Американского общества анестезиологов по периоперационному контролю крови *. Анестезиология . 2015 Февраль 122 (2): 241-75. [Медлайн].
Коднер П., Цинат М. При травмах уместно массивное переливание крови. TraumaCare . 2005. 15 (3): 148-152.
Carson JL, Stanworth SJ, Roubinian N, Fergusson DA, Triulzi D, Doree C и др. Пороги переливания и другие стратегии для руководства переливанием аллогенных эритроцитов. Кокрановская база данных Syst Rev . 2016, 12 октября: CD002042. [Медлайн].
Пороги переливания и другие стратегии для руководства переливанием аллогенных эритроцитов. Кокрановская база данных Syst Rev . 2016, 12 октября: CD002042. [Медлайн].
Lustenberger T, Frischknecht A, Brüesch M, Keel MJ. Соотношения компонентов крови у пациентов с массивными переливаниями и тупыми травмами — ковариативный анализ, зависящий от времени. Дж. Травма . 2011 ноябрь 71 (5): 1144-51. [Медлайн].
van de Watering LMG, Hermans J, Houbiers JGA, et al. Положительное влияние истощения лейкоцитов в перелитой крови на послеоперационные осложнения у пациентов, перенесших кардиохирургические операции: рандомизированное клиническое исследование. Тираж . 1998. 97: 562-568.
Холкомб Дж. Б., Дженкинс Д., Ри П., Йоханнигман Дж., Махони П., Мехта С. и др. Реанимация для контроля повреждений: прямое лечение ранней коагулопатии травмы. Дж. Травма . 2007 февраль 62: 307-310. [Медлайн].
Дж. Травма . 2007 февраль 62: 307-310. [Медлайн].
Шах А., Стэнворт С.Дж., МакКечни С. Доказательства и триггеры переливания крови и продуктов крови. Анестезия . 2015, январь 70, Приложение 1: 10-9, e3-5. [Медлайн].
Pybus S, MacCormac A, Houghton A, Martlew V, Thachil J. Несоответствие свежезамороженной плазмы для тестов на аномальную коагуляцию. J R Coll Врачи Edinb . 2012. 42 (4): 294-300. [Медлайн].
Müller MC, Arbous MS, Spoelstra-de Man AM, Vink R, Karakus A, Straat M и др. Переливание свежезамороженной плазмы тяжелобольным пациентам с коагулопатией перед инвазивными процедурами: рандомизированное клиническое испытание (CME). Переливание крови .2015, январь, 55 (1): 26–35; викторина 25. [Medline].
Leissinger CA, Blatt PM, Hoots WK, Ewenstein B. Роль концентратов протромбинового комплекса в обращении антикоагуляции варфарина: обзор литературы. Ам Дж. Гематол . 2008 Февраль 83 (2): 137-43. [Медлайн].
Роль концентратов протромбинового комплекса в обращении антикоагуляции варфарина: обзор литературы. Ам Дж. Гематол . 2008 Февраль 83 (2): 137-43. [Медлайн].
Tran HA, Chunilal SD, Harper PL, Tran H, Wood EM, Gallus AS, et al. Обновление согласованных рекомендаций по отмене варфарина. Med J Aust . 2013 4 марта 198 (4): 198-9.[Медлайн].
Целлер М.П., Аль-Хабси К.С., Хеддл, штат Нью-Мексико. Профилактические переливания тромбоцитов: должны ли они остаться в прошлом? Curr Opin Hematol . 2014 21 ноября (6): 521-7. [Медлайн].
Сквайрс Дж. Э. Показания к переливанию тромбоцитов у больных тромбоцитопенией. Переливание крови . 2015 Апрель 13 (2): 221-6. [Медлайн].
Crighton GL, Estcourt LJ, Wood EM, Trivella M, Doree C, Stanworth S. Стратегия трансфузии тромбоцитов только для лечения по сравнению с профилактической для предотвращения кровотечений у пациентов с гематологическими нарушениями после миелосупрессивной химиотерапии или трансплантации стволовых клеток. Кокрановская база данных Syst Rev . 2015 30 сентября. CD010981. [Медлайн].
Стратегия трансфузии тромбоцитов только для лечения по сравнению с профилактической для предотвращения кровотечений у пациентов с гематологическими нарушениями после миелосупрессивной химиотерапии или трансплантации стволовых клеток. Кокрановская база данных Syst Rev . 2015 30 сентября. CD010981. [Медлайн].
Llewelyn CA, Hewitt PE, Knight RS, Amar K, Cousens S, Mackenzie J, et al. Возможная передача варианта болезни Крейтцфельда-Якоба при переливании крови. Ланцет . 2004 г. 7 февраля.363: 417-421. [Медлайн].
Даути HA, Woolley T, Thomas GO. Массовое переливание. JR Армейский медицинский корпус . 2011 сентябрь 157 (3 приложение 1): S277-83. [Медлайн].
Карлесс PA, Генри Д.А., Мокси А.Дж., О’Коннелл Д.Л., Браун Т., Фергюссон Д.А. Спасение клеток для минимизации периоперационных переливаний аллогенной крови. Кокрановская база данных систематических обзоров . 18 октября 2006 г. 4: CD001888: [Medline].
Кокрановская база данных систематических обзоров . 18 октября 2006 г. 4: CD001888: [Medline].
Hillyer CD, Lankford KV, Roback JD, Gillespie TW, Silberstein LE.Переливание ВИЧ-серопозитивному пациенту: иммуномодуляция, вирусная реактивация и ограничение воздействия EBV (HHV-4), CMV (HHV-5) и HHV-6, 7 и 8. Transfus Med Rev . 1999, 13 января: 1-17. [Медлайн].
Гилл Р. Практическое ведение большой кровопотери. Анестезия . 2015, январь 70, Приложение 1: 54-7, e19-20. [Медлайн].
Nunez TC, Voskresensky IV, Dossett LA, Shinall R, Dutton WD, Cotton BA. Раннее предсказание массивного переливания крови при травме: просто как ABC (оценка потребления крови) ?. Дж. Травма . 2009 Февраль 66 (2): 346-52. [Медлайн].
Cotton BA, Dossett LA, Haut ER, Shafi S, Nunez TC, Au BK, et al. Многоцентровая проверка упрощенной оценки для прогнозирования массивного переливания крови при травме. Дж. Травма . 2010 июл.69 Приложение 1: S33-9. [Медлайн].
Многоцентровая проверка упрощенной оценки для прогнозирования массивного переливания крови при травме. Дж. Травма . 2010 июл.69 Приложение 1: S33-9. [Медлайн].
Holcomb JB, del Junco DJ, Fox EE, Wade CE, Cohen MJ, Schreiber MA и др. Проспективное обсервационное многоцентровое исследование переливания больших травм (PROMMTT): сравнительная эффективность меняющегося во времени лечения с конкурирующими рисками. JAMA Surg . 2013 Февраль 148 (2): 127-36. [Медлайн].
Holcomb JB, Tilley BC, Baraniuk S, et al. Переливание плазмы, тромбоцитов и эритроцитов в соотношении 1: 1: 1 против 1: 1: 2 и смертность у пациентов с тяжелой травмой: рандомизированное клиническое исследование PROPPR. ЯМА . 2015 г. 3 февраля. 313 (5): 471-82. [Медлайн].
Blajchman MA. Клинические преимущества лейкоредукции продуктов крови. Дж. Травма .2006. 60: S83-S90.
Дж. Травма .2006. 60: S83-S90.
Боффард К.Д., Риу Б., Уоррен Б., Чунг П.И., Ризоли С., Россент Р. и др. Рекомбинантный фактор VIIa в качестве дополнительной терапии для контроля кровотечения у пациентов с тяжелыми травмами: два параллельных рандомизированных плацебо-контролируемых двойных слепых клинических испытания. Дж. Травма . 2005 Июль 59: 8-15. [Медлайн].
Goodnough LT, Shander A, Spence R. Бескровная медицина: клиническая помощь без переливания аллогенной крови. Переливание крови .2003 май. 43: 668-676. [Медлайн].
Силлиман СС. Двухэтапная модель острого повреждения легких, связанного с переливанием крови. Crit Care Med . 2006 май. 34: S124-S131. [Медлайн].
Hauser CJ, Boffard K, Dutton R, Bernard GR, Croce MA, Holcomb JB и др. Результаты исследования CONTROL: эффективность и безопасность рекомбинантного активированного фактора VII в лечении рефрактерного травматического кровотечения. Дж. Травма . 2010 сентябрь 69 (3): 489-500.[Медлайн].
Результаты исследования CONTROL: эффективность и безопасность рекомбинантного активированного фактора VII в лечении рефрактерного травматического кровотечения. Дж. Травма . 2010 сентябрь 69 (3): 489-500.[Медлайн].
Робертс И., Шакур Х., Коутс Т., Хант Б., Балогун Е., Барнетсон Л. и др. Исследование CRASH-2: рандомизированное контролируемое исследование и экономическая оценка влияния транексамовой кислоты на смерть, сосудистые окклюзионные события и потребность в переливании крови у пациентов с кровотечением и травмой. Оценка медицинских технологий . 2013 17 марта (10): 1-79. [Медлайн].
Моррисон Дж. Дж., Дубоз Дж. Дж., Расмуссен Т. Э., Середина зимы MJ. Военное применение транексамовой кислоты в исследовании неотложной реанимации после травм. Арка Сург . 2012 Февраль 147 (2): 113-9. [Медлайн].
Наполитано Л.М., Коэн М.Дж., Коттон Б.А., Шрайбер М.А., Мур Э. Транексамовая кислота при травмах: как ее использовать ?. J Хирург для неотложной помощи при травмах . 2013 июнь 74 (6): 1575-86. [Медлайн].
Рамирес RJ, Spinella PC, Bochicchio GV. Обновление транексамовой кислоты при травмах. Клиника интенсивной терапии . 2017 января 33 (1): 85-99. [Медлайн].
Английский SW, Макинтайр Л.Анемия и переливание эритроцитов. Винсент Дж. Л., Абрахам Э., Мур Ф. А., Кочанек П. М., Финк МП. Учебник интенсивной терапии . 7-е изд. Филадельфия: Эльзевьер; 2017. 958-963.
Callum JL, Pinkerton PH, Lima A, et al. Bloody Easy 4: Переливание крови, альтернативы крови и реакции на переливание — руководство по трансфузионной медицине . 4-е изд. Региональная координационная сеть по крови Онтарио; 2016.
Книппен МА. Острое повреждение легких, связанное с переливанием крови. AJN . 2006 июн.106 (6): 61-64. [Медлайн].
Opelz G, Sengar DP, Mickey MR, Terasaki PI. Влияние переливания крови на последующую трансплантацию почек. Протокол трансплантологии . 1973. 5: 253-259. [Медлайн].
Корвин Х.Л., Геттингер А., Перл Р.Г., Финк М.П., Леви М.М., Абрахам Э. и др. Исследование CRIT: Анемия и переливание крови у тяжелобольных — Текущая клиническая практика в Соединенных Штатах. Crit Care Med .2004. 32 (1): 39-52. [Медлайн].
Сегал Дж. Б., Бласко-Кольменарес Э., Норрис Э. Дж., Гуаллар Э. Предоперационная острая нормоволемическая гемодилюция: метаанализ. Переливание крови . 2004 Май. 44: 632-644. [Медлайн].
Gajic O, Gropper MA, Hubmayr RD. Отек легких после переливания: как отличить перегрузку кровообращения, связанную с переливанием крови, от острого повреждения легких, связанного с переливанием крови. Crit Care Med . 2006 май. 34: S109-S113.[Медлайн].
Monk TG, Goodnough LT, Brecher ME, Colberg JW, Andriole GL, Catalona WJ. Проспективное рандомизированное сравнение трех стратегий сохранения крови при радикальной простатэктомии. Анестезиология . 1999 Июль 91: 24-33. [Медлайн].
Toy P, Gajic O, Bacchetti P, et al. Острое повреждение легких, связанное с переливанием крови: частота возникновения и факторы риска. Кровь . 2012 16 февраля. 119 (7): 1757-67. [Медлайн].
Lin Y, Saw CL, Hannach B, Goldman M.Меры по профилактике острого повреждения легких, связанного с переливанием крови, и их влияние в Службе крови Канады. Переливание крови . 2012 Март 52 (3): 567-74. [Медлайн].
Эллисон Дж., Фини С. Успешное применение полимеризованного кровезаменителя гемоглобина у критически анемичного Свидетеля Иеговы. Саут Мед Дж. . 2004 Декабрь 97: 1257-1258. [Медлайн].
Hebert PC, Wells G, Blajchman MA, Marshall J, Martin C, Pagliarello G и др.Многоцентровое рандомизированное контролируемое клиническое исследование требований к переливанию крови в отделениях интенсивной терапии. N Engl J Med . 1999 11 февраля. 340: 409-417. [Медлайн].
Heiss MM, Mempel W, Delanoff C, Jauch KW, Gabka C, Mempel M и др. Рецидив опухоли, модулированный переливанием крови: первые результаты рандомизированного исследования аутологичного и аллогенного переливания крови в хирургии колоректального рака. Дж. Клин Онкол . 1994, 12 сентября: 1859-1867. [Медлайн].
Дженсен Л.С., Андерсен А.Дж., Кристиансен П.М., Хокланд П., Юл СО, Мэдсен Г. и др.Послеоперационная инфекция и функция естественных клеток-киллеров после переливания крови у пациентов, перенесших плановую колоректальную операцию. Br J Surg . 1992 июн. 79: 513-516. [Медлайн].
Sturm B, Laggner H, Ternes N, Goldenberg H, Scheiber-Mojdehkar B. Внутривенные препараты железа и аскорбиновая кислота: влияние на хелатируемое и биодоступное железо. Почки Инт . 2005 г., 67: 1161-1170. [Медлайн].
Vamvakas EC.Пневмония как осложнение переливания продуктов крови у тяжелобольных: иммуномодуляция, связанная с переливанием крови (TRIM). Crit Care Med . 2006 май. 34: S151-S159. [Медлайн].
Тарттер П.И., Мохандас К., Азар П., Эндрес Дж., Каплан Дж., Спивак М. Рандомизированное исследование, сравнивающее переливание эритроцитарной крови с и без истощения лейкоцитов для хирургии желудочно-кишечного тракта. Am J Surg . 1998 ноябрь 176: 462-466. [Медлайн].
Rohde JM, Dimcheff DE, Blumberg N, Saint S, Langa KM, Kuhn L, et al.Инфекция, связанная с оказанием медицинской помощи, после переливания эритроцитов: систематический обзор и метаанализ. ЯМА . 2014 апр. 2, 311 (13): 1317-26. [Медлайн].
Holst LB, Petersen MW, Haase N, Perner A, Wetterslev J. Ограничительная или либеральная стратегия переливания для переливания эритроцитов: систематический обзор рандомизированных испытаний с метаанализом и последовательным анализом испытаний. BMJ . 2015 24 марта. 350: h2354. [Медлайн].
Педен А.Х., глава МВД, Ричи Д.Л., Белл Д.Е., Айронсайд Д.В.Доклиническая vCJD после переливания крови у пациента, гетерозиготного по PRNP-кодону 129. Ланцет . 2004 7-13 августа. 364: 527-529. [Медлайн].
Hess JR, Lawson JH. Коагулопатия травмы в сравнении с диссеминированным внутрисосудистым свертыванием. Дж. Травма . 2006 июнь 60: S12-S19. [Медлайн].
Росс С.Д., Аллен И.Е., Генри Д.Х., моряк С, Серкус Б., Гудноу ЛТ. Клинические преимущества и риски, связанные с эпоэтином и дарбэпоэтином у пациентов с анемией, вызванной химиотерапией: систематический обзор литературы. Клин Тер . 2006 июн. 28: 801-831. [Медлайн].
Мур Б. Острое повреждение легких, связанное с переливанием крови (TRALI): Клиническая картина, лечение и прогноз. Crit Care Med . 2006. 34: S114-S117.
Isbister JP. Терапия компонентами крови. Винсент Дж. Л., Абрахам Э., Мур Ф. А., Кочанек П. М., Финк МП. Учебник интенсивной терапии . 7-е изд. Филадельфия: Эльзевьер; 2017. 964-970.
Амато А, Пескатори М.Периоперационные переливания крови при рецидиве колоректального рака. Кокрановская база данных систематических обзоров . 2006. 1: CD005033:
Билгин YM, ван де Уотеринг LM, Eijsman L, Versteegh MI, Brand R, van Oers MH, et al. Двойное слепое рандомизированное контролируемое исследование эффекта переливания эритроцитов с пониженным содержанием лейкоцитов в хирургии сердечного клапана. Тираж . 2004 8 июня. 109: 2755-2760. [Медлайн].
Goodnough LT, Леви JH, Мерфи MF.Представления о переливании крови у взрослых. Ланцет . 2013 25 мая. 381 (9880): 1845-54. [Медлайн].
Мартин В., Фермер С.Л., Рен М.Н., Таулер С.К., Бетта Дж., Шандер А. и др. Теория и практика бескровной хирургии. Transfus Apheresis Sci . 2002, 27 августа: 29-43. [Медлайн].
Сауайя А., Мур Ф.А., Мур Е.Э., Хенель Дж. Б., Рид Р.А., Лезотт, округ Колумбия. Ранние предикторы полиорганной недостаточности после травм. Арка Сург .1994, январь 129: 39-45. [Медлайн].
Браун Дж. Б., Эмерик К. М., Браун Д. Л., Уайтингтон П. Ф., Алонсо Е. М.. Рекомбинантный фактор VIIa улучшает коагулопатию, вызванную печеночной недостаточностью. J Педиатр Гастроэнтерол Нутр . 2003 сентябрь 37: 268-272. [Медлайн].
Розенчер Н, Пуассон Д., Альби А., Аперс М, Барре Дж, Самама С.М. Две инъекции эритропоэтина вылечивают умеренную анемию у большинства пациентов, ожидающих ортопедической операции. Кан Дж Анаэст .2005 Февраль 52: 160-165. [Медлайн].
Ганнон CJ, Наполитано Л.М. Тяжелая анемия после желудочно-кишечного кровотечения у Свидетелей Иеговы: новые стратегии лечения. Crit Care Med . 2002 30 августа: 1893-1895. [Медлайн].
Робинсон Ю., Хостманн А., Матенов А., Эртель В., Оберхольцер А. Эритропоэз у пациентов с множественными травмами. Дж. Травма . 2006 ноябрь 61: 1285-1291. [Медлайн].
Стаббс Младший.Альтернативы переливанию продуктов крови тяжелобольным: эритропоэтин. Crit Care Med . 2006. 34: S160-S169.
Fergusson DA, Hébert PC, Mazer CD, Fremes S, MacAdams C, Murkin JM и др. Сравнение аналогов апротинина и лизина в кардиохирургии высокого риска. N Engl J Med . 2008 29 мая. 358 (22): 2319-31. [Медлайн].
Gould SA, Moore EE, Hoyt DB, Burch JM, Haenel JB, Garcia J, et al. Первое рандомизированное испытание полимеризованного гемоглобина человека в качестве кровезаменителя при острой травме и неотложной хирургии. Дж. Ам Колл Сург . 1998, август 187 (2): 113-20; обсуждение 120-2. [Медлайн].
Mackenzie CF, Moon-Massat PF, Shander A, Javidroozi M, Greenburg AG. Когда кровь не подходит: факторы, влияющие на выживаемость после использования переносчика кислорода на основе гемоглобина у 54 пациентов с опасной для жизни анемией. Анест Аналг . 2010 г. 1. 110 (3): 685-93. [Медлайн].
Натансон С., Керн С.Дж., Лурье П., Бэнкс С.М., Вулф С.М. Бесклеточные кровезаменители на основе гемоглобина и риск инфаркта миокарда и смерти: метаанализ. ЯМА . 2008 21 мая. 299 (19): 2304-12. [Медлайн].
Habib FA, Schulman C, Cohn SM, et al. Учебник интенсивной терапии . 7-е изд. Филадельфия: Эльзевьер; 2017. 73-78.
Mair DC, Hirschler N, Eastlund T. Стратегии управления донорами крови и компонентами для предотвращения острого повреждения легких, связанного с переливанием крови (TRALI). Crit Care Med . 2006 май. 34: S137-S143. [Медлайн].
Анемия увеличивает риск смерти у очень пожилых людей — ScienceDaily
Анемия у очень пожилых людей в возрасте 85 лет и старше, по-видимому, связана с повышенным риском смерти, согласно новому исследованию, опубликованному в CMAJ (журнал Канадской медицинской ассоциации).
Исследование было частью Лейденского исследования для людей старше 85 лет, в котором приняли участие 562 человека в возрасте 85 лет в Нидерландах и наблюдали за ними до 90 лет. У 27% участников в начале исследования была анемия (распространенная анемия) и В последующий период эпизодическая анемия развивалась у 24% людей без анемии в начале исследования.
Анемия у пожилых людей обычно связана с повышенной смертностью, а также снижением подвижности, когнитивными нарушениями, депрессией, падениями и переломами, госпитализацией и снижением качества жизни.Это может значительно повлиять на потребности и расходы в области здравоохранения в стареющих западных обществах.
В исследуемой группе риск смерти был одинаковым среди мужчин и женщин, а также среди людей в учреждениях длительного ухода и в обществе.
«Мы обнаружили сильную независимую связь между распространенной анемией у участников в возрасте 85 лет и риском смерти», — пишет г-жа Венди ден Эльзен из Медицинского центра Лейденского университета и соавторы, подтверждая результаты предыдущих исследований людей в Нидерландах и Северная Америка.«Мы обнаружили, что случайная анемия у участников старше 85 лет оказала даже более сильное влияние на смертность, чем распространенная анемия в возрасте 85 лет».
После корректировки на другие заболевания негативное влияние анемии на когнитивные способности и физические функции было нейтрализовано. Авторы приходят к выводу, что связанное с этим функциональное снижение, по-видимому, в основном связано с сопутствующими заболеваниями.
В соответствующем комментарии д-р Марк Кларфилд из Университета Бен-Гуриона и д-р Ора Палтиель из Хадасса-Еврейского университета в Израиле пишут: «При необъяснимой анемии у пожилых пациентов мы, возможно, никогда не сможем понять, является ли основная причина или анемия. несет ответственность за смерть.Они предупреждают, что необходимы доказательства того, что регулярное лечение необъяснимой анемии более полезно, чем вредно.
История Источник:
Материалы предоставлены журналом Canadian Medical Association Journal . Примечание. Содержимое можно редактировать по стилю и длине.
Таблица уровней гемоглобина— Информация о железе в организме
Опубликовано: 20.07.2015 — Обновлено: 08.12.2020
Автор: Disabled World — Контактное лицо: Disabled World (www.disabled-world.com)
Сводка *: Информация о высоком и низком уровне гемоглобина в крови, включая таблицу для печати и список продуктов с высоким содержанием железа. Немного низкий уровень гемоглобина не всегда является признаком болезни, для некоторых людей это может быть нормальным явлением. Железо — это минерал, который необходим для выработки здоровых эритроцитов и гемоглобина.
Главный дайджест
Что такое гемоглобин (Hb, Hgb)?
Гемоглобин (также обозначается как гемоглобин — Hb или Hgb) — железосодержащий металлопротеин, переносящий кислород, в красных кровяных тельцах всех позвоночных (за исключением рыб семейства Channichthyidae), а также в тканях некоторых беспозвоночных.Гемоглобин в крови переносит кислород от органов дыхания (легких или жабр) к остальным частям тела (то есть тканям). Там он высвобождает кислород, чтобы обеспечить аэробное дыхание, чтобы обеспечить энергией функции организма в процессе, называемом метаболизмом.
- Железо
- Важный элемент для производства крови. Около 70 процентов железа в организме содержится в красных кровяных тельцах, называемых гемоглобином, и в мышечных клетках, называемых миоглобином.
- Анемия
- Термин, обозначающий уровень эритроцитов или гемоглобина в крови ниже нормы.Этот термин произошел от греческого слова anaimia, что означает недостаток крови.
Симптомы анемии Часто включают:
- Обморок
- Бледная кожа
- Слабость
- Боль в груди
- Сердцебиение
- Одышка
- Синдром беспокойных ног
График уровня гемоглобина
| Нормальные диапазоны подсчета гемоглобина, широко принимаемые врачами | |
|---|---|
| Детский | |
| Рождение: | 13.От 5 до 24,0 г / дл (в среднем 16,5 г / дл) |
| <1 мес .: | от 10,0 до 20,0 г / дл (в среднем 13,9 г / дл) |
| 1-2 мес: | от 10,0 до 18,0 г / дл (в среднем 11,2 г / дл) |
| 2-6 месяцев: | от 9,5 до 14,0 г / дл (в среднем 12,6 г / дл) |
| от 0,5 до 2 лет: | от 10,5 до 13,5 г / дл (в среднем 12,0 г / дл) |
| От 2 до 6 лет: | от 11,5 до 13,5 г / дл (в среднем 12,5 г / дл) |
| 6-12 лет: | 11.От 5 до 15,5 г / дл (в среднем 13,5) |
| Самки | |
| Возраст 12-18 лет: | от 12,0 до 16,0 г / дл (в среднем 14,0 г / дл) |
| Возраст> 18 лет: | от 12,1 до 15,1 г / дл (в среднем 14,0 г / дл) |
| Мужчины | |
| 12-18 лет: | от 13,0 до 16,0 г / дл (в среднем 14,5 г / дл) |
| > 18 лет: | от 13,6 до 17,7 г / дл (в среднем 15,5 г / дл) |
Низкий уровень гемоглобина
Немного низкий уровень гемоглобина не всегда является признаком болезни, для некоторых людей это может быть нормальным явлением.У беременных женщин обычно низкий уровень гемоглобина. Низкий уровень гемоглобина обычно определяется как менее 13,5 граммов гемоглобина на децилитр (135 граммов на литр) крови для мужчин и менее 12 граммов на децилитр (120 граммов на литр) для женщин. У детей определение зависит от возраста и пола.
Заболевания и состояния, при которых ваше тело вырабатывает меньше красных кровяных телец, включают:
- Рак
- Цирроз
- Лейкемия
- Отравление свинцом
- Апластическая анемия
- Множественная миелома
- Некоторые лекарства
- Железодефицитная анемия
- Хроническая болезнь почек
- Лимфома Неходжкина
- Витаминодефицитная анемия
- Миелодиспластические синдромы
- Гипотиреоз (недостаточная активность щитовидной железы)
- Лимфома Ходжкина (болезнь Ходжкина)
- Кровопотеря от кровотечения (внутреннего или внешнего)
Уровень железа
Железо — это минерал, необходимый для выработки здоровых эритроцитов и гемоглобина.Низкий уровень железа может вызвать чувство усталости, а чрезвычайно низкий уровень железа может вызвать повреждение органов. Низкий показатель крови может быть вызван недостаточным употреблением продуктов, богатых железом, слишком частой сдачей крови, хроническими заболеваниями или другими невидимыми причинами. Суточную потребность в железе часто можно удовлетворить за счет приема добавок железа. Сульфат железа 325 мг перорально один раз в день и с пищей с высоким содержанием железа. Также рекомендуются продукты с высоким содержанием витамина С, потому что витамин С помогает организму усваивать железо.Продукты с высоким содержанием железа включают:
- Ростки фасоли
- Свекла
- Брокколи
- Брюссельская капуста
- Капуста
- Цыпленок
- Кукуруза
- Рыба
- Зеленая фасоль
- Зелень всякая
- Кале
- Баранина
- Постная говядина
- Лимская фасоль
- Печень
- Мидии
- Свинина
- Картофель
- Моллюски
- Горох
- Тофу
- Помидоры
- Турция
- Телятина
Высокий уровень гемоглобина
Высокий уровень гемоглобина в основном связан с низким уровнем кислорода в крови (гипоксия), который присутствует в течение длительного периода времени.Причины высокого уровня гемоглобина включают:
- Бернс
- Обезвоживание
- ХОБЛ тяжелой степени
- Тяжелое копчение
- Истинная полицитемия
- Сильная рвота
- Жизнь на большой высоте
- Экстремальные физические упражнения
- Отказ правой половины сердца
- Врожденные пороки сердца, присутствующие при рождении.
- Рубцевание или утолщение легких (фиброз легких) и другие тяжелые заболевания легких
- Редкие заболевания костного мозга, приводящие к аномальному увеличению количества клеток крови (истинная полицитемия)
Тест на гемоглобин A1c
Тест на гемоглобин A1c, также называемый HbA1c, тест на гликированный гемоглобин или гликогемоглобин, является важным анализом крови, который показывает, насколько хорошо контролируется ваш диабет.Гемоглобин A1c обеспечивает средний контроль уровня сахара в крови за последние 2–3 месяца и используется вместе с домашним мониторингом уровня сахара в крови для корректировки лекарств от диабета.
- Для людей без диабета нормальный диапазон теста на гемоглобин A1c составляет от 4% до 5,6%.
- Уровни гемоглобина A1c от 5,7% до 6,4% указывают на повышенный риск диабета.
- Уровни 6,5% или выше указывают на диабет.
Цель для людей с диабетом — уровень гемоглобина A1c ниже 7%.Чем выше уровень гемоглобина A1c, тем выше риск развития осложнений, связанных с диабетом.
Графики уровня гемоглобина для печати
Диаграмма 1
Таблица уровней гемоглобина человека для печати.
Диаграмма 2
Альтернативная версия: Диаграмма уровня гемоглобина показывает идеальный диапазон для женщин, мужчин и детей младшего возраста.
Об авторе
Disabled World (Disabled-World.Com) — это независимое сообщество людей с ограниченными возможностями, созданное в 2004 году для предоставления новостей об инвалидах, обзоров вспомогательных технологий и спортивных мероприятий для инвалидов, а также общей информации для людей с ограниченными возможностями и пожилых людей. , их семья и / или опекуны.Не забудьте заглянуть на нашу домашнюю страницу, чтобы найти информативные обзоры, эксклюзивные истории и инструкции. Вы также можете найти нас в Twitter, Facebook и LinkedIn.
Сопутствующие медицинские калькуляторы Документы
* Заявление об ограничении ответственности: Disabled World предоставляет только общую информацию. Представленные материалы никоим образом не предназначены для замены профессиональной медицинской помощи квалифицированным практикующим врачом и не должны рассматриваться как таковые. Любое стороннее предложение или реклама на disabled-world.com не означает одобрения Disabled World.Ознакомьтесь с нашей Политикой в отношении рекламы для получения дополнительной информации. Сообщите нам устаревшую или неточную информацию.
Цитируйте страницу: Журнал: Мир инвалидов . Язык: английский (США). Автор: Disabled World. Дата публикации в электронном виде: 20 июля 2015 г. - Последняя редакция: 8 декабря 2020 г. Заголовок: Таблица уровней гемоглобина - информация о железе в организме , источник: Таблица уровней гемоглобина - информация о железе в организме .Получено 2021-04-30, из https://www.disabled-world.com/calculators-charts/hemoglobin-iron.php - Ссылка: DW # 286-11491.
Критическая десатурация гемоглобина произойдет перед возвращением в непарализованное состояние после внутривенного введения 1 мг / кг сукцинилхолина | Анестезиология
Эти результаты имеют несколько важных значений для клинического лечения пациента с затрудненным проходимостью дыхательных путей. Во-первых, поскольку у данного пациента неизвестно, как быстро будет метаболизироваться сукцинилхолин, наш анализ показывает, что рекомендация о том, чтобы пациенту было разрешено проснуться (достичь функционального восстановления), может быть логически выполнена только при наличии некоторого уровня V с кольцом . E .Таким образом, если V с кольцом E = 0 (т. Е. Полная ситуация «не может вентилировать / не интубировать»), тогда следует немедленно приступить к спасательному варианту (например, ввести дыхательные пути ларингеальной маски, Combitube (Sheridan Corp., Argyle, NY), институт транстрахеальной струйной вентиляции, хирургические дыхательные пути). Во-вторых, в этом анализе не учитывались центральные респираторные депрессивные эффекты всех одновременно вводимых общих анестетиков (которые, конечно, должны присутствовать). Следовательно, с этой точки зрения, этот анализ следует рассматривать как недооценку времени до функционального восстановления и периода опасности.Недооценка времени функционального восстановления и периода опасности подкрепляет первые два вывода, приведенные выше. В-третьих, если бы у здорового пациента с массой тела 70 кг наблюдалось снижение сердечного выброса, уменьшение исходного альвеолярного объема, снижение концентрации гемоглобина или увеличение потребления кислорода после внутривенного введения сукцинилхолина в дозе 1 мг / кг, то скорость десатурации артериального гемоглобина даже увеличилась. быть больше, чем показано на рисунке 1. Следовательно, с этой точки зрения, анализ также может быть недооценкой отрицательной разницы между временем десатурации и временем функционального восстановления.Наконец, наш анализ включал только глобальные физиологические переменные, которые влияли на время десатурации гемоглобина, и не учитывал региональные патологические факторы, такие как критические стенозы сосудов, которые могли увеличить продолжительность и интенсивность опасности для региона.
Таким образом, этот анализ показывает, что у подавляющего большинства пациентов с апноэ, вызванным сукцинилхолином внутривенно в дозе 1 мг / кг, десатурация гемоглобина, представляющая значительную или опасную для жизни, происходит до функционального восстановления.Однако интенсивность и продолжительность опасности, возможно, были недооценены этим анализом из-за предположений, что альвеолярная денитрогенизация завершена, что функциональное восстановление включает восстановление проходимости дыхательных путей, что одновременно вводимые анестетики могут эффективно задерживать функциональное восстановление, что физиологические параметры могут изменяться таким образом, чтобы уменьшить время до десатурации гемоглобина, а региональные патологические переменные могут повысить степень опасности. Следовательно, если V с кольцом E считается равным 0 или близким к 0, достижение функционального восстановления до значительной десатурации нереалистично, и необходимо активнее и раньше задействовать вариант спасения.У большинства пациентов анализ риска и пользы будет отдавать предпочтение введению ларингеальной маски в дыхательные пути или Combitube перед установкой транстрахеальной струйной вентиляции или проведением хирургического вмешательства в дыхательные пути. [18]
.

 Точную картину можно получить только после анализа крови.
Точную картину можно получить только после анализа крови.



