Global-Vet — Главная
GOBALVET GROUP Компания была основана в 2003 году, как оптовая компания, осуществляющая поставки ветеринарных препаратов для ветклиник и аптек города Москвы и городам России. В 2004 году была открыта компания «АВК», осуществляющая сопровождение регистрации лекарственных средств, организации профильных образовательных мероприятий для ветеринарных врачей, дизайн и производство рекламы. Вскоре Компания стала осуществлять поставки по всей территории Российской Федерации. В 2007 году открывается первый филиал в городе Санкт-Петербург, затем с 2008 по 2010 филиалы в городах Белгород (2008), Краснодар (2009), Новосибирск (2009) и подразделение в Республике Казахстан. В 2008 году был заключен первый контракт с одним из крупнейших европейских производителей лекарственных средств в Великобритании, запущено контрактное производство, зарегистрирована собственная торговая марка Globalvet. На данный момент в портфеле компании более 15 эксклюзивных контрактов с производителями Российских, Европейских и Азиатских стран и поставляет на локальный рынок не только эксклюзивные продукты, но и более 150 наименований под брендом Globalvet. Параллельно Компания выходит на новый для нее сегмент — это предприятия агропромышленного комплекса. 2010 год считается годом образования холдинга Globalvet Group. В 2013 новое направление деятельности компании по работе с сегментом предприятия промышленной переработки продуктов питания, в связи с чем произошло развитие товарной категории моющие и дезинфицирующие средства. В период с 2014 по 2019 годы были открыты еще несколько филиалов в городах: Воронеж (2014 г.), Ростов-на-Дону (2015 г.), Самара (2017 г.), Екатеринбург (2017г.), Красноярск (2018 г.), Владивосток (2019 г.). В 2016 году было принято решение об организации специализированной розницы, и был открыт зоомагазин в г. Краснодар, затем в городах Воронеж и Ростов-на-Дону, и интернет-магазин с точкой доступа в городах Санкт-Петербург, Новосибирск, Краснодар, Воронеж, Ростов-на-Дону. На сегодняшний день группа компаний представлена в более 30 городах Российской Федерации и Республики Казахстан в виде подразделений и территориальных представителей компании и является одним из лидеров в области поставок товаров, связанных со здоровьем животных и безопасностью продуктов животного происхождения.
ООО «ГЛОБАЛ-ВЕТ» — управляющее звено Globalvet group® и первая российская компания, импортирующая под собственной зарегистрированной торговой маркой Globalvet® препараты производства европейских и российских лидеров фармацевтической и химической отраслей. За последние восемь лет ООО «Глобал-Вет» было введено на российский рынок несколько сотен продуктов. Ежегодно ассортимент компании расширяется.
ТОРГОВЫЕ МАРКИ КОМПАНИИ ПРЕДСТАВЛЕНЫ НАПРАВЛЕНИЯМИ:
• GLOBALVET VET PRODUCTS® (антибактериальные, нестероидные противовоспалительные, противомаститные, противопаразитарные препараты пр-ва Великобритании, Бельгии), кормовые добавки для птиц и кроликов пр-ва Франции).
• GLOBALVET PET PRODUCTS® (средства ухода за животными пр-ва Дании).
• GLOBALVET CLEAN PRODUCTS® (санитарные препараты пр-ва России и Франции).
• GLOBALVET CARE PRODUCTS® (ветеринарные гели пр-ва России).
• ANIMAL-ID® (средства электронной идентификации пр-ва Испании).
Продукция Globalvet на сегодняшний день успешно применяется в животноводческих и птицеводческих холдингах, крупнейших ветеринарных клиниках для мелких домашних животных во всех регионах России и Казахстана. Кроме собственных торговых марок Globalvet group в своем ассортименте эксклюзивно представляет продукцию производителей: Kela, Vetoquinol, Novadan, Fish Corp 2000, FBK.
В СОСТАВЕ GLOBALVET GROUP® РАБОТАЮТ ТОРГОВЫЕ ПОДРАЗДЕЛЕНИЯ:
ООО «Торговая Группа Глобал-Вет» и ООО «Глобал-Клин». Торговые подразделения представляют в своём ассортименте не только продукцию Globalvet®, но и полный ассортимент продукции для мелких домашних и сельскохозяйственных животных, являются дистрибьютором таких крупнейших производителей, как MSD Animal Health, Elanco, Zoetis, Orion pharma.
Склады группы компаний находятся в Москве, Санкт-Петербурге, Белгороде, Воронеже, Самаре, Краснодаре, Ростове-на-Дону, Новосибирске, Екатеринбурге, Красноярске, Владивостоке и в г. Алма-Ата.
Большая часть сотрудников, занимающихся продажами и закупками в компании имеют ветеринарное образование.
Автопарк компании на сегодняшний день насчитывает более 80 автомобилей.
Консалтинговое подразделение Globalvet group® — компания AGROVETCONSULTING (ООО «АВК»), выполняет работы по регистрации ветеринарных препаратов «под ключ», организации ветеринарных семинаров, рекламной поддержке продаж, маркетинговой аналитике.
GLOBALVET GROUP® работает без посредников в области регистрации, внешнеэкономической деятельности, маркетинга и рекламы. В стоимость продукции от Globalvet не заложены «лишние» расходы на посреднические услуги, что помогает обеспечить оптимальную стоимость продукции, качество которой может служить эталоном в области ветеринарной фармацевтики.
Мы помогаем повысить экономическую эффективность деятельности организаций, работающих в области бизнеса продукции для мелких домашних и сельскохозяйственных животных.
Дексакел 50 мл — Инструкция
Стерильный водный иньекционный раствор
Состав
Дексаметазона фосфат eq. 2 mg dexamethasone
наполнители до 1 мл.
Свойства
Дексаметазон очень сильный синтетический глюкокортикостероид, противовоспалительный эффект которого в 30 раз сильнее, чем у кортизона и в 7-10 раз сильнее, чем у преднизолона. В добавление к его противовоспалительным качествам, дексаметазон также демонстрирует экстраординарные антиаллергические, антистрессовые и глюконеогенетические свойства.
Показания
Метаболические процессы, такие как: кетоз у крупного рогатого скота или послеродовая токсемия у овец и свиноматок.
Неинфекционные воспалительные процессы, особенно острые мышечноскелетные воспаления, такие как: артрит, периартрит, тендовагинит, бурсит, вывихи, воспаления мышц, костей и сухожилий.
При острых инфекционных заболеваниях (напр. острый мастит, метрит, пневмония)в комбинации с соответствующей антибактериальной терапией.
Аллергическое состояние, напр. астма, аллергические поражения кожи (экзема, кропивница, чесотка…), ламинит у лошадей и крупного рогатого скота, укуси змей.
Стрессовое и шоковое состояние.
Токсимия во время последней стадии беременности (напротяжении 2 — 4 дней)
Дозировка и применение
Путем внутривенной, внутримышечной или подкожной (собаки) иньекции:
Кошки, собаки: (0.1-0.2 мг/кг массы тела) 0.25-0.5 мл/5 кг
Крупный рогатый скот, лошади: (2.5-5 мг/100 кг массы тела 5-10 мл/400 кг
При необходимости повторить с 2х-дневным интервалом у собак и кошек и 3-4х дневным интервалом у других животных.
Для иницирования отела у коров (дается напротяжении 1 недели перед рождением телят):(5 мг/100 кг массы тела) 2.5 мл/100 кг.
Послеродовая токсемия и инициирование отела у овец и коз: (2.5 мг/10 кг массы тела) ± 6 мл/50 кг
Шоковая терапия: путем медленной I.V ін’єкції при большой дозе (10-x), повторить через 8-12 часов.
Путем внутрисуставной иньекции: соответственно массе тела животных: від 0.25 до 4 мл.
Противопоказания
Cердечная и почечная недостаточность, гиперкортицизм (синдром Кушинга), диабет, остеопороз, вирусемия, симультанная вакцинация.
Предупреждение
Если инфекция присутствует либо подозревается, кортикоидную терапию необходимо назначать вместе с соответствующей антимикробной терапией (ослабление имунной реакции).
Поскольку резкий отказ от хронического употребления может привести к адренокортикальной недостаточности (симптомы гипокортицизма), рекомендуется постепенный отказ после долгосрочного курса употребления.
Форма выпуска
Флаконы по 50 мл.
Хранение
Хранить в прохладном (до 15°C), защищенном от света месте.
Дексакел 50 мл
Стерильный водный иньекционный растворСостав
Дексаметазона фосфат eq. 2 mg dexamethasone
наполнители до 1 мл.
Свойства
Дексаметазон очень сильный синтетический глюкокортикостероид, противовоспалительный эффект которого в 30 раз сильнее, чем у кортизона и в 7-10 раз сильнее, чем у преднизолона. В добавление к его противовоспалительным качествам, дексаметазон также демонстрирует экстраординарные антиаллергические, антистрессовые и глюконеогенетические свойства.
Показания
Метаболические процессы, такие как: кетоз у крупного рогатого скота или послеродовая токсемия у овец и свиноматок.
При острых инфекционных заболеваниях (напр. острый мастит, метрит, пневмония)в комбинации с соответствующей антибактериальной терапией.
Аллергическое состояние, напр. астма, аллергические поражения кожи (экзема, кропивница, чесотка…), ламинит у лошадей и крупного рогатого скота, укуси змей.
Стрессовое и шоковое состояние.
Токсимия во время последней стадии беременности (напротяжении 2 — 4 дней)
Дозировка и применение
Путем внутривенной, внутримышечной или подкожной (собаки) иньекции:
Кошки, собаки: (0.1-0.2 мг/кг массы тела) 0.25-0.5 мл/5 кг
Крупный рогатый скот, лошади: (2.5-5 мг/100 кг массы тела 5-10 мл/400 кг
Овцы, козы, телята: (2-4 мг/50 кг) 1-2 мл/50 кг
При необходимости повторить с 2х-дневным интервалом у собак и кошек и 3-4х дневным интервалом у других животных.
Послеродовая токсемия и инициирование отела у овец и коз: (2.5 мг/10 кг массы тела) ± 6 мл/50 кг
Шоковая терапия: путем медленной I.V ін’єкції при большой дозе (10-x), повторить через 8-12 часов.
Путем внутрисуставной иньекции: соответственно массе тела животных: від 0.25 до 4 мл.
Противопоказания
Cердечная и почечная недостаточность, гиперкортицизм (синдром Кушинга), диабет, остеопороз, вирусемия, симультанная вакцинация.
Предупреждение
Если инфекция присутствует либо подозревается, кортикоидную терапию необходимо назначать вместе с соответствующей антимикробной терапией (ослабление имунной реакции).
Поскольку резкий отказ от хронического употребления может привести к адренокортикальной недостаточности (симптомы гипокортицизма), рекомендуется постепенный отказ после долгосрочного курса употребления.
Форма выпуска
Хранение
Хранить в прохладном (до 15°C), защищенном от света месте.
Декса кел 0,2% (50 мл)
Декса-кел 02 (50 мл)
Инструкция по применению Декса-кел 02
Стерильный водный иньекционный раствор
СОСТАВ: Дексаметазона фосфат eq. 2 mg dexamethasone
наполнители до 1 мл.
СВОЙСТВА: ДЕКСАМЕТАЗОН очень сильный синтетический глюкокортикостероид, противовоспалительный эффект которого в 30 раз сильнее, чем у кортизона и в 7-10 раз сильнее, чем у преднизолона. Вдобавление к его противовоспалительным качествам, дексаметазон также демонстрирует экстраординарные антиаллергические, антистрессовые и глюконеогенетические свойства.
ПОКАЗАНИЯ: Метаболические процессы, такие как: кетоз у крупного рогатого скота или послеродовая токсемия у овец и свиноматок.
Неинфекционные воспалительные процессы, особенно острые мышечноскелетные воспаления, такие как: артрит, периартрит, тендовагинит, бурсит, вывихи, воспаления мышц, костей и сухожилий.
При острых инфекционных заболеваниях (напр. острый мастит, метрит, пневмония) в комбинации с соответствующей антибактериальной терапией.
Аллергическое состояние, напр. астма, аллергические поражения кожи (экзема, кропивница, чесотка…), ламинит у лошадей и крупного рогатого скота, укуси змей. Стрессовое и шоковое состояние. Токсимия во время последней стадии беременности (напротяжении 2 — 4 дней)
ДОЗИРОВКА И ПРИМЕНЕНИЕ: Путем внутривенной, внутримышечной или подкожной (собаки) иньекции:
Кошки, собаки: (0.1-0.2 мг/кг массы тела) 0.25-0.5 мл/5 кг
Крупный рогатый скот, лошади: (2.5-5 мг/100 кг массы тела 5-10 мл/400 кг
Овцы, козы, телята: (2-4 мг/50 кг) 1-2 мл/50 кг
При необходимости повторить с 2х-дневным интервалом у собак и кошек и 3-4х дневным интервалом у других животных.
Для иницирования отела у коров (дается напротяжении 1 недели перед рождением телят): (5 мг/100 кг массы тела) 2.5 мл/100 кг.
Послеродовая токсемия и инициирование отела у овец и коз: (2.5 мг/10 кг массы тела) ± 6 мл/50 кг
Шоковая терапия: путем медленной I.V ін’єкції при большой дозе (10-x), повторить через 8-12 часов.
Путем внутрисуставной иньекции: соответственно массе тела животных: від 0.25 до 4 мл.
ПРОТИВОПОКАЗАНИЯ, ПОБОЧНЫЕ ДЕЙСТВИЯ, ПРЕДОСТЕРЕЖЕНИЯ: Противопоказания: сердечная и почечная недостаточность, гиперкортицизм (синдром Кушинга), диабет, остеопороз, вирусемия, симультанная вакцинация.
Если инфекция присутствует либо подозревается, кортикоидную терапию необходимо назначать вместе с соответствующей антимикробной терапией (ослабление имунной реакции).
Поскольку резкий отказ от хронического употребления может привести к адренокортикальной недостаточности (симптомы гипокортицизма), рекомендуется постепенный отказ после долгосрочного курса употребления.
ХРАНЕНИЕ: хранить в прохладном (до 15°C), защищенном от света месте.
Производитель: КЕЛА Н. В. (KELA N.V. ), Бельгия.
Упаковка: флакон 50 мл
1. Передовой опыт, новинки и инновации в животноводстве (свиноводство, молочное животноводство, птицеводство, кролиководство и другие): http://bit.ly/fap-novoe
2. Группы в Телеграм-канале для общения на выставках, конференциях и семинарах: http://bit.ly/fap-calendar
3. Промо услуги для предприятий, работающих в сфере животноводства: http://bit.ly/fap-promo
4. Консультации по кормлению, лечению, составлению рационов и содержанию сельскохозяйственных животных: http://bit.ly/consulting-fap
5. Календарь выставок, конференций и семинаров по животноводству: http://bit.ly/fap-calendar
6. Племпредприятия, продажа племенных животных и генетического материала: http://bit.ly/fap-plem
7. Производители и дистрибьюторы препаратов, комбикормов, премиксов и кормовых добавок для животноводства: http://bit.ly/fap-premix-firms
8. Производители и дистрибьюторы техники, оборудования, IT решений и услуг для животноводства: http://bit.ly/fap-mechanism-firms
9. Срочные события, новости и информация в животноводстве: http://bit.ly/fap-fast-info
дексакел — словарь ветеринарных терминов — ВЦ Зоовет
Декса — кел 02
Стерильный водный иньекционный раствор
Состав
Дексаметазона фосфат eq. 2 mg dexamethasone
наполнители до 1 мл.
Свойства
Дексаметазон очень сильный синтетический глюкокортикостероид, противовоспалительный эффект которого в 30 раз сильнее, чем у кортизона и в 7-10 раз сильнее, чем у преднизолона. В добавление к его противовоспалительным качествам, дексаметазон также демонстрирует экстраординарные антиаллергические, антистрессовые и глюконеогенетические свойства.
Показания
Метаболические процессы, такие как: кетоз у крупного рогатого скота или послеродовая токсемия у овец и свиноматок.
Неинфекционные воспалительные процессы, особенно острые мышечноскелетные воспаления, такие как: артрит, периартрит, тендовагинит, бурсит, вывихи, воспаления мышц, костей и сухожилий.
При острых инфекционных заболеваниях (напр. острый мастит, метрит, пневмония)в комбинации с соответствующей антибактериальной терапией.
Аллергическое состояние, напр. астма, аллергические поражения кожи (экзема, кропивница, чесотка…), ламинит у лошадей и крупного рогатого скота, укуси змей.
Стрессовое и шоковое состояние.
Токсимия во время последней стадии беременности (напротяжении 2 — 4 дней)
Дозировка и применение
Путем внутривенной, внутримышечной или подкожной (собаки) иньекции:
Кошки, собаки: (0.1-0.2 мг/кг массы тела) 0.25-0.5 мл/5 кг
Крупный рогатый скот, лошади: (2.5-5 мг/100 кг массы тела 5-10 мл/400 кг
Овцы, козы, телята: (2-4 мг/50 кг) 1-2 мл/50 кг
При необходимости повторить с 2х-дневным интервалом у собак и кошек и 3-4х дневным интервалом у других животных.
Для иницирования отела у коров (дается напротяжении 1 недели перед рождением телят):(5 мг/100 кг массы тела) 2.5 мл/100 кг.
Послеродовая токсемия и инициирование отела у овец и коз: (2.5 мг/10 кг массы тела) ± 6 мл/50 кг
Шоковая терапия: путем медленной I.V ін’єкції при большой дозе (10-x), повторить через 8-12 часов.
Путем внутрисуставной иньекции: соответственно массе тела животных: від 0.25 до 4 мл.
Противопоказания
Cердечная и почечная недостаточность, гиперкортицизм (синдром Кушинга), диабет, остеопороз, вирусемия, симультанная вакцинация.
Предупреждение
Если инфекция присутствует либо подозревается, кортикоидную терапию необходимо назначать вместе с соответствующей антимикробной терапией (ослабление имунной реакции).
Поскольку резкий отказ от хронического употребления может привести к адренокортикальной недостаточности (симптомы гипокортицизма), рекомендуется постепенный отказ после долгосрочного курса употребления.
Форма выпуска
Флаконы по 50 мл.
Хранение
Хранить в прохладном (до 15°C), защищенном от света месте.
Производитель
КЕЛА Н.В.
ул. Ленаартсевег 48
2320 Хоогстратен, Бельгия
Дексакел 50 мл
Стерильный водный иньекционный раствор
Состав
Дексаметазона фосфат eq. 2 mg dexamethasone
наполнители до 1 мл.
Свойства
Дексаметазон очень сильный синтетический глюкокортикостероид, противовоспалительный эффект которого в 30 раз сильнее, чем у кортизона и в 7-10 раз сильнее, чем у преднизолона. В добавление к его противовоспалительным качествам, дексаметазон также демонстрирует экстраординарные антиаллергические, антистрессовые и глюконеогенетические свойства.
Показания
Метаболические процессы, такие как: кетоз у крупного рогатого скота или послеродовая токсемия у овец и свиноматок.
Неинфекционные воспалительные процессы, особенно острые мышечноскелетные воспаления, такие как: артрит, периартрит, тендовагинит, бурсит, вывихи, воспаления мышц, костей и сухожилий.
При острых инфекционных заболеваниях (напр. острый мастит, метрит, пневмония)в комбинации с соответствующей антибактериальной терапией.
Аллергическое состояние, напр. астма, аллергические поражения кожи (экзема, кропивница, чесотка…), ламинит у лошадей и крупного рогатого скота, укуси змей.
Стрессовое и шоковое состояние.
Токсимия во время последней стадии беременности (напротяжении 2 — 4 дней)
Дозировка и применение
Путем внутривенной, внутримышечной или подкожной (собаки) иньекции:
Кошки, собаки: (0.1-0.2 мг/кг массы тела) 0.25-0.5 мл/5 кг
Крупный рогатый скот, лошади: (2.5-5 мг/100 кг массы тела 5-10 мл/400 кг
Овцы, козы, телята: (2-4 мг/50 кг) 1-2 мл/50 кг
При необходимости повторить с 2х-дневным интервалом у собак и кошек и 3-4х дневным интервалом у других животных.
Для иницирования отела у коров (дается напротяжении 1 недели перед рождением телят):(5 мг/100 кг массы тела) 2.5 мл/100 кг.
Послеродовая токсемия и инициирование отела у овец и коз: (2.5 мг/10 кг массы тела) ± 6 мл/50 кг
Шоковая терапия: путем медленной I.V ін’єкції при большой дозе (10-x), повторить через 8-12 часов.
Путем внутрисуставной иньекции: соответственно массе тела животных: від 0.25 до 4 мл.
Противопоказания
Cердечная и почечная недостаточность, гиперкортицизм (синдром Кушинга), диабет, остеопороз, вирусемия, симультанная вакцинация.
Предупреждение
Если инфекция присутствует либо подозревается, кортикоидную терапию необходимо назначать вместе с соответствующей антимикробной терапией (ослабление имунной реакции).
Поскольку резкий отказ от хронического употребления может привести к адренокортикальной недостаточности (симптомы гипокортицизма), рекомендуется постепенный отказ после долгосрочного курса употребления.
Форма выпуска
Флаконы по 50 мл.
Хранение
Хранить в прохладном (до 15°C), защищенном от света месте.
Дексалека (синтетический глюкокортикостероид) — дексаметозон в форме инъекция для животных. Противовоспалительное, антигистаминное (противоаллергенное), антитоксическое, противошоковое средство
Дексалека раствор для инъекций синтетический глюкокортикостероид В 1 мл препарата - 4 мг дексаметазона натрия фосфата, что эквивалентно 3 мг дексаметазона.
инструкция по применению
Назначение:
Оказывает противовоспалительное, противоаллергическое, десенсибилизирующее, противоотечное, противошоковое, антитоксическое действие на организм животных.
- ОДНА ИНЪЕКЦИЯ НА КУРС ЛЕЧЕНИЯ
- ОПТИМАЛЬНАЯ ДОЗА СОКРАЩАЕТ ЗАТРАТЫ НА ЛЕЧЕНИЕ
- КОРОТКИЙ СРОК ОЖИДАНИЯ ПО МОЛОКУ (2 ДНЯ)
Применение:
Препарата применяют в качестве противовоспалительного, противоотечного и антиаллергического средства в комплексной терапии заболеваний животных различной этиологии. При заболеваниях, осложненных бактериальной инфекцией, препарат применяют совместно с антибактериальными средствами широкого спектра действия.
Препарат вводят внутримышечно. ДОЗЫ:
лошади, крупный рогатый скот — 4 — 8,8 мл/500 кг массы тела
овцы, козы, телята, свиньи — 0,15 — 0,3 мл/10 кг массы тела
собаки, кошки — 0,15 — 0,4 мл/5 кг массы тела
Период ожидания
Мясо: свинина — 48 дней, говядина — 48 дней, конина — 24 дня
Молоко — 2 дня (6 доек)
Форма выпуска
Стеклянные флаконы по 100 мл.
Срок годности
2 года от даты изготовления.
Условия хранения
Хранить в сухом, защищенном от света месте при температуре от + 5°С до + 25°С.
Рекомендуемое руководство по расширенному и ограниченному повторному использованию фильтрующих респираторов с маской N95 в медицинских учреждениях | NIOSH
Рекомендуемое руководство по расширенному и ограниченному повторному использованию фильтрующих респираторов с маской N95 в медицинских учреждениях
Фон
В этом документе рекомендуются методы расширенного и ограниченного повторного использования сертифицированных NIOSH фильтрующих респираторов N95 (обычно называемых «респираторами N95»). Рекомендации предназначены для использования профессионалами, которые руководят программами защиты органов дыхания в учреждениях здравоохранения, чтобы защитить медицинских работников от связанных с работой рисков контакта с инфекционными респираторными заболеваниями.
Запасы респираторов N95 могут истощиться во время пандемии гриппа (1-3) или широко распространенных вспышек других инфекционных респираторных заболеваний. (4) Существующие руководящие принципы CDC рекомендуют комбинацию подходов к сохранению материалов и защите медицинских работников в таких обстоятельствах. Настоящее руководство рекомендует учреждениям здравоохранения:
- Свести к минимуму количество людей, которым необходимо использовать средства защиты органов дыхания, за счет преимущественного использования технических и административных средств контроля;
- Используйте альтернативы респираторам N95 (например,g., другие классы фильтрующих респираторов с маской, эластомерных полумасковых и полнолицевых респираторов с очисткой воздуха, респираторов с механической очисткой воздуха), где это возможно;
- Внедрить методы, позволяющие расширенное и / или ограниченное повторное использование респираторов N95, когда это приемлемо; и
- В первую очередь используйте респираторы N95 для тех сотрудников, которые подвергаются наибольшему риску заражения или возникновения осложнений инфекции.
В этом документе основное внимание уделяется одной из вышеперечисленных стратегий — расширенному использованию и ограниченному повторному использованию только респираторов N95; пожалуйста, проконсультируйтесь с веб-сайтом CDC или NIOSH для получения рекомендаций, касающихся реализации других рекомендуемых подходов для экономии расходных материалов респираторов N95.
Существуют также неэкстренные ситуации (например, тесный контакт с больными туберкулезом), в которых повторное использование респиратора N95 рекомендовано в медицинских учреждениях и широко практикуется. (5-9) Этот документ служит дополнением предыдущего руководства по этой теме.
Определения
Расширенное использование относится к практике ношения одного и того же респиратора N95 при неоднократных близких контактах с несколькими пациентами без снятия респиратора между контактами с пациентом.Длительное использование хорошо подходит для ситуаций, когда несколько пациентов инфицированы одним и тем же респираторным патогеном, и пациенты помещаются вместе в специальные залы ожидания или больничные палаты. Расширенное использование было рекомендовано как вариант для сохранения респираторов во время предыдущих вспышек респираторных патогенов и пандемий. (10, 11)
Повторное использование 1 относится к практике использования одного и того же респиратора N95 для многократных встреч с пациентами, но его удаления («снятие») после каждого контакта.Респиратор хранится в промежутках между встречами, чтобы его снова надеть («надеть») до следующего контакта с пациентом. Для патогенов, у которых контактная передача (например, фомиты) не вызывает беспокойства, повторное использование не в экстренных случаях практикуется в течение десятилетий. (7) Например, для профилактики туберкулеза CDC рекомендует повторно использовать респиратор, классифицируемый как одноразовый. рабочий, пока он остается в рабочем состоянии 2 и используется в соответствии с местными процедурами инфекционного контроля.(9) Даже когда повторное использование респиратора N95 практикуется или рекомендуется, существуют ограничения, которые ограничивают количество повторных использований одного и того же FFR. Таким образом, повторное использование респиратора N95 часто называют «ограниченным повторным использованием». Ограниченное повторное использование было рекомендовано и широко используется как вариант для сохранения респираторов во время предыдущих вспышек респираторных патогенов и пандемий. (2, 3, 10-12)
Реализация
Решение о внедрении политики, разрешающей расширенное или ограниченное повторное использование респираторов N95, должно приниматься профессионалами, которые управляют программой защиты органов дыхания учреждения, в консультации со своими отделами гигиены труда и инфекционного контроля при участии органов здравоохранения штата / местного населения. отделы.Решение о внедрении этих методов следует принимать в каждом конкретном случае с учетом характеристик респираторных патогенов (например, пути передачи, распространенность заболевания в регионе, скорость заражения и тяжесть заболевания) и местных условий (например, количество доступных одноразовых респираторов N95, текущая частота использования респираторов, успех других стратегий сохранения респираторов и т. д.). Некоторые медицинские учреждения могут пожелать внедрить расширенное использование и / или ограниченное повторное использование до того, как возникнет нехватка респираторов, чтобы в периоды пикового спроса были доступны соответствующие запасы.Для неэкстренных (рутинных) ситуаций также следует обращаться к текущим рекомендациям CDC (6, 9), относящимся к этому патогену.
В следующих разделах описаны конкретные шаги по реализации этих рекомендаций, минимизации проблем, вызванных расширенным и повторным использованием, и ограничению рисков, которые могут возникнуть в результате этих практик.
Рекомендации по расширенному использованию респиратора
Более длительное использование предпочтительнее повторного использования, поскольку предполагается, что при этом будет меньше касаний респиратора и, следовательно, меньше риск контактной передачи.См. Раздел «Риски расширенного и повторного использования респираторов» для получения дополнительной информации о передаче данных через контакт и других рисках, связанных с этими методами.
Ключевым моментом для безопасного длительного использования является то, что респиратор должен поддерживать свою форму и функционировать. Работники других отраслей обычно используют респираторы N95 в течение нескольких часов без перерыва. Опыт работы в этих условиях показывает, что респираторы могут работать в рамках своих проектных спецификаций в течение 8 часов непрерывного или периодического использования.В некоторых исследованиях (14, 15) в качестве испытуемых привлекались медицинские работники, и многие из этих испытуемых успешно носили респиратор N95 на работе в течение нескольких часов, прежде чем им понадобилось его снимать. Таким образом, максимальная продолжительность непрерывного использования на непыльных рабочих местах в медицинских учреждениях обычно диктуется гигиеническими соображениями (например, респиратор был выброшен из-за загрязнения) или практическими соображениями (например, необходимость использования туалета, перерывы на обед и т. Д.) , а не заранее определенное количество часов.
Если разрешено продолжительное использование респираторов N95, администраторы программы защиты органов дыхания должны обеспечить соблюдение административных и технических мер контроля для ограничения потенциального загрязнения поверхности респиратора N95 (например, использование барьеров для предотвращения попадания капель спрея) и рассмотреть возможность дополнительного обучения и напоминаний (например, плакаты) для персонала, чтобы подчеркнуть необходимость сведения к минимуму ненужного контакта с поверхностью респиратора, строгого соблюдения правил гигиены рук и надлежащей техники надевания и снятия средств индивидуальной защиты (СИЗ).(16) Медицинские учреждения должны разработать четко изложенные процедуры, чтобы посоветовать персоналу предпринять следующие шаги для уменьшения передачи контакта после надевания:
- Утилизируйте респираторы N95 после использования во время процедур образования аэрозоля.
- Утилизируйте респираторы N95, загрязненные кровью, респираторными или носовыми выделениями или другими биологическими жидкостями пациентов.
- Утилизируйте респираторы N95 при тесном контакте или выходе из зоны обслуживания любого пациента, коинфицированного инфекционным заболеванием, требующим контактных мер предосторожности.
- Рассмотрите возможность использования очищаемой маски для лица (предпочтительно 3 ) вместо респиратора N95 и / или других шагов (например, маскировка пациентов, использование технических средств контроля) для уменьшения поверхностного загрязнения.
- Выполните гигиену рук водой с мылом или дезинфицирующим средством для рук на спиртовой основе до и после прикосновения к респиратору или его регулировки (при необходимости для комфорта или поддержания формы).
Само по себе длительное использование вряд ли ухудшит защиту органов дыхания. Однако медицинские учреждения должны разработать четко изложенные процедуры, чтобы рекомендовать персоналу:
- Выбросьте респиратор, который явно поврежден или через него трудно дышать.
Рекомендации по повторному использованию респиратора
Невозможно определить максимально возможное количество безопасных повторных использований респиратора N95 в качестве общего числа, применяемого во всех случаях. На безопасное повторное использование N95 влияет ряд переменных, которые со временем влияют на работу респиратора и загрязнение. (18, 19) Однако производители респираторов N95 могут иметь конкретные рекомендации относительно повторного использования своего продукта. что респираторы N95 выбрасываются до того, как они станут серьезным риском контактной передачи или их функциональность не снизится.
Если разрешено повторное использование респираторов N95, администраторы программы защиты органов дыхания должны обеспечить соблюдение административных и технических мер контроля для ограничения потенциального загрязнения поверхности респиратора N95 (например, использование барьеров для предотвращения попадания капель спрея) и рассмотреть возможность дополнительного обучения и / или напоминаний (например, , плакаты) для персонала, чтобы подчеркнуть необходимость сведения к минимуму ненужного контакта с поверхностью респиратора, строгого соблюдения правил гигиены рук и надлежащей техники надевания и снятия СИЗ, включая физический осмотр и проверку пломб пользователя.(16) Медицинские учреждения должны разработать четко прописанные процедуры, чтобы рекомендовать персоналу предпринять следующие шаги для уменьшения передачи контактным путем:
- Утилизируйте респираторы N95 после использования во время процедур образования аэрозоля.
- Утилизируйте респираторы N95, загрязненные кровью, респираторными или носовыми выделениями или другими биологическими жидкостями пациентов.
- Утилизируйте респираторы N95 при тесном контакте с любым пациентом, ко-инфицированным инфекционным заболеванием, требующим контактных мер предосторожности.
- Рассмотрите возможность использования очищаемой маски для лица (предпочтительно 3 ) вместо респиратора N95 и / или других шагов (например, маскировка пациентов, использование технических средств контроля), когда это возможно, для уменьшения поверхностного загрязнения респиратора.
- Повесьте использованные респираторы в специально отведенном месте для хранения или храните их в чистом дышащем контейнере, таком как бумажный пакет, между использованием. Чтобы свести к минимуму возможное перекрестное заражение, храните респираторы так, чтобы они не касались друг друга и чтобы человек, использующий респиратор, был четко идентифицирован.Контейнеры для хранения следует регулярно утилизировать или чистить.
- Вымойте руки водой с мылом или дезинфицирующим средством для рук на спиртовой основе до и после прикосновения к респиратору или его регулировки (при необходимости для комфорта или поддержания формы).
- Не прикасайтесь к внутренней части респиратора. При случайном контакте с внутренней стороной респиратора выбросьте респиратор и выполните гигиену рук, как описано выше.
- Используйте чистые (нестерильные) перчатки при надевании использованного респиратора N95 и проверке герметичности пользователя.Выбросьте перчатки после того, как наденете респиратор N95 и произведены любые регулировки, чтобы респиратор удобно сидел на вашем лице с хорошей герметичностью.
Чтобы снизить вероятность снижения защиты, вызванного потерей функциональности респиратора, руководители программ защиты органов дыхания должны проконсультироваться с производителем респиратора относительно максимального количества надеваний или способов использования, которые они рекомендуют для моделей респираторов N95, используемых в этом учреждении. Если руководство производителя недоступно, предварительные данные (19, 20) предлагают ограничить количество повторных использований не более чем пятью использованиями на устройство, чтобы обеспечить достаточный запас прочности.Руководству следует рассмотреть возможность дополнительного обучения и / или напоминаний для пользователей, чтобы усилить потребность в правильных методах надевания респиратора, включая осмотр устройства на предмет физических повреждений (например, не растянуты ли ремни настолько, что они больше не обеспечивают достаточного натяжения для респиратора для герметизации к лицу ?, Не сломана ли насадка для носа или другие приспособления? и т. д.). Медицинские учреждения должны предоставить персоналу четко прописанные процедуры по адресу:
- Следуйте инструкциям производителя, включая проверку печати.
- Соблюдайте максимальное количество надеваний, указанное работодателем (или до пяти, если производитель не дает рекомендаций), и рекомендуемые процедуры проверки.
- Выбросьте респиратор, который явно поврежден или через него трудно дышать.
- Упакуйте или храните респираторы между использованием, чтобы они не повредились или не деформировались.
Вторичное облучение может произойти в результате повторного использования респиратора, если респираторы используются совместно пользователями и хотя бы один из пользователей является заразным (симптоматическим или бессимптомным).Таким образом, респираторы N95 должны использоваться только одним человеком. Для предотвращения случайного использования респираторов в медицинских учреждениях следует разработать четко изложенные процедуры информирования пользователей по следующему адресу:
- Маркировать контейнеры, используемые для хранения респираторов, или маркировать сам респиратор (например, на ремнях (11)) между использованиями именем пользователя, чтобы уменьшить случайное использование респиратора другим человеком.
Риски длительного использования и повторного использования респираторов
Несмотря на то, что расширенное использование и повторное использование респираторов имеет потенциальную выгоду в виде экономии ограниченных запасов одноразовых респираторов N95, эта практика вызывает опасения.Некоторые устройства не были одобрены FDA для повторного использования (21). В инструкциях для пользователя продукта некоторых производителей рекомендуется выбрасывать продукт после каждого использования (т. Е. «Только для одноразового использования»), в то время как другие разрешают повторное использование, если это разрешено политикой инфекционного контроля учреждения. (19) Наиболее значительный риск передачи инфекции при контакте с ним. поверхность загрязненного респиратора. Одно исследование показало, что медсестры в среднем наносили 25 прикосновений за смену к лицу, глазам или респиратору N95 во время длительного использования. (15) Контактная передача происходит при прямом контакте с другими, а также при косвенном контакте при прикосновении и загрязнении поверхностей, к которым затем прикасаются другие люди.
Респираторные патогены на поверхности респиратора потенциально могут быть перенесены прикосновением к рукам пользователя и, таким образом, рискуют вызвать инфекцию при последующем прикосновении к слизистым оболочкам лица (т. Е. При самоинокуляции). В то время как исследования показали, что некоторые респираторные патогены (22-24) остаются заразными на поверхностях респираторов в течение продолжительных периодов времени, в исследованиях микробного переноса (25-27) и реаэрозолизации (28-32) более ~ 99,8% оставались в ловушке на поверхности респиратора. респиратор после работы или после имитации кашля или чихания.
Респираторы также могут быть заражены другими патогенами, полученными от пациентов, коинфицированных обычными патогенами здравоохранения, которые имеют более длительную выживаемость в окружающей среде (например, устойчивые к метициллину Staphylococcus aureas, устойчивые к ванкомицину энтерококки, Clostridium difficile, норовирус и т. Д.). Эти организмы могут затем заразить руки владельца и, в свою очередь, передаваться через самоинокуляцию или другим людям через прямую или косвенную контактную передачу.
Риски контактной передачи при расширенном использовании и повторном использовании могут зависеть от типов выполняемых медицинских процедур и использования эффективных технических и административных средств контроля, которые влияют на степень загрязнения респиратора из-за распыления капель или осаждения аэрозольных частиц.Например, медицинские процедуры, генерирующие аэрозоль, такие как бронхоскопия, индукция мокроты или эндотрахеальная интубация, вероятно, вызовут более высокие уровни загрязнения поверхности респиратора, в то время как контроль источников загрязнения пациентов (например, просьба пациентов носить маски для лица), использование маски для лица поверх одноразовый респиратор N95 или использование технических средств контроля, таких как местная вытяжная вентиляция
.Как разработать инструкции по использованию для маркировки CE медицинских устройств — специалисты по сертификации
Чрезвычайно важно, чтобы медицинские устройства имели маркировку CE, потому что только эти устройства могут быть размещены на рынке. Знак CE показывает, что устройство соответствует требованиям законодательства в отношении медицинских устройств.
Частью процесса маркировки CE является разработка инструкции по применению (далее: IFU). Теперь, когда мы узнали, почему так важна маркировка CE на устройствах, давайте посмотрим, какие устройства подходят для составления инструкций по применению.
Медицинские изделия подразделяются на классы (I, IIa, IIb, III для медицинских изделий / Список A и B для устройств для диагностики in vitro) в зависимости от фактора риска. В Регламенте о медицинских устройствах (ЕС) 2017/745 (далее: MDR) говорится, что исключение сделано для медицинских устройств класса I и класса IIa.
Важно отметить, что IFU необходим, когда для устройств требуются конкретные инструкции по комплексной процедуре очистки, процедуре стерилизации или информация о том, как и когда повторно использовать устройство.
Какую информацию должен содержать IFU?
В соответствии с MDR IFU должен содержать следующую информацию:
- Торговое наименование устройства.
- Название и адрес производителя.
- Указание на то, что устройство содержит или включает в себя лекарственные вещества, ткани или клетки человеческого или животного происхождения.
- Информация об условиях хранения и обращения.
- Указание на его стерильное состояние и метод стерилизации, если устройство поставлено в стерильном состоянии.
- Предназначен ли прибор для одноразового использования или нет.
- Информация об использовании in vivo.
- Назначение устройства, а также предполагаемые пользователи и группы пациентов.
- Ожидаемые клинические преимущества.
- Тактико-технические характеристики устройства.
- Подходящая информация для медицинского работника по работе с устройством.
- Любые остаточные риски и т. Д. Должны быть доведены до сведения пациента.
- Технические характеристики, необходимые пользователю для правильного использования устройства.
- Подробная информация о любой подготовительной работе с устройством перед его использованием или во время его использования, например стерилизация или калибровка.
- Любые требования к специальной подготовке.
- Информация для проверки правильности установки устройства.
- Инструкции при повреждении или непреднамеренном открытии упаковки.
- Инструкция по стерилизации перед использованием.
- Информация для разрешения повторного использования.
- Указание на то, что устройство может быть повторно использовано только в том случае, если он отремонтирован под ответственность производителя в соответствии с законодательством.
- Информация о характеристиках и технических факторах, которые могут представлять опасность при повторном использовании устройства.
- Если устройство предназначено для использования вместе с другими устройствами и какими именно.
- Информация об излучении.
- Информация об ограничениях устройства.
- Информация о материалах имплантируемого устройства.
- Информация о безопасной утилизации устройства.
- Обстоятельства, при которых пользователь должен проконсультироваться с врачом, если устройство используется неспециалистом
- Дата выпуска и дата пересмотра IFU.
- Уведомление о необходимости сообщать о серьезных инцидентах.
Важность IFU
Составление IFU способствует снижению риска медицинских изделий. В большинстве случаев важно составить IFU.
Что нужно учитывать при составлении IFU?
Очень важно помнить, что не все вышеперечисленные инструкции применимы ко всем медицинским устройствам. Это может показаться утомительным процессом, потому что это так, и именно здесь вы к нам обращаетесь.
Специалисты по сертификации обслуживание и поддержка
Мы не только специализируемся на составлении чертежей IFU, но и помогаем вам облегчить выполнение 5 важных шагов для маркировки CE, а именно:
- Разделение по медицинскому статусу и классу
- Подтверждение соответствия основным требованиям
- Техническая документация
- Оценка соответствия
- Декларация соответствия
Если у вас есть какие-либо вопросы по этой теме, свяжитесь с нами по электронной почте: info @certification-expert.com или по телефону +31 (0) 850073210.
.Структура досье в CTD-формате
| Полное регистрационное досье состоит из 5 модулей: |
1. Модуль 1: АДМИНИСТРАТИВНАЯ ИНФОРМАЦИЯ
1.1 Содержание.
1,2. Форма заявки.
1,3. Краткое описание характеристик продукта, маркировки и инструкции по медицинскому применению:
1.3.1. Краткое описание характеристик продукта.
1.3.2. Маркировка.
1.3.3. Инструкция по медицинскому применению.
1.3.4. Макеты и образцы.
1.3.5. Сводка характеристик продукта, уже утвержденных в стране-производителе / заявителе.
1,4. Информация о независимых экспертах:
1.4.1. Информация об эксперте по качеству.
1.4.2. Информация о доклиническом эксперте.
1.4.3. Информация о клиническом эксперте.
1.5 Особые требования для различных типов приложений.
Приложение к Модулю 1. Оценка экологического риска
МОДУЛЬ 2: РЕЗЮМЕ CTD
2.1. Содержание модулей 2 — 5.
2.2. Введение.
2.3. Общее резюме качества.
2,4. Доклинический обзор:
2,5. Клинический обзор
2,6. Доклиническое заключение
2.6.1. Письменное резюме фармакологии.
2.6.2. Резюме по фармакологии в виде таблиц.
2.6.3. Письменное резюме фармакокинетики.
2.6.4. Сводная таблица фармакокинетики.
2.6.5. Письменное резюме токсикологии.
2.6.6. Резюме токсикологии в виде таблицы.
2,7. Клиническое заключение:
2.7.1. Резюме биофармацевтических исследований и связанных аналитических методов.
2.7.2. Резюме клинических фармакологических исследований.
2.7.3. Резюме клинической эффективности.
2.7.4. Резюме клинической безопасности.
2.7.5. Литературные ссылки.
2.7.6 Конспекты индивидуальных исследований.
МОДУЛЬ 3: КАЧЕСТВО.
ХИМИЧЕСКАЯ, ФАРМАЦЕВТИЧЕСКАЯ И БИОЛОГИЧЕСКАЯ ИНФОРМАЦИЯ ДЛЯ ЛЕКАРСТВЕННЫХ ПРОДУКТОВ, СОДЕРЖАЩИХ ХИМИЧЕСКИЕ И / ИЛИ БИОЛОГИЧЕСКИЕ АКТИВНЫЕ ВЕЩЕСТВА
3.1. Оглавление.
3.2. Основные данные.
3.2.S. Действующее (ые) вещество (а).
3.2.S.1. Общая информация:
3.2.S.1.1. Номенклатура.
3.2.S.1.2. Структура.
3.2.S.1.3. Общая недвижимость
3.2.S.2. Производство действующего (-ых) вещества (-ов):
3.2.S.2.1. Производитель (и).
3.2.S.2.2. Описание производственного процесса и контроля процесса.
3.2.S.2.3. Контроль материалов.
3.2.S.2.4. Контроль критических шагов и промежуточных звеньев.
3.2.S.2.5. Проверка и / или оценка процесса.
3.2.S.2.6. Разработка производственного процесса.
3.2.S.3. Характеристика действующего (-ых) вещества (-ов).
3.2.S.3.1. Выяснение структуры и других характеристик.
3.2.S.3.2. Примеси.
3.2.S.4. Контроль действующего вещества (веществ).
3.2.S.4.1. Технические характеристики.
3.2.S.4.2. Аналитические процедуры.
3.2.S.4.3. Валидация аналитических процедур.
3.2.S.4.4. Пакетный анализ.
3.2.S.4.5. Обоснование спецификации.
3.2.S.5. Справочные стандарты или материалы.
3.2.S.6. Система контейнера / укупорки.
3.2.S.7. Стабильность:
3.2.S.7.1. Обзор стабильности и выводы.
3.2.S.7.2. Протокол стабильности после утверждения и обязательство по стабильности.
3.2.S.7.3. Данные о стабильности.
3.2.P. Готовый лекарственный препарат:
3.2.P.1. Описание и состав лекарственного средства.
3.2.P.2. Фармацевтическая разработка:
3.2.P.2.1. Состав лекарственных средств.
3.2.P.2.1.1. Действующее (ые) вещество (а).
3.2.P.2.1.2. Вспомогательные вещества.
3.2.P.2.2. Лекарственный препарат.
3.2.P.2.2.1. Разработка рецептур.
3.2.P.2.2.2. Избыточные.
3.2.P.2.2.3. Физико-химические и биологические свойства.
3.2.P.2.3. Разработка производственного процесса.
3.2.P.2.4. Система контейнера / укупорки.
3.2.P.2.5. Микробиологические признаки.
3.2.P.2.6. Совместимость.
3.2.P.3. Производство лекарственного препарата:
3.2.P.3.1. Производитель (и)
3.2.P.3.2. Формула партии
3.2.P.3.3. Описание производственного процесса и контроля процесса.
3.2.P.3.4. Контроль критических шагов и промежуточных звеньев.
3.2.P.3.5. Проверка и / или оценка процесса.
3.2.P.4. Контроль вспомогательных веществ:
3.2.P.4.1. Характеристики.
3.2.P.4.2. Аналитические процедуры.
3.2.P.4.3. Валидация аналитических процедур.
3.2.P.4.4. Обоснование технических условий.
3.2.P.4.5. Вспомогательные вещества человеческого или животного происхождения.
3.2.P.4.6. Новые вспомогательные вещества.
3.2.P.5. Контроль лекарственного препарата:
3.2.P.5.1. Характеристики).
3.2.P.5.2. Аналитические процедуры.
3.2.P.5.3. Валидация аналитических процедур.
3.2.P.5.4. Пакетный анализ.
3.2.P.5.5. Характеристика примесей.
3.2.P.5.6. Обоснование спецификации (й).
3.2.P.6. Справочные стандарты и материалы.
3.2.P.7. Контейнер / укупорочная система.
3.2.P.8. Стабильность:
3.2.P.8.1. Обзор стабильности и заключение
3.2.P.8.2. Протокол стабильности после утверждения и обязательство по стабильности
3.2.P.8.3. Данные по устойчивости
3.2.A. Приложения:
3.2.A.1. Помещения и оборудование.
3.2.A.2. Оценка безопасности посторонних агентов.
3.2.A.3. Новые вспомогательные вещества.
3.2.R. Дополнительная информация.
3.3. Литературные ссылки.
Модуль 4: ОТЧЕТЫ О ДОКЛИНИЧЕСКИХ ИССЛЕДОВАНИЯХ
4.1. Оглавление.
4.2. Отчеты об исследованиях.
4.2.1. Фармакология:
4.2.1.1. Первичная фармакодинамика.
4.2.1.2. Вторичная фармакодинамика.
4.2.1.3. Фармакология безопасности.
4.2.1.4. Фармакодинамические взаимодействия.
4.2.2. Фармакокинетика:
4.2.2.1. Аналитические методы и отчеты о валидации.
4.2.2.2. Поглощение.
4.2.2.3. Распространение.
4.2.2.4. Обмен веществ.
4.2.2.5. Выведение.
4.2.2.6. Фармакокинетические взаимодействия (доклинические).
4.2.2.7. Другие фармакокинетические исследования.
4.2.3. Токсикология:
4.2.3.1. Токсичность при однократном приеме.
4.2.3.2. Токсичность при повторном приеме.
4.2.3.3. Генотоксичность
4.2.3.4. Канцерогенность.
4.2.3.5. Репродуктивная токсичность и токсичность для развития.
4.2.3.6. Местная толерантность.
4.2.3.7. Другие исследования токсичности.
4.3. Литературные ссылки.
МОДУЛЬ 5: ОТЧЕТЫ О КЛИНИЧЕСКИХ ИССЛЕДОВАНИЯХ
5.1. Оглавление.
5.2. Табличный список всех клинических исследований.
5.3. Отчеты о клинических исследованиях:
5.3.1. Отчеты о биофармацевтических исследованиях.
5.3.2. Отчеты об исследованиях фармакокинетики с использованием человеческих биоматериалов.
5.3.3. Отчеты фармакокинетических исследований человека.
5.3.4. Отчеты о фармакодинамических исследованиях человека
5.3.5. Отчеты об исследованиях эффективности и безопасности.
5.3.6. Отчеты о пострегистрационном опыте.
5.3.7. Образцы форм историй болезни и индивидуальных списков пациентов.
5.4. Литературные ссылки.
.Инструкции по набору для тестирования| DanceSafe
Ниже представлена наша последняя таблица цветов реагентов с инструкциями (последнее обновление — июнь 2019 г.). Прокрутите вниз, чтобы найти конкретные инструкции по тестированию МДМА, кокаина и ЛСД, а также инструкции по использованию тест-полосок на фентанил.
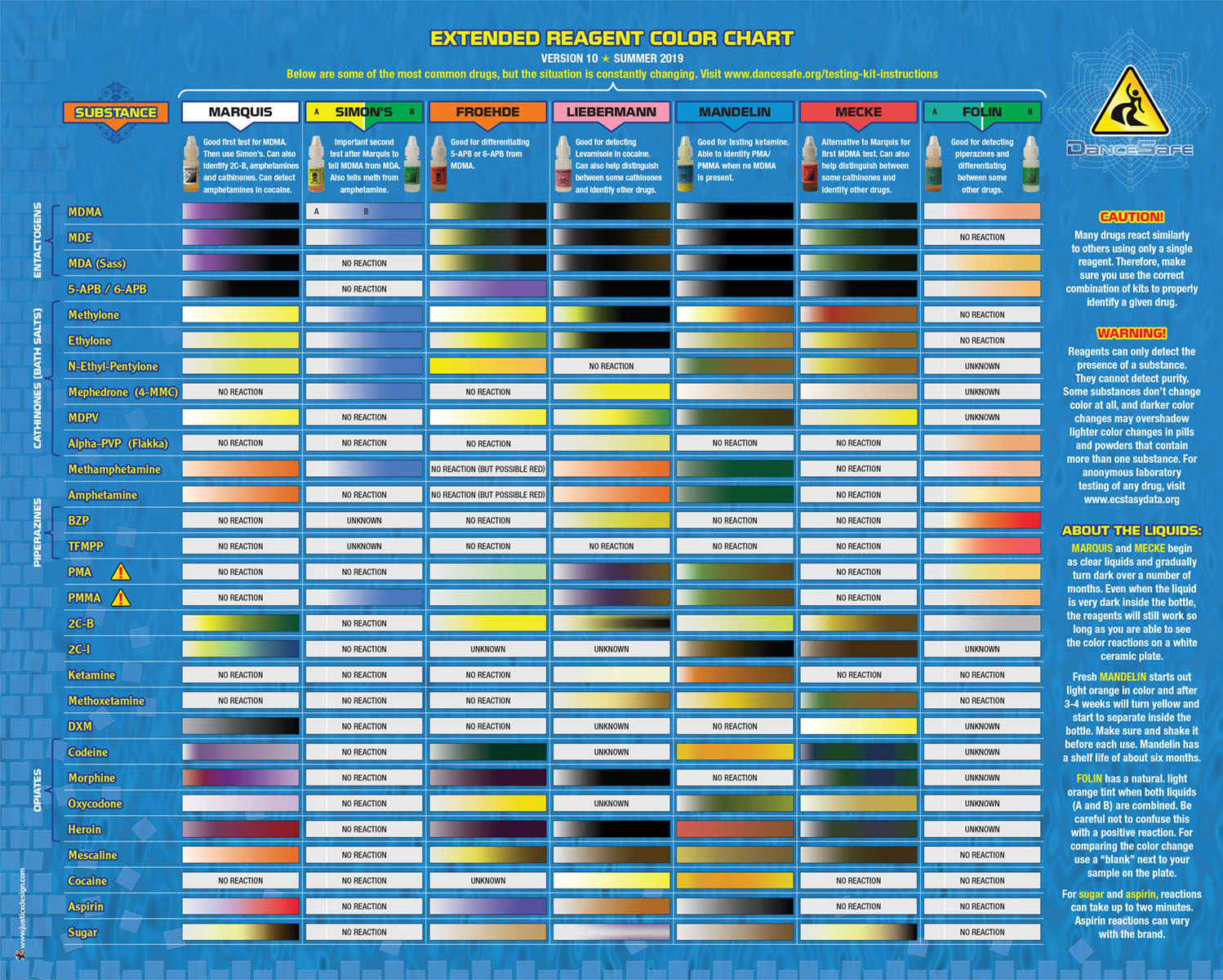
Полная инструкция
ВАЖНАЯ ИНФОРМАЦИЯ: Никогда не открывайте более одного флакона с реагентом одновременно. Если вы перепутаете крышки и установите неправильную крышку на неправильный флакон с реактивами, это может привести к перекрестному загрязнению реактивов и их разрушению.Обязательно проводите тесты в хорошо освещенном месте. Будьте осторожны при использовании реагентов, так как они содержат химические вещества, которые могут повредить кожу (рекомендуется носить латексные перчатки). Держите растворы подальше от глаз и рта. Кроме того, не забывайте полностью убирать после каждого теста.
- Нанесите крошечный кусочек таблетки или порошка на большую белую керамическую тарелку. Используйте столько порошка, чтобы увидеть на тарелке.
- Выньте флакон с реактивом из безопасного пластикового контейнера. Снимите крышку и переверните флакон на пару дюймов над порошком.Выдавите на порошок одну каплю из флакона. Будьте осторожны, не позволяйте флакону с капельницей касаться порошка, иначе вы испортите и испортите остальной реагент. Заменить колпачок.
- Сразу обратите внимание на изменение цвета. Используйте соответствующие столбцы цветовой таблицы, прилагаемой к вашему набору, для оценки вашего теста.
Если реагент либо не меняет цвет в течение первых 30 секунд, либо дает другую последовательность изменения цвета, тогда таблетка определенно не содержит ни одного из вышеперечисленных веществ.Он также может быть сильно фальсифицирован одним или несколькими неизвестными веществами. Вы можете использовать другие реагенты DanceSafe на новых образцах, чтобы проверить наличие других веществ. Как можно скорее промойте испытательные поверхности водой с мылом.
Примечание по использованию реагентов Саймона и Фолина
Этапы аналогичны тем, что вы делали с другими нашими реагентами. Однако для этих двух реагентов требуется две бутылки с жидкостью (бутылки «А» и «В»). Вы еще раз соскребите крошечный кусочек таблетки на чистую белую тарелку, осторожно добавьте каплю жидкости из бутылки «A» (после этого плотно закрыв крышку), а затем добавьте к ней каплю жидкости из бутылки «B». .
Инструкции по хранению и обращению
Реагенты DanceSafe — это в первую очередь серная кислота с другими потенциально опасными химическими веществами, и они достаточно сильны, чтобы обжечь кожу и одежду. Беречь от глаз и рта. При работе с бутылкой и крышкой надевайте латексные перчатки. Если вы его испачкали, быстро смойте водой с мылом. Также промойте испытательные поверхности водой с мылом. Выбросьте нежелательные реагенты в раковину с проточной водой и пищевой содой. Храните все наборы для тестирования в холодном темном месте, например в холодильнике, между использованием.
ПРИМЕЧАНИЕ. Реагенты DanceSafe могут определять только присутствие , а не количество или чистоту определенного вещества. Реакции темного цвета будут иметь тенденцию отменять реакции на другие вещества, также содержащиеся в таблетке. Положительная или отрицательная реакция на какое-либо вещество не означает, что лекарство безопасно. Никакие наркотики не безопасны на 100%. Принимайте правильные решения.
Инструкция по тестированию МДМА

Инструкции по тестированию на кокаин

Инструкция по тестированию LSD

Инструкции по тест-полоскам на фентанил

