Гипопластическая и апластическая анемия: признаки, диагноз, лечение.
Гипопластическая и апластическая анемия – Anaemia hipoplastica et aplastica –называются остро протекающие заболевания системы крови, развивающееся в результате недостаточности (истощения) костномозгового кроветворения и проявляющиеся нормоцитарной, иногда макроцитарной, нормохромной анемией с сопутствующей тромбо- и гранулоцитопенией (панцитопенией).
Этиология. Причины дефицитных анемий – алиментарные факторы: недостаток в рационе кормления животных протеина, отдельных аминокислот, микроэлементов (железа, меди, кобальта), витаминов (В12, А, Д, С и других). Гипопластические анемии могут служить симптомами хронических гастро-энтероколитов, гепатитов, дистрофий печени, обусловленных пониженной усвояемостью питательных веществ (даже при полноценном кормление животных). Миелотоксические анемии у животных возникают в результате инфекций, инвазий и интоксикаций, чаще при хроническом течении (туберкулез, паратуберкулез, лептоспироз, листериоз, диктиокаулез, аскаридоз, мониезиоз, микозы, кетозы, эндометриты и др.). Анапластические анемии являются следствием воздействия на организм животного в больших дозах ионизирующей радиации (лучевая болезнь), отравления бензолом, соединениями свинца, ртути и других тяжелых интоксикациях.
Патогенез изучен слабо. Под влиянием вышеуказанных этиологических факторов у больного животного вначале развивается гипоплазия, а затем наступает аплазия костного мозга, если доза того или иного фактора достаточно долговременная. Причинные факторы, подавляющие костно — мозговое кроветворение, не вызывают разрушения эритроцитов, анемия развивается в основном за счет уменьшения их регенерации, да и не только их, а и всех клеточных элементов костного мозга. Поэтому наряду с развитием анемии отмечается лейкопения и тромбопения. Происходит одновременно повышение ломкости и порозности кровеносных сосудов, в результате у больного животного появляются кровоизлияния. В последующем пониженная фагоцитарная активность элементов соединительной ткани на фоне лейкопении и резко сниженной способности выработки антител ведет к развитию у животного бактериемии и сепсису.
Патологоанатомические изменения. Слизистые и серозные оболочки у павших животных бледные, часто с точечными и полосчатыми кровоизлияниями. В селезенке кровоизлияния. В легких, иногда в печени, почках и желудочно – кишечном тракте застойная гиперемия. В паренхиматозных органах и коже нередко устанавливаем некрозы. Костный мозг, особенно в трубчатых костях — бледный, местами желтый – жировой. В миокарде, печени и почках выраженная дистрофия.
Клинические признаки. На фоне основного заболевания (инфекция, инвазия, отравление) при гипопластической анемии у больного животного прогрессирует общая слабость, быстрая утомляемость, угнетение, отмечаем снижение продуктивности и работоспособности, появляются симптомы расстройства желудочно- кишечного тракта, сухость и взъерошенность кожного покрова, понижается эластичность кожи. При клиническом исследование больного животного устанавливаем характерный признак болезни — бледность видимых слизистых оболочек, склеры и кожи. При апластической анемии в сильной степени выражены общая слабость (иногда больные животные не в состоянии стоять на ногах), животные апатичные, при клиническом осмотре отмечаем бледность видимых слизистых оболочек и кровоизлияния на слизистых оболочках и коже.
Наряду с развитием у больного животного анемии отмечаем быстрое снижение количества лейкоцитов в крови и клеточных элементов в костном мозге. Количество гранулоцитов крови, молодых эритробластических форм и гранулофилоцитов в костном мозге снижается до минимума.
В лейкоцитарной формуле происходит нарастание процента нейтрофилов, а в миелограмме – миелобластических форм. При стахиоботриотоксикозе, чуме количество лейкоцитов крови снижается до 500-100 в 1мм³, резко выражен относительный лимфоцитоз, нейтропения, эозинофилы и моноциты исчезают, нарастает тромбопения. СОЭ ускорена. В костном мозге миелоидные элементы подвергаются дегенеративным изменениям. При тяжелом течении апластической анемии костный мозг становится опустошенным – отмечается бледность клеточными элементами костного мозга (панмиелофтиз). При исследовании обнаруживают в основном только гистиоцитарные и плазматические клетки, и единичные эритробластические формы.
В результате уменьшения массы кроветворной ткани эритропоэз становится явно недостаточным для поддержания состава крови на необходимом уровне; анемия прогрессирует, ее характер может отклонится в сторону гиперхромии. Гемоглобинизация эритроблостав совершается по типу эмбрионального эритропоэза; исчезновение ядра из клетки замедленно и совершается только путем кариорексиса.
Течение чаще острое и отличается своей злокачественностью. На фоне аплазии кроветворной ткани в организме развиваются вторичные инфекции, очаги некрозов, кровотечения и сепсис. Но бывают случаи медленного течения, причем патологические симптомы анемии постепенно усиливаются.
Диагноз на апластическую анемию ставится с учетом анамнеза (интоксикация, инфекция, инвазия), клинических симптомов (анемия, слабость) и анализа крови. Гематологически при гипо- и апластических анемиях устанавливают понижение уровня гемоглобина, лейкопению с преобладанием зрелых форм нейтрофилов, повешенную СОЭ. Характерной особенностью этих групп анемий в отличие от постгеморрагических и гемолитических является пониженное содержание в каждом эритроците гемоглобина при незначительном уменьшении в крови количества эритроцитов, что обуславливает низкий цветовой показатель (обычно хромных) эритроцитов, измененных патологических форм и размеров: пойкилоцитоз, анизоцитоз, большое количество микроцитов (малых размеров по сравнению с нормой), встречаются анулоциты (в виде колец), шизоцыты (в виде обрывков) и др. При исследовании пунктата костного мозга обнаруживают бледность клеточными элементами всех ростков, кровоизлияния.
Дифференциальный диагноз. Заболевание необходимо дифференцировать от гипопластических анемий, анемий при лейкозах у животных, лучевой болезни, ИНАН лошадей, чумы свиней.
Прогноз неблагоприятный.
Лечение. Прежде чем приступить к лечению, необходимо устранить этиологические факторы вызвавшие заболевание и угнетающие кроветворение. При наличии у больного животного тех или иных инвазионных, инфекционных заболеваний и отравлений необходимо проводить соответствующее лечение при данных заболеваниях. Больных животных обеспечивают полноценным рационом кормления с достаточным количеством содержания протеина, полным набором аминокислот, витаминов, макро- и микроэлементов. Для стимулирования костно- мозгового кроветворения необходимо применять препараты железа, кобальта, меди, мышьяка, кампонол, витамины К, В12, фолиевую кислоту и другие. Хорошее лечебное действие оказывает переливание гомогенной стабилизированной крови, внутримышечные или подкожные введения гомогенной или гетерогенной крови, гамма — и полиглобулинов согласно инструкциям и в дозах исходя из наставления по их применению.
При нарастающих симптомах интоксикации при комплексном лечении применяют сердечные средства, 20-40% раствор глюкозы с аскорбиновой кислотой.
При септических осложнениях применяют антибиотики, в том числе современные цефалоспоринового ряда. При полном истощении костного мозга лечить больное животное не целесообразно.
Апластическая анемия — симптомы, лечение, причины, прогноз
 Апластическая анемия – это наследственная или приобретенная патология крови, обусловленная поражением стволовых клеток костного мозга, вследствие которого развивается глубокое угнетение гемопоэза. Первые сведения о апластической анемии были получены еще в 1888 году, однако как самостоятельная нозологическая единица апластическая анемия была зарегистрирована только в 1904 году.
Апластическая анемия – это наследственная или приобретенная патология крови, обусловленная поражением стволовых клеток костного мозга, вследствие которого развивается глубокое угнетение гемопоэза. Первые сведения о апластической анемии были получены еще в 1888 году, однако как самостоятельная нозологическая единица апластическая анемия была зарегистрирована только в 1904 году.
Гипопластическая анемия относится к самой тяжелой форме нарушения кроветворения, так как летальность при апластической анемии достигает порога 80%.
Не следует путать апластичесую анемию, которая является отдельной нозологической формой с гипопластическим синдромом, который является лишь одним из многочисленных проявлений различных заболеваний, сопровождающихся нарушением функции кроветворения костного мозга.
К счастью, частота встречаемости случаев апластической анемии не превышает 5 эпизодов на 1000000 населения, но опасность данной патологии заключается в том, что она поражает в основном лиц детского и молодого возраста. Половая принадлежность не имеет влияния на течение и исход заболевания.
Апластическая анемия причины
Данная патология относится к категории полиэтиологичных заболеваний, то есть существует множество причин, одна из которых может занять доминирующую позицию и спровоцировать нарушение в системе кроветворения у того или иного больного. Кроме того, различают так называемые факторы риска, то есть предрасполагающие факторы, совокупность которых может не только поспособствовать развитию заболевания, но и усугубить течение патологического процесса. К счастью, в большинстве случаев удается распознать этиологический фактор, который стал первопричиной развития признаков анемии, но встречаются ситуации, когда определить этиопатогенетический фактор не удается и в таком случае устанавливается диагноз «идиопатическая апластическая анемия».
Часто апластиче
15. Гипо- и апластические анемии. Этиология, патогенез, картина крови.
АНЕМИИ ВСЛЕДСТВИЕ УГНЕТЕНИЯ ИЛИ ИСТОЩЕНИЯ КОСТНОГО МОЗГА. Они являются синдромом характерным для ряда патологических состояний, при которых наряду с панцитопенией снижается кроветворение в костном мозге.
К анемиям этого типа относятся гипопластические,апластические иметапластические анемии. Для всех анемий характерно угнетение кроветворения, носящее тотальный характер и проявляющееся уменьшением в периферической крови всех элементов, имеющих миелоидное происхождение — эритроцитов, лейкоцитов (гранулоцитов) и тромбоцитов, т.е. панцитопении. Картина костного мозга при всех разновидностях этих анемий поражает скудностью родоначальных элементов гемопоэза.Причинами гипо- и апластических анемиймогут быть различные экзо- и эндогенные факторы.Экзогенные факторы:ионизирующая радиация, токсические (бензол) и цитостатические химические вещества (эмбихин, допан, 6-меркаптопурин, миелосан, антагонисты фолиевой кислоты — аминоптерин), лекарства, обладающие токсико-аллергизирующим эффектом (пирамидон, атофан, барбитураты, сульфаниламиды, антибиотики, особенно левомицитин), инфекционные поражения костного мозга (врожденная анемия Фанкони).
К эндогенным этиологическим факторам относятся: гипотиреоз, гипопитуитаризм, доброкачественные опухоли тимуса, остеомиэлосклероз.
О том, что при апластических анемиях поражается в первую очередь стволовая клетка костного мозга, свидетельствует благотворный эффект трансплантации костного мозга.
Особое место занимают метапластические анемии, развивающиеся в результате метастазов раковой опухоли в костный мозг. В таких случаях картина анемии может сочетаться с появлением в крови миелоидной реакции, иногда анемия вообще не выражена, а в переферической крови находят значительное количество недифференцированных клеток гранулоцитарного и эритроцитарного ряда.
КАРТИНА КРОВИ при гипо- и апластических анемияххарактеризуется резким снижением всех костномозговых элементов — эритроцитов, лейкоцитов, тромбоцитов. Значительно снижается свертываемость крови, резко ослаблена фагоцитарная активность лейкоцитов и больные обычно погибают от кровотечения или сепсиса. Цветовой показатель обычно не изменен, пойкилоцитоз и
анизоцитоз не отмечаются. Наиболее важным и характерным признаком таких анемий является сочетание резкой анемии и почти полного отсутствия ретикулоцитов в крови. Соотношение эритроцитов и плазмы резко изменено и составляет 1:9. Столь резкое снижение показателя гематокрита (10 об.%) позволяет говорить об абсолютном уменьшении эритроцитов — олигоцитемической нормо или гиповолемии. Весьма типичным является резкое ускорение СОЭ до 90 мм в час.
16. Гемолитические анемии. Виды, причины, механизмы развития, картина крови.

17. нарушение физиологических функций и компенсаторно-приспособительные реакции при анемиях

18. гемолитическая болезнь новорожденных

19. железодефицитные и апластические анемии у детей


20. лейкоцитарная формула и ее нарушения в условиях патологии.

См. след вопросы, если хочешь подробнее описать
21.Лейкоцитытозы,Их виды, причины. Фазы лейкоцитарной реакции при инфекционных процессах.
Виды:
1.Истинный —Увеличение числа лейкоцитов, т.е. лейкоцитоз, может быть связано с усилением гемопоэза. обусловлен рядом физиологических причин: лейкоцитоз новорожденных, достигающий 10-20 Г/л, во время беременности и в предменструальном периоде. Относительный лейкоцитоз связан с увеличением определенных форм лейкоцитов
2.Распределительный-лейкоцитоз может быть связан с перераспределением лейкоцитов между различными участками сосудистого русла Распределительный лейкоцитоз чаще всего наблюдается в физиологических условиях. К группе причин, вызывающих такой лейкоцитоз, относятся:
физическая работа, пищеварение, эмоциональный стресс. Отличительными признаками распределительного лейкоцитоза является отсутствие изменений в лейкоцитарной формуле и функциональной активности клеток. (он бывает физиологическим и патологическим)
3. Патологический лейкоцитоз- чаще всего встречается при воспалительных процессах и лихорадке, сопровождающих инфекционные заболевания, являясь защитной реакцией организма против инфекта, интоксикации,
кровопотери, опухоли. Введение чужеродных белков также приводят к развитию лейкоцитоза.
4. ЛЕЙКОЦИТОЗ НЕИТРОФИЛЬНОГО ТИПА или НЕЙТРО-
ФИЛИЯ. Существует несколько типов нейтрофильного лейкоцитоза, в зависимости от того, насколько сильно выражено раздражение костно-мозговой ткани, насколько сильна регенерация. Эти типы нейтрофильного лейкоцитоза отличаются Друг от друга соотношением отдельных форм лейкоцитов между собой и харак-
теризуются различной степенью регенеративного сдвига ядра или, по Арнету, сдвига ядра влево.
А) НЕЙТРОФИЛЬНЫЙ ЛЕЙКОЦИТОЗ БЕЗ СДВИГА. Эта разновидность нейтрофилии, протекающая с увеличением абсолютного количества сегментоядерных лейкоцитов и сохраненным соотношением нейтрофильных форм, наблюдается при некоторых легко протекающих инфекциях, при нефрите, а также в первые сутки инфаркта миокарда, физиологическом лейкоцитозе, при введении норадреналина.
Б) НЕЙТРОФИЛЬНЫЙ ЛЕЙКОЦИТОЗ С ГИПОРЕГЕНЕРАТИВНЫМ
СДВИГОМ характеризуется преимущественным увеличением содержания палочкоядерных форм свыше 6 %. Наблюдается при легко текущих инфекционных заболеваниях, ангине, после некоторых операций, при аппендиците и т.д.
В) НЕЙТРОФИЛЬНЫЙ ЛЕЙКОЦИТОЗ С РЕГЕНЕРАТИВНЫМ СДВИ-
ГОМ характеризуется, наряду с возрастанием числа палочкоядерных форм, увеличением юных или метамиелоцитов. Этот тип нейтрофилии регистрируется при крупозной пневмонии, сыпном тифе, абсцессах, малярии и др.
Г) НЕЙТРОФИЛЬНЫЙ ЛЕЙКОЦИТОЗ С ГИПЕРРЕГЕНЕРАТИВНЫМ
СДВИГОМ сопровождается столь выраженным раздражением костного мозга,что в крови, кроме увеличенного содержания палочкоядерных и юных нейтрофилов, появляются миелоциты. Если подобная картина сопровождается не увеличением общего количества лейкоцитов, а уменьшением их числа, это указывает на начинающуюся депрессию регенераторных возможностей костного мозга, что является неблагоприятным прогностическим признаком. Наблюдается этот тип при тяжелых инфекционных заболеваниях, сепсисе, эмпиемах легкого, тяжелых перитонитах и т.д.
5. «ЛЕЙКЕМОИДНАЯ РЕАКЦИЯ», т.е. напоминающая лейкоз протекает с появлением большого количества нормальных и патологических клеток, начиная с метамиелоцитов и кончая миелобластами. (Лейкемоидные
реакции бывают нейтрофильные, эозинофильные, моноцитарные, в виде реакций двух и трех ростков кроветворения (эритроцитоз, тромбоцитоз, лейкоцито)
6. ЭОЗИНОФИЛЬНЫЕ ЛЕЙКОЦИТОЗЫ. Эозинофилы представ-
ляются наиболее чувствительными клетками по отношению к инфекции и ин-
токсикаци, но потом они исчезают. Эозинофилия наблюдается в период выздоровления после многих инфекционных заболеваний. Появление эозинофилов в этот период является первым признаком благоприятного симптома. Увеличение эозинофилов при аллергии обусловлено наличием в них ферментов, разрушающих такие медиаторы как гистамин и простагландины, а также инактивирующих гепарин.
7. БАЗОФИЛЬНЫЙ ЛЕЙКОЦИТОЗ. Наблюдается при сенсибилизации,
хроническом миелоидном лейкозе. Базофилы функционально объединены с тучными клетками в клеточную систему гепариноцитов. Кроме того, в базофилах и тучных клетках содержится большое количество других биологически активных веществ — гистамина, простагландинов. Базофилы и тучные клетки могут освобождать гепарин и гистамин при дегрануляции клеток. При анафилактическом и пептонном шоках отмечается резкое увеличение содержания гепарина и гистамина в крови и одновременно с этим наблюдается уменьшение гранул в тканевых тучных клетках и базофилах.
8. МОНОЦИТАРНЫЙ ЛЕЙКОЦИТОЗ (МОНОЦИТОЗ) является признаком раздражения ретикуло-эндотелиальной системы, ее ответной реакцией на
инфекцию и интоксикацию. Поэтому моноцитоз наблюдается при ряде инфекционных заболеваний, например натуральной оспе, кори, сыпном тифе и т.д. моноцитоз является предвестником начинающегося кризиса ряда инфекционных заболеваний и рассматривается как «моноцитарная фаза защиты».
9. ЛИМФОЦИТАРНЫЙ ЛЕЙКОЦИТОЗ (ЛИМФОЦИТОЗ)
может наблюдаться и в физиологических условиях и при патологических процессах. Лимфоцитоз наблюдается при многих инфекцион-
ных заболеваниях. Увеличение количества лимфоцитов связано с ваготонией,как это наблюдается после лихорадочного периода, и с алколозом
Изменение лейкоцитов в крови могут носить двоякий характер: 1.немедленный-связанный с перераспределением крови
2.более замедленный, обусловленный процессом клеточного деления
Распределение лейкоцитов осуществляется под влиянием нервных и гуморальных стимулов при помощи изменения просвета сосудов кровеносного
русла, кровяного давления, скорости кровотока и т.п
Фазы реакции: Лейкоцитарные реакции протекают в виде лейкоцитоза или лейкопении.
22.Лейкопении. Причины. Механизмы развития
Уменьшение общего количества лейкоцитов, или лейкопения, представляет
собой в подавляющем большинстве случаев функциональное состояние системы лейкоцитов, связанное с нарушением процесса кроветворения, с повышением разрушения лейкоцитов, или же процессами кровераспределения.
Причины:
НАРУШЕНИЯ КРОВЕТВОРЕНИЯ
2.Повышенной потери или РАЗРУШЕНИИ ЛЕЙКОЦИТОВ, при недостаточных компенсаторных возможностях костного мозга
3. перераспределение крови в организме.
Задержка лейкоцитов в сосудах органов-депо может наблюдаться при некоторых инфекциях, сопровождающихся лейкопенией. Селезенка может задерживать большие количества крови, так как является основным депонирующим органом.
Наибольшее значение среди всех разновидностей лейкопений принадлежит,
бесспорно, уменьшению количества зернистых лейкоцитов или агранулоцитозу.АГРАНУЛОЦИТОЗ может развиваться в результате действия различных причин. Это может быть поражение костного мозга и подавление гранулопоэза. В таких случаях, по сути дела, мы имеем лейкопению, связанную с нарушением кроветворения. Однако значительно чаще встречаются агранулоцитоз лекарственного происхождения, и в этих случаях по своему механизму он связан с разрушением лейкоцитов как в крови, так и в костном мозге в результате иммунологического конфликта. Основные
симптомы заключаются в появлении некротических явлений и язв в полости
рта, зева, гортани, реже легкого, кишечника, кожи, а в разгар болезни развивается картина сепсиса. Изменения крови при агранулоцитозе характеризуются резкой лейкопенией (количество лейкоцитов 1000 и меньше в 1 мкл) нейтропенией,вплоть до полного исчезновения нейтрофилов, и эозинопенией, на фоне которых наблюдается относительный лимфоцитоз

23.Понятие лейкоза. Классификация и этиология лейкоза.
Лейкоз представляет собой заболевание, при котором происходит опухо-
левая мутация гемопоэтической ткани и на определенном этапе увеличение количества лейкоцитов в крови, нередко с преобладанием лейкозных клеток. Лейкозы являются первичными опухолевыми процессами костного мозга.
Основной признак:любого лейкоза является пролиферация
одной из лейкопоэтических тканей. что пролиферация эта носит генерализованный, непрерывный и неопластический
характер, продолжается вплоть до смерти организма-хозяина,
КЛАССИФИКАЦИЯ ЛЕЙКОЗОВ
1.Острые. (Начинается он постепенно, но манифестация очень быстрая. Характеризуется бессимптомным началом с постепенным развитием слабости, недомогания, болей в костях и суставах с субфебрильной температурой, Нередко заболевание начинается внезапно по типу острого сепсиса или ангины)
1.Недифференцированный
2. Миелобластный
3. Лимфобластный и плазмобластный
4. Монобластный (миеломонобласт-
ный)
5. Эритромиелобластный
6. Мегакариобластный
Апластическая анемия | Орфанные заболевания
Одной из патологий костномозгового кроветворения, угнетающей продукцию кровяных клеток — лейкоцитов, эритроцитов и тромбоцитов, является апластическая анемия. Симптоматика заболевания обусловлена тромбоцитопенией, лейкопенией и анемией. Ключевые признаки апластической анемии: кожные геморрагии, кровоточивость слизистых оболочек, слабость, одышка, воспаления, инфекции. Диагноз подтверждается на основе результатов гистоморфологического анализа биоптата, миело- и гемограммы. При апластической анемии применяют иммуносупрессивную терапию, гемотрансфузии, ТКМ.
Общие сведения, что такое апластическая анемия (разновидности, формы)
Апластическая или гипопластическая анемия (АА) представляет собой тяжелое расстройство гемопоэза, сопровождающееся инфекционными осложнениями, а также геморрагическим и анемическим синдромом. В 1988 году патология была впервые описана немецким иммунологом и лауреатом Нобелевской премии П. Эрлихом (Paul Ehrlich). Как правило, при апластической анемии нарушена выработка всех видов кровяных клеток, но в некоторых случаях костный мозг не способен нормально вырабатывать только эритроциты. На основе данного фактора заболевание разделяют на парциальную и истинную апластическую анемию (пангемоцитопению). Встречаемость болезни составляет 2-4 случая на 1 млн. населения в год. Может возникать как у детей, так и взрослых с аналогичной частотой у обоих полов. Пик заболеваемости у детей приходится на 9-10 лет, у взрослых 25-27 и 50-60 лет.
Существует приобретенная и врожденная форма апластической анемии. В первом случае заболевание развивается на протяжении жизни вследствие эндогенных факторов и внешних воздействий. Во втором, апластическая анемия возникает на фоне хромосомных нарушений. Этиология приобретенной формы в большинстве случаев не известна. Лишь у 20 % пациентов идентифицируют этиологический фактор приобретенной АА. Врожденная форма заболевания характерна для детей 8-10 лет. В зависимости от происхождения, апластическую анемию классифицируют на идиопатическую, гепатит-ассоциированную, поствирусную и лекарственную форму различной степени тяжести.
МКБ-10. Апластической анемии присвоен код D61.9.
Причины
Исследователи доказали, что угнетение гемопоэза обусловлено возникновением в крови и костном мозге естественных киллеров и цитотоксических T-лимфоцитов, которые подавляют пролиферацию гемопоэтических клеток-предшественников.
К ряду основных причин развития АА относят:
- Взаимодействие с вредными химическими и физическими агентами (мышьяк, гербициды, соли золота и металлов, бензольные соединения и др.), а также высокодозное ионизирующее облучение.
- Использование медпрепаратов с миелотоксическим эффектом, в том числе, цитостатиков, психотропов, антибактериальных, антитиреоидных и других средств. Развитие тяжелой формы апластической анемии нередко провоцирует прием нестероидных противовоспалительных средств.
- Поражение вирусными агентами. Наиболее часто апластическую анемию вызывает перенесенный гепатит. Реже подавлению миелопоэза способствует грипп, цитомегалия, доброкачественный лимфобластоз, вирус иммунодефицита человека.
Кроме того, АА развивается на фоне наследственности, туберкулеза, иммунных заболеваний (карцинома тимуса, синдром Шульмана, гипогаммаглобулинемия и т.д.), интоксикации, лучевой болезни. Были описаны случаи анемии, вызванной беременностью. Апластические анемии без выявленной причины развития, относят к идиопатической форме.
Патогенез
Нарушение дифференцировки или повреждение гемопоэтических стволовых клеток лежит в основе патогенеза апластической анемии. В случае приобретенной формы болезни на фоне влияния этиологических факторов активируются Т-лимфоциты, вырабатывающие пептидные информационные молекулы (цитокины), которые поражают клетки-предшественники кроветворения, что приводит к пангемоцитопении. Врожденной апластической анемии предшествуют кариотипические отклонения от нормы, вследствие которых нарушается восстановление дезоксирибонуклеиновой кислоты и прекращается процесс синтеза стволовых клеток.
Классификация
Апластическую анемию классифицируют не только в соответствии с причинными факторами. Патологию также разделяют на острую, подострую и хроническую форму в зависимости от времени течения патопроцесса. Острая форма протекает до 30 дней, подострая с 1 до 6 месяцев, а хроническая от полугода и более. По уровню снижения показателей крови выделяют сверхтяжелую, тяжелую и умеренную форму АА.
Симптомы апластической анемии
Дефицит тромбоцитов, лейкоцитов и эритроцитов сопровождается следующими проявлениями:
- Геморрагический синдром, при котором отмечается повышенная кровоточивость десен, меноррагии, появление петехий, носовые кровотечения. При тяжелых формах АА возможны желудочно-кишечные и маточные кровотечения, гематурии (наличие крови в моче).
- Анемический синдром характеризуется частыми головокружениями, повышенной утомляемостью, общей слабостью. Часто у пациентов наблюдается одышка, бледность кожи, покалывания в области сердца, учащенный пульс, головные боли, шум в ушах.
- Инфекционные осложнения. Недостаток лейкоцитов в крови приводит к частым инфекционным заболеваниям (ОРВИ, пневмония, стоматит и др.), которые плохо поддаются терапии.
В случае врожденной апластической анемии симптоматика проявляется у детей до 9-10 лет. Кроме аплазии костного мозга наблюдается микроцефалия (недоразвитие черепа и мозга), порок развития мочеполовой системы у мальчиков, гипоплазия почек, тугоухость. Также врожденная апластическая анемия у детей может сопровождаться аномалиями конечностей, низкорослостью, гиперпигментацией кожи.
Осложнения
Наиболее опасные осложнения данной патологии — внутримозговое кровоизлияние, затяжные инфекционные процессы, анемическая кома, геморрагия внутренних органов, иммунодефицит.
Диагностика
При подозрениях на апластическую анемию для безошибочной постановки диагноза врачи после физикального осмотра назначают комплексное обследование, состоящее из следующих процедур:
- Клинический анализ крови, определяющий компонентную долю всех трех видов кровяных клеток, а также уровень ретикулоцитов и гемоглобина.
- МРТ, КТ — методы исследования масштабности поражения костной ткани, состояния внутренних органов, лимфатических узлов.
- Биопсия костного мозга — забор биоптата костного мозга для цитогистологии, позволяющей выявить патоизменения в системе кроветворения и составе крови, установить степень тяжести АА.
- Молекулярно-генетические тесты на предмет хромосомных аномалий.
Кроме того, пациентам назначают рентгеновскую томографию и рентген грудной клетки, УЗИ малого таза и брюшной полости, эхокардиографию. АА дифференцируют с лейкемией миелодиспластическими синдромами и разными видами анемии.
Лечение апластической анемии
Для пациентов с гипопластической анемией в больницах функционируют спецотделения, где обеспечивают абсолютную изоляцию и стерильные условия, что исключает осложнения на фоне инфекций. Разработка протокола лечения зависит от тяжести течения болезни, сопутствующих патологий. В терапевтическую программу входит несколько методов:
- Применение антибактериальных, противовирусных и анаболических препаратов, а также иммунодепрессантов, гликопротеидов, стероидных гормонов.
- Поэтапная иммуносупрессивная терапия, при которой в течение года и более используют антитимоцитарный глобулин и циклоспорин А. Данные средства улучшают функцию кроветворения и позволяют добиться длительной выживаемости. Абсолютные противопоказания к иммуносупрессивной терапии — дыхательная и сердечнососудистая недостаточность, тяжелые соматические состояния.
- Трансфузионная терапия — переливание донорского тромбоконцентрата и эритроцитарной массы с целью восполнения дефицита кровяных телец. Может также потребоваться дискретный плазмаферез (очищение плазмы центрифугированием).
При неэффективности других вариантов лечения сверхтяжелой формы апластической анемии хирурги проводят аллогенную трансплантацию костного мозга (ТКМ), которая является хорошей перспективой для долгосрочного выживания. Если для пересадки стволовых клеток нет совместимого донора, врачи пересаживают реципиенту донорские клетки периферической крови. При апластической анемии умеренной степени тяжести могут назначать малоинвазивную спленэктомию (тотальное удаление селезенки).
Профилактика и прогноз
В качестве профилактических мер следует избегать негативного воздействия экзогенных факторов, неправильного использования медпрепаратов. Прогностическая картина определяется тяжестью течения и формой АА. Инфекционные осложнения, частые кровотечения и прогрессивное течение болезни значительно ухудшают прогноз. Стойкой и длительной ремиссии удается достичь практически в 87 % случаев после ТКМ.
что это такое, симптомы, причины и лечение
Апластическая анемия — это частный случай нарушения синтеза эритроцитов, сопровождается падением концентрации гемоглобина в результате отклонения в работе костного мозга.
В отличие от прочих форм нарушения, например железодефицитной, мегалобластной, патология куда сложнее излечивается, имеет худшие прогнозы.
Клиническая картина сама крайне опасна, несет большую угрозу для существования организма. Процесс дает кровотечения различной локализации, которые трудно остановить.
Диагностика представляет определенные сложности по причине отсутствия специфических клинических признаков, если проводить исследование рутинными способами.
Лечение строго стационарное. Длительность его неопределенно высокая, зависит от тяжести патологического процесса, характера его течения, агрессивности, стадии, также индивидуальных особенностей организма человека, первичной причины становления нарушения.
Механизм становления нарушения
В основе патогенеза расстройства лежит группа патогенетических факторов. Можно назвать четыре основных момента, которые и играют роль в формировании диагноза.
Прием некоторых лекарственных препаратов
Искусственное угнетение синтеза эритроцитов и незрелых клеток-предшественников.
Работу костного мозга нарушает группа медикаментов. Таким эффектом обладают цитостатики, которые активно применяются в лечении опухолей, особенно злокачественных.
Иммунодепрессанты, противосудорожные средства, лекарства для борьбы с малярией, некоторые гормональные медикаменты, а также фармакологические наименования для коррекции работы щитовидной железы.
Так или иначе побочный эффект не может длиться долго, но гипопластическая анемия протекает остро, достаточно и одного эпизода, чтобы создать большие риски для жизни. Отмена медикаментов становится первым шагом на пути к выздоровлению.
Вирусные поражения
Угнетать работу костного мозга могут и некоторые инфекционные структуры. В частности такой способностью обладают агенты гепатита, цитомегаловирус, штамм герпеса четвертого типа (Эпштейна-Барр). В том числе микобактерии туберкулеза.
При остром течении названных патологий апластической анемии может и не быть. Однако резко вырастают риски развития в ближайшем будущем.
Взаимодействие с химическими отравляющими компонентами
Гербицидами, средствами на основе ртути, мышьяка, бензола, органических спиртов, также прочих веществ, щелочных металлов, синильной кислоты.
Восстановление в таком случае требует исключения влияния отравляющего соединения на организм человека.
Воздействие ионизирующего излучения
Радиация сказывается на состоянии костного мозга в большей степени, что и провоцирует возможные кровотечения у пораженных людей. По мере выздоровления апластическая анемия постепенно отходит.
Названные этиологические факторы — это провокаторы, они выступают виновниками начала расстройства.
Далее же отклонение движется по одному выверенному сценарию.
Угнетается работа красного костного мозга и процесс кроветворения. Он перестает генерировать незрелые клетки, предшественники форменных, полноценных.
Отсюда снижение концентрации эритроцитов, а значит и гемоглобина, который участвует в перемещении кислорода по тканям и органам через кровеносное русло. Происходит замещение красного костного мозга — желтым, что только усугубляет аплазию.

Недостаточная транспортировка кислорода вызывает гипоксию. Клетки не могут дышать. Страдают все ткани организма.
Падает концентрация тромбоцитов, повышается текучесть крови, растут риски летальных кровотечений.
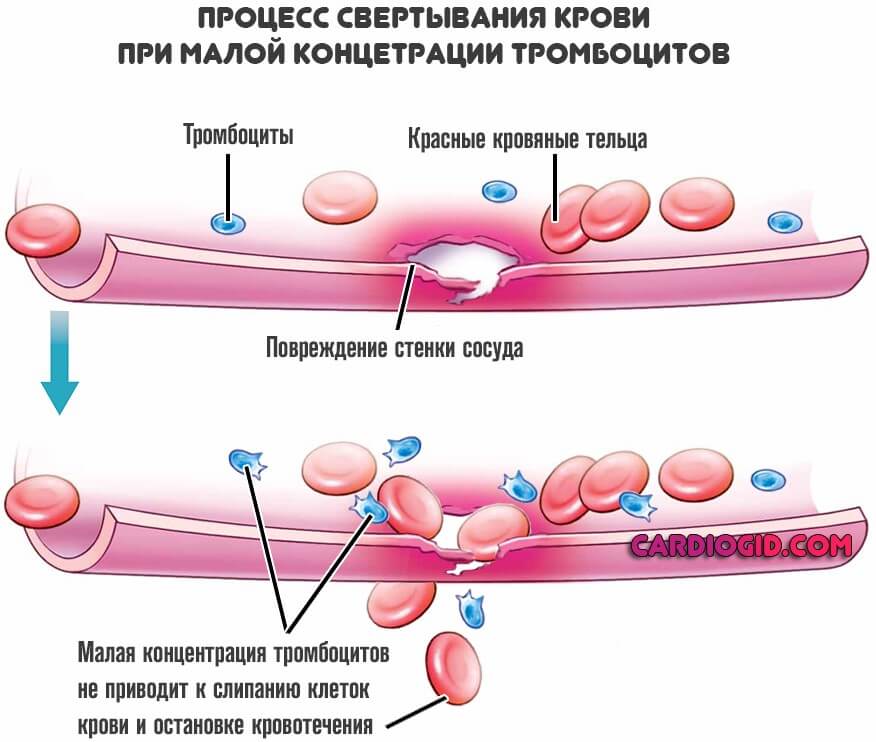
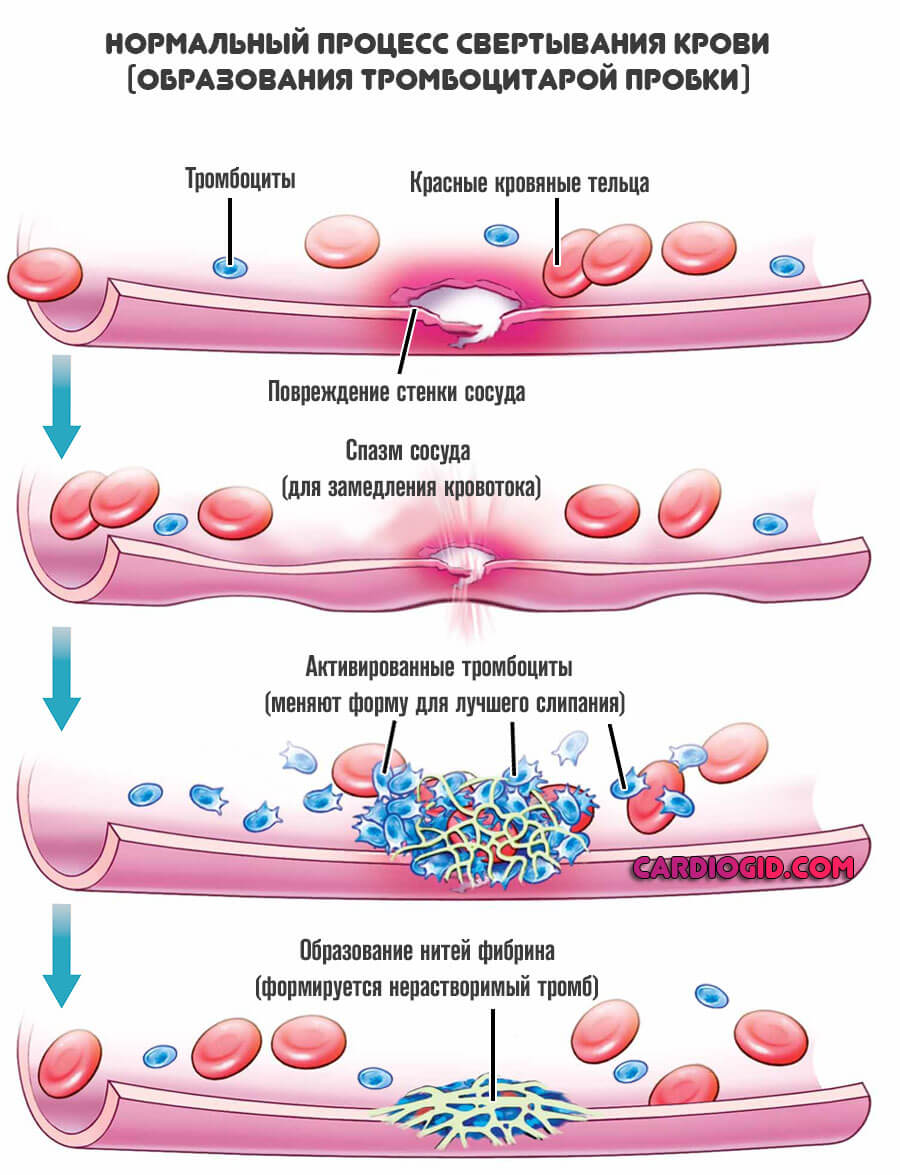
Восстановление заключается в избавлении от причины проблемы. Только так можно рассчитывать на излечение. Для грамотного терапевтического влияния требуется знать точный механизм.
Классификация
Типизацию проводят по степени тяжести апластической анемии. По этому критерию выделяют три основных формы болезни.
- Легкая. Сопровождается минимальными изменениями синтеза клеток. Возникает избыточная выработка некоторых химических веществ. Однако на этой стадии человек пока не замечает симптомов.
В редких случаях возможно образование на коже небольших язв, красных пятен. Кроме того, возникают носовые кровотечения. Обнаруживаются базовые анемические симптомы: головная боль, слабость, тошнота, прочие, в том числе снижение работоспособности. Это идеальный момент для начала лечения.
- Средняя степень. Дает уже выраженную клинику, которую трудно не заметить. Присутствуют полные геморрагические и анемические проявления. Качество жизни серьезно снижается. Летальные риски отмечаются, но пока сравнительно низкие. Показатели тромбо- и гранулоцитов находятся в пределах умеренного снижения.
- Тяжелая степень. Клиника полная, есть реальные риски смерти.
Это крайняя фаза, она же терминальная. Наблюдаются массивные нарушения работы организма, критические осложнения влекут за собой смерть пациента. Не всегда эффект дают даже полные лечебные мероприятия.
Второй способ классификации — по характеру заболевания.
Выделяют:
- Врожденную форму. Часто обнаруживаются генетические дефекты в качестве непосредственного фактора-виновника нарушения. У детей и молодых людей до 25 лет манифестация диагноза наблюдается наиболее часто. Второй пик приходится на период после 50, но уже гораздо реже.
- Приобретенную форму апластической анемии. Встречается почти в 80% случаев. Становится результатом заболеваний. В том числе онкологических, эндокринных расстройств и других возможных.
Используется классификация по агрессивности и характеру течения:
- Острая форма. Сопровождается резким падением количества форменных клеток крови, выраженной клинической картиной. Наиболее часто встречается именно этот тип процесса. О нем говорят в том случае, если симптоматический комплекс наблюдается в течении до 1 месяца.
- Подострая форма. От 30 дней до полугода. Сопровождается относительно вялой клинической картиной. Однако опасность от этого меньше не становится.
- Хронический тип. Длительность свыше 6 месяцев.
Наконец, классифицировать заболевание можно по происхождению, этиологии.
Соответственно называют:
- Первичное расстройство. Обусловлено генетическими дефектами. Присутствует с человеком явно или скрыто с самого рождения.
- Вторичная форма. Встречается в результате перенесенных прочих отклонений.
Не всегда врач с ходу и даже после тщательной диагностики может обнаружить причины патологического процесса, в такой ситуации говорят об идиопатической апластической анемии.
По мере дальнейшего обследования возможен пересмотр диагноза. В зависимости от итогов диагностики.
Симптомы
Клиническая картина определяется двумя основными синдромами. Первый — собственно анемический. Результат недостаточного питания тканей организма, также кислородного голодания.
Проявления таковы:
- Слабость. Астенические явления — это симптомы апластической анемии, которые присутствуют на протяжении всего периода течения патологического процесса. Восстановление спонтанное.
- Одышка. После незначительной физической нагрузки. Также в состоянии полного покоя.
- Тахикардия. Увеличение частоты сердечных сокращений до 120-150 ударов в минуту. Независимо от текущего положения тела, характера активности (или ее отсутствия).
- Тошнота, рвота. Временные явления. Переносятся пациентом тяжело. Возникают периодически.
- Головная боль. Интенсивность может быть самой разной. Локализация также. Сопровождается прочими неврологическими проявлениями. В том числе со стороны органов зрения.
- Мерцание мушек в глазах. Фотопсии. Ложное ощущение света в поле видимости. Результат раздражения затылочной доли мозга, ирритации коры и недостаточного кислородного обеспечения.

- Головокружение. Нарушение нормальной ориентации в пространстве, также координации движений.
- Сонливость. В течение дня. Независимо от количества часов отдыха в сутки. В ночное время возможен обратный эффект.
- Общее снижение работоспособности.
- Когнитивные нарушения. Падение качества и скорости мышления, памяти. Временное расстройство.
- Обморочные состояния. Особенно после вставания с места и перемены положения тела в пространстве.
Второй синдром в рамках диагноза — геморрагический. Сопровождается типичными признаками:
- Частые инфекционные поражения. В результате нарушения работы защитных сил организма. Регулярно возникают острые респираторные заболевания. Кроме того, повышаются риски приобретения опасных расстройств по типу ВИЧ, туберкулеза. Сопротивляемость существенно падает.
- Носовые кровотечения. В результате снижения концентрации тромбоцитов, которые ответственны за нормальную свертываемость. Повышается проницаемость капилляров, их ломкость.
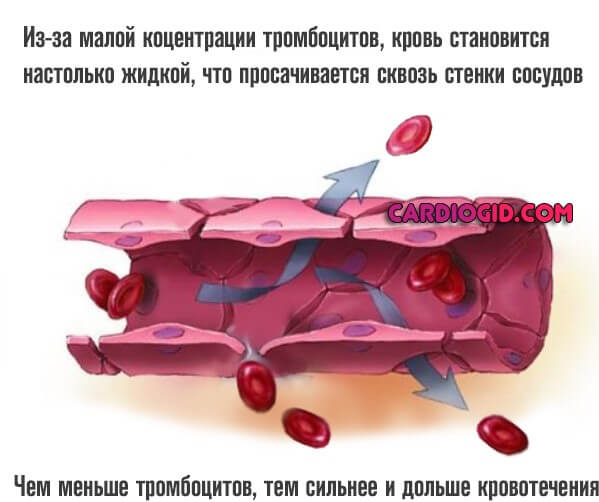
- Меноррагия. Расстройство менструального цикла. Обильные месячные возникают у каждой второй больной женщины. В том числе возможны и вне циклических изменений. Спонтанно.
- Стоматиты. Нарушения целостности слизистых оболочек органов, полости рта, носа. Образование язв, прочих дефектов.

- Увеличение размеров селезенки. Вплоть до критического состояния с разрывом органа, массивным кровотечением и потенциальной вероятностью гибели пациента от осложнений. Сепсиса.
- Общее снижение иммунитета. Сказывается инфекционными поражениями, прочими состояниями.
- Высыпания на коже. Петехии (небольшие красные пятна), сосудистые звезды, гематомы, синяки — характерные признаки апластической анемии. Возникают из за малой концентрации тромбоцитов в крови.

Аплазия костного мозга потенциально смертельное расстройство, симптоматика нарастает постоянно, по мере прогрессирования патологического процесса. Восстановление должно быть срочным.
Причины
Факторы становления множественны. Среди непосредственных виновников можно назвать:
- Перенесенные инфекционные расстройства. Гепатит разных видов, туберкулез, поражение герпетическими агентами.
- Применение некоторых лекарственных средств, как уже было сказано ранее.
- Облучение радиацией. В том числе при длительном воздействии небольших некритичных доз. Особенно подвержены этому расстройству работники АЭС, служащие на подлодках, прочие категории.
- Врожденные генетические аномалии.
- Доказана связь с беременностью. Однако специалисты пока не могут сказать, является ли гестация непосредственной причиной начала аномальных изменений в организме или же выступает провокатором манифестации расстройства.
- Заболевания лимфатической системы.
- Опухоли, особенно злокачественные.
Несмотря на всю эффективность диагностики, причины можно обнаружить не всегда. Примерно в 50% случаев речь идет об идиопатической разновидности анемии. Когда провокатора найти невозможно. По крайней мере, в момент выставления диагноза и его верификации.
Потребуется еще не одна неделя, а то и месяцы работы в этом направлении, динамическое наблюдение за состоянием больного.
Диагностика
Обследование представляет довольно серьезные трудности, поскольку надежных критериев пока нет, также врачи ограничены в выборе методик. Задача ложится на плечи гематолога.
Среди возможных мероприятий:
- Устный опрос больного. Нужно установить все присутствующие жалобы, чтобы составить полную клиническую картину. Это важно, поскольку позволяет выдвинуть гипотезы относительно состояния человека.
- Сбор анамнеза. Перенесенные ранее болезни, момент развития, начала симптоматических проявлений, вредные привычки, образ жизни, особенно важно установить семейную историю болезней.
- Общий анализ крови. Лабораторное исследование используется для оценки концентрации форменных клеток (эритроцитов), уровня гемоглобина, прочих показателей. Довольно информативная методика несмотря на простоту.
- Обязательно проводится исследование биохимическое. Оценке подлежат печеночные пробы, уровни специфических веществ: билирубина, щелочной фосфатазы.
- Хорошей методикой ранней диагностики и верификации диагноза выступает пункция костного мозга для забора материала (биопсия). Используется наиболее часто в качестве крайней меры. Ввиду инвазивности (травматичности) применяется не всегда.
- Возможно назначение консультации генетика. По показаниям.

Диагностика требует терпения, хотя время на полное обследование есть не всегда. По мере дальнейшего или повторного курса возможен пересмотр изначально установленного заболевания.
Лечение
Эффективных медикаментозных методик практически нет. Основная задача — борьба с первопричиной, это может потребовать больших усилий.
Терапия в обязательном порядке проходит в стационаре. Пациента помещают в практически стерильные условия. Изолируют, чтобы не спровоцировать инфекционного поражения.
Практикуется несколько методов терапии анемии апластического типа:
- Влияние на иммунитет. Применяются препараты для коррекции работы защитных сил организма, обычно это иммуносупрессоры параллельно с гормонами.
- Переливание крови, а именно форменных клеток — тромбоцитарной и эритроцитарной массы. Мера временная, позволяющая восполнить дефицит этих телец. Переливание не делают при аутоиммунных заболеваниях.
- Возможно проведение плазмафереза. Очищения жидкой фракции крови, чтобы не провоцировать осложнения и замедлить прогрессирование патологического процесса.
Наиболее эффективный и, пожалуй, единственно действенный способ лечения апластической анемии в долгосрочной перспективе, это пересадка костного мозга. Ввиду малого количества совместимых доноров, велика вероятность длительного ожидания.
Речь идет о годах. Потому применение столь эффективной методики практикуется сравнительно редко.
На весь период лечения необходимо отказаться от курения, спиртного, прочих вредных привычек.
В целом же, устранение причины апластической анемии, ее симптомов — крупная проблема гематологии, задача восстановления решается с большим трудом.
Прогноз
Перспективы довольно туманны. Заболевание слишком серьезно для того, чтобы давать усредненные выкладки по прогнозу жизни. На вероятность выздоровления влияет группа факторов:
- Тяжесть патологического процесса, его агрессивности.
- Характер и длительность течения расстройства.
- Скорость прогрессирования.
- Семейная история.
- Возраст. Чем старше пациент, тем хуже в целом прогнозы. Хотя возможны и исключения.
- Наличие геморрагического синдрома.
- Присутствие и степень инфекционных осложнений.
Чем больше негативных факторов присутствует, тем меньше шансы на успешное восстановление.
В то же время нужно иметь в виду, что трансплантация костного мозга позволяет добиться положительного исхода почти в 90% случаев. Вопрос только в подборе донора.
Возможные осложнения
Среди последствия, с которыми встречаются пациенты:
- Выраженные массивные кровотечения. Потенциально летальные.
- Разрыв селезенки.
- Инвалидность, смертельный исход.
При остром течении прогнозы существенно хуже, меньше времени на реагирование, диагностику, помощь. Риски больше.
Угнетение костномозгового кроветворения (аплазия) провоцирует анемию, нарушение снабжения тканей организма, кислородом. Помимо этого, изменяются реологические свойства крови и присутствуют реальные угрозы смерти от осложнений.
Важно провести качественное лечение в условиях стационара. Основная проблема заключается в малом арсенале методик восстановления, курации.
Однако даже без возможности сиюминутной трансплантации есть все шансы устранения основных проявлений заболевания, поддержки организма. Это позволяет «протянуть» до подбора донора и коррекции.
Характерный признак гипопластической и апластической анемии
Содержание статьи
Какие бывают болезни крови
- Распространенность среди населения
- Причины
- Классификации
- Болезни с анемическим синдромом
- Болезни с проявлением язвенно-некротических изменений
- Болезни с геморрагическими изменениями
- Болезни с увеличением лимфоузлов
- Болезни с повышением температуры тела
- Болезни с выраженной интоксикацией
- Болезни с болями в суставах и костях
- Болезни с иммунодефицитом
- Болезни с нарушение содержания белка в плазме
- Болезни с увеличением печени и селезенки
- Как предупредить болезни крови
Заболевания крови связаны с различными нарушениями количества форменных элементов, их строения, размеров или свойств плазмы. В медицине более принят термин «системные заболевания крови». Он представляет более широкое понятие и включает патологию органов, продуцирующих эритроциты, тромбоциты и лейкоциты (костный мозг, лимфатические узлы и селезенку).
Распространенность среди населения
Многие годы безуспешно боретесь с ГИПЕРТОНИЕЙ?
Глава Института: «Вы будете поражены, насколько просто можно вылечить гипертонию принимая каждый день…
Читать далее »
По количеству больных заболевания крови не входят в «15 болезней», определенных Всемирной Организацией Здравоохранения как наиболее распространенные в мире.
Но в России статистика указывает на очень неутешительные цифры: по сравнению с 1990 годом заболеваемость населения болезнями системы крови выросла в 3,6 раза.
Это вызвало необходимость развития гематологических исследований, поиска средств борьбы с патологией, дополнительного расширения количества профильных коек в специализированных стационарах, обучения врачей всех специальностей.
От врачей первичного звена требуется знать, какие клинические проявления бывают связаны с патологией крови и кроветворных органов, чтобы своевременно направить пациента к гематологу.
Причины
Изучено множество причин, приводящих к изменениям в крови. Но остается еще больше загадок. Ученые считают, что вправе указывать в таких случаях на факторы риска.
- острые и хронические кровопотери приводят к нарушениям кровообразования, усиленному распаду клеток при анемиях;
- мутации генома человека под воздействием химических веществ (цитостатиков, антибиотиков, пром
7.4. Апластическая анемия.
Апластическая анемия – разнородная группа гематологических заболеваний, морфологическим признаком которых является панцитопения в периферической крови и глубокая гипоплазия или аплазия миелоидной ткани. Развитие апластической анемии обусловлено большим числом эндогенных и экзогенных факторов, вызывающих качественные и количественные изменениями со стороны стволовой клетки и ее микроокружения.
Эпидемиология.
Апластическая анемия — достаточно редкое заболевание: его средняя частота в Европе и США составляет 4-6 случаев на 1 миллион жителей в год. Чаще всего апластическая анемия развивается у лиц до 20 и старше 65 лет, что может быть связано с преобладанием этиологической роли вирусов у лиц молодого возраста и химических веществ — у пожилых людей. Свое подтверждение эта гипотеза находит в исследованиях, проведенных в Китае и Юго-Восточной Азии. Эти регионы, где частота апластической анемии в 3-4 раза выше среднемировой, характеризуются широким распространением вирусных заболеваний (в особенности гепатита) и использованием в сельском хозяйстве ядохимикалиев без адекватной защиты.
Этиология и патогенез.
Причину апластической анемии удается выявить менее, чем у 50% больных. В зависимости от этиологических факторов выделяют: врожденные (наследственные) и приобретенные формы заболевания.
К врожденным формам относятся анемия Фанкони, амегакариоцитарная аплазия и апластическая анемия, развивающаяся у больных с негаматологической патологией (синдром Дауна). В группу приобретенных входят первичная (этиологический фактор неизвестен) и вторичная апластическая анемия, которая может возникать при воздействии ионизирующей радиации, химических веществ (бензин, толуол), при вирусных инфекциях (гепатиты В и С, ВИЧ-инфекция, вирус Эпштейна-Барр, парвовирусы), иммунных заболеваниях (системная красная волчанка, эозинофильный фасциит), тимоме и др.
В основе патогенеза апластической анемии лежит внутренний дефект кроветворной стволовой клетки, приводящий к нарушению ее пролиферации и дифференцировки. В реализации факторов, приводящих к изменению в стволовой клетке, имеют значение состояние кроветворного микроокружения (стромы костного мозга), а также иммунопатологические воздействия, обусловленные внешними и/или внутренними факторами.
Клиническая картина.
Течение апластической анемии различно: в одних случаях заболевание возникает внезапно и быстро приводит к летальному исходу, в других протекает более латентно, особенно у лиц пожилого возраста.
Наиболее распространенной является приобретенная первичная апластическая анемия. При этой форме чаще страдают мужчины в возрасте 18-20 лет. Длительность заболевания до первичного обращения за врачебной помощью составляет в среднем от 1 до 3 месяцев. При отсутствии своевременной диагностики апластическая анемия характеризуется неуклонным прогрессированием.
Клинические проявления заболевания тесно связаны с выраженностью изменений в периферической крови (анемия, лейко- и нейтропения, тромбоцитопения) и включают 3 синдрома: анемический, геморрагический и инфекционных осложнений. Как правило, первые симптомы обусловлены анемией. Часто одновременно развивается геморрагический синдром различной степени выраженности (кровоизлияния на коже по петехиально-пятнистому типу, носовые, десневые, в более тяжелых случаях — маточные и желудочно-кишечные кровотечения, кровоизлияния в сетчатку и головной мозг). Иногда геморрагический синдром в начале заболевания настолько выражен, что дает повод к ошибочному диагнозу (это более характерно для редкой формы апластической анемии — амегакариоцитарной аплазии). Синдром инфекционных осложнений в начале заболевания возникает редко (при клинически раритетной форме апластической анемии, характеризующейся преимущественным угнетением нейтропоэза). При прогрессировании заболевания инфекционные осложнения (язвенно-некротическое поражение полости рта, миндалин, пневмония, сепсис и др.) доминируют в клинической картине и, наряду с геморрагическим синдромом, являются одной из основных причин летальных исходов.
В некоторых случаях апластическая анемия проявляется одноростковой цитопенией с соответствующей клинической симптоматикой (чаще — парциальная красноклеточная аплазия, реже — амегакариоцитарная аплазия или угнетение нейтропоэза).
При объективном исследовании больных обращает внимание мраморная бледность кожи и видимых слизистых оболочек. Увеличения селезенки, печени и лимфатических узлов не отмечается; более того, наличие органомегалии и лимфоаденопатии исключает апластическую анемию).
