Гемобластозы
• Гемобластозы — опухолевые заболевания кроветворной и лимфатической ткани. Гемобластозы подразделяют на системные заболевания — лейкозы, а также регионарные — лимфомы.
Отличия между лейкозами и лимфомами заключаются не только в наличии или отсутствии системности поражения. Известно, что в терминальной стадии лимфомы дают обширное мета-стазирование, в том числе и в костный мозг. Другим важным отличием лейкозов от лимфом является то, что при лейкозах опухоль первично возникает на «территории» костного мозга, а при лимфомах костный мозг поражается вторично в результате ме-тастазирования.
При лейкозах опухолевые клетки, как правило, обнаруживаются в крови, поэтому в литературе используется термин для обозначения лейкозов, предложенный еще Р.Вирховым, «лейкемия».
Эпидемиология. Опухоли кроветворной и лимфоидной ткани в числе пяти самых распространенных опухолей человека. Среди опухолей детей первых 5 лет жизни на их долю приходится 30 % случаев.
Этиология. Как все опухоли, гемобластозы могут вызываться разнообразными мутагенными факторами экзогенного и эндогенного происхождения, действующими на стволовые и полустволовые клетки-предшественницы. Большое значение в возникновении ряда гемобластозов имеет наследственный фактор.
Роль ионизирующей радиации в возникновении гемобластов Доказывается наблюдениями за пациентами, заболевшими лейкозами и лимфомами через определенное время после атомной бомбардировки Японии, аварий на АЭС, ядерных испытаний. Описаны случаи заболеваний у людей, получавших радиотерапию, а также у врачей-радиологов. Известен цитогенетический маркер радиационного поражения — кольцевидная хромосома. Достоверно установлена связь между радиационным поражением и развитием острого и хронического миелолейкоза, острого эри-тромиелоза и острого лимфобластного лейкоза у детей.
Роль химических канцерогенов доказывается данными экспериментов, наблюдениями за пациентами, работавшими на вредных предприятиях с использованием бензола, а также за больными, получавшими цитостатическую терапию по поводу других онкологических заболеваний. Использование таких цитостатических препаратов, как мелфалан, азатиоприн, лейкеран, миелосан, антибиотика левомицетина, может приводить к возникновению острого и хронического миелолейкоза, острого миеломонобластного лейкоза и эритромиелоза.
Роль наследственности в развитии гемобластозов подтверждается частым развитием лейкозов у людей с наследственными заболеваниями со спонтанными разрывами хромосом (болезни Дауна, Блума, анемия Фанкони), с нерасхождением половых хромосом (болезни Клайнфелтера, Тернера), а также существованием «лейкозных семей». Нередко лейкозы развиваются у пациентов с наследственными дефектами иммунитета (атаксия телеагиэктазия, или синдром Луи-Бар, синдром Вискотта — Олдриджа, болезнь Братона).
Патогенез. Множество этиологических факторов, воздействуя на стволовые и полустволовые гемопоэтические клетки, пр» водят к одинаковым результатам — злокачественной трансформации. Следовательно, существует так называемое узкое место, через которое могут осуществлять свое воздействие различив агенты. Такое место, вероятнее всего, находится в геноме клеток, где располагаются протоонкогены и антионкогены. При этом могут происходить усиление экспрессии, амплификация, точечная мутация или другие изменения протоонкогенов, превращение их в клеточные онкогены, что приводит к развитию опухоли. Хромосомные перестройки могут привести к передислокации протоонкогена в зону влияния гена-энхансера, превращению его в клеточный онкоген и усилению экспрессии. Так, при лимфоме Беркитта происходит реципрокная транслокация между хромосомами 8 и 14q32. Клеточный онкоген c-myc из хромосомы 8 перемещается на хромосому 14 и попадает в зону действия генов, регулирующих синтез тяжелых цепочек иммуноглобулинов. Описанные изменения сочетаются также с точечной мутацией N-ras.
При хроническом миелолейкозе нередко встречается филадельфийская хромосома, образовавшаяся в результате реципрокной транслокации между хромосомами 9 и 22. Образуется новый ген-гибрид c-abl-bcr, белковый продукт которого обладает тирозинкиназной активностью. Онкогены обычно встраиваются в разрывы хромосом. Так, при В-лимфоцитарных лимфомах и лейкозах происходят разрывы в хромосоме 14 в локусе 32q, где локализуются гены тяжелых цепочек иммуноглобулинов. При Т-лимфоцитарных лейкозах и лимфомах — в локусе 11q гена а-цепочек рецепторов Т-лимфоцитов.
Морфогенез. Развитие гемобластозов начинается с малигнизации одной стволовой или полустволовой клетки, дающей пул опухолевых клеток. Это означает, что все гемобластозы имеют моноклоновое происхождение. Моноклоновость происхождения подтверждается экспериментальными и клиническими данными по обнаружению во всех опухолевых клетках одного и того же больного клоновой метки — хромосомной или изоферментной. Например, во всех опухолевых клетках при хроническом миелолейкозе присутствует филадельфийская хромосома.
Стволовые клетки составляют примерно 0,01—0,001 % всей популяции костномозговых клеток. Рост и дифференцировка стволовых и полустволовых клеток-предшественниц управляются факторами роста (схема 34) и стромальным микроокружением, что подтверждается экспериментами с клеточными культурами где рост и дифференцировка клеток происходят только в Присутствии факторов роста или стромальных клеток. Стромальные клетки, вероятно, также выделяют факторы роста, святые с их клеточными мембранами, а также гепарансульфатами стромы, обеспечивая тем самым локальный рост.
Схема 34. Структура гемопоэтической системы

1 – Колониеформирующая клетка, син. колониеобразующая клетка (КОЕ).
Результаты работ по изучению морфологии и клеточной кинетики гемобластозов, в первую очередь лейкозов, показали, что при развитии опухолей происходит не только малигнизация на уровне стволовых и полустволовых клеток-предшественниц, но также развивается блок дифференцировки в пуле опухолевых клеток.
ЛЕЙКОЗЫ
При лейкозах опухолевая ткань первоначально разрастается на «территории» костного мозга и постепенно замещает нормальные ростки кроветворения. Механизмы этого явления мал изучены. Вероятно, речь идет не о простом механическом вытеснении, а скорее о подавлении нормальных ростков клоном лейкозных клеток с участием особых факторов и контактного торможения. В результате этого процесса у больных лейкозами закономерно развиваются различные варианты цитопений — анемия, тромбоцитопения, лимфоцитопения, гранулоцитопения, что приводит к повышенной кровоточивости, кровоизлияниям, подавлению иммунитета с присоединением инфекционных осложнений.
Метастазирование при лейкозах сопровождается появлением лейкозных инфильтратов в различных органах — печени, селезенке, лимфатических узлах и др. В органах могут развиваться изменения, обусловленные обтурацией сосудов опухолевыми клетками — инфаркты, язвенно-некротические осложнения.
Принципы классификации лейкозов. Выделяют пять основных принципов классификации: по характеру течения лейкозов; по степени дифференцировки опухолевых клеток; в соответствии с цитогенезом; на основе иммунного фенотипа опухолевых клеток; по общему числу лейкоцитов и наличию бластных клеток в периферической крови.
По характеру течения выделяют острые, протекающие менее года, и хронические, существующие длительное время.
По степени дифференцировки опухолевых клеток выделяют недифференцированные, властные и цитарные лейкозы.
При высоком блоке дифференцировки лейкозные клетки могут напоминать стволовые и властные клетки первых четырех классов клеток-предшественниц [Чертков И.Л., Воробьев А.И., 1993]. Поэтому по степени дифференцировки эти лейкозы называют властными и недифференцированными. Поскольку они протекают остро, то можно говорить, что острые лейкозы — это бластные и недифференцированные лейкозы.
При низком блоке дифференцировки лейкозные клетки напоминают процитарные и цитарные клетки-предшественницы, лейкозы протекают менее злокачественно, хронически и называются цитарными.
Цитогенетические варианты лейкозов основываются на представлениях о кроветворении (см. схему 34). Острые лейкозы по цитогенезу подразделяются на лимфобластный, миелобластный, монобластный, миеломонобластный, эритромиелобластный, мегакариобластный, недифференцированный. Иронические лейкозы представлены лейкозами миелоцитарного происхождения (хронический миелоцитарный лейкоз, хронический нейтрофильный лейкоз, хронический эозинофильный лейкоз, хронический базофильный лейкоз, миелосклероз и др.), лимфоцитарного происхождения (хронический лимфолейкоз, парапротеинемические лейкозы: миеломная болезнь, первичная макроглобулинемия Вальденстрема, болезнь тяжелых цепей Франклина; лимфоматоз кожи — болезнь Сезари и др.), моноцитарц 0, го происхождения (хронический моноцитарный лейкоз, гистиоцитоз X).
Иммунный фенотип опухолевых клеток в настоящее время стало возможным проводить более точное типирование опухолевых клеток в зависимости от их иммунного фенотипа по экспрессии CD19, CD20, CD5, легких цепочек иммуноглобулинов и других антигенных маркеров.
По общему числу лейкоцитов в периферической крови и наличию лейкозных клеток выделяют лейкемические (более 50 — 80 • 109/л лейкоцитов, в том числе бластов), сублейкемические (50—80 • 109/л, в том числе бласты), лейкопенические (содержание лейкоцитов в периферической крови ниже нормы, но есть бласты), алейкемические (содержание лейкоцитов в периферической крови ниже нормы, бласты отсутствуют).
Морфологическое исследование имеет большое значение в диагностике лейкозов. Основными методами прижизненной морфологической диагностики являются исследования мазков периферической крови и биоптатов костного мозга, которые получают при трепанации гребешка подвздошной кости или пункции грудины, а также других органов.
Гемобластозы — Медицинский справочник
 Гемобластозы
ГемобластозыГемобластозы – костномозговые и внекостномозговые неопластические процессы, представленные двумя группами заболеваний — миелопролиферативными (лейкозами) и лимфопролиферативными (гематосаркомами). Общими для всех форм гемобластозов являются гиперпластический, интоксикационный, геморрагический, анемический, иммунодефицитный синдромы. Диагностика гемобластозов включает общий анализ крови; проведение стернальной пункции, трепанобиопсии, биопсии лимфоузлов с исследованием материала; инструментальных исследований (УЗИ, рентгенографии, МСКТ). Лечение гемобластозов, главным образом, химиолучевое; в некоторых случаях может быть показана трансплантация костного мозга.
Гемобластозы
 Гемобластозы
ГемобластозыГемобластозы – злокачественные опухолевые заболевания, характеризующиеся первичным поражением кроветворной и лимфатической тканей. За последние десятилетия частота гемобластозов неуклонно растет: ежегодно в России, западноевропейских странах и США регистрируется 7-11 случаев опухолей кроветворной ткани на 100 тыс. населения. В структуре онкологической заболеваемости, среди злокачественных опухолей прочих локализаций, гемобластозы занимают 5-6 место. Замечено, что мужчины болеют гемобластозами чаще женщин, а сельские жители реже, чем городское население. У детей первых 5 лет жизни с абсолютной частотой преобладает острый лимфобластный лейкоз, у лиц в возрасте 20-45 лет – хронический миелолейкоз. Поиск адекватных путей профилактики, раннего выявления и эффективного лечения гемобластозов является острейшей проблемой онкогематологии.
Классификация гемобластозов
В структуре гемобластозов выделяют миелопролиферативные и лимфопролиферативные заболевания. Первые представлены лейкозами (лейкемией) – злокачественными опухолями кроветворной ткани с первичным поражением костного мозга; вторые – гематосаркомами, или лимфомами – внекостномозговыми объемными образованиями с первичным локальным ростом, преимущественно в лимфоузлах.
При этом по мере прогрессирования, лейкозы и гематосаркомы могут трансформироваться друг в друга. Так, при лейкозах может возникать метастазирование опухолевых клеток в плевру, брюшину, яички, лимфоузлы, мозговые оболочки. В то же время, на определенном этапе развития гематосаркомы в патологические процессы может вовлекаться костный мозг, т. е. происходить лейкемизация с развитием изменений крови, характерных для лейкоза. В некоторых случаях гемобластоз изначально развивается, как лимфома-лейкоз – заболевание, сочетающее признаки костномозгового и внекостномозгового поражения.
На основании морфологических различий клеток, образующих опухолевый субстрат, лейкозы делятся на острые и хронические. В основе острых лейкозов лежит пролиферация бластных клеток, хронических — преимущественно зрелых и промежуточных клеток. Основные клинико-гематологические формы острого лейкоза представлены: о. лимфобластным лейкозом детей и взрослых, о. миелобластным, о. монобластным, о. миеломонобластным, о. мегакариобластным и другими лейкозами.
Хронические лейкозы подразделяются на миелопролиферативные и лимфопролиферативные. К ним относятся следующие виды гемобластозов: хронический миелолейкоз, хронический лимфолейкоз, хр. эритромиелоз, полицитемия, миеломная болезнь и пр. Другая группа гематобластозов – гематосаркомы представлены лимфогранулематозом (лимфомой Ходжкина) и нелимфогранулематозными/неходжкинскими лимфомами.
Причины гемобластозов
Гемобластозы принадлежат к заболеваниям полиэтиологического характера с окончательно невыясненными причинами. Тем не менее, доподлинно установлены некоторые канцерогенные факторы, увеличивающие риск возникновения гематобластозов. В первую очередь, это радиационное воздействие на организм различного происхождения: ультрафиолетовое и ионизирующее излучение, лучевая и радиоизотопная диагностика, лучевая терапия по поводу других онкологических заболеваний.
Мутагенным действием на клетки обладают химические вещества (бензол), многие лекарственные препараты (хлорамфеникол, фенилбутазон и др.), в том числе, цитостатики (метотрексат, циклофосфан, хлорамбуцил и др.). Этим объясняется тот факт, что у онкобольных, получающих химиолучевую терапию по поводу первичной злокачественной опухоли, нередко развиваются вторичные гемобластозы.
Повышенную вероятность лейкозной трансформации миелоидных или лимфоидных клеток предопределяют некоторые хромосомные дефекты, в частности, синдром Дауна, синдром Луи-Бар, анемия Фанкони, синдром Клайнфельтера и др. В происхождении гемобластозов доказана этиологическая роль вирусных факторов (вируса Эпштейна-Барра, ретровирусов) и обменных нарушений (расстройства метаболизма триптофана и тирозина).
Симптомы гемобластозов
Гемобластозы сопровождаются многочисленными местными и системными проявлениями. Манифестация гемобластозов может быть острой, напоминающей клинику ОРВИ, или медленной, латентной. Наиболее типичными для различных форм гемобластозов являются интоксикационный, пролиферативный (гиперпластический), геморрагический, анемический синдромы и синдром инфекционных осложнений.
В большинстве случаев первыми признаками гемобластозов служат неспецифические симптомы общей интоксикации – длительное немотивированное повышение температуры, утомляемость, потливость, астенизация. Гиперпластический синдром при гемобластозах характеризуется генерализованной лимфаденопатией (увеличением шейных, подмышечных, паховых лимфоузлов), гепато- и спленомегалией. Типичны оссалгии, вызванные увеличением объема костного мозга. Вследствие сдавления верхней полой вены увеличенными внутригрудными лимфоузлами появляются отеки лица, шеи, верхних конечностей, одышка (т. н. синдром верхней полой вены).
Геморрагические проявления гемобластозов включают повышенную склонность к образованию подкожных и подслизистых кровоизлияний, возникновению десневых, носовых, желудочно-кишечных кровотечений, ДВС-синдрома. Вследствие вторичного иммунодефицита у больных с гемобластозами снижается сопротивляемость к инфекциям, поэтому у них легко возникают пневмонии, септицемия, внутрибольничные инфекции, которые могут иметь молниеносное течение и заканчиваться летально.
В течении гемобластозов выделяют стадии обострения и ремиссии (полной и неполной). О полной ремиссии говорят в случае отсутствия клинических признаков гемобластоза в течение месяца, нормализации картины крови, определения в миелограмме менее 5% бластных клеток.
Диагностика гемобластозов
Основанием для подозрения на гемобластоз (кроме клинической картины заболевания), служат изменения гемограммы (количества эритроцитов и тромбоцитов, количества и морфологии лейкоцитов, лимфоцитов). Эти отклонения от нормы могут быть различны, в зависимости от формы и вида гемобластоза. Все пациенты с отклонениями в общем анализе крови для уточнения диагноза должны направляться к гематологу.
На следующем диагностическом этапе для оценки кроветворения и определения характера гемобластоза проводится стернальная пункция или трепанобиопсия, пункционная или открытая биопсия лимфатических узлов. Полученный материал подвергается цитохимическому, цитогенетическому, гистологическому исследованиям. По показаниям выполняется УЗИ печени и селезенки, рентгенография ОГК и МСКТ грудной клетки, рентгенография черепа, ребер, позвоночника, костей таза. Проведение дифференциальной диагностики требуется, главным образом, между различными формами гемобластозов.
Лечение гемобластозов
Лечение гемобластозов осуществляется длительно и поэтапно: сначала в специализированном отделении стационара, затем – в гематологическом кабинете поликлиники. Для различных видов гемобластозов разработаны стандартизованные программы лечения. К общим принципам относится помещение больного в асептические условия (изолированные палаты с повышенным уровнем защиты от проникновения инфекции), проведение терапии, направленной на индукцию и консолидацию ремиссии. Обычно в качестве первой линии терапии гемобластозов избирается высокодозная моно- или полихимиотерапия цитостатическими препаратами. При достижении положительной динамики по результатам миелограммы, дозировка химиопрепаратов снижается до поддерживающей. С целью коррекции картины крови осуществляется заместительная гемотрансфузионная терапия (переливание эритро-, тромбомассы). Профилактика инфекционных осложнений предполагает назначение антибактериальных и антимикотических препаратов. В дополнение к цитостатической терапии может быть показано проведение гормональной терапии, локального облучения лимфоузлов, селезенки, выполнение спленэктомии.
Лекарственная терапия гемобластозов может осложняться цитостатической болезнью, включающей агранулоцитоз, септицемию, некротическую энтеропатию; сывороточным гепатитом, дистрофическими изменениями печени, апластической анемией и др. Эффективным и перспективным методом лечения гемобластозов является трансплантация костного мозга, однако основная сложность данной процедуры заключается в подборе HLA-совместимого донора.
Прогноз и профилактика гемобластозов
Прогноз зависит от формы гемобластоза, своевременности, правильности и полноты проведенных лечебных курсов. Так, при лимфогранулематозе полную ремиссию удается достичь у более 90% больных, при остром лейкозе – у 60-70%, что позволяет продлить жизнь пациентов на годы. Многим больным гемобластозами удается преодолеть 5-летний порог выживаемости и даже добиться полного выздоровления. Между тем, анализ эпидемиологических данных за последние десятилетия позволяет прогнозировать увеличение числа случаев гемобластозов в ближайшее время.
О профилактике гемобластозов можно говорить только с позиции снижения контакта с потенциально опасными факторами — источниками ионизирующего излучения, химическими веществами, вирусными агентами. Практически здоровым людям ежегодно рекомендуется сдавать общий анализ крови.
Вконтакте
Google+
LiveJournal
Одноклассники
Мой мир
Гемобластозы: классификация, симптомы, лечение, прогноз
Гемобластозы – это большая группа злокачественных опухолей, возникающих из кроветворных клеток. Устаревшее название этой категории болезней – лейкемия, симптомы которой впервые описал немецкий врач Вирхов еще в 1845 году. В переводе с латыни, лейкемия означает белокровие. С тех пор представления о том, что такое лейкемия, сильно изменились. Современная медицина чаще оперирует наименованием лейкоз крови. Эта группа заболеваний чаще встречается у детей, составляя до 30% всей педиатрической онкопатологии. У взрослых лейкоз (в быту известный как рак крови), встречается не более чем в 5% случаев всех злокачественных опухолей, но прогноз гораздо хуже, чем у детей.
Причины лейкоза
Как при любой злокачественной опухоли, причины рака крови – изменения генома клетки, которые вызывает активное деление и рост злокачественной опухоли. В этом плане лейкоз крови ничем не отличается от других злокачественных опухолей. Только при гемобластозах злокачественно изменяются клетки – предшественники крови. ДНК изменяется под воздействием канцерогенных факторов, которые можно разделить на 3 большие группы:
- Химические. Всего известно более 1500 канцерогенных химических соединений: афлатоксины (продукты жизнедеятельности плесеней), соли тяжелых металлов, некоторые лекарства (например, средства, используемые для высокодозной химиотерапии).
- Физические. Рентгеновское излучение и проникающая радиация.
- Биологические, или онкогенные вирусы. Это вирус Эпштейна-Барр, вирус Т-клеточного лейкоза и другие.

На самом деле, однократный контакт с канцерогеном не означает немедленного и непременного развития той или иной формы лейкоза. Они увеличивают вероятность изменения генома клетки, но нормальная иммунная система обычно успевает обнаружить злокачественное перерождение и справиться с опухолью. Онкологические болезни, в том числе лейкемия, появляется, когда таких мутаций становится слишком много или иммунная система ослаблена и не способна своевременно отреагировать. Как правило, рак крови развивается не только под воздействием одной причины возникновения, при лейкемии играют роль и различные предрасполагающие факторы.
- генетическая предрасположенность: наследуется не сам рак, а «нестабильность» генома клеток-предшественников крови;
- ухудшение противоопухолевой защиты организма.
Виды лейкозов
Все предшественники клеток крови делятся на лимфоидный росток и миелоидный росток. Лимфоидный росток крови – это предшественники лимфоцитов и сами лимфоциты на ранней стадии развития. Миелоидный росток – предшественники гранулоцитов, нейтрофилов, эритроцитов и тромбоцитов. Соответственно, первая классификация лейкозов, по виду измененных клеток, делит их на лимфоидные и миелоидные. У детей преобладают лимфоидные, у взрослых – миелоидные.
Если обычные болезни делятся на острые и хронические исходя из того, насколько долго они протекают, лейкемии подразделяют на острые и хронические исходя из того, успевают ли созревать клетки крови.
- При хронических лейкозах в крови выявляются весь нормальный ряд созревающих клеток крови, но бластных (самых юных) форм намного больше нормы. Чаще встречается у взрослых.
- Для острых лейкозов характерен лейкемический провал: много бластных клеток, есть зрелые клетки, но переходные формы исчезают. Чаще возникает у детей.
И те и другие, в свою очередь делятся на различные виды лейкозов по происхождению:
1. Костномозгового происхождения:
a. острые лейкозы (острый лимфобластный, острый нелимфобластный).
b. хронические лейкозы (хронический миелолейкоз, идиопатический миелофиброз, эритремия, тромбоцитемия, хронический лимфолейкоз).
c. парапротеинемические гемобластозы (миеломная болезнь, болезнь Вальденстрема).
2. Внекостномозгового происхождения:
a. лимфогранулематоз,
b. неходжкинские лимфомы.
Также лейкемии подразделяются по видам измененных клеток и их генетическим особенностям, точнее, тем изменениям в генотипе, которые объединяют всю массу лимфоидно измененных клеток. Эта классификация делит лейкозы на несколько десятков подвидов, поэтому подробно воспроизводить ее нет смысла.

Симптомы лейкемии
Если говорить в общем, то проявления болезни связаны с тем, что такое лейкоз. Нормальное кроветворение угнетается, и преобладать начинают бластные клетки, которые неспособны выполнять свои функции. Симптомы лейкоза у взрослых, равно как и у детей зависят не от возраста, а от формы заболевания.
Острый лейкоз
Симптомы можно объединить в несколько групп – синдромов:
- Гиперпластический. Увеличиваются в размерах лимфоузлы, миндалины, печень и селезенка, иногда на коже появляются лейкозные инфильтраты, которые выглядят как красновато-синеватые бляшки.
- Интоксикационный. Повышается температура до 37-38 ( у детей возможно и выше), появляется ломота в костях и мышцах, пропадает аппетит. Считается, что проявления интоксикационного синдрома – это первые признаки рака крови, но они возникают далеко не у всех больных. У детей интоксикация обычно выражена ярче, чем аналогичные признаки лейкоза у взрослых.
- Анемический. Лейкозные клетки заполоняют собой кроветворные органы и нарушают производство и развитие нормальных клеток крови. Уменьшается гемоглобин и количество эритроцитов. У30% пациентов, имеющих острый лейкоз, гемоглобин падает ниже 60 г/л, при норме у взрослых 120-140. Рак крови вызывает такие же симптомы анемии, как и пищевой дефицит железа: бледность, общая слабость, головокружение. Поскольку женщины легче переносят анемию, эти симптомы рака крови у женщин могут долго оставаться незамеченными.
- Геморрагический. Страдает и выработка тромбоцитов, из-за чего нарушается свертывание крови. Могут проявляться как мелкоточечными кровоизлияниями (так называемой геморрагической сыпью), так и обильными кровотечениями: носовыми, желудочно-кишечными. Признаки лейкемии у женщин могут выглядеть как обильные маточные кровотечения. Кровоизлияние может произойти и в мозг, в этом случае появятся симптомы геморрагического инсульта: расстройства чувствительности, параличи, потеря сознания.
- Инфекционных осложнений. Среди функций клеток крови – борьба и чужеродными агентами, этим занимаются лимфоциты. Поскольку нормальных клеток становится все меньше, снижается и сопротивляемость инфекции. Инфекционные осложнения возникают у 80-85% больных и проявляются пневмониями, гнойными процессами, вплоть до сепсиса. Возможны и тяжелые вирусные инфекции, в том числе генерализованные формы герпеса, цитомегаловирус.
- Нейролейкоза. Как и любая раковая опухоль, лейкоз формирует метастазы – лейкемические инфильтраты. Они не разрушают собственные ткани органов, но раздвигают их, вызывая сдавление. Формируясь в замкнутой полости черепа, лейкемические инфильтраты проявляются симптомами, схожими с признаками опухоли мозга. Сдавление крупных нервов вызывает боли, нарушения чувствительности. Встречается у 50% пациентов.
Диагноз острого лейкоза выставляют после пункции костного мозга, главный признак – более 30% бластных клеток.

Хронический лейкоз
Часто проявления болезни стерты, невыражены, из-за чего визит к врачу порой откладывается на много лет, в течение которых человек страдает лейкемией, сам не зная об этом. Среди всего многообразия видов чаще всего встречаются хронический миелоидный лейкоз и хронический лимфолейкоз.
Хронический миелоидный лейкоз проявляется:
- анемией;
- болями в костях;
- общей слабостью;
- увеличением печени и селезенки;
- признаками общей интоксикации,
- лейкоцитоз (избыток лейкоцитов крови) со сдвигом формулы влево – увеличением количества незрелых форм; часто увеличенное количество тромбоцитов.
Хронический лимфолейкоз
Опухолевый субстрат при этом – зрелые лимфоциты. На ранних стадиях проявляется неспецифическими признаками интоксикации – общая слабость, недомогание, температура около 37, потливость, исхудание. Далее присоединяется желтуха, геморрагические проявления. Становится заметно увеличение лимфоузлов. В крови уменьшается количество эритроцитов и тромбоцитов, зато количество лейкоцитов может достигать 600х10*9/л, при норме 4-6х10*9/л. Причем 80-95% из них – зрелые лимфоциты. Они заполняют не только кровь, но и лимфоузлы, печень и селезенку.
Лечение
Лечение рака крови в общих чертах одинаково для всех видов лейкемии. Для разных видов лейкоза используются разные препараты, но если говорить в общем, рак крови лечится цитостатиками. Химиопрепараты уничтожают костный мозг, после чего пациенту «подсаживают» его от донора (трансплантация костного мозга). При хроническом лимфолейкозе лейкемия лечится, как правило, без пересадки костного мозга, так как в этом случае процедура вызывает много осложнений.
Кроме этого, лечение лейкемии дополняется симптоматической терапией. Проводится дезинтоксикация, инфекции уничтожаются антибиотиками и противовирусными, при угрозе кровотеченией переливают тромбоцитарную массу, и так далее. В целом, лечение рака крови любой разновидности – это сложный и длительный процесс.
Эффективней всего лечить рак крови получается у пациентов до 30 лет, в более старшем возрасте лечение имеет сомнительную результативность.
Профилактика лейкоза не разработана.
Запись интервью
причины, симптомы, диагностика, лечение, профилактика
Представляет собой злокачественное опухолевое образование, характеризующееся развитием костномозговых и внекостномозговых неопластических процессов, которые представлены двумя типами заболеваний – миелопролиферативными и лимфопролиферативными.
Причины
Гемобластозы – это заболевания, отличающиеся полиэтиологическим течением, причины развития которых до конца не изучены. Однако выделен целый ряд факторов с канцерогенным действием, которые значительно повышают вероятность развития недуга. К таким факторам относят гамма-излучение, ультрафиолетовое излучение, лучевую и радиоизотопную диагностику, лучевую терапию, которая проводится в связи с наличием у больного других онкологических заболеваний.
Помимо этого, одним из факторов способных вызвать данные патологические процессы является мутагенное воздействие на клетки, которое способны оказывать некоторые химические вещества, некоторые лекарственные средства, что объясняет тот факт, что очень часто у онкобольных, получающих химиолучевую терапию по поводу первичной злокачественной опухоли, довольно часто отмечается развитие вторичного гемобластоза.
Симптомы
Гемобластозы обусловлены развитием разнообразной симптоматики, обусловленной наличием местных и системных проявлений. Иногда заболевание характеризуется острым началом, в этом случае его симптомы напоминают клиническую картину острого респираторного заболевания. При латентном течении больного длительное время может ничего не беспокоить.
В большинстве случаев заболевание дебютирует с возникновения симптомов общей интоксикации. В этом случае у больного возникает продолжительное беспричинное повышение температуры, усиленное потоотделение, упадок сил и астенизация. Гиперпластический синдром при гемобластозах обусловлен развитием генерализованной лимфаденопатии, а также возникновением гепато- и спленомегалии. У большинства больных отмечается развитие оссалгии, обусловленной увеличением объема костного мозга. В результате компрессии верхней полой вены отмечается увеличение внутригрудных лимфоузлов, появление отеков лица, шеи, верхних конечностей и одышки.
При геморрагических проявлениях гемобластозов у больных выявляется предрасположенность к образованию подкожных и подслизистых кровоизлияний, возникновение десневых, носовых, желудочно-кишечных кровотечений и ДВС-синдрома. На фоне вторичного иммунодефицита у пациентов с гемобластозами отмечается снижение сопротивляемости к инфекционным поражениям, вследствие чего они подвержены развитию воспаления легких, септицемии, внутрибольничных инфекций, отличающихся молниеносным течением.
В клинической картине недуга выделяют две фазы – ремиссии (полной и частичной) и обострения. При полной ремиссии у больного не отмечается развития клинической симптоматики на протяжении как минимум одного месяца, происходит нормализация картины крови. На этом этапе в миелограммебольного обнаруживается меньше 5% бластных клеток.
Диагностика
Наличие изменений в гемограмме может указывать на наличие у больного гемобластоза. Такие изменения могут зависеть от формы и типа гемобластоза. Все больные с отклонениями в общем анализе крови для уточнения диагноза должны направляться на консультацию к гематологу.
Для подтверждения диагноза больному может быть назначено проведение стернальной пункции или трепанобиопсии, также может потребоваться проведение пункционной или открытой биопсии лимфатических узлов с дальнейшим цитохимическим, цитогенетическим, гистологическим исследованием биоптата. По показаниям может потребоваться проведение ультразвукового исследования печени и селезенки, рентгенография грудной клетки, рентгенография черепа, ребер, позвоночника и костей таза.
Лечение
Гемобластозы требуют длительного поэтапного лечения. Для различных видов гемобластозов разработаны стандартные схемы лечения. К общим принципам относится помещение больного в асептические условия, проведение терапии, направленной на индукцию и консолидацию ремиссии. Обычно в качестве первой линии терапии гемобластозов избирается высокодозная моно- или полихимиотерапия цитостатическими средствами. При достижении положительной динамики по результатам миелограммы, дозировка химиопрепаратов снижается до поддерживающей. Для коррекции формулы крови может потребоваться проведение заместительной гемотрансфузионной терапии, основанной на переливании эритро- итромбоцитарных массы.
Профилактика
Схема профилактики гемобластозов не разработана, однако для снижения вероятности их развития рекомендуется не вступать в контакт с потенциально опасными факторами, такими как источник и ионизирующего излучения, химические вещества и вирусы.
6. Анемия как клинический синдром гемобластозов. Диагностика гемобластозов в условиях поликлиники. Дифференциальный диагноз гемобластозов.
Анемия — клинико-гематологический синдром, характеризующийся уменьшением содержания гемоглобина в единице объема крови, чаще при одновременном уменьшении количества эритроцитов, что приводит к развитию кислородного голодания тканей.
Принято считать анемией снижение уровня гемоглобина ниже 130 г/л и количества эритроцитов ниже 4* 12/л у мужчин и ниже 120 г/л и 3,5* 10/л у женщин
ГЕМОБЛАСТОЗАМИ называют группу опухолей, возникших из кроветворных клеток. Они подразделяются на две группы:
лейкозы — опухоль, исходящая из родоначальных (стволовых) кроветворных клеток с первичным поражением костного мозга.
гематосаркомы — внекостномозговые первоначально локальные опухоли (преимущественно в лимфатических узлах) с возможной их генерацией в кроветворные органы, включая костный мозг.
Несколько реже других гемобластозов встречаются лимфоцитомы (лимфомы) — опухоли, состоящие из зрелых лимфоцитов или образованные разрастаниями, идентичными лимфатическому узлу, но мало или совсем не поражающие костный мозг. Лимфомы разделяют на лимфогранулематоз (болезнь Ходжкина, ходжкинская лимфома) и неходжкинские лимфомы (недифференцированные, высоко- и малодифференцированные, лимфомы Беркитта, грибовидный микоз и др.).
Лейкозы делятся на острые и хронические. В основу классификации лейкозов положена степень зрелости и морфологическая характеристика опухолевых клеток, составляющих субстрат того или иного лейкоза в костном мозге. К острым лейкозам относят опухолевые заболевания системы крови, основным субстратом которых являются бластные клетки: миелобласты, лимфобласты, монобласты, эритробласты, промиелоцитарные и недифференцируемые бласты. Вариант острого лейкоза определяют цитохимически по наличию или отсутствию в бластах пероксидазы, липидов, гликогена, кислых мукополисахаридов, неспецифической эстеразы, фосфатаз и др.
В соответствии с этим острые лейкозы подразделяют на: лимфобластный, миелобластный, промиелоцитарный, миеломонобластный, монобластный, эритромиелоз, мегакариобластный, плазмобластный, недифференцированный, малопроцентарный (количество бластов в костном мозге не более 15-20%) как вариант миелодиспластического синдрома (МДС).
К хроническим относят лейкозы, при которых основная опухолевая масса костного мозга и крови состоит из созревающих или зрелых клеток (лимфоцитов — при хроническом лимфолейкозе, миелоцитов, юных, палочкоядерных и сегментоядерных — при хроническом миелолейкозе, эритроцитов — при эритремии, плазмоцитов — при миеломе). В соответствии с этим выделяют: хронический миелолейкоз, доброкачественный сублейкемический миелоидный лейкоз (миелофиброз, остеомиелосклероз), эритремию, хронический моноцитарный лейкоз, хронический лимфолейкоз, миеломную болезнь,макроглобулинемию Вальденстрема.
Анемический синдром при гемобластозах.
Анемический синдром при гемобластозах является закономерным явлением и проявлением основного заболевания.
Наиболее часто в общеклинической и гематологической практике встречаются следующие варианты гемобластозов:
Острый лимфобластный лейкоз
Острый нелимфобластный лейкоз
Хронический миелоидный лейкоз
Хронический лимфолейкоз
Лимфогранулематоз
Неходжкинские лимфомы
Миелодиспластический синдром
Идиопатический миелофиброз
Множественная миелома
Макроглобулинемия Вальденстрема
Анемический синдром может носить как первичный, так и вторичный (ятрогенный) характер.
В развитии анемического синдрома при гемобластозах играют роль различные механизмы, в зависимости от формы и стадии болезни.
Уменьшение числа эритроцитов в периферической крови при гемобластозах обусловлено следующими механизмами в чистом виде или их комбинациями:
поражение эритроцитарного ростка костного мозга, вытеснение, замещение его патологической тканью следовательно, недостаточной продукцией эритроцитов;
повышенным разрушением эритроцитов, в том числе и при проведении терапии гемобластозов;
потерями значительных количеств эритроцитов вследствие кровопотери при выраженном геморрагическом синдроме.
Развитию анемии могут способствовать нарушение продукции эндогенного эритропоэтина, укорочение продолжительности жизни эритроцитов, дефицит железа в следствии повышенной кровоточивости при синдроме гипервязкости. Анемия может усугубляться гемодилюцией, обусловленной увеличением объема плазмы у больных с высоким уровнем парапротеина. Во всех случаях анемия приводит к развитию гипоксии с соответствующими клиническими проявлениями.
Клиника анемического синдрома при гемобластозах.
Основной симптом анемии — слабость и быстрая утомляемость. Также может наблюдаться:
Бледность
Сердцебиение
Одышка или чувство нехватки воздуха
Боли в области сердца
Головокружение
Головные боли
Похолодание пальцев
Легкая, а иногда и средняя степень тяжести анемии может оставаться бессимптомной и обнаруживаться только при анализе крови. Однако с увеличением степени снижения гемоглобина признаки и симптомы анемии проявляются.
Отличительными особенностями анемий при гемобластозах являются выраженный эритронормобластоз и лейкемоидная картина крови, в некоторых случаях может развиться панцитопения.
Возможные варианты анемии при наиболее часто встречающихся гемобластозах:
Для острого промиелоцитарного лейкоза характерно развитие тяжелого ДВС-синдрома с появлением геморрагии, внутрисосудистого гемолиза. У некоторых больных с острым лейкозом большее значение в анемизации получает геморрагический синдром, связанный с глубокой тромбоцитопенией.
Миелодиспластический синдром — заболевание, при котором анемия долгое время является ведущим клиническим проявлением. Как правило, носит нормохромный характер. У лиц пожилого возраста может наблюдаться сочетание миелоидной дисплазии с дефицитом витамина В-12.
При хроническом миелоидном лейкозе анемия так же носит нормохромный характер, однако, развивается, как правило, в исходе заболевания -бластном кризе.
Иммунный гемолиз более свойственен лимфопролиферативным опухолям (хронический лимфолейкоз, неходжкинские лимфомы) и может носить весьма выраженный характер.
Множественная миелома — у 60-70% больных при первичном обращении выявляется анемия, как правило, нормоцитарная, нормохромная. При болезни Вальденстрема анемический синдром развивается медленно (иногда в течение нескольких лет). Ведущую роль в его генезе играет лей кемическое подавление эритропоэза, гемолиз (аутоиммунная гемолитическая анемия с неполными тепловыми агглютининами регистрируется в 5% случаев), железодефицитная анемия в момент постановки диагноза отмечается у 25% пациентов с болезнью Вальденстрема. Ее патогенез изучен недостаточно. Наиболее вероятной причиной считается нарушение всасывания железа в тонком кишечнике. Как и при множественной миеломе, анемия может усугубляться гемодилюцией, обусловленной увеличением объема плазмы у больных с высоким уровнем парапротеина.
Больные с гемобластозами, не имеющие поражения костного мозга, часто имеют легкую или умеренную нормохромную нормоцитарную анемию, этиология которой включает много факторов. У этих пациентов обычно снижен уровень сывороточного железа и общей железосвязывающей способности сыворотки, повышен ферритин, что свидетельствует о блокаде в переносе железа из запасов в эритроидные предшественники. Кроме того, у некоторых больных (миелодиспластический синдром, остеомиелофиброз) обнаружен сниженный ответ на эритропоэтин. Уровень эритропоэтина может быть выше нормы, но значительно ниже соответствующего данной степени анемии.
Диагностика гемобластозов.
Клинические симптомы лейкозов: анемический, гиперпластический, гемморагический, интоксикационный, инфекционный, язвенно-некротический при острых лейкозах наблюдаются следующие изменения:
1) Периферическая кровь.
Анемия нормохромная нормоцитарная, ретикулоцитопения, тромбоцитопения, изменение общего количества лейкоцитов (увеличение или норма), появление бластов в периферической крови(бластный криз -более 10% бластов в периферической крови), уменьшение количества зрелых нейтрофилов (нейтропения), феномен «провала»( отсутствие промежуточных форм между бластами и зрелыми гранулоцитами), увеличение СОЭ, уменьшение эозинофилов и базофилов
2) миелограмма
Количество бластов 30% и более, выраженная редукция эритроидного, гранулоцитарного, мегакариоцитарного ростков
3) трепанобиопсия крыла подвздошной кости с гистологическим исследованием — бласты.
4) цитохимическое исследование, иммунологические и цитогенетические методы — изменения, характерные для конкретного варианта острого лейкоза
5) общий анализ мочи — изменения неспецифичны, протеинурия, микрогематурия, возможна цилиндрурия.
При хронических лейкозах:
1. Периферическая кровь:
Анемия нормохромная, нормоцитарная, нейтрофильный лейкоцитоз с появлением молодых форм (промиелоцитов, миелоцитов, метамиелоцитов), базофильно-эозинофильная ассоциация, чаще увеличение количества тромбоцитов, лимфопения (при ХМЛ) либо резкое увеличение лимфоцитов более 10*10/л и более, увеличение СОЭ.
2. Миелограмма — гиперклеточный костный мозг, представлены все элементы с наличием переходных форм в большом количестве 3) цитогенетический анализ, иммунофенотипирование Маркером ХМЛ является филадельфийская хромосома
Диагностика множественной миеломы
1) клиническая триада Калера — боли в костях, опухоли, переломы;
2) белок Бенс-Джонса в моче;
остеолитические очаги на рентгенограмме;
периферическая кровь: плазматические клетки, анемия, увеличение СОЭ;
протеинограмма: М-градиент, сывороточный парапротеин IgG более 35 г/л, IgA более 20 г/л; .
миелограмма: плазматических клеток более 30%.
Лечение анемического синдрома при гемобластозах:
Прежде всего, это лечение самого гемобластоза. Одним из критериев достижения ремиссии является нормализация уровня гемоглобина.
Следует ли больным гемобластозами, получающими химиотерапию, назначать эритропоэтин? Однозначного ответа на этот вопрос нет. К безусловным плюсам применения эритропоэтина можно отнести возможность уменьшения количества трансфузий эритроцитов. Доказана эффективность эритропоэтина у больных с почечной недостаточностью, некоторых групп с миелодиспластическим синдромом, остеомиелофиброзом.
Нарушение синтеза ДНК (метотрексат, мелфалан, пуринетол, антагонисты ииримидинов, гидроксимочевина) приводит к дефициту витамина В12 и фолиевой кислоты. При применении этих препаратов ожидается увеличение среднего объема эритроцита.
В большинстве же остальных случаев, лечение анемического синдрома при гемобластозах сводится к заместительным трансфузиям эритроцитарной массы.
При решении вопроса в большинстве же остальных случаев, лечение анемического синдрома при гемобластозах сводится к заместительным трансфузиямэритроцитарной массы.
При решении вопроса о назначении трансфузий больным с хронической анемией следует основываться на результатах оценки тяжести основного заболевания, выраженности физиологической адаптации к анемии, объема физической активности, необходимой данному больному.
9.4 Гемобластозы.
Группа опухолевых поражений кроветворной ткани, характерной особенностью которых является патологическое разрастание её из-за дефекта созревания на уровне бластных клеток.
Этиология неизвестна.
Факторы риска:
инфекция,
интоксикация,
ионизирующая радиация,
экологические проблемы.
Клиника:
Синдром интоксикации (лихорадка, некротическая ангина).
Астенический синдром (слабость, утомляемость, снижение веса).
Анемический синдром.
Геморрагический синдром.
Гиперпластический синдром (увеличение лимфатических узлов, печени, селезенки).
Диагностика:
Анализ крови клинический.
Стернальная пункция.
Биопсия лимфоузлов.
Компьютерная томография.
Лечение:
Антибиотики.
Цитостатики (винкристин, метатрексат).
Глюкокортикоиды.
Лучевая терапия.
Симптоматическая терапия.
Пересадка костного мозга.
Стандарты сестринской деятельности при гемобластозах.
Возможные нарушения потребностей.
Физиологические потребности
Выживание:
Питаться (снижение аппетита, язвенно–некротические поражения ротовой полости).
Дышать (сдавление дыхательных путей увеличенными лимфатическими узлами, одышка).
Спать (тяжёлое состояние, боли, зуд).
Двигаться (общая слабость).
Безопасность:
Быть чистым (кровотечения, язвенно–некротические поражения слизистых, пролежни).
Поддерживать состояние (выраженная общая слабость, нарушения сознания).
Поддерживать температуру (лихорадка).
Психо-социальные:
Принадлежность:
Общаться (длительное пребывание в стационаре, ограничение контактов в связи с боязнью инфекционных осложнений, облысение)
Познавательные:
Достижение успеха, гармонии.
Иметь жизненные ценности (отсутствие адаптации к болезни из-за тяжести заболевания и развития осложнений, страх смерти, депрессия).
Самореализация:
Играть, учиться, работать (ограничение трудоспособности в быту).
Инвалидизация.
Изменение образа жизни (из-за частых госпитализаций).
Возможные проблемы пациента.
Физиологические:
Слабость.
Боли в костях.
Быстрая утомляемость.
Повышенная кровоточивость.
Геморрагии.
Язвенно — некротическое поражение слизистых.
Ограничение физической активности.
Лихорадка.
Нарушение сознания.
Зуд кожи.
2) Психологические:
Социальная изоляция.
Чувство отчаяния и безнадежности.
Тревога, беспокойство.
Депрессия, суицидные мысли.
Неадекватное отношение к болезни.
Зацикленность.
Страх проведения медицинских манипуляций.
Социальные проблемы:
Изменение образа жизни.
Частые и длительные госпитализации.
Изменения бытовых и семейных процессов.
Снижение трудоспособности.
Духовные проблемы:
Дефицит духовного участия.
Отсутствие жизненных ценностей (гармонии, успеха).
5) Потенциальные проблемы:
Риск развития инфекционных осложнений.
Риск облысения.
Риск кровотечения.
Риск развития патологических переломов.
Риск развития нейролейкемии.
Проблема: Слабость вследствие анемической гипоксии.
Цель: Пациент сможет себя обслуживать к моменту выписки.
План сестринского вмешательства.
М/с объяснит сущность состояния и окажет психологическую поддержку.
М/с обеспечит соблюдение лечебно-охранительного режима.
М/с обеспечит помощь пациенту при осуществлении физиологических потребностей(быть чистым, опрятным, пить, есть, выделять).
М/с обеспечит частое проветривание палаты не менее 4 раз в день по 15 минут.
М/с обеспечит приём высококалорийной витаминизированной пищи (диета № 15 гематол.).
М/с обеспечит удобное комфортное положение в постели, проведет профилактику пролежней.
М/с даст рекомендации по физической нагрузке, будет дозировать и осуществлять контроль.
М/с обеспечит транспортировку пациента на каталке в диагностические кабинеты, забор анализов в палате.
М/с обеспечит выполнение лечебных назначений врача (приём лекарственных препаратов внутрь и парентерально).
Проблема. Беспокойство по поводу неблагоприятного исхода заболевания.
Цель: У пациента появится уверенность в благоприятном исходе заболевания.
План сестринского вмешательства:
М/с окажет психологическую поддержку пациенту, вселяя уверенность в улучшение, ориентируя на помощь с его стороны.
М/с будет акцентировать внимание пациента на симптомы положительной динамики состояния.
М/с приведет пример успешного лечения заболевания у другого пациента, находящегося на лечении.
М/с проведет беседу с родственниками пациента, ориентируя их на создание благополучного психологического климата.
По назначению врача м/с обеспечит приём седативных препаратов.
М/с обеспечит досуг пациента (чтение литературы, просмотр телепередач развлекательного характера).
Лекция №4 ГЕМОБЛАСТОЗЫ
Лекция 4
ГЕМОБЛАСТОЗЫ
• Гемобластозы — опухолевые заболевания кроветворной и лимфатической ткани. Гемобластозы подразделяют на системные заболевания — лейкозы, а также регионарные — лимфомы.
Отличия между лейкозами и лимфомами заключаются не только в наличии или отсутствии системности поражения. Известно, что в терминальной стадии лимфомы дают обширное мета-стазирование, в том числе и в костный мозг. Другим важным отличием лейкозов от лимфом является то, что при лейкозах опухоль первично возникает на «территории» костного мозга, а при лимфомах костный мозг поражается вторично в результате ме-тастазирования.
При лейкозах опухолевые клетки, как правило, обнаруживаются в крови, поэтому в литературе используется термин для обозначения лейкозов, предложенный еще Р.Вирховым, «лейкемия».
В последние годы в литературе широко обсуждается вопрос о существовании предопухолевой стадии лейкозов и лимфом. Предлагаются термины «предлейкоз» и «предлимфома» для обозначения состояний с различными качественными и количественными изменениями кроветворной ткани, нередко предшествующими развитию гемобластозов.
Эпидемиология. Опухоли кроветворной и лимфоидной ткани в числе пяти самых распространенных опухолей человека. Среди опухолей детей первых 5 лет жизни на их долю приходится 30 % случаев.
Этиология. Как все опухоли, гемобластозы могут вызываться разнообразными мутагенными факторами экзогенного и эндогенного происхождения, действующими на стволовые и полустволовые клетки-предшественницы. Большое значение в возникновении ряда гемобластозов имеет наследственный фактор.
Роль ионизирующей радиации в возникновении гемобласто-юв доказывается наблюдениями за пациентами, заболевшими
311
лейкозами и лимфомами через определенное время после атомной бомбардировки Японии, аварий на АЭС, ядерных испытаний. Описаны случаи заболеваний у людей, получавших радиотерапию, а также у врачей-радиологов. Известен цитогенетический маркер радиационного поражения — кольцевидная хромосома. Достоверно установлена связь между радиационным поражением и развитием острого и хронического миелолейкоза, острого эри-тромиелоза и острого лимфобластного лейкоза у детей.
Роль химических канцерогенов доказывается данными экспериментов, наблюдениями за пациентами, работавшими на вредных предприятиях с использованием бензола, а также за больными, получавшими цитостатическую терапию по поводу других онкологических заболеваний. Использование таких цитостатиче-ских препаратов, как мелфалан, азатиоприн, лейкеран, миелосан, антибиотика левомицетина, может приводить к возникновению острого и хронического миелолейкоза, острого миеломонобласт-ного лейкоза и эритромиелоза.
Роль вирусов в качестве этиологического фактора гемобла-стозов трактуется неоднозначно. В развитии гемобластозов человека доказано участие лишь двух вирусов: вируса Эпштейна — Барр (африканская лимфома Беркитта) и Т-лимфоцитарного вируса лейкоза человека первого типа (Т-клеточная лимфома и Т-клеточные лейкозы). Имеются экспериментальные данные, доказывающие прямое канцерогенное действие вирусов на гемопо-этические клетки посредством вирусных онкогенов. Однако в большинстве ситуаций внедрение вирусов в клетку вызывает лишь иммортализацию (бессмертие) последней, на фоне которой возникают дополнительные перестройки генома, ведущие к злокачественной трансформации (многоступенчатый канцерогенез).
Роль наследственности в развитии гемобластозов подтверждается частым развитием лейкозов у людей с наследственными заболеваниями со спонтанными разрывами хромосом (болезни Дауна, Блума, анемия Фанкони), с нерасхождением половых хро мосом (болезни Клайнфелтера, Тернера), а также существовани ем «лейкозных семей». Нередко лейкозы развиваются у пациен тов с наследственными дефектами иммунитета (атаксия-телеан гиэктазия, или синдром Луи-Бар, синдром Вискотта — Олдрид жа, болезнь Братона).
Патогенез. Множество этиологических факторов, воздейст вуя на стволовые и полустволовые гемопоэтические клетки, при водят к одинаковым результатам — злокачественной трансфор мации. Следовательно, существует так называемое узкое место через которое могут осуществлять свое воздействие различные агенты. Такое место, вероятнее всего, находится в геноме кле
312
ток, где располагаются протоонкогены и антионкогены. При этом могут происходить усиление экспрессии, амплификация, точечная мутация или другие изменения протоонкогенов, превращение их в клеточные онкогены, что приводит к развитию опухоли. Хромосомные перестройки могут привести к передислокации протоонкогена в зону влияния гена-энхансера, превращению его в клеточный онкоген и усилению экспрессии. Так, при лим-фоме Беркитта происходит реципрокная транслокация между хромосомами 8 и 14q32. Клеточный онкоген с-тус из хромосомы 8 перемещается на хромосому 14 и попадает в зону действия генов, регулирующих синтез тяжелых цепочек иммуноглобулинов. Описанные изменения сочетаются также с точечной мутацией N-ras.
При хроническом миелолейкозе нередко встречается филадельфийская хромосома, образовавшаяся в результате реципрок-ной транслокации между хромосомами 9 и 22. Образуется новый ген-гибрид c-abl-bcr, белковый продукт которого обладает тиро-зинкиназной активностью. Онкогены обычно встраиваются в разрывы хромосом. Так, при В-лимфоцитарных лимфомах и лейкозах происходят разрывы в хромосоме 14 в локусе 32q, где локализуются гены тяжелых цепочек иммуноглобулинов. При Т-лим-фоцитарных лейкозах и лимфомах — в локусе llq гена а-цепо-чек рецепторов Т-лимфоцитов.
Морфогенез. Развитие гемобластозов начинается с малигни-зации одной стволовой или полустволовой клетки, дающей пул опухолевых клеток. Это означает, что все гемобластозы имеют моноклоновое происхождение. Моноклоновость происхождения подтверждается экспериментальными и клиническими данными по обнаружению во всех опухолевых клетках одного и того же больного клоновой метки — хромосомной или изоферментной. Например, во всех опухолевых клетках при хроническом миелолейкозе присутствует филадельфийская хромосома.
Стволовые клетки составляют примерно 0,01—0,001 % всей популяции костномозговых клеток. Рост и дифференцировка стволовых и полустволовых клеток-предшественниц управляются факторами роста (схема 34) и стромальным микроокружением, что подтверждается экспериментами с клеточными культурами, где рост и дифференцировка клеток происходят только в присутствии факторов роста или стромальных клеток. Стро-мальные клетки, вероятно, также выделяют факторы роста, свя-заные с их клеточными мембранами, а также гепарансульфата-ми стромы, обеспечивая тем самым локальный рост.
313
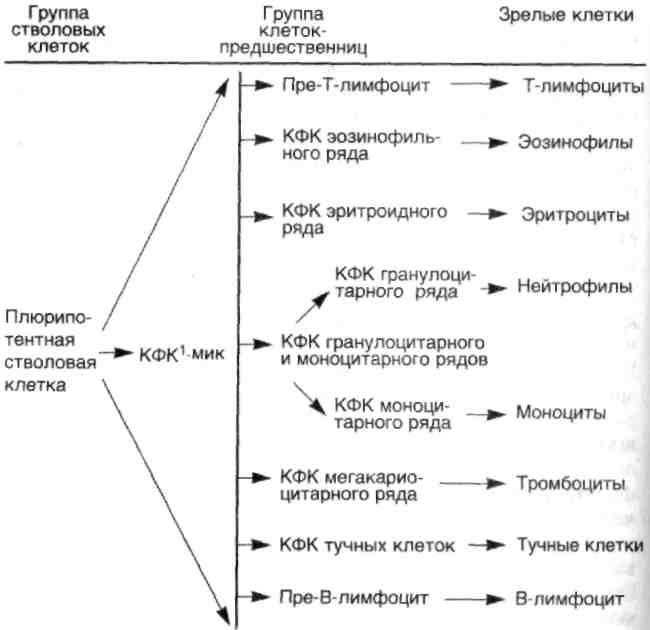
Схема 34. Структура гемопоэтической системы
1 Колониеформирующая клетка, син, колониеобразующая клетка (КОЕ).Результаты работ по изучению морфологии и клеточной кинетики гемобластозов, в первую очередь лейкозов, показали, что при развитии опухолей происходит не только малигнизация на уровне стволовых и полустволовых клеток-предшественниц, но также развивается блок дифференцировки в пуле опухолевых клеток.
ЛЕЙКОЗЫ
При лейкозах опухолевая ткань первоначально разрастается на «территории» костного мозга и постепенно замещает нормальные ростки кроветворения. Механизмы этого явления мало изучены. Вероятно, речь идет не о простом механическом вытеснении, а скорее о подавлении нормальных ростков клоном лей-козных клеток с участием особых факторов и контактного тор
314
можения. В результате этого процесса у больных лейкозами закономерно развиваются различные варианты цитопений — анемия, тромбоцитопения, лимфоцитопения, гранулоцитопения, что приводит к повышенной кровоточивости, кровоизлияниям, подавлению иммунитета с присоединением инфекционных осложнений.
Метастазирование при лейкозах сопровождается появлением лейкозных инфильтратов в различных органах — печени, селезенке, лимфатических узлах и др. В органах могут развиваться изменения, обусловленные обтурацией сосудов опухолевыми клетками — инфаркты, язвенно-некротические осложнения.
Принципы классификации лейкозов. Выделяют пять основных принципов классификации: по характеру течения лейкозов; по степени дифференцировки опухолевых клеток; в соответствии с цитогенезом; на основе иммунного фенотипа опухолевых клеток; по общему числу лейкоцитов и наличию бластных клеток в периферической крови.
По характеру течения выделяют острые, протекающие менее года, и хронические, существующие длительное время.
По степени дифференцировки опухолевых клеток выделяют недифференцированные, властные и цитарные лейкозы.
При высоком блоке дифференцировки лейкозные клетки могут напоминать стволовые и бластные клетки первых четырех классов клеток-предшественниц [Чертков И.Л., Воробьев А.И., 1993]. Поэтому по степени дифференцировки эти лейкозы называют властными и недифференцированными. Поскольку они протекают остро, то можно говорить, что острые лейкозы — это бластные и недифференцированные лейкозы.
При низком блоке дифференцировки лейкозные клетки напоминают процитарные и цитарные клетки-предшественницы, лейкозы протекают менее злокачественно, хронически и называются цитарными.
Цитогенетические варианты лейкозов основываются на представлениях о кроветворении (см. схему 34). Острые лейкозы по цитогенезу подразделяются на лимфобластный, миелобластный, монобластный, миеломонобластный, эритроми-елобластный, мегакариобластный, недифференцированный. Хронические лейкозы представлены лейкозами миелоцитарного происхождения (хронический миелоцитарный лейкоз, хронический нейтрофильный лейкоз, хронический эозинофильный лейкоз, хронический базофильный лейкоз, миелосклероз и др.), лим-фоцитарного происхождения (хронический лимфолейкоз, пара-протеинемические лейкозы: миеломная болезнь, первичная мак-роглобулинемия Вальденстрема, болезнь тяжелых цепей Франк-
315
лина; лимфоматоз кожи — болезнь Сезари и др.), моноцитарно-го происхождения (хронический моноцитарный лейкоз, гистио-цитоз X).
Иммунный фенотип опухолевых клеток.В настоящее время стало возможным проводить более точное ти-пирование опухолевых клеток в зависимости от их иммунного фенотипа по экспрессии CD 19, CD20, CD5, легких цепочек иммуноглобулинов и других антигенных маркеров.
По общему числу лейкоцитов в периферической крови и наличию лейкозных клеток выделяют лейкемические (более 50—80 • 109/л лейкоцитов, в том числе бластов), сублейкемические (50—80 • 109/л, в том числе бласты), лейкопенические (содержание лейкоцитов в периферической крови ниже нормы, но есть бласты), алейкемические (содержание лейкоцитов в периферической крови ниже нормы, бласты отсутствуют).
Морфологическое исследование имеет большое значение в диагностике лейкозов. Основными методами прижизненной морфологической диагностики являются исследования мазков периферической крови и биоптатов костного мозга, которые получают при трепанации гребешка подвздошной кости или пункции грудины, а также других органов.
Острые лейкозы
Различные формы острого лейкоза имеют стереотипные морфологические проявления: лейкозная инфильтрация костного мозга в виде очаговых и диффузных инфильтратов из клеток с крупными светлыми ядрами, содержащими по нескольку ядрышек. Размеры и очертания ядер, а также ширина ободка цитоплазмы могут варьировать. Бласты составляют 10—20 % костномозговых клеток. Цитогенетическую принадлежность бластов, как правило, можно выявить только с помощью специальных методов исследования — цитохимических и иммуногистохимиче-ских. Применяются реакции на пероксидазу, окраска на липиды Суданом черным, ШИК-реакция, гистоферментохимические реакции на выявление неспецифической эстеразы, хлорацетатэсте-разы, кислой фосфатазы, Иммуногистохимически возможно определение маркеров В-, Т-лимфоцитов, клеток миелоидного и моноцитарного рядов.
В периферической крови и в костном мозге описывается феномен лейкемического провала («hiatus leucemicus»), развивающийся за счет наличия только бластных и дифференцированных клеток и отсутствия промежуточных форм.
В костномозговой ткани происходят вытеснение нормальных клеток гемопоэза опухолевыми, истончение и резорбция ретику-
лярных волокон, нередко развивается миелофиброз. При цито-статической терапии происходит опустошение костного мозга с гибелью бластных форм, увеличивается число жировых клеток и разрастается соединительная ткань.
Лейкозные инфильтраты в виде диффузных или очаговых скоплений обнаруживаются в лимфатических узлах, селезенке и печени. Это приводит к увеличению размеров этих органов. В печени характерно развитие жировой дистрофии. В связи с лейкоз-ной инфильтрацией слизистых оболочек полости рта и ткани миндалин появляются некротический гингивит, тонзиллит — некротическая ангина. Иногда присоединяется вторичная инфекция и развивается сепсис, приводящий больных к смерти.
В результате тромбоцитопении, повреждения печени и стенок сосудов у больных острыми лейкозами нередко возникает геморрагический синдром вплоть до развития смертельных осложнений — кровоизлияний в головной мозг и желудочно-кишечных кровотечений.
Использование активной цитостатической терапии повлияло на течение острых лейкозов, т.е. привело к индуцированному лекарственному патоморфозу. В связи с этим в настоящее время выделяют следующие клинические стадии заболевания: первая атака, ремиссия (полная или неполная), рецидив (первый, повторный).
Наибольшее значение среди острых лейкозов имеют острый лимфобластный и острый миелобластный лейкозы.
Острый лимфобластный лейкоз. Самый распространенный лейкоз в детском и юношеском возрасте. Пик заболеваемости приходится на возраст от 1 года до 6 лет. Протекает с поражением костного мозга, лимфатических узлов, селезенки, вилочковой железы, а также других органов. Центральная нервная система обычно вовлекается при рецидивах заболевания после химиотерапии. В костном мозге, периферической крови и в других органах обнаруживаются опухолевые клетки типа лимфобластов с ШИК-положительными гранулами в цитоплазме, не дающие реакций на пероксидазу, эстеразы и не содержащие липиды.
В 2/3 случаев в опухолевых клетках обнаруживаются цитоге-нетические нарушения в виде полиплоидии, филадельфийской хромосомы и реципрокной транслокации между хромосомами 8 и 14.
Цитогенез острого лимфобластного лейкоза связан с предшественниками Т- и В-лимфоцитов. На Т-клеточные лейкозы в странах Европы приходится 10—15 % наблюдений. Преобладают В-клеточные лейкозы.
Руководствуясь иммунологическими фенотипами опухолевых клеток, выделяют несколько форм лимфобластного лейкоза, что имеет значение для выбора терапии и прогноза. Преобладающие
316
317
В-лимфобластные лейкозы представлены ранним, промежуточным и поздним вариантами, отличающимися по экспрессии пара-глобулина CD 10, поверхностного иммуноглобулина и активности терминальной диоксинуклеотидтрансферазы. Маркерами Т-лимфобластного лейкоза являются антигены CD7 и Т-рецепто-ров.
У детей преобладает промежуточный вариант, у взрослых — ранний и промежуточный. Прогноз у детей значительно лучше, чем у взрослых. Выживаемость составляет соответственно 60 и 30 %. Наихудший прогноз при Т-лимфобластном лейкозе.
Острый миелобластный лейкоз. Наиболее частая форма заболевания у взрослых с относительно хорошим прогнозом — ремиссии наступают у 70—80 % больных, полные ремиссии — у 25 % больных.
Описываются наблюдения развития острого миелобластного лейкоза у людей, подвергшихся радиационному воздействию, контактирующих с бензолом (кожевенная индустрия в Турции, производство синтетических клеев и др.), принимавших цитоста-тические препараты, а также у страдающих наследственными заболеваниями — болезнью Дауна, анемией Фанкони, синдромом Блума.
Опухолевые клетки имеют типичные для миелобластов цитохимические маркеры: ШИК-положительную диффузно окрашенную цитоплазму, содержат липиды, пероксидазу, эстеразы. Опухолевые клетки инфильтрируют костный мозг, приобретающий макроскопически пиоидный вид, селезенку, печень, лимфатические узлы, слизистую оболочку желудочно-кишечного тракта, что сопровождается язвенно-некротическими и геморрагическими осложнениями. В 1/3 случаев лейкозные инфильтраты обнаруживаются в легких («лейкозный пневмонит»), в 114 — в оболочках мозга («лейкозный менингит»). По иммунологическим фенотипам выделяют 6 вариантов заболевания.
Больные умирают от кровоизлияний в головной мозг, желудочно-кишечных кровотечений и инфекционных осложнений. Лечение цитостатиками изменило проявления заболевания, удлинило жизнь больным.
Хронические лейкозы
Хронические лейкозы отличаются от острых цитарной диф-ференцировкой опухолевых клеток, более длительным стадийным течением.
Первая стадия заболеваний характеризуется присутствием одного клона опухолевых клеток, течет годами, относительно доброкачественно, хронически и называется м о н о -клоновой, доброкачественной.
318
ь Вторая стадия обусловлена появлением вторичных опухолевых клонов, характеризуется быстрым, злокачественным течением с появлением множества бластов и называется злокачественной, поликлоновой стадией, или стадией властного криза. 80% больных хроническими лейкозами погибают в стадии властного криза.
Результаты цитогенетических исследований показали, что злокачественная трансформация кроветворных клеток при хронических лейкозах может происходить на очень ранних стадиях — на стадиях стволовых клеток. Цитарный характер лейкозов обусловлен низким блоком дифференцировки в опухолевых клетках.
При хронических лейкозах лейкозные инфильтраты обнаруживаются в костном мозге, где в связи с длительными течением и цитостатической терапией нередко развивается миелофиброз в печени, селезенке и лимфатических узлах, которые иногда достигают значительных размеров.
Хронические лимфоцитарные лейкозы. Эти формы лейкозов объединяются в две группы. Первая — хронический лимфолей-коз и примыкающие к нему болезнь Сезари (лимфоматоз кожи), Т-клеточный лимфоцитарный лейкоз, пролимфоцитарный лейкоз (В-клеточный), волосато-клеточный лейкоз (В-клеточный). Вторая группа — парапротеинемические лейкозы. Наибольшее значение имеет хронический лимфолейкоз.
Хронический лимфолейкоз. Встречается обычно у лиц старше 40 лет, чаще в пожилом возрасте. Мужчины болеют в два раза чаще женщин. Заболеваемость достигает 6 случаев на 100 000 населения.
Цитогенез — в 95 % случаев из ранних В-клеток. Опухолевые клетки напоминают пролимфоциты и малые лимфоциты и экс-прессируют параглобулины CD 19, CD20, CD5.
В клинической картине преобладают лимфаденопатия, анемия (нередко аутоиммунная), тромбоцитопения, гранулоцитопе-ния, имеются выраженная иммунодепрессия и предрасположенность к инфекционным осложнениям. Прогноз относительно хороший, заболевание протекает длительно с высокими показателями выживаемости. Однако в финале может развиться властный криз.
Лейкозные инфильтраты диффузно поражают костный мозг, лимфатические узлы, которые могут достигать значительных размеров, образуя мягкие или плотноватые пакеты, а также сдавливать соседние органы. Селезенка резко увеличена, в отдельных случаях ее масса составляет несколько килограммов. Печень увеличена в меньшей степени.
Больные умирают обычно от инфекционных осложнений. Описаны наблюдения трансформации хронического лимфолеи-коза в неходжкинские лимфомы.
319
Парапротеинемические лимфолейкозы.В эту группу входят три заболевания — миеломная болезнь, первичная макроглобулинемия Вальденстрема и болезнь тяжелых цепей Франклина. Особенностью парапротеинемических лейкозов, которые также называются злокачественными иммунопро-лиферативными заболеваниями, является способность опухолевых клеток синтезировать однородные иммуноглобулины или их фрагменты — парапротеины, что связано с цитогенезом опухолевых клеток. Опухолевые клетки при парапротеинемических лейкозах дифференцируются по плазмоцитарному типу, сохраняя в извращенной форме особенность плазматических клеток синтезировать иммуноглобулины.
Наибольшее значение среди парапротеинемических лейкозов имеет миеломная болезнь.
Миеломная болезнь (болезнь Рустицкого — Калера, множественная миелома, генерализованная плазмоцитома) встречается в основном у взрослых. Описаны единичные наблюдения у людей моложе 30 лет. Свое название заболевание и опухолевая клетка получили в связи с преимущественной локализацией процесса на «территории» костного мозга (миелон — костный мозг).
Выделяют несколько вариантов миеломной болезни в зависимости от характера распространения миеломных инфильтратов в костном мозге, от характера миеломных клеток и от типа синтезируемого парапротеина.
По характеру распространенности опухолевого инфильтрата в костном мозге выделяют диффузную, диффузно-узловатую, множественно-узловатую формы миеломы; по клеточному составу — плазмоцитарную, плазмобластную, полиморфно-клеточную и мелкоклеточную миелому [Струков А.И., 1959].
В зависимости от способности секретировать различные типы парапротеинов различают несколько вариантов миеломной болезни: несекретирующие, диклоновые миеломы, миелому Бенс-Джонса, G-, А-, М-миеломы. Наиболее часто встречаются G-, А-миелома, миелома Бенс-Джонса, на долю которых приходится 75, 20 и 15 % наблюдений соответственно.
Опухолевая ткань разрастается преимущественно в плоских костях (череп, ребра, таз) и в позвоночнике, инициируя в них ос-теолизис, остеопороз. На рентгенограмме очаги поражения имеют вид гладкостенных пробоин. Полости образуются в местах роста миеломных клеток за счет активации ими остеокластов, осуществляющих лизис и резорбцию костной ткани (пазушное рассасывание). Высказываются предположения, что в качестве активирующих остеокласты субстанций могут выступать интер-лейкин-1 и бета-трансформирующий фактор роста, выделяемые миеломными клетками. Помимо костного мозга, опухолевые ин-фильтраты могут обнаруживаться и в других органах.
Осложнения миеломной болезни развиваются вследствие деструкции костной ткани — патологические переломы, боли в ко-
320
стях, а также из-за продукции парапротеинов — амилоидоз (AL-амилощоз), парапротеинемическая кома и парапротеиноз органов.
Хронические миелоцитарные лейкозы. Группа лейкозов, содержащих опухолевые клетки типа процитарных и цитарных предшественников миелоидного ряда. В эту группу входят хронический миелоцитарный лейкоз с или без филадельфийской хромосомы, ювенильный хронический миелоцитарный лейкоз, хронический нейтрофильный лейкоз, хронический эозинофильный лейкоз, первичный миелофиброз (мегакариоцитарная диффе-ренцировка опухолевых клеток). Разнообразие форм хронических миелоцитарных лейкозов обусловлено существованием общей клетки-предшественницы гранулоцитарного, моноцитарно-го, мегакариоцитарного, эозинофильного и базофильного ростков. При развитии всех этих форм злокачественная трансформация, вероятно, происходит на уровне плюрипотентной стволовой клетки миелоидного ростка, так как цитогенетические маркеры можно обнаружить во всех ветвях этого ростка.
Хронический миелолейкоз представляет наибольший практический интерес. Это нередкое заболевание, на долю которого приходится 15 % всех случаев лейкоза. В США ежегодно регистрируется 2500 новых случаев. Встречается в любом возрасте, немного чаще у лиц мужского пола. В развитии заболевания имеют значение те же этиологические факторы, что и при остром миелобластном лейкозе.
Цитогенетическим маркером заболевания является филадельфийская хромосома, свидетельствующая также и о плохом прогнозе.
Заболевание протекает в две или даже три стадии: хроническая стадия, промежуточная (выделяется клиницистами, так как требует особых терапевтических мероприятий) и бласттранс-формации.
Хроническая стадия длится 3—4 года, нередко не имеет клинических проявлений. Морфологически в эту стадию обнаруживают сплено- и гепатомегалию, анемию. В костном мозге, периферической крови, в селезенке, печени и лимфатических узлах обнаруживают увеличение про- и цитарных форм миелоидного ростка, имеющих маркеры одного опухолевого клона.
Промежуточная стадия сопровождается нарастанием слабости, повышением температуры тела, появлением клеток с новыми цитогенетическими отклонениями, резистентных к применявшимся ранее цитостатикам, прогрессированием сплено- и гепато-мегалии. Эта стадия длится несколько месяцев, но при правильно назначенном лечении может быть пролонгирована.
Стадия бласттрансформации — властного криза — заканчивается смертью больных, несмотря на проводимую терапию, в
321
очень короткие сроки. В инфильтратах в костном мозге и во внутренних органах, а также в периферической крови появляются бластные формы (12—25 %), опухолевые клоны с новыми цито-генетическими нарушениями.
У 10 % больных заболевание заканчивается миелофиброзом, обусловленным действием цитостатиков. Другой причиной мие-лофиброза может быть двухростковая пролиферация клеток типа цитарных предшественников грануло- и мегакариоцитарного ростков. Последние продуцируют фактор роста тромбоцитов, активирующий фибробласты.
На аутопсии имеются характерные изменения внутренних органов: пиоидный костный мозг, значительные сплено- и генато-мегалия, умеренное увеличение лимфатических узлов.
ЛИМФОМЫ
• Лимфомы — регионарные злокачественные опухоли лимфо-идной ткани. Имеют моноклоновое происхождение, что используется при их диагностике и дифференциальной диагностике с реактивными гиперпластическими процессами в лимфоидной ткани.
Диагноз лимфом устанавливается прежде всего при биопсии
лимфатических узлов.
Классификация. В настоящее время используется несколько классификаций лимфом: H.Rappoport (1966), R.G.Lukes — R.D.Collins (1973—1974), R.E.A.L., кильская и ВОЗ, включающая в себя обе эти классификации.
Классификация лимфом [R.E.A.L. и кильская, 1996]
