Синдром недостаточности кровотока в артериях вертебробазилярной системы
Максимова М.Ю., Пирадов М.А.РМЖ. 2018. №7. С. 4-8
Статья посвящена проблеме синдрома недостаточности кровотока в артериях вертебробазилярной системы. Представлены методы диагностики и лечения вертебробазилярной недостаточности, которое должно быть направлено на предупреждение ее прогрессирования, улучшение кровоснабжения мозга, коррекцию отдельных синдромов и симптомов.
Самостоятельное клиническое понятие «синдром недостаточности кровотока в артериях вертебробазилярной системы» сформировалось в 1950-х гг., в период пересмотра взглядов на патогенез ишемических нарушений мозгового кровообращения (НМК) и становления концепции о ведущей роли при этом сосудистой мозговой недостаточности [1].
Особенности строения и функций этой артериальной системы, обеспечивающей питание жизненно важных структур мозга, и своеобразие клинической симптоматики при нарушениях кровотока в ней обусловили выделение ее в последней версии международной классификации в самостоятельный симптомокомплекс — «синдром вертебробазилярной артериальной системы» в рамках «преходящих транзиторных церебральных ишемических приступов (атак) и родственных синдромов» (Международная классификация болезней 10-го пересмотра, G45. 0).
0).
Еще раньше группой экспертов Всемирной организации здравоохранения «вертебробазилярная недостаточность» определялась как «обратимое нарушение функции мозга, вызванное уменьшением кровоснабжения области, питаемой позвоночными и базилярной артериями». Подчеркивались ишемическая природа и обратимый характер нарушений, однако не указывалась длительность неврологической симптоматики, что ранее не позволяло отнести их к транзиторным ишемическим атакам (ТИА) и что стало возможным в настоящее время. Нарушения кровотока в артериях вертебробазилярной системы составляют около 70% всех ТИА. Инсульт с локализацией очаговых изменений в областях мозга, получающих кровь по артериям этой системы, развивается в 2,5 раза реже, чем в регионах, относящихся к бассейнам артерий каротидной системы [1].
Причины синдрома недостаточности кровотока в артериях вертебробазилярной системы
К основным причинам синдрома недостаточности кровотока в артериях вертебробазилярной системы, обусловленного артериальной гипертензией (АГ) и атеросклерозом (АС), относятся [1, 2]:- атеростеноз или атерооблитерация одной из позвоночных артерий;
- характерная для АГ извитость артерий, которая в ряде случаев может привести к перегибу позвоночной артерии с формированием септального стеноза и нарушению кровотока в ней;
- врожденные аномалии позвоночных артерий (гипоплазия одной из позвоночных артерий, латеральное смещение устья позвоночной артерии), при которых недостаточность кровотока по одной из позвоночных артерий компенсируется другой позвоночной артерией, однако на фоне АС и АГ наступает декомпенсация;
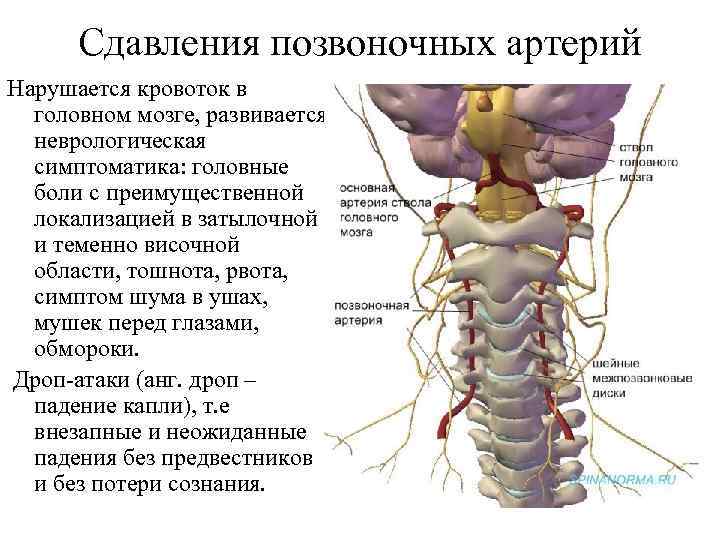
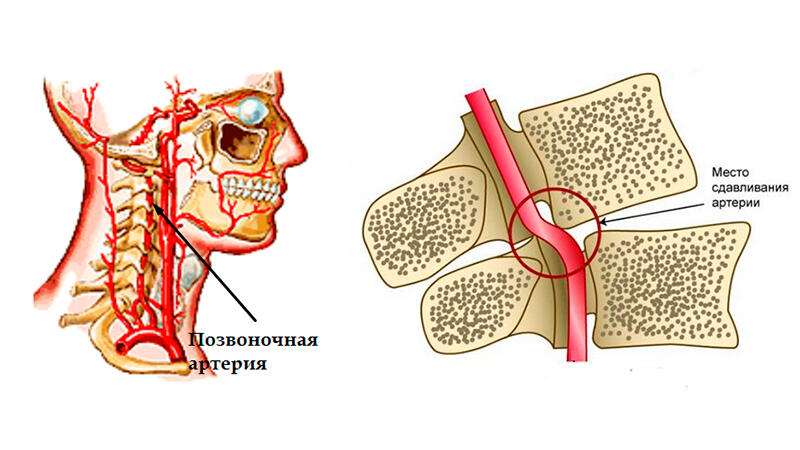
- сдавление позвоночной артерии остеофитом в костном канале шейного отдела позвоночника, суставным отростком при нестабильности шейного отдела позвоночника, добавочным шейным ребром, спазмированной мышцей шеи (задняя лестничная мышца, длинная мышца шеи, нижняя косая мышца головы), что чаще всего наблюдается при врожденном аномально высоком вхождении позвоночной артерии в позвоночный канал — на уровне 3–5 шейных позвонков.

Cиндром недостаточности кровотока в артериях вертебробазилярной системы может также наблюдаться:
- при подключичном «синдроме обкрадывания», при котором в результате окклюзии подключичной артерии поступление крови не только во всю вертебробазилярную систему, но и в руку осуществляется лишь по одной позвоночной артерии;
- при окклюзии или выраженном атеростенозе обеих внутренних сонных артерий (ВСА), т. к. в кровоснабжении полушарий большого мозга значительную роль играет вертебробазилярная система и при определенных условиях может возникнуть «синдром обкрадывания»;
- при нарушениях общей гемодинамики.
Для подключичного «синдрома обкрадывания» характерен феномен, когда у больного во время интенсивной работы руки (кровоснабжаемой ретроградно из контралатеральной позвоночной артерии) возникают стволовые симптомы — чаще всего головокружение.
Определенный вклад в развитие синдрома недостаточности кровотока в вертебробазилярной системе могут вносить изменения реологических свойств крови (повышение уровня фибриногена, вязкости крови, агрегации тромбоцитов и гематокрита, увеличение ригидности эритроцитов), приводящие к ухудшению микроциркуляции.
Диагностика недостаточности кровотока в артериях вертебробазилярной системы
Субъективные данные
Диагноз недостаточности кровотока в артериях вертебробазилярной системы основывается на характерном симптомокомплексе, объединяющем несколько групп клинических симптомов, встречающихся у больных АС и АГ. Это зрительные и глазодвигательные расстройства, нарушения статики и координации движений, вестибулярные нарушения. При этом предположительный диагноз определяется на основе не менее двух из указанных симптомов. Они кратковременны и нередко проходят сами по себе, хотя являются признаком нарушений кровотока в артериях этой системы, что требует клинического и инструментального обследования. Особенно необходим тщательный анамнез для уточнения обстоятельств возникновения тех или иных симптомов [1, 2].Зрительные нарушения включают в себя ощущение неясности видения, фотопсии, скотомы, изменения полей зрения, снижение остроты зрения и связаны с преходящей ишемией затылочных долей мозга.
 Неясность видения в форме пелены перед глазами и затуманивания зрения нередко возникает на высоте головной боли. Фотопсии проявляются в виде вспышек цветных точек, чаще всего красных или зеленых, черных, со светлым ореолом, а также пятен, огненных молний, линий, колец, зигзагов. От радужных кругов, характерных для глаукомы, фотопсии отличаются тем, что их появление не связано с внешним источником света; они возникают и при закрытых глазах. Изменение полей зрения наблюдается обычно в форме
Неясность видения в форме пелены перед глазами и затуманивания зрения нередко возникает на высоте головной боли. Фотопсии проявляются в виде вспышек цветных точек, чаще всего красных или зеленых, черных, со светлым ореолом, а также пятен, огненных молний, линий, колец, зигзагов. От радужных кругов, характерных для глаукомы, фотопсии отличаются тем, что их появление не связано с внешним источником света; они возникают и при закрытых глазах. Изменение полей зрения наблюдается обычно в форме их концентрического сужения. Снижение остроты зрения часто развивается после появления головной боли и прогрессирует; зрение заметно ухудшается в период приступов головной боли и после них.
Глазодвигательные нарушения проявляются в виде преходящей диплопии с негрубыми парезами мышц глаза и нарушенной конвергенцией. У большинства больных эти нарушения относятся к начальным проявлениям заболевания, а у четверти из них служат одной из главных жалоб при вертебробазилярной недостаточности.

Статическая и динамическая атаксия относится также к числу постоянных симптомов, которые проявляются жалобами больных на неустойчивость и пошатывание при ходьбе и стоянии. Координация движений нарушена значительно меньше, стойкое изменение ее встречается, как правило, при инфарктах мозжечка.
Вестибулярные нарушения проявляются в виде внезапного головокружения — системного, для которого характерно ощущение «вращения предметов», «перевернутой комнаты», и несистемного с ощущением «укачивания», тошнотой, реже рвотой. Обнаруживается также спонтанный нистагм, иногда только после специальных проб с поворотами головы в сторону и фиксацией ее в этих позах (проба Де Клейна). Развитие головокружения связывают с ишемией или преддверно-улиткового органа, или вестибулярных ядер и их связей. Вестибулярные ядра наиболее чувствительны к ишемии и гипоксии.
При этом головокружение как моносимптом может расцениваться в качестве признака нарушения кровотока в артериях вертебробазилярной системы только в сочетании с другими признаками его нарушения у больных с относительно стойким отоневрологическим симптомокомплексом.
 Менее известны, хотя встречаются нередко, оптико-вестибулярные расстройства. К ним относятся симптомы «колеблющейся тени» и «конвергентного головокружения», при которых больные испытывают головокружение или неустойчивость при мелькании света и тени или при взоре, направленном вниз.
Менее известны, хотя встречаются нередко, оптико-вестибулярные расстройства. К ним относятся симптомы «колеблющейся тени» и «конвергентного головокружения», при которых больные испытывают головокружение или неустойчивость при мелькании света и тени или при взоре, направленном вниз.Характерными симптомами являются приступы внезапного падения без потери сознания («дроп-атаки»), возникающие обычно при резких поворотах или запрокидывании головы. Описан синкопальный вертебральный синдром Унтерхарншайдта, при котором наблюдаются утрата сознания и гипотония мышц при отсутствии данных за эпилепсию и другие пароксизмальные состояния.
К проявлениям диэнцефальных расстройств относятся резкая общая слабость, непреодолимая сонливость, нарушения ритма сна и бодрствования, а также различные вегетативно-висцеральные нарушения, внезапное повышение артериального давления (АД), нарушения сердечного ритма. Эти нарушения связаны с ишемией структур ретикулярной формации ствола мозга.
Описанный симптомокомплекс дополнен в настоящее время другими признаками, которые в сочетании с ними также позволяют судить о недостаточности кровотока в артериях вертебробазилярной системы. На различных стадиях вертебробазилярной недостаточности больные нередко предъявляют жалобы на снижение памяти («забывчивость»), расстройства концентрации и неустойчивость активного внимания. Чаще всего снижается память на имена, числа, недавно происшедшие события. Снижается способность к запоминанию нового материала, становится труднее удерживать в памяти прочитанное, забывается то, что намечено к осуществлению, возникает необходимость записывать. Больным становится трудно осмыслить большое количество информации, что приводит у лиц, занятых умственным трудом, к определенному снижению работоспособности, ограничению творческих возможностей. В то же время профессиональная память и память на прошлые события сохраняются. Это больше относится к оперативной памяти, чем к логической. Нередко снижение памяти и работоспособности расценивается окружающими как результат переутомления, а не как проявление сосудистой мозговой недостаточности.
 При нейропсихологическом исследовании отмечаются сохранность уровня обобщения, соответствие суждений общеобразовательному и культурному уровню, сохранность запаса представлений и навыков.
При нейропсихологическом исследовании отмечаются сохранность уровня обобщения, соответствие суждений общеобразовательному и культурному уровню, сохранность запаса представлений и навыков.Нарушения когнитивных функций существенно снижают качество жизни, а также оказывают влияние на прогрессирование сосудистой мозговой недостаточности.
Снижение памяти на текущие события у больных с вертебробазилярной недостаточностью связано с хронической ишемией медиальных частей височных долей, прежде всего гиппокампа и сосцевидных тел. При вертебробазилярной недостаточности отмечаются и приступы транзиторной глобальной ишемии, при которой на несколько часов нарушается оперативная память (способность к запоминанию новой информации). Больной выглядит рассеянным, он дезориентирован в пространстве и времени, иногда возбужден, настойчиво пытается выяснить у окружающих, где находится, как оказался здесь, но будучи не в состоянии запомнить ответы, постоянно задает одни и те же вопросы. С возвращением способности к запоминанию восстанавливается и ориентация, амнезируется лишь сам эпизод.

Причиной острой амнезии может служить и острое НМК в бассейнах обеих задних мозговых артерий. В этом случае амнезии могут сопутствовать ограничение полей зрения (односторонняя или двусторонняя гемианопсия), зрительная агнозия, алексия, амнестическая афазия, нарушение чувствительности.
Сочетание ряда характерных симптомов позволяет диагностировать синдром недостаточности кровотока в артериях вертебробазилярной системы, хотя при этом определяются лишь ишемический характер НМК и локализация очага ишемии, а не причины, обусловившие этот характер.
Объективные данные
Наиболее доступными и безопасными для определения недостаточности кровотока в артериях вертебробазилярной системы являются неврологический осмотр и ультразвуковые методы исследования сосудистой системы мозга.Среди объективных признаков, выявляемых при неврологическом осмотре, следует прежде всего назвать нистагм, статическую и динамическую атаксию. В пробе Ромберга больной отклоняется в сторону.
 Ходьба с закрытыми глазами выявляет у пациента с недостаточностью кровотока в вертебробазилярной системе шаткость и стойкое отклонение в одну из сторон. При проведении пробы Унтербергера пациента просят маршировать на одном месте с закрытыми глазами в течение 1–3 мин. В норме он остается на месте или незначительно смещается относительно исходной точки либо слегка поворачивается вокруг оси. Патологическими считаются смещение вперед более чем на 1 м и поворот более чем на 40–60° (после 50 шагов на месте). Подобным образом интерпретируют результаты пробы Бабинского — Вейля («звездная проба»). Пациента просят с закрытыми глазами сделать два шага вперед, развернуться на 180° и сделать два шага назад. Любые отклонения в сторону или ротация указывают на нарушение функции вестибулярного лабиринта. Если пациента просят пройти в прямом и обратном направлении несколько раз, то в результате отклонения в одну из сторон траектория его движения напоминает очертания звезды (отсюда название пробы).
Ходьба с закрытыми глазами выявляет у пациента с недостаточностью кровотока в вертебробазилярной системе шаткость и стойкое отклонение в одну из сторон. При проведении пробы Унтербергера пациента просят маршировать на одном месте с закрытыми глазами в течение 1–3 мин. В норме он остается на месте или незначительно смещается относительно исходной точки либо слегка поворачивается вокруг оси. Патологическими считаются смещение вперед более чем на 1 м и поворот более чем на 40–60° (после 50 шагов на месте). Подобным образом интерпретируют результаты пробы Бабинского — Вейля («звездная проба»). Пациента просят с закрытыми глазами сделать два шага вперед, развернуться на 180° и сделать два шага назад. Любые отклонения в сторону или ротация указывают на нарушение функции вестибулярного лабиринта. Если пациента просят пройти в прямом и обратном направлении несколько раз, то в результате отклонения в одну из сторон траектория его движения напоминает очертания звезды (отсюда название пробы).Необходимо также измерить АД на обеих руках в положении сидя и лежа.
 К объективным признакам синдрома относятся разница пульса и АД на руках и шум в надключичной области. При значительном снижении систолического АД (более 20 мм рт. ст.) в вертикальном положении симптоматику, напоминающую недостаточность кровотока в вертебробазилярной системе, следует отнести за счет ортостатической гипотензии. Для подключичного «синдрома обкрадывания» характерен феномен, когда у больного на фоне интенсивной работы рукой возникают стволовые симптомы — чаще головокружение.
К объективным признакам синдрома относятся разница пульса и АД на руках и шум в надключичной области. При значительном снижении систолического АД (более 20 мм рт. ст.) в вертикальном положении симптоматику, напоминающую недостаточность кровотока в вертебробазилярной системе, следует отнести за счет ортостатической гипотензии. Для подключичного «синдрома обкрадывания» характерен феномен, когда у больного на фоне интенсивной работы рукой возникают стволовые симптомы — чаще головокружение.Ультразвуковая допплерография позволяет получать данные о кровотоке в позвоночных артериях, линейной скорости и направлении потоков крови в них. Компрессионно-функциональные пробы дают возможность оценить состояние и ресурсы коллатерального кровообращения, кровоток в сонных, височных, надблоковых и других артериях. Дуплексное сканирование позволяет определить состояние стенки артерий, строение и поверхность атеросклеротических бляшек, стенозирующих эти артерии. Транскраниальная допплерография с фармакологическими пробами имеет значение для определения церебрального гемодинамического резерва.
 Исключительно информативны данные о состоянии магистральных артерий головы (МАГ) и интрацеребральных артерий, получаемые при КТ и МРТ в режиме ангиографии. При рентгенографии шейной части позвоночника могут быть получены данные о состоянии структур вокруг позвоночных артерий и воздействии этих структур на позвоночные артерии и кровоток в них; при этом используются функциональные пробы.
Исключительно информативны данные о состоянии магистральных артерий головы (МАГ) и интрацеребральных артерий, получаемые при КТ и МРТ в режиме ангиографии. При рентгенографии шейной части позвоночника могут быть получены данные о состоянии структур вокруг позвоночных артерий и воздействии этих структур на позвоночные артерии и кровоток в них; при этом используются функциональные пробы.Особое место в ряду инструментальных методов занимает отоневрологическое исследование, особенно если оно подкрепляется электронистагмографическими и электрофизиологическими данными о слуховых вызванных потенциалах, характеризующих состояние структур ствола мозга, а также МPТ этих структур.
Алгоритм применения перечисленных инструментальных методов исследования определяется логикой построения клинического диагноза.
Лечение вертебробазилярной недостаточности
Лечение вертебробазилярной недостаточности направлено на предупреждение ее прогрессирования, улучшение кровоснабжения мозга, коррекцию отдельных синдромов и симптомов.
Наиболее эффективными мерами в этом направлении являются исключение или коррекция основных факторов риска развития вертебробазилярной недостаточности, к которым относятся курение, гиперлипидемия, АС артерий мозга, АГ, сахарный диабет, ожирение, заболевания сердца, нарушения реологических свойств крови, психоэмоциональное перенапряжение, злоупотребление алкоголем [3].
Большое место в профилактике прогрессирования вертебробазилярной недостаточности занимают оздоровительные мероприятия, климатолечение на местных курортах, в условиях мелкогорья, на морских курортах, бальнеолечение (радоновые, рапные, углекислые, сульфидные, йодобромные ванны). Нужны умеренные физические нагрузки (лечебная гимнастика, ходьба, плавание) и регулярные умственные нагрузки.
Диета не должна быть тягостной для больного (не переедать, ограничить потребление животных жиров, легкоусвояемых углеводов и продуктов, богатых холестерином, уменьшить общую калорийность пищи, ввести в рацион свежие овощи и фрукты, изделия из муки грубого помола, рыбные продукты).
 Исключается курение и ограничивается потребление алкоголя.
Исключается курение и ограничивается потребление алкоголя.При лечении вертебробазилярной недостаточности следует провести следующие мероприятия: раннее ее выявление; определение выраженности клинической симптоматики; исключение или коррекция основных факторов риска развития сердечно-сосудистых заболеваний; динамическое наблюдение; своевременное начало лечения; его длительность и непрерывность; лечение сопутствующих соматических, неврологических и психических нарушений; медицинская, профессиональная и социальная реабилитация.
К методам медикаментозного лечения хронических НМК относятся: гипотензивная терапия, применение гиполипидемических средств, улучшение кровоснабжения мозга с использованием антитромботических препаратов, нейропротекционная терапия [3, 4].
Одним из наиболее перспективных с позиции доказательной медицины нейропротекционных препаратов является цитиколин [4, 5]. Цитиколин — природное эндогенное соединение, известное также как цитидин-5’-дифосфохолин (ЦДФ-холин), представляет собой мононуклеотид, состоящий из рибозы, цитозина, пирофосфата и холина.
 При пероральном приеме цитиколин быстро абсорбируется и в стенке кишечника и печени гидролизуется на холин и цитидин. Эти вещества поступают в системный кровоток, проходят через гематоэнцефалический барьер и вновь соединяются, образуя в пределах центральной нервной системы цитиколин [6]. Фосфатидилхолин мембран клеток головного мозга под действием фосфолипаз в условиях ишемии распадается до жирных кислот и свободных радикалов. За счет восстановления активности Na+/K+-АТФ-азы клеточной мембраны, снижения активности фосфолипазы A2 и участия в синтезе фосфатидилхолина реализуется мембраностабилизирующий эффект цитиколина. Кроме того, цитиколин влияет на образование свободных жирных кислот, синтез ацетилхолина и увеличение содержания норадреналина и дофамина в нервной ткани. Цитиколин также способен ингибировать глутамат-индуцированный апоптоз и усиливать механизмы нейропластичности [7].
При пероральном приеме цитиколин быстро абсорбируется и в стенке кишечника и печени гидролизуется на холин и цитидин. Эти вещества поступают в системный кровоток, проходят через гематоэнцефалический барьер и вновь соединяются, образуя в пределах центральной нервной системы цитиколин [6]. Фосфатидилхолин мембран клеток головного мозга под действием фосфолипаз в условиях ишемии распадается до жирных кислот и свободных радикалов. За счет восстановления активности Na+/K+-АТФ-азы клеточной мембраны, снижения активности фосфолипазы A2 и участия в синтезе фосфатидилхолина реализуется мембраностабилизирующий эффект цитиколина. Кроме того, цитиколин влияет на образование свободных жирных кислот, синтез ацетилхолина и увеличение содержания норадреналина и дофамина в нервной ткани. Цитиколин также способен ингибировать глутамат-индуцированный апоптоз и усиливать механизмы нейропластичности [7].Первые исследования цитиколина, проведенные в конце ХХ в., касались пациентов с сосудистой деменцией.
 Так, R. Lozano et al. (1986) наблюдали 2067 пожилых пациентов, находившихся на лечении в отделениях гериатрической психиатрии, и выявили положительное влияние 2-месячного курса терапии цитиколином на выраженность нейропсихологических симптомов [8]. В исследовании B. Chandra (1992), посвященном оценке эффективности препарата у 146 пациентов с сосудистой деменцией, было продемонстрировано, что терапия цитиколином в дозе 750 мг/сут
Так, R. Lozano et al. (1986) наблюдали 2067 пожилых пациентов, находившихся на лечении в отделениях гериатрической психиатрии, и выявили положительное влияние 2-месячного курса терапии цитиколином на выраженность нейропсихологических симптомов [8]. В исследовании B. Chandra (1992), посвященном оценке эффективности препарата у 146 пациентов с сосудистой деменцией, было продемонстрировано, что терапия цитиколином в дозе 750 мг/сут в/в в течение 2 мес. приводила к достоверному улучшению показателей когнитивных функций (оценке по шкале MMSE) по сравнению с плацебо. Более того, эффект от терапии сохранялся через 10 мес. после окончания курса лечения [9].
В 2005 г. был опубликован Кокрановский обзор эффективности цитиколина в терапии когнитивных и поведенческих нарушений, обусловленных хронической цереброваскулярной недостаточностью, у пожилых пациентов [10]. В обзор вошли результаты 14 рандомизированных плацебо-контролируемых исследований с участием 1336 пациентов. Средняя доза цитиколина в указанных исследованиях составила 1000 мг/сут, продолжительность лечения — 3 мес.
 Эффективность лечения оценивалась по тестам на показатели памяти, внимания, поведения. В обзоре продемонстрированы позитивное влияние цитиколина на поведенческие нарушения, а также улучшение памяти.
Эффективность лечения оценивалась по тестам на показатели памяти, внимания, поведения. В обзоре продемонстрированы позитивное влияние цитиколина на поведенческие нарушения, а также улучшение памяти.Единственным существенным ограничением данного обзора являлась небольшая продолжительность включенных в него клинических исследований.
В последующие годы исследователи сосредоточились на изучении эффективности препарата у пациентов с умеренными когнитивными расстройствами (УКР) и постинсультными когнитивными нарушениями. Так, по данным М. В. Путилиной (2009), уже на начальных этапах проявлений когнитивных нарушений у пациентов с хронической сосудисто-мозговой недостаточностью применение цитиколина (в дозировке 1000 мг в/м или в/в в течение 10 сут с последующим пероральным приемом в виде раствора для приема внутрь в течение 3 мес.) способствует регрессу данных нарушений. Кроме того, препарат положительно влияет на сопутствующие эмоционально-аффективные и поведенческие расстройства в этой группе больных [11].
В 2013 г. опубликованы результаты двух контролируемых исследований, оценивающих влияние препарата на когнитивные функции у пациентов с хроническими цереброваскулярными заболеваниями. В плацебо-контролируемом исследовании L. Alvarez-Sabin et al. (2013) приняли участие 347 пожилых пациентов (средний возраст — 67,2±11,3 года), перенесших инсульт и имевших когнитивные нарушения. В группе активного лечения (172 пациента) цитиколин назначался в дозе 2000 мг/сут per os в течение 6 мес., далее по 1000 мг/сут еще 6 мес. Критериями эффективности лечения являлись результаты нейропсихологического обследования (батарея тестов на память, внимание, исполнительные (регуляторные) функции, ориентацию во времени), а также оценка клинических исходов по модифицированной шкале Рэнкина через 6 и 12 мес. после начала лечения. На фоне длительной терапии цитиколином отмечались замедление прогрессирования когнитивных расстройств и лучшее функциональное восстановление (по сравнению с плацебо) за счет улучшения внимания, регуляторных функций и ориентации во времени [12].
Исследование IDEALE было посвящено оценке эффективности цитиколина в длительной терапии сосудистых УКР у пожилых пациентов. 349 пациентам с УКР преимущественно сосудистого генеза назначался цитиколин (265 больных) в дозе 1000 мг/сут per os в течение 9 мес. или плацебо (84 пациента). Терапия цитиколином не влияла на показатели функциональной повседневной деятельности по сравнению с плацебо. Вместе с тем на фоне лечения цитиколином отмечалась положительная динамика когнитивных функций при их оценке по шкале MMSE (улучшение через 9 мес. в среднем на 0,5 балла), в группе плацебо наблюдалось прогрессирование когнитивных нарушений (через 9 мес. — ухудшение в среднем на 1,9 балла) (р=0,0001). Таким образом, длительная терапия цитиколином сопряжена со снижением темпов прогрессирования когнитивных нарушений у пациентов с сосудистыми УКР [13].
В последнее время широко внедряются в практику новые воспроизведенные лекарственные формы. Среди них — отечественный препарат Нейпилепт. Препарат выпускается из японской субстанции компании KYOWA в виде раствора 125 и 250 мг/мл для в/в и в/м введения, а также двух пероральных форм — раствора для приема внутрь 100 мг/мл во флаконах по 30 мл и 100 мл.
 Объем флакона 100 мл соответствует форме выпуска оригинального препарата в саше.
Объем флакона 100 мл соответствует форме выпуска оригинального препарата в саше.В рамках пострегистрационных многоцентровых рандомизированных исследований были проведены сравнение Нейпилепта с оригинальным препаратом у 152 пациентов в остром периоде ишемического инсульта в каротидной системе (РКИ № 396 от 24.06.2013) [14] и изучение эффективности и безопасности его пероральной формы
у 128 пациентов с когнитивными нарушениями (РКИ № 145 от 26.03.2015) [15]. Результаты исследований продемонстрировали сопоставимые с оригинальным препаратом переносимость и эффективность Нейпилепта при указанных состояниях [16, 17].
Заключение
Следует подчеркнуть, что своевременно начатое и систематически проводимое лечение может предотвратить прогрессирование сосудисто-мозговой недостаточности и значительно улучшить качество жизни пациентов. Особое значение приобретают адекватность и эффективность приема цитиколина (Нейпилепта). Адекватность терапии подразумевает курсовой прием препарата, а также сотрудничество пациента и лечащего врача при назначении и проведении лечения, целями которого являются сохранение трудоспособности и поддержание качества жизни пациента.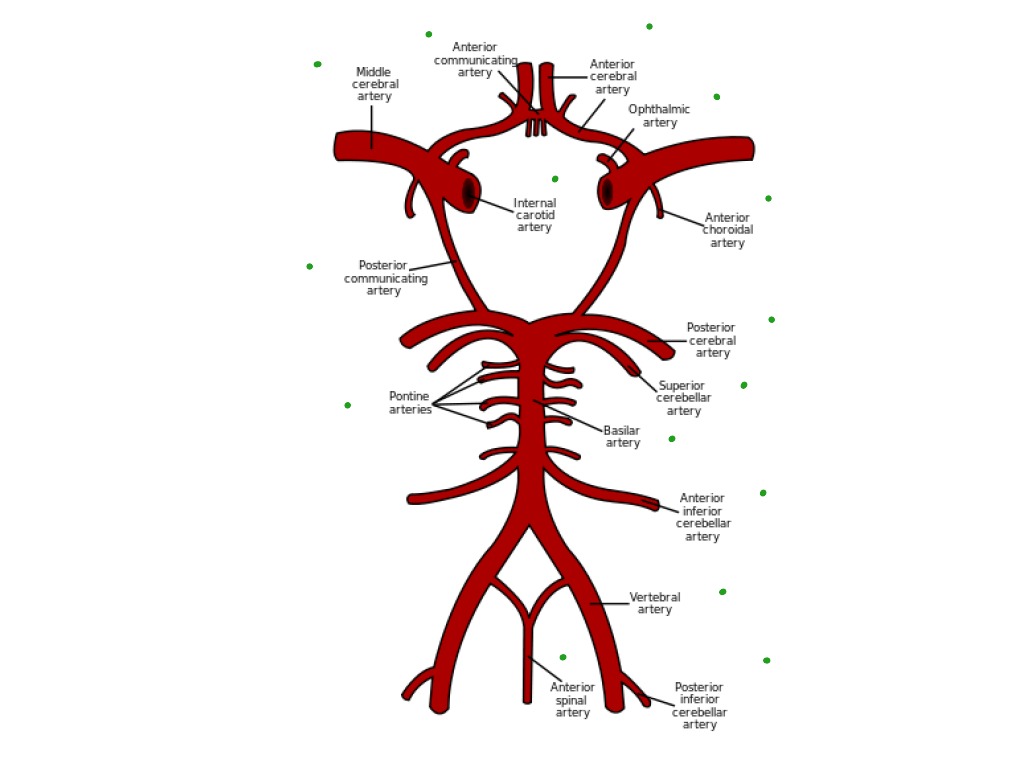 Могут быть рекомендованы следующие направления оценки эффективности лечения вертебробазилярной недостаточности (уже через 6–12 мес. от начала лечения): уменьшение или исчезновение церебральных жалоб, улучшение когнитивных функций (в первую очередь памяти).
Могут быть рекомендованы следующие направления оценки эффективности лечения вертебробазилярной недостаточности (уже через 6–12 мес. от начала лечения): уменьшение или исчезновение церебральных жалоб, улучшение когнитивных функций (в первую очередь памяти).Оригинальная статья опубликована на сайте РМЖ (Русский медицинский журнал): https://www.rmj.ru/articles/nevrologiya/Sindrom_nedostatochnosti_krovotoka_varteriyah_vertebrobazilyarnoy_sistemy/#ixzz5NyXkC9vV
Форма записи на приём…
Синдром позвоночной артерии. / Статьи / «Авиценна» в Волгограде
16/11/20
Синдром позвоночной артерии.
Синдром позвоночной артерии – это целый комплекс симптомов, которые возникают при нарушении кровотока по позвоночным артериям.
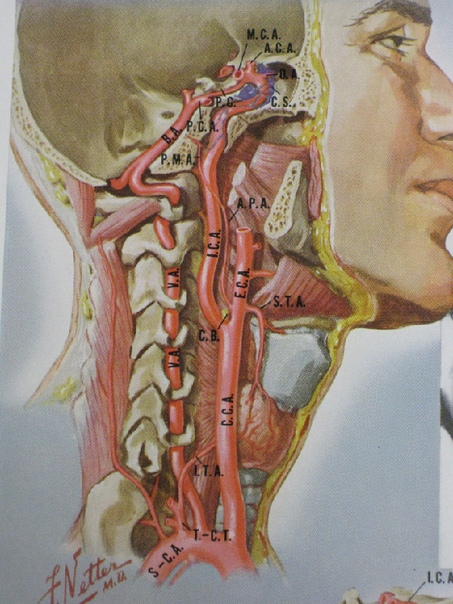
Разберемся почему это может произойти. Для понимания стоит вспомнить анатомию. Кровоснабжение головного мозга осуществляется парными сосудами общей сонной и позвоночной артериями. Диаметр общей сонной артерии в два раза больше диаметра позвоночной .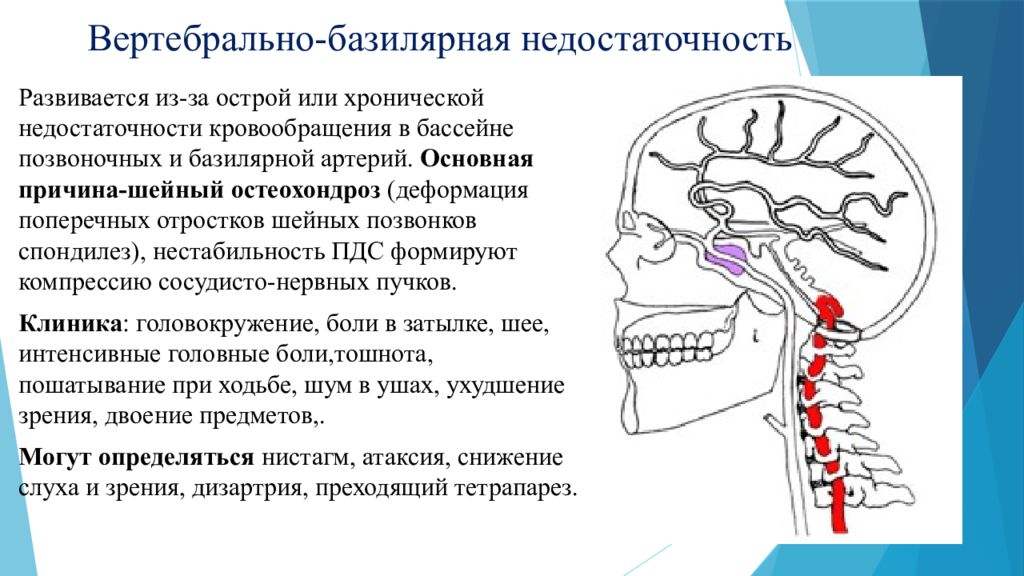 Очевидно, что основной кровоток головного мозга обеспечивается общей сонной артерией и его нарушение приводит к серьезным сосудистым катастрофам, в частности к инфаркту мозга. Вклад позвоночной артерии в обеспечение кровоснабжения головного мозга более «скромный», но, несмотря на это, именно патология позвоночной артерии чаще всего заставляет пациентов обращаться к врачу с жалобами. Позвоночные артерии берут свое начало от подключичных артерий в грудной полости и проходят к головному мозгу через канал, образованный поперечными отростками шейных позвонков . С одной стороны, сосуд внутри костного канала защищен от возможного неблагоприятного воздействия, с другой стороны патология шейного отдела позвоночника может создать дополнительные факторы повреждения или компрессии артерии.
Очевидно, что основной кровоток головного мозга обеспечивается общей сонной артерией и его нарушение приводит к серьезным сосудистым катастрофам, в частности к инфаркту мозга. Вклад позвоночной артерии в обеспечение кровоснабжения головного мозга более «скромный», но, несмотря на это, именно патология позвоночной артерии чаще всего заставляет пациентов обращаться к врачу с жалобами. Позвоночные артерии берут свое начало от подключичных артерий в грудной полости и проходят к головному мозгу через канал, образованный поперечными отростками шейных позвонков . С одной стороны, сосуд внутри костного канала защищен от возможного неблагоприятного воздействия, с другой стороны патология шейного отдела позвоночника может создать дополнительные факторы повреждения или компрессии артерии.
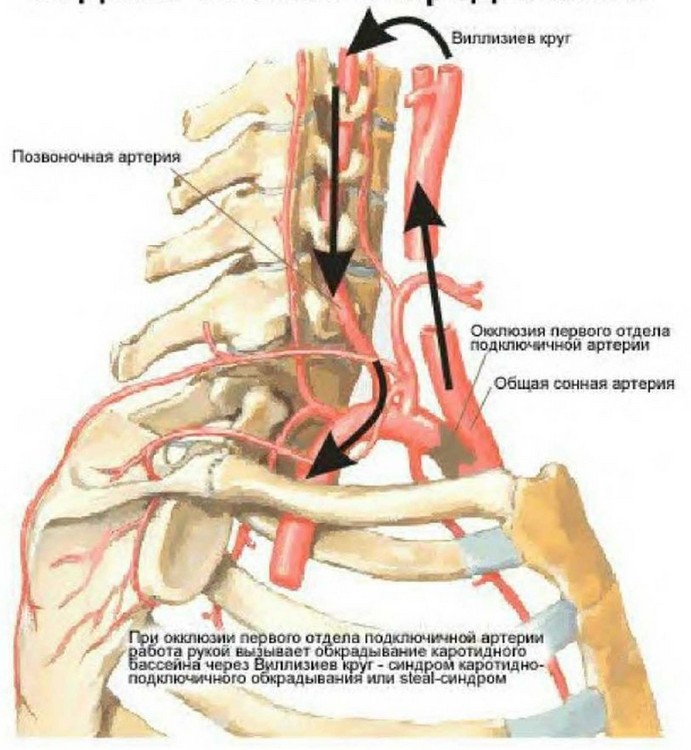
Несмотря на то, что по данным литературы наиболее частая причина поражения позвоночной артерии это атросклероз, в последние годы все чаще диагностируется синдром позвоночной артерии у лиц, не достигших периода атеросклеротических изменений в сосудах.
Увеличилась частота обнаружения особенностей анатомического строения, аномалии хода, патологических изгибов или врожденной узости просвета сосуда, так называемой гипоплазии.
Важной, и не всегда устранимой причиной может стать компрессия сосуда извне. Чаще всего это связано с остеохондрозом шейного отдела позвоночника, травмами, аномалиями строения позвонков , сколиозом.
В случае сочетания нескольких факторов, риск развития синдрома позвоночной артерии выше.
Все основные симптомы связаны с недостатком кровоснабжения соответствующих областей нервной системы . Характерно, что симптомы зависят от движений головы и как правило усиливаются при длительном вынужденном положении головы или резких поворотах и наклонах.
 Частой жалобой является головная боль ноющего или пульсирующего характера в области затылка и висков . Очень характерной жалобой является головокружение. Оно описывается пациентами по разному, от легкой неустойчивости при ходьбе, до ощущения вращения тела, сопровождается потемнением в глазах и шумом в ушах. Шум в ушах ( тиннитус) может быть и самостоятельным симптомом, независимым от наличия головокружения.
Частой жалобой является головная боль ноющего или пульсирующего характера в области затылка и висков . Очень характерной жалобой является головокружение. Оно описывается пациентами по разному, от легкой неустойчивости при ходьбе, до ощущения вращения тела, сопровождается потемнением в глазах и шумом в ушах. Шум в ушах ( тиннитус) может быть и самостоятельным симптомом, независимым от наличия головокружения.
Нарушение кровоснабжения в бассейне позвоночных артерий сопровождается и вегетативныеми проявлениями – чувство жара, потливость, гипергидроз ладоней ( влажные руки) который часто сопровождается жалобой на холодные ладони.
Диагностика данного синдрома на сегодняшний день не представляет больших технических трудностей. Ультразвуковое дуплексное сканирование позволяет не только увидеть ход сосуда, вовремя диагностировать аномалии строения, но и оценить скорость кровотока внутри просвета сосуда, наличие холестериновых бляшек и степень их стабильности, а соответственно оценить риск инсульта. По результатам ультразвукового исследования можно предположить наличие компрессии на сосуды извне, например при остеохондрозе, и вовремя провести дополнительные исследования- ренгенографию или МРТ , КТ шейного отдела позвоночника.
К лечению данного синдрома нужно подходить комплексно. Первое это устранить причины на которые мы можем повлиять- лечение остеохондроза , коррекция осанки.

В заключении хочется напомнить, что одна из причин нарушения кровотока в позвоночных артериях это патология шейного отдела позвоночника. В современном мире мы почти все проводим большое количество времени за компьютерами, нагружая шейный отдел. Делайте паузы, занимайтесь физкультурой, проявляйте заботу о себе!
С уважением, Сарычева Татьяна
«Болезнь легче предупредить, чем лечить». Не я это сказал, но делаю это ежедневно.
Активная профилактика мозгового ишемического инсульта – это лечение спондилогенной вертебрально-базилярной недостаточности .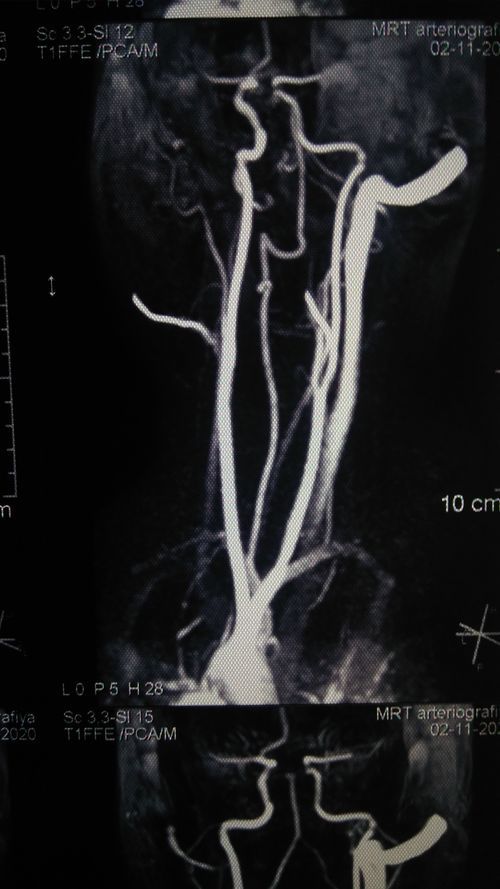
Сухие цифры медицинской статистики сообщают, что 450 тысяч человек в России ежегодно переносят инсульт. В одной только Москве с этим диагнозом госпитализируются до 2 тысяч больных в месяц, число это ежегодно растет. Рост этот тем тревожнее, чем больший процент людей трудоспособного возраста поражает этот тяжелый недуг. Нужно учесть, что на 100 тысяч населения умирает 175 человек, 31% выживших нуждаются в постороннем уходе, 20% может ходить, и только около 20% возвращаются к труду и привычной жизни. 80% не вернувшихся к труду ложатся тяжелым бременем на семьи, становясь не статистическим показателем, а конкретным несчастьем.
Что же можно сделать, чтобы противостоять этому злу? Об этом беседа корреспондента журнала с руководителем Центра мануальной терапии г. Москвы, д.м.н., профессором кафедры неврологии и нейрохирургии РГМУ Анатолием Сителем.
— Известно, что остеохондрозом позвоночника страдают практически все люди старше 25-30 лет, иными словами можно констатировать, что практически все пациенты, перенесшие инсульт одновременно страдают и остеохондрозом. Я знаю, что Вы занимаетесь, в основном, заболеваниями позвоночника, а есть ли какая-то прямая связь между патологией позвоночного столба и инсультом?
Я знаю, что Вы занимаетесь, в основном, заболеваниями позвоночника, а есть ли какая-то прямая связь между патологией позвоночного столба и инсультом?
— Конечно, такая связь есть, и очень тесная. Особенностью шейного отдела позвоночника является его наибольшая подвижность, по сравнению с грудным и поясничным отделами. Эта кажущаяся подвижность обусловлена действительно высокой подвижностью головы, особенно в области головных суставов ( соединениях черепа с атлантом и атланта с аксизом), на долю которых приходится до 50-55% всего объема движений головы, и только 20-45% обеспечивается движениями в средне- и нижнешейном отделах позвоночника. При этом в шее, из-за унковертебральных сочленений, резко ограничены наклоны в стороны и ротация по вертикальной оси. Наибольший объем движений обеспечивается в шейном отделе позвоночника при движении головы в сагиттальной плоскости – это сгибание вперед и разгибание назад. В поперечных отростках шейных позвонков, попарно расположенных по бокам от тел позвонков, как нитка через бусины, проходят позвоночные артерии (аа.
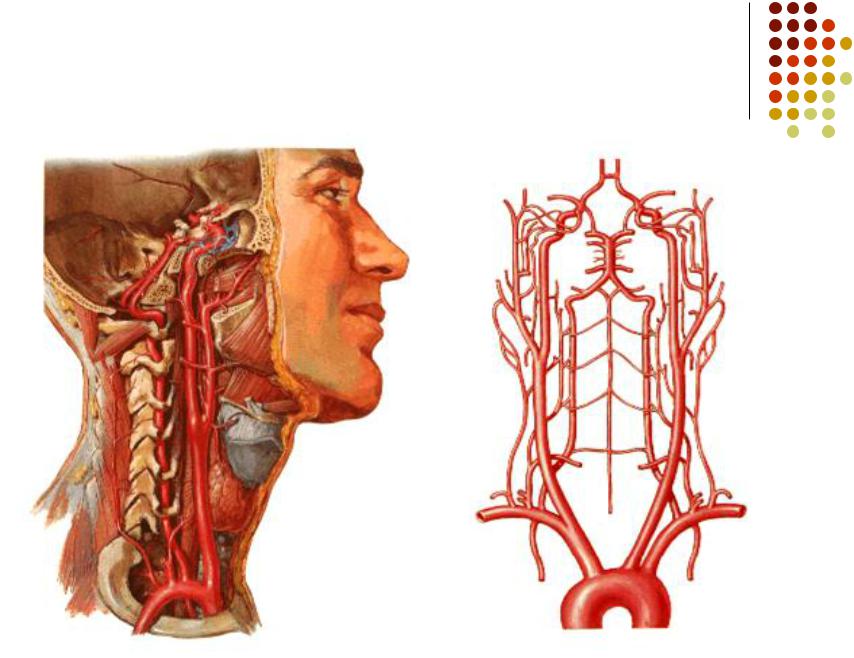
передних рогов шейного отдела спинного мозга. Поднимаясь выше на 2-2,5 см, позвоночные артерии отдают задние нижние мозжечковые артерии, затем соединяются в основную артерию (а. basilaris), которая далее, делясь на разнокалиберные ветви и веточки, обеспечивает кровообращение в стволе головного мозга и мозжечке, а две ее самые крупные конечные ветви или задние мозговые артерии кровоснабжают затылочные доли мозга и часть височных долей. Вся эта артериальная система называется вертебрально-базилярной системой, а стволовые отделы мозга, которые она кровоснабжает – вертебрально-базилярным бассейном. Качество кровоснабжения в вертебрально-базилярном бассейне целиком и полностью зависит от кровотока в экстрацеребральных или внечерепных отделах позвоночных артерий, т.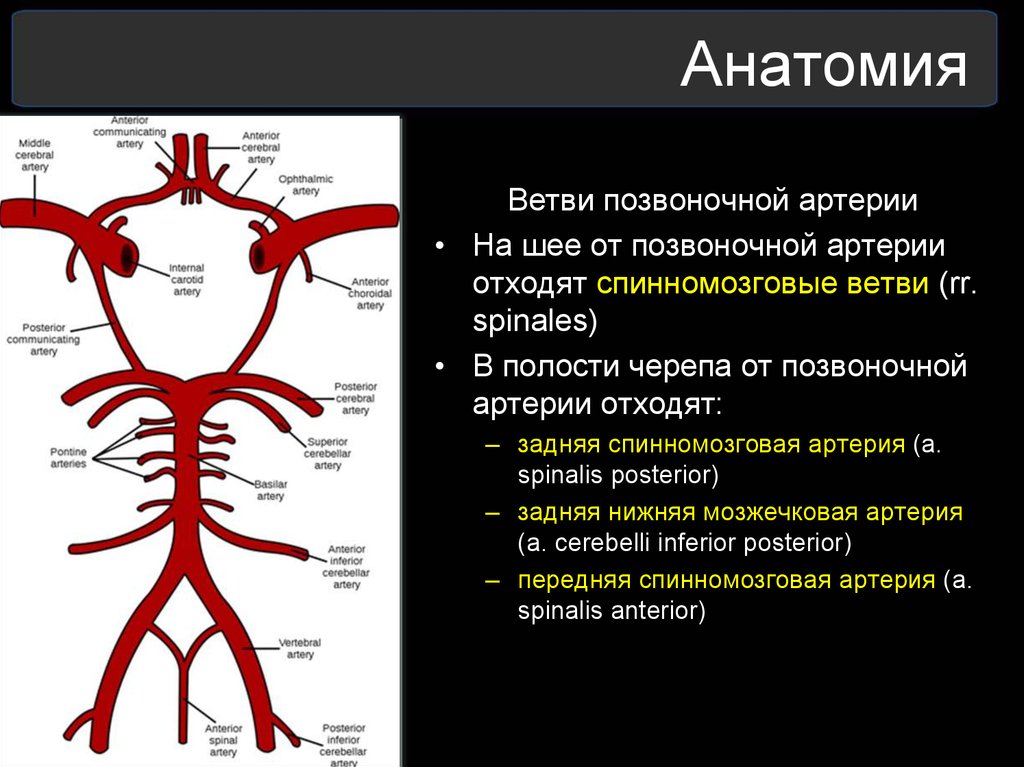
— Но ведь окруженные костными кольцами, в отличии, например, от сонных артерий, которые практически лежат под кожей и ничем не защищены, позвоночные артерии в своем канале должны себя чувствовать абсолютно защищенными? Или это не так?
— Эта защищенность тоже кажущаяся. Дело в том, что в норме артерия висит точно в центре отверстия поперечного отростка при помощи тонких соединительнотканных тяжей, и при любом движении в шейных суставах в пределах физиологической подвижности позвоночная артерия не страдает, иными словами, движения головы и шеи в норме не оказывают воздействия на функцию позвоночной артерии. Другое дело, в условиях развития функциональных блокад позвоночных двигательных сегментов. Анатомической единицей позвоночника является позвонок, а функциональной – позвоночный двигательный сегмент (ПДС): два позвонка и диск между ними, кроме того, каждый позвонок имеет еще много суставных соединений с выше и нижележащими позвонками.
При развитии функциональных блокад подвижность в блокированных сегментах резко снижается, а в других компенсаторно повышается, образуются подвывихи позвонков и уже в этих условиях, как правило, развивается гипоциркуляция по одной из позвоночных артерий и компенсаторная гиперемия — усиление кровотока по противоположной артерии. Этот функциональный «перекос» может долго обеспечивать компенсацию кровообращения в вертебрально-базилярной системе, но при этом компенсаторные возможности системы в целом резко уменьшаются, что приводит к развитию субкомпенсации. Дальнейшее влияние
патологических факторов, увеличение количества функциональных блокад, или увеличение нагрузки на вертебрально-базилярную систему, приводит к декомпенсации или проявлениям вертебрально-базилярной недостаточности, а затем может развиться ишемический инсульт в вертебрально-базилярном бассейне. По механизму мозгового обкрадывания, когда дефицит кровообращения в вертебрально-базилярной системе ведет к перетоку части крови из каротидного бассейна по анастомозам Вилизиевого круга на основание мозга и обеднению (обкрадыванию) кровотока в бассейне внутренних сонных артерий, может развиваться дисциркуляция уже в ветвях сонных артерий и ишемический инсульт в бассейне сонных артерий..
По механизму мозгового обкрадывания, когда дефицит кровообращения в вертебрально-базилярной системе ведет к перетоку части крови из каротидного бассейна по анастомозам Вилизиевого круга на основание мозга и обеднению (обкрадыванию) кровотока в бассейне внутренних сонных артерий, может развиваться дисциркуляция уже в ветвях сонных артерий и ишемический инсульт в бассейне сонных артерий..
— А как же определить, нужно человеку лечиться или нет, и каков риск развития инсульта из-за остеохондроза в шейном отделе позвоночника, и можно ли действительно активно и эффективно противостоять этой сосудистой катастрофе?
— Это как раз и есть самое трудное и самое важное в нашей работе. Дело в том, что длительное существование гипоциркуляции, недостаточного кровотока создает условия для развития остеофитов, костных выростов, которые сначала мягкие, хрящевидные, позже, если им ничто не мешает, они пропитываются кальцием и становятся угрозой для сосудистых и нервных образований в канале позвоночной артерии, особенно, если растут внутрь костного кольца или кзади, в направлении позвоночной артерии и сопровождающих ее вен и нервов.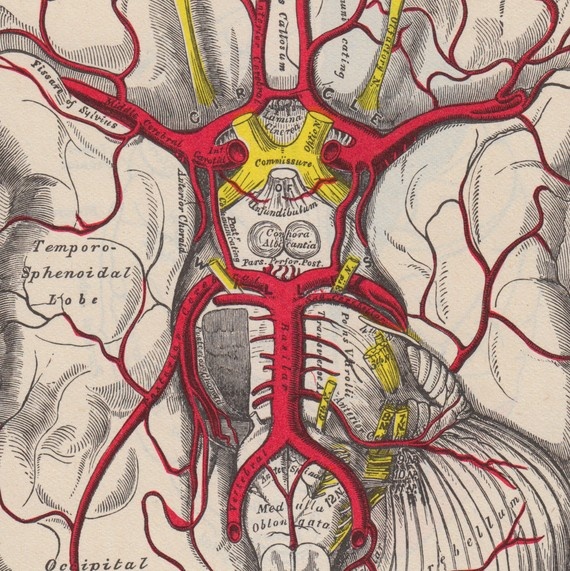 Но, если артерия функционирует достаточно, хорошо пульсирует, то такой остеофит развиться не может.
Но, если артерия функционирует достаточно, хорошо пульсирует, то такой остеофит развиться не может.
Отсюда вывод: необходимо постоянное поддержание нормального функционирования позвоночных артерий и профилактика развития остеофитов, приводящих к необратимой гипоциркуляции по позвоночной артерии и в вертебрально-базилярной системе в целом.
Теперь о диагностике. Для того, чтобы диагностировать и разработать план действий, мы должны как можно лучше знать, изучить противника, которому приходиться противостоять. Диагностические критерии вертебрально-базилярной недостаточности сформулированы давно и до недавнего времени казалось, что и причины ее и патогенез хорошо изучены. Но, часто, к сожалению, и клиницисты, и специалисты по функциональной и ультразвуковой диагностике, и научные работники путают причину и следствие. ВОЗ определяет вертебрально-базилярную недостаточность (ВБН) как «обратимое нарушение функций мозга, вызванное уменьшением кровоснабжения области, питаемой позвоночными и основной артериями» (ВОЗ, 1970). По Международной классификации болезней (МКБ-10) ВБН классифицирована под названием «Синдром вертебрально-базилярной артериальной системы» (рубрика G45), класса V, («Сосудистые заболевания нервной системы»). По Российской классификации ВБН – это преходящие нарушения мозгового кровообращения (ПНМК), в
По Международной классификации болезней (МКБ-10) ВБН классифицирована под названием «Синдром вертебрально-базилярной артериальной системы» (рубрика G45), класса V, («Сосудистые заболевания нервной системы»). По Российской классификации ВБН – это преходящие нарушения мозгового кровообращения (ПНМК), в
частности, транзиторные ишемические атаки (ТИА) и дисциркуляторная энцефалопатия с преимущественным проявлением в вертебрально-базилярном бассейне. Все вышеприведенные определения неудачны, так как если следовать им, то ВБН появляется тогда, когда имеют место клинические проявления болезни.
На самом деле, вертебрально-базилярная недостаточность – это несоответствие между возможностью мозга потреблять, и возможностью вертебрально — базилярной системы обеспечить необходимый объем кровотока. И если при любой нагрузке на вертебрально — базилярную систему она обеспечивает кровообращение, то вертебрально – базилярной недостаточности нет. Если же при определенных условиях, например, поворот или запрокидывание головы, перемена положения тела, длительная работа за компьютером, возникает мозговая дисфункция в вертебрально – базилярном бассейне, то недостаточность имеет место и необходимо определить ее генез, уровень компенсации и стадию.
Если же при определенных условиях, например, поворот или запрокидывание головы, перемена положения тела, длительная работа за компьютером, возникает мозговая дисфункция в вертебрально – базилярном бассейне, то недостаточность имеет место и необходимо определить ее генез, уровень компенсации и стадию.
— Но, наверное, это очень сложно, нужна специальная аппаратура и оборудование, особо подготовленные специалисты? Можно ли это осуществить в условиях районной поликлиники?
— Оборудование, которым мы пользуемся, производится в России, оно доступно, специалистов готовят и у нас и на многих других кафедрах, необходимо желание и знания в пределах институтской программы, а главное четкое и полное обследование и умелое лечение пациентов. Главное, чтобы врачи не увлекались красочностью сложных методик исследования, а полностью использовали бы на благо больного все данные, которые дают доступные методики и постоянно отслеживали клиническую динамику.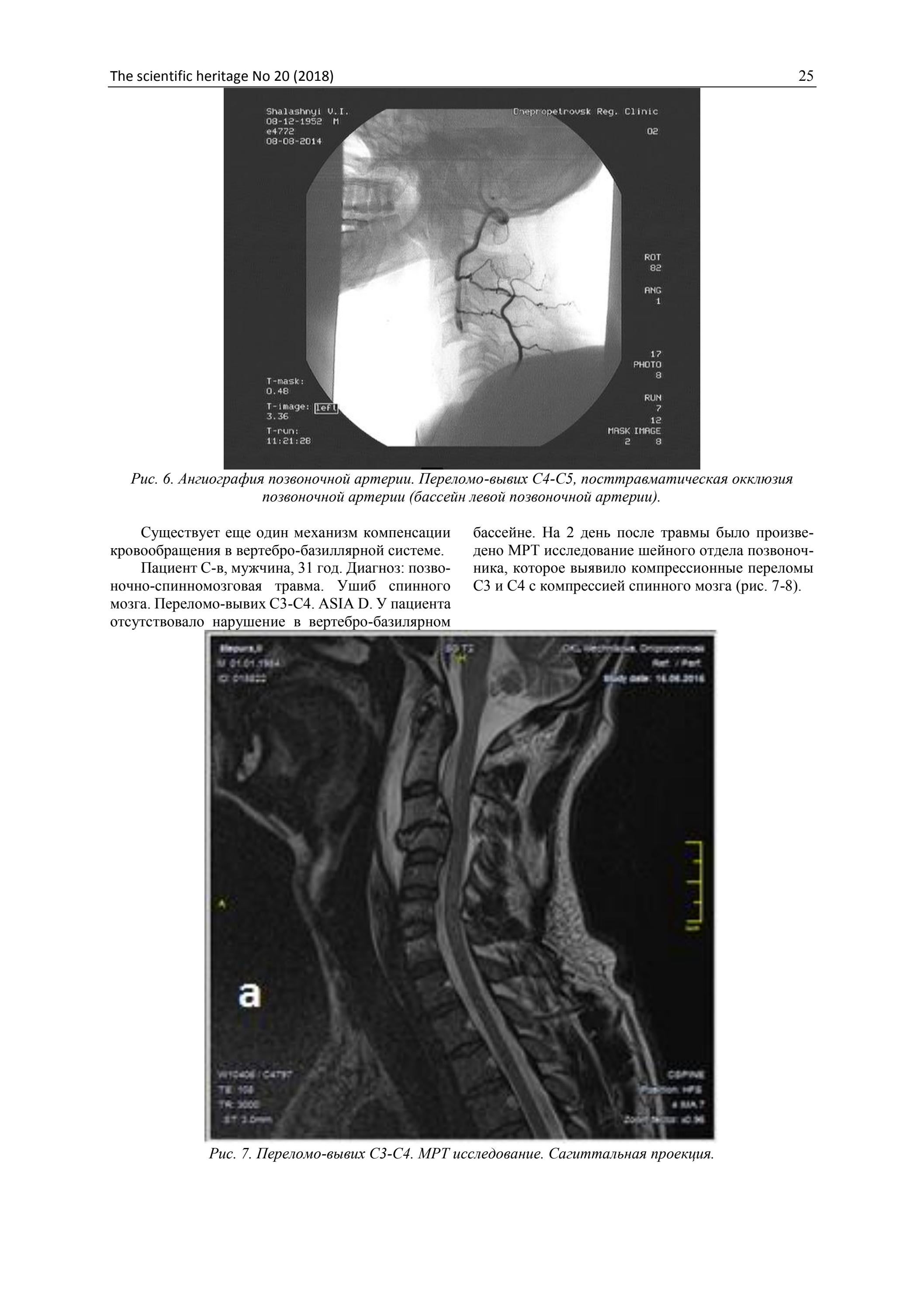
На большом количестве клинического материала и данных инструментальных исследований нам удалось выяснить причинно-следственные связи патогенеза сподилогенной
вертебрально – базилярной недостаточности. Связь дефицита и асимметрии кровотока по позвоночным артериям наиболее тесная не столько с проявлениями остеохондроза, определяемыми рентгенографически или методами нейровизуализации (КТ, МРТ), эта связь наиболее выражена с наличием функциональных блокад и мозаикой их распределения в позвоночнике.
То, что функциональные блокады ПДС — это первопричина развития сподилогенной вертебрально – базилярной недостаточности, подтверждается тем, что вертебрально – базилярная недостаточность может быть выявлена и у очень молодых людей и даже у детей, у которых нет никаких признаков остеохондроза и дегенеративных заболеваний, а имеются только статико-динамические нарушения в виде неправильной осанки и изменения физиологических изгибов позвоночника. За счет этих молодых людей можно объяснить
За счет этих молодых людей можно объяснить
отмечаемое в последние годы, по литературным данным, «помоложение» инсульта, т. е. возникновение его в более раннем возрасте.
Нами определены 4 стадии вертебрально – базилярной недостаточности, критериями оценки которых являются данные клиники (жалобы, анамнез, неврологический статус), данные мануальной диагностики (наличие и мозаика распределения функциональных блокад в позвоночных двигательных сегментах), результаты рентгенспондилографии, обязательно включающие функциональное рентгенологическое исследование (наклоны шейного отдела позвоночника кпереди и кзади, ультразвуковой допплерографии брахиоцефальных артерий и вен (УЗДГ, БЦА и В) и динамики большинства показателей, выявляемых после первого сеанса мануальной терапии.
Первая стадия.
Ангиогиодистоническая стадия, характеризуется преобладанием субъективной симптоматики над объективно выявляемыми изменениями со стороны неврологического статуса, имеется фон вегетативной дисфункции, легкие кратковременные головокружения, периоды нечеткости зрения.
Функциональные блокады выявляются в краниоцервикальном сочленении, области шейно-грудного перехода, и пояснице, являющейся сопряженном сегментом для шейного отдела позвоночника, так как имеет с ним соименную кривизну – лордоз. Также для этой стадии характерен синдром нижней косой мыщцы головы, рефлекторная контрактура мышц шеи, синдром передней грудной стенки, межлопаточный болевой синдром.
Рентгенография выявляет несимметричное стояние зуба аксиса, выпрямление шейного лордоза, гипокинезию в нижнем шейном отделе при наклоне головы кпереди и кзади, признаки остеохондроза в двух-трех двигательных сегментах.
Допплерография отмечает разницу по форме огибающих спектров линейной скорости кровотока (ЛСК) по позвоночным артериям, признаки артериальной ангиодистонии, различия показателей ЛСК по абсолютным значениям (средняя скорость) не превышает 15%. Ротация головы меняет характеристики кровотока на 0-15%.
Исследования, проводимые после первого сеанса мануальной терапии, выявляют значительное увеличение объема движений и регресс гипертонуса мышц шеи, увеличение кровотока по позвоночным артериям, прирост ЛСК по обеим ПА составляет от 25 до 50%. Асимметрия выстояния зуба аксиса регрессирует.
Вторая стадия. Сосудисто – ишемическая. Вторая стадия характеризуется более интенсивными и более длительными приступами головокружений, приступами головных болей, часто в половине головы, начинающиеся, как правило, болью в шее или заушной области, отмечаются периоды нарушения слуха в виде его снижения, шумов, гула в ухе,
нарушения равновесия, зрительные расстройства в виде мушек, тумана перед глазами, болями в области сердца, не связанных с нагрузкой, экстрасистолией.
Функциональные блокады, в отличии от первой стадии, выявляются и в среднем и верхнем шейных отделах. Функциональные ограничения подвижности при ротации головы в стороны выражены, сама ротация болезненна.
Функциональные ограничения подвижности при ротации головы в стороны выражены, сама ротация болезненна.
Рентгенография выявляет уже не сглаженность, а выпрямление шейного лордоза, признаки остеохондроза выявляются во всех двигательных сегментах, стойкие функциональные блокады выявляются в нижнем шейном отделе.
Допплерография показывает асимметрию ЛСК по позвоночным артериям, превышающую 30%, при ротации кровоток снижается на 30-50% от исходных значений.
Исследования, проводимые после первого сеанса мануальной терапии выявляют значительное увеличение объема движений, увеличение кровотока по позвоночным артериям, с сохранением ассиметрии в пределах 15% (допустимые значения), прирост ЛСК по обеим ПА составляет от 50%. Рентгенологическая картина мало меняется.
Третья стадия. Ишемическая, характеризуется клинически более выраженной картиной, тяжелыми приступами головной боли, когда анальгетики и нестероидные противовоспалительные препараты не приносят облегчения, головокружения с тошнотой и рвотой, приступы drop — attak.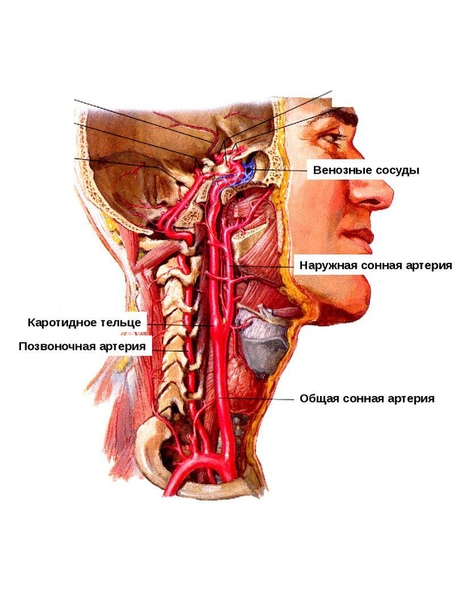 Приступы провоцируются запрокидыванием головы кзади и резким поворотом в сторону, при перемещении пациента на эскалаторе или в транспорте.
Приступы провоцируются запрокидыванием головы кзади и резким поворотом в сторону, при перемещении пациента на эскалаторе или в транспорте.
Функциональные блокады выявляются во всех сегментах шейного отдела позвоночника и поясничном отделе.
Рентгенография отмечает признаки остеохондроза шейного отдела позвоночника во всех двигательных сегментах, часто кифотизацию в одном или нескольких сегментах шейного отдела позвоночника, признаки протрузий межпозвонковых дисков.Функциональные рентгенограммы выявляют не более одного- двух мобильных двигательных сегментов в среднешейном отделе позвоночника и стойкие функциональные блокады выше и ниже их.
Допплерография показывает разницу кровотока по сторонам до 100% (сигнал от одной позвоночной артерии не получен, или абортивный, фрагментарный), ротация головы в стороны выявляет асимметрию до 100% (ротационная компрессия одной из позвоночных артерий). Всегда имеются признаки венозной дисциркуляции.
Всегда имеются признаки венозной дисциркуляции.
После первого сеанса мануальной терапии наблюдается увеличение объема движений в шейных позвоночных двигательных сегментах, регресс нарушений зрения, что субъективно отмечается как улучшение четкости зрения, уменьшение головной боли и головокружения. Допплерография выявляет рост ЛСК по позвоночным артериям и регресс признаков венозной дисциркуляции.
Четвертая стадия клинически совпадает с дисциркуляторной энцефалопатией III стадии по Российской классификации. У больного имеются признаки перенесенных инсультов в полушариях и стволе головного мозга, стойкий неврологический дефицит, рентгенологическая картина представлена деформирующим спондилезом, признаки болезни Форестье, остеопорозом III ст. Допплерография выявляет атеросклеротическое стенозирование, выраженную асимметрию по сторонам, при этом динамические нарушения мало выявлены из-за резкого ограничения подвижности в шейных позвоночных двигательных сегментах. IV стадия является противопоказанием для проведения мануальной терапии, так как высока угроза осложнений.
IV стадия является противопоказанием для проведения мануальной терапии, так как высока угроза осложнений.
Определение стадии ВБН имеет не столько академический интерес, сколько практическое значение. Если нам в процессе лечения удается добиться перехода III стадии во II, то можно говорить об успешном лечении и прогнозировать положительный эффект от дальнейшего применения мануальной терапии.
Вертебрально-базилярная недостаточность — это состояние хроническое. Регулярное лечение ее, так как это состояние хроническое, позволяет не только улучшить качество жизни, но и проводить профилактику сосудистых катастроф- мозговых ишемических инсультов в бассейнах вертебрально-базилярных и сонных артерий.
Пресс – служба ГКУ ДЗ ЗАО.
Головокружение, обусловленное патологией шейного отдела позвоночника | #07/09
Головокружение и отоневрологические симптомы описаны при различных видах патологии в области шеи: травматических повреждениях шеи и спинного мозга [4, 5, 10], шейном остеохондрозе [2], окклюзии позвоночной артерии (ПА) [1, 3, 12] и инсультах, обусловленных повреждениями ПА [1, 11, 13, 15], диссекции ПА, в связи с движением шеи или манипуляцией на шейном отделе позвоночника [6, 7, 8, 9, 11, 14].
Выделение вертеброгенного головокружения обусловлено распространенностью патологии среди лиц молодого возраста, тяжестью течения заболевания, разнообразием симптоматики, возникновением инсультов при манипуляциях на шее.
Отличительной особенностью вертеброгенного головокружения является острое начало, связанное с определенной позицией головы (наклон вперед, запрокидывание назад, резкий поворот в сторону и др.), часто утром, после сна. Головокружение, которое возникает в результате изменения позиции головы, может быть обусловлено как раздражением внутреннего уха, так и центральных вестибулярных структур головного мозга (ствола, мозжечка). Компрессия артерий развивается при остеофитах и боковых грыжах дисков в унковертебральных областях, передних экзостозах суставных отростков, а также при подвывихе.
К анатомо-топографическим особенностям ПА относится расположение большей части ее экстракраниального отдела в канале позвоночника, где происходит ее смещение и сдавление остеофитами или суставными отростками при различных дегенеративных заболеваниях, в частности при остеохондрозе (рис.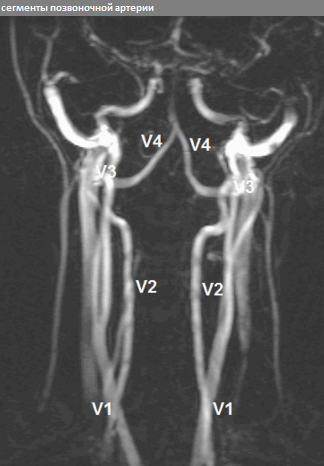 1).
1).
Отоневрологическое обследование пациента позволяет провести точную топическую диагностику, а также дифференциальную диагностику от периферического головокружения, обусловленного другими заболеваниями: болезнью Меньера, доброкачественным пароксизмальным позиционным головокружением, вестибулярным нейронитом.
Барре (1926), впервые обративший внимание на связь отоневрологических симптомов с патологией в области шеи, описал их под названием «задний шейный симпатический синдром», указывая при этом на значение связи головы и шеи при помощи симпатической нервной системы.
Показано, что углубленное исследование ПА с учетом не только диаметра и особенностей кровотока, но и с применением функциональных проб позволяет выявить моменты, важные для дифференциальной диагностики между гемодинамически значимой и незначимой экстравазальной компрессией ПА.
Повреждающее действие экстравазальных факторов компрессии направлено, прежде всего, на ее нервное сплетение.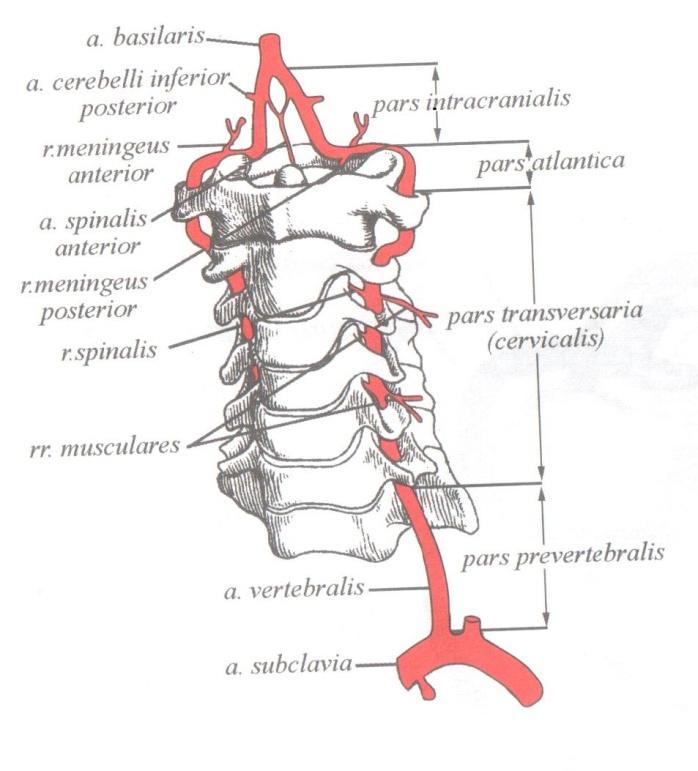 Раздражение позвоночного нерва, повышая тонус ПА, может уменьшить скорость объемного кровотока в ней на 30% от исходной величины, на 40% в ветвях основной артерии, в частности внутреннего уха [1].
Раздражение позвоночного нерва, повышая тонус ПА, может уменьшить скорость объемного кровотока в ней на 30% от исходной величины, на 40% в ветвях основной артерии, в частности внутреннего уха [1].
Таким образом, функциональное состояние позвоночного нерва и структурные изменения ПА являются основой для развития недостаточности кровотока в вертебрально-базилярной системе (ВБС) на экстра- и интракраниальном уровне. Как подчеркивают различные авторы, кохлеовестибулярный синдром может развиваться при недостаточности кровообращения в ВБС как в области внутреннего уха, так и в области вестибулярных ядер и проводящих путей ствола головного мозга, мозжечка.
Кроме нарушений кровоснабжения ВБС, в патогенезе вертеброгенного головокружения также играет роль нарушенная проприоцептивная нервная импульсация со стороны структур шеи. Движения в измененных остеохондрозом и спондилоартрозом суставах шейных позвонков, дисках, а также возникающее тоническое напряжение мышц способствуют развитию неадекватной афферентной импульсации и неправильной оценке вестибулярной системой информации о позиции головы, что вызывает ощущение головокружения и нарушения равновесия.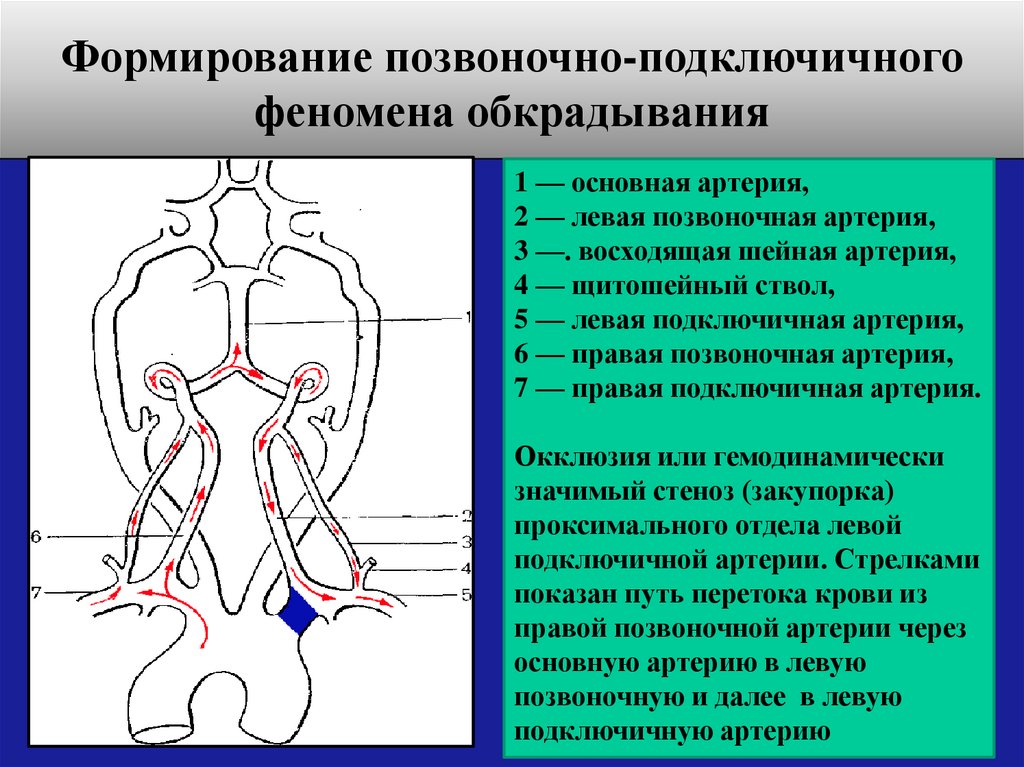
Целью проведенной на базе НЦ неврологии РАМН работы было выявление клинических особенностей и отоневрологической симптоматики у больных с вертеброгенным головокружением на фоне патологических изменений в шейном отделе позвоночника, а также сопоставление вестибулярных нарушений со структурными изменениями ПА, уровнем артериального давления, состоянием внутренних яремных вен.
Нами проведено обследование 115 больных с острой и хронической недостаточностью кровообращения в ВБС, в том числе 47 пациентов с наличием дегенеративно-дистрофических изменений в шейном отделе позвоночника, из них у 33 — дегенеративные изменения (остеохондроз), у 9 — краниовертебральная патология, аномалия Киммерли, у 4 больных аномалия вхождения ПА в канал на уровне С4, стеноз позвоночного канала — у одной больной. Возраст больных колебался от 28 до 74 лет.
Основными заболеваниями, на фоне которых развивались вестибулярные нарушения, были артериальная гипертония (АГ) в сочетании с атеросклерозом, вегетативно-сосудистая дистония, остеохондроз.
Всем больным проведено полное классическое отоневрологическое обследование, включающее исследование спонтанных и экспериментальных вестибулярных реакций (вращательная и калорическая пробы) и слуха. Исследование слухового анализатора проводилось с использованием аудиометрии и слуховых вызванных потенциалов.
Структурные изменения магистральных артерий головы (МАГ) и гемодинамические показатели кровотока по ПА и внутренней сонной артерии (ВСА) изучали с помощью ультразвукового дуплексного сканирования МАГ (ДС МАГ) с функциональными пробами, в ряде случаев при проведении спиральной компьютерной томографии (СКТ), магнитно-резонансой ангиографии.
Нарушения мозгового кровообращения у пациентов с патологией шейного отдела позвоночника
на правах рукописи
НЕДАЛЬ ХУССЕЙН
НАРУШЕНИЯ МОЗГОВОГО КРОВООБРАЩЕНИЯ У ПАЦИЕНТОВ С ПАТОЛОГИЕЙ ШЕЙНОГО ОТДЕЛА ПОЗВОНОЧНИКА
14. «ЯШ £г. в час. на заседании
«ЯШ £г. в час. на заседании
диссертационного совета Д 208.049.01 при Московском областном научно-исследовательском клиническом институте имени М.Ф.Владимирского по адресу: 129110, Москва, ул. Щепкина 61/2, 15 корп., конференцзал.
С диссертацией можно ознакомиться в научно-медицинской библиотеке Московского областного научно-исследовательского клинического института имени М.Ф.Владимирского.
Авторефератразослан 2005 г.
Ученый секретарь диссертационного совета,
д.м.н., профессор П.В.Астахов.
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ Актуальность исследования.
Сосудистые заболевания головного мозга составляют до 50% всех сердечнососудистых заболеваний человека. При патологии шейного отдела позвоночника, по данным В.Н. Верещагина (1980), в 70 % случаев происходят нарушения мозгового кровообращения в вертебробазилярной системе, что, по данным Fisher СМ., 1975, Cartlidge, 1977, нередко приводит к развитию инфарктов в стволовых отделах головного мозга и вызывает инвалидизацию больных, а нередко заканчивается высокой летальностью.
Патология шейного отдела позвоночника и спинного мозга проявляется большим числом заболеваний: шейным остеохондрозом, нестабильностью тел позвонков, грыжами межпозвонковых дисков, шейной миелопатией, травмами шейного отдела позвоночника и их последствиями. При этом, как правило, проявляется заинтересованность магистральчых артериальных стволов и внутренней яремной вены в области шеи; нарушения мозгового кровообращения при этом формируются в виде очагов ишемии; нарушения кровоснабжения мозговой ткани ишемического генеза могут проявляться в бассейне позвоночной артерии, а также внутренней сонной артерии (передней, средней или задней мозговых артерий). При этом также проявляется венозная дисциркуляция (В.Н. Верещагин, 1999).
В этой связи практически важным и перспективным является всестороннее изучение закономерностей сосудистых нарушений в вертебробазилярном бассейне при патологии позвоночной артерии. В возникновении регионарных нарушений мозгового кровообращения в вертебробазилярном бассейне (ВББ) помимо аномалий развития магистральных артерий головы особую роль играет патология позвоночника. Сложные взаимоотношения позвоночных артерий с костями, связками и мышцами шейного отдела, высокая чувствительность стволовых структур головного мозга, снабжаемых кровью основной артерии, образующейся при слиянии двух позвоночных артерий, определяют полиэтиологичность вертебробазилярной недостаточности (Иванов Л.А., 1982; Бассиль Т.Э., 1989; Метелкина Л.П., 2000).
Сложные взаимоотношения позвоночных артерий с костями, связками и мышцами шейного отдела, высокая чувствительность стволовых структур головного мозга, снабжаемых кровью основной артерии, образующейся при слиянии двух позвоночных артерий, определяют полиэтиологичность вертебробазилярной недостаточности (Иванов Л.А., 1982; Бассиль Т.Э., 1989; Метелкина Л.П., 2000).
Известно, что в патогенезе недостаточности мозгового кровообращения в вертебрально-базилярном сосудистом бассейне важную роль играет остеохондроз шейного отдела позвоночника и патология кранио-цервикального перехода (П. Дуус, 1997; YJ. Leu, 1980; A.V. Wu, 1980). Одним из возможных механизмов развития недостаточности кровообращения служат экстравазальная компрессия позвоночных
артерий и раздражение шейных симпатических узлов, приводящие к ирритации вазопрессорных мезодиэнцефальных структур (Рамешвили Т.Е. и др., 2001).
Патоморфологические и нейровизуализационные находки у больных с синдромом поражения вертебрально-базилярного бассейна весьма разнообразны. Так, в Oxford Community Stroke Project (OCSP) наблюдались 109 пациентов с синдромом поражения вертебрально-базилярного бассейна. Из 90 пациентов, которым в течение 28 дней с момента начала инсульта была выполнена компьютерная томография (КТ) или проведена аутопсия, у девяти (10%) имелось кровоизлияние в мозг. В другом исследовании у 7 из 39 (18%) пациентов с клиникой вертебрально-базилярной недостаточности наблюдалось паренхиматозное внутримозговое кровоизлияние. При обследовании 81 пациента лишь у 19 был выявлен инфаркт в зоне кровоснабжения вертебрально-базилярного бассейна, у 60 не было обнаружено очагов, и у двух был выявлен инфаркт в бассейнах других мозговых артерий (окклюзия ветви средней мозговой артерии и множественные небольшие глубинные инфаркты).
Так, в Oxford Community Stroke Project (OCSP) наблюдались 109 пациентов с синдромом поражения вертебрально-базилярного бассейна. Из 90 пациентов, которым в течение 28 дней с момента начала инсульта была выполнена компьютерная томография (КТ) или проведена аутопсия, у девяти (10%) имелось кровоизлияние в мозг. В другом исследовании у 7 из 39 (18%) пациентов с клиникой вертебрально-базилярной недостаточности наблюдалось паренхиматозное внутримозговое кровоизлияние. При обследовании 81 пациента лишь у 19 был выявлен инфаркт в зоне кровоснабжения вертебрально-базилярного бассейна, у 60 не было обнаружено очагов, и у двух был выявлен инфаркт в бассейнах других мозговых артерий (окклюзия ветви средней мозговой артерии и множественные небольшие глубинные инфаркты).
В более позднем исследовании сообщалось, что в 61% случаев у пациентов с вертебробазилярной недостаточностью при КТ были выявлены инфаркты мозжечка, ствола мозга или инфаркты в бассейне задней мозговой артерии, а у остальных пациентов очагов выявлено не было. (Lazorthes D.F. et al., 2000).
(Lazorthes D.F. et al., 2000).
Приведенные данные свидетельствуют о сложной взаимосвязи развития нарушений мозгового кровообращения с патологией шейного отдела позвоночника. Нарушения кровоснабжения мозговой ткани ишемического генеза могут проявляться в бассейне позвоночной артерии, а также внутренней сонной артерии (передней, средней или задней мозговых артерий). При этом также будет проявляться и венозная дисциркуляция.
В настоящее время может быть применен комплекс клинического обследования больных с нарушениями мозгового кровообращения, который дает возможность осуществить всестороннюю характеристику причин, механизмов развития и особенностей проявления церебральной ишемии. Исследовательский алгоритм включает в себя: клинико-неврологическое обследование; параклиническое — отоневрологическое и нейроофтальмологическое обследование; инструментальное исследование показателей церебральной гемодинамики при помощи ультразвуковой допплерографии с дуплексным сканированием артерий мозга; определение состояния ткани мозга при его острой либо хронической ишемии с помощью компьютерной и магнитно-резонансной томографии; и в завершение —
рентгенконтрастную ангиографию головного мозга, которая предоставляет объективную количественную характеристику сосудистого поражения и особенностей перестройки мозгового кровотока. Особое значение в настоящее время имеют радионуклидные методы исследования кровообращения головного мозга -радиоизотопная ангиография и однофотонная эмиссионная компьютерная томография. В работе И.Ю. Швера с соавторами (1997) отмечена роль ОФЭКТ при стенозирующих процессах каротидных артерий. Коваль И.В. и другие (2000) показали важность радионуклидной диагностики при сосудистой патологии экстра-и интракраниального расположения.
Особое значение в настоящее время имеют радионуклидные методы исследования кровообращения головного мозга -радиоизотопная ангиография и однофотонная эмиссионная компьютерная томография. В работе И.Ю. Швера с соавторами (1997) отмечена роль ОФЭКТ при стенозирующих процессах каротидных артерий. Коваль И.В. и другие (2000) показали важность радионуклидной диагностики при сосудистой патологии экстра-и интракраниального расположения.
Таким образом, в ряде исследований иностранных и отечественных авторов приводятся аргументированные данные о взаимосвязи нарушений церебрального кровообращения с патологией шейного отдела позвоночника. С другой стороны, современные возможности неинвазивной диагностики позволяют достоверно оценить состояние мозгового кровообращения в динамике. В то же время нет работ, в которых бы при различной патологии шейного отдела позвоночника и спинного мозга одновременно целенаправленно исследовались и анализировались нарушения кровообращения в системе артериальных магистральных стволов внутренней сонной и позвоночной артерий и внутренней яремной вены в области шеи, а также особенности нарушений мозгового кровообращения.
Вышеизложенное определяет актуальность и целесообразность настоящего исследования.
Цель работы: Исследовать зависимость развития нарушений мозгового кровообращения от различных патологических процессов шейного отдела позвоночника.
Задачи исследования:
1. Определить диагностическую значимость рентгенологических методов исследования и ультразвуковой допплерографии (УЗДГ) у пациентов с патологией шейного отдела позвоночника осложненной, вертебробазилярной недостаточностью.
2. Изучить характер и степень выраженности нарушений мозгового кровообращения у пациентов с различными патологическими процессами в области шейного отдела позвоночника.
3. Определить диагностическую ценность радионуклидных методов исследования -однофотонной эмиссионной компьютерной томографии и вертебральной ангиосцинтиграфии и синусосцинтиграфии — в верификации нарушений мозгового кровообращения у пациентов с патологией шейного отдела позвоночника.
4. Изучить особенности нарушений артериального и венозного мозгового кровообращения у пациентов с патологией шейного отдела позвоночника.
Изучить особенности нарушений артериального и венозного мозгового кровообращения у пациентов с патологией шейного отдела позвоночника.
5. Исследовать корреляционные взаимоотношения особенностей нарушений кровообращения в вертебробазилярной системе и нарушений мозгового кровообращения у пациентов с патологией шейного отдела позвоночника.
6. На основании полученных результатов выяснить патогенез развития нарушений мозгового кровообращения при патологии шейного отдела позвоночника.
Научная новизна:
Впервые при патологии шейного отдела позвоночника и спинного мозга была исследована гемодинамика в каротидном и вертебробазилярном бассейне с учетом венозной фазы кровообращения. Разработаны диагностические критерии гемодинамических нарушений кровообращения головного мозга у исследованной категории больных. Показана патогенетическая связь нарушений мозгового кровообращения с патологией шейного отдела позвоночника.
Практическая значимость:
Разработан комплекс диагностических исследований при патологии шейного отдела позвоночника и спинного мозга, позволяющий выявить связь нарушений мозгового кровообращения с патологией шейного отдела позвоночника.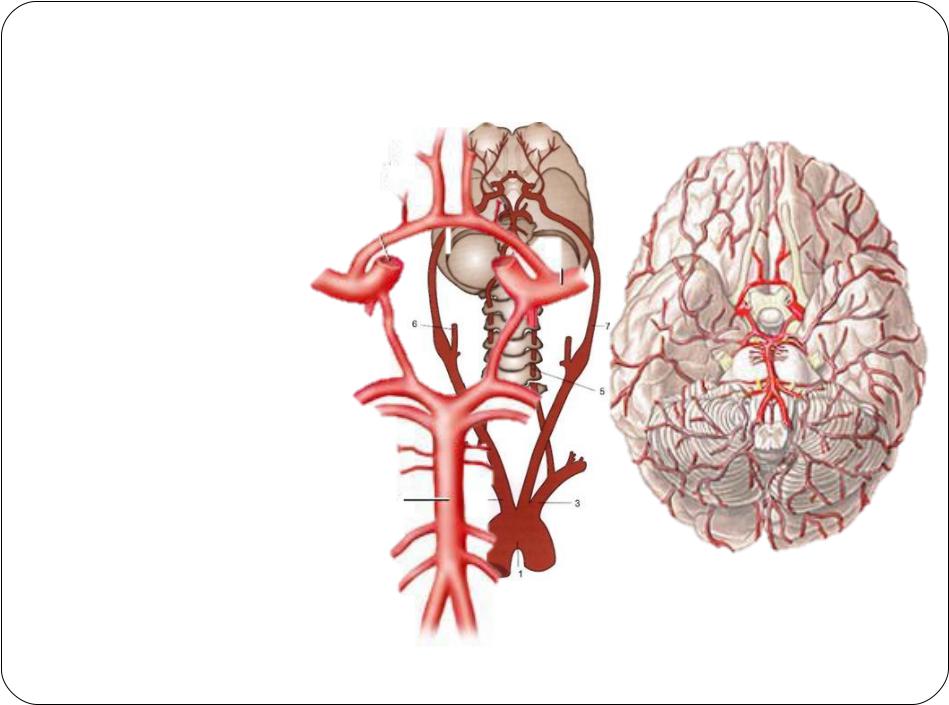 Разработаны практические рекомендации по проведению вертебральной ангиосцинтиграфии и однофотонной эмиссионной компьютерной томографии у пациентов с патологией шейного отдела позвоночника в амбулаторных условиях и в стационаре. Описаны основные виды нарушений мозгового кровообращения при различных патологических процессах в шейном отделе позвоночника, которые могут служить ориентиром для разработки адекватной терапии или выбора метода оперативной коррекции.
Разработаны практические рекомендации по проведению вертебральной ангиосцинтиграфии и однофотонной эмиссионной компьютерной томографии у пациентов с патологией шейного отдела позвоночника в амбулаторных условиях и в стационаре. Описаны основные виды нарушений мозгового кровообращения при различных патологических процессах в шейном отделе позвоночника, которые могут служить ориентиром для разработки адекватной терапии или выбора метода оперативной коррекции.
Апробация работы и публикации.
Основные положения диссертации представлены и доложены на международном нейрохирургическом симпозиуме в г. Санкт-Петербурге 12 июля 2001 г. Апробация работы проведена на совместной научной конференции клиник травматологии и ортопедии, а также кафедры травматологии и ортопедии ФУВ и нейрохирургии МОНИКИ 15 сентября 2004 г. По материалам диссертации опубликовано 11 научных работ.
Объем и структура диссертации.
Работа изложена на 142 страницах машинописного текста, включает 10 таблиц, 11 иллюстраций, состоит из введения, обзора литературы, четырех глав собственных исследований, обсуждения полученных результатов, выводов, практических рекомендаций и приложения. Список использованной литературы включает 211 источник (81 отечественных и 190 зарубежных авторов).
Список использованной литературы включает 211 источник (81 отечественных и 190 зарубежных авторов).
Общая характеристика материала и методов исследования.
Материалом для выполнения данного исследования послужили результаты всестороннего и углубленного обследования 50 пациентов с различной патологией шейного отдела позвоночника и спинного мозга, находившихся на амбулаторном и стационарном лечении в клинике МОНИКИ в период с января 2000 по октябрь 2003 года.
Мужчин было 26 (52%), женщин — 24 (48%). Все пациенты были старше 19 лет, при этом в возрастном промежутке от 19 до 49 лет находилось 20 (40%) больных, старше 50 лет было 30 (60%) пациентов. 39 (18%) больных находились на амбулаторном лечении, 11 (22%) человек лечились стационарно. У большинства пациентов диагностирован остеохондроз шейного отдела позвоночника — 19 (38%) наблюдений. В 5(10%) случаях остеохондроз сочетался с грыжей межпозвонкового диска. У 14(28%) больных выявлен остеохондроз шейного отдела позвоночника в сочетании с вертебробазилярной недостаточностью, в 1 (14%) наблюдениях определен стеноз ВСА и ПА. У 1 (2%) больного установлен диагноз шейной миелопатии и у 4(8%) пациентов была травма шейного отдела позвоночника, осложнившаяся подвывихом СШ — 3 наблюдения, и С1-С11-1 наблюдение.
У 1 (2%) больного установлен диагноз шейной миелопатии и у 4(8%) пациентов была травма шейного отдела позвоночника, осложнившаяся подвывихом СШ — 3 наблюдения, и С1-С11-1 наблюдение.
Минимальная длительность заболевания до обращения за помощью в МОНИКИ составила 2 года, максимальная -12 лет.
При поступлении пациента в МОНИКИ обследование начинали с подробного сбора анамнеза, физикального обследования, исследования неврологического статуса, проведения стандартных лабораторных исследований, рентгенологического исследования шейного отдела позвоночника и ультразвуковой допплерографии (УЗДГ), в том числе транскраниальной УЗДГ.
Основными методами диагностики НМК при патологии шейного отдела позвоночника явились радиологические методы исследования — однофотонная эмиссионная компьютерная томография (ОФЭКТ) и вертебральная ангиосцинтиграфия, синусосцинтиграфия.
ОФЭКТ представляет собой изотопную методику, в которой томограммы головного мозга получаются при помощи вращающейся гамма-камеры или
специального ОФЭКТ-сканера с компьютерной обработкой параметров излучаемой радиации и последующей реконструкцией. Для ОФЭКТ-сканирования использовали изотопы (Ceretec), с помощью которого отражаются различия регионарной перфузии, и Xenon 133, который позволяет количественно измерить регионарный мозговой кровоток. Принцип метода состоит в том, что введенный внутривенно РФП при первом пассаже по сосудам головного мозга свободно проникает через гематоэнцефалический барьер и распространяется в мозговой ткани пропорционально региональному кровоснабжению головного мозга, связываясь с липидами головного мозга (рис. 1).
Для ОФЭКТ-сканирования использовали изотопы (Ceretec), с помощью которого отражаются различия регионарной перфузии, и Xenon 133, который позволяет количественно измерить регионарный мозговой кровоток. Принцип метода состоит в том, что введенный внутривенно РФП при первом пассаже по сосудам головного мозга свободно проникает через гематоэнцефалический барьер и распространяется в мозговой ткани пропорционально региональному кровоснабжению головного мозга, связываясь с липидами головного мозга (рис. 1).
, пациягге ■..’•■ Радитиье»я/«а2
BOSgWCV’ • .. ПОЯ
; t истории бом»ив U3. I пбуж. npmi
It*« 20 ut-100
Ф.И.О. пацианФ* Родит«льская/622 возраст Пол
f негордо С-слвэнн 622 t амбул. карты
Рис. 1 однофотонная эмиссионная компьютерная томография больной И 1960 г.р. — норма.
При исследовании получали 9 или 12 снимков толщиной 10 или 14 мм. Анализ и обработку информации проводили путем визуальной оценки томосцинтиграмм в аксиальной плоскости, а также при вторичной реконструкции в сагиттальной и фронтальной плоскостях. Кроме того, проводили количественную оценку величины перфузии РФП в зонах, соответствующих бассейнам магистральных артериальных стволов.
Кроме того, проводили количественную оценку величины перфузии РФП в зонах, соответствующих бассейнам магистральных артериальных стволов.
Для производства ангиосцинтиграфии использовали пленарную гамма-камеру Pho 1Y (Nuclear Chicago, USA), оснащенную ЮМ, совместимым с персональным компьютером. Запись динамических сцинтиграмм начинали через 54-57 секунд после введения РФП. Фиксировали 40 кадров со скоростью 1 кадр в секунду (рис. 2).
Ангиосцинтиграммы оценивали по качественным (визуальным) признакам и количественным критериям. Основу радионуклидного признака составляет пространственно-временное распределение РФП по магистральным артериальным стволам и основным венозным коллекторам головы и шеи. Для количественного анализа динамических параметров использовали программное обеспечение «Сцинтипро».
Вертебральная ангиосцинтиграфия (ВА) позволяла выявлять патологию в позвоночных, задних мозговых и средних мозговых артериях. Фаза визуализации основных венозных коллекторов применялась в качестве отдельной методики исследования — синусосцинтиграфии.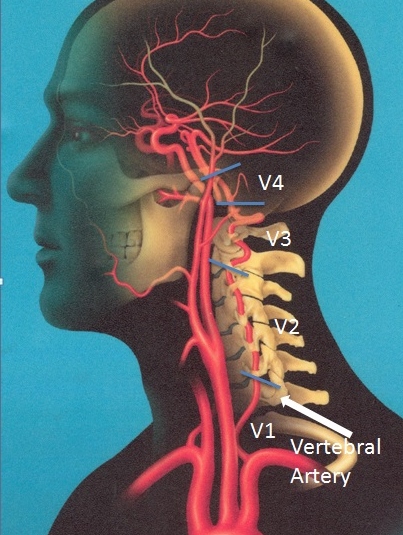 На синусосцинтиграммах четко
На синусосцинтиграммах четко
визуализировался верхний сагиттальный синус, синусный сток (СС), поперечные синусы, сигмовидные синусы, а также яремные вены. При качественной оценке сцинтиграмм отмечали наличие или отсутствие асимметрии распределения РФП в парных структурах. Наряду с этим регистрировалась деформация или смещение сосудов, неравномерность (прерывистость) распределения РФП в них; очаги повышенного или пониженного накопления РФП как в области синусов, так и в области яремных вен; может отмечаться феномен «культи» или «стоп синдром».
Результаты собственных исследований.
Остеохондроз шейного отдела позвоночника, по нашим данным, сопровождался нарушениями мозгового кровообращения в большинстве наблюдений.
При этом на вертебральной ангиосцинтиграфии выявлены нарушения кровотока по левой позвоночной артерии у 9 (47,4%) пациентов, по правой — у 3(15,8%) больных, по обеим позвоночным артериям — у 7(36,8%). Всего лишь в двух наблюдениях не выявлено нарушений кровотока (табл. 1).
1).
Таблица 1
Характер нарушений мозгового кровообращения у пациентов с остеохондрозом шейного отдела позвоночника.
Характер нарушений мозгового кровообращения Нарушения кровотока по левой ПА (п=9) Нарушения кровотока по правой ПА (п=3) Нарушения ! кровотока по обеим ПА (п=7)
Снижение венозного
кровотока по левым венозным 9 — 4 ‘
коллекторам и левой яремной вене (снижение на 1045%)
Снижение венозного
кровотока по правым — 3 3
венозным коллекторам и
правой яремной вене
Снижение кровотока по левой СМА 5 2
Снижение кровотока по левой ЗМА 5 2
Снижение кровотока по
правой СМА 3 6
Снижение кровотока по правой ЗМА — 3 6
Очаги гипоперфузии в левом
полушарии 2
Очаги гипоперфузии в правом
полушарии
Очаги гипоперфузии в обоих 3 3 6
полушариях
Очаги гипоперфузии в ткани
мозжечка 2 3 3
У всех 9 пациентов с патологией кровотока по левой позвоночной артерии отмечены нарушения венозного кровотока головного мозга. Нарушения кровотока по мозговым артериям по данным ВА диагностированы у 5 пациентов из 9, у этих же больных, по данным однофотонная эмиссионная компьютерная томография (ОФЭКТ), отмечены очаги гипоперфузии в корковых областях полушарий головного мозга.
Нарушения кровотока по мозговым артериям по данным ВА диагностированы у 5 пациентов из 9, у этих же больных, по данным однофотонная эмиссионная компьютерная томография (ОФЭКТ), отмечены очаги гипоперфузии в корковых областях полушарий головного мозга.
При снижении кровотока по правой ПА нарушения мозгового кровообращения более выражены. Во всех 3 наблюдениях выявлены очаги гипоперфузии (по данным ОФЭКТ) в височно-затылочных областях обоих полушарий, в двух наблюдениях -очаги гипоперфузии в ткани мозжечка. При ВА и синусосцинтиграфии определяется снижение кровотока по СМА и ЗМА, а также по правым венозным коллекторам и правой яремной вене.
При патологических изменениях обеих позвоночных артерий во всех наблюдениях отмечалось снижение кровотока по СМА и ЗМА. Отмечены снижение и ассимметрия кровотока по венозным коллекторам, в двух случаях диагностирована желудочковая гидроцефалия. По данным ОФЭКТ, во всех 8 случаях отмечены очаги гипоперфузии в коре обоих полушарий головного мозга, в 3 наблюдениях имелись очаги гипоперфузии в мозжечке.
При анализе радиологических данных у пациентов с клиническими проявлениями вертебробазилярной недостаточности на фоне остеохондроза шейного отдела позвоночника нарушения венозного оттока отмечены у всех 14 больных. При анализе результатов ВА преимущественные нарушения кровотока в системе левой ПА отмечены в 7 (50%) наблюдениях из 14, в системе левой ПА — также у половины пациентов. Характер нарушений мозгового кровотока у пациентов с остеохондрозом, осложненным вертебробазилярной недостаточностью, приведен в таблице 2.
Таблица 2
Характер нарушений мозгового кровотока у пациентов с остеохондрозом,
осложненным вертебробазилярной недостаточностью
Характер нарушений мозгового кровообращения Нарушения кровотока по левой ПА (п=7) Нарушения кровотока по правой ПА (п=7)
Снижение венозного
кровотока по левым венозным 3 5
коллекторам и левой яремной
вене
Снижение венозного
кровотока по правым — 5
венозным коллекторам и
правой яремной вене
Снижение кровотока по левой СМА 1
Снижение кровотока по левой ЗМА 3 -
Снижение кровотока по правой СМА 5
Снижение кровотока по
правой ЗМА 5
Очаги гипоперфузии в левом
полушарии 4
Очаги гипоперфузии в правом
полушарии 2
Очаги гипоперфузии в обоих
полушариях 5
Очаги гипоперфузии в ткани
мозжечка 2
Нарушения мозгового кровотока по левой ЗМА сопровождали аналогичные нарушения со стороны левой ПА в 3 случаях из 7, еще в одном наблюдении отмечалось снижения кровотока по средней мозговой артерии. В остальных 3 случаях среди НМК превалировала венозная дисциркуляция. По данным ОФЭКТ очаги гипоперфузии в коре головного мозга выявлены у 4 пациентов из 7, нарушений кровоснабжения мозжечка отмечено не было.
В остальных 3 случаях среди НМК превалировала венозная дисциркуляция. По данным ОФЭКТ очаги гипоперфузии в коре головного мозга выявлены у 4 пациентов из 7, нарушений кровоснабжения мозжечка отмечено не было.
При нарушениях кровотока по правой ПА в двух наблюдениях снижения кровотока по мозговым артериям при ВА не выявлено, на ОФЭКТ обнаружены очаги гиперперфузии. В остальных 5 случаях выявлено снижение кровотока по правой СМА и ЗМА, на ОФЭКТ обнаружены очаги гипоперфузии в корковых лобно-базально-височных отделах и в мозжечке. В двух наблюдениях диагностирована гидроцефалия.
Таким образом, радиологическая картина НМК при вертебробазилярной недостаточности сопоставима с таковой при остеохондрозе шейного отдела позвоночника без клинических признаков вертебробазилярной недостаточности (ВБН). Отмечается достоверно более частое поражения бассейна правой ПА.
При остеохондрозе шейного отдела позвоночника, осложненном грыжей межпозвонкового диска, у 5 пациентов диагностированы следующие нарушения мозгового кровообращения (табл. 3).
Таблица 3
Характер нарушений мозгового кровотока у пациентов с остеохондрозом,
осложненным грыжей межпозвонкового диска
Характер нарушений мозгового кровообращения Нарушения кровотока по левой ПА (п=2) Нарушения кровотока по правой ПА (п=2) Нарушения кровотока по обеим ПА (п=1)
Снижение венозного кровотока по левым венозным коллекторам и левой яремной вене 2 1
Снижение венозного кровотока по правым венозным коллекторам и правой яремной вене 2
Снижение кровотока по левой СМА 1 — -
Снижение кровотока по левой ЗМА 1 — -
Снижение кровотока по правой СМА — 1 -
Очаги гипоперфузии в обоих полушариях — 1
Грыжа межпозвонкового диска СУ-СУ выявлена у двух пациентов. В обоих наблюдениях нарушения мозгового кровообращения ограничивались нарушениями кровотока по левой позвоночной артерии и венозной дисциркуляцией; очагов гипоперфузии в ткани мозга не выявлено.
У больной с грыжей диска СУ1-СУП обнаружено (по данным ВА) в артериальной фазе снижение кровотока в левой ПА на 23%. Снижена линейная скорость по СМА на 20% и задней мозговой артерии на 20% слева. При синусосцинтиграфии отмечено снижение кровотока по левым венозным коллекторам.
Грыжа диска СП-СШ (2 больных) сопровождалась, по данным ОФЭКТ, наличием очагов гипоперфузии в лобно-височных отделах обоих полушарий. Поражения мозжечка не отмечено. В одном из наблюдений синусосцинтиграфия выявила снижение кровотока по венозным коллекторам справа, в другом — слева.
В целом, нарушения мозгового кровообращения при остеохондрозе шейного отдела позвоночника в сочетании с грыжами межпозвонковых дисков наблюдались у
всех пациентов. Это свидетельствует о патогенетической взаимосвязи НМК и такого, казалось бы, заболевания, как грыжи межпозвонковых дисков.
Характер нарушений мозгового кровотока у 4 пациентов с травмой шейного отдела позвоночника представлен в следующей таблице.
Таблица 4
Характер нарушений мозгового кровотока у пациентов с травмой шейного отдела позвоночника
Характер нарушений мозгового кровообращения Нарушения кровотока по левой ПА (п=4) Нарушения кровотока по правой ПА (п=0) Нарушения кровотока по обеим ПА (п=0)
Снижение венозного кровотока по левым венозным коллекторам и левой яремной вене Очаги гипоперфузии в левом полушарии 3
1 — -
У пациентов с подвывихом CIV позвонка вертебральная ангиосцинтиграфия выявила снижение кровотока по левой позвоночной артерии, а синиусосцинтиграфия — снижение кровотока по левым венозным коллекторам — по ПС — на 14-26%, по СС — на 25-37%, по левой яремной вене — на 15-41%. Очаги гипоперфузии в лобных корковых отделах выявлены при ОФЭКТ лишь у 1 больного При подвывихе С1-СП с асимметрией зуба СП — отклонением вправо — обнаружена радиологическая картина деформации левой позвоночной артерии при достаточном кровотоке.
Таким образом, постгравматические изменения при подвывихе CIY осложнялись нарушениями кровотока по левой позвоночной артерии и снижением кровотока по левым венозным коллекторам. Наличие очагов ишемии в области коры головного мозга отмечено у 1 пациента.
В ходе исследования был изучен характер НМК при различных вариантах клинического течения остеохондроза шейного отдела позвоночника, грыжах межпозвонковых дисков, последствий травм шейного отдела позвоночника. Все указанные патологические процессы приводят к нарушениям кровотока в позвоночных артериях. При этом существует всего два патогенетических механизма, обуславливающих развитие нарушений кровообращения в позвоночных артериях и, как следствие, в вертебробазилярном бассейне.
Это, во-первых, синдром вертеброгенно обусловленного раздражения (ирритации) периваскулярного симпатического сплетения позвоночной артерии.
Во-вторых — это прямое компримирующее воздействие на позвоночную артерию (сдавление позвоночной артерии унковертебральными остеофитами, грыжей диска, суставными отростками позвонков и т.д.)
По нашему мнению, прямое компримирующее воздействие на позвоночную артерию всегда вызывает ирритацию периваскулярного симпатического сплетения сосуда. В этой связи мы выделили две группы причин развития нарушений кровообращения в позвоночных артериях:
1. Ирритация периваскулярного симпатического сплетения ПА
2. Сочетание прямого компримирующего воздействия на ПА и ирритации периваскулярного симпатического сплетения сосуда.
В соответствии с этим пациенты были разделены на две соответствующие клинические группы. Характер нарушений мозгового кровообращения у пациентов этих клинических групп, по данным однофотонная эмиссионная компьютерная томография (ОФЭКТ) и вертебральная ангиосцинтиграфия (ВА) синусосцинтиграфии приведен в таблице 5.
При поражении левой ПА у пациентов первой группы основным вариантом НМК явилось нарушение венозного оттока по левым венозным коллекторам и яремной вене, выявленное более чем у половины больных.
Аналогичная патология превалировала и у пациентов с поражением правой ПА. При сочетанном поражении левой ПА нарушения венозного оттока при синусосцинтиграфии диагностированы у всех пациентов 2 группы.
Однако самые выраженные НМК отмечены при сочетанном (компримирующее воздействие, сопровождающееся ирритацией) поражении правой ПА Снижение венозного оттока наблюдалось практически у всех больных, причем как по правым, так и по левым венозным коллекторам. Также у всех пациентов присутствовали очаги гипоперфузии левого или обоих полушарий головного мозга.
При анализе приведенных данных обращает на себя внимание тот факт, что снижение венозного кровотока по левым венозным коллекторам и левой яремной вене достоверно (р<0,01) чаще — 11 случаев у 12 больных (91,7%) против 12 наблюдений у 31 пациента (38,7%) — наблюдалось во 2 группе пациентов. При этом в 2 случаях у пациентов 1 группы и в 3 — у пациентов второй группы — отмечено нарушение оттока крови по левым венозным коллекторам и яремной вене при патологии правой позвоночной артерии.
Таблица 5
Характер нарушений мозгового кровообращения в зависимости от патогенеза развития нарушений кровотокав ПА.
Снижение венозного кровотока по правым венозным коллекторам и правой яремной вене также достоверно (р<0,05) чаще было отмечено во второй группе больных (41,7% против 19,4%).
Нарушения мозгового кровообращения, выявленные при вертебральной ангиосцинтиграфии — снижение кровотока по левой и правой СМА, а также снижение кровотока по левой и правой ЗМА также достоверно (р<0,05) чаще наблюдались у пациентов 2 группы.
Очаги гипоперфузии в левом и правом полушарии, обоих полушариях и ткани мозжечка, выявленные при ОФЭКТ, также достоверно (р<0,05) чаще отмечены при
сочетании прямого компримирующего воздействия на ПА и ирритации периваскулярного симпатического сплетения, чем при наличии изолированной ирритации.
Меньшую частоту и степень выраженности нарушений мозгового кровообращения у пациентов 1 группы можно объяснить наличием периодов «расслабления» ПА при общем снижении тонуса симпатической нервной системы, а также при временном ослаблении воздействия ирригирующего фактора в результате изменения позы пациента и проводимой медикаментозной терапии.
В результате проведенных исследований НМК при патологии шейного отдела позвоночника выявлены во всех клинических группах пациентов. Следует отметить, что степень выявленных НМК не коррелировала с клинической симптоматикой и длительностью заболевания. Основным способом диагностики НМК стали радионуклидные исследования, в частности ОФЭКТ, вертебральная ангиосцинтиграфия и синусосцинтиграфия.
Для объяснения патогенеза развития НМК в бассейнах задней и средней мозговых артерий при патологии позвоночных артерий важное значение имеет синдром вертебробазилярной недостаточности. Группой экспертов ВОЗ «вертебрально-базилярная недостаточность» определялась как «обратимое нарушение функции мозга, вызванное уменьшением кровоснабжения области, питаемой позвоночными и основной артериями».
В вертебробазилярном бассейне находятся структуры, отвечающие за жизненно важные функции организма. В связи с этим можно предположить, что нарушение кровоснабжения ствола мозга из вертебробазилярной системы вызывает перераспределение крови из бассейнов ЗМА и СМА через базилярную артерию, тем самым вызывая нарушения кровообращения в бассейнах задней и средней мозговых артерий, возникновение «очагов гипоперфузии ишемического генеза» в корковых отделах обоих полушарий и снижение кровотока по венозным коллекторам и яремным венам. При этом благодаря механизмам саморегуляции мозгового кровотока во многих случаях сохраняется адекватное артериальное кровоснабжение при патологических изменениях венозного оттока. По нашему мнению, так можно объяснить превалирование нарушений венозного оттока среди НМК у пациентов с патологией шейного отдела позвоночника.
Превалирование патологии левой позвоночной артерии у анализируемой категории больных, вероятно, связано с большей нагрузкой на нее из-за более интенсивной деятельности левого полушария головного мозга у большинства людей- «правшей». По аналогии с работой сложного механизма, у которого
наиболее частым поломкам подвержена самая «нагруженная» деталь, левая ПА чаще подвержена патологическим изменениям.
Для объяснения более тяжелых НМК у пациентов с патологией шейного отдела позвоночника при нарушениях функций правой позвоночной артерии считаем целесообразным предложить «эволюционную теорию».
В процессе эволюции человеческий организм лучше приспособился к более частым «поломкам» в системе левой ПА и выработал соответствующие компенсаторные механизмы. При патологии правой ПА компенсаторные механизмы менее совершенны, что и ведет к большей тяжести НМК у пациентов с патологией шейного отдела позвоночника при превалирующей патологии правой позвоночной артерии.
Впрочем, приведенные объяснения имеют скорее теоретическое значение. Главным итогом проведенного исследования мы считаем осознание того факта, что безопасные, на первый взгляд, патологические процессы в области шейного отдела позвоночника, на самом деле сопровождаются выраженными нарушениями мозгового кровообращения и являются предпосылками развития таких грозных и опасных для жизни осложнений, как ишемический инсульт.
В результате проведенного исследования сделаны следующие выводы:
1. Применение рентгенологических методов диагностики и УЗД Г позволяет выявить нарушения кровообращения в вертебробазилярной системе практически у всех пациентов с патологией шейного отдела позвоночника, при этом достоверно чаще диагностируется патология левой позвоночной артерии.
2. Практически у всех пациентов с различными патологическими процессами в области шейного отдела позвоночника отмечаются нарушения мозгового кровообращения: нарушения артериального кровотока в бассейнах задней и средней мозговых артерий, очаги гипоперфузии ишемического генеза в области корковых отделов, а также нарушения оттока по венозным коллекторам и яремным венам.
3. Радионуклидные методы исследования — однофотонная эмиссионная томографии и вертебральная ангиосцинтиграфия (синусосцинтиграфия) позволяет диагностировать нарушения мозгового кровообращения у пациентов с патологией шейного отдела позвоночника до появления соответствующей симптоматики.
4. Среди патологических изменений мозгового кровотока у пациентов с
патологией шейного отдела позвоночника наиболее часты нарушения оттока крови по венозным коллекторам и яремным венам (96% наблюдений), в большинстве наблюдений сопровождающиеся явлениями гипоперфузии различных участков коры головного мозга.
5. Нарушениям кровообращения в вертебробазилярной системе сопутствуют нарушения мозгового кровообращения в каротидной системе. При этом снижение кровотока по правой позвоночной артерии при патологии шейного отдела позвоночника встречается достоверно реже, чем по левой ПА, и сопровождается достоверно более выраженными нарушениями мозгового кровообращения.
6. Нарушения мозгового кровообращения при патологии шейного отдела позвоночника обусловлены действием механизмов ауторегуляции МК и связаны с перераспределением крови между вертебробазилярным бассейном и бассейнами ЗМА и СМА (компенсаторный сброс крови из бассейнов СМА и ЗМА при значительном снижении кровотока в вертебробазилярном бассейне).
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
1. В диагностический алгоритм у пациентов с патологией шейного отдела позвоночника следует включать методы исследования мозгового кровообращения, наиболее эффективными из которых являются однофотонная эмиссионная компьютерная томография, вертебральная ангиосцинтиграфия и синусосцинтиграфия.
2. При разработке комплекса консервативных лечебных мероприятий и определении показаний к оперативному лечению у пациентов с патологией шейного отдела спинного мозга следует учитывать наличие сопутствующих НМК, в особенности при отсутствии технических возможностей для их диагностики.
3. При разработке профилактических мероприятий и санитарно-просветительской работе следует обращать особое внимание на важность раннего выявления и лечения пациентов с патологией шейного отдела спинного мозга, что в итоге будет способствовать снижению смертности от ишемического инсульта.
Список работ, опубликованных по теме диссертации.
1. Патогенетическое лечение вертеброгенных шейных миелопатий. //Повышение эффективности профилактики, диагностики и лечения заболеваний нервной системы — Москва, 1999, с.161-162 /Хусейн Н.А. Киселев А.М., Выборов М.П., Лобов М А./
2. Комбинированное лечение вертеброгенных миелопатий.// Повышение эффективности профилактики, диагностики и лечения заболеваний нервной системы — Москва,1991, с.121-123 / Хусейн Н.А. Киселев А.М., Лобов МА/
3. Диагностика и лечение недостаточности кровообращения при краниовертебральном синдроме// Современные проблемы хирургии -Москва, 1993с. 68-69 /Хусейн НА, Киселев А.М., Выборов М.П./
4. Клинико-компьютерные параллели при нарушении кровообращения в вертебрально-базиллярной системе//Современные аспекты клинической хирургии — Москва, 1992, с.131-133 / Хусейн НА . Киселев А.М., Выборов М.Ш
5. Хирургическая коррекция и стабилизация застарелых повреждений шейного
отдела позвоночника//Актуальные вопросы клинической медицины — Москва, 1995. с. 133-135 / Хусейн Н.А.Киселев А.М., Кедров А.В./
6. Нарушения кровообращения при патологии шейного отдела
позвоночника//Вестник практической неврологии — Москва, 1998, с.74-75 / Хусейн Н.А. Киселев А.М., Выборов М.П., Лобов МЛ., Кедров А.В./
7. Хирургическое лечение недостаточности кровоснабжения шейного отдела
позвоночника//Современные аспекты клинической медицины. — Москва, 1996, с. 131-132 /с Хусейн НА , Киселев А.М.. Качков ИЛ., Кедров А.В., Макаренко М.Ф./
8. Передняя стабилизация шейного отдела позвоночника имплантантами на основе гидроксиапатита при травматических повреждениях. // Съезд молодых ученых академии медицинских наук «Новое в реконструктивной хирургии» — Москва, 2004, с. 185-186 / НЛ Хусейн. А.М Киселев., ЛЛ. Рамирез, И.В. Есин., П.В. Кротенков, А.В. Кедров, Р.Г. Биктимиров/
9. Хирургические аспекты болевых синдромов шейного остеохондроза// Клинические и теоретические аспекты боли — Москва, 2001, с.111-112 / Хусейн Н.А.Киселев А.М., Качков И.А., Карякин Н.Н./
10. Surgical correction and stabilization of spine // Fist interdisciplinary world congress on spinal surgery — Berlin, 2000, p.215 /Kiselev A. Hussein N.A /
11. Surgical decompression & stabilization of spine//10 European Congress of Neurosurgery — Berlin,1995, p. 132-133 / Cachkov I., Bictimirov R., Makarenko M., Kedrov A., Anochin A., Hussein N.A./
11 &ЕВ ?G05 1399
Нарушения кровотока в позвоночных артериях при нестабильности в двигательных сегментах шейного отдела позвоночника
005010038
На правах рукописи. УДК: 616.134.9:616.711.1
Рудковский Андрей Иосифович
НАРУШЕНИЯ КРОВОТОКА В ПОЗВОНОЧНЫХ АРТЕРИЯХ ПРИ НЕСТАБИЛЬНОСТИ В ДВИГАТЕЛЬНЫХ СЕГМЕНТАХ ШЕЙНОГО ОТДЕЛА ПОЗВОНОЧНИКА
14.01.11 — «Нервные болезни»
— 1 С 0ЕЗШ
Автореферат диссертации на соискание ученой степени кандидата медицинских наук
Москва-2012
005010038
Работа выполнена в Государственном бюджетном образовательном учреждении высшего профессионального образования «Московский государственный медико — стоматологический университет» Министерства здравоохранения и социального развития Российской Федерации (ГБОУ ВПО МГМСУ Минздравсоцразвития России).часов на заседании диссертационного
совета ДМ 208.041.04 при ГБОУ ВПО МГМСУ Министерства здравоохранения и социального развития Российской Федерации по адресу: ул. Долгоруковская, Д-4, стр.7.
Почтовый адрес: 127473, г. Москва, ул. Делегатская, д.20/1.
С диссертацией можно ознакомиться в библиотеке Московского государственного Медико-стоматологического университета (127206, Москва, ул. Вучетича, д. 10а).
Автореферат разослан
Ученый секретарь диссертационного совета
кандидат медицинских наук доцент Т.Ю.Хохлова
Актуальность исследования
Современные статические нагрузки приводят к широкому распространению патологии позвоночника: в частности шейного отдела, с блоками в одних и нестабильностью в других позвоночно-двигательных сешентах, что вызывает неуклонное возрастание доли поражений головного мозга, локализованных в зоне кровоснабжения вертебрально-базилярной системы. Второй сегмент позвоночных артерий составляет по длине около 70% сосуда [В.Г.Лелюк 2004] и располагается в канале поперечных отростков, следовательно, на кровотоке в вертебрально-базилярной системе сказывается любое нарушение подвижности шейных двигательных сегментов [А.Б.Ситель 2007].
При оценке взаимосвязи патологии шейного отдела позвоночника и нарушений кровотока в вертебрально-базилярной системе [М-Шаупеэ 2009], имеется вероятность развития ишемических процессов не только в бассейне позвоночных артерий, но вследствие обкрадывания передней части Виллизиева круга за счет задней, в зонах, кровоснабжаемых сонными артериями, [Н.ТЫе1 2005, Ь.С.ТЬотаз 2008].
В основе клинических проявлений патологии шейного отдела позвоночника существенная роль принадлежит расстройствам венозного кровообращения [А.Б.Ситель 2008]. Кровоток в мелких венах позвоночных сплетений изменяется под воздействием компрессионных влияний остеофитов, а также при патобиомеханических нарушениях в позвоночно-двигательных сегментах шейного отдела позвоночника. Нарушение венозной циркуляции в позвоночном сплетении приводит к изменениям оттока из полости черепа, что в свою очередь служит физиологическим базисом для формирования церебральной симптоматики, а в конечном итоге — и для развития картины венозной энцефалопатии [И.Д.Стулин 2009].
Для коррекции нарушения объема движений в позвоночных двигательных сегментах успешно применяются многочисленные методики, включая мануальную терапию. При наличии нестабильности двигательного сегмента до-
пустимо применение мягхотканевых техник мануальной терапии
[О.Г.Бугровецкая 2003].
Связь клинических проявлений недостаточности кровообращения в вертебрально-базилярной системе и расстройств венозного кровотока с конкретными уровнями поражения шейных двигательных сегментов освещена недостаточно полно. Также неполны представления о роли мягкотканевых техник мануальной терапии в коррекции нестабильности шейных позвоночнодвигательных сегментов и о возможностях ультразвуковых методов оценки кровотока в позвоночных артериях [И.Д.Стулин 2005], как инструменте определения показаний к мануальной терапии и контроля ее качества [Шмырев В.И 2007, Гойденко В.С 2008].
Цель исследования
Оптимизировать диагностический алгоритм при нестабильности в шейных позвоночно-двигательных сегментах с целью повышения качества лечения пациентов с вертеброгенными заболеваниями нервной системы.
Задачи исследования
1) Исследовать варианты нарушений кровотока в позвоночных артериях на экстра- и интракраниальном уровне и венозного оттока в позвоночном сплетении при нестабильности в шейных позвоночно-двигательных сегментах.
2) Изучить корреляции вариантов нарушения кровотока в позвоночных артериях и уровней сегментарной нестабильности.
3) Отработать алгоритм диагностики нестабильности в шейных позвоночно-двигательных сегментах на основе клинических, рентгенологических и ультразвуковых критериев.
4) Оценить эффективность мягкотканевых техник мануальной терапии для коррекции нестабильности шейных позвоночно-двигательных сегментов и нарушений гемоциркуляции в системе позвоночных артерий.
Научная новизна работы
В результате проведенного исследования получены новые данные:
1) описаны различные сочетания нарушений кровотока в позвоночных артериях и венах при нестабильности шейного отдела позвоночника;
2) выявлены изменения церебрального гемодинамического резерва при экстравазальных воздействиях на позвоночные артерии;
3) подтверждена связь характера нарушения кровотока в вертебральнобазилярной системе с уровнем нестабильности шейных позвоночнодвигательных сегментов;
4) доказана эффективность мягкотканевых мануальных методик в коррекции нестабильности шейных позвоночно-двигательных сегментов и нарушений гемоциркуляции в системе позвоночных артерий.
Практическая значимость
Проведенные исследования позволили расширить наши представления о влиянии патологии шейного отдела позвоночника на кровоток в вертебральнобазилярной системе, продемонстрировали зависимость характера сосудистых расстройств от уровня сегментарных нарушений.
Обосновано применение ультразвуковой допплерографии и маятниковой пробы для оценки наличия и типа сосудистых расстройств в системе позвоночных артерий, как критерия для определения показаний к проведению мануальной терапии и контроля эффективности лечения.
Основные положения, выносимые на защиту
1) Нестабильность позвоночно-двигательных сегментов шейного отдела позвоночника вызывает нарушение параметров кровотока не только в позвоночных артериях, но во всех отделах вертебрально-базилярной системы, а также венозного оттока из полости черепа.
2) Существует взаимосвязь между некоторыми вариантами нестабильности и блокирования шейных позвоночно-двигательных сегментов и типом изменения кровотока в позвоночных артериях.
3) Ультразвуковая допплерография артерий вертебрально-базилярной системы — адекватный инструмент определения возможности проведения мануальной терапии и контроля эффективности лечения.
4) Мягкотканевые техники мануальной терапии дают длительный эффект при коррекции стато-динамических нарушений шейного отдела позвоночника как в плане восстановления физиологической подвижности позвоночнодвигательных сегментов, так и для коррекции расстройств артериального и венозного кровотока в области головы и шеи.
Внедрение в практику
Практические разработки внедрены в городской поликлинике №20 г. Москвы, в Московском научно-практическом центре оториноларингологии.
Личное участие
Автором лично было проведено клинико-инструментальное обследование 70 пациентов, сопоставление полученных результатов с данными рентгеновских и нейровизуализаци-онных методов диагностики, применяемых при патологии шейного отдела позвоночника и для оценки состояния церебральных функций. В ходе сбора материала для диссертационной работы Рудковским А.И. освоены методики исследования ауторегуляции мозгового кровотока и отработан алгоритм комплексной мануальной и ультразвуковой диагностики при нестабильности в шейных позвоночно-двигательных сегментах (ПДС).
Апробация работы
Полученные в результате проведенных исследований материалы были доложены на 32-ой Итоговой конференции молодых учёных (Москва, 2010), на XX юбилейной научно-практической конференции Всероссийской Ассоциации Мануальной Медицины и Московского Профессионального Объединения мануальных терапевтов (Москва, 2010), на Российской научно-практической конференции «Нарушения мозгового кровообращения, диагностика, профилактика, лечение» (Пятигорск, 2010), Международной научной конференции «АНГИО-ДОП — 2011» — нейросонология и церебральная гемодинамика.
Диссертация апробирована 26 октября 2011 года на совместном заседании кафедры неврологии лечебного факультета и кафедры рефлекторной и мануальной терапии ФПДО МГМСУ.
Публикации
По теме диссертации опубликовано 7 работ, в том числе 2 работы в журналах, рекомендованных ВАК Минобрнауки РФ.
Объем и структура диссертации
Разделы диссертации: введение, обзор литературы, материалы и методы исследования, результаты собственных исследований, заключение, выводы и практические рекомендации. Работа изложена на 123 страницах печатного текста, иллюстрирована 29 таблицами и 22 рисунками. Библиографический указатель содержит 177 источников: 124 отечественных и 53 зарубежных.
МАТЕРИАЛЫ И МЕТОДЫ
Проведено обследование и лечение 50 пациентов (16 мужчин и 34 женщин), обратившихся на прием к неврологу и мануальному терапевту в связи с жалобами на боли в шейной и затылочной областях. В исследование включались пациенты, заболевание которых расценивалось как «цервикогенная головная боль» в соответствии с Международной классификацией головных болей [48] — код 11.2.1, что соответствует коду 044.841 в Международной классификации болезней 10-ого пересмотра. .
В случае выявления признаков, характерных для определенных компрессионных синдромов, таких как синдром передней лестничной мышцы, синдром нижней косой мышцы головы или синдром позвоночной артерии, пациенты в исследование не включались.
В основную группу входили мужчины и женщины в возрасте 25-35 лет; средний возраст по группе составил 31,8 ± 6,3 года. Таблица 1 подтверждает сопоставимость групп по полу и возрасту.
Состав Основная гр. Контрольная гр.
Мужчины Количество (чел) 16 8
Возраст (лет) 33,7 ±4,8 30,0 ± 5,9
Женщины Количество (чел) 34 12
Возраст (лет) 29,3 ± 6,6 33,1 ±6,4
Всего Количество (чел) 50 20
Возраст (лет) 31,8 ±6,3 32,6 ±7,1
Методы исследования. В процессе работы в обеих группах проводилось изучение анамнестических и клинических данных, включая подробное исследование неврологического и ортопедического статуса с выполнением функциональных проб; оценка результатов дополнительных методов исследования. Полученная информация вносилась в индивидуальные карты и обрабатывалась статистически.
Неврологическое и ортопедическое исаедование осуществлялось перед началом терапии, сразу после курса и спусп 6-7 месяцев после курса лечения. Основной жалобой обследованных пациштов были головные боли шейнозатылочной локализации без иррадиацич в отдаленные области: монотонные ноющие или давящие, средней интеъсивности (5-7 баллов по Визуальноаналоговой шкале боли — ВАШ). Половина обследованных отмечала усиление болей при резком повороте головы. Еоли возникали эпизодически не более 15 дней месяца с характерными обострениями в весенний и осенний периоды. Помимо болей, 90% больных отмечали периодическое ызникновение в зонах, соответствующих болевому региону, парестезий: чувство холода, покалывания, «ползания мурашек».
Длительность заболевания составила от 6 месязев до 12 лет. Все пациенты были обследованы в первую неделю очередного->бострения; терапия начиналась в день обращения после установленного цика обследований.
Всем пациентам выполнялось функциональное рентгенологическое исследование на дигитальном аппарате Precision RXi (GE, USA), включающее снимки в прямой и боковой проекции, снимки с наклонами головы вперед и назад в боковой проекции. Определялся показатель нестабильности для всех позвоночно-двигательных сегментов шейного отдела позвоночника. При наличии клинических признаков патологии шейных корешков выполнялась магнитнорезонансная томография шейного отдела позвоночника. Рентгенологическое исследование повторялось через 6-7 месяцев после курса мануальной терапии (МТ).
Первичная оценка состояния артерий шеи осуществлялась при помощи линейного датчика сканера «Сономед 500» (Спектромед, Москва): после исключения аномалий развития брахиоцефальных артерий регистрировались параметры скорости и резистивности потоков. Затем проводилось допплеромет-рическое исследование кровотока в церебральных артериях: датчиком 2 МГц на допплеровском анализаторе «Сономед 300» (Спектромед, Москва) транстемпоральным и субокципитальным доступом по стандартной методике. У всех обследованных удалось лоцировать средние (СМА), передние (ПМА), задние (ЗМА), позвоночные артерии (ПА) с обеих сторон и основную артерию (ОА). С помощью компрессионных проб оценивались функции соединительных артерий. При оценке линейной скорости кровотока (ЛСК) в лоцируемых артериях принимались во внимание симметричность (равенство) JICK в парных сосудах, а также соответствие ЛСК возрастным нормативам [В.Г.Лелюк 2001] и соблюдение пропорций между ЛСК в экстра- и интракраниальных артериях [М.М.Одинак 2000].Следующим этапом проводилось исследование позвоночных артерий в третьем сегменте после троекратного повторения поворотов головы на максимальный угол из стороны в сторону (маятниковая проба — МП). При этом регистрировалась допплерограмма, соответствующая третьему сердечному циклу, в стандартной позиции после завершения движений. Перед допплерографическими тестами проводилось измерение артериального давления электронным тонометром. Завершала исследование проба с задержкой ды-
хания на выдохе в течение 20 с, через 5 минут проводилась вторая проба с гипервентиляцией в течение 20 с. Оценивались параметры скорости, резистивно-сти и кинематики потоков в брахиоцефальных и церебральных артериях в покое и во время второго-третьего сердечных циклов по окончании проб. Во всех группах при пробах с апноэ и шпервентиляцией для средней мозговой (СМА), задней мозговой (ЗМА), позвоночной (ПА) и основной (ОА) артерий вычислялись индексы вазодилятации, вазоконстрикции и вазомоторной реактивности по стандартным формулам.
Ультразвуковое исследование с функциональными пробами повторялось через сутки после окончания курса мануальной терапии и вновь, спустя 6-7 месяцев.
После завершения диагностических процедур пациентам основной группы проводилась мягкотканевая мануальная терапия — 6-8 процедур с интервалом 2-4 дня до достижения стойкой ремиссии. В качестве лечебного воздействия использовались растяжение и протяжение, прессура, постизометрическая релаксация, постреципрокная релаксация, сочетание постизометрической релаксации (ПИР) и прессуры. Последовательность применения различных технических приёмов определялась индивидуальной степенью болезненности и функциональных двигательных расстройств. При выраженном болевом синдроме допускался прием анальгезирующих и миорелаксирующих средств, местное применение обезболивающих и противовоспалительных мазей.
Статистическая обработка полученных результатов выполнена при помощи стандартных функций программы “Excel 2007”. Прк оценке количественных признаков использовался критерий Стьюдента с поправкой Бонферрони для множественных сравнений. Различия между сравнщаемыми величинами признавались статистически достоверными при уровне значимости р<0,02.
ПОЛУЧЕННЫЕ РЕЗУЛЬТАТЫ
При неврологическом обследовании лиц из основной группы зарегистрирован ряд патологических феноменов (Табл.1).
Симптомы Количество пациентов (чел,%)
До лечения После лечения Через 6 месяцев
Угнетение рефлексов с рук 7 (14%) 2 (4%) 3 (6%)
Оживление рефлексов с рук 8 (16%) 2 (4%) 4 (8%)
Повышение тонуса шейных мышц 50(100%) 3 (6%) 30 (60%)
Болезненность при пальпации мышц шеи 25 (50%) 0 (0%) 5 (10%)
Гипестезия по типу «полукуртки» 4 (8%) 1 (2%) 1 (2%)
В результате проведенного лечения болевой синдром у всех пациентов был купирован, а количество неврологических симптомов достоверно снизилось (р<0,01). Спустя полгода после завершения курса терапии жалобы на легкую (2-3 балла по ВАШ) эпизодическую боль в шейном отделе позвоночника предъявляли 11 человек, неврологическая симптоматика вновь появилась у 60% больных основной группы.
Мануальное тестирование в контрольной группе выявило единичные функциональные блоки ПДС, а в основной группе — целый спектр болезненных феноменов. Повторное тестирование после завершения курса лечения выявило достоверное улучшение двигательной активности шейных ПДС по показателям объема движений, уменьшения количества триггерных точек и гипертонусов в мышцах шеи, а также по уменьшению количества функциональных блоков. Через полгода после курса лечения существенно возросла частота патологии в мышечно-суставном аппарате шейного отдела позвоночника (Табл.2), однако до уровня, значительно ниже исходного.
и
Феномены мануального тестирования Количество пациентов (чел, %)
До лечения После лечения Через 6 месяцев
Ограничение движений и болезненность при активной ротации головы 50(100%) 0 (0%) 50 (100%)
Ограничение движений и болезненность при пассивной ротации головы 39 (78%) 0 (0%) 39 (78%)
Наличие триггерных точек в мышцах шеи и головы 37 (74%) 2(4%) 37 (74%)
Функциональные блоки ПДС на уровне С0-С1-С2 42 (84%) 2 (4%) 27 (54%)
С2-С3-С4-С5 6 (12%) 0 (0%) 2 (4%)
С5-С6-С7 28 (56%) 1 (2%) 19 (38%)
Гипертонус мышц верхнешейного отдела 50(100%) 2 (4%) 34 (68%)
нижнешейного отдела 50(100%) 1 (2%) 28 (56%)
При рентгенологическом исследовании нарушений статики шейного отдела позвоночника в группе контроля выявлено не было. При этом в основной группе отмечены многочисленные симптомы нарушения статики и динамики шейного отдела позвоночника, проявления остеохондроза (Табл.З).
Рентгенографическая картина через 6 месяцев после курса лечения в основной группе по-прежнему выявляла нарушение статики в виде сглаженности или выпрямления физиологического лордоза, кифозирования или сколиоза (в 6 случаях с ротацией позвонков). Нестабильность одного ПДС подтверждена у 14 пациентов, двух ПДС — у 14 пациентов, а в 22 случаях выявлена нестабильность трех ПДС. Нестабильность сустава Крювелье зарегистрирована у 12 пациентов, симптом фиксации дуги атланта к затылочной кости у 3 пациентов. Степень выраженности остеохондроза за полгода наблюдения не претерпела существенных изменений.
Таблица 3. Рентгенологическое исследование пациентов основной группы (50 чел).
Выявленные изменения Количество пациентов (чел, %)
До лечения Через 6 месяцев
Нарушение статики Выпрямление 28 (56%) 12* (24%)
Локальный кифоз 6 (12%) 3 (6%)
Сколиоз 26 (52%) 18* (36%)
Ротация 8 (16%) 6(12%)
Нестабильность сустава Крювелье 21 (42%) 12* (24%)
Симптом “прилипания” 8 (16%) 3* (6%)
Нестабильность ПДС одного 6(12%) 14* (28%)
двух 16(32%) 14(28%)
трёх 28 (56%) 22 (44%)
Показатель нестабильности <3 мм 22 (44%) 32 (64%)
> 3 мм 28 (56%) 18* (36%)
Проявления остеохондроза 50 (100%) 50(100%)
* — достоверное снижение (р<0,01)
Таким образом, через 6 месяцев после курса мануальной терапии пациенты субъективно чувствовали себя лучше; зарегистрировано увеличение подвижности шейных ПДС, снижение количества мышечных гипертонусов и функциональных блоков, что соответствовало улучшению статики шейного отдела позвоночника и нормализации двигательной активности в области кранио-цервикального перехода.
Количество нестабильных ПДС через полгода после лечения (Рис.1) снизилось недостоверно, однако достоверно уменьшилось количество пациентов с высокой степенью нестабильности шейных сегментов.
Рисунок 1. Динамика количества блокированных шейных ПДС в процессе лечения пациентов основной группы (%).
Ультразвуковая диагностика состояния позвоночных артерий позволила оценить характер асимметрии кровотока в них (Табл.4). Исходно ускоренную ЛСК, также как и ускорение ЛСК после маятниковой пробы (МП), расценивали как проявление ирритации сплетения позвоночной артерии, приводящей к ан-гиоспастической реакции. Снижение линейной скорости кровотока (ЛСК) в позвоночных артериях (ПА), исходное или результирующее, можно объяснить как результат компремирующих экстравазальных влияний. После курса МТ соответственно стабилизации клинической картины зафиксировано двукратное возрастание доли пациентов с симметричным кровотоком в ПА.
Таблица 5. Варианты соотношений ЛСК в ПА пациентов основной группы (50 чел).
Исходные ЛСК Количество (чел,%)
До лечения После лечения Через 6 месяцев
равные, соответствующие возрасту ускоренные относительно возраста сниженные относительно возраста ускорение в одной ПА снижение в одной ПА 16(32%) 8 (16%) 2 (4%) 19 (38%) 5 (10%) 35 (70%) 2 (4%) 1 (2%) 10(20%) 2 (4%) 30 (60%) 4 (8%) 1 (2%) 13 (26%) 2 (4%)
Соотношения ЛСК в ПА при третьем исследовании в основной изучаемой группе не отличались существенно от картины, полученной при втором исследовании, хотя заметна тенденция к снижению доли больных с симметричными потоками в ПА и возрастанию доли больных с ускоренным кровотоком.
Маятниковая проба позволила получить важную информацию о характере взаимоотношений позвонков и ПА (Табл.5). Принималось во внимание изменение ЛСК в ПА после пробы не менее чем на 20% от исходного уровня. После курса МТ изменение ЛСК в ПА в результате МП, превышающее 20%, было отмечено лишь у 10 человек основной группы. Следует отметить, что у этих пациентов также была достигнута клиническая ремиссия.
Таблица 6. Варианты изменения ЛСК в позвоночных артериях после проведения маятниковой пробы пациентам основной группы (50 чел).
Изменение ЛСК Количество (чел, %)
До лечения После лечения Через 6 месяцев
Отсутствие изменений Ускорение в одной ПА Ускорение в двух ПА Снижение в одной ПА Снижение в двух ПА Ускорение в одной ПА и снижение в другой ПА 4 (8%) 6(12%) 6 (12%) 14 (28%) 12 (24%) 7 (14%) 40 (80%) 4 (8%) 3 (6%) 0 (0%) 0 (0%) 3 (6%) 28 (56%) 8 (16%) 2 (4%) 7(14%) 2 (4%) 3 (6%)
Проведение МП через полгода после МТ, несмотря на отсутствие клинических признаков неблагополучия, выявило снижение доли пациентов с отсутствием реакции на повороты головы и возрастание количества лиц с изменением ЛСК в ПА более 20% после пробы (Рис.2).
100%
90%
80%
Рисунок 2, Дина-
60%
40%
30%
20%
10%
0%
70%
50%
Р
мика результатов маятниковой пробы у пациентов основной группы в процессе лечения.
До лечения После Через 6 мес лечения
Разброс ЛСК в брахиоцефальных и интракраниальных артериях внутри групп был достаточно велик, и сравнение их не выявило достоверной разницы между группами, однако различия показателей резистивности потоков в экстра-и интракраниальных сосудах пациентов двух групп носили более определенный характер: зафиксировано достоверное повышение индекса периферического сопротивления (Пурсело) для ПА (экстра- и интракраниально) в основной группе.
Исходные уровни ЛСК в артериях головы и шеи после МТ также существенно не различались между основной и контрольной группами. Не было отмечено достоверного отличия уровней ЛСК первого и второго исследования. При отсутствии достоверной разницы показателей резистивности потоков между основной и контрольной группами, после курса МТ выявлено достоверное снижение индекса Пурсело на 18-23% в ПА и ОА у пациентов основной группы относительно исходных величин.
Через полгода после курса МТ не отмечено достоверных отличий параметров скорости и резистивности мозгового кровотока между группами обследуемых, а также не зарегистрировано существенных различий во всех трех измерениях. Следует отметить, что пациенты основной группы через 6 месяцев после курса лечения находились в состоянии клинической ремиссии.
Интересная информация была получена при сравнении индексов реактивности внутричерепных артерий: вазодилатации (ИД), вазоконстрикции (Ж) и вазомоторной реактивности (ИВМР) в ПА, ОА и ЗМА, а также в основной
интракраниальной ветви каротидной системы — СМА. В СМА существенных различий всех трех показателей не было отмечено, в то же время в ПА, ОА и ЗМА у пациентов основной группы зарегистрировано достоверное повышение Ж, приводящее при сходном уровне ИД к достоверному росту ИВМР в 1,5-1,9 раза в этих сосудах.
После курса МТ выявлено снижение Ж и ИВМР в ПА, ОА и ЗМА у пациентов основной группы, что привело к исчезновению значимых различий между группами. Таким образом, можно сделать вывод, что гемодинамический резерв больных восстановился до физиологического возрастного уровня.
Через полгода после курса МТ показатели реактивности церебральных сосудов, вычисленные на основании измерений, проведенных на фоне ремиссии, не выявили значимой разницы между группами как в ВБС, так и КС. Таким образом, стабильность вазомоторных реакций интракраниальных артерий сохранялась после проведения курса мануальной терапии в течение длительного времени, т.е. церебральный гемодинамический резерв поддерживался у пациентов на физиологическом уровне, что служит одним из доказательств многоплановой эффективности мануальной терапии при лечении болевых синдромов на фоне нестабильности шейных ПДС.
В процессе исследования оценивался не только артериальный, но и венозный кровоток в области головы и шеи; при этом учитывались не только показатели скорости потоков, но и абсолютное количество вен, доступных локации (Табл.6).
Достоверной разницы ЛСК в венах головы и шеи между группами и между тремя исследованиями каждой группы получено не было, однако следует отметить, что количество лоцированных венозных стволов у пациентов основной группы до лечения было существенно выше, чем у лиц контрольной группы (Рис.З). После проведенного лечения количество доступных для локации вен у пациентов резко снизилось, а затем несколько повысилось спустя полгода после курса мануальной терапии. Также отметим, что у 7 пациентов с высокими ЛСК в ВР (18-22 см/с) и в ПВС (20-25 см/с) после курса мануальной терапии
скорости потоков в ВР снизились до нормативных значений (10-12 см/с), а ПВС у всех этих пациентов не поддавалось локации.
Таблица 7. Динамика показателей венозного оттока от головы в процессе курса
лечения цервикокраниалгии.
До лечения После лечения Через 6 месяцев
Осн. группа Контр. группа Осн. группа Контр. группа Осн. группа Контр. группа
ЯВ ЛСК (см/с) 16,7 ±5,7 13,4 ±5,2 13,1 ±4,9 12,6 ±4,8 14,5 ±5,0 13,2 ±5,7
НВ ЛСК (см/с) 13,8 ±3,2 9,8 ±2,9 10,8 ±3,8 11,2 ±3,1 11,9 ±4,3 9,5 ±3,5
Кол-во 46 4 21 3 30 4
ПВС ЛСК (см/с) 16,3 ±4,2 11 13,3 ±4,0 12,2 ±3,2 12,3 ±3,9 10,4 ±3,0
Кол-во 65 1 22 2 30 2
ВР ЛСК (см/с) 15,9 ±4,8 11 ±3,7 12,5 ±4,6 12 ±3,2 13,2 ±4,4 10 ±3.6
Кол-во 72 3 30 3 40 3
СМВ ЛСК (см/с) 15,4 ±4,7 12 12,4 ±4,1 15 12,9 ±4,5 13,4 ±3,8
Кол-во 40 1 18 1 26 2
ЯВ — яремная вена, НВ — надблоковая вена, ПВС — позвоночное венозное спле-
тение, ВР — вена Розенталя, СМВ — средняя мозговая вена.
Рисунок 3. Сравнительная характеристика удельного количества лоцированных венозных стволов (по оси ординат) у пациентов основной группы в процессе лечения и у лиц контрольной группы.
Основная группа
а Контрольная группа
До После Через 6
лечения лечения адес
Широко распространена точка зрения на процесс формирования нестабильности ПДС, как на проявление физиологической компенсации — аутомобилизации с растяжением напряженных мышц и связок, приводящей к повышенной подвижности сегментов, соседствующих с блокированными ПДС и восстановлением общего объема движений шеи. На наш взгляд, развитие нестабильности ПДС, как реакция на патологический процесс блокирования в соседнем сегменте, также является патологическим феноменом.
Следует учитывать, что условия современной жизни требуют длительного поддержания головы в фиксированном положении — учеба в школе, институте, работа за компьютером, вождение автомобиля. Такие нагрузки способствуют ограничению подвижности в верхних и нижних сегментах шейного отдела и избыточной подвижности на среднем уровне.
Вышеизложенное обусловило наш подход к терапии краниоцервикальных болевых синдромов. Помимо общепринятых противовоспалительных и миоре-лаксирующих средств, физиотерапевтических процедур, нам представляется патогенетически обоснованным применение мягкотканевых техник мануальной терапии, так как манипуляции являются более резким, жёстким, иногда травмирующим воздействием. Мягкотканевое воздействие осуществляется не на нестабильные позвоночно-двигательные сегменты со слабым опорным комплексом, а на соседствующие блокированные сегменты с ограничением подвижности.
В основной группе обследованных нами пациентов до начала терапии блоки шейных ПДС, ограничение объема активных движений и мышечные ги-пертонусы выявлялись во всех случаях. После курса МТ лишь у 2 пациентов из 50 сохранялись блоки и локальные мышечные гипертонусы, выраженность которых была существенно ниже, чем до лечения. У остальных 48 пациентов удалось достигнуть полного деблокирования шейных ПДС. Через 6 месяцев после окончания курса терапии’ у двух третей пациентов отмечалось возобновление болевого синдрома в легкой форме, с соответствующим возрастанием числа блокированных сегментов, гипертонусов и ограничением подвижности шейно-
го отдела позвоночника. Это наблюдение согласуется с данными А.Ю.Нефедова (2004) о темпах деблокирования и блокирования шейных ПДС при мануальной терапии.
Функциональное рентгеновское исследование до курса мануальной терапии выявило патологическую подвижность шейных ПДС с показателем нестабильности менее 3 мм у 22 больных основной группы, а с показателем нестабильности 3 мм и более у 28 человек. Повторное рентгенологическое исследование, проведенное через полгода после курса мануальной терапии показало достоверное снижение количества пациентов с показателем нестабильности ПДС более 3 мм — у 18 человек. Также достоверно уменьшилось количество больных с нестабильностью в суставе Крювелье и со сколиозом (преимущественно за счет сколиозов первой степени).
Абсолютные значения ЛСК в экстра- и интракраниальных артериях пациентов основной и контрольной групп не различались достоверно. Также не было зарегистрировано достоверных различий ЛСК у пациентов основной группы до и после лечения. Тем не менее, обращает на себя внимание достоверное повышение индекса периферического сопротивления экстра- и интракранильных сегментов ПА у пациентов основной группы до лечения.
МП при отсутствии патологических влияний на ПА не вызывает изменения ЛСК в них более, чем на 10-15%, в случае же экстравазального воздействия на ПА предлагаемая проба обеспечивает механическое воздействие на одну или обе артерии. Изменение ЛСК и показателей периферического сопротивления артерий после завершения пробы позволяет делать предположение о доминировании определенных патофизиологических механизмов. Повышение ЛСК и периферического сопротивления в ПА после пробы свидетельствует о повышении тонуса сосуда и может быть следствием «раздражающего» действия остеофитов или измененных унковертебральных сустаюв на периартериальное нервное сплетение, особенно при избыточной подзижности в двигательных сегментах шейного уровня. Снижение ЛСК в ПА после МП может указывать на
появившееся или усилившееся во время пробы экстравазальное препятствие кровотоку.
Исследование исходной реактивности церебральных артерий показало достоверное повышение ИК в артериях ВБС относительно показателей группы контроля, что соответствует преобладанию спастических реакций, и связанное с этим достоверное возрастание гемоданамического резерва в ВБС, характеризующего увеличение компенсаторных возможностей артериальной системы, находящейся в «стрессе» экстравазального воздействия.
После курса мануальной терапии у 70% пациентов зарегистрированы симметричные потоки в ПА, отмечено достоверное снижение индекса Пурсело в экстра- и интракраниальных сегментах ПА, а также в ОА по сравнению с исходными показателями. МП у 80% больных не вызвала изменения ЛСК в ПА, что указывает на регресс спастических явлений и повышение стабильности шейных ЦДС: в результате лечения достоверно уменьшилось количество больных с патологическими результатами МП. Не отмечено достоверных различий в ИК и ИВМР пациентов двух групп: оба параметра достоверно снизились у лиц основной группы в ПА, ОА и ЗМА — в большей степени именно в ЗМА.
Через полгода после проведенного лечения у всех пациентов продолжалась клиническая ремиссия. Тем не менее, отмечено снижение доли пациентов с симметричными потоками в ПА до 60%. После МП доля лиц с неизменными ЛСК в ПА также снизилась до 56%. Следует отметить, что несмотря на зарегистрированные признаки ухудшения условий кровотока в системе ПА, ИК и ИВМР оставались на «после терапевтическом» уровне.
Говоря о венозном оттоке от головы, следует отметить двукратное уменьшение количества лоцируемых венозных стволов в основной группе после курса мануальной терапии, что, по-видимому, в большей степени связано с регрессом гипертонусов шейных мышц, оказывающих компрессионное воздействие на поверхностные и глубокие венозные сплетения. Определенные тенденции изменения венозного кровотока по показателю ЛСК с учетом отсутствия достоверных различий между измерениями также были зафиксированы: ЛСК во всех
исследуемых венах непосредственно после курса мануальной терапии снижалась, а спустя шесть месяцев отмечалось повышение ЛСК, не достигающей, однако, исходного уровня.
Таким образом, отношения костных, связочных, мышечных, сосудистых и нервных структур шеи сложны и взаимозависимы. Несмотря на тонкие механизмы обеспечения подвижности шейных сегментов с одновременным сохранением безопасности структур, расположенных внутри и вблизи позвонков, даже начальные стадии блокирования ПДС могут приводить к экстравазальным воздействиям на артерии и вены шеи. Результатом такого воздействия является утяжеление клинической картины заболевания. Интенсивность болевого синдрома не однозначно связана со степенью выраженности циркуляторных расстройств, количеством блоков ПДС и нарушениями статики шейного отдела позвоночника. Однако, характер артериальных и венозных потоков в сосудах шеи, а также варианты их изменений при повторных поворотах головы дают существенную дополнительную информацию о функционировании такого важного и сложного отдела организма, как шея.
В связи с этим необходимо подчеркнуть, что в комплекс диагностических процедур, помимо рентгенологического и ортопедического тестирования, следует включать ультразвуковое исследование кровотока в брахиоцефальных сосудах с проведением маятниковой пробы. Ультразвуковая диагностика наряду с пробой де Клейна позволяет уточнить возможность и объем мануальных приемов, дает дополнительную информацию о патофизиологической картине страдания и возможность контролировать эффективность терапии.
22
ВЫВОДЫ
1. Нестабильность шейных ПДС, сочетающуюся с блокированием смежных сегментов, мышечно-тоническими феноменами и болевым синдромом, сопровождают следующие явления:
— нарушение симметричности потоков в позвоночных артериях и характе-
ра их реагирования на повторные повороты головы;
— повышение индекса периферического сопротивления в экстра- и интра-
краниальных сегментах позвоночных артерий;
— повышение индекса вазоконстрикции и вазомоторной реактивности в
позвоночной, основной и задней мозговой артериях;
— затруднение венозного оттока из полости черепа, проявляющееся рез-
ким увеличением количества лоцируемых венозных стволов.
2. Определенные стато-динамические нарушения в шейных ПДС коррелируют с вариантами сосудистых расстройств:
— блок сегментов Сц-С\ и С1-С2 сочетается с низкими ЛСК в обеих ПА
при отсутствии их реакции на маятниковую пробу;
— нестабильность в сегментах С3-С4 и С4-С5 сочетается с дискордантны-
ми изменениями ЛСК в ПА после маятниковой пробы.
3. Ультразвуковое исследование сосудов шеи и головы, включающее маятниковую и дыхательные пробы, позволяет конкретизировать тип нарушения кровотока в вертебрально-базилярной системе и венах шеи при нестабильности шейных ПДС, а также дает возможность контролировать эффект мануальной терапии в процессе лечения.
4. Мягкотканевые техники мануальной терапии обеспечивают длительный эффект при лечении клинических проявлений нестабильности шейных ПДС, обусловленный коррекцией опорной системы шеи и нарушений кровотока в позвоночных артериях и венах шеи.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
1) При выявлении цервико-краниальных ирритативных феноменов и подозрении на нестабильность шейных ПДС необходимо в алгоритм обследования включать не только функциональное ренгенотрафическое исследование шейного отдела позвоночника, но и ультразвуковую допплерографию шейных и интракраниальных артерий и вен.
2) Допплерографическое исследование артерий и вен шеи должно включать в себя маятниковую пробу (трехкратный поворот головы из стороны в сторону) с регистрацией линейной скорости кровотока и индекса периферического сопротивления в обеих позвоночных артериях до и после пробы.
3) Допплерографическое исследование интракраниальных сосудов должно включать в себя регистрацию кровотока не только артериального, но и венозного; а также проведение дыхательных проб — с задержкой дыхания и с гипервентиляцией — с регистрацией линейной скорости кровотока в задней мозговой артерии до и после проб и с последующим вычислением индекса вазоконстрик-ции.
4) Допплерографическое исследование церебрального кровотока в полном объеме целесообразно проводить при первичной диагностики цервикальной патологии, после курса мануальной терапии и при ухудшении самочувствия пациента в отдаленном периоде.
СПИСОК НАУЧНЫХ РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ
1. Бугровецкая О.Г., Рудковский А.И., Тардса М.В., Аршинов Б.В. Влияние пробы с повторными поворотами головь на кровоток в позвоночных артериях у больных с краниоцервикалгий // Нейродиагностика и высокие биомеханические технологии. 2010. N4 с.31-35.
2. Рудковский А.И., Стулин И.Д., Тар;ов М.В., Бугровецкая О.Г. Клиническое значение пробы с повторным* поворотами головы при допплеро-графическом исследовании кровггока в позвоночных артериях и позво-
ночном венозном сплетении // Мануальная терапия. 2010. — №3(39) с. 39.
3. Рудковский А.И. Изменение кровотока в позвоночных артериях при маятниковой пробе у пациентов с шейными болевыми синдромами // Материалы 32 Итоговой конференции молодых учёных. М., МГМСУ, 2010, с.344.
4. Рудковский А.И., Тардов М.В., Бугровецкая О.Г. Особенности допплеро-графических параметров кровотока в позвоночных артериях при экстра-вазальных воздействиях // Сборник научных трудов. XX юбилейная научно-практическая конференция Всероссийской Ассоциации Мануальной Медицины и Московского Профессионального Объединения мануальных терапевтов. М., 2010 с 47.
5. Рудковский А.И., Тардов М.В., Бугровецкая О.Г. Нарушение кровообращения в вертебро-базиллярной системе: некоторые варианты экстрава-зальных воздействий на позвоночные артерии // Материалы Российской научно-практической конференции. Нарушения мозгового кровообращения, диагностика, профилактика, лечение. Пятигорск. ООО «Издательство Реалтайм», 2010, с. 105.
6. Рудковский А. И., Стулин И. Д., Тардов М. В., Бугровецкая О. Г. Изменения кровотока в позвоночных артериях у больных с цервикалгией после пробы с повторными поворотами головы / Медицина критических состояний; 2010: №5: стр.24-29.
7. Тардов М.В., Бугровецкая О.Г., Рудковский А.И. Нарушения кровотока в позвоночных артерияхпри нестабильности в шейных позвоночных двигательных сегментах / Научное издание «Ангиодоп-2011». Сборник научных трудов международной научной конференции «Нейросонология и церебральная гемодинамика. Актуальные вопросы ангионеврологии. Школа ультразвуковой диагностики.» // Под ред.проф. Вознюка И.А.; СПб.: Изд-во «Альта Астра», ISBN 978-5-905498-03-9:2011.-C.20-24.
Заказ № 386. Объем 1 п.л. Тираж 100 экз.
Отпечатано в ООО «Петроруш». г.Москва, ул.Палиха 2а.тел.(499)250-92-06 www.postator.ru
как выявить с помощью МРТ
Відповідно до Закону України «Про захист населення від інфекційних хвороб», приймаючи до уваги офіційні рекомендації ВООЗ та МОЗ, медичним центром «Юнімед» затверджено план протиепідемічної готовності та тимчасово (на час дії встановленого в Україні карантину) запроваджено особливі Правила внутрішнього розпорядку, які, серед іншого, передбачають наступні заходи та обмеження щодо надання медичних послуг:1. Перебувати на території медичного центру пацієнти/відвідувачі можуть виключно у захисних медичних масках та бахілах (МЦ «Юнімед» забезпечує зазначеними засобами захисту кожного пацієнта/відвідувача на безоплатній основі).
2. Перед входом до медичного центру пацієнти/відвідувачі зобов’язані здійснити дезінфікуючу обробку рук спиртовмісними дезінфікуючими засобами (засоби дезінфекції надаються пацієнтам/відвідувачам МЦ «Юнімед» на безоплатній основі).
3. При наявності ознак хвороби (нежить, кашель, чхання, сльозотеча тощо) у пацієнта/відвідувача, персонал медичного центру має право здійснити вимірювання температури тіла безконтактними інфрачервоними термометрами.
4. Супровід пацієнта безпосередньо до приміщень медичного центру здійснюється іншими особами лише у виключних випадках, коли пацієнт не може самостійно пересуватись та/або пройти діагностику (малолітні/неповнолітні особи, пацієнти у супроводі співробітників реанімації тощо).
5. Персонал медичного центру має право відмовити у доступі до приміщень центру та подальшому веденні пацієнта у випадках, коли на вимогу співробітника медичного центру пацієнт/відвідувач відмовляється дотримуватись заходів, передбачених Правилами внутрішнього розпорядку та/або у разі виявлення підвищеної температури тіла пацієнта/відвідувача більше 37 градусів.
6. Наполегливо рекомендуємо пацієнтам після проходження діагностичної процедури очікувати висновки за межами території медичного центру або використовувати для отримання результатів електронний сервіс «MedOffice» (medoffice.zp.ua).
Невиконання вказаних положень Правил загрожуватиме життю і здоров’ю населення, а отже буде причиною відмови від ведення пацієнта згідно ст. ст. 11, 29 ЗУ «Про захист населення від інфекційних хвороб» та ст. 34 Закону України «Основи законодавства України про охорону здоров’я».
Вертебробазилярная недостаточность — StatPearls — NCBI Bookshelf
Непрерывное обучение
Вертебробазилярная недостаточность (VBI) представляет собой неадекватный кровоток через задний круг кровообращения головного мозга, который снабжается двумя позвоночными артериями, которые сливаются в основную артерию. Вертебробазилярная сосудистая сеть также известна как заднее кровообращение и снабжает такие области, как ствол мозга, таламус, гиппокамп, мозжечок, затылочные и медиальные височные доли.Инсульт может произойти либо из-за окклюзии позвоночной или основной артерии, либо из-за эмбола, расположенного проксимальнее головного мозга. В экстренной ситуации VBI — важный дифференциальный диагноз, который следует учитывать. Его проявления могут иметь общие черты с другими этиологиями, включая лабиринтит, вестибулярный неврит и доброкачественное пароксизмальное позиционное головокружение (ДППГ). В этом упражнении рассматривается оценка и лечение вертебробазилярной недостаточности и подчеркивается роль членов межпрофессиональной команды в сотрудничестве для обеспечения хорошо скоординированной помощи и улучшения результатов для затронутых пациентов.
Цели:
Проанализировать типичные результаты визуализации, связанные с вертебробазилярной недостаточностью.
Обобщите доступные варианты вторичной профилактики вертебробазилярной недостаточности.
Обзор патофизиологии вертебробазилярной недостаточности.
Объясните важность сотрудничества и общения между членами межпрофессиональной группы для обеспечения соблюдения режима лечения, чтобы предотвратить дальнейшие эпизоды и улучшить результаты для пациентов, страдающих вертебробазилярной недостаточностью.
Введение
Вертебробазилярная недостаточность (VBI) определяется недостаточным кровотоком через задний круг кровообращения головного мозга, снабжаемый 2 позвоночными артериями, которые сливаются, образуя базилярную артерию. Вертебробазилярные артерии снабжают мозжечок, продолговатый мозг, средний мозг и затылочную кору. Когда кровоснабжение этих областей нарушено, это может привести к тяжелой инвалидности и / или смерти. Поскольку поражен мозжечок, выжившие часто остаются с дисфункцией многих органов, включая атаксию, гемиплегию, аномалии взгляда, дизартрию, дисфагию и паралич черепных нервов.К счастью, у многих пациентов поражаются мелкие сосуды, поэтому неврологический дефицит бывает легким и локализованным.
Термин VBI был введен в употребление в 1950-х годах после того, как К. Миллер Фишер использовал каротидную недостаточность для описания транзиторных ишемических атак (ТИА) на территориях, снабжаемых сонными артериями, и поэтому часто используется для описания кратких эпизодов транзиторных ишемических атак на вертебробазилярной территории. . Вертебробазилярная сосудистая сеть, также известная как заднее кровообращение, снабжает такие области, как ствол мозга, таламус, гиппокамп, мозжечок, затылочные и медиальные височные доли.Хотя первоначально у пациентов могут быть бессимптомные симптомы, значительное накопление атеросклеротических бляшек со временем может привести к ишемическим событиям. Инсульт может произойти либо из-за окклюзии позвоночной или базилярной артерии, либо из-за эмбола, который может попасть в более проксимальный отдел мозга [1]. В условиях неотложной помощи VBI является важным диагнозом, который следует учитывать, поскольку многие симптомы могут проявляться так же, как и другие доброкачественные этиологии, такие как лабиринтит, вестибулярный неврит и доброкачественное пароксизмальное позиционное головокружение (ДППГ).
Этиология
Определенные факторы риска предрасполагают пациентов к VBI, особенно те, которые обостряют атеросклероз. Эти факторы риска включают курение, гипертонию, возраст, пол, семейный анамнез и генетику, а также гиперлипидемию. Более того, пациенты с ишемической болезнью сердца или заболеванием периферических артерий в анамнезе относятся к группе повышенного риска [2]. Другие этиологические причины могут включать кардиоэмболические состояния, такие как фибрилляция предсердий, инфекционный эндокардит, расслоение позвоночной артерии и состояния системной гиперкоагуляции.
Эпидемиология
Около четверти инсультов и ТИА происходят в вертебробазилярном распределении. Как и атеросклеротическое заболевание, вертебробазилярное заболевание возникает в более позднем возрасте, особенно в возрасте от 7 до 8 лет, с преобладанием мужского пола. У 25% пожилых людей наблюдается нарушение равновесия и повышенный риск падений в результате VBI. Подобно другим типам синдромов инсульта, афроамериканцы более распространены, чем другие этнические группы, из-за множества причин, включая генетику, более высокую распространенность гипертонии и различия в оказании медицинской помощи.
Патофизиология
Как и другие типы инсультов, инфаркт может возникнуть в результате эмболии, тромбоза in situ или лакунарного заболевания, вторичного по отношению к хронической гипертензии. Обычно причиной VBI являются 2 процесса ишемии: гемодинамическая недостаточность и эмболия. В отличие от сонных артерий, эмболия позвоночных артерий встречается нечасто. Донорские участки эмболии могут включать дугу аорты, начало позвоночной артерии или проксимальные подключичные артерии. Однако в большинстве случаев это связано с атеросклеротическим заболеванием.
Гемодинамика
Снижение перфузии вызывает большую часть VBI. Гемодинамическая ишемия возникает из-за недостаточного кровотока через базилярную артерию, особенно у пожилых людей и пациентов с диабетом с плохим симпатическим контролем. Симптомы обычно воспроизводимы и непродолжительны, редко вызывая инфаркт. Для возникновения гемодинамической ишемии должна быть окклюзия обеих позвоночных артерий или базилярной артерии. Кроме того, должен быть неполный вклад сонной артерии через заднюю соединительную артерию в Виллизиевом круге.Другие причины снижения перфузии включают антигипертензивные препараты, сердечную аритмию, нарушение работы кардиостимулятора и васкулит. Таким образом, абсолютно необходимо провести полное обследование, включая ЭКГ, чтобы исключить кардиогенные причины. Окклюзии в других кровеносных сосудах, такие как синдром подключичного обкрадывания, также могут вызывать VBI, «украшая» кровоток из ствола мозга, когда кровь течет по пути наименьшего сопротивления через позвоночную артерию при наличии проксимального стеноза / окклюзии подключичной артерии.
Эмболия
VBI также может происходить из атеросклеротических бляшек, которые позже отламываются, образуя эмболы. Тем не менее, эмболы могут также развиться в результате дефектов интимы, вторичных по отношению к травме, сдавлению, и в редких случаях из-за фиброзно-мышечной дисплазии, аневризмы или расслоения. Возможно, до одной трети случаев происходит внутричерепно, так как дистальные эмболы образуются из поражений подключичной, позвоночной или базилярной артерии. Большинство поражений, которые образуются экстракраниально, возникают из-за накопления атеросклероза в одной из позвоночных артерий и редко в безымянной или подключичной артериях.В очень небольшом количестве случаев тромбы могут возникать из эктатической или веретенообразной аневризмы основной артерии, которая затем может эмболизировать более дистальные ветви [3] [4] [5].
Токсикокинетика
Дифференциация VBI от полушарного инсульта
Поражения в результате VBI имеют определенные клинические особенности, которые позволяют дифференцировать их от полушарных инсультов:
Общие признаки дисметрии, такие как атаксия и атаксия
Если поражен черепной нерв, клинические признаки обычно ипсилатеральные по отношению к поражению, а кортикоспинальные клинические особенности видны на противоположной ноге и руке из-за перекрещивания.
Дисфагия и дизартрия часто встречаются при VBI
При поражении ствола головного мозга может присутствовать односторонний синдром Горнера
Тошнота, головокружение, нистагм и рвота обычны при поражении вестибулярной системы
Вовлечение затылочной доли приводит к зрительно-пространственным дефектам или дефектам поля зренияВ целом когнитивные нарушения и афазия (корковые дефициты) отсутствуют
Анамнез и физика
Наиболее частые находки в анамнезе пациента, позволяющие предположить, что VBI включают факторы риска сердечно-сосудистых заболеваний, таких как атеросклероз и пожилой возраст.Следует провести тщательный сбор анамнеза и медицинский осмотр, уделяя особое внимание не только неврологическому, но и кардиологическому обследованию на предмет таких состояний, как аритмия, которые также могут вызывать симптомы. Симптомы VBI являются результатом ишемии различных частей мозга, снабжаемых задним кровообращением.
Симптомы включают:
Головокружение (наиболее частый симптом)
Головокружение / обморок: 60% пациентов с VBI имеют по крайней мере 1 эпизод головокружения.
«Приступы падения:» Пациент внезапно почувствовал слабость в коленях и упал
Диплопия / потеря зрения
Парестезия
Путаница
Дисфагия / дизартрия
000 900Измененное сознание
Атаксия
Контралатеральная двигательная слабость
Снижение температуры и боли
Недержание мочи
Если VBI переходит в инфаркт ствола мозга, может возникнуть несколько синдромов. локализация, такая как латеральный медуллярный синдром, медиальный медуллярный синдром, синдром базилярной артерии и окклюзия лабиринтной артерии.Другими аспектами анамнеза, которые следует отметить во время физического осмотра, являются воспроизводимые симптомы при смене положения головы, то есть обморок при повороте головы в сторону (синдром Боу-Хантера) или во время разгибания головы [6] [7] [8].
Физический осмотр
Результаты являются обычными после инсульта позвоночной артерии и могут включать следующее:
Изменение уровня сознания
Гемипарез
Изменение размера зрачка и реактивности
Черепной нерв параличи (обычно паралич отводящего нерва)
Покачивание глаз
Паралич вертикального взгляда (поражение CN lll)
Паралич горизонтального взгляда (поражение CN 6
Паралич лицевого нерва
05
паралич лицевого нерва дизартрия, дисфония, дисфагия, дизартрия, слабость лица)Контратральгемианопия с сохранением желтого пятна (поражение задней мозговой артерии)
Ипсилатеральная потеря температуры и лицевая боль, синдром Хорнера (часть медуллярного синдрома)
быть приняты, чтобы исключить другие более доброкачественные c состояния, которые также могут вызывать аналогичные симптомы, такие как лабиринтит, вестибулярный неврит и доброкачественное пароксизмальное позиционное головокружение (ДППГ).Головокружение — частый симптом VBI. Это также центральный симптом более доброкачественных периферических вестибулярных расстройств. В отделении неотложной помощи особенно важно различать головокружение, вызванное периферическими вестибулярными нарушениями, и центральными вестибулярными проблемами, чаще всего связанными с вертебробазилярной недостаточностью (VBI), которые могут потребовать госпитализации. Головокружение само по себе не может быть диагностировано как ТИА или ВБИ. Головокружение при наличии признаков или симптомов ствола мозга является диагностическим признаком ТИА вертебробазилярной территории.Очень важно физикальное обследование для выявления признаков ствола мозга или аномалий черепных нервов. Полезно наличие признаков или симптомов контралатеральной конечности. Тип нистагма, такой как вертикальный нистагм или нистагм с изменением направления, указывает на VBI. Если выполнить и правильно интерпретировать тест с выталкиванием головы, можно отличить периферическое головокружение от центрального головокружения из-за VBI у постели больного. Положительный тест на толчок головой указывает на периферическую причину головокружения.
Инсульт позвоночной артерии связан с множеством синдромов в зависимости от клинических проявлений.Некоторые из этих синдромов включают:
Синдром блокировки
Боковой медуллярный синдром
Межъядерная офтальмоплегия
Инфаркт мозжечка
05
Синдром задней мозговой артерииДвусторонний значимый стеноз VA, то есть стеноз более 60% В ОБЕИХ артериях. Или стеноз доминирующей позвоночной артерии (VA) превышает 60%, если контралатераль гипопластична, заканчивается задней нижней мозжечковой артерией (PICA) или окклюзирована.
Симптоматическая эмболия, предположительно возникшая из-за поражения позвонка
Симптоматическое восстановление аневризмы или если аневризма больше 1.На 5 см вне зависимости от симптомов.
Тромбоз глубоких вен
Аспирационная пневмония
MI
Тромбоэмболия легочной артерии
Пролежни
9002Исходящее состояние
Гастритис
управляется межпрофессиональной командой, в которую входят врач отделения неотложной помощи, невролог, радиолог, терапевт и специалист по инсульту.Большинство пациентов становятся инвалидами, а выздоровление выживших может занять годы.
В то время как окончательное лечение проводится под наблюдением невролога, лечащий врач и практикующая медсестра должны обучать пациентов предотвращению дальнейших эпизодов. После инсульта позвоночной артерии у большинства пациентов наблюдается значительная инвалидность, и выздоровление затягивается. Этим пациентам требуется обширная реабилитация для улучшения речи, глотания и походки. Кроме того, необходимо решить многие проблемы медсестер, включая тренировку кишечника и мочевого пузыря, питание, безопасность пациентов, профилактику пролежней и выполнение повседневной жизнедеятельности.
Кроме того, пациенты часто впадают в депрессию, и настоятельно рекомендуется проконсультироваться с медсестрой по психическому здоровью.
Пациенту следует отговаривать от курения, соблюдать режим приема лекарств, поддерживать здоровый вес, следить за уровнем холестерина и регулярно заниматься физическими упражнениями. Из-за риска повторного инсульта наблюдение крайне важно. Тем, кто продолжает принимать варфарин, необходимо регулярно проверять МНО.
Речевая терапия, трудотерапия и физиотерапия являются неотъемлемой частью лечения, и большинству пациентов требуется обширная реабилитация в течение многих месяцев.Медсестра по уходу на дому часто необходима, чтобы следить за выздоровлением и прогрессом пациента. Вся команда должна общаться, чтобы гарантировать, что пациент получает оптимальную медицинскую помощь.
Результаты для пациентов с вертебробазилярной недостаточностью зависят от тяжести инсульта, возраста, сопутствующей патологии и степени неврологического дефицита.
Повышение квалификации / обзорные вопросы
Рисунок
Анатомия позвоночной артерии. Изображение любезно предоставлено О. Чайгасаме
Рисунок
Подача позвоночной артерии.Предоставлено доктором Йоханнесом Соботта, (общественное достояние; https://commons.wikimedia.org/wiki/File:Sobo_1909_3_548.png)
Ссылки
- 1.
- Caplan L, Chung CS, Wityk R, Glass T , Тапиа Дж., Паздера Л., Чанг Х.М., Даше Дж., Чавес К., Веммос К., Лири М., Девитт Л., Пессин М. Регистр заднего кровообращения в медицинском центре Новой Англии в Новой Англии: I. Методы, база данных, распределение поражений головного мозга, инсульт механизмы и результаты. J Clin Neurol. 2005 Апрель; 1 (1): 14-30. [Бесплатная статья PMC: PMC2854928] [PubMed: 20396469]
- 2.
- Lima Neto AC, Bittar R, Gattas GS, Bor-Seng-Shu E, Oliveira ML, Monsanto RDC, Bittar LF. Патофизиология и диагностика вертебробазилярной недостаточности: обзор литературы. Int Arch Otorhinolaryngol. 2017 июл; 21 (3): 302-307. [Бесплатная статья PMC: PMC5495592] [PubMed: 28680502]
- 3.
- Наджафи М.Р., Тогхианифар Н., Абдар Исфахани М., Наджафи М.А., Моллакучакян М.Дж. Долихоэктазия в вертебробазилярных артериях, представленная как транзиторные ишемические атаки: отчет о клиническом случае. ARYA Atheroscler.2016 Янв; 12 (1): 55-8. [Бесплатная статья PMC: PMC4834182] [PubMed: 27114738]
- 4.
- Yuh SJ, Alkherayf F, Lesiuk H. Долихоэктазия позвоночных базилярных и внутренних сонных артерий: отчет о клиническом случае и обзор литературы. Surg Neurol Int. 2013; 4: 153. [Бесплатная статья PMC: PMC3872646] [PubMed: 24381796]
- 5.
- Lou M, Caplan LR. Вертебробазилярная дилатативная артериопатия (долихоэктазия). Ann N Y Acad Sci. 2010 Янв; 1184: 121-33. [PubMed: 20146694]
- 6.
- Go G, Hwang SH, Park IS, Park H.Ротационная компрессия позвоночной артерии: синдром охотника за луком. J Korean Neurosurg Soc. 2013 сентябрь; 54 (3): 243-5. [Бесплатная статья PMC: PMC3836934] [PubMed: 24278656]
- 7.
- Ян YJ, Chien YY, Cheng WC. Вертебробазилярная недостаточность, связанная с шейным спондилезом. Отчет о болезни и обзор литературы. Чангэн И Сюэ За Чжи. 1992 июн; 15 (2): 100-4. [PubMed: 1515970]
- 8.
- Buch VP, Madsen PJ, Vaughan KA, Koch PF, Kung DK, Ozturk AK. Ротационная вертебробазилярная недостаточность из-за компрессии стойкого варианта первой межсегментарной позвоночной артерии: клинический случай.J Neurosurg Spine. 2017 Февраль; 26 (2): 199-202. [PubMed: 27716015]
- 9.
- Paşaolu L. Компьютерная томографическая ангиография вертебробазилярной системы при центральном головокружении. Медицина (Балтимор). 2017 Март; 96 (12): e6297. [Бесплатная статья PMC: PMC5371445] [PubMed: 28328808]
- 10.
- Caplan LR. Атеросклеротическое заболевание позвоночной артерии шеи. Варианты лечения Curr Cardiovasc Med. 2003 июл; 5 (3): 251-256. [PubMed: 12777203]
- 11.
- Compter A, van der Worp HB, Schonewille WJ, Vos JA, Boiten J, Nederkoorn PJ, Uyttenboogaart M, Lo RT, Algra A, Kappelle LJ., Исследователи VAST. Стентирование по сравнению с медикаментозным лечением у пациентов с симптоматическим стенозом позвоночной артерии: рандомизированное открытое исследование фазы 2. Lancet Neurol. 2015 июн; 14 (6): 606-14. [PubMed: 25
9]
- 12.
- Коджак Б., Коркмазер Б., Ислак С., Кочер Н., Кизилкилыч О. Эндоваскулярное лечение стеноза экстракраниальной позвоночной артерии. Мир J Radiol. 2012 Сентябрь 28; 4 (9): 391-400. [Бесплатная статья PMC: PMC3460226] [PubMed: 23024840]
- 13.
- Рахеджа А., Таусский П., Кумпати Г.С., Кулдвелл В.Т.Шунтирование подключичной к экстракраниальной позвоночной артерии у пациента с вертебробазилярной недостаточностью: трехмерное операционное видео. Oper Neurosurg (Хагерстаун). 01 марта 2018; 14 (3): 312. [PubMed: 28973539]
- 14.
- Генри М., Полидору А., Генри I, Ад Полидору И., Хюгель И.М., Анагностопулу С. Ангиопластика и стентирование стеноза экстракраниальной позвоночной артерии. Int Angiol. 2005 декабрь; 24 (4): 311-24. [PubMed: 16355087]
Вертебробазилярная недостаточность — StatPearls — Книжная полка NCBI
Непрерывное обучение
Вертебробазилярная недостаточность (VBI) представляет собой неадекватный кровоток через задний круг кровообращения головного мозга, который обеспечивается двумя сливающимися артериями. образуют базилярную артерию.Вертебробазилярная сосудистая сеть также известна как заднее кровообращение и снабжает такие области, как ствол мозга, таламус, гиппокамп, мозжечок, затылочные и медиальные височные доли. Инсульт может произойти либо из-за окклюзии позвоночной или основной артерии, либо из-за эмбола, расположенного проксимальнее головного мозга. В экстренной ситуации VBI — важный дифференциальный диагноз, который следует учитывать. Его проявления могут иметь общие черты с другими этиологиями, включая лабиринтит, вестибулярный неврит и доброкачественное пароксизмальное позиционное головокружение (ДППГ).В этом упражнении рассматривается оценка и лечение вертебробазилярной недостаточности и подчеркивается роль членов межпрофессиональной команды в сотрудничестве для обеспечения хорошо скоординированной помощи и улучшения результатов для затронутых пациентов.
Цели:
Проанализировать типичные результаты визуализации, связанные с вертебробазилярной недостаточностью.
Обобщите доступные варианты вторичной профилактики вертебробазилярной недостаточности.
Обзор патофизиологии вертебробазилярной недостаточности.
Объясните важность сотрудничества и общения между членами межпрофессиональной группы для обеспечения соблюдения режима лечения, чтобы предотвратить дальнейшие эпизоды и улучшить результаты для пациентов, страдающих вертебробазилярной недостаточностью.
Введение
Вертебробазилярная недостаточность (VBI) определяется недостаточным кровотоком через задний круг кровообращения головного мозга, снабжаемый 2 позвоночными артериями, которые сливаются, образуя базилярную артерию.Вертебробазилярные артерии снабжают мозжечок, продолговатый мозг, средний мозг и затылочную кору. Когда кровоснабжение этих областей нарушено, это может привести к тяжелой инвалидности и / или смерти. Поскольку поражен мозжечок, выжившие часто остаются с дисфункцией многих органов, включая атаксию, гемиплегию, аномалии взгляда, дизартрию, дисфагию и паралич черепных нервов. К счастью, у многих пациентов поражаются мелкие сосуды, поэтому неврологический дефицит бывает легким и локализованным.
Термин VBI был введен в употребление в 1950-х годах после того, как К. Миллер Фишер использовал каротидную недостаточность для описания транзиторных ишемических атак (ТИА) на территориях, снабжаемых сонными артериями, и поэтому часто используется для описания кратких эпизодов транзиторных ишемических атак на вертебробазилярной территории. . Вертебробазилярная сосудистая сеть, также известная как заднее кровообращение, снабжает такие области, как ствол мозга, таламус, гиппокамп, мозжечок, затылочные и медиальные височные доли. Хотя первоначально у пациентов могут быть бессимптомные симптомы, значительное накопление атеросклеротических бляшек со временем может привести к ишемическим событиям.Инсульт может произойти либо из-за окклюзии позвоночной или базилярной артерии, либо из-за эмбола, который может попасть в более проксимальный отдел мозга [1]. В условиях неотложной помощи VBI является важным диагнозом, который следует учитывать, поскольку многие симптомы могут проявляться так же, как и другие доброкачественные этиологии, такие как лабиринтит, вестибулярный неврит и доброкачественное пароксизмальное позиционное головокружение (ДППГ).
Этиология
Определенные факторы риска предрасполагают пациентов к VBI, особенно те, которые обостряют атеросклероз. Эти факторы риска включают курение, гипертонию, возраст, пол, семейный анамнез и генетику, а также гиперлипидемию.Более того, пациенты с ишемической болезнью сердца или заболеванием периферических артерий в анамнезе относятся к группе повышенного риска [2]. Другие этиологические причины могут включать кардиоэмболические состояния, такие как фибрилляция предсердий, инфекционный эндокардит, расслоение позвоночной артерии и состояния системной гиперкоагуляции.
Эпидемиология
Около четверти инсультов и ТИА происходят в вертебробазилярном распределении. Как и атеросклеротическое заболевание, вертебробазилярное заболевание возникает в более позднем возрасте, особенно в возрасте от 7 до 8 лет, с преобладанием мужского пола.У 25% пожилых людей наблюдается нарушение равновесия и повышенный риск падений в результате VBI. Подобно другим типам синдромов инсульта, афроамериканцы более распространены, чем другие этнические группы, из-за множества причин, включая генетику, более высокую распространенность гипертонии и различия в оказании медицинской помощи.
Патофизиология
Как и другие типы инсультов, инфаркт может возникнуть в результате эмболии, тромбоза in situ или лакунарного заболевания, вторичного по отношению к хронической гипертензии.Обычно причиной VBI являются 2 процесса ишемии: гемодинамическая недостаточность и эмболия. В отличие от сонных артерий, эмболия позвоночных артерий встречается нечасто. Донорские участки эмболии могут включать дугу аорты, начало позвоночной артерии или проксимальные подключичные артерии. Однако в большинстве случаев это связано с атеросклеротическим заболеванием.
Гемодинамика
Снижение перфузии вызывает большую часть VBI. Гемодинамическая ишемия возникает из-за недостаточного кровотока через базилярную артерию, особенно у пожилых людей и пациентов с диабетом с плохим симпатическим контролем.Симптомы обычно воспроизводимы и непродолжительны, редко вызывая инфаркт. Для возникновения гемодинамической ишемии должна быть окклюзия обеих позвоночных артерий или базилярной артерии. Кроме того, должен быть неполный вклад сонной артерии через заднюю соединительную артерию в Виллизиевом круге. Другие причины снижения перфузии включают антигипертензивные препараты, сердечную аритмию, нарушение работы кардиостимулятора и васкулит. Таким образом, абсолютно необходимо провести полное обследование, включая ЭКГ, чтобы исключить кардиогенные причины.Окклюзии в других кровеносных сосудах, такие как синдром подключичного обкрадывания, также могут вызывать VBI, «украшая» кровоток из ствола мозга, когда кровь течет по пути наименьшего сопротивления через позвоночную артерию при наличии проксимального стеноза / окклюзии подключичной артерии.
Эмболия
VBI также может происходить из атеросклеротических бляшек, которые позже отламываются, образуя эмболы. Тем не менее, эмболы могут также развиться в результате дефектов интимы, вторичных по отношению к травме, сдавлению, и в редких случаях из-за фиброзно-мышечной дисплазии, аневризмы или расслоения.Возможно, до одной трети случаев происходит внутричерепно, так как дистальные эмболы образуются из поражений подключичной, позвоночной или базилярной артерии. Большинство поражений, которые образуются экстракраниально, возникают из-за накопления атеросклероза в одной из позвоночных артерий и редко в безымянной или подключичной артериях. В очень небольшом количестве случаев тромбы могут возникать из эктатической или веретенообразной аневризмы основной артерии, которая затем может эмболизировать более дистальные ветви [3] [4] [5].
Токсикокинетика
Дифференциация VBI от полушарного инсульта
Поражения в результате VBI имеют определенные клинические особенности, которые позволяют дифференцировать их от полушарных инсультов:
Общие признаки дисметрии, такие как атаксия и атаксия
Если поражен черепной нерв, клинические признаки обычно ипсилатеральные по отношению к поражению, а кортикоспинальные клинические особенности видны на противоположной ноге и руке из-за перекрещивания.
Дисфагия и дизартрия часто встречаются при VBI
При поражении ствола головного мозга может присутствовать односторонний синдром Горнера
Тошнота, головокружение, нистагм и рвота обычны при поражении вестибулярной системы
Вовлечение затылочной доли приводит к зрительно-пространственным дефектам или дефектам поля зрения
В целом когнитивные нарушения и афазия (корковые дефициты) отсутствуют
Головокружение (наиболее частый симптом)
Головокружение / обморок: 60% пациентов с VBI имеют по крайней мере 1 эпизод головокружения.
«Приступы падения:» Пациент внезапно почувствовал слабость в коленях и упал
Диплопия / потеря зрения
Парестезия
Путаница
Дисфагия / дизартрия
000 900Измененное сознание
Атаксия
Контралатеральная двигательная слабость
Снижение температуры и боли
Недержание мочи
Изменение уровня сознания
Гемипарез
Изменение размера зрачка и реактивности
Черепной нерв параличи (обычно паралич отводящего нерва)
Покачивание глаз
Паралич вертикального взгляда (поражение CN lll)
Паралич горизонтального взгляда (поражение CN 6
Паралич лицевого нерва
05
паралич лицевого нерва дизартрия, дисфония, дисфагия, дизартрия, слабость лица)Контратральгемианопия с сохранением желтого пятна (поражение задней мозговой артерии)
Ипсилатеральная потеря температуры и лицевая боль, синдром Хорнера (часть медуллярного синдрома)
Синдром блокировки
Боковой медуллярный синдром
Межъядерная офтальмоплегия
Инфаркт мозжечка
05
Синдром задней мозговой артерииДвусторонний значимый стеноз VA, то есть стеноз более 60% В ОБЕИХ артериях. Или стеноз доминирующей позвоночной артерии (VA) превышает 60%, если контралатераль гипопластична, заканчивается задней нижней мозжечковой артерией (PICA) или окклюзирована.
Симптоматическая эмболия, предположительно возникшая из-за поражения позвонка
Симптоматическое восстановление аневризмы или если аневризма больше 1.На 5 см вне зависимости от симптомов.
Тромбоз глубоких вен
Аспирационная пневмония
MI
Тромбоэмболия легочной артерии
Пролежни
9002Исходящее состояние
Гастритис
управляется межпрофессиональной командой, в которую входят врач отделения неотложной помощи, невролог, радиолог, терапевт и специалист по инсульту.Большинство пациентов становятся инвалидами, а выздоровление выживших может занять годы.
В то время как окончательное лечение проводится под наблюдением невролога, лечащий врач и практикующая медсестра должны обучать пациентов предотвращению дальнейших эпизодов. После инсульта позвоночной артерии у большинства пациентов наблюдается значительная инвалидность, и выздоровление затягивается. Этим пациентам требуется обширная реабилитация для улучшения речи, глотания и походки. Кроме того, необходимо решить многие проблемы медсестер, включая тренировку кишечника и мочевого пузыря, питание, безопасность пациентов, профилактику пролежней и выполнение повседневной жизнедеятельности.
Кроме того, пациенты часто впадают в депрессию, и настоятельно рекомендуется проконсультироваться с медсестрой по психическому здоровью.
Пациенту следует отговаривать от курения, соблюдать режим приема лекарств, поддерживать здоровый вес, следить за уровнем холестерина и регулярно заниматься физическими упражнениями. Из-за риска повторного инсульта наблюдение крайне важно. Тем, кто продолжает принимать варфарин, необходимо регулярно проверять МНО.
Речевая терапия, трудотерапия и физиотерапия являются неотъемлемой частью лечения, и большинству пациентов требуется обширная реабилитация в течение многих месяцев.Медсестра по уходу на дому часто необходима, чтобы следить за выздоровлением и прогрессом пациента. Вся команда должна общаться, чтобы гарантировать, что пациент получает оптимальную медицинскую помощь.
Результаты для пациентов с вертебробазилярной недостаточностью зависят от тяжести инсульта, возраста, сопутствующей патологии и степени неврологического дефицита.
Повышение квалификации / обзорные вопросы
Рисунок
Анатомия позвоночной артерии. Изображение любезно предоставлено О. Чайгасаме
Рисунок
Подача позвоночной артерии.Предоставлено доктором Йоханнесом Соботта, (общественное достояние; https://commons.wikimedia.org/wiki/File:Sobo_1909_3_548.png)
Ссылки
- 1.
- Caplan L, Chung CS, Wityk R, Glass T , Тапиа Дж., Паздера Л., Чанг Х.М., Даше Дж., Чавес К., Веммос К., Лири М., Девитт Л., Пессин М. Регистр заднего кровообращения в медицинском центре Новой Англии в Новой Англии: I. Методы, база данных, распределение поражений головного мозга, инсульт механизмы и результаты. J Clin Neurol. 2005 Апрель; 1 (1): 14-30. [Бесплатная статья PMC: PMC2854928] [PubMed: 20396469]
- 2.
- Lima Neto AC, Bittar R, Gattas GS, Bor-Seng-Shu E, Oliveira ML, Monsanto RDC, Bittar LF. Патофизиология и диагностика вертебробазилярной недостаточности: обзор литературы. Int Arch Otorhinolaryngol. 2017 июл; 21 (3): 302-307. [Бесплатная статья PMC: PMC5495592] [PubMed: 28680502]
- 3.
- Наджафи М.Р., Тогхианифар Н., Абдар Исфахани М., Наджафи М.А., Моллакучакян М.Дж. Долихоэктазия в вертебробазилярных артериях, представленная как транзиторные ишемические атаки: отчет о клиническом случае. ARYA Atheroscler.2016 Янв; 12 (1): 55-8. [Бесплатная статья PMC: PMC4834182] [PubMed: 27114738]
- 4.
- Yuh SJ, Alkherayf F, Lesiuk H. Долихоэктазия позвоночных базилярных и внутренних сонных артерий: отчет о клиническом случае и обзор литературы. Surg Neurol Int. 2013; 4: 153. [Бесплатная статья PMC: PMC3872646] [PubMed: 24381796]
- 5.
- Lou M, Caplan LR. Вертебробазилярная дилатативная артериопатия (долихоэктазия). Ann N Y Acad Sci. 2010 Янв; 1184: 121-33. [PubMed: 20146694]
- 6.
- Go G, Hwang SH, Park IS, Park H.Ротационная компрессия позвоночной артерии: синдром охотника за луком. J Korean Neurosurg Soc. 2013 сентябрь; 54 (3): 243-5. [Бесплатная статья PMC: PMC3836934] [PubMed: 24278656]
- 7.
- Ян YJ, Chien YY, Cheng WC. Вертебробазилярная недостаточность, связанная с шейным спондилезом. Отчет о болезни и обзор литературы. Чангэн И Сюэ За Чжи. 1992 июн; 15 (2): 100-4. [PubMed: 1515970]
- 8.
- Buch VP, Madsen PJ, Vaughan KA, Koch PF, Kung DK, Ozturk AK. Ротационная вертебробазилярная недостаточность из-за компрессии стойкого варианта первой межсегментарной позвоночной артерии: клинический случай.J Neurosurg Spine. 2017 Февраль; 26 (2): 199-202. [PubMed: 27716015]
- 9.
- Paşaolu L. Компьютерная томографическая ангиография вертебробазилярной системы при центральном головокружении. Медицина (Балтимор). 2017 Март; 96 (12): e6297. [Бесплатная статья PMC: PMC5371445] [PubMed: 28328808]
- 10.
- Caplan LR. Атеросклеротическое заболевание позвоночной артерии шеи. Варианты лечения Curr Cardiovasc Med. 2003 июл; 5 (3): 251-256. [PubMed: 12777203]
- 11.
- Compter A, van der Worp HB, Schonewille WJ, Vos JA, Boiten J, Nederkoorn PJ, Uyttenboogaart M, Lo RT, Algra A, Kappelle LJ., Исследователи VAST. Стентирование по сравнению с медикаментозным лечением у пациентов с симптоматическим стенозом позвоночной артерии: рандомизированное открытое исследование фазы 2. Lancet Neurol. 2015 июн; 14 (6): 606-14. [PubMed: 25
9]
- 12.
- Коджак Б., Коркмазер Б., Ислак С., Кочер Н., Кизилкилыч О. Эндоваскулярное лечение стеноза экстракраниальной позвоночной артерии. Мир J Radiol. 2012 Сентябрь 28; 4 (9): 391-400. [Бесплатная статья PMC: PMC3460226] [PubMed: 23024840]
- 13.
- Рахеджа А., Таусский П., Кумпати Г.С., Кулдвелл В.Т.Шунтирование подключичной к экстракраниальной позвоночной артерии у пациента с вертебробазилярной недостаточностью: трехмерное операционное видео. Oper Neurosurg (Хагерстаун). 01 марта 2018; 14 (3): 312. [PubMed: 28973539]
- 14.
- Генри М., Полидору А., Генри I, Ад Полидору И., Хюгель И.М., Анагностопулу С. Ангиопластика и стентирование стеноза экстракраниальной позвоночной артерии. Int Angiol. 2005 декабрь; 24 (4): 311-24. [PubMed: 16355087]
Вертебробазилярная недостаточность — StatPearls — Книжная полка NCBI
Непрерывное обучение
Вертебробазилярная недостаточность (VBI) представляет собой неадекватный кровоток через задний круг кровообращения головного мозга, который обеспечивается двумя сливающимися артериями. образуют базилярную артерию.Вертебробазилярная сосудистая сеть также известна как заднее кровообращение и снабжает такие области, как ствол мозга, таламус, гиппокамп, мозжечок, затылочные и медиальные височные доли. Инсульт может произойти либо из-за окклюзии позвоночной или основной артерии, либо из-за эмбола, расположенного проксимальнее головного мозга. В экстренной ситуации VBI — важный дифференциальный диагноз, который следует учитывать. Его проявления могут иметь общие черты с другими этиологиями, включая лабиринтит, вестибулярный неврит и доброкачественное пароксизмальное позиционное головокружение (ДППГ).В этом упражнении рассматривается оценка и лечение вертебробазилярной недостаточности и подчеркивается роль членов межпрофессиональной команды в сотрудничестве для обеспечения хорошо скоординированной помощи и улучшения результатов для затронутых пациентов.
Цели:
Проанализировать типичные результаты визуализации, связанные с вертебробазилярной недостаточностью.
Обобщите доступные варианты вторичной профилактики вертебробазилярной недостаточности.
Обзор патофизиологии вертебробазилярной недостаточности.
Объясните важность сотрудничества и общения между членами межпрофессиональной группы для обеспечения соблюдения режима лечения, чтобы предотвратить дальнейшие эпизоды и улучшить результаты для пациентов, страдающих вертебробазилярной недостаточностью.
Введение
Вертебробазилярная недостаточность (VBI) определяется недостаточным кровотоком через задний круг кровообращения головного мозга, снабжаемый 2 позвоночными артериями, которые сливаются, образуя базилярную артерию.Вертебробазилярные артерии снабжают мозжечок, продолговатый мозг, средний мозг и затылочную кору. Когда кровоснабжение этих областей нарушено, это может привести к тяжелой инвалидности и / или смерти. Поскольку поражен мозжечок, выжившие часто остаются с дисфункцией многих органов, включая атаксию, гемиплегию, аномалии взгляда, дизартрию, дисфагию и паралич черепных нервов. К счастью, у многих пациентов поражаются мелкие сосуды, поэтому неврологический дефицит бывает легким и локализованным.
Термин VBI был введен в употребление в 1950-х годах после того, как К. Миллер Фишер использовал каротидную недостаточность для описания транзиторных ишемических атак (ТИА) на территориях, снабжаемых сонными артериями, и поэтому часто используется для описания кратких эпизодов транзиторных ишемических атак на вертебробазилярной территории. . Вертебробазилярная сосудистая сеть, также известная как заднее кровообращение, снабжает такие области, как ствол мозга, таламус, гиппокамп, мозжечок, затылочные и медиальные височные доли. Хотя первоначально у пациентов могут быть бессимптомные симптомы, значительное накопление атеросклеротических бляшек со временем может привести к ишемическим событиям.Инсульт может произойти либо из-за окклюзии позвоночной или базилярной артерии, либо из-за эмбола, который может попасть в более проксимальный отдел мозга [1]. В условиях неотложной помощи VBI является важным диагнозом, который следует учитывать, поскольку многие симптомы могут проявляться так же, как и другие доброкачественные этиологии, такие как лабиринтит, вестибулярный неврит и доброкачественное пароксизмальное позиционное головокружение (ДППГ).
Этиология
Определенные факторы риска предрасполагают пациентов к VBI, особенно те, которые обостряют атеросклероз. Эти факторы риска включают курение, гипертонию, возраст, пол, семейный анамнез и генетику, а также гиперлипидемию.Более того, пациенты с ишемической болезнью сердца или заболеванием периферических артерий в анамнезе относятся к группе повышенного риска [2]. Другие этиологические причины могут включать кардиоэмболические состояния, такие как фибрилляция предсердий, инфекционный эндокардит, расслоение позвоночной артерии и состояния системной гиперкоагуляции.
Эпидемиология
Около четверти инсультов и ТИА происходят в вертебробазилярном распределении. Как и атеросклеротическое заболевание, вертебробазилярное заболевание возникает в более позднем возрасте, особенно в возрасте от 7 до 8 лет, с преобладанием мужского пола.У 25% пожилых людей наблюдается нарушение равновесия и повышенный риск падений в результате VBI. Подобно другим типам синдромов инсульта, афроамериканцы более распространены, чем другие этнические группы, из-за множества причин, включая генетику, более высокую распространенность гипертонии и различия в оказании медицинской помощи.
Патофизиология
Как и другие типы инсультов, инфаркт может возникнуть в результате эмболии, тромбоза in situ или лакунарного заболевания, вторичного по отношению к хронической гипертензии.Обычно причиной VBI являются 2 процесса ишемии: гемодинамическая недостаточность и эмболия. В отличие от сонных артерий, эмболия позвоночных артерий встречается нечасто. Донорские участки эмболии могут включать дугу аорты, начало позвоночной артерии или проксимальные подключичные артерии. Однако в большинстве случаев это связано с атеросклеротическим заболеванием.
Гемодинамика
Снижение перфузии вызывает большую часть VBI. Гемодинамическая ишемия возникает из-за недостаточного кровотока через базилярную артерию, особенно у пожилых людей и пациентов с диабетом с плохим симпатическим контролем.Симптомы обычно воспроизводимы и непродолжительны, редко вызывая инфаркт. Для возникновения гемодинамической ишемии должна быть окклюзия обеих позвоночных артерий или базилярной артерии. Кроме того, должен быть неполный вклад сонной артерии через заднюю соединительную артерию в Виллизиевом круге. Другие причины снижения перфузии включают антигипертензивные препараты, сердечную аритмию, нарушение работы кардиостимулятора и васкулит. Таким образом, абсолютно необходимо провести полное обследование, включая ЭКГ, чтобы исключить кардиогенные причины.Окклюзии в других кровеносных сосудах, такие как синдром подключичного обкрадывания, также могут вызывать VBI, «украшая» кровоток из ствола мозга, когда кровь течет по пути наименьшего сопротивления через позвоночную артерию при наличии проксимального стеноза / окклюзии подключичной артерии.
Эмболия
VBI также может происходить из атеросклеротических бляшек, которые позже отламываются, образуя эмболы. Тем не менее, эмболы могут также развиться в результате дефектов интимы, вторичных по отношению к травме, сдавлению, и в редких случаях из-за фиброзно-мышечной дисплазии, аневризмы или расслоения.Возможно, до одной трети случаев происходит внутричерепно, так как дистальные эмболы образуются из поражений подключичной, позвоночной или базилярной артерии. Большинство поражений, которые образуются экстракраниально, возникают из-за накопления атеросклероза в одной из позвоночных артерий и редко в безымянной или подключичной артериях. В очень небольшом количестве случаев тромбы могут возникать из эктатической или веретенообразной аневризмы основной артерии, которая затем может эмболизировать более дистальные ветви [3] [4] [5].
Токсикокинетика
Дифференциация VBI от полушарного инсульта
Поражения в результате VBI имеют определенные клинические особенности, которые позволяют дифференцировать их от полушарных инсультов:
Общие признаки дисметрии, такие как атаксия и атаксия
Если поражен черепной нерв, клинические признаки обычно ипсилатеральные по отношению к поражению, а кортикоспинальные клинические особенности видны на противоположной ноге и руке из-за перекрещивания.
Дисфагия и дизартрия часто встречаются при VBI
При поражении ствола головного мозга может присутствовать односторонний синдром Горнера
Тошнота, головокружение, нистагм и рвота обычны при поражении вестибулярной системы
Вовлечение затылочной доли приводит к зрительно-пространственным дефектам или дефектам поля зрения
В целом когнитивные нарушения и афазия (корковые дефициты) отсутствуют
Головокружение (наиболее частый симптом)
Головокружение / обморок: 60% пациентов с VBI имеют по крайней мере 1 эпизод головокружения.
«Приступы падения:» Пациент внезапно почувствовал слабость в коленях и упал
Диплопия / потеря зрения
Парестезия
Путаница
Дисфагия / дизартрия
000 900Измененное сознание
Атаксия
Контралатеральная двигательная слабость
Снижение температуры и боли
Недержание мочи
Изменение уровня сознания
Гемипарез
Изменение размера зрачка и реактивности
Черепной нерв параличи (обычно паралич отводящего нерва)
Покачивание глаз
Паралич вертикального взгляда (поражение CN lll)
Паралич горизонтального взгляда (поражение CN 6
Паралич лицевого нерва
05
паралич лицевого нерва дизартрия, дисфония, дисфагия, дизартрия, слабость лица)Контратральгемианопия с сохранением желтого пятна (поражение задней мозговой артерии)
Ипсилатеральная потеря температуры и лицевая боль, синдром Хорнера (часть медуллярного синдрома)
Синдром блокировки
Боковой медуллярный синдром
Межъядерная офтальмоплегия
Инфаркт мозжечка
05
Синдром задней мозговой артерииДвусторонний значимый стеноз VA, то есть стеноз более 60% В ОБЕИХ артериях. Или стеноз доминирующей позвоночной артерии (VA) превышает 60%, если контралатераль гипопластична, заканчивается задней нижней мозжечковой артерией (PICA) или окклюзирована.
Симптоматическая эмболия, предположительно возникшая из-за поражения позвонка
Симптоматическое восстановление аневризмы или если аневризма больше 1.На 5 см вне зависимости от симптомов.
Тромбоз глубоких вен
Аспирационная пневмония
MI
Тромбоэмболия легочной артерии
Пролежни
9002Исходящее состояние
Гастритис
управляется межпрофессиональной командой, в которую входят врач отделения неотложной помощи, невролог, радиолог, терапевт и специалист по инсульту.Большинство пациентов становятся инвалидами, а выздоровление выживших может занять годы.
В то время как окончательное лечение проводится под наблюдением невролога, лечащий врач и практикующая медсестра должны обучать пациентов предотвращению дальнейших эпизодов. После инсульта позвоночной артерии у большинства пациентов наблюдается значительная инвалидность, и выздоровление затягивается. Этим пациентам требуется обширная реабилитация для улучшения речи, глотания и походки. Кроме того, необходимо решить многие проблемы медсестер, включая тренировку кишечника и мочевого пузыря, питание, безопасность пациентов, профилактику пролежней и выполнение повседневной жизнедеятельности.
Кроме того, пациенты часто впадают в депрессию, и настоятельно рекомендуется проконсультироваться с медсестрой по психическому здоровью.
Пациенту следует отговаривать от курения, соблюдать режим приема лекарств, поддерживать здоровый вес, следить за уровнем холестерина и регулярно заниматься физическими упражнениями. Из-за риска повторного инсульта наблюдение крайне важно. Тем, кто продолжает принимать варфарин, необходимо регулярно проверять МНО.
Речевая терапия, трудотерапия и физиотерапия являются неотъемлемой частью лечения, и большинству пациентов требуется обширная реабилитация в течение многих месяцев.Медсестра по уходу на дому часто необходима, чтобы следить за выздоровлением и прогрессом пациента. Вся команда должна общаться, чтобы гарантировать, что пациент получает оптимальную медицинскую помощь.
Результаты для пациентов с вертебробазилярной недостаточностью зависят от тяжести инсульта, возраста, сопутствующей патологии и степени неврологического дефицита.
Повышение квалификации / обзорные вопросы
Рисунок
Анатомия позвоночной артерии. Изображение любезно предоставлено О. Чайгасаме
Рисунок
Подача позвоночной артерии.Предоставлено доктором Йоханнесом Соботта, (общественное достояние; https://commons.wikimedia.org/wiki/File:Sobo_1909_3_548.png)
Ссылки
- 1.
- Caplan L, Chung CS, Wityk R, Glass T , Тапиа Дж., Паздера Л., Чанг Х.М., Даше Дж., Чавес К., Веммос К., Лири М., Девитт Л., Пессин М. Регистр заднего кровообращения в медицинском центре Новой Англии в Новой Англии: I. Методы, база данных, распределение поражений головного мозга, инсульт механизмы и результаты. J Clin Neurol. 2005 Апрель; 1 (1): 14-30. [Бесплатная статья PMC: PMC2854928] [PubMed: 20396469]
- 2.
- Lima Neto AC, Bittar R, Gattas GS, Bor-Seng-Shu E, Oliveira ML, Monsanto RDC, Bittar LF. Патофизиология и диагностика вертебробазилярной недостаточности: обзор литературы. Int Arch Otorhinolaryngol. 2017 июл; 21 (3): 302-307. [Бесплатная статья PMC: PMC5495592] [PubMed: 28680502]
- 3.
- Наджафи М.Р., Тогхианифар Н., Абдар Исфахани М., Наджафи М.А., Моллакучакян М.Дж. Долихоэктазия в вертебробазилярных артериях, представленная как транзиторные ишемические атаки: отчет о клиническом случае. ARYA Atheroscler.2016 Янв; 12 (1): 55-8. [Бесплатная статья PMC: PMC4834182] [PubMed: 27114738]
- 4.
- Yuh SJ, Alkherayf F, Lesiuk H. Долихоэктазия позвоночных базилярных и внутренних сонных артерий: отчет о клиническом случае и обзор литературы. Surg Neurol Int. 2013; 4: 153. [Бесплатная статья PMC: PMC3872646] [PubMed: 24381796]
- 5.
- Lou M, Caplan LR. Вертебробазилярная дилатативная артериопатия (долихоэктазия). Ann N Y Acad Sci. 2010 Янв; 1184: 121-33. [PubMed: 20146694]
- 6.
- Go G, Hwang SH, Park IS, Park H.Ротационная компрессия позвоночной артерии: синдром охотника за луком. J Korean Neurosurg Soc. 2013 сентябрь; 54 (3): 243-5. [Бесплатная статья PMC: PMC3836934] [PubMed: 24278656]
- 7.
- Ян YJ, Chien YY, Cheng WC. Вертебробазилярная недостаточность, связанная с шейным спондилезом. Отчет о болезни и обзор литературы. Чангэн И Сюэ За Чжи. 1992 июн; 15 (2): 100-4. [PubMed: 1515970]
- 8.
- Buch VP, Madsen PJ, Vaughan KA, Koch PF, Kung DK, Ozturk AK. Ротационная вертебробазилярная недостаточность из-за компрессии стойкого варианта первой межсегментарной позвоночной артерии: клинический случай.J Neurosurg Spine. 2017 Февраль; 26 (2): 199-202. [PubMed: 27716015]
- 9.
- Paşaolu L. Компьютерная томографическая ангиография вертебробазилярной системы при центральном головокружении. Медицина (Балтимор). 2017 Март; 96 (12): e6297. [Бесплатная статья PMC: PMC5371445] [PubMed: 28328808]
- 10.
- Caplan LR. Атеросклеротическое заболевание позвоночной артерии шеи. Варианты лечения Curr Cardiovasc Med. 2003 июл; 5 (3): 251-256. [PubMed: 12777203]
- 11.
- Compter A, van der Worp HB, Schonewille WJ, Vos JA, Boiten J, Nederkoorn PJ, Uyttenboogaart M, Lo RT, Algra A, Kappelle LJ., Исследователи VAST. Стентирование по сравнению с медикаментозным лечением у пациентов с симптоматическим стенозом позвоночной артерии: рандомизированное открытое исследование фазы 2. Lancet Neurol. 2015 июн; 14 (6): 606-14. [PubMed: 25
9]
- 12.
- Коджак Б., Коркмазер Б., Ислак С., Кочер Н., Кизилкилыч О. Эндоваскулярное лечение стеноза экстракраниальной позвоночной артерии. Мир J Radiol. 2012 Сентябрь 28; 4 (9): 391-400. [Бесплатная статья PMC: PMC3460226] [PubMed: 23024840]
- 13.
- Рахеджа А., Таусский П., Кумпати Г.С., Кулдвелл В.Т.Шунтирование подключичной к экстракраниальной позвоночной артерии у пациента с вертебробазилярной недостаточностью: трехмерное операционное видео. Oper Neurosurg (Хагерстаун). 01 марта 2018; 14 (3): 312. [PubMed: 28973539]
- 14.
- Генри М., Полидору А., Генри I, Ад Полидору И., Хюгель И.М., Анагностопулу С. Ангиопластика и стентирование стеноза экстракраниальной позвоночной артерии. Int Angiol. 2005 декабрь; 24 (4): 311-24. [PubMed: 16355087]
Лечение вертебробазилярной недостаточности, недостаточности вертебробазилярной артерии, синдрома окклюзии ротационной позвоночной артерии или синдрома Боу-Хантера
Росс Хаузер, Мэриленд
Вертебробазилярная недостаточность — синдром Боу Хантера — нестабильность шейного отдела шеи.Каждый раз, когда я поворачиваю голову, у меня кружится голова. Иногда я почти теряю сознание.
Сложность и проблемы лечения нестабильности шейки матки в полной мере проявляются в спорах и недоразумениях, связанных с диагностикой вертебробазилярной недостаточности, также называемой недостаточностью вертебробазилярной артерии, синдромом окклюзии ротационной позвоночной артерии или синдромом Боу-Хантера. Тот факт, что этот один диагноз или описание симптомов известны как минимум под четырьмя диагностическими названиями, должен быть достаточным доказательством того, что пациенты и их врачи иногда не уверены, с чем они имеют дело.
Как пациент, у которого диагностирован один из этих диагностических тегов, вы, вероятно, не понаслышке знаете, что ваш путь лечения прошел много поворотов. Некоторые верны, некоторые нет, но поскольку вы читаете эту статью, ваш путь исцеления, вероятно, далек от завершения.
Когда пациент приходит в наш центр, мы садимся с ним и начинаем обсуждать его симптомы, лечение и их историю болезни вплоть до этого момента в нашем кабинете для осмотра. Посмотрим, звучит ли это знакомо.
Каждый раз, когда я поворачиваю голову, у меня кружится голова. Иногда я почти теряю сознание
- Многие пациенты говорят нам, что они наконец обратились за медицинской помощью, потому что после длительного периода симптомов, в том числе иногда или каждый раз, когда он / она поворачивает голову, у них головокружение, головокружение, и иногда им приходилось хвататься за что-то, потому что они казалось, что они упадут в обморок.
Нечеткое, нечеткое зрение, звон в ушах и нарушение постурального баланса
- Во время этих эпизодов у пациента также будет нечеткое, нечеткое зрение, , звон в ушах, и проблемы с постуральным равновесием , даже при ходьбе.В более продвинутых ситуациях и, безусловно, более пугающим для этого пациента является «атака падения», когда он внезапно и, казалось бы, без всякой причины упадет на землю, а затем встанет, как будто ничего не произошло, через несколько секунд. Конечно, для этого пациента «как будто ничего не произошло» — это не то, что происходит в их голове. Большое беспокойство вызывает.
Когда они пошли к своему лечащему врачу, говорит нам пациент, врач начал подозревать, что у них, у пациента, была какая-то закупорка крови в мозгу.
- В процессе исключения врач начал смотреть на атеросклероз или затвердение артерий. Эта проблема может быть заподозрена у пациентов старшего возраста, страдающих диабетом, высоким кровяным давлением или гипертонией, курящих, страдающих ожирением или ведущих очень плохой образ жизни, лишенный активности или физических упражнений. Скорее всего, если бы вы были в этой группе риска, вы бы получили направление к сосудистому хирургу, чтобы он мог осмотреться. Однако эта группа пациентов может страдать как атеросклерозом, так и вертебробазилярной недостаточностью.В этой группе пациентов с помощью компрессии вращения шеи не потребуется много усилий, чтобы перекрыть приток крови к мозгу в артериях, которые закупорены изнутри. Здесь хирурги могут срочно рекомендовать операцию по декомпрессии.
А что, если бы у вас не было высокого кровяного давления, диабета и не было избыточного веса? Тогда диагностика становится еще более сложной.
Давайте остановимся на этом, чтобы объяснить некоторые моменты. Возможно, вы уже проводили собственное исследование, поскольку мы обнаружили, что люди, страдающие от симптомов, подобных указанным выше, много читали в Интернете.Мы сделаем краткое резюме и видео-презентацию с Россом Хаузером, доктором медицины.
Головокружение, проблемы с равновесием и колебания артериального давления могут быть вызваны нестабильностью верхнего отдела шейки матки
Краткие обучающие моменты этого видео
- Многие люди страдают необъяснимым головокружением, проблемами с равновесием, колебаниями артериального давления, аритмией, учащенным сердцебиением ИЛИ их пульс может быть очень низким.
- Они ходят к кардиологу или нескольким кардиологам и другим врачам, и никто, кажется, не знает причины их проблем с сердцем.
- Мы обнаружили, что во многих из этих случаев человек страдает нестабильностью шейки матки, особенно верхней шейки матки.
- Чувствительные нервы, которые сообщают мозгу, что происходит от момента к моменту, в отношении частоты сердечных сокращений и артериального давления, переносятся блуждающим нервом и языкоглоточным нервом. Если сообщения, которые эти сенсорные нервы должны передавать в мозг, заблокированы или нарушены, могут развиться описанные сердечные симптомы.
- Для получения дополнительной информации по этому вопросу см. Нашу статью Может ли нестабильность шейного отдела позвоночника вызвать учащенное сердцебиение и проблемы с артериальным давлением?
Каждый раз, когда пациент поворачивал голову, у него был риск инсульта.Никто не знал почему. «Поэтому пациентам с инфарктом заднего кровообращения неизвестного происхождения рекомендуется тщательное обследование позвоночных артерий с врачами, обращающими особое внимание на уровень атлантоаксиального сустава».
Врачи отделения неврологии больницы Китано Медицинского исследовательского института Тадзуке Кофукай, Япония, сообщили о болезни 61-летнего мужчины, перенесшего повторный инсульт. У этого мужчины была «невидимая» проблема нестабильности шейного отдела шеи, которая сдавливала его артерии.Вот краткое изложение этого случая, опубликованное в журнале Internal Medicine . ( 1 )
Проблема сжатия между C1-C2
- Позвоночные артерии уязвимы для механического напряжения между атлантом и осью, и последующее расслоение позвоночной артерии может вызвать инфаркт заднего кровообращения (заблокированный, сжатый кровоток в затылке).
- В данном случае у пациента были двусторонние аневризмы позвоночных артерий, которые стали причиной повторного инсульта.
Его врачи не увидели очевидной причины закупорки кровотока, но заподозрили, что это компрессия в области C1-C2. Инсульты прекратились после того, как пациенту установили шейный воротник
- Локализация аневризм и динамическая ангиография с движением шеи позволили предположить, что инсульты были связаны с хроническим механическим повреждением позвоночных артерий, хотя патологии скелета обнаружено не было. Рецидивы прекратились, и обе аневризмы уменьшились после фиксации шейного воротника и после комбинированного применения антитромботических средств (антикоагулянтов).Поэтому пациентам с инфарктом заднего кровообращения неизвестного происхождения рекомендуется тщательное обследование позвоночных артерий с врачами, обращающими особое внимание на уровень атлантоаксиального сустава.
При стабилизации шеи шейным воротником аневризмы уменьшились, повторяющиеся инсульты прекратились
Некоторые ключевые комментарии:
- В шее пациента не было ничего очевидного, что указывало бы на анатомическую травму шеи. Нестабильности шейного отдела шеи пациента не наблюдалось.
- Обнаружена проблема с изображениями, связанными с движением шеи. Когда он повернул шею, динамическая ангиография зафиксировала сдавление артерий. См. Наше обсуждение DMX ниже. Digital Motion X-Ray — это рентгеновский фильм, который мы используем, чтобы наблюдать эти типы «невидимых» сжатий во время движения.
- Когда шея была стабилизирована шейным воротником, аневризмы уменьшились, повторяющиеся инсульты прекратились.
Простая обработка шейного воротника
У нас есть обширная статья Шейные ошейники — почему одним людям они помогают, а другим нет? В этой статье мы обсуждаем использование шейного воротника или шейного вытяжения в попытке облегчить симптомы пациента, растягивая позвонки, чтобы уменьшить давление и боль в нервах, которые пересекают шейные позвонки.Для многих пациентов это облегчит симптомы. Для некоторых пациентов шейный воротник может вызвать больше проблем, чем он был предназначен для помощи.
Что мы видим на этом изображении?
Изображение ниже демонстрирует три части того, как шейный ортез может помочь при нестабильности шейного отдела позвоночника. Пациентке делают Digital Motion X-ray (DMX), чтобы мы могли наблюдать за движением ее шеи.
- В первой части пациентка упирается подбородком в грудь, на ней нет ошейника.DMX выявляет крайнюю гипермобильность при сгибании шейки матки
- Во второй части пациентка пытается упереться подбородком в грудь, при этом она носит шейный воротник. DMX фиксирует снижение гипермобильности шейного отдела позвоночника примерно на 50%.
- В третьей части пациенту дают более поддерживающий ошейник. При ношении воротника нестабильность шейки матки практически устраняется. Подчеркнем, что ошейник — это не лекарство, а средство подавления симптомов.
Мне сказали идти домой и не поворачивать голову.
Кто-нибудь расскажет нам историю, которая выглядит примерно так. Однажды, обычный день, как и любой другой, они вставали с постели и читали, чтобы приступить к своей физически сложной работе. Внезапно, вставая, они страдали от сильного головокружения и падали обратно на кровать, они лежали на кровати почти до состояния паралича, почти обездвиженные. К тому времени, как они смогли вызвать медицинскую помощь, начались тошнота и рвота.В реанимации сделали КТ, МРТ, МРА. Лечащие врачи вернулись к ним и сказали, что «все в норме». Один специалист-ортопед прокомментировал тяжелый дегенеративный артрит и костные шпоры в точках C1-c2. В качестве запоздалого решения дегенеративное заболевание диска также было отмечено в C4-C7, C4-C5 или C5-C6.
Все, казалось, ломали голову над тем, что вызвало это «супер головокружение». Человек из этой истории сказал, что у него не было ни головной боли, ни боли до события.Ничего не складывалось. На консультации невролога удалось подтвердить компрессию позвоночной артерии. В этот момент человек, рассказавший историю, сказал, что они получили свой первый «действительно хороший» медицинский совет. Им сказали идти домой и не поворачивать головы.
Затем они получили совет, что, поскольку тот, кто выполняет тяжелую физическую работу и может иметь собственный бизнес, не хочет слышать, ортопед и нейрохирург предложат план операции по сращению шейки матки.Они будут отсутствовать на работе на несколько месяцев.
«В настоящее время известны различные виды головокружения, вызванные движением шеи».
История болезни за ноябрь 2020 г., опубликованная в BioMed Central Neurology ( 2 ), посвящена проблемам со зрением, связанным с нистагмом. У нас есть более подробная статья об этом состоянии здесь: Нистагм — осциллопсия, вызванная нестабильностью шейного отдела позвоночника и болью в шее .
В данной истории болезни лечащие врачи отметили:
«Синдром охотника за луком (BHS) известен как одно из заболеваний шейки матки, вызывающее головокружение, но детали его головокружения, особенно нистагм и движение глаз, все еще не полностью изучены.
Пациентка, 47 лет, обратилась с жалобами на головокружение, вызванное поворотом головы.
Когда она повернула голову влево, появился левосторонний нистагм, за которым последовала тупость правой руки.
После того, как ее голова была возвращена в центральное положение, появился мускулистый нистагм (глаза поднимаются вверх, а затем предпринимаются корректирующие действия, чтобы снова опустить их), который сменился правым нистагмом. По симптомам и изображениям ей поставили диагноз BHS.Головокружение было вылечено изменением рецепта, сделанного в ее прошлой истории болезни: гипертонией.
Заключение: «Головокружение при синдроме охотника за луком сопровождает нистагм. В данном случае наблюдался переходный нистагм в сторону здоровой стороны. Затем направление нистагма было изменено на пораженную сторону с помощью нистагма сильного удара. . . В настоящее время известны различные виды головокружения, вызванные движением шеи. Синдром Боу-Хантера — редкое заболевание среди головокружений, но мы должны рассматривать его как другой диагноз для пациентов с головокружением.Для постановки окончательного диагноза необходимы точное собеседование и надлежащее обследование ».
В этой истории болезни врачи сосредоточили свое внимание на гипертонии. В нашем центре мы уделяем особое внимание шейному отделу позвоночника как средоточию множества симптомов, от которых могут страдать пациенты. У многих людей причиной симптомов является слабость связок шейного отдела позвоночника. Прочные соединительные ленты удерживают шейный отдел позвоночника на месте.
Аномальные костные структуры или развитие костной шпоры
Как уже отмечалось, и как мы будем постоянно видеть в медицинских исследованиях, поворот головы из стороны в сторону может имитировать симптомы у пациента с диагнозом синдрома ротационной окклюзии позвоночной артерии.
В статье в журнале Interventional Neurology ( 3 ) описана роль аномальных костных структур и развивающихся костных шпор.
«Синдром охотника за луком, также известный как синдром окклюзии ротационной позвоночной артерии, является редким, но поддающимся лечению типом симптоматической вертебробазилярной недостаточности, возникающей в результате механической окклюзии или стеноза позвоночной артерии во время вращения или разгибания головы и шеи. Симптомы синдрома Лоу-Хантера варьируются от преходящего головокружения до инсульта заднего кровообращения.Основной патологией является динамический стеноз или сдавление позвоночной артерии аномальными костными структурами с вращением или разгибанием шеи во многих случаях, такими как остеофит (костная шпора), грыжа диска (нестабильность шейного отдела позвоночника), шейный спондилез (более нестабильность шейного отдела позвоночника), сухожильные связки (сухожилия шеи слабые и снижают способность мышц шейного отдела позвоночника приводить к движению) или опухоли ».
Больной 19 лет. Все было нормально, только он потерял сознание.
Многие люди приходят в наш центр и задают вопрос, который звучит примерно так: «Почему никто другой не считал нестабильность шейки матки проблемой?» На самом деле, нестабильность шейки матки часто признается проблемой, но, когда мы начали эту статью, когда симптом или состояние могут определяться как минимум четырьмя разными диагностическими метками, возникает путаница.
Для нас также важно отметить, что мы не единственный центр, который это видит. Однако мы являемся центром, который решает эти проблемы без хирургического вмешательства.
Давайте посмотрим на историю болезни, представленную в журнале Radiology Case Reports , ( 4 ), опубликованном в ноябре 2020 года. Случай представлен с нашими пояснительными примечаниями: В этом случае мы сначала перейдем к заключению: «Bow Hunter’s синдром следует дифференцировать от шейного спондилеза позвоночной артерии и ишемического инсульта. У них есть похожие симптомы, такие как головокружение, нарушение сознания, , которые легко спутать клинически ». Теперь дело:
«20 марта 2019 года 19-летний студент мужского пола после уборки в классе испытал головокружение примерно через полчаса после того, как поднял глаза, сопровождавшееся вращением визуальных объектов, бинокулярной чернотой и нарушением сознания, но без тошноты. , рвота или шум в ушах.
В местной больнице не было обнаружено явных отклонений от нормы на МРТ головы, шейного и поясничного отделов позвоночника. В это время пациент чувствовал головокружение при ходьбе и нормальное состояние, когда сидел или лежал. Пациент не подтвердил травм черепно-мозгового и шейного отделов в анамнезе.
. . . Пациенту выполнено обследование методом динамической компьютерной томографической ангиографии (КТА) головы и шеи. Динамическая компьютерная томография головы и шеи показала, что когда пациент находится в нейтральном положении, двусторонняя позвоночная артерия (видна) хорошо, а правая позвоночная артерия тоньше левой.Пациенту было предложено повернуться на 90 ° влево, где виртуальная реальность и мультипланарная реконструкция (высокое разрешение изображения) позвоночной артерии показали локальное прерывание кровотока верхнего края уровня C2 правой позвоночной артерии и контралатерального позвоночная артерия развита хорошо.
Пациенту было приказано повернуть голову на 90 ° вправо, после чего реконструкция MPR позвоночной артерии и искривленной поверхности показала локальное прерывание кровотока верхнего края левой позвоночной артерии на уровне C2, и контралатеральная позвоночная артерия развивалась хорошо. Пациенты прошли другие лабораторные исследования и получили симптоматическое лечение, такое как улучшение кровообращения и защита мозга ».
В этом случае динамическая компьютерная томографическая ангиография использовалась для обнаружения проблем с вращением, а для облегчения симптомов у пациента использовались методы лечения и лекарства. Ниже при лечении пациентов того же типа мы также используем различные методы тестирования, но, поскольку я объясню наши методы лечения, они связаны с лечением нестабильности шейки матки, которая позволяет костям шеи сдавливать вены и артерии.
«Синдром охотника за луком: зловещая причина головокружения и обморока, которую нельзя упускать» Обнаружена слабость связок
Выше название медицинской статьи от апреля 2020 г. ( 5 ). Он поступает из отделения радиологии больницы принцессы Маргарет, Гонконг. Послушайте, что сказали эти исследователи:
Патогенез синдрома охотника за луком связан с извилистым анатомическим курсом позвоночной артерии вдоль шейного отдела позвоночника, который делает артерию чувствительной к внешнему сжатию, повторяющемуся сдвиговому напряжению, приводящему к гемодинамическим (потере кровотока) событиям у пациентов из группы риска. при вращении головы и шеи.Остеофиты (костные шпоры), грыжа межпозвоночного диска, связочная гипертрофия (слабость связок) или шейная мышца являются факторами риска синдрома охотника за луками.
Хотя синдром Охотника за луками встречается редко, его нельзя упускать из виду из-за его специфической связи с поворотом головы и шеи и потенциального риска ишемического инсульта в задней части кровообращения. .
Синдром охотника с луком чаще встречается у мужчин и людей в возрасте от 50 до 70 лет. Общие клинические проявления включают головокружение и обморок (обморок).Другие симптомы включают нистагм (проблемы со зрением), рвоту (рвоту) , синдром Хорнера (расширение зрачка , опущенное веко ) и, в редких случаях, моторный и сенсорный дефицит.
Визуализация (диагностика) имеет решающее значение для постановки диагноза синдрома Боу Хантера, определения причины и места внешнего сжатия и оценки таких осложнений, как инфаркт.
У девочки 12 лет был инсульт, и во время операции по сращению шейки матки наблюдалась патологическая дряблость связок.
В исследовании, проведенном в июне 2020 года в журнале Journal of Children’s Neurology ( 6 ), исследователи из отдела детской неврологии факультета неврологии Медицинской школы Университета Индианы проанализировали медицинскую литературу и отметили: позвоночная артерия с поворотом головы, приводящим к ишемии, а иногда и инсульту, редко описывается у детей ».
Авторы рассмотрели литературу и представили новый случай.
Основные моменты исследования:
- Было найдено 12 статей (медицинских исследований) с описанием 25 пациентов; в сочетании с нашим случаем было 26 пациентов.
- Возраст от 1 до 18 лет. Большинство (88,5%, 23/26) составляли мужчины.
- Лечебные процедуры включали аспирин, клопидогрель, абциксимаб, эноксапарин, варфарин и шейный воротник.
- Стентирование использовалось в 2 случаях, но длительное время не помогло.
- Хирургическое лечение включало декомпрессию, артродез шейки матки или их комбинацию. Мы представляем новый случай 12-летней девочки с рецидивирующим инсультом, у которой была двусторонняя компрессия сосудов, видимая только на провокационной ангиографии с поворотом головы.Она была направлена на сращение шейки матки, и аномальную слабость связок во время операции .
Некоторым детям может потребоваться операция. Для некоторых детей мы считаем, что можем решить проблему ненормальной дряблости связок с помощью нехирургических методов лечения, как мы описываем ниже.
Что-то давит на ваши позвоночные артерии — ротационная окклюзия позвоночной артерии
Эта статья будет сосредоточена на одном аспекте вертебробазилярной недостаточности, которая возникает при повороте головы (окклюзия ротационной позвоночной артерии), вызванном нестабильностью шейного отдела шеи.Вертебробазилярная недостаточность может быть вызвана многими причинами, как описано выше, среди которых преобладает атеросклероз. Эта статья предназначена для пациентов, которые были проверены на атеросклероз и все еще ищут ответы. Ответ, который мы представим, — это исправление нестабильности шейного отдела шеи путем укрепления шейных связок и прикрепления сухожилий и восстановления естественного изгиба шеи.
Декомпрессионная хирургия
Ваш путь к исправлению симптомов, вероятно, привел вас к новому пониманию медицинских терминов и медицинских специальностей.Возможно, вы прошли отоларингологическое обследование у специалиста по уху, носу и горлу. Возможно, вы обсуждали возможные решения с отоларингологом или хирургом. Вы начинаете часто слышать слово «декомпрессия». Декомпрессия означает операцию по удалению части шейных позвонков для предотвращения компрессии или чего-либо, давящего на позвоночную артерию в «точке удара».
Это то, что вы знаете или должны знать.
Позвоночные артерии снабжают мозг 20% кровотока через базилярную артерию.Вертебробазилярная недостаточность возникает при нарушении кровотока. Как только серьезный атеросклероз исключен как непосредственный риск инсульта, врачи должны изучить лежащую в основе нестабильность верхнего отдела шейки матки. Это, конечно, наше мнение. Мы собираемся перейти к исследованию ниже.
Позвоночные артерии проходят вверх через шейные позвонки (по одному с каждой стороны) через отверстия (или «отверстия») в костном выступе, называемом поперечным отростком позвонков.
Что мы видим на следующем изображении?
На этой иллюстрации ясно видна позвоночная артерия, проходящая через C1-C2.Если C1-C2 движутся и гипермобильны, они могут давить и сдавливать позвоночную артерию. Это может вызвать ощущение головокружения и обморока. Это видно на рентгеновском снимке ниже.
Что мы видим на этом изображении?
На этом рентгеновском снимке, когда пациент смотрит вниз, между C1-c2 открывается промежуток в 6 мм. Когда пациент смотрит вверх, 0 мм, места нет. Все между этими двумя поверхностями сжато. Если бы у пациента было только статичное изображение шейного отдела позвоночника в согнутой или нейтральной позе, «все было бы неправильно.«Что не так, обнаруживается только тогда, когда пациент поднимает подбородок вверх.
Когда позвоночные артерии попадают в верхний шейный отдел позвоночника в точке С1, они проходят по змеевидному пути до головного мозга. Именно здесь эти артерии подвержены риску «перекручивания» и, следовательно, прекращения притока крови к мозгу.
Как это вызвано нестабильностью шейки матки?При обычном вращении шеи (то есть при взгляде через плечо) C1 вращается над зубцами («точка поворота» или одонтоидный процесс) C2, что делает возможным вращение головы.Это простое вращение может частично сжать позвоночные артерии (точнее, артерию с той же стороны, на которую вы смотрите) при нормальном движении. У человека с нестабильным шейным отделом позвоночника и гипермобильности шеи это может происходить более регулярно и вызывать многие из описанных выше симптомов. Один из наиболее распространенных симптомов вертебробазилярной недостаточности — это падение, которое, как мы упоминали выше, может привести к внезапному падению человека на землю без предупреждения (но остается в сознании).Было высказано предположение, что приступы падения могут возникать из-за временной потери кровотока к стволу головного мозга (от позвоночных артерий).
Как мы также упоминали выше, другие симптомы включают головокружение, , обморок, помутнение зрения, зрительные и слуховые расстройства, , покраснение, потливость, слезотечение, насморк, головокружение, онемение и покалывание, а также затруднение глотания. или разговаривает. Следует отметить, что нестабильность по всему шейному отделу позвоночника может вызвать перекручивание позвоночных артерий, проходящих через каждый позвонок, но это часто связано с верхним шейным отделом позвоночника.
В исследовании нашей клиники, опубликованном в The Open Orthopaedics Journal ( 7 ), мы писали, что капсульные связки являются основными стабилизирующими структурами фасеточных суставов шейного отдела позвоночника и являются основным источником хронической боли в шее. . Такая боль часто отражает состояние нестабильности в шейном отделе позвоночника и является симптомом, общим для ряда состояний, таких как грыжа диска, шейный спондилез , хлыстовая травма и связанное с хлыстом расстройство , постконтузионный синдром , вертебробазилярная недостаточность и шейно-краниальный синдром .При травме капсульных связок они удлиняются и становятся рыхлыми, что вызывает чрезмерное движение шейных позвонков. В верхнем шейном отделе позвоночника (C0-C2) это может вызывать такие симптомы, как раздражение нервов и вертебробазилярная недостаточность с сопутствующим головокружением, шумом в ушах, головокружением, лицевой болью, болью в руке и мигренозной головной болью .
Что мы видим на этом изображении?
Шейный отдел позвоночника переплетен с нервами и кровеносными сосудами. Нестабильность шейного отдела позвоночника может сдавливать или защемлять нервы и артерии, вызывая множество симптомов в зависимости от того, как пациент двигает головой.Нестабильность шейного отдела позвоночника может вызвать ограничение и сжатие жизненно важных артерий и нервов, которые снабжают кровью и чувствительностью мозг, лицо и шею.
Исследования и лечение
В медицинской литературе вертебробазилярная недостаточность и синдром Хантера-Боу рассматриваются как «несколько» или «крайне редкие» расстройства. Тем не менее, вы столкнулись с приступами падения, приступами головокружения и связанными с ними симптомами. Существует очень мало исследований вариантов лечения, кроме представленных историй болезни, чтобы проиллюстрировать трудности и путаницу, связанные с этими случаями.Мы собираемся представить доказательства того, что нестабильность позвонков из-за нарушения или ослабления шейных связок и прикрепления сухожилий между мышцами и позвонками играет важную роль.
Хирургия декомпрессии и шейного спондилодеза
К этому времени вашего пути к здоровью вам, возможно, порекомендовали пройти операцию по сращению шейки матки или декомпрессию шейки матки, чтобы отрезать часть позвонка, вызывающую защемление компрессии вашей позвоночной артерии.Обсуждая плюсы и минусы хирургии, всегда лучше использовать хирургические исследования, представленные хирургами.
В медицинском журнале Stroke , ( 8 ) хирурги из отделения неврологии больницы Пусанского национального университета в Южной Корее представили следующие результаты:
- «На основе их безопасности, эффективности и хорошего долгосрочного результата хирургические методы лечения, включая декомпрессию шейного отдела позвоночника или спондилодез шейного отдела позвоночника, были рекомендованы
как вариант лечения первой линии при окклюзии ротационной позвоночной артерии. - Хотя артродез шейного отдела позвоночника обеспечивает полное купирование симптомов и отсутствие повторной окклюзии позвоночной артерии, большинство пациентов после операции испытывают значительно ограниченный диапазон движений головы, что ограничивает повседневную активность.
- Однако декомпрессия шейки матки не ограничивает физиологические движения шеи, но имеет проблему высокой частоты повторной окклюзии из-за послеоперационного сращивания между позвоночной артерией и прилегающими мягкими тканями.
- Другой альтернативой является установка эндоваскулярного стента в здоровую позвоночную артерию для увеличения кровотока во время вращения головы.Однако его эффективность и долгосрочные результаты остаются неопределенными, и его нельзя проводить у всех пациентов ».
Успех хирургов при консервативном лечении:
- «Наше исследование показало благоприятный долгосрочный результат консервативного лечения окклюзии ротационной позвоночной артерии. Ни у одного из наших пациентов с консервативным лечением не развился инсульт заднего кровообращения, а у 4 из них симптомы исчезли во время последующего наблюдения, возможно, из-за спонтанного разрешения внешней компрессии или центральной адаптации.Наши результаты показывают, что консервативные методы лечения безопасны и могут рассматриваться как лечение первой линии при окклюзии ротационной позвоночной артерии ».
Давайте рассмотрим это исследование и сведем его в несколько учебных пунктов
- Спондилодез шейного отдела позвоночника — уменьшает или излечивает симптомы. Может быть необходимо некоторым пациентам. За постоянную способность поворачивать шею приходится расплачиваться, включая невозможность после этого управлять автомобилем, потому что вы не можете «смотреть в обе стороны».”
- Хирургия декомпрессии шейки матки — менее успешно, возможны операции в будущем
- Консервативное лечение, в данном случае антикоагулянты, а также обучение и обучение тому, как избежать быстрого движения головы, оказались столь же эффективными, как операция слияния.
В медицинской литературе очень мало описаний консервативных методов лечения без хирургического вмешательства
Если вы просмотрели медицинскую литературу, посвященную синдрому Боу-Хантера, описанному как тип вертебробазилярной недостаточности, вы мало что увидите в плане консервативного безоперационного лечения, но много статей, описывающих различные хирургические вмешательства, которые могут быть применены, и некоторые хирурги предпочитают именно один операция над другим.Во многих статьях также обсуждается логическое развитие последовательных операций, которые потребуются пациенту.
Синдром охотника из лука назван так из-за случая, представленного научному сообществу в 1978 году нейрохирургом Б.Ф. Соренсеном ( 9 ) молодого охотника из лука, который после стрельбы из лука получил травму позвоночной артерии из-за того, как он держал лук.
В 2014 году хирурги из неврологического института Барроу дали своим коллегам-врачам и пациентам оценку их 15-летнего опыта лечения синдрома охотника с луком.Это исследование было опубликовано в журнале World Neurosurgery . ( 10 )
- «В Неврологический институт Барроу поступило 14 пациентов с симптомами синдрома охотника за луком, и у 11 из этих пациентов было подтверждено динамическое сжатие позвоночной артерии при ангиографии.
- Место сжатия было сосредоточено на
- C1-2 (50%) или C5-7 (50%).
- Сдавленной позвоночной артерией обычно была левая артерия (72.7%), а в 54,5% случаев поворот головы в контралатеральную сторону вызывал симптоматическую динамическую компрессию.
- Хирургическая декомпрессия из переднего (44,4%) или заднего (55,6%) доступа в конечном итоге была выполнена 9 пациентам. Во всех случаях выполнялась только декомпрессия; однако у 1 пациента через 5 лет развилась нестабильность шейки матки, потребовавшая переднего инструментального спондилодеза.
Здесь рекомендация заключалась в том, что операция по декомпрессии может помочь в краткосрочной перспективе, но, как упоминалось в исследовании выше, могут быть долгосрочные осложнения, включая нестабильность шейки матки, которая может потребовать дополнительных операций, включая слияние, которое действительно желают немногие пациенты.
Исследования на протяжении января 2019 года постоянно обсуждают краткосрочные преимущества компрессионной хирургии по сравнению с долгосрочными последствиями, ведущими к сращению шейки матки. Фактически, в исследовании, проведенном в феврале 2019 года, проводится сравнение хирурга и хирурга. Он поступил из Медицинской школы Икана на горе Синай в Нью-Йорке и был опубликован в журнале Spine ( 11 ).
«При изучении большой институциональной выборки и еще большей национальной выборки это исследование показало, что хирурги-ортопеды чаще сталкиваются с периоперационным кровотечением, требующим переливания, чем хирурги-неврологи.Если рассматривать госпитальные осложнения в целом, то в национальной выборке хирурги-ортопеды с большей вероятностью столкнутся с госпитальными осложнениями, чем неврологические хирурги, при выполнении задней декомпрессии и спондилодеза шейки матки ».
Когда синтез «лучший», только ответ.
При шейном спондилодезе существует множество проблем, и их следует использовать в крайнем случае. Часто пациенты говорят нам, что их врачи очень уверены в том, что операция пройдет хорошо, но пациенты по-прежнему опасаются, даже напуганы.Бывают случаи, когда может потребоваться операция. Это когда костная шпора или костное разрастание само по себе давит на артерию. Этот тип проблемы характерен для кого-то намного старше по возрасту и страдающего очень запущенным остеохондрозом шейки матки.
Безоперационное лечение — Стабильность шейного отдела позвоночника и восстановление лордоза — Восстановление и восстановление связок позвоночника. Что мы видим на этом изображении?
Шейный отдел позвоночника имеет естественный изгиб.Он действует как пружина или амортизатор для головы. Когда эта кривая исчезает из-за травмы, синдрома гипермобильности суставов или дегенеративного заболевания шейного отдела позвоночника, не только артерии и нервы между позвонками не защищены от воздействия ходьбы, бега, прыжков или неровной езды на автомобиле, они подвергаются воздействию компрессия из-за нестабильности шейного отдела позвоночника, вызванной шейными связками, которые также были повреждены в результате травмы или износа и больше не удерживают шею в правильном положении.
В этом разделе мы поговорим о реальных нехирургических вариантах лечения вертебробазилярной недостаточности и связанных с ней симптомов.
Выше мы кратко говорили о средствах для разжижения крови и обучении пациентов избегать определенных поворотов головы, это методы лечения, которые позволяют подавить симптомы и управлять ими. В этом разделе мы обсудим использование простых инъекций декстрозы или инъекций тромбоцитов для восстановления стабильности шейного отдела позвоночника путем устранения и восстановления поврежденной опорной ткани шеи.
Атлантоаксиальная нестабильность: гипермобильность C1 и C2 вызывает вертебробазилярную недостаточность
Атлантоаксиальная нестабильность — это аномальное чрезмерное движение сустава между атлантом (C1) и осью (C2). Это соединение является уникальным в шейном отделе позвоночника, поскольку C1 и C2 не имеют формы шейных позвонков. Они более плоские, чтобы служить платформой для поднятия головы. Связочный пучок, поддерживающий этот сустав, представляет собой прочные ленты, которые обеспечивают прочность и стабильность, позволяя при этом гибкость движений головы и обеспечивая беспрепятственный доступ (предотвращение грыжи или «защемления») кровеносных сосудов, которые проходят через них в мозг.
Фиксация связок обычно не является первым выбором среди более традиционных врачей при лечении вертебробазилярной недостаточности. Как мы видели, операция слияния или декомпрессии. Повреждение шейной связки следует более широко рассматривать как ключевой метод лечения вертебробазилярной недостаточности.В статье 2015 г., опубликованной в журнале Journal of Prolotherapy , (12) , наша исследовательская группа писала, что повреждение шейной связки следует более широко рассматривать как , лежащую в основе патофизиологии (причину) атлантоаксиальной нестабильности и первичную причину шейная миелопатия (заболевание), в том числе проблемы вертебробазилярной недостаточности.Это продолжение серии опубликованных исследований, проводимых Caring Medical по проблемам нестабильности шейки матки, включая статью «Хроническая боль в шее: связь между слабостью капсульной связки и нестабильностью шейки матки » 2014 года, о которой мы упоминали выше.
Доктора не так просто понять, что вертебробазилярная недостаточность вызвана повреждением связок.
Пациенты страдают от серьезных проблем, вызванных незначительным повреждением связок, и причина остается незамеченной.Проблемы вертебробазилярной недостаточности не изолированы друг от друга. Пациент, страдающий вертебробазилярной недостаточностью, скорее всего, будет страдать от многих проблем, поскольку все они связаны с повреждением верхней шейной связки и нестабильностью шейки матки. Как показано ниже, это включает подвывих шейки матки (смещение шейных позвонков). Одна из причин вертебробазилярной недостаточности — это смещение шейки матки и его «защемление» или «грыжа» не диска, а самих артерий, как мы предложили выше.Это создает ситуацию ишемии (повреждение кровеносных сосудов).
Проблемы вертебробазилярной недостаточности не изолированы друг от друга. Пациент, страдающий вертебробазилярной недостаточностью, вероятно, будет страдать от многих проблем, поскольку все они связаны с повреждением шейных связок верхней части шеи и нестабильностью шейки маткиИсследование нестабильности шейки матки и пролотерапия
Caring Medical опубликовала десятки статей о Инъекции пролотерапии в качестве лечения трудноизлечимых заболеваний опорно-двигательного аппарата .Мы собираемся сослаться на два из этих исследований, поскольку они касаются нестабильности шейки матки и множества связанных с ней симптомов, включая проблему вертебробазилярной недостаточности.
В нашем исследовании, упомянутом ранее в этой статье, мы опубликовали исчерпывающий обзор проблем, связанных с ослаблением поврежденных шейных связок шеи.
Вот что мы написали: «На сегодняшний день нет единого мнения по поводу диагноза нестабильности шейного отдела позвоночника или традиционных методов лечения, которые облегчают проблемы с хронической нестабильностью шеи, подобные упомянутым выше.В таких случаях пациенты часто ищут альтернативные методы лечения боли и облегчения симптомов. Пролотерапия — одно из таких методов лечения, которое предназначено для острых и хронических травм опорно-двигательного аппарата, включая те, которые вызывают хроническую боль в шее, связанную с основной нестабильностью суставов и слабостью связок. Хотя эти классификации симптомов должны быть очевидными признаками пациента, находящегося в бедственном положении, причина проблем не так очевидна. Более того, к сожалению, часто нет корреляции между гипермобильностью или подвывихом позвонков, клиническими признаками или симптомами или неврологическими признаками или симптомами.Иногда симптомы отсутствуют, что еще больше расширяет и без того очень широкий спектр возможных диагнозов нестабильности шейки матки ».
В этом исследовании мы продемонстрировали, что шейные связки шеи являются основными стабилизирующими структурами шейных фасеточных суставов шейного отдела позвоночника и являются основным источником хронической боли в шее, а в случае симптомов вертебробазилярной недостаточности — шейного отдела позвоночника. нестабильность.
Пролотерапия называется техникой регенеративной инъекции (RIT), потому что она основана на предпосылке, что процесс регенеративного / репаративного заживления может восстанавливать и восстанавливать поврежденные структуры мягких тканей.Это простая инъекционная процедура, которая решает очень сложные проблемы.
Мы предполагаем, что во многих случаях хронической боли в шее причиной может быть лежащая в основе нестабильность сустава из-за слабости капсульной связки. В настоящее время варианты лечебного лечения этого типа нестабильности шейки матки неубедительны и неадекватны. Основываясь на клинических исследованиях и опыте с пациентами, которые посещали нашу клинику хронической боли с жалобами на хроническую боль в шее, мы утверждаем, что пролотерапия предлагает потенциально лечебный вариант лечения хронической боли в шее, связанной с ослаблением капсульной связки и лежащей в основе нестабильностью шейки матки.”
Актуальное лечение пролотерапией
Caring Medical опубликовала десятки статей о Инъекции пролотерапии в качестве лечения трудноизлечимых заболеваний опорно-двигательного аппарата. Мы собираемся сослаться на наше исследование 2014 года, в котором мы опубликовали исчерпывающий обзор проблем, связанных с ослаблением поврежденных шейных связок шеи.
Это видео переходит к 1:05, где начинается собственно лечение.
У этого пациента лечится область C1-C2.Росс Хаузер, доктор медицины, делает уколы.
Пролотерапия, изгиб шеи и кровоток
В феврале 2016 г. статья появилась в журнале Medical Science Monitor: International Medical Journal of Experimental and Clinical Research . ( 13 ) Исследователи медицинского университета в Турции сделали следующие наблюдения:
- «Позвоночные артерии проходят в поперечном отверстии каждого шейного позвонка.Учитывая, что позвоночные артерии проходят в анатомическом отношении к шейному отделу позвоночника, мы предположили, что потеря шейного лордоза может повлиять на гемодинамику позвоночных артерий. (Уменьшение притока крови к мозгу) ».
- «(Наше) исследование показало значительную связь между потерей шейного лордоза и снижением гемодинамики позвоночной артерии, включая диаметр, объем потока и пиковую систолическую скорость».
Это исследование, с помощью которого мы получили эмпирические данные за более чем 27-летнюю практику регенеративной медицины.Чтобы исправить проблемы, связанные с шейным отделом позвоночника, нужно восстановить естественную кривизну шеи. Это часть нашей заботливой терапии коррекции шейки матки (CCRT), разработанной Россом Хаузером, доктором медицины. Эта программа была эволюционным продуктом десятилетий лечения пациентов с заболеваниями шеи, включая нестабильность шейки матки и остеохондроз, чтобы предоставить долгосрочных решения для лечения. Симптомы, связанные с нестабильностью шейки матки. CCRT сочетает в себе индивидуализированные протоколы для объективного документирования нестабильности позвоночника, укрепления ослабленной связочной ткани, соединяющей позвонки, восстановления нормальной биомеханики и стимулирования восстановления лордоза.
Новое исследование: Исправьте проблемы потери лордоза: немедленно увеличьте церебральный кровоток
В медицинском журнале Brain Circulation (январь-март 2019 г.) ( 14 ) врачи выписали результаты анализа пациентов с цервикальным лордозом. Они написали, что если вы восстановите естественный изгиб шеи, вы можете немедленно увеличить церебральный кровоток, поскольку давление в мозговой артерии снижается.
Вот основные выводы этого исследования.Они представляют собой хорошее резюме того, что мы обсуждали в этой статье:
- Утрата лордоза шейного отдела позвоночника связана со снижением гемодинамики (кровотока) позвоночной артерии.
- Основываясь на тесной анатомической взаимосвязи между шейным отделом позвоночника, позвоночными артериями и сосудистой сетью головного мозга, исследователи предположили, что улучшение шейного гиполордоза увеличивает коллатеральную (сбоку) гемодинамику мозговых артерий и кровообращение.
Вертебробазилярная недостаточность вызывает множество проблем.Устранение нестабильности шейки матки — это не то, что можно просто и легко вылечить, требуется комплексная нехирургическая программа, чтобы стабилизировать нестабильность пациента и уменьшить симптомы. Мы считаем, что если вы переходили от клинициста к клиницисту, от практикующего к терапевту, от врача к доктору, то с большой вероятностью у вас возникнут проблемы с нестабильностью шейного отдела шеи, вызванные слабостью и повреждением шейных связок. Наши методы лечения пролотерапии декстрозой и в некоторых случаях пролотерапии плазмой, обогащенной тромбоцитами, могут быть ответом.
Как мне узнать, хороший ли я кандидат?
Мы надеемся, что вы нашли эту статью информативной и помогли ответить на многие вопросы, которые могут у вас возникнуть в связи с проблемами, с которыми вы можете столкнуться. Как и вы, мы хотим убедиться, что вы подходите для нашей клиники, прежде чем принять ваш случай. Хотя наша миссия — помочь как можно большему количеству людей с хронической болью, к сожалению, мы не можем принять все случаи. У нас есть многоэтапный процесс, поэтому наша команда может действительно узнать вас и ваше дело, чтобы убедиться, что вы подходите для уникального тестирования и лечения, которое мы предлагаем здесь.
Если вы хотите получить более подробную информацию о ваших проблемах, напишите нам: Получите помощь и информацию от нашего заботливого медицинского персонала
Список литературы
1 Комацу К., Одзаки А., Ивасаки К., Мацумото С. Двусторонние аневризмы позвоночной артерии на уровне атлантоаксиального сустава, вызывающие рецидивный инсульт. Медицина внутренних органов. 2016 15 ноября; 55 (22): 3365-8. [Google Scholar]
2 Nomura Y, Toi T, Ogawa Y, Oshima T, Saito Y.Переходный нистагм в описании случая синдрома охотника за луком. BMC неврология. 2020 Декабрь; 20 (1): 1-4. [Google Scholar]
3 Дуань Дж., Сюй Дж., Ши Дж., Цао Ю. Достижения в патогенезе, диагностике и лечении синдрома охотника с луком: всесторонний обзор литературы. Интервенционная неврология. 2016; 5 (1-2): 29-38. [Google Scholar]
4 Ши К., Ван Л., Доу И, Ян Ф, Цяо И., Чжан Х. Динамическая КТ-ангиография головы и шеи в диагностике синдрома Лоу-Хантера: отчет о клиническом случае.Отчеты о случаях радиологии. 2020 1 ноября; 15 (11): 2275-7. [Google Scholar]
5 Wong SC, Chan TS, Chan CH, Ma JK. Синдром охотника за луками: зловещая причина головокружения и обморока, которую нельзя упускать. Гонконгский медицинский журнал. 2020 1 апреля; 150: e1. [Google Scholar]
6 Golomb MR, Ducis KA, Martinez ML. Синдром Боу-Хантера у детей: обзор литературы и представление нового случая у 12-летней девочки. Журнал детской неврологии. 2020 июн 8: 08830738208. [Google Scholar]
7 Хаузер Р., Стейлен Д., Гордин К. Биология пролотерапии и ее применение при клинической нестабильности шейного отдела позвоночника и хронической боли в шее: ретроспективное исследование.Европейский журнал профилактической медицины. Vol. 3, No. 4, 2015, pp. 85-102. doi: 10.11648 / j.ejpm.20150304.11 [Google Scholar]
8 Choi KD, Choi JH, Kim JS, Kim HJ, Kim MJ, Lee TH, Lee H, Moon IS, Oh HJ, Kim JI. Окклюзия ротационной позвоночной артерии: механизмы и отдаленные результаты. Инсульт. 2013 1 января: СТРОКЕГА-113. [Google Scholar]
9 Соренсен Б.Ф. Охотничий ход из лука. Нейрохирургия. 1978 1 мая; 2 (3): 259-61. [Google Scholar]
10 Zaidi HA, Albuquerque FC, Chowdhry SA, Zabramski JM, Ducruet AF, Spetzler RF.Диагностика и лечение синдрома охотника за луком: 15-летний опыт работы в неврологическом институте Барроу. Мировая нейрохирургия. 2014 1 ноября; 82 (5): 733-8. [Google Scholar]
11 Снайдер Д. Д., Нейфер С. Н., Гал Дж. С., Дойч Британская Колумбия, Ротрок Р., Хантер С., Кариди Дж. М.. Оценка вариабельности частоты госпитальных осложнений между хирургическими услугами для пациентов, перенесших заднюю декомпрессию шейки матки и спондилодез. Позвоночник. 2019 1 февраля; 44 (3): 163-8.
12 Хаузер Р., Стейлен-Матиас Д., Фишер П.Нестабильность верхнего отдела шейки матки травматического происхождения, леченная пролотерапией декстрозой: описание случая. Журнал пролотерапии . 2015; 7: e932-e935.
13 Bulut MD, Alpayci M, enköy E, Bora A, Yazmalar L, Yavuz A, Gülşen İ. Снижение гемодинамики позвоночных артерий у пациентов с потерей шейного лордоза. Монитор медицинской науки: международный медицинский журнал экспериментальных и клинических исследований. 2016; 22: 495. [Google Scholar]
14 . Кац Е.А., Кац С.Б., Федорчук К.А., Лайтстоун Д.Ф., Банах С.Дж., Подолл Д.Д.На увеличение церебрального кровотока указывает увеличение площади церебральных артерий и интенсивности пикселей на магнитно-резонансной ангиограмме головного мозга после коррекции шейного лордоза. Циркуляция мозга. 1 января 2019; 5 (1): 19. [Google Scholar]Диагностика и лечение стеноза позвоночной артерии | QJM: Международный медицинский журнал
Введение
Примерно четверть ишемических инсультов затрагивает заднее или вертебробазилярное кровообращение. 1, 2 Стеноз позвоночной артерии может возникать в ее экстра- или внутричерепной части и может составлять до 20% ишемических инсультов в области заднего кровообращения. 3– 6 Стенотические поражения, особенно в начале позвоночной артерии, не редкость. В ангиографическом исследовании 4748 пациентов с ишемическим инсультом определенная степень стеноза проксимальной экстракраниальной позвоночной артерии наблюдалась в 18% случаев справа и 22,3% слева. 7 Это второе по частоте место стеноза после стеноза внутренней сонной артерии в области бифуркации сонной артерии. Такие стенозирующие поражения в настоящее время потенциально поддаются лечению эндоваскулярными методами. 8
В отличие от стеноза сонной артерии оптимальному лечению стеноза позвоночной артерии уделялось ограниченное внимание и мало изучено. Это частично отражает трудности с адекватной визуализацией позвоночной артерии и ограниченные возможности хирургического лечения.Однако недавние улучшения в визуализации и появление ангиопластики позвоночной артерии открыли новые возможности для лечения этого заболевания.
Мы рассматриваем анатомию позвоночной артерии, то, что известно о естественном течении болезни позвоночной артерии, роль визуализации в диагностике стеноза позвоночной артерии и методы лечения стеноза позвоночной артерии.
Анатомия
Позвоночная артерия возникает из надзаднего отдела первой части подключичной артерии.В 6% случаев левая позвоночная артерия отходит непосредственно от дуги аорты. В отличие от внутренней сонной артерии, которая является почти прямым продолжением своего материнского сосуда и общей сонной артерии, позвоночная артерия разветвляется почти под прямым углом к своему питающему сосуду. Позвоночная артерия диаметром 3–5 мм имеет гораздо меньший относительный калибр, чем подключичная, при этом лишь небольшое количество подключичной крови обычно направляется в каждый позвонок. Эти различия в анатомии вполне могут отражаться в неодинаковой динамике кровотока между происхождением каротидного и вертебробазилярного церебрального кровообращения, с последующей предрасположенностью к образованию другого типа атеросклеротической бляшки.Считается, что бляшечное заболевание в происхождении позвоночной артерии «более гладкое» и менее склонно к изъязвлению с образованием вторичных тромбов. 9 Различия между морфологией бляшек сонной и позвоночной артерий были выведены на основании ангиографических данных, но существует мало опубликованных патологических данных, подтверждающих это. 10
Анатомически позвоночную артерию можно разделить на три экстракраниальные части и внутричерепную часть (рис. 1). Первая часть проходит от начала до точки, в которой она входит в поперечные отверстия пятого или шестого шейного позвонка.Во второй части он проходит в межпозвонковых отверстиях, пока не выходит в качестве третьей части позади атласа и направляется к большому затылочному отверстию. Последняя внутричерепная часть начинается, когда она проникает в твердую мозговую оболочку и паутинную оболочку у основания черепа, и заканчивается, когда она встречается с противоположной позвоночной артерией, образуя срединную базилярную артерию на уровне медуллопонтинного соединения. В своей экстракраниальной части позвоночная артерия отдает небольшие спинные ветви к надкостнице и телам позвонков, а мышечные ветви — к глубоким окружающим мышцам области.Короткая четвертая внутричерепная часть отдает большие передние и задние спинномозговые артерии к мозговому веществу и спинному мозгу, мелкие проникающие сосуды — к мозговому веществу и его самой большой ветви — задней нижней мозжечковой артерии (PICA), которая снабжает небольшую часть спинного мозга и спинного мозга. мозжечок. Иногда эта ветвь PICA отсутствует, и коллатеральные сосуды затем питают латеральный мозг. По мере того, как он входит в череп, стенка позвоночной артерии демонстрирует заметные изменения с уменьшением толщины адвентициального и медиального слоев и уменьшением эластичных волокон в средней и внешней эластической пластине. 11
Примерно у 15% здорового населения одна позвоночная артерия является атретической (<2 мм в диаметре) и вносит небольшой вклад в кровоток в базилярной артерии. Также часты и меньшие степени асимметрии. Левый позвонок преобладает примерно в 50% случаев; правые в 25% и только в оставшейся четверти случаев - две позвоночные артерии аналогичного калибра. Эти вариации не имеют клинического значения или не имеют большого значения, если только они не связаны с происхождением позвоночной артерии или стенозом проксимальной подключичной артерии.
Рисунок 1.
Четыре части позвоночной артерии.
Рисунок 1.
Четыре части позвоночной артерии.
Стеноз экстракраниальной позвоночной артерии
Экстракраниальная позвоночная артерия поражена несколькими патологическими процессами, вызывающими инсульт. Самым распространенным из них является атеросклеротическое заболевание — основное внимание в этом обзоре, — но другие включают расслоение позвоночной артерии, фиброзную полосу на шее, внешнюю компрессию во второй и третьей ее частях из-за травмы шейных позвонков или остеофитического соударения и компрессии, а также васкулит, чаще всего гигантоклеточный артериит.
Патологоанатомические исследования показали атеросклеротический стеноз в области происхождения позвоночной артерии в случаях цереброваскулярной смерти. Кроме того, атеросклеротическое заболевание первой части позвоночной артерии обычно связано с аналогичным заболеванием внутренней сонной артерии. 12, 13 Однако было получено очень мало патологических образцов из in vivo случаев, поскольку эндартерэктомия по поводу стеноза позвонка выполняется редко, а операция шунтирования не дает образцов.Несмотря на возможные различия во внешнем виде бляшек при поражении экстракраниальных позвонков и внутренних сонных артерий, 10 обычно считается, что эти два участка имеют общий патогенез с инсультом в результате образования эмболов на месте атеросклеротической бляшки. 14 Гемодинамический инсульт, однако, реже возникает из-за стеноза позвоночной артерии, 9 , потому что обе позвоночные артерии переходят в одну базилярную артерию. Кроме того, в отличие от ВСА, позвоночная артерия отдает многочисленные ветви в шее, что способствует значительному коллатеральному кровоснабжению, которое часто восстанавливает дистальную артерию после окклюзии в начале.
Популяционных данных о распространенности стеноза экстракраниальной позвоночной артерии нет. На сегодняшний день исследований было проведено небольшое количество групп специалистов. 15 Самые большие опубликованные серии взяты из Регистра заднего кровообращения Медицинского центра Новой Англии. 16 Из 407 пациентов, у которых были симптомы инсульта заднего кровообращения или транзиторной ишемической атаки (ТИА), либо того и другого, у 80 (20%) был обнаружен стеноз первой части позвоночной артерии> 50%.Инсульт в задней части кровообращения определялся визуализирующими исследованиями, а вертебробазилярный ТИА был диагностирован опытными неврологами по инсульту с использованием критериев Каплана. 17 Стеноз был продемонстрирован с помощью традиционной или магнитно-резонансной ангиографии (МРА). Чуть менее половины (37/80) имели окклюзию позвоночной артерии, а 15% (12/80) имели двустороннее поражение. Четверть (22/80) этих случаев также имели внутричерепную позвоночную артерию или базилярное заболевание, которое могло быть причиной симптомов. Однако почти у половины пациентов (38/80) стеноз позвоночного происхождения был единственной идентифицированной причиной инсульта, что позволяет предположить, что стеноз позвоночной артерии был причиной не менее 10% зарегистрированных событий.Профиль факторов риска для этих пациентов был аналогичен профилю инсульта переднего кровообращения, а средний возраст для группы составлял 62,5 года. Распределение по этнической принадлежности было таким же, как и по регистру в целом, но преобладали мужчины в группе со стенозом по происхождению позвоночной артерии. На сегодняшний день в этой группе не опубликовано никаких данных о последующем наблюдении.
В отличие от болезни сонной артерии прогноз симптоматического стеноза позвоночной артерии неизвестен. Единственная опубликованная проспективная серия стеноза позвоночной артерии была получена из клиники Кливленда, 18 и включала преимущественно бессимптомные случаи.Это была проспективная коллекция 96 случаев стеноза позвоночной артерии, подтвержденного ангиографией на ≥50%, из которых 89 имели стеноз в начале, а восемь имели внутричерепное заболевание позвоночной или основной артерии. Исключались случаи окклюзии или оперативные вмешательства, предположительно по симптоматике. Пятилетнее наблюдение показало умеренное общее повышение частоты инсультов на 5,25% в год, но только у 18 были симптомы заднего кровообращения на момент ангиографии. У большинства из них действительно были симптомы переднего кровообращения, а у 74 был ассоциированный стеноз внутренней сонной артерии> 50%, 52 из которых перенесли каротидную эндартерэктомию.Возможно, неудивительно, что выживаемость всей группы была связана с их сонной артерией и сопутствующим сердечным заболеванием. Только два из 23 инсультов, замеченных во время наблюдения, были в заднем кровообращении, и в обоих случаях на момент обращения к врачу имел место сопутствующий стеноз базилярной артерии. Ни в одном из изолированных стенозов экстракраниальных позвоночных артерий не развился инфаркт заднего кровообращения.
Внутричерепной позвоночный стеноз
Стеноз внутричерепной позвоночной артерии в четвертом сегменте позвоночной артерии часто также затрагивает базилярную артерию и в большей степени связан с инфарктом ствола мозга, чем стеноз экстракраниальной позвоночной артерии.В основном о нем сообщалось у пациентов с симптомами, и считается, что он чаще встречается у японцев, китайцев и чернокожих американцев, чем у кавказцев. 19, 20 В серии наблюдений Cleveland Clinic с участием 44 пациентов со стенозом дистальной позвоночной или основной артерии у 38 были симптомы заболевания заднего кровообращения. 21 Из них только 16 имели поражение только позвоночной артерии, и в двух случаях поражалась экстракраниальная позвоночная артерия. Однако через шесть лет наблюдения частота ТИА заднего кровообращения, инсульта и смерти была выше, чем в группе пациентов с экстракраниальной позвоночной артерией, при этом общая частота инсультов составляла 7% в год.
В проспективном нерандомизированном исследовании аспирина против варфарина для вторичной профилактики стеноза задней внутричерепной артерии кровообращения> 50%, 22 37/68 случаев касались позвоночной артерии. Общая частота инсультов, связанная со стенозом одиночной внутричерепной позвоночной артерии (31 из 68 случаев), составила 13,7% в год при среднем сроке наблюдения 13,8 месяцев. Частота повторных инсультов на территории стенозированной позвоночной артерии была ниже — 7,8% в год. В группе варфарина частота повторных инсультов была ниже, но их количество было небольшим, а лечение не было рандомизированным, что затрудняло определенные выводы об эффективности варфарина.
Регистр заднего кровообращения Медицинского центра Новой Англии выявил 75 случаев тяжелой симптоматической окклюзионной болезни внутричерепной позвоночной артерии и предположил, что первичная локализация заболевания находится дистальнее источника PICA. 23 Двустороннее поражение внутричерепных позвоночных артерий также было обычным явлением (42 из 430 пациентов в регистре). 24 Эмболия из сердечных источников и стеноз экстракраниальной позвоночной артерии оказались наиболее частой причиной инсульта «проксимального» заднего кровообращения (мозгового и мозжечкового инсульта). 25 Эти случаи с сопутствующей базилярной болезнью и дистальным отделом заднего кровообращения были связаны с плохим исходом, и, в отличие от небольших клинических исследований в Кливленде, распределение стеноза, по-видимому, имело прогностическое значение.
Роль визуализации в диагностике
Золотым стандартом диагностики стеноза позвоночной артерии остается цифровая субтракционная ангиография (DSA), хотя она имеет небольшую заболеваемость и связанную с ней смертность. 26– 28 Стеноз в начале позвоночной артерии можно не заметить при стандартных видах дуги, так как подключичная артерия наложена на первый сегмент позвоночной артерии, и требуются дополнительные виды под углом.
Первоначальным неинвазивным исследованием выбора при заболевании экстракраниальных позвоночных артерий является ультразвуковое исследование, 29 и некоторая часть 80–90% всех позвоночных артерий могут быть озвучены. 30 Однако, используя только ультразвуковую допплерографию, происхождение артерии можно визуализировать только у 60% пациентов. 31 Это можно улучшить до 80% за счет использования цветного доплеровского изображения потока. 32 Более поздние серии исследований, в которых использовалась энергетическая допплеровская визуализация в сочетании с методами цветового потока, показали преимущество перед традиционными методами с точки зрения чувствительности для обнаружения значительного стеноза, которая в некоторых исследованиях приближается к 100% без снижения специфичности. 33 Повышенная точность оценки скорости потока может быть достигнута путем снятия показаний как с нижней (C5-6), так и с высокой (C1-2) шейных областей. 34 Тем не менее, методика, как и все ультразвуковые исследования, сильно зависит от пользователя.
Транскраниальный допплеровский ультразвук (ТКД) может использоваться для обнаружения стеноза внутричерепной позвоночной артерии с чувствительностью до 80% и специфичностью 80–97% по сравнению с DSA. 35, 36 Однако более чем в половине случаев степень стеноза недооценивается, и окклюзия сосудов может быть пропущена. Еще одно возможное применение TCD — обнаружение эмболов от стеноза, 37 , и многие исследования выявили бессимптомную эмболизацию у пациентов с симптоматическим стенозом сонной артерии. 38 Однако таких исследований атеросклеротического стеноза позвоночной артерии не проводилось, хотя TCD использовался для мониторинга во время чрескожной транслюминальной ангиопластики (ЧТА) стеноза позвонков.
Спиральная или спиральная компьютерная томографическая ангиография (КТА) позволяет визуализировать экстракраниальную позвоночную артерию без рисков, связанных с катетерной ангиографией, но ее использование не было полностью подтверждено с точки зрения DSA. В одном многообещающем исследовании 24 пациентов с симптомами вертебробазилярной ишемии КТА визуализировала позвоночное происхождение во всех случаях и смогла обнаружить все стенотические поражения экстракраниальных позвоночных артерий, обнаруженные с помощью DSA.Кроме того, считалось, что это дает дополнительные диагностические преимущества в различении «изогнутых» и действительно атеросклеротических стенозированных сосудов. 39 В другом исследовании из 14 поражений, наблюдаемых при DSA у пациентов с острым ишемическим инсультом в области заднего кровообращения, 13 были обнаружены при КТА, но только семь из этих 13 могли быть зарегистрированы как стеноз или окклюзия. 40 В том же исследовании 103 инсультов заднего кровообращения была обнаружена менее хорошая корреляция между КТА и Допплером.
Магнитно-резонансная томография (МРТ), используемая отдельно, может обнаружить внутричерепную болезнь позвоночных артерий, 41, 42 , но ее лучше всего использовать в сочетании с магнитно-резонансной ангиографией (МРА) для оценки как экстра-, так и внутричерепных позвоночных артерий.Обзор опыта реестра Медицинского центра Новой Англии по сравнению MRA с DSA показал, что MRA имеет более высокую чувствительность для выявления базилярного стеноза, чем экстракраниальная или внутричерепная болезнь позвоночных артерий. Чувствительность составила 100% для двух независимых наблюдателей, идентифицировавших 12 стенозов в 39 базилярных артериях. У 62 пациентов с экстракраниальным позвоночным стенозом происхождение позвоночной артерии не всегда было хорошо продемонстрировано, что приводило к более низким результатам чувствительности. Чувствительность к стенозу внутричерепной позвоночной артерии была наименее впечатляющей, и повреждения были пропущены, особенно на стыке внутричерепной и экстракраниальной частей позвоночной артерии. 43 Важной ловушкой при МРА является завышение сведений об окклюзии в случаях стеноза высокой степени. Это связано с тем, что времяпролетная MRA полагается на связанные с потоком улучшения для изображения судов и, следовательно, предоставляет информацию о характеристиках потока; низкий расход может проявляться как отсутствие сосуда. Отношение сигнал / шум можно улучшить за счет добавления контрастных веществ, и МРА с усилением контраста представляется многообещающим. На сегодняшний день сообщения сосредоточены на заболевании сонной артерии, но также есть предполагаемое улучшение по сравнению с традиционной МРА в обнаружении поражений в начале экстракраниальной позвоночной артерии. 44 Однако существует специфическая проблема визуализации истоков позвоночных артерий из-за ограничений конструкции катушки и уменьшения сигнала в пространственных пределах катушки. Этот недостаток сигнала может усугубить проблемы с дифференциацией низкого потока из-за стеноза и окклюзии высокой степени, и не обязательно помогает при использовании контраста.
Лечение
Лечение
Само медикаментозное лечение было стандартным лечением инсульта заднего кровообращения, хотя, за исключением кардиоэмболических причин, оно обычно игнорировало специфический патофизиологический процесс, лежащий в основе события.На сегодняшний день не проводилось рандомизированных испытаний использования различных антиагрегантов или антикоагулянтов на фоне антиагрегантной терапии в известных случаях атеросклеротического стеноза экстракраниальных позвоночных артерий.
Точно так же не было завершенных рандомизированных исследований стеноза внутричерепной позвоночной артерии, хотя есть одно небольшое ретроспективное нерандомизированное исследование. Это сравнивало антикоагулянтную терапию с варфарином с МНО 1,6–1,8 с аспирином в дозе 325 мг в случаях симптоматической основной внутричерепной артерии, стеноза, подтвержденного ангиографией на 50–99%. 22 Ожидаются результаты продолжающегося проспективного рандомизированного исследования варфарина и аспирина при стенозе большой внутричерепной артерии. 45
Хирургическое лечение
Операция по поводу стеноза позвоночной артерии может быть выполнена путем эндартерэктомии или реконструкции.
Эндартерэктомия по поводу атеросклеротического стеноза в исходной и проксимальной части экстракраниальной позвоночной артерии выполняется через надключичный разрез с начала 1960-х годов с переменным успехом. 46 Процедура технически сложна из-за плохого доступа к источнику сосуда, и многие хирурги прибегают к ключичной остеотомии, чтобы улучшить ее. Осложнения, включая лимфоцеле, свищи, паралич голосовых связок и пневмоторакс, хорошо известны. Аналогичные проблемы с доступом существуют при эндартерэктомии стеноза внутричерепной позвоночной артерии, которая обычно включает ограниченную субокципитальную краниотомию. Несмотря на то, что это технически выполнимая операция, показатели успеха низкие, и реваскуляризация является предпочтительным хирургическим лечением в подходящих случаях. 47, 48
Реконструкция при стенозе экстракраниальной позвоночной артерии включает транспозицию позвоночной артерии, обычно в общую или внутреннюю сонную артерию, 46, 49 , но также сообщалось о транспозиции в подключичную и тироцервикальную артерии. стволовые артерии. Эндартерэктомия сонной или позвоночной артерии часто выполняется во время процедуры транспозиции. Результаты 369 реконструкций экстракраниальных позвоночных артерий (252 проксимальных, 117 дистальных) из группы Berguer, 46, 50, 51 показали низкий комбинированный коэффициент инсульта и смертности при проксимальной реконструкции менее 2% и совокупный коэффициент проходимости 92% при 10-летнем наблюдении.При реконструкции дистальной экстракраниальной позвоночной артерии комбинированная частота инсульта и смертности составила около 6%, а совокупная проходимость — 80% через 5 лет, что аналогично стандартной экстракраниальной каротидной эндартерэктомии. Тем не менее, 70% пациентов, перенесших реконструкцию дистальной экстракраниальной позвоночной артерии, умерли через 5 лет после операции, в основном из-за сердечного заболевания. 97% выживших не имели инсульта при аналогичном периоде наблюдения. Кроме того, хирургические осложнения были значительными: частота возникновения синдрома Хорнера составила 10% после экстракраниальной реконструкции и аналогичная частота послеоперационных лимфоцеле.При реконструкции дистального отдела позвоночной артерии тромбоз транспонированного сосуда и необходимость экстренной трансплантации вены наблюдались в 11% случаев. В других сериях описан паралич голосовых связок и повреждение диафрагмального нерва как другие заметные осложнения. 52 Сообщалось также о транспозиционной хирургии стеноза внутричерепной позвоночной артерии, хотя количество случаев меньше, а показатели успеха не так высоки с точки зрения разрешения симптомов вертебробазилярной ишемии, в то время как количество осложнений выше. 53, 54
Эндоваскулярное лечение
В последние годы хирургические операции выполняются реже в случаях, не поддающихся лечению. Это связано с тем, что в настоящее время появляется все больше литературы о сериях случаев, предполагающих, что эндоваскулярное вмешательство с чрескожной транслюминальной ангиопластикой (ЧТА) и стентированием является безопасным и эффективным лечением атеросклеротического стеноза экстракраниальной позвоночной артерии, особенно в области происхождения позвоночной артерии. 55– 63 По мере того, как техника развивалась на основе эндоваскулярного вмешательства на коронарных артериях, появилась тенденция к использованию стентов с расширяющейся стенкой в качестве первичной процедуры (рис. 2). Некоторые ранние отчеты, в которых выполнялась только ЧТА при стенозе VA по происхождению, были связаны с заметной частотой рестеноза, сравнимой с таковой при стенозе устной почечной артерии при ЧТА, частично из-за отдачи стенки сосуда. 64, 65 Частоту рестеноза в разных сериях трудно сравнивать из-за различных методов, используемых для визуализации экстракраниальных позвоночных артерий во время наблюдения, как внутри, так и между сериями.Из коронарной литературы есть некоторые предположения об улучшении проходимости и рестеноза стентированных сосудов, а также о снижении частоты тромбоэмболии при использовании стентов. 66, 67 Считается, что это уменьшение тромбообразования и тромбоэмболии происходит из-за защитного слоя фиброзной и неоинтимальной ткани, растущего над сеткой стента и покрывающего атерогенные ткани стенки сосуда. Еще одним преимуществом первичного стентирования является снижение скорости расслоения интимы во время процедуры.На сегодняшний день серия с первичным развертыванием стентов до стенотических поражений 50% и более в экстракраниальных позвоночных артериях, 56, 59, 61– 63 продемонстрировала высокий уровень технического успеха 98–100 % в улучшении ангиографического вида стеноза. Не сообщалось о серьезных осложнениях процедуры: не было случаев смерти во время операции и инсультов, связанных с заболеванием заднего кровообращения, в текущих краткосрочных (6–25 месяцев) отчетах о наблюдении.Сообщается, что частота периоперационной ТИА заднего кровообращения составляет от 0 до 3%. Однако эти результаты получены из серии отобранных случаев, и требуются данные рандомизированных контролируемых исследований. До тех пор использование такого вмешательства, вероятно, останется в основном экспериментальным.
То же можно сказать и об эндоваскулярном вмешательстве при стенозе внутричерепной позвоночной артерии. Само состояние, которое часто связано с сопутствующим стенозом базилярной артерии, несет в себе больший риск инсульта, чем стеноз экстракраниальной позвоночной артерии — примерно в 17 раз больше, чем ожидаемая частота инсульта у нормальной популяции, соответствующей возрасту и полу. 21 Однако вмешательство с помощью ЧТА и стентирования при таких поражениях было зарегистрировано только в отдельных небольших сериях пациентов. Сообщается, что внутричерепное стентирование является технически более сложной процедурой, чем эндоваскулярное экстракраниальное вмешательство, и соотношение пользы и риска более неопределенное. 68– 73 Лучшее лечение стеноза внутричерепной позвоночной артерии остается спорным из-за неопределенности в отношении преимуществ ЧТА и отсутствия приемлемых хирургических альтернатив, в то время как оптимальное антитромботическое лечение внутричерепного стеноза также неясно.На практике такое вмешательство рекомендуется только при хирургическом вмешательстве, в отдельных случаях в специализированных центрах после того, как «лучшее» лечение оказалось безуспешным. 69, 74
Рис. 2.
a Ангиограмма, показывающая стеноз происхождения правой позвоночной артерии. b Ангиографический вид после РТА и установки стента.
Рис. 2.
a Ангиограмма, показывающая стеноз происхождения правой позвоночной артерии. b Ангиографический вид после РТА и установки стента.
Заключение
Стеноз позвоночной артерии — важная этиология инсульта заднего кровообращения. Улучшения в неинвазивной визуализации предоставляют лучшую анатомическую информацию об окклюзионной болезни позвоночной артерии. Это должно позволить лучше понять естественную историю этого болезненного процесса с точки зрения его способности вызывать инсульт и смерть. До тех пор, пока естественный анамнез не станет более ясным, трудно полностью оценить конкретные виды лечения и вмешательства, хотя эндоваскулярное вмешательство с первичным стентированием стеноза экстракраниальной позвоночной артерии является многообещающим потенциальным лечением.
GC — научный сотрудник по клиническим исследованиям, финансируемый Ассоциацией инсультов.
Список литературы
1Bamford J, Sandercock P, Dennis M, Burn J, Warlow C. Классификация и естественная история клинически идентифицируемых подтипов церебрального инфаркта.
Ланцет
1991
;337
:1521
–6.2Bogousslavsky J, van Melle G, Regli F. Регистр инсультов в Лозанне: анализ 1000 последовательных пациентов с первым инсультом.
Ход
1988
;19
:1083
–92,3Каплан Л.Р., Амаренко П., Розенгарт А., Лафраншиз Е.Ф., Тил П.А., Белкин М., ДеВитт Л.Д., Пессин М.С. Эмболия от окклюзионного поражения позвоночной артерии.
Неврология
1992
;42
:1505
–12,4Джордж Б., Лауриан К. Вертебро-базилярная ишемия. Его связь со стенозом и окклюзией позвоночной артерии.
Acta Neurochir (Wien)
1982
;62
:287
–95.5Корошец В.Дж., Роппер А.Х. Эмболия артерии-артерии, вызывающая инсульт в заднем кровообращении.
Неврология
1987
;37
:292
–5,6Pessin MS, Daneault N, Kwan ES, Eisengart MA, Caplan LR. Местная эмболия от окклюзии позвоночной артерии.
Ход
1988
;19
:112
–15,7Хасс В.К., Филдс WS, Норт Р.Р., Кирчефф II, Чейз Н.Е., Бауэр РБ. Совместное исследование окклюзии экстракраниальной артерии.II. Артериография, методики, участки и осложнения.
JAMA
1968
;203
:961
–8,8Crawley F, Clifton A, Brown MM. Поддающиеся лечению поражения, продемонстрированные на вертебральной ангиографии при ишемических событиях в области заднего кровообращения.
Br J Radiol
1998
;71
:1266
–70,9Caplan LR. Инсульт: клинический подход , 3-е изд. Баттерворт-Хайнеманн,
2000
.10Imparato AM, Riles TS, Kim GE.Ангиопластика шейного отдела позвоночника при ишемии ствола головного мозга.
Хирургия
1981
;90
:842
–52,11Wilkinson IM. Позвоночная артерия: экстракраниальное и внутричерепное строение.
Arch Neurol
1972
;27
:392
–6.12Castaigne P, Lhermitte F, Gautier JC, Escourolle RD, Derouesne C, Agopian P, Popa C. Артериальные окклюзии в позвоночно-базилярной системе.
Мозг
1973
;96
:133
–54.13Hutchinson EC, Yates PO. Шейный отдел позвоночной артерии: клинико-патологическое исследование.
Мозг
1956
;79
:319
–31,14Caplan LR. Повторное посещение эмболии головного мозга.
Неврология
1993
;43
:1281
–7,15Chen WH, Ho DS, Ho SL, Cheung RT, Cheng SW. Распространенность болезни экстракраниальных сонных и позвоночных артерий у китайских пациентов с ишемической болезнью сердца.
Ход
1998
;29
:631
–4.16Wityk RJ, Chang HM, Rosengart A, Han WC, DeWitt LD, Pessin MS, Caplan LR. Заболевание проксимальных экстракраниальных позвоночных артерий в Регистре заднего кровообращения Медицинского центра Новой Англии.
Arch Neurol
1998
;55
:470
–8,17Caplan LR. Заболевание заднего кровообращения: клинические данные, диагностика и лечение , 1-е изд. Кембридж, Массачусетс, издательство Blackwell Scientific,
1996
,18Муфарридж Н.А., Литтл-младший, Фурлан А.Дж., Уильямс Дж., Маржевски Д.Дж.Стеноз позвоночной артерии: отдаленное наблюдение.
Ход
1984
;15
:260
–3,19Каплан Л. Р., Горелик П. Б., Хиер ДБ. Раса, пол и окклюзионные цереброваскулярные заболевания: обзор.
Ход
1986
;17
:648
–55.20Фельдманн Э., Данео Н., Кван Э., Хо К.Дж., Пессин М.С., Лангенберг П., Каплан Л.Р. Китайско-белые различия в распределении окклюзионных цереброваскулярных заболеваний.
Неврология
1990
;40
:1541
–5.21Муфарридж Н.А., Литтл-младший, Фурлан А.Дж., Лезерман-младший, Уильямс Г.В. Стеноз базилярной и дистальной позвоночной артерии: отдаленное наблюдение.
Ход
1986
;17
:938
–42.22Прогноз для пациентов с симптоматическим стенозом позвоночной или базилярной артерии. Группа исследования симптоматического внутричерепного заболевания варфарин-аспирин (WASID).
Ход
1998
;29
:1389
–92,23Мюллер-Купперс М., Граф К.Дж., Пессин М.С., ДеВитт Л.Д., Каплан Л.Р.Заболевания внутричерепных позвоночных артерий в Регистре заднего кровообращения Медицинского центра Новой Англии.
евро Neurol
1997
;37
:146
–56,24Шин Х. К., Ю К. М., Чанг Х. М., Каплан Л. Р.. Двустороннее внутричерепное заболевание позвоночной артерии в Медицинском центре Новой Англии, Регистр заднего кровообращения.
Arch Neurol
1999
;56
:1353
–8,25Граф К.Дж., Пессин М.С., ДеВитт Л.Д., Каплан Л.Р. Инфаркты заднего кровообращения проксимальной внутричерепной территории в Регистре заднего кровообращения Медицинского центра Новой Англии.
евро Neurol
1997
;37
:157
–68,26Бертелут Д., Леклерк Х, Лейс Д., Кривошич Р., Пруво Дж. Церебральная ангиография: изучение осложнений в 450 последовательных процедурах.
J Radiol
1999
;80
:843
–8,27Hankey GJ, Warlow CP, Molyneux AJ. Осложнения церебральной ангиографии у пациентов с легкой ишемией сонной артерии, рассматриваемой для каротидной эндартерэктомии.
J Neurol Neurosurg Psychiatry
1990
;53
:542
–8.28Hankey GJ, Warlow CP, Sellar RJ. Церебральный ангиографический риск при легком цереброваскулярном заболевании.
Ход
1990
;21
:209
–22.29de Bray JM, Pasco A, Tranquart F, Papon X, Alecu C, Giraudeau B, Dubas F, Emile J. Точность цветного допплера при количественной оценке стенозов проксимальных позвоночных артерий.
Цереброваск Дис
2001
;11
:335
–40,30Куль В., Теттенборн Б., Эйке Б.М., Висбек А., Мекес С.Цветное дуплексное ультразвуковое исследование начала позвоночной артерии: нормальные значения скорости кровотока.
J Нейровизуализация
2000
;10
:17
–21,31Visona A, Lusiani L, Castellani V, Ronsisvalle G, Bonanome A, Pagnan A. Эхо-доплеровская (дуплексная) система для выявления окклюзионной болезни позвоночной артерии: сравнение с ангиографией.
J Ultrasound Med
1986
;5
:247
–50,32Bartels E, Flugel KA.Преимущества цветной допплеровской визуализации для оценки позвоночных артерий.
J Neuroimaging
1993
;3
:229
–33.33Ries S, Steinke W, Devuyst G, Artemis N, Valikovics A, Hennerici M. Power Doppler визуализация и цветная допплеровская визуализация потока для оценки нормальных и патологических позвоночных артерий.
J Neuroimaging
1998
;8
:71
–4,34Джонсон К., Грант Р., Дэнси Б., Тейлор Дж., Спайрополус П.Измерение кровотока в позвоночной артерии с помощью цветного дуплексного ультразвукового допплера: установление достоверности выбранных параметров.
Man Ther
2000
;5
:21
–9.35Cher LM, Chambers BR, Smidt V. Сравнение транскраниального допплера с DSA при вертебробазилярной ишемии.
Clin Exp Neurol
1992
;29
:143
–8.36de Bray JM, Missoum A, Dubas F, Emile J, Lhoste P. Обнаружение вертебробазилярных внутричерепных стенозов: транскраниальная допплерография в сравнении с ангиографией.
J Ultrasound Med
1997
;16
:213
–18.37Маркус Х. Транскраниальное допплеровское обнаружение циркулирующих церебральных эмболов: обзор.
Ход
1993
;24
:1246
–50,38Siebler M, Kleinschmidt A, Sitzer M, Steinmetz H, Freund HJ. Церебральная микроэмболия при симптоматическом и бессимптомном стенозе внутренней сонной артерии высокой степени.
Неврология
1994
;44
:615
–18.39Фаррес М.Т., Грабенвогер Ф., Магометшниг Х., Траттниг С., Хеймбергер К., Ламмер Дж. Спиральная КТ-ангиография: исследование стенозов и кальциноза в начале позвоночной артерии.
Нейрорадиология
1996
;38
:738
–43,40Граф Дж., Скутта Б., Кун Ф. П., Ферберт А. Результаты компьютерной томографической ангиографии у 103 пациентов после сосудистых событий в заднем кровообращении: потенциал и клиническая значимость.
J Neurol
2000
;247
:760
–6.41Uchino A, Ohnari N, Ohno M. МРТ окклюзии внутричерепной позвоночной артерии.
Нейрорадиология
1989
;31
:403
–7,42Мейдер П., Меули Р., Гудинчет Ф., Богоуславски Дж. Магнитно-резонансная ангиография при вертебро-базилярных ишемических нарушениях.
Schweiz Rundsch Med Prax
1996
;85
:272
–7,43Бхаделиа Р.А., Бенгоа Ф., Геснер Л., Патель С.К., Узун Дж., Вольперт С.М., Каплан Л.Р. Эффективность МР-ангиографии в обнаружении и характеристике окклюзионных заболеваний вертебробазилярной системы.
J Comput Assist Tomogr
2001
;25
:458
–65,44Phan T, Huston J, III, Bernstein MA, Riederer SJ, Brown RD, Jr. Магнитно-резонансная ангиография сосудов шейки матки с контрастированием: опыт с 422 пациентами.
Ход
2001
;32
:2282
–6,45Benesch CG, Chimowitz MI. Лучшее лечение стеноза внутричерепной артерии? 50 лет неопределенности. Следователи ВАСИД.
Неврология
2000
;55
:465
–6.46Бергер Р. Вертебробазилярная ишемия: показания, методы и результаты хирургического лечения. В: Сосудистая хирургия , 5 изд. Филадельфия, WB Saunders,
2000
:1823
–37,47Ausman JI, Diaz FG, Sadasivan B, Dujovny M. Внутричерепная вертебральная эндартерэктомия.
Нейрохирургия
1990
;26
:465
–71,48Осман Дж. И., Диас Ф. Г., Пирс Дж. Э., Лос-Рейес, Р. А., Лойхтер В., Мехта Б., Патель С.Эндартерэктомия позвоночной артерии от С2 до задней нижней мозжечковой артерии внутричерепно.
Surg Neurol
1982
;18
:400
–4.49Koskas F, Kieffer E, Rancurel G, Bahnini A, Ruotolo C, Illuminati G. Прямая транспозиция дистальной шейной позвоночной артерии во внутреннюю сонную артерию.
Ann Vasc Surg
1995
;9
:515
–24,50Berguer R, Andaya LV, Bauer RB. Шунтирование позвоночной артерии.
Arch Surg
1976
;111
:976
–9,51Berguer R, Bauer RB. Реконструкция позвоночной артерии: успешный метод у отдельных пациентов.
Ann Surg
1981
;193
:441
–7,52Диас Ф.Г., Осман Дж. И., Лос Рейес Р. А., Пирс Дж., Шронц С., Пак Х., Тюркотт Дж. Хирургическая реконструкция проксимальной позвоночной артерии.
J Neurosurg
1984
;61
:874
–81.53Хопкинс Л.Н., Мартин Н.А., Хэдли М.Н., Спецлер Р.Ф., Будни Дж., Картер Л.П. Вертебробазилярная недостаточность. Часть 2. Микрохирургическое лечение внутричерепной вертебробазилярной болезни.
J Neurosurg
1987
;66
:662
–74,54Sundt T., Piepgras D. Операция шунтирования от затылочной до задней нижней мозжечковой артерии.
J Neurosurg
1978
;48
:916
–28,55Bruckmann H, Ringelstein EB, Buchner H, Zeumer H.Чрескожная транслюминальная ангиопластика позвоночной артерии: терапевтическая альтернатива оперативной реконструкции стенозов проксимальных позвоночных артерий.
J Neurol
1986
;233
:336
–9,56Честейн HD, Кэмпбелл М.С., Айер С., Рубин Г.С., Витек Дж., Матур А., Аль Мубарак Н.А., Терри Дж. Б., Йейтс В., Кретцер К., Альред Д., Гомес С.Р. Установка стента экстракраниальной позвоночной артерии: результаты стационарного и последующего наблюдения.
J Neurosurg
1999
;91
:547
–52.57Courtheoux P, Theron J, Maiza D, Henriet JP, Pelouze GA, Derlon JM, Commeau P, Evrard C. Чрескожная транслюминальная ангиопластика при атероматозном стенозе проксимальных надаортальных стволов: брахиоцефального ствола и подключичной артерии.
J Mal Vasc
1986
;11
:113
–19,58Higashida RT, Tsai FY, Halbach VV, Dowd CF, Smith T., Fraser K, Hieshima GB. Транслюминальная ангиопластика при атеросклеротическом поражении позвоночных и базилярных артерий.
J Neurosurg
1993
;78
:192
–8,59Дженкинс Дж.С., Уайт Си Джей, Рами С.Р., Коллинз Т.Дж., Чилакамарри В.К., МакКинли К.Л., Джейн С.П. Стентирование позвоночной артерии.
Катетер Cardiovasc Interv
2001
;54
:1
–5,60Качел Р., Эндерт Дж., Баше С., Гроссманн К., Глейзер Ф. Х. Чрескожная транслюминальная ангиопластика (дилатация) стенозов сонных, позвоночных и безымянных артерий.
Cardiovasc Intervent Radiol
1987
;10
:142
–6.61Malek AM, Higashida RT, Phatouros CC, Lempert TE, Meyers PM, Gress DR, Dowd CF, Halbach VV. Лечение ишемии заднего отдела кровообращения с помощью экстракраниальной чрескожной баллонной ангиопластики и установки стента.
Ход
1999
;30
:2073
–85,62Мукерджи Д., Роффи М., Кападиа С.Р., Бхатт Д.Л., Байзер С., Зиада К.М., Калахасти В., Хьюз К., Ядав Дж.С. Чрескожное вмешательство при симптоматическом стенозе позвоночной артерии с использованием коронарных стентов.
J Инвазивный кардиол
2001
;13
:363
–6.63Piotin M, Spelle L, Martin JB, Weill A, Rancurel G, Ross IB, Rufenacht DA, Chiras J. Чрескожная транслюминальная ангиопластика и стентирование проксимальной позвоночной артерии при симптоматическом стенозе.
AJNR Am J Neuroradiol
2000
;21
:727
–31,64Crawley F, Brown MM, Clifton AG. Ангиопластика и стентирование сонных и позвоночных артерий.
Postgrad Med J
1998
;74
:7
–10.65Стори Г.С., Маркс М.П., Даке М., Норбаш А.М., Штейнберг Г.К. Стентирование позвоночной артерии после чрескожной транслюминальной ангиопластики: техническое примечание.
J Neurosurg
1996
;84
:883
–7.66Roubin GS, Cannon AD, Agrawal SK, Macander PJ, Dean LS, Baxley WA, Breland J. Интракоронарное стентирование при остром и угрожающем закрытии, осложняющем чрескожную транслюминальную коронарную ангиопластику.
Обращение
1992
;85
:916
–27.67Wakhloo AK, Tio FO, Lieber BB, Schellhammer F, Graf M, Hopkins LN. Саморасширяющиеся нитиноловые стенты в позвоночных артериях собак: гемодинамика и реакция тканей.
AJNR Am J Neuroradiol
1995
;16
:1043
–51.68Alazzaz A, Thornton J, Aletich VA, Debrun GM, Ausman JI, Charbel F. Внутричерепная чрескожная транслюминальная ангиопластика при артериосклеротическом стенозе.
Arch Neurol
2000
;57
:1625
–30.69Gomez CR, Orr SC. Ангиопластика и стентирование для первичного лечения стенозов внутричерепных артерий.
Arch Neurol
2001
;58
:1687
–90,70Мори Т., Казита К., Мори К. Церебральная ангиопластика и стентирование при внутричерепном позвоночном атеросклеротическом стенозе.
AJNR Am J Neuroradiol
1999
;20
:787
–9.71Мори Т., Казита К., Чокью К., Мима Т., Мори К. Краткосрочные артериографические и клинические результаты после церебральной ангиопластики и стентирования по поводу внутричерепного вертебробазилярного и каротидного окклюзионного атеросклеротического поражения.
AJNR Am J Neuroradiol
2000
;21
:249
–54,72Нахсер, Хенкес Х., Вебер В., Берг-Даммер Э, Юсри Т.А., Кун Д. Внутричерепной вертебробазилярный стеноз: ангиопластика и последующее наблюдение.
AJNR Am J Neuroradiol
2000
;21
:1293
–301,73Расмуссен П.А., Перл Дж., Барр Дж. Д., Маркарян Г. З., Кацан И., Сила С., Кригер Д., Фурлан А. Дж., Масарик Т. Дж.. Стент-ассистированная ангиопластика внутричерепного вертебробазилярного атеросклероза: первый опыт.
J Neurosurg
2000
;92
:771
–8,74Chimowitz MI. Ангиопластика или стентирование не подходят в качестве терапии первой линии при внутричерепном стенозе.
Arch Neurol
2001
;58
:1690
–2.© Ассоциация врачей
Стеноз внутричерепной артерии, Mayfield Brain & Spine, Цинциннати, Огайо
Обзор
Внутричерепной стеноз — это сужение артерии внутри головного мозга.Накопление бляшек (атеросклероз) внутри стенки артерии снижает приток крови к мозгу. Достаточно серьезный атеросклероз, вызывающий симптомы, сопряжен с высоким риском инсульта и может привести к повреждению мозга и смерти. Лечение направлено на снижение риска инсульта за счет контроля или удаления образования зубного налета и предотвращения образования тромбов.
Кровоснабжение головного мозга
Чтобы понять артериальный стеноз, полезно знать, как кровь циркулирует в головном мозге (см. Анатомия мозга).Кровь перекачивается из сердца и переносится в мозг по двум парным артериям, внутренним сонным артериям и позвоночным артериям (рис. 1). Внутренние сонные артерии питают передние (передние) области, а позвоночные артерии снабжают задние (задние) области мозга. Пройдя через череп, правая и левая позвоночные артерии соединяются вместе, образуя единую базилярную артерию. Базилярная артерия и внутренние сонные артерии соединяются друг с другом в кольце в основании мозга, которое называется Уиллисовым кругом.Артерии, наиболее подверженные стенозу, — это внутренняя сонная артерия (ВСА), средняя мозговая артерия (СМА), позвоночные артерии и базилярная артерия.
Рисунок 1. Внутричерепной стеноз — это сужение артерии внутри головного мозга из-за накопления бляшки внутри артерии. Артерии, наиболее подверженные стенозу, — это внутренняя сонная артерия, средняя мозговая артерия, позвоночные артерии и базилярная артерия.Что такое стеноз внутричерепной артерии?
Внутричерепной стеноз — это сужение артерий внутри головного мозга.Подобно стенозу сонной артерии на шее, он вызывается накоплением налета на внутренней стенке кровеносных сосудов. Это сужение кровеносных сосудов вызывает снижение притока крови к области мозга, кровоснабжающей пораженные сосуды. Стеноз внутричерепной артерии может привести к инсульту тремя способами:
- Зубной налет может становиться все больше и больше, сильно сужая артерию и уменьшая приток крови к мозгу. Зубной налет может в конечном итоге полностью заблокировать (закупорить) артерию.
- Зубной налет может сделать стенку артерии шероховатой и деформировать ее, вызывая образование тромбов и блокируя приток крови к мозгу.
- Зубной налет может разорваться и оторваться, перемещаясь вниз по течению, чтобы застрять в меньшей артерии и блокировать кровоток к мозгу.
Какие симптомы?
Симптомами стеноза внутричерепной артерии являются транзиторная ишемическая атака (ТИА) или инсульт, которые можно описать с помощью мнемоники FAST:
.F: при слабости или обвисании лица, особенно на одной стороне
A: при слабости рук или ног, покалывании или онемении, особенно на одной стороне
S: при невнятной речи
T: на время .Если у вас или у вашего близкого появятся эти симптомы, пора немедленно позвонить в службу экстренной помощи.Симптомы ТИА и инсульта похожи. ТИА возникают, когда приток крови к мозгу временно прерывается, а затем восстанавливается. Симптомы обычно длятся пару минут, а затем полностью исчезают, и человек приходит в норму. Однако нельзя игнорировать TIA; они являются предупреждением о том, что надвигается ишемический инсульт и необратимая травма головного мозга. Если у вас или у вашего близкого появятся эти симптомы, вам следует немедленно позвонить в службу 911.
Каковы причины?
Атеросклероз — основная причина стеноза внутричерепной артерии. Оно может начаться в раннем взрослом возрасте, но симптомы могут не проявляться в течение нескольких десятилетий. У некоторых людей быстро прогрессирует атеросклероз в возрасте тридцати лет, у других — в возрасте пятидесяти или шестидесяти лет. Атеросклероз начинается с повреждения внутренней стенки артерии, вызванного высоким кровяным давлением, диабетом, курением и повышенным уровнем «плохого» холестерина. Другие факторы риска включают ожирение, сердечные заболевания, семейный анамнез и пожилой возраст.
Внутричерепной стеноз связан с несколькими состояниями, включая болезнь моямоя, радиационно-индуцированное повреждение сосудов (васкулопатия), высокое кровяное давление, высокий уровень холестерина и диабет.
Кто пострадал?
Внутричерепной стеноз является причиной от 8 до 10% инсультов в США и затрагивает одни этнические группы больше, чем другие. В эти группы входят афроамериканцы, американцы азиатского происхождения и латиноамериканцы. Пациенты с поражением внутричерепной артерии, как правило, моложе, чем пациенты с поражением сонной артерии на шее.
Как ставится диагноз?
Врач узнает как можно больше о ваших симптомах, текущих и предыдущих медицинских проблемах, текущих лекарствах и семейном анамнезе. Он или она проведет медицинский осмотр. Для обнаружения сужения внутричерепных артерий будут выполнены один или несколько диагностических визуализирующих тестов:
- Компьютерная томография-ангиография или КТ-ангиограмма — это неинвазивный рентгеновский снимок, который позволяет получить подробные изображения анатомических структур головного мозга.Он включает введение контрастного вещества в кровоток, чтобы можно было увидеть артерии головного мозга. Этот тип теста обеспечивает наилучшее изображение как кровеносных сосудов (с помощью ангиографии), так и мягких тканей (с помощью КТ). Это позволяет врачам увидеть суженную артерию и определить, насколько она сужена.
- Магнитно-резонансная ангиография (МРА) аналогична КТ-ангиограмме. Контрастный краситель вводится через капельницу для освещения кровеносных сосудов шеи.
- Ангиограмма — это минимально инвазивный тест, в котором используются рентгеновские лучи и контрастное вещество, вводимое в артерии через катетер в паху. Это позволяет врачам визуализировать все артерии и вены в головном мозге. Он несет низкий риск необратимых неврологических осложнений. Помимо определения области заболевания, ангиография дает ценную информацию о степени стеноза и форме бляшки (рис. 2).
- Транскраниальный допплер Ультразвук — это быстрый и недорогой тест, используемый для измерения скорости кровотока по кровеносным сосудам в головном мозге. Техники измеряют скорость кровотока, испуская высокочастотную звуковую волну от ультразвукового зонда. Разные скорости кровотока отображаются на экране компьютера разными цветами. Чем медленнее кровоток, тем выше риск инсульта.
- Компьютерная томография (КТ) Perfusion — это неинвазивный тест, который определяет кровоток в головном мозге и используется при планировании операции.Он включает введение контрастного вещества в кровоток, чтобы врачи 1) могли изучить, сколько крови достигает головного мозга, и 2) могли определить, какие области мозга наиболее подвержены риску инсульта. Во время теста назначают лекарство под названием Диамокс (ацетазоламид) для расширения артерий. Этот препарат представляет собой своего рода «стресс-тест» для мозга и похож на стресс-тест, используемый для сердца.
- Позитронно-эмиссионная томография (ПЭТ) позволяет врачу изучать функции мозга, наблюдая, как глюкоза (сахар) метаболизируется в головном мозге.Небольшое количество радиоактивной глюкозы попадает в кровоток. Сканер ПЭТ делает снимки мозга, которые интерпретируются компьютером. Результаты могут помочь врачам обнаружить аномалии.
Какие методы лечения доступны?
Целью лечения является снижение риска инсульта. Варианты лечения внутричерепного стеноза различаются в зависимости от степени сужения и наличия у вас симптомов, похожих на инсульт.Пациентам сначала назначают лекарства, и им рекомендуется изменить образ жизни, чтобы снизить риск инсульта. Хирургия ограничивается пациентами, симптомы которых не поддаются лечению.
Лекарства
Внутричерепной стеноз можно лечить с помощью лекарств, сводящих к минимуму факторы риска, включая высокий уровень холестерина и артериальное давление. Если вы курите, вам могут назначить лекарства, которые помогут вам бросить курить. Пациентам с диабетом будет рекомендовано строго контролировать уровень сахара в крови с помощью здоровой диеты и тщательного наблюдения.- Разжижитель крови Лекарства, также называемые антикоагулянтами (аспирин, плавикс, кумадин), позволяют крови легче проходить через суженные артерии и предотвращают свертывание крови. Исследования показывают, что аспирин и кумадин обладают схожими преимуществами. Поскольку антикоагулянты связаны с повышенным риском кровотечения, пациенты могут находиться под наблюдением на предмет аномального кровотечения. Аспирин имеет меньше побочных эффектов, чем кумадин, и связан с меньшим риском кровотечения или кровотечения [1].У пациентов, принимающих кумадин, необходимо периодически контролировать кровь; Пациентам, принимающим аспирин и / или Плавикс, наблюдение не требуется.
- Лекарства , снижающие уровень холестерина, помогают уменьшить образование дополнительных бляшек при атеросклерозе. Эти лекарства могут снизить уровень холестерина ЛПНП (липопротеинов низкой плотности) в среднем на 25-30% в сочетании с диетой с низким содержанием жиров и холестерина.
- Артериальное давление лекарства (диуретики, ингибиторы АПФ, блокаторы ангиотензина, бета-блокаторы, блокаторы кальциевых каналов и т. Д.)) помогают контролировать и регулировать кровяное давление. Поскольку высокое кровяное давление является основным фактором риска инсульта, рекомендуется регулярно проверять кровяное давление и регулярно принимать лекарства.
Хирургия
Целью хирургического вмешательства является предотвращение инсульта путем удаления или уменьшения образования бляшек и расширения артерии, чтобы обеспечить больший приток крови к мозгу. Хирургическое лечение рассматривается для пациентов, симптомы которых не поддаются лечению.Например, у тех, кто продолжает страдать от ТИА или инсульта, у пациентов со стенозом высокой степени и у тех, у кого недостаточное кровоснабжение определенной области мозга.- Баллонная ангиопластика / стентирование — это малоинвазивная эндоваскулярная процедура, при которой происходит сжатие бляшки и увеличение диаметра артерии (рис. 3). Эндоваскулярное лечение означает, что процедура проводится внутри артерии, из кровотока, с помощью небольшого гибкого катетера.Катетер вводят в бедренную артерию в паху во время ангиограммы. Затем катетер продвигается по кровотоку к месту, где расположена артерия, суженная бляшкой. Затем в суженную артерию медленно надувается небольшой баллон, чтобы расширить ее и прижать бляшку к стенке артерии. Рис. 3. Во время ангиопластики катетер с баллонным наконечником помещается в суженный сосуд. Баллон надувается, сжимая бляшку и открывая артерию. После удаления баллона на бляшку помещают саморасширяющуюся сетчатую трубку, называемую стентом, чтобы удерживать артерию открытой.Стент остается в артерии навсегда.
Цель состоит в том, чтобы уменьшить стеноз менее чем на 50%, поскольку небольшое увеличение диаметра сосуда приводит к значительному увеличению притока крови к мозгу. Затем баллон сдувается и удаляется. В некоторых случаях саморасширяющаяся сетчатая трубка, называемая стентом, помещается поверх бляшки, удерживая артерию открытой. Осложнения после ангиопластики могут включать инсульт, разрыв стенки сосуда от катетера или баллона и спазм сосудов.
Ангиопластика обычно рекомендуется пациентам со стенозом артерий высокой степени (более 70%) и рецидивирующими симптомами ТИА или инсульта, несмотря на медикаментозное лечение [2].Ангиопластика / стентирование может успешно уменьшить стеноз до менее 30% без осложнений у 60–80% пациентов [3].
- Шунтирование мозговой артерии — это хирургическая процедура, которая перенаправляет кровоток вокруг области, заблокированной бляшками. Для этой процедуры необходимо сделать отверстие в черепе, что называется трепанацией черепа. Донорская артерия от черепа отделяется от своего нормального положения на одном конце, перенаправляется внутрь черепа и соединяется с артерией на поверхности мозга.Артерия черепа теперь снабжает кровью мозг и обходит заблокированный сосуд (см. Хирургия шунтирования мозгового кровообращения). Осложнения шунтирования могут включать инсульт, спазм сосудов и тромбообразование в донорском сосуде.
Шунтирование обычно рекомендуется, когда артерия заблокирована на 100% и ангиопластика невозможна. Результаты обходного анастомоза сильно различаются в зависимости от места и типа обходного анастомоза. Спросите своего хирурга, каких результатов вы можете ожидать.
Клинические испытания
Клинические испытания — это научные исследования, в ходе которых новые методы лечения — лекарства, диагностика, процедуры и другие методы лечения — тестируются на людях, чтобы убедиться, что они безопасны и эффективны.Постоянно проводятся исследования по повышению уровня медицинского обслуживания. Информацию о текущих клинических испытаниях, включая право на участие, протокол и места проведения, можно найти в Интернете. Исследования могут спонсироваться Национальными институтами здравоохранения (см. Clinicaltrials.gov), а также частными промышленными и фармацевтическими компаниями (см. Centerwatch.com).Восстановление и профилактика
Несмотря на медикаментозное лечение, пациенты, перенесшие инсульт или ТИА из-за стеноза внутричерепной артерии, сталкиваются с 12–14% -ным риском повторного инсульта в течение 2-летнего периода после первоначального инсульта.В некоторых группах высокого риска годовой риск повторного инсульта может превышать 20% [4].
После ангиопластики рестеноз может возникнуть у 7,5–32,4% пациентов и обычно не имеет симптомов. Долгосрочный результат профилактики инсульта после ангиопластики еще не известен, но краткосрочные результаты многообещающие и в настоящее время изучаются в клинических испытаниях.
Важно понимать, что атеросклероз — прогрессирующее заболевание. Чтобы предотвратить инсульт, ваш врач может попросить вас бросить курить, ограничить употребление алкоголя, поддерживать хороший контроль уровня сахара в крови (если у вас диабет), снизить уровень холестерина и принимать лекарства в соответствии с предписаниями.
Источники и ссылки
Если у вас есть дополнительные вопросы, свяжитесь с Mayfield Brain & Spine по телефону 800-325-7787 или 513-221-1100.
Источники
- Chimowitz MI, et al. Сравнение варфарина и аспирина при симптоматическом стенозе внутричерепных артерий. N Engl J Med 352 (13): 1305-16, 2005
- Meyers PM и др.: Показания для выполнения внутричерепных эндоваскулярных нейроинтервенционных процедур: научное заявление.Тираж 119: 2235–2249, 2009 г. .
- Рингер А.Дж., Абруццо Т. и др. Ангиопластика и стентирование для лечения внутричерепного стеноза. In, Геморрагический и ишемический инсульт: хирургические, интервенционные, визуальные и медицинские подходы. Нью-Йорк, Тим, 2010
- Куреши А.И. и др. Консенсус-конференция по внутричерепному атеросклеротическому заболеванию: обоснование, методология и результаты. J Neuroimaging 19 Suppl 1: 1S-10S, 2009.
Ссылки
StrokeAssociation.orgStroke.org
ангиопластика: эндоваскулярная процедура с использованием катетера с баллонным наконечником для увеличения сужения артерии.
атеросклероз: заболевание артериальных кровеносных сосудов, при котором стенки артерий утолщаются и становятся твердыми бляшками. Бляшки состоят из холестерина и других липидов, воспалительных клеток и отложений кальция; также называется «затвердение артерий».”
ишемический инсульт: инсульт, вызванный прерыванием или блокировкой притока богатой кислородом крови к определенной области мозга; вызвано сгустком крови, атеросклерозом, спазмом сосудов или пониженным кровяным давлением.
Холестерин ЛПНП: Холестерин липопротеинов низкой плотности является первичной молекулой холестерина. Высокий уровень ЛПНП, прозванного «плохим» холестерином, увеличивает риск атеросклероза.
стент : трубчатое устройство, которое вставляется в сосуд или проход, чтобы держать его открытым.
преходящая ишемическая атака (ТИА): «мини-инсульт», вызванный, когда приток крови к мозгу временно прерывается, а затем восстанавливается; не вызывает необратимого повреждения мозга.
спазм сосудов : аномальное сужение или сужение артерий из-за раздражения стенки сосуда или кровью в субарахноидальном пространстве.
обновлено> 4.2018
рассмотрено> Эндрю Рингер, доктор медицины, клиника Мэйфилд, Цинциннати, ОгайоСертифицированная медицинская информация Mayfield материалов написаны и разработаны клиникой Mayfield Clinic.Мы соблюдаем стандарт HONcode в отношении достоверной информации о здоровье. Эта информация не предназначена для замены медицинских рекомендаций вашего поставщика медицинских услуг.
Стеноз позвоночной артерии — обзор
Японское исследование MELT было организовано для определения безопасности и клинической эффективности внутриартериальной инфузии урокиназы (Великобритания) у пациентов с инсультом в течение 6 часов от начала. Популяция пациентов была аналогична исследованию PROACT, где пациенты с ишемическим инсультом, поступившие в течение 6 часов с момента начала и показавшие ангиографические окклюзии части M1 или M2 средней мозговой артерии, были рандомизированы в британские или контрольные группы.Клинические исходы оценивали по модифицированной шкале Рэнкина (mRS), шкале инсульта Национального института здравоохранения (NIHSS) и индексу Бартеля (BI). Первичным результатом был процент пациентов, достигших независимого статуса, определяемого как mRS от 0 до 2. После одобрения IV rt-PA в Японии Независимый комитет по мониторингу рекомендовал прекратить испытание. На тот момент рандомизацию прошли 114 пациентов, по 57 пациентов в каждой группе. Первичная конечная точка независимого результата через 90 дней была несколько чаще в британской группе, чем в контрольной группе (49.1% и 38,6%; ИЛИ 1,54; 95% ДИ 0,73–3,23), но не достиг статистической значимости ( P = 0,35). Однако отличный функциональный результат (модифицированная шкала Рэнкина от 0 до 1) через 90 дней, заранее запланированная вторичная конечная точка, был более частым в британской группе, чем в контрольной группе (42,1% и 22,8%; P = 0,045; ИЛИ, 2,46; 95% ДИ 1,09–5,54). В группе из Великобритании было значительно больше пациентов с шкалой инсульта 0 или 1 Национального института здоровья через 90 дней, чем в контрольной группе ( P = 0.02). Кумулятивная смертность за 90 дней составила 5,3% в группе Великобритании и 3,5% в контрольной группе ( P = 1,00), а симптоматическое внутричерепное кровоизлияние в течение 24 часов после лечения произошло у 9% и 2%, соответственно ( P ). = 0,21). Исследователи и редакторы пришли к выводу, что, несмотря на преждевременное прерывание исследования и отсутствие статистической значимости первичной конечной точки, вторичный анализ предполагает, что внутриартериальный фибринолиз может повысить вероятность отличного функционального результата. 35
Внутриартериальный тромболизис в заднем кровообращении
Инсульт в области заднего кровообращения в некоторых отношениях отличается от ишемического инсульта в распределении сонных артерий. Сообщения о естественном течении инсульта из-за окклюзии базиляра или двусторонней окклюзии позвоночной артерии показывают мрачный прогноз со смертностью 70–80%. 36–40 Кроме того, развитие клинических признаков инсульта заднего кровообращения отличается от такового при переднем кровообращении.В переднем круге кровообращения появление симптомов часто сопровождается резкой закупоркой сосуда. В области заднего кровообращения может наблюдаться постепенное развитие симптомов, а не внезапный серьезный клинический дефицит. 36,41,42 Это вызывает трудности с точным определением времени появления симптомов и, следовательно, с оценкой сроков восстановления перфузии. Кроме того, пациенты с инфарктами заднего кровообращения часто имеют тяжелую внутричерепную болезнь крупных артерий. 43,44 Внутричерепной атеросклероз с супервентирующим тромбозом in situ чаще встречается в заднем круге кровообращения, чем при инсульте переднего кровообращения (рис. 65-2). Следовательно, фибринолитические агенты могут очистить только один компонент окклюзионного поражения, оставляя высокий потенциал для повторного тромбоза. 15,23,27 Учитывая потенциально более медленное прогрессирование инфаркта заднего кровообращения и снижение риска геморрагической трансформации из-за меньшего объема ткани, подверженной риску, терапия внутриартериальным тромболизисом после 6 часов может быть более эффективной и безопасной. в заднем, чем переднем, кровообращении.Сообщенные серии включали пациентов в срок до 24 часов после появления симптомов. 15,17,27,45,46
Mitchell et al. Сообщили о нерандомизированном пилотном исследовании, оценивающем безопасность и эффективность IA-урокиназы у пациентов с инсультом заднего кровообращения. 47 Шестнадцать пациентов прошли курс лечения в течение 24 часов с момента появления симптомов. Полная или частичная реканализация первоначально была достигнута у 13 из 16 пациентов (82%). Из них у двух произошла повторная окклюзия в течение 24 часов с окончательной степенью реканализации 69%.Шестимесячный функциональный статус оценивался неврологом, который не знал о степени реканализации с хорошим результатом, определенным как равный или превышающий 60 по индексу Бартеля. 11 (69%) пациентов выжили, девять (56%) с хорошим результатом. результат, в то время как двое (13%) остались инвалидами. Реканализация коррелировала с улучшением выживаемости. Авторы приходят к выводу, что ИА тромболизис в заднем круге кровообращения является безопасным и возможным, способным обеспечить реканализацию у значительного числа пациентов.
После этого первоначального пилотного исследования было проведено рандомизированное австралийское исследование инсульта урокиназы. 48 Пациенты с острым ишемическим инсультом заднего кровообращения в возрасте от 18 до 85 лет были рандомизированы для получения IA урокиназы или плацебо. Все пациенты получали острую антикоагулянтную терапию (5000 МЕ гепарина внутриартериально с последующей внутривенной гепаринизацией до целевого АЧТВ 60–80 секунд в течение минимум 2 дней), а затем перорально принимали варфарин до целевого МНО 1,5–2,5 в течение 6 месяцев. Лечение необходимо было начать в течение 24 часов после начала инсульта. Исследование было прекращено в июне 2003 г. из-за медленного набора и вывода урокиназы с рынка.Шестнадцать пациентов были набраны до завершения исследования. Исследователи сообщили о результатах для этих 16 пациентов. 48 Анализируя первичный результат, семь из восьми пациентов в группе антикоагуляции и четыре из восьми пациентов в группе урокиназы были мертвы или инвалидами через 6 месяцев (отношение шансов [OR], 0,14; 95% доверительный интервал [CI], 0,02 –1,43; P = 0,28). В протоколе указан анализ подгрупп в зависимости от времени до лечения. Из восьми пациентов, пролеченных в течение 12 часов после появления симптомов, пятеро получили урокиназу, а трое — нет.Выживаемость без инвалидности составляла 2/5 для пациентов с урокиназой и 1/3 для тех, кто получал только антикоагулянты (OR, 1,3; 95% CI, 0,07–26,6). Из восьми пациентов, пролеченных между 12 и 24 часами после появления симптомов, трое получали урокиназу, а пятеро — нет; Выживаемость без инвалидности составляла 2/3 для пациентов с урокиназой и 0/5 для тех, кто получал только антикоагулянты (OR 0,05; 95% ДИ 0,0–1,9). Среди выживших средний показатель mRS был один в группе лечения по сравнению с тремя в контрольной группе. Было восемь смертей; по четыре в каждой группе.Было одно бессимптомное кровоизлияние в мозг в группе урокиназы и ни одного в группе антикоагуляции.
Хотя это небольшое исследование не предоставляет окончательных доказательств для ведения пациентов с острым инсультом заднего кровообращения, оно может предоставить полезную информацию для планирования будущих исследований. Несмотря на то, что пациенты, получавшие лечение в течение 12 часов или дольше, казалось, получали пользу от тромболизиса IA, ни один из пациентов в группе антикоагуляции не чувствовал себя хорошо, если лечился более 12 часов.
Оценка
Визуализация позвоночных и базилярных артерий с помощью артериографии важна для диагностики и лечения.Неинвазивная КТА или МРА обычно используется для визуализации позвоночно-базилярной системы для определения стеноза или окклюзии. КТА дает хорошие изображения как внутричерепных, так и экстракраниальных сосудов [9]. Экстракраниальный сосуд может потребовать МРА с контрастированием из-за артефактов глотания. При проведении КТА следует соблюдать осторожность, учитывая нефротоксичность контраста и радиационного воздействия. При нарушении функции почек контраст с гадолинием MR может также привести к редкому осложнению нефрогенного системного фиброза (NSF), также известного как нефрогенная фиброзирующая дермопатия (NFD).МРТ всегда является лучшим методом визуализации при проблемах ствола мозга и задней черепной ямки, особенно острого инфаркта ствола мозга, с диффузионно-взвешенной визуализацией.
Другая патология, такая как кавернома ствола мозга или поражения мозжечкового моста, включая акустическую шванному и дермоидные / эпидермоидные кисты, которые могут быть убедительно идентифицированы с помощью МРТ. Дуплексное ультразвуковое исследование также может использоваться для выявления аномалий позвоночной артерии, хотя и с некоторыми ограничениями. Хотя визуализировать V1 и V2 сложно, дуплексное ультразвуковое исследование может обнаружить изменения скорости потока от стеноза проксимального отдела позвоночника или подключичного обкрадывания.Для пациентов старше 45 лет обследование должно включать выявление факторов риска, которые могут вызвать VBI, таких как уровень холестерина, липидов, уровень сахара в крови, артериальное давление и отказ от курения. Если пациенту моложе 45 лет, показано дальнейшее обследование, чтобы исключить кардиоэмболическую причину, состояния гиперкоагуляции, расслоение позвонков и фиброзно-мышечную дисплазию.
Анализ крови должен включать полный общий анализ крови, электролиты, функцию почек, профиль коагуляции, липидный профиль и функцию печени.У более молодых пациентов следует также исследовать наличие люпинового антикоагулянта, лейденской мутации белков C, S и фактора V.
ЭКГ может выявить ишемические изменения, аритмию (фибрилляцию предсердий) или ИМ.
Молодые пациенты также должны пройти эхокардиограмму для определения наличия вегетаций, пороков клапанов, шунтов справа налево или тромбов.
Лечение / ведение
Как и в случае ишемических инсультов в переднем круге кровообращения, лечение вертебробазилярной болезни требует незамедлительного лечения.Предыдущие транзиторные эпизоды (ТИА) могут сигнализировать о начале инфаркта в будущем. Если установлено, что причина эмболии является кардиогенной, скорее всего, из-за фибрилляции предсердий или механических клапанов сердца, то показана антикоагулянтная терапия. Расслоение позвонка, вторичное по отношению к травме, хотя и не так часто, но также может быть источником эмболии, которую можно лечить снова с помощью антитромботических средств. В противном случае лечение зависит от снижения таких факторов риска, как курение, холестерин и гипертония. В острых случаях симптомы часто зависят от давления / перфузии.Возможно, потребуется увеличить перфузию с помощью внутривенного введения жидкости и попытаться избежать снижения артериального давления. В долгосрочной перспективе более строгий контроль артериального давления важен для вторичной профилактики инсульта. Подобно всем типам ишемических событий, вторичная профилактика потребует комплексного подхода, включая контроль АД, отказ от курения, строгий контроль уровня сахара в крови, использование статинов, изменение образа жизни, включая диету и упражнения [10]. Хирургические возможности очень ограничены [11]. Это зависит от расположения налета и эффективности ремонта.Чем дальше от головного мозга находится окклюзия, тем выше вероятность хирургического вмешательства [12]. Критерии хирургического вмешательства зависят от:
Существует 2 варианта хирургического восстановления: открытое хирургическое вмешательство и эндоваскулярное лечение. Открытое хирургическое вмешательство включает обходной трансплантат над стенозированной зоной. Прямая транспозиция артерии помещает артерию в соседний здоровый сосуд и соединяет две части [13]. Наиболее распространенной процедурой является эндоваскулярная реконструкция, при которой стент вводится через катетер в паху. Затем в стенозированную позвоночную артерию помещают баллон с последующим размещением стента [14].
Все пациенты с инсультом позвоночной артерии должны быть госпитализированы в отделение интенсивной терапии, особенно если они гемодинамически нестабильны, имеют неустойчивые неврологические симптомы, имеют другие сопутствующие заболевания и являются кандидатами на тромболитическую терапию.
После стабилизации состояния пациента решение о лечении зависит от продолжительности симптомов. Если пациенты поступают в течение 4,5 часов после появления симптомов, tPA эффективен. Можно использовать антикоагулянты, но нет доказательств того, что они могут улучшить исходы.
Ангиопластика часто выполняется пациентам со стенозом базилярной артерии, но ее роль в инсульте позвоночной артерии остается неопределенной.
Прогноз
Прогноз после инсульта позвоночной артерии зависит от тяжести, возраста пациента и других сопутствующих заболеваний. Также существует 10-15% риск рецидива. Даже при незначительном инсульте заболеваемость высока. Выжившие пациенты часто нуждаются в обширной реабилитации в течение многих месяцев, и даже тогда могут наблюдаться остаточные неврологические нарушения.
Осложнения
Анамнез и физика
Наиболее частые находки в анамнезе пациента, позволяющие предположить, что VBI включают факторы риска сердечно-сосудистых заболеваний, таких как атеросклероз и пожилой возраст.Следует провести тщательный сбор анамнеза и медицинский осмотр, уделяя особое внимание не только неврологическому, но и кардиологическому обследованию на предмет таких состояний, как аритмия, которые также могут вызывать симптомы. Симптомы VBI являются результатом ишемии различных частей мозга, снабжаемых задним кровообращением.
Симптомы включают:
Если VBI переходит в инфаркт ствола мозга, может возникнуть несколько синдромов. локализация, такая как латеральный медуллярный синдром, медиальный медуллярный синдром, синдром базилярной артерии и окклюзия лабиринтной артерии.Другими аспектами анамнеза, которые следует отметить во время физического осмотра, являются воспроизводимые симптомы при смене положения головы, то есть обморок при повороте головы в сторону (синдром Боу-Хантера) или во время разгибания головы [6] [7] [8].
Физический осмотр
Результаты являются обычными после инсульта позвоночной артерии и могут включать следующее:
быть приняты, чтобы исключить другие более доброкачественные c состояния, которые также могут вызывать аналогичные симптомы, такие как лабиринтит, вестибулярный неврит и доброкачественное пароксизмальное позиционное головокружение (ДППГ).Головокружение — частый симптом VBI. Это также центральный симптом более доброкачественных периферических вестибулярных расстройств. В отделении неотложной помощи особенно важно различать головокружение, вызванное периферическими вестибулярными нарушениями, и центральными вестибулярными проблемами, чаще всего связанными с вертебробазилярной недостаточностью (VBI), которые могут потребовать госпитализации. Головокружение само по себе не может быть диагностировано как ТИА или ВБИ. Головокружение при наличии признаков или симптомов ствола мозга является диагностическим признаком ТИА вертебробазилярной территории.Очень важно физикальное обследование для выявления признаков ствола мозга или аномалий черепных нервов. Полезно наличие признаков или симптомов контралатеральной конечности. Тип нистагма, такой как вертикальный нистагм или нистагм с изменением направления, указывает на VBI. Если выполнить и правильно интерпретировать тест с выталкиванием головы, можно отличить периферическое головокружение от центрального головокружения из-за VBI у постели больного. Положительный тест на толчок головой указывает на периферическую причину головокружения.
Инсульт позвоночной артерии связан с множеством синдромов в зависимости от клинических проявлений.Некоторые из этих синдромов включают:
Оценка
Визуализация позвоночных и базилярных артерий с помощью артериографии важна для диагностики и лечения.Неинвазивная КТА или МРА обычно используется для визуализации позвоночно-базилярной системы для определения стеноза или окклюзии. КТА дает хорошие изображения как внутричерепных, так и экстракраниальных сосудов [9]. Экстракраниальный сосуд может потребовать МРА с контрастированием из-за артефактов глотания. При проведении КТА следует соблюдать осторожность, учитывая нефротоксичность контраста и радиационного воздействия. При нарушении функции почек контраст с гадолинием MR может также привести к редкому осложнению нефрогенного системного фиброза (NSF), также известного как нефрогенная фиброзирующая дермопатия (NFD).МРТ всегда является лучшим методом визуализации при проблемах ствола мозга и задней черепной ямки, особенно острого инфаркта ствола мозга, с диффузионно-взвешенной визуализацией.
Другая патология, такая как кавернома ствола мозга или поражения мозжечкового моста, включая акустическую шванному и дермоидные / эпидермоидные кисты, которые могут быть убедительно идентифицированы с помощью МРТ. Дуплексное ультразвуковое исследование также может использоваться для выявления аномалий позвоночной артерии, хотя и с некоторыми ограничениями. Хотя визуализировать V1 и V2 сложно, дуплексное ультразвуковое исследование может обнаружить изменения скорости потока от стеноза проксимального отдела позвоночника или подключичного обкрадывания.Для пациентов старше 45 лет обследование должно включать выявление факторов риска, которые могут вызвать VBI, таких как уровень холестерина, липидов, уровень сахара в крови, артериальное давление и отказ от курения. Если пациенту моложе 45 лет, показано дальнейшее обследование, чтобы исключить кардиоэмболическую причину, состояния гиперкоагуляции, расслоение позвонков и фиброзно-мышечную дисплазию.
Анализ крови должен включать полный общий анализ крови, электролиты, функцию почек, профиль коагуляции, липидный профиль и функцию печени.У более молодых пациентов следует также исследовать наличие люпинового антикоагулянта, лейденской мутации белков C, S и фактора V.
ЭКГ может выявить ишемические изменения, аритмию (фибрилляцию предсердий) или ИМ.
Молодые пациенты также должны пройти эхокардиограмму для определения наличия вегетаций, пороков клапанов, шунтов справа налево или тромбов.
Лечение / ведение
Как и в случае ишемических инсультов в переднем круге кровообращения, лечение вертебробазилярной болезни требует незамедлительного лечения.Предыдущие транзиторные эпизоды (ТИА) могут сигнализировать о начале инфаркта в будущем. Если установлено, что причина эмболии является кардиогенной, скорее всего, из-за фибрилляции предсердий или механических клапанов сердца, то показана антикоагулянтная терапия. Расслоение позвонка, вторичное по отношению к травме, хотя и не так часто, но также может быть источником эмболии, которую можно лечить снова с помощью антитромботических средств. В противном случае лечение зависит от снижения таких факторов риска, как курение, холестерин и гипертония. В острых случаях симптомы часто зависят от давления / перфузии.Возможно, потребуется увеличить перфузию с помощью внутривенного введения жидкости и попытаться избежать снижения артериального давления. В долгосрочной перспективе более строгий контроль артериального давления важен для вторичной профилактики инсульта. Подобно всем типам ишемических событий, вторичная профилактика потребует комплексного подхода, включая контроль АД, отказ от курения, строгий контроль уровня сахара в крови, использование статинов, изменение образа жизни, включая диету и упражнения [10]. Хирургические возможности очень ограничены [11]. Это зависит от расположения налета и эффективности ремонта.Чем дальше от головного мозга находится окклюзия, тем выше вероятность хирургического вмешательства [12]. Критерии хирургического вмешательства зависят от:
Существует 2 варианта хирургического восстановления: открытое хирургическое вмешательство и эндоваскулярное лечение. Открытое хирургическое вмешательство включает обходной трансплантат над стенозированной зоной. Прямая транспозиция артерии помещает артерию в соседний здоровый сосуд и соединяет две части [13]. Наиболее распространенной процедурой является эндоваскулярная реконструкция, при которой стент вводится через катетер в паху. Затем в стенозированную позвоночную артерию помещают баллон с последующим размещением стента [14].
Все пациенты с инсультом позвоночной артерии должны быть госпитализированы в отделение интенсивной терапии, особенно если они гемодинамически нестабильны, имеют неустойчивые неврологические симптомы, имеют другие сопутствующие заболевания и являются кандидатами на тромболитическую терапию.
После стабилизации состояния пациента решение о лечении зависит от продолжительности симптомов. Если пациенты поступают в течение 4,5 часов после появления симптомов, tPA эффективен. Можно использовать антикоагулянты, но нет доказательств того, что они могут улучшить исходы.
Ангиопластика часто выполняется пациентам со стенозом базилярной артерии, но ее роль в инсульте позвоночной артерии остается неопределенной.
Прогноз
Прогноз после инсульта позвоночной артерии зависит от тяжести, возраста пациента и других сопутствующих заболеваний. Также существует 10-15% риск рецидива. Даже при незначительном инсульте заболеваемость высока. Выжившие пациенты часто нуждаются в обширной реабилитации в течение многих месяцев, и даже тогда могут наблюдаться остаточные неврологические нарушения.
Осложнения
Анамнез и физика
Наиболее частые находки в анамнезе пациента, позволяющие предположить, что VBI включают факторы риска сердечно-сосудистых заболеваний, таких как атеросклероз и пожилой возраст.Следует провести тщательный сбор анамнеза и медицинский осмотр, уделяя особое внимание не только неврологическому, но и кардиологическому обследованию на предмет таких состояний, как аритмия, которые также могут вызывать симптомы. Симптомы VBI являются результатом ишемии различных частей мозга, снабжаемых задним кровообращением.
Симптомы включают:
Если VBI переходит в инфаркт ствола мозга, может возникнуть несколько синдромов. локализация, такая как латеральный медуллярный синдром, медиальный медуллярный синдром, синдром базилярной артерии и окклюзия лабиринтной артерии.Другими аспектами анамнеза, которые следует отметить во время физического осмотра, являются воспроизводимые симптомы при смене положения головы, то есть обморок при повороте головы в сторону (синдром Боу-Хантера) или во время разгибания головы [6] [7] [8].
Физический осмотр
Результаты являются обычными после инсульта позвоночной артерии и могут включать следующее:
быть приняты, чтобы исключить другие более доброкачественные c состояния, которые также могут вызывать аналогичные симптомы, такие как лабиринтит, вестибулярный неврит и доброкачественное пароксизмальное позиционное головокружение (ДППГ).Головокружение — частый симптом VBI. Это также центральный симптом более доброкачественных периферических вестибулярных расстройств. В отделении неотложной помощи особенно важно различать головокружение, вызванное периферическими вестибулярными нарушениями, и центральными вестибулярными проблемами, чаще всего связанными с вертебробазилярной недостаточностью (VBI), которые могут потребовать госпитализации. Головокружение само по себе не может быть диагностировано как ТИА или ВБИ. Головокружение при наличии признаков или симптомов ствола мозга является диагностическим признаком ТИА вертебробазилярной территории.Очень важно физикальное обследование для выявления признаков ствола мозга или аномалий черепных нервов. Полезно наличие признаков или симптомов контралатеральной конечности. Тип нистагма, такой как вертикальный нистагм или нистагм с изменением направления, указывает на VBI. Если выполнить и правильно интерпретировать тест с выталкиванием головы, можно отличить периферическое головокружение от центрального головокружения из-за VBI у постели больного. Положительный тест на толчок головой указывает на периферическую причину головокружения.
Инсульт позвоночной артерии связан с множеством синдромов в зависимости от клинических проявлений.Некоторые из этих синдромов включают:
Оценка
Визуализация позвоночных и базилярных артерий с помощью артериографии важна для диагностики и лечения.Неинвазивная КТА или МРА обычно используется для визуализации позвоночно-базилярной системы для определения стеноза или окклюзии. КТА дает хорошие изображения как внутричерепных, так и экстракраниальных сосудов [9]. Экстракраниальный сосуд может потребовать МРА с контрастированием из-за артефактов глотания. При проведении КТА следует соблюдать осторожность, учитывая нефротоксичность контраста и радиационного воздействия. При нарушении функции почек контраст с гадолинием MR может также привести к редкому осложнению нефрогенного системного фиброза (NSF), также известного как нефрогенная фиброзирующая дермопатия (NFD).МРТ всегда является лучшим методом визуализации при проблемах ствола мозга и задней черепной ямки, особенно острого инфаркта ствола мозга, с диффузионно-взвешенной визуализацией.
Другая патология, такая как кавернома ствола мозга или поражения мозжечкового моста, включая акустическую шванному и дермоидные / эпидермоидные кисты, которые могут быть убедительно идентифицированы с помощью МРТ. Дуплексное ультразвуковое исследование также может использоваться для выявления аномалий позвоночной артерии, хотя и с некоторыми ограничениями. Хотя визуализировать V1 и V2 сложно, дуплексное ультразвуковое исследование может обнаружить изменения скорости потока от стеноза проксимального отдела позвоночника или подключичного обкрадывания.Для пациентов старше 45 лет обследование должно включать выявление факторов риска, которые могут вызвать VBI, таких как уровень холестерина, липидов, уровень сахара в крови, артериальное давление и отказ от курения. Если пациенту моложе 45 лет, показано дальнейшее обследование, чтобы исключить кардиоэмболическую причину, состояния гиперкоагуляции, расслоение позвонков и фиброзно-мышечную дисплазию.
Анализ крови должен включать полный общий анализ крови, электролиты, функцию почек, профиль коагуляции, липидный профиль и функцию печени.У более молодых пациентов следует также исследовать наличие люпинового антикоагулянта, лейденской мутации белков C, S и фактора V.
ЭКГ может выявить ишемические изменения, аритмию (фибрилляцию предсердий) или ИМ.
Молодые пациенты также должны пройти эхокардиограмму для определения наличия вегетаций, пороков клапанов, шунтов справа налево или тромбов.
Лечение / ведение
Как и в случае ишемических инсультов в переднем круге кровообращения, лечение вертебробазилярной болезни требует незамедлительного лечения.Предыдущие транзиторные эпизоды (ТИА) могут сигнализировать о начале инфаркта в будущем. Если установлено, что причина эмболии является кардиогенной, скорее всего, из-за фибрилляции предсердий или механических клапанов сердца, то показана антикоагулянтная терапия. Расслоение позвонка, вторичное по отношению к травме, хотя и не так часто, но также может быть источником эмболии, которую можно лечить снова с помощью антитромботических средств. В противном случае лечение зависит от снижения таких факторов риска, как курение, холестерин и гипертония. В острых случаях симптомы часто зависят от давления / перфузии.Возможно, потребуется увеличить перфузию с помощью внутривенного введения жидкости и попытаться избежать снижения артериального давления. В долгосрочной перспективе более строгий контроль артериального давления важен для вторичной профилактики инсульта. Подобно всем типам ишемических событий, вторичная профилактика потребует комплексного подхода, включая контроль АД, отказ от курения, строгий контроль уровня сахара в крови, использование статинов, изменение образа жизни, включая диету и упражнения [10]. Хирургические возможности очень ограничены [11]. Это зависит от расположения налета и эффективности ремонта.Чем дальше от головного мозга находится окклюзия, тем выше вероятность хирургического вмешательства [12]. Критерии хирургического вмешательства зависят от:
Существует 2 варианта хирургического восстановления: открытое хирургическое вмешательство и эндоваскулярное лечение. Открытое хирургическое вмешательство включает обходной трансплантат над стенозированной зоной. Прямая транспозиция артерии помещает артерию в соседний здоровый сосуд и соединяет две части [13]. Наиболее распространенной процедурой является эндоваскулярная реконструкция, при которой стент вводится через катетер в паху. Затем в стенозированную позвоночную артерию помещают баллон с последующим размещением стента [14].
Все пациенты с инсультом позвоночной артерии должны быть госпитализированы в отделение интенсивной терапии, особенно если они гемодинамически нестабильны, имеют неустойчивые неврологические симптомы, имеют другие сопутствующие заболевания и являются кандидатами на тромболитическую терапию.
После стабилизации состояния пациента решение о лечении зависит от продолжительности симптомов. Если пациенты поступают в течение 4,5 часов после появления симптомов, tPA эффективен. Можно использовать антикоагулянты, но нет доказательств того, что они могут улучшить исходы.
Ангиопластика часто выполняется пациентам со стенозом базилярной артерии, но ее роль в инсульте позвоночной артерии остается неопределенной.
Прогноз
Прогноз после инсульта позвоночной артерии зависит от тяжести, возраста пациента и других сопутствующих заболеваний. Также существует 10-15% риск рецидива. Даже при незначительном инсульте заболеваемость высока. Выжившие пациенты часто нуждаются в обширной реабилитации в течение многих месяцев, и даже тогда могут наблюдаться остаточные неврологические нарушения.

