Что такое pH? Шкала и методы измерения pH
Сегодня аббревиатуру pH можно увидеть не только на уроках химии, но и на упаковках товаров бытовой химии, личной гигиены, косметики и прочих. Что такое pH мы объясним буквально на пальцах в нашей статье, а также расскажем о методах его измерения.
Показатель Ph еще называют водородным, по значению которого судят, каким является раствор — кислым, нейтральным или щелочным. Измерить показатель pH можно с помощью индикаторов — веществ, изменяющих цвет в разной среде.
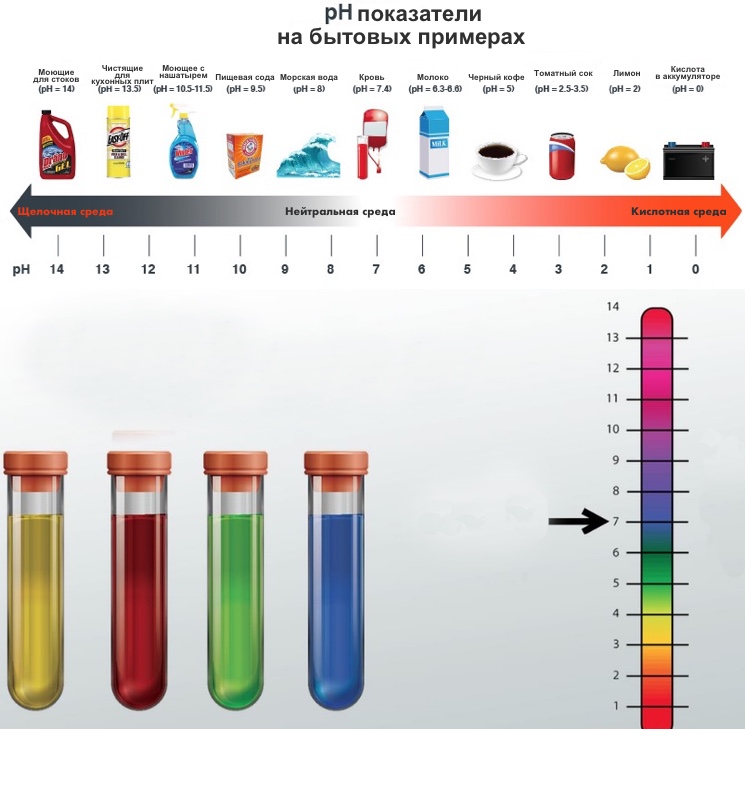
Шкала pH — показатель кислого, нейтрального или щелочного раствора
Водородный показатель pH (сокращенное от английского «power of hydrogen») позволяет судить о том, каким является раствор — кислым, нейтральным или щелочным.
Обычный интервал значений pH от 1 до 14. Значение pH определяется концентрацией ионов водорода в растворе. Нейтральные (ни кислые, ни щелочные) растворы характеризуются значением pH около 7. Чем ниже значения pH, тем сильнее кислота. Уксусная кислота, считающаяся слабой, имеет pH около 5. Сильные кислоты имеют значение pH, близкое к нулю, или даже отрицательное значение pH.
Видео для более углубленного изучения pH. Необходимы базовые знания по химии.
Щелочные растворы имеют pH выше 7; pH растворов сильных щелочей, таких как гидроксид натрия, NaOH, равен 14, а может быть и больше.
От чего зависит уровень кислотности
При добавлении кусочков цинка к соляной кислоте металл быстро реагирует и растворяется. Однако даже концентрированная лимонная кислота не оказывает никакого действия на цинк. Органические кислоты, такие как лимонная и уксусная, являются слабыми кислотами. Неорганические, такие как серная, соляная, относятся к сильным кислотам.
Растворы сильных кислот состоят только из ионов водорода и ионов кислотного остатка. Растворы более слабых кислот содержат также и неионизируемые молекулы.
Измерение pH
Простейший способ измерения pH среды — использование индикатора. Индикаторы — это вещества, принимающие различную окраску при разных значениях pH.
Лакмус, например, — это индикатор растительного происхождения, который краснеет в кислой среде и и синеет в щелочной. С помощью лакмуса или лакмусовой бумажки можно узнать, кислая среда или щелочная. Другие индикаторы меняют цвет в более узких интервалах pH.
Метиловый оранжевый, например, изменяет цвет в интервале pH 3-4,5. Использование комбинаций индикаторов позволяет довольно точно определить водородный показатель.
Более точно измерить pH раствора можно прибором, называемым pH-метром. В нем используется специальный электрод, регистрирующий концентрацию ионов водорода, а значения выводятся на шкалу.
Незначительное изменение pH влияет на живущие в воде организмы. Для измерения pH воды биологи используют электронные pH-метры, измеряющие водородный показатель среды с точностью до 0,1.
Ионизация и сила кислоты
Значение pH сильной кислоты показывает, что все ее молекулы диссоциированы (расщеплены) на ионы водорода и ионы кислородного остатка. Слабые кислоты ионизированы только частично, и только небольшая часть их молекул диссоциирована с образованием ионов водорода. В итоге их растворы являются менее кислыми, чем растворы сильных кислот. Аналогично слабые основания дают лишь небольшое количество гидроксид-ионов.
Что такое кислотно-щелочной баланс (pH). Как он влияет на здоровье
Соотношение кислоты и щелочи в каком-либо растворе называется кислотно-щелочным равновесием (КЩР) или балансом. КЩР характеризуется специальным показателем pH (сила водорода), который показывает число водородных атомов в данном растворе.
- В нейтральной среде pH равно 7,0
- В кислой среде pH ниже 7 (от 6,9 до 0)
- В щелочной среде pH выше 7 (от 7,1 до 14,0)
Тело человека на 70-80% состоит из воды, и имеет определенное кислотно-щелочное соотношение, характеризуемое показателем pH.
Кислотность жидкостей внутри человеческого организма в норме совпадает с кислотностью крови и находится в пределах от 7,35 до 7,45 pH.
Организм постоянно стремится уравновесить это соотношение, поддерживая строго определенный уровень pH. Этот параметр оказывает существенное влияние на все биохимические процессы в организме
Кислотность плазмы артериальной крови человека колеблется в пределах от 7,37 до 7,43 рН, составляя в среднем 7,4 рН.
Кислотно-щелочное равновесие в крови человека является одним из самых стабильных параметров, поддерживающее кислые и щелочные компоненты в определенном равновесии в очень узких границах. Даже небольшой сдвиг от указанных пределов может привести к тяжелой патологии. При сдвиге в кислотную сторону возникает состояние, называемое ацидозом, в щелочную — алколозом. Изменение кислотности крови выше 7,8 рН или ниже 6,8 рН несовместимо с жизнью. Кислотность эритроцитов составляет 7,28–7,29 рН.
Мы привыкли оценивать пищу с позиций калорийности, содержания белков, углеводов, жиров, витаминов и других веществ. Но любой продукт имеет еще один фундаментальный показатель — кислотную нагрузку пищи.
Американские ученые в начале 21 века сделали подлинное открытие, когда выявили, что у любого продукта есть еще один фундаментальный показатель, который имеет критическое значение для нашего здоровья. Это кислотная нагрузка пищи. Она складывается из соотношения в пище компонентов, которые в ходе метаболизма образуют либо кислоту, либо щелочь.
Кислотная нагрузка измеряется по принципу кислота минус щелочь.
Когда в пище преобладают компоненты, образующие серную кислоту (серосодержащие аминокислоты в белках) или органические кислоты (жиры, углеводы), то кислотная нагрузка имеет положительную величину.
Если в пище больше компонентов, образующих щелочь (органические соли магния, кальция, калия), то кислотная нагрузка представляет собой отрицательную величину.
Неправильное питание — причина хронического закисления организма
По данным антропологов рацион древнего человека состоял на 1/3 из нежирного мяса диких животных и на 2/3 из растительной пищи. В этих условиях питание носило исключительно щелочной характер.
Кислотная нагрузка пищи древнего человека составляла в среднем минус 78.
Ситуация принципиально изменилась с возникновением аграрной цивилизации, когда человек стал употреблять в пищу много зерновых культур, молочные продукты и жирное мясо одомашненных животных.
Но особенно драматические сдвиги в питании произошли в конце 20 века, когда рацион заполонили промышленно обработанные «кислые» продукты питания.
Эти изменения в составе диеты были названы факторами риска в патогенезе «болезней цивилизации», включая атеросклероз, гипертонию, остеопороз, диабет 2 типа.
Кислотная нагрузка пищи современного человека составляет плюс 48.
Диета современного человека богата насыщенными жирами, простыми сахарами, поваренной солью и бедна клетчаткой, магнием и калием. В ней доминируют рафинированные и обработанные продукты, сахар, мучные изделия, множество всяких полуфабрикатов.
Что представляет собой пища современного человека? Это пицца, чипсы, глазированные сырки, новоявленные чудо-молочные продукты, кондитерские изделия, прохладительные сладкие напитки. Эта пища имеет кислые валентности.
Ежедневное «кислотное» питание приводит к хроническому пожизненному закислению (ацидозу) внутренней среды организма.
pH крови — одна из самых жестких физиологических констант организма, которая выдерживается в узких границах. При воздействии закисляющих или ощелачивающих факторов организм использует компенсаторные механизмы, буферные системы крови, а также прибегает к помощи легких, почек, органов ЖКТ и других органов. В процессе жизнедеятельности организма требуются как кислые, так и щелочные продукты распада, причем кислых образуется в 20 раз больше нежели щелочных. Поэтому защитные системы организма, обеспечивающие неизменность его кислотно-щелочного равновесия, «настроены» на нейтрализацию и выведение прежде всего кислых продуктов распада. В целом устойчивость организма к ощелачиванию в несколько раз выше, чем к закислению.
Для организма предпочтительнее состояние, приближающееся к легкому компенсированному алкалозу (ощелачиванию), т.к. в этих условиях более активно протекают процессы энергообразования, синтеза белков и липидов, минеральный обмен и др. В действительности же чаще встречается состояние, близкое к компенсированному ацидозу (закисленности). Однако постоянная нагрузка на компенсаторные системы может привести к их декомпенсации, что в первую очередь проявится в нарушениях в обмене веществ не только в пределах клетки, но и в масштабах целого организма. Компенсированный ацидоз может вредить организму незаметно, но постоянно в течение нескольких месяцев и даже лет.
Как организм управляет уровнем кислотности?
При длительных отклонениях от равновесия в кислую сторону, скелет, как депо кальция и магния, может быть привлечен к компенсаторным процессам, т.к. поддержание кислотно-щелочного равновесия в организме с участием скелета высокопроизводительно.Организм не допускает выхода pH крови за заданные пределы, но достигается это дорогой ценой. В жертву приносится скелет: в целях ощелачивания, вымываются из костей щелочные буферы — кальций и магний.
По данным последних мировых научных исследований:
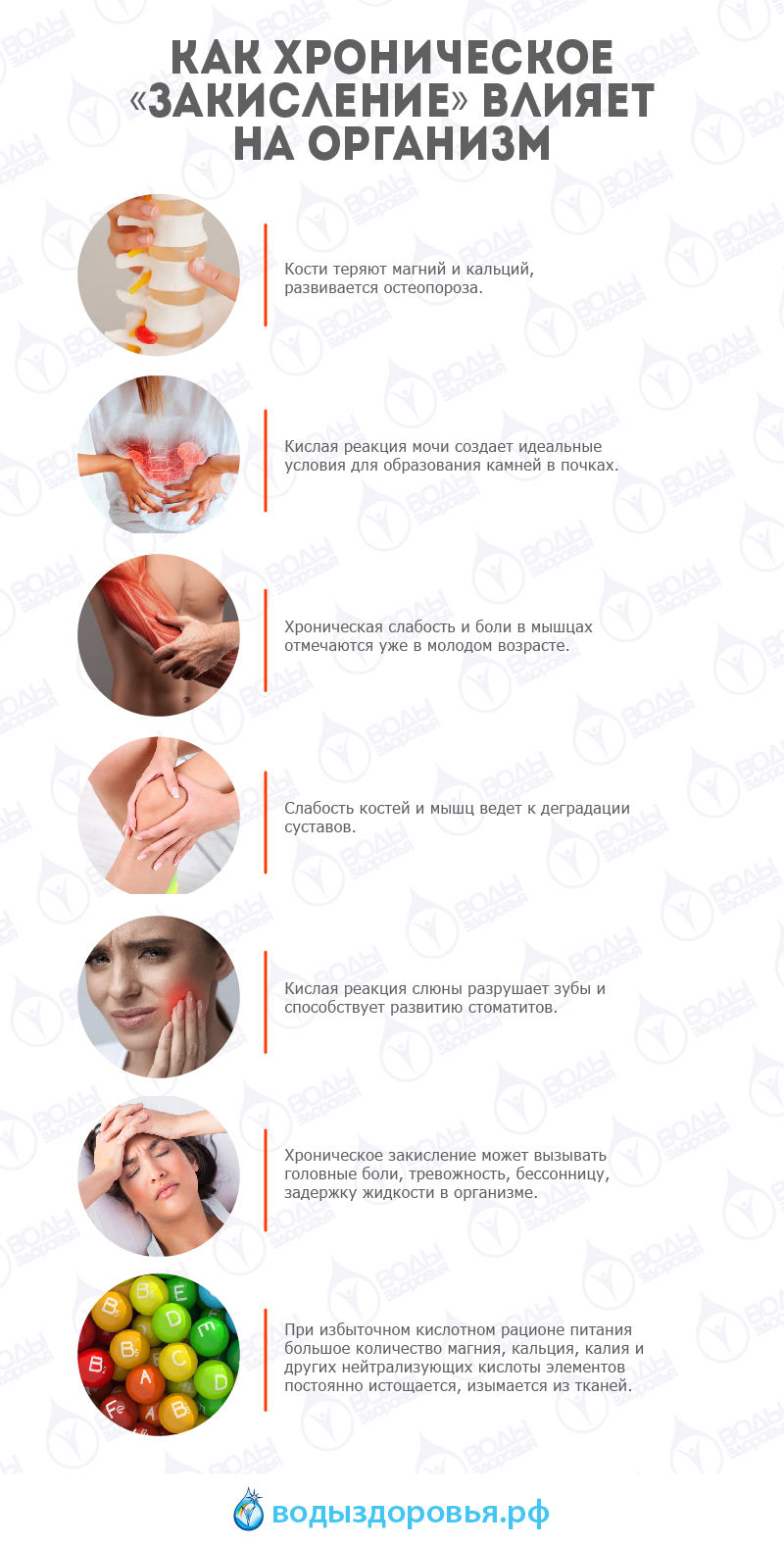
- Кости сначала теряют магний. В первую очередь уходит магний, затем кальций. Отсюда ускоренное развитие остеопороза.
- Разрушаются мышцы. Хроническая слабость и боли в мышцах отмечаются уже в молодом возрасте.
- Слабость костей и мышц ведет к деградации суставов.
- Кислая реакция мочи создает идеальные условия для образования камней в почках. Это принимает характер эпидемии. Хроническое нарушение работы почек вызывает развитие воспалительных заболеваний и почечной недостаточности.
- Кислая реакция слюны разрушает зубы и способствует развитию стоматитов.
- Хроническое закисление может вызывать головные боли, тревожность, бессонницу, задержку жидкости в организме.
- При избыточном кислотном рационе питания большое количество магния, кальция, калия и других нейтрализующих кислоты элементов постоянно истощается, изымается из тканей, и они должны быть обязательно восполнены, иначе очень скоро последуют симптомы болезней.
Магний и его роль в организме
В силу своих биологических эффектов, магний для организма может быть даже важнее кальция. По присутствию в организме магний, наряду с кальцием, натрием и калием, входит в первую четверку минералов в организме, а по содержанию внутри клетки занимает второе место после калия.
Без магния не может быть усвоен кальций. Магний уравновешивает поступление кальция, и препятствует его выведению. Магний особенно необходим для костной ткани, около 60% его содержится в костях и зубах, причем из этого количества примерно треть может быть оперативно мобилизована для нужд организма. 20% магния находится в мышцах, 19% — в других энергоемких органах организма (мозг, сердце, печень, почки и др.) и 1% — во внеклеточной жидкости. В крови 60-75% магния находится в ионизированной форме.
Причины дефицита магния
Рафинированная пища; структура питания — приготовление пищи по системе фаст-фуд (быстрой пищи) — приводит к потерям 70-80% магния.
В большинстве самых распространенных продуктов питания магний представлен скудно. Настоящими пожирателями магния являются столь любимая детьми кола, сладости. Прием большого количества кофеина: кофе, чай, прохладительные напитки (колы), шоколад и др. Чрезмерное употребление сахара ведет к усиленному выбросу магния с мочой. Недостаток магния усугубляется обеднённостью почв. Загрязняющие агенты (органические удобрения, промышленные отходы, тяжелые металлы, пестициды) снижают проникновение магния из почвы в культуры.
Дефицит магния может наблюдаться не только при нарушении питания, но и при увеличении потребности в нем: при физической и умственной нагрузке, стрессе, психоэмоциональном напряжении, например, если ребенок посещает школу с усиленной подготовкой, занимается спортом (т.е. имеет повышенную нагрузку на нервную систему). Другими причинами дефицита магния являются нарушение всасывания (поносы, запоры), заболевания ЖКТ, злоупотребление слабительными.
Повышенное выведение через почки (почечный ацидоз, диабет, мочегонные средства, алкоголь).
Применение лекарств (противозачаточные, эстрогенные, бета-блокаторы, ингибиторы АПФ, сердечные гликозиды, противотуберкулезные, антибиотики, цитостатики.
Нехватка магния влечет за собой дефицит цинка, меди, кальция, калия, кремния и дальнейшее их замещение токсичными тяжелыми металлами: свинцом, кадмием, алюминием. Огромную негативную роль играет широкое распространение различных диет для похудения. Избыточное употребление животного белка — мода на различные белковые диеты — сдвигает pH в кислую сторону, и повышает экскрецию солей мочевой кислоты.
Биологические эффекты магния
Магний — один из главных энергетиков клетки. Все энергетические процессы в организме идут при обязательном участии магния. 80-90% внутриклеточного магния находится в комплексе с АТФ.
Магний влияет на вход кальция в клетку (управление кальциевыми каналами). В этом отношении магний выступает как физиологический антагонист кальция и препятствует излишней функциональной активности клеток. Например, он предупреждает избыточное сокращение мышечных клеток (мышечные спазмы, спазмы сосудов при гипертонии и болях в сердце, спазмы бронхов при бронхиальной астме, спазмы кишечника и др.).
Магний защищает нервную систему от разрушительных стрессов и психоэмоционального напряжения. Магний является «изоляционным материалом» для проведения нервного импульса, тормозит избыточное его прохождение.
Магний поддерживает клеточный и гуморальный иммунитет, оказывает противовоспалительное и противоаллергическое действие.
Магний поддерживает соли мочи в растворенном состоянии, и препятствует их осаждению. Подавляет камнеобразование в почках, даже в незначительных концентрациях угнетает кристаллизацию. Ионы магния связывают в моче до 40% щавелевой кислоты. Предотвращают осаждение соединений кальция. Из-за недостатка магния (а его запасы истощаются гораздо быстрее, чем полагали ранее) кальций начинает порождать болезни. Магний, особенно в форме цитрата, сокращает абсорбцию оксалатов в кишечнике и его мочевую экскрецию. Таким образом, магнию отводится еще одна роль в здоровье человека, особенно это касается потребление магния в форме цитрата.
Магний участвует в процессах обезвреживания токсинов в печени, защищает от радиации.
Магний защищает от попадания тяжелых металлов в организм (напр. свинца), и выводит их из обмена веществ.
Магний необходим для укрепления костной ткани, зубов, волос и ногтей.
Итак, магний, как никакой другой элемент, важен для протекания многих метаболических процессов в организме. Неслучайно он созвучен с латинским словом «magnum», одно из значений которого означает «великий».
Магний, как и другие элементы в организме человека, не синтезируется, он поступает в наш организм с водой и пищей, его называют главным металлом жизни.
Уважаемые читатели!
Спасибо, что читаете наш блог! Получайте самые интересные публикации раз в месяц оформив подписку. Новым читателям предлагаем попробовать нашу воду бесплатно, при первом заказе выберите 12 бутылок (2 упаковки) минеральной воды BioVita или питьевой воды Stelmas. Операторы свяжутся с Вами и уточнят детали. Тел. 8 (800) 100-15-15
* Акция для Москвы, МО, Санкт-петербурга, ЛО
Спасибо за подписку на нашу рассылку
Нормы pH питьевой и водопроводной воды
Водородный показатель (pH) считается наиважнейшей характеристикой питьевой воды. Он отвечает за баланс щелочей и кислот в организме человека. Таким образом, от pH зависит ход химических реакций и биологических процессов в клетках.
Что такое pH
Сокращение из двух букв берет свое начало в латинском языке. Оно расшифровывается как «сила водорода» и означает меру активности заряженных частиц данного элемента. Чтобы рассчитать величину показателя pH, измеряют концентрацию ионов водорода. Затем из полученного числа извлекается десятичный логарифм и умножается на (-1). Математическая формула выглядит так: pH = -lg[H+].
По сути, водородный показатель — это соотношение в жидкости ионов H+ и OH—, которые образуются при распаде молекул воды. Идеальным называют соотношение 1:1, т.е. pH=7. Таким значением обладает дистиллированная вода.
Величина показателя напрямую связана с температурой воды и ее взаимодействием с воздухом. Если в закрытом сосуде pH будет равняться 7, то с попаданием в жидкости диоксида углерода значение опустится до 5,2.
На водородный показатель также влияют вещества, растворяющиеся в воде. Добавление одних веществ повышает кислотность, других – ее понижает. Это явление позволяет оценить чистоту жидкости, даже когда визуально она не имеет примесей.
Нормы pH для питьевой воды
Границы допустимых значений водородного показателя определяет СанПиН 2.1.4.1074-01 «Питьевая вода». Согласно данному документу, норма pH питьевой воды из-под крана не должна выходить за рамки 6-9 баллов.
Однако ученые ставят более строгие границы: от 6,5 до 8,5. Это связано с нейтральностью человеческой крови: считается, что для человека наиболее благоприятна вода со сходным значением показателя. В идеале напиток должен иметь pH=7,5. Такая вода благотворно влияет на обменные процессы в организме человека. И именно из-за этого после сладкой газировки во рту остается неприятная сухость: химические примеси в таком напитке понижают pH организма.
Значения pH различных напитковВода с низким значением водородного показателя, то есть кислая, может применяться для умывания (она эффективно удаляет загрязнения с поверхности тела). Щелочная вода, имеющая больше 7-9 баллов, улучшает состояние организма (если не злоупотреблять ей).
Чтобы всегда пить воду с полезным значением водородного показателя, рекомендуется использовать систему фильтров для питьевой воды (например, обратный осмос под кухонной раковиной).
Приобрести такое оборудование можно в интернет-магазине компании «Кванта +».
Водородный показатель бутилированной воды обычно указывается на этикетке. Благодаря этому подобрать нужную бутылку в магазине не составляет труда.
Методы определения pH
Чтобы узнать, вода с каким водородным показателем попадает в чайник, не обязательно обращаться в платные лаборатории. Достаточно применить один из распространенных индикаторов, и сразу станет ясно, нуждается ли вода в дополнительной обработке.
Лакмусовая бумага
Лакмусовая бумага – наиболее дешевый и простой вариант определения pH среды. Этот индикатор меняет цвет при взаимодействии с водой, водородный показатель которой отличается от нейтрального. Таким свойством бумагу наделяет пропитка красящими веществами, вступающими в реакцию с водой. В бумаге присутствует более полутора десятка различных красителей. Чаще всего они имеют естественное происхождение, т.е. получаются из растений и лишайников.
При попадании бумаги в щелочную среду, она синеет. В кислотную – краснеет. Для более точного определения pH воды используют специальную цветовую шкалу.
pН-метр
Чтобы с высокой точностью измерить водородный показатель жидкости, используют прибор под названием «pH-метр». Его цена значительно превышает стоимость бумаги или полосок. Однако он позволяет устанавливать значение кислотности воды с точностью до сотых долей.
 Компактный бытовой pH-метр
Компактный бытовой pH-метрДанные устройства делятся на лабораторные и бытовые. В условиях жилой квартиры или офиса удобнее всего пользоваться вторым видом. Бытовые pH-метры делятся на группы в зависимости от:
- наличия автоматической калибровки;
- наличия защиты от влаги;
- точности получаемых значений.
Калибровка прибора проводится с помощью буферных растворов.
Совет: чтобы не усложнять себе жизнь, для использования в домашних условиях стоит приобрести измеритель с автоматической калибровкой
Определение pH с помощью тест-полосок
Чтобы быстро и удобно померить уровень pH воды, применяют индикаторные полоски. Их можно приобрести в зоомагазине, где они продаются для определения уровня кислотности в аквариумах.
Такую полоску достаточно на мгновение опустить в водопроводную воду, чтобы получить результат – влажная часть бумаги практически мгновенно меняет цвет.
Упаковка тест-полосок с цветовой шкалойКроме того, тест-полоски можно сделать дома своими руками. Для этого нужно в течение получаса отваривать красную капусту, а затем около десяти минут вымачивать в остывшем растворе обычную принтерную бумагу. Если после высыхания капнуть на текст-полоску кислотой, она покраснеет. Если капнуть щелочью – пожелтеет.
Значение уровня pH для водопроводной воды и других сред
Величина pH для обычной питьевой воды зависит от материала водопровода, состава исходной воды и температуры на улице. Однако она всегда остается в диапазоне 6,5-9,5. Если водородный показатель сильно отличается от норм, значит, где-то произошла поломка или в воду попали посторонние загрязнения.
Водородный показатель воды в бассейне должен оставаться в пределах 7,5-8 баллов. Резкое падение его уровня ниже 7 приводит к повышению токсичности такой жидкости, купаться в ней не стоит.
При этом не стоит забывать, что для прочих растворов и веществ кислотность может быть значительно выше или ниже нормальной водной. Например, лимонный сок имеет pH=2,5, кофе – 5, а мыло для рук – 10. При этом молоко, которое часто употребляют при изжоге в надежде снизить кислотность желудка, имеет близкие к нейтральному значения pH=6,6-6,9.
Выводы
Водородный показатель воды – важный показатель, влияющий на самочувствие человека. Отклонение этой величины от нормы свидетельствует о проблемах в водопроводе, на это стоит обращать внимание. Чтобы определить pH воды для питья, можно воспользоваться лакмусовой бумагой или pH-метром. Результат измерения покажет, насколько безопасна жидкость.
Приобрести приборы для проверки качества воды можете также в нашем магазине.
Что такое pH воды и на что он влияет?
Читайте в этой статье:
Что такое pH и какая его норма для воды
Как измерить pH воды
pH в организме человека
Определение и норма pH для воды
pH — это водородный показатель вещества, который отражает его кислотность. Аббревиатура образована от лат. potentia hydrogeni — сила водорода. Уровень pH отвечает за свойства и качество воды. Нормальным и оптимальным показателем уровня pH питьевой воды считается промежуток от 7,0 до 8,0. Такую воду ещё называют нейтральной. Если показатель будет выше 7, то вода будет иметь щелочную реакцию, а при пониженном показателе (меньше 7) — кислую.
Таким образом, различают следующие воды: слабощелочные, щелочные, сильнощелочные, слабокислые, кислые, сильнокислые и нейтральные. Для каждого вида воды есть свой pH-показатель:
сильнокислые воды < 3 (лимонный сок)
кислые воды 3 — 5 (пиво, вино, апельсиновый сок)
слабокислые воды 5 — 6.5 (чёрный кофе, молоко)
нейтральные воды 6.5 — 7.5 (чистая вода при от 100 до 22°С)
слабощелочные воды 7.5 — 8.5 (чистая вода при 0°С)
щелочные воды 8.5 — 9.5 (раствор пищевой соды)
сильнощелочные воды > 9.5-11 (хлорная известь, нашатырный спирт)
Показатель pH 0 — это уже кислота, а pH больше 14 — щелочь.
В составе щелочной воды преобладают натрий, гидрокарбонатные ионы и магнезия, что смещает её кислотность в щелочную сторону и придаёт ей иные свойства.
Для питьевой и хозяйственно-бытовой воды оптимальным считается уровень рН в диапазоне от 6 до 9 единиц. Если человек будет употреблять воду с отклонением нормы показателя, то это плохо скажется на его здоровье и самочувствии.
Измерение уровня pH
Измерение возможно с помощью специальных индикаторов или с помощью специального электронного измерителя (его называют рН-мером). Однако, наиболее популярным методом измерения является лакмусовый индикатор.
Принцип действия таков: небольшое количество воды наливается в одноразовый стаканчик или специальную пробирку (иногда идёт в наборе с тестом) и в неё капается несколько капель реактива. При взаимодействии с водой образуется определённый цвет (в зависимости от уровня pH воды). Расшифровать результаты довольно просто — в комплекте есть специально разработанная колориметрическая шкала с указанием значений pH.
Достаточно просто сравнить цвет тестируемой воды (или любой другой жидкости) с колориметрической шкалой и определить уровень pH в воде.
Норма pH для поверхностных водных систем составляет 6,5–8,5, а для подземных — 6–8,5.
Уровень pH и здоровье
В нашем организме очень важно поддерживать водно-солевой и кислотно-щелочной баланс. От этого зависит здоровье и самочувствие человека. Если уровень кислотности в нашем организме повысится, то усилится рост патогенной флоры (благоприятной среды для множества бактерий). В щелочной среде они как правило, не выживают.
В организме человека много биологических жидкостей — кровь, желудочный сок, моча, слюна т.д. Врачи часто определяют их уровень pH для проверки здоровья пациента и диагностирования болезни. Например, при заболевании гастритом человек обязательно должен знать, какой именно у него гастрит: с повышенной или пониженной кислотностью — от этого зависят методы лечения и самочувствие больного.
Для того, чтобы поддерживать оптимальный кислотно-щелочной баланс в организме, здоровому человеку нужно правильно питаться и пить чистую качественную воду с нормальным нейтральным или слабощелочным уровнем pH.
Будьте здоровы!
© Журнал «Аква Мелоди»
Дата публикации: 26.06.2019
Воды, с повышенным pH:
Что такое pH?
Можете ли вы себе представить, что развитие многих болезней зависит от одной причины? Многие специалисты диетологи и фитотерапевты эту скрытую опасность теперь обозначают двумя словами: кислота и щелочь.
Высокая кислотность разрушает наиважнейшие системы в организме, и он становится беззащитен перед болезнями. Сбалансированная pH-среда обеспечивает нормальное протекание метаболических процессов в организме, помогая ему бороться с заболеваниями. Здоровый организм имеет запас щелочных веществ, которые он использует в случае необходимости.
Что такое pH?
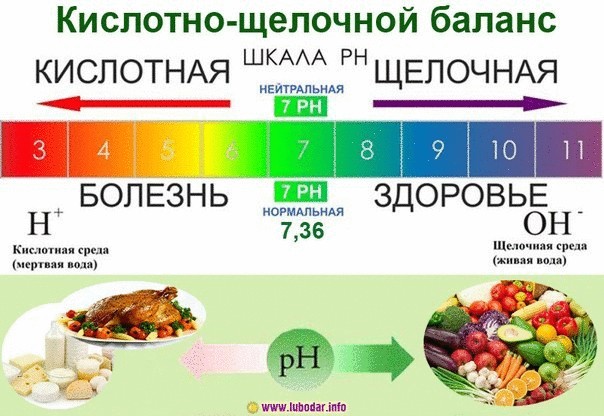
Соотношение кислоты и щелочи в каком-либо растворе называется кислотно-щелочным равновесием (КЩР), хотя физиологи считают, что более правильно называть это соотношение кислотно-щелочным состоянием. КЩР характеризуется специальным показателем pH (power Hidrogen – «сила водорода»), который показывает число водородных атомов в данном растворе. При pH равном 7,0 говорят о нейтральной среде. Чем ниже уровень pH – тем среда более кислая (от 6,9 до 0). Щелочная среда имеет высокий уровень pH (от 7,1 до 14,0).
Тело человека на 80% состоит из воды, поэтому вода – это одна из наиболее важных его составляющих. Тело человека имеет определенное кислотно-щелочное соотношение, характеризуемое pH (водородным) показателем. Значение показателя pH зависит от соотношения между положительно заряженными ионами (формирующими кислую среду) и отрицательно заряженными ионами (формирующими щелочную среду). Организм человека постоянно стремится уравновесить это соотношение, поддерживая строго определенный уровень pH. При нарушенном балансе могут возникать множество серьезных заболеваний.
рН, или показатель кислотно-щелочного равновесия.
Это мера относительной концентрации водородных (Н+) и гидроксильных (ОН—) ионов в жидкой системе и выражается в масштабе от 0 (полное насыщение ионами водорода Н+) до 14 (полное насыщение гидроксильными ионами ОН—), дистиллированная вода считается нейтральной с рН 7,0.
0 — сильнейшая кислота, 14 — сильнейшая щелочь, 7 – нейтральное вещество.
Если в любой из жидкостных сред организма происходит повышение концентрации (Н+) ионов, то возникает смещение pH в кислую сторону, то есть, происходит закисление среды. Это называется ещё кислотным сдвигом.
И наоборот — повышение концентрации (ОН-) ионов вызывает смещение значения pH в щелочную сторону, или щелочной сдвиг.
Наш организм имеет слабощелочную среду. Кислотно-щелочной баланс в нашем организме постоянно поддерживается на одном стабильном уровне и в очень узком диапазоне: от 7,26 до 7,45. И даже незначительное изменение рН крови, выходящее за эти границы, может привести к болезням.
Изменение показателей рН-баланса могут привести к печальным последствиям.
Повышенная кислотность в организме.
Из-за неправильного питания и употребления в пищу кислых продуктов, а также недостатка воды происходит закисление организма. Люди употребляют много жиров, мяса, молочных продуктов, зерновых культур, сахара, мучных и кондитерских изделий, всевозможных полуфабрикатов и других переработанных, рафинированных продуктов, практически не содержащих клетчатки, минералов и витаминов, не говоря уже о ферментах и ненасыщенных жирных кислотах.
Для того, чтобы противостоять этому – снизить концентрацию кислоты и удалить ее от жизненно важных органов – организм задерживает воду, что отрицательно влияет на обмен веществ: организм быстрее изнашивается, кожа становится сухой, морщинистой. К тому же при закисленности организма ухудшается перенос кислорода к органам и тканям, организм плохо усваивает минералы, а некоторые минералы, такие как Ca, Na, K, Mg выводятся из организма. Организму приходится тратить колоссальное количество ресурсов и энергии на нейтрализацию лишних кислот, вызывая тем самым определённый дисбаланс в биохимических реакциях. Так как щелочных резервов, поступающих извне, явно не хватает, то организм вынужден задействовать свои внутренние ресурсы — кальций, магний, железо, калий. В результате снижается гемоглобин, развивается остеопороз. Когда железо гемоглобина крови используется для нейтрализации кислоты, человек ощущает усталость. Если на эти нужды расходуется кальций, появляется бессонница, раздражительность. Вследствие снижения щелочного резерва нервной ткани нарушается умственная деятельность.
От недостатка минералов страдают жизненно важные органы, повышается риск сердечно сосудистых заболеваний, снижается иммунитет, появляется хрупкость костей и многое другое. Если в организме находится большое количество кислоты и нарушены механизмы ее вывода (с мочой и калом, с дыханием, с потом и т.д.), организм подвергается сильнейшей интоксикации. Единственный выход – это ощелачивание организма.
В глобальном масштабе, закисление организма приводит к возникновению более чем 200(!) заболеваний, например: катаракты, дальнозоркости, артрозов, хондрозов, желче- и мочекаменной болезней, и даже онкологии!
А люди ещё удивляются: «Откуда столько болезней у человечества? Почему они постоянно болеют? Почему они дряхлеют с возрастом?»
Да хотя бы потому, что более 90% пищи, которую они едят — это «кислые» продукты, и всё, что они пьют (кроме чистой воды, свежевыжатых соков и травяного чая без сахара) — имеет pH от 4,5 до 2,5 — то есть ещё больше закисляет организмы людей!
Состояние повышенной кислотности называется — Ацидоз. Невыявленный вовремя ацидоз может вредить организму незаметно, но постоянно в течение нескольких месяцев и даже лет.опубликовано econet.ru
P.S. И помните, всего лишь изменяя свое потребление — мы вместе изменяем мир! © econet
Что такое pH. Влияние показателя pH на здоровье человека
Химическая реакция:
рН = 1 / log [H +] = -Iog [H +]
рН 6 в десять раз более кислотный, чем рН 7, рН 5 в сто раз более кислотный, чем рН 7.
Шкала рН колеблется от кислотного рН 0 до щелочного рН 14. Нейтральный показатель рН 7.
При рН 7, показатели воды имеют одинаковую концентрацию ионов Н+ и ОН-.
Растворы с рН менее 7 являются кислыми , потому что они содержат более высокую концентрацию ионов H +.
Вещества с рН выше 7, щелочные поскольку они содержат более высокую концентрацию ОН-, чем Н+.
Шкала рН -логарифмическая шкала, построенная таким образом, что изменение одной единицы рН означает десятикратное изменение концентрации ионов водорода.
Чистая вода без примесей имеет рН около 7; кислые водные растворы имеют pH менее 7 , щелочные- pH более pH7.
Раствор сильной кислоты, такой как соляная имеет рН 0.
Раствор сильной щелочи, такой как гидроксид натрия имеет рН 14.
Таким образом, измерение значений рН измеряется в основном в диапазоне от 0 до 14.

Ацидоз и причины его возникновения.
Наиболее распространенным расстройством кислотно-щелочного баланса является ацидоз, что означает кислотную перегрузку в организме и определяется падением рН ниже 7,35.
Ткани живого организма весьма чувствительны к колебаниям показателя pH — за пределами допустимого диапазона (7,37—7,44), происходит денатурация белков: разрушаются клетки, ферменты теряют способность выполнять свои функции, возможна гибель организма.
Поэтому кислотно-щелочной баланс в организме жёстко регулируется. Существует несколько буферных систем, которые связывают ионы водорода и препятствуют каким-либо изменениям показателя рН. Бикарбонатная буферная система имеет особо важное значение: избыток протонов (H+, ионов водорода) взаимодействует с ионами бикарбоната (HCO3−) с образованием угольной кислоты (h3CO3). В дальнейшем уменьшение количества угольной кислоты происходит в результате ускоренного выделения углекислого газа (CO2) в результате гипервентиляции лёгких (концентрация определяется давлением в альвеолярной газовой смеси)
Уровень pH человеческого организма
Зубной налет может сформировать кислую среду, что может привести к деминерализации и разрушению эмали зубов.
Ферменты и другие белки имеют оптимальные показатели рН и могут стать инактивированными или денатурированными за пределами этого диапазона. Вся внутренняя ткань организма (за исключением ядра клетки) имеет рН около 6,8.
Плазма крови и другие жидкости, которые окружают клетки в организме имеют рН 7,3 до 7,45. РН крови 6,9 и ниже может вызвать очень серьезные последствия для здоровья организма.
Плохое питание, нездоровый образ жизни и стресс ухудшают наше пищеварение, вымывает из костей кальций мешает поджелудочной железе поддерживать нужное количество водного щелочной раствора для балансирования уровня кислоты в организме.
| | Адрес этой страницы (вложенность) в справочнике dpva.ru: главная страница / / Техническая информация / / Химический справочник / / Кислотность pH. Водородный показатель pH. Таблицы показателей pH. Перевод единиц кислотности. / / pH. Что такое pH . Водородный показатель. Кислые и основные (щелочные) свойства растворов / сред. Поделиться:
| |||||||||||||||||||||||||||||||||||||||||||
