Рак почки
Вам поставили диагноз: рак почки?Наверняка Вы задаётесь вопросом: что же теперь делать?
Подобный диагноз всегда делит жизнь на «до» и «после». Все эмоциональные ресурсы пациента и его родных брошены на переживания и страх. Но именно в этот момент необходимо изменить вектор «за что» на вектор «что можно сделать».
Очень часто пациенты чувствуют себя безгранично одинокими вначале пути. Но вы должны понимать — вы не одни. Мы поможем вам справиться с болезнью и будем идти с Вами рука об руку через все этапы вашего лечения.
Предлагаем Вашему вниманию краткий, но очень подробный обзор рака почки.
Его подготовили высоко квалифицированные специалисты Отдела репродуктивных органов и мочевыводящих путей Московского научно-исследовательского онкологического института имени П.А. Герцена – филиала ФГБУ «НМИЦ радиологии» Минздрава России А.С. Калпинский и аспирант А.
Данная брошюра содержит информацию о диагностике и лечении рака почки. Здесь собраны все основные методики лечения данного заболевания, в том числе, последние разработки отечественных и зарубежных ученых-онкологов.
Мы хотим Вам помочь победить рак!
Ежегодно в России выявляется более 22 тысяч новых случаев рака почки. Если рак почки диагностируется на первой и второй стадиях, то в большинстве случаях, после проведенного противоопухолевого лечения, можно полностью излечиться от данного заболевания.
Филиалы и отделения, где лечат рак почкиМНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиала ФГБУ «НМИЦ радиологии» Минздрава России.
ВступлениеУ каждого человека есть две почки бобовидной формы коричнево-красного цвета, расположенные в поясничной области по обеим сторонам от позвоночника. Почки фильтруют кровь и выводят из организма лишние минералы, соли и воду. Каждый день через почки проходит примерно 190 литров крови и образуется 2 литра мочи. Также почки вырабатывают гормоны, которые необходимы для контроля артериального давления, выработку клеток крови и другое. Ренин – регулирует артериальное давление, Эритропоэтин – стимулирует выработку эритроцитов, Кальцитриол – регулирует уровень кальция в крови.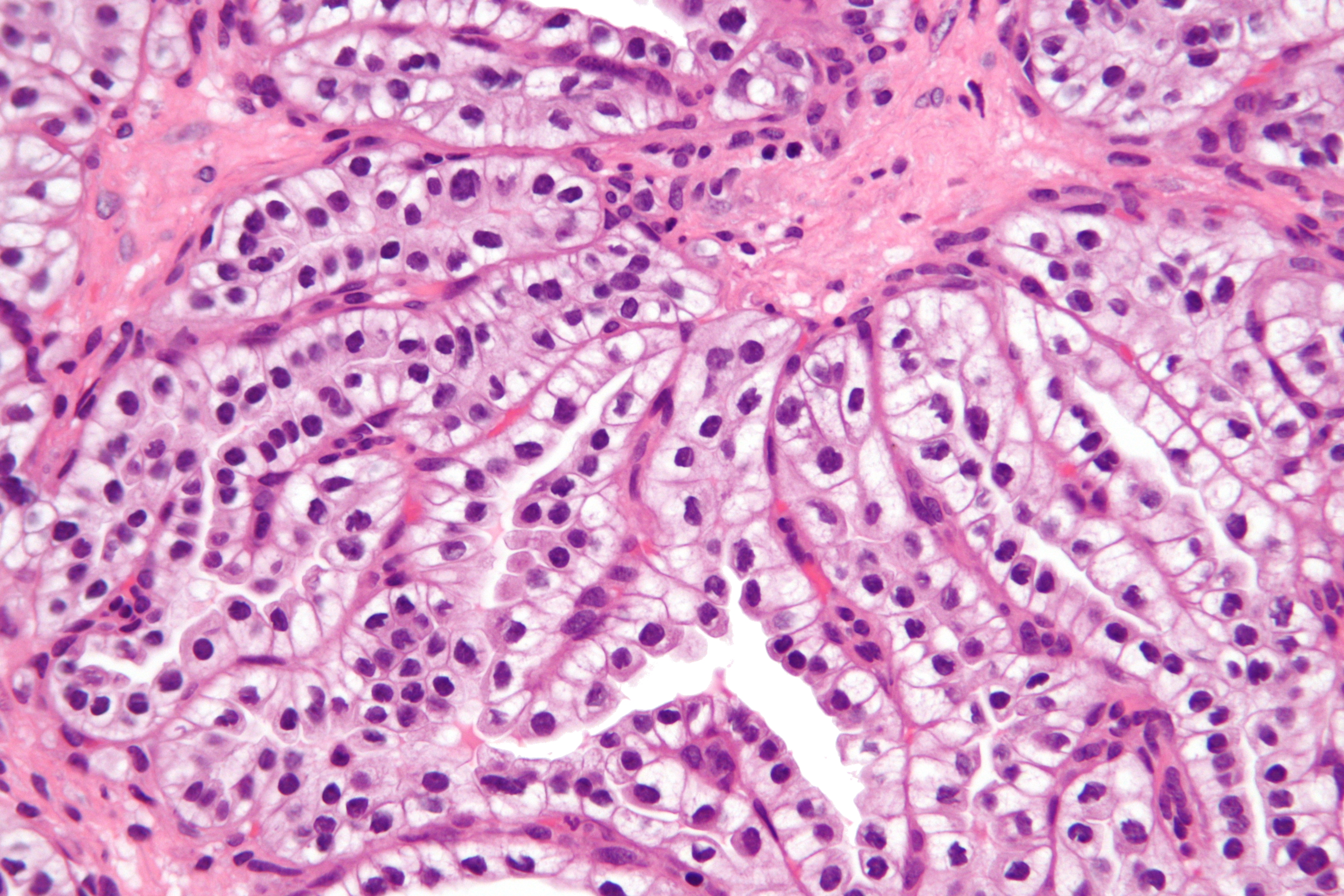
Рак — это не одно заболевание, а группа различных заболеваний, характерной особенностью которых является бесконтрольное деление клеток и распространение в другие органы и ткани. Опухоль может появиться почти в любой ткани и органе человеческого организма, который состоит из триллионов клеток. Ежесекундно в организме происходит деление, клетки стареют или повреждаются и умирают, их место занимают новые клетки. Однако, иногда этот упорядоченный процесс образования и деления новых клеток может выйти из-под контроля за счет нарушения процессов регуляции тканевого роста. Если механизм контроля деления клетки «ломается», то возникает неконтролируемый рост и деление. В данной ситуации речь идет о генетических мутациях в клетках.
Злокачественные опухоли обладают способностью к распространению в другие органы и окружающие их ткани. Эти процессы называются метастазированием и инвазивным ростом соответственно. Метастазы – это клетки опухоли, которые отделились от основной, первичной опухоли, и с током крови или лимфы попали в другие органы, где сформировали новые опухолевые очаги такой же разновидности, как и первичная опухоль.
В отличие от злокачественных опухолей доброкачественные опухоли не метастазируют и не обладают способностью к инвазии, хотя могут быть довольно больших размеров. После удаления доброкачественных опухолей редко на их месте снова могут появиться новые (рецидивные) опухоли.
В настоящее время имеется несколько классификаций почечных онкологических заболеваний, однако, наиболее распространенной формой рака почки является светлоклеточный почечно-клеточный рак, который встречается примерно в 75 – 80% случаях. Развивается он из проксимальных почечных канальцев, которые образуют фильтрационную систему почек. В каждой почке есть тысячи таких крошечных фильтров.
Существуют также другие разновидности почечно-клеточного рака (папиллярный почечно-клеточный рак, рак собирательных трубочек Беллини/медуллярный почечно-клеточный рак, хромофобный почечно-клеточный рак
Развивается он из проксимальных почечных канальцев, которые образуют фильтрационную систему почек. В каждой почке есть тысячи таких крошечных фильтров.
Существуют также другие разновидности почечно-клеточного рака (папиллярный почечно-клеточный рак, рак собирательных трубочек Беллини/медуллярный почечно-клеточный рак, хромофобный почечно-клеточный рак
Описанные здесь симптомы характерны для опухолей почек, однако они не являются специфичными и могут быть вызваны различными другими состояниями. На ранних стадиях, когда опухоль небольшого размера зачастую никаких субъективных симптомов не возникает. При дальнейшем развитии и распространении заболевания, клиническая картина становится более выраженной и часто люди, которые не проходят ежегодное обследование, обращаются к врачу уже на поздних стадиях, когда опухоль начинает интенсивно расти, оттесняет соседние органы или распространяется (метастазирует) в другие органы: легкие, кости, лимфатические узлы, печень и т. д.
д.
Проконсультируйтесь с вашим врачом, если вы отмечаете:
Постоянную тянущую боль в области живота или спины
Повышенную утомляемость
Необъяснимую, иногда быструю потерю веса
Лихорадку, не вызванную другим заболеваниями
Потерю аппетита
Анемию
Факторы риска
Наличие факторов риска не означает, что обязательно появится опухоль почки, однако это увеличивает такую вероятность.
К факторам риска возникновения рака почек относят:
Курение
Ожирение
Артериальная гипертензия
Наличие опухолей почек у ваших близких родственников
Наличие определенных генетических заболеваний
Бесконтрольный прием обезболивающих препаратов в течение длительного времени
Большинство опухолей почек выявляют на ранней стадии, когда они ограничены капсулой почки, однако часть опухолей выявляют на распространенной стадии.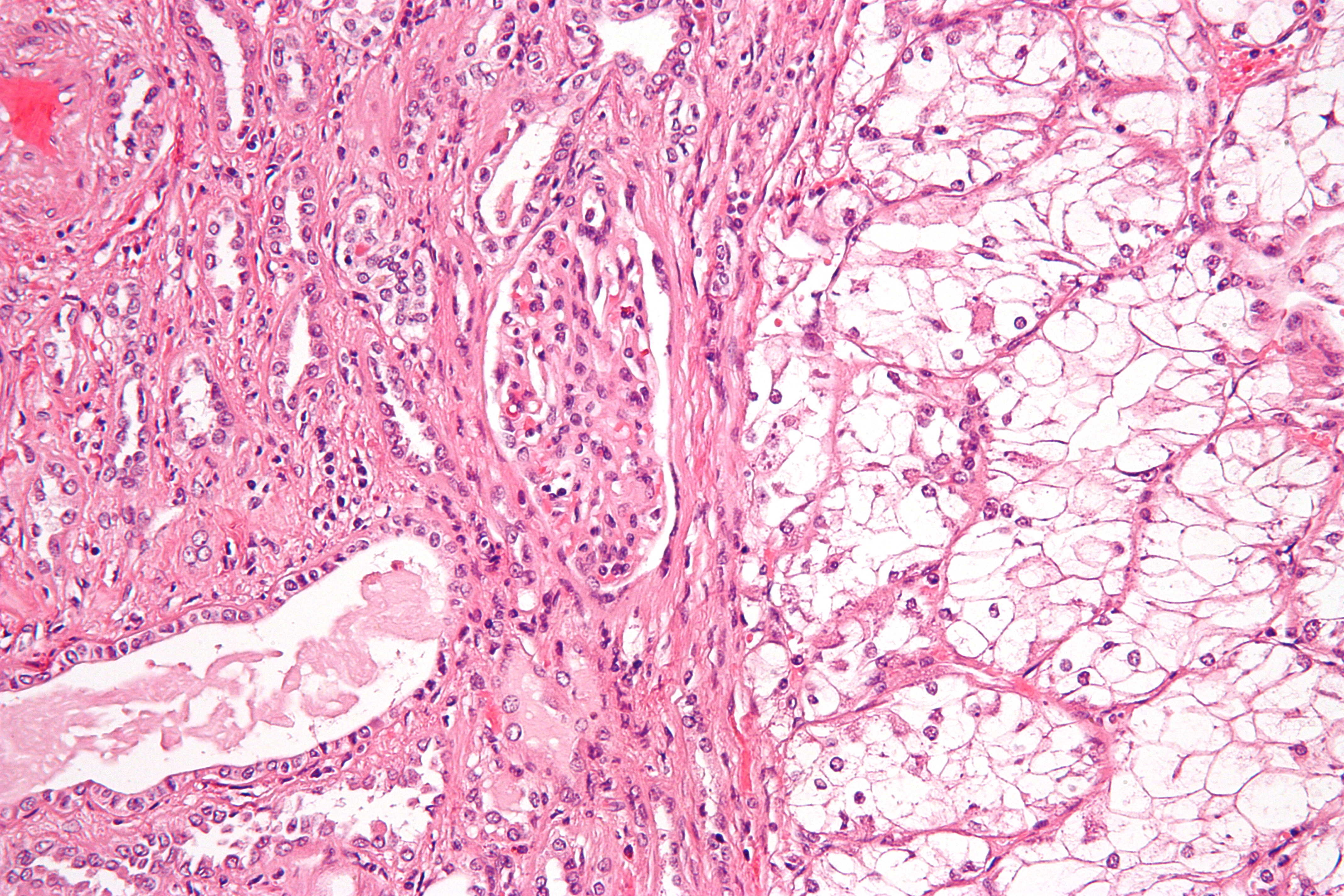
Общий анализ мочи является одним из составляющих стандартного медицинского осмотра, во время которого можно выявить клетки крови в моче (макрогематурия), что иногда является первым признаком опухоли почки или верхних мочевых путей. Однако также макрогематурия может свидетельствовать об инфекциях мочеполовой системы, мочекаменной болезни и не является специфическим критерием опухоли.
Инструментальные методы обследования, такие как компьютерная томография (КТ) и магнитно-резонансная томография (МРТ) позволяют выявлять даже небольшие опухоли, однако использование их в рутинной практике нецелесообразно из-за высокой стоимости. Альтернативой этим исследованиям может служить ультразвуковое исследование, которое может выявлять небольшие по размеру опухолевые образования почки.
В настоящее время основным методом диагностики рака почки является биопсионное исследование, во время которого получают небольшое количество ткани новообразования, и затем врач-морфолог исследует этот материал под микроскопом в поисках опухолевых клеток.
Стадии рака почки I стадия: в почке есть опухоль, но она не выходит за пределы органа и по размеру не превышает 7 см.
II стадия: опухоль также находится в почке, но большим размером, чем при I стадии (≥7см)

IV стадия: опухоль распространяется дальше, теперь уже не только в жировую клетчатку почки, но и в надпочечник, лимфатические узлы и отдаленные органы, например, легкие, печень, кости, головной мозг.Лечение рака почки
Существуют международные рекомендации лечения больных раком почки, в которых в зависимости от размера и/или распространенности опухоли есть соответствующие алгоритмы. В настоящее время существуют следующие виды лечения рака почки: хирургическое лечение, лекарственная системная терапия, радиотерапия, активное наблюдение.
Основным методом лечения местнораспространённых форм рака почки является хирургический. Выполняются следующие виды операций:
Резекция почки (удаление фрагмента почки с опухолью): во время операции хирург удаляет только опухоль в пределах здоровых тканей для сохранения функции почки. Иногда эта операция жизненно необходима, например, при единственной почке, при функционально непригодной второй почки (поликистоз почки, вторично или первично сморщенная почка, дефекты развития и др).Резекция почки является основным методом лечения начальной стадии рака почки, но в некоторых случаях, при удачном расположении опухоли, может быть применена у больных со II стадией. Результаты этой операции во многом зависят от опыта врача. Резекция почки может выполняться открытым доступом – через брюшную полость, с осуществлением доступа через стенку живота, через поясничный доступ, или лапароскопическим доступом. Эндоскопический метод резекции почки обладает рядом преимуществ: небольшие кожные разрезы, меньший послеоперационный болевой синдром и короткий койко-день с возможностью быстрого восстановления и возврата к привычной жизнедеятельности и работе.
Иногда эта операция жизненно необходима, например, при единственной почке, при функционально непригодной второй почки (поликистоз почки, вторично или первично сморщенная почка, дефекты развития и др).Резекция почки является основным методом лечения начальной стадии рака почки, но в некоторых случаях, при удачном расположении опухоли, может быть применена у больных со II стадией. Результаты этой операции во многом зависят от опыта врача. Резекция почки может выполняться открытым доступом – через брюшную полость, с осуществлением доступа через стенку живота, через поясничный доступ, или лапароскопическим доступом. Эндоскопический метод резекции почки обладает рядом преимуществ: небольшие кожные разрезы, меньший послеоперационный болевой синдром и короткий койко-день с возможностью быстрого восстановления и возврата к привычной жизнедеятельности и работе.
Радикальная нефрэктомия (полное удаление почки): этот вариант хирургического лечения в основном применяется при местно-распространённых и больших опухолях почки, но также может использоваться при глубоко и неудобно расположенных опухолях почки. В случае большой опухоли верхнего полюса почки необходимо удалять и надпочечник с окружающей жировой клетчаткой. Данный вид операции называется адреналэктомия. Кроме того, при наличии информации о распространенной опухоли почки с или без наличия увеличенных лимфатических узлов, расположенных вдоль сосудов почки или аорты и нижней полой вены, обязывает хирургов выполнить парааортальную лимфаденэктомию, т.е. убрать всю клетчатку вдоль этих сосудов с увеличенными лимфатическими узлами. Выполнение радикальной нефрэктомии, как и резекции, также возможно в различных вариантах: открытом или эндоскопическом.
В случае большой опухоли верхнего полюса почки необходимо удалять и надпочечник с окружающей жировой клетчаткой. Данный вид операции называется адреналэктомия. Кроме того, при наличии информации о распространенной опухоли почки с или без наличия увеличенных лимфатических узлов, расположенных вдоль сосудов почки или аорты и нижней полой вены, обязывает хирургов выполнить парааортальную лимфаденэктомию, т.е. убрать всю клетчатку вдоль этих сосудов с увеличенными лимфатическими узлами. Выполнение радикальной нефрэктомии, как и резекции, также возможно в различных вариантах: открытом или эндоскопическом.
Аблативные методики. Чаще всего рак почки развивается у пациентов старшего возраста (средний возраст 60 лет), у которых помимо опухоли присутствуют тяжелые сопутствующие заболевания, которые не позволяют выполнить хирургическое лечение. Для таких пациентов есть альтернативные аблативные методики: криоабляция и радиочастотная термоабляция опухоли. Криоабляция и радиочастотная термоабляция опухоли почки отличаются характером воздействия, т. е. либо охлаждением опухоли до экстремально низких или нагревом до крайне высоких температур. Выполнение аблативных методик возможно в различных вариантах, как в чрескожном варианте, так и при необходимости эндоскопическом. Чрескожный вариант выполняют под краткосрочным внутривенным наркозом. Методика заключается в том, что под контролем УЗИ, через стенку живота в центр опухоли устанавливают специальный электрод, после чего в зависимости от методики проводят нагревание опухоли до высоких температур или 2 цикла замораживания и оттаивания, вследствие чего опухолевые клетки погибают.
е. либо охлаждением опухоли до экстремально низких или нагревом до крайне высоких температур. Выполнение аблативных методик возможно в различных вариантах, как в чрескожном варианте, так и при необходимости эндоскопическом. Чрескожный вариант выполняют под краткосрочным внутривенным наркозом. Методика заключается в том, что под контролем УЗИ, через стенку живота в центр опухоли устанавливают специальный электрод, после чего в зависимости от методики проводят нагревание опухоли до высоких температур или 2 цикла замораживания и оттаивания, вследствие чего опухолевые клетки погибают.
Учитывая, что почки парный орган, даже выполнение нефрэктомии для пациента не смертельно, т.к. впоследствии оставшаяся почка берет на себя функции обеих, увеличивается в размерах и чаще всего адекватно функционирует. В некоторых, редких ситуациях, при наличии опухолей обеих почек и невозможности выполнить резекцию почек, жизненно необходимым может быть удаление обеих почек. В таком случае у пациента существует два возможных варианта компенсации функции почки: пересадка донорской почки или пожизненный гемодиализ (запрограммированный процесс очищения крови на специальном аппарате).
Несмотря на условную радикальность хирургического лечения, пациентам с отдаленным метастазами необходимо дополнительное лекарственное лечение с применением таргетных или иммуно-онкологических препаратов.
Ежегодно фармацевтические компании разрабатывают новые лекарственные препараты, которые еще не входят в существующие стандарты лечения, в связи с чем проводятся клинические исследования для оценки эффективности этих препаратов. Целью такого исследования является улучшение методов лечения рака, внедрение новых более эффективных препаратов и, как следствие, улучшение выживаемости пациентов. Если тот или иной препарат или методика в исследовании продемонстрировали свою эффективность и лучшие показатели выживаемости по сравнению с предшествующим стандартом лечения, то при ежегодном обновлении рекомендаций их также включают в алгоритмы лечения.
Иммунотерапия опухоли
Иммунотерапия способствует активизации собственных защитных ресурсов организма, а именно иммунитета. Вещества, вырабатываемые организмом или синтезированные в лаборатории, используют для повышения сопротивляемости организма и для борьбы с опухолью. Цитокины — это группа белков организма, которые активируют иммунную систему. Наиболее часто используемые цитокины для лечения рака почки — интерлейкин-2 (ИЛ-2) и интерферон-альфа.
Вещества, вырабатываемые организмом или синтезированные в лаборатории, используют для повышения сопротивляемости организма и для борьбы с опухолью. Цитокины — это группа белков организма, которые активируют иммунную систему. Наиболее часто используемые цитокины для лечения рака почки — интерлейкин-2 (ИЛ-2) и интерферон-альфа.
Интерлейкин-2 (ИЛ-2)
Ранее интерлейкин-2 использовался в качестве терапии первой линии для лечения рака почки, но учитывая тяжелые побочные явления и появление новых более эффективных таргетных препаратов, в настоящее время его применят только у строго отобранных больных, так как имеет серьезные побочные реакции. Онкологи предпочитают назначать интерлейкин 2 относительно здоровым и крепким пациентам либо тем, кто плохо отвечает на таргетные препараты.
Интерферон-альфа
У Интерферона-альфа менее серьезные нежелательные явления, чем у ИЛ-2. Интерферон-альфа в настоящее время не применяется в качестве самостоятельной терапии.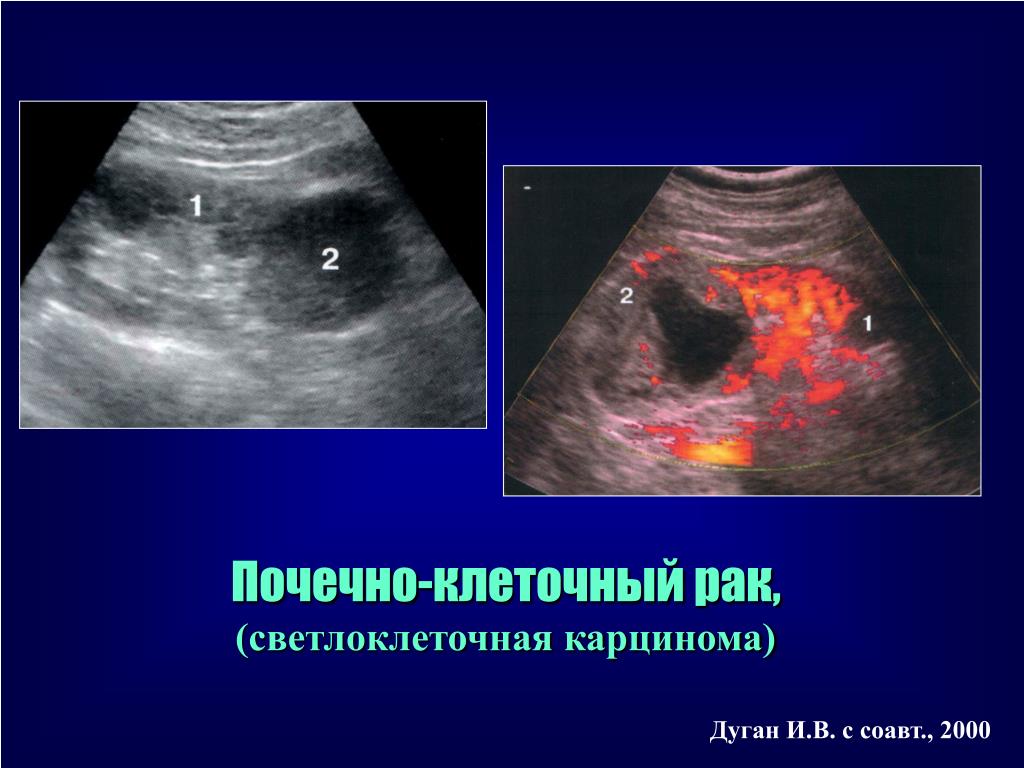 Его используют в комбинации с таргетным препаратом Бевацизумабом (Авастин).
Его используют в комбинации с таргетным препаратом Бевацизумабом (Авастин).
Иммунотерапия ингибиторами иммунных контрольных точек
Иммунная система защищает организм от болезни; для этого она должна отличать патогены/патологические клетки от собственных здоровых тканей организма. Иммунная система может идентифицировать и уничтожать клетки опухоли, если последняя продуцирует опухоль-специфичные антигены. Этот процесс называется иммунным надзором. Текущий иммунный ответ регулируется «пунктами иммунного контроля». Они предотвращают повреждение здоровых тканей организма. Опухолевые клетки иногда используют эти контрольно-пропускные пункты, чтобы «скрыться» от иммунной системы. Новые препараты – ингибиторы PD-1 и PD-L1 – фактически лишают их этой возможности.
Ниволумаб (Опдиво) — блокирует белок «запрограмированной смерти» PD-1, который находится на Т-лимфоците и сдерживает иммунные клетки от патологической реакции с нормальными клетками организма. Клетки опухоли синтезируют белок «запрограммированной смерти» PD-1 и тем самым скрываются от иммунной системы подобно нормальным клеткам организма. Блокируя белок PD-1, Ниволумаб повышает иммунный ответ против опухоли, что приводит к уменьшению первичного очага и метастазов или замедляет их рост. Механизм возможного развития побочных эффектов связан с тем, что блокирование белка «запрограмированной смерти» PD-1 приводит не только к активации противоопухолевого иммунитета, но и возможной аутоиммунной реакции на здоровые клетки организма, что может вызвать серьезные или даже опасные для жизни побочные эффекты, связанные с поражением легких, кишечника, печени, почек или т.д. Важно своевременно сообщать о любых новых побочных эффектах вашему врачу.
Клетки опухоли синтезируют белок «запрограммированной смерти» PD-1 и тем самым скрываются от иммунной системы подобно нормальным клеткам организма. Блокируя белок PD-1, Ниволумаб повышает иммунный ответ против опухоли, что приводит к уменьшению первичного очага и метастазов или замедляет их рост. Механизм возможного развития побочных эффектов связан с тем, что блокирование белка «запрограмированной смерти» PD-1 приводит не только к активации противоопухолевого иммунитета, но и возможной аутоиммунной реакции на здоровые клетки организма, что может вызвать серьезные или даже опасные для жизни побочные эффекты, связанные с поражением легких, кишечника, печени, почек или т.д. Важно своевременно сообщать о любых новых побочных эффектах вашему врачу.
Благодаря достижениям молекулярной биологии и генетики мы больше знаем о молекулярных и генетических изменениях происходящих в опухолевых клетках. В настоящее время эра иммунотерапии цитокинами сменилась эрой таргетной терапии рака почки, препаратами, способными прицельно влиять на молекулярном уровне на опухоль. Такая терапия в значительной степени отличается от химиотерапии и иммунотерапии за счет менее выраженных побочных эффектов. Как известно, ни химиотерапия, ни лучевая терапия не продемонстрировали своей эффективности при раке почки.
Такая терапия в значительной степени отличается от химиотерапии и иммунотерапии за счет менее выраженных побочных эффектов. Как известно, ни химиотерапия, ни лучевая терапия не продемонстрировали своей эффективности при раке почки.
Таргетные препараты в настоящее время являются основными в лекарственной терапии рака почки, они используются как в первой, так и во второй линии терапии. Таргетные препараты блокируют образование новых сосудов (неоангиогенез), питающих опухоль через выработку необходимых белков (тирозинкиназ и факторов роста с их рецепторами), которые помогают опухоли расти и развиваться. В большинстве случаев таргетные препараты уменьшают или замедляют рост существующих опухолевых очагов в течение продолжительного времени. Однако с течением времени даже на фоне терапии таргетными препаратами, может развиться прогрессирование опухолевого процесса, что потребует смены препарата первой линии терапии на препарат второй линии. В настоящее время продолжаются исследования сравнивающие эффективность одних препаратов с другими, с оценкой целесообразности последовательного их применения или использования в комбинации.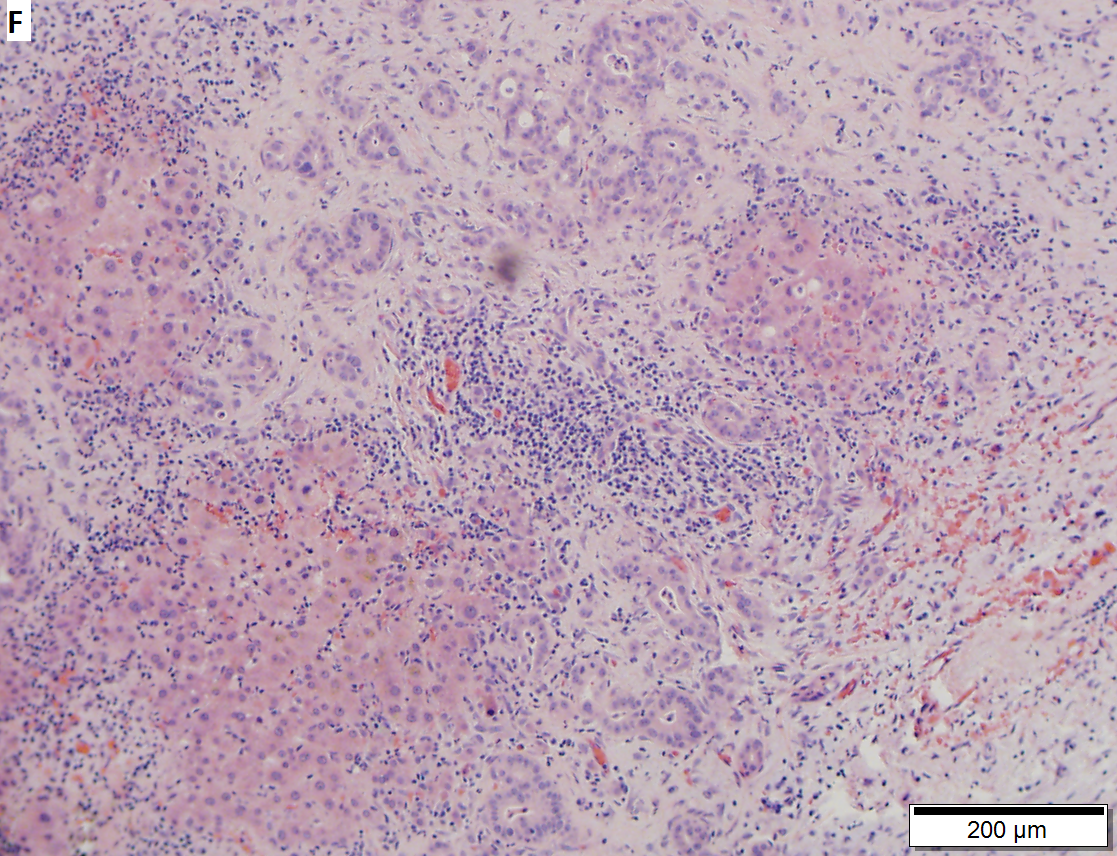
Основные таргетные препараты при раке почки:
Сунитиниб (Сутент)
Сунитиниб блокирует несколько тирозинкиназ и неоангиогенез. Препарат выпускается в таблетках по 50 мг; 37,5 мг и 25 мг и используется только в терапии первой линии у больных светлоклеточными и несветлоклеточными вариантами рака почки. Стандартный режим приема по 50 мг один раз в день в течение 4 недель с последующими 2 неделями перерыва. В случае выраженной непереносимости препарата, необходимо обратиться к врачу.
Бевацизумаб (Авастин)
Бевацизумаб замедляет рост новых кровеносных сосудов за счет блокирования фактора роста сосудов. Для лечения распространенного рака почки применяется в комбинации с интерфероном-альфа.
Пазопаниб (Вотриент)
Пазопаниб — это еще один препарат, который блокирует несколько тирозинкиназ, участвующих в росте раковых клеток, и образовании новых кровеносных сосудов опухоли. Препарат выпускается в таблетках по 400 мг и используется только в терапии первой линии у больных светлоклеточными вариантами рака почки.
Препарат выпускается в таблетках по 400 мг и используется только в терапии первой линии у больных светлоклеточными вариантами рака почки.
Сорафениб (Нексавар)
Сорафениб блокирует неоангиогенез через воздействие на внутриклеточные белки (тирозинкиназы), которые важны для роста и развития опухолевых клеток. Препарат выпускается в таблетках по 200 мг и принимается по 2 таблетки два раза в день. Препарат преимущественно рекомендуется применять в терапии второй и последующих линий после иммунотерапии цитокинами или у больных, получивших ранее терапию ингибиторами тирозинкиназ и ингибиторами mTOR, но также в некоторых случая возможно его применение в первой линии.
Темсиролимус (Торизел)
Темсиролимус блокирует клеточный белок mTOR , который стимулирует рост и деление клеток. В исследованиях продемонстрировано, что наилучшие результаты этот препарат показал у больных неблагоприятного прогноза и у пациентов с несветлоклеточными вариантами опухоли в первой линии.
Эверолимус (Афинитор)
Эверолимустакже блокирует белок mTOR, но чаще всего используется в качестве второй и последующих линии таргетной терапии, после неэффективности ингибиторов тирозинкиназ (Сорафениба, Сунитиниба, Пазопаниба). Препарат выпускается в таблетках по 10 мг и 5 мг.
Акситиниб (Инлита)
Ингибирует несколько белков тирозинкиназ, в том числе участвующих в образовании новых кровеносных сосудов. Препарат используется во второй линии терапии и выпускается в дозировках 5 мг, 3 мг и 1 мг. Стандартным режимом приема является 5 мг по 1 таблетке 2 раза в день, но существуют и альтернативные варианты приема у пациентов, так у хорошо переносящих начальную дозировку без побочных эффектов возможно применение препарата в дозе 7мг или 10 мг дважды в сутки.
Кабозантиниб (Кабометикс)
Относится к мультикиназным ингибиторам, блокирующим факторы роста сосудов и развития опухоли. Препарат выпускается в таблетках по 60 мг, 40 мг и 20 мг, и используется только в терапии второй и последующих линий у больных раком почки.
Ленватиниб (Ленвима)
также относится к мультикиназным ингибиторам, блокирующим неоангиогенез. Препарат выпускается в таблетках по 10 мг и 4 мг, и используется только в терапии второй и последующих линий у больных распространенным раком почки. Ленватиниб необходимо принимать в дозе 18 мг (таблетка 10 мг и 2 таблетки по 4 мг) один раз в день в комбинации с препаратом Эверолимус в дозе 5 мг один раз в день. В случае выраженной непереносимости препарата, необходимо обратиться к врачу, который поможет скорректировать дозу препаратов, если это необходимо, и справиться с нежелательными эффектами.
Рак почки устойчив к химиотерапии, в связи с чем она не используется в лечении рака почки. Однако некоторые химиопрепараты, такие как Винбластин, Флуксуридин, 5-фторурацил (5-ФУ), Капецитабин и Гемцитабин, эффективны для некоторых вариантов рака почки, таких как рак собирательных трубочек Беллини и опухоль Вильмса. Побочные эффекты химиотерапии индивидуальны и зависят от препарата и используемой дозы.
Лучевая терапия в качестве самостоятельного метода лечения первичной опухоли почки не продемонстрировала своей эффективности и в настоящее время продолжаются исследования по оценке стереотаксической лучевой терапии в лечении рака почки начальных стадий. На сегодняшний день лучевую терапию рекомендуют применять с паллиативной целью для облегчения болевого синдрома у пациентов с метастазами в костях и для лечения метастазов в головном мозге.
Активное наблюдение после лечения рака почкиМетодика активного наблюдения заключается в тщательном динамическом наблюдении за темпом роста опухоли почки посредством регулярных обследований (КТ, ПЭТ/КТ, МРТ и УЗИ). Тактику активного наблюдения применяют, как правило, у пожилых или ослабленных пациентов с небольшой опухолью почки (менее 4 см), которым нельзя выполнить других радикальных методов лечения.
Прогноз рака почкиУ многих пациентов после установления диагноза, возникает вопрос о возможной продолжительности жизни. Согласно существующей статистике имеется множество возможных причин смерти человека, среди которых первые места занимают сердечно-сосудистые заболевания (такие как инфаркт, инсульт), а также травмы и отравления. Эти состояния, как правило, развиваются остро. Онкологические заболевания и рак почки в частности, к острым состояниям не относится, он является хроническим заболеванием с периодами стабилизации и возможным прогрессированием. Ваш врач, основываясь на статистике выживаемости пациентов с аналогичным диагнозом, может привести примерные показатели выживаемости в зависимости от стадии рака почки. В онкологии существуют показатели 5-летней выживаемости. Эти показатели характеризуют группу больных, которые прожили 5 лет после установления диагноза без прогрессирования. Несомненно, многие пациенты живут гораздо дольше и некоторые могут погибнуть совершенно от других (неопухолевых) причин. Стоит помнить, что это всего лишь статистика и за последние 5-10 лет в онкологии, и в лечении рака почки, произошли кардинальные изменения с появлением новых высокоэффективных препаратов, что значительно улучшило прогноз и увеличило продолжительность жизни пациентов.
Согласно существующей статистике имеется множество возможных причин смерти человека, среди которых первые места занимают сердечно-сосудистые заболевания (такие как инфаркт, инсульт), а также травмы и отравления. Эти состояния, как правило, развиваются остро. Онкологические заболевания и рак почки в частности, к острым состояниям не относится, он является хроническим заболеванием с периодами стабилизации и возможным прогрессированием. Ваш врач, основываясь на статистике выживаемости пациентов с аналогичным диагнозом, может привести примерные показатели выживаемости в зависимости от стадии рака почки. В онкологии существуют показатели 5-летней выживаемости. Эти показатели характеризуют группу больных, которые прожили 5 лет после установления диагноза без прогрессирования. Несомненно, многие пациенты живут гораздо дольше и некоторые могут погибнуть совершенно от других (неопухолевых) причин. Стоит помнить, что это всего лишь статистика и за последние 5-10 лет в онкологии, и в лечении рака почки, произошли кардинальные изменения с появлением новых высокоэффективных препаратов, что значительно улучшило прогноз и увеличило продолжительность жизни пациентов.
На выживаемость влияет множество факторов: время установления диагноза, стадия, гистологическая структура опухоли, возраст, общее состояние пациента и некоторые лабораторные показатели крови. Ваш врач, зная вашу историю болезни и лабораторные анализы, может рассказать вам к какой группе риска вы относитесь.
Стадии и шансы на выживание
I стадия. Опухоль имеет небольшие размеры, дочерние образования отсутствуют. Прогнозы оптимистические, во всех случаях ожидается выздоровление; II стадия. Опухоль характеризуется четкими очертаниями, она четко просматривается на снимке, имеет единственное метастатическое образование в ближнем лимфоузле. Прогнозы позитивные: большинство пациентов выздоравливает;
III стадия. На этой стадии опухоль условно оперируемая. Количество вылеченных пациентов меньшее, прогнозы удовлетворительные;
IV стадия.Хирургия становится возможной только в случае обнаружения в опухоли и больных тканях некроза. Он приводит к стремительной интоксикации всего организма и к быстрой смерти пациента. Если некротических процессов нет, метастазирование обширное, ткани с вторичными опухолями неоперабельны, то хирургическое вмешательство противопоказано и операция не делается. Прогнозы негативные.
Он приводит к стремительной интоксикации всего организма и к быстрой смерти пациента. Если некротических процессов нет, метастазирование обширное, ткани с вторичными опухолями неоперабельны, то хирургическое вмешательство противопоказано и операция не делается. Прогнозы негативные.
ФГБУ «НМИЦ радиологии» Минздрава России обладает всеми необходимыми технологиями лучевого, химиотерапевтического и хирургического лечения, включая расширенные и комбинированные операции. Все это позволяет выполнить необходимые этапы лечения в рамках одного Центра, что исключительно удобно для пациентов.
1. Урологическое отделение МНИОИ имени П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России
Заведующий – к.м.н, ВОРОБЬЁВ Николай Владимирович
тел.: +7(495) 150-11-22
2. Отделение лучевого и хирургического лечения урологических заболеваний с группой брахитерапии рака предстательной железы МРНЦ имени А.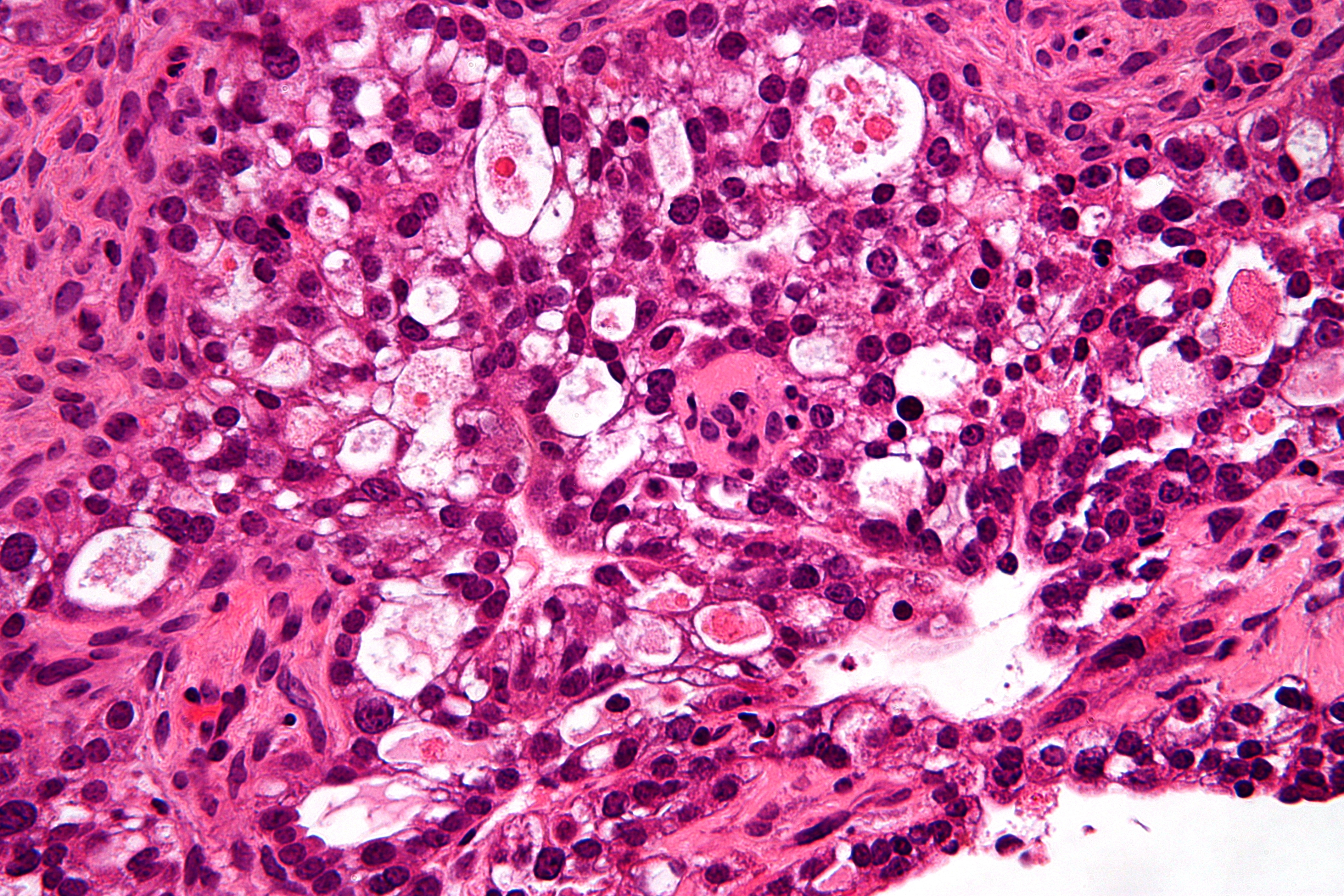 Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России г. Обнинск, Калужской области
Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России г. Обнинск, Калужской области
Заведующий — д.м.н., профессор КАРЯКИН Олег Борисович
тел.: +7 (484) 399-31-30
3. Онкологическое-урологическое отделение НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиала ФГБУ «НМИЦ радиологии» Минздрава России
Заведующий отделением – к.м.н. КАЧМАЗОВ Александр Александрович
тел.: +7(499) 110 40 67
Почечно-клеточный рак. Светлоклеточная карцинома почки. — 24Radiology.ru
Почечно-клеточная карцинома является типичным шарообразным образованием. Почечно-клеточная карцинома является случайной находкой выявленная у пациентов, обратившихся с жалобами не связанными с патологии мочевыделительной системы.
Пик заболеваемости 60-70 лет. Почечно-клеточная карцинома связана с наследственными синдромами такими, как синдром Хиппель-Линдау, туберозным склерозом и Бирт-Хогг-Дубе.
Самый распространённый подтип почечно-клеточной карциномы является светло-клеточная карцинома почек, затем папиллярная и хромофобная почечно-клеточная карцинома. Медуллярная и кистозных многокамерная почечно-клеточная карцинома встречается крайне редко.
Медуллярная и кистозных многокамерная почечно-клеточная карцинома встречается крайне редко.
Светло-клеточная карцинома.
Светло-клеточная карцинома почек составляет 70% случаев рака почек.
Данная опухоль чаще больших размеров и прорастает из почечной коры. Светло-клеточная карцинома является гиперваскулярным образованием с неоднородным содержимым, как следствие некроза, кровоизлияний, кальцинирования или образование внутри кист. В редких случаях почечно-клеточная карцинома содержит внеклеточный жир, соответственно, образование с включением жира и кальцинатов следует рассматривать, как почечно-клеточную карциному.
Характерной особенностью светлоклеточной карциномы явлечётся значительное усиление в кортикомедуллярную фазу.
Хотя трудности бывают, когда образование небольших размеров и локализуется в почечной коре, которая также хорошо контрастируется.
Поэтому нефрографическая фаза при образованиях такой локализации и размеров является для оценки наиболее важной так, как паренхима контрастируется гомогеннее и сильнее, чем опухоль, что хорошо заметно на ниже приведённых изображениях.
На МРТ светло-клеточная карцинома визуализируется, как гипоинтенсивное образование на Т1 и гиперинтенсивное на Т2. Как правило, почечно-клеточная карцинома не имеет экстрацеллюлярного жира, что, соответственно, отличает её от ангиомиолипомы. Хотя в 80% случаях светло-клеточной карциномы есть внутриклеточный жир, что приводит к снижению сигнала на Т1 opposed-phase в сравнении с in-phase изображениями. В данных ситуациях не стоит делать вывод о том, что жир внеклеточный, который характерен в большей степени для ангиомиолипомы. Болезнь Фон-Гиппель-Линдау ассоциирована с развитием светло-клеточной карциномы почек, чаще мультифокальной и билатеральной. Пациенты со светло-клеточной карциномой имеет 5-летнюю выживаемость, что является прогнозом хуже, чем у пациентов с папиллярной и хромофобной карциномой.
Порядка 5% всех светло-клеточных карцином имеют инфильтративный характер роста. Несмотря на то, что это лишь небольшая часть от всех почечно-клеточных карцинома, нельзя забывать про них при построении дифференциального ряда бобовидных образований почки с инфильтративным типом роста. Почечно-клеточные карциномы с инфильтративным типом роста являются агрессивными и гиперваскулярными, которые изменяют внутреннюю архитектуру почек, но не наружные контуры, а изменения лоханки схожи с изменениями при переходно-клеточном раке почки.
Почечно-клеточные карциномы с инфильтративным типом роста являются агрессивными и гиперваскулярными, которые изменяют внутреннюю архитектуру почек, но не наружные контуры, а изменения лоханки схожи с изменениями при переходно-клеточном раке почки.
Используемая литература.
Классификация рака почки. Клиническая картина
Морфологическая классификация
В основе традиционных классификаций рака почки лежат особенности морфологии клетки и клеточного ядра. Современные классификации учитывают данные морфологических, цитогенетических и молекулярных исследований и выделяют 5 видов рака почки:
- Светлоклеточный – 60-85%
- Хромофильный (Папиллярный) — 7-14%
- Хромофобный – 4-10%
- Онкоцитарный – 2-5%
- Рак собирательных протоков – 1-2%
О прогностической значимости различных вариантов почечно-клеточного рака будет сказано ниже.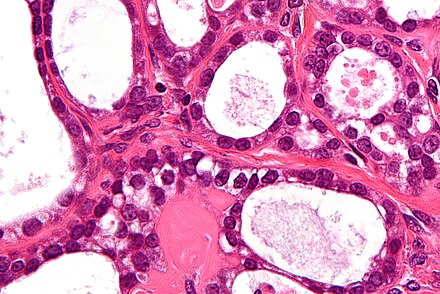
Метастазирование
Рак почки метастазирует гематогенным и лимфогенным путем. Метастазы обнаруживаются у 25% пациентов на момент установления диагноза . Выживаемость данных больных составляет от 6 до 12 месяцев и только 10% переживают 2 года. Приблизительно у 30-50% больных в различные сроки после нефрэктомии появляются метахронные метастазы. Прогноз последней группы несколько лучше, однако, 5-летняя выживаемость не превышает 9%. По данным Saitoh et al. (1982) наиболее частыми локализациями множественных метастазов являются легкие 76%, лимфатические узлы 64%, кости 43%, печень 41%, ипсилатеральный и контралатеральный надпочечник 19% и 11,5%, контралатеральная почка 25%, головной мозг 11.2%. Солитарные метастазы или метастатическое поражение только одного органа имеет место только в 8-11% случаев.
Говоря о течении метастатической болезни при раке почки, нельзя не упомянуть о случаях спонтанной регрессии и стабилизации. Спонтанная регрессия отмечается у 0,4%-0,8% больных раком почки. Это касается в подавляющем большинстве случаев регрессии легочных метастазов. Стабилизация болезни, определяемая, как отсутствие роста и появления новых метастазов, наблюдается у 20-30% больных. С такой же частотой отмечается стабилизация болезни (отсутствие роста первичной опухоли) у больных раком почки без метастазов. Этот феномен должен учитываться при решении вопроса о хирургическом или системном лечении больных с высоким риском, которые в действительности, могут прожить дольше без всякого лечения.
Это касается в подавляющем большинстве случаев регрессии легочных метастазов. Стабилизация болезни, определяемая, как отсутствие роста и появления новых метастазов, наблюдается у 20-30% больных. С такой же частотой отмечается стабилизация болезни (отсутствие роста первичной опухоли) у больных раком почки без метастазов. Этот феномен должен учитываться при решении вопроса о хирургическом или системном лечении больных с высоким риском, которые в действительности, могут прожить дольше без всякого лечения.
Классификация рака почки
Почечно-клеточный рак характеризуется весьма вариабельным клиническим течением, что обусловлено генетической гетерогенностью и морфологическим разнообразием данной группы опухолей.
В настоящее время в России, как и во многих странах, используется классификация, предложенная Международным противораковым союзом ((UICC) tumor, node, metastasis (TNM)), подробно освещающая степень распространенности опухолевого процесса с целью определения лечебной тактики.
TNM клиническая классификация почечно-клеточного рака (2002)
Т — первичная опухоль
ТХ — первичная опухоль не может быть оценена
Т0 — нет данных о первичной опухоли
Т1 — опухоль не более 7 см в наибольшем измерении, ограниченная почкой
- T1a — опухоль до 4 см
- T1b — опухоль 4-7 см
Т2 — опухоль более 7 см в наибольшем измерении, ограниченная почкой
Т3 — опухоль распространяется в крупные вены, или инвазирует надпочечник, или окружающие ткани, но не выходит за пределы фасции Герота
- Т3а — опухолевая инвазия надпочечника или паранефральной клетчатки впределах фасции Герота
- Т3b — опухоль распространяется в почечную вену или нижнюю полую вену ниже диафрагмы
- Т3с — опухоль распространяется в нижнюю полую вену выше диафрагмы или инвазирует ее стенку.
Т4 — Опухоль распространяется за пределы фасции Герота
Рисунок 1.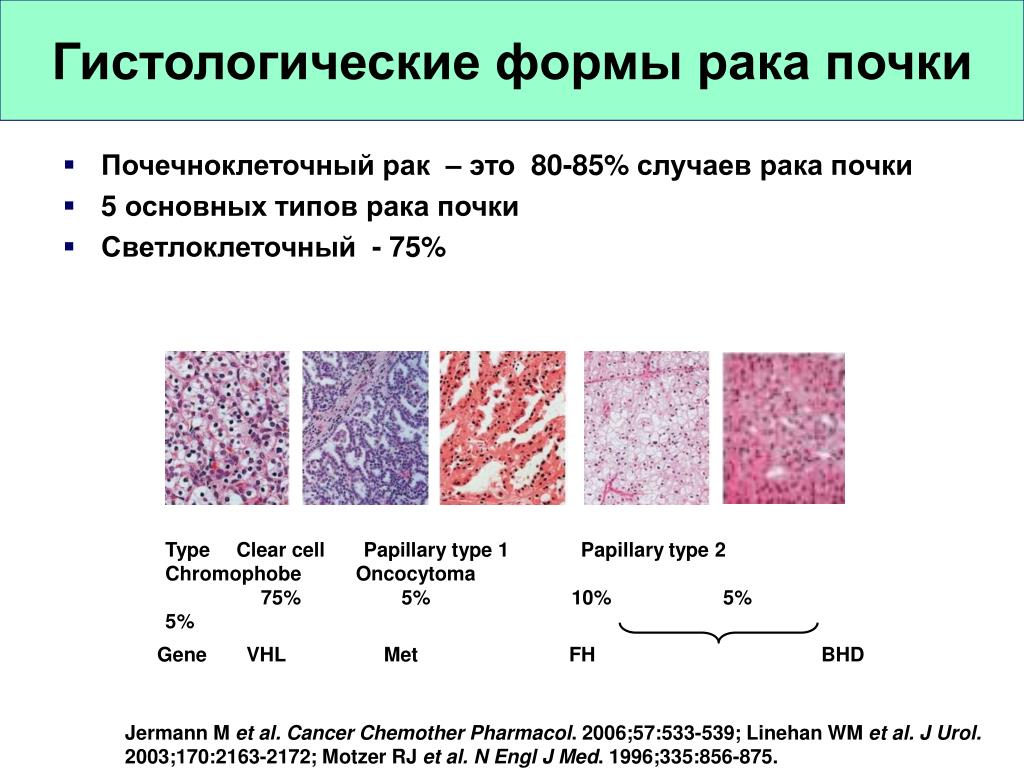 Схематическое изображение стадий Т1 и Т2
Схематическое изображение стадий Т1 и Т2
Рисунок 2. Схематическое изображение стадий Т3а и Т3b
N — регионарные лимфатические узлы
NX — регионарные лимфатические узлы не могут быть оценены
N0 — нет метастазов в регионарных лимфатические узлах
N1 — метастаз в одном регионарном лимфатическом узле
N2 — метастазы более чем в одном регионарном лимфатическом узле
М — отдаленные метастазы
МХ — отдаленные метастазы не могут быть оценены
М0 — нет отдаленных метастазов
М1 — отдаленные метастазы
pTNM — патологоанатомическая классификация
pT, pN и pM категории соответствуют T, N и М категориям
G — гистопаталогическая градация
GX — степень дифференцировки не может быть оценена
G1 — высоко дифференцированная опухоль
G2 — умеренно дифференцированная опухоль
G3-4 — низко дифференцированная/недифференцированная опухоль
Группировка по стадиям
|
Стадия I |
Т1 |
N0 |
M0 |
|
Cтадия II |
T2 |
N0 |
M0 |
|
Стадия III |
T1 |
N1 |
M0 |
|
Т2 |
N1 |
M0 |
|
|
T3 |
N0, N1 |
M0 |
|
|
Стадия IV |
T4 |
N0, N1 |
M0 |
|
любая Т |
N2 |
M0 |
|
|
любая Т |
любая N |
M1 |
Факторы прогноза
Клинические факторы
Одним из важнейших направлений современной онкоурологии является выделение факторов, позволяющих составить индивидуальный прогноз и определить оптимальную тактику лечения больных раком почки.
По данным ряда авторов прогностически неблагоприятным являются: тяжелое общее состояние больного, наличие клинических симптомов заболевания на момент установления диагноза, снижение массы тела более чем на 10%. Напротив, возраст, пол и национальность не влияют на прогноз. В ряде исследований продемонстрировано достоверное неблагоприятное влияние на выживаемость увеличения скорости оседания эритроцитов (СОЭ), гаптоглобулина, ферритина, С-реактивного белка, орозомукоида, ?-1-антитрипсина, интерлейкина-6.
У больных диссеминированным почечно-клеточным раком прогностическое значение имеют анемия, гиперкалиемия, гипоальбуминемия и повышение уровня щелочной фосфатазы сыворотки крови.
Показано влияние на исход заболевания таких факторов, как хромогранин А, нейронспецифическая энолаза (NSE), раковый антиген 125 (СА-125), опухоль-ассоциированный ингибитор трипсина (TATI) и эритропоэтин. В настоящее время проводятся исследования, посвященные изучению генетических маркеров в крови и моче, которые могут позволить составить индивидуальный прогноз больных раком почки.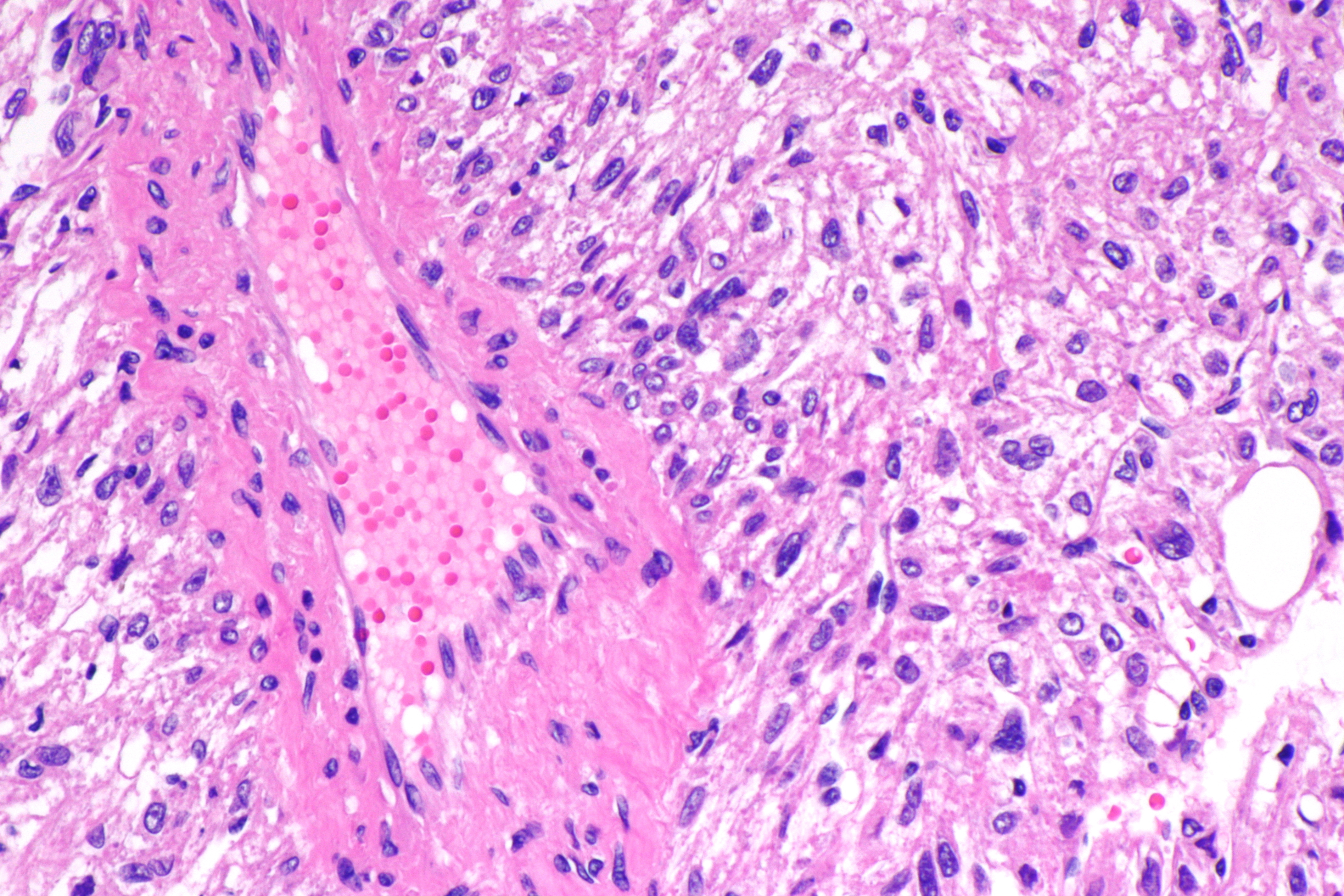
Патоморфологические факторы
Стадия опухолевого процесса (Т), отражающая анатомическую распространенность новообразования, является наиболее значимым фактором прогноза при раке почки. Пациенты с опухолью, ограниченной почкой, имеют лучший прогноз. Инвазия за пределы капсулы Герота (T3a) уменьшает выживаемость на 27%, наличие опухолевого тромбоза почечной и нижней полой вен (T3b-c) – на 40% (таблица 1, рисунок 3).
Рисунок 3. Выживаемость 2507 больных раком почки в зависимости от стадии Т
Таблица 1. Выживаемость 2507 больных раком почки в зависимости от стадии Т
|
Стадия T |
5-летняя выживаемость (%) |
|
I |
75,8 |
|
II |
66,8 |
|
IIIa |
39 |
|
IIIb-с |
25,7 |
|
IV |
14,3 |
Инвазия в коллатеральные вены и капилляры также является неблагоприятным фактором прогноза.

Наличие метастазов в лимфатические узлы у больных раком почки ассоциировано с крайне плохим прогнозом.
5 лет переживает от 5% до 30% пациентов (рисунок 4).
Рисунок 4. Выживаемость 2507 больных раком почки в зависимости от стадии N
Появление отдаленных метастазов резко ухудшает прогноз при раке почки. 5-летняя выживаемость больных диссеминированным раком почки составляет 14,6%, что достоверно меньше, чем в группе пациентов с локализованной опухолью (57,3%) (р=0,0000) (рисунок 5). При наличии отдаленных метастазов стадия Т почечно-клеточного рака прогностического значения не имеет.
Большая продолжительность жизни при диссеминированном почечно-клеточном раке наблюдается при метахронном появлении метастазов и солитарных опухолевых очагах, локализующихся в одном органе. Одним из наиболее важных прогностических факторов является возможность радикального удаления всех определяемых метастазов.
Рисунок 5. Выживаемость 2507 больных раком почки в зависимости от стадии М
Гистопатоморфологические признаки
Большинство современных гистологических классификаций принимает во внимание морфологические признаки клеточного ядра, которые являются независимыми факторами прогноза, занимающими второе место по значимости после стадии заболевания. 5-летняя выживаемость пациентов с опухолями GI составляет 76%, GII – 72%, GIII – 51%, GIV – 35%.
Плоидность ДНК коррелирует с целлюлярной кинетикой почечно-клеточного рака: в диплоидных опухолях отмечается более низкий уровень фракции клеток, находящихся в S-фазе, а также более продолжительное время удвоения опухоли, чем в анеуплоидных клонах, что ассоциировано с благоприятным прогнозом .
На выживаемость больных раком почки влияет митотический индекс. Выявлено, что при наличии менее 1 фигуры митоза на 10 полей зрения при малом увеличении 10-летняя выживаемость составляет 67%, более 1 – 16%.
Генетические факторы
Как было отмечено выше, современные классификации рака почки учитывают не только морфологические, но и цитогенетические особенности опухоли, обуславливающие различное клиническое течение.
Традиционный (не папиллярный) рак составляет 75% всех эпителиальных опухолей почки и характеризуется наличием делеции хромосомы 3р. Только в опухолях данного типа имеет место мутация гена VHL. Данный тип рака почки имеет более высокий метастатический потенциал и отличается худшей выживаемостью по сравнению с папиллярной и хромофобной формами.
При папиллярной форме рака почки обычно выявляется комбинация трисомий по 7,17,3q,8,12,16 и 20 хромосомам, а также утрата Y хромосомы. Папиллярная карцинома часто бывает двухсторонней и мультифокальной, ассоциирована с лучшей выживаемостью, чем традиционный, но худшей, чем хромофобный тип опухоли (рисунок 6).
Для хромофобного рака характерно уменьшение количества хромосом в сочетании с гетерозиготностью по хромосомам 1,2,6,10,13,17,21,X и гипоплоидным содержанием ДНК. Данная форма почечно-клеточного рака имеет низкий метастатический потенциал. Выживаемость больных хромофобными опухолями больше, чем в группе пациентов с папиллярной и традиционной формами рака почки.
Рак собирательных протоков является редкой опухолью, составляющей 1%-2% всех случаев почечно-клеточного рака. Рак собирательных протоков является очень агрессивной опухолью с высоким метастатическим потенциалом.
Таким образом, генетические альтерации детерминируют туморогенез и степень злокачественности опухолевого процесса при различных формах почечно-клеточного рака.
Рисунок 6. Выживаемость больных в зависимости от формы почечно-клеточного рака
Факторы регуляции клеточного цикла
В ряде исследований отмечено прогностическое значение изменений, происходящих в системе регуляции клеточного цикла в процессе развития опухоли. Система регуляции клеточного цикла представлена протеинами, такими как циклины, циклин-зависимые киназы (CDK), CDK-ингибиторы и специфические фосфорилированные и нефосфорилированные субстраты. Белки-регуляторы клеточного цикла являются продуктами экспрессии протоонкогенов. Трансформация протоонкогена в онкоген является одной из ключевых аберраций туморогенеза, приводящей к нарушению регуляции клеточного цикла, обуславливающему повреждение механизмов контроля за клеточным ростом, пролиферацией и апоптозом.
Факторы ангиогенеза
Ангиогенез является важнейшим фактором, определяющим прогрессию опухоли и оказывающим существенное влияние на прогноз больных почечно-клеточным раком. Увеличение новообразования более чем на 1 мм требует появления новых сосудов. Существенную роль в туморогенезе играет сосудистый эндотелиальный фактор роста (VEGF). В настоящее время проводятся исследования, посвященные изучению прогностической роли других факторов (фактора некроза опухоли (TNF-?), основного фактора роста фибробластов (bFGF)) и ингибиторов ангиогенеза (ангиостатина, фактора некроза опухоли (TNF-?)).
Клинические проявления рака почки
Классическая триада симптомов, описываемая ранее при раке почки у 15% больных (боль, макрогематурия и пальпируемая опухоль), в настоящее время встречается редко. В большинстве случаев заболевание протекает бессимптомно.
Клинические проявления возникают в основном при поздних стадиях. Среди местных симптомов наиболее часто отмечаются боль и гематурия. Боли в пояснице и животе возникают при инвазии или компрессии растущей опухолью окружающих структур, а также при почечной колике, обусловленной окклюзией мочеточников сгустками крови. Острая боль может быть следствием кровоизлияния в опухоль или ее разрыва с формированием забрюшинной гематомы. Прощупываемая опухоль – третий местный симптом рака почки, бывает положительным у 12-15% на момент установления диагноза. Появление варикоцеле отмечают до 3.3% больных .
Артериальная гипертензия — непостоянный симптом, (вызываемый сдавлением сегментарных артерий, окклюзией мочеточника, метастазами в головной мозг, формированием артерио-венозных шунтов, или повышенной секрецией опухолью ренина) наблюдается у 15% больных раком почки.
Синдром сдавления нижней полой вены (НПВ) (отеки ног, варикоцеле, расширение подкожных вен живота, тромбоз глубоких вен нижних конечностей, протеинурия) развивается у 50% больных при опухолевом тромбозе НПВ или при компрессии НПВ опухолью и увеличенными лимфатическими узлами.
Рак почки характеризуется большим разнообразием паранеопластических синдромов, наблюдаемых более чем у половины больных. Одной из функций нормальной почечной паренхимы является продукция различных биологически активных веществ (эритропоэтин, ренин, простагландины, простациклины, тромбоксаны, образование активной формы витамина D). Наличие опухоли может приводить к повышенной секреции вышеуказанных субстанций, либо к продукции других гормонов, таких как паратгормон, инсулин, глюкагон, человеческий хорионический гонадотропин. В результате у пациентов может отмечаться артериальная гипертензия, эритроцитоз, гиперкальциемия, гипертермия и др. Появление вышеуказанных симптомов может быть единственным проявлением заболевания и должно настораживать врача в отношении возможного опухолевого поражения почек. После радикального удаления опухоли паранеопластические проявления, как правило, исчезают, но могут возникнуть вновь при развитии местного рецидива или отдаленных метастазов. Таким образом, последние могут быть использованы для мониторинга заболевания.
Редкой формой паранеопластического синдрома является амилоидоз (1.7%). Сохраняющий после нефрэктомии амилоидоз является крайне неблагоприятным фактором прогноза.
До сих пор непонятным остается возникновение в ряде случаев печеночной недостаточности при отсутствии ее метастатического поражения. При этом у больных раком почки отмечается гипоальбуминемия, повышение щелочной фосфатазы, лейкопения, лихорадка, возможно появление очагов некроза печеночной паренхимы (синдром Штафера). Восстановление функции печени после нефрэктомии является благоприятным прогностическим признаком.
Особенное место в клинической картине рака почки занимают симптомы, обусловленные метастазированием, так как более 25% больных имеют отдаленные метастазы на момент установления диагноза. Первым проявлением поражения легких являются кашель и кровохарканье. Костные метастазы могут манифестировать болевым синдромом, развитием патологических переломов, компрессией спинного мозга, появлением пальпируемой опухоли. Поражение головного мозга сопровождается быстрым появлением и нарастанием неврологической симптоматики. Множественные метастазы в печень могут проявляться желтухой.
Такие общие симптомы, как анемия, высокая СОЭ, потеря аппетита, похудание, слабость являются признаками поздних стадий.
Рак почки: диагностика и лечение
Рак почки занимает десятое место по уровню заболеваемости среди злокачественных новообразований. Однако по динамике прироста уступает только раку простаты – количество новых диагностированных случаев увеличивается на 2,5% в год.
Что такое рак почки? Почка – парный орган бобовидной формы, лежащий на задней стенке брюшной полости позади брюшины по бокам позвоночного столба на уровне последнего грудного и двух верхних поясничных позвонков. Почки фильтруют кровь, выводя отходы жизнедеятельности с мочой, которая производится микроскопическими проксимальными канальцами и течет по мочеточникам в мочевой пузырь.
В большинстве случаев рак развивается из эпителия канальцев и собирательных трубочек (почечно-клеточный рак). Но иногда новообразование может формироваться из эпителия чашечно-лоханочной системы (переходно-клеточный рак).
Обычно новообразование представляет собой единую массу внутри почки. Однако орган может содержать более одной опухоли, а иногда рак поражает сразу обе почки.
Виды рака почки
Почечно-клеточная карцинома является самой распространенной формой рака почки. Ее типы включают светлоклеточную, папиллярную, хромофобную карциному, а также карциному собирающего протока.
Светлоклеточная карцинома составляет 80% всех случаев почечно-клеточного рака. На втором месте по частоте заболеваемости стоят папиллярные карциномы почек – они диагностируются в 10-15% случаев и зачастую хорошо поддаются лечению. Примерно в 5% встречаются хромофобные опухоли. Наиболее редкие (менее 1% случаев), но одновременно и наиболее агрессивные и трудные в лечении, — карциномы собирающих отделов почечных канальцев.
В педиатрии наиболее часто встречается опухоль Вильмса. В 90% случаев этот вида рака диагностируется у детей младше 5 лет.
Рак мочевого тракта (переходно-клеточный рак), возникший в почечной лоханке или мочеточнике, называется уротелиальной карциномой. Он не является, по сути, раком почки, хотя нередко и называется таковым.
Причины и группы риска
Несмотря на многочисленные исследования в данной области, однозначно причины развития злокачественных клеток в почке не установлены. Специалисты выделяют несколько факторов риска, повышающих шансы заболеть.
Курение. Получение канцерогенов вместе с табачным дымом считается главным провоцирующим фактором возникновения рака почки.
Возраст. Большинство случаев заболевания диагностируется у лиц старше 50-ти, пик заболеваемости приходится на 60-70 лет.
Пол. Мужчины вдвое чаще подвержены раку почек, чем женщины. У мужчин заболевание занимает восьмое место среди всех видов онкологии, а у женщин – одиннадцатое.
Наличие хронических заболеваний. Ожирение, гипертония, поздние стадии неонкологических болезней почек, длительный диализ могут спровоцировать развитие злокачественной опухоли в этом органе.
Наследственность. От родителей к детям передаются редкие заболевания почек, такие как болезнь фон Гиппеля-Линдау или наследственная папиллярная почечно-клеточная карцинома. Кроме того, наличие среди родственников двух и более человек с диагностированным раком почки повышает шансы заболеть этим видом онкологии.
Работа на вредных производствах. Воздействие асбеста, кадмия, кокса, бензина, гербицидов и органических растворителей также могут спровоцировать появление карциномы в почке.
Симптомы
Из-за особенности расположения почек многие люди не ощущают новообразования до тех пор, пока опухоль не достигнет довольно больших размеров. Кроме того, признаки рака почки неспецифичны и варьируются от человека к человеку. Потому болезнь нередко диагностируется на поздней стадии.
Гематурия (кровь в моче). Наиболее часто встречающийся симптом рака почек. При запущенном онкологическом процессе выраженная гематурия приводит к анемии и острой задержке мочи. Однако гематурия может быть вызвана другими заболеваниями, поэтому она не обязательно означает, что у пациента рак.
Уплотнение сбоку туловища или на пояснице. На поздних стадиях заболевания новообразование достигает большого размера, и пациент может прощупать бугристое уплотнение у себя в животе.
Боль в боку, животе или пояснице. Из-за растяжки почечной капсулы и сдавливания нервных окончаний опухолью возникает постоянная ноющая боль в нижней части грудной клетки с переходом на поясницу. Однако этот признак неспецифичен, так как может сопровождать многие другие заболевания.
Отечность. При раке почки происходит сдавливание нижней полой вены, что ведет к отечности ног и даже к тромбозу глубоких вен.
Изменение самочувствия. Онкологическая интоксикация, сопровождающая развитие рака любой локализации, приводит к апатии, утомляемости, потере аппетита и веса, необъяснимому повышению температуры в течение нескольких недель.
Стадии заболевания
Стадирование производится с учетом размеров опухоли, ее отношения к окружающим анатомическим структурам, наличия местных и отдаленных метастазов:
1-я стадия. Первичная опухоль до 7 сантиметров в наибольшем измерении, локализована в почке.
2-я стадия. Первичная опухоль более 7 сантиметров в наибольшем измерении, но не выходит за пределы почки.
3-я стадия. Новообразование распространяется на близлежащие органы: один лимфатический узел, надпочечники, слой прилегающей жировой ткани, почечную вену, нижнюю полую вену.
4-я стадия. Рак распространяется за слой жировой ткани вокруг почки и захватывает два и более лимфатических узла, а также другие органы – кишечник, поджелудочную железу, печень или легкие.
Диагностика
Диагностическое обследование пациентов с подозрением на рак почки может включать следующие процедуры:
Лабораторные методы. Анализы крови (общий и биохимический) и мочи. Ультразвуковое исследование. Современные аппараты УЗИ позволяют выявить рак почки на ранних стадиях.
Компьютерная томография (КТ). Рентгеновское послойное исследование органов брюшной полости и забрюшинного пространства. Выполняется как без контраста, так и с болюсным контрастированием, то есть — с внутривенным введением рентгеноконтрастного препарата при помощи специального автоматического шприца. Стандартное КТ-исследование позволяет выявить патологические изменения в почках. На снимке, сделанном после ввода контраста, более точно виден характер изменений органа, близлежащих лимфоузлов, артерий, вен, а также функциональное состояние почек.
Магнитно-резонансная томография (МРТ). Благодаря высокой разрешающей способности высокопольных (1,5Т) и сверхвысокопольных (3Т) магнитно-резонансных томографов, дополнительным уникальным программам с очень тонкими срезами, в ходе исследования можно увидеть изменения структуры почек размером до нескольких миллиметров, выявить патологические процессы на их начальной стадии, а также провести дифференциальную диагностику патологических образований. При наличии объемных опухолей врач может назначить МРТ с контрастным болюсным усилением. Оно позволяет оценить степень кровоснабжения опухоли и судить о доброкачественном или злокачественном характере.
Так как технология основана на применении магнитного резонанса, а не рентгеновских лучей, МР-томография показана в тех случаях, когда необходимо снизить лучевую нагрузку на пациента (частые рентгеновские исследования, детский возраст).
Биопсия почки. Биопсия и тонкоигольная аспирационная биопсия используются тогда, когда визуальные исследования не могут определить характер новообразования. В почку вводится тонкая длинная игла для забора крошечного образца ткани, который изучают под микроскопом.
Фьюжен биопсия. Современное направление в методике забора материала для гистологического анализа, сочетающее возможности магнитно-резонансной или компьютерной томографии и ультразвуковой диагностики. Перед проколом выполняется исследование на аппаратах КТ или МРТ. Основываясь на его результатах, врач планирует место прокола, рассчитывает ход биопсийной иглы и глубину проникновения. Сама биопсия проводится под контролем УЗИ. Метод обеспечивает максимальную точность попадания в пораженный участок.
Лечение
Хирургическая операция
Ведущий метод в лечении рака почки. Опухоли, которые не выходят за пределы почки или области вокруг нее, обычно удаляются хирургическим путем. Выполняются как открытые полостные операции, так и малоинвазивные, например, лапораскопические.
Существует несколько вариантов операции на почке:
— радикальная нефрэктомия. Это удаление целой почки вместе с окружающей жировой тканью. Иногда также удаляются надпочечник и ближайшие лимфоузлы;
— частичная нефрэктомия (операция с сохранением почки). Удаляется только раковая часть почки вместе с прилегающей здоровой тканью вокруг нее. Оптимальна для опухолей размером 4 сантиметра или менее. Частота рецидивов для раков первой стадии, удаленных радикальной или частичной нефрэктомией, составляет примерно 5%.
Удаление обеих почек – не приговор. Трансплантация органа, а также современная заместительная терапия, например, гемодиализ (способ очищения крови при помощи специального оборудования), позволяет пациентам жить гораздо дольше, чем с неизлеченным раком.
Альтернативы хирургическому вмешательству. В тех случаях, когда удаление опухоли невозможно из-за характера новообразования или состояния здоровья пациента, применяются другие технологии:
— абляция. Данные технологии используют тепло или холод для лечения опухолей и их удаления. Криоабляция замораживает раковые клетки до -140 градусов по Цельсию при помощи длинного тонкого щупа, вставленного в опухоль. После этого проводятся тщательное рентгеновское или другое сканирование, чтобы убедиться, что новообразование уничтожено. Радиочастотная абляция аналогична криоабляции, но вместо холода используется тепло. Способы идеальны для небольших опухолей почек у пациентов, для которых хирургия считается слишком рискованной;
— эмболизация. Под ультразвуковым или рентгеновским контролем в сосуд, питающий опухоль, вводится зонд и закупоривает его. Лишенная притока крови опухоль погибает.
Традиционная химиотерапия обычно неэффективна против опухолей почек. Вместо нее применяются более современные методы лекарственной терапии.
Направленная терапия. Опухоли почек пронизаны кровеносными сосудами, которые уязвимы для анти-ангиогенных лекарств. Это новое поколение препаратов разрушает кровеносные сосуды, идущие к опухоли, не повреждая нормальные, тем самым лишая раковые клетки питания.
Иммунотерапия. Почечно-клеточная карцинома иногда реагирует на иммунотерапию, которая показана при метастазировании рака. Однако побочные эффекты не очень хорошо переносятся многими пациентами.
Лучевая терапия. Радиация играет ограниченную роль в лечение рака почки. Опухоли, расположенные в этом органе, не очень чувствительны к облучению в отличие от здоровых почек. В некоторых случаях радиация может быть использована для того, чтобы уменьшить боль и другие симптомы, когда рак почек распространился на кости, мозг и другие части тела.
Помимо облучения на обычных линейных ускорителях, лечение на которых может занять 2-3 месяца, в Центре онкологии, радиохирургии и радиотерапии МИБС применяют так называемую конформную лучевую терапию. При этом современном подходе конфигурация облучающего пучка и интенсивность излучения скрупулезно рассчитываются с помощью специальных программ. Это позволяет добиться точного соответствия распределения дозы радиации форме новообразования, подать на мишень – в центр опухоли – максимально высокую дозу облучения, одновременно щадя периферийные нормальные ткани.
Лечение на аппарате Кибер-нож
Роботизированная радиохирургическая система Кибер-нож может использоваться в качестве альтернативы хирургическому вмешательству при первичном раке почки и особенно эффективно — в случае метастатического поражения. Метод дает возможность лечить пациентов, которым по состоянию здоровья не показана полостная операция, а также тех, кто сам отказывается от хирургического вмешательства.
Решение о выборе тактики лечения конкретного пациента в МИБС принимается коллегиально врачами клинических и диагностических специальностей. На каждом этапе составляется индивидуальный план дальнейшего наблюдения и контроля эффекта, включающий все самые информативные диагностические методы, применяющиеся сегодня в ведущих онкологических центрах Европы и США.
Почечно-клеточный рак: лечение в Минске
Рак почки лечение 1, 2, 3 стадии. Симптомы, признаки, метастазы, прогноз.
Почки – парные органы, располагающиеся по обе стороны от позвоночника в пространстве между органами брюшной полости и мышцами спины. Каждую почку окружает жировая ткань, сверху от почки располагается надпочечник.
Почки являются органами мочевой системы. Они продуцируют мочу, с которой выводится избыток воды и солей из организма, а также продукты жизнедеятельности человека. Моча собирается в почечной лоханке и выводится по мочеточнику в мочевой пузырь.
Какие бывают опухоли почки?
В почке встречаются два основных вида злокачественных опухолей – опухоли, развивающиеся из ткани самой почки – почечно-клеточный рак и опухоли, развивающиеся из почечной лоханки.
Из доброкачественных опухолей наиболее распространенными являются ангиомиолипомы (опухоли, состоящие из жировой, мышечной тканей и сосудов). Эти опухоли имеют характерные признаки, которые можно выявить при специальном рентгеновском обследовании (компьютерная томография). При больших размерах ангиомиолипомы нужно удалять, поскольку они могут легко повреждаться даже при небольших травмах и приводить к опасному внутреннему кровотечению.
Как часто встречается рак почки?
Рак почки составляет 4 % от всех выявленных злокачественных новообразований. Опухоли почки встречаются преимущественно у людей в возрасте 50-70 лет, хотя это заболевание может встречаться у подростков и даже детей. У мужчин опухоли почки встречаются немного чаще, чем у женщин, а у городского населения чаще по сравнению с сельским.
В Республике Беларусь в 2010 году выявлено 1833 новых случаев этого заболевания. Заболеваемость злокачественными новообразованиями почки в Республике Беларусь постоянно увеличивается и в 2010 году составила 19 на 100 000 жителей.
Какие факторы предрасполагают к развитию рака почки?
- Курение является одним из наиболее значительных факторов риска рака почки. У курящих вероятность заболеть раком почки увеличивается примерно в 2 раза по сравнению с некурящими;
- Ожирение, особенно у женщин;
- Злоупотребление болеутоляющими средствами также может способствовать развитию этого заболевания;
- Профессиональные факторы. Риск этого заболевания повышен у рабочих металлургической промышленности, кожевенного производства и при работе с асбестом и кадмием. Необходимо подчеркнуть, что влияние последних факторов не очень большое и признается не всеми специалистами;
- Генетические факторы, проявляющиеся в случаях семейного рака почки (например, синдром Фон Гиппель-Линдау). В этих случаях характерно развитие заболевания в молодом возрасте, частое развитие опухолей в обеих почках и возникновение множественных очагов рака в почке.
Симптомы рака почки
Поскольку почки находятся глубоко в теле человека, часто опухоли растут очень долго и достигают больших размеров, прежде чем появляются признаки, позволяющие их заподозрить.
До появления в медицине сложных методов обследования диагноз рака почки можно было заподозрить на основании трех симптомов:
- боль в пояснице;
- наличия крови в моче;
- пальпируемой опухоли.
Сейчас эти симптомы говорят о запущенной стадии рака почки и встречаются редко. Большинство опухолей в настоящее время выявляются случайно при ультразвуковом исследовании, выполняемом по поводу других заболеваний или симптомов:
- Одним из самых частых симптомов рака почки является появление крови в моче. Нередко вслед за этим в области почки возникают острые боли, обусловленные закупоркой мочеточника кровяными сгустками, которые проходят после отхождения сгустков с мочой;
- Боль в поясничной области является вторым по частоте симптомом рака почки. Боль может носить тупой характер, что связано с растяжением фиброзной капсулы почки или сдавлением опухолью нервных сплетений. Острые боли в пояснице, как правило, связаны с кровотечением и образованием сгустков, препятствующих оттоку мочи;
- Наличие опухоли в области почки, которую возможно прощупать, характерно для распространенного опухолевого процесса.
- Иногда при опухолях почки наблюдается расширение вен около яичка. Если такое расширение происходит внезапно или после 40 лет, необходимо обратиться к врачу, поскольку это может быть симптомом серьезной патологии.
Рак почки отличает высокая частота развития разнообразных проявлений, связанных с выработкой опухолью различных биологически активных веществ, что дало основание назвать рак почки “терапевтической опухолью”.
Опухоли почки могут вырабатывать разнообразные белковые субстанции, способные приводить к повышению температуры тела, увеличению уровня кальция в крови, снижению или повышению количества эритроцитов, повышению давления, ускорению СОЭ, нарушению свертываемости крови.
Все эти состояния проходят после полного удаления опухоли. Возврат этих симптомов, как правило, говорит о рецидиве заболевания или развитии отдаленных метастазов.
Диагностика рака почки
При подозрении на опухоль почки или при наличии неспецифических болей в пояснице в настоящее время широко используется ультразвуковое исследование (УЗИ) почек.
Преимуществами этого исследования является его низкая стоимость, доступность, безопасность, отсутствие вредного воздействия рентгеновских лучей. При УЗИ можно четко отличить обычную кисту почки от опухоли или подозрительного образования, требующего выполнения компьютерной томографии.
Недостатками УЗИ являются не вполне надежные результаты у тучных больных, иногда опухоль трудно выявить из-за экранирования ультразвука ребрами или газом в кишечнике. Кроме этого, результаты исследования зависят от опыта и квалификации врача, выполняющего УЗИ.
Методы лечения рака почки
Главным фактором, влияющим на выбор способа лечения при раке почки, является распространенность опухоли, в основном наличие или отсутствие отсевов опухоли в другие органы – метастазов.
Хирургическое лечение
Наиболее часто при этой патологии выполняется операция по удалению почки с опухолью и окружающими тканями, включающими окружающую почку жировые ткани, лимфоузлы и иногда надпочечника (радикальная нефрэктомия).
В ряде случае для полного удаления опухоли из организма требуется удаление прилежащих к опухоли других органов.
У отдельных пациентов при небольших размерах опухоли выполняется лапароскопическая радикальная нефрэктомия. Такая операция проводится без большого разреза через несколько небольших проколов. Удаленная почка с опухолью обычно извлекается через небольшой разрез внизу живота.
Преимуществом такого вмешательства является более быстрое восстановление организма после операции.
У части больных раком почки опухоль может прорастать в венозную систему почки и даже выходить в самую крупную вену человеческого организма – нижнюю полую вену. В этих случаях операция значительно усложняется и может сопровождаться большой кровопотерей.
В настоящее время значительно участилось выполнение так называемого органосохраняющего лечения опухолей почки. При небольших размерах опухоли и благоприятной их локализации возможно полное удаление опухоли с прилежащим участком ткани почки без удаления всей почки (резекция почки).
Окончательное решение о проведении той или иной операции принимает хирург после анализа данных компьютерной томографии. При маленьких опухолях у очень пожилых пациентов с противопоказаниями к хирургическому лечению допустимо применять наблюдение. При таком подходе операция проводится только при увеличении опухоли в размерах, что происходит только у небольшого количества таких больных.
Альтернативным способом лечения небольших опухолей почки является радиочастотная абляция – уничтожение опухоли при помощи специального зонда, генерирующего высокую температуру, вводимого в опухоль под контролем ультразвукового исследования, компьютерной томографии или лапароскопии.
Преимуществом такого лечения является малая травматичность и хорошая переносимость пожилыми или тяжело больными пациентами. У ряда больных раком почки при первичном обращении уже определяются отдаленные метастазы.
Несмотря на неутешительный прогноз при таком распространенном заболевании, некоторые мероприятия могут продлить жизнь больных или улучшить ее качество. Так, хотя удаление почки при метастатическом раке почки не может излечить больного, установлено, что эта операция позволяет более эффективно лечить это заболевания при помощи лекарственных препаратов, прежде всего иммунотерапии.
Лучевая терапия
Рак почки слабо чувствителен к облучению. В настоящее время лучевая терапия при раке почки используется исключительно с обезболивающей целью у больных с метастазами в костях либо при поражении головного мозга.
Химиотерапия
До настоящего времени результаты применения традиционных противоопухолевых химиопрепаратов у больных раком почки остаются малоутешительными. При раке почки применялись практически все существующие химиопрепараты. К сожалению, ни один из химиопрепаратов не показал эффективности при раке почки.
Иммунотерапия
В настоящее время иммунотерапия при метастатическом раке почки является одним из эффективных методов лечения. В основном при раке почки применяют два иммунологических препарата – интерлейкин-2 и интерферон-альфа. При сходной эффективности обеих препаратов меньше побочных эффектов развивается при лечении интерфероном, поэтому в клинической практике преимущественно используется интерферон.
Таргетная терапия
В последние годы разработан ряд новых препаратов «нацеленного» действия на различные молекулярные механизмы развития опухоли. Применение ряда средств при распространенном раке почки оказалось более эффективным, чем традиционная иммунотерапия.
Тем не менее, в настоящее время эти препараты характеризуются крайне высокой стоимостью, что препятствует их широкому внедрению в клиническую практику. Изучение возможностей использования препаратов таргетной терапии в настоящее время продолжается.
Гипертермия и гипергликемия
Неудовлетворенность результатами лечения больных распространенными формами злокачественных новообразований явилась толчком к поиску принципиально новых способов, усиливающих возможности химиолучевой терапии. В настоящее имеются данные об эффективности общей гипертермии при лечении распространенного рака почки. Повышенная температура кроме прямого деструктивного действия на опухоль, может усиливать действие противоопухолевых препаратов.
Какое наблюдение требуется после проведенного лечения?
После завершения лечения необходимо периодически проходить обследование для своевременного выявления рецидива или прогрессирования заболевания. Для граждан Республики Беларусь с онкологическими заболеваниями наблюдение осуществляется в онкологических диспансерах по месту жительства.
Как часто следует проходить обследование, а также объем необходимых исследований определит Ваш врач в зависимости от стадии заболевания и проведенного лечения.
В стандартный объем обследования входит:
- УЗИ органов брюшной полости;
- рентгенография органов грудной клетки;
- общий и биохимический анализ крови;
- общий анализ мочи.
Рак почки| Блог UNIM
Рак почки, или почечно-клеточный рак – злокачественная опухоль, которая развивается из клеток, выстилающих почечные канальцы, составляет до 90% всех злокачественных новообразований почек у взрослых. В зависимости от гистологического строения выделяют следующие типы почечно-клеточного рака:
— Светлоклеточный рак почки – составляет до 80% случаев рака почки. Свое название получил из-за того, что клетки опухоли под микроскопом выглядят круглыми, имеют оптически пустую («светлую») цитоплазму.
— Папиллярный рак почки встречается в 10-15% случаев. Гистологически выделяют тип 1 и тип 2 (обычно более агрессивный). Также папиллярный рак почки может быть наследственным. При наследственном папиллярном почечноклеточном раке опухоли возникают в обеих почках (билатерально) и нескольких областях одной почки (мультифокально). Эти опухоли очень агрессивны и быстро метастазируют. У пациентов с наследственной формой почечноклеточного рака также развиваются опухоли кожи, а у женщин – матки.
— Хромофобный почечноклеточный рак составляет примерно 5% случаев рака почки. Этот вид рака отличается медленным ростом и низкой вероятностью появления метастазов.
— Рак из собирательных канальцев (протоков Беллини) – редкий агрессивный вид рака, который развивается из выстилки собирательных канальцев.
— Неклассифицируемые — до 5% случаев рака почки невозможно отнести ни к одной из вышеперечисленных групп.
— Редкие опухоли почек:
— Саркомы – развиваются из стромы почки (лейомиосаркома, липосаркома, злокачественная фиброзная гистиоцитома)
— Нефробластома (опухоль Вильмса) – самая частая злокачественная опухоль почек у детей, исключительно редко встречается у взрослых старше 20 лет.
— Медуллярный рак – развивается в мозговом веществе почки. Обычно развивается у молодых людей, чаще выходцев из Африки, в большинстве случаев ассоциирован с серповидноклеточной анемией.
— Мелкоклеточный рак
— Карциноид
— Переходно-клеточные опухоли почечной лоханки и мочеточника (по клиническим и гистологическим особенностям больше напоминает рак мочевого пузыря, чем почечноклеточный рак).
Симптомы почечно-клеточного рака обычно появляются только после врастания опухоли в окружающие ткани и органы – больные обнаруживают примесь крови в моче, боль в спине и боку, иногда замечают наличие опухоли живота.
Диагностика почечно-клеточного рака включает компьютерную томографию, ультразвуковое исследование, рентгенографию органов грудной клетки, по показаниям перед операцией выполняется биопсия.
Лечение рака почки – хирургическое: стандартом является удаление почки с опухолью (нефрэктомия). В некоторых случаях (наличие опухоли в обеих почках, отсутствие второй почки, почечная недостаточность, наследственные формы рака).
Почечно-клеточный рак
Почечно-клеточный рак является типичным шарообразным образованием, часто является случайной находкой у пациентов, обратившихся с жалобами не относящимися к патологии мочевыделительной системы. Пик заболеваемости составляет 60-70 лет. Почечно-клеточный рак связана с наследственными синдромами такими, как синдром Гиппель-Ландау, туберозным склерозом и Бирт-Хогг-Дубе.
Самый распространённый гистологический подтип почечно-клеточного рака является светлоклеточный рак почки, он составляет 70% случаев всех раков почек. Затем следуют папиллярный и хромофобный почечно-клеточный рак. Медуллярный и мультикистозный почечно-клеточные раки встречаются крайне редко. Пациенты с светлоклеточным раком имеет 5-летнюю выживаемость, что гораздо ниже, чем у пациентов с папиллярной и хромофобной карциномой.
Стадирование смотрите — Почечно-клеточный рак (TNM классификация)
Почечно-клеточный рак — это опухоль больших размеров, локализующаяся в корковом веществе. Светлоклеточный рак отностится к гиперваскулярному типу опухолей с неоднородной структурой за счет некрозов, кровоизлияний, кальцинирования или кист. В редких случаях почечно-клеточный рак содержит внеклеточный жир, соответственно, образование с включением жира и кальцинатов следует рассматривать, как почечно-клеточный рак.
Характерной особенностью почечно-клеточного рака явлечётся значительное усиление в кортикомедуллярную фазу.
Трудности возникают, когда образование небольших размеров локализуется в корковом веществе (которое также активно контрастируется), поэтому нефрографическая фаза при образованиях такой локализации и размеров является важной, поскольку паренхима контрастируется однороднее и сильнее чем опухоль.
При МРТ почечно-клеточный рак визуализируется, как гипоинтенсивное образование на Т1 ВИ и гиперинтенсивное на Т2 ВИ. Как правило, почечно-клеточный рак не имеет экстрацеллюлярного жира, что, соответственно, отличает его от ангиомиолипомы. Однако в 80% случаев при почечно-клеточном раке имеется внутриклеточный жир, что приводит к снижению сигнала на Т1 opposed-phase в сравнении с in-phase изображениями.
Порядка 5% всех почечно-клеточных раков характеризутся инфильтративным типом роста, однако они имеют более агрессивный характер роста, изменяют внутреннюю архитектуру почек (но не наружные контуры), а изменения лоханки схожи с изменениями при переходноклеточном раке почки.
Данная публикация является предварительным набоском, и внечение дополнений и уточнений только приветствуется.
Светлоклеточная почечно-клеточная карцинома
Что такое светлоклеточная почечно-клеточная карцинома?
Светлоклеточная почечно-клеточная карцинома, или ccRCC, является разновидностью рака почки. Почки расположены по обе стороны от позвоночника по направлению к пояснице. Почки работают, очищая кровь от отходов жизнедеятельности. Светлоклеточная почечно-клеточная карцинома также называется обычной почечно-клеточной карциномой.
Светлоклеточная почечно-клеточная карцинома названа в честь того, как опухоль выглядит под микроскопом.Клетки в опухоли выглядят прозрачными, как пузыри.
Насколько распространен ccRCC?
У взрослых ccRCC является наиболее распространенным типом рака почки и составляет около 80% всех случаев почечно-клеточной карциномы. CCRCC чаще встречается у взрослых, чем у детей. Почечно-клеточная карцинома составляет 2-6% случаев рака почки у детей и молодых людей.
Как диагностируется цПКР?
Пациенты с CCRCC могут испытывать боль или чувствовать усталость. Иногда у пациентов нет заметных симптомов.Симптомы могут включать:
- Кровь в моче
- Боль
- Похудание
- Чувство усталости
- Лихорадка
- Шишка в боку
У людей без симптомов эти опухоли могут быть обнаружены, если у человека есть визуализирующий тест по другой причине.
Визуализация: Если есть подозрение на наличие светлоклеточного почечно-клеточного рака, ваш врач будет использовать визуализацию, такую как рентген, КТ или МРТ, чтобы оценить размер опухоли.Они также проверит наличие признаков того, что опухоль распространилась на другие части тела.
Биопсия: Чтобы проверить, является ли опухоль ccRCC, ваш врач выполнит биопсию, взяв небольшой образец из опухоли с помощью иглы. Эксперт, называемый патологом, изучит клетки образца под микроскопом, чтобы увидеть, что это за опухоль.
Как лечится ccRCC?
Лечение людей с CCRCC включает хирургическое вмешательство и иммунотерапию. Лечение будет зависеть от того, насколько вырос рак.
Хирургия: После того, как будет диагностирован цПКР, вам может быть проведена операция по удалению опухоли и части почки, окружающей ее. На ранней стадии рака почки удаляется часть пораженной раком почки. Если ccRCC находится в середине почки или если опухоль большая, иногда необходимо удалить всю почку. На более поздних стадиях ПКР удаление почки является спорным вопросом, но может быть целесообразным у некоторых пациентов.
Иммунотерапия: Иммунотерапия помогает иммунной системе организма бороться с раковыми клетками.
Таргетная терапия: Таргетная терапия направлена на изменения в раковых клетках, которые помогают им расти, делиться и распространяться. Некоторые методы таргетной терапии, которые используются для лечения светлоклеточного рака почек, включают кабозантиниб, акситиниб, сунитиниб, сорафениб и пазопаниб.
Могут использоваться другие методы лечения, не связанные с удалением почки, например:
- Лучевая терапия , при которой радиация убивает опухолевые клетки
- Термическая абляция , при которой для уничтожения опухолевых клеток используется тепло
- Кризохирургия , в которой используется жидкий азот для замораживания и уничтожения опухолевых клеток
Работает ли ccRCC в семьях?
ccRCC может работать в семьях.Почти все случаи ccRCC, протекающие в семьях, обнаруживаются у людей с генетическим заболеванием, называемым синдромом Фон Гиппеля-Линдау, но другие наследственные состояния также могут быть связаны с ccRCC. Люди с синдромом фон Гиппеля-Линдау имеют мутации в гене VHL.
Как образуется ccRCC?
Ученые постоянно работают над тем, чтобы понять, как формируется рак, но это может быть трудно доказать. Поскольку ccRCC может передаваться в семьях, мы знаем, что изменения в гене VHL важны для возникновения ccRCC.Ген VHL также изменен в ccRCC у людей без семейного анамнеза синдрома фон Гиппеля-Линдау. Ученые многое узнали о том, что ген VHL делает в организме. Это дало ученым подсказки о методах лечения ccRCC.
Каков прогноз для людей с CCRCC?
Оценка того, как болезнь повлияет на вас в долгосрочной перспективе, называется прогнозом. Все люди разные, и прогноз будет зависеть от многих факторов, таких как
.- Где опухоль в вашем теле
- Если рак распространился на другие части вашего тела
- Какая часть опухоли удалена во время операции
Если вам нужна информация о своем прогнозе, важно поговорить со своим врачом.NCI также имеет ресурсы, которые помогут вам понять прогноз рака.
Врачи оценивают выживаемость ccRCC по тому, как группы людей с ccRCC делали это в прошлом. Поскольку у детей очень мало пациентов с раком почки, эти показатели могут быть неточными. Они также не принимают во внимание разрабатываемые новые методы лечения.
Имея это в виду, пациенты с CCRCC с меньшими опухолями имеют больше шансов на выживание, чем пациенты с большими опухолями. 5-летняя выживаемость пациентов с CCRCC составляет 50-69%.Когда ccRCC уже велик или распространился на другие части тела, лечение затруднено, и 5-летняя выживаемость составляет около 10%.
Что такое рак почки?
Рак почки — это тип рака, который начинается в почке. Рак начинается, когда клетки тела начинают бесконтрольно расти. Чтобы узнать больше о том, как рак начинается и распространяется, см. Что такое рак?
Чтобы понять рак почки, полезно знать о нормальной структуре и функции почек.
Почки
Почки — это пара бобовидных органов, каждый размером с кулак. Они прикреплены к верхней задней стенке живота и защищены нижней грудной клеткой. Одна почка находится слева, а другая — справа от позвоночника. Верхнюю и нижнюю части каждой почки иногда называют верхним полюсом и нижним полюсом .
Небольшой орган, называемый надпочечником, расположен на вершине каждой почки.Каждая почка и надпочечник окружены жиром и тонким фиброзным слоем, известным как фасция Герота .
Основная задача почек — удалять лишнюю воду, соль и продукты жизнедеятельности из крови, поступающей из почечных артерий. Эти вещества становятся мочой. Моча собирается в центре каждой почки в области, называемой почечной лоханкой , , а затем покидает почки через длинные тонкие трубки, называемые мочеточниками , . Мочеточники ведут в мочевой пузырь, где моча хранится до момента мочеиспускания.
Почки выполняют и другие функции:
- Они помогают контролировать кровяное давление, вырабатывая гормон под названием ренин .
- Они помогают убедиться, что в организме достаточно красных кровяных телец, вырабатывая гормон под названием эритропоэтин . Этот гормон заставляет костный мозг производить больше красных кровяных телец.
Наши почки важны, но мы можем работать только с одной почкой. Многие люди в Соединенных Штатах живут нормальной, здоровой жизнью, имея всего одну почку.
У некоторых людей почки вообще не работают, и они выживают с помощью медицинской процедуры, называемой диализом . В наиболее распространенной форме диализа используется специально разработанный аппарат, который фильтрует кровь так же, как настоящая почка.
Типы рака почки
Почечно-клеточный рак
Почечно-клеточная карцинома (ПКР), также известная как почечно-клеточный рак или почечно-клеточная аденокарцинома, является наиболее распространенным типом рака почки. Около 9 из 10 случаев рака почек являются почечно-клеточными карциномами.
Хотя ПКР обычно растет как единичная опухоль в почке, иногда имеется 2 или более опухолей в одной почке или даже опухоли в обеих почках одновременно.
Существует несколько подтипов ПКР, основанных в основном на том, как раковые клетки выглядят в лаборатории. Знание подтипа ПКР может быть фактором при выборе лечения, а также может помочь вашему врачу определить, может ли ваш рак быть вызван наследственным генетическим синдромом. См. «Факторы риска рака почки » для получения дополнительной информации о синдромах наследственного рака почки.
Светлоклеточный почечно-клеточный рак
Это наиболее распространенная форма почечно-клеточного рака. Около 7 из 10 человек с ПКР есть этот вид рака. При осмотре в лаборатории клетки, из которых состоит ПКР, выглядят очень бледными или прозрачными.
Почечно-клеточный рак непрозрачных клеток
Папиллярный почечно-клеточный рак : Это второй по распространенности подтип — примерно 1 из 10 ПКР относится к этому типу. Эти виды рака образуют выступы в виде мизинца (называемые сосочков ) в некоторых, если не в большинстве, опухолях.Некоторые врачи называют эти раковые образования хромофильными , потому что клетки поглощают определенные красители и выглядят розовыми при взгляде под микроскопом.
Хромофобный почечно-клеточный рак : На этот подтип приходится около 5% (5 случаев из 100) ПКР. Клетки этих видов рака также бледные, как и прозрачные клетки, но намного больше и имеют некоторые другие особенности, которые можно распознать при очень внимательном рассмотрении.
Редкие типы почечно-клеточного рака: Эти подтипы очень редки, каждый составляет менее 1% ПКР:
- Коллекторный канал ПКР
- Многоточечный кистозный ПКР
- Медуллярный рак
- Муцинозная трубчатая и веретено-клеточная карцинома
- ПКР, ассоциированный с нейробластомой
Неклассифицированная почечно-клеточная карцинома : В редких случаях почечно-клеточный рак помечается как неклассифицированный , потому что их внешний вид не соответствует ни одной из других категорий или потому что существует более одного типа раковых клеток.
Другие виды рака почек
Другие типы рака почек включают карциномы переходных клеток, опухоли Вильмса и саркомы почек.
Переходно-клеточная карцинома : Из каждых 100 случаев рака почек от 5 до 10 являются переходно-клеточными карциномами (TCC), также известными как уротелиальные карциномы .
Переходно-клеточная карцинома возникает не в почках, а в выстилке почечной лоханки (там, где мочеточники встречаются с почками).Эта выстилка состоит из клеток, называемых переходными клетками , , которые выглядят как клетки, выстилающие мочеточники и мочевой пузырь. Раковые образования, которые развиваются из этих клеток, выглядят как другие уротелиальные карциномы, такие как рак мочевого пузыря, если внимательно изучить их в лаборатории. Как и рак мочевого пузыря, эти виды рака часто связаны с курением сигарет и воздействием определенных канцерогенных химических веществ на рабочем месте.
Люди с ОКР часто имеют те же признаки и симптомы, что и люди с почечно-клеточным раком — кровь в моче и, иногда, боли в спине.
Для получения дополнительной информации о переходно-клеточной карциноме см. Рак мочевого пузыря.
Опухоль Вильмса (нефробластома) : Опухоли Вильмса почти всегда возникают у детей. Этот вид рака очень редко встречается у взрослых. Чтобы узнать больше об этом типе рака, см. Опухоль Вильмса.
Почечная саркома : Почечная саркома — это редкий тип рака почки, который начинается в кровеносных сосудах или соединительной ткани почек. Они составляют менее 1% всех случаев рака почек.
Саркомы более подробно рассматриваются в статье «Саркома — рак мягких тканей у взрослых».
Доброкачественные (незлокачественные) опухоли почек
Некоторые опухоли почек доброкачественные (не раковые). Это означает, что они не метастазируют (не распространяются) в другие части тела, хотя могут расти и вызывать проблемы.
Доброкачественные опухоли почек можно лечить, удаляя или разрушая их, используя те же методы лечения, которые используются при раке почки, например хирургическое вмешательство или радиочастотную абляцию.Выбор лечения зависит от многих факторов, таких как размер опухоли и наличие каких-либо симптомов, количество опухолей, наличие опухоли в обеих почках и общее состояние здоровья человека.
Ангиомиолипома : Ангиомиолипома — наиболее распространенная доброкачественная опухоль почек. Чаще они встречаются у женщин. Они могут развиваться спорадически или у людей с туберозным склерозом — генетическим заболеванием, которое также влияет на сердце, глаза, мозг, легкие и кожу.
Эти опухоли состоят из различных типов соединительных тканей (кровеносных сосудов, гладких мышц и жира). Если они не вызывают никаких симптомов, за ними часто можно просто внимательно наблюдать. Если они начинают вызывать проблемы (например, боль или кровотечение), возможно, их нужно лечить.
Онкоцитома : Онкоцитомы — это доброкачественные опухоли почек, которые встречаются нечасто и иногда могут достигать больших размеров. Они чаще встречаются у мужчин и обычно не распространяются на другие органы, поэтому их часто излечивает хирургическое вмешательство.
Остальная часть нашей информации о раке почки посвящена почечно-клеточной карциноме, а не менее распространенным типам опухолей почек.
Рак почки: Введение | Cancer.Net
НА ЭТОЙ СТРАНИЦЕ: Вы найдете основную информацию об этом заболевании и частях тела, на которые оно может повлиять. Это первая страница руководства Cancer.Net по раку почки. Используйте меню для просмотра других страниц. Думайте об этом меню как о дорожной карте для этого полного руководства.
О почках
У каждого человека 2 почки, которые расположены выше талии по обе стороны от позвоночника. Эти красновато-коричневые органы в форме бобов размером с небольшой кулак. Они расположены ближе к задней части тела, чем к передней.
Почки фильтруют кровь, удаляя примеси, лишние минералы и соли, а также лишнюю воду. Каждый день почки фильтруют около 200 литров крови, чтобы произвести 2 литра мочи. Почки также вырабатывают гормоны, которые помогают контролировать кровяное давление, выработку эритроцитов и другие функции организма.
У большинства людей 2 почки. Каждая почка работает независимо. Это означает, что организм может функционировать менее чем с одной почкой. С диализом, механизированным процессом фильтрации, можно жить без функционирующих почек. Диализ может проводиться через кровь, это называется гемодиализом, или через брюшную полость пациента, что называется перитонеальным диализом.
О раке почки
Рак почки начинается, когда здоровые клетки в одной или обеих почках изменяются и выходят из-под контроля, образуя массу, называемую опухолью коркового слоя почек.Опухоль может быть злокачественной, вялотекущей или доброкачественной. Злокачественная опухоль является раковой, то есть может расти и распространяться на другие части тела. Вялотекущая опухоль также является злокачественной, но этот тип опухоли редко распространяется на другие части тела. Доброкачественная опухоль означает, что опухоль может расти, но не распространяется.
Типы рака почки
Есть несколько видов рака почки:
Почечно-клеточный рак. Почечно-клеточная карцинома — наиболее распространенный тип рака почки у взрослых, на который приходится около 85% диагнозов.Этот тип рака развивается в проксимальных почечных канальцах, которые составляют систему фильтрации почек. В каждой почке есть тысячи этих крошечных фильтрующих элементов. Варианты лечения почечно-клеточного рака обсуждаются далее в этом руководстве.
Карцинома уротелия. Это также называется переходноклеточной карциномой. На его долю приходится от 5% до 10% случаев рака почек, диагностированных у взрослых. Карцинома уротелия начинается в области почек, где моча собирается перед перемещением в мочевой пузырь, называемую почечной лоханкой.Этот тип рака почки рассматривается как рак мочевого пузыря, потому что оба типа рака начинаются в одних и тех же клетках, выстилающих почечную лоханку и мочевой пузырь.
Саркома. Саркома почки встречается редко. Этот тип рака развивается в мягких тканях почек; тонкий слой соединительной ткани, окружающей почку, называемый капсулой; или окружающий жир. Саркома почки обычно лечится хирургическим путем. Однако саркома обычно возвращается в область почек или распространяется на другие части тела.После первой операции могут быть рекомендованы дополнительные операции или химиотерапия.
Опухоль Вильмса. Опухоль Вильмса чаще всего встречается у детей и лечится не так, как рак почки у взрослых. Опухоли Вильмса составляют около 1% случаев рака почек. Этот тип опухоли с большей вероятностью поддается лечению с помощью лучевой терапии и химиотерапии, чем другие типы рака почки в сочетании с хирургическим вмешательством. Это привело к другому подходу к лечению.
Лимфома. Лимфома может увеличивать обе почки и связана с увеличенными лимфатическими узлами, называемыми лимфаденопатией, в других частях тела, включая шею, грудь и брюшную полость. В редких случаях лимфома почки может проявляться как единичное опухолевое образование в почке и может включать увеличенные регионарные лимфатические узлы. Если возможна лимфома, ваш врач может выполнить биопсию (см. Диагностика) и порекомендовать химиотерапию вместо операции.
Типы клеток рака почки
Знание того, какой тип клеток составляет опухоль почки, помогает врачам спланировать лечение.Патологи выявили более 30 различных типов клеток рака почки. Патолог — это врач, который специализируется на интерпретации лабораторных тестов и оценке клеток, тканей и органов для диагностики заболеваний. Компьютерная томография (КТ) или магнитно-резонансная томография (МРТ) (см. Диагностика) не всегда могут показать разницу между доброкачественными, вялотекущими или злокачественными опухолями коркового слоя почек до операции.
Ниже перечислены наиболее распространенные типы клеток рака почки. В общем, степень опухоли относится к степени дифференцировки клеток, а не к тому, насколько быстро они растут.Дифференциация описывает, насколько раковые клетки похожи на здоровые. Чем выше оценка, тем больше вероятность распространения или метастазирования клеток с течением времени.
Очистить ячейку. Около 70% случаев рака почки состоят из светлых клеток. Светлые клетки варьируются от медленно растущих (степень 1) до быстрорастущих (степень 4). Иммунотерапия и таргетная терапия (см. Типы лечения) особенно эффективны при лечении светлоклеточного рака почки.
Папиллярный. Папиллярный рак почки обнаруживается у 10-15% пациентов. Он разделен на 2 различных подтипа, называемых типом 1 и типом 2. Локальный папиллярный рак почки часто лечится хирургическим путем. Если папиллярный рак почки распространяется или метастазирует, его часто лечат препаратами, блокирующими кровеносные сосуды. Использование иммунотерапии для лечения метастатического папиллярного рака все еще исследуется. Многие врачи рекомендуют лечение метастатического папиллярного рака путем клинических испытаний.
Саркоматоидные признаки. Каждый из подтипов опухоли рака почки (светлоклеточный, хромофобный и папиллярный, среди прочих) может демонстрировать сильно дезорганизованные черты под микроскопом. Патологоанатомы часто называют их «саркоматоидными». Это не отдельный подтип опухоли, но когда эти особенности видны, врачи понимают, что это очень агрессивная форма рака почки. Есть многообещающие научные исследования вариантов иммунотерапевтического лечения людей с опухолью с саркоматоидными признаками. Совсем недавно это были комбинации ипилимумаба (Ервой) и ниволумаба (Опдиво), а также комбинации атезолизумаба (Тецентрик) и бевацизумаба (Авастин).
Медуллярный. Это редкий и очень агрессивный рак, но все еще считается опухолью коркового слоя почек. Это чаще встречается у чернокожих людей и тесно связано с серповидно-клеточной анемией или серповидно-клеточной анемией. Признак серповидной клетки означает, что человек унаследовал ген серповидной клетки от родителя. Комбинации химиотерапии с ингибиторами кровеносных сосудов в настоящее время являются рекомендуемыми вариантами лечения, основанными на некоторых научных данных, и продолжаются клинические испытания, чтобы лучше определить варианты лечения.
Собирательный проток: Карцинома собирательного протока чаще встречается у людей в возрасте от 20 до 30 лет. Он начинается в собирательных протоках почек. Следовательно, карцинома собирательного протока тесно связана с переходно-клеточной карциномой (см. Выше «Уротелиальная карцинома»). Это рак, который трудно успешно лечить в долгосрочной перспективе, даже при сочетании системной химиотерапии и хирургического вмешательства.
Хромофоб. Хромофоб — еще один необычный рак, который может образовывать вялотекущие опухоли, которые маловероятны для распространения, но становятся агрессивными, если они распространяются.Клинические испытания продолжаются, чтобы найти лучшие способы лечения этого типа рака.
Онкоцитома. Это медленнорастущий тип рака почек, который редко, если вообще когда-либо, распространяется. Методом выбора является хирургическое вмешательство при больших объемных опухолях.
Ангиомиолипома. Ангиомиолипома — доброкачественная опухоль, которая имеет уникальный вид на компьютерной томографии и при просмотре под микроскопом. Обычно у него меньше шансов на рост и распространение. Обычно его лечат хирургическим путем или, если оно небольшое, под активным наблюдением (см. Типы лечения).Значительное кровотечение — редкое явление, но более вероятно у беременных и женщин в пременопаузе. Агрессивная форма ангиомиолипомы, называемая эпителиоидной, в редких случаях может поражать почечную вену и нижнюю полую вену и распространяться на близлежащие лимфатические узлы или органы, такие как печень.
Нужны дополнительные сведения?
Если вы хотите получить более подробную информацию, изучите эти связанные элементы. Обратите внимание, что по этим ссылкам вы попадете в другие разделы Рака.Нетто:
Следующий раздел в этом руководстве — Статистика . Это помогает объяснить количество людей, у которых диагностирован рак почки, и общие показатели выживаемости. Используйте меню, чтобы выбрать другой раздел для чтения в этом руководстве.
Виды и сорта | Рак почки
Тип рака почки, который у вас есть, говорит вам, в какой тип клетки он начался. Эта информация поможет вашему врачу решить, какое лечение вам нужно.
Почечно-клеточный рак
Почечно-клеточный рак — наиболее распространенный тип рака почки у взрослых.Ее еще называют почечно-клеточной аденокарциномой. Более 80 из 100 (более 80%) случаев рака почки являются почечно-клеточными раками.
При почечно-клеточном раке раковые клетки начинаются со слизистой оболочки канальцев (самых маленьких трубок внутри нефронов). Канальцы помогают фильтровать кровь и вырабатывать мочу.
Основные типы
Основные виды почечно-клеточного рака:
- светлоклеточные — около 80 из 100 случаев рака почки (75%)
- папиллярный — около 15 из 100 почечно-клеточного рака (15%)
- хромофобный почечно-клеточный рак — около 5 из 100 почечно-клеточного рака (5%)
Редкие типы
Редкие типы почечно-клеточного рака включают карциному собирательных протоков и медуллярную карциному почек.Иногда рак почки может содержать более одного типа клеток.
Другой редкий тип — саркоматоид. Это означает, что под микроскопом клетки рака почки выглядят как клетки саркомы. Саркома — это рак соединительной ткани (например, мышц, нервов, жира, кровеносных сосудов и фиброзных тканей). Рак почки саркоматоидного типа может иметь иные перспективы, чем другие типы рака почки.
Переходно-клеточный рак почки или мочеточника
Переходно-клеточный рак означает, что раковые клетки возникли в переходных клетках, выстилающих почечную лоханку или мочеточник.Почечная лоханка — это центральная область почек, где моча собирается перед тем, как попасть по мочеточнику в мочевой пузырь.
Лечение этого типа рака почки аналогично лечению рака мочевого пузыря.
Опухоль Вильмса
Тип рака почки, называемый опухолью Вильмса, может поражать детей. Это отличается от рака почки у взрослых.
Степень рака почки
Степень означает, насколько раковые клетки похожи на нормальные клетки.Специалист (патолог) рассматривает клетки под микроскопом. Патолог будет смотреть на центр клетки (ядро), а также на размер и форму клеток.
Чем больше раковые клетки выглядят как нормальные клетки, тем ниже оценка. Они имеют тенденцию расти медленнее и с меньшей вероятностью распространятся на другую часть тела (метастазы).
Чем меньше раковые клетки выглядят как нормальные клетки, тем выше оценка. Они имеют тенденцию к более быстрому росту и с большей вероятностью распространятся на другие части тела.
Рак почки относится к 1-4 степени. Это называется системой Фурмана. Оценка 1 — это самая низкая оценка, а оценка 4 — самая высокая оценка.
Оценка сообщает вашему врачу, как может вести себя рак и какое лечение вам нужно. Главный фактор при выборе лучшего лечения — распространился ли ваш рак за пределы почек или нет.
Онтогенез светлоклеточной почечно-клеточной карциномы и механизмы летальности
Bray, F. et al. Глобальная статистика рака 2018: оценки GLOBOCAN заболеваемости и смертности от 36 раковых заболеваний во всем мире в 185 странах. CA Cancer J. Clin. 68 , 394–424 (2018).
Артикул PubMed Google Scholar
Йонаш, Э., Гао, Дж. И Ратмелл, У. К. Почечно-клеточная карцинома. BMJ 349 , g4797 (2014).
PubMed PubMed Central Статья Google Scholar
Hagemeijer, A., Hoehn, W. & Smit, E.M. Цитогенетический анализ клеточных линий карциномы почек человека общего происхождения (NC 65). Cancer Res. 39 , 4662–4667 (1979).
CAS PubMed Google Scholar
Szucs, S., Muller-Brechlin, R., DeRiese, W. & Kovacs, G. Делеция 3p: единственная потеря хромосом при первичной почечно-клеточной карциноме. Cancer Genet. Cytogenet. 26 , 369–373 (1987).
CAS PubMed Статья Google Scholar
Yoshida, M.A. et al. Перестройка хромосомы 3 при почечно-клеточном раке. Cancer Genet. Cytogenet. 19 , 351–354 (1986).
CAS PubMed Статья Google Scholar
Latif, F. et al. Идентификация гена-супрессора опухоли болезни фон Гиппеля-Линдау. Наука 260 , 1317–1320 (1993).
CAS PubMed Статья Google Scholar
Varela, I. et al. Секвенирование экзома выявляет частую мутацию гена PBRM1 комплекса SWI / SNF при карциноме почек. Природа 469 , 539–542 (2011).
CAS PubMed PubMed Central Статья Google Scholar
Pena-Llopis, S. et al. Потеря BAP1 определяет новый класс почечно-клеточной карциномы. Нат. Genet. 44 , 751–759 (2012).
CAS PubMed PubMed Central Статья Google Scholar
Dalgliesh, G. L. et al. Систематическое секвенирование карциномы почек выявляет инактивацию генов, модифицирующих гистоны. Природа 463 , 360–363 (2010).
CAS PubMed PubMed Central Статья Google Scholar
Исследовательская сеть Атласа генома рака. Комплексная молекулярная характеристика светлоклеточного почечно-клеточного рака. Природа 499 , 43–49 (2013).
Klatte, T. et al. Цитогенетический профиль позволяет прогнозировать прогноз пациентов со светлоклеточным почечно-клеточным раком. J. Clin. Онкол. 27 , 746–753 (2009).
PubMed Статья Google Scholar
La Rochelle, J. et al. Делеции хромосомы 9p указывают на агрессивный фенотип светлоклеточной почечно-клеточной карциномы. Рак 116 , 4696–4702 (2010).
PubMed Статья Google Scholar
Monzon, F.A. et al. Потеря хромосомы 14q определяет молекулярный подтип светлоклеточной почечно-клеточной карциномы, связанный с плохим прогнозом. Мод. Патол. 24 , 1470–1479 (2011).
CAS PubMed PubMed Central Статья Google Scholar
Shen, C. et al. Генетические и функциональные исследования указывают на то, что HIF1alpha является геном-супрессором рака почки 14q. Рак Discov. 1 , 222–235 (2011).
CAS PubMed PubMed Central Статья Google Scholar
Jiang, F. et al. Построение моделей эволюционного дерева почечно-клеточного рака на основе сравнительных данных геномной гибридизации. Cancer Res. 60 , 6503–6509 (2000).
CAS PubMed Google Scholar
Браннон А. Р. и др. Молекулярная стратификация светлоклеточного почечно-клеточного рака с помощью консенсусной кластеризации выявляет различные подтипы и паттерны выживаемости. Гены рака 1 , 152–163 (2010).
CAS PubMed PubMed Central Статья Google Scholar
Rini, B. et al. Анализ 16 генов для прогнозирования рецидива после операции при локализованной почечно-клеточной карциноме: исследования по разработке и проверке. Ланцет Онкол. 16 , 676–685 (2015).
CAS PubMed Статья Google Scholar
Gerlinger, M. et al. Внутриопухолевая гетерогенность и разветвленная эволюция выявлены с помощью мультирегионального секвенирования. N. Engl. J. Med. 366 , 883–892 (2012).
CAS PubMed PubMed Central Статья Google Scholar
Turajlic, S. et al. Детерминированные эволюционные траектории влияют на рост первичной опухоли: TRACERx Renal. Ячейка 173 , 595–610.e11 (2018).
CAS PubMed PubMed Central Статья Google Scholar
Mitchell, T. J. et al. Определение времени знаковых событий в эволюции светлоклеточного почечно-клеточного рака: TRACERx Renal. Ячейка 173 , 611–623.e17 (2018).
CAS PubMed PubMed Central Статья Google Scholar
Turajlic, S. et al. Отслеживание эволюции рака позволяет выявить ограниченные пути к метастазам: TRACERx Renal. Ячейка 173 , 581–594.e12 (2018).
CAS PubMed PubMed Central Статья Google Scholar
Monzon, F.A. et al. Полногеномные массивы SNP как потенциальный диагностический инструмент для обнаружения характерных хромосомных аберраций в опухолях почечного эпителия. Мод. Патол. 21 , 599–608 (2008).
CAS PubMed Статья Google Scholar
Wang, L. et al. Полное экзомное секвенирование рака поджелудочной железы человека и характеристика геномной нестабильности, вызванной гаплонедостаточностью и полным дефицитом MLh2. Genome Res. 22 , 208–219 (2012).
CAS PubMed PubMed Central Статья Google Scholar
Chiang, Y.C. et al. Гаплонедостаточность SETD2 для метилирования микротрубочек является одним из первых факторов нестабильности генома при почечно-клеточной карциноме. Cancer Res. 78 , 3135–3146 (2018).
CAS PubMed PubMed Central Статья Google Scholar
Fei, S. S. et al. Факторы, специфичные для пациента, влияют на паттерны соматической изменчивости при опухолях почек при болезни фон Гиппеля-Линдау. Нат. Commun. 7 , 11588 (2016).
CAS PubMed PubMed Central Статья Google Scholar
Бахум, С. Ф. и Кэнтли, Л. С. Многогранная роль хромосомной нестабильности в раке и его микросреде. Ячейка 174 , 1347–1360 (2018).
CAS PubMed PubMed Central Статья Google Scholar
Kalsbeek, D. & Golsteyn, R.M. Адаптация контрольной точки G2 / M-фазы и образование микроядер как механизмы, которые способствуют нестабильности генома в клетках человека. Внутр. J. Mol. Sci. 18 , 2344 (2017).
PubMed Central Статья CAS Google Scholar
Подримай-Бытыки, А. и др. Частоты микроядер, нуклеоплазматических мостиков и ядерных зачатков как биомаркеры геномной нестабильности у пациентов с уротелиально-клеточной карциномой. Sci. Отчетность 8 , 17873 (2018).
CAS PubMed PubMed Central Статья Google Scholar
Lonser, R. R. et al. Болезнь фон Гиппеля-Линдау. Ланцет 361 , 2059–2067 (2003).
CAS PubMed Статья Google Scholar
Хо, Т. Х. и Йонаш, Э. Синдромы генетического рака почки. J. Natl Compr. Canc. Netw. 12 , 1347–1355 (2014).
CAS PubMed Статья Google Scholar
Nickerson, M. L. et al. Улучшенная идентификация изменений гена фон Хиппеля-Линдау в светлоклеточных опухолях почек. Clin. Cancer Res. 14 , 4726–4734 (2008).
CAS PubMed PubMed Central Статья Google Scholar
Максвелл, П. Х. и др. Индуцируемый гипоксией фактор-1 модулирует экспрессию генов в солидных опухолях и влияет как на ангиогенез, так и на рост опухоли. Proc. Natl Acad. Sci. США 94 , 8104–8109 (1997).
CAS PubMed Статья Google Scholar
Flamme, I., Krieg, M. & Plate, K. H. Повышение регуляции фактора роста эндотелия сосудов в стромальных клетках гемангиобластом коррелирует с повышением регуляции фактора транскрипции HRF / HIF-2alpha. Am. J. Pathol. 153 , 25–29 (1998).
CAS PubMed PubMed Central Статья Google Scholar
Krieg, M. et al. Повышение регуляции индуцируемых гипоксией факторов HIF-1alpha и HIF-2alpha в нормоксических условиях в клетках карциномы почек за счет потери функции гена-супрессора опухоли фон Хиппеля-Линдау. Онкоген 19 , 5435–5443 (2000).
CAS PubMed Статья Google Scholar
Максвелл, П. Х. и др. Белок-супрессор опухолей VHL нацелен на индуцируемые гипоксией факторы для кислородзависимого протеолиза. Nature 399 , 271–275 (1999).
CAS PubMed Статья Google Scholar
Кейт Б., Джонсон Р. С. и Саймон М. С. HIF1альфа и HIF2альфа: соперничество братьев и сестер в росте и прогрессировании гипоксической опухоли. Нат. Rev. Cancer 12 , 9–22 (2011).
PubMed PubMed Central Статья CAS Google Scholar
Takahashi, A. et al. Заметно повышенное количество информационных РНК для фактора роста эндотелия сосудов и фактора роста плаценты при почечно-клеточной карциноме, связанной с ангиогенезом. Cancer Res. 54 , 4233–4237 (1994).
CAS PubMed Google Scholar
Ху, К. Дж., Ван, Л. Ю., Чодош, Л. А., Кейт, Б. и Саймон, М. С. Дифференциальная роль индуцируемого гипоксией фактора 1альфа (HIF-1альфа) и HIF-2альфа в регуляции гипоксических генов. Мол. Cell Biol. 23 , 9361–9374 (2003).
CAS PubMed PubMed Central Статья Google Scholar
Raval, R. R. et al. Противопоставление свойств индуцируемого гипоксией фактора 1 (HIF-1) и HIF-2 при почечно-клеточной карциноме, ассоциированной с фон Хиппелем-Линдау. Мол. Cell Biol. 25 , 5675–5686 (2005).
CAS PubMed PubMed Central Статья Google Scholar
Кэрролл, В.А. и Эшкрофт, М. Роль фактора, индуцируемого гипоксией (HIF) -1альфа, по сравнению с HIF-2альфа в регуляции генов-мишеней HIF в ответ на гипоксию, инсулиноподобный фактор роста-I или потеря функции фон Хиппеля-Линдау: последствия для воздействия на путь HIF. Cancer Res. 66 , 6264–6270 (2006).
CAS PubMed Статья Google Scholar
Ким, Дж. У., Чернышев, И., Семенца, Г. Л. и Данг, С. В. HIF-1-опосредованная экспрессия киназы пируватдегидрогеназы: метаболический переключатель, необходимый для клеточной адаптации к гипоксии. Cell Metab. 3 , 177–185 (2006).
PubMed Статья CAS Google Scholar
Semenza, G. L. et al. Элементы ответа на гипоксию в промоторах гена альдолазы A, енолазы 1 и лактатдегидрогеназы A содержат важные сайты связывания для фактора 1, индуцируемого гипоксией. J. Biol. Chem. 271 , 32529–32537 (1996).
CAS Статья PubMed Google Scholar
Zhang, H. et al. Митохондриальная аутофагия — это HIF-1-зависимый адаптивный метаболический ответ на гипоксию. Дж.Биол. Chem. 283 , 10892–10903 (2008).
CAS PubMed PubMed Central Статья Google Scholar
Bellot, G. et al. Индуцируемая гипоксией аутофагия опосредуется индуцируемым гипоксией фактором индукции BNIP3 и BNIP3L через их домены Bh4. Мол. Cell Biol. 29 , 2570–2581 (2009).
CAS PubMed PubMed Central Статья Google Scholar
О’Брайан, Дж. П. и др. axl, трансформирующий ген, выделенный из первичных клеток миелоидного лейкоза человека, кодирует новую рецепторную тирозинкиназу. Мол. Cell Biol. 11 , 5016–5031 (1991).
PubMed PubMed Central Статья Google Scholar
Лемке, Г. Биология рецепторов ТАМ. Колд Спринг Харб. Перспектива. Биол. 5 , a009076 (2013).
PubMed PubMed Central Статья CAS Google Scholar
Lai, C., Gore, M. и Lemke, G. Структура, экспрессия и активность Tyro 3, рецепторной тирозинкиназы, связанной с нервной адгезией. Онкоген 9 , 2567–2578 (1994).
CAS PubMed Google Scholar
Rankin, E. B. et al. Прямая регуляция передачи сигналов GAS6 / AXL с помощью HIF способствует метастазированию в почки через SRC и MET. Proc. Natl Acad. Sci. США 111 , 13373–13378 (2014).
CAS PubMed Статья Google Scholar
Zhou, L. et al. Ориентация на MET и AXL преодолевает устойчивость к терапии сунитинибом при почечно-клеточной карциноме. Онкоген 35 , 2687–2697 (2015).
PubMed PubMed Central Статья CAS Google Scholar
Rankin, E. B. et al. Инактивация ядерного транслокатора рецептора арилгидроуглерода (Arnt) подавляет сосудистые опухоли, связанные с болезнью фон Хиппеля-Линдау, у мышей. Мол. Cell Biol. 25 , 3163–3172 (2005).
CAS PubMed PubMed Central Статья Google Scholar
Fu, L., Wang, G., Shevchuk, MM, Nanus, DM & Gudas, LJ Создание мышиной модели болезни почек Фон Гиппеля-Линдау, приводящей к раку почек, путем экспрессии конститутивно активного мутанта HIF1alpha. Cancer Res. 71 , 6848–6856 (2011).
CAS PubMed PubMed Central Статья Google Scholar
Fu, L., Wang, G., Shevchuk, M. M., Nanus, D. M. & Gudas, L.J. Активация HIF2alpha в клетках проксимальных канальцев почек вызывает аномальное отложение гликогена, но не вызывает онкогенез. Cancer Res. 73 , 2916–2925 (2013).
CAS PubMed PubMed Central Статья Google Scholar
Schietke, R.E. et al. Экспрессия HIF-2альфа в почечных канальцах требует инактивации VHL и вызывает фиброз и кисты. PLoS One 7 , e31034 (2012).
CAS PubMed PubMed Central Статья Google Scholar
Schonenberger, D. et al. Формирование почечных кист и опухолей у мышей с дефицитом vhl / trp53 требует HIF1alpha и HIF2alpha. Cancer Res. 76 , 2025–2036 (2016).
CAS PubMed Статья Google Scholar
Zhang, J. & Zhang, Q. VHL и передача сигналов гипоксии: за пределами HIF при раке. Биомедицины 6 , 35 (2018).
PubMed Central Статья CAS Google Scholar
Guo, J. et al. pVHL подавляет киназную активность Akt зависимым от пролин-гидроксилирования образом. Наука 353 , 929–932 (2016).
CAS PubMed PubMed Central Статья Google Scholar
Ан, Дж. И Реттиг, М. Б. Механизм опосредованного белком фон Хиппеля-Линдау подавления активности ядерного фактора каппа B. Мол. Cell Biol. 25 , 7546–7556 (2005).
CAS PubMed PubMed Central Статья Google Scholar
Yang, H. et al. pVHL действует как адаптер, способствующий ингибирующему фосфорилированию NF-kappaB агониста Card9 с помощью CK2. Мол. Ячейка 28 , 15–27 (2007).
PubMed PubMed Central Статья CAS Google Scholar
Peri, S., Devarajan, K., Yang, D.H., Knudson, A.G. и Balachandran, S. Мета-анализ идентифицирует NF-kappaB как терапевтическую мишень при раке почек. PLoS One 8 , e76746 (2013).
CAS PubMed PubMed Central Статья Google Scholar
Hu, L. et al. TBK1 является синтетической летальной мишенью при раке с потерей VHL. Рак Discov. 10 , 460–475 (2020).
CAS PubMed Статья Google Scholar
Metcalf, J. L. et al. K63-убиквитилирование VHL с помощью SOCS1 опосредует репарацию двухцепочечных разрывов ДНК. Онкоген 33 , 1055–1065 (2014).
CAS PubMed Статья Google Scholar
Scanlon, S.E., Hegan, D.C., Sulkowski, P.L. и Glazer, P.M. Подавление гомологически зависимой репарации двухцепочечных разрывов ДНК индуцирует чувствительность к ингибитору PARP в VHL-дефицитной почечно-клеточной карциноме человека. Oncotarget 9 , 4647–4660 (2018).
PubMed Статья Google Scholar
Эспана-Агусти, Дж., Уоррен, А., Чу, С. К., Адамс, Д. Дж. И Матакиду, А. Потеря PBRM1 устраняет VHL-зависимый репликационный стресс, способствуя канцерогенезу почек. Нат. Commun. 8 , 2026 (2017).
PubMed PubMed Central Статья CAS Google Scholar
Zhou, L. et al. Резюме: Tip60-зависимая репарация гомологичной рекомбинации ДНК нарушена при VHL-дефицитной светлоклеточной почечно-клеточной карциноме. Cancer Res. 78 , 1364 (2018).
Google Scholar
Чжан Дж.и другие. Фактор транскрипции субстрата VHL ZHX2 как онкогенный фактор в светлоклеточной почечно-клеточной карциноме. Наука 361 , 290–295 (2018).
PubMed PubMed Central Статья CAS Google Scholar
Calzada, M. J. et al. Белок-супрессор опухоли фон Хиппеля-Линдау регулирует сборку межклеточных соединений в раковых клетках почек посредством механизмов, независимых от факторов, индуцируемых гипоксией. Cancer Res. 66 , 1553–1560 (2006).
CAS PubMed Статья Google Scholar
Stickle, N.H. et al. Модификация pVHL с помощью NEDD8 необходима для сборки фибронектинового матрикса и подавления развития опухоли. Мол. Cell Biol. 24 , 3251–3261 (2004).
CAS PubMed PubMed Central Статья Google Scholar
Ohh, M. et al. Белок-супрессор опухоли фон Хиппеля-Линдау необходим для правильной сборки внеклеточного фибронектинового матрикса. Мол. Ячейка , , 1, , 959–968 (1998).
CAS PubMed Статья Google Scholar
Курбан Г. и др. Сборка коллагенового матрикса управляется взаимодействием белка-супрессора опухоли фон Хиппеля-Линдау с гидроксилированным коллагеном IV альфа 2. Онкоген 27 , 1004-1012 (2008).
CAS PubMed Статья Google Scholar
Курбан, Г., Худон, В., Дуплан, Э., Ох, М. и Пауза, А. Характеристика пути фон Хиппеля Линдау, участвующего в ремоделировании внеклеточного матрикса, клеточной инвазии и ангиогенезе. Cancer Res. 66 , 1313–1319 (2006).
CAS PubMed Статья Google Scholar
Клиффорд, С. К. и Махер, Э. Р. Болезнь фон Хиппеля-Линдау: клинические и молекулярные перспективы. Adv. Cancer Res. 82 , 85–105 (2001).
CAS PubMed Статья Google Scholar
Hoffman, M. A. et al. Мутанты белка фон Гиппеля-Линдау, связанные с заболеванием VHL типа 2C, сохраняют способность подавлять HIF. Гум. Мол. Genet. 10 , 1019–1027 (2001).
CAS PubMed Статья Google Scholar
Tang, N., Mack, F., Haase, V.H., Simon, M.C. & Johnson, R.S. Функция pVHL важна для отложения эндотелиального внеклеточного матрикса. Мол. Cell Biol. 26 , 2519–2530 (2006).
CAS PubMed PubMed Central Статья Google Scholar
Lolkema, M. P. et al. Подавление опухоли белком фон Гиппель-Линдау требует фосфорилирования кислого домена. J. Biol.Chem. 280 , 22205–22211 (2005).
CAS PubMed Статья Google Scholar
German, P. et al. Зависимое от фосфорилирования расщепление регулирует протеостаз и функцию фон Хиппеля Линдау. Онкоген 35 , 4973–4980 (2016).
CAS PubMed PubMed Central Статья Google Scholar
Хергович, А., Lisztwan, J., Barry, R., Ballschmieter, P. & Krek, W. Регулирование стабильности микротрубочек с помощью белка-супрессора опухоли von Hippel-Lindau pVHL. Нат. Cell Biol. 5 , 64–70 (2003).
CAS PubMed Статья Google Scholar
Schermer, B. et al. Белок-супрессор опухолей фон Хиппеля-Линдау контролирует цилиогенез, ориентируя рост микротрубочек. J. Cell Biol. 175 , 547–554 (2006).
CAS PubMed PubMed Central Статья Google Scholar
Эстебан, М. А., Хартен, С. К., Тран, М. Г. и Максвелл, П. Х. Формирование первичных ресничек в почечном эпителии регулируется белком-супрессором опухоли фон Хиппеля-Линдау. J. Am. Soc. Нефрол. 17 , 1801–1806 (2006).
CAS PubMed Статья Google Scholar
Lutz, M. S. & Burk, R. D. Формирование первичных ресничек требует функции гена von Hippel-Lindau в клетках, происходящих из почек. Cancer Res. 66 , 6903–6907 (2006).
CAS PubMed Статья Google Scholar
Девлин Л. А. и Сэйер Дж. А. Почечные цилиопатии. Curr. Opin. Genet. Dev. 56 , 49–60 (2019).
CAS PubMed Статья Google Scholar
Гасанов Э. и др. Убиквитинирование и регуляция AURKA определяет гипоксию-независимую активность лигазы E3 VHL. Онкоген 36 , 3450–3463 (2017).
CAS PubMed PubMed Central Статья Google Scholar
Thoma, C. R. et al. Потеря VHL вызывает разориентацию веретена и нестабильность хромосом. Нат. Cell Biol. 11 , 994–1001 (2009).
CAS PubMed Статья Google Scholar
Hell, M. P., Duda, M., Weber, T. C., Moch, H. & Krek, W. Функции супрессора опухолей VHL в контроле митотической верности. Cancer Res. 74 , 2422–2431 (2014).
CAS PubMed Статья Google Scholar
Hell, M. P. et al. miR-28-5p способствует хромосомной нестабильности при VHL-ассоциированном раке, ингибируя трансляцию Mad2. Cancer Res. 74 , 2432–2443 (2014).
CAS PubMed Статья Google Scholar
Янку, Ф., Яп, Т. А. и Мерик-Бернстам, Ф. Нацеливание на путь PI3K при раке: делаем ли мы успехи? Нат. Преподобный Clin. Онкол. 15 , 273–291 (2018).
CAS PubMed Статья Google Scholar
Хоригучи, А., Оя, М., Учида, А., Марумо, К. и Мураи, М.Повышенная активация Akt и ее влияние на клинико-патологические особенности почечно-клеточного рака. J. Urol. 169 , 710–713 (2003).
CAS PubMed Статья Google Scholar
Sourbier, C. et al. Путь фосфоинозитид-3-киназа / Akt: новая мишень в терапии почечно-клеточного рака человека. Cancer Res. 66 , 5130–5142 (2006).
CAS PubMed Статья Google Scholar
Yang, J. et al. Ориентация на PI3K при раке: механизмы и достижения в клинических испытаниях. Мол. Рак 18 , 26 (2019).
PubMed PubMed Central Статья Google Scholar
Kim, J. et al. Цитоплазматическая секвестрация p27 посредством фосфорилирования AKT в почечно-клеточной карциноме. Clin. Cancer Res. 15 , 81–90 (2009).
CAS PubMed PubMed Central Статья Google Scholar
Хаазе В. Х., Гликман Дж. Н., Соколовский М. и Яениш Р. Сосудистые опухоли в печени с целевой инактивацией опухолевого супрессора фон Хиппеля-Линдау. Proc. Natl Acad. Sci. США 98 , 1583–1588 (2001).
CAS PubMed Статья Google Scholar
Hickey, M. M., Lam, J. C., Bezman, N. A., Rathmell, W. K. & Simon, M. C. Мутация фон Хиппеля-Линдау у мышей воспроизводит чувашскую полицитемию посредством передачи сигналов фактора 2альфа, индуцируемого гипоксией, и эритропоэзиса селезенки. J. Clin. Вкладывать деньги. 117 , 3879–3889 (2007).
CAS PubMed PubMed Central Google Scholar
Lee, C. M. et al. Мутация гена VHL типа 2B снижает дозировку HIF in vitro и in vivo. Онкоген 28 , 1694–1705 (2009).
CAS PubMed PubMed Central Статья Google Scholar
Gnarra, J.R. et al. Дефектный плацентарный васкулогенез вызывает эмбриональную летальность у мышей с дефицитом VHL. Proc. Natl Acad. Sci. USA 94 , 9102–9107 (1997).
CAS PubMed Статья Google Scholar
Фрю, И. Дж. И Мох, Х. Более четкое представление о молекулярной сложности светлоклеточного почечно-клеточного рака. Annu. Преподобный Патол. 10 , 263–289 (2015).
CAS PubMed Статья Google Scholar
Ранкин, Э. Б., Томашевски, Дж. Э. и Хааз, В. Х. Развитие почечных кист у мышей с условной инактивацией опухолевого супрессора фон Гиппеля-Линдау. Cancer Res. 66 , 2576–2583 (2006).
CAS PubMed PubMed Central Статья Google Scholar
Mathia, S. et al. Действие фактора, индуцируемого гипоксией, на печень и почки мышей с делецией белка фон Хиппель-Линдау на основе Pax8-rtTA. Acta Physiol. 207 , 565–576 (2013).
CAS Статья Google Scholar
Schley, G. et al. Стабилизация индуцируемых гипоксией факторов транскрипции в толстой восходящей конечности защищает от ишемического острого повреждения почек. J. Am. Soc. Нефрол. 22 , 2004–2015 (2011).
CAS PubMed PubMed Central Статья Google Scholar
Лубенский И.А. и др. Аллельные делеции гена VHL, обнаруженные при множественных микроскопических светлоклеточных поражениях почек у пациентов с болезнью фон Гиппеля-Линдау. Am. J. Pathol. 149 , 2089–2094 (1996).
CAS PubMed PubMed Central Google Scholar
Paraf, F. et al. Поражения почек при болезни фон Гиппеля-Линдау: иммуногистохимическая экспрессия молекул дифференцировки нефрона, молекул адгезии и белков апоптоза. Гистопатология 36 , 457–465 (2000).
CAS PubMed Статья Google Scholar
Albers, J. et al. Комбинированная мутация Vhl и Trp53 вызывает кисты и опухоли почек у мышей. EMBO Mol. Med. 5 , 949–964 (2013).
CAS PubMed PubMed Central Статья Google Scholar
Фрю, И.J. et al. Белки-супрессоры опухолей pVHL и PTEN совместно подавляют образование кист почек. EMBO J. 27 , 1747–1757 (2008).
CAS PubMed PubMed Central Статья Google Scholar
Harlander, S. et al. Комбинированная мутация в Vhl, Trp53 и Rb1 вызывает у мышей светлоклеточный почечно-клеточный рак. Нат. Med. 23 , 869–877 (2017).
CAS PubMed PubMed Central Статья Google Scholar
Gu, Y. F. et al. Моделирование почечно-клеточного рака у мышей: инактивация Bap1 и Pbrm1 приводит к степени злокачественности опухоли. Рак Discov. 7 , 900–917 (2017).
CAS PubMed PubMed Central Статья Google Scholar
Nargund, A. M. et al. Белок SWI / SNF PBRM1 сдерживает вызванную потерей VHL светлоклеточную почечную карциному. Cell Rep. 18 , 2893–2906 (2017).
CAS PubMed PubMed Central Статья Google Scholar
Lee, H. et al. BAF180 регулирует клеточное старение и гомеостаз гемопоэтических стволовых клеток через p21. Oncotarget 7 , 19134–19146 (2016).
PubMed PubMed Central Статья Google Scholar
де Кубас, А. А. и Ратмелл, В. К. Эпигенетические модификаторы: активность при почечно-клеточной карциноме. Нат. Преподобный Урол. 15 , 599–614 (2018).
PubMed Статья Google Scholar
Thompson, M. Polybromo-1: субъединица, нацеленная на хроматин комплекса PBAF. Biochimie 91 , 309–319 (2009).
CAS PubMed Статья Google Scholar
Pulice, J. L. & Kadoch, C. Состав и функция SWI / SNF комплексов ремоделирования хроматина млекопитающих при заболеваниях человека. Колд Спринг Харб. Symp. Quant. Биол. 81 , 53–60 (2016).
PubMed Статья Google Scholar
Kim, S.H. et al. Прогностическое значение тканевых маркеров BAP1, PBRM1, pS6, PTEN, TGase2, PD-L1, CA9, PSMA и Ki-67 при локализованной почечно-клеточной карциноме: ретроспективное исследование тканевых микроматриц с использованием иммуногистохимии. PLoS One 12 , e0179610 (2017).
PubMed PubMed Central Статья CAS Google Scholar
Wang, Z. et al. Саркоматоидная почечно-клеточная карцинома имеет отчетливый молекулярный патогенез, профиль мутации драйвера и транскрипционный ландшафт. Clin. Cancer Res. 23 , 6686–6696 (2017).
CAS PubMed PubMed Central Статья Google Scholar
Gao, W., Li, W., Xiao, T., Liu, XS & Kaelin, WG Jr. Инактивация гена-супрессора опухоли PBRM1 усиливает HIF-ответ в VHL — / — ясно клеточная карцинома почек. Proc. Natl Acad. Sci. США 114 , 1027–1032 (2017).
CAS PubMed Статья Google Scholar
Liao, L. et al. Множественные опухолевые супрессоры регулируют HIF-зависимую петлю отрицательной обратной связи через ISGF3 при светлоклеточном раке почек человека. eLife 7 , e37925 (2018).
PubMed PubMed Central Статья Google Scholar
Liu, X. D. et al. Потеря PBRM1 определяет фенотип неиммуногенной опухоли, связанный с резистентностью к ингибиторам контрольной точки при карциноме почек. Нат. Commun. 11 , 2135 (2020).
CAS PubMed PubMed Central Статья Google Scholar
Cai, W. et al. PBRM1 действует как считыватель лизина-ацетилирования p53 для подавления роста опухоли почек. Нат. Commun. 10 , 5800 (2019).
CAS PubMed PubMed Central Статья Google Scholar
Xue, Y. et al. Комплекс ремоделирования хроматина SWI / SNF-B человека связан с дрожжевыми rsc и локализуется на кинетохорах митотических хромосом. Proc. Natl Acad. Sci. США 97 , 13015–13020 (2000).
CAS PubMed Статья Google Scholar
Huang, J., Hsu, J. M. & Laurent, B.C. Комплекс ремоделирования нуклеосомы RSC необходим для ассоциации Cohesin с плечами хромосом. Мол. Ячейка 13 , 739–750 (2004).
CAS PubMed Статья Google Scholar
Baetz, KK, Krogan, NJ, Emili, A., Greenblatt, J. & Hieter, P. Скрининг модификатора гаплонедостаточности генома ctf13-30 / CTF13 идентифицирует дрожжевой комплекс ремоделирования хроматина RSC, который необходим для образования сестринских хроматид. сплоченность. Мол. Cell Biol. 24 , 1232–1244 (2004).
CAS PubMed PubMed Central Статья Google Scholar
Браунли, П. М., Чемберс, А.L., Cloney, R., Bianchi, A. & Downs, J. A. BAF180 способствует сплоченности и предотвращает нестабильность генома и анеуплоидию. Cell Rep. 6 , 973–981 (2014).
CAS PubMed PubMed Central Статья Google Scholar
Clark, D. J. et al. Комплексная протеогеномная характеристика светлоклеточного почечно-клеточного рака. Ячейка 179 , 964–983.e31 (2019).
CAS PubMed PubMed Central Статья Google Scholar
Hakimi, A.A. et al. Транскриптомное профилирование микросреды опухоли выявляет отдельные подгруппы светлоклеточного почечно-клеточного рака — данные рандомизированного исследования III фазы. Рак Discov. 9 , 510–525 (2019).
CAS PubMed PubMed Central Статья Google Scholar
Jensen, D. E. et al. BAP1: новая убиквитин гидролаза, которая связывается с пальцем BRCA1 RING и усиливает опосредованное BRCA1 подавление роста клеток. Онкоген 16 , 1097–1112 (1998).
CAS PubMed Статья Google Scholar
Kapur, P. et al. Влияние мутаций BAP1 и PBRM1 на выживаемость при спорадической светлоклеточной почечно-клеточной карциноме: ретроспективный анализ с независимой проверкой. Ланцет Онкол. 14 , 159–167 (2013).
CAS PubMed PubMed Central Статья Google Scholar
Scheuermann, J. C. et al. Гистон h3A деубиквитиназная активность репрессивного комплекса Polycomb PR-DUB. Природа 465 , 243–247 (2010).
CAS PubMed PubMed Central Статья Google Scholar
Endoh, M. et al. Моноубиквитинирование гистона h3A является решающим шагом в опосредовании PRC1-зависимой репрессии онтогенетических генов для поддержания идентичности ES-клеток. PLoS Genet. 8 , e1002774 (2012).
CAS PubMed PubMed Central Статья Google Scholar
Dey, A. et al. Потеря опухолевого супрессора BAP1 вызывает миелоидную трансформацию. Наука 337 , 1541–1546 (2012).
CAS PubMed PubMed Central Статья Google Scholar
Cejas, P. et al. Сигнатуры энхансеров стратифицируют и предсказывают исходы нефункциональных нейроэндокринных опухолей поджелудочной железы. Нат. Med. 25 , 1260–1265 (2019).
CAS PubMed PubMed Central Статья Google Scholar
Peng, J. et al. Стабилизация MCRS1 с помощью BAP1 предотвращает хромосомную нестабильность при почечно-клеточной карциноме. Cancer Lett. 369 , 167–174 (2015).
CAS PubMed Статья Google Scholar
Kobayashi, A. et al. Six2 определяет и регулирует мультипотентную популяцию самообновляющихся предшественников нефронов на протяжении всего развития почек у млекопитающих. Стволовые клетки клеток 3 , 169–181 (2008).
CAS PubMed PubMed Central Статья Google Scholar
Wang, S. S. et al. Bap1 необходим для функции почек и взаимодействует с Vhl в онкогенезе почек. Proc. Natl Acad. Sci.США 111 , 16538–16543 (2014).
CAS PubMed Статья Google Scholar
Joseph, R. W. et al. Потеря экспрессии белка BAP1 является независимым маркером плохого прогноза у пациентов со светлоклеточной почечно-клеточной карциномой низкого риска. Рак 120 , 1059–1067 (2014).
CAS PubMed Статья Google Scholar
Hsieh, J. J. et al. Геномные биомаркеры рандомизированного исследования, сравнивающего эверолимус первой линии и сунитиниб у пациентов с метастатической почечно-клеточной карциномой. Eur. Урол. 71 , 405–414 (2017).
CAS PubMed Статья Google Scholar
Farley, M. N. et al. Новая мутация зародышевой линии в BAP1 предрасполагает к семейной светлоклеточной почечно-клеточной карциноме. Мол. Cancer Res. 11 , 1061–1071 (2013).
CAS PubMed PubMed Central Статья Google Scholar
Lickwar, C. R. et al. Путь Set2 / Rpd3S подавляет криптическую транскрипцию независимо от длины гена или частоты транскрипции. PLoS One 4 , e4886 (2009 г.).
PubMed PubMed Central Статья CAS Google Scholar
Хакер, К.E. et al. Анализ структуры / функции повторяющихся мутаций в белке SETD2 показывает критическую и консервативную роль остатка домена SET в поддержании стабильности белка и триметилирования гистона h4 Lys-36. J. Biol. Chem. 291 , 21283–21295 (2016).
CAS PubMed PubMed Central Статья Google Scholar
Fahey, C.C. и Davis, I.J. УСТАНОВКА стадии для развития рака: SETD2 и последствия утраченного метилирования. Колд Спринг Харб. Перспектива. Med. 7 , a026468 (2017).
PubMed PubMed Central Статья CAS Google Scholar
Park, I. Y. et al. Двойное ремоделирование хроматина и цитоскелета с помощью SETD2. Ячейка 166 , 950–962 (2016).
CAS PubMed PubMed Central Статья Google Scholar
Giaccia, A.J. Новое звено хроматина и цитоскелета при раке. Мол. Cancer Res. 14 , 1173–1175 (2016).
CAS PubMed PubMed Central Статья Google Scholar
Сирвай, Р. Н. Х. и др. SETD2 представляет собой актин-лизинметилтрансферазу. Препринт на bioRxiv https://doi.org/10.1101/2020.04.13.034629 (2020).
Karki, M. et al. Цитоскелетная функция PBRM1, считывающая метилированные микротрубочки.Препринт на bioRxiv https://doi.org/10.1101/2020.04.21.053942 (2020).
Пили, П. Г., Танг, К., Миллс, Г. Б. и Яп, Т. А. Современные стратегии для нацеливания реакции на повреждение ДНК при раке. Нат. Преподобный Clin. Онкол. 16 , 81–104 (2019).
CAS PubMed Статья Google Scholar
Александров Л. Б. и др. Сигнатуры мутационных процессов при раке человека. Природа 500 , 415–421 (2013).
CAS PubMed PubMed Central Статья Google Scholar
Dere, R., Perkins, AL, Bawa-Khalfe, T., Jonasch, D. & Walker, CL β-катенин связывает фон Хиппель-Линдау с киназой Aurora и потерей первичных ресничек в почечных клетках. карцинома. J. Am. Soc. Нефрол. 26 , 553–564 (2014).
PubMed PubMed Central Статья CAS Google Scholar
Zhang, M. et al. HDAC6 деацетилирует и убиквитинат MSh3 для поддержания надлежащих уровней MutSalpha. Мол. Ячейка 55 , 31–46 (2014).
PubMed PubMed Central Статья CAS Google Scholar
Li, F. et al. Гистоновая метка h4K36me3 регулирует репарацию ошибочного спаривания ДНК человека посредством взаимодействия с MutSalpha. Ячейка 153 , 590–600 (2013).
CAS PubMed PubMed Central Статья Google Scholar
Naqvi, R.A. et al. Анализ гиперметилирования генов восстановления несоответствия (hmlh2 и hmsh3) при местно-распространенном раке молочной железы у индийских женщин. Гум. Патол. 39 , 672–680 (2008).
CAS PubMed Статья Google Scholar
Альтавилла Г., Фассан М., Бусатто Г., Орсолан М. и Джакомелли Л. Нестабильность микросателлитов и экспрессия hMLh2 и hMSh3 в опухолях почек. Онкол.Реп. 24 , 927–932 (2010).
CAS PubMed Статья Google Scholar
Jasin, M. & Rothstein, R. Ремонт разрывов цепей путем гомологичной рекомбинации. Колд Спринг Харб. Перспектива. Биол. 5 , а012740 (2013).
PubMed PubMed Central Статья CAS Google Scholar
Холл, Дж.M. et al. Связь семейного рака груди с ранним началом с хромосомой 17q21. Наука 250 , 1684–1689 (1990).
CAS PubMed Статья Google Scholar
Hall, J. M. et al. Закрытие гена рака груди на хромосоме 17q. Am. J. Hum. Genet. 50 , 1235–1242 (1992).
CAS PubMed PubMed Central Google Scholar
Wooster, R. et al. Идентификация гена предрасположенности к раку груди BRCA2. Nature 378 , 789–792 (1995).
CAS PubMed Статья Google Scholar
Antoniou, A.C. et al. Риск рака груди в семьях с мутациями в PALB2. N. Engl. J. Med. 371 , 497–506 (2014).
PubMed PubMed Central Статья CAS Google Scholar
Свифт, М., Моррелл, Д., Мэсси, Р. Б. и Чейз, К. Л. Заболеваемость раком в 161 семье, пострадавшей от атаксии-телеангиэктазии. N. Engl. J. Med. 325 , 1831–1836 (1991).
CAS PubMed Статья Google Scholar
Bindra, R. S. et al. Подавление Rad51 и снижение гомологичной рекомбинации в гипоксических раковых клетках. Мол. Cell Biol. 24 , 8504–8518 (2004).
CAS PubMed PubMed Central Статья Google Scholar
Bindra, R. S. et al. Индуцированное гипоксией подавление экспрессии BRCA1 с помощью E2F. Cancer Res. 65 , 11597–11604 (2005).
CAS PubMed Статья Google Scholar
Скэнлон, С. Э. и Глейзер, П. М. Гипоксический стресс способствует острой активации и хроническому подавлению белков анемии фанкони. Мол. Cancer Res. 12 , 1016–1028 (2014).
CAS PubMed PubMed Central Статья Google Scholar
Roe, J. S. et al. Фосфорилирование белка фон Хиппель-Линдау киназой 2 контрольной точки регулирует трансактивацию p53. Cell Cycle 10 , 3920–3928 (2011).
CAS PubMed Статья Google Scholar
Tang, J. et al. Ацетилирование ограничивает ассоциацию 53BP1 с поврежденным хроматином, способствуя гомологичной рекомбинации. Нат. Struct. Мол. Биол. 20 , 317–325 (2013).
CAS PubMed PubMed Central Статья Google Scholar
Sun, Y., Jiang, X., Chen, S., Fernandes, N. & Price, B.D. Роль гистонацетилтрансферазы Tip60 в ацетилировании и активации ATM. Proc.Natl Acad. Sci. США 102 , 13182–13187 (2005).
CAS PubMed Статья Google Scholar
Pfister, S. X. et al. SETD2-зависимое триметилирование гистона h4K36 необходимо для восстановления гомологичной рекомбинации и стабильности генома. Cell Rep. 7 , 2006–2018 (2014).
CAS PubMed PubMed Central Статья Google Scholar
Carvalho, S. et al. SETD2 необходим для репарации двухцепочечных разрывов ДНК и активации p53-опосредованной контрольной точки. eLife 3 , e02482 (2014).
PubMed PubMed Central Статья CAS Google Scholar
Aymard, F. et al. Транскрипционно активный хроматин рекрутирует гомологичную рекомбинацию на двухцепочечных разрывах ДНК. Нат. Struct. Мол. Биол. 21 , 366–374 (2014).
CAS PubMed PubMed Central Статья Google Scholar
Kanu, N. et al. Потеря функции SETD2 способствует разветвленной эволюции рака почки из-за стресса репликации и нарушения репарации ДНК. Онкоген 34 , 5699–5708 (2015).
CAS PubMed PubMed Central Статья Google Scholar
Li, L.И Ван, Ю. Перекрестная связь между эпигенетическими метками гистонов h4K36me3 и h5K16ac в репарации двухцепочечных разрывов ДНК. J. Biol. Chem. 292 , 11951–11959 (2017).
CAS PubMed PubMed Central Статья Google Scholar
Ismail, I.H. et al. Мутации зародышевой линии в BAP1 нарушают его функцию в репарации двухцепочечных разрывов ДНК. Cancer Res. 74 , 4282–4294 (2014).
CAS PubMed Статья Google Scholar
Peng, G. et al. Полногеномное транскриптомное профилирование репарации гомологичной рекомбинационной ДНК. Нат. Commun. 5 , 3361 (2014).
PubMed PubMed Central Статья CAS Google Scholar
Pilie, P. G. et al. Дефицит гомологичной репарации при почечно-клеточной карциноме с мутациями VHL. J. Clin. Онкол. 36 , 585 (2018).
Артикул Google Scholar
Картер, С. Л., Эклунд, А. К., Кохан, И. С., Харрис, Л. Н. и Салласи, З. Признак хромосомной нестабильности, выведенный из профилей экспрессии генов, позволяет прогнозировать клинический исход при множественных раковых заболеваниях человека. Нат. Genet. 38 , 1043–1048 (2006).
CAS PubMed Статья Google Scholar
МакГранахан, Н., Баррелл, Р. А., Эндесфельдер, Д., Новелли, М. Р., Свантон, К. Хромосомная нестабильность рака: терапевтические и диагностические проблемы. EMBO Rep. 13 , 528–538 (2012).
CAS PubMed PubMed Central Статья Google Scholar
Gordan, J. D. et al. Эффекты HIF-альфа на c-Myc различают два подтипа спорадической VHL-дефицитной светлоклеточной карциномы почек. Cancer Cell 14 , 435–446 (2008).
CAS PubMed PubMed Central Статья Google Scholar
Wolfer, A. et al. Регуляция MYC состояния метастатических раковых клеток с неблагоприятным прогнозом. Proc. Natl Acad. Sci. США 107 , 3698–3703 (2010).
CAS PubMed Статья Google Scholar
Джамал-Ханджани, М., Кесада, С.А., Ларкин, Дж. И Суантон, К.Трансляционные последствия неоднородности опухоли. Clin. Cancer Res. 21 , 1258–1266 (2015).
CAS PubMed PubMed Central Статья Google Scholar
Malouf, G.G. et al. Геномная характеристика почечно-клеточного рака с саркоматоидной дедифференцировкой выявляет повторяющиеся геномные изменения. Eur. Урол. 70 , 348–357 (2016).
CAS PubMed Статья Google Scholar
Bi, M. et al. Геномная характеристика саркоматоидной трансформации в светлоклеточной почечно-клеточной карциноме. Proc. Natl Acad. Sci. США 113 , 2170–2175 (2016).
CAS PubMed Статья Google Scholar
Хиншоу, Д. К. и Шевде, Л. А. Микроокружение опухоли врожденно модулирует прогрессирование рака. Cancer Res. 79 , 4557–4566 (2019).
CAS PubMed PubMed Central Статья Google Scholar
Chevrier, S. et al. Иммунный атлас светлоклеточного почечно-клеточного рака. Ячейка 169 , 736–749 e718 (2017).
CAS PubMed PubMed Central Статья Google Scholar
Senbabaoglu, Y. et al. Характеристика иммунного микроокружения опухоли при светлоклеточном почечно-клеточном раке позволяет идентифицировать прогностические и иммунотерапевтически важные сигнатуры информационной РНК. Genome Biol. 17 , 231 (2016).
PubMed PubMed Central Статья CAS Google Scholar
Ko, J. S. et al. Сунитиниб опосредует обратное накопление миелоидных клеток-супрессоров у пациентов с почечно-клеточной карциномой. Clin. Cancer Res. 15 , 2148–2157 (2009).
CAS PubMed Статья Google Scholar
Wang, T. et al. Эмпирический подход с использованием опухолевых трансплантатов для анализа микросреды опухоли при почечно-клеточной карциноме позволяет выявить недостающее звено с прогностическими воспалительными факторами. Рак Discov. 8 , 1142–1155 (2018).
CAS PubMed PubMed Central Статья Google Scholar
Miao, D. et al. Геномные корреляты ответа на терапию иммунными контрольными точками при светлоклеточном почечно-клеточном раке. Наука 359 , 801–806 (2018).
CAS PubMed PubMed Central Статья Google Scholar
McDermott, D. F. et al. Клиническая активность и молекулярные корреляты ответа на атезолизумаб отдельно или в комбинации с бевацизумабом по сравнению с сунитинибом при почечно-клеточной карциноме. Нат. Med. 24 , 749–757 (2018).
CAS PubMed PubMed Central Статья Google Scholar
Bindea, G. et al. Пространственно-временная динамика внутриопухолевых иммунных клеток выявляет иммунный ландшафт при раке человека. Иммунитет 39 , 782–795 (2013).
CAS PubMed Статья Google Scholar
Yoshihara, K. et al. Определение чистоты опухоли и примеси стромальных и иммунных клеток по данным экспрессии. Нат. Commun. 4 , 2612 (2013).
PubMed PubMed Central Статья CAS Google Scholar
Уинслоу, С., Леандерссон, К., Эдшо, А. и Ларссон, С. Прогностические сигнатуры стромальных генов при раке груди. Breast Cancer Res. 17 , 23 (2015).
PubMed PubMed Central Статья CAS Google Scholar
Heng, D. Y. et al. Факторы прогноза общей выживаемости у пациентов с метастатической почечно-клеточной карциномой, получавших препараты, нацеленные на фактор роста эндотелия сосудов: результаты большого многоцентрового исследования. J. Clin. Онкол. 27 , 5794–5799 (2009).
CAS PubMed Статья Google Scholar
Сунг, С. К., Шу, Х. К., Макдермотт, М. В., Снид, П. К. и Ларсон, Д. А. Стереотаксическая радиохирургия при злокачественной меланоме головного мозга. Surg. Clin. North Am. 76 , 1399–1411 (1996).
CAS PubMed Статья Google Scholar
Braun, D.A. et al. Клиническая проверка изменений PBRM1 как маркера ответа ингибитора иммунных контрольных точек при почечно-клеточной карциноме. JAMA Oncol. 5 , 1631–1633 (2019).
PubMed Central Статья Google Scholar
Zisman, A. et al. Улучшенное прогнозирование почечно-клеточного рака с использованием интегрированной системы стадирования. J. Clin. Онкол. 19 , 1649–1657 (2001).
CAS PubMed Статья Google Scholar
Frank, I. et al. Модель прогнозирования исходов для пациентов со светлоклеточным почечно-клеточным раком, получавших радикальную нефрэктомию, на основе стадии опухоли, размера, степени и некроза: оценка SSIGN. J. Urol. 168 , 2395–2400 (2002).
PubMed Статья Google Scholar
Каттан, М. В., Рейтер, В., Моцер, Р. Дж., Кац, Дж. И Руссо, П. Послеоперационная прогностическая номограмма почечно-клеточного рака. J. Urol. 166 , 63–67 (2001).
CAS PubMed Статья Google Scholar
Bettegowda, C. et al. Обнаружение циркулирующей опухолевой ДНК на ранних и поздних стадиях злокачественных новообразований человека. Sci. Пер. Med. 6 , 224ra224 (2014).
Артикул CAS Google Scholar
Cohen, J. D. et al. Выявление и локализация хирургически резектабельных раковых опухолей с помощью анализа крови на несколько аналитов. Наука 359 , 926–930 (2018).
CAS PubMed PubMed Central Статья Google Scholar
Pal, S. K. et al. Эволюция профиля циркулирующей опухолевой ДНК от первой линии до последующей терапии метастатической почечно-клеточной карциномы. Eur. Урол. 72 , 557–564 (2017).
CAS PubMed Статья Google Scholar
Merker, J. D. et al. Анализ ДНК циркулирующих опухолей у больных раком: совместный обзор Американского общества клинической онкологии и Коллегии американских патологов. Arch. Патол. Лаборатория. Med. 142 , 1242–1253 (2018).
CAS PubMed Статья Google Scholar
Rouzier, R.и другие. Молекулярные подтипы рака груди по-разному реагируют на предоперационную химиотерапию. Clin. Cancer Res. 11 , 5678–5685 (2005).
CAS PubMed Статья Google Scholar
Travis, W. D. et al. Классификация опухолей легких Всемирной организации здравоохранения 2015 г .: влияние генетических, клинических и радиологических достижений после классификации 2004 г. J. Thorac. Онкол. 10 , 1243–1260 (2015).
PubMed Статья Google Scholar
Turcotte, S. et al. Молекула, нацеленная на почечно-клеточную карциному с дефицитом VHL, индуцирующая аутофагию. Cancer Cell 14 , 90–102 (2008).
CAS PubMed PubMed Central Статья Google Scholar
Ding, Z. et al. Генетические и фармакологические стратегии рефункционализации мутантного белка von Hippel Lindau R167Q. Cancer Res. 74 , 3127–3136 (2014).
CAS PubMed PubMed Central Статья Google Scholar
Ding, Z. et al. Агенты, стабилизирующие мутированный белок фон Хиппеля-Линдау (VHL): результаты высокопроизводительного скрининга для выявления соединений, которые модулируют протеостаз VHL. J. Biomol. Экран. 17 , 572–580 (2012).
CAS PubMed PubMed Central Статья Google Scholar
Gameiro, P.A. et al. In vivo HIF-опосредованное восстановительное карбоксилирование регулируется уровнями цитрата и сенсибилизирует VHL-дефицитные клетки к депривации глутамина. Cell Metab. 17 , 372–385 (2013).
CAS PubMed PubMed Central Статья Google Scholar
Национальная медицинская библиотека США. ClinicalTrials.gov https://clinicaltrials.gov/ct2/show/NCT03428217 (2019).
Национальная медицинская библиотека США. ClinicalTrials.gov https://clinicaltrials.gov/ct2/show/NCT03163667 (2019).
Courtney, K. D. et al. Фаза I исследования повышения дозы PT2385, первого в своем классе антагониста фактора-2альфа, индуцируемого гипоксией, у пациентов с ранее пролеченным прогрессирующим светлоклеточным почечно-клеточным раком. J. Clin. Онкол. 36 , 867–874 (2018).
CAS PubMed Статья Google Scholar
Chen, W. et al. Воздействие на почечно-клеточную карциному с помощью антагониста HIF-2. Природа 539 , 112–117 (2016).
CAS PubMed PubMed Central Статья Google Scholar
Национальная медицинская библиотека США. ClinicalTrials.gov https://clinicaltrials.gov/ct2/show/NCT03634540 (2020).
Национальная медицинская библиотека США. ClinicalTrials.gov https: // Clinicaltrials.gov / ct2 / show / NCT03401788 (2020).
Jonasch, E. et al. Открытое исследование фазы II для оценки PT2977 для лечения почечно-клеточного рака, связанного с болезнью фон Хиппеля-Линдау. J. Clin. Онкол. 37 , TPS680 (2019).
Артикул Google Scholar
Jonasch, E. et al. Фаза II исследования перорального ингибитора HIF-2α MK-6482 при почечно-клеточной карциноме, связанной с болезнью Фон Хиппеля-Линдау. J. Clin. Онкол. 38 , 5003–5003 (2020).
Артикул Google Scholar
LaFave, L. M. et al. Потеря функции BAP1 приводит к EZh3-зависимой трансформации. Нат. Med. 21 , 1344–1349 (2015).
CAS PubMed PubMed Central Статья Google Scholar
Schoumacher, M. et al. Клетки увеальной меланомы устойчивы к ингибированию EZh3 независимо от статуса BAP1. Нат. Med. 22 , 577–578 (2016).
CAS PubMed Статья Google Scholar
Pfister, S. X. et al. Ингибирование WEE1 избирательно убивает злокачественные опухоли с дефицитом гистона h4K36me3 из-за голодания по dNTP. Cancer Cell 28 , 557–568 (2015).
CAS PubMed PubMed Central Статья Google Scholar
Terzo, E.A. et al. Потеря SETD2 повышает чувствительность клеток к ингибированию PI3Kbeta и AKT. Oncotarget 10 , 647–659 (2019).
PubMed PubMed Central Статья Google Scholar
Motzer, R.J. et al. Эффективность эверолимуса при запущенной почечно-клеточной карциноме: двойное слепое рандомизированное плацебо-контролируемое исследование III фазы. Ланцет 372 , 449–456 (2008).
CAS Статья PubMed Google Scholar
Hudes, G. et al. Темсиролимус, интерферон альфа или оба препарата для лечения прогрессирующей почечно-клеточной карциномы. N. Engl. J. Med. 356 , 2271–2281 (2007).
CAS PubMed Статья Google Scholar
Jonasch, E. et al. Рандомизированное исследование фазы 2 МК-2206 в сравнении с эверолимусом при рефрактерной почечно-клеточной карциноме. Ann. Онкол. 28 , 804–808 (2017).
CAS PubMed PubMed Central Статья Google Scholar
Ibrahim, Y.H. et al. Ингибирование PI3K ухудшает экспрессию BRCA1 / 2 и повышает сенсибилизацию BRCA-ориентированного тройного отрицательного рака молочной железы к ингибированию PARP. Рак Discov. 2 , 1036–1047 (2012).
CAS PubMed PubMed Central Статья Google Scholar
Juvekar, A. et al. Комбинация ингибитора PI3K с ингибитором PARP обеспечивает эффективную терапию рака молочной железы, связанного с BRCA1. Рак Discov. 2 , 1048–1063 (2012).
CAS PubMed PubMed Central Статья Google Scholar
Escudier, B. et al. Рандомизированное контролируемое двойное слепое исследование III фазы (AVOREN) по сравнению бевацизумаб / интерферон-α2a в сравнении с плацебо / интерфероном-α2a в качестве терапии первой линии при метастатической почечно-клеточной карциноме. J. Clin. Онкол. 25 , 3 (2007).
Артикул Google Scholar
Rini, B. I. et al. Бевацизумаб плюс интерферон альфа в сравнении с монотерапией интерфероном альфа у пациентов с метастатической почечно-клеточной карциномой: CALGB . J. Clin. Онкол. 26 , 5422–5428 (2008).
CAS PubMed PubMed Central Статья Google Scholar
Rini, B. I. et al. Сравнительная эффективность акситиниба и сорафениба при запущенной почечно-клеточной карциноме (AXIS): рандомизированное исследование фазы 3. Ланцет 378 , 1931–1939 (2012).
Артикул CAS Google Scholar
Motzer, R.J. et al. Сунитиниб в сравнении с интерфероном альфа при метастатической почечно-клеточной карциноме. N. Engl. J. Med. 356 , 115–124 (2007).
CAS PubMed Статья Google Scholar
Choueiri, T. K. et al. Кабозантиниб в сравнении с эверолимусом при запущенной почечно-клеточной карциноме. N. Engl. J. Med. 373 , 1814–1823 (2015).
CAS PubMed PubMed Central Статья Google Scholar
Escudier, B. et al. Сорафениб при запущенной светлоклеточной почечно-клеточной карциноме. N. Engl. J. Med. 356 , 125–134 (2007).
CAS PubMed Статья Google Scholar
Штернберг, К.N. et al. Пазопаниб при местнораспространенном или метастатическом почечно-клеточном раке: результаты рандомизированного исследования III фазы. J. Clin. Онкол. 28 , 1061–1068 (2010).
CAS PubMed Статья Google Scholar
Motzer, R.J. et al. Пазопаниб в сравнении с сунитинибом при метастатическом почечно-клеточном раке. N. Engl. J. Med. 369 , 722–731 (2013).
CAS PubMed Статья Google Scholar
Jonasch, E. et al. Исследование фазы II, включающее две недели приема сунитиниба и перерыв в течение одной недели у пациентов с метастатической почечно-клеточной карциномой. J. Clin. Онкол. 36 , 1588–1593 (2018).
CAS PubMed PubMed Central Статья Google Scholar
Jonasch, E. et al. Пилотное испытание терапии сунитинибом у пациентов с болезнью фон Хиппеля-Линдау. Ann. Онкол. 22 , 2661–2666 (2011).
CAS PubMed PubMed Central Статья Google Scholar
Kawakami, F. et al. Лиганд 1 запрограммированной гибели клеток и статус инфильтрирующих опухоль лимфоцитов у пациентов с почечно-клеточной карциномой и саркоматоидной дедифференцировкой. Рак 123 , 4823–4831 (2017).
CAS PubMed PubMed Central Статья Google Scholar
Joseph, R. W. et al. Экспрессия PD-1 и PD-L1 при почечно-клеточной карциноме с саркоматоидной дифференцировкой. Cancer Immunol. Res. 3 , 1303–1307 (2015).
CAS PubMed PubMed Central Статья Google Scholar
Raychaudhuri, R. et al. Ингибирование иммунных контрольных точек при саркоматоидном почечно-клеточном раке: новая парадигма лечения. Clin. Генитурин. Рак 15 , e897 – e901 (2017).
PubMed Статья Google Scholar
Paolino, M. et al. Рецепторы E3-лигазы Cbl-b и ТАМ регулируют метастазирование рака через естественные клетки-киллеры. Природа 507 , 508–512 (2014).
CAS PubMed PubMed Central Статья Google Scholar
Паолино М. и Пеннингер Дж. М. Роль рецепторов семейства ТАМ в функции иммунных клеток: значение для терапии рака. Раки 8 , 97 (2016).
PubMed Central Статья CAS Google Scholar
Национальная медицинская библиотека США. ClinicalTrials.gov https://clinicaltrials.gov/ct2/show/NCT03141177 (2020).
Хеемскерк, Б., Квистборг, П. и Шумахер, Т. Н. Антигеном рака. EMBO J. 32 , 194–203 (2013).
CAS PubMed Статья Google Scholar
Le, D. T. et al. Блокада PD-1 в опухолях с дефицитом репарации несовпадений. N. Engl. J. Med. 372 , 2509–2520 (2015).
CAS PubMed PubMed Central Статья Google Scholar
Le, D. T. et al. Дефицит репарации несоответствия предсказывает ответ солидных опухолей на блокаду PD-1. Наука 357 , 409–413 (2017).
CAS PubMed PubMed Central Статья Google Scholar
Motzer, R.J. et al. Ниволумаб в сравнении с эверолимусом при запущенной почечно-клеточной карциноме. N. Engl. J. Med. 373 , 1803–1813 (2015).
CAS PubMed PubMed Central Статья Google Scholar
Motzer, R.J. et al. Сравнение ниволумаба и ипилимумаба с сунитинибом при запущенной почечно-клеточной карциноме. N. Engl. J. Med. 378 , 1277–1290 (2018).
CAS PubMed PubMed Central Статья Google Scholar
Ву, С. Р., Корралес, Л. и Гаевски, Т. Ф. Путь STING и микросреда опухоли, воспаленной Т-клетками. Trends Immunol. 36 , 250–256 (2015).
CAS PubMed PubMed Central Статья Google Scholar
Оценка участков метастазов светлоклеточной, папиллярной и хромофобной почечно-клеточной карциномы и их связь с выживаемостью | Онкология | Открытие сети JAMA
Ключевые моментыВопрос При метастатической почечно-клеточной карциноме (ПКР) различаются ли паттерны метастазирования между гистологическими подтипами и связаны ли участки метастазирования с выживаемостью?
Выводы В этом когортном исследовании, включавшем 10105 пациентов, характер метастазирования значительно варьировался между метастатическим светлоклеточным ПКР, папиллярным ПКР и хромофобным ПКР.Места метастазирования были связаны с выживаемостью во всех гистологических подтипах.
Значение Эти данные подчеркивают клиническую и биологическую вариабельность между гистологическими подтипами метастатического ПКР и предполагают, что паттерны метастазов могут отражать различия в биологии основного заболевания.
Важность Существует значительная биологическая и клиническая изменчивость между гистологическими вариантами метастатической почечно-клеточной карциномы (мПКР).Данные о паттернах метастазов в гистологических вариантах мПКР немногочисленны.
Объектив Охарактеризовать участки метастазирования и их связь с выживаемостью в трех наиболее распространенных гистологических вариантах мПКР: светлоклеточный (ccRCC), папиллярный (pRCC) и хромофобный (chrRCC).
Дизайн, обстановка и участники В этом многоцентровом международном когортном исследовании база данных Международного консорциума баз данных мПКР (IMDC) использовалась для выявления последовательных пациентов, начавших системную терапию мПКР в период с 2002 по 2019 год.Пациенты со смешанным гистологическим подтипом были исключены. Статистический анализ проводился с февраля по июнь 2020 года.
Экспозиции Были собраны данные о гистологическом подтипе и участках метастатического поражения на момент первого начала системной терапии.
Основные результаты и мероприятия Основными исходами были распространенность поражения метастатических очагов и общая выживаемость (ОВ) с момента начала системной терапии. Пациенты с множественными участками метастазирования были включены в анализ всех групп, в которые у них были метастазы.
Результаты Всего подходили для анализа 10105 пациентов. Средний возраст (межквартильный размах) на момент постановки диагноза составил 60 (53-67) лет, 7310 (72,4%) были мужчинами и 8526 (84,5%) перенесли нефрэктомию. Из них 9252 (92%) имели ccRCC, 667 (7%) имели pRCC и 186 (2%) имели chrRCC. Среднее количество участков метастазирования составляло 2 (диапазон 0-7). При CCRCC наиболее частыми участками метастазов были легкие (70%; 6189 из 8804 пациентов [448 отсутствуют]), лимфатические узлы (45%; 3874 из 8655 пациентов [597 отсутствуют]), кость (32%; 2847 из 8817 пациентов. [435 отсутствуют]), печень (18%; 1560 из 8804 [448 отсутствуют]) и надпочечники (10%; 678 из 6673 пациентов [2579 отсутствуют]).Сайты метастазов различались между подтипами. Метастазы в легких, надпочечниках, головном мозге и поджелудочной железе чаще встречались при CCRCC, поражение лимфатических узлов чаще было в pRCC, а метастазы в печень чаще встречались при chrRCC. Медиана OS для ccRCC варьировала в зависимости от места метастатического поражения, в пределах от 16 месяцев (95% ДИ, 13,7–18,8 месяцев) для плевры и 50 месяцев (95% ДИ, 41,1–55,5 месяцев) для поджелудочной железы. По сравнению с ccRCC, пациенты с pRCC, как правило, имели более низкую OS, независимо от места метастазирования.
Выводы и актуальность Сайты метастатического поражения различаются в зависимости от гистологического подтипа мПКР и связаны с ОС. Эти данные подчеркивают клиническую и биологическую изменчивость между гистологическими подтипами мПКР. Характер метастатического распространения может отражать различия в биологии основного заболевания. Приветствуется дальнейшая работа по изучению различий в иммунных, молекулярных и генетических профилях между метастатическими участками и гистологическими подтипами.
Почечно-клеточный рак (ПКР) включает гетерогенную группу злокачественных новообразований, возникающих из нефрона.Имея более десятка признанных гистологических вариантов почечно-клеточных опухолей, 1 ПКР могут широко варьироваться по своим генетическим, патологическим и клиническим характеристикам. Три наиболее распространенных гистологических варианта ПКР включают светлоклеточный ПКР (ccRCC), папиллярный ПКР (pRCC) и хромофобный ПКР (chrRCC), что составляет от 75% до 85%, от 10% до 15% и от 5% до 10% всего почки. раки соответственно. 2 , 3 Комплексные молекулярные и генетические анализы, проведенные с помощью программы «Атлас генома рака» (TCGA), продемонстрировали, что эти подтипы ПКР биологически различны. 4 -6 Ожидается, что клиническое поведение подтипов ПКР также неоднородно, что, вероятно, является результатом различий в биологии основного заболевания между гистологическими вариантами. 7 -11
Одним из проявлений различных биологических основ и вытекающего из этого клинического поведения является характер распространения заболевания у пациентов с метастатическим ПКР (мПКР). Наиболее частые места поражения метастазами при ccRCC хорошо охарактеризованы и включают легкие, лимфатические узлы, кости и печень. 12 , 13 Однако частота поражения менее распространенных метастатических участков для этого подтипа недостаточно описана. Кроме того, участки метастазов в pRCC и chrRCC не были так хорошо охарактеризованы в литературе, и как картина распространения этих гистологических вариантов сравнивается с ccRCC, неясно.
Поскольку участки метастатического поражения могут отражать различия в биологии основного заболевания, клиническое поведение мПКР может варьироваться в зависимости от характера поражения органов, даже в пределах одного гистологического подтипа.Действительно, в отдельных сериях сообщалось, что пациенты с мПКР, метастазировавшим в эндокринные органы, такие как поджелудочная железа, могут иметь необычные клинические результаты, которые могут быть результатом благоприятной биологии основного заболевания. 14 , 15 Альтернативно, метастазы в другие органы, такие как печень, кости и / или мозг, связаны с плохими исходами у пациентов с мПКР. 13 , 16 , 17
Используя клиническую базу данных Международного консорциума баз данных мПКР (IMDC) — большую международную базу данных, состоящую из более чем 11000 пациентов из более чем 40 учреждений по всему миру — мы стремились охарактеризовать и сравнить частоту поражения метастатических участков по 3 основным гистологическим подтипам ПКР и оценить связь между местом метастатического поражения и выживаемостью.
Дизайн исследования и отбор пациентов
Используя базу данных IMDC, мы провели анализ последовательных пациентов с мПКР из 40 международных центров. Данные были собраны из больничных и аптечных записей в период с 1 января 2005 г. по 31 декабря 2019 г. с использованием единого программного обеспечения для баз данных и шаблонов.Все участвующие центры получили одобрение местного совета по этике исследований до начала сбора данных. Отказ от согласия был одобрен местными советами по этике исследований всех участвующих учреждений, чтобы способствовать максимальному охвату местных популяций пациентов и минимизировать предвзятость. Все данные о пациентах были деидентифицированы. Результаты представлены в соответствии с Руководством по отчетности по усилению отчетности наблюдательных исследований в эпидемиологии (STROBE).
Были включены все пациенты с метастатическим CCRCC, pRCC и chrRCC, которые начали системную терапию в период с 2002 по 2019 гг.Были собраны участки метастатического поражения, известные на момент первого начала системной терапии метастатического заболевания. Пациенты со смешанным гистологическим профилем (т.е. 2 или более гистологических подтипа при гистопатологической оценке) были исключены.
Данные, касающиеся демографических характеристик пациента, исходных характеристик, факторов риска IMDC (гемоглобин ниже нижнего предела нормы, количество тромбоцитов больше верхнего предела нормы, количество нейтрофилов больше верхнего предела нормы, скорректированный кальций больше верхнего предела нормального состояния, рабочего статуса по Карновски <80% и времени от постановки диагноза до лечения <1 года), 18 детали опухоли и лечения, участки метастатического поражения и выживаемость были извлечены из IMDC.Представляющими интерес показателями исходов были распространенность поражения метастатических очагов и общая выживаемость (ОВ). ОВ рассчитывали от момента начала системной терапии первой линии до смерти по любой причине или цензурировали во время последнего наблюдения.
Демографические характеристики пациентов и исходные характеристики описываются с использованием пропорций (%) для категориальных переменных и медиан (размах или межквартильный размах [IQR]) для непрерывных переменных.Различия в категориальных и непрерывных переменных оценивались с помощью теста χ 2 и теста Краскела-Уоллиса, соответственно. ОС оценивалась по методу Каплана-Мейера. χ 2 тестирование и лог-ранговое тестирование использовались для оценки различий в местах метастазирования и OS, соответственно. Отношения рисков (HR) были рассчитаны с использованием многомерного регрессионного анализа Кокса и скорректированы для контроля дисбаланса в индивидуальных факторах риска IMDC. Сообщается, что все ОР ОС сравнивают вовлеченные и не вовлеченные участки метастазирования (ОР> 1 означает худшую ОС).Пациенты с множественными участками метастазирования были включены в анализ всех групп, в которые у них были метастазы.
P <0,05 считалось значимым. Все статистические проверки были двусторонними. При обнаружении недостающих данных использовался метод удаления дела. Статистическое программное обеспечение SAS версии 9.4 (SAS Institute) использовалось для проведения статистического анализа с февраля по июнь 2020 года.
Из 11514 пациентов 10105 (88%) подходили для анализа и имели доступные данные.Из них средний возраст (IQR) на момент постановки диагноза составлял 60 (53-67) лет, 7310 (72,4%) были мужчинами, 8526 (84,5%) перенесли нефрэктомию и 1034 (12,6%) имели саркоматоидные признаки. Было 9252 пациента с ПКР (92%), 667 пациентов с ПКР (7%) и 186 пациентов с хроническим ПКР (2%). Пациенты с chrRCC с меньшей вероятностью были мужчинами (54%; 101 из 186 пациентов) и с большей вероятностью имели саркоматоидные признаки (21%; 37 из 176 пациентов). Большинство пациентов получали лечение в Северной Америке (50%; 5072 пациента) или Европе (35%; 3515 пациентов).По всей когорте группы риска IMDC были: 19% благоприятных (1530 пациентов), 57% промежуточных (4621 пациент) и 25% плохих (2002 пациенты). Пациенты с пПКР с наименьшей вероятностью имели заболевание благоприятного риска IMDC (14%; 71 пациент) и наиболее вероятно имели заболевание низкого риска IMDC (29%; 150 пациентов). Большинство пациентов получали таргетную терапию VEGF в первой линии (88%; 8895 пациентов). Пациенты с pRCC и chrRCC с меньшей вероятностью получали таргетную терапию VEGF первой линии (71% [475 из 667 пациентов] и 72% [134 из 186 пациентов] соответственно).Базовые характеристики приведены в таблице 1.
Среднее количество участков метастазирования составляло 2 (диапазон 0–7 участков). (Пациенты с 0 задокументированными участками метастазов могут иметь рецидивы и / или метастазы в области, не зарегистрированные в базе данных IMDC [например, локорегиональный рецидив, кожа и мягкие ткани, околоушная железа, другие атипичные участки].) Наиболее распространенные участки поражения метастазами во всей когорте были легкие, лимфатические узлы, кости, печень, надпочечники и мозг.Менее частые места метастазирования (<5%) включали поджелудочную железу, плевру, брюшину, селезенку, щитовидную железу и кишечник.
Сайты метастазирования по гистологическому варианту показаны на рисунке 1. Места метастазирования значительно различались между гистологическими подтипами (eTable 1 в Приложении). Метастазы в легких, надпочечниках, головном мозге и поджелудочной железе чаще встречались при CCRCC, лимфатические узлы и перитонеальные метастазы чаще встречались при pRCC, а метастазы в печень чаще встречались при chrRCC. Примерно у трети пациентов были метастазы в кости всех трех гистологических подтипов.Частота метастазов в мозг составляла 8% при ccRCC, 3% при pRCC и 2% при chrRCC (рис. 1).
IMDC групп риска по участкам метастатического поражения ccRCC представлены на электронном рисунке в Приложении. Пациенты с метастазами в поджелудочную железу и щитовидную железу имели самый высокий уровень заболевания с благоприятным риском (34% и 37% соответственно) и самый низкий уровень заболевания с низким риском (12% и 17% соответственно). Участки с тенденцией к заболеванию повышенного риска (благоприятный риск <20% и низкий риск> 30%) были костями, печенью, плеврой и кишечником.
Пациенты с метастатическим поражением только 1 участка наблюдались у 3047 пациентов с ПКР (33%), 248 пациентов с ПКР (37%) и 80 пациентов с хроническим ПКР (43%) ( P = 0,001). При CCRCC наиболее частыми участками одиночных метастазов были легкие (54%; 1652 из 3036 пациентов [11 отсутствуют]), кость (18%; 557 из 3038 пациентов [9 отсутствуют]), лимфатические узлы (16%; 481 из 2955 пациентов). пациентов [92 пропавших без вести]) и печени (6%; 193 из 3033 пациентов [14 пропавших без вести]). На всех остальных сайтах было меньше 3%.Поджелудочная железа и мозг были единичным местом метастазирования у 2,3% (51 из 2186 пациентов [861 отсутствующий]) и 1,4% (43 из 3030 пациентов [17 пропавших без вести]), соответственно.
Среднее количество одновременно задействованных сайтов для каждого сайта метастазирования показано в eTable 2 в Приложении. Не было значимой связи между возрастом на момент постановки диагноза мПКР и количеством метастатических участков.
Мы выполнили апостериорный исследовательский анализ скорости дифференцировки саркоматоидов у пациентов с хроническим ПКР.Мы обнаружили, что частота дифференцировки саркоматоидов среди пациентов с метастатическим хроническим ПКР и поражением легких, лимфатических узлов, костей и печени составляет 38%, 23%, 14% и 18% соответственно.
Выживаемость существенно варьировала в зависимости от места поражения метастазом. Результаты OS по участкам метастатического поражения у пациентов с ccRCC показаны на рисунке 2. Для этих пациентов медиана OS варьировалась от 16 месяцев (плевра) до 50 месяцев (поджелудочная железа).Метастазы в печень, мозг и плевру были связаны с самым коротким медианным временем выживаемости (<18 месяцев).
Из-за меньшего числа пациентов в когортах pRCC и chrRCC OS была рассчитана только для 4 наиболее распространенных участков метастазов (легкие, лимфатические узлы, кости и печень). По сравнению с пациентами с ПКР, пациенты с ПКР имели более низкую выживаемость по всем участкам метастазов. Напротив, пациенты с chrRCC обычно имели более длительное время OS по сравнению с пациентами с ccRCC, за заметным исключением пациентов с поражением легких.Среди пациентов с метастазами в легкие медиана выживаемости была ниже у пациентов с chrRCC по сравнению с ccRCC (14,1 месяца [95% ДИ, 8,2–23,8 месяца] против 25,1 месяца [24,1–26,0 месяцев]; P <0,001). Различия в OS не достигли значимости у пациентов с метастазами в печень. Результаты ОВ по участкам метастазирования и гистологическому профилю представлены в Таблице 2.
Результаты нашего когортного исследования показывают, что паттерны метастазирования значительно различаются среди 3 наиболее распространенных гистологических подтипов ПКР и что участки поражения метастазами связаны с выживаемостью.Насколько нам известно, они представляют собой самые большие когорты для характеристики участков метастазирования и отчета о результатах, специфичных для метастатического ccRCC, pRCC и chrRCC.
Для всех 3 гистологических вариантов 5 наиболее частых участков метастатического поражения были одинаковыми: легкие, лимфатические узлы, кость, печень и надпочечники. Однако доля пациентов с метастазами в каждый участок органа часто существенно различалась между подтипами. Например, у пациентов с метастатическим ccRCC вероятность метастазов в легкие была почти в два раза выше, чем у пациентов с chrRCC, тогда как в случае метастазов в печень верно обратное.
Наши результаты в значительной степени согласуются с предыдущими данными, представленными для каждого гистологического подтипа. В таблице 3 приведены показатели вовлечения метастазов в ряде проспективных и ретроспективных серий пациентов с метастатическим ПКР: 12 , 13,19 -21 pRCC, 22 , 23 и chrRCC. 24 Наши данные заметно согласуются с данными рандомизированных клинических и ретроспективных исследований, о которых сообщалось ранее.
Из этих предыдущих исследований 2 ретроспективных наблюдательных исследования, проведенных Chandrasekar et al. 13 и Bianchi et al. 12 , в наименьшей степени соответствовали нашим данным, особенно с учетом сообщаемой частоты метастазов в легкие. Однако мы отмечаем несколько ключевых различий в дизайне исследования, которые могут объяснить эти расхождения. А именно, оба исследования не были специфичными для пациентов с ccRCC, использовали административные базы данных популяционного уровня (эпиднадзор, эпидемиология и конечные результаты и общенациональная стационарная выборка, соответственно), основанные на диагностических кодах для выявления метастатических участков, и не собирали специально данные в время начала системной терапии первой линии при метастатическом поражении.Кроме того, в последнем исследовании 12 метастазов в забрюшинное пространство и / или средостение было зарегистрировано отдельно от других метастазов в лимфатические узлы, что, по крайней мере, частично может объяснить необычно низкую частоту метастазов в лимфатические узлы. Нас обнадеживает то, что наши данные хорошо согласуются с результатами знаковых проспективных рандомизированных клинических исследований ccRCC. 19 -21
В этом исследовании пациенты с метастазами в плевру, головной мозг, печень и кости имели самые короткие медианные значения OS.Последние 3 сайта, как хорошо известно, связаны с меньшей выживаемостью при мПКР, 16 с плевральным местом метастазирования, что представляет собой новое открытие. Напротив, метастазы в эндокринные органы (поджелудочная железа, щитовидная железа, надпочечники), хотя и относительно нечастые, были связаны с благоприятными исходами общей выживаемости. Этот результат согласуется с предыдущими данными по более мелким избранным когортам. 14 , 25 , 26 Увеличенное время ОВ, особенно у пациентов с метастазами в поджелудочную железу и щитовидную железу, свидетельствует о благоприятной биологии заболевания в этой группе пациентов.
Действительно, элегантная работа TRACERx Renal Consortium продемонстрировала, что клиническое разнообразие мПКР основано на различных паттернах развития рака. 27 Здесь у пациентов с метастазами поджелудочной железы был отмечен значительно более низкий индекс нестабильности генома по сравнению со всеми другими участками метастатической ткани, что может быть связано с их превосходными клиническими результатами. Другие группы также сообщили об уникальном биологическом профиле ccRCC, который метастазировал в поджелудочную железу. 28
Мы были удивлены, отметив поразительную разницу в OS для пациентов с метастатическим chrRCC с метастазами в легкие (14 месяцев) по сравнению с лимфатическими узлами, костями и печенью (26–28 месяцев) (Таблица 2). Это было особенно примечательно, учитывая, что пациенты с ccRCC или pRCC и метастазами в легкие в нашем исследовании на самом деле имели самую длинную медианную OS из этих участков. Эти результаты могут быть частично связаны с методологическими ограничениями, истинными различиями в биологии основного заболевания или и тем, и другим.С точки зрения дизайна исследования, пациенты с вялотекущими опухолями chrRCC, поражающими легкие, могли быть предпочтительно выбраны для местного лечения (например, метастазэктомии), что привело к смещению в сторону пациентов с худшим прогнозом, начинающих системную терапию. Однако есть данные, свидетельствующие о том, что пациенты с хроническим почечно-клеточным раком и метастазами в легкие могут иметь уникальную биологию заболевания по сравнению с другими участками метастазов. Недавнее исследование 109 пациентов с метастатическим chrRCC показало, что пациенты с метастазами в легкие имели более высокую скорость дифференцировки саркоматоидов (49%), чем другие участки метастазирования, включая лимфатические узлы, кости и печень (29%, 15% и 20%, соответственно). 24 Чтобы оценить эти результаты, мы выполнили аналогичный апостериорный исследовательский анализ нашей собственной когорты пациентов с chrRCC и получили аналогичные результаты со скоростью дифференциации саркоматоидов среди пациентов с метастатическим chrRCC и вовлечением легких, лимфатических узлов, костей и печень — 38%, 23%, 14% и 18% соответственно. Рекомендуются дальнейшие усилия по исследованию того, подтверждаются ли эти предварительные и неожиданные результаты данными других когорт.
Метастазы в головной мозг представляют особый интерес, поскольку они, как правило, связаны с очень плохим прогнозом, высокой степенью заболеваемости, требуют специальной оценки (т. Е. Не регистрируются при рутинной визуализации поперечного сечения тела) и относительно не поддаются обычным системным исследованиям. терапия.8% -ная частота вовлечения головного мозга в ПКПК, а также более низкая частота метастазов в мозг при ПКР и хроническая ПКР, отмеченная в нашем исследовании, согласуются с предыдущими данными. 12 , 13,29 , 30 Очень низкая частота метастазов в мозг при pRCC (3%) и chrRCC (2%) предполагает, что скрининг бессимптомных пациентов на метастазы в мозг в этих группах может иметь меньшую ценность, чем в пациенты с CCRCC. Однако следует отметить, что фактическая частота метастазов в головной мозг может быть выше, чем указано здесь, поскольку небольшие или бессимптомные метастазы в головной мозг могли не быть обнаружены, если не выполнялась стандартная визуализация мозга.
По сравнению с нашими ожидаемыми пропорциями гистологических вариантов, основанными на данных локализованного ПКР, наши наблюдаемые уровни pRCC (7%) и chrRCC (2%) были ниже, чем ожидалось. Это открытие частично может быть объяснено ранее продемонстрированной тенденцией локализованных гистологических вариантов неядерных клеток к более низкому риску рецидива и / или смерти после хирургической резекции, что приводит к асимметричным пропорциям в нашей когорте, состоящей исключительно из пациентов с метастатическим заболеванием. 8 , 9,31 Кроме того, на меньшую долю пациентов с pRCC и chrRCC в нашем исследовании также может частично повлиять тот факт, что наша когорта включала только тех, кто начал системную терапию. Пациенты с этими гистологическими подтипами, возможно, с меньшей вероятностью будут получать системную терапию, поскольку эффективность текущих стандартов лечения мПКР, как правило, считается меньшей в вариантах с непрозрачными клетками. 32
Сильные стороны и ограничения
Сильные стороны нашего исследования включают очень большой размер выборки, международный многоцентровый характер, согласованность результатов с ранее сообщенными цифрами и подробный индивидуальный обзор медицинских карт для каждого пациента, что приводит к очень детализированным и надежным данным.Кроме того, учитывая большой размер выборки, мы смогли сообщить об исходах для редких когорт, включая пациентов с pRCC и chrRCC, в дополнение к менее частым местам метастазирования в ccRCC. Насколько нам известно, это также первое исследование, в котором сравнивалась частота поражения метастатических участков среди гистологических вариантов из одной когорты.
У нашего исследования есть несколько важных ограничений. Во-первых, база данных IMDC включает только пациентов с мПКР, которые начали системное лечение метастатического заболевания.Таким образом, пациенты с метастатическим заболеванием, управляемым альтернативными стратегиями, включая активное наблюдение, терапию, направленную на метастазирование (например, метастазэктомию, стереотаксическую лучевую терапию тела) и / или только лучшую поддерживающую терапию, и никогда не начинающие системную терапию, не учитываются. Следовательно, вероятно, существуют незначительные группы пациентов с относительно вялотекущим заболеванием (группы активного наблюдения и лечения метастазов) или очень агрессивным заболеванием (группа наилучшей поддерживающей терапии), которые не были включены в исследование.В частности, это ограничение может привести к смещению в сторону недооценки количества очень благоприятных участков метастазирования (например, поджелудочной железы, щитовидной железы) и участков с очень плохим прогнозом (например, головного мозга). Во-вторых, были некоторые участки метастазов, которые не были зафиксированы, в том числе метастазы в мягких тканях (кожа, мышцы, жировая ткань) и околоушные железы, а также перинефрические локорегиональные рецидивы. В-третьих, хотя количество участков метастатического поражения было собрано и представлено, общее количество метастатических поражений на пациента не было зафиксировано.В-четвертых, мы не смогли разделить pRCC на известные патологически и генетически разные подтипы, тип 1 и тип 2. 32 В-пятых, мы не смогли сообщить, какие исследования базовой стадии проводились у каждого пациента. Учитывая, что рутинное использование определенных базовых исследований стадии, вероятно, варьируется между практикующими врачами и учреждениями (например, поперечная визуализация мозга и специальная визуализация костей), в практических моделях, вероятно, были несоответствия, которые могли привести к недооценке показателей поражения метастатических участков .
В этом когортном исследовании участки метастазирования различались в зависимости от гистологического подтипа мПКР и были связаны с ОС. Эти данные подчеркивают клиническую и биологическую изменчивость между гистологическими подтипами мПКР. Метастазы в эндокринные органы нечасты, но связаны с самой длинной средней ОС, тогда как метастазы в плевру, мозг, печень и кости связаны с плохой ОС. Эти контрольные значения полезны для консультирования пациентов и разработки дизайна исследования.Приветствуются дальнейшие исследования для характеристики различий в иммунных, молекулярных и генетических профилях между метастатическими участками и гистологическими подтипами.
Принято к публикации: 12 августа 2020 г.
Опубликовано: 21 января 2021 г. doi: 10.1001 / jamanetworkopen.2020.21869
Открытый доступ: Это статья в открытом доступе, распространяемая в соответствии с условиями CC -По лицензии. © 2021 Дудани С. и др. Открытая сеть JAMA .
Автор, ответственный за переписку: Дэниел Ю. К. Хенг, доктор медицины, магистр здравоохранения, FRCPC, Онкологический центр Тома Бейкера, Университет Калгари, 1331 29th St NW, Калгари, Альберта T2N 4N2, Канада ([email protected]).
Вклад авторов: Доктора Дудани и Хенг имели полный доступ ко всем данным в исследовании и несли ответственность за целостность данных и точность анализа данных.
Концепция и дизайн: Dudani, de Velasco, Wells, Pasini, Pal, Heng.
Сбор, анализ или интерпретация данных: Dudani, de Velasco, Wells, Gan, Donskov, Porta, Fraccon, Pasini, Lee, Hansen, Bjarnason, Beuselinck, Yuasa, Kroger, Kanesvaran, Reaume, Canil, Choueiri, Хенг.
Составление рукописи: Дудани, Пазини, Пал, Хенг.
Критический пересмотр рукописи для важного интеллектуального содержания: Дудани, де Веласко, Уэллс, Ган, Донсков, Порта, Фраккон, Ли, Хансен, Бьярнасон, Беселинк, Пал, Юаса, Крогер, Канесваран, Реом, Каниил, Шуэйр , Хэн.
Статистический анализ: Dudani, Wells, Heng.
Административная, техническая или материальная поддержка: Dudani, de Velasco, Gan, Porta, Yuasa, Kroger, Kanesvaran, Choueiri, Heng.
Наблюдение: Ли, Хансен, Чуэири, Хэн.
Раскрытие информации о конфликте интересов: Д-р де Веласко сообщил о получении грантов и личных гонораров от компаний Pfizer, Roche и Ipsen; а также личные гонорары от Bristol-Myers Squibb, Astellas, Janssen, Bayer, Merck и MSD помимо представленных работ.Доктор Уэллс сообщил, что получал личные гонорары от Pfizer помимо представленных работ. Доктор Донсков получил гранты от Pfizer, Ipsen и MSD, помимо представленных работ. Доктор Порта сообщил, что получал личные гонорары от Bristol-Myers Squibb, MSD, Astra Zeneca, Pfizer, Novartis, Ipsen, EUSA, Eisai, General Electric и Roche за пределами представленных работ. Д-р Хансен сообщил о получении гранта / исследовательской поддержки от Novartis, Bristol-Myers Squibb, Genetech, AstraZeneca / Medimmune, Merck, Karyopharm, GSK, Boerhinger-Ingelheim, Pfizer и Roche; и получение консультационных услуг от Merck (оплачивается), GSK (оплачивается), Bristol-Myers Squibb (не оплачивается) и Eisai (оплачивается) вне представленных работ.Д-р Бойзелинк сообщил о получении гонорара за консультационные услуги от компаний Bristol-Myers Squibb, Pfizer, Merck и AstraZeneca; гонорары докладчикам от Bristol-Myers Squibb, Merck; и гранты на исследования от Bristol-Myers Squibb, все помимо представленных работ. Доктор Пал сообщил, что получал личные гонорары от Genentech, Aveo, Eisai, Roche, Pfizer, Novartis, Exelixis, BMS, Ipsen и Astellas за пределами представленных работ. Доктор Канесваран сообщил о получении грантов и личных гонораров от MSD, Bristol-Myers Squibb, Eisai, Ipsen и Pfizer помимо представленных работ.Доктор Реом сообщил, что во время проведения исследования получал личные гонорары от компаний Bayer, Pfizer, Bristol-Myers Squibb, Astra Zeneca, Novartis, Eisai, Ipsen, Merck и Roche. Д-р Канил сообщил о получении личных гонораров от компаний Bayer, Janssen, Pfizer, Ipsen, Bristol-Myers Squibb, Roche, Eisai и AstraZeneca; и гранты на поездки на образование от Sanofi Genzyme, Janssen, Pfizer и Amgen. Д-р Choueiri сообщил о получении грантов и личных гонораров от компаний AstraZeneca, Bristol-Myers Squibb, Merck, Exelixis, Roche, Pfizer и Novartis во время проведения исследования; гранты, личные гонорары и нефинансовая поддержка от Pfizer, гранты от Exelixis, Bristol-Myers Squibb, Merck, Roche / Genentech, а также гранты, личные гонорары от Novartis помимо представленных работ.Д-р Хенг сообщил о получении грантов от Pfizer, Novartis, Bristol-Myers Squibb, Ipsen, Merck и Eisai помимо представленных работ. О других раскрытиях информации не сообщалось.
1.Сригли JR, Делахант B, Eble JN, и другие; Панель ISUP почечных опухолей. Ванкуверская классификация почечной неоплазии Международного общества урологической патологии (ISUP). Am J Surg Pathol . 2013; 37 (10): 1469-1489. DOI: 10.1097 / PAS.0b013e318299f2d1 PubMedGoogle ScholarCrossref 5.Linehan ВМ, Спеллман PT, Рикеттс CJ, и другие; Сеть исследований атласа генома рака. Комплексная молекулярная характеристика папиллярной почечно-клеточной карциномы. N Engl J Med . 2016; 374 (2): 135-145. DOI: 10.1056 / NEJMoa1505917 PubMedGoogle ScholarCrossref 7.Malouf GG, Джозеф RW, Шах AY, Таннир НМ. Почечно-клеточная карцинома с непрозрачными клетками: биологические открытия, терапевтические проблемы и возможности. Clin Adv Hematol Oncol .2017; 15 (5): 409-418.PubMedGoogle Scholar11.Yip SM, Руис Моралес Ю.М., Донсков F, и другие. Результаты метастатической хромофобной почечно-клеточной карциномы (chrRCC) в эпоху таргетной терапии: результаты Международного консорциума базы данных по метастатическим почечным клеткам (IMDC). Рак почки . 2017; 1 (1): 41-47. DOI: 10.3233 / KCA-160002 PubMedGoogle ScholarCrossref 13.Chandrasekar Т, Клаассен Z, Гольдберг H, Кулькарни GS, Гамильтон RJ, Флешнер NE.Метастатическая почечно-клеточная карцинома: модели и предикторы метастазов — современная популяционная серия. Урол Онкол . 2017; 35 (11): 661.e7-661.e14. DOI: 10.1016 / j.urolonc.2017.06.060PubMedGoogle ScholarCrossref 14.Grassi П, Дусе L, Джильоне P, и другие. Клиническое влияние метастазов поджелудочной железы при почечно-клеточной карциноме: многоцентровый ретроспективный анализ. PLoS One . 2016; 11 (4): e0151662. DOI: 10.1371 / journal.pone.0151662 PubMedGoogle Scholar15.Gravis G, Chanez B, Дероса L, и другие; Группа поперечных каналов почек. Влияние железистых метастазов на общую выживаемость пациентов с метастатической светлоклеточной почечно-клеточной карциномой в эпоху антиангиогенной терапии. Урол Онкол . 2016; 34 (4): 167.e17-167.e23. DOI: 10.1016 / j.urolonc.2015.10.015PubMedGoogle ScholarCrossref 17.Beuselinck B, Удар S, Рикс О, и другие. Негативное влияние метастазов в кости на исход светлоклеточного почечно-клеточного рака, леченного сунитинибом. Энн Онкол . 2011; 22 (4): 794-800. DOI: 10.1093 / annonc / mdq554 PubMedGoogle ScholarCrossref 18.Heng ДЙ, Се W, Риган ММ, и другие. Факторы прогноза общей выживаемости у пациентов с метастатической почечно-клеточной карциномой, получавших препараты, нацеленные на фактор роста эндотелия сосудов: результаты большого многоцентрового исследования. Дж. Клин Онкол . 2009; 27 (34): 5794-5799. DOI: 10.1200 / JCO.2008.21.4809PubMedGoogle ScholarCrossref 19.Motzer RJ, Таннир Нью-Мексико, Макдермотт DF, и другие; CheckMate 214 Следователи.Сравнение ниволумаба и ипилимумаба с сунитинибом при запущенной почечно-клеточной карциноме. N Engl J Med . 2018; 378 (14): 1277-1290. DOI: 10.1056 / NEJMoa1712126 PubMedGoogle ScholarCrossref 20.Rini БИ, Плимак Скорая помощь, Стус V, и другие; KEYNOTE-426 Следователи. Пембролизумаб плюс акситиниб в сравнении с сунитинибом при запущенной почечно-клеточной карциноме. N Engl J Med . 2019; 380 (12): 1116-1127. DOI: 10.1056 / NEJMoa1816714 PubMedGoogle ScholarCrossref 21.Rini Б.И., Паулз Т, Аткинс МБ, и другие; IMmotion151 Study Group.Сравнение атезолизумаба и бевацизумаба с сунитинибом у пациентов с ранее нелеченым метастатическим почечно-клеточным раком (IMmotion151): многоцентровое открытое рандомизированное контролируемое исследование фазы 3. Ланцет . 2019; 393 (10189): 2404-2415. DOI: 10.1016 / S0140-6736 (19) 30723-8 PubMedGoogle ScholarCrossref 22.Escudier B, Молини V, Бракарда S, и другие. Открытое исследование фазы 2 монотерапии эверолимусом первой линии у пациентов с папиллярно-метастатической почечно-клеточной карциномой: окончательный анализ RAPTOR. Eur J Cancer . 2016; 69: 226-235. DOI: 10.1016 / j.ejca.2016.08.004PubMedGoogle ScholarCrossref 23.Choueiri Т.К., Вайшампаян U, Розенберг JE, и другие. Фаза II и исследование биомаркеров двойного ингибитора MET / VEGFR2 форетиниба у пациентов с папиллярной почечно-клеточной карциномой. Дж. Клин Онкол . 2013; 31 (2): 181-186. DOI: 10.1200 / JCO.2012.43.3383 PubMedGoogle ScholarCrossref 24.Ged Y, Чен Ю.Б., Кнежевич А, и другие.Метастатическая хромофобная почечно-клеточная карцинома: наличие или отсутствие саркоматоидной дифференцировки определяет клинический курс и результаты лечения. Clin Genitourin Cancer . 2019; 17 (3): e678-e688. DOI: 10.1016 / j.clgc.2019.03.018 PubMedGoogle ScholarCrossref 26.Beutner U, Леоварди C, Bork U, и другие. Выживаемость после метастазирования почечно-клеточной карциномы в щитовидную железу: опыт единого центра и систематический обзор литературы. Щитовидная железа .2015; 25 (3): 314-324. DOI: 10.1089 / thy.2014.0498 PubMedGoogle ScholarCrossref 29.Cagney DN, Мартин AM, Каталано PJ, и другие. Заболеваемость и прогноз пациентов с метастазами в головной мозг при диагностике системных злокачественных новообразований: популяционное исследование. Нейро Онкол . 2017; 19 (11): 1511-1521. DOI: 10.1093 / neuonc / nox077 PubMedGoogle ScholarCrossref 30.Sun М, Де Веласко G, Брастианос ПК, и другие. Развитие метастазов в мозг у пациентов с почечно-клеточной карциномой: эпидемиологические тенденции, выживаемость и клинические факторы риска с использованием популяционной когорты. Евро Urol Focus . 2019; 5 (3): 474-481. DOI: 10.1016 / j.euf.2017.12.007 PubMedGoogle ScholarCrossref 31.Beck С.Д., Патель Мичиган, Снайдер Я, и другие. Влияние папиллярных и хромофобных клеток на выживаемость без признаков заболевания после нефрэктомии по поводу почечно-клеточного рака. Энн Сург Онкол . 2004; 11 (1): 71-77. DOI: 10.1007 / BF02524349 PubMedGoogle ScholarCrossrefПрогноз светлоклеточного почечно-клеточного рака (ccRCC) на основе оценки риска на основе шести днРНК: исследование, основанное на данных секвенирования РНК | Журнал трансляционной медицины
Lasser C, Shelke GV, Yeri A, Kim DK, Crescitelli R, Raimondo S, Sjostrand M, Gho YS, Van Keuren Jensen K, Lotvall J. Две отдельные сигнатуры внеклеточной РНК, выделяемые одним типом клеток, идентифицированным с помощью микрочипа и следующего: секвенирование поколений. RNA Biol. 2017; 14: 58–72.
PubMed Статья Google Scholar
Барас А.С., Митчелл С.Дж., Майерс Дж.Р., Гупта С., Венг Л.С., Эштон Дж.М., Корниш ТК, Пандей А., Галушка М.К. miRge — мультиплексный метод обработки данных малых РНК-Seq для определения энтропии микроРНК.PLoS ONE. 2015; 10: e0143066.
PubMed PubMed Central Статья Google Scholar
Ravo M, Cordella A, Rinaldi A, Bruno G, Alexandrova E, Saggese P, Nassa G, Giurato G, Tarallo R, Marchese G, Rizzo F, Stellato C, Biancardi R, Troisi J, Di Spiezio Сардо А., Зулло Ф., Вайс А., Гуида М. Нарушение регуляции малой некодирующей РНК в канцерогенезе эндометрия. Oncotarget. 2015; 6: 4677–91.
PubMed PubMed Central Статья Google Scholar
Hombach S, Kretz M. Некодирующие РНК: классификация, биология и функционирование. Adv Exp Med Biol. 2016; 937: 3–17.
CAS PubMed Статья Google Scholar
Вей З., Батагов А.О., Картер Д.Р., Кричевский А.М. РНК фетальной бычьей сыворотки мешает внеклеточной РНК, полученной из культуры клеток. Научный доклад 2016; 6: 31175.
CAS PubMed PubMed Central Статья Google Scholar
Lefebvre FA, Benoit Bouvrette LP, Perras L, Blanchet-Cohen A, Garnier D, Rak J, Lecuyer E. Сравнительный транскриптомный анализ внеклеточных везикул человека и дрозофилы . Научный доклад 2016; 6: 27680.
CAS PubMed PubMed Central Статья Google Scholar
Сигель Р.Л., Миллер К.Д., Джемаль А. Статистика рака, 2017. CA Cancer J Clin. 2017; 67: 7–30.
Артикул Google Scholar
Chen W, Zheng R, Baade PD, Zhang S, Zeng H, Bray F, Jemal A, Yu XQ, He J. Статистика рака в Китае, 2015. CA Cancer J Clin. 2016; 66: 115–32.
Артикул Google Scholar
Kuthi L, Jenei A, Hajdu A, Nemeth I, Varga Z, Bajory Z, Pajor L., Ivanyi B. Факторы прогноза подтипов почечно-клеточной карциномы, диагностированных в соответствии с классификацией опухолей почек ВОЗ 2016 г .: исследование 928 пациентов. Pathol Oncol Res. 2016 г.https://doi.org/10.1007/s12253-016-0179-x.
PubMed Статья Google Scholar
Malouf GG, Su X, Zhang J, Creighton CJ, Ho TH, Lu Y, Raynal NJ, Karam JA, Tamboli P, Allanick F, Mouawad R, Spano JP, Khayat D, Wood CG, Jelinek J , Таннир НМ. Сигнатура метилирования ДНК выявляет онтогенез клеток почечно-клеточного рака. Clin Cancer Res. 2016; 22: 6236–46.
CAS PubMed PubMed Central Статья Google Scholar
Zhao H, Leppert JT, Peehl DM. Защитная роль рецептора андрогенов в светлоклеточном почечно-клеточном раке основана на данных анализа TCGA. PLoS ONE. 2016; 11: e0146505.
PubMed PubMed Central Статья Google Scholar
He X, Sun F, Guo F, Wang K, Gao Y, Feng Y, Song B, Li W, Li Y. Нокдаун длинной некодирующей РНК FTX подавляет пролиферацию, миграцию и инвазию в почечно-клеточную карциному клетки. Oncol Res. 2017; 25: 157–66.
PubMed Статья Google Scholar
Chen J, Chen Y, Gu L, Li X, Gao Y, Lyu X, Chen L, Luo G, Wang L, Xie Y, Duan J, Peng C, Ma X. LncRNAs действуют как прогностические и диагностические биомаркеры почечно-клеточного рака: систематический обзор и метаанализ. Oncotarget. 2016; 7: 74325–36.
PubMed PubMed Central Google Scholar
Цао И, Сюй Р., Сюй Х, Чжоу И, Цуй Л., Хэ Х.Подавление днРНК CASC2 с помощью микроРНК-21 увеличивает пролиферацию и миграцию клеток почечно-клеточной карциномы. Мол Мед Реп. 2016; 14: 1019–25.
CAS PubMed Статья Google Scholar
Лю З., Ян Х.Й., Ся С.Ю., Чжан С., Сю Ю.С. Подавление длинной некодирующей РНК TRIM52-AS1 действует как опухолевый супрессор при почечно-клеточной карциноме. Мол Мед Реп. 2016; 13: 3206–12.
CAS PubMed Статья Google Scholar
Лю Х., Чен П., Цзян Ц., Хань Дж., Чжао Б., Ма И, Мардан М. Скрининг ключевых мишеней днРНК, связанных с метастазами светлоклеточной карциномы почек. Медицина. 2016; 95: e2507.
PubMed PubMed Central Статья Google Scholar
Сяо Х, Тан К., Лю П, Чен К., Ху Дж, Цзэн Дж, Сяо В., Ю Г, Яо В., Чжоу Х, Ли Х, Пан И, Ли А., Е З, Ван Дж. , Xu H, Huang Q. LncRNA MALAT1 функционирует как конкурирующая эндогенная РНК, чтобы регулировать экспрессию ZEB2 путем размягчения miR-200 в светлоклеточной карциноме почки.Oncotarget. 2015; 6: 38005–15.
PubMed PubMed Central Google Scholar
Герлински М., Коул С., Скофилд П., Шурч Н.Дж., Шерстнев А., Сингх В., Вробель Н., Гарби К., Симпсон Г., Оуэн-Хьюз Т., Блэкстер М., Бартон Дж. Статистические модели для данных РНК-seq получены из 48-кратного эксперимента с двумя условиями. Биоинформатика. 2015; 31: 3625–30.
PubMed PubMed Central Статья Google Scholar
Tang W, Liao Z, Zou Q. Какой тест статистической значимости лучше всего обнаруживает онкомиРНК в раковых тканях? Исследовательский анализ. Oncotarget. 2016; 7: 85613–23.
PubMed PubMed Central Google Scholar
Tang RX, Chen WJ, He RQ, Zeng JH, Liang L, Li SK, Ma J, Luo DZ, Chen G. Идентификация прогностической сигнатуры на основе RNA-Seq с пятью lncRNAs для плоскоклеточного рака легкого . Oncotarget. 2017. https: // doi.org / 10.18632 / oncotarget.17098.
PubMed PubMed Central Статья Google Scholar
Zeng JH, Liang L, He RQ, Tang RX, Cai XY, Chen JQ, Luo DZ, Chen G. Комплексное исследование новой дифференциально экспрессируемой сигнатуры профиля экспрессии днРНК для оценки выживаемости пациентов с колоректальной аденокарциномой . Oncotarget. 2017; 8: 16811–28.
PubMed PubMed Central Google Scholar
Xu W, Xu B, Yao Y, Yu X, Cao H, Zhang J, Liu J, Sheng H. Сверхэкспрессия и биологическая функция IQGAP3 при раке поджелудочной железы человека. Am J Transl Res. 2016; 8: 5421–32.
CAS PubMed PubMed Central Google Scholar
Langkilde A, Olsen LC, Saetrom P, Drablos F, Besenbacher S, Raaby L, Johansen C., Iversen L. Анализ пути кожи пациентов с псориазом после лечения адалимумабом выявляет новые ранние события в противовоспалительном механизме анти-TNF-альфа.PLoS ONE. 2016; 11: e0167437.
PubMed PubMed Central Статья Google Scholar
Лю П., Сун М., Цзян В., Чжао Дж., Лян С., Чжан Х. Идентификация мишеней miRNA-221 и miRNA-222 при устойчивом к фулвестранту раке молочной железы. Oncol Lett. 2016; 12: 3882–8.
CAS PubMed PubMed Central Статья Google Scholar
Sumimoto H, Takano A, Teramoto K, Daigo Y.Сигнал протеинкиназы, активируемой митогеном RAS, необходим для усиления экспрессии PD-L1 при раке легких человека. PLoS ONE. 2016; 11: e0166626.
PubMed PubMed Central Статья Google Scholar
Ma B, Liao T, Wen D, Dong C, Zhou L, Yang S, Wang Y, Ji Q. Длинная межгенная некодирующая РНК 271 указывает на худший прогноз папиллярного рака щитовидной железы. Научный доклад 2016; 6: 36973.
CAS PubMed PubMed Central Статья Google Scholar
Ван XL, Ши В.П., Ши Х.С., Лу С.К., Ван К., Сун С., Хе Дж.С., Джин В.Г., Ур XX, Цзоу Х., Шу Ю.С. Нокдаун TRIM65 подавляет пролиферацию, миграцию и инвазию клеток рака легких: терапевтическая мишень при раке легких человека. Oncotarget. 2016; 7: 81527–40.
PubMed PubMed Central Google Scholar
Zeng JH, Xiong DD, Pang YY, Zhang Y, Tang RX, Luo DZ, Chen G. Идентификация молекулярных мишеней для диагностики рака пищевода с использованием данных miRNA-seq и RNA-seq из Атласа генома рака: исследование 187 случаев.Oncotarget. 2017; 8: 35681–99.
PubMed PubMed Central Google Scholar
Xia L, Li D, Lin C, Ou S, Li X, Pan S. Сравнительное исследование совместного биоинформатического анализа основного потенциала ‘neimmiR’, miR-212-3P / miR-132-3P, участие в эпилепсии и ее новой роли в развитии рака у человека. Oncotarget. 2017; 8: 40668–82.
PubMed PubMed Central Google Scholar
Ilias A, Lagnel J, Kapantaidaki DE, Roditakis E, Tsigenopoulos CS, Vontas J, Tsagkarakou A. Транскрипционный анализ устойчивости к неоникотиноидам в средиземноморских (MED) популяциях B. tabaci выявил новые цитохромы P450s, но не мутации nAChR, связанные с фенотип. BMC Genomics. 2015; 16: 939.
PubMed PubMed Central Статья Google Scholar
Чжао Дж., Цзэн Х, Сун П, Ву Х, Ши Х.AKT1 как ген-концентратор PageRank связан с меланомой, и его функциональная аннотация тесно связана с сигнальным путем эстрогена, который может регулировать рост меланомы. Онкол Реп. 2016; 36: 2087–93.
CAS PubMed Статья Google Scholar
Амбатипуди С., Герстунг М., Пандей М., Самант Т., Патил А., Кейн С., Десаи Р.С., Шаффер А.А., Беренвинкель Н., Махимкар МБ. Полногеномный анализ экспрессии и количества копий позволяет идентифицировать гены-драйверы при гингивобуккальном раке.Гены Хромосомы Рак. 2012; 51: 161–73.
CAS PubMed Статья Google Scholar
Cui X, Li Y, Yang L, You L, Wang X, Shi C, Ji C, Guo X. Пептидомный анализ грудного молока у женщин, рожающих макросомный плод, выявляет множество средств защиты для младенцев. Oncotarget. 2016; 7: 63514–25.
PubMed PubMed Central Google Scholar
Ян Л., Линь XL, Лян В., Фу С.В., Линь В.Ф., Тиан XQ, Гао Ю.Дж., Чен Х.Й., Дай Дж., Ге З.З. Высокая экспрессия GPR116 указывает на плохой результат выживания и способствует прогрессированию опухоли при колоректальной карциноме. Oncotarget. 2017; 8: 47943–56.
PubMed PubMed Central Google Scholar
Денг М., Блондо Дж. Дж., Шмидт Д., Пернер С., Мюллер С. К., Эллингер Дж. Идентификация новых дифференциально экспрессируемых транскриптов днРНК и мРНК в светлоклеточной почечно-клеточной карциноме путем профилирования экспрессии.Геномические данные. 2015; 5: 173–5.
PubMed PubMed Central Статья Google Scholar
Blondeau JJ, Deng M, Syring I, Schrodter S, Schmidt D, Perner S, Muller SC, Ellinger J. Идентификация новых длинных некодирующих РНК в светлоклеточной почечно-клеточной карциноме. Clin Epigenet. 2015; 7: 10.
Артикул Google Scholar
Fachel AA, Tahira AC, Vilella-Arias SA, Maracaja-Coutinho V, Gimba ER, Vignal GM, Campos FS, Reis EM, Verjovski-Almeida S.Анализ экспрессии и in silico характеристика интронных длинных некодирующих РНК в почечно-клеточной карциноме: возникающие функциональные ассоциации. Молочный рак. 2013; 12: 140.
PubMed PubMed Central Статья Google Scholar
He HT, Xu M, Kuang Y, Han XY, Wang MQ, Yang Q. Биомаркер и потенциал конкурирующей эндогенной РНК опухолеспецифической длинной некодирующей РНК в хромофобной почечно-клеточной карциноме. Oncotargets Ther. 2016; 9: 6399–406.
CAS Статья Google Scholar
Лю Т., Суй Дж., Чжан И, Чжан Х.М., Ву В.Дж., Ян С., Сюй С.Ю., Хун ВМ, Пэн Х, Инь Л.Х., Пу ИП, Лян Г.Й. Всесторонний анализ нового профиля днРНК выявляет потенциальные прогностические биомаркеры светлоклеточной почечно-клеточной карциномы. Oncol Rep. 2018; 40 (3): 1503–14.
CAS PubMed Google Scholar
Qu L, Wang ZL, Chen Q, Li YM, He HW, Hsieh JJ, Xue S, Wu ZJ, Liu B, Tang H, Xu XF, Xu F, Wang J, Bao Y, Wang AB , Wang D, Yi XM, Zhou ZK, Shi CJ, Zhong K, Sheng ZC, Zhou YL, Jiang J, Chu XY, He J, Ge JP, Zhang ZY, Zhou WQ, Chen C, Yang JH, Sun YH, Wang LH.Прогностическое значение длинной некодирующей сигнатуры РНК при локализованной светлоклеточной почечно-клеточной карциноме. Eur Urol. 2018; 74 (6): 756–63.
CAS PubMed Статья Google Scholar
Li M, Wang Y, Cheng L, Niu W, Zhao G, Raju JK, Huo J, Wu B, Yin B, Song Y, Bu R. Длинные некодирующие РНК в почечно-клеточной карциноме: a систематический обзор и клиническое значение. Oncotarget. 2017. https://doi.org/10.18632/oncotarget.17053.
PubMed PubMed Central Статья Google Scholar
Shi D, Qu Q, Chang Q, Wang Y, Gui Y, Dong D. Пятикратная некодирующая сигнатура РНК для улучшения прогноза светлоклеточного почечно-клеточного рака. Oncotarget. 2017. https://doi.org/10.18632/oncotarget.17506.
PubMed PubMed Central Статья Google Scholar
Chen K, Zeng J, Tang K, Xiao H, Hu J, Huang C, Yao W, Yu G, Xiao W, Guan W, Guo X, Xu H, Ye Z. miR-490-5p подавляет рост опухоли в почечно-клеточной карциноме за счет воздействия на PIK3CA.Biol Cell. 2016; 108: 41–50.
CAS PubMed Статья Google Scholar
Varet H, Brillet-Guéguen L, Coppée JY, Dillies MA. SARTools: конвейер R на основе DESeq2 и EdgeR для всестороннего дифференциального анализа данных RNA-Seq. PLoS ONE. 2016; 11 (6): e0157022.
PubMed PubMed Central Статья Google Scholar
Сяо З, Гао З, Дуань И, Юань З, Ке Ю.Подавление miR-19a оказывает ингибирующее действие на метастатическую почечно-клеточную карциному за счет нацеливания на PIK3CA и инактивации передачи сигналов Notch in vitro. Онкол Реп. 2015; 34: 739–46.
CAS PubMed Статья Google Scholar
Ebos JM. Толкать зверя. Оценка воздействия метастазов, вызванных лечением. Cancer Res. 2015; 75: 3427–35.
CAS PubMed Статья Google Scholar
Ma X, Shen D, Li H, Zhang Y, Lv X, Huang Q, Gao Y, Li X, Gu L, Xiu S, Bao X, Duan J, Zhang X. MicroRNA-185 подавляет пролиферацию клеток и индуцирует апоптоз клеток путем нацеливания на VEGFA непосредственно в инактивированной по Хиппель-Линдау светлоклеточной почечно-клеточной карциноме. Урол Онкол. 2015; 33: 169.e161-111.
Артикул Google Scholar
Чен Ю.С., Мэн Ф., Ли Х.Л., Лю QH, Хоу П.Ф., Бай Дж., Чжэн Дж. Дайсер подавляет инвазию, опосредованную MMP-2, и ангиогенез, индуцированный VEGFA, и служит многообещающим прогностическим биомаркером светлоклеточной почечно-клеточной карциномы человека.Oncotarget. 2016; 7: 84299–313.
PubMed PubMed Central Google Scholar
Ван Дж., Вэнь Дж., Йи Р., Лю Ф, Чжоу Дж., Лю Дж., Ли Кью, Ян З, Су X. Высокая селективность ингибиторов PI3 Kβ при SETD2-мутированной почечной светлоклеточной карциноме. J BUON. 2015; 20: 1267–75.
PubMed Google Scholar
Huang JL, Liao Y, Qiu MX, Li J, An Y. Длинная некодирующая РНК CCAT2 способствует пролиферации и инвазии клеток посредством регулирования пути передачи сигналов Wnt / бета-катенина в светлоклеточной почечно-клеточной карциноме.Tumor Biol. 2017; 39: 1010428317711314.
PubMed Google Scholar
Li M, Pei X, Wang G, Zhan J, Du J, Jiang H, Tang Y, Zhang H, He H. Kindlin2 способствует прогрессированию светлоклеточной почечно-клеточной карциномы через сигнальный путь Wnt. Онкол Реп. 2017; 38: 1551–60.
CAS PubMed Статья Google Scholar
Brooks SA, Brannon AR, Parker JS, Fisher JC, Sen O, Kattan MW, Hakimi AA, Hsieh JJ, Choueiri TK, Tamboli P, Maranchie JK, Hinds P, Miller CR, Nielsen ME, Rathmell WK .ClearCode34: прогностический индикатор риска локализованной светлоклеточной почечно-клеточной карциномы. Eur Urol. 2014; 66: 77–84.
CAS PubMed PubMed Central Статья Google Scholar
Рини Б.И., Эскудье Б., Мартини Дж. Ф. Подтверждение оценки рецидива по 16 генам у пациентов с локорегиональной почечно-клеточной карциномой высокого риска по результатам исследования III фазы адъювантного сунитиниба.
