Почему понижены нейтрофилы и что с этим делать
Нейтрофилы — это один из видов белых кровяных телец (лейкоцитов). Все лейкоциты помогают организму бороться с инфекциями. Конкретно нейтрофилы особенно важны при бактериальных заболеваниях, например ангине или бронхите.
Сниженный уровень нейтрофилов в крови называют нейтропенией. Это состояние означает, что ваша иммунная система ослабла и не может эффективно противостоять бактериям. То есть вы более уязвимы для всевозможных инфекций.
Какой уровень нейтрофилов считается низким
Нейтропению диагностируют, если количество нейтрофилов в крови оказывается менее 1 500 на микролитр. Некоторые врачи считают , что порог составляет 1 800 на микролитр.
По степени тяжести состояние характеризуют так:
- 1 000–1 500/мкл — лёгкая нейтропения;
- 500–1 000/мкл — умеренная;
- менее 500/мкл — тяжёлая.
Как узнать, что нейтрофилы понижены
Часто люди с нейтропенией даже не догадываются о том, что в их крови не хватает белых кровяных телец: лёгкая форма не имеет симптомов. В более сложных случаях нарушение может проявлять себя:
- то и дело повторяющимися бактериальными инфекциями: отитами, гингивитами, кожными воспалениями;
- отёчностью;
- регулярными и на первый взгляд необъяснимыми повышениями температуры.
Однако по симптомам нейтропению устанавливают крайне редко. В большинстве случаев снижение уровня нейтрофилов обнаруживается случайно — при анализе крови, который делают по каким‑то другим причинам.
Впрочем, даже если первое исследование показало, что нейтрофилов недостаточно, о нейтропении говорить рано. Количество лейкоцитов в крови может меняться с течением времени, то повышаясь, то снижаясь, и это абсолютно нормально. Поэтому лечащий врач предложит вам повторить общий анализ крови, прежде чем поставит диагноз.
Когда надо срочно обращаться за помощью
В тяжёлых случаях дефицита нейтрофилов даже «родные» бактерии — те, что живут в здоровом желудочно‑кишечном тракте или, положим, на слизистой рта, — могут вызвать серьёзное заболевание. А любая инфекция способна почти молниеносно стать смертельной.
А любая инфекция способна почти молниеносно стать смертельной.
Как можно быстрее свяжитесь со своим врачом или, в зависимости от состояния, вызывайте скорую, если на фоне диагностированной нейтропении наблюдаете один, а тем более сразу несколько из перечисленных симптомов :
- Лихорадка. О ней говорят, если температура поднялась выше 38 °C.
- Озноб и потливость.
- Навязчивый или сильный кашель, если его не было ранее. Также опасным признаком является усиление уже существующего кашля.
- Одышка.
- Боль во рту.
- Боль в горле.
- Любые заметные изменения в мочеиспускании: резь, боль, раздражение кожи и слизистой, изменение цвета и консистенции мочи.
- Диарея.
- Рвота.
- Покраснение или отёк вокруг малейшей царапины или пореза.
- Выделения из влагалища, которых не было ранее.
- Жёсткая шея. Об этом признаке говорят, если вам больно поворачивать или наклонять голову либо вы не можете откинуть её назад.
- Ощутимая боль в любой части тела (ноге, руке, животе, грудной клетке), если её не было ранее.
Почему понижены нейтрофилы
Нейтропения возникает , когда нейтрофилы расходуются или разрушаются быстрее, чем костный мозг успевает их производить. Либо же если он сам по себе не способен вырабатывать их в достаточном количестве. Это может быть вызвано разными заболеваниями или состояниями.
Вот самые распространённые причины , из‑за которых понижается уровень нейтрофилов в крови.
1. Инфекции
Нейтрофилы падают при следующих заболеваниях:
- Мононуклеоз (вирус Эпштейна — Барр).
- Гепатиты. Чаще всего трёх типов: А, В, С, в острой и хронической формах.
- Ветрянка.
- Корь.
- Туберкулёз.
- Болезнь Лайма.
- Сальмонеллёзная инфекция.
- ВИЧ/СПИД.
- Сепсис (заражение крови).
2. Некоторые аутоиммунные заболевания
К ним относятся:
- Ревматоидный артрит.

- Системная красная волчанка.
- Гранулематоз с полиангиитом.
- Болезнь Крона.
3. Заболевания костного мозга и крови
Например, апластическая анемия, миелодиспластические синдромы, миелофиброз (необычный тип рака костного мозга) или лейкемия — рак крови.
4. Химиотерапия, применяемая при лечении рака
Такие процедуры необходимы: они уничтожают злокачественные образования. Однако вместе с раковыми клетками под раздачу попадают и здоровые, нейтрофилы в том числе.
5. Приём некоторых лекарств
Понизить уровень нейтрофилов могут:
- Препараты, которые применяют для лечения избыточной активности щитовидной железы (гипертиреоза).
- Антибиотики, включая распространённые, например на основе пенициллина.
- Противовирусные средства.
- Противовоспалительные лекарства. В частности, те, что используют для терапии язвенного колита или ревматоидного артрита.
- Антипсихотические средства.
- Препараты для лечения сердечной аритмии.
6. Недостаток витаминов или минералов
Уровень нейтрофилов может понизиться, если вы не получаете в нужном количестве витамин В12, фолиевую кислоту или медь.
7. Влияние недоизученных факторов
Иногда нейтропения бывает врождённой. А в некоторых случаях её причины и вовсе установить не получается — тогда говорят об идиопатическом (неизвестной природы) нарушении.
Что делать с нейтропенией
Некоторые типы нейтропении в терапии не нуждаются : они рассматриваются как индивидуальная особенность. Другие успешно корректируются отменой лекарств, вызвавших такой побочный эффект, или, например, лечением основного инфекционного заболевания — ветрянки, кори, гепатита.
Однако решать, что делать в вашем конкретном случае, должен только квалифицированный врач — терапевт или другой специалист, который обнаружил нарушение.
Читайте также 🩸🧬🦠
повышены нейтрофилы понижены лимфоциты у ребенка
Здравствуйте, Дорогие читатели! С вами Екатерина. И сегодня я хочу рассказать про белые кровяные клетки нейтрофилы и лимфоциты. Почему повышены нейтрофилы и понижены лимфоциты у ребёнка.
И сегодня я хочу рассказать про белые кровяные клетки нейтрофилы и лимфоциты. Почему повышены нейтрофилы и понижены лимфоциты у ребёнка.
Содержание статьи
Разговор в поликлинике
Недавно сидя в поликлинике, при чуть открытой двери, я услышала разговор мамочки с педиатром о том, что в анализах ребёнка повышены лимфоциты. В ожидании своей очереди я задумалась, а все ли мамы знают, что такое лимфоциты и за что они отвечают. Так вот давайте разберемся.
Белые кровяные клетки или лейкоциты — это клетки, которые используют ваше тело для борьбы с инфекциями. Существуют различные типы лейкоцитов, каждый из которых отвечает за борьбу с различными микробами.
Итак, давайте познакомимся с ними поближе.
Нейтрофилы
Нейтрофилы — это тип лейкоцитов, который защищает нас от инфекций. Они составляют примерно 40-60 % лейкоцитов в нашем организме и являются первыми клетками, которые встают на защиту нашего организма от бактериальных инфекций.
Нормальное количество нейтрофилов составляет от 2500 до 7500 на микролитр крови.
Количество нейтрофилов может быть высоким например при инфекциях или лейкемии. Физический или эмоциональный стресс, также может повысить его уровень. Низкое количество нейтрофилов также может быть заболеванием лейкемии, некоторыми инфекциями, дефицитом витамина B12, химиотерапией и другим.
Самое главное, что эти кровяные клетки помогают нам в борьбе с бактериальными инфекциями и количество лимфоцитов увеличивается при вирусных заболеваниях. Уровень лейкоцитов, зависит от возраста и пола ребёнка.
Костный мозг генерирует в организме запас белых клеток крови, поэтому любое заболевание, которое влияет на костный мозг, может уменьшить количество клеток в кровотоке. Например, подавляющие бактериальные инфекции могут разрушать нейтрофилы быстрее, чем они производятся. Вирусы могут проникать в костный мозг и влиять на выработку лейкоцитов.
И есть ещё один тип белых кровях клеток, с которым я считаю, вы должны познакомиться.
Лимфоциты
Лимфоциты — этот тип белых кровяных клеток, выполняет несколько функций в иммунной системе, включая защиту от бактерий, вирусов, грибков и паразитов.
Лимфоциты уничтожают вирусы и борются с хроническими инфекциями.
Изменение показателей лимфоцитов, в общем анализе говорит, о нарушении функции кроветворения или инфекции в организме.
Лимфоциты обычно составляют от 20 до 40% всех лейкоцитов в кровотоке.
Низкое количество лимфоцитов, называется лимфоцитопения, обычно происходит потому, что:
- ваше тело не производит достаточно лимфоцитов
- лимфоциты попали в селезенку или лимфатические узлы
Лимфоцитопения может указывать на ряд различных заболеваний, такие какие как грипп или легкие инфекции, не являющиеся серьезными для большинства людей.
Обычно снижение лимфоцитов наблюдается на поздних стадиях Вич-инфекции, так как Т-лимфоциты разрушаются.
Анализ крови
Когда анализ крови показал пониженные сегментно-ядерные нейтрофилы и повышенные лимфоциты:
- Часть клеток крови могла погибнуть в результате борьбы с бактериальной или вирусной инфекцией.
- Организм находится в процессе выведения продуктов распада и погибших клеток.
- Если в пределах нормы, то нет смысла в специальном лечении.
Если общее число лимфоцитов повышено, а нейтрофилов понижено
На лейкоциты также могут влиять травмы, перенесённые операции, ожег, внутренние болезни, лекарственные препараты, стресс.
В том числе и заболевания:
Туберкулёз, ВИЧ, заболевания щитовидной железы и т.д.
Грамотный врач поможет расшифровать анализы вашего малыша и назначить адекватное лечение. Самое главное не паниковать, все разрешимо.
Всем пока!
С уважением, Екатерина
★ Нейтрофилия — заболевания крови .. Информация
Пользователи также искали:
как повысить нейтрофилы,
моноциты повышены нейтрофилы понижены,
нейтрофилы норма,
нейтрофилы понижены у ребенка,
нейтрофилы понижены,
нейтрофилы повышены,
нейтрофилы за что отвечают,
палочкоядерные нейтрофилы,
нейтрофилы,
понижены,
нейтрофилы понижены,
повышены,
как повысить нейтрофилы,
нейтрофилы понижены у ребенка,
палочкоядерные нейтрофилы,
нейтрофилы за что отвечают,
отвечают,
нейтрофилы норма,
норма,
повысить,
моноциты,
ребенка,
палочкоядерные,
Нейтрофилия,
нейтрофилы повышены,
моноциты повышены нейтрофилы понижены,
нейтрофилия,
заболевания крови.
Лимфоциты повышены нейтрофилы понижены у ребенка причины | У ребенка повышены
Почему бывают лимфоциты повышены, а нейтрофилы понижены у ребенка или взрослого
Общий анализ крови – один из наиболее часто проходимых обследований. По расшифровке ее состава выявляются различные патологии и нетипичные для здорового человека состояния.
Кровь в организме человека выполняет ряд функций, основные из которых – транспортная и защитная.
- Транспортировка газов, питательных веществ, метаболических продуктов.
- Гомеостаз, как одна из функций, связан с поддержанием водного баланса организма, кислотно-основного равновесия и температуры.
- Защита организма от инородных микротел. Осуществляется за счет присутствия антител – так называемых иммунных клеток.
- Гемостаз – физиологическое свойство. Проявляется за счет коагулятивных способностей.
Состав крови
Основными нерастворимыми элементами в крови являются эритроциты, лейкоциты и тромбоциты. Они в свою очередь образуют группы белых и красных кровяных телец. Мы не будем останавливаться на каждом элементе в отдельности. В этом материале мы поговорим о том, что значит пониженные сегментоядерные нейтрофилы и повышенные лимфоциты.
Лимфоцитами называется определенный вид лейкоцитов (прим. лейкоциты – белые кровяные тельца, основная функция – защитная), отвечающий за формирование иммунного барьера человеческого организма. Их задача – распознавание и уничтожение клеток вирусов, различных инфекций, грибков, а также патогенных новообразований. Синтезируются эти тельца в костном мозге, а оттуда уже попадают в кровь.
Нейтрофилы – это тоже вид лейкоцитов, наиболее многочисленный. Они очень необычные по своим способностям. Как только в организме появляется очаг инфекции, они устремляются туда на борьбу с микробами. Из-за этого понижается их уровень в составе крови. Нейтрофил поглощает патогенную клетку, нейтрализует ее внутри себя, но и сам в результате гибнет.
Нейтрофил поглощает патогенную клетку, нейтрализует ее внутри себя, но и сам в результате гибнет.
Лейкоциты также имеют и другие разновидности: эозинофилы, базофилы, моноциты и пр. При исследовании анализа крови из всех лейкоцитов больше внимания уделяется лимфоцитам, нейтрофилам и эозинофилам.
Когда лимфоциты повышены?
Наличие любого чужеродного элемента в организме – сигнал к увеличению числа лимфоцитов. Это нормальная иммунная реакция. Так при простудных заболеваниях и инфекционном мононуклеозе число этих телец резко возрастает. Зато при наличии вируса гриппа, наоборот, их число падает меньше нормы.
Когда нейтрофилы повышены?
Нейтрофилы представлены 2-мя разновидностями: сегментоядерные и палочкоядерные. Вторые – это еще молодые тела, которые со временем трансформируются в зрелые сегментоядерные элементы. И уже от их количества зависит способность организма противостоять инфекции. Как только начинается процесс уничтожения инородных тел, уровень зрелых нейтрофилов снижается, тогда как незрелых – растет.
Если анализ крови показал пониженные сегментоядерные нейтрофилы и повышенные лимфоциты, то в организме протекает острый бактериальный процесс или массовая инфекция.
Лейкоцитный уровень рассматривается отдельно у детей и взрослых. Что говорит результат анализа в разном возрасте, об этом далее.
Лимфоциты повышены, нейтрофилы понижены у ребенка и взрослого
Определяется лейкоцитарная формула – процентное соотношение между разными видами лейкоцитных тел. В норме уровень зрелых и незрелых нейтрофилов у детей распределяется так:
- до 1 года: сегментоядерные нейтрофилы – 15-45%, палочкоядерные – 0,5-4,5%;
- до 6 лет: сегментоядерные нейтрофилы – 25-60%, палочкоядерные – 0,5-4,5%;
- с 7 лет: сегментоядерные нейтрофилы – 30-60%, палочкоядерные – до 6%.
Уменьшение числа зрелых и увеличение незрелых – признак инфекционного заболевания.
Уровень лимфоцитов у детей обычно достаточно высокий – 40-72%.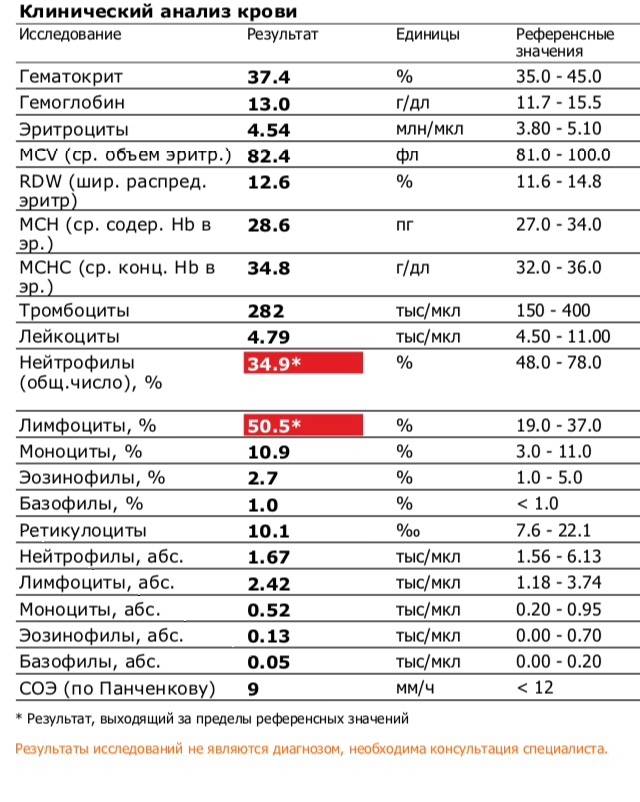
Даже без анализа крови по состоянию ребенка можно судить о наличии инфекционного поражения организма. Высокая температура на уровне 38-40 градусов, сильный жар – первые признаки того, что у ребенка повышены лимфоциты и понижены нейтрофилы. То есть инфекционный процесс в самом разгаре.
В таком случае маленькому пациенту назначается противовирусная терапия. Тем не менее, результат анализа крови при наличии упомянутых симптомов прольет свет на природу недомогания. Ведь аналогичная симптоматика наблюдается также при паразитарной инфекции. Если к внешним признакам добавляется сухой кашель на фоне отсутствия хрипов в легких, тогда это точно не наш случай, а паразиты.
При хронических вирусных инфекциях наблюдается аналогичная картина: низкий уровень нейтрофилов и высокий лимфоцитов. Иногда – это результат недавней вирусной инфекции. Требуется обследовать малыша на возможные вирусные патологии.
Лейкоцитарная формула у взрослого (в норме):
- сегментоядерные нейтрофилы – 30-60%;
- палочкоядерные нейтрофилы – до 6%;
- лимфоциты – 22-50%.
Отклонение от нормы свидетельствует о воспалительном процессе, с которым в данный момент борется иммунная система. На что еще могут указывать значения, когда у взрослого повышены лимфоциты и понижены нейтрофилы?
- туберкулезная палочка;
- вирусная инфекция;
- дисфункция щитовидки;
- острая или хроническая форма лимфолейкоза.
- вирусная инфекция;
- реакция организма на медикаментозную терапию;
- реакция организма на последствия лучевой терапии.
В таком случае требуется провести комплексное обследование на предмет выявления природы расстройства. Дополнительно сдают анализ мочи, мазок, проводятся рентгенография, УЗИ и другие необходимые исследования.
Дополнительно сдают анализ мочи, мазок, проводятся рентгенография, УЗИ и другие необходимые исследования.
Только комплексная диагностика поможет выявить причину и очаг недомогания, а также назначить адекватную терапию. Заметим, что в большинстве случаев в медикаментозное лечение включаются антибиотики. Своевременная качественная диагностики и эффективное лечение особенно важны в отношении детей. Ведь различного рода инфекции могут быть весьма опасны для здоровья и жизни малыша.
Читайте другие интересные рубрики
Что означает, если нейтрофилы понижены, лимфоциты повышены?
Клинический анализ крови позволяет определить содержание многих элементов крови и дать общую картину происходящих в организме пациента изменений. По количеству гемоглобина можно определить анемию, при увеличении или уменьшении концентрации эритроцитов можно предположить наличие различных заболеваний и так далее. В этой статье мы рассмотрим, что может означать анализ крови, если в нейнейтрофилы понижены, лимфоциты повышены.
Лимфоциты повышены
Для начала следует разобраться, что такое лимфоциты и какую функцию они выполняют в организме.
Лимфоциты – это белые кровяные клетки иммунной системы из рода лейкоцитов. Они играют очень важную, более того, основную роль в иммунной системе защиты от антител, регулируя деятельность других клеток иммунитета и непосредственно контактируя с клетками-жертвами, продуцируя антитела и таким образом вырабатывая клеточный (гуморальный) иммунитет.
Другими словами, лимфоциты повышены могут быть при любых вирусных инфекциях, туберкулёзе, остром или же хроническом лимфолейкозе, лимфосаркоме, гипертиреозе и при других проблемах щитовидной железы, а также в случае любой патогеннойинвазии.
Состояние, при котором в крови лимфоциты повышены, называется лимфоцитозом .Он диагностируется у взрослых, если у них в крови лимфоцитов больше 3,6х109/л. Для детей нормальный уровень определяется в зависимости от возраста и варьирует от 9,0 до 32,0х109/л.
Нейтрофилы понижены
Нейтрофилы также являются клетками кровеносной системы, основной ролью которых является защита организма от различных инфекций. Это тоже клетки иммунной системы, относящиеся к лейкоцитам. Живут нейтрофилы очень мало, максимум сутки, в зависимости от развития или, наоборот, отсутствия воспалительного инфекционного процесса.
Понижение нейтрофилов бывает при любых воспалительных и вирусных процессах, агранулоцитозоме, анемии и в результате приёма ряда препаратов, а также вследствие лучевой терапии или из-за радиационного облучения.
Нейтрофилы понижены, лимфоциты повышены
Таким образом, на основе всего вышенаписанного можно сделать вывод, что при одновременном понижении нейтрофилов и повышении лейкоцитов, скорее всего, в организме у человека есть очаг инфекции, вероятно вирусной. Если при этом отсутствуют симптомы заболевания, то речь может идти о носительстве вируса. Поэтому, если у вас нейтрофилы понижены, лимфоциты повышены, обязательно надо пройти полное обследование, сдать анализы на самые значимые инфекции (гепатит С и В, ВИЧ), выявить очаг и, разумеется, пройти курс лечения.
Поделитесь с друзьями!
Причины повышенных лимфоцитов у детей, что делать с этим?
Состав крови чутко реагирует на любые процессы, которые протекают в организме. Если у ребенка повышены лимфоциты, это сигнализирует о наличии воспалительного процесса. Конкретизировать расположение и характер воспаления можно с помощью дополнительных исследований. У детей до 5 лет повышенное содержание лимфоцитов является разновидностью нормы.
Расшифровку данных должен проводить тот врач, который наблюдает ребенка, поскольку именно он знает индивидуальные особенности организма.
Почему лимфоциты и моноциты повышены?
Клетки иммунной системы имеют специализацию по функциям, главная задача всех клеток — это нейтрализация патогенных микроорганизмов. К категории лейкоцитов относятся лимфоциты и моноциты — неокрашенные клетки крови.
Моноциты производятся костным мозгом, это клетки-защитники, которые активно участвуют в поглощении болезнетворных бактерий. Нормальный уровень содержания моноцитов — от 3 до 11% от общего количества всех лейкоцитов крови. Если анализ показывает, что лимфоциты и моноциты повышены, это может свидетельствовать о следующем:
- наличие злокачественной опухоли;
- мононуклеоз, риккетсиоз;
- грибковая, вирусная или бактериальная инфекция;
- ревматоидный артрит и полиартрит;
- саркоидоз;
- заболевания кишечника: колит, энтерит;
- заболевания сердца и сосудов;
- эндокардит;
- паротит.
Если моноциты повышены, а все другие группы клеток иммунной системы в норме, можно заподозрить заболевания костного мозга.
Моноцитоз нужно рассматривать как серьезное нарушение, лечить заболевание надо в условиях стационара. Первоочередная задача врача — это исключить рак костного мозга, провести все необходимые обследования и выяснить причину, по которой моноциты повышены у ребенка. При обширных воспалительных процессах, сепсисе, флегмоне показатели иммунных клеток в крови увеличены в процентном соотношении. Количество лимфоцитов остается повышенным в течение всего времени болезни и некоторое время после выздоровления. Если до анализа ребенок перенес серьезное заболевание, это может искажать результаты исследования.
Виды повышения лимфоцитов
Причины, по которым изменяется уровень клеток-защитников, могут быть серьезными (гепатит, сифилис, туберкулез) или не очень (грибковая инфекция, кандидоз). Чтобы выяснить, почему иммунная система выбросила в кровь большое количество клеток-защитников, нужно обследовать наиболее вероятные очаги воспаления. Лимфоцитозом называется состояние, при котором содержание лимфоцитов повышено совместно или изолированно от других видов иммунных клеток. Есть 2 разновидности лимфоцитоза:
- Реактивный лимфоцитоз.
 Возникает как естественный ответ на травму, прием некоторых лекарственных средств или инфекционное заболевание. У грудного ребенка может являться ответом на инфекцию матери. Повышенные лимфоциты определяются при таких вирусных инфекциях, как грипп, герпес, аденовирус, цитомегаловирус и др.
Возникает как естественный ответ на травму, прием некоторых лекарственных средств или инфекционное заболевание. У грудного ребенка может являться ответом на инфекцию матери. Повышенные лимфоциты определяются при таких вирусных инфекциях, как грипп, герпес, аденовирус, цитомегаловирус и др. - Злокачественный лимфоцитоз. Это наименее благоприятная причина. Высокое содержание лимфоцитов в крови свидетельствует о лимфобластном лейкозе, лимфоме, лимфолейкозе и других злокачественных онкологических заболеваниях.
Показатели анализа крови рассматриваются не отдельно, а в пропорциональном соотношении. Повторный анализ крови позволяет отслеживать динамику состояния пациента.
Если повышены лимфоциты в крови из-за инфекции, то спустя 1 месяц с момента выздоровления показатели должны прийти в норму. Если повышение произошло из-за злокачественной опухоли, показатели нормализуются только после устранения провоцирующего фактора.
Что означает повышение лимфоцитов при понижении нейтрофилов?
Еще одна разновидность лейкоцитов, которая имеет важное диагностическое значение, — нейтрофилы. Это клетки, которые специализируются на поглощении патогенных микроорганизмов, активированные нейтрофилы поступают прямо в очаг воспаления. Повышенный уровень лимфоцитов всегда свидетельствует о воспалительном процессе, а пониженный уровень нейтрофилов говорит о том, что клетки-защитники активно проникают из крови к зоне патологического процесса.
Каждая клетка иммунной системы имеет свою степень зрелости. Наличие большого количества иммунных молодых клеток любого вида свидетельствует об активном их производстве, то есть воспалительный процесс актуален и происходит прямо сейчас. Наличие зрелых и старых клеток говорит о перенесенном заболевании, то есть воспалительный процесс больше не актуален, клетки не пригодились в борьбе с инфекцией, это остаточное явление. Если у ребенка повышены лимфоциты и понижены нейтрофилы, нужно постараться совместно с врачом установить очаг воспалительного процесса.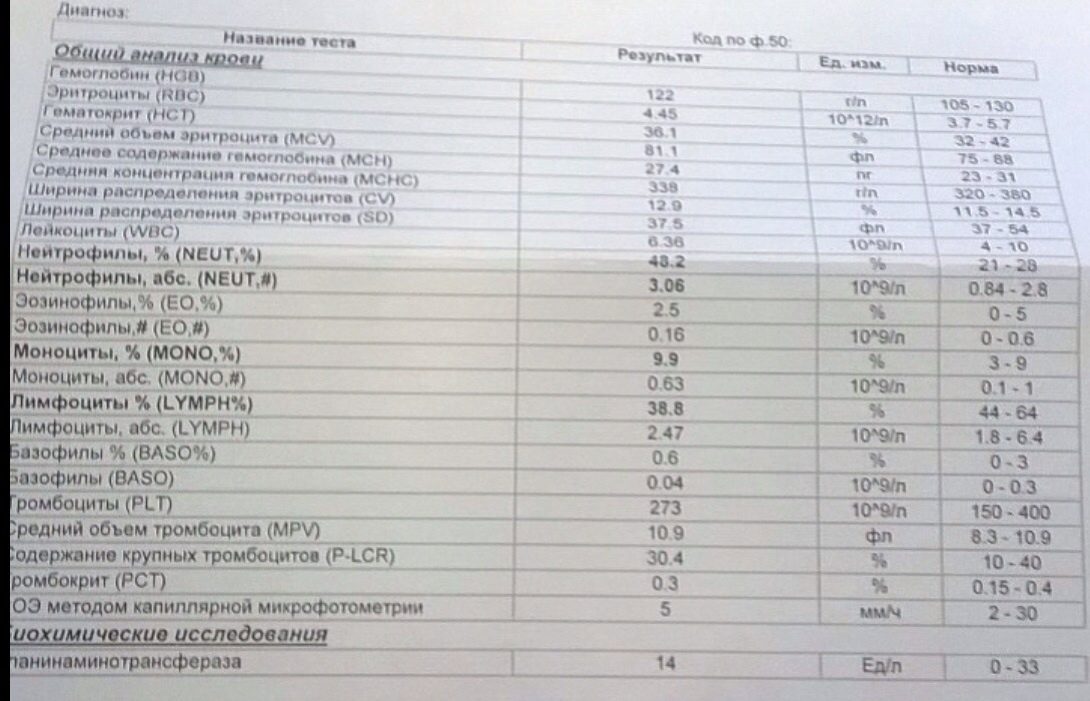 Некоторые заболевания проявляются очевидными симптомами, например, грипп, а некоторые находятся в инкубационном периоде, протекают без симптомов. Когда у ребенка повышены лимфоциты и понижены нейтрофилы, а никаких симптомов заболеваний нет и все другие анализы в норме, нужно повторить исследование крови через 3 недели.
Некоторые заболевания проявляются очевидными симптомами, например, грипп, а некоторые находятся в инкубационном периоде, протекают без симптомов. Когда у ребенка повышены лимфоциты и понижены нейтрофилы, а никаких симптомов заболеваний нет и все другие анализы в норме, нужно повторить исследование крови через 3 недели.
Как проводится расшифровка анализов?
Единицы измерения, в которых представлены исследования, могут различаться в зависимости от лаборатории. Почему повышены лимфоциты в крови у ребенка, должен объяснить лечащий врач с учетом:
- возраста ребенка, некоторые лаборатории используют нормативы для взрослых при обследовании детей;
- перенесенных в течение последнего времени инфекций;
- текущего состояния здоровья.
Без сбора анамнеза и прояснения всей клинической картины невозможно выявить причину повышения лимфоцитов, моноцитов или нейтрофилов. Часто родители пытаются самостоятельно разобраться в анализах и поставить на основании результатов диагноз, но это попросту невозможно без дополнительных исследований. Повод для беспокойства есть в том случае, если помимо повышения лимфоцитов есть следующие симптомы:
- ребенок теряет вес, аппетит отсутствует;
- ребенок вялый, не может сосредоточиться, неактивный;
- цвет кожи бледный или желтоватый.
Иммунная система справляется с очагом воспаления, если лимфоциты повышены, нейтрофилы понижены, а самочувствие ребенка удовлетворительное. Выяснить причину нетипичных данных анализа нужно обязательно, поскольку заболевания во время инкубационного периода могут не давать ярких симптомов. Поставить диагноз и подобрать лечение поможет педиатр.
Источники: http://ladyspecial.ru/zdorovie/narodnaya-mediczina/bolezni-i-lechenie/nejtrofily-povysheny-limfotsity-ponizheny, http://www.happy-giraffe.ru/community/33/forum/post/25729/, http://rebenokzabolel.ru/diagnostika/u-rebenka-povysheny-limfocity. html
html
Комментариев пока нет!
Понижены нейтрофилы, повышены лимфоциты
Прежде всего, стоит разобраться, что собой представляют нейтрофилы и лимфоциты. И те, и другие клетки являются лейкоцитами (к ним также относятся моноциты, эозинофилы и базофилы), однако их роль в физиологических и патологических процессах, происходящих в организме человека, кардинально отличается.
Нейтрофилы
Нейтрофилы (или нейтрофильные гранулоциты) – это клетки крови, которые содержат внутри себя гранулы с ферментами, предназначенными для уничтожения бактерий и грибов. Гранулоциты этого типа бывают зрелыми и незрелыми, к зрелым клеткам относятся сегментоядерные нейтрофилы. Они являются самыми сильными «пожирателями» бактериальных агентов. В условиях острого инфекционного процесса, когда, уничтожая бактерии, зрелые клетки массово гибнут, костный мозг начинает активно вырабатывать новые нейтрофильные лейкоциты, поэтому в крови появляются их незрелые формы – юные и палочкоядерные.
Пониженные нейтрофилы (уменьшение их абсолютного количества) принято называть нейтропенией. Развитие такого состояния могут спровоцировать различные факторы: прием некоторых лекарственных средств, вирусные инфекции, тяжелые бактериальные болезни (например, туберкулез), заболевания костного мозга, аутоиммунные недуги, радиоактивное облучение и многое другое.
Лимфоциты
Лимфоциты – это клетки, обеспечивающие нормальное функционирование всех звеньев иммунной системы человека. Именно лимфоциты обнаруживают и распознают чужеродные агенты, проникнувшие в организм, а также синтезируют антитела против них. Основная специализация клеток данного типа – борьба с вирусными инфекциями, поэтому и не удивительно, что при любом банальном насморке, вызванном ОРВИ, количество лимфоцитарных телец в крови увеличивается.
Повышенные лимфоциты могут доминировать в анализе крови еще несколько недель после выздоровления – такое состояние называют лимфоцитозом. Помимо вирусных инфекций, вызвать его развитие могут различные заболевания лимфатической системы, а также такие болезни как туберкулез, токсоплазмоз, бруцеллез, коклюш и пр.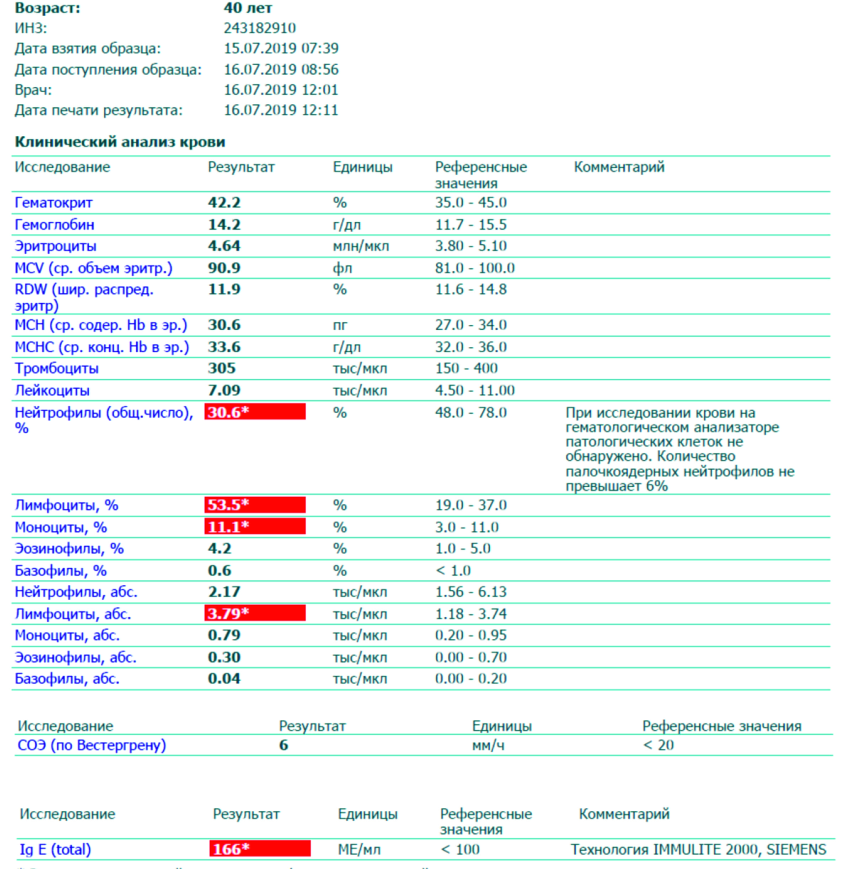
Нормальные показатели
Лейкоцитарная формула не является стабильной, процентное соотношение клеток лейкоцитарного ряда постоянно меняется и не всегда по патологическим причинам. Особенно вариабельно количество нейтрофилов и лимфоцитов в крови, причем связано это с физиологическими процессами, происходящими в организме.
Например, в раннем детском возрасте (до 2 лет) лимфоцитов всегда больше, чем нейтрофильных гранулоцитов. В 4 – 5 лет этих клеток примерно одинаковое количество. У взрослых же их соотношение меняется – преобладают нейтрофилы. Таким образом, рассматривая результаты анализа крови, необходимо всегда учитывать возраст обследуемого. Средние нормы по возрастам:
- для взрослого: нейтроф. сегментоядерные – 47 – 72%, лимфоциты – 19 – 37%;
- для ребенка 1 года: нейтроф. сегментоядерные – 20 – 35%, лимфоциты – 45 – 65%;
- для ребенка 10 лет: нейтроф. сегментоядерные – 40 – 60%, лимфоциты – 30 – 45%.
Чем объясняется снижение нейтрофилов и повышение лимфоцитов?
Прежде всего, стоит уточнить, что такие понятия как низкие нейтрофилы и высокие лимфоциты нельзя интерпретировать одинаково в разных ситуациях. Например, у взрослого человека нейтрофилов может быть 45% – это близко к нижней границе нормы, а может быть и 20% – это уже явная нейтропения. Такая же ситуация возможна и с лимфоцитами, поэтому в расшифровке анализов играет роль каждый процент и абсолютное количество клеток (рассчитывается по специальным формулам).
Так, незначительные изменения в анализе крови (например, если нейтрофильные клетки слегка снижены, а лимфоциты немного повышены) могут свидетельствовать о том, что человек находится на стадии выздоровления после перенесенного острого инфекционного заболевания (преимущественно вирусного, хотя нередко подобное отмечается и после затяжных бактериальных инфекций). В свою очередь, выраженные лимфоцитоз и нейтропения обнаруживаются обычно в острой стадии недуга.
Если же в момент сдачи анализа никаких проявлений болезни у человека не было, и он не болел перед этим, но количество лимфоцитов в его крови повышено, а нейтрофильные гранулоциты снижены, стоит искать скрытый очаг инфекции в организме. Например, такая картина характерна для хронических вирусных гепатитов. У часто болеющих детей виновниками умеренного лимфоцитоза и нейтропении чаще всего бывают цитомегаловирус и вирус Эпштейна-Бар. Помимо этого, подобные изменения в крови происходят при аллергических реакциях и глистных инвазиях.
Например, такая картина характерна для хронических вирусных гепатитов. У часто болеющих детей виновниками умеренного лимфоцитоза и нейтропении чаще всего бывают цитомегаловирус и вирус Эпштейна-Бар. Помимо этого, подобные изменения в крови происходят при аллергических реакциях и глистных инвазиях.
Таким образом, оценивая результаты анализа крови (в частности изменения количества нейтрофилов и лимфоцитов), необходимо, во-первых, обращать внимание на возраст человека, во-вторых, на наличие у него симптомов заболевания на момент исследования или незадолго до него, а, в-третьих, на абсолютные значения определяемых показателей.
Роль соотношения количества нейтрофилов и лимфоцитов в дифференциальной диагностике между туберкулезом легких и бактериальной внебольничной пневмонией
Резюме
Предпосылки
Дифференциальный диагноз между туберкулезом легких (ТБ) и бактериальной внебольничной пневмонией часто вызывает осложнения. . Отношение количества нейтрофилов к лимфоцитам (NLR), удобный маркер воспаления, оказалось полезным биомаркером для прогнозирования бактериемии.Мы исследовали полезность NLR для дифференциации легочного туберкулеза от бактериальной ВП в стране с промежуточным бременем туберкулеза.
Методы
Мы ретроспективно проанализировали клинические и лабораторные характеристики 206 пациентов с подозрением на туберкулез легких или бактериальную ВП с января 2009 года по февраль 2011 года. Диагностическая способность NLR для дифференциальной диагностики была оценена и сравнена с C-реактивной белок.
Результаты
Уровни NLR в сыворотке были значительно ниже у пациентов с легочным туберкулезом, чем у пациентов с бактериальной ВП (3.67 ± 2,12 против 14,64 ± 9,72, P <0,001). NLR <7 было оптимальным пороговым значением для дифференциации пациентов с легочным туберкулезом от пациентов с бактериальной ВП (чувствительность 91,1%, специфичность 81,9%, прогностическая ценность положительного результата 85,7%, прогностическая ценность отрицательного результата 88,5%). Площадь под кривой для NLR (0,95, 95% доверительный интервал [ДИ], 0,91–0,98) была значительно больше, чем у С-реактивного белка (0,83, 95% ДИ, 0,76–0,88; P = 0,0015). .
Площадь под кривой для NLR (0,95, 95% доверительный интервал [ДИ], 0,91–0,98) была значительно больше, чем у С-реактивного белка (0,83, 95% ДИ, 0,76–0,88; P = 0,0015). .
Выводы
NLR, полученный на начальном этапе диагностики, является полезным лабораторным маркером для дифференциации пациентов с легочным туберкулезом от пациентов с бактериальной ВП в стране со средним бременем туберкулеза.
Ключевые слова: C-реактивный белок, лимфоциты, нейтрофилы, пневмония, туберкулез
ВВЕДЕНИЕ
Внебольничная пневмония (ВП) является одной из наиболее важных инфекционных причин смерти в Корее [1]. Ранняя диагностика и соответствующее назначение антибиотиков имеют важное значение для снижения заболеваемости и смертности от пневмонии [2]. Многие исследования, проведенные в странах с высоким бременем туберкулеза (ТБ), показали, что Mycobacterium tuberculosis является частой причиной ВП; однако часто бывает трудно отличить легочный ТБ от бактериальной ВП на начальной стадии диагностики [3, 4].Клинические и рентгенографические признаки туберкулеза часто неспецифичны, а чувствительность микроскопического исследования откашливаемой мокроты на кислотоустойчивые бациллы составляет всего 50-60% [5].
Задержки в диагностике легочного туберкулеза могут отрицательно сказаться на заболеваемости и смертности пациентов. Кроме того, может происходить внутрибольничная передача легочного туберкулеза другим госпитализированным пациентам и медицинским работникам. Недавно в некоторых исследованиях было высказано предположение, что биомаркеры, такие как С-реактивный белок (СРБ), прокальцитонин и растворимый запускающий рецептор, экспрессируемые на миелоидных клетках, могут играть роль в различении легочного ТБ от бактериальной ВП [6-8].Однако не все эти биомаркеры доступны в странах с высоким бременем ТБ.
Отношение количества нейтрофилов к лимфоцитам (NLR) — это легко вычисляемый лабораторный маркер, используемый для оценки системного воспаления. Недавнее исследование продемонстрировало полезность лимфоцитопении для прогнозирования бактериемии путем комбинирования обычных маркеров инфекции [9]. Кроме того, де Ягер и др. [10] продемонстрировали, что лимфоцитопения и NLR превосходят уровень CRP, а также количество лейкоцитов (WBC) и нейтрофилов для прогнозирования бактериемии в отделении неотложной помощи.
Недавнее исследование продемонстрировало полезность лимфоцитопении для прогнозирования бактериемии путем комбинирования обычных маркеров инфекции [9]. Кроме того, де Ягер и др. [10] продемонстрировали, что лимфоцитопения и NLR превосходят уровень CRP, а также количество лейкоцитов (WBC) и нейтрофилов для прогнозирования бактериемии в отделении неотложной помощи.
В этом исследовании мы исследовали роль NLR в различении пациентов с активным легочным туберкулезом от пациентов с бактериальной ВП и сравнили диагностическую способность NLR с показателями CRP и WBC.
МЕТОДЫ
1. Пациенты
В это ретроспективное когортное исследование были включены последовательные взрослые пациенты старше 18 лет с подозрением на ВП с января 2009 года по февраль 2011 года. Пациенты с подозрением на ВП были определены как пациенты с недавно появившимися респираторными симптомами или признаками, аномальными инфильтратами на рентгенограмме грудной клетки и не госпитализированные недавно.
Критерии исключения включали использование антибиотиков в течение более 24 часов на момент регистрации, состояния, которые, как известно, влияют на общее и дифференциальное количество лейкоцитов, такие как гематологические нарушения, хронические воспалительные состояния, текущая стероидная терапия и / или история использования стероидов в течение 3 лет. за несколько месяцев до госпитализации, прохождение химиотерапии или лучевой терапии в течение 4 недель до включения в исследование, отсутствие дифференциального подсчета лейкоцитов или данных по СРБ или изменение диагноза на другой, такой как тромбоэмболия легочной артерии, отек легких или рак легких, во время наблюдения.
Были собраны демографические данные и рассчитана оценка группы по исследованию исходов у пациентов с пневмонией (PORT) [11]. Наблюдательный совет учреждения одобрил это исследование, и оно было проведено в соответствии с Хельсинкской декларацией.
2. Диагностика легочного туберкулеза или бактериального ВП
Пациенты были отнесены к группе легочного туберкулеза, когда 1) M. tuberculosis было культивировано из мокроты или жидкости бронхиального лаважа, или 2) концентрация аденозиндезаминазы составляла ≥70 МЕ / дл по данным экссудативного плеврального выпота с преобладанием лимфоцитов в сочетании с паренхиматозным поражением легкого, предполагающим легочный ТБ.Пациенты считались имеющими бактериальную ВП, когда 1) клинические признаки и новая инфильтрация на рентгенограмме грудной клетки были очевидны и полностью исчезли после лечения соответствующими антибиотиками, 2) посевы мокроты или лаважа были M. tuberculosis -отрицательными во время клинического наблюдения и 3) вирусные возбудители не обнаружены.
tuberculosis было культивировано из мокроты или жидкости бронхиального лаважа, или 2) концентрация аденозиндезаминазы составляла ≥70 МЕ / дл по данным экссудативного плеврального выпота с преобладанием лимфоцитов в сочетании с паренхиматозным поражением легкого, предполагающим легочный ТБ.Пациенты считались имеющими бактериальную ВП, когда 1) клинические признаки и новая инфильтрация на рентгенограмме грудной клетки были очевидны и полностью исчезли после лечения соответствующими антибиотиками, 2) посевы мокроты или лаважа были M. tuberculosis -отрицательными во время клинического наблюдения и 3) вирусные возбудители не обнаружены.
Для микробиологического выявления пациентов с бактериальной ВП мы выполнили окрашивание мокроты по Граму, посевы и посевы крови. Анализы на антигены в моче также использовали для обнаружения Legionella pneumophila и Streptococcus pneumoniae в соответствии с клиническими показаниями.У некоторых пациентов вирус был выделен из образцов носоглоточного секрета с использованием платформы ПЦР в реальном времени для обнаружения вируса гриппа A или B, аденовируса, метапневмовируса человека, респираторно-синцитиального вируса, риновируса и вируса парагриппа.
3. Воспалительные маркеры
Дифференциальное количество лейкоцитов и СРБ определяли до лечения антибиотиками. Общее количество лейкоцитов, нейтрофилов и лимфоцитов определяли с использованием гематологического анализатора Sysmex XE-2100 (Sysmex Corp., Кобе, Япония).NLR определяли как абсолютное количество нейтрофилов, деленное на абсолютное количество лимфоцитов. Уровни CRP измеряли с помощью автоматического турбидиметрического иммуноанализа с латексным усилением (Dimension; Dade Behring, Newark, NJ, USA; TBA-200FR; Toshiba, Tokyo, Japan) в течение 1 часа после сбора образца. Дифференциальное количество лейкоцитов, NLR и уровень CRP сравнивали между пациентами с легочным туберкулезом и пациентами с бактериальной ВП. Эти воспалительные маркеры также сравнивались между пациентами с легочным туберкулезом и пациентами с пневмонией легкой степени тяжести с индексом тяжести пневмонии PORT I или II класса риска.
4. Статистический анализ
Непрерывные данные представлены как среднее ± стандартное отклонение. Различия в непрерывных переменных между группами определяли с использованием теста Стьюдента t или теста Манна-Уитни U . Категориальные данные представлены в виде частот. Различия между категориальными переменными анализировали с помощью критерия хи-квадрат Пирсона или точного критерия Фишера. Корреляцию между NLR и CRP анализировали с помощью критерия ранговой корреляции Спирмена.Анализ кривой ROC был проведен, чтобы определить наиболее полезные пороговые уровни для NLR, CRP, количества лейкоцитов, количества нейтрофилов и лимфоцитов, чтобы определить наибольшую сумму чувствительности и специфичности для различения легочного ТБ от бактериальной ВП. Способность NLR, CRP, количества лейкоцитов, нейтрофилов и лимфоцитов отличать легочный туберкулез от бактериального ВП сравнивалась с использованием площади под кривой (AUC). Значение P ≤0,05 считалось статистически значимым. Все статистические анализы были выполнены с использованием SPSS 19.0 (SPSS Inc., Чикаго, Иллинойс, США).
РЕЗУЛЬТАТЫ
1. Пациенты
Мы включили в это исследование 206 пациентов (), из которых 112 (54,4%) имели туберкулез легких и 94 (45,6%) имели бактериальную ВП. Средний возраст пациентов с легочным туберкулезом и бактериальной ВП составлял 54 года (диапазон от 20 до 86 лет) и 70 лет (от 18 до 86 лет), соответственно. Исходные клинические характеристики перечислены в.
Блок-схема пациента.
Сокращения: WBC, лейкоцит; CRP, C-реактивный белок; FU, продолжение; ВП, внебольничная пневмония; Туберкулез, туберкулез; КУБ, кислотно-фастбациллы.
Таблица 1
Исходные клинические характеристики исследуемой популяции
Среди пациентов с легочным туберкулезом 98 (87,5%) имели M. tuberculosis респираторных проб с положительным посевом. У остальных пациентов был плевральный выпот и инфильтрация легких на рентгенограмме, совместимая с туберкулезом. Неудача лечения произошла у одного пациента.
Неудача лечения произошла у одного пациента.
Возбудители болезни определены у 27 (28,7%) пациентов с бактериальной ВП. Streptococcus pneumoniae был обнаружен у 17 пациентов с помощью тестов на антигены в моче, посева респираторных образцов или посева крови.Другими идентифицированными патогенами были Klebsiella pneumonia (N = 4), Escherichia coli (N = 2), метициллин-чувствительный Staphylococcus aureus (N = 1), метициллин-устойчивый S. aureus (N = 1). , Acinetobacter baumannii (N = 1) и Stenotrophomonas maltophila (N = 1). Среднее значение PSI составило 111,03. Семьдесят четыре пациента (78,7%) были отнесены к группе риска выше III класса риска PSI. У 20 пациентов (21,3%) была диагностирована пневмония легкой степени тяжести.Внутрибольничная летальность в группе ВП составила 12,8% (N = 12).
2. Маркеры воспаления
Среднее и медианное значения NLR составили 9,69 ± 9,02 и 6,36 соответственно. Общее количество лейкоцитов и нейтрофилов, NLR и CRP были значительно ниже у пациентов с легочным ТБ, чем у пациентов с бактериальной ВП, тогда как количество лимфоцитов было значительно выше у пациентов с легочным ТБ, чем у пациентов с бактериальной ВП ().
Таблица 2
Базовые лабораторные характеристики исследуемой популяции
Мы провели анализ подгрупп пациентов с легкой пневмонией (N = 20, классы риска I и II PSI) и пациентов с легочным туберкулезом для оценки диагностической способности NLR. .Общее количество лейкоцитов (7,19 ± 2,48 против 12,59 ± 5,41, P <0,001), количество нейтрофилов (4,79 ± 2,14 против 10,38 ± 4,78, P <0,001), NLR (3,67 ± 2,12 против 9,65 ± 6,41, P <0,001) и CRP (6,57 ± 7,31 против 17,48 ± 10,76, P <0,001) также были значительно ниже у пациентов с легочным туберкулезом, чем у пациентов с пневмонией легкой степени тяжести. Однако количество лимфоцитов существенно не различается между группами.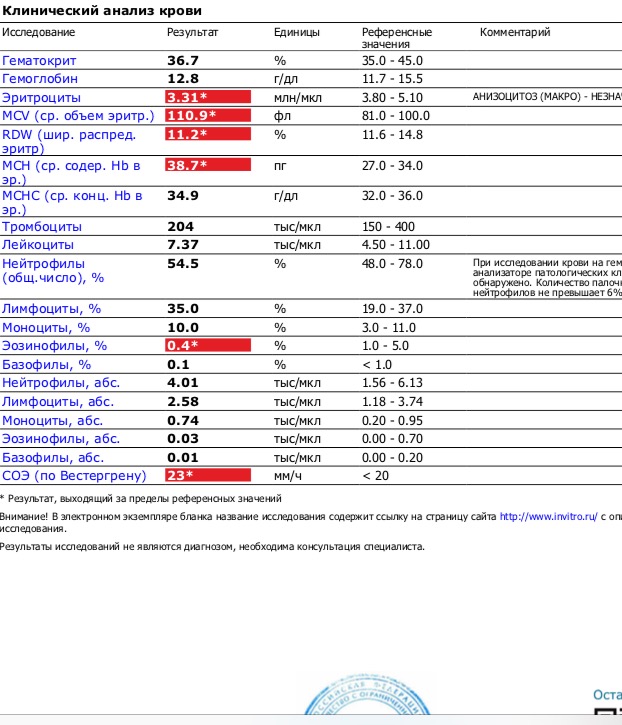
Самая сильная корреляция была отмечена между NLR и количеством нейтрофилов (r = 0.832, P = 0,01). Положительная корреляция была также обнаружена между NLR и CRP (r = 0,562, P = 0,01), а также между NLR и количеством лейкоцитов (r = 0,738, P = 0,01). Отрицательная корреляция была выявлена между NLR и количеством лимфоцитов (r = -0,644, P = 0,01).
3. Диагностическая точность для дифференциации легочного ТБ от бактериальной ВП
Значение NLR <7,0 было определено как оптимальное пороговое значение для дифференциации пациентов с легочным ТБ от пациентов с бактериальной ВП, что дало 91 балл.Чувствительность 1%, специфичность 81,9%, прогностическая ценность положительного результата 85,7% и прогностическая ценность отрицательного результата 88,5% (). Пороговое значение для CRP было менее 7,0 мг / дл. Используя это пороговое значение, CRP показал 67,5% чувствительность и 85,1% специфичность, 79,4% положительную прогностическую ценность и 75,5% отрицательную прогностическую ценность. NLR AUC (AUC, 0,93; 95% доверительный интервал [CI], 0,88-0,96) был значительно выше, чем у CRP (AUC, 0,83; 95% CI, 0,76-0,88; P = 0,0015) (). AUC NLR также была значительно выше, чем у количества лейкоцитов (AUC, 0.86; 95% ДИ 0,81-0,91; P = 0,0016), количество нейтрофилов (AUC, 0,89; 95% ДИ, 0,84-0,93; P = 0,0197) и количество лимфоцитов (AUC, 0,74; 95% ДИ, 0,68-0,80; P <0,0001 ). У пациентов с легкой пневмонией NLR AUC (AUC, 0,87; 95% ДИ, 0,76-0,92) был значительно выше, чем у количества лимфоцитов (AUC, 0,61; 95% ДИ, 0,52-0,69; P = 0,0019). Однако не было значимой разницы в AUC между NLR и CRP (AUC, 0,81; 95% ДИ, 0,72-0,88; P = 0.5721), количество NLR и лейкоцитов (AUC, 0,81; 95% ДИ, 0,73-0,87; P = 0,3523), а также NLR и количество нейтрофилов (AUC, 0,86; 95% ДИ, 0,79-0,91; P = 0,8466 ).
ROC-кривые C-реактивного белка (CRP) и отношения нейтрофилов к лимфоцитам (NLR) для дифференциации туберкулеза от бактериальной внебольничной пневмонии. Площадь под кривой для NLR (AUC, 0,93; 95% доверительный интервал [CI], 0,88-0,96) была значительно больше, чем для CRP (AUC, 0,83; 95% CI, 0,76-0,88) ( P = 0 .0015).
Площадь под кривой для NLR (AUC, 0,93; 95% доверительный интервал [CI], 0,88-0,96) была значительно больше, чем для CRP (AUC, 0,83; 95% CI, 0,76-0,88) ( P = 0 .0015).
Таблица 3
Диагностическая валидность NLR, CRP и WBC с дифференциальным подсчетом для дифференциации легочного ТБ от бактериальной ВП
ОБСУЖДЕНИЕ
В этом исследовании последовательных пациентов, набранных из клинических учреждений, NLR был полезным лабораторным маркером для различения между пациентами с легочным туберкулезом и другими бактериальными ВП на начальном этапе диагностики при промежуточной распространенности туберкулеза. Результаты этого исследования включали следующее: 1) уровни NLR в сыворотке были значительно ниже у пациентов с легочным туберкулезом, чем у пациентов с бактериальной ВП; 2) NLR <7 было оптимальным пороговым значением для дифференциации пациентов с легочным туберкулезом от пациентов с бактериальной ВП; 3) Диагностическая способность NLR превосходила возможности CRP, количества лейкоцитов, нейтрофилов и лимфоцитов для дифференциации пациентов с легочным туберкулезом от пациентов с бактериальной ВП.Это первое исследование, демонстрирующее диагностическую способность NLR различать легочный ТБ и бактериальную ВП.
Корея является страной с промежуточным бременем туберкулеза: в 2009 г. было впервые диагностировано около 43 000 случаев туберкулеза легких [12]. Частота выявления M. tuberculosis у пациентов с подозрением на ВП достигает 12% в Гонконге [4] и 21% в Сингапуре [13]; Распространенность туберкулеза в этих странах такая же, как в Корее. Отличить легочный туберкулез от ВП важно для общественного здравоохранения; Немедленная изоляция и раннее лечение противотуберкулезными препаратами имеют важное значение для пациентов с легочным туберкулезом.Однако отличить легочный ТБ от ВП только на основании анамнеза, физикального обследования и рентгенологических данных часто бывает сложно. Следовательно, необходим быстрый и доступный тест, чтобы отличить легочный туберкулез от ВП.
Физиологические иммунные ответы циркулирующих лейкоцитов на различные стрессовые события характеризуются увеличением количества нейтрофилов и уменьшением количества лимфоцитов. Увеличение общего количества лейкоцитов и нейтрофилов является воспалительной реакцией, особенно вызванной бактериальной инфекцией [14].Лимфоцитопения также описывается как диагностический маркер бактериальной инфекции [9]. Следовательно, считается, что NLR имеет более сильную дискриминационную способность для прогнозирования бактериемии по сравнению с дискриминацией, основанной только на нейтрофилии или лимфоцитопении. Goodman et al. [15] первоначально предположили полезность NLR для диагностики пациентов с подозрением на аппендицит. В их исследовании NLR был более чувствительным параметром бактериальной инфекции, чем увеличение количества лейкоцитов. Zahorec et al.[14] провели проспективное продольное обсервационное исследование, в котором они сообщили о корреляции между тяжестью клинического течения и лимфоцитопенией у пациентов с тяжелым сепсисом и септическим шоком в онкологическом отделении интенсивной терапии. Они предложили использовать NLR в качестве дополнительного маркера инфекции в отделении интенсивной терапии [14]. Недавно de Jager et al. [10] продемонстрировали, что лимфоцитопения и NLR были лучшими прогностическими факторами бактериемии, чем обычные параметры, такие как уровень CRP, количество лейкоцитов и нейтрофилов в отделении неотложной помощи.В настоящее время NLR вызывает интерес как средство прогнозирования выживаемости в различных клинических ситуациях, от онкологических до сердечно-сосудистых заболеваний [16-19].
NLR плевральной жидкости был оценен как дополнительный диагностический инструмент у пациентов с туберкулезным плевритом [20, 21]. CD4 + Т-лимфоциты и макрофаги играют важную роль в патогенезе ТБ, поскольку участвует клеточный иммунитет. Напротив, нейтрофилия является первичным клеточным явлением во время развития бактериальной ВП.Следовательно, NLR образцов крови может быть хорошим лабораторным маркером для дифференциации пациентов с легочным туберкулезом от пациентов с бактериальной ВП.
В этом исследовании общие лейкоциты с дифференциальным подсчетом, CRP и NLR значительно различались в группе легочного ТБ и группе бактериальной ВП. NLR был самым мощным дискриминационным маркером, о чем свидетельствует его высокая AUC. Подсчет нейтрофилов был вторым лучшим отличительным маркером, за ним следовали количество лейкоцитов, CRP и лимфоцитов.Примечательно, что легко поддающиеся оценке параметры общего анализа крови, такие как общее количество лейкоцитов и нейтрофилов, также продемонстрировали значительную различительную способность, хотя и меньшую, чем у NLR. Более того, их чувствительность, специфичность и точность были относительно высокими.
NLR можно легко определить при обычном лабораторном обследовании, и это простое соотношение доступно в большинстве учреждений. Кроме того, NLR — более простой и менее дорогой метод по сравнению с другими воспалительными биомаркерами, такими как CRP, прокальцитонин и растворимый запускающий рецептор, экспрессируемый на миелоидных клетках, которые недавние исследования предложили в качестве маркеров дифференциальной диагностики [6-8].
Однако в этом исследовании есть несколько ограничений. Во-первых, он был ретроспективным, нерандомизированным и проводился в едином центре; таким образом, это было предметом систематической ошибки отбора. Необходимы исследования с привлечением большего размера выборки и проспективный анализ. Во-вторых, патогены, вызывающие ВП, могли быть идентифицированы только у меньшинства пациентов. Однако патогены, вызывающие ВП, четко не определены [22, 23]. В-третьих, другие воспалительные маркеры, такие как прокальцитонин, не были включены и сравнивались с NLR в текущем анализе.Однако прокальцитонин — дорогостоящее обследование, которое доступно не во всех больницах.
В заключение, текущее исследование показало, что NLR, полученный из одного образца крови на начальном этапе диагностики, является очень полезным лабораторным маркером для дифференциации пациентов с легочным туберкулезом от пациентов с бактериальной ВП. Диагностическая способность NLR превосходит возможности CRP, лейкоцитов, нейтрофилов и лимфоцитов. Следовательно, NLR следует включать в рутинные обследования пациентов с неоднозначным диагнозом между легочным туберкулезом и бактериальной ВП.
Роль соотношения количества нейтрофилов и лимфоцитов в дифференциальной диагностике между легочным туберкулезом и бактериальной внебольничной пневмонией
Реферат
Предпосылки
Дифференциальный диагноз между легочным туберкулезом (ТБ) и бактериальной внебольничной пневмонией часто бывает (ТБ) и бактериальной внебольничной пневмонией испытывающий. Отношение количества нейтрофилов к лимфоцитам (NLR), удобный маркер воспаления, оказалось полезным биомаркером для прогнозирования бактериемии.Мы исследовали полезность NLR для дифференциации легочного туберкулеза от бактериальной ВП в стране с промежуточным бременем туберкулеза.
Методы
Мы ретроспективно проанализировали клинические и лабораторные характеристики 206 пациентов с подозрением на туберкулез легких или бактериальную ВП с января 2009 года по февраль 2011 года. Диагностическая способность NLR для дифференциальной диагностики была оценена и сравнена с C-реактивной белок.
Результаты
Уровни NLR в сыворотке были значительно ниже у пациентов с легочным туберкулезом, чем у пациентов с бактериальной ВП (3.67 ± 2,12 против 14,64 ± 9,72, P <0,001). NLR <7 было оптимальным пороговым значением для дифференциации пациентов с легочным туберкулезом от пациентов с бактериальной ВП (чувствительность 91,1%, специфичность 81,9%, прогностическая ценность положительного результата 85,7%, прогностическая ценность отрицательного результата 88,5%). Площадь под кривой для NLR (0,95, 95% доверительный интервал [ДИ], 0,91–0,98) была значительно больше, чем у С-реактивного белка (0,83, 95% ДИ, 0,76–0,88; P = 0,0015). .
Выводы
NLR, полученный на начальном этапе диагностики, является полезным лабораторным маркером для дифференциации пациентов с легочным туберкулезом от пациентов с бактериальной ВП в стране со средним бременем туберкулеза.
Ключевые слова: C-реактивный белок, лимфоциты, нейтрофилы, пневмония, туберкулез
ВВЕДЕНИЕ
Внебольничная пневмония (ВП) является одной из наиболее важных инфекционных причин смерти в Корее [1]. Ранняя диагностика и соответствующее назначение антибиотиков имеют важное значение для снижения заболеваемости и смертности от пневмонии [2]. Многие исследования, проведенные в странах с высоким бременем туберкулеза (ТБ), показали, что Mycobacterium tuberculosis является частой причиной ВП; однако часто бывает трудно отличить легочный ТБ от бактериальной ВП на начальной стадии диагностики [3, 4].Клинические и рентгенографические признаки туберкулеза часто неспецифичны, а чувствительность микроскопического исследования откашливаемой мокроты на кислотоустойчивые бациллы составляет всего 50-60% [5].
Задержки в диагностике легочного туберкулеза могут отрицательно сказаться на заболеваемости и смертности пациентов. Кроме того, может происходить внутрибольничная передача легочного туберкулеза другим госпитализированным пациентам и медицинским работникам. Недавно в некоторых исследованиях было высказано предположение, что биомаркеры, такие как С-реактивный белок (СРБ), прокальцитонин и растворимый запускающий рецептор, экспрессируемые на миелоидных клетках, могут играть роль в различении легочного ТБ от бактериальной ВП [6-8].Однако не все эти биомаркеры доступны в странах с высоким бременем ТБ.
Отношение количества нейтрофилов к лимфоцитам (NLR) — это легко вычисляемый лабораторный маркер, используемый для оценки системного воспаления. Недавнее исследование продемонстрировало полезность лимфоцитопении для прогнозирования бактериемии путем комбинирования обычных маркеров инфекции [9]. Кроме того, де Ягер и др. [10] продемонстрировали, что лимфоцитопения и NLR превосходят уровень CRP, а также количество лейкоцитов (WBC) и нейтрофилов для прогнозирования бактериемии в отделении неотложной помощи.
В этом исследовании мы исследовали роль NLR в различении пациентов с активным легочным туберкулезом от пациентов с бактериальной ВП и сравнили диагностическую способность NLR с показателями CRP и WBC.
МЕТОДЫ
1. Пациенты
В это ретроспективное когортное исследование были включены последовательные взрослые пациенты старше 18 лет с подозрением на ВП с января 2009 года по февраль 2011 года. Пациенты с подозрением на ВП были определены как пациенты с недавно появившимися респираторными симптомами или признаками, аномальными инфильтратами на рентгенограмме грудной клетки и не госпитализированные недавно.
Критерии исключения включали использование антибиотиков в течение более 24 часов на момент регистрации, состояния, которые, как известно, влияют на общее и дифференциальное количество лейкоцитов, такие как гематологические нарушения, хронические воспалительные состояния, текущая стероидная терапия и / или история использования стероидов в течение 3 лет. за несколько месяцев до госпитализации, прохождение химиотерапии или лучевой терапии в течение 4 недель до включения в исследование, отсутствие дифференциального подсчета лейкоцитов или данных по СРБ или изменение диагноза на другой, такой как тромбоэмболия легочной артерии, отек легких или рак легких, во время наблюдения.
Были собраны демографические данные и рассчитана оценка группы по исследованию исходов у пациентов с пневмонией (PORT) [11]. Наблюдательный совет учреждения одобрил это исследование, и оно было проведено в соответствии с Хельсинкской декларацией.
2. Диагностика легочного туберкулеза или бактериального ВП
Пациенты были отнесены к группе легочного туберкулеза, когда 1) M. tuberculosis было культивировано из мокроты или жидкости бронхиального лаважа, или 2) концентрация аденозиндезаминазы составляла ≥70 МЕ / дл по данным экссудативного плеврального выпота с преобладанием лимфоцитов в сочетании с паренхиматозным поражением легкого, предполагающим легочный ТБ.Пациенты считались имеющими бактериальную ВП, когда 1) клинические признаки и новая инфильтрация на рентгенограмме грудной клетки были очевидны и полностью исчезли после лечения соответствующими антибиотиками, 2) посевы мокроты или лаважа были M. tuberculosis -отрицательными во время клинического наблюдения и 3) вирусные возбудители не обнаружены.
Для микробиологического выявления пациентов с бактериальной ВП мы выполнили окрашивание мокроты по Граму, посевы и посевы крови. Анализы на антигены в моче также использовали для обнаружения Legionella pneumophila и Streptococcus pneumoniae в соответствии с клиническими показаниями.У некоторых пациентов вирус был выделен из образцов носоглоточного секрета с использованием платформы ПЦР в реальном времени для обнаружения вируса гриппа A или B, аденовируса, метапневмовируса человека, респираторно-синцитиального вируса, риновируса и вируса парагриппа.
3. Воспалительные маркеры
Дифференциальное количество лейкоцитов и СРБ определяли до лечения антибиотиками. Общее количество лейкоцитов, нейтрофилов и лимфоцитов определяли с использованием гематологического анализатора Sysmex XE-2100 (Sysmex Corp., Кобе, Япония).NLR определяли как абсолютное количество нейтрофилов, деленное на абсолютное количество лимфоцитов. Уровни CRP измеряли с помощью автоматического турбидиметрического иммуноанализа с латексным усилением (Dimension; Dade Behring, Newark, NJ, USA; TBA-200FR; Toshiba, Tokyo, Japan) в течение 1 часа после сбора образца. Дифференциальное количество лейкоцитов, NLR и уровень CRP сравнивали между пациентами с легочным туберкулезом и пациентами с бактериальной ВП. Эти воспалительные маркеры также сравнивались между пациентами с легочным туберкулезом и пациентами с пневмонией легкой степени тяжести с индексом тяжести пневмонии PORT I или II класса риска.
4. Статистический анализ
Непрерывные данные представлены как среднее ± стандартное отклонение. Различия в непрерывных переменных между группами определяли с использованием теста Стьюдента t или теста Манна-Уитни U . Категориальные данные представлены в виде частот. Различия между категориальными переменными анализировали с помощью критерия хи-квадрат Пирсона или точного критерия Фишера. Корреляцию между NLR и CRP анализировали с помощью критерия ранговой корреляции Спирмена.Анализ кривой ROC был проведен, чтобы определить наиболее полезные пороговые уровни для NLR, CRP, количества лейкоцитов, количества нейтрофилов и лимфоцитов, чтобы определить наибольшую сумму чувствительности и специфичности для различения легочного ТБ от бактериальной ВП. Способность NLR, CRP, количества лейкоцитов, нейтрофилов и лимфоцитов отличать легочный туберкулез от бактериального ВП сравнивалась с использованием площади под кривой (AUC). Значение P ≤0,05 считалось статистически значимым. Все статистические анализы были выполнены с использованием SPSS 19.0 (SPSS Inc., Чикаго, Иллинойс, США).
РЕЗУЛЬТАТЫ
1. Пациенты
Мы включили в это исследование 206 пациентов (), из которых 112 (54,4%) имели туберкулез легких и 94 (45,6%) имели бактериальную ВП. Средний возраст пациентов с легочным туберкулезом и бактериальной ВП составлял 54 года (диапазон от 20 до 86 лет) и 70 лет (от 18 до 86 лет), соответственно. Исходные клинические характеристики перечислены в.
Блок-схема пациента.
Сокращения: WBC, лейкоцит; CRP, C-реактивный белок; FU, продолжение; ВП, внебольничная пневмония; Туберкулез, туберкулез; КУБ, кислотно-фастбациллы.
Таблица 1
Исходные клинические характеристики исследуемой популяции
Среди пациентов с легочным туберкулезом 98 (87,5%) имели M. tuberculosis респираторных проб с положительным посевом. У остальных пациентов был плевральный выпот и инфильтрация легких на рентгенограмме, совместимая с туберкулезом. Неудача лечения произошла у одного пациента.
Возбудители болезни определены у 27 (28,7%) пациентов с бактериальной ВП. Streptococcus pneumoniae был обнаружен у 17 пациентов с помощью тестов на антигены в моче, посева респираторных образцов или посева крови.Другими идентифицированными патогенами были Klebsiella pneumonia (N = 4), Escherichia coli (N = 2), метициллин-чувствительный Staphylococcus aureus (N = 1), метициллин-устойчивый S. aureus (N = 1). , Acinetobacter baumannii (N = 1) и Stenotrophomonas maltophila (N = 1). Среднее значение PSI составило 111,03. Семьдесят четыре пациента (78,7%) были отнесены к группе риска выше III класса риска PSI. У 20 пациентов (21,3%) была диагностирована пневмония легкой степени тяжести.Внутрибольничная летальность в группе ВП составила 12,8% (N = 12).
2. Маркеры воспаления
Среднее и медианное значения NLR составили 9,69 ± 9,02 и 6,36 соответственно. Общее количество лейкоцитов и нейтрофилов, NLR и CRP были значительно ниже у пациентов с легочным ТБ, чем у пациентов с бактериальной ВП, тогда как количество лимфоцитов было значительно выше у пациентов с легочным ТБ, чем у пациентов с бактериальной ВП ().
Таблица 2
Базовые лабораторные характеристики исследуемой популяции
Мы провели анализ подгрупп пациентов с легкой пневмонией (N = 20, классы риска I и II PSI) и пациентов с легочным туберкулезом для оценки диагностической способности NLR. .Общее количество лейкоцитов (7,19 ± 2,48 против 12,59 ± 5,41, P <0,001), количество нейтрофилов (4,79 ± 2,14 против 10,38 ± 4,78, P <0,001), NLR (3,67 ± 2,12 против 9,65 ± 6,41, P <0,001) и CRP (6,57 ± 7,31 против 17,48 ± 10,76, P <0,001) также были значительно ниже у пациентов с легочным туберкулезом, чем у пациентов с пневмонией легкой степени тяжести. Однако количество лимфоцитов существенно не различается между группами.
Самая сильная корреляция была отмечена между NLR и количеством нейтрофилов (r = 0.832, P = 0,01). Положительная корреляция была также обнаружена между NLR и CRP (r = 0,562, P = 0,01), а также между NLR и количеством лейкоцитов (r = 0,738, P = 0,01). Отрицательная корреляция была выявлена между NLR и количеством лимфоцитов (r = -0,644, P = 0,01).
3. Диагностическая точность для дифференциации легочного ТБ от бактериальной ВП
Значение NLR <7,0 было определено как оптимальное пороговое значение для дифференциации пациентов с легочным ТБ от пациентов с бактериальной ВП, что дало 91 балл.Чувствительность 1%, специфичность 81,9%, прогностическая ценность положительного результата 85,7% и прогностическая ценность отрицательного результата 88,5% (). Пороговое значение для CRP было менее 7,0 мг / дл. Используя это пороговое значение, CRP показал 67,5% чувствительность и 85,1% специфичность, 79,4% положительную прогностическую ценность и 75,5% отрицательную прогностическую ценность. NLR AUC (AUC, 0,93; 95% доверительный интервал [CI], 0,88-0,96) был значительно выше, чем у CRP (AUC, 0,83; 95% CI, 0,76-0,88; P = 0,0015) (). AUC NLR также была значительно выше, чем у количества лейкоцитов (AUC, 0.86; 95% ДИ 0,81-0,91; P = 0,0016), количество нейтрофилов (AUC, 0,89; 95% ДИ, 0,84-0,93; P = 0,0197) и количество лимфоцитов (AUC, 0,74; 95% ДИ, 0,68-0,80; P <0,0001 ). У пациентов с легкой пневмонией NLR AUC (AUC, 0,87; 95% ДИ, 0,76-0,92) был значительно выше, чем у количества лимфоцитов (AUC, 0,61; 95% ДИ, 0,52-0,69; P = 0,0019). Однако не было значимой разницы в AUC между NLR и CRP (AUC, 0,81; 95% ДИ, 0,72-0,88; P = 0.5721), количество NLR и лейкоцитов (AUC, 0,81; 95% ДИ, 0,73-0,87; P = 0,3523), а также NLR и количество нейтрофилов (AUC, 0,86; 95% ДИ, 0,79-0,91; P = 0,8466 ).
ROC-кривые C-реактивного белка (CRP) и отношения нейтрофилов к лимфоцитам (NLR) для дифференциации туберкулеза от бактериальной внебольничной пневмонии. Площадь под кривой для NLR (AUC, 0,93; 95% доверительный интервал [CI], 0,88-0,96) была значительно больше, чем для CRP (AUC, 0,83; 95% CI, 0,76-0,88) ( P = 0 .0015).
Таблица 3
Диагностическая валидность NLR, CRP и WBC с дифференциальным подсчетом для дифференциации легочного ТБ от бактериальной ВП
ОБСУЖДЕНИЕ
В этом исследовании последовательных пациентов, набранных из клинических учреждений, NLR был полезным лабораторным маркером для различения между пациентами с легочным туберкулезом и другими бактериальными ВП на начальном этапе диагностики при промежуточной распространенности туберкулеза. Результаты этого исследования включали следующее: 1) уровни NLR в сыворотке были значительно ниже у пациентов с легочным туберкулезом, чем у пациентов с бактериальной ВП; 2) NLR <7 было оптимальным пороговым значением для дифференциации пациентов с легочным туберкулезом от пациентов с бактериальной ВП; 3) Диагностическая способность NLR превосходила возможности CRP, количества лейкоцитов, нейтрофилов и лимфоцитов для дифференциации пациентов с легочным туберкулезом от пациентов с бактериальной ВП.Это первое исследование, демонстрирующее диагностическую способность NLR различать легочный ТБ и бактериальную ВП.
Корея является страной с промежуточным бременем туберкулеза: в 2009 г. было впервые диагностировано около 43 000 случаев туберкулеза легких [12]. Частота выявления M. tuberculosis у пациентов с подозрением на ВП достигает 12% в Гонконге [4] и 21% в Сингапуре [13]; Распространенность туберкулеза в этих странах такая же, как в Корее. Отличить легочный туберкулез от ВП важно для общественного здравоохранения; Немедленная изоляция и раннее лечение противотуберкулезными препаратами имеют важное значение для пациентов с легочным туберкулезом.Однако отличить легочный ТБ от ВП только на основании анамнеза, физикального обследования и рентгенологических данных часто бывает сложно. Следовательно, необходим быстрый и доступный тест, чтобы отличить легочный туберкулез от ВП.
Физиологические иммунные ответы циркулирующих лейкоцитов на различные стрессовые события характеризуются увеличением количества нейтрофилов и уменьшением количества лимфоцитов. Увеличение общего количества лейкоцитов и нейтрофилов является воспалительной реакцией, особенно вызванной бактериальной инфекцией [14].Лимфоцитопения также описывается как диагностический маркер бактериальной инфекции [9]. Следовательно, считается, что NLR имеет более сильную дискриминационную способность для прогнозирования бактериемии по сравнению с дискриминацией, основанной только на нейтрофилии или лимфоцитопении. Goodman et al. [15] первоначально предположили полезность NLR для диагностики пациентов с подозрением на аппендицит. В их исследовании NLR был более чувствительным параметром бактериальной инфекции, чем увеличение количества лейкоцитов. Zahorec et al.[14] провели проспективное продольное обсервационное исследование, в котором они сообщили о корреляции между тяжестью клинического течения и лимфоцитопенией у пациентов с тяжелым сепсисом и септическим шоком в онкологическом отделении интенсивной терапии. Они предложили использовать NLR в качестве дополнительного маркера инфекции в отделении интенсивной терапии [14]. Недавно de Jager et al. [10] продемонстрировали, что лимфоцитопения и NLR были лучшими прогностическими факторами бактериемии, чем обычные параметры, такие как уровень CRP, количество лейкоцитов и нейтрофилов в отделении неотложной помощи.В настоящее время NLR вызывает интерес как средство прогнозирования выживаемости в различных клинических ситуациях, от онкологических до сердечно-сосудистых заболеваний [16-19].
NLR плевральной жидкости был оценен как дополнительный диагностический инструмент у пациентов с туберкулезным плевритом [20, 21]. CD4 + Т-лимфоциты и макрофаги играют важную роль в патогенезе ТБ, поскольку участвует клеточный иммунитет. Напротив, нейтрофилия является первичным клеточным явлением во время развития бактериальной ВП.Следовательно, NLR образцов крови может быть хорошим лабораторным маркером для дифференциации пациентов с легочным туберкулезом от пациентов с бактериальной ВП.
В этом исследовании общие лейкоциты с дифференциальным подсчетом, CRP и NLR значительно различались в группе легочного ТБ и группе бактериальной ВП. NLR был самым мощным дискриминационным маркером, о чем свидетельствует его высокая AUC. Подсчет нейтрофилов был вторым лучшим отличительным маркером, за ним следовали количество лейкоцитов, CRP и лимфоцитов.Примечательно, что легко поддающиеся оценке параметры общего анализа крови, такие как общее количество лейкоцитов и нейтрофилов, также продемонстрировали значительную различительную способность, хотя и меньшую, чем у NLR. Более того, их чувствительность, специфичность и точность были относительно высокими.
NLR можно легко определить при обычном лабораторном обследовании, и это простое соотношение доступно в большинстве учреждений. Кроме того, NLR — более простой и менее дорогой метод по сравнению с другими воспалительными биомаркерами, такими как CRP, прокальцитонин и растворимый запускающий рецептор, экспрессируемый на миелоидных клетках, которые недавние исследования предложили в качестве маркеров дифференциальной диагностики [6-8].
Однако в этом исследовании есть несколько ограничений. Во-первых, он был ретроспективным, нерандомизированным и проводился в едином центре; таким образом, это было предметом систематической ошибки отбора. Необходимы исследования с привлечением большего размера выборки и проспективный анализ. Во-вторых, патогены, вызывающие ВП, могли быть идентифицированы только у меньшинства пациентов. Однако патогены, вызывающие ВП, четко не определены [22, 23]. В-третьих, другие воспалительные маркеры, такие как прокальцитонин, не были включены и сравнивались с NLR в текущем анализе.Однако прокальцитонин — дорогостоящее обследование, которое доступно не во всех больницах.
В заключение, текущее исследование показало, что NLR, полученный из одного образца крови на начальном этапе диагностики, является очень полезным лабораторным маркером для дифференциации пациентов с легочным туберкулезом от пациентов с бактериальной ВП. Диагностическая способность NLR превосходит возможности CRP, лейкоцитов, нейтрофилов и лимфоцитов. Следовательно, NLR следует включать в рутинные обследования пациентов с неоднозначным диагнозом между легочным туберкулезом и бактериальной ВП.
Роль соотношения количества нейтрофилов и лимфоцитов в дифференциальной диагностике между легочным туберкулезом и бактериальной внебольничной пневмонией
Реферат
Предпосылки
Дифференциальный диагноз между легочным туберкулезом (ТБ) и бактериальной внебольничной пневмонией часто бывает (ТБ) и бактериальной внебольничной пневмонией испытывающий. Отношение количества нейтрофилов к лимфоцитам (NLR), удобный маркер воспаления, оказалось полезным биомаркером для прогнозирования бактериемии.Мы исследовали полезность NLR для дифференциации легочного туберкулеза от бактериальной ВП в стране с промежуточным бременем туберкулеза.
Методы
Мы ретроспективно проанализировали клинические и лабораторные характеристики 206 пациентов с подозрением на туберкулез легких или бактериальную ВП с января 2009 года по февраль 2011 года. Диагностическая способность NLR для дифференциальной диагностики была оценена и сравнена с C-реактивной белок.
Результаты
Уровни NLR в сыворотке были значительно ниже у пациентов с легочным туберкулезом, чем у пациентов с бактериальной ВП (3.67 ± 2,12 против 14,64 ± 9,72, P <0,001). NLR <7 было оптимальным пороговым значением для дифференциации пациентов с легочным туберкулезом от пациентов с бактериальной ВП (чувствительность 91,1%, специфичность 81,9%, прогностическая ценность положительного результата 85,7%, прогностическая ценность отрицательного результата 88,5%). Площадь под кривой для NLR (0,95, 95% доверительный интервал [ДИ], 0,91–0,98) была значительно больше, чем у С-реактивного белка (0,83, 95% ДИ, 0,76–0,88; P = 0,0015). .
Выводы
NLR, полученный на начальном этапе диагностики, является полезным лабораторным маркером для дифференциации пациентов с легочным туберкулезом от пациентов с бактериальной ВП в стране со средним бременем туберкулеза.
Ключевые слова: C-реактивный белок, лимфоциты, нейтрофилы, пневмония, туберкулез
ВВЕДЕНИЕ
Внебольничная пневмония (ВП) является одной из наиболее важных инфекционных причин смерти в Корее [1]. Ранняя диагностика и соответствующее назначение антибиотиков имеют важное значение для снижения заболеваемости и смертности от пневмонии [2]. Многие исследования, проведенные в странах с высоким бременем туберкулеза (ТБ), показали, что Mycobacterium tuberculosis является частой причиной ВП; однако часто бывает трудно отличить легочный ТБ от бактериальной ВП на начальной стадии диагностики [3, 4].Клинические и рентгенографические признаки туберкулеза часто неспецифичны, а чувствительность микроскопического исследования откашливаемой мокроты на кислотоустойчивые бациллы составляет всего 50-60% [5].
Задержки в диагностике легочного туберкулеза могут отрицательно сказаться на заболеваемости и смертности пациентов. Кроме того, может происходить внутрибольничная передача легочного туберкулеза другим госпитализированным пациентам и медицинским работникам. Недавно в некоторых исследованиях было высказано предположение, что биомаркеры, такие как С-реактивный белок (СРБ), прокальцитонин и растворимый запускающий рецептор, экспрессируемые на миелоидных клетках, могут играть роль в различении легочного ТБ от бактериальной ВП [6-8].Однако не все эти биомаркеры доступны в странах с высоким бременем ТБ.
Отношение количества нейтрофилов к лимфоцитам (NLR) — это легко вычисляемый лабораторный маркер, используемый для оценки системного воспаления. Недавнее исследование продемонстрировало полезность лимфоцитопении для прогнозирования бактериемии путем комбинирования обычных маркеров инфекции [9]. Кроме того, де Ягер и др. [10] продемонстрировали, что лимфоцитопения и NLR превосходят уровень CRP, а также количество лейкоцитов (WBC) и нейтрофилов для прогнозирования бактериемии в отделении неотложной помощи.
В этом исследовании мы исследовали роль NLR в различении пациентов с активным легочным туберкулезом от пациентов с бактериальной ВП и сравнили диагностическую способность NLR с показателями CRP и WBC.
МЕТОДЫ
1. Пациенты
В это ретроспективное когортное исследование были включены последовательные взрослые пациенты старше 18 лет с подозрением на ВП с января 2009 года по февраль 2011 года. Пациенты с подозрением на ВП были определены как пациенты с недавно появившимися респираторными симптомами или признаками, аномальными инфильтратами на рентгенограмме грудной клетки и не госпитализированные недавно.
Критерии исключения включали использование антибиотиков в течение более 24 часов на момент регистрации, состояния, которые, как известно, влияют на общее и дифференциальное количество лейкоцитов, такие как гематологические нарушения, хронические воспалительные состояния, текущая стероидная терапия и / или история использования стероидов в течение 3 лет. за несколько месяцев до госпитализации, прохождение химиотерапии или лучевой терапии в течение 4 недель до включения в исследование, отсутствие дифференциального подсчета лейкоцитов или данных по СРБ или изменение диагноза на другой, такой как тромбоэмболия легочной артерии, отек легких или рак легких, во время наблюдения.
Были собраны демографические данные и рассчитана оценка группы по исследованию исходов у пациентов с пневмонией (PORT) [11]. Наблюдательный совет учреждения одобрил это исследование, и оно было проведено в соответствии с Хельсинкской декларацией.
2. Диагностика легочного туберкулеза или бактериального ВП
Пациенты были отнесены к группе легочного туберкулеза, когда 1) M. tuberculosis было культивировано из мокроты или жидкости бронхиального лаважа, или 2) концентрация аденозиндезаминазы составляла ≥70 МЕ / дл по данным экссудативного плеврального выпота с преобладанием лимфоцитов в сочетании с паренхиматозным поражением легкого, предполагающим легочный ТБ.Пациенты считались имеющими бактериальную ВП, когда 1) клинические признаки и новая инфильтрация на рентгенограмме грудной клетки были очевидны и полностью исчезли после лечения соответствующими антибиотиками, 2) посевы мокроты или лаважа были M. tuberculosis -отрицательными во время клинического наблюдения и 3) вирусные возбудители не обнаружены.
Для микробиологического выявления пациентов с бактериальной ВП мы выполнили окрашивание мокроты по Граму, посевы и посевы крови. Анализы на антигены в моче также использовали для обнаружения Legionella pneumophila и Streptococcus pneumoniae в соответствии с клиническими показаниями.У некоторых пациентов вирус был выделен из образцов носоглоточного секрета с использованием платформы ПЦР в реальном времени для обнаружения вируса гриппа A или B, аденовируса, метапневмовируса человека, респираторно-синцитиального вируса, риновируса и вируса парагриппа.
3. Воспалительные маркеры
Дифференциальное количество лейкоцитов и СРБ определяли до лечения антибиотиками. Общее количество лейкоцитов, нейтрофилов и лимфоцитов определяли с использованием гематологического анализатора Sysmex XE-2100 (Sysmex Corp., Кобе, Япония).NLR определяли как абсолютное количество нейтрофилов, деленное на абсолютное количество лимфоцитов. Уровни CRP измеряли с помощью автоматического турбидиметрического иммуноанализа с латексным усилением (Dimension; Dade Behring, Newark, NJ, USA; TBA-200FR; Toshiba, Tokyo, Japan) в течение 1 часа после сбора образца. Дифференциальное количество лейкоцитов, NLR и уровень CRP сравнивали между пациентами с легочным туберкулезом и пациентами с бактериальной ВП. Эти воспалительные маркеры также сравнивались между пациентами с легочным туберкулезом и пациентами с пневмонией легкой степени тяжести с индексом тяжести пневмонии PORT I или II класса риска.
4. Статистический анализ
Непрерывные данные представлены как среднее ± стандартное отклонение. Различия в непрерывных переменных между группами определяли с использованием теста Стьюдента t или теста Манна-Уитни U . Категориальные данные представлены в виде частот. Различия между категориальными переменными анализировали с помощью критерия хи-квадрат Пирсона или точного критерия Фишера. Корреляцию между NLR и CRP анализировали с помощью критерия ранговой корреляции Спирмена.Анализ кривой ROC был проведен, чтобы определить наиболее полезные пороговые уровни для NLR, CRP, количества лейкоцитов, количества нейтрофилов и лимфоцитов, чтобы определить наибольшую сумму чувствительности и специфичности для различения легочного ТБ от бактериальной ВП. Способность NLR, CRP, количества лейкоцитов, нейтрофилов и лимфоцитов отличать легочный туберкулез от бактериального ВП сравнивалась с использованием площади под кривой (AUC). Значение P ≤0,05 считалось статистически значимым. Все статистические анализы были выполнены с использованием SPSS 19.0 (SPSS Inc., Чикаго, Иллинойс, США).
РЕЗУЛЬТАТЫ
1. Пациенты
Мы включили в это исследование 206 пациентов (), из которых 112 (54,4%) имели туберкулез легких и 94 (45,6%) имели бактериальную ВП. Средний возраст пациентов с легочным туберкулезом и бактериальной ВП составлял 54 года (диапазон от 20 до 86 лет) и 70 лет (от 18 до 86 лет), соответственно. Исходные клинические характеристики перечислены в.
Блок-схема пациента.
Сокращения: WBC, лейкоцит; CRP, C-реактивный белок; FU, продолжение; ВП, внебольничная пневмония; Туберкулез, туберкулез; КУБ, кислотно-фастбациллы.
Таблица 1
Исходные клинические характеристики исследуемой популяции
Среди пациентов с легочным туберкулезом 98 (87,5%) имели M. tuberculosis респираторных проб с положительным посевом. У остальных пациентов был плевральный выпот и инфильтрация легких на рентгенограмме, совместимая с туберкулезом. Неудача лечения произошла у одного пациента.
Возбудители болезни определены у 27 (28,7%) пациентов с бактериальной ВП. Streptococcus pneumoniae был обнаружен у 17 пациентов с помощью тестов на антигены в моче, посева респираторных образцов или посева крови.Другими идентифицированными патогенами были Klebsiella pneumonia (N = 4), Escherichia coli (N = 2), метициллин-чувствительный Staphylococcus aureus (N = 1), метициллин-устойчивый S. aureus (N = 1). , Acinetobacter baumannii (N = 1) и Stenotrophomonas maltophila (N = 1). Среднее значение PSI составило 111,03. Семьдесят четыре пациента (78,7%) были отнесены к группе риска выше III класса риска PSI. У 20 пациентов (21,3%) была диагностирована пневмония легкой степени тяжести.Внутрибольничная летальность в группе ВП составила 12,8% (N = 12).
2. Маркеры воспаления
Среднее и медианное значения NLR составили 9,69 ± 9,02 и 6,36 соответственно. Общее количество лейкоцитов и нейтрофилов, NLR и CRP были значительно ниже у пациентов с легочным ТБ, чем у пациентов с бактериальной ВП, тогда как количество лимфоцитов было значительно выше у пациентов с легочным ТБ, чем у пациентов с бактериальной ВП ().
Таблица 2
Базовые лабораторные характеристики исследуемой популяции
Мы провели анализ подгрупп пациентов с легкой пневмонией (N = 20, классы риска I и II PSI) и пациентов с легочным туберкулезом для оценки диагностической способности NLR. .Общее количество лейкоцитов (7,19 ± 2,48 против 12,59 ± 5,41, P <0,001), количество нейтрофилов (4,79 ± 2,14 против 10,38 ± 4,78, P <0,001), NLR (3,67 ± 2,12 против 9,65 ± 6,41, P <0,001) и CRP (6,57 ± 7,31 против 17,48 ± 10,76, P <0,001) также были значительно ниже у пациентов с легочным туберкулезом, чем у пациентов с пневмонией легкой степени тяжести. Однако количество лимфоцитов существенно не различается между группами.
Самая сильная корреляция была отмечена между NLR и количеством нейтрофилов (r = 0.832, P = 0,01). Положительная корреляция была также обнаружена между NLR и CRP (r = 0,562, P = 0,01), а также между NLR и количеством лейкоцитов (r = 0,738, P = 0,01). Отрицательная корреляция была выявлена между NLR и количеством лимфоцитов (r = -0,644, P = 0,01).
3. Диагностическая точность для дифференциации легочного ТБ от бактериальной ВП
Значение NLR <7,0 было определено как оптимальное пороговое значение для дифференциации пациентов с легочным ТБ от пациентов с бактериальной ВП, что дало 91 балл.Чувствительность 1%, специфичность 81,9%, прогностическая ценность положительного результата 85,7% и прогностическая ценность отрицательного результата 88,5% (). Пороговое значение для CRP было менее 7,0 мг / дл. Используя это пороговое значение, CRP показал 67,5% чувствительность и 85,1% специфичность, 79,4% положительную прогностическую ценность и 75,5% отрицательную прогностическую ценность. NLR AUC (AUC, 0,93; 95% доверительный интервал [CI], 0,88-0,96) был значительно выше, чем у CRP (AUC, 0,83; 95% CI, 0,76-0,88; P = 0,0015) (). AUC NLR также была значительно выше, чем у количества лейкоцитов (AUC, 0.86; 95% ДИ 0,81-0,91; P = 0,0016), количество нейтрофилов (AUC, 0,89; 95% ДИ, 0,84-0,93; P = 0,0197) и количество лимфоцитов (AUC, 0,74; 95% ДИ, 0,68-0,80; P <0,0001 ). У пациентов с легкой пневмонией NLR AUC (AUC, 0,87; 95% ДИ, 0,76-0,92) был значительно выше, чем у количества лимфоцитов (AUC, 0,61; 95% ДИ, 0,52-0,69; P = 0,0019). Однако не было значимой разницы в AUC между NLR и CRP (AUC, 0,81; 95% ДИ, 0,72-0,88; P = 0.5721), количество NLR и лейкоцитов (AUC, 0,81; 95% ДИ, 0,73-0,87; P = 0,3523), а также NLR и количество нейтрофилов (AUC, 0,86; 95% ДИ, 0,79-0,91; P = 0,8466 ).
ROC-кривые C-реактивного белка (CRP) и отношения нейтрофилов к лимфоцитам (NLR) для дифференциации туберкулеза от бактериальной внебольничной пневмонии. Площадь под кривой для NLR (AUC, 0,93; 95% доверительный интервал [CI], 0,88-0,96) была значительно больше, чем для CRP (AUC, 0,83; 95% CI, 0,76-0,88) ( P = 0 .0015).
Таблица 3
Диагностическая валидность NLR, CRP и WBC с дифференциальным подсчетом для дифференциации легочного ТБ от бактериальной ВП
ОБСУЖДЕНИЕ
В этом исследовании последовательных пациентов, набранных из клинических учреждений, NLR был полезным лабораторным маркером для различения между пациентами с легочным туберкулезом и другими бактериальными ВП на начальном этапе диагностики при промежуточной распространенности туберкулеза. Результаты этого исследования включали следующее: 1) уровни NLR в сыворотке были значительно ниже у пациентов с легочным туберкулезом, чем у пациентов с бактериальной ВП; 2) NLR <7 было оптимальным пороговым значением для дифференциации пациентов с легочным туберкулезом от пациентов с бактериальной ВП; 3) Диагностическая способность NLR превосходила возможности CRP, количества лейкоцитов, нейтрофилов и лимфоцитов для дифференциации пациентов с легочным туберкулезом от пациентов с бактериальной ВП.Это первое исследование, демонстрирующее диагностическую способность NLR различать легочный ТБ и бактериальную ВП.
Корея является страной с промежуточным бременем туберкулеза: в 2009 г. было впервые диагностировано около 43 000 случаев туберкулеза легких [12]. Частота выявления M. tuberculosis у пациентов с подозрением на ВП достигает 12% в Гонконге [4] и 21% в Сингапуре [13]; Распространенность туберкулеза в этих странах такая же, как в Корее. Отличить легочный туберкулез от ВП важно для общественного здравоохранения; Немедленная изоляция и раннее лечение противотуберкулезными препаратами имеют важное значение для пациентов с легочным туберкулезом.Однако отличить легочный ТБ от ВП только на основании анамнеза, физикального обследования и рентгенологических данных часто бывает сложно. Следовательно, необходим быстрый и доступный тест, чтобы отличить легочный туберкулез от ВП.
Физиологические иммунные ответы циркулирующих лейкоцитов на различные стрессовые события характеризуются увеличением количества нейтрофилов и уменьшением количества лимфоцитов. Увеличение общего количества лейкоцитов и нейтрофилов является воспалительной реакцией, особенно вызванной бактериальной инфекцией [14].Лимфоцитопения также описывается как диагностический маркер бактериальной инфекции [9]. Следовательно, считается, что NLR имеет более сильную дискриминационную способность для прогнозирования бактериемии по сравнению с дискриминацией, основанной только на нейтрофилии или лимфоцитопении. Goodman et al. [15] первоначально предположили полезность NLR для диагностики пациентов с подозрением на аппендицит. В их исследовании NLR был более чувствительным параметром бактериальной инфекции, чем увеличение количества лейкоцитов. Zahorec et al.[14] провели проспективное продольное обсервационное исследование, в котором они сообщили о корреляции между тяжестью клинического течения и лимфоцитопенией у пациентов с тяжелым сепсисом и септическим шоком в онкологическом отделении интенсивной терапии. Они предложили использовать NLR в качестве дополнительного маркера инфекции в отделении интенсивной терапии [14]. Недавно de Jager et al. [10] продемонстрировали, что лимфоцитопения и NLR были лучшими прогностическими факторами бактериемии, чем обычные параметры, такие как уровень CRP, количество лейкоцитов и нейтрофилов в отделении неотложной помощи.В настоящее время NLR вызывает интерес как средство прогнозирования выживаемости в различных клинических ситуациях, от онкологических до сердечно-сосудистых заболеваний [16-19].
NLR плевральной жидкости был оценен как дополнительный диагностический инструмент у пациентов с туберкулезным плевритом [20, 21]. CD4 + Т-лимфоциты и макрофаги играют важную роль в патогенезе ТБ, поскольку участвует клеточный иммунитет. Напротив, нейтрофилия является первичным клеточным явлением во время развития бактериальной ВП.Следовательно, NLR образцов крови может быть хорошим лабораторным маркером для дифференциации пациентов с легочным туберкулезом от пациентов с бактериальной ВП.
В этом исследовании общие лейкоциты с дифференциальным подсчетом, CRP и NLR значительно различались в группе легочного ТБ и группе бактериальной ВП. NLR был самым мощным дискриминационным маркером, о чем свидетельствует его высокая AUC. Подсчет нейтрофилов был вторым лучшим отличительным маркером, за ним следовали количество лейкоцитов, CRP и лимфоцитов.Примечательно, что легко поддающиеся оценке параметры общего анализа крови, такие как общее количество лейкоцитов и нейтрофилов, также продемонстрировали значительную различительную способность, хотя и меньшую, чем у NLR. Более того, их чувствительность, специфичность и точность были относительно высокими.
NLR можно легко определить при обычном лабораторном обследовании, и это простое соотношение доступно в большинстве учреждений. Кроме того, NLR — более простой и менее дорогой метод по сравнению с другими воспалительными биомаркерами, такими как CRP, прокальцитонин и растворимый запускающий рецептор, экспрессируемый на миелоидных клетках, которые недавние исследования предложили в качестве маркеров дифференциальной диагностики [6-8].
Однако в этом исследовании есть несколько ограничений. Во-первых, он был ретроспективным, нерандомизированным и проводился в едином центре; таким образом, это было предметом систематической ошибки отбора. Необходимы исследования с привлечением большего размера выборки и проспективный анализ. Во-вторых, патогены, вызывающие ВП, могли быть идентифицированы только у меньшинства пациентов. Однако патогены, вызывающие ВП, четко не определены [22, 23]. В-третьих, другие воспалительные маркеры, такие как прокальцитонин, не были включены и сравнивались с NLR в текущем анализе.Однако прокальцитонин — дорогостоящее обследование, которое доступно не во всех больницах.
В заключение, текущее исследование показало, что NLR, полученный из одного образца крови на начальном этапе диагностики, является очень полезным лабораторным маркером для дифференциации пациентов с легочным туберкулезом от пациентов с бактериальной ВП. Диагностическая способность NLR превосходит возможности CRP, лейкоцитов, нейтрофилов и лимфоцитов. Следовательно, NLR следует включать в рутинные обследования пациентов с неоднозначным диагнозом между легочным туберкулезом и бактериальной ВП.
Роль соотношения количества нейтрофилов и лимфоцитов в дифференциальной диагностике между легочным туберкулезом и бактериальной внебольничной пневмонией
Реферат
Предпосылки
Дифференциальный диагноз между легочным туберкулезом (ТБ) и бактериальной внебольничной пневмонией часто бывает (ТБ) и бактериальной внебольничной пневмонией испытывающий. Отношение количества нейтрофилов к лимфоцитам (NLR), удобный маркер воспаления, оказалось полезным биомаркером для прогнозирования бактериемии.Мы исследовали полезность NLR для дифференциации легочного туберкулеза от бактериальной ВП в стране с промежуточным бременем туберкулеза.
Методы
Мы ретроспективно проанализировали клинические и лабораторные характеристики 206 пациентов с подозрением на туберкулез легких или бактериальную ВП с января 2009 года по февраль 2011 года. Диагностическая способность NLR для дифференциальной диагностики была оценена и сравнена с C-реактивной белок.
Результаты
Уровни NLR в сыворотке были значительно ниже у пациентов с легочным туберкулезом, чем у пациентов с бактериальной ВП (3.67 ± 2,12 против 14,64 ± 9,72, P <0,001). NLR <7 было оптимальным пороговым значением для дифференциации пациентов с легочным туберкулезом от пациентов с бактериальной ВП (чувствительность 91,1%, специфичность 81,9%, прогностическая ценность положительного результата 85,7%, прогностическая ценность отрицательного результата 88,5%). Площадь под кривой для NLR (0,95, 95% доверительный интервал [ДИ], 0,91–0,98) была значительно больше, чем у С-реактивного белка (0,83, 95% ДИ, 0,76–0,88; P = 0,0015). .
Выводы
NLR, полученный на начальном этапе диагностики, является полезным лабораторным маркером для дифференциации пациентов с легочным туберкулезом от пациентов с бактериальной ВП в стране со средним бременем туберкулеза.
Ключевые слова: C-реактивный белок, лимфоциты, нейтрофилы, пневмония, туберкулез
ВВЕДЕНИЕ
Внебольничная пневмония (ВП) является одной из наиболее важных инфекционных причин смерти в Корее [1]. Ранняя диагностика и соответствующее назначение антибиотиков имеют важное значение для снижения заболеваемости и смертности от пневмонии [2]. Многие исследования, проведенные в странах с высоким бременем туберкулеза (ТБ), показали, что Mycobacterium tuberculosis является частой причиной ВП; однако часто бывает трудно отличить легочный ТБ от бактериальной ВП на начальной стадии диагностики [3, 4].Клинические и рентгенографические признаки туберкулеза часто неспецифичны, а чувствительность микроскопического исследования откашливаемой мокроты на кислотоустойчивые бациллы составляет всего 50-60% [5].
Задержки в диагностике легочного туберкулеза могут отрицательно сказаться на заболеваемости и смертности пациентов. Кроме того, может происходить внутрибольничная передача легочного туберкулеза другим госпитализированным пациентам и медицинским работникам. Недавно в некоторых исследованиях было высказано предположение, что биомаркеры, такие как С-реактивный белок (СРБ), прокальцитонин и растворимый запускающий рецептор, экспрессируемые на миелоидных клетках, могут играть роль в различении легочного ТБ от бактериальной ВП [6-8].Однако не все эти биомаркеры доступны в странах с высоким бременем ТБ.
Отношение количества нейтрофилов к лимфоцитам (NLR) — это легко вычисляемый лабораторный маркер, используемый для оценки системного воспаления. Недавнее исследование продемонстрировало полезность лимфоцитопении для прогнозирования бактериемии путем комбинирования обычных маркеров инфекции [9]. Кроме того, де Ягер и др. [10] продемонстрировали, что лимфоцитопения и NLR превосходят уровень CRP, а также количество лейкоцитов (WBC) и нейтрофилов для прогнозирования бактериемии в отделении неотложной помощи.
В этом исследовании мы исследовали роль NLR в различении пациентов с активным легочным туберкулезом от пациентов с бактериальной ВП и сравнили диагностическую способность NLR с показателями CRP и WBC.
МЕТОДЫ
1. Пациенты
В это ретроспективное когортное исследование были включены последовательные взрослые пациенты старше 18 лет с подозрением на ВП с января 2009 года по февраль 2011 года. Пациенты с подозрением на ВП были определены как пациенты с недавно появившимися респираторными симптомами или признаками, аномальными инфильтратами на рентгенограмме грудной клетки и не госпитализированные недавно.
Критерии исключения включали использование антибиотиков в течение более 24 часов на момент регистрации, состояния, которые, как известно, влияют на общее и дифференциальное количество лейкоцитов, такие как гематологические нарушения, хронические воспалительные состояния, текущая стероидная терапия и / или история использования стероидов в течение 3 лет. за несколько месяцев до госпитализации, прохождение химиотерапии или лучевой терапии в течение 4 недель до включения в исследование, отсутствие дифференциального подсчета лейкоцитов или данных по СРБ или изменение диагноза на другой, такой как тромбоэмболия легочной артерии, отек легких или рак легких, во время наблюдения.
Были собраны демографические данные и рассчитана оценка группы по исследованию исходов у пациентов с пневмонией (PORT) [11]. Наблюдательный совет учреждения одобрил это исследование, и оно было проведено в соответствии с Хельсинкской декларацией.
2. Диагностика легочного туберкулеза или бактериального ВП
Пациенты были отнесены к группе легочного туберкулеза, когда 1) M. tuberculosis было культивировано из мокроты или жидкости бронхиального лаважа, или 2) концентрация аденозиндезаминазы составляла ≥70 МЕ / дл по данным экссудативного плеврального выпота с преобладанием лимфоцитов в сочетании с паренхиматозным поражением легкого, предполагающим легочный ТБ.Пациенты считались имеющими бактериальную ВП, когда 1) клинические признаки и новая инфильтрация на рентгенограмме грудной клетки были очевидны и полностью исчезли после лечения соответствующими антибиотиками, 2) посевы мокроты или лаважа были M. tuberculosis -отрицательными во время клинического наблюдения и 3) вирусные возбудители не обнаружены.
Для микробиологического выявления пациентов с бактериальной ВП мы выполнили окрашивание мокроты по Граму, посевы и посевы крови. Анализы на антигены в моче также использовали для обнаружения Legionella pneumophila и Streptococcus pneumoniae в соответствии с клиническими показаниями.У некоторых пациентов вирус был выделен из образцов носоглоточного секрета с использованием платформы ПЦР в реальном времени для обнаружения вируса гриппа A или B, аденовируса, метапневмовируса человека, респираторно-синцитиального вируса, риновируса и вируса парагриппа.
3. Воспалительные маркеры
Дифференциальное количество лейкоцитов и СРБ определяли до лечения антибиотиками. Общее количество лейкоцитов, нейтрофилов и лимфоцитов определяли с использованием гематологического анализатора Sysmex XE-2100 (Sysmex Corp., Кобе, Япония).NLR определяли как абсолютное количество нейтрофилов, деленное на абсолютное количество лимфоцитов. Уровни CRP измеряли с помощью автоматического турбидиметрического иммуноанализа с латексным усилением (Dimension; Dade Behring, Newark, NJ, USA; TBA-200FR; Toshiba, Tokyo, Japan) в течение 1 часа после сбора образца. Дифференциальное количество лейкоцитов, NLR и уровень CRP сравнивали между пациентами с легочным туберкулезом и пациентами с бактериальной ВП. Эти воспалительные маркеры также сравнивались между пациентами с легочным туберкулезом и пациентами с пневмонией легкой степени тяжести с индексом тяжести пневмонии PORT I или II класса риска.
4. Статистический анализ
Непрерывные данные представлены как среднее ± стандартное отклонение. Различия в непрерывных переменных между группами определяли с использованием теста Стьюдента t или теста Манна-Уитни U . Категориальные данные представлены в виде частот. Различия между категориальными переменными анализировали с помощью критерия хи-квадрат Пирсона или точного критерия Фишера. Корреляцию между NLR и CRP анализировали с помощью критерия ранговой корреляции Спирмена.Анализ кривой ROC был проведен, чтобы определить наиболее полезные пороговые уровни для NLR, CRP, количества лейкоцитов, количества нейтрофилов и лимфоцитов, чтобы определить наибольшую сумму чувствительности и специфичности для различения легочного ТБ от бактериальной ВП. Способность NLR, CRP, количества лейкоцитов, нейтрофилов и лимфоцитов отличать легочный туберкулез от бактериального ВП сравнивалась с использованием площади под кривой (AUC). Значение P ≤0,05 считалось статистически значимым. Все статистические анализы были выполнены с использованием SPSS 19.0 (SPSS Inc., Чикаго, Иллинойс, США).
РЕЗУЛЬТАТЫ
1. Пациенты
Мы включили в это исследование 206 пациентов (), из которых 112 (54,4%) имели туберкулез легких и 94 (45,6%) имели бактериальную ВП. Средний возраст пациентов с легочным туберкулезом и бактериальной ВП составлял 54 года (диапазон от 20 до 86 лет) и 70 лет (от 18 до 86 лет), соответственно. Исходные клинические характеристики перечислены в.
Блок-схема пациента.
Сокращения: WBC, лейкоцит; CRP, C-реактивный белок; FU, продолжение; ВП, внебольничная пневмония; Туберкулез, туберкулез; КУБ, кислотно-фастбациллы.
Таблица 1
Исходные клинические характеристики исследуемой популяции
Среди пациентов с легочным туберкулезом 98 (87,5%) имели M. tuberculosis респираторных проб с положительным посевом. У остальных пациентов был плевральный выпот и инфильтрация легких на рентгенограмме, совместимая с туберкулезом. Неудача лечения произошла у одного пациента.
Возбудители болезни определены у 27 (28,7%) пациентов с бактериальной ВП. Streptococcus pneumoniae был обнаружен у 17 пациентов с помощью тестов на антигены в моче, посева респираторных образцов или посева крови.Другими идентифицированными патогенами были Klebsiella pneumonia (N = 4), Escherichia coli (N = 2), метициллин-чувствительный Staphylococcus aureus (N = 1), метициллин-устойчивый S. aureus (N = 1). , Acinetobacter baumannii (N = 1) и Stenotrophomonas maltophila (N = 1). Среднее значение PSI составило 111,03. Семьдесят четыре пациента (78,7%) были отнесены к группе риска выше III класса риска PSI. У 20 пациентов (21,3%) была диагностирована пневмония легкой степени тяжести.Внутрибольничная летальность в группе ВП составила 12,8% (N = 12).
2. Маркеры воспаления
Среднее и медианное значения NLR составили 9,69 ± 9,02 и 6,36 соответственно. Общее количество лейкоцитов и нейтрофилов, NLR и CRP были значительно ниже у пациентов с легочным ТБ, чем у пациентов с бактериальной ВП, тогда как количество лимфоцитов было значительно выше у пациентов с легочным ТБ, чем у пациентов с бактериальной ВП ().
Таблица 2
Базовые лабораторные характеристики исследуемой популяции
Мы провели анализ подгрупп пациентов с легкой пневмонией (N = 20, классы риска I и II PSI) и пациентов с легочным туберкулезом для оценки диагностической способности NLR. .Общее количество лейкоцитов (7,19 ± 2,48 против 12,59 ± 5,41, P <0,001), количество нейтрофилов (4,79 ± 2,14 против 10,38 ± 4,78, P <0,001), NLR (3,67 ± 2,12 против 9,65 ± 6,41, P <0,001) и CRP (6,57 ± 7,31 против 17,48 ± 10,76, P <0,001) также были значительно ниже у пациентов с легочным туберкулезом, чем у пациентов с пневмонией легкой степени тяжести. Однако количество лимфоцитов существенно не различается между группами.
Самая сильная корреляция была отмечена между NLR и количеством нейтрофилов (r = 0.832, P = 0,01). Положительная корреляция была также обнаружена между NLR и CRP (r = 0,562, P = 0,01), а также между NLR и количеством лейкоцитов (r = 0,738, P = 0,01). Отрицательная корреляция была выявлена между NLR и количеством лимфоцитов (r = -0,644, P = 0,01).
3. Диагностическая точность для дифференциации легочного ТБ от бактериальной ВП
Значение NLR <7,0 было определено как оптимальное пороговое значение для дифференциации пациентов с легочным ТБ от пациентов с бактериальной ВП, что дало 91 балл.Чувствительность 1%, специфичность 81,9%, прогностическая ценность положительного результата 85,7% и прогностическая ценность отрицательного результата 88,5% (). Пороговое значение для CRP было менее 7,0 мг / дл. Используя это пороговое значение, CRP показал 67,5% чувствительность и 85,1% специфичность, 79,4% положительную прогностическую ценность и 75,5% отрицательную прогностическую ценность. NLR AUC (AUC, 0,93; 95% доверительный интервал [CI], 0,88-0,96) был значительно выше, чем у CRP (AUC, 0,83; 95% CI, 0,76-0,88; P = 0,0015) (). AUC NLR также была значительно выше, чем у количества лейкоцитов (AUC, 0.86; 95% ДИ 0,81-0,91; P = 0,0016), количество нейтрофилов (AUC, 0,89; 95% ДИ, 0,84-0,93; P = 0,0197) и количество лимфоцитов (AUC, 0,74; 95% ДИ, 0,68-0,80; P <0,0001 ). У пациентов с легкой пневмонией NLR AUC (AUC, 0,87; 95% ДИ, 0,76-0,92) был значительно выше, чем у количества лимфоцитов (AUC, 0,61; 95% ДИ, 0,52-0,69; P = 0,0019). Однако не было значимой разницы в AUC между NLR и CRP (AUC, 0,81; 95% ДИ, 0,72-0,88; P = 0.5721), количество NLR и лейкоцитов (AUC, 0,81; 95% ДИ, 0,73-0,87; P = 0,3523), а также NLR и количество нейтрофилов (AUC, 0,86; 95% ДИ, 0,79-0,91; P = 0,8466 ).
ROC-кривые C-реактивного белка (CRP) и отношения нейтрофилов к лимфоцитам (NLR) для дифференциации туберкулеза от бактериальной внебольничной пневмонии. Площадь под кривой для NLR (AUC, 0,93; 95% доверительный интервал [CI], 0,88-0,96) была значительно больше, чем для CRP (AUC, 0,83; 95% CI, 0,76-0,88) ( P = 0 .0015).
Таблица 3
Диагностическая валидность NLR, CRP и WBC с дифференциальным подсчетом для дифференциации легочного ТБ от бактериальной ВП
ОБСУЖДЕНИЕ
В этом исследовании последовательных пациентов, набранных из клинических учреждений, NLR был полезным лабораторным маркером для различения между пациентами с легочным туберкулезом и другими бактериальными ВП на начальном этапе диагностики при промежуточной распространенности туберкулеза. Результаты этого исследования включали следующее: 1) уровни NLR в сыворотке были значительно ниже у пациентов с легочным туберкулезом, чем у пациентов с бактериальной ВП; 2) NLR <7 было оптимальным пороговым значением для дифференциации пациентов с легочным туберкулезом от пациентов с бактериальной ВП; 3) Диагностическая способность NLR превосходила возможности CRP, количества лейкоцитов, нейтрофилов и лимфоцитов для дифференциации пациентов с легочным туберкулезом от пациентов с бактериальной ВП.Это первое исследование, демонстрирующее диагностическую способность NLR различать легочный ТБ и бактериальную ВП.
Корея является страной с промежуточным бременем туберкулеза: в 2009 г. было впервые диагностировано около 43 000 случаев туберкулеза легких [12]. Частота выявления M. tuberculosis у пациентов с подозрением на ВП достигает 12% в Гонконге [4] и 21% в Сингапуре [13]; Распространенность туберкулеза в этих странах такая же, как в Корее. Отличить легочный туберкулез от ВП важно для общественного здравоохранения; Немедленная изоляция и раннее лечение противотуберкулезными препаратами имеют важное значение для пациентов с легочным туберкулезом.Однако отличить легочный ТБ от ВП только на основании анамнеза, физикального обследования и рентгенологических данных часто бывает сложно. Следовательно, необходим быстрый и доступный тест, чтобы отличить легочный туберкулез от ВП.
Физиологические иммунные ответы циркулирующих лейкоцитов на различные стрессовые события характеризуются увеличением количества нейтрофилов и уменьшением количества лимфоцитов. Увеличение общего количества лейкоцитов и нейтрофилов является воспалительной реакцией, особенно вызванной бактериальной инфекцией [14].Лимфоцитопения также описывается как диагностический маркер бактериальной инфекции [9]. Следовательно, считается, что NLR имеет более сильную дискриминационную способность для прогнозирования бактериемии по сравнению с дискриминацией, основанной только на нейтрофилии или лимфоцитопении. Goodman et al. [15] первоначально предположили полезность NLR для диагностики пациентов с подозрением на аппендицит. В их исследовании NLR был более чувствительным параметром бактериальной инфекции, чем увеличение количества лейкоцитов. Zahorec et al.[14] провели проспективное продольное обсервационное исследование, в котором они сообщили о корреляции между тяжестью клинического течения и лимфоцитопенией у пациентов с тяжелым сепсисом и септическим шоком в онкологическом отделении интенсивной терапии. Они предложили использовать NLR в качестве дополнительного маркера инфекции в отделении интенсивной терапии [14]. Недавно de Jager et al. [10] продемонстрировали, что лимфоцитопения и NLR были лучшими прогностическими факторами бактериемии, чем обычные параметры, такие как уровень CRP, количество лейкоцитов и нейтрофилов в отделении неотложной помощи.В настоящее время NLR вызывает интерес как средство прогнозирования выживаемости в различных клинических ситуациях, от онкологических до сердечно-сосудистых заболеваний [16-19].
NLR плевральной жидкости был оценен как дополнительный диагностический инструмент у пациентов с туберкулезным плевритом [20, 21]. CD4 + Т-лимфоциты и макрофаги играют важную роль в патогенезе ТБ, поскольку участвует клеточный иммунитет. Напротив, нейтрофилия является первичным клеточным явлением во время развития бактериальной ВП.Следовательно, NLR образцов крови может быть хорошим лабораторным маркером для дифференциации пациентов с легочным туберкулезом от пациентов с бактериальной ВП.
В этом исследовании общие лейкоциты с дифференциальным подсчетом, CRP и NLR значительно различались в группе легочного ТБ и группе бактериальной ВП. NLR был самым мощным дискриминационным маркером, о чем свидетельствует его высокая AUC. Подсчет нейтрофилов был вторым лучшим отличительным маркером, за ним следовали количество лейкоцитов, CRP и лимфоцитов.Примечательно, что легко поддающиеся оценке параметры общего анализа крови, такие как общее количество лейкоцитов и нейтрофилов, также продемонстрировали значительную различительную способность, хотя и меньшую, чем у NLR. Более того, их чувствительность, специфичность и точность были относительно высокими.
NLR можно легко определить при обычном лабораторном обследовании, и это простое соотношение доступно в большинстве учреждений. Кроме того, NLR — более простой и менее дорогой метод по сравнению с другими воспалительными биомаркерами, такими как CRP, прокальцитонин и растворимый запускающий рецептор, экспрессируемый на миелоидных клетках, которые недавние исследования предложили в качестве маркеров дифференциальной диагностики [6-8].
Однако в этом исследовании есть несколько ограничений. Во-первых, он был ретроспективным, нерандомизированным и проводился в едином центре; таким образом, это было предметом систематической ошибки отбора. Необходимы исследования с привлечением большего размера выборки и проспективный анализ. Во-вторых, патогены, вызывающие ВП, могли быть идентифицированы только у меньшинства пациентов. Однако патогены, вызывающие ВП, четко не определены [22, 23]. В-третьих, другие воспалительные маркеры, такие как прокальцитонин, не были включены и сравнивались с NLR в текущем анализе.Однако прокальцитонин — дорогостоящее обследование, которое доступно не во всех больницах.
В заключение, текущее исследование показало, что NLR, полученный из одного образца крови на начальном этапе диагностики, является очень полезным лабораторным маркером для дифференциации пациентов с легочным туберкулезом от пациентов с бактериальной ВП. Диагностическая способность NLR превосходит возможности CRP, лейкоцитов, нейтрофилов и лимфоцитов. Следовательно, NLR следует включать в рутинные обследования пациентов с неоднозначным диагнозом между легочным туберкулезом и бактериальной ВП.
Бесплатное обновление до WBC
введение
Отношение нейтрофилов / лимфоцитов (NLR) привлекает все большее внимание во многих областях медицины в течение последних пяти лет. В настоящее время в PubMed опубликовано 2230 публикаций по этому поводу, в основном за последние несколько лет. В этом посте мы попытаемся создать основу для понимания этого соотношения.
обзоропределение и физиология
NLR — это просто количество нейтрофилов, деленное на количество лимфоцитов.При физиологическом стрессе количество нейтрофилов увеличивается, а количество лимфоцитов уменьшается. NLR сочетает в себе оба этих изменения, что делает его более чувствительным, чем любое из них по отдельности:
Эндогенный кортизол и катехоламины могут быть основными движущими силами NLR. Известно, что повышенный уровень кортизола увеличивает количество нейтрофилов, одновременно уменьшая количество лимфоцитов. 1 Точно так же эндогенные катехоламины (например, адреналин) могут вызывать лейкоцитоз и лимфопению. 2 Также вероятно участие цитокинов и других гормонов.
Таким образом, NLR — это , а не исключительно как указание на инфекцию или воспаление. Любая причина физиологического стресса может увеличить NLR (например, гиповолемический шок).
NLR быстро увеличивается после острого физиологического стресса (<6 часов). 3 Такое быстрое время отклика может сделать NLR лучшим отражением острого стресса, чем лаборатории, которые реагируют медленнее (например.грамм. количество лейкоцитов или бандемия). 4
Расчети приблизительный диапазон значений
NLR может быть вычислено с использованием либо абсолютных значений ячеек, либо процентов , как показано здесь:
Интерпретация NLR зависит от клинического контекста. Однако, чтобы дать некоторое представление о том, как это интерпретировать:
- Нормальный NLR примерно 1-3.
- NLR от 6 до 9 предполагает легкий стресс (например, пациент с неосложненным аппендицитом).
- Критически больные пациенты часто имеют NLR ~ 9 или выше (иногда достигая значений, близких к 100).
Это только очень общая интерпретация NLR. Клинический контекст должен значительно влиять на интерпретацию NLR. Например, воспалительные расстройства могут иметь тенденцию к повышению NLR больше, чем невоспалительные расстройства. Таким образом, пациент с сепсисом и NLR 15 может не сильно болеть, тогда как пациент с тромбоэмболией легочной артерии и NLR 15 вызывает большее беспокойство.
NLR против сдвига влево (т. Е. Бандемия)
NLR имеет некоторое сходство с бандемией — оба могут использоваться для распознавания физиологического стресса при отсутствии сильно отклоняющегося от нормы количества лейкоцитов.
Основным преимуществом NLR перед бандемией может быть то, что его можно более воспроизводимо измерить. В литературе существует по крайней мере три различных определения палочкоядерных нейтрофилов. 4 Это приводит к значительным различиям между больницами в отношении нормального диапазона и чувствительности к бандемии.
подводных камня NLR
Следует отметить следующие подводные камни: 5
- Экзогенный стероид : Может напрямую увеличивать NLR.
- Активное гематологическое заболевание : Лейкоз, цитотоксическая химиотерапия или фактор, стимулирующий колонии гранулоцитов (G-CSF), могут влиять на количество клеток.
- ВИЧ : Некоторые исследования исключали пациентов с ВИЧ. В целом польза NLR для этой популяции пациентов остается неясной.Можно ожидать, что пациенты с запущенным СПИДом и хронической лимфопенией будут иметь более высокий исходный NLR.
Литература переполнена исследованиями с использованием NLR для всего, от сепсиса до рака и синдрома беспокойных ног. 6 Однако, если NLR является показателем на каждое заболевание, то на самом деле это показатель без заболевания . Очевидно, что NLR не может быть волшебным тестом для каждого состояния.
Чтобы использовать NLR с умом, нам нужно задавать правильный вопрос в нужное время.Например, давайте рассмотрим два возможных использования NLR:
.- (a) Отличие септического шока от кардиогенного шока среди популяции пациентов с шоком в отделении интенсивной терапии.
- (b) Выявление токсического шока от аденовируса среди популяции пациентов с вирусными симптомами.
В первом сценарии все пациентов испытывают сильный физиологический стресс (от септического шока или кардиогенного шока). Во втором сценарии пациенты с токсическим шоком будут испытывать больший физиологический стресс, чем пациенты с гриппом.Таким образом, в сценарии (а) NLR не удастся, но в сценарии (b) может быть успешным.
Ключом к использованию NLR является поиск клинического сценария, в котором уровень физиологического стресса выявляется. Таким образом, критически важны контекст и клинический вопрос. Есть примерно три разумных способа использования NLR:
, использование № 1: диагностика, основанная на обнаружении
скрытого физиологического стресса среди пациентов с аналогичными проявлениямиЭто иллюстрируют два примера:
- Среди пациентов, поступающих в отделение неотложной помощи с вирусными симптомами, большинство из них имеют незначительные вирусные заболевания, но у некоторых будет менингит или бактериемия (сценарий (b) выше).
- Среди пациентов, поступивших в неотложную помощь с болью в правом нижнем квадранте, у большинства будет гастроэнтерит, но у некоторых будет аппендицит.
Ключевым моментом здесь является то, что в узком клиническом контексте конкретных диагнозов часто связаны с более высокими уровнями физиологического стресса (например, аппендицит вызывает больше физиологического стресса, чем гастроэнтерит). Напротив, NLR не обязательно сможет определять диагнозы, связанные с аналогичным уровнем физиологического стресса (например, ).грамм. менингит против токсического шока).
использование # 2: прогноз для пациентов с известным диагнозом
Среди группы пациентов с известным диагнозом NLR может выявить самые больные пациенты. Как и в примере №1 выше, ключевым моментом здесь является то, что мы начинаем с довольно однородной группы пациентов. Затем NLR позволяет нам определить, какие пациенты испытывают наибольший физиологический стресс (что подразумевает худший прогноз).
использование # 3: индивидуальная траектория во времени
Анализ динамики NLR у отдельного пациента может дать некоторую информацию о степени физиологического стресса, которому он подвергается.Снижение NLR может быть благоприятным признаком, тогда как увеличение NLR может указывать на неэффективность лечения. Прогнозируемые траектории NLR будут варьироваться в зависимости от диагноза и ожидаемого клинического течения.
примеры: диагностикадиагноз аппендицит
Недавний мета-анализ NLR для диагностики аппендицита объединил 17 исследований, чтобы сделать следующие выводы: 7
- NLR> 4.7 на 89% чувствительна и на 90% специфична для диагностики аппендицита.
- NLR> 8,8 является 77% чувствительным и 100% специфичным для диагноза осложненного аппендицита.
Роль NLR в диагностике аппендицита остается дискуссионной. Однако кажется очевидным, что NLR является значительным улучшением количества лейкоцитов (и, возможно, он должен заменить количество лейкоцитов при любом диагностическом рассмотрении).
диагноз бактериемии
В нескольких исследованиях оценивалась способность NLR обнаруживать бактериемию, в основном в гетерогенных популяциях пациентов, обращающихся в отделение неотложной помощи.Его производительность оставляет желать лучшего. Мета-анализ показывает, что с порогом ~ 10, NLR имеет чувствительность 72% и специфичность 60%. 8
Тем не менее, NLR легко превосходит количество лейкоцитов (что здесь ужасно). 9,10
Эффективность NLR для бактериемии среди недифференцированных пациентов ограничена из-за гетерогенной природы этой популяции (рисунок ниже). Многие пациенты испытывают тяжелый физиологический стресс (с повышенным NLR) без бактериемии .С другой стороны, некоторые пациенты с бактериемией переносят это на удивление хорошо и не очень больны. Короче говоря, — нереально, — ожидать от NLR хороших результатов в этом контексте. Это не отказ самого теста, а скорее нарушение его правильного применения.
диагностика септического шока
Ljungstrom et al. Оценили эффективность нескольких маркеров среди 1572 пациентов, поступивших в отделение неотложной помощи с клиническим подозрением на сепсис. 11 Как показано ниже, ни один тест не был выдающимся. В целом, NLR имел схожую эффективность по сравнению с лактатом или прокальцитонином:
Здесь показаны характеристики различных тестовых пороговых значений:
При пороговом значении 3 (верхний предел нормы) NLR имеет более высокую чувствительность к сепсису, чем любой другой тест (95%). Таким образом, нормальный NLR (<3) свидетельствует против сепсиса. В качестве альтернативы, если NLR значительно больше 10, это подтверждает диагноз сепсиса. Промежуточные значения попадают в серую зону.
Ограничения NLR здесь аналогичны ограничениям, с которыми мы сталкивались при бактериемии, описанной выше: в гетерогенной популяции пациентов трудно интерпретировать NLR. Тем не менее, экстремальные значения NLR могут быть информативными.
примеры: прогнозпрогноз тромбоэмболии легочной артерии
В нескольких исследованиях оценивалось использование NLR для прогнозирования смертности при тромбоэмболии легочной артерии. Мета-анализ показывает, что NLR может более точно предсказывать смертность, чем тропонин. 12,13
Одним из ограничений вышеупомянутого метаанализа является то, что в различных исследованиях использовались разные значения отсечения для NLR (в большинстве исследований использовались пороговые значения между 5,5–5,9, но в одном исследовании использовалось пороговое значение 9,2). Данные двух наиболее противоречивых исследований показаны ниже: 14,15
Несмотря на разногласия между исследованиями, следующая интерпретация NLR в контексте PE может быть разумной:
Проблема в PE всегда состоит в том, чтобы интегрировать бесчисленное множество прогностических индикаторов (например, ).грамм. если КТ показывает напряжение правого желудочка, то эхокардиограмма, показывающая то же самое, может показаться пугающей, но она не добавляет новой информации). Таким образом, неясно, насколько NLR может добавить к прогнозу пациента, у которого уже были выполнены многочисленные прогностические тесты (например, тропонин, натрийуретический пептид мозга, эхокардиограмма, лактат). Одной из потенциальных ролей NLR может быть ранний сигнал о том, что пациент относится к группе высокого риска, потому что NLR, как правило, будет получен с помощью начальной лабораторной панели (таким образом, сразу же доступен для всех пациентов).
прогноз острого панкреатита
NLR довольно хорошо предсказывает тяжелый панкреатит (площадь под кривой ROC ~ 0,75) и смертность (площадь под кривой ROC ~ 0,8). 16–20 NLR превосходит С-реактивный белок — тест, который иногда рекомендуется для прогнозирования при панкреатите. 20,21 В таблице ниже показано приблизительное руководство по интерпретации NLR в контексте острого панкреатита.
При стратификации риска при панкреатите не следует уделять слишком много внимания NLR (другие факторы, такие как функция органов, гораздо более важны).Однако, если есть желание использовать прогностический лабораторный тест в качестве решающего аргумента, который поможет направить решение, NLR может предоставить некоторую информацию.
прогноз септического шока
Это немного сложно. Прежде чем мы перейдем к NLR, найдите время, чтобы рассмотреть взаимосвязь между кортизолом и смертностью при септическом шоке. Как показано выше, это соотношение немного напоминает J-образную кривую: 22
- Низкий уровень кортизола может коррелировать с несколько повышенной смертностью — это может отражать истощение надпочечников или лежащую в основе надпочечников недостаточность.Отсутствие любого ответа кортизола является патологическим , что делает пациента уязвимым для стресса.
- Промежуточные уровни кортизола , похоже, коррелируют с лучшей выживаемостью.
- Самый высокий уровень кортизола коррелирует с худшей выживаемостью — эти пациенты подвергаются чрезвычайно интенсивному физиологическому стрессу.
Данные, касающиеся NLR, отражают эту J-образную кривую: 23
Это подчеркивает важность использования NLR на основе фактических данных. Априори можно было ожидать, что низкий NLR будет иметь благоприятный прогноз. Однако в контексте септического шока нормальный NLR дезадаптивный — и это фактически несет неблагоприятный прогноз . Интересно предположить, что пациенты с сепсисом с NLR <2 имеют вялую эндогенную реакцию на стресс и, следовательно, могут получить пользу от поддержки экзогенными стероидами и катехоламинами. Другой причиной плохих результатов в группе с низким NLR является нейтропения, связанная с раком.
Это означает, что в целом прогноз должен сочетать и NLR и степень гемодинамической нестабильности пациента. Как предложено ниже, низкий NLR может быть обнадеживающим только у гемодинамически стабильного пациента :
примеры: траекториятраектория бактериемии
Terradas 2012 оценил тенденции NLR среди пациентов с бактериемией (рисунок ниже). 24 Среди выживших NLR снизился за несколько дней.С другой стороны, у не выживших постоянно были повышенные значения NLR. Это говорит о том, что стойкое повышение NLR в течение нескольких дней является плохим прогностическим признаком, поднимающим вопрос о неэффективности лечения:
траектория внутричерепного кровоизлияния
Wang 2018 сообщил о тенденциях NLR среди пациентов со спонтанным внутричерепным кровоизлиянием (рисунок ниже). 25 Не выжившие испытали увеличение NLR на в течение 24-48 часов, тогда как у выживших было стабильное NLR.Исходно у всех пациентов был довольно низкий NLR, что позволяет предположить, что внутричерепное кровоизлияние не обязательно вызывает сильную системную стрессовую реакцию.
в целом: использование NLR для определения траектории
В этом разделе снова подчеркивается важность интерпретации NLR в надлежащем контексте . Для пациента с бактериемией тогда NLR будет изначально высоким, но должен уменьшиться с терапией. В качестве альтернативы, в контексте внутричерепного кровоизлияния, NLR начинается с низкого уровня, и обычно остается низким у выживших.Невозможно сделать универсального утверждения относительно NLR при различных болезненных состояниях; кинетика будет варьироваться в зависимости от естественного течения любого конкретного заболевания.
выводыNLR — далеко не идеальный тест. Однако недостаток точности компенсируется скоростью и стоимостью. Почти все пациенты получат дифференциальный подсчет клеток при поступлении, поэтому NLR является бесплатным и доступен сразу после госпитализации (данные находятся прямо в таблице).Большинству пациентов также будут сделаны серийные анализы крови во время госпитализации, что позволит отслеживать NLR в течение долгого времени.
Имеет смысл использовать NLR вместо подсчета лейкоцитов. В каждом исследовании, напрямую сравнивающем NLR с количеством лейкоцитов, NLR оказался гораздо более точным. Наше использование количества лейкоцитов в качестве клинического маркера основано на инерции — мы к этому привыкли, и он доступен немедленно. Автоматическое определение количества лейкоцитов делает практически невозможным отказ от использования этого теста.Учитывая доступность NLR, использование NLR для замены лейкоцитов на кажется естественной эволюцией.
Цель этого поста — не , чтобы побудить всех немедленно начать принимать важные клинические решения на основе NLR. Скорее, он предназначен как стимул для того, чтобы обратить внимание на NLR. Начните изучать NLR ваших пациентов и подумать, как это согласуется с их диагнозами и прогнозами. Со временем это позволит откалибровать ваше клиническое суждение о том, как NLR может вписаться в вашу популяцию пациентов и клинический контекст.
- Отношение нейтрофилов к лимфоцитам (NLR) легко рассчитывается из дифференциального подсчета клеток. Таким образом, он доступен сразу (бесплатно) для всех ваших пациентов.
- NLR — это отражение физиологического стресса, возможно, наиболее непосредственно связанного с уровнями кортизола и катехоламинов.
- NLR может быть полезным инструментом для сортировки пациентов, которые более больны, по сравнению с менее больными (это , а не , специфичный для инфекции).
- NLR оказался более полезным, чем количество лейкоцитов (WBC), когда их сравнивают напрямую.В конечном счете, NLR может быть логической заменой WBC. В некоторых ситуациях NLR может конкурировать с более дорогими биомаркерами (например, прокальцитонином, лактатом).
- В определенных клинических условиях (например, панкреатит, тромбоэмболия легочной артерии) NLR может иметь удивительно хорошее прогностическое значение.
Список литературы
1.
Онсруд М., Торсби Э. Влияние гидрокортизона in vivo на некоторые субпопуляции лимфоцитов крови человека. I. Влияние на активность естественных клеток-киллеров. Сканд Дж. Иммунол . 1981; 13 (6): 573-579. https://www.ncbi.nlm.nih.gov/pubmed/7313552.2.
Беншоп Р., Родригес-Фейерхан М., Щедловски М. Катехоламин-индуцированный лейкоцитоз: ранние наблюдения, текущие исследования и будущие направления. Иммунное поведение мозга . 1996; 10 (2): 77-91. https://www.ncbi.nlm.nih.gov/pubmed/8811932.6.
Варим С., Акар Б., Уяник М. и др.Связь между соотношением нейтрофилов и лимфоцитов, новым маркером системного воспаления, и синдромом беспокойных ног. Сингапур Мед. J . 2016; 57 (9): 514-516. https://www.ncbi.nlm.nih.gov/pubmed/27662970.7.
Хаджибанде С., Хаджибандех С., Хоббс Н., Мансур М. Соотношение нейтрофилов и лимфоцитов позволяет прогнозировать острый аппендицит и различает осложненный и неосложненный аппендицит: систематический обзор и метаанализ. Am J Surg .Апрель 2019 г. https://www.ncbi.nlm.nih.gov/pubmed/31056211.8.
Jiang J, Liu R, Yu X и др. Соотношение нейтрофилов и лимфоцитов как диагностический маркер бактериемии: систематический обзор и метаанализ. Am J Emerg Med . Октябрь 2018 г. https://www.ncbi.nlm.nih.gov/pubmed/30413366.9.
de J, van W, Mathoera R, de J-L, van der, Wever P. Лимфоцитопения и соотношение количества нейтрофилов и лимфоцитов предсказывают бактериемию лучше, чем обычные маркеры инфекции в отделении неотложной помощи. Crit Care . 2010; 14 (5): R192. https://www.ncbi.nlm.nih.gov/pubmed/21034463.10.
Лоусби Р., Гомес С., Джарман И. и др. Соотношение нейтрофилов и лимфоцитов как ранний индикатор инфекции кровотока в отделении неотложной помощи. Emerg Med J . 2015; 32 (7): 531-534. https://www.ncbi.nlm.nih.gov/pubmed/25183249.11.
Ljungström L, Pernestig A, Jacobsson G, Andersson R, Usener B, Tilevik D. Диагностическая точность прокальцитонина, соотношения нейтрофилов и лимфоцитов, C-реактивного белка и лактата у пациентов с подозрением на бактериальный сепсис. PLoS One . 2017; 12 (7): e0181704. https://www.ncbi.nlm.nih.gov/pubmed/28727802.12.
Ван К., Ма Дж., Цзян З., Мин Л. Прогностическое значение соотношения нейтрофилов и лимфоцитов и соотношения тромбоцитов и лимфоцитов при острой тромбоэмболии легочной артерии: систематический обзор и метаанализ. Инт Ангиол . 2018; 37 (1): 4-11. https://www.ncbi.nlm.nih.gov/pubmed/28541022.13.
Bajaj A, Saleeb M, Rathor P, Sehgal V, Kabak B, Hosur S.Прогностическое значение тропонинов при острой немассивной тромбоэмболии легочной артерии: метаанализ. Сердце легкое . 2015; 44 (4): 327-334. https://www.ncbi.nlm.nih.gov/pubmed/25976228.14.
Караташ М., Ипек Г., Онук Т. и др. Оценка прогностической ценности отношения нейтрофилов к лимфоцитам и отношения тромбоцитов к лимфоцитам у пациентов с тромбоэмболией легочной артерии. Acta Cardiol Sin . 2016; 32 (3): 313-320. https://www.ncbi.nlm.nih.gov/pubmed/27274172.15.
Кайрак М., Эрдоган Х., Солак Ю. и др. Прогностическое значение отношения нейтрофилов к лимфоцитам у пациентов с острой тромбоэмболией легочной артерии: рестроспективное исследование. Сердце легкого Circ . 2014; 23 (1): 56-62. https://www.ncbi.nlm.nih.gov/pubmed/23856365.16.
Jeon T, Park J. Клиническое значение соотношения нейтрофилов и лимфоцитов как раннего прогностического маркера неблагоприятных исходов у пациентов с острым панкреатитом. Мир Дж. Гастроэнтерол . 2017; 23 (21): 3883-3889.https://www.ncbi.nlm.nih.gov/pubmed/28638228.17.
Хан Ц., Цзэн Дж., Лин Р. и др. Полезность соотношения нейтрофилов к лимфоцитам и секвестрации жидкости в качестве раннего предиктора тяжелого острого панкреатита. Научная репутация . 2017; 7 (1): 10704. https://www.ncbi.nlm.nih.gov/pubmed/28878366.18.
Zhang Y, Wu W, Dong L, Yang C, Fan P, Wu H. Отношение нейтрофилов к лимфоцитам предсказывает стойкую органную недостаточность и внутрибольничную смертность в азиатско-китайской популяции острого панкреатита. Медицина (Балтимор) . 2016; 95 (37): e4746. https://www.ncbi.nlm.nih.gov/pubmed/27631223.19.
Ван И, Фуэнтес Х, Аттар Б., Джайсвал П., Деметрия М. Оценка прогностической ценности отношения нейтрофилов к лимфоцитам у пациентов с острым панкреатитом, вызванным гипертриглицеридемией. Панкреатология . 2017; 17 (6): 893-897. https://www.ncbi.nlm.nih.gov/pubmed/278.
20.
Ли Ю., Чжао Ю., Фэн Л., Го Р. Сравнение прогностических значений маркеров воспаления у пациентов с острым панкреатитом: ретроспективное когортное исследование. BMJ Открыть . 2017; 7 (3): e013206. https://www.ncbi.nlm.nih.gov/pubmed/28348184.21.
Чо С., Юнг С., Ли К., Ким Дж. Отношение нейтрофилов к лимфоцитам и соотношение тромбоцитов к лимфоцитам может предсказать тяжесть желчнокаменного панкреатита. БМК Гастроэнтерол . 2018; 18 (1): 18. https://www.ncbi.nlm.nih.gov/pubmed/29370777.24.
Террадас Р., Грау С., Бланч Дж. И др. Число эозинофилов и соотношение нейтрофилов и лимфоцитов как прогностические маркеры у пациентов с бактериемией: ретроспективное когортное исследование. PLoS One . 2012; 7 (8): e42860. https://www.ncbi.nlm.nih.gov/pubmed/223.
25.
Ван Ф., Сюй Ф., Цюань Й. и др. Раннее увеличение отношения нейтрофилов к лимфоцитам предсказывает 30-дневную смертность у пациентов со спонтанным внутримозговым кровоизлиянием. CNS Neurosci Ther . 2019; 25 (1): 30-35. https://www.ncbi.nlm.nih.gov/pubmed/29767470.
Джош — создатель PulmCrit.org. Он доцент кафедры легочной медицины и реанимации в Университете Вермонта.
Последние сообщения Джоша Фаркаса (посмотреть все)Несмотря на положительные исследования, отношение нейтрофилов к лимфоцитам не готово для клинического использования
Основываясь на доступных клинических данных, соотношение нейтрофилов и лимфоцитов (NLR) пациента является привлекательным кандидатом в прогностический биомаркер для пациентов с мочеполовой и другими формами рака, что свидетельствует о серии недавно опубликованных исследований. Но результаты неоднозначны, и еще слишком рано для его повседневного использования для стратификации пациентов, предупреждают исследователи.
Полный анализ крови (CBC) — это рутинное клиническое обследование пациентов с диагнозом рака, и прогностические биомаркеры, основанные на таких лабораторных данных, были бы желанным дополнением к критериям стратификации пациентов.
Недавние исследования показывают, что исходные — и даже послеоперационные — NLR пациентов (измеренные путем деления количества нейтрофилов на количество лимфоцитов) могут быть прогностическим маркером исходов при нескольких типах рака. 1-5
Продолжить чтение
Связь NLR с исходами онкологических больных биологически правдоподобна, потому что NLR является показателем воспалительных процессов.
К сожалению, это также оставляет NLR неспецифическим для прогрессирования опухоли, что, вероятно, осложняется такими сопутствующими заболеваниями, как метаболический синдром, диабет, гипертония, дисфункция щитовидной железы, инфекция и другие состояния или расстройства, влияющие на воспаление, не говоря уже о лекарствах, используемых для лечения этих состояний. 6
«Некоторые люди говорят, что NLR является мерой системного воспалительного состояния и что это может повлиять на прогрессирование рака», — пояснил Эрик Охерхольм, доктор медицинских наук, врач по радиационной онкологии в больнице Пенсильванского университета в Филадельфии.«Другие исследователи отметили, что пациенты с высоким уровнем нейтрофилов также имеют высокий уровень сигналов, способствующих росту [цитокинов], для опухолей. А низкий уровень лимфоцитов может означать, что иммунная система организма не может хорошо реагировать на рак. Таким образом, высокий уровень нейтрофилов плюс низкий уровень лимфоцитов (высокий NLR) может отражать среду, которая способствует прогрессированию рака ».
СВЯЗАННЫЙ: Соотношение нейтрофилов и лимфоцитов может предсказать выживаемость при раке головы и шеи
Недавние исследования показали, что NLR предсказывает прогрессирование, рецидив и даже общую выживаемость пациентов при раке мочеполовой системы, таком как рак мочевого пузыря и светлоклеточный почечно-клеточный рак. 1,2
«Повышенный предоперационный NLR связан с плохим прогнозом у пациентов с метастатическим раком почки», — заключили авторы одного исследования. 2 «Предоперационная NLR — полезный инструмент, который может прогнозировать прогноз, стратифицировать пациентов для послеоперационного наблюдения и помогать принимать решения о лечении».
Но другие эксперты, с которыми связался консультант по терапии рака , призвали к осторожности.
Neutrophilia — обзор | Темы ScienceDirect
Нейтрофилия
Нейтрофилия может развиться в результате увеличения производства и / или высвобождения нейтрофилов из костного мозга, уменьшения движения нейтрофилов из крови в ткани или чистого движения нейтрофилов от MNP к CNP, как показано на Рисунке 5-31.Нейтрофилия быстро развивается в крови после высвобождения катехоламинов (норадреналина и адреналина), как это происходит при ранних физических нагрузках, страхе или возбуждении. Это происходит в результате смещения нейтрофилов от MNP к CNP. 43 Количество ячеек обычно не превышает двукратного значения нормы, и сдвига влево не происходит (Таблица 5-1). Продолжительные упражнения, особенно в жаркой среде, также приводят к высвобождению кортизола, что может усилить нейтрофилию, как обсуждается ниже. 65 У некоторых животных может быть сопутствующий лимфоцитоз.Эффекты лейкограммы должны вернуться к норме в течение 30 минут после удаления раздражителя. 226
Повышенное эндогенное высвобождение или экзогенное введение глюкокортикоидных стероидов оказывает сильное влияние на количество циркулирующих кровяных телец в течение нескольких часов после высвобождения или введения. Возможные причины повышенного эндогенного высвобождения глюкокортикоидов включают боль, травмы, длительный эмоциональный стресс, интенсивные продолжительные упражнения, высокую температуру тела и гиперадренокортицизм. 65,111 Продолжительность воздействия зависит от природы вводимого экзогенного глюкокортикоида (длительного или короткого действия). Нейтрофилия возникает из-за того, что глюкокортикоиды вызывают повышенное высвобождение зрелых нейтрофилов из запасов костного мозга и снижение выхода нейтрофилов из крови в ткани. 77,111,226 Вызванное глюкокортикоидами высвобождение нейтрофилов из костного мозга снижается у пожилых людей. 83 В CNP также присутствует более высокая доля нейтрофилов по сравнению с MNP, но размер MNP на самом деле не может быть уменьшен, потому что общий пул нейтрофилов крови увеличивается.Абсолютное количество нейтрофилов редко превышает норму в два раза, и сдвиг влево практически отсутствует. Глюкокортикоиды также вызывают лимфопению и эозинопению у всех домашних животных (см. Таблицу 5-1). Моноцитоз обычно наблюдается у собак и иногда у кошек. 226 Степень нейтрофилии со временем уменьшается, но лимфопения и эозинопения сохраняются, пока концентрация глюкокортикоидов в плазме увеличивается. Например, у большинства собак с гиперадренокортицизмом, зависимым от гипофиза, наблюдается лимфопения и эозинопения с нормальным количеством нейтрофилов. 281,334
Нейтрофилия без значительного сдвига влево также может присутствовать в связи с кровотечением, гемолизом, некрозом, токсичностью химических веществ и лекарств, злокачественными новообразованиями, легким воспалением и некоторыми хроническими воспалительными состояниями. Механизм, вызывающий нейтрофилию при этих расстройствах, не всегда ясен. Различные состояния, включая гипертермию, могут привести к повышению концентрации гемопоэтических факторов роста (особенно G-CSF) в кровотоке, что приводит к увеличению выработки и высвобождения нейтрофилов. 132,340,468 Воспалительные цитокины IL-1 и TNF-α вызывают нейтрофилию, стимулируя выработку факторов роста, таких как G-CSF и GM-CSF. 421 При легких воспалительных состояниях и некоторых хронических воспалительных состояниях повышенная периферическая потребность в нейтрофилах удовлетворяется за счет увеличения производства и высвобождения зрелых нейтрофилов из костного мозга.
Реакция нейтрофилов на воспалительные раздражители у жвачных животных более приглушена, чем у других домашних животных.Нейтрофилия встречается реже, а нейтропения чаще встречается в ответ на острые бактериальные инфекции у жвачных животных по сравнению с другими видами. Общее количество лейкоцитов от 20 до 30 × 10 3 / мкл считается заметно повышенным у жвачных животных. Обнаружение повышенных концентраций белков острой фазы, таких как гаптоглобин и фибриноген, может свидетельствовать о хроническом воспалении, которое может не отображаться на лейкограмме. 452
Заметный сдвиг влево часто связан с воспалительными состояниями.Это могут быть инфекционные (особенно бактериальные) 251,311 или неинфекционные (повреждение тканей, иммуноопосредованные) нарушения. 17 215 247 317 Наличие значительного сдвига влево указывает на то, что стимул к высвобождению нейтрофилов из костного мозга больше, чем может быть обеспечен высвобождением только из запасов зрелых нейтрофилов. Регенеративные сдвиги влево обычно рассматриваются как адекватная реакция костного мозга в тот момент. Однако наличие значительной цитоплазматической токсичности требует осторожного прогноза.Заметный лейкоцитоз (общее количество лейкоцитов более 50 000 / мкл) с нейтрофилией и заметный сдвиг влево, по крайней мере, к миелоцитам, связанный с воспалительным состоянием, называется «лейкемоидной реакцией», потому что он напоминает картину крови, наблюдаемую при CML. Сдвиги влево, связанные с лейкемоидными реакциями, обычно упорядочены, причем зрелые сегментированные нейтрофилы являются наиболее многочисленными нейтрофильными клетками, полосы являются следующими по численности, метамиелоциты менее многочисленны, а миелоциты присутствуют в наименьшем количестве.При наличии лейкемоидной реакции подозревают локализованное гнойное воспалительное состояние, такое как пиометра. 226
Заболевания, которые могут стимулировать крайний нейтрофильный лейкоцитоз у собак и кошек (количество лейкоцитов выше 50 000 / мкл с нейтрофилами более 25 000 / мкл), включают инфекции (такие как пиоторакс, пиелонефрит, септический перитонит, пиометра, абсцесс, гепатит), иммуноопосредованные расстройства (такие как иммуноопосредованная гемолитическая анемия, гломерулонефрит, полиартрит и васкулит), неоплазия (например, лимфома, острый и хронический миелоидный лейкоз и опухоли тучных клеток) и некроз тканей (вызванный такими заболеваниями, как как травма, панкреатит, тромбоз и перитонит желчи). 289 290 Сообщалось о нейтрофильном лейкоцитозе до 200 000 / мкл у собак с инфекцией H. americanum , которая вызывает пиогранулематозный миозит. 296 Крайний лейкоцитоз также возникает в течение первых 3 недель после инъекции токсичной дозы эстрогена собакам. Эта нейтрофильная гиперпластическая фаза в костном мозге сопровождается генерализованной гипоплазией или аплазией и смертью или медленным выздоровлением. 485 Нейтрофилия у животных с широким спектром опухолей может быть результатом воспаления или некроза внутри опухоли; но нейтрофилия также может возникать как паранеопластический феномен, вторичный по отношению к продукции факторов роста, таких как G-CSF и GM-CSF, опухолью. 301,418,456
Животные с ХМЛ имеют стойкую выраженную нейтрофилию с выраженным сдвигом влево, который может распространяться на миелобласты. Этот диагноз обычно устанавливается путем исключения воспалительных причин и документирования сопутствующего возникновения дополнительных пролиферативных аномалий в крови и костном мозге.


 Возникает как естественный ответ на травму, прием некоторых лекарственных средств или инфекционное заболевание. У грудного ребенка может являться ответом на инфекцию матери. Повышенные лимфоциты определяются при таких вирусных инфекциях, как грипп, герпес, аденовирус, цитомегаловирус и др.
Возникает как естественный ответ на травму, прием некоторых лекарственных средств или инфекционное заболевание. У грудного ребенка может являться ответом на инфекцию матери. Повышенные лимфоциты определяются при таких вирусных инфекциях, как грипп, герпес, аденовирус, цитомегаловирус и др.