Иммуноглобулины класса М (IgM)
Иммуноглобулины М – это иммуноглобулины, которые вырабатываются первыми в самом начале иммунного ответа – «антитела тревоги». Как только организм сталкивается с чужеродным антигеном, плазматические клетки «запускают» синтез IgМ. Этим обеспечиваются гуморальные защитные механизмы.
Содержание иммуноглобулинов М в кровотоке составляет около 5% от общего числа всех иммуноглобулинов. Каждая молекула IgМ состоит из пяти субъединиц и двух антигенсвязывающих центров. Средний период полувыведения – 5 дней, за этот временной промежуток из крови выводится половина образованных антител IgМ.
При встрече с чужеродным агентом IgМ усиливают фагоцитоз, то есть его поглощение и переваривание. Передача IgМ от матери к плоду через плаценту невозможна из-за высокой молекулярной массы данного иммуноглобулина. Поэтому обнаружение их у плода указывает на внутриутробное инфицирование. К классу IgМ относятся ревматоидный фактор и антибактериальные антитела.
При встрече организма с определенным антигеном начинают вырабатываться специфические IgМ. Они образуются при первичном контакте с бактерией или чужеродным агентом. Первые антитела класса IgG появляются в кровотоке на несколько дней позже. Уровень IgМ повышается в первые несколько недель с момента заболевания, затем постепенно уменьшается, вплоть до полного исчезновения. На смену IgМ приходят IgG, которые длительно или пожизненно циркулируют в крови (в зависимости от вида микроорганизма), обеспечивая надёжную и долгую защиту организма.
Чрезмерная продукция иммуноглобулина М встречается при гиперстимуляции всех клонов В-лимфоцитов, либо клонов В-лимфоцитов, отвечающих за выработку именно IgМ. Повышение уровня IgМ встречается при остром инфекционном процессе и при некоторых иммунопролиферативных заболеваниях (миеломная болезнь, макроглобулинемия Вальденстрема).
Врождённый дефицит IgМ встречается редко, чаще выработка имуноглобулина М угнетается факторами, подавляющими гуморальный иммунитет.
Показания к выполнению анализа
Оценка гуморального иммунитета при частых рецидивирующих и хронических бактериальных инфекций органов дыхания (гайморит, фронтит, пневмония), отитах, менингите.
Выявление иммунодефицитных состояний.
Диагностика внутриутробного инфицирования плода.
Диагностика макроглобулинемии Вальденстрема.
Оценка состояния иммунной системы при новообразованиях, системных заболеваниях соединительной ткани, болезнях крови.
Подготовка к исследованию
Кровь на исследование сдают утром натощак, исключается даже чай или кофе. Допустимо пить обычную воду.
Временной интервал от последнего приёма пищи до сдачи анализа – не менее восьми часов.
Исключить физическую активность за 30 минут до забора крови.
Материал для исследования
Венозная кровь.
Интерпретация результатов
Норма:
Возраст | Уровень IgM, г/л |
< 12 месяцев | 0,4 — 1,0 |
12 месяцев — 10 лет | 0,8 — 1,5 |
Женщины > 10 лет | 0,7 — 2,8 |
Мужчины > 10 лет | 0,6 — 2,5 |
Повышение:
1. Острые и хронические гнойные инфекции органов дыхания и желудочно-кишечного тракта.
2. Внутриутробные инфекции у новорождённых (токсоплазмоз, краснуха, герпетическая инфекция, цитомегаловирусная инфекция).
3. Системные болезни соединительной ткани (системная красная волчанка, ревматоидный артрит, дерматомиозиты).
4. Паразитарные заболевания.
5. Множественная миелома (тип IgМ).
6. Болезни печени (цирроз печени).
7. Муковисцидоз.
8. Бессимптомная моноклональная (IgМ) гаммапатия.
9. Макроглобулинемия Вальденстрема.
10. Появление в крови холодовых агглютининов.
11. Кандидоз кожи и слизистых оболочек.
Снижение:
1. Агаммаглобулинемия (болезнь Брутона) – врожденная недостаточность гуморального иммунитета.
2. Селективный дефицит IgМ.
3. Новообразования системы крови (лейкоз).
4. СПИД.
5. Приём цитостатиков.
6. Потери белка при ожогах, энтеропатиях.
7. Нефротический синдром, почечная недостаточность.
Иммуноглобулины класса М вырабатываются организмом в качестве гуморального ответа иммунной системы на первый контакт организма с антигеном, поэтому повышение их уровня характерно для острых воспалительных процессов. Уровень IgM увеличивается сразу же после инфицирования организма и постепенно снижается в течение нескольких недель после него, при этом избыточный уровень этого иммуноглобулина может быть связан как с активным инфекционным процессом, так и рядом иммунопролиферативных заболеваний. Также выработка IgM может быть понижена, это связано с врожденными или приобретенными факторами, которые истощают гуморальный иммунитет, хотя такие состояния встречаются крайне редко. Данное исследование проводят для оценки гуморального иммунитета, в ходе диагностики состояний иммунодефицита, а также при проведении дифференциальной диагностики инфекций с острым или хроническим характером. Показателен анализ при исследовании внутриутробных инфекций, его назначают пациентам с аутоиммунными заболеваниями, заболеваниями крови и новообразованиями, а также пациентам, которые принимают препараты иммуноглобулинов. Анализ может назначаться пациентам, которые часто болеют инфекционными заболеваниями рецидивирующего характера, также он является частью комплексных обследований иммунной системы у пациентов с иммунодефицитом, новообразованиями тканей лимфоидной или кровеносной системы.
В организме человека этот вид антител вырабатывается для обеспечения ответа иммунной системы на первый контакт с антигеном. Поэтому повышение уровня этих иммуноглобулинов в крови свидетельствует о развитии у человека острого воспалительного процесса.
В норме у детей и взрослых увеличение концентрации этих антител происходит сразу же после инфицирования и держатся они на этом уровне несколько дней, постепенно спадая. Порой избыточная их выработка свидетельствует не только об острой стадии инфекционного заболевания, но и ряде иммунопролиферативных болезней. Дефицит же значений глобулинов IgM в крови является показателем врожденного или приобретенного гуморального иммунитета у женщин и мужчин.
Показания к анализу крови на общий иммуноглобулин М
Назначается данное исследование в первую очередь пациентам с:
- аутоиммунными заболеваниями;
- иммунодефицитом;
- новообразованиями в кровеносной или лимфоидной системе;
- инфекциями в острой или хронической форме;
- регулярными рецидивами инфекций.
Наш центр предлагает всем желающим сдать кровь на сывороточные иммуноглобулины IgM и IgA по доступной цене. Все показатели мы оформляем в форме таблицы с детальной ее расшифровкой.
Основная задача иммуноглобулина заключается в поддержании иммунитета, благодаря выявлению и уничтожению вирусов, микроорганизмов, чужеродных клеток, онкологических клеток. Иммуноглобулины носят еще одно название — антитела.

Для чего нужен?
В теле человека иммуноглобулины находятся на поверхности В-лимфоцитов, присутствуют в сыворотке крови, в тканевой жидкости, а также в секретах, вырабатываемых железами слизистых оболочек. Различные классы антител обеспечивают всестороннюю защиту организма от заболеваний, образуя гуморальный иммунитет. В организме человека встречается 5 классов иммуноглобулинов: G, M, A, E, D. Друг от друга они отличаются составом аминокислот, структурой, распространенностью и некоторыми функциями. Основными функциями иммуноглобулинов являются:
- Распознавание чужеродных веществ (микроорганизмов или его токсинов).
- Связь с антигеном и образование иммунного комплекса.
- Участие в удалении или уничтожении образовавшихся иммунных комплексов.
- Защита человека от повторного инфицирования. Иммуноглобулин против перенесенных заболеваний длительно (иногда на всю жизнь) сохраняется в организме, защищая человека от повторного инфицирования.

В некоторых случаях начинают вырабатываться «дефектные» антитела, которые атакуют собственный организм. Этот процесс характерен для аутоиммунных заболеваний, таких как системная красная волчанка, ревматоидный артрит, склеродермия и многих других. Таким пациентам внутривенное введение иммуноглобулинов показано для повышения содержания антител в крови до физиологического уровня для предотвращения инфекционных заболеваний и создания пассивного иммунитета.
За что отвечает?
Иммуноглобулины М — это особая фракция белков (гамма-глобулиновая), отвечающая за защитные функции организма. Зрелые В-клетки, отвечающие за их выработку, называют плазматическими. Активация производства «защитников» происходит в момент атаки бактерий, паразитов, грибов и других чужеродных органических веществ. Иммуноглобулин М должен быть в норме, так как он ответственен за состояния иммунной системы. Любые отклонения, как в большую, так и в меньшую сторону считаются патологией. В таблице ниже указаны нормы для детей по возрастам.
| Пол пациента | Норма иммуноглобулин М (г/л) |
| У женщин | 0,5-3,2 |
| У мужчин | 0,6-3,7 |
У взрослых наиболее вероятные заболевания, при которых повышается концентрация иммуноглобулина это:
- Гепатит;
- Цирроз печени;
- Грибковые инфекции;
- Опухоли.

Если класс IgM повышен, но другие типы иммуноглобулина ниже нормы, такие результаты свидетельствуют о развитии гипер-IgM-синдрома. Суть данного заболевания в неспособности В-клеток запоминать выбранных до этого классы, а также формирование дегенеративных процессов в лимфоидной ткани. Выше нормы IgM может быть и у здорового человека.
- Эстроген;
- Хлорпромазин;
- Метилпреднизол;
- Фенитоин;
- Д — пеницилламин;
- Карбамазепин.

При их приеме происходит иммунизация организма. Эффект сохраняется на протяжении 6 месяцев. Также повышению первичных защитных функций способствуют спортивные тренировки, физические нагрузки и стрессовые ситуации.
Что показывает иммуноглобулин М и G?
Результаты указанных двух иммунологических анализов могут быть различны в количественном и качественном отношениях. В зависимости от сочетания двух факторов выделяют следующие вариации:
- Оба показателя отрицательны. В данном случае отсутствует инфицирование цитомегаловирусом. Это крайне редкая ситуация, которая в медицинской практике встречается не более чем в 2% случаев. Считается скорее казуистикой, чем нормой. Речь, как уже было сказано, идет о высоковирулентном организме.
- Anti cmv IgG отрицательный, IgM повышен. Означает острую фазу болезни, поскольку иммунитет как таковой еще не сформировался. Процесс характеризуется яркой симптоматикой. Что означает Cmv IgG положительный, IgM также положительный? Положительные (повышенные) результаты по двум показателям означают подострую фазу. Организм уже приспособился к начавшейся болезни и деятельности вируса и начал формировать стойкий иммунитет для пожизненного сдерживания цитомегаловируса.
- Анализ на IgG положительный, на IgM — отрицательный. Подобная разновидность сочетания обозначает переход болезни в латентную стадию. При сохранении нормального иммунитета цитомегалия не развивается. Подобное соотношение результатов встречается в клинической практике наиболее часто. Результат наблюдается едва ли не у каждого представителя человеческого рода. Однако в период вынашивания плода высокие значение (выше нормы) IgG могут повлечь повторную цитомегалию и проблемы с ребенком.

Что показывает иммуноглобулин G?
Иммуноглобулин группы G представляет собой сочетание белков в крови, которое именуется гликопротеинами. Это антитела, которые вырабатывают клетки иммунитета в качестве защитной реакции на внедрение различных инфекционных агентов и патогенных инородных организмов. Уровень содержания иммуноглобулина g в плазме крови может способствовать в установлении клинической картины и формировании диагноза. Как правило, кровь берут из вены для лабораторного исследования при помощи различных реактивов. Что может показать этот ИГ:
- Наличие онкологических болезней.
- ВИЧ-инфекцию.
- Краснуху.
- Аллерген.
- Паразитов.
- Вирусы.
- Бактерии.
- Степень выраженности воспалительного процесса.
- Нарушения работы лимфатической системы.

Основной задачей иммуноглобулинов G является выявление патогенных организмов и меры их ликвидации. Это могут быть различные аллергены, грибки, вирусные агенты, бактериальная флора. ИГ защищает организм от их вредоносного влияния и препятствует размножению вредоносных микроорганизмов. Кроме того, выполнятся следующие задачи:
- Активизируется фагоцитоз.
- Молниеносно образуется уникальное сочетание белковых компонентов, действие которых направлено на ликвидации патогенов.
- Во время беременности обеспечивается защита не только матери, но и ребенку, так как клетки IgG имеют способность проникновения через плацентарные стенки.

Что показывает иммуноглобулин Е общий?
Иммуноглобулин Е — специфический показатель аллергической реакции. Взаимодействие с чужеродным веществом приводит к борьбе антител с антигеном, что приводит к аллергии со следующими симптомами:
- насморк с сухой заложенностью носа, прозрачными слизистыми выделениями без запаха, приступами чихания, повышенной чувствительностью слизистой носа;
- дерматит с кожной гиперемией, отечностью кожного покрова, зудом, жжением;
- приступы кашля;
- бронхиальная астма — хроническая патология, вызванная уменьшением просвета бронхов с хрипами, кашлевыми приступами, одышкой;
- анафилаксия — мгновенный иммунный ответ на раздражающее вещество.

Количество общего IgE взрослого человека отличается от детских показателей. Обратим внимание на таблицу, в которой представлены нормы содержания иммуноглобулина Е в плазме крови взрослых и детей:
| Возраст | Норма IgE общего, МЕ / мл |
| дети первого года жизни | 0 — 29 |
| 1 — 2 года | 0 — 49 |
| 2 — 3 года | 0 — 45 |
| 3 — 9 лет | 0 — 53 |
| 9 — 15 лет | 0 — 200 |
| взрослые | 0 — 100 |
Воздействие аллергенов провоцирует резкое повышение IgE и указывает на такие патологии как:
- воспалительное поражение кожи;
- бронхиальная астма;
- аллергический ринит;
- аллергический гастроэнтерит;
- крапивница и отек Квинке;
- анафилактоидные реакции.

Уровень антител, отвечающих за поддержание иммунной системы, не только повышается, но и понижается. Резкое уменьшение количества белка в крови указывает на синдром Луи-Бара — нейродегенеративное наследственное заболевание. Болезнь формируется из-за дефектов Т-лимфоцитов — красных клеток крови.
У взрослого повышен иммуноглобулин Е: причины
У людей, склонных к аллергии в крови иммуноглобулин е повышен. Что это значит? Это свидетельствует о том, что в организме вырабатывается большое количество антител, которые выполняют защитную функцию. Однако, чрезмерное превышение нормы Ige негативно влияет на здоровье и может быть признаком серьезного аутоиммунного процесса. Повышение иммуноглобулина е у детей и взрослых означает развитие тяжелых аллергических реакций. Обычно это происходит в случаях:
- Сильной аллергии.
- Бронхиальной астмы.
- Поллиноза.
- Атопического дерматита.

Также высокая концентрация вещества в крови бывает при заражении гельминтами. Превышение показателей может иметь неаллергический характер и указывать на наличие серьезных заболеваний:
- Синдром иммунодефицита.
- Злокачественные опухоли.
- Миелома.
- Онкологические заболевания крови (лейкозы).
- Анемия.

Другая причина повышения глобулина е у взрослых — генетическое заболевание гипер- Ige-синдром, при котором содержание глобулина е выше нормы в несколько десятков раз (до 50 тыс единиц/мл). Это выражается следующими симптомами:
- постоянные аллергические риниты;
- рецидивирующая пневмония;
- хронический кандидоз;
- прогрессирующий остеопороз;
- тяжелый атопический дерматит;
- искривление позвоночника.

Пациенты с данным синдромом имеют повышенный риск заболевания раком и системными аутоиммунными болезнями.
Повышен иммуноглобулин Е у ребенка
Допустимое количество иммуноглобулина Е определяется возрастом пациента. Это необходимо учитывать при интерпретации результатов анализов.
| Возраст ребенка | Допустимые значения (кЕ/л) |
| 1-3 месяца | 0-2 |
| 3-6 месяцев | менее 10 |
| 6-12 месяцев | менее 20 |
| 4-5 лет | от 10 до 50 |
| 5-15 лет | менее 60 |
Количество Ig E в сыворотке крови здорового человека крайне мало. Если организм сталкивается с аллергеном или глистами, то уровень иммуноглобулина Е значительно повышается и держится на этой отметке в течение 5-14 дней. У людей с аллергией на пыльцу в период цветения растений этот показатель выше, чем в другие временные промежутки. Повышенное количество Ig E в сыворотке крови у ребенка может быть при отклонениях, указанных ниже:
- аллергии;
- пищевой непереносимости;
- глистной инвазии;
- Ig E миеломе;
- синдроме Вискотта-Олдрича
- бронхопульмональном аспергиллезе;
- синдроме Ди-Джорджи;
- селективной нехватке иммуноглобулина А.
- Если уровень Ig Е меньше нормы, то обычно это свидетельствует об одной из следующих патологий:
- опухоли;
- синдроме Луи-Барра;
- агаммаглобулинемии.

При таких заболеваниях, как аллергический ринит, атопический дерматит и аллергическая бронхиальная астма (если имеется повышенная сенсибилизация к большому количеству аллергенов) уровень Ig E в сыворотке крови достаточно высок. Если человек слишком чувствителен только к одному раздражителю, то показатель, указанный выше, бывает повышен незначительно.
Как сдавать анализ на иммуноглобулин?
Чтобы получить адекватную оценку своей иммунной системы, важно подготовиться к сдаче анализа. И хотя эти правила подготовки не отличаются от тех, которые следует придерживаться для любого другого биохимического анализа крови, их не следует забывать.
- Сдавайте анализ с утра, на голодный желудок.
- За 12 часов до сдачи крови не употребляйте пищу, впрочем, количество выпиваемой воды строго не регулируется.
- За сутки откажитесь от алкоголя, жаренной и жирной пищи.
- Также за сутки старайтесь не перенапрягать свое тело физически и избегать эмоциональных стрессов. При сдаче крови на иммуноглобулин, физический и психологический стресс могут исказить результаты в несколько раз.
- Если вы употребляете какие-то лекарства (например, пероральные контрацептивы) или проходите медицинское лечение, сообщите об этом врачу или лаборанту, который будет принимать у вас анализ.
- По возможности воздержитесь от курения за 30-60 минут до анализа.

Подготовка к анализу на иммуноглобулин схожа с любым другим биохимическим анализом крови. Плазму крови сдают только натощак, чтобы после последнего приема пищи прошло более 8 часов, пить газированную воду также нельзя. По возможности убрать из рациона:
- все виды жареной, копченой еды;
- алкоголь за двое суток до исследования.

Курить сутки до сдачи крови не стоит. Желательно не нагружать тело тяжелой физической и умственной активностью около 3-х дней до анализа. Нужно избегать стрессов за двое суток.
Иммуноглобулин М и G при коронавирусе
Для своевременного распознавания и уничтожения клеток вредоносных микроорганизмов нашей иммунной системой предусмотрена выработка антител. В первую очередь обращайте внимание на интерпретацию результатов теста на антитела к COVID-19 самой клиникой, где вы сдавали анализ.
Количественный и полуколичественный тесты:
- IgM < 1. IgG < 10. Данный результат показывает, что у вас нет иммунитета к коронавирусу и вы им не болели. Несмотря на отмену множества ограничений, старайтесь продолжать ограничивать контакты с людьми, в общественных местах носите маску и перчатки.
- IgM от 1 до 2. IgG < 10. У вас нет выработанных антител, но, возможно, сейчас переносите его без симптомов. Максимально сократите контакты даже с близкими на неделю, а потом повторно сдайте анализ. При ухудшении самочувствия — вызывайте скорую.
- IgM: ≥ 2. IgG: < 10. Вы болеете коронавирусом прямо сейчас, даже если у вас нет симптомов и вы себя хорошо чувствуете. Оставайтесь дома, соблюдайте режим самоизоляции в течение 14 дней. Информация о данных результатах передана в поликлинику, к вам придет врач и назначит лечение — легкую форму коронавируса COVID-19 успешно лечат дома.
- IgM: ≥ 2. IgG: ≥ 10. У вас уже выработались антитела, но, возможно, вы еще болеете. Максимально сократите контакты даже с близкими на неделю, а потом повторно сдайте анализ. При ухудшении самочувствия — вызывайте скорую. Помните, что даже если у вас есть антитела — старайтесь соблюдать меры предосторожности — носите маску и перчатки.
- IgM: < 2. IgG: ≥ 10. У вас есть иммунитет к коронавирусу. Это значит, что вы уже переболели им (возможно — бессимптомно) и у вас выработались антитела. Но так как коронавирусная инфекция до конца не изучена учеными, просим все равно соблюдать меры предосторожности — носите маску и перчатки.

Иммуноглобулин при укусе клеща
На данный вопрос нельзя ответить — да или нет. Нужно понимать, что после введения иммуноглобулина вероятность развития клещевого энцефалита снижается сразу на 95%. Если все же болезнь возникла, то она будет проходить в облегченной форме. Еще один немаловажный момент: максимальная эффективность препарата возможна при его попадании в организм в течение суток после укуса. На вторые сутки вирусы клещевого энцефалита уже начинают проникать вглубь клеток. Клещи являются переносчиками как минимум шести заболеваний.
Инъекция на третьи сутки — слабая попытка или последний шанс что-то исправить. Четыре дня спустя уже бесполезно проводить процедуру.
Чаще, чем энцефалитом, от клеща можно заразиться боррелиозом. Данное заболевание быстро лечится антибиотиками, особенно если его вовремя диагностировать. Однако иммуноглобулин действует лишь против клещевого энцефалита. Введение иммуноглобулина, по сути, является попыткой предотвратить заболевание, но никак не гарантией от него. Идеальный вариант — делать положенные прививки для вырабатывания собственного иммунитета, ведь только такие антитела способны сохраняться длительный период. Поэтому людям, живущим в опасных регионах, в плане нападения клещей, нужно обязательно вакцинироваться.

Антирезусный иммуноглобулин при беременности
Всем подряд беременным женщинам антирезусный иммуноглобулин не требуется. Как уже говорилось, природа предусмотрела возможность вынашивания плода, поэтому даже чрезмерно ретивый иммунитет будущей мамы на самых ранних сроках начинает подавляться прогестероном, что и обеспечивает вынашивание ребенка даже в случаях, когда иммунитет изначально был «против». Для производства иммуноглобулина, который способен предотвратить конфликт, используются клетки человеческой крови, что особым образом очищены и включают антитела.
Сыворотка-антирезус, по своей сути, является растворенной в физиологическом растворе фракцией белка, вычлененного из донорской крови, тщательно проверенной предварительно на ВИЧ, сифилис и гепатиты. В состав средства введены неполные анти-Rho (D) -антитела. Транспортировка их в кровь беременной помогает предотвратить резус-сенсибилизацию. Укол препарата назначается в следующих случаях:
- При вынашивании плода и после появления на свет ребенка с положительным резус-фактором. Это очень важно для последующих беременностей, поскольку в следующий раз антител в крови будущей мамы будет еще больше, поэтому негативные последствия для малыша станут более вероятны.
- После выкидыша или искусственного прерывания беременности женщинам с резус-отрицательной кровью.
- После внематочной или замершей беременности.
- При наличии угрозы выкидыша в любом триместре, если у будущей матери резус-отрицательный статус.

Современные препараты иммуноглобулинов
При разных болезнях и патологических состояниях возможно использование определенных видов иммуноглобулинов:
- Нормальные человеческие. На основе сыворотки донорской крови, предполагают внутримышечное введение. Применяются при гипоиммуноглобулинемии и в борьбе с некоторыми видами микроорганизмов.
- Препараты моноклональных антител. Популярны инфликсимаб (к примеру, применяют при сепсисе, ревматоидном артрите), омализумаб (эффективен при атопической бронхиальной астме).
- Специфические иммуноглобулины. Используются часто при верифицированной инфекции (хламидии, Эпштейна-Барр, герпес 1,2,6 типов, цитомегаловирус и пр.).
- Препараты с IgG в составе. Эффективны при некоторых аутоиммунных заболеваниях и гипоиммуноглобулинемии тяжелой формы. Вводятся внутривенно.
- Иммуноглобулины с содержанием IgM. Рекомендованы при бактериальном сепсисе.
Комбинированные лекарственные средства — совместно с иммуноглобулинами используются и другие действующие вещества (к примеру, при добавлении интерферона выходит кипферон).

Иммуноглобулины часто применяются в современной медицине для предупреждения многих заболеваний:
- гепатиты А и В;
- герпес;
- краснуха;
- корь;
- ветряная оспа и пр.

Профилактика проводится посредством внутривенного введения нормального иммуноглобулина или же внутримышечно — гамма-глобулина. Такой метод помогает повысить сопротивляемость организма вирусам и бактериям.
Важность иммуноглобулинов
Иммуноглобулин, гамма-глобулин, антитела — вещества, вырабатываемые в организме здорового человека с целью защиты от различных заболеваний. В норме компоненты можно найти в сыворотке крови, межклеточной жидкости, в некоторых секретах. Располагаются они обычно на поверхности В-лимфоцитов, обеспечивая всестороннюю защиту от патологий органов и систем. Помимо гуморального, существует клеточный иммунитет, отвечающий за регенерацию, обновление и защиту клеток с помощью специальных компонентов, называемых макрофагами.
Стоит отметить, что вещества отвечают за гуморальный иммунитет, то есть тот, который распространяется на все жидкости в организме человека.
Существует два типа иммунного ответа: специфический и неспецифический. Гамма-глобулин отвечает за выработку первого, нейтрализует патогенные бактерии и другие вещества. Компонент обладает и другими функциями:
- первым реагирует на проникновение микроорганизмов;
- образует специальный иммунный комплекс, связываясь с антигеном;
- быстро удаляет образовавшиеся иммунные комплексы;
- формирует иммунитет против многих заболеваний, перенесенных ранее, предупреждает повторное инфицирование.

Иногда специалисты отмечают, что собственные антитела атакуют клетки организма, меняя свое направление. Состояние обычно связано с системными патологиями, например, красной волчанкой тяжелой формы, артритом.
admin
Автор статьи
Поделитесь статьей с друзьями

Рейтинг статьи
0Как узнать, заразен ли человек коронавирусом
Недавно мне позвонила встревоженная подруга. В апреле она переболела «чем-то, очень похожим на коронавирус», вызванный на дом врач мазок на «корону» не взял. А на днях, после выхода на работу, сотрудникам делали экспресс-тест на антитела. Он показал иммуноглобулины (так называются антитела на медицинском языке) класса G. Это, как думают многие, означает: болезнь закончилась, теперь есть иммунная защита. Потом у подруги появилась возможность сдать тест на антитела снова, на другой тест-системе. Новый результат шокировал: есть иммуноглобулины М, сигналящие об острой фазе болезни. Антител G не обнаружено…
Судя по обсуждениям в соцсетях, подобные и другие запутанные истории при тестировании на коронавирус не единичны. Мы собрали самые типичные ситуации и вопросы и разобрали их вместе с опытным экспертом по лабораторным исследованиям, руководителем научного центра молекулярно-генетических исследований ДНКОМ Андреем Исаевым.
1. Мой работодатель заказал экспресс-тесты. У меня не обнаружено ни антител М, ни G. Все в порядке, беспокоиться не о чем?
— Если ни антител, ни симптомов у вас нет, то главная задача — не заболеть. Для этого нужно соблюдать правила гигиены, социальную дистанцию и масочный режим.
Если вы собираетесь повидаться с людьми из группы риска (те, кому за 60, онкологические больные и т. д.), то для безопасности сдайте ПЦР-тест. Это мазок из ротоглотки и носоглотки для обнаружения генетического материала вируса. Если результат теста отрицательный, то, скорее всего, нет риска заразить окружающих.

Глава научного центра молекулярно-генетических исследований ДНКОМ Андрей Исаев.
2. Тест показал у меня антитела класса М. Я точно болен, инфекция в разгаре?!
— Иммуноглобулины М очень нестабильные. Плюс нередко «фонят»: то есть, к примеру, тест обнаруживает такие антитела не к нынешнему коронавирусу, а к сезонным коронавирусам, которыми человек переболел в виде обычных простуд. Поэтому в значительной части тест-систем исследование иммуноглобулинов М даже не предусматривается.
Если же такие антитела обнаружены экспресс-тестом или классическим тестом на антитела (он называется ИФА, иммуноферментный анализ), то нужно сдать мазок на ПЦР-анализ. Если он отрицательный и никаких симптомов нет, значит, человек не выделяет вирус. То есть не заразен. Можно ходить на работу, вести обычную жизнь.
Если ПЦР положительный — нужно садиться на изоляцию.
3. У меня обнаружены антитела М (IgM) в очень маленьком количестве и антитела G (IgG). Это значит, что я уже точно не заразен?
— Нет, точно утверждать этого нельзя. С одной стороны, антитела М могут «фонить» (см. выше), вы могли успешно переболеть и получить защитные антитела G. С другой стороны, это не гарантирует, что вирус перестал выделяться (см. ниже вопрос 4).
Выяснить, заразен человек или нет, можно только путем сдачи мазка на ПЦР.
4. Верно ли, что все, у кого обнаружены антитела класса G, надежно защищены от коронавируса и точно не заразны?
— Дает ли наличие антител защиту от повторных заболеваний COVID-19, сегодня точных данных нет. Ведутся исследования. Пока можно делать предположения, опираясь на истории иммунной защиты у переболевших наиболее близким родственником нынешнего коронавируса — SARS-CoV-1, который вызвал атипичную пневмонию в 2002 — 2003 гг. У перенесших эту инфекцию иммунитет сохранялся в среднем в течение около 2 лет. Так что есть гипотеза, что и после нынешнего коронавируса может быть такая иммунная защита. Но, опять же, еще не понятно, какой титр (уровень, концентрация) антител будет гарантировать иммунный «отпор» при повторных заражениях.
Что касается заразности, то есть прецеденты: у человека выявлялись иммуноглобулины G, а при проверке ПЦР-тестом обнаруживался генетический материал вируса. Это означает, что пациент уже сам вроде бы выздоровел, приобрел иммунитет, но выделение вируса еще продолжается. Он может заражать остальных. Обнаружить это можно с помощью ПЦР-теста.
Так что не следует забывать: у заболевших выделение вируса может сохраняться вплоть до почти полутора месяцев — описаны случаи 41 — 42-дневного периода выделения SARS-CoV-2. Обнаружить это можно с помощью ПЦР-теста.
5. Есть ли на самом деле подтвержденные случаи повторного заражения?
— Нет, однозначных, убедительных подтверждений повторного заболевания COVID-19 после полного выздоровления нет. Скорее, может идти речь о неточности диагностики, в частности, ложноотрицательных результатах. Плюс не следует забывать, что у заболевших выделение вируса может сохраняться вплоть до почти полутора месяцев после исчезновения симптомов. Тогда ПЦР-анализ покажет наличие вируса, и это могут принять за повторное заражение.
Поделиться видео </>Корреспондент «КП» сдала анализ на иммунитет к COVID-19.Михаил ФРОЛОВ
ЧИТАЙТЕ ТАКЖЕ
Все о тестах на COVID: офисным работникам — экспресс-анализ, у больных ищут вирус, у остальных — антитела
«Комсомолка» выяснила, какие виды тестирования на коронавирус сейчас есть в России, насколько они достоверны и в каких жизненных ситуациях нужны (подробности)
ВОЗ: бессимптомные носители коронавируса заражают других людей очень редко
Однако зачастую болезнь протекает в слабовыраженной форме, а не бессимптомно, предупреждают инфекционисты (подробности)
Иммуноглобулин вводят внутримышечно в верхний наружный квадрант ягодичной мьшщы или наружную поверхность бедра. Запрещается вводить препарат внутривенно. Перед инъекцией ампулы с препаратом выдерживают в течение 2-х часов при комнатной температуре.
Вскрытие ампул и процедуру введения осуществляют при строгом соблюдении правил асептики и антисептики. Во избежание образования пены препарат набирают в шприц иглой с широким просветом.
Препарат во вскрытой ампуле хранению не подлежит. Непригоден к применению препарат в ампулах с нарушенной целостностью или маркировкой, при изменении физических свойств (изменение цвета, помутнение раствора, наличие не разбивающихся хлопьев), при истекшем сроке годности и несоблюдении условий хранения.
Доза иммуноглобулина и кратность его введения зависят от показаний к применению.
Профилактика гепатита А
Препарат вводят однократно в дозах: детям от 1 до 6 лет — 0,75 мл, до 10 лет — 1,5 мл, старше 10 лет и взрослым — 3 мл. Повторное введение иммуноглобулина в случае необходимости профилактики гепатита А показано не ранее, чем через 2 мес.
Профилактика кори
Препарат вводят однократно с 3-месячного возраста лицам, не болевшим корью и непривитым против инфекции, не позднее 6 сут после контакта с больным. Дозу препарата детям (1,5 или 3 мл) устанавливают в зависимости от состояния здоровья и времени, прошедшего с момента контакта. Взрослым, а также детям при контакте со смешанными инфекциями препарат вводят в дозе 3 мл.
Профилактика и лечение гриппа
Препарат вводят однократно в дозах: детям до 2 лет — 1,5 мл, от 2 до 7 лет — 3 мл, старше 7 лет и взрослым — 4,5-6 мл. При лечении тяжелых форм гриппа показано повторное (через 24-48 ч) введение иммуноглобулина в той же дозе.
Профилактика коклюша
Препарат вводят двукратно с интервалом в 24 ч в разовой дозе 3 мл детям, не болевшим коклюшем и не привитым (не полностью привитым) против коклюша, в возможно более ранние сроки после контакта с больным, но не позже 3 суток.
Профилактика менингококковой инфекции
Препарат вводят однократно детям в возрасте от 6 мес до 7 лет не позднее 7 сут после контакта с больным генерализованной формой менингококковой инфекции в дозах 1,5 мл (детям до 3 лет) и 3 мл (детям старше 3 лет).
Профилактика полиомиелита
Препарат вводят однократно в дозах 3-6 мл непривитым или неполноценно привитым полиомиелитной вакциной детям в возможно более ранние сроки после контакта с больным полиомиелитом.
Лечение гипо- и агаммаглобулинемии
Препарат вводят в дозе 1 мл на 1 кг массы тела, рассчитанную дозу можно ввести в 2-3 приема с интервалом в 24 ч. Последующие введения иммуноглобулина проводят по показаниям не ранее, чем через 1 месяц.
Повышение резистентности организма в период реконвалесценции острых инфекционных заболеваний с затяжным течением и при хронических пневмониях.
Препарат вводят в разовой дозе 0,15-0,2 мл на 1 кг массы тела. Кратность введения (до 4-х инъекций) определяет врач; интервалы между инъекциями составляют 2-3 сут.
Иммуноглобулин M — Immunoglobulin M
Иммуноглобулин М ( IgM ) является одной из нескольких форм антител , которые вырабатываются позвоночных. IgM является самым большим антителом, и это первое антитело появляться в ответ на первоначальное воздействие на антиген . В случае людей и других млекопитающих , которые были изучены, в селезенке , где plasmablasts , ответственный за выработку антител проживает, является основным местом производства конкретного класса IgM.
Вступление
Иммуноглобулины , также известные как антитела, включают семейство белков , которые происходят в пяти основных формах, также называемые классы или изотипы — IgM, IgD, IgG, IgE и IgA. Иммуноглобулины продуцируются позвоночных животных , как часть нормального иммунного ответа на микробные , например, бактериальной или вирусной инфекции,. Связывание иммуноглобулинов к микробу может иметь немедленные эффекты , такие как блокирование вторжения и может мобилизовать другие компоненты иммунной системы , чтобы уничтожить или иным образом инактивации микробов, тем самым обеспечивая защиту от инфекционных заболеваний. Молекулярные структуры , которые микроорганизмы , присутствующие в иммунную систему и вызывать иммуноглобулин (антитела) производство совместно обозначают как антигены .
Хотя все позвоночные, которые были изучены — от рыб до человека — производить IgM, существуют значительные различия между IgMs разных видов. Эта статья сфокусирована на человека и мыши IgM, которые оба хорошо изученной и имеют очень сходные свойства. По большей части IgM, получают плазматические клетки в селезенке и лимфатических узлах и секретируется в сыворотку крови, где он, как правило, при концентрации ~ 1,5 мг / мл. В данной статье описана структура сывороточного IgM, в отличие от других форм, таких как рецептор IgM мембраны.
Иммуноглобулины состоят из двух типов белковой цепи-тяжелой цепи и легкой цепи. Тяжелые цепи, которые определяют класс иммуноглобулина, имеют пять различных типов, обозначаются греческими буквами, μ, δ, γ, ε и α, соответствующие классам, IgM, IgD, IgG, IgE и IgA, соответственно. Легкие цепи бывают двух типов, обозначаемых Х и х. Каждая цепь сама делится на две функциональные части, переменной (V) области и константной (С) области. В V домены легкой и тяжелой цепи сложены вместе, чтобы сформировать структуру, которая связывает антиген; различные домены V связывают различные антигены, т.е. связывание антигена иммуноглобулина является антиген-специфическая. Ввиду того, что V домены могут иметь место в почти неограниченном разнообразии аминокислотных последовательностей, иммуноглобулины в совокупности обладают потенциалом связывания с практически любой молекулярной структурой. Домены иммуноглобулина C взаимодействуют с другими физиологическими компонентами, например, рецепторы клеточного иммуноглобулина и системы комплемента. Таким образом, константный домен иммуноглобулина может помочь мобилизовать фагоцитарные клетки или систему комплемента действовать на антиген, с которым он связан с помощью вариабельного домена.
история
Исследование IgM началось с доклада в 1937 году , что лошади гипервакцинации с пневмококк полисахарида , полученного антитела , которое было гораздо больше , чем типичный кролика гамма-глобулина, с молекулярной массой 990000 дальтон. В соответствии со своим большим размером, новое антитело было первоначально упоминаются как гамма-макроглобулин, а затем в последующей терминологии как IgM-М для «макро». В V домены нормального иммуноглобулина весьма неоднородны, что отражает их роль в защите от большого разнообразия инфекционных микробов, и эта неоднородность препятствует детальный структурный анализ IgM. Два источника однородного IgM был впоследствии обнаружен. Во- первых, белок с высокой молекулярной массой , который вырабатывается некоторыми множественной миеломой пациентов была признана опухоль производства γ-макроглобулина, и теперь мы знаем , что , поскольку опухоль представляет собой клон IgM производит однородна. В 1960 — е годы были разработаны методы для индукции иммуноглобулинов-продуцирующих опухолей (плазмоцитомы) у мышей, таким образом , также обеспечивая источник однородных иммуноглобулинов различных изотипов, включая IgM (рассмотрены в). Совсем недавно, экспрессия модифицированных генов иммуноглобулина в культуре ткани может быть использована для получения IgM с конкретными чередованиями и , таким образом , чтобы идентифицировать молекулярные требования для функций , представляющего интереса.
Состав
Иммуноглобулины включают легкие цепи и тяжелые цепи. Легкая цепь (λ или κ) представляет собой белки ~ 220 аминокислот, состоит из вариабельного домена, VL (сегмент приблизительно 110 аминокислот), а также константный домен, CL (длина также около 110 аминокислот). Μ тяжелая цепь IgM представляет собой белка из ~ 576 аминокислот и включает вариабельный домен (VH ~ 110 аминокислот), четыре различных домены константной области (Cμ1, Cμ2, Cμ3, Cμ4, каждый из ~ 110 аминокислот) и «хвостовик» из ~ 20 аминокислот. Мю тяжелой цепи несет олигосахариды в пяти остаткам аспарагина. Олигосахариды на мыши и человек IgM были частично охарактеризованы с помощью различных методов, включая ЯМР, лектину, связывающие различные хроматографические системы и ферментативную чувствительность (обзор в). Структура олигосахаридов на каждом участке изменяется в деталях, и преобладающие олигосахариды — biantennary, триантенный, высокая манноза-различаются между сайтами.
 Рисунок 1. Схематическая модель IgM
Рисунок 1. Схематическая модель IgM A) мкл гетеродимера, иногда называют halfmer с переменной (VH, VL) и константной области (Cμ1, Cμ2, Cμ3, Cμ4tp; CL) домены. Цистеины , которые опосредуют дисульфидные связи между цепями М показаны в виде красных стрел, таким образом , что цистеин дисульфидных связей появляются в виде красную двойной стрелки (красный алмаз).
Б) IgM «мономер» (мкл) 2. Дисульфидные связи между доменами Cμ2 представлены красной двойной стрелкой.
С, D) Две модели J-цепи , содержащей IgM пентамера , которые появились в различных изданиях в разное время. Как и в (B), дисульфидные связи между доменами Cμ2 и дисульфидными связями между доменами Cμ4tp представлены красной двойной стрелкой; представлены дисульфидные связи Cμ3 (для ясности) длинными стрелками двуглавых. Связи, то есть, между цепью дисульфидных связей .М цепей, обозначается как электрических соединений. В (С) дисульфидные связи Cμ3 присоединиться к мю цепи параллельно с дисульфидными связями Cμ4tp, и эти дисульфидные связи соединяют мю цепи последовательно с дисульфидными связями Cμ2. В (D) дисульфидные связи Cμ2 и Cμ4tp присоединиться к мю цепи параллельно и оба типа присоединиться к мю цепи последовательно с дисульфидными связями Cμ3. (Рисунок воспроизведен с разрешения издателя и авторов).
Мультимерный структура IgM схематически показан на рисунке 1. Рисунок 1A показывает «гетеродимер», состоящий из одной легкой цепи, обозначенная L, и одной тяжелой цепи, обозначаемой ц. Эти тяжелые и легкие цепи удерживаются вместе и дисульфидными связями (изображено в виде красных треугольников) и нековалентными взаимодействиями.
На фигуре 1В показаны два мкл единиц, связанных дисульфидной связью в доменах Cμ2; это (мкл) 2 структура часто упоминается как «мономер» IgM, так как оно аналогично в некотором смысле к структуре иммуноглобулина G (IgG).
На основе его скорости седиментации и появления в электронных микрофотографий, был сделан вывод, что IgM является главным образом «пентамера», то есть полимер, состоящий из пяти «мономеров» [(мкл) 2] 5, и первоначально был изображен моделями на фигурах 1C и 1D, с дисульфидными связями между доменами Cμ3 и между задними частями. Кроме того, показано, что пентамерный IgM включает в себя третий белок, то J цепь. J цепь (Дж для присоединения) была обнаружена в качестве ковалентно связанного компонента полимерного IgA и IgM. J цепь представляет собой небольшие (~ 137 аминокислот), кислый белок. Как показано, J цепь соединяет две μ цепи через дисульфидные связи с участием цистеина в фитингах.
Молекулярные требования к формированию полимерного IgM
Он был первоначально ожидались, что J цепь будет иметь важное значение для формирования полимерных иммуноглобулинов, и действительно полимеризация IgA сильно зависит (но не совсем) на J цепи. В противоположность этому, полимерный IgM эффективно образует в отсутствие J цепи.
Преобладающая форма человека и мыши IgM является пентамером. Для сравнения, IgM, от лягушки (Xenopus) преимущественно гексамер, IgM, из костистых рыб преимущественно тетрамеры и IgM из хрящевых рыб (акулы) преимущественно пентамер. Преобладание пентамера у мыши и человека IgM несмотря на это, было очевидно, что эти IgM могло существовать также гексамере. Последующие исследования с использованием системы экспрессии рекомбинантных ДНК показали, что гексамеры являются основной формой мыши IgM, когда IgM производится в условиях, когда включение J цепи предотвращается, либо путем получения IgM в клетках, которые испытывают недостаток J цепи или производя IgM с ц тяжелой цепи, которая испытывает недостаток цистеина в хвостовом. Таким образом, гексамерный IgM, никогда не содержит цепь J; пентамерный IgM, может быть сформирован таким образом, чтобы включать в себя или не включать в себя J цепи.
Важное различие между ц и гамма тяжелых цепей является наличие остатков цистеина для образования дисульфидных связей между тяжелыми цепями. В случае гаммы тяжелой цепи, только между & gamma связь образуются с помощью цистеинов в петле, и, соответственно, каждая γ цепи связывается только с одним другой гаммой цепи. В отличии от этого, домены Cμ2 и Cμ3 и хвостовой каждый включают цистеин, которые образуют дисульфидные св зите с другими мкм цепью. Цистеины в доменах Cμ2 опосредуют образование мономерного IgM (2 мкл). Хвостовик вместе с включенным цистеином является необходимым и достаточным для образования полимерных иммуноглобулинов. То есть, удаление хвостового из мю тяжелой цепи предотвращает образование полимерного IgM. И наоборот, клетки, экспрессирующие & gamma тяжелую цепь, которая была модифицирована, чтобы включать в себя хвостовик получения полимерного IgG.
Роль цистеина в области Cμ3 является более тонкой. Фигуры 1C и 1D представляют возможные модели для пентамерного IgM. В этих моделях каждая μ цепь предполагается связать два других мю цепи. Тем не менее, ни одна из моделей в одиночку в полной мере может объяснить структуру полимерного IgM. Например, модель на фиг.1C предсказывает, что дисульфидная связь между доменами Cμ2 имеет важное значение для создания дисульфидной связи полимерного IgM. Модель на рисунке 1D предсказывает, что дисульфид связь между доменами Cμ3 имеет важное значение. В самом деле дисульфид связаны, полимерные, IgM, все еще может быть сделано, если какой-либо один из трех цистеинов отсутствует. В контексте моделей, в которых каждая цепь μ взаимодействует только с двумя другими х цепей, эти результаты свидетельствуют о том, что некоторые молекулы, как на рисунке 1C и некоторые, как на рисунке 1D. Тем не менее, наличие трех цистеинов для μ между цепью связи предполагает, что мю цепь может связываться друг с три другой мю цепи, как показан на рисунке 2. В том же духе фиг.2С представлена модель J цепи, содержащий пентамер, который отражает доказательства того, что J цепь присоединяется мю цепи, которые не присоединились к другим М- цепей по цистеинам в доменах Cμ3. Эти и другие модели, как регулярные и нерегулярные обсуждаются в другом месте.
Рисунок 2. Некоторые альтернативные способы связывания М цепейА, В) Эти цифры показывают две из многих возможных моделей между ц дисульфида цепи связи в гексамерного IgM. Как и на фиг.1, дисульфидные связи Cμ2 и дисульфидные связи Cμ4tp представлены красной двойной стрелкой, и дисульфидные связи Cμ3 представлены длинными стрелками двуглавый. В обеих моделях A и B каждого типа дисульфидных связей (Cμ2-Cμ2; Cμ3-Cμ3; Cμ4tp-Cμ4tp) присоединяется к мю цепи последовательно с каждым из остальных. Методы выделения этих и других моделей обсуждаются в работе [28].
С) Это представление пентамерного IgM иллюстрирует , как J цепь может быть соединена с ц цепи, которые не связаны с помощью Cμ3 дисульфидных связей
Пентамерный IgM обычно представлен как содержащие одну J цепи полимера за, но в действительности измерение J цепи стехиометрии варьировалось от одной молекулы J полимера на три молекул J на полимер. Широкий диапазон может быть связан с техническими проблемами, такими как неполное радиомечение или нечетко Оухтерлони в количественной линии. Однако изменение может быть также связано с неоднородностью в препаратах IgM, то есть, различные препараты могли бы существенно отличались по содержанию J-содержащих и J-дефицитных полимеров.
Третичная и четвертичная структура ц константной области
Для того, чтобы получить представление о детальной трехмерной структуры ц цепи, отдельные домены Cμ2, Cμ3 и Cμ4tp были произведены отдельно в E.coli, а затем анализировали с помощью различных методов, включая скорость оседания, рентгеновской кристаллографии и ЯМР спектроскопии. Как и в случае других иммуноглобулинов, домены мю тяжелой цепи имеют характерные вышележащую бету-листов, содержащие семь нитей, стабилизированные дисульфидные связи внутри домена. В целом, константная область IgM имеет «грибовидную» структуру, где домены Cμ2-Cμ3 являются диском аналогичен головкой гриба и доменов Cμ4tp выступают как короткий стебель.
функция
IgM, взаимодействует с несколькими другими физиологическими молекулами:
- IgM , может связывать комплемент компонент C1 и активировать классический путь , ведущий к опсонизации из антигенов и цитолиза .
- IgM , связывается с polyimmunoglobulin рецептором (pIgR) в процессе , который приносит IgM к слизистой поверхности, такие как кишки просвет и в грудное молоко. Это связывание зависит от J цепи.
- Два других рецепторов , которые связываются с Fc-IgM — Fcα / μ-R и Fcμ-R — были обнаружены. Fcα / μ-R, как pIgR, связывает полимерный IgM и IgA. Fcα / μ-R , может опосредовать эндоцитоз , и его экспрессия в кишечнике предполагает роль в иммунитете слизистых оболочек. Fcμ-R (ранее известный как Toso / FAIM3) связывает IgM исключительно и может опосредовать клеточное поглощение IgM-конъюгированного антигена. Инактивация соответствующих генов в нокаут-мышей приводит к фенотипу , но физиологические функции этих рецепторов до сих пор неизвестно
Регулирование иммунного ответа
Специфические иммуноглобулины , которые вводят в животное вместе с их антигеном могут влиять на реакцию антитела к этому же антигену. Эндогенные антитела , полученные после первичной иммунизации могут также влиять на реакцию антитела к бустер — иммунизации, предполагая , что подобные эффекты возникают в ходе физиологических условий. В «регуляторные» эффекты могут быть положительными или отрицательными. То есть, в зависимости от типа антигена и изотипа антитела, эффект может быть подавление или усиление иммунного ответа. Такие эффекты хорошо иллюстрируется экспериментами с участием иммунизации ксеногенных (иностранных) эритроцитов (красные клетки). Например, когда IgG вводят вместе с ксеногенными эритроцитами, эта комбинация вызывает почти полное подавление эритроцита-специфическая реакцию антител. Этот эффект используется в клинике для предотвращения резус-отрицательных матерей от быть иммунизированы против плода резус-положительных эритроцитов, и его использование значительно снижает частоту гемолитической болезни новорожденных. В отличии от эффекта IgG, антиген-специфические IgM , может значительно повысить ответ антител, особенно в случае больших антигенов. Таким образом, когда IgM , специфичные для эритроцитов вводят в животных (включая человека) вместе с эритроцитами, гораздо сильнее реакция антител к эритроцитам индуцируется , чем когда эритроциты вводить отдельно. Несколько линий доказательств указывают на то, что способность IgM активировать комплемент требуется для его усиливающего эффекта. То есть, IgM-опосредованное повышение не происходит у животных , которые были истощены для компонент С3 комплемента, ни у мутантных животных отсутствует комплемент рецепторы 1 и 2. Аналогична, мутант IgM , который не может активировать комплемент не усиливать иммунный ответ. Возможное объяснение IgM-опосредованное усиление является то , что В — лимфоцитам захватить IgM-антиген-комплемент комплексов и транспортные комплексы в районы в селезенке , где генерируются эффективные иммунные ответы. Поскольку IgM , получает в начале иммунного ответа, это может иметь большое значение в инициации реакции антител.
Синтез
В клетках зародышевой линии (спермы и OVA) генов , которые кодируют в конечном итоге иммуноглобулины не в функциональной форме (см V (D) J рекомбинации ). В случае тяжелой цепи, три сегмента зародышевой линии, обозначенный V, D и J лигируют вместе и примыкают к ДНК , кодирующих М константной области тяжелой цепи. В начале онтогенеза, B — клетки экспрессируют как М и б тяжелые цепи; совместная экспрессия этих двух тяжелых цепей, каждая из несущих ту же область V зависит от альтернативного сплайсинга и альтернативных сайтов поли-А — аддитивных. Выражение других изотипов (γ, ε и α) осуществляется с помощью другого типа перегруппировки ДНК, этот процесс называется переключение класса иммуноглобулинов .
Клиническое значение
IgM является первым иммуноглобулин выражается в плоде человека (около 20 недель) и филогенетический самое раннее антитела развиваться.
IgM антитела появляются на ранних стадиях инфекции , и , как правило , вновь, в меньшей степени, после дальнейшего воздействия. IgM антитела не проходят через плаценту человека (только изотипа IgG ).
Эти два биологические свойства IgM сделать его полезным в диагностике инфекционных заболеваний. Демонстрация IgM антител в сыворотке крови пациента указывает на недавнюю инфекцию, или в сыворотке новорожденного указывает внутриматочной инфекции (например , синдром врожденной краснухи ).
Развитие анти-донор IgM после трансплантации органов не связанно с отторжением трансплантата, но он может иметь защитный эффект.
IgM в нормальной сыворотке часто встречаются связываться со специфическими антигенами, даже при отсутствии предварительной иммунизации. По этой причине IgM , иногда называют «естественным антитело». Это явление, вероятно , из — за высокой авидности IgM , которые позволяют ему связывать обнаруживаемой даже слабо перекрестно реагирующих антигенов , которые в природе. Так , например, антитела IgM , которые связываются с красных кровяных клеток A и B антигенов может быть сформирована в начале жизни в результате воздействия А- и В-подобных веществ, которые присутствуют на бактерии или , возможно , также и на растительных материалов.
IgM антитела в основном ответственны за слипание ( склеивание ) из красных кровяных клеток , если получатель переливания крови получает кровь, которая не совместима с их типом крови .
Смотрите также
Рекомендации
внешняя ссылка
Иммуноглобулин М — Википедия Переиздано // WIKI 2
Иммуноглобулин М ( IgM ) является одним из нескольких изотипов антител (также известных как иммуноглобулины), которые вырабатываются позвоночными. IgM является самым большим антителом, и это первое антитело, которое появляется в ответ на первоначальное воздействие антигена. [1] [2] В случае людей и других млекопитающих, которые были изучены, селезенка, в которой находятся плазменные взрывы, ответственные за выработку антител, является основным участком специфической продукции IgM. [3] [4]
Энциклопедия YouTube
1/5
Просмотров:3 264
158 674
198 507
8 652
58 869
✪ IgM, IgD: структура, свойства и функции (FL-Immuno / 40)
✪ Видео 15 Ig-антитела и функция иммуноглобулина
✪ Иммунология — Антитела (Функция)
Structure Структура и функции иммуноглобулинов / Типы и функции структуры антител
Содержание
История
Исследование IgM началось с сообщения в 1937 году о том, что лошади, гипериммунизированные пневмококковым полисахаридом, продуцировали антитела, которые были намного крупнее, чем типичный кроличий γ-глобулин, [5] с молекулярной массой 990 000 дальтон. [6] В соответствии с его большими размерами новое антитело первоначально называлось γ-макроглобулином, а затем в последующей терминологии IgM-M для «макро». V-домены нормального иммуноглобулина являются высоко гетерогенными, что отражает их роль в защите от большого числа инфекционных микробов, и эта гетерогенность препятствовала детальному структурному анализу IgM. Впоследствии были обнаружены два источника гомогенного IgM. Во-первых, было признано, что высокомолекулярный белок, продуцируемый некоторыми пациентами с множественной миеломой, представляет собой продуцируемый опухолью γ-макроглобулин, и теперь мы знаем, что поскольку опухоль является клоном, продуцируемый ею IgM является гомогенным. [7] В 1960-х годах были разработаны методы для индукции иммуноглобулин-продуцирующих опухолей (плазмоцитом) у мышей, что также обеспечило источник гомогенных иммуноглобулинов различных изотипов, включая IgM (обзор в [8] ). В последнее время экспрессия сконструированных генов иммуноглобулина в тканевой культуре может быть использована для продуцирования IgM с конкретными изменениями и, таким образом, для определения молекулярных требований к интересующим признакам.
Структура
Иммуноглобулины включают легкие цепи и тяжелые цепи.Легкая цепь (λ или κ) представляет собой белок из ~ 220 аминокислот, состоящий из вариабельного домена VL (сегмент приблизительно из 110 аминокислот) и константного домена CL (также длиной приблизительно 110 аминокислот). Тяжелая цепь IgM представляет собой белок из ~ 576 аминокислот и включает вариабельный домен (VH ~ 110 аминокислот), четыре различных домена константной области (Cµ1, Cµ2, Cµ3, Cµ4, каждая ~ 110 аминокислот) и «Хвостовая часть» из ~ 20 аминокислот. Тяжелая цепь µ содержит олигосахариды с пятью остатками аспарагина.Олигосахариды на IgM мыши и человека были частично охарактеризованы различными методами, включая ЯМР, связывание лектина, различные хроматографические системы и чувствительность к ферментам (обзор в [9] ). Структура олигосахаридов на каждом сайте варьируется в деталях, и преобладающие олигосахариды — двухлетние, трехлетние, с высоким содержанием маннозы — различаются между сайтами.
![Figure 1. Schematic model of IgM A) The µL heterodimer, sometimes called a halfmer, with variable (VH, VL) and constant region (Cµ1, Cµ2, Cµ3, Cµ4tp; CL) domains. The cysteines that mediate disulfide bonds between µ chains are shown as red arrowheads, so that a cysteine disulfide bond appears as a red double arrowhead (red diamond). B) The IgM “monomer” (µL)2. The disulfide bonds between Cµ2 domains are represented by a red double arrowhead. C, D) Two models for J chain-containing IgM pentamer that have appeared in various publications at various times. As in (B), the disulfide bonds between Cµ2 domains and the disulfide bonds between Cµ4tp domains are represented by a red double arrowhead; the Cµ3 disulfide bonds are represented (for clarity) by long double-headed arrows. The connectivity, i.e., the inter-chain disulfide bonding of the µ chains, is denoted like electrical connectivity. In (C) the Cµ3 disulfide bonds join µ chains in parallel with the Cµ4tp disulfide bonds, and these disulfide bonds join µ chains in series with the Cµ2 disulfide bonds. In (D) the Cµ2 and Cµ4tp disulfide bonds join µ chains in parallel and both types join µ chains in series with the Cµ3 disulfide bonds. (Figure reproduced with permission of the publisher and authors[10]).](/800/600/https/wiki2.org/wikipedia/commons/thumb/e/e4/Schematic_model_of_IgM.jpg/im244-371px-Schematic_model_of_IgM.jpg) Рисунок 1. Схематическая модель IgM
Рисунок 1. Схематическая модель IgM A) Мкл гетеродимера, иногда называемого полумером, с вариабельной (VH, VL) и константной областью (Cµ1, Cµ2, Cµ3, Cµ4tp; CL) доменов.Цистеины, которые опосредуют дисульфидные связи между µ-цепями, показаны в виде красных стрелок, поэтому цистеин-дисульфидная связь отображается в виде красной двойной стрелки (красный ромб).
B) IgM «мономер» (мкл) 2. Дисульфидные связи между доменами Cµ2 представлены красной двойной стрелкой.
C, D) Две модели пентамера, содержащего J-цепь IgM, которые появлялись в различных публикациях в разное время. Как и в (B), дисульфидные связи между доменами Cµ2 и дисульфидные связи между доменами Cµ4tp представлены красной двойной стрелкой; дисульфидные связи Cµ3 представлены (для ясности) длинными двуглавыми стрелками.Связность, то есть межцепочечная дисульфидная связь µ-цепей, обозначается как электрическая связность. В (C) дисульфидные связи Cµ3 соединяются с µ-цепями параллельно с дисульфидными связями Cµ4tp, и эти дисульфидные связи последовательно соединяются с µ-цепями с дисульфидными связями Cµ2. В (D) дисульфидные связи Cµ2 и Cµ4tp соединяют µ-цепи параллельно, и оба типа последовательно соединяют µ-цепи с дисульфидными связями Cµ3. (Рисунок воспроизведен с разрешения издателя и авторов [10] ).
Мультимерная структура IgM схематически показана на рисунке 1. На рисунке 1А показан «гетеродимер», состоящий из одной легкой цепи, обозначенной L, и одной тяжелой цепи, обозначенной µ. Тяжелые и легкие цепи удерживаются вместе как дисульфидными связями (изображенными в виде красных треугольников), так и нековалентными взаимодействиями.
На фигуре 1B показаны две единицы мкл, связанные дисульфидной связью в доменах Cµ2; эту (мкл) 2 структуру часто называют «мономером» IgM, так как она в некотором смысле аналогична структуре иммуноглобулина G (IgG).
На основании его скорости оседания и появления на электронных микрофотографиях, было сделано заключение, что IgM является в основном «пентамером», то есть полимером, состоящим из пяти «мономеров» [(µL) 2] 5, и первоначально был изображен модели на рисунках 1C и 1D с дисульфидными связями между доменами Cµ3 и между концевыми частями. [11] [12] Также показано, что пентамерный IgM включает третий белок, J-цепь. J-цепь (J для присоединения) была открыта как ковалентно связанный компонент полимерных IgA и IgM. [13] [14] J цепь представляет собой небольшой (~ 137 аминокислот) кислый белок. Как показано, J-цепь соединяется с двумя µ-цепями через дисульфидные связи с участием цистеинов в хвостовых частях. [15]
Молекулярные требования для формирования полимерного IgM
Первоначально предполагалось, что J-цепь будет важна для образования полимерных иммуноглобулинов, и действительно, полимеризация IgA сильно зависит (но не абсолютно) от J-цепи. [16] [17] Напротив, полимерный IgM эффективно образуется в отсутствие J-цепи. [18] [19]
Преобладающей формой IgM человека и мыши является пентамер. Для сравнения, IgM из лягушки (Xenopus) является преимущественно гексамером, [20] [21] IgM из костной рыбы является преимущественно тетрамером, а IgM из хрящевой рыбы (акула) является преимущественно пентамером. [22] [23] Несмотря на преобладание пентамера в IgM мыши и человека, было очевидно, что эти IgM также могут существовать в виде гексамера. [24] [25] Последующие исследования с использованием систем экспрессии рекомбинантной ДНК показали, что гексамер является основной формой мышиного IgM, когда IgM продуцируется в условиях, где предотвращается включение J-цепи, либо путем продуцирования IgM в клетках которые лишены J-цепи [18] или из-за производства IgM с µ-тяжелой цепью, в которой отсутствует цистеин в хвостовой части. [26] [27] Таким образом, гексамерный IgM никогда не содержит J-цепь; Пентамерный IgM может быть сформирован так, чтобы включать или не включать J-цепь. [28]
Важным отличием между тяжелыми цепями µ и γ является наличие цистеинов для образования дисульфидных связей между тяжелыми цепями. В случае γ-тяжелой цепи единственные меж-γ-связи образуются цистеинами в шарнире, и, соответственно, каждая γ-цепь связывается только с одной другой γ-цепью. В противоположность этому, домены Cµ2 и Cµ3 и хвостовая часть содержат цистеин, который образует дисульфидную связь с другой µ-цепью.Цистеины в доменах Cµ2 опосредуют образование мономерного IgM (мкл) 2. Хвостовая часть наряду с включенным цистеином необходима и достаточна для образования полимерных иммуноглобулинов. То есть удаление хвостовой части из тяжелой цепи µ предотвращает образование полимерного IgM. [29] И наоборот, клетки, экспрессирующие тяжелую цепь γ, которая была модифицирована для включения хвостовой части, продуцируют полимерный IgG. [30] [31] [32]
Роль цистеина в домене Cµ3 более тонкая.Фигуры 1C и 1D представляют возможные модели пентамерного IgM. В этих моделях каждая µ-цепь предназначена для связывания двух других µ-цепей. Однако ни одна из моделей не может полностью объяснить структуру полимерного IgM. Например, модель на рисунке 1C предсказывает, что дисульфидная связь между доменами Cµ2 важна для получения дисульфидно-связанных полимерных IgM. Модель на рисунке 1D предсказывает, что дисульфидная связь между доменами Cµ3 является существенной. На самом деле, связанный с дисульфидом полимерный IgM все же может быть получен, если отсутствует один из трех цистеинов.В контексте моделей, в которых каждая µ-цепь взаимодействует только с двумя другими µ-цепями, эти результаты показывают, что некоторые молекулы похожи на рис. 1C, а некоторые — на рис. 1D. Тем не менее, наличие трех цистеинов для связывания между µ-цепями предполагает, что каждая из µ-цепей может связывать три другие µ-цепи, как показано на рисунке 2. В том же духе на рисунке 2C представлена модель пентамера, содержащего J-цепь, который отражает доказательства того, что J-цепь соединяется с µ-цепями, которые не связаны с другими µ-цепями цистеинами в доменах Cµ3Эти и другие модели, как регулярные, так и неправильные, обсуждаются в другом месте. [27] [33]
Рисунок 2. Некоторые альтернативные способы связывания µ-цепей
A, B) На этих фигурах изображены две из многих возможных моделей дисульфидной связи между µ-цепями в гексамерном IgM. Как и на рисунке 1, дисульфидные связи Cµ2 и дисульфидные связи Cµ4tp представлены красной двойной стрелкой, а дисульфидные связи Cµ3 представлены длинными двуглавыми стрелками. В обеих моделях A и B каждый тип дисульфидной связи (Cµ2-Cµ2; Cµ3-Cµ3; Cµ4tp-Cµ4tp) соединяет µ-цепи последовательно друг с другом.Методы различения этих и других моделей обсуждаются в [28].
C) Это представление пентамерного IgM показывает, как J-цепь может быть связана с µ-цепями, которые не связаны через Cµ3 дисульфидные связи
Пентамерный IgM обычно представлен как содержащий одну J-цепь на полимер, но в действительности измерения стехиометрии J-цепи варьировались от одной молекулы J на полимер до трех молекул J на полимер. [34] [35] [36] [37] Широкий диапазон может быть вызван техническими проблемами, такими как неполная радиоактивная метка или неточное количественное определение линии Ухтерлони.Однако изменение также может быть обусловлено гетерогенностью препаратов IgM, то есть различные препараты могут существенно различаться по содержанию J-содержащих и J-дефицитных полимеров.
Третичная и четвертичная структура константной области µ
Чтобы лучше понять детальную трехмерную структуру µ-цепи, отдельные домены Cµ2, Cµ3 и Cµ4tp были получены отдельно в E.coli и затем проанализированы различными методами, включая скорость осаждения, рентгеновскую кристаллографию и ЯМР спектроскопия.Как и в случае других иммуноглобулинов, домены тяжелой цепи имеют характерные вышележащие β-листы, включающие семь нитей, стабилизированные дисульфидными связями внутри домена. В целом, константная область IgM имеет «грибоподобную» структуру, где домены Cµ2-Cµ3 представляют собой диск, аналогичный головке гриба, а домены Cµ4tp выступают в виде короткого стебля. [38]
Функция
IgM взаимодействует с несколькими другими физиологическими молекулами:
- IgM может связывать комплементный компонент C1 и активировать классический путь, приводящий к опсонизации антигенов и цитолизу.
- IgM связывается с рецептором полииммуноглобулина (pIgR) в процессе, который переносит IgM на поверхности слизистой оболочки, такие как просвет кишечника и в грудное молоко. Это связывание зависит от J-цепи. [39]
- Были обнаружены два других Fc-рецептора, которые связывают IgM — Fcα / µ-R и Fcµ-R. Fcα / µ-R, подобно pIgR, связывает полимерные IgM и IgA. Fcα / µ-R может опосредовать эндоцитоз, и его экспрессия в кишечнике предполагает роль в иммунитете слизистой оболочки. Fcµ-R (ранее известный как Toso / Faim3) связывает исключительно IgM и может опосредовать клеточное поглощение IgM-конъюгированного антигена. [40] Инактивация соответствующих генов у нокаутированных мышей вызывает фенотип, но физиологические функции этих рецепторов все еще не определены [41]
Регуляция иммунного ответа
Специфические иммуноглобулины, которые вводят животным вместе с их антигеном, могут влиять на реакцию антител на этот же антиген. [42] Эндогенные антитела, продуцируемые после первичной иммунизации, также могут влиять на реакцию антител на бустерную иммунизацию, что позволяет предположить, что подобные эффекты возникают при физиологических условиях.«Регулирующие» эффекты могут быть как положительными, так и отрицательными. То есть, в зависимости от типа антигена и изотипа антитела, эффект может быть подавлением или усилением ответа антитела. Такие эффекты хорошо иллюстрируются экспериментами по иммунизации ксеногенными (чужеродными) эритроцитами (эритроцитами). Например, когда IgG вводят вместе с ксеногенными эритроцитами, эта комбинация вызывает почти полное подавление реакции антител, специфичных к эритроцитам.Этот эффект используется клинически для предотвращения иммунизации резус-отрицательных матерей против резус-положительных эритроцитов плода, и его применение резко снизило частоту гемолитических заболеваний у новорожденных. [43] В отличие от эффекта IgG, антиген-специфический IgM может значительно усиливать реакцию антител, особенно в случае больших антигенов. [44] Таким образом, когда IgM, специфичный для эритроцитов, инъецируют животным (включая людей) вместе с эритроцитами, индуцируется гораздо более сильный ответ антител на эритроциты, чем когда эритроциты вводят отдельно.Несколько линий доказательств указывают на то, что способность IgM активировать комплемент необходима для его усиливающего эффекта. Таким образом, IgM-опосредованное усиление не происходит ни у животных, которые были истощены по компоненту С3 комплемента, ни у мутантных животных, не имеющих рецепторов комплемента 1 и 2. Аналогично, мутантный IgM, который не может активировать комплемент, не усиливает иммунный ответ. Возможное объяснение IgM-опосредованного усиления состоит в том, что В-лимфоциты захватывают комплексы IgM-антиген-комплемент и транспортируют комплексы в области селезенки, где генерируются эффективные иммунные ответы.Поскольку IgM вырабатывается на ранней стадии иммунного ответа, это может быть важно при инициации ответов антител.
Синтез
В клетках зародышевой линии (сперматозоиды и яйцеклетки) гены, которые в конечном итоге будут кодировать иммуноглобулины, не находятся в функциональной форме (см. V (D) J-рекомбинация). В случае тяжелой цепи три сегмента зародышевой линии, обозначенные V, D и J, лигируют вместе и присоединяют к ДНК, кодирующей константную область тяжелой цепи µ. В начале онтогенеза B-клетки экспрессируют тяжелые цепи как µ, так и δ; коэкспрессия этих двух тяжелых цепей, каждая из которых несет один и тот же V-домен, зависит от альтернативного сплайсинга и альтернативных сайтов добавления поли-А.Экспрессия других изотипов (γ, ε и α) осуществляется посредством другого типа перестройки ДНК, процесса, называемого переключением класса иммуноглобулина. [45]
Клиническое значение
IgM — это первый иммуноглобулин, экспрессированный в человеческом плоде (около 20 недель), [46] и филогенетически самое раннее антитело, которое должно появиться. [47]
IgM-антитела появляются на ранних стадиях инфекции и обычно появляются в меньшей степени после дальнейшего воздействия.Антитела IgM не проходят через плаценту человека (только изотип IgG).
Эти два биологических свойства IgM делают его полезным в диагностике инфекционных заболеваний. Демонстрация антител IgM в сыворотке пациента указывает на недавнюю инфекцию или в сыворотке новорожденного указывает на внутриутробную инфекцию (например, синдром врожденной краснухи).
Развитие антидонорного IgM после трансплантации органов не связано с отторжением трансплантата, но может оказывать защитное действие. [48]
IgM в нормальной сыворотке часто связывают со специфическими антигенами даже в отсутствие предварительной иммунизации. [49] По этой причине IgM иногда называют «природным антителом». Это явление, вероятно, связано с высокой авидностью IgM, которая позволяет ему детектируемо связываться даже со слабо перекрестно реагирующими антигенами, которые встречаются в природе. Например, антитела IgM, которые связываются с антигенами эритроцитов A и B, могут образовываться в раннем возрасте в результате воздействия A- и B-подобных веществ, которые присутствуют на бактериях или, возможно, также на растительных материалах. Collins, C .; Цуй, Ф. З .; Шульман М.Дж. (2002). «Дифференциальная активация комплемента человека и морской свинки пентамерным и гексамерным IgM». Европейский журнал иммунологии . 32 (6): 1802–1810. DOI: 10.1002 / 1521-4141 (200206) 32: 6 <+1802 :: АИД-IMMU1802> 3.0.CO; 2-С. PMID 12115664. .
Эти примеры взяты из Кембриджского английского корпуса и из источников в Интернете. Любые мнения в примерах не соответствуют мнению редакторов Cambridge Dictionary или издательства Cambridge University Press или его лицензиаров.
Больше примеров Меньше примеров
Лечение миокардита остается спорным (иммуносупрессия, иммуномодуляция иммуноглобулинами, интерферон или противовирусная терапия?).После заражения не наблюдалось увеличения иммуноглобулинов ни в одной группе. Переливание альбумина и иммуноглобулинов было необходимо каждые 2 недели, а также замещение кальцием, магнием и, позднее, цинком.Лечение проводится с помощью внутривенного введения иммуноглобулина +/- стероидов, и для любых будущих переливаний следует давать соответствующие антиген-отрицательные клеточные компоненты.Обнаружение связывающего фактора иммуноглобулина с помощью иммуноферментного анализа с использованием двух моноклональных антител. После превращения в кавопульмональное соединение симптомы регрессировали, и замена альбумином и иммуноглобулином больше не требовалась.Множественная миелома характеризуется пролиферацией одного клона плазматических клеток, продуцирующих один иммуноглобулина . ,Иммуноглобулин М (IgM) — Структура и функции
Home »Клинические проявления вируса гепатита A» Иммуноглобулин M (IgM) — структура и функции
Последнее обновление: Sagar Aryal
- Иммуноглобулин М (IgM) — это рецептор антигена на В-клетках и первое антитело, вырабатываемое при иммунном ответе.
- Он присутствует как на В-клетках, так и в виде растворимой молекулы в крови.
- Из-за своего большого размера (900 кДа) IgM обнаруживается главным образом во внутрисосудистом пространстве, то есть в кровотоке, а также в лимфатической жидкости.
- сывороточный IgM существует в виде пентамера и составляет приблизительно 10% от нормального содержания человеческого сывороточного Ig. Это третий самый распространенный человеческий иммуноглобулин.
- Он преобладает в первичных иммунных реакциях на большинство антигенов и является наиболее эффективным фиксирующим комплемент иммуноглобулин.
- Плазмабласты, которые находятся в селезенке, как полагают, являются основным местом специфического производства IgM.

Состав IgM
Иммуноглобулин М является третьим наиболее распространенным сывороточным иммуноглобулином и принимает одну из двух форм:
- Пентамер, в котором все тяжелые цепи идентичны и все легкие цепи идентичны
- мономер (обнаружен на B-лимфоцитах как рецепторы B-клеток)
- На поверхности B-клетки эта молекула экспрессируется на плазматической мембране в виде мономера с четырехцепочечным звеном — двумя µ H-цепями и двумя L-цепями.
- В этой форме это В-клеточный рецептор антигена, причем каждая из Н-цепей содержит дополнительный гидрофобный домен для закрепления в мембране.
- В крови IgM состоит из пяти четырехцепочечных единиц (пентамер), удерживаемых вместе дисульфидными мостиками на карбоксиконцевом конце μ-цепей.
- Каждый из пяти мономеров в структуре пентамера состоит из двух легких цепей (каппа или лямбда) и двух тяжелых цепей. Однако, в отличие от IgG, тяжелая цепь в мономерах IgM состоит из одной вариабельной и четырех константных областей, причем дополнительный константный домен заменяет шарнирную область. J-цепь
- также связана с IgM в крови и инициирует полимеризацию ее субъединиц во время ее секреции из плазматической клетки.
Функции / Значение IgM
- IgM является первым произведенным антителом и основным медиатором первичного иммунного ответа.
- Его эффективность в сочетании с антигеном имеет особое значение до тех пор, пока в организме не будут синтезированы достаточные количества антител IgG.
- Он отвечает за агглютинацию, нейтрализацию и цитолитические реакции и имеет жизненно важное значение в реакциях активации и агглютинации комплемента для борьбы с патогенами.
- IgM взаимодействует с несколькими другими физиологическими молекулами, такими как связывается с компонентом С1 комплемента и активирует классический путь, связывается с рецептором полииммуноглобулина (pIgR) в процессе, который переносит IgM на поверхности слизистой оболочки, такие как просвет кишечника и в грудное молоко и т. Д., И играют роль в защите слизистой оболочки.
- IgM является первым классом иммуноглобулинов, который синтезируется новорожденным и играет роль в патогенезе некоторых аутоиммунных заболеваний.
- Хотя IgM-антитела обычно имеют низкоаффинные сайты связывания с антигеном, у них есть десять комбинирующих сайтов на молекулу, которые могут взаимодействовать друг с другом.Таким образом, он обладает высокой авидностью к антигенам и очень эффективен для каждой молекулы в борьбе с патогенами, особенно на ранних стадиях иммунного ответа.
- Повышенные уровни IgM могут быть признаком недавней инфекции или воздействия антигена.
Список литературы
- https://www.thermofisher.com/np/en/home/lifescience/antibodies/antibodies-learning-center/antibodies-resource-library/antibody-methods/immunoglobulin-igm-class.html
- https: //www.sciencedirect.ru / themes / биохимия-генетика-молекулярная биология / иммуноглобулин-m
- https://www.bio-rad-antibodies.com/igm-antibodies-immunoglobulin-m.html
- Lydyard, P.M., Whelan, A., & Fanger, M.W. (2005). Иммунология (2-е изд.). Лондон: BIOS Scientific Publishers.
- Playfair, J. & Chain, B. (2001). Иммунология с первого взгляда. Лондон: Blackwell Publishing.
- Brooks, G.F., Jawetz, E., Melnick, J.L. & Adelberg, E.A. (2010). Медицинская микробиология Jawetz, Melnick & Adelberg.Нью-Йорк: МакГроу Хилл Медикал.
Категории Иммунология Теги Антитела, IgM, функции IgM, структура IgM, иммуноглобулин, иммуноглобулин M, иммуноглобулин M (IgM) Почтовая навигация ,
Иммуноглобулины: Это антитела, присутствующие в крови, которые вырабатываются В-клетками и используются иммунной системой для идентификации и нейтрализации посторонних объектов, таких как бактерии, вирусы и любые посторонние объекты. Эти иммуноглобулины распознают антигенную часть инородного тела, попадающую в организм человека, которая может представлять собой бактерии, вирусы, грибки, споры, раковые клетки и т. Д.
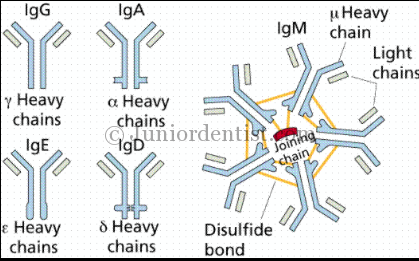
Здесь мы собираемся обсудить некоторые важные аспекты о каждом типе иммуноглобулина.
Иммуноглобулин G:
- Иммуноглобулин G назван так из-за присутствия гамма-H-цепи
- Он также называется теплым иммуноглобулином .
- IgG имеет период полураспада 23 дня
- IgG содержит 80% иммуноглобулинов
- Это основной сывороточный иммуноглобулин
- IgG делится на 4 подкласса: IgG1, IgG2, IgG3, IgG4, которые делятся на сыворотку человека в концентрации 65%, 23%, 8%, 4%
- IgG — самый маленький иммуноглобулин
- Он присутствует в сыворотке крови в концентрации 8-16 мг на мл
- IgG является единственным материнским иммуноглобулином, который проникает через плаценту и отвечает за обеспечение естественного пассивного иммунитета у новорожденного
- Классическая фиксация комплимента положительна
- Преобладающий иммуноглобулин, присутствующий в десневой кривикулярной жидкости — GCF
- секретируется в молоке
Иммуноглобулин М:
- Также называется ХОЛОДНЫМ иммуноглобулином .
- Он назван так из-за присутствия му H цепи
- IgM имеет период полураспада 5 дней
- IgM содержит 5-8% иммуноглобулинов
- Это самый ранний иммуноглобулин, синтезируемый плодом для противодействия инфекциям
- Это старейший иммуноглобулин класса
- антител IgM являются недолговечными с периодом полураспада 5 дней, следовательно, присутствие IgM в сыворотке указывает на недавнюю инфекцию
- IgM также активирует классический путь фиксации комплимента
- Наличие IgM у плода или новорожденного указывает на внутриутробную инфекцию и будет полезно при диагностике врожденных инфекций, таких как сифилис, краснуха, ВИЧ-инфекция.и т. д.
- И IgG, и IgM участвуют в реакции гиперчувствительности типа II или цитотоксическом типе
Иммуноглобулин A:
- Назван так из-за наличия альфа-цепи H
- IgA имеет период полураспада 6 дней
- IgA встречается в 2 формах, т.е. сывороточный IgA и секреторный IgA
- Это второй самый распространенный класс иммуноглобулинов, имеющий 10-13% общего иммуноглобулина
- Это преобладающий иммуноглобулин в слюне
- Это иммуноглобулин, присутствующий в экзокринной секреции, называемый секреторным IgA, который вырабатывается слизистым и железистым эпителием, который защищает сыворотку igA от протеолиза
- IgA встречается в 2 формах 1.Сыворотка IgA 2. Секреторная IgA
- активирует альтернативный путь фиксации комплимента
- секретируется в молоке
Иммуноглобулин E:
- Назван так из-за наличия цепи Epsilon H
- IgE имеет период полураспада 2-8 дней
- процент IgE от всех иммуноглобулинов составляет 1%
- Обладает уникальным свойством теплостойкости, т.е. IgE инактивируется при 56 градусах Цельсия за 1 час.
- Имеет сродство к тучным клеткам одного вида (гомоцитотропизм)
- Опосредует реакцию Prausunitz-Kustner, метод обнаружения атопического антитела
- Он отвечает за анафилактический тип реакций гиперчувствительности: например, контакт Dermatiis
- Это главным образом производится в перевязках дыхательных путей и кишечника
- Считается, что он играет особую роль в паразитарных реакциях.
- Повышение уровня IgE наблюдается при аллергических состояниях, таких как сенная лихорадка, экзема и астма.
Иммуноглобулин D:
- Назван так из-за наличия цепи Delta H
- Это структурно напоминает IgG
- IgD и IgM служит рецепторами распознавания антигенов
- Активирует В-лимфоциты для выработки или подавления антител
Об авторе
Варун Пандула
Я Варун, стоматолог из Хайдарабада, Индия, пытаюсь помочь всем понять проблемы и методы лечения зубов, а также упростить стоматологическое образование для студентов-стоматологов и стоматологического братства.Если у вас есть какие-либо сомнения, не стесняйтесь связаться со мной или оставить комментарий в сообщении, спасибо за посещение.
,