Свертывающая и противосвертывающая системы крови.
4
Наличие определенного объема крови в сосудах, ее жидкое состояние – необходимое условие существование организма. Эти задачи решаются работой свертывающей и противосвертывающей системы. Нарушение равновесия между ними сопровождается тяжелыми последствиями (потерей крови или внутрисосудистым тромбообразованием).
Гемостаз – остановка крови. Возникает при повреждении стенки сосудов.
Обеспечивается:
1) сужением сосуда при повреждении.
2) реакцией тромбоцитов – адгезией.
3) реакцией факторов гемостаза, содержащихся в плазме, форменных элементах и тканях. Они образуют свертывающую систему крови.
Характеристика факторов свертывания крови.
Тромбоциты. У здоровых людей их 200 – 400 ∙ 109 в л., продолжительность жизни 8 – 12 суток. Образуется из стволовой клетки. СК → КПМ → ТПГК → мегакариоцит → тромбоцит.
Днем больше чем ночью.
Свойства:
1) Могут образовывать отростки, которыми прикреплюется к поврежденным стенкам сосудов, закупоривая сосуд.
№ фактора | Название фактора |
I | фибриноген |
II | протромбин |
| III | тканевой протромбин |
IV | Са2+ |
V – VI | проакцелерин и акцелерин |
VII | конвертин |
VIII | антигемофильный глобулин А |
IX | антигемофильный глобулин В и фактор Кристмаса |
X | Стюарта – Прауэра |
XI | плазменный предшественник тромбопластина |
XII | фактор Хагемана |
XIII | фибринстабилизирующий |
3) Участвуют в восстановлении эндотелия сосудов, доставляя макромолекулы клеткам эндотелия.
Эритроциты.
1) Содержат почти все факторы свертываемости крови найденные в тромбоцитах
2) К их поверхности прикрепляются фибриновые нити при образовании фибринового тромба.
Лейкоциты.
1) Содержат вещества способствующие тромбообразованию, но их мало.
2) Лейкоциты активируют разрушение тромба – фибринолиз.
3) Выделяют гепарин, препятствующий свертыванию крови.
Роль тканей в гемостазе (особенно стенки сосудов).
1) Содержит активный тромбопластин, необходимый в образовании тромба.
2) Вещества вызывающие адгезию и агрегацию тромбоцитов.
3) Содержат вещества, активирующие и тормозящие разрушение тромба и тромбообразование.
Виды гемостаза.
↓ ↓
сосудистотромбоцитарный коагуляционный
Сосудистотромбоцитарный.
Роль:
1) обеспечивает остановку кровотечения из сосудов микроциркулярного русла и в сосудах с низким АД;
Фазы.
1 Рефлекторный спазм поврежденных сосудов. Обеспечивается БАВ, которые выделяются из разрушенных тромбоцитов (серотонин, НА, Адр.) – временно прекращают кровотечение. Эта реакция увеличивается при охлаждении поврежденного участка.
2 процесс. Спазм сосудов дополняется: адгезией тромбоцитов.
В силу электростатического взаимодействия (тромбоцит “- „), обнажаются волокна коллагена стенки «+», происходит прилипание тромбоцитов к стенке (3 – 10с).
3 стадия. Обратимая агрегация (скучивание) тромбоцитов. Начинается почти одновременно с адгезией. Катализатор этого процесса АДФ, выделяемая из поврежденных тканей сосуда – внешняя АДФ, из тромбоцитов и эритроцитов – «внутренняя». Образуется рыхлая тромбоцитарная пробка, пропускающая плазму – белый тромб.
4 стадия. Необратимая агрегация – тромбоцитарная пробка становится непроницаемой для плазмы. Происходит это под влиянием тромбина, который меняет структуру мембраны тромбоцитов, и они сливаются в гомогенную массу.
5 Ретракция белого тромба. Это сокращение и уплотнение белого тромба, за счет сокращения нитей фибрина.
Этим путем (сосудисто-тромбоцитарным) останавливается кровотечение из сосудов МЦР за 3 – 4 минуты при бытовых травмах.
Коагуляционный гемостаз.
При ранении сосудов с высоким давлением остановка кровотечения начинается также с сосудисто-тромбоцитарных реакций. Но образующийся при этом белый тромб не в состоянии остановить кровотечение. Начиная с 4ой стадии сосудисто-тромбоцитарного гемостаза, включаются биохимические процессы коагуляционного гемостаза, который заканчивается превращением фибриногена в фибрин. Это превращение происходит поэтапно. Механизм свертывания разработан Шмидтом и развита Моравицем.
Стадии коагуляционного гемостаза.
2. Свёртывающая, противосвёртывающая, фибринолитическая системы крови.
Остановка кровотечения, т.е. гемостаз может осуществляться двумя путями. При повреждении мелких сосудов она происходит за счет первичного или сосудисто-тромбоцитарного гемостаза. Он обусловлен сужением сосудов и закупоркой отверстия склеившимися тромбоцитами. При повреждении этих сосудов происходит прилипание или адгезия тромбоцитов к краям раны. Из тромбоцитов начинают выделяться АДФ, адреналин и серотонин. Серотонин и адреналин суживают сосуд. Затем АДФ вызывает агрегацию, т.е. склеивание тромбоцитов. Это обратимая агрегация. После, под влиянием тромбина, образующегося в процессе вторичного гемостаза, развивается необратимая агрегация большого количества тромбоцитов. Образуется тромбоцитарный тромб, который уплотняется, т.е. происходит его ретракция. За счет первичного гемостаза кровотечение останавливается в течение 1-3 минут.
Вторичный гемостаз или гемокоагуляция, это ферментативный процесс образования желеобразного сгустка — тромба. Он происходит в результате перехода растворенного в плазме белка фибриногена в нерастворимый фибрин. Образование фибрина осуществляется в несколько этапов и при участии ряда факторов свертывания крови. Они называются прокоагулянтами, так как до кровотечения находятся в неактивной форме. В зависимости от местонахождения факторы свертывания делятся на плазменные, тромбоцитарные, тканевые, эритроцитарные и лейкоцитарные. Основную роль в механизмах тромбообразования играют плазменные и тромбоцитарные факторы.
Выделяют следующие плазменные факторы, обозначаемые римскими цифрами:
I. Фибриноген. Это растворимый белок плазмы крови.
II., 2-глобулин.
III. Тромбопластин. Комплекс фосфолипидов, выделяющийся из тканей и тромбоцитов при их повреждении.
IV. Ионы кальция.
V. Проакцелерин, -глобулин.
VI. Изъят из классификации, так как является активным V фактором.
VII. Проконвертин, -глобулин.
VIII. Антигемофильный глобулин А. -глобулин.
IX. Антигемофильный глобулин В. Фактор Кристмаса. Фермент протеаза.
X. Фактор Стюарта-Прауэра.
XI. Плазменный предшественник тромбопластина. Фактор Розенталя. Иногда называют антигемофильным глобулином С. Протеаза.
XII. Фактор Хагемана. Протеаза.
XIII. Фибринстабилизирующий фактор. Транспептидаза.
Все плазменные прокоагулянты, кроме тромбопластина и ионов кальция синтезируются в печени.
Имеется 12 тромбоцитарных факторов свертывания. Они обозначаются арабскими цифрами. Основные из них:
3. Участвует в образовании плазменной протромбиназы.
4. Антагонист гепарина.
6. Тромбостенин. Вызывает укорочение нитей фибрина.
10. Серотонин. Суживает сосуды, ускоряет свертывание крови.
Свертывание крови происходит в три фазы:
I. Образование активной протромбиназы. Существует 2 ее формы — тканевая и плазменная. Тканевая образуется при выделении поврежденными тканями тромбопластина и его взаимодействии с IV, V, VII и X плазменными прокоагулянтами. Тромбопластин и VII фактор-проконвертин, активируют Х фактор — Стюарта-Прауэра. После этого X фактор связывается с V — проакцелерином. Этот комплекс является тканевой протромбиназой. Для этих процессов нужны ионы кальция. Это внешний механизм активации процесса свертывания. Его длительность 15 сек.
Внутренний механизм запускается при разрушении тромбоцитов. Он обеспечивает образование плазменной протромбиназы. В этом процессе участвуют тромбопластин тромбоцитов, IV, V, VIII, IX, X, XI и XII плазменные факторы и 3 тромбоцитарный. Тромбопластин активирует XII фактор Хагемана, который вместе с 3 фактором тромбоцитов переводит в активную форму XI, фактор Розенталя. Активный XI фактор активирует IX — антигемофильный глобулин В. После этого формируется комплекс из активного IX фактора, VIII — антигемофильного глобулина А, 3 тромбоцитарного фактора и ионов кальция. Этот комплекс обеспечивает активацию X факторa — Стюарта-Прауэра. Комплекс активного X, V фактора — проакцелерина и 3 фактора тромбоцитов является плазменной протромбиназой. Продолжительность этого процесса 2-10 мин.
II. Переход протромбина в тромбин. Под влиянием протромбиназы и IV фактора — ионов кальция, переходит в тромбин. В эту же фазу под действием тромбина происходит необратимая агрегация тромбоцитов.
III. Образование фибрина. Под влиянием тромбина, ионов кальция и XIII — фибринстабилизирующего фактора, фибриноген переходит в фибрин. На первом этапе под действием тромбина фибриноген расщепляется на 4 цепи фибрина мономера. Соединяясь между собой они формируют волокна фибрина-полимера. После этого XIII фактор, активируемый ионами кальция и тромбином, стимулирует образование прочной сети нитей фибрина. В этой сети задерживаются форменные элементы крови. Возникает тромб.
На этом процесс тромбообразования не заканчивается. Под влиянием 6 фактора тромбоцитов — тромбостенина нити фибрина укорачиваются. Происходит ретракция т.е. уплотнение тромба. Одновременно сокращающиеся нити фибрина стягивают края раны, что способствует ее заживлению.
При отсутствии какого-либо прокоагулянта свертывание крови нарушается. Например встречаются врожденные нарушения выработки фибриногена — гипофибринемия, синтеза проакцелерина и проконвертина в печени. При наличии патологического гена в Х-хромосоме нарушается синтез антигемофильного глобулина А и возникает классическая гемофилия. При генетической недостаточности антигемофильного глобулина В, X, XI, XII, XIII факторов также ухудшается свертывание крови. При тромбоцитопении гемокоагуляция также нарушается.
Так как жирорастворимый витамин К имеет исключительное значение для синтеза протромбина, VII, IX и X плазменных факторов, его недостаток в печени ведет к нарушению механизмов свертывания. Это наблюдается при нарушениях функций печени, ухудшении всасывания жиров, угнетении желчеобразования.
Фибринолиз
После заживления стенки сосуда необходимость в тромбе отпадает. Начинается процесс его растворения — фибринолиз. Кроме того, небольшое количество фибриногена постоянно переходит в фибрин. Поэтому фибринолиз необходим и для уравновешивания этого процесса. Фибринолиз такой же цепной процесс, как и свертывание крови. Он осуществляется ферментной фибринолитической системой. В крови содержится неактивный фермент — плазминоген. Под действием ряда других ферментов он переходит в активную форму — плазмин. Плазмин по составу близок к трипсину. Под влиянием плазмина от фибрина отщепляются белки, которые становятся растворимыми. В последующем они расщепляются пептидазами крови до аминокислот. Активация плазминогена происходит несколькими путями. Во-первых, он может активироваться плазмокиназами эндотелиальных и других клеток. Особенно много плазмокиназ в мышечных клетках матки. Во-вторых, его может активировать XII фактор Хагемана совместно с ферментом калликреином. В третьих, переводит его в активную форму фермент урокиназа, образующийся в почках. При инфицировании организма активатором плазминогена может служить стрептокиназа бактерий. Поэтому инфекция попавшая в рану, распространяется по сосудистому руслу. В клинике стрептокиназу используют для лечения тромбозов. Фибринолиз продолжается в течение нескольких суток. Для инактивации плазмина в крови находятся его антагонисты — антиплазмины. Их действие направлено на сохранение тромба. Поэтому во внутренних слоях тромба преобладает плазмин, наружных — антиплазмин.
Противосвертывающая система
В здоровом организме не возникает внутрисосудистого свертывания крови, потому что имеется и система противосвертывания. Обе системы находятся в состоянии динамического равновесия. В противосвертывающую систему входят естественные антикоагулянты. Главный из них антитромбин III. Он обеспечивает 70-80% противосвертывающей способности крови. Антитромбин III тормозит активность тромбина и предотвращает свертывание на II фазе. Свое действие он оказывает через гепарин. Это полисахарид, который образует комплекс с антитромбином. После связывания антитромбина с гепарином, этот комплекс становится активным антикоагулянтом. Другими компонентами этой системы являются антитромбопластины. Это белки C и S, которые синтезируются в печени. Они инактивируют V и VIII плазменные факторы. В мембране эндотелия сосудов имеется белок тромбомодулин, который активирует белок С. Благодаря этому предупреждается возникновение тромбозов. При недостатке этого белка С в крови возникает наклонность к тромбообразованию. Кроме того, имеются антагонисты антигемофильных глобулинов А и В.
Факторы, влияющие на свертывание крови
Нагревание крови ускоряет ферментативный процесс свертывания, охлаждение замедляет его. При механических воздействиях, например встряхивании флакона с кровью, свертывание ускоряется из-за разрушения тромбоцитов. Так как ионы кальция участвуют во всех фазах свертывания крови, увеличение их концентрации ускоряет, уменьшение замедляет его. Соли лимонной кислоты — цитраты связывают кальций и предупреждают свертывание. Поэтому их используют в качестве консервантов крови. Для лечения заболеваний, при которых повышена свертываемость крови, используют фармакологические антикоагулянты. Их делят на антикоагулянты прямого и непрямого действия. К первым относятся гепарины, а также белок слюны медицинских пиявок — гирудин. Они непосредственно тормозят фазы свертывания крови. К антикоагулянтам непрямого действия производные кумаровой кислоты — дикумарин, неодикумарин и др. Они тормозят синтез факторов свертывания в печени. Антикоагулянты применяются при опасности внутрисосудистого свертывания. Например тромбозах сосудов мозга, сердца легких и т.д. Естественными антикоагулянтами являются и компоненты противосвертывающей системы — гепарин, антитромбин III, антитромбопластины, антагонисты антигемофильных глобулинов.
26. Свертывающая и противосвертывающая системы крови.
Механизмы активации белков свертывания крови условно подразделяют на внутренний (кровяной) и внешний (тканевый). Инициирование фибринообразования без участия фактора III — тканевого тромбопластина, например, на участке незначительного повреждения сосудистого эндотелия, происходит по внутреннему механизму. А активация свертывания при значительном повреждении стенки сосуда происходит по внешнему механизму. Оба механизма – и внешний, и внутренний, замыкаются, сходятся на активации фактора Х.
Внутренний механизм активации. Функционирование внутреннего, или кровяного, механизма активации свертывания крови начинается с активации фактора ХII (Хагемана). Он может активироваться под влиянием отрицательно заряженной поверхности коллагенов субэндотелия и поверхности активированных тромбоцитов. Спонтанно активированный фактор XII воздействует на прекалликреин посредством реакции ограниченного протеолиза. Калликреин воздействует на фактор Фитцжеральда (кининоген). В результате кининоген превращается в кинин. Кинин в свою очередь активирует фактор ХI. При этом активированные молекулы фактора ХI способны в дальнейшем осуществлять активацию других неактивных молекул этого же фактора. Кроме того, активация фактора ХI может происходить и при непосредственном влиянии на него активного фактора ХII. В свою очередь, активная форма фактора ХI, в присутствии ионов Са2+, осуществляет активацию фактора IX. Активированный фактор IХ образует комплекс с фактором VIII и в присутствии ионов Са2+ и фактора 3 тромбоцитов активирует фактор Х.
Внешний механизм активации. Начинается с попадания в кровь тканевого фактора (фактор III) при травматических повреждениях сосуда и прилегающих к нему тканей. Тканевой фактор обладает высоким сродством к циркулирующему в крови фактору VII. В присутствии ионов Са2+ тканевой фактор образует комплекс с фактором VII, в результате чего фактор VII активируется. Активный фактор VII воздействует на фактор Х и превращает его в активную форму. В этом месте внешний и внутренний пути активации свертывания крови объединяются, и далее идет единый процесс. Активная форма фактора Х совместно с фактором V и тромбоцитарным фактором 3 и в присутствии ионов Са2+ образуют комплекс, обладающий способностью активировать фактор II, т.е. превращать протромбин в тромбин. Далее тромбин действует на фибриноген, в результате чего последний превращается в фибрин, кровь в месте повреждения сосуда вследствие образования фибрина загустевает, в сгусток попадают тромбоциты и многочисленные эритроциты, после чего сгусток уплотняется и прочно закупоривает дефект в стенке сосуда.
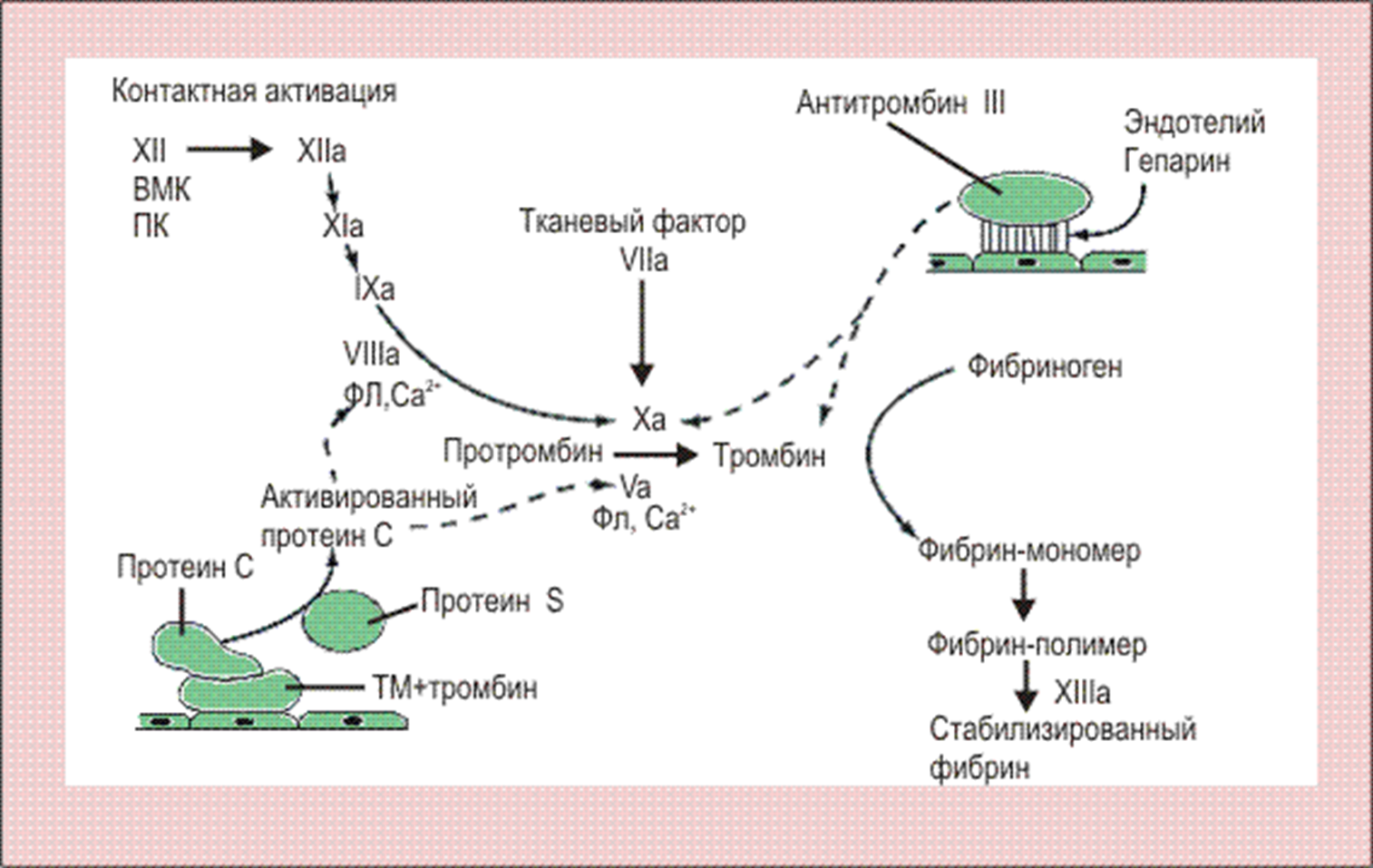
Противосвертывающую систему крови можно разделить на две отдельных системы – антикоагулянтную систему и фибринолитическую (плазминовую) системы. Функция антикоагулянтной системы состоит в сохранении крови в жидком состоянии, функция фибринолитической системы состоит в растворении уже образовавшегося кровяного тромба.
Антикоагулянтная система представлена первичными и вторичными антигоагулянтами. Первичные антикоагулянты синтезируются в организме как обособленные вещества и постоянно с определенной скоростью выделяются в кровоток. Там они взаимодействуют с активными факторами свертывания крови, нейтрализуя их, и тем самым сохраняют кровь в жидком состоянии. Они не действуют на неактивные формы факторов свертывания.
Примером первичного антикоагулянта является гепарин. Гепарин является сульфатированным полисахаридом с молекулярной массой около 12000 Да. Синтезируется в тучных клетках. Не проникает через плаценту. В большом количестве содержится в печени и легких. С фибриногеном и плазмином образует комплексы и тем самым ингибирует их активность. В малых концентрациях ингибирует реакцию между факторами IX, VIII и 3. Тормозит некоторые функции тромбоцитов. Экзогенный гепарин инактивируется главным образом в печени, но около 20 % его выделяется с мочой.
Вторичные антикоагулянты образуются из факторов свертывания и других белков в результате их протеолиза в процессе свертывания крови и фибринолиза. Фибринолитическая система организма осуществляет расщепление фибринового сгустка, в результате которого происходит восстановление просвета сосуда. Фибринолиз начинается одновременно с ретракцией сгустка, но идет медленнее. Фибринолитическая система состоит из плазминового звена – основного звена фибринолиза, и неплазминового звена – фибринолитических компонентов лейкоцитов, тромбоцитов и эритроцитов, непосредственно расщепляющих фибрин. Плазминовая система включает четыре основных компонента – плазминоген (профибринолизин), плазмин (фибринолизин), активаторы проферментов фибринолиза и его ингибиторы. Плазминоген – белок, широко распространенный в организме. Он обнаруживается в плаценте, сперме, миометрии, эндометрии, но, главным образом, в плазме крови, где его концентрация достигает 0,2 г/л. Под действием некоторых активаторов плазминоген превращается в плазмин. Плазмин способен расщеплять фибрин и фибриноген, а также факторы свертывания крови XII и VIII.
Регуляция свертывания крови. Регуляция свертывания крови осуществляется посредством нейрогуморальных механизмов. Возбуждение симпатической нервной системы, возникающее при стрессовых ситуациях, страхе, боли, а также повышенная секреция адреналина мозговым слоем надпочечников резко ускоряют свертывание крови, вызывая состояние, называемое гиперкоагулемией. Тем самым организм в случае физического повреждения подготавливается к более быстрому тромбообразованию. Основная роль в этом механизме принадлежит адреналину и норадреналину. Выбрасываемый в кровоток адреналин способствует высвобождению из сосудистой стенки тромбопластина, который быстро превращается в крови в протромбиназу. Под действием адреналина в крови также активируется фактор Хагемана. Процесс свертывания крови может регулироваться условнорефлекторно через автономную нервную систему и эндокринные механизмы. Значение условнорефлекторной гиперкоагуляции состоит в подготовке организма к защите от кровопотери.
4. Противосвертывающая система. Противосвертывающие механизмы
Несмотря на то, что в циркулирующей крови содержатся все необходимые для ее свертывания факторы, она остается жидкой. Это один из параметров гомеостаза.
Механизмы, поддерживающие жидкое состояние крови:
Гладкая поверхность эндотелия сосудов (предотвращается активация фактора Хагемана, агрегация тромбоцитов).
Отрицательные заряды стенки сосудов и форменных элементов крови, что обеспечивает отталкивание их друг от друга.
Стенки сосудов покрыты слоем (тонким) растворимого фибрина, обладающего способностью адсорбировать активные факторы свертывания крови.
Большая скорость тока крови (препятствует образованию большой концентрации активаторов гемокоагуляции в одном месте).
Наличие естественных антикоагулянтов.
В организме имеются 2 группы антикоагулянтов:
1. Первичные (предшествующие, имеются в крови до начала свертывания крови).
2. Вторичные (образуются в процессе свертывания крови или фибринолиза).
Первичные антикоагулянты ― антитромбопластины, антитромбины.
Антитромбин II (гепарин). Гепарин тормозит все фазы гемокоагуляции.
Антитромбин III ― плазменный фактор гепарина. Переводящий тромбин в неактивный метатромбин.
Антитромбин IV.
Тромбоксан ― тормозит агрегацию тромбоцитов.
Вторичные антикоагулянты. Функция вторичных антикоагулянтов заключается в ограничении внутрисосудистого свертывания крови.
Антитромбин I (фибрин). Способен адсорбировать значительное (до 90%) количество тромбина.
Антикоагулянты, образующиеся при фибринолизе (продукты деградации протромбина, фибриногена и фибрина).
Антикоагулянты, применяемые в лабораторной клинической практике:
1. Гепарин.
2. Лимонная кислота и ее соли (лимоннокислый натрий) 0,5% раствор.
Скорость свертывания крови ускоряется при:
Нарушении стенки сосудов.
Увеличении образования тромбопластина.
Увеличении поступления в организм витамина К.
Увеличении образования фибриногена.
Повышении температуры.
Повышенной смачиваемости стенок пробирки (in vitro).
Повышенном содержании в крови аминокислот.
Снижении процесса фибринолиза.
Скорость свертывания крови замедляется при:
Снижении образования тромбопластина.
Недостаточности всасывания витамина К в желудочно-кишечном тракте.
Повышенной выработке антикоагулянтов.
Понижении образования фибриногена.
Заболеванием, связанным с несвертываемостью крови, вследствие наследственной недостаточности отдельных плазменных факторов свертывания, является гемофилия. Различают следующие виды гемофилий:
Гемофилия типа А ― нарушена I фаза свертывания (образование тромбопластина). При отсутствии FVIII (антигемофильного глобулина А). Нарушаются также II и III фазы.
Гемофилия типа В ― отсутствие FIX (фактора Кристмаса).
Гемофилия типа С — отсутствие FXI (плазменного предшественника тромбопластина).
Гемофилия типа D ― при отсутствии FXII (фактора Хагемана).
Гемофилией болеют преимущественно мужчины.
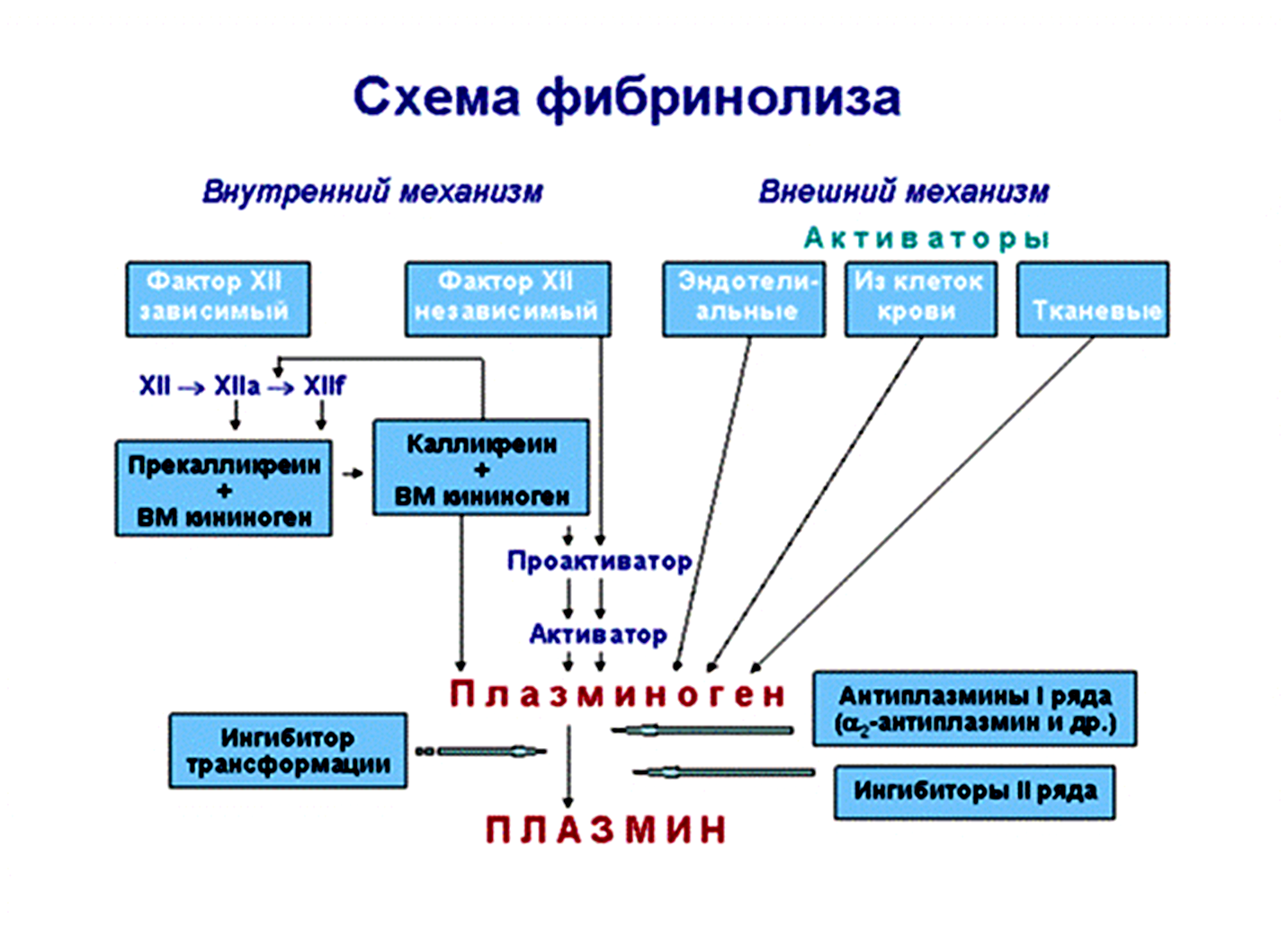
5. Фибринолиз.
Фибринолиз ― растворение сгустка крови. Считается, что в крови постоянно происходит превращение небольшого количества фибриногена в фибрин, который подвергается растворению — фибринолизу.
И только при повреждении ткани процесс образования фибрина преобладает над фибринолизом и наступает местное (локальное) свертывание крови. Главная функция фибринолиза ― восстановление просвета (реканализация) кровеносного сосуда, закупоренного тромбом.
Фибринолиз начинается сразу же и одновременно с ретракцией сгустка и протекает в 2 фазы:
I фаза ― превращение плазменного неактивного (профермента) плазминогена в активную его форму ― плазмин.
II фаза ― расщепление фибрина (тромба) до пептидов и аминокислот под влиянием протеолитического действия плазмина.
Фактором, обеспечивающим фибинолиз, является плазминоген (белок плазмы), который под влиянием тканевых или кровяных факторов (фибринокиназ) превращается в активную форму ― плазмин.
Противосвертывающие механизмы.
В нормальных условиях кровь в сосудах всегда находится в жидком состоянии, хотя условия для образования внутрисосудистых тромбов существуют постоянно. Поддержание жидкого состояния крови обеспечивается по принципу саморегуляции с формированием соответствующей функциональной системы. Главными аппаратами реакций этой функциональной системы являются свертывающая я противосвертывающая системы. В настоящее время принято выделять две Противосвертывающие системы — первую и вторую.
Первая противосвертывающая система (ППС) осуществляет нейтрализацию тромбина в циркулирующей крови при условии его медленного образования и в небольших количествах. Нейтрализация тромбина осуществляется теми антикоагулянтами, которые постоянно находятся в крови и поэтому ППС функционирует постоянно. К таким веществам относятся:
• фибрин, который адсорбирует часть тромбина;
• антитромбины (известно 4 вида антитромбинов), они препятствуют превращению протромбина в тромбин;
• гепарин — блокирует фазу перехода протромбина в тромбин и фибриногена в фибрин, а также тормозит первую фазу свертывания крови;
• продукты лизиса (разрушения фибрина), которые обладают антитромбиновой активностью, тормозят образование протромбиназы;
• клетки ретикуло-эндотелиальной системы поглощают тромбин плазмы крови.
При быстром лавинообразном нарастании количества тромбина в крови ППС не может предотвратить образование внутрисосудистых тромбов. В этом случае в действие вступает вторая противосвертывающая система (ВПС), которая обеспечивает поддержание жидкого состояния крови в сосудах рефлекторно-гуморальным путем по следующей схеме. Резкое повышение концентрации тромбина в циркулирующей крови приводит к раздражению сосудистых хеморецепторов. Импульсы от них поступают в гигантоклеточное ядро ретикулярной формации продолговатого мозга, а затем по эфферентным путям к ретикуло-эндотелиальной системе (печень, легкие и др.). В кровь выделяются в больших количествах гепарин и вещества, которые осуществляют и стимулируют фибринолиз (например, активаторы плазминогена).
Гепарин ингибирует первые три фазы свертывания крови, вступает в связь с веществами, которые принимают участие в свертывании крови. Образующиеся при этом комплексы с тромбином, фибриногеном, адреналином, серотонином, фактором XIII и др. обладают антикоагулянтной активностью и литическим действием на нестабилизированный фибрин.
Следовательно, поддержание крови в жидком состоянии осуществляется благодаря действию ППС и ВПС.
Регуляция системы свертывания.
Регуляция свертывания крови осуществляется с помощью нейрогуморальных механизмов. Возбуждение симпатического отдела вегетативной нервной системы, возникающее при страхе, боли, при стрессовых состояниях, приводит к значительному ускорению свертывания крови, что называется гиперкоагуляцией. Основная роль в этом механизме принадлежит адреналину и норадреналину. Адреналин запускает ряд плазменных и тканевых реакций.
Во-первых, высвобождение из сосудистой стенки тромбопластина, который быстро превращается в тканевую протромбиназу.
Во-вторых, адреналин активирует фактор XII, который является инициатором образования кровяной протромбиназы.
В-третьих, адреналин активирует тканевые липазы, которые расщепляют жиры и тем самым увеличивается содержание жирных кислот в крови, обладающих тромбопластической активностью.
В-четвертых, адреналин усиливает высвобождение фосфолипидов из форменных элементов крови, особенно из эритроцитов.
Раздражение блуждающего нерва или введение ацетилхолина приводит к выделению из стенок сосудов веществ, аналогичных тем, которые выделяются при действии адреналина. Следовательно, в процессе эволюции в системе гемокоагуляции сформировалась лишь одна защитно-приспособительная реакция — гиперкоагулемия, направленная на срочную остановку кровотечения. Идентичность сдвигов гемокоагуляции при раздражении симпатического и парасимпатического отделов вегетативной нервной системы свидетельствует о том, что первичной гипокоагуляции не существует, она всегда вторична и развивается после первичной гиперкоагуляции как результат (следствие) расходования части факторов свертывания крови.
Ускорение гемокоауляции вызывает усиление фибринолиза, что обеспечивает расщепление избытка фибрина. Активация фибринолиза наблюдается при физической работе, эмоциях, болевом раздражении.
На свертывание крови оказывают влияние высшие отделы ЦНС, в том числе и кора больших полушарий головного мозга, что подтверждается возможностью изменения гемокоауляции условно-рефлекторно. Она реализует свои влияния через вегетативную нервную систему и эндокринные железы, гормоны которых обладают вазоактивным действием. Импульсы из ЦНС поступают к кроветворным органам, к органам, депонирующим кровь, и вызывают увеличение выхода крови из печени, селезенки, активацию плазменных факторов. Это приводит к быстрому образованию протромбиназы. Затем включаются гуморальные механизмы, которые поддерживают и продолжают активацию свертывающей системы и одновременно снижают действия противосвертывающей. Значение условно-рефлекторной гиперкоагуляции состоит, видимо, в подготовке организма к защите от кровопотери.
Система свертывания крови входит в состав более обширной системы — системы регуляции агрегатного состояния крови и коллоидов (PACK), которая поддерживает постоянство внутренней среды организма и ее агрегатное состояние на таком уровне, который необходим для нормальной жизнедеятельности путем обеспечения поддержания жидкого состояния крови, восстановления свойств стенок сосудов, которые изменяются даже при нормальном их функционировании.
Несмотря на наличие очень мощной свертывающей системы, кровь находится в живом организме в жидком состоянии в связи с наличием противосвертывающей системы. В ее образовании, так же как в формировании системы свертывания крови, участвует ряд факторов плазмы крови, тромбоцитов и тканей. К ним относят антикоагулянты – антитромбопластины, антитромбины, а также фибринолитическую систему крови. Считается, что в организме существуют специфические ингибиторы для каждого фактора свертывания крови (антиакцелерин, антиконвертин и др.). Снижение активности этих ингибиторов повышает свертываемость крови и способствует образованию тромбов. Повышение же их активности, наоборот, затрудняет свертывание крови и может сопровождаться геморрагией. Сочетание явлений рассеянного тромбоза и геморрагии может быть обусловлено нарушением регуляторных взаимоотношений свертывающей и противосвертывающей систем.
Наиболее быстродействующими компонентами противосвертывающей системы являются антитромбины. Они относятся к прямым или первичным антикоагулянтам, так как находятся в активной форме, а не в виде предшественников. Предполагают наличие в плазме около 6 различных антитромбинов, наиболее изученным из которых является гепарин, препятствующий действию тромбина на фибриноген и тормозящий превращение протромбина в тромбин. Гепарин предупреждает свертывание крови как in vivo, так и in vitro. Антагонистом его является прежде всего протамина сульфат.
Образующиеся в процессе свертывания крови и фибринолиза вторичные антикоагулянты представляют собой «отработанные» факторы свертывания. Так образовавшийся фибрин адсорбирует и нейтрализует 90% тромбина, поэтому его называют антитромбином I. Содержание фибриногена, а2 – антигепарина и антитромбина III в плазме крови животных (крысы, морские свинки, кролики и др.) сопоставимо с таковым человека.
В кровеносных сосудах имеются хеморецепторы, способные реагировать на появление в крови активного тромбина, связанные с нейрогуморальным механизмом, регулирующим образование антикоагулянтов. Таким образом, если тромбин появляется в циркулирующей крови в условиях нормального нейрогуморального контроля, то в этом случае он не только не вызывает свертывания, но, напротив, рефлекторно стимулирует образование антикоагулянтов и, тем самым, выключает свертывающий механизм. Не менее важно применение так называемых искусственных антикоагулянтов. Например, учитывая стимуляцию витамином К синтеза в печени протромбина, проакцелерина, проконвертина, фактора Прауэра-Стюарта, для снижения активности противосвертывающей системы крови назначают антикоагулянты типа антивитаминов К, которые тормозят в клетках печени синтез перечисленных факторов свертывания крови. Эффект наблюдается не сразу, а спустя несколько часов и даже суток.
1.8. Регуляция свертывания крови.
В норме внутрисосудистого свертывания крови не происходит, либо протекает в очень незначительной степени. Тонкая регуляция процесса свертывания крови является результатом взаимодействия многих факторов и систем:
1. Присутствие в плазме целого ряда ингибиторов прокоагулянтов.
2. Многие факторы прочно связываются со сгустком — это ограничивает их действие.
3. Концентрация прокоагулянтов уменьшается вследствие их разведения протекающей кровью. Поэтому тромбы не образуются в сосудах с быстрым кровотоком, но возникают при венозном стазе (при варикозном расширении вен).
4. Прокоагулянты из крови удаляются печенью.
В целом механизм регуляции свертывания крови нейрогуморальный. В организме существуют специальные хеморецепторы (особенно каротидной и аортальной зон), реагирующие на концентрацию в крови тромбина, плазмина и других факторов свертывающей и противосвертывающей систем. Основным интегративным регулятором вегетативных и эндокринных влияний на РАСК является гипоталамус.
Возбуждение симпатической нервной системы (-адренорецепторов) повышает скорость свертывания крови (гиперкоагуляция). Это отмечается при стрессовых состояниях, страхе, боли, сопровождающиеся выделением адреналина надпочечниками.
Под влиянием адреналина:
Высвобождается тромбопластин стенкой сосуда.
Активируется FXII Хагемана ( контактный фактор), который активирует кровяной протромбопластин.
Стимулируется появление в крови тканевых липаз, вызывающих гидролиз жиров, продукты которого повышают тромбопластическую активность.
Активируется высвобождение фосфолипидов из эритроцитов.
Глюкокортикоиды, соматотропный гормон, антидиуретический гормон, кальцитонин, тестостерон, прогестерон первично вызывают гиперкоагуляцию и вторично активируют фибринолиз.
Свертывание крови предотвращается действием сложного рефлекторно-гуморального противосвертывающего механизма.
При появлении в сосудистом русле малых концентрации медленнообразующегося тромбина происходит его прямая нейтрализация естественными антикоагулянтами плазмы (антитромбинами, гепарином). Быстрое и резкое нарастание концентрации тромбина вызывает возбуждение специальных хеморецепторов в сосудах, реагирующих на определенную его концентрацию. Импульсы по афферентным путям поступают в ЦНС. В результате рефлекторно в крови появляются вещества (гепарин и активаторы фибринолиза), блокирующие процесс свертывания.
Часть тромбина удаляется из плазмы в результате поглощения его клетками мононуклеарной фагоцитарной системы (МФС).
Гепарин:
Блокирует образование тромбопластина.
Инактивирует тромбин. Более того, образуются комплексы, способные лизировать фибрин.
Вместе с ним рефлекторно увеличивается количество активаторов плазминогена.
Избыток прокоагулянтов выделяется почками, ЖКТ.
Раздражение парасимпатической нервной системы (n. vagus) приводит к выделению из стенок сосудов веществ, аналогичных тем, что и под влиянием адреналина. Таким образом, в процессе эволюции сформировалась только защитно-приспособительная реакция — гиперкоагулемия, направленная на остановку кровотечения.
Однотипность изменения гемокоагуляции при возбуждении симпатической и парасимпатической нервной системы подтверждает тот факт, что первичной гипокоагуляции нет. Она, если и возникает, то всегда вторична и развивается после гиперкоагулемии вследствие израсходования части прокоагулянтов.
В регуляции свертывания крови принимает участие кора головного мозга. Ее действие реализуется через вегетативную нервную систему и железы внутренней секреции, гормоны которых обладают вазоактивным действием. Как сокращение, так и расширение сосудов приводит к освобождению естественных антикоагулянтов, активаторов фибринолиза и тромбопластина.
Система свертывания крови является составной частью большой системы регуляции агрегатного состояния крови (система РАСК), которая поддерживает гомеостаз и обеспечивает :
Жидкое состояние крови.
Восстановление свойств стенок сосудов.
Поддерживает на оптимальном уровне содержание факторов свертывания на случай травмирования органов, тканей, сосудов.
2. Свёртывающая, противосвёртывающая, фибринолитическая системы крови.
Остановка кровотечения, т.е. гемостаз может осуществляться двумя путями. При повреждении мелких сосудов она происходит за счет первичного или сосудисто-тромбоцитарного гемостаза. Он обусловлен сужением сосудов и закупоркой отверстия склеившимися тромбоцитами. При повреждении этих сосудов происходит прилипание или адгезия тромбоцитов к краям раны. Из тромбоцитов начинают выделяться АДФ, адреналин и серотонин. Серотонин и адреналин суживают сосуд. Затем АДФ вызывает агрегацию, т.е. склеивание тромбоцитов. Это обратимая агрегация. После, под влиянием тромбина, образующегося в процессе вторичного гемостаза, развивается необратимая агрегация большого количества тромбоцитов. Образуется тромбоцитарный тромб, который уплотняется, т.е. происходит его ретракция. За счет первичного гемостаза кровотечение останавливается в течение 1-3 минут.
Вторичный гемостаз или гемокоагуляция, это ферментативный процесс образования желеобразного сгустка — тромба. Он происходит в результате перехода растворенного в плазме белка фибриногена в нерастворимый фибрин. Образование фибрина осуществляется в несколько этапов и при участии ряда факторов свертывания крови. Они называются прокоагулянтами, так как до кровотечения находятся в неактивной форме. В зависимости от местонахождения факторы свертывания делятся на плазменные, тромбоцитарные, тканевые, эритроцитарные и лейкоцитарные. Основную роль в механизмах тромбообразования играют плазменные и тромбоцитарные факторы.
Выделяют следующие плазменные факторы, обозначаемые римскими цифрами:
I. Фибриноген. Это растворимый белок плазмы крови.
II., 2-глобулин.
III. Тромбопластин. Комплекс фосфолипидов, выделяющийся из тканей и тромбоцитов при их повреждении.
IV. Ионы кальция.
V. Проакцелерин, -глобулин.
VI. Изъят из классификации, так как является активным V фактором.
VII. Проконвертин, -глобулин.
VIII. Антигемофильный глобулин А. -глобулин.
IX. Антигемофильный глобулин В. Фактор Кристмаса. Фермент протеаза.
X. Фактор Стюарта-Прауэра.
XI. Плазменный предшественник тромбопластина. Фактор Розенталя. Иногда называют антигемофильным глобулином С. Протеаза.
XII. Фактор Хагемана. Протеаза.
XIII. Фибринстабилизирующий фактор. Транспептидаза.
Все плазменные прокоагулянты, кроме тромбопластина и ионов кальция синтезируются в печени.
Имеется 12 тромбоцитарных факторов свертывания. Они обозначаются арабскими цифрами. Основные из них:
3. Участвует в образовании плазменной протромбиназы.
4. Антагонист гепарина.
6. Тромбостенин. Вызывает укорочение нитей фибрина.
10. Серотонин. Суживает сосуды, ускоряет свертывание крови.
Свертывание крови происходит в три фазы:
I. Образование активной протромбиназы. Существует 2 ее формы — тканевая и плазменная. Тканевая образуется при выделении поврежденными тканями тромбопластина и его взаимодействии с IV, V, VII и X плазменными прокоагулянтами. Тромбопластин и VII фактор-проконвертин, активируют Х фактор — Стюарта-Прауэра. После этого X фактор связывается с V — проакцелерином. Этот комплекс является тканевой протромбиназой. Для этих процессов нужны ионы кальция. Это внешний механизм активации процесса свертывания. Его длительность 15 сек.
Внутренний механизм запускается при разрушении тромбоцитов. Он обеспечивает образование плазменной протромбиназы. В этом процессе участвуют тромбопластин тромбоцитов, IV, V, VIII, IX, X, XI и XII плазменные факторы и 3 тромбоцитарный. Тромбопластин активирует XII фактор Хагемана, который вместе с 3 фактором тромбоцитов переводит в активную форму XI, фактор Розенталя. Активный XI фактор активирует IX — антигемофильный глобулин В. После этого формируется комплекс из активного IX фактора, VIII — антигемофильного глобулина А, 3 тромбоцитарного фактора и ионов кальция. Этот комплекс обеспечивает активацию X факторa — Стюарта-Прауэра. Комплекс активного X, V фактора — проакцелерина и 3 фактора тромбоцитов является плазменной протромбиназой. Продолжительность этого процесса 2-10 мин.
II. Переход протромбина в тромбин. Под влиянием протромбиназы и IV фактора — ионов кальция, переходит в тромбин. В эту же фазу под действием тромбина происходит необратимая агрегация тромбоцитов.
III. Образование фибрина. Под влиянием тромбина, ионов кальция и XIII — фибринстабилизирующего фактора, фибриноген переходит в фибрин. На первом этапе под действием тромбина фибриноген расщепляется на 4 цепи фибрина мономера. Соединяясь между собой они формируют волокна фибрина-полимера. После этого XIII фактор, активируемый ионами кальция и тромбином, стимулирует образование прочной сети нитей фибрина. В этой сети задерживаются форменные элементы крови. Возникает тромб.
На этом процесс тромбообразования не заканчивается. Под влиянием 6 фактора тромбоцитов — тромбостенина нити фибрина укорачиваются. Происходит ретракция т.е. уплотнение тромба. Одновременно сокращающиеся нити фибрина стягивают края раны, что способствует ее заживлению.
При отсутствии какого-либо прокоагулянта свертывание крови нарушается. Например встречаются врожденные нарушения выработки фибриногена — гипофибринемия, синтеза проакцелерина и проконвертина в печени. При наличии патологического гена в Х-хромосоме нарушается синтез антигемофильного глобулина А и возникает классическая гемофилия. При генетической недостаточности антигемофильного глобулина В, X, XI, XII, XIII факторов также ухудшается свертывание крови. При тромбоцитопении гемокоагуляция также нарушается.
Так как жирорастворимый витамин К имеет исключительное значение для синтеза протромбина, VII, IX и X плазменных факторов, его недостаток в печени ведет к нарушению механизмов свертывания. Это наблюдается при нарушениях функций печени, ухудшении всасывания жиров, угнетении желчеобразования.
Фибринолиз
После заживления стенки сосуда необходимость в тромбе отпадает. Начинается процесс его растворения — фибринолиз. Кроме того, небольшое количество фибриногена постоянно переходит в фибрин. Поэтому фибринолиз необходим и для уравновешивания этого процесса. Фибринолиз такой же цепной процесс, как и свертывание крови. Он осуществляется ферментной фибринолитической системой. В крови содержится неактивный фермент — плазминоген. Под действием ряда других ферментов он переходит в активную форму — плазмин. Плазмин по составу близок к трипсину. Под влиянием плазмина от фибрина отщепляются белки, которые становятся растворимыми. В последующем они расщепляются пептидазами крови до аминокислот. Активация плазминогена происходит несколькими путями. Во-первых, он может активироваться плазмокиназами эндотелиальных и других клеток. Особенно много плазмокиназ в мышечных клетках матки. Во-вторых, его может активировать XII фактор Хагемана совместно с ферментом калликреином. В третьих, переводит его в активную форму фермент урокиназа, образующийся в почках. При инфицировании организма активатором плазминогена может служить стрептокиназа бактерий. Поэтому инфекция попавшая в рану, распространяется по сосудистому руслу. В клинике стрептокиназу используют для лечения тромбозов. Фибринолиз продолжается в течение нескольких суток. Для инактивации плазмина в крови находятся его антагонисты — антиплазмины. Их действие направлено на сохранение тромба. Поэтому во внутренних слоях тромба преобладает плазмин, наружных — антиплазмин.
Противосвертывающая система
В здоровом организме не возникает внутрисосудистого свертывания крови, потому что имеется и система противосвертывания. Обе системы находятся в состоянии динамического равновесия. В противосвертывающую систему входят естественные антикоагулянты. Главный из них антитромбин III. Он обеспечивает 70-80% противосвертывающей способности крови. Антитромбин III тормозит активность тромбина и предотвращает свертывание на II фазе. Свое действие он оказывает через гепарин. Это полисахарид, который образует комплекс с антитромбином. После связывания антитромбина с гепарином, этот комплекс становится активным антикоагулянтом. Другими компонентами этой системы являются антитромбопластины. Это белки C и S, которые синтезируются в печени. Они инактивируют V и VIII плазменные факторы. В мембране эндотелия сосудов имеется белок тромбомодулин, который активирует белок С. Благодаря этому предупреждается возникновение тромбозов. При недостатке этого белка С в крови возникает наклонность к тромбообразованию. Кроме того, имеются антагонисты антигемофильных глобулинов А и В.
Факторы, влияющие на свертывание крови
Нагревание крови ускоряет ферментативный процесс свертывания, охлаждение замедляет его. При механических воздействиях, например встряхивании флакона с кровью, свертывание ускоряется из-за разрушения тромбоцитов. Так как ионы кальция участвуют во всех фазах свертывания крови, увеличение их концентрации ускоряет, уменьшение замедляет его. Соли лимонной кислоты — цитраты связывают кальций и предупреждают свертывание. Поэтому их используют в качестве консервантов крови. Для лечения заболеваний, при которых повышена свертываемость крови, используют фармакологические антикоагулянты. Их делят на антикоагулянты прямого и непрямого действия. К первым относятся гепарины, а также белок слюны медицинских пиявок — гирудин. Они непосредственно тормозят фазы свертывания крови. К антикоагулянтам непрямого действия производные кумаровой кислоты — дикумарин, неодикумарин и др. Они тормозят синтез факторов свертывания в печени. Антикоагулянты применяются при опасности внутрисосудистого свертывания. Например тромбозах сосудов мозга, сердца легких и т.д. Естественными антикоагулянтами являются и компоненты противосвертывающей системы — гепарин, антитромбин III, антитромбопластины, антагонисты антигемофильных глобулинов.
