Аполипопротеины — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 27 октября 2017; проверки требует 1 правка. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 27 октября 2017; проверки требует 1 правка.Аполипопротеины (устаревшее аполипопротеиды) — это белковые, как правило амфифильные, составляющие липопротеинов, специфически связывающиеся с соответствующими липидами при формировании липопротеиновой частицы[1].
Например, существует несколько разновидностей транспортных аполипопротеинов, специфически связывающихся с холестерином и различающихся по молекулярной массе, степени растворимости в плазме крови, периоду полужизни в плазме и другим биологическим свойствам (в частности, атерогенным свойствам).[источник не указан 3162 дня]
Синтез аполипопротеинов осуществляется в печени. Среди факторов, влияющих на синтез аполипопротеинов различного типа, можно выделить состав питания, гормоны (инсулин, глюкагон, тироксин, эстрогены, андрогены), употребление алкоголя и различных медикаментов (статины, ниацин).
| Аполипопротеин | Липопротеин | Функция |
|---|---|---|
| А1 | ЛВП[2], хиломикроны | Основной белок ЛВП. Активатор лецитин-холестеролацилтрансферазы (ЛХАТ). Обмениваемый между липопротеинами. Синтезируется в печени и кишечнике. |
| А2 | ЛВП, хиломикроны | Основной белок ЛВП. Синтезируется в печени. |
| А4 | Хиломикроны, ЛВП | Основной белок хиломикронов. Минорный белок ЛВП. Обмениваемый между липопротеинами. Синтезируется в печени и кишечнике. Может активировать ЛХАТ. |
| A5 | ЛВП, ЛОНП[3] | Стимулятор апоC2-активируемого липолиза триглицеридов. |
| B-100 | ЛНП[2], ЛОНП, ЛПП | Основной белок ЛНП. Лиганд для ЛНП-рецептора. Синтезируется в печени. |
| B-48 | Хиломикроны, остатки хиломикронов | Основной белок хиломикронов. Синтезируется в кишечнике. |
| C1 | ЛОНП, ЛВП, хиломикроны | Активатор ЛХАТ. Обмениваемый между липопротеинами. |
| C2 | ЛОНП, ЛВП, хиломикроны | Активатор внепечёночной липопротеинлипазы. Обмениваемый между липопротеинами. |
| C3 | ЛОНП, ЛВП, хиломикроны | Может подавлять липопротеинлипазу и активировать ЛХАТ. Обмениваемый между липопротеинами. |
| C4 | ЛОНП, ЛВП | |
| D | ЛВП | Переносчик ряда веществ, в том числе ацилхолестеролов. Синтезируется в печени, в ЦНС. |
| E | ЛОНП, ЛВП, хиломикроны, остатки хиломикронов | Лиганд для рецепторов липопротеинов в печени и периферических тканях. Синтезируется в печени и мозге. |
| H | окисленные ЛНП | Регуляция прокоагулянтной активности |
| L1 | ЛВП | |
| L2 | ||
| L3 | ||
| L4 | ||
| L5 | ||
| L6 | ||
| M |
Присутствие аполипопротеинов в липопротеинах[править | править код]
| A1 | A2 | A4 | A5 | B-100 | B-48 | C1 | C2 | C3 | C4 | D | E | H | L1 | L2 | L3 | L4 | L5 | L6 | |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ЛВП | + | + | + | + | + | + | + | + | + | + | + | ||||||||
| ЛНП | + | + | |||||||||||||||||
| ЛПП | + | + | + | ||||||||||||||||
| ЛОНП | + | + | + | + | + | + | + | ||||||||||||
| Хиломикроны | + | + | + | + | + | + | + | + | + |
- ↑ Марри Р., Греннер Д., Мейес П., Родуэлл В., «Биохимия человека». М., «Мир», 1993, т. I, стр. 258
- ↑ 1 2 Марри Р., Греннер Д., Мейес П., Родуэлл В., «Биохимия человека». М., «Мир», 1993, т. I, стр. 259
- ↑ Pennacchio LA, Olivier M, Hubacek JA, et al (October 2001). «An apolipoprotein influencing triglycerides in humans and mice revealed by comparative sequencing». Science (New York, N.Y.) 294 (5540): 169–73. DOI:10.1126/science.1064852. PMID 1588264
что это такое, причины повышенных показателей
Жиры, аналогично остальным участникам обмена веществ, выполняют свою определенную функцию в организме, по этому их концентрация в крови должна поддерживаться на должном уровне. Но перед тем как попасть в общий кровоток, они связываются с белками-переносчиками. Иначе мелкие капли жира закупорят просветы сосудов, и обескровят соответствующие участки тканей. В роли транспортного белка выступает аполипопротеин. Существует несколько его разновидностей, причем каждая входит в состав конкретно своего жиробелкового комплекса.

Что такое аполипопротеин (апобелок)
Чтобы понять, что собой представляют аполипопротеины, необходимо кратко ознакомиться с липидным обменом.
- Жиры поступают в организм с пищей и продуцируются им самим.
- Поступившие в кишечник липиды расщепляются до малейших частиц, способных проникать через стенки кровеносных и лимфатических капилляров. Они связываются с аполипопротеином, образуя хиломикроны, и свободно перемещаются с лимфой или кровью.
- Синтез собственных жиров происходит в основном в печеночных клетках, а остальной небольшой их процент – во всех других. Синтезированные липиды также связываются с белками и выходят в общий кровоток.
- В состав липопротеидов обязательно входят триглицериды, холестерин, фосфолипиды и, конечно же, – аполипопротеины. В зависимости от фракции они содержат и небольшое количество других веществ (например, жирорастворимых витаминов).
- Сначала жиробелковые соединения состоят из крупного жирного компонента и мелкого протеинового. Но постепенно они «обрастают» аполипопротеинами, в результате чего их плотность увеличивается. Схематически процесс выглядит так: липопротеиды с очень низкой плотностью → с промежуточной плотностью → с низкой плотностью.
- Так появляются основные переносчики жиров в организме – ЛПНП, составляющие основную массу липопротеидов в плазме крови. Кроме основных функций, они еще и способны проникать во внутренний слой сосудистых стенок и откладываться в нем. Поэтому ЛПНП называют «плохим холестерином».
- В норме же низкоплотные липопротеиды фиксируются на специфических рецепторах клеток-потребителей, и под действием ферментов отщепляют свои составные части.
- Они используются в разных целях: фосфолипиды идут на восстановление поврежденных мембран, холестерин попадает внутрь цитоплазмы или встраивается в средний слой клеточной оболочки, а триглицериды обеспечивают эти процессы энергией.
- Все, что не употребилось клеткой, обратно связывается с белком. Во вновь образованных соединениях уже мало жирной составляющей и много белковой. Это липопротеиды высокой плотности, которые транспортируются в печень, где превращаются в желчные кислоты.
Читайте также: Что такое липопротеины? [таблица по видам и функциям]
Апобелки относятся к простым протеинам, состоящим только из аминокислот. В формуле аполипопротеинов нет соединений других групп, и остов их молекул короче, чем у сложных белков (отсюда и префикс «апо», в медицине означающий «укорочение»). Для удобства транспортные белки синтезируются рядом с местом «обитания» липидов – в печени и кишечнике. Печеночные клетки вырабатывают тот протеин, который необходим для транспорта синтезированных ими жиров, а эпителий тонкой кишки производит белок, связывающий поступившие извне липиды.

Изменение количества любых белков-переносчиков неизбежно приводит к нарушению жирового обмена. Дисбаланс возникает при:
- генетических поломках, при которых не вырабатывается или производится мало аполипопротеинов;
- гормональных нарушениях, вызванных патологией надпочечников, поджелудочной железы, яичников или семенников;
- погрешности в рационе, в том числе – злоупотреблении спиртными напитками;
- приеме некоторых лекарственных средств.
Каждый перечисленный фактор является абсолютным показанием к проведению биохимического анализа крови на липидный профиль, включающий и определение концентрации аполипопротеинов разных классов. Кроме того, липидограмма входит в комплекс обязательного обследования больных ожирением, гипертонией, аутоиммунными заболеваниями, сахарным диабетом, ишемической болезнью сердца и церебральным атеросклерозом, особенно после перенесенных инфаркта или инсульта. Также рекомендуется проведение анализа у женщин старше 55-летнего возраста и у мужчин старше 45-летнего.
Так какие аполипопротеины за что отвечают? Постоянны ли их референсные значения? И чем грозит изменение концентрации белков-транспортировщиков?
Аполипопротеин А-1
Существует несколько фракций аполипопротеина А, но для оценки состояния жирового обмена важны показатели именно А-1. Это белковый компонент высокоплотных липопротеидов и хиломикронов, состоящий из 243 аминокислот. Его химическая структура оригинальна: один конец белковой спирали, связанный с липидным компонентом, жирорастворимый, другой же – свободный – водорастворимый.
- Хиломиконы – продукт работы кишечника. Они образуются в его эпителии путем слияния мельчайших жировых капель, поступивших из пищи, с транспортными белками. Оформленные хиломикроны через лимфатическое русло поступают в легочную ткань, а затем через кровеносное – в печень, мышцы и лактирующие молочные железы. Апо А1 – не единственный белковый компонент хиломикронов: в крови он быстро отщепляется, оставляя жиробелковые частицы «на попечение» апо В-48 и апо Е. Поэтому большой роли в развитии атеросклеротического поражения сосудов этот белок-переносчик не играет.
- Освободившиеся аполипопротеины А-1 переносятся на липопротеиды высокой плотности. Но главным поставщиком апо А1 для ЛПВП остается печень. Высокоплотные липопротеины являются основными соединениями, выводящими холестерол из организма, в связи с чем их называют «хорошим холестерином». Для диагностики атерогенного риска как раз важен именно показатель аполипопротеина А-1, входящего в состав ЛПВП.
Нормы показателя
Нормальный уровень жиров, в том числе и холестерина, в плазме крови меняется в зависимости от возраста. Зависим он и от пола. Соответственно, меняется и содержание их переносчиков. Все референтные показатели сведены в одну таблицу, по которой врачи оценивают состояние жирового обмена исходя из возрастной и половой принадлежности. В зрелом возрасте аполипопротеин А1 у мужчин не должен выходить за пределы 1,04-2,02 грамма в литре крови, у женщин – за границы 1,08-2,25.

Расшифровка результатов
Если уровень апо А1 в анализе крови понижен, следует искать:
- печеночную патологию с недостаточностью;
- почечные заболевания с недостаточностью;
- сахарный диабет;
- заболевания, сопровождающиеся застоем желчи (гепатит, цирроз печени, желчнокаменная болезнь).
Недостаток транспорта ЛПВП в печень с последующей их утилизацией грозит повышением уровня холестерина, а значит, является атерогенным фактором.
Состояния, когда аполипопротеин А1 повышен, встречаются намного реже, и связаны они с наследственностью, алкоголизмом, а преходящая А1-гиперпротеинемия – с предшествующей интенсивной физической нагрузкой. Высокое содержание в крови апо А1 не сопровождается патологическими изменениями, поэтому не имеет клинического значения.
Аполипопротеин B
Является антиподом предыдущего в плане развития атеросклероза. Его основная форма – В-100 – переносит ЛПНП, а половинная изоформа – В-48 – транспортирует хиломикроны и содержится в продуктах их распада. В состав В-100 входит 4536 аминокислот. Это – самый крупный белок-переносчик липидов, который без связи с ними не существует. Синтезируется, как и сами низкоплотные липопротеины, в печени.
Именно апо В-100 фиксирует ЛПНП к рецепторам клеток, в том числе и эндотелия внутренней оболочки сосудов. А значит, благодаря ему в артериальных стенках откладывается субстрат будущей атеросклеротической бляшки. Значения апо В-48 благодаря связи с хиломикронами врачей не интересуют.
Нормы показателя
Аналогично другим апо-белкам, нормальный уровень В-100 колеблется. У взрослых мужчин он находится в интервале 0,66-1,33 граммов в литре крови, а у женщин – в пределах 0,6-1.17. Его концентрация в плазме даже более показательна, чем содержание холестерина. Кроме того, при известных цифрах апо В и апо А1 легко рассчитать дополнительный коэффициент атерогенности, поделив первое на второе. Соответственно, если аполипопротеин В повышен, а фракция А-1 понижена, риск развития атеросклероза резко возрастает.

Расшифровка результатов
Повышенный уровень фракции В-100 развивается при тех же состояниях, что и фракции А1. Следствием его гиперпротеинемии закономерно является атеросклеротическое изменение сосудистой стенки и/или сердечных клапанов. Снижение содержания В-фракции возникает при тяжелых инфекциях, снижении функции щитовидной железы, нарушении кишечного всасывания, генных поломках. Гипопротеинемия не вызывает развитие атеросклероза или приводит к регрессу уже существующего.
Аполипопротеин E
Входит в состав хиломикронов и ЛПОНП, включает 299 аминокислот, параллельно синтезируется в печени и веществе головного мозга. Взаимное проникновение невозможно: гематоэнцефалический барьер не пропускает отдельно синтезированные вещества туда и обратно. На обмен жиров концентрация аполипопротеинов Е особо не влияет. Основная их «заслуга» состоит в миелинизации холестерином оболочек нервных стволов: чем больше они им загружены, тем больше вероятность развития симптомов болезни Альцгеймера.
Читайте также: Холестерин (холестерол) — что это такое? Кратко о главном
Аполипопротеиды разных классов хороши только при нормальной их концентрации. Отклонение в ту или иную сторону кардинально влияет на жировой обмен и его последствия. Чтобы обезопасить себя от проявлений жиробелкового дисбаланса, стоит регулярно контролировать их содержание: до 45 – 55 лет без сердечнососудистой и гормональной патологии – раз в пятилетку, а при ее наличии и после указанного возрастного рубежа – 1 раз в год. Изменения, выявленные в начале обменного расстройства, намного легче поддаются коррекции, чем устоявшиеся.
Липопротеинлипаза — Википедия
Материал из Википедии — свободной энциклопедии
Липопротеинлипаза (ЛПЛ, КФ 3.1.1.34) — фермент, относящийся к классу липаз. ЛПЛ расщепляет триглицериды самых крупных по размеру и богатых липидами липопротеинов плазмы крови — хиломикронов и липопротеинов очень низкой плотности (ХМ и ЛПОНП)). ЛПЛ регулирует уровень липидов в крови, что определяет её важное значение в атеросклерозе.
ЛПЛ синтезируется в большинстве тканей организма кроме печени, где синтезируется специфическая печёночная липаза. Наиболее богаты липопротеинлипазой сердце, скелетные мышцы и жировая ткань.
Генетические нарушения липопротеинлипазы[править | править код]
Найдены три наиболее распространённых мутации ЛПЛ. Самая распространённая мутация встречается у 16-22 % населения. Эта точечная мутация (S447X) приводит к образованию стоп-кодона на месте серина-447 и таким образом синтезируется сокращённая копия фермента. Две другие мутации встречаются у примерно 3 % населения (D9N и N291S). Все эти мутации хотя и не блокируют каталитической активности ЛПЛ, но повышают риск атеросклероза при наличии других неблагоприятных факторов (например, слишком калорийное питание)[источник не указан 233 дня].
- Zechner R. The tissue-specific expression of lipoprotein lipase: implications for energy and lipoprotein metabolism (англ.) // Curr. Opin. Lipidol. : journal. — 1997. — Vol. 8, no. 2. — P. 77—88. — DOI:10.1097/00041433-199704000-00005. — PMID 9183545.
- Fisher R.M., Humphries S.E., Talmud P.J. Common variation in the lipoprotein lipase gene: effects on plasma lipids and risk of atherosclerosis (англ.) // Atherosclerosis : journal. — 1998. — Vol. 135, no. 2. — P. 145—159. — DOI:10.1016/S0021-9150(97)00199-8. — PMID 9430364.
- Beisiegel U. Lipoprotein metabolism (англ.) // Eur. Heart J. (англ.)русск. : journal. — 1998. — Vol. 19 Suppl A. — P. A20—3. — DOI:10.1093/eurheartj/19.Abstract_Supplement.1. — PMID 9519338.
- Pentikäinen M.O., Oksjoki R., Oörni K., Kovanen P.T. Lipoprotein lipase in the arterial wall: linking LDL to the arterial extracellular matrix and much more (англ.) // Arterioscler. Thromb. Vasc. Biol. (англ.)русск. : journal. — 2002. — Vol. 22, no. 2. — P. 211—217. — DOI:10.1161/hq0102.101551. — PMID 11834518.
- Lichtenstein L., Berbée J.F., van Dijk S.J., van Dijk K.W., Bensadoun A., Kema I.P., Voshol P.J., Müller M., Rensen P.C., Kersten S. Angptl4 upregulates cholesterol synthesis in liver via inhibition of LPL- and HL-dependent hepatic cholesterol uptake (англ.) // Arterioscler. Thromb. Vasc. Biol. (англ.)русск. : journal. — 2007. — November (vol. 27, no. 11). — P. 2420—2427. — DOI:10.1161/ATVBAHA.107.151894. — PMID 17761937.
- Lichtenstein L., Mattijssen F., de Wit N.J., Georgiadi A., Hooiveld G.J., van der Meer R., He Y., Qi L., Köster A., Tamsma J.T., Tan N.S., Müller M., Kersten S. Angptl4 protects against severe proinflammatory effects of saturated fat by inhibiting fatty acid uptake into mesenteric lymph node macrophages (англ.) // Cell Metab. (англ.)русск. : journal. — 2010. — December (vol. 12, no. 6). — P. 580—592. — DOI:10.1016/j.cmet.2010.11.002. — PMID 21109191.
Рецептор липопротеинов низкой плотности — Википедия
Материал из Википедии — свободной энциклопедии
| Рецептор липопротеинов низкой плотности | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
 PDB rendering based on 1ajj. | ||||||||||
| ||||||||||
| Идентификаторы | ||||||||||
| Символ | LDLR ; FH; FHC; LDLCQ2 | |||||||||
| Внешние ID | OMIM: 606945 MGI: 96765 HomoloGene: 55469 ChEMBL: 3311 GeneCards: LDLR Gene | |||||||||
| Профиль экспрессии РНК | ||||||||||
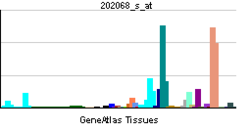 | ||||||||||
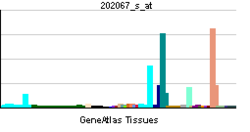 | ||||||||||
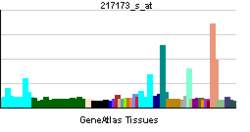 | ||||||||||
| Больше информации | ||||||||||
| Ортологи | ||||||||||
| Вид | Человек | Мышь | ||||||||
| Entrez | 3949 | 16835 | ||||||||
| Ensembl | ENSG00000130164 | ENSMUSG00000032193 | ||||||||
| UniProt | P01130 | P35951 | ||||||||
| RefSeq (мРНК) | NM_000527 | NM_001252658 | ||||||||
| RefSeq (белок) | NP_000518 | NP_001239587 | ||||||||
| Локус (UCSC) | Chr 19: 11.09 – 11.13 Mb | Chr 9: 21.72 – 21.75 Mb | ||||||||
| Поиск в PubMed | [1] | [2] | ||||||||
Рецептор липопротеинов низкой плотности (ЛПНП-рецептор, англ. low density lipoprotein receptor, LDL Receptor) — белок, опосредующий эндоцитоз липопротеинов низкой плотности, обогащённых холестерином. ЛПНП-рецептор представляет собой мембранный белок, специфически распознающий апоВ-100 и апоЕ. За открытие этого важнейшего рецептора липидного метаболизма Майкл Браун и Джозеф Голдштейн получили Нобелевскую премию по физиологии и медицине в 1985 году. Это стало результатом их работ по наследственной гиперхолестеринемии.
ЛПНП-рецептор синтезируется практически во всех ядерных клетках организма. Активация или ингибирование транскрипции белка регулируется уровнем холестерина в клетке. При недостатке холестерина клетка инициирует синтез ЛПНП-рецептора, а при избытке — наоборот, блокирует его. ЛПНП-рецептор синтезируется на рибосомах эндоплазматического ретикулума и модифицируется в аппарате Гольджи, после чего в составе везикул транспортируется к мембране клетки.
В клеточной мембране ЛПНП-рецептор локализован в клатриновых кавеолах (англ. clathrin-coated pits). Два основных лиганда этого рецептора — это апоВ-100 и апоЕ. При взаимодействии с лигандом рецептор связывает холестерин ЛПНП через адаптин, при этом кавеола замыкается в везикулу и уходит с поверхности клетки внутрь в процессе эндоцитоза. После этого рецептор либо деградирует в лизосомах, либо рециркулирует опять к мембране. Около 70 % ЛПНП поглощается за счёт рецепторного эндоцитоза клетками печени. Так как избыточные ЛПНП значительно повышают риск атеросклероза из-за неспецифического накопления в стенках сосудов, ЛПНП-рецептор является одним из важнейших регуляторных элементов обмена липидов крови.
ЛПНП-рецептор состоит из нескольких независимых доменов и участков. Он включает лиганд — связывающий домен, предшественник эпидермального фактора роста — подобный домен (англ. epidermal growth factor precursor homology domain, EGFP domain), домен с высоким уровнем гликозилирования, трансмембранный участок и С-концевой цитозольный участок. Первые три домена находятся с наружной стороны клетки, то есть являются внеклеточными.
- Лиганд — связывающий домен — находится на N-конце молекулы белка. Он состоит из 7 повторяющихся фрагментов (около 40 аминокислот каждый) с 50 % степенью гомологии. Фрагменты связаны друг с другом дисульфидными связями и координированы ионом кальция Ca2+. Они образуют октагональную структуру, которая связывает лиганд. Для связывания апоВ необходимы повторы 2—7, которые как бы «охватывают» ЛПНП. Для связывания апоЕ нужен только повтор 5, который считается самым древним повтором и предшественником остальных.
- EGFP — подобный домен — имеет 30 % гомологию с EGFP и состоит из 3 повторов: A, B и C. Первые два повтора тесно связаны друг с другом, а повтор С структурно отделён от них и участвует в процессе высвобождения лиганда. Когда лиганд-рецепторный комплекс попадает в эндосому и кислотность окружения опускается до pH 5.0, повтор С EGFP-подобного домена входит в контакт с лигандом и удаляет его из комплекса.
- Третий домен ЛПНП-рецептора высокогликозилирован и предположительно эволюционно появился для вынесения лиганд-связывающего домена за пределы внеклеточного матрикса. Однако удаление этого домена из молекулы не изменяет активность рецептора.
- Трансмембранный фрагмент состоит из гидрофобных аминокислот и пересекает клеточную мембрану.
- Наконец, С-концевой участок ЛПНП-рецептора локализован в цитоплазме клетки и содержит сигнальную последовательность, ответственную за интернализацию рецептора.
Ген ЛПНП-рецептора состоит из 18 экзонов. Первый экзон содержит сигнальную последовательность для транспорта белка от эндоплазматического ретикулума к плазматической мембране. Экзоны 2—6 кодируют лиганд-связывающий домен; экзоны 7—14 — EGFP-подобный домен; экзон 15 — гликозилируемый участок; экзоны 16—17 — трансмембранный участок; наконец, экзоны 17—18 кодируют цитозольный участок.
Рецептор липопротеинов очень низкой плотности — Википедия
Материал из Википедии — свободной энциклопедии
Рецептор липопротеинов очень низкой плотности (ЛПОНП-рецептор; англ. Very Low Density Lipoprotein Receptor, VLDLR) по структуре схож с рецептором липопротеинов низкой плотности, но не способен связывать липопротеины низкой плотности. Рецептор VLDLR играет роль в метаболизме липопротеинов очень низкой плотности. Экспрессия VLDLR высока в сердце, скелетных мышцах, жировой ткани; VLDLR совместно с рецептором LDLR связывает и захватывает остаточные липопротеины: липопротеины промежуточной плотности и хиломикронные ремнанты. [1]
В мозге VLDLR является одним из рецепторов рилина — белка внеклеточного матрикса, регулирующего миграцию и позиционирование нейробластов в развивающемся и взрослом мозге, влияющего на процессы синаптической пластичности.
Редкая аутосомно-рецессивно наследуемая мутация, обнаруживаемая у членов секты гуттеритов и затрагивающая в основном ген VLDLR, приводит к потере рецепторов этого типа и к нарушениям, аналогичным тем, что наблюдаются у мышей при отсутствии рецептора. Это заболевание, первоначально именовавшееся «синдромом нарушенного равновесия» (англ. Disequilibrium syndrome, DES), получило в 2005 году название «VLDLR-ассоциированная мозжечковая гипоплазия» (англ. VLDLR-associated cerebellar hypoplasia, VLDLRCH).[2][3] При заболевании наблюдается уменьшение мозжечка, упрощение рисунка извилин мозга, непрогрессирующая мозжечковая атаксия, задержка умственного развития.[4] Болезнь является одним из двух известных нарушений сигнального пути рилина у людей, наряду с синдромом Норман-Робертс.
- ↑ Takahashi S., Sakai J., Fujino T., Hattori H., Zenimaru Y., Suzuki J., Miyamori I., Yamamoto T.T. The very low-density lipoprotein (VLDL) receptor: characterization and functions as a peripheral lipoprotein receptor (англ.) // J. Atheroscler. Thromb. : journal. — 2004. — Vol. 11, no. 4. — P. 200—208. — PMID 15356379.
- ↑ Boycott K.M., Flavelle S., Bureau A., et al. Homozygous deletion of the very low density lipoprotein receptor gene causes autosomal recessive cerebellar hypoplasia with cerebral gyral simplification (англ.) // Am. J. Hum. Genet. (англ.)русск. : journal. — 2005. — Vol. 77, no. 3. — P. 477—483. — DOI:10.1086/444400. — PMID 16080122.free full text
- ↑ CEREBELLAR HYPOPLASIA, VLDLR-ASSOCIATED; VLDLRCH — данные из генетического каталога заболеваний OMIM.
- ↑ Moheb L.A., Tzschach A., Garshasbi M., Kahrizi K., Darvish H., Heshmati Y., Kordi A., Najmabadi H., Ropers H.H., Kuss A.W. Identification of a nonsense mutation in the very low-density lipoprotein receptor gene (VLDLR) in an Iranian family with dysequilibrium syndrome (англ.) // Eur J Hum Genet (англ.)русск. : journal. — 2007. — DOI:10.1038/sj.ejhg.5201967. — PMID 18043714.
Липопротеины — Википедия. Что такое Липопротеины
 Липопротеины. Структура
Липопротеины. СтруктураЛипопротеи́ны (липопротеиды) — класс сложных белков, простетическая группа которых представлена каким-либо липидом. Так, в составе липопротеинов могут быть свободные жирные кислоты, нейтральные жиры, фосфолипиды, холестериды.
Липопротеины представляют собой комплексы, состоящие из белков (аполипопротеинов; сокращенно — апо-ЛП) и липидов, связь между которыми осуществляется посредством гидрофобных и электростатических взаимодействий.
Липопротеины подразделяют на свободные, или растворимые в воде (липопротеины плазмы крови, молока и др.), и нерастворимые, т. е. структурные (липопротеины мембран клетки, миелиновой оболочки нервных волокон, хлоропластов растений).
Среди свободных липопротеинов (они занимают ключевое положение в транспорте и метаболизме липидов) наиболее изучены липопротеины плазмы крови, которые классифицируют по их плотности. Чем выше содержание в них липидов, тем ниже плотность липопротеинов. Различают липопротеины очень низкой плотности (ЛОНП), низкой плотности (ЛНП), высокой плотности (ЛВП) и хиломикроны. Каждая группа липопротеинов очень неоднородна по размерам частиц (наиболее крупные — хиломикроны) и содержанию в ней апо-липопротеинов. Все группы липопротеинов плазмы содержат полярные и неполярные липиды в разных соотношениях.
Виды липопротеинов
| Вид | Размеры | Функция |
|---|---|---|
| Липопротеины высокой плотности (ЛВП) | 8-11 нм | Транспорт холестерина от периферийных тканей к печени |
| Липопротеины низкой плотности (ЛНП) | 18-26 нм | Транспорт холестерина, триацилглицеридов и фосфолипидов от печени к периферийным тканям |
| Липопротеины промежуточной (средней) плотности ЛПП (ЛСП) | 25-35 нм | Транспорт холестерина, триацилглицеридов и фосфолипидов от печени к периферийным тканям |
| Липопротеины очень низкой плотности (ЛОНП) | 30-80 нм | Транспорт холестерина, триацилглицеридов и фосфолипидов от печени к периферийным тканям |
| Хиломикроны | 75-1200 нм | Транспорт холестерина и жирных кислот, поступающих с пищей, из кишечника в периферические ткани и печень |
Нековалентная связь в липопротеинах между белками и липидами имеет важное биологическое значение. Она обусловливает возможность свободного обмена липидов и модуляцию свойств липопротеинов в организме.
Липопротеины являются:
Метаболизм липопротеинов
 Метаболизм липопротеинов
Метаболизм липопротеиновХиломикроны образуются в лимфатической системе ворсинок кишечника. Они переносят до половины всех триацилглицеролов и холестерина лимфы. Новосинтезированные хиломикроны содержат интегральный белок В-48. Апопротеин В встраивается в липопротеины в гЭПР, где синтезируются триацилглицеролы. В аппарате Гольджи к белкам добавляются углеводы. Они высвобождаются из клеток кишечника обратным пиноцитозом. После этого хиломикроны поступают в лимфатические сосуды ворсинок и уносятся лимфой. Попадая в кровоток, они получают апопротеины С и Е от ЛВП. На стенках капилляров находится липопротеинлипаза (ЛПЛ) (прикрепляется к ним протеогликановыми цепями гепарансульфата). В печени также есть своя липаза, но она менее эффективно атакует хиломикроны. Апопротеин С2 активирует липопротеинлипазу, которая расщепляет триглицериды хиломикрона до ди- и моноглицеридов, а затем — до свободной жирной кислоты и глицерола. Жирные кислоты транспортируются в мышечные и жировые ткани или связываются с альбумином в крови. По мере липолиза хиломикроны теряют большинство своих триацилглицеролов, относительное содержание холестерина и его эфиров увеличивается. Диаметр остатка хиломикрона уменьшается. Апопротеин С2 возвращается на ЛВП, апопротеин Е сохраняется. Остатки хиломикронов поглощаются печенью. Поглощение осуществляется через рецепторный эндоцитоз, с помощью рецепторов апопротеина Е. В печени эфиры холестерина и триацилглицеролы окончательно гидролизуются.
ЛОНП переносят триацилглицеролы, а также фосфолипиды, холестерин и его эфиры из печени в другие ткани. Метаболизм ЛОНП похож на метаболизм хиломикронов. Интегральным белком их является другой апопротеин В, В-100. ЛОНП высвобождаются из клеток печени обратным пиноцитозом, после чего через слой эпителиальных клеток поступают в капилляры печени. В крови на них переносятся апопротеины С2 и Е с ЛВП. Триацилглицеролы ЛОНП, как в случае с хиломикронами, расщепляются при активации ЛПЛ с помощью апопротеина С2, свободные жирные кислоты поступают в ткани. По мере расщепления триацилглицеролов диаметр ЛОНП уменьшается, и они превращаются в ЛПП. Эфир-холестерин-переносящий белок (апопротеин D в составе ЛВП) переносит на ЛОНП эфиры холестерина от ЛВП в обмен на фосфолипиды и триглицериды.
Половина ЛПП поглощается печенью с помощью рецепторного эндоцитоза через рецепторы апопротеина Е и B-100. Триацилглицериды ЛПП гидролизуются печёночной липазой. Апопротеины С2 и Е возвращаются на ЛВП. частица превращается в ЛНП. Относительное содержание холестерина в ЛНП значительно увеличивается, диаметр частицы сокращается. (Они также переносят триглицериды, каротиноиды, витамин Е и др.) ЛНП поглощаются клетками печени (70%) и внепечёночных тканей с помощью рецепторного эндоцитоза. Однако лигандом теперь, в основном, служит белок В-100. Рецептор называется «рецептором ЛНП».
ЛВП обеспечивают обратный транспорт холестерина из внепечёночных тканей к печени. ЛВП синтезируются в печени. В новообразованных ЛВП содержатся апопротеины А1 и А2. Апопротеин А1 синтезируется также в кишечнике, где входит в состав хиломикронов, но при липолизе в крови быстро переносятся на ЛВП. Апопротеин С синтезируется в печени, выделяется в кровоток и уже в кровотоке переносится на ЛВП. Новообразованный ЛВП похож на диск: фосфолипидный бислой, включающий свободный холестерин и апопротеин. Апопротеин А1 — активатор фермента лецитинхолестеринацилтрансферазы (ЛХАТ). Этот фермент связан с поверхностью ЛВП в плазме крови. ЛХАТ катализирует реакцию между фосфолипидом ЛВП и свободным холестерином частицы. При этом образуются эфиры холестерина и лизолецитин. Неполярные эфиры холестерина перемещаются внутрь частицы, освобождая место на поверхности для захвата нового холестерина, лизолецитин — на альбумин крови. Неполярное ядро раздвигает бислой, ЛВП приобретает сферическую форму. Этерифицированный холестерин переносится с ЛВП на ЛОНП, ЛНП и хиломикроны специальным белком ЛВП — переносчиком эфиров холестерола (апопротеин D), в обмен на фосфолипиды и триглицериды. ЛВП поглощается клетками печени с помощью рецепторного эндоцитоза через рецептор апопротеина Е.
Специфичности рецепторов апопротеинов Е и В-100 частично пересекаются. Они находятся на поверхности мембран клеток в клатриновой кавеоле. При соединении с лигандами кавеола замыкается в везикулу и липопротеин эндоцитируется. В лизосомах эфиры холестерина гидролизуются и холестерин поступает в клетку.
Литература
- Кольман Я., Рём К.-Г., «Наглядная биохимия», пер.с нем., М., «Мир», 2009.
- Марри Р., Греннер Д., Мейес П., Родуэлл В. «Биохимия человека», в 2 т. М., «Мир», 2003.
