Высокочувствительный СРБ как прогностический маркер долгосрочного результата при ювенильном идиопатическом артрите
Цели:
Исследование было проведено для того, чтобы оценить, является ли повышение уровня C- реактивного белка (СРБ), включая его повышение в пределах нормального диапазона значений, предиктором неблагоприятного долгосрочного прогноза течения заболевания при ювенильном идиопатическом артрите (ЮИА).
Методы:
Пациенты с недавно диагностированным ЮИА были проспективно включены в исследование с 1997 по 2000 год. Критерии включения заключались в наличии образцов исходной сыворотки крови в течение 12 месяцев после начала заболевания и 8-летних данных клинической оценки течения заболевания. Пациенты с системным дебютом ЮРА не были включены. СРБ измеряли высокочувствительным ELISA (предел обнаружения 0,2 мг /л).
Результаты:
Было включено сто тридцать участников со средним сроком наблюдения 97 месяцев (диапазон 95- 100). При последующем наблюдении 38% пациентов находились в состоянии ремиссии без приема лекарственных средств.
Выводы:
Результаты этого исследования показывают, что исходные концентрации СРБ выше 10 мг/л предсказывают плохой результат при 8-летнем наблюдении. Мы не смогли продемонстрировать прогностическое значение вариаций СРБ в пределах нормального диапазона значений.
https://www.ncbi.nlm.nih.gov/pubmed/28283733
Повышенные уровни С-реактивного белка у пациентов с COVID-19
Уважаемые коллеги!
Несмотря на то, что С-реактивный белок (СРБ) является ранним маркером воспаления, возникающего при инфекции, и его уровни обычно значительно не увеличивается при вирусной респираторной инфекции, у тяжело больных пациентов с COVID-19 наблюдалось значительное увеличение значений СРБ. Это согласуется с наблюдениями, сделанными во время ОРВИ эпидемии в 2003 году у пациентов с птичьим гриппом h2N1 и H7N9 [1]. Одной из возможных причин является перепроизводство воспалительных цитокинов, которые участвуют в защите возбудителя. Цитокины могут быть причиной более серьезных симптомов и повреждения альвеолы, и тем самым стимулировать выработку СРБ. [2-4] По этой причине исследование уровня СРБ полезно в раннем обследовании пациентов с коронавирусом.
Это согласуется с наблюдениями, сделанными во время ОРВИ эпидемии в 2003 году у пациентов с птичьим гриппом h2N1 и H7N9 [1]. Одной из возможных причин является перепроизводство воспалительных цитокинов, которые участвуют в защите возбудителя. Цитокины могут быть причиной более серьезных симптомов и повреждения альвеолы, и тем самым стимулировать выработку СРБ. [2-4] По этой причине исследование уровня СРБ полезно в раннем обследовании пациентов с коронавирусом.
Исследования пациентов с COVID-19 показали, что уровни СРБ напрямую коррелируют с тяжестью и прогрессированием заболевания. Недавно опубликованное исследование [5] показало, что низкие уровни СРБ часто встречаются как у пациентов, которым не требуется кислород (среднее значение 11 мг/ л, межквартильный диапазон 1-20 мг/л) так и у пациентов, у которых развилась гипоксемия (среднее значение 66 мг/л, интерквартильный диапазон 48-98 мг/л).
Другое исследование [6] было сосредоточено на изучении предикторов (to predict – предсказывать) летального исхода в случаях COVID-19. В этом исследовании было показано, что повышенные воспалительные маркеры в крови являются хорошими предикторами при COVID-19. Сравнение уровней СРБ с риском смертности показало, что у выживших пациентов средний уровень СРБ составлял ~ 40 мг/л, в то время как у умерших — в среднем 125 мг/л.
В этом исследовании было показано, что повышенные воспалительные маркеры в крови являются хорошими предикторами при COVID-19. Сравнение уровней СРБ с риском смертности показало, что у выживших пациентов средний уровень СРБ составлял ~ 40 мг/л, в то время как у умерших — в среднем 125 мг/л.
Информация для заказа:
|
Каталожный номер |
Используемый анализатор |
|
С-реактивный белок (CRP FS) производства DiaSys Diagnostic System GmbH |
|
|
1 7002 99 10 935 |
Открытые системы |
|
1 7002 99 10 962 |
ВМ6010/С |
|
D 1 7002 99 10 935 |
Серия DIRUI CS |
|
|
Серия FURUNO СА |
|
1 7002 99 10 920 |
Respons 910 |
|
СРБ-ИММУНОТУРБИДИМЕТРИЧЕСКИЙ ДДС производства АО «ДИАКОН-ДС» |
|
|
20 602 |
Clima MC-15 |
|
С-реактивный белок универсальный / высокочувствительный (CRP U-hs) производства DiaSys Diagnostic System GmbH |
|
|
1 7045 99 10 930 |
Открытые системы |
|
D 1 7045 99 10 930 |
Серия DIRUI CS |
|
F 1 7045 99 10 930 |
Серия FURUNO СА |
|
1 7045 99 10 920 |
Respons 910 |
Литература:
[1] N. Chen u. a., „Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptive study“, Lancet Lond. Engl., Bd. 395, Nr. 10223, S. 507–513, 15 2020, doi: 10.1016/S0140-6736(20)30211-7.
Chen u. a., „Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptive study“, Lancet Lond. Engl., Bd. 395, Nr. 10223, S. 507–513, 15 2020, doi: 10.1016/S0140-6736(20)30211-7.
[2] D. Vasileva und A. Badawi, „C-reactive protein as a biomarker of severe h2N1 influenza“, Inflamm. Res. Off. J. Eur. Histamine Res. Soc. Al, Bd. 68, Nr. 1, S. 39–46, Jan. 2019, doi: 10.1007/s00011-018-1188-x.
[3] W. Wu u. a., „A new perspective on C-reactive protein in H7N9 infections“, Int. J. Infect. Dis. IJID Off. Publ. Int. Soc. Infect. Dis., Bd. 44, S. 31–36, März 2016, doi: 10.1016/j.ijid.2016.01.009.
[4] K.-J. Huang u. a., „An interferon-gamma-related cytokine storm in SARS patients“, J. Med. Virol., Bd. 75, Nr. 2, S. 185–194, Feb. 2005, doi: 10.1002/jmv.20255.
[5] B. E. Young u. a., „Epidemiologic Features and Clinical Course of Patients Infected With SARS-CoV-2 in Singapore“, JAMA, März 2020, doi: 10. 1001/jama.2020.3204.
1001/jama.2020.3204.
[6] Q. Ruan, K. Yang, W. Wang, L. Jiang, und J. Song, „Clinical predictors of mortality due to COVID-19 based on an analysis of data of 150 patients from Wuhan, China“, Intensive Care Med., März 2020, doi: 10.1007/s00134-020-05991-x.
Клиническое значение высокочувствительного С-реактивного белка при системной склеродермии | Невская
1. Алекперов Р.Т., Баранов А.А., Абаитова Н.Е. Клинические ассоциации С-реактивного белка при системной склеродермии. Тер.архив, 2006, 78 (6), 30-35.
2. Гусева Н.Г. Системная склеродермия и псевдосклеродермические синдромы. М., 1993, 13.
3. Невская Т.А., Гусева Н.Г., Раденска-Лоповок С.Г., Сперанский А.И. Т-клеточные иммунные нарушения при ранней системной склеродермии. Ревматология, 2006, 4, 17-24.
Ревматология, 2006, 4, 17-24.
4. Akram M. R., Handler C. E., Williams M. et al. Angiographically proven coronary artery disease in scleroderma. Rheumatology, 2004, 30, 2435-2501.
5. Barnes E.V., Narain S., Naranjo A. et al. High sens itivity C-reactive prote in in system ic lupus erythematosus: relation to disease activity, clinical present ation and implications for cardiovascular risk. Lupus, 2005,14(8), 576-582.
6. Bell S.A., Faust H., Schm id A., Meurer M. Autoantibodies to C-reactive protein (CRP) and other acute-phase proteins in systemic autoimmune diseases. Clin.Exp.Immunol., 1998, 113(3), 327-332.
7. Bisoendial J., Kastelein M.P., Levels JHM. et al. Activation of inflammation and coagulation after infusion of C-reactive protein in humans.
8. Black S., Kushner I., Samols D. C-reactive protein. J.Biol.Chem., 2004, 47, 487-490.
9. Blann A.D., Illingworth K., Jayson M.I. Mechanisms of end othe lial cell damage in system ic sclerosis and Raynaud’s phenomenon. J.Rheumatol., 1993, 20(8), 1325-1330.
10. Borba E.F., Borges C.T., Bonfa E. Lipoprote in profile in limited systemic sclerosis. Rheumatol. Int., 2005, 25(5), 379-383.
11. Bradley J., McAliste r O., Elborn S. Pulmonary function, inflamm ation, exercise capacity and quality of life in cystic fibrosis. Eur.Respir. J., 2001, 17(4), 712-715.
12. Cutolo M. , Sulli A., Pizzorni C., Accardo S. Nailfold vide ocapillaroscopy assessment of microvascular damage in systemic sclerosis. J. Rheumatol., 2000, 27, 155-160.
, Sulli A., Pizzorni C., Accardo S. Nailfold vide ocapillaroscopy assessment of microvascular damage in systemic sclerosis. J. Rheumatol., 2000, 27, 155-160.
13. Danenberg H.D., Szalai A.S., Swaminathan R.V. et al. Increased th rombosis afte r arte rial injury in human C-reactive prote in-transgen ic mice. Circulation, 2003, 108, 512-520.
14. Forreste r J.S. Comm on ancest ors: chronic progressive diseases have the same pathogenesis. Clin. Cardiol., 2004, 27(4), 186-190.
15. Fujita J., Yamadori I., Suemitsu I. et al. Clinical features of non-specific inte rst itial pne umonia. Respir. Med., 1999, 93(2), 113-118.
16. Hatt ori Y., Mats umura M., Kasai K. Vascular smooth muscle cell activation by C-reactive protein. Cardivasc.res., 2003, 58, 186-195.
Cardivasc.res., 2003, 58, 186-195.
17. Jialal I., Devaraj S., Ven ugopal S.K. C-reactive prote in: risk or med iator in athe rogenes is? Hypertension, 2004, 44, 6-11.
18. Levy H., Kalish L.A., Hunt ingt on I. et al. Inflamm atory markers of lung dise ase in adult patients with cyst ic fibrosis. Ped iatr. Pulmonol., 2007, 42(3), 256-262.
19. Li J.J., Fang C.H. C-reactive protein isn’t only an inflammatory marker but also a direct cause of cardiovascular disease. Med.Hypothesis, 2004, 62, 499-506.
20. Lippi G., Caramaschi P., Montagnana M. et al. Lipoprotein-а and the lipid profile in patients with systemic sclerosis. Clin. Chim. Acta, 2006, 364(1- 2), 345-348.
21. Medsger T.A., Silman A.J., Steen V.D. et al. A disease severity scale for systemic sclerosis: development and testing. J.Rheumatol., 1999, 26, 2159-2167.
Medsger T.A., Silman A.J., Steen V.D. et al. A disease severity scale for systemic sclerosis: development and testing. J.Rheumatol., 1999, 26, 2159-2167.
22. Merkel P., Herlyn K., Martin R. et al. Measuring Disease Activity and Functional Status in Patients With Sclerode rma and Raynaud’s Phen omen on. Arthr.Rheum., 2002, 46, 2410-2420.
23. Nagata N., Nagatomo H., Yoshii C. et al. Features of idiopathic pulmonary fibrosis with organizing pneumonia. Respirat., 1997, 64(5), 331-335.
24. Nakada Y., Simajiri M., Shimabukuro M. et al. An elderly case of idiopathic retroperitoneal fibrosis. Nippon Ronen Igakkai Zasshi, 1991, 28(6), 811- 816.
25. Ohhata I., Ochi T., Hanamoto S. et al. Prognosis of idiopathic interstitial pneumonia. Nihon Kyobu Shikkan Gakkai Zasshi., 1994, 32(11), 1049-1055.
Prognosis of idiopathic interstitial pneumonia. Nihon Kyobu Shikkan Gakkai Zasshi., 1994, 32(11), 1049-1055.
26. Pandolfi A. C-reactive protein: a potential new molecular link between inflammation, thrombosis and vascular cell proliferation. Cardiovasc.Res ., 2005, 68, 3-4.
27. Sari I., Okan T., Akar S. et al. Atherosclerotic lesion of the vessels in systemic lupus erythematosus in males: relations with concentration of C-reactive protein. Te r. Arkh., 2005, 77(6), 61-65.
28. Smith E.A., Kahaleh M.B., LeRoy E.C. The acute phase response in scleroderma. Differing responses to intravenous PGE1. Clin.Exp.Rheumatol., 1986, 4(4), 341-345.
29. Stafford L., Englert H., Gover J. and Bertouch J. Distribution of macrovascular disease in scleroderma. Ann.Rheum.Dis., 1998, 57, 476-479
Distribution of macrovascular disease in scleroderma. Ann.Rheum.Dis., 1998, 57, 476-479
30. Steen V.D., Medsger T.A. Jr. The value of the Health Assessment Quest ionn aire and special patient — generated scales to demonstrate change in systemic sclerosis patients over time. Arthr.Rheum., 1997, 40, 1984–1991.
31. Stuart R.A., Littlewood A.J., Maddison P.J., Hall N.D. Elevated serum interleukin-6 levels associated with active disease in systemic connective tissue disorders. Clin.Exp.Rheumatol., 1995,13(1), 17-22.
32. Svenungsson E., Jensen-Urstad K., Heimbьrger M. et al. Risk Factors for Cardiovascular Disease in Systemic Lupus Erythematosus. Circulation, 2001, 104, 1887.
33. Tada Y., Onoue H., Koarada S. et al. A case of idiopath ic fibrosing med iast initis presented with bilateral pleural effusion. Nihon Rinsho Meneki Gakkai Kaishi, 2002, 25(2), 177-180.
Tada Y., Onoue H., Koarada S. et al. A case of idiopath ic fibrosing med iast initis presented with bilateral pleural effusion. Nihon Rinsho Meneki Gakkai Kaishi, 2002, 25(2), 177-180.
34. Trojanowska M., Le Roy E.C., Kekes B. and Krieg T. Pathogenesis of fibrosis: type I collagen and the skin. J.Mol.Med., 1998, 76, 266-274.
35. Valentini G., Della Rossa A., Bombardieri S.at al. European multicentre study of define disease activity variables and development of preliminary activity indexes. Ann.Rheum.Dis., 2001, 60, 592- 598.
36. Verma S., Kaliszewski M.A., Li S. et al. C-reactive prote in atten uates end othe lial progen itor cell survival, different iation, and function. Furthe r evidence of a mechanistic link between C-reactive prote in and cardiovascular dise ase . Circulation, 2004, 109, 2058-2067.
Circulation, 2004, 109, 2058-2067.
Анализ на С-реактивный белок высокочувствительный (hs СРБ)
Диагностическое направление
Риск развития сердечно-сосудистых заболеваний
Общая характеристика
Относится к белкам острой фазы воспаления. В условиях воспаления синтез СРБ в печени многократно увеличивается, и подъем его концентрации в плазме/сыворотке крови обнаруживается спустя 6 и более часов после начала воспалительного заболевания либо повреждения ткани. Беременность не влияет на уровень СРБ (можно использовать для дифференциальной диагностики наличия воспаления при увеличении СОЭ). Высокочувствительные методы определения СРБ позволяют определять его изменение не только в условиях острого, но и хронического, низкой степени выраженности эндогенного воспаления. Повышение hsСРБ в интервале концентраций
Показания для назначения
1. Диагностика и оценка риска развития атеросклероза, ССЗ.2. Мониторинг и контроль эффективности лечения хронического воспаления.3. Определение риска сердечно-сосудистых осложнений у пациентов с атеросклерозом, сахарным диабетом.
Диагностика и оценка риска развития атеросклероза, ССЗ.2. Мониторинг и контроль эффективности лечения хронического воспаления.3. Определение риска сердечно-сосудистых осложнений у пациентов с атеросклерозом, сахарным диабетом.
Маркер
Маркер вялотекущего сосудистого воспаления при заболеваниях артерий (атеросклерозе).
Клиническая значимость
1. Оценка риска развития инфаркта миокарда у больных с острым коронарным синдромом.2. Оценка риска развития сердечно-сосудистых заболеваний или ишемических событий у лиц, у которых в настоящее время отсутствуют клинические проявления болезни.
Состав показателей:
СРБ высокочувствительный
Метод: ИммунотурбидиметрияДиапазон измерений: 0,16-200,0
Единица измерения: Миллиграмм на литр
Референтные значения:
Возраст
Комментарии
Выполнение возможно на биоматериалах:
Биологический материал
Условия доставки
Контейнер
Объем
Сыворотка
Условия доставки:
24 Час. при температуре от 2 до 25 градусов Цельсия
при температуре от 2 до 25 градусов Цельсия
Контейнер:
Вакутейнер с разделительным гелем
Объем:
8.5 Миллилитров
Капиллярная кровь
Условия доставки:
24 Час. при температуре от 2 до 25 градусов Цельсия
при температуре от 2 до 25 градусов Цельсия
Контейнер:
Микровет с активатором свертывания крови
Объем:
500 Микролитр
Правила подготовки пациента
Стандартные условия: Утром до 11-00, натощак, через 8-12 часов периода голодания. Возможно: в течение рабочего дня отделений МЛ «ДИЛА» (должна быть исключена жирная пища).
Возможно: в течение рабочего дня отделений МЛ «ДИЛА» (должна быть исключена жирная пища).
Вы можете добавить данное исследование в корзину на этой странице
Интерференция:
- Нейтропения, прием эстрогенов, оральных контрацептивов.
Интерпретация:
- Атеросклероз, ССЗ, чувствителен и появляется менее чем за 2 часа при: инфаркте миокарда, травме, хирургических вмешательствах и инфекции.
С-реактивный белок (СРБ), количественный, высокочувствительный
Анализ крови
Для получения достоверных результатов исследования необходимо предоставить информацию работнику лаборатории о систематическом приёме лекарственных средств, сроке беременности, дне МОЦ, диагнозе.
Основные правила:
- Кровь следует сдавать натощак, рекомендуется соблюдение 8-12-часового периода голодания, возможно употребление небольшого количества воды.
- Важно отказаться от приема алкоголя и курения за 12 часов до cдачи анализов;
- Свести к минимуму физическую активность.
- Исключить прием медицинских препаратов; в случае невозможности отмены лекарств необходимо уведомить об этом представителя лаборатории.
- Все анализы крови сдают до проведения рентгенографии, КТ, УЗИ и физиотерапевтических процедур.
- Детей младше 5-ти лет перед сдачей крови желательно поить теплой кипяченой водой (до 200мл).
- Для грудных детей перед сдачей крови необходимо выдержать максимально возможную паузу между кормлениями.
Исследование системы гемостаза (коагулограмма)
- Повторную сдачу крови на исследование ПТИ желательно проводить в одно и тоже время.
- Пациенты, которые принимают антитромботические препараты, не должны нарушать график приёма в день сдачи, если нет особых рекомендаций врача.

- Кровь сдается натощак, после 8-12 часов голодания. За двое суток до сдачи крови следует придерживаться диеты, исключить жирную, острую и солёную пищу.
Липидный комплекс
- Повторную сдачу крови на исследование ПТИ желательно проводить в одно и тоже время.
- Пациенты, которые принимают антитромботические препараты, не должны нарушать график приёма в день сдачи, если нет особых рекомендаций врача.

- Кровь сдается натощак, после 8-12 часов голодания. За двое суток до сдачи крови следует придерживаться диеты, исключить жирную, острую и солёную пищу.
Липидный комплекс
Для сдачи крови на липидный обмен (холестерин, липопротеины, триглицериды) за 2 суток стоит начать соблюдать диету, исключить жирную, жареную, острую и солёную пищу, не злоупотреблять углеводами и отказаться от алкоголя.
Пролактин
- Кровь следует сдавать утром, в течение трех часов после пробуждения.
- Важен половой покой за сутки до сдачи, отсутствие физических нагрузок и нервного напряжения.
- Перед сдачей крови исключить перегрев и переохлаждение тела (не посещать баню, сауну, массажи).
- Перед исследованием исключить пальпацию молочных желез.
Половые гормоны
Женские половые гормоны сдаются в определенные дни менструального цикла (ЛГ, ФСГ — на 3-5 день цикла, эстрадиол — на 5-7 или на 21-23 день цикла; прогестерон — на 21-23 день цикла, тестостерон и пролактин — в любой день), если врач не назначил другие дни.
При сдаче тестов репродуктивной панели женщинам следует обязательно указывать день менструального цикла или срок беременности с целью учета цикличности гормональных колебаний.
Пренатальный скрининг 1 и 2 триместра
Необходимо строго соблюдать рекомендации врача относительно дат и времени прохождения ультразвукового исследования (УЗИ) и забора крови.
Пренатальный скрининг 1-го триместра проводится на 8-13 неделе беременности.
Пренатальный скрининг 2-го триместра – на 14-19 неделе беременности.
PRISCA I триместра – 10-13 неделя беременности.
PRISCA IІ триместра – 14-22 неделя беременности.
Тестостерон
- Важно согласовать день сдачи крови на тестостерон со своим лечащим врачом.
- Следует воздержаться от сдачи анализа в течение суток после УЗИ, флюорографии или рентгена, а также физиотерапевтических процедур и ректального обследования.
- При приеме гормональных препаратов обязательно сообщить об этом представителю лаборатории.

ПСА (простатический специфический антиген)
- В течение 2 суток перед сдачей крови необходимо воздержаться от эякуляции.
- После любых урологических манипуляций, ректального обследования, массажа простаты, цисто- и колоноскопии выдержать минимальный трехдневный срок. Оптимальным является посещение лаборатории через 6-7 дней. После биопсии простаты сдачу анализа стоит отложить на месяц.
- В течение 3 дней до забора биоматериала рекомендуется воздержаться от походов в сауну и занятий спортом (особенно велосипедным).

- В течение 2 суток перед сдачей крови необходимо воздержаться от эякуляции.
- После любых урологических манипуляций, ректального обследования, массажа простаты, цисто- и колоноскопии выдержать минимальный трехдневный срок. Оптимальным является посещение лаборатории через 6-7 дней. После биопсии простаты сдачу анализа стоит отложить на месяц.
- В течение 3 дней до забора биоматериала рекомендуется воздержаться от походов в сауну и занятий спортом (особенно велосипедным).
Анализы в KDL. С-реактивный белок ультрачувствительный
С-реактивный белок (СРБ) – один из белков острой фазы, содержание которого в крови повышается при воспалении и инфекционных заболеваниях. Существует два типа тестов, которые измеряют уровень СРБ: стандартный и ультрачувствительный. Стандартный анализ измеряет белок в диапазоне до 1000 мг/л и используется в диагностике инфекционных и острых воспалительных заболеваний; ультрачувствительный позволяет выявлять небольшое повышение СРБ – от 0,5 до 10 мг/л, которое обычно наблюдается при вялотекущих воспалительных процессах в стенках сосудов, связанных с атеросклерозом и сердечно-сосудистыми заболеваниями. Эти процессы могут длиться годами, незаметно, ничем себя не проявляя, их помогает выявить ультрачувствительный анализ на СРБ, что позволяет использовать его для оценки риска развития заболеваний сердца.
Эти процессы могут длиться годами, незаметно, ничем себя не проявляя, их помогает выявить ультрачувствительный анализ на СРБ, что позволяет использовать его для оценки риска развития заболеваний сердца.
Согласно научным исследованиям, даже при нормальном холестерине умеренно повышенный уровень С-реактивного белка в районе верхних границ нормы в течение длительного времени напрямую связан с развитием атеросклероза и иной патологии сосудов. При врожденных пороках сердца у пациентов с умеренно повышенным СРБ также увеличен риск развития инфаркта миокарда, инсульта, внезапной сердечной смерти и заболеваний периферических артерий. Своевременно сделанный ультрачувствительный тест на С-реактивный белок позволяет спрогнозировать риск развития патологии сердечно-сосудистой системы и вовремя принять меры для его снижения.
В каких случаях обычно назначают исследование?
- Для определения рисков и прогноза развития сердечно-сосудистых заболеваний;
- При комплексном обследовании пациентов старше 50 лет;
- Для прогноза развития осложнений у пациентов с диагностированным атеросклерозом, ишемической болезнью сердца, стенокардией и гипертонической болезнью;
- Для наблюдения за эффективностью лечения после перенесенных сердечно-сосудистых заболеваний, в том числе после операций на сердце.

Что именно определяется в процессе анализа?
Происходит измерение концентрации С-реактивного белка в низком диапазоне в образце сыворотки крови пациента методом иммунотурбидиметрии.
Что означают результаты теста?
Риски развития сердечно-сосудистых заболеваний определяются в зависимости от концентрации СРБ. Если она ниже 1 мг/л – риск минимален, от 1 до 3 мг/л – риск считается умеренным; при уровне от 3 до 10 мг/л можно говорить о высоком риске развития сердечной патологии. Если показатель превышает 10 мг/л, то речь идет об остром воспалительном или инфекционном процессе.
Следует помнить о том, что СРБ может повышаться при беременности, физических нагрузках, приеме оральных контрацептивов и гормонов. Статины и нестероидные противовоспалительные препараты наоборот снижают уровень этого маркера.
Ультрачувствительный тест на СРБ может быть неэффективен для людей, страдающих хроническими воспалительными заболеваниями, такими как ревматоидный артрит, поскольку у таких пациентов уровень С-реактивного белка постоянно повышен.
Сроки выполнения теста.
Обычно результат анализа можно получить через 1-2 дня после взятия крови.
Как подготовиться к анализу?
Следует придерживаться общих правил подготовки к взятию крови из вены. С подробной информацией можно ознакомиться в соответствующем разделе статьи.
С-реактивный белок ультрачувствительный
С-реактивный белок (СРБ) – сложный белок — гликопротеин, который синтезируется в печени. Название белок получил из-за способности вступать в реакцию преципитации с С-полисахаридом пневмококков.Традиционно СРБ рассматривают как классический белок острой фазы воспаления, который является наиболее чувствительным лабораторным маркером инфекции, воспаления и тканевого повреждения.
В зависимости от цели исследования определение концентрации СРБ проводят классическими или высокочувствительными методами. Классические методы предназначены для выявления повышенного уровня СРБ при остром воспалении и тканевом повреждении в пределах диапазона концентраций 5–500 мг/л. При концентрации СРБ меньше 5 мг/л констатируют отсутствие системного воспалительного ответа, причем достаточно долгое время точное определение концентрации СРБ не считали клинически значимым.
При концентрации СРБ меньше 5 мг/л констатируют отсутствие системного воспалительного ответа, причем достаточно долгое время точное определение концентрации СРБ не считали клинически значимым.
Высокочувствительный анализ СРБ (hsСРБ– high sensitive) позволяет измерять концентрации СРБ ниже 5 мг/л. Данное исследование используется для оценки базального уровня СРБ. Базальный уровень СРБ – уровень данного белка, который стабильно выявляется у практически здоровых лиц, а также у пациентов при отсутствии острого воспалительного процесса или вне обострения заболеваний.
Сердечно-сосудистые заболевания. В результате многочисленных и широкомасштабных исследований установлено, что измерения базовых уровней СРБ имеет прогностическое значение, которое позволяет оценить степень риска развития:
– острого инфаркта миокарда;
– мозгового инсульта;
– внезапной сердечной смерти у лиц, не страдающих сердечно-сосудистыми заболеваниями.
При остром коронарном синдроме дестабилизацию (разрыв) атеромы и образование тромба связывают с процессами воспаления. У больных нестабильной стенокардией повышенный базовый уровень hsСРБ встречается значительно чаще (у 70% пациентов), чем при стенокардии напряжения (20% пациентов).
Риск ранней летальности. При стратификации риска ранней (до 14 дней) летальности у больных с нестабильной стенокардией и острым инфарктом миокарда наиболее
информативно сочетанное определение hsСРБ и уровня сердечного тропонина Т. Повышение этих обоих маркеров риска указывает на высокий риск летального исхода.
Первичная и вторичная профилактики сердечно-сосудистых заболеваний и их осложнений. Несмотря на то, что hsСРБ является независимым предиктором риска сердечно-сосудистых заболеваний и осложнений, анализ большого количества клинических данных выявил корреляции между уровнем hsСРБ и рядом классических факторов риска (таких как курение, ожирение, инсулинорезистентность). Базовый уровень СРБ может определять эффективность лечения сердечно сосудистых заболеваний и их осложнений. При отказе от курения, регулярной физической нагрузке, умеренном потреблении алкоголя, лечении ожирения снижается базовый уровень hsСРБ и снижается коронарный риск. Прием аспирина для профилактики сосудистых осложнений эффективен только у лиц с исходно повышенным базовым уровнем hsСРБ. Прием статинов с целью профилактики ИБС также эффективен у лиц с повышенным базовым уровнем hsСРБ.
Базовый уровень СРБ может определять эффективность лечения сердечно сосудистых заболеваний и их осложнений. При отказе от курения, регулярной физической нагрузке, умеренном потреблении алкоголя, лечении ожирения снижается базовый уровень hsСРБ и снижается коронарный риск. Прием аспирина для профилактики сосудистых осложнений эффективен только у лиц с исходно повышенным базовым уровнем hsСРБ. Прием статинов с целью профилактики ИБС также эффективен у лиц с повышенным базовым уровнем hsСРБ.
Атеросклероз. Большую роль в атерогенезе, включая инициацию, развитие повреждения сосудистой стенки, нестабильности атеромы и возникновение тромботических осложнений, играет воспаление. Согласно текущей концепции атерогенеза, атеросклероз – это длительное, вялотекущее хроническое воспаление в интиме сосуда. Это делает понятной связь между медиаторами воспаления и факторами риска развития атеросклероза. Малоактивное, вялотекущее воспаление, которое обнаруживается по изменению hsСРБ, прогнозирует риск развития атеросклеротических осложнений.
Таким образом, hsСРБ — независимый предиктор острого инфаркта миокарда у практически здоровых лиц среднего возраста обоего пола, у пожилых, у больных ИБС. Также уровень hsСРБ несет самостоятельную прогностическую информацию и дополняет данные традиционных факторов риска атерогенеза.
Кровь рекомендуется сдавать утром (в период с 8 до 11 часов), натощак (не менее 8 и не более 14 часов голодания, воду пить можно).
Материал для исследования: сыворотка крови.
Интерпретация результатов содержит аналитическую информацию для лечащего врача. Лабораторные данные входят в комплекс всестороннего обследования пациента, проводимого врачом и не могут быть использованы для самодиагностики и самолечения.
Повышенный уровень hsСРБ может наблюдаться при:
§ сахарном диабете;
§ уремии;
§ гипертонии;
§ повышенной физической нагрузке;
§ низкой физической активности;
§ нарушениях сна;
§ хронической усталости;
§ злоупотреблении алкоголя;
§ депрессии;
§ приеме оральных гормональных контрацептивов;
§ заместительной гормональной терапии;
§ в третьем триместре беременности.
При измерении hsСРБ необходимо принимать во внимание факторы, влияющие на уровень СРБ. Оценка риска кардиоваскулярных заболеваний с помощью hsСРБ может быть показательной только в комплексе с определением показателей липидного обмена и расчета соотношения общего холестерина и холестеринов высокой и низкой плотности или в сочетании с определением соотношения концентраций Апо В / Апо А.
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.

- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, используйте кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или уточнить у системного администратора.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie
потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Чтобы предоставить доступ без файлов cookie
потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файлах cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файле cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
SRB Cytotoxicity Assay | Canvax Biotech
Home »Анализ на основе клеток
Для чувствительного, воспроизводимого и простого в использовании колориметрического анализа для определения цитотоксичности
Обзор продукта:
Сульфородамин B (SRB), чувствительный к анализу цитотоксичности, анализ является чувствительным и простой в использовании анализ, основанный на способности SRB связываться с белковыми компонентами клеток, которые были прикреплены к планшетам для культивирования тканей. SRB представляет собой ярко-розовый краситель на основе амиоксантена с двумя сульфоновыми группами, которые связываются с основными аминокислотными остатками в слабокислой среде и диссоциируют в основных условиях.
SRB представляет собой ярко-розовый краситель на основе амиоксантена с двумя сульфоновыми группами, которые связываются с основными аминокислотными остатками в слабокислой среде и диссоциируют в основных условиях.
Поскольку связывание SRB является стехиометрическим, количество красителя, экстрагированного из окрашенных клеток, прямо пропорционально клеточной массе. Фиксированный краситель растворяется и измеряется фотометрически при OD 540 нм с эталонным фильтром 690 нм. Значения OD коррелируют с общим содержанием белка и, следовательно, с числом клеток.
Запрос ценыДоступность: В наличии! Готов к отправке сразу
Каталожные номера, размеры и цены
| Кат.№ | Размер | Цена |
| CA050 | 1000 анализов | 95 € |
Хотите протестировать бесплатный образец? Пожалуйста, обращайтесь по телефону Free Sample Request.
Мы также предлагаем этот Продукт с другими характеристиками или размерами ( Custom Solutions ), в больших количествах ( массовых запросов, ) или на основе OEM ( OEM Partnerships ).
Примечание. Цены могут отличаться в зависимости от страны, поскольку могут взиматься дополнительные расходы из-за налогов, пересылки или таможенных сборов.
Преимущества и особенности
- Чувствительный.
- Простота в использовании.
- Fast: позволяет избежать чувствительных ко времени измерений.
- Воспроизводимый.
- Отличная линейность.
- Хорошее соотношение сигнал / шум.
- Стабильная конечная точка.
- Без риска: на продукт распространяется наша 100% гарантия качества.
Включает
Включает на 1000 анализов:
-0. 4 г SRB Dye
4 г SRB Dye
— 100 мл фиксирующего реагента
— 100 мл промывочного раствора красителя (10x)
— 200 мл SRB солюбилизирующего буфера
Загрузить документацию
Applications
- Определение токсичности, гибели, жизнеспособности или пролиферации клеток .
- Просеивание с высокой пропускной способностью.
Совет
- Меры предосторожности: Некоторые компоненты этого набора потенциально канцерогены или вызывают коррозию; желательно работать в капюшоне, в очках, перчатках и маске.
Хранение, доставка и гарантия
- Поставляется в: Температура окружающей среды.
- Хранение: Комнатная температура.
- Рекомендации: Защищайте продукт от света.
- Срок годности: 24 месяца со дня покупки при правильном хранении.
Цитаты
- Ньокки, Д., Капур, С.
 , Нитти, П., Каваллуцци, М. М., Лентини, Г., Денора, Н.,… и Маццокка, А.(2019). Новые антагонисты рецептора 6 лизофосфатидной кислоты подавляют рост гепатоцеллюлярной карциномы, влияя на функцию митохондрий. Журнал молекулярной медицины , 1-13.
, Нитти, П., Каваллуцци, М. М., Лентини, Г., Денора, Н.,… и Маццокка, А.(2019). Новые антагонисты рецептора 6 лизофосфатидной кислоты подавляют рост гепатоцеллюлярной карциномы, влияя на функцию митохондрий. Журнал молекулярной медицины , 1-13.
Заявление о безопасности
Этот продукт был разработан, спроектирован и продан исключительно для исследовательских целей, а — только для использования in vitro (RUO) . Продукт не тестировался для использования в диагностике или для разработки лекарств, а также не подходит для введения людям или животным.Для получения дополнительной информации, пожалуйста, проверьте его паспорт безопасности материала, доступный на этом веб-сайте.
Часто задаваемые вопросы
Есть вопросы? Посетите наш раздел часто задаваемых вопросов GO
Отзывы клиентов
Прозрачный свет на сульфатредуцирующие бактерии
Безхимическая УФ-дезинфекция для обратной закачки морской и пластовой воды является высокоэффективным методом предотвращения роста SRB.
Поскольку морская вода, а в последнее время и обратная закачка пластовой воды используется для увеличения добычи нефти (повышение нефтеотдачи), необходимость контроля микробиологической активности становится одной из приоритетных задач операторов во всем мире.В частности, сульфатредуцирующие бактерии (SRB), которые потребляют растворенные сульфаты в морской воде и производят сероводород (h3S), вызывают серьезную озабоченность из-за связанных с ними рисков микробной коррозии (MIC), закисания скважин, закупорки резервуаров сульфидом железа (FeS). ) и повреждение технологического оборудования и инфраструктуры.
В естественных условиях SRB присутствуют в морской воде, которая используется для многих приложений на море, таких как охлаждающая вода, системы пожаротушения и вода для закачки в скважины.SRB обычно бездействуют в аэробных средах и активируются только при попадании в анаэробные условия, такие как сеть трубопроводов или нефтяной резервуар. Такие стадии процесса, как вакуумная деаэрация, могут привести к увеличению или возникновению проблем раньше, чем ожидалось. Помимо образования h3S, бактерии могут размножаться и выделять внеклеточные полисахариды, которые могут «склеивать» клетки вместе, образуя липкие слизи или биопленки, рискуя дальнейшим повреждением оборудования и / или вызывая закупорку пористых пластов породы, снижая урожайность и разрушая объект закачка и повышение нефтеотдачи.
Помимо образования h3S, бактерии могут размножаться и выделять внеклеточные полисахариды, которые могут «склеивать» клетки вместе, образуя липкие слизи или биопленки, рискуя дальнейшим повреждением оборудования и / или вызывая закупорку пористых пластов породы, снижая урожайность и разрушая объект закачка и повышение нефтеотдачи.
Обычно операторы обычно вводят химические биоциды, например гипохлорит или глутаральдегид как при непрерывном дозировании, так и при периодическом дозировании — «шоковое дозирование» — для нацеливания на SRB и другие бактерии, присутствующие в воде для инъекций.
Как и многие микроорганизмы, SRB могут размножаться со значительной скоростью. При правильных условиях количество SRB обычно удваивается каждые 20 минут. С более чем 220 штаммами SRB этот быстрый репродуктивный цикл и естественная генетическая изменчивость, которая встречается у всех микроорганизмов, привели к тому, что виды SRB естественным образом развили толерантность или иммунитет ко многим утвержденным биоцидам, используемым в море. Часто переход на альтернативный биоцид дает лишь временное решение, пока бактерии снова не станут устойчивыми или невосприимчивыми и снова не потребуется альтернативный метод биоцида (война на истощение).
Часто переход на альтернативный биоцид дает лишь временное решение, пока бактерии снова не станут устойчивыми или невосприимчивыми и снова не потребуется альтернативный метод биоцида (война на истощение).
Исследование SrB4O7: Sm2 + в качестве многомодового датчика температуры с высокой чувствительностью, применяемые материалы и интерфейсы ACS
Исследование SrB4O7: Sm2 + как многомодового датчика температуры с высокой чувствительностьюПрикладные материалы и интерфейсы ACS ( ЕСЛИ 8.
 758
) Pub Дата: 2016-12-07 00:00:00 , DOI: 10.1021 / acsami.6b10917 Чжунминь Цао, Сяньтао Вэй, Лу Чжао, Юнху Чен, Минь Инь
758
) Pub Дата: 2016-12-07 00:00:00 , DOI: 10.1021 / acsami.6b10917 Чжунминь Цао, Сяньтао Вэй, Лу Чжао, Юнху Чен, Минь Инь Sm 2+ -легированный SrB 4 O 7 синтезирован для высокочувствительной термометрии. Высокое соотношение интенсивностей термочувствительной флуоресценции и время жизни флуоресценции были достигнуты в широком диапазоне температур. При 500 K относительная чувствительность измерения температуры составляла 2,16% K –1 для отношения интенсивностей флуоресценции и 3,36% K –1 для времени жизни флуоресценции. Кроме того, цвет флуоресценции резко изменился от темно-красного при комнатной температуре до зеленого при 700 К. На основе этого изменения цвета было получено видимое температурное поле на кварцевом стекле, покрытом нашим образцом, что сделало видимыми теплопроводность и распределение к человеческому глазу.Температуру температурного поля определяли двумя методами. Эти выдающиеся свойства в сочетании с высокой чувствительностью, многомодовым измерением температуры и термической стабильностью образца делают SrB 4 O 7 : Sm 2+ перспективным материалом для высокочувствительных термометрических приложений.
Высокое соотношение интенсивностей термочувствительной флуоресценции и время жизни флуоресценции были достигнуты в широком диапазоне температур. При 500 K относительная чувствительность измерения температуры составляла 2,16% K –1 для отношения интенсивностей флуоресценции и 3,36% K –1 для времени жизни флуоресценции. Кроме того, цвет флуоресценции резко изменился от темно-красного при комнатной температуре до зеленого при 700 К. На основе этого изменения цвета было получено видимое температурное поле на кварцевом стекле, покрытом нашим образцом, что сделало видимыми теплопроводность и распределение к человеческому глазу.Температуру температурного поля определяли двумя методами. Эти выдающиеся свойства в сочетании с высокой чувствительностью, многомодовым измерением температуры и термической стабильностью образца делают SrB 4 O 7 : Sm 2+ перспективным материалом для высокочувствительных термометрических приложений.
Ограничения анализа 3- (4,5-диметилтиазол-2-ил) -2,5-дифенил-2H-тетразолийбромида (МТТ) по сравнению с тремя обычно используемыми анализами подсчета клеток | BMC Research Notes
Для облегчения обсуждения в таблице 1 перечислены некоторые преимущества и недостатки каждого метода подсчета клеток. Несмотря на то, что в многочисленных исследованиях сравнивались анализы подсчета клеток, это, по-видимому, первый отчет, в котором сравниваются анализы NRU, MTT, RES и SRB in vitro в одинаковых условиях. В этом исследовании сравнивали методы подсчета клеток на основе линейного диапазона, воспроизводимости и влияния ингибиторов гликолиза.
Несмотря на то, что в многочисленных исследованиях сравнивались анализы подсчета клеток, это, по-видимому, первый отчет, в котором сравниваются анализы NRU, MTT, RES и SRB in vitro в одинаковых условиях. В этом исследовании сравнивали методы подсчета клеток на основе линейного диапазона, воспроизводимости и влияния ингибиторов гликолиза.
Линейный диапазон
Линейный диапазон каждого анализа с использованием диапазона концентраций клеток в течение 24 и 72 часов инкубации без воздействия какого-либо лекарственного средства показал сопоставимые результаты для трех различных используемых линий клеток.Результаты, полученные для линии клеток MDA-MB-231 с указанными 95% доверительными полосами, указывающими процент данных, которые можно объяснить с помощью регрессионного анализа, а также оптическая плотность, полученная для 50 и 100 клеток / лунка, показаны в Рисунок 1. После обоих периодов инкубации анализ SRB показывает наименьшую вариабельность, как видно с узкими 95% -ными доверительными полосами, что указывает на то, что этот анализ потенциально является наиболее точным и чувствительным к изменениям числа клеток. Наибольшая вариация линейного диапазона наблюдалась для анализа МТТ, что указывает на то, что опыт оператора с анализом, а также многие другие экспериментальные параметры могут влиять на полученные результаты.
После обоих периодов инкубации анализ SRB показывает наименьшую вариабельность, как видно с узкими 95% -ными доверительными полосами, что указывает на то, что этот анализ потенциально является наиболее точным и чувствительным к изменениям числа клеток. Наибольшая вариация линейного диапазона наблюдалась для анализа МТТ, что указывает на то, что опыт оператора с анализом, а также многие другие экспериментальные параметры могут влиять на полученные результаты.
Линейный диапазон четырех тестов подсчета клеток с использованием клеток MDA-MB-231. Четыре различных анализа подсчета клеток были выполнены после 24 и 72 часов инкубации при шести возрастающих исходных плотностях клеток. Сплошная линия представляет собой аппроксимацию данных методом наименьших квадратов. Пунктирные линии представляют собой доверительные интервалы 95%. Графики для 24-часового периода инкубации отображают плотность клеток до 10 000 клеток / лунку, а 72-часовой период инкубации отображает плотность клеток до 5000 клеток / лунку (n = 4).
Высокие значения фоновой абсорбции, полученные в результате анализа МТТ при самых низких плотностях посева через 24 часа, предполагают, что этот анализ менее чувствителен при количестве клеток ниже 1000 клеток / лунку. Анализы RES и SRB позволили точно обнаружить различия в количестве клеток до 500 клеток / лунку. Несмотря на то, что низкая плотность посева используется не часто, цитотоксические эффекты новых терапевтических агентов могут приводить к такому уменьшению числа клеток. Для скрининга новых терапевтических агентов анализ SRB кажется лучше, чем анализ MTT из-за большей чувствительности.
Очевидно, что сигнал поглощения прямо пропорционален количеству клеток, которое, как ожидается, будет увеличиваться со временем инкубации. Это наиболее четко видно после 72 ч инкубации, когда проводился анализ МТТ (рис. 1). Однако в некоторых сообщениях указывается, что количество производимых кристаллов формазана зависит не только от количества клеток [33,36]. Анализ МТТ основан на превращении тетразолиевого красителя в формазан в основном митохондриальными янтарными дегидрогеназами, хотя цитозольные ферменты, такие как никотинамидадениндинуклеотид (НАДН) редуктаза и флавиноксидаза, также могут быть задействованы [4].Было показано, что скорость превращения в формазан связана с метаболической активностью клетки, и поэтому снижение внутриклеточной концентрации глюкозы может привести к уменьшению количества образующихся кристаллов формазана [36]. Другой фактор, который, как сообщается, влияет на превращение в формазан, — это количество митохондрий, присутствующих в клетке. Соответственно, более крупные клетки с большим количеством митохондрий имеют более высокую скорость превращения тетразолия [33]. Сообщалось также, что дефектные митохондрии сохраняют способность восстанавливать тетразолий [37].Взятые вместе, эти факторы могут привести к неверной оценке количества сот.
Анализ МТТ основан на превращении тетразолиевого красителя в формазан в основном митохондриальными янтарными дегидрогеназами, хотя цитозольные ферменты, такие как никотинамидадениндинуклеотид (НАДН) редуктаза и флавиноксидаза, также могут быть задействованы [4].Было показано, что скорость превращения в формазан связана с метаболической активностью клетки, и поэтому снижение внутриклеточной концентрации глюкозы может привести к уменьшению количества образующихся кристаллов формазана [36]. Другой фактор, который, как сообщается, влияет на превращение в формазан, — это количество митохондрий, присутствующих в клетке. Соответственно, более крупные клетки с большим количеством митохондрий имеют более высокую скорость превращения тетразолия [33]. Сообщалось также, что дефектные митохондрии сохраняют способность восстанавливать тетразолий [37].Взятые вместе, эти факторы могут привести к неверной оценке количества сот.
Коэффициент детерминации (r 2 ), показывающий, насколько точно полученная кривая роста может соответствовать статистике нелинейной регрессии для тестируемых клеточных линий и периодов инкубации, показан в таблице 2. An r 2 значение менее 0,9 было рассчитано для анализов MTT и NRU после 24 ч инкубации с использованием клеточных линий MCF-7 и MCF-12A соответственно, в то время как значение r 2 было меньше 0.9 было рассчитано для анализов MTT и RES после 72 ч инкубации. Анализ SRB был единственным анализом, для которого статистика нелинейной регрессии могла быть точно подогнана к экспериментальным данным, полученным после обоих проверенных значений времени инкубации, что позволяет предположить, что наиболее надежные результаты будут получены с использованием анализа SRB.
An r 2 значение менее 0,9 было рассчитано для анализов MTT и NRU после 24 ч инкубации с использованием клеточных линий MCF-7 и MCF-12A соответственно, в то время как значение r 2 было меньше 0.9 было рассчитано для анализов MTT и RES после 72 ч инкубации. Анализ SRB был единственным анализом, для которого статистика нелинейной регрессии могла быть точно подогнана к экспериментальным данным, полученным после обоих проверенных значений времени инкубации, что позволяет предположить, что наиболее надежные результаты будут получены с использованием анализа SRB.
Данные, полученные в ходе этого исследования относительно широкого линейного диапазона анализа SRB, подтверждают опубликованные результаты [38].Для анализа SRB был рассчитан наивысший средний коэффициент детерминации, что указывает на большую предсказательную силу анализа. Из четырех анализов анализ SRB является единственным истинным методом подсчета клеток, поскольку он не полагается на метаболическую функцию или активность живых клеток для количественного определения количества клеток [22]. Вместо этого анализ основан на способности SRB связываться с основными аминокислотами в слабокислых условиях, в то время как связанное пятно высвобождается в сильно щелочных условиях [22]. Этот подход исключает влияние различных биологических параметров, таких как повышенная скорость метаболизма или количество клеточных митохондрий, на процесс количественной оценки.Эти данные показывают, что анализ SRB, по-видимому, является наиболее эффективным для обнаружения небольших или больших изменений числа клеток.
Из четырех анализов анализ SRB является единственным истинным методом подсчета клеток, поскольку он не полагается на метаболическую функцию или активность живых клеток для количественного определения количества клеток [22]. Вместо этого анализ основан на способности SRB связываться с основными аминокислотами в слабокислых условиях, в то время как связанное пятно высвобождается в сильно щелочных условиях [22]. Этот подход исключает влияние различных биологических параметров, таких как повышенная скорость метаболизма или количество клеточных митохондрий, на процесс количественной оценки.Эти данные показывают, что анализ SRB, по-видимому, является наиболее эффективным для обнаружения небольших или больших изменений числа клеток.
Хамид и его коллеги, которые провели обширное исследование по сравнению анализов МТТ и RES, пришли к выводу, что, хотя оба анализа полезны в качестве анализов цитотоксичности, анализ RES больше подходит для HTS, поскольку он более чувствителен [34]. В настоящем исследовании линейный диапазон для анализа RES был немного шире, чем для теста MTT; но, что более важно, общий коэффициент детерминации, рассчитанный для анализа RES, был лучше, чем для анализа MTT. Однако следует учитывать, что в этом исследовании использовалась версия анализа RES, основанная на поглощении, и что чувствительность и селективность анализа будут дополнительно улучшены с помощью детектирования флуоресценции. В отличие от анализа МТТ, анализ восстановления резазурина предлагает преимущество, позволяющее проводить последующие анализы, поскольку реагенты и краситель, используемые в анализе RES, не влияют на жизнеспособность клеток [35]. В отличие от МТТ и других тестов на основе тетразолия, которые отменяют дыхание, краситель RES действует как акцептор электронов на последней стадии дыхательной цепи и не оказывает токсического действия [32].К сожалению, сообщалось, что FCS влияет на анализ RES [19], но это препятствие можно легко преодолеть, удалив среду для культивирования клеток в конце периода инкубации и используя бессывороточную среду в качестве растворителя для резазуринового красителя вместо полного среда для культивирования клеток.
Однако следует учитывать, что в этом исследовании использовалась версия анализа RES, основанная на поглощении, и что чувствительность и селективность анализа будут дополнительно улучшены с помощью детектирования флуоресценции. В отличие от анализа МТТ, анализ восстановления резазурина предлагает преимущество, позволяющее проводить последующие анализы, поскольку реагенты и краситель, используемые в анализе RES, не влияют на жизнеспособность клеток [35]. В отличие от МТТ и других тестов на основе тетразолия, которые отменяют дыхание, краситель RES действует как акцептор электронов на последней стадии дыхательной цепи и не оказывает токсического действия [32].К сожалению, сообщалось, что FCS влияет на анализ RES [19], но это препятствие можно легко преодолеть, удалив среду для культивирования клеток в конце периода инкубации и используя бессывороточную среду в качестве растворителя для резазуринового красителя вместо полного среда для культивирования клеток.
Воспроизводимость
Повышенная воспроизводимость означает необходимость меньшего количества повторений экспериментов и, следовательно, меньшего количества реагентов и расходных материалов для получения надежных данных. Нельзя недооценивать значение затрат и времени эксперимента.Сравнение воспроизводимости анализов, полученных в концентрациях ингибиторов гликолиза IC 50 , рассчитанных после четырех независимых экспериментов с внутренними троекратными повторами, обеспечивает эффективное средство для ранжирования анализов по воспроизводимости. Результаты статистики нелинейной регрессии были использованы для построения кривых доза-ответ для каждого анализа на линии клеток MCF-7 после 24- и 72-часового инкубационного периода (рис. 2). Похоже, что точки данных для анализов MTT и SRB наиболее близко напоминают кривые доза-ответ, предполагая, что эти анализы дадут наиболее надежные результаты.После трех экспериментальных повторов анализ SRB показал самую низкую общую вариабельность как в 24-, так и в 72-часовой периоды времени и для всех трех тестируемых клеточных линий (таблица 3), что означает, что для получения надежных результатов в этом анализе потребуется меньше экспериментальных повторов.
Нельзя недооценивать значение затрат и времени эксперимента.Сравнение воспроизводимости анализов, полученных в концентрациях ингибиторов гликолиза IC 50 , рассчитанных после четырех независимых экспериментов с внутренними троекратными повторами, обеспечивает эффективное средство для ранжирования анализов по воспроизводимости. Результаты статистики нелинейной регрессии были использованы для построения кривых доза-ответ для каждого анализа на линии клеток MCF-7 после 24- и 72-часового инкубационного периода (рис. 2). Похоже, что точки данных для анализов MTT и SRB наиболее близко напоминают кривые доза-ответ, предполагая, что эти анализы дадут наиболее надежные результаты.После трех экспериментальных повторов анализ SRB показал самую низкую общую вариабельность как в 24-, так и в 72-часовой периоды времени и для всех трех тестируемых клеточных линий (таблица 3), что означает, что для получения надежных результатов в этом анализе потребуется меньше экспериментальных повторов.
Влияние 3-бромпирувата на рост клеток MCF-7. На графиках представлены результаты, полученные после 24 и 72 часов инкубации, по результатам четырех анализов подсчета клеток.Обратите внимание, что шкалы ошибок меньше на графиках 72-часовой инкубации, и во многих точках данных они попадают в пределы символа (n = 3).
На графиках представлены результаты, полученные после 24 и 72 часов инкубации, по результатам четырех анализов подсчета клеток.Обратите внимание, что шкалы ошибок меньше на графиках 72-часовой инкубации, и во многих точках данных они попадают в пределы символа (n = 3).
Концентрации ингибиторов гликолиза IC 50 можно было определить только в обеих точках времени инкубации с помощью анализов NRU и SRB, но не с помощью анализа MTT (рисунок 2, дополнительный файл 1), что может указывать на недостаточную чувствительность этого метода. проба.Однако в предыдущем исследовании сообщалось о концентрации IC 50 84,6 ± 15,4 мкМ для 3-BrPA с использованием клеток MCF-7 после 16 ч инкубации с использованием анализа MTT, в котором кристаллы формазана солюбилизировали с использованием раствора изопропанола [39]. После 16-часовой инкубации только небольшой процент клеток MCF-7 разделился бы, и меньшее количество клеток стало бы доступным для преобразования тетразолиевого красителя в формазановый продукт, что позволяет предположить, что концентрация IC 50 через 24 часа должна быть возможной. Однако разница в используемом растворителе для солюбилизации, изопропанол, в отличие от ДМСО, может повлиять на полученные результаты.
После 16-часовой инкубации только небольшой процент клеток MCF-7 разделился бы, и меньшее количество клеток стало бы доступным для преобразования тетразолиевого красителя в формазановый продукт, что позволяет предположить, что концентрация IC 50 через 24 часа должна быть возможной. Однако разница в используемом растворителе для солюбилизации, изопропанол, в отличие от ДМСО, может повлиять на полученные результаты.
Исследования интерференции
Потенциальные помехи между ингибиторами гликолиза и красителями, используемыми в каждом из анализов подсчета клеток, были исследованы с использованием бесклеточных анализов, и результаты показаны на рисунке 3. Поглощение тетразолиевого красителя, использованного в анализе МТТ, действительно не остается постоянным, когда любой из ингибиторов гликолиза инкубируется с красителем в течение 4 часов в бесклеточной системе. Интересно отметить, что абсорбция не демонстрирует последовательного дозозависимого изменения в присутствии всех ингибиторов гликолиза: абсорбция увеличивается дозозависимым образом при воздействии 3-BrPA, но снижается при воздействии 2DG и LON. Никаких помех, измеренных по изменению цвета, не наблюдалось для анализов NRU, SRB или RES с любым из протестированных ингибиторов гликолиза (см. Дополнительный файл 2).
Никаких помех, измеренных по изменению цвета, не наблюдалось для анализов NRU, SRB или RES с любым из протестированных ингибиторов гликолиза (см. Дополнительный файл 2).
Вмешательство трех ингибиторов гликолиза в тест МТТ в бесклеточной системе. После 4 часов инкубации с (A) 2-дезоксиглюкоза, (B) 3-бромпируват и (C) лонидамин интерференция наблюдалась для анализа МТТ (n = 3).
Ранее сообщалось о взаимодействии между ингибиторами гликолиза и анализами подсчета клеток [11]. Из трех ингибиторов гликолиза, выбранных для этого исследования, 3-бромпируват и 2-дезоксиглюкоза ингибируют гексокиназу, фермент, ответственный за превращение глюкозы в глюкозо-6-фосфат на первой лимитирующей стадии гликолитического пути [24]. Аналог глюкозы 2DG конкурирует за преобразование гексокиназой с глюкозой. Продукт этого превращения, 2-дезоксиглюкозо-6-фосфат, не метаболизируется последующими гидролитическими ферментами, и поэтому клетки медленно умирают от голода [24].
Наблюдаемое вмешательство между ингибиторами гликолиза и тетразолиевым красителем МТТ было значительным (приблизительно 2-кратное увеличение поглощения) и убедительно свидетельствует о том, что этот анализ не подходит для использования с ингибиторами гликолиза. Это подтверждает ранее опубликованные данные о взаимодействии между 3-BrPA и анализами на основе тетразолия [11]. Данные, полученные в этом исследовании, предполагают вмешательство 2DG в анализ МТТ. Однако о предыдущих исследованиях с использованием 2DG и теста MTT сообщалось без какого-либо упоминания о вмешательстве со стороны 2DG [40].Снижение абсорбции, отмеченное после инкубации МТТ с 2DG и LON, не может быть объяснено на основе доступной информации, и задействованный механизм требует дальнейшего изучения. Интересно, что анализ RES, который основан на аналогичном механизме восстановления, что и анализ MTT, не выявил влияния какого-либо из трех ингибиторов гликолиза (дополнительный файл 1). Отсутствие интерференции, наблюдаемой в анализах SRB и NRU, можно объяснить различными мишенями связывания красителя, обеспечивающими цвет в этих анализах. Насколько известно автору, на сегодняшний день не опубликовано никаких сообщений о влиянии экспериментальных соединений на анализ SRB.
Насколько известно автору, на сегодняшний день не опубликовано никаких сообщений о влиянии экспериментальных соединений на анализ SRB.
Чувствительность лапатиниба при карциноме носоглотки модулируется SIRT2-опосредованным деацетилированием FOXO3 | BMC Cancer
Wei WI, Sham JST. Карцинома носоглотки. Ланцет. 2005; 365 (9476): 2041–54.
PubMed Статья PubMed Central Google ученый
Mahdavifar N, Ghoncheh M, Mohammadian-Hafshejani A, Khosravi B, Salehiniya H.Эпидемиология и неравенство в заболеваемости и смертности от рака носоглотки в Азии. Уважение к общественному здравоохранению Осон. 2016; 7 (6): 360–72.
PubMed PubMed Central Статья Google ученый
млн ДБЯ, Чан УВД. Недавние взгляды на роль химиотерапии в лечении распространенной карциномы носоглотки. Рак. 2005. 103 (1): 22–31.
PubMed Статья PubMed Central Google ученый
Hsu CH, Chen CL, Hong RL, Chen KL, Lin JF, Cheng AL. Прогностическое значение множественной лекарственной устойчивости 1, глутатион- S -трансферазы-π и p53 при запущенной карциноме носоглотки, леченной системной химиотерапией. Онкология. 2002. 62 (4): 305–12.
CAS PubMed Статья PubMed Central Google ученый
Jiang R-D, Zhang L-X, Yue W, Zhu Y-F, Lu H-J, Liu X и др. Создание линии клеток CNE2 / DDP, устойчивой к лекарственным средствам карциномы носоглотки, и скрининг генов лекарственной устойчивости; 2003 г. п. 337–45.
п. 337–45.
Google ученый
Cheung HW, Jin D-Y, Ling M-t, Wong YC, Wang Q, Tsao SW, et al. Экспрессия 2, недостаточная для остановки митоза, вызывает хемосенсибилизацию к повреждающему ДНК агенту, цисплатину, в клетках карциномы носоглотки. Cancer Res. 2005; 65 (4): 1450.
CAS PubMed Статья PubMed Central Google ученый
Ван Дж, Ван Х, Чжао Л., Фан С., Ян З., Гао Ф и др.Подавление Р-гликопротеина связано с устойчивостью к цисплатину и VP-16 в клеточных линиях рака легких человека. Anticancer Res. 2010. 30 (9): 3593–8.
CAS PubMed PubMed Central Google ученый
Pan Y, Zhou F, Zhang R, Claret FX. Статический ингибитор Stat3 проявляет мощную противоопухолевую активность и вызывает химио- и радиочувствительность при карциноме носоглотки. PLoS One. 2013; 8 (1): e54565.
CAS PubMed PubMed Central Статья Google ученый
Ma BB, Poon TC, To KF, Zee B, Mo FK, Chan CM и др. Прогностическое значение опухолевого ангиогенеза, Ki 67, онкопротеина p53, рецептора эпидермального фактора роста и экспрессии белка рецептора HER2 при недифференцированной карциноме носоглотки — перспективное исследование. Голова Шея. 2003. 25 (10): 864–72.
PubMed Статья PubMed Central Google ученый
Джин О., Чен С., Ли Дж. , Яо К. Экспрессия мРНК CerbB-2 и EGFR в карциномах носоглотки и перикарциноматозных тканях человека.Хунань И Кэ Да Сюэ Сюэ Бао. 1997. 22 (6): 487–90.
, Яо К. Экспрессия мРНК CerbB-2 и EGFR в карциномах носоглотки и перикарциноматозных тканях человека.Хунань И Кэ Да Сюэ Сюэ Бао. 1997. 22 (6): 487–90.
CAS PubMed Google ученый
Ма BB, Луи Ф.В., Пун Ф.Ф., Вонг С.К., То К.Ф., Вонг Э. и др. Доклиническая активность гефитиниба в некератинизирующих клеточных линиях карциномы носоглотки и биомаркеры ответа. Исследуйте новые наркотики. 2010. 28 (3): 326–33.
CAS Статья Google ученый
Лю Л., Хуанг П., Ван З., Чен Н., Тан С., Линь З. и др.Ингибирование киназы eEF-2 повышает чувствительность клеток карциномы носоглотки человека к апоптозу, индуцированному лапатинибом, по путям Src и Erk. BMC Рак. 2016; 16: 813.
PubMed PubMed Central Статья CAS Google ученый
Луи VWY, Lau CPY, Ho K, Ng MHL, Cheng SH, Tsao S-W, et al. Антиинвазионные, антипролиферативные и аноикисенсибилизирующие действия лапатиниба в клетках карциномы носоглотки. Исследуйте новые наркотики.2011; 29 (6): 1241–52.
CAS Статья Google ученый
Wilson MSC, Brosens JJ, Schwenen HDC, Lam EW-F. FOXO и FOXM1 при раке: ось FOXO-FOXM1 формирует результат химиотерапии рака. Curr Drug Targets. 2011; 12 (9): 1256–66.
CAS PubMed Статья Google ученый
Olmos Y, Brosens JJ, Lam EW. Взаимодействие между белками SIRT и факторами транскрипции супрессоров опухолей в химиотерапевтической устойчивости рака.Обновление лекарственного сопротивления. 2011; 14 (1): 35–44.
2011; 14 (1): 35–44.
CAS PubMed Статья Google ученый
Дайтоку Х., Сакамаки Джи, Фукамизу А. Регулирование факторов транскрипции FoxO посредством ацетилирования и межбелковых взаимодействий. Mol Cell Res. 2011; 1813 (11): 1954–60.
CAS Google ученый
Jiang L, Wang P, Chen H. Сверхэкспрессия FOXM1 связана с метастазами карциномы носоглотки.Ups J Med Sci. 2014; 119 (4): 324–32.
PubMed PubMed Central Статья Google ученый
Hou Y, Zhu Q, Li Z, Peng Y, Yu X, Yuan B и др. Ось FOXM1 – ABCC5 способствует устойчивости к паклитакселу в клетках карциномы носоглотки. Cell Death Dis. 2017; 8 (3): e2659.
Cell Death Dis. 2017; 8 (3): e2659.
CAS PubMed PubMed Central Статья Google ученый
Шоу З, Линь Л., Лян Дж., Ли Дж-Л, Чен Х-Й.Экспрессия и прогноз FOXO3a и HIF-1α при карциноме носоглотки. J Cancer Res Clin Oncol. 2012. 138 (4): 585–93.
CAS PubMed Статья Google ученый
Шу СН, Ян В.К., Ши Ю.Л., Куо М.Л., Хуанг Т.С. Остановка клеточного цикла G2 / M и активация циклин-зависимых киназ, связанная с индуцированным низкими дозами паклитакселом апоптозом суб-G1. Апоптоз. 1997. 2 (5): 463–70.
CAS PubMed Статья Google ученый
Song LB, Yan J, Jian SW, Zhang L, Li MZ, Li D и др. Молекулярные механизмы онкогенеза и метастазирования в сублинии клеток карциномы носоглотки. Ай Чжэн. 2002. 21 (2): 158–62.
PubMed Google ученый
Huang PY, Hong MH, Zhang X, Mai HQ, Luo DH, Zhang L. Сверхэкспрессия и мутация C-KIT в клеточных линиях карциномы носоглотки и реактивность иматиниба на этих клеточных линиях. Чин Дж. Рак. 2010. 29 (2): 131–5.
PubMed Статья Google ученый
Хуанг Д.П., Хо Дж. Х., Пун Ю. Ф., Чу ЕС, Пила Д., Луи М. и др. Создание клеточной линии (NPC / HK1) из дифференцированной плоскоклеточной карциномы носоглотки. Int J Cancer. 1980. 26 (2): 127–32.
CAS PubMed Статья Google ученый
Cheung ST, Huang DP, Hui AB, Lo KW, Ko CW, Tsang YS и др. Клеточная линия карциномы носоглотки (C666-1), постоянно несущая вирус Эпштейна-Барра. Int J Cancer. 1999. 83 (1): 121–6.
CAS PubMed Статья Google ученый
van der Vos KE, Coffer PJ. Расширяющаяся сеть транскрипционных генов-мишеней FOXO. Антиоксидный окислительно-восстановительный сигнал. 2011; 14 (4): 579–92.
PubMed Статья CAS Google ученый
Чуа К.Ф., Мостославский Р., Ломбард Д.Б., Панг В.В., Сайто С., Франко С. и др. SIRT1 млекопитающих ограничивает репликативную продолжительность жизни в ответ на хронический генотоксический стресс.Cell Metab. 2005. 2 (1): 67–76.
CAS PubMed Статья Google ученый
Paik JH, Kollipara R, Chu G, Ji H, Xiao Y, Ding Z, et al. FoxOs являются избыточными супрессорами опухолей, ограниченными по клону, и регулируют гомеостаз эндотелиальных клеток. Cell. 2007. 128 (2): 309–23.
CAS PubMed PubMed Central Статья Google ученый
Weiss JM, Bagley S, Hwang W-T, Bauml J, Olson JG, Cohen RB, et al.Капецитабин и лапатиниб для лечения первой линии метастатического / рецидивирующего плоскоклеточного рака головы и шеи. Рак. 2016; 122 (15): 2350–5.
CAS PubMed Статья Google ученый
Machiels J-PH, Haddad RI, Fayette J, Licitra LF, Tahara M, Vermorken JB, et al. Афатиниб в сравнении с метотрексатом в качестве терапии второй линии у пациентов с рецидивирующей или метастатической плоскоклеточной карциномой головы и шеи, прогрессирующей на фоне терапии платиной или после нее (LUX-Head & Neck 1): открытое рандомизированное исследование фазы 3. Ланцет Онкол. 2015; 16 (5): 583–94.
Ланцет Онкол. 2015; 16 (5): 583–94.
CAS PubMed Статья Google ученый
Харрингтон К.Дж., Темам С., Д’Круз А., Джайн М.М., Д’Онофрио И., Манихас Г.М. и др. Окончательный анализ: рандомизированное слепое плацебо-контролируемое исследование III фазы адъювантного послеоперационного лапатиниба (L) с одновременной химиотерапией и лучевой терапией (CH-RT) у пациентов с высоким риском плоскоклеточного рака головы и шеи ( СКЧН). J Clin Oncol.2014; 32 (15_suppl): 6005.
Артикул Google ученый
Яо С., Фан Л.Й., Лам Е.В. Ось FOXO3-FOXM1: ключевая мишень против рака и модулятор устойчивости к лекарствам от рака. Semin Cancer Biol. 2018; 50: 77–89.
CAS PubMed PubMed Central Статья Google ученый
Myatt SS, Lam EW. Новые роли белков вилки-бокса (Fox) при раке.Nat Rev Рак. 2007. 7 (11): 847–59.
CAS PubMed Статья PubMed Central Google ученый
Xia W, Bacus S, Hegde P, Husain I., Strum J, Liu L, et al. Модель приобретенной ауторезистентности к мощному ингибитору тирозинкиназы ErbB2 и терапевтическая стратегия для предотвращения ее возникновения при раке груди. Proc Natl Acad Sci U S. A. 2006; 103 (20): 7795–800.
CAS PubMed PubMed Central Статья Google ученый
Karadedou CT, Gomes AR, Chen J, Petkovic M, Ho KK, Zwolinska AK, et al. FOXO3a подавляет экспрессию VEGF через FOXM1-зависимые и независимые механизмы при раке груди. Онкоген. 2012. 31 (14): 1845–58.
Онкоген. 2012. 31 (14): 1845–58.
CAS PubMed Статья PubMed Central Google ученый
Wu J, Tang QIN, Zhao S, Zheng F, Wu YAN, Tang GE и др. Индукция и взаимодействие FOXO3a и p53, регулируемая внеклеточными сигналами, опосредованная передачей сигналов киназы, способствует ингибированию куркумином роста клеток карциномы носоглотки.Int J Oncol. 2014. 45 (1): 95–103.
CAS PubMed PubMed Central Статья Google ученый
Чжоу В-Дж, Дэн Р., Фэн Г-К, Чжу Х-Ф. G-квадруплексный лиганд SYUIQ-5 индуцирует аутофагию путем ингибирования пути Akt-FOXO3a в раковых клетках носоглотки; 2009. с. 1049–53.
Google ученый
Lam EW, Brosens JJ, Gomes AR, Koo CY. Белки коробки вилки: камертоны для гармонии транскрипции.Nat Rev Рак. 2013. 13 (7): 482–95.
CAS PubMed Статья PubMed Central Google ученый
Ho KK, McGuire VA, Koo CY, Muir KW, de Olano N, Maifoshie E, et al. Фосфорилирование FOXO3a на Ser-7 с помощью p38 способствует его ядерной локализации в ответ на доксорубицин. J Biol Chem. 2012. 287 (2): 1545–55.
CAS PubMed Статья PubMed Central Google ученый
Сантерс А., Мадурейра ПА, Померанц К.М., Оберт М., Бросенс Дж. Дж., Кук С. Дж. И др. Индуцированная паклитакселом ядерная транслокация FOXO3a в клетках рака груди опосредуется c-Jun Nh3-концевой киназой и Akt. Cancer Res. 2006; 66 (1): 212–20.
Cancer Res. 2006; 66 (1): 212–20.
CAS PubMed Статья PubMed Central Google ученый
McGovern UB, Francis RE, Peck B., Guest SK, Wang J, Myatt SS, et al. Гефитиниб (Iressa) подавляет экспрессию FOXM1 через FOXO3a при раке груди.Mol Cancer Ther. 2009. 8 (3): 582–91.
CAS PubMed Статья Google ученый
Mora Vidal R, Regufe da Mota S, Hayden A, Markham H, Douglas J, Packham G, et al. Ингибирование семейства рецепторов эпидермального фактора роста указывает на то, что митоген-активируемая протеинкиназа P38 является потенциальной терапевтической мишенью при раке мочевого пузыря. Урология. 2018; 112: 225 e1–7.
Артикул Google ученый
Gschwantler-Kaulich D, Grunt TW, Muhr D, Wagner R, Kolbl H, Singer CF. HER-специфические TKI оказывают свое противоопухолевое действие на клеточные линии рака молочной железы через участие STAT5 и JNK. PLoS One. 2016; 11 (1): e0146311.
PubMed PubMed Central Статья CAS Google ученый
Carr JR, Park HJ, Wang Z, Kiefer MM, Raychaudhuri P. FoxM1 опосредует устойчивость к герцептину и паклитакселу. Cancer Res.2010. 70 (12): 5054–63.
CAS PubMed PubMed Central Статья Google ученый
Миранда СКВ, Ян Дж.Б., Хельма DCS, Эрик ВФЛ. FOXO и FOXM1 при раке: ось FOXO-FOXM1 формирует результат химиотерапии рака. Curr Drug Targets. 2011; 12 (9): 1256–66.
Артикул Google ученый
Jiang L, Wang P, Chen L, Chen H. Понижающая регуляция FoxM1 тиострептоном или малой интерферирующей РНК подавляет пролиферацию, способность к трансформации и ангиогенез, а также вызывает апоптоз клеток карциномы носоглотки.Int J Clin Exp Pathol. 2014. 7 (9): 5450–60.
CAS PubMed PubMed Central Google ученый
Ван Ф., Нгуен М., Цинь FX-F, Тонг К. SIRT2 деацетилирует FOXO3a в ответ на окислительный стресс и ограничение калорийности. Ячейка старения. 2007. 6 (4): 505–14.
CAS Статья Google ученый

Брюнет А., Суини Л. Б., Стерджилл Дж. Ф., Чуа К. Ф., Грир П. Л., Лин И. и др.Стресс-зависимая регуляция факторов транскрипции FOXO деацетилазой SIRT1. Наука. 2004; 303 (5666): 2011.
CAS PubMed Статья PubMed Central Google ученый
Khongkow M, Olmos Y, Gong C, Gomes AR, Monteiro LJ, Yague E, et al. SIRT6 модулирует устойчивость к паклитакселу и эпирубицину и выживаемость при раке молочной железы. Канцерогенез. 2013. 34 (7): 1476–86.
CAS PubMed Статья PubMed Central Google ученый
Ху Ц., Вэй В., Чен Х, Вудман С.Б., Яо Ю., Николлс Дж. М. и др. Глобальный взгляд на онкогенный ландшафт карциномы носоглотки: комплексный анализ на генетическом уровне и уровне экспрессии. PLoS One. 2012; 7 (7): e41055.
PLoS One. 2012; 7 (7): e41055.
CAS PubMed PubMed Central Статья Google ученый
Пек Б., Чен С.Й., Хо К.К., Ди Фрушиа П., Мятт С.С., Кумбес Р.К. и др. Ингибиторы SIRT вызывают гибель клеток и ацетилирование p53, воздействуя на SIRT1 и SIRT2.Mol Cancer Ther. 2010. 9 (4): 844–55.
CAS PubMed PubMed Central Статья Google ученый
Дан Л., Клименкова О., Климианкоу М., Клусман Дж. Х., ван ден Хеувель-Эйбринк М.М., Рейнхардт Д. и др. Роль активации сиртуина 2 никотинамидфосфорибозилтрансферазой в аберрантной пролиферации и выживании клеток миелоидного лейкоза. Haematologica. 2012. 97 (4): 551–9.
CAS PubMed PubMed Central Статья Google ученый
He X, Nie H, Hong Y, Sheng C, Xia W, Ying W. Активность SIRT2 необходима для выживания клеток глиомы C6. Biochem Biophys Res Commun. 2012; 417 (1): 468–72.
CAS PubMed Статья Google ученый
Wilking-Busch MJ, Ndiaye MA, Liu X, Ahmad N. Опосредованный РНК-интерференцией нокдаун SIRT1 и / или SIRT2 в меланоме: идентификация последующих мишеней с помощью крупномасштабного протеомного анализа. J Proteome. 2018; 170: 99–109.
CAS Статья Google ученый
Мацусита Н., Таками Ю., Кимура М., Тачиири С., Ишиаи М., Накаяма Т. и др. Роль НАД-зависимых деацетилаз SIRT1 и SIRT2 в радиационной и цисплатин-индуцированной гибели клеток в клетках позвоночных. Гены клеток. 2005. 10 (4): 321–32.
Гены клеток. 2005. 10 (4): 321–32.
CAS PubMed Статья Google ученый
Ван Ф, Чан Чан, Чен К, Гуань Х, Линь ХК, Тонг К.Деацетилирование FOXO3 с помощью SIRT1 или SIRT2 приводит к Skp2-опосредованному убиквитинированию и деградации FOXO3. Онкоген. 2011; 31: 1546.
PubMed Статья CAS Google ученый
Электрохимический иммуносенсор на основе высокочувствительного углеродного электрода с трафаретной печатью, модифицированного нанопластинками графена, модифицированного аминогруппами
[1]
А. Мартин и А. Эскарпа, Тенденции в аналитической химии Графен: новейшее взаимодействие между химией и электрохимией, т. 56, стр.13–26, (2014).
Мартин и А. Эскарпа, Тенденции в аналитической химии Графен: новейшее взаимодействие между химией и электрохимией, т. 56, стр.13–26, (2014).
DOI: 10.1016 / j.trac.2013.12.008
[2] Б.Чжан, Ю. Ван и Г. Чжай, Биомедицинские применения материалов на основе графена, Матер. Sci. Англ. С, т. 61, p.953–964, (2016).
[3]
Г. Беруэлл, С. Тейшейра, А. Кастейн и О. Гай, Синтез и характеристика эпитаксиального графена, модифицированного (3-аминопропил) триэтоксисиланом, т. 806, с.95–102, (2015).
Беруэлл, С. Тейшейра, А. Кастейн и О. Гай, Синтез и характеристика эпитаксиального графена, модифицированного (3-аминопропил) триэтоксисиланом, т. 806, с.95–102, (2015).
DOI: 10.4028 / www.scientific.net / msf.806.95
[4] С.Тейшейра, Р. С. Конлан, О. Дж. Гай и М. Г. Ф. Сейлз, Новый электрод с одностенными углеродными нанотрубками, напечатанный методом трафаретной печати, в качестве иммуносенсора на хорионический гонадотропин человека, Electrochim. Acta, т. 136, с.323–329, (2014).
DOI: 10. 1016 / j.electacta.2014.05.105
1016 / j.electacta.2014.05.105
[5] Л.Hou, Y. Cui, M. Xu, Z. Gao, J. Huang и D. Tang, Импедиметрический иммуноанализ сэндвич-типа, меченный оксидом графена, с усилением чувствительности на основе ферментативного окисления 4-хлор-1-нафтола, Biosens. Биоэлектрон., Т. 47. С. 149–156, (2013).
DOI: 10.1016 / j.bios.2013.02.035
[6]
С.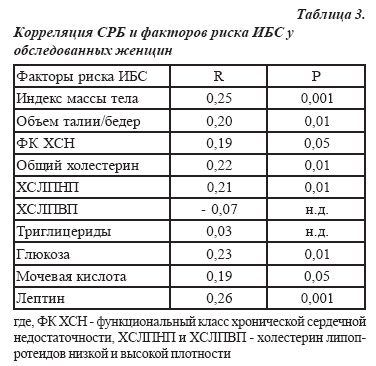 Rauf, G. K. Mishra, J. Azhar, R. K. Mishra, K. Y. Goud, M. A. H. Nawaz, J. L. Marty и A. Hayat, одноразовый электрохимический иммуносенсор на основе обогащенного карбоновыми группами оксида графена для обнаружения биомаркеров рака. Biochem., Т. 545, стр.13–19, (2018).
Rauf, G. K. Mishra, J. Azhar, R. K. Mishra, K. Y. Goud, M. A. H. Nawaz, J. L. Marty и A. Hayat, одноразовый электрохимический иммуносенсор на основе обогащенного карбоновыми группами оксида графена для обнаружения биомаркеров рака. Biochem., Т. 545, стр.13–19, (2018).
DOI: 10.1016 / j.ab.2018.01.007
[7]
С.Ли, З. Ван, Дж. Цзя, К. Хоу, Х. Хао и Х. Чжан, Получение многослойных углеродных нанотрубок, функционализированных гидроксилом и (3-аминопропил) триэтоксисиланом, для использования в качестве проводящих наполнителей в полиуретановом композите, (2016 г. ) ).
) ).
DOI: 10.1002 / pc.24054
[8] Ю.Цзэн, Дж. Бао, Ю. Чжао, Д. Хо, М. Чен, Ю. Ци, М. Ян, Х. Фа и К. Хоу, электрохимический иммуноанализ сэндвич-типа для сверхчувствительного обнаружения немелкоклеточного легкого биомаркер рака CYFRA21-1, Bioelectrochemistry, vol. 120. С. 183–189. (2018).
DOI: 10.1016 / j.bioelechem.2017.11.003
[9]
Т. T. N. Lien, Y. Takamura, E. Tamiya и M. C. Vestergaard, Модифицированный электрод с трафаретной печатью для разработки высокочувствительного импедиметрического иммуносенсора без меток для обнаружения бета-амилоидных пептидов, Anal. Чим. Acta, т. 892, с.69–76, (2015).
T. N. Lien, Y. Takamura, E. Tamiya и M. C. Vestergaard, Модифицированный электрод с трафаретной печатью для разработки высокочувствительного импедиметрического иммуносенсора без меток для обнаружения бета-амилоидных пептидов, Anal. Чим. Acta, т. 892, с.69–76, (2015).
DOI: 10.1016 / j.aca.2015.08.036
[10]
Р.Монтес, Ф. Сеспедес и М. Баеза, Высокочувствительный электрохимический иммуносенсор для обнаружения IgG на основе оптимизированных жестких биокомпозитов, Biosens. Биоэлектрон., Т. 78, с. 505–512, (2016).
505–512, (2016).
DOI: 10.1016 / j.bios.2015.12.059
[11] Дж.Ким, П. Зейдлер, Л. С. Ван и С. Филл, Journal of Colloid and Interface Science Formation, структура и реакционная способность органических пленок с концевыми аминогруппами на кремниевых подложках, J. Colloid Interface Sci., Vol. 329, нет. 1, с.114–119, (2009).
DOI: 10.1016 / j.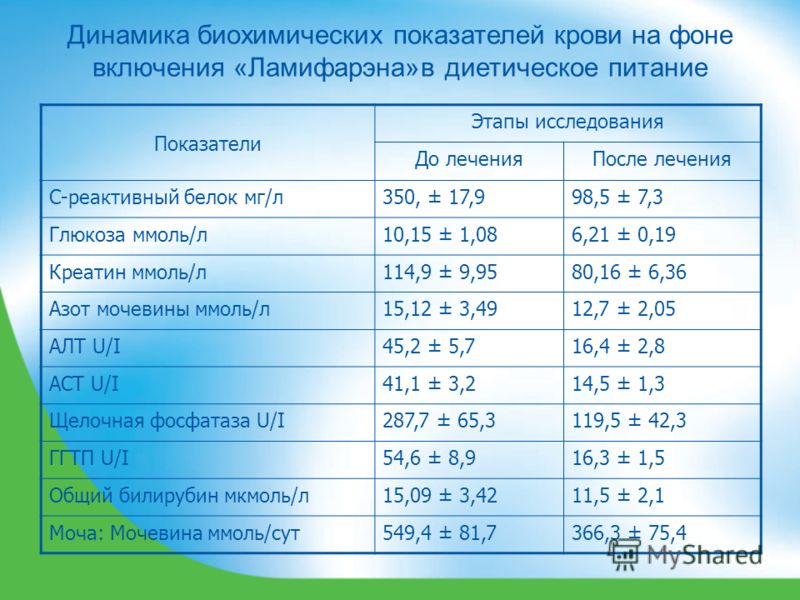 jcis.2008.09.031
jcis.2008.09.031
[12] Н.Сива, К. Гунда, М. Сингх, Л. Норман, К. Каур и С. К. Митра, Оптимизация прикладной науки о поверхности и характеристика иммобилизации биомолекул на кремниевых субстратах с использованием (3-аминопропил) триэтоксисилана (APTES) и линкера глутаральдегида, Прил. . Серфинг. Sci., Т. 305, с. 522–530, (2014).
DOI: 10.1016 / j.apsusc.2014.03.130
.




 , Нитти, П., Каваллуцци, М. М., Лентини, Г., Денора, Н.,… и Маццокка, А.(2019). Новые антагонисты рецептора 6 лизофосфатидной кислоты подавляют рост гепатоцеллюлярной карциномы, влияя на функцию митохондрий. Журнал молекулярной медицины , 1-13.
, Нитти, П., Каваллуцци, М. М., Лентини, Г., Денора, Н.,… и Маццокка, А.(2019). Новые антагонисты рецептора 6 лизофосфатидной кислоты подавляют рост гепатоцеллюлярной карциномы, влияя на функцию митохондрий. Журнал молекулярной медицины , 1-13.