Нитроглицерин — это… Что такое Нитроглицерин?
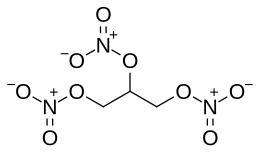
Нитроглицерин (глицеринтринитрат, тринитроглицерин, тринитрин, НГЦ) — сложный эфир глицерина и азотной кислоты. Исторически сложившееся название «нитроглицерин» с точки зрения современной номенклатуры является несколько некорректным, поскольку нитроглицерин является нитроэфиром, а не «классическим» нитросоединением. Широко известен благодаря своим взрывчатым (и в некоторой степени лекарственным) свойствам. Химическая формула O2NOCH2CH(ONO2)CH2ONO2. Впервые синтезирован итальянским химиком Асканьо Собреро в 1847 году, первоначально был назван «пироглицерин» (итал. pyroglycerina).
Согласно номенклатуре IUPAC именуется 1,2,3-тринитроксипропан.
Получение
В лаборатории получают этерификацией глицерина смесью концентрированной азотной и серной кислот. Кислоты и глицерин должны быть очищены от примесей. Для этерификации предварительно при постоянном перемешивании и охлаждении смешивают кислоты, изготавливая таким образом нитрующую смесь, и добавляют по каплям глицерин при постоянном охлаждении колбы льдом и контроле температуры.
Описание реакции: 2H2SO4 + HNO3 ↔ H2SO4 · H2O + NO2 HSO4 Реакция равновесна с сильным смещением равновесия влево.
Затем реакционную смесь кислот и глицерина выдерживают непродолжительное время, при охлаждении льдом. Жидкость расслаивается на два слоя. Нитроглицерин легче нитрующей смеси и всплывает в виде мутного слоя.
Описание реакции: HOCH2-CHOH-CH2OH + 3NO2HSO4 → CHONO2(CH2ONO2)2 + 3H2SO4
Нитроглицерин отделяют от нитрующей смеси, и промывают содовым раствором до полной нейтрализации кислот. В промышленности получают непрерывным нитрованием глицерина нитрующей смесью в специальных инжекторах. В связи с возможной опасностью взрыва, НГЦ не хранят, а сразу перерабатывают в бездымный порох или взрывчатые вещества. Подробное описание лабораторного получения нитроглицерина, техника безопасности при работе с ним и занимательные эксперименты приведены в статье Нитроглицерин (Химия и Химики № 6 2011) На настоящий момент это наиболее подробная и достоверная информация о нитроглицерине в сети.
Физико-химические свойства
Сложный эфир глицерина и азотной кислоты. Прозрачная вязкая нелетучая жидкость (как масло), склонная к переохлаждению. Смешивается с органическими растворителями, почти нерастворим в воде[1] (0.13 % при 20 °C, 0,2 % при 50 °C, 0,35 % при 80 °C, по другим данным[источник не указан 1317 дней] 1,8 % при 20 °C и 2,5 % при 50 °C). При нагревании с водой до 80 °C гидролизуется. Быстро разлагается щёлочами.
Токсичен, всасывается через кожу, вызывает головную боль. Очень чувствителен к удару, трению, высоким температурам, резкому нагреву и т. п. Чувствительность к удару для груза 2 кг — 4 см (гремучая ртуть — 2 см, тротил — 100 см). Весьма опасен в обращении. При осторожном поджигании в малых количествах неустойчиво горит синим пламенем. Температура кристаллизации 13,5 °C (стабильная модификация, лабильная кристаллизуется при 2,8 °C). Кристаллизуется со значительным увеличением чувствительности к трению. При нагревании до 50 °C начинает медленно разлагаться и становится ещё более взрывоопасным. Температура вспышки около 200 °C. Теплота взрыва 6,535 МДж/кг. Температура взрыва 4110 °C. Несмотря на высокую чувствительность, восприимчивость к детонации довольно низка — для полного взрыва необходим капсюль-детонатор № 8. Скорость детонации 7650 м/с. 8000-8200 м/c — в стальной трубе диаметром 35 мм, инициирован с помощью детонатора № 8. В обычных условиях жидкий НГЦ часто детонирует в низкоскоростном режиме 1100—2000 м/с. Плотность 1,595 г/см³, в твёрдом виде — 1,735 г/см³. Твёрдый нитроглицерин менее чувствителен к удару, но более к трению, поэтому очень опасен. Объем продуктов взрыва 715 л/кг. Фугасность и бризантность сильно зависят от способа инициирования, при использовании слабого детонатора мощность сравнительно невелика. Фугасность в песке — 390 мл, в воде — 590 мл (кристаллического несколько выше), работоспособность (фугасность) в свинцовой бомбе 550 см³. Применяется как компонент некоторых жидких ВВ, динамитов и главным образом бездымных порохов (пластификатор — нитроцеллюлоза). Кроме того, в малых концентрациях применяется в медицине.
Применение
Я пью его в мельчайших дозах,
На сахар капаю раствор,
А он способен бросить в воздух
Любую из ближайших гор.
Он, растворенный в желатине
И превращенный в динамит,
В далекой золотой долине,
Взрывая скалы, загремит.
И содрогнулся шнур бикфордов,
Сработал капсюля запал,
И он разламывает твердый,
Несокрушимый минерал.
Сердечной боли он – причина,
И он один лекарство мне –
Так разъяснила медицина
В фармакологии
Нитроглицерин относится к категории веществ, называемых вазодилататорами — средствам, понижающим кровяное давление, расслабляет гладкую мускулатуру кровеносных сосудов, бронхов, желчных и мочевых путей, желудочно-кишечного тракта. Основное применение имеет при стенокардии, главным образом для купирования острых приступов спазмов коронарных сосудов. Для предупреждения приступов он мало пригоден из-за кратковременности действия. Иногда применяется при эмболии центральной артерии сетчатки, а также функциональных холицистопатиях.
Применяется в виде таблеток по 0,5 мг для помещения под язык; а также в 1 % спиртовом растворе.
Во взрывотехнике
Нитроглицерин широко применялся во взрывотехнике. В чистом виде он очень неустойчив и опасен. После открытия Собреро нитроглицерина, в 1853 г. русский химик Зинин предложил использовать его в технических целях. Спустя 10 лет инженер Петрушевский первым начал производить его в больших количествах, под его руководством нитроглицерин был применён в горном деле в 1867 г. Альфред Нобель в 1863 г. изобрёл инжектор-смеситель для производства нитроглицерина и капсюль-детонатор, а в 1867 г. — динамит, получаемый смешением нитроглицерина с кизельгуром (диатомитом, инфузорной землёй).
В литературе и кино
Герои приключенческого романа «Таинственный остров» (1874) Жюль Верна использует нитроглицерин для подрыва гранитной скалы. Автор подробно описывает процесс получения нитроглицерина из природных веществ, обнаруженных на острове (хотя Жюль Верн намеренно опустил один из важных этапов синтеза). Писатель характеризует это вещество следующим образом[3]:
Действительно, это был нитроглицерин — ужасное вещество, обладающее в десять раз большей взрывчатой силой, чем порох, и причинившее уже так много несчастий. Правда, с тех пор как нитроглицерин научились превращать в динамит, смешивая его с каким-нибудь пористым веществом — например, глиной или сахаром, способным удержать опасную жидкость, им можно пользоваться с меньшим риском. Но в то время, когда колонисты действовали на острове Линкольна, динамит ещё не был известен.
Основная часть сюжета фильма «Плата за страх» (1953) заключается в процессе перевозки нитроглицерина на грузовиках.
В романе Чака Паланика «Бойцовский клуб» (1996) и одноимённом фильме (1999) главный герой получает нитроглицерин путём плавления мыла и добавления глицерина в азотную кислоту.
Возьмите одну часть 98%-ной дымящей азотной кислоты, и смешайте с тремя частями концентрированной серной кислоты. Делать это надо на ледяной бане. Затем добавляйте глицерин по капле из глазной пипетки. Вы получили нитроглицерин.
— Ч. Паланик «Бойцовский клуб»
В фильме «Вертикальный предел» (2000) есть эпизод с самопроизвольной детонацией жидкого нитроглицерина от прямого воздействия солнечных лучей.
В сериале Побег сезон 2 серия 9 в ботаническом саду находят ящик с ампулами нитроглицерина, который спрятал Майкл Скофилд.
В фильме «Легенда Зорро» (2005) главный злодей демонстрирует нитроглицерин заказчикам, также финальная сцена фильма происходит в поезде, перевозящем нитроглицерин.
В многосерийном фильме «Террористка Иванова» Полина Иванова хочет отомстить следователю за смерть мужа, взорвав отделение милиции при помощи нитроглицерина.
В фильме Серджио Леоне «За пригоршню динамита» один из главных персонажей — ирландский террорист (исполняемый Кобурном) обвешан динамитными шашками и бутылями нитроглицерина. В начале фильма он демонстрирует взрывчатые свойства последнего, капая каплю на камень.
Примечания
См. также
Ссылки
 | В этой статье не хватает ссылок на источники информации. Информация должна быть проверяема, иначе она может быть поставлена под сомнение и удалена. Эта отметка установлена 14 мая 2011. |
Шаблон:АТХ код C01
Нитроглицерин — Википедия
| Нитроглицерин | |
| Общие | |
|---|---|
| Систематическое наименование | 1,2,3-тринитроксипропан |
| Сокращения | НГЦ |
| Традиционные названия | нитроглицерин |
| Хим. формула | C3H5N3O9 |
| Физические свойства | |
| Состояние | тяжёлая, маслянистая бесцветная жидкость |
| Молярная масса | 227,0865 ± 0,0061 г/моль |
| Плотность | 1,595 г/см³ |
| Термические свойства | |
| Т. плав. | 13 °C |
| Т. кип. | 160 °C |
| 140 ± 1 °F[1] и 122 ± 1 °F[1] | |
| Т. свспл. | 270 °C |
| Давление пара | 0,0003 ± 0,0001 мм рт.ст.[1] |
| Химические свойства | |
| Растворимость в воде | 0,138 г/100 мл |
| Классификация | |
| Рег. номер CAS | 55-63-0 |
| PubChem | 4510 |
| Рег. номер EINECS | 200-240-8 |
| SMILES | |
| InChI | |
| RTECS | QX2100000 |
| ChEBI | 28787 |
| Номер ООН | 0143, 0144, 1204, 3064 и 3319 |
| ChemSpider | 4354 |
| Безопасность | |
| ПДК | 2 мг/м3 |
| ЛД50 | 105 мг/кг (крысы, перорально), 1450 мг/кг (морские свинки, перорально), 210 мг/кг (LD100 человек, перорально) |
| Токсичность | высокотоксичен, взрывоопасен, особенно опасны его пары, при втирании в кожу вызывает сильное и продолжительное отравление. |
| NFPA 704 | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Нитроглицерин (1,2,3-тринитроксипропан; также глицеринтринитрат, тринитроглицерин, тринитрин, НГЦ) — органическое соединение, сложный эфир глицерина и азотной кислоты.
Исторически сложившееся русское название «нитроглицерин» с точки зрения современной номенклатуры является некорректным, поскольку нитроглицерин является не нитросоединением, а нитроэфиром (эфиром азотной кислоты). В терминах номенклатуры IUPAC имеет наименование 1,2,3-тринитроксипропан. Химическая формула O2NOCH2CH(ONO2)CH2ONO2.
Широко известен благодаря своим взрывчатым и лекарственным свойствам. Впервые синтезирован итальянским химиком Асканьо Собреро в 1847 году, первоначально был назван «пироглицерин» (итал. pyroglycerina).
Получение
В лаборатории получают этерификацией глицерина смесью концентрированной азотной и серной кислот. Кислоты и глицерин должны быть очищены от примесей. Для обеспечения безопасности процесса и хорошего выхода по глицерину кислотная смесь должна иметь малое содержание воды. Процесс начинают со смешения олеума (или лабораторной 98%-й серной кислоты) и меланжа. Смешение кислот производят при охлаждении для предотвращения термического разложения концентрированной азотной кислоты. Глицерин вносят из капельной воронки при интенсивном перемешивании и постоянном охлаждении колбы льдом (можно с добавлением пищевой соли). Контроль температуры осуществляют ртутным или электронным термометром. Процесс смешения кислот можно выразить в упрощенном виде следующей реакцией[2]:
- 2h3SO4+HNO3→h3SO4⋅h3O+NO2HSO4{\displaystyle {\mathsf {2H_{2}SO_{4}+HNO_{3}\rightarrow H_{2}SO_{4}\cdot H_{2}O+NO_{2}HSO_{4}}}}
Реакция равновесная с сильным смещением равновесия влево. Серная кислота необходима для связывания воды в прочные сольваты и для протонирования молекул азотной кислоты с целью образования катионов нитрозония NO2+. Положительный заряд делокализован по всем электронным орбиталям катиона, что обеспечивает его устойчивость.
Затем реакционную смесь кислот и глицерина выдерживают непродолжительное время при охлаждении льдом. Жидкость расслаивается на два слоя. Нитроглицерин легче нитрующей смеси и всплывает в виде мутного слоя. Процесс этерификации проводят при температурах в районе 0˚С. При более низких температурах скорость процесса мала, при более высоких температурах процесс становится опасным и резко уменьшается выход продукта. Превышение температуры выше 25 °С грозит взрывом, поэтому синтез должен проводиться при строжайшем температурном контроле. Уравнение этерификации глицерина азотной кислотой в присутствии серной кислоты можно упрощенно записать следующим образом:
- Ch3OH-CH(OH)-Ch3OH+3NO2HSO4→Ch3ONO2-CHONO2-Ch3ONO2{\displaystyle {\mathsf {CH_{2}OH{\text{-}}CH(OH){\text{-}}CH_{2}OH+3NO_{2}HSO_{4}\rightarrow CH_{2}ONO_{2}{\text{-}}CHONO_{2}{\text{-}}CH_{2}ONO_{2}}}}
Верхний слой из реакционного стакана (колбы) сразу сливают в большой объём холодной воды при перемешивании. Температура воды должна быть 6—15 °C, объём — не менее, чем в 100—110 раз превосходить объём полученного НГЦ. Кислоты растворяются в воде, а нитроглицерин оседает на дно ёмкости в виде мутных капель бежевого цвета. Воду сливают и заменяют новой порцией холодной воды с добавлением небольшого количества соды (1—3 % по массе). Окончательную промывку производят небольшим количеством содового раствора до нейтральной реакции водной фазы. Для получения максимально чистого нитроглицерина (например, для исследовательских целей) производят последнюю очистку промывкой водой, что позволяет отделить остатки соды и нитрата натрия. Недостатки лабораторного получения НГЦ во многом связаны с необходимостью использования большого объёма промывных вод, что резко снижает выход продукта из-за безвозвратных потерь НГЦ на растворимость в воде, на практике эти потери могут достигать 30—50 % от всего полученного продукта[3]. Большой объём промывных вод, напротив, позволяет максимально быстро и безопасно промыть НГЦ. Недостаточная промывка НГЦ от кислотных примесей и продуктов неполной этерификации приводит к очень низкой устойчивости продукции (пороха, ТРТ, БВВ и пр.) и делает НГЦ крайне опасным.
В промышленности получают непрерывным нитрованием глицерина нитрующей смесью в специальных инжекторах. Полученную смесь сразу разделяют в сепараторах (преимущественно системы Биацци[4]). После промывки нитроглицерин используют в виде водной эмульсии, что упрощает и делает более безопасным его транспортировку между цехами. В связи с возможной опасностью взрыва НГЦ не хранят, а сразу перерабатывают в бездымный порох или взрывчатые вещества.
Большую часть производственных помещений предприятия, производящего НГЦ, занимают цеха по очистке и переработке жидких стоков и других отходов производства. Наиболее перспективные технологии данного направления основаны на замкнутых циклах использования оборотных сред (промывная вода, отработанная кислотная смесь и др.)[3].
Физико-химические свойства
Сложный эфир глицерина и азотной кислоты. Прозрачная вязкая нелетучая жидкость (как масло), склонная к переохлаждению. Смешивается с органическими растворителями, почти нерастворим в воде[5] (0,13 % при 20 °C, 0,2 % при 50 °C, 0,35 % при 80 °C). При нагревании с водой до 80 °C гидролизуется. Быстро разлагается щёлочами.
Токсичен, всасывается через кожу, вызывает головную боль. Очень чувствителен к удару, трению, высоким температурам, резкому нагреву и т. п. Чувствительность к удару для груза 2 кг — 4 см (гремучая ртуть — 2 см, тротил — 100 см). Весьма опасен в обращении. При осторожном поджигании в малых количествах неустойчиво горит синим пламенем. Температура кристаллизации — 13,5 °C (стабильная модификация, лабильная кристаллизуется при 2,8 °C). Кристаллизуется со значительным увеличением чувствительности к трению. При нагревании до 50 °C начинает медленно разлагаться и становится ещё более взрывоопасным. Температура вспышки — около 200 °C. Теплота взрыва — 6,535 МДж/кг. Температура взрыва — 4110 °C. Несмотря на высокую чувствительность, восприимчивость к детонации довольно низка — для полного взрыва необходим капсюль-детонатор № 8. Скорость детонации — 7650 м/с. 8000-8200 м/c — в стальной трубе диаметром 35 мм, инициирован с помощью детонатора № 8. В обычных условиях жидкий НГЦ часто детонирует в низкоскоростном режиме 1100—2000 м/с. Плотность — 1,595 г/см³, в твёрдом виде — 1,735 г/см³. Твёрдый нитроглицерин менее чувствителен к удару, но более — к трению, поэтому очень опасен. Объём продуктов взрыва — 715 л/кг. Фугасность и бризантность сильно зависят от способа инициирования, при использовании слабого детонатора мощность сравнительно невелика. Фугасность в песке — 390 мл, в воде — 590 мл (кристаллического несколько выше), работоспособность (фугасность) в свинцовой бомбе — 550 см³. Применяется как компонент некоторых жидких ВВ, динамитов и главным образом бездымных порохов (для пластификации нитратов целлюлозы). Кроме того, в малых концентрациях применяется в медицине.
Применение
Я пью его в мельчайших дозах,
На сахар капаю раствор,
А он способен бросить в воздух
Любую из ближайших гор.
Он, растворенный в желатине
И превращенный в динамит,
В далекой золотой долине,
Взрывая скалы, загремит.
И содрогнулся шнур бикфордов,
Сработал капсюля запал,
И он разламывает твердый,
Несокрушимый минерал.
Сердечной боли он – причина,
И он один лекарство мне –
Так разъяснила медицина
В холодной горной стороне.
В фармакологии
Нитроглицерин относится к категории веществ, называемых вазодилататорами — средствам, понижающим кровяное давление, расслабляет гладкую мускулатуру кровеносных сосудов, бронхов, желчных и мочевых путей, желудочно-кишечного тракта. Основное применение имеет при стенокардии, главным образом для купирования острых приступов спазмов коронарных сосудов. Для предупреждения приступов он мало пригоден из-за кратковременности действия. Иногда применяется при эмболии центральной артерии сетчатки, а также функциональных холецистопатиях.
Применяется в виде таблеток по 0,5 мг для помещения под язык; а также в 1%-м спиртовом растворе.
Во взрывотехнике
Нитроглицерин широко применялся во взрывотехнике. В чистом виде он очень неустойчив и опасен. После открытия Собреро нитроглицерина, в 1853 году русский химик Зинин предложил использовать его в технических целях. Спустя 10 лет инженер Петрушевский первым начал производить его в больших количествах, под его руководством нитроглицерин был применён в горном деле в 1867 году. Альфред Нобель в 1863 году изобрёл инжектор-смеситель для производства нитроглицерина и капсюль-детонатор, а в 1867 году — динамит, получаемый смешением нитроглицерина с кизельгуром (диатомитом, инфузорной землёй).
В литературе и кино
- Герой приключенческого романа «Таинственный остров» (1874) Жюль Верна использует нитроглицерин для подрыва гранитной скалы. Автор подробно описывает процесс получения нитроглицерина из природных веществ, обнаруженных на острове (хотя Жюль Верн намеренно опустил один из важных этапов синтеза). Писатель характеризует это вещество следующим образом[7]:
Действительно, это был нитроглицерин — ужасное вещество, обладающее в десять раз большей взрывчатой силой, чем порох, и причинившее уже так много несчастий. Правда, с тех пор как нитроглицерин научились превращать в динамит, смешивая его с каким-нибудь пористым веществом — например, глиной или сахаром, способным удержать опасную жидкость, им можно пользоваться с меньшим риском. Но в то время, когда колонисты действовали на острове Линкольна, динамит ещё не был известен.
- Основная часть сюжета фильма «Плата за страх» (1953) заключается в процессе перевозки нитроглицерина на грузовиках.
Возьмите одну часть 98%-й дымящей азотной кислоты и смешайте с тремя частями концентрированной серной кислоты. Делать это надо на ледяной бане. Затем добавляйте глицерин по капле из глазной пипетки. Вы получили нитроглицерин.
- В сериале «Побег» сезон 2 серия 9 в ботаническом саду находят ящик с ампулами нитроглицерина, который спрятал Майкл Скофилд.
- В сериале «Остаться в живых» сезон 1 серии 24-25 на корабле «Черная скала» находят динамит (нитроглицерин, стабилизированный пористым веществом)
- В фильме «Легенда Зорро» (2005) главный злодей демонстрирует нитроглицерин заказчикам, также финальная сцена фильма происходит в поезде, перевозящем нитроглицерин.
- В многосерийном фильме «Террористка Иванова» Полина Иванова хочет отомстить следователю за смерть мужа, взорвав отделение милиции при помощи нитроглицерина.
- В фильме Серджио Леоне «За пригоршню динамита» один из главных персонажей — ирландский террорист (Джеймс Коберн) обвешан динамитными шашками и бутылями нитроглицерина. В начале фильма он демонстрирует взрывчатые свойства последнего, капая каплю на камень.
Токсичность нитроглицерина
Нитроглицерин высокотоксичен. Токсичность нитроглицерина объясняется тем, что он легко и быстро всасывается через кожу и слизистые оболочки (в особенности этому способствует слизистая ротовой полости, дыхательных путей и лёгких) в кровь[8]. Токсичной дозой для человека считается 25—50 мг. Доза в 50—75 мг вызывает сильное отравление: происходит понижение АД, появляется сильная головная боль, головокружение, покраснение лица, сильное жжение в горле и под «ложечкой», возможна одышка, обморок, нередко наблюдается тошнота, рвота, колики, светобоязнь, недолговременные и проходящие расстройства зрения, параличи (особенно глазных мышц), шум в ушах, биение артерий, замедление пульса, синюшность, похолодание конечностей. Хроническое действие нитроглицерина (хроническое отравление организма нитроглицерином наблюдалось у работников, производящих динамит), вдыхание, а также приём внутрь больших доз (100—150 мг/кг) может привести к летальному исходу. LD100 для человека составляет 210 мг/кг, смерть наступает в течение 2 минут. Нитроглицерин также может вызывать сильное раздражение кожи. У работающих с динамитом развиваются упорные язвы под ногтями и на концах пальцев, высыпания на подошвах и между пальцами рук, сухость кожи и трещины. Втирание в кожу 1 капли нитроглицерина вызвало общее отравление, длившееся 10 часов[8]. ПДК для рабочей зоны составляет 2 мг/м3[5].
Примечания
Ссылки
Нитроглицерин — Википедия. Что такое Нитроглицерин
| Нитроглицерин | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | 1,2,3-тринитроксипропан |
| Сокращения | НГЦ |
| Традиционные названия | нитроглицерин |
| Хим. формула | C3H5N3O9 |
| Физические свойства | |
| Состояние | тяжёлая, маслянистая бесцветная жидкость |
| Молярная масса | 227,0865 ± 0,0061 г/моль |
| Плотность | 1,595 г/см³ |
| Термические свойства | |
| Т. плав. | 13 °C |
| Т. кип. | 160 °C |
| 140 ± 1 °F[1] и 122 ± 1 °F[1] | |
| Т. свспл. | 270 °C |
| Давление пара | 0,0003 ± 0,0001 мм рт.ст.[1] |
| Химические свойства | |
| Растворимость в воде | 0,138 г/100 мл |
| Классификация | |
| Рег. номер CAS | 55-63-0 |
| PubChem | 4510 |
| Рег. номер EINECS | 200-240-8 |
| SMILES | |
| InChI | |
| RTECS | QX2100000 |
| ChEBI | 28787 |
| Номер ООН | 0143, 0144, 1204, 3064 и 3319 |
| ChemSpider | 4354 |
| Безопасность | |
| ПДК | 2 мг/м3 |
| ЛД50 | 105 мг/кг (крысы, перорально), 115 мг/кг (мыши, перорально), 1450 мг/кг (морские свинки, перорально), 210 мг/кг (LD100 человек, перорально) |
| Токсичность | высокотоксичен, взрывоопасен, особенно опасны его пары, при втирании в кожу вызывает сильное и продолжительное отравление.     |
| NFPA 704 |  |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Нитроглицерин (1,2,3-тринитроксипропан; также глицеринтринитрат, тринитроглицерин, тринитрин, НГЦ) — органическое соединение, сложный эфир глицерина и азотной кислоты.
Исторически сложившееся русское название «нитроглицерин» с точки зрения современной номенклатуры является некорректным, поскольку нитроглицерин является не нитросоединением, а нитроэфиром (эфиром азотной кислоты). В терминах номенклатуры IUPAC имеет наименование 1,2,3-тринитроксипропан. Химическая формула O2NOCH2CH(ONO2)CH2ONO2.
Широко известен благодаря своим взрывчатым и лекарственным свойствам. Впервые синтезирован итальянским химиком Асканьо Собреро в 1847 году, первоначально был назван «пироглицерин» (итал. pyroglycerina).
Получение
В лаборатории получают этерификацией глицерина смесью концентрированной азотной и серной кислот. Кислоты и глицерин должны быть очищены от примесей. Для обеспечения безопасности процесса и хорошего выхода по глицерину кислотная смесь должна иметь малое содержание воды. Процесс начинают со смешения олеума (или лабораторной 98%-й серной кислоты) и меланжа. Смешение кислот производят при охлаждении для предотвращения термического разложения концентрированной азотной кислоты. Глицерин вносят из капельной воронки при интенсивном перемешивании и постоянном охлаждении колбы льдом (можно с добавлением пищевой соли). Контроль температуры осуществляют ртутным или электронным термометром. Процесс смешения кислот можно выразить в упрощенном виде следующей реакцией[2]:
- 2h3SO4+HNO3→h3SO4⋅h3O+NO2HSO4{\displaystyle {\mathsf {2H_{2}SO_{4}+HNO_{3}\rightarrow H_{2}SO_{4}\cdot H_{2}O+NO_{2}HSO_{4}}}}
Реакция равновесная с сильным смещением равновесия влево. Серная кислота необходима для связывания воды в прочные сольваты и для протонирования молекул азотной кислоты с целью образования катионов нитрозония NO2+. Положительный заряд делокализован по всем электронным орбиталям катиона, что обеспечивает его устойчивость.
Затем реакционную смесь кислот и глицерина выдерживают непродолжительное время при охлаждении льдом. Жидкость расслаивается на два слоя. Нитроглицерин легче нитрующей смеси и всплывает в виде мутного слоя. Процесс этерификации проводят при температурах в районе 0˚С. При более низких температурах скорость процесса мала, при более высоких температурах процесс становится опасным и резко уменьшается выход продукта. Превышение температуры выше 25 °С грозит взрывом, поэтому синтез должен проводиться при строжайшем температурном контроле. Уравнение этерификации глицерина азотной кислотой в присутствии серной кислоты можно упрощенно записать следующим образом:
- Ch3OH-CH(OH)-Ch3OH+3NO2HSO4→Ch3ONO2-CHONO2-Ch3ONO2{\displaystyle {\mathsf {CH_{2}OH{\text{-}}CH(OH){\text{-}}CH_{2}OH+3NO_{2}HSO_{4}\rightarrow CH_{2}ONO_{2}{\text{-}}CHONO_{2}{\text{-}}CH_{2}ONO_{2}}}}
Верхний слой из реакционного стакана (колбы) сразу сливают в большой объём холодной воды при перемешивании. Температура воды должна быть 6—15 °C, объём — не менее, чем в 100—110 раз превосходить объём полученного НГЦ. Кислоты растворяются в воде, а нитроглицерин оседает на дно ёмкости в виде мутных капель бежевого цвета. Воду сливают и заменяют новой порцией холодной воды с добавлением небольшого количества соды (1—3 % по массе). Окончательную промывку производят небольшим количеством содового раствора до нейтральной реакции водной фазы. Для получения максимально чистого нитроглицерина (например, для исследовательских целей) производят последнюю очистку промывкой водой, что позволяет отделить остатки соды и нитрата натрия. Недостатки лабораторного получения НГЦ во многом связаны с необходимостью использования большого объёма промывных вод, что резко снижает выход продукта из-за безвозвратных потерь НГЦ на растворимость в воде, на практике эти потери могут достигать 30—50 % от всего полученного продукта[3]. Большой объём промывных вод, напротив, позволяет максимально быстро и безопасно промыть НГЦ. Недостаточная промывка НГЦ от кислотных примесей и продуктов неполной этерификации приводит к очень низкой устойчивости продукции (пороха, ТРТ, БВВ и пр.) и делает НГЦ крайне опасным.
В промышленности получают непрерывным нитрованием глицерина нитрующей смесью в специальных инжекторах. Полученную смесь сразу разделяют в сепараторах (преимущественно системы Биацци[4]). После промывки нитроглицерин используют в виде водной эмульсии, что упрощает и делает более безопасным его транспортировку между цехами. В связи с возможной опасностью взрыва НГЦ не хранят, а сразу перерабатывают в бездымный порох или взрывчатые вещества.
Большую часть производственных помещений предприятия, производящего НГЦ, занимают цеха по очистке и переработке жидких стоков и других отходов производства. Наиболее перспективные технологии данного направления основаны на замкнутых циклах использования оборотных сред (промывная вода, отработанная кислотная смесь и др.)[3].
Физико-химические свойства
Сложный эфир глицерина и азотной кислоты. Прозрачная вязкая нелетучая жидкость (как масло), склонная к переохлаждению. Смешивается с органическими растворителями, почти нерастворим в воде[5] (0,13 % при 20 °C, 0,2 % при 50 °C, 0,35 % при 80 °C). При нагревании с водой до 80 °C гидролизуется. Быстро разлагается щёлочами.
Токсичен, всасывается через кожу, вызывает головную боль. Очень чувствителен к удару, трению, высоким температурам, резкому нагреву и т. п. Чувствительность к удару для груза 2 кг — 4 см (гремучая ртуть — 2 см, тротил — 100 см). Весьма опасен в обращении. При осторожном поджигании в малых количествах неустойчиво горит синим пламенем. Температура кристаллизации — 13,5 °C (стабильная модификация, лабильная кристаллизуется при 2,8 °C). Кристаллизуется со значительным увеличением чувствительности к трению. При нагревании до 50 °C начинает медленно разлагаться и становится ещё более взрывоопасным. Температура вспышки — около 200 °C. Теплота взрыва — 6,535 МДж/кг. Температура взрыва — 4110 °C. Несмотря на высокую чувствительность, восприимчивость к детонации довольно низка — для полного взрыва необходим капсюль-детонатор № 8. Скорость детонации — 7650 м/с. 8000-8200 м/c — в стальной трубе диаметром 35 мм, инициирован с помощью детонатора № 8. В обычных условиях жидкий НГЦ часто детонирует в низкоскоростном режиме 1100—2000 м/с. Плотность — 1,595 г/см³, в твёрдом виде — 1,735 г/см³. Твёрдый нитроглицерин менее чувствителен к удару, но более — к трению, поэтому очень опасен. Объём продуктов взрыва — 715 л/кг. Фугасность и бризантность сильно зависят от способа инициирования, при использовании слабого детонатора мощность сравнительно невелика. Фугасность в песке — 390 мл, в воде — 590 мл (кристаллического несколько выше), работоспособность (фугасность) в свинцовой бомбе — 550 см³. Применяется как компонент некоторых жидких ВВ, динамитов и главным образом бездымных порохов (для пластификации нитратов целлюлозы). Кроме того, в малых концентрациях применяется в медицине.
Применение
Я пью его в мельчайших дозах,
На сахар капаю раствор,
А он способен бросить в воздух
Любую из ближайших гор.
Он, растворенный в желатине
И превращенный в динамит,
В далекой золотой долине,
Взрывая скалы, загремит.
И содрогнулся шнур бикфордов,
Сработал капсюля запал,
И он разламывает твердый,
Несокрушимый минерал.
Сердечной боли он – причина,
И он один лекарство мне –
Так разъяснила медицина
В холодной горной стороне.
В фармакологии
Нитроглицерин относится к категории веществ, называемых вазодилататорами — средствам, понижающим кровяное давление, расслабляет гладкую мускулатуру кровеносных сосудов, бронхов, желчных и мочевых путей, желудочно-кишечного тракта. Основное применение имеет при стенокардии, главным образом для купирования острых приступов спазмов коронарных сосудов. Для предупреждения приступов он мало пригоден из-за кратковременности действия. Иногда применяется при эмболии центральной артерии сетчатки, а также функциональных холецистопатиях.
Применяется в виде таблеток по 0,5 мг для помещения под язык; а также в 1%-м спиртовом растворе.
Во взрывотехнике
Нитроглицерин широко применялся во взрывотехнике. В чистом виде он очень неустойчив и опасен. После открытия Собреро нитроглицерина, в 1853 году русский химик Зинин предложил использовать его в технических целях. Спустя 10 лет инженер Петрушевский первым начал производить его в больших количествах, под его руководством нитроглицерин был применён в горном деле в 1867 году. Альфред Нобель в 1863 году изобрёл инжектор-смеситель для производства нитроглицерина и капсюль-детонатор, а в 1867 году — динамит, получаемый смешением нитроглицерина с кизельгуром (диатомитом, инфузорной землёй).
В литературе и кино
- Герой приключенческого романа «Таинственный остров» (1874) Жюль Верна использует нитроглицерин для подрыва гранитной скалы. Автор подробно описывает процесс получения нитроглицерина из природных веществ, обнаруженных на острове (хотя Жюль Верн намеренно опустил один из важных этапов синтеза). Писатель характеризует это вещество следующим образом[7]:
Действительно, это был нитроглицерин — ужасное вещество, обладающее в десять раз большей взрывчатой силой, чем порох, и причинившее уже так много несчастий. Правда, с тех пор как нитроглицерин научились превращать в динамит, смешивая его с каким-нибудь пористым веществом — например, глиной или сахаром, способным удержать опасную жидкость, им можно пользоваться с меньшим риском. Но в то время, когда колонисты действовали на острове Линкольна, динамит ещё не был известен.
- Основная часть сюжета фильма «Плата за страх» (1953) заключается в процессе перевозки нитроглицерина на грузовиках.
Возьмите одну часть 98%-й дымящей азотной кислоты и смешайте с тремя частями концентрированной серной кислоты. Делать это надо на ледяной бане. Затем добавляйте глицерин по капле из глазной пипетки. Вы получили нитроглицерин.
- В сериале «Побег» сезон 2 серия 9 в ботаническом саду находят ящик с ампулами нитроглицерина, который спрятал Майкл Скофилд.
- В сериале «Остаться в живых» сезон 1 серии 24-25 на корабле «Черная скала» находят динамит (нитроглицерин, стабилизированный пористым веществом)
- В фильме «Легенда Зорро» (2005) главный злодей демонстрирует нитроглицерин заказчикам, также финальная сцена фильма происходит в поезде, перевозящем нитроглицерин.
- В многосерийном фильме «Террористка Иванова» Полина Иванова хочет отомстить следователю за смерть мужа, взорвав отделение милиции при помощи нитроглицерина.
- В фильме Серджио Леоне «За пригоршню динамита» один из главных персонажей — ирландский террорист (Джеймс Коберн) обвешан динамитными шашками и бутылями нитроглицерина. В начале фильма он демонстрирует взрывчатые свойства последнего, капая каплю на камень.
Токсичность нитроглицерина
Нитроглицерин высокотоксичен. Токсичность нитроглицерина объясняется тем, что он легко и быстро всасывается через кожу и слизистые оболочки (в особенности этому способствует слизистая ротовой полости, дыхательных путей и лёгких) в кровь[8]. Токсичной дозой для человека считается 25—50 мг. Доза в 50—75 мг вызывает сильное отравление: происходит понижение АД, появляется сильная головная боль, головокружение, покраснение лица, сильное жжение в горле и под «ложечкой», возможна одышка, обморок, нередко наблюдается тошнота, рвота, колики, светобоязнь, недолговременные и проходящие расстройства зрения, параличи (особенно глазных мышц), шум в ушах, биение артерий, замедление пульса, синюшность, похолодание конечностей. Хроническое действие нитроглицерина (хроническое отравление организма нитроглицерином наблюдалось у работников, производящих динамит), вдыхание, а также приём внутрь больших доз (100—150 мг/кг) может привести к летальному исходу. LD100 для человека составляет 210 мг/кг, смерть наступает в течение 2 минут. Нитроглицерин также может вызывать сильное раздражение кожи. У работающих с динамитом развиваются упорные язвы под ногтями и на концах пальцев, высыпания на подошвах и между пальцами рук, сухость кожи и трещины. Втирание в кожу 1 капли нитроглицерина вызвало общее отравление, длившееся 10 часов[8]. ПДК для рабочей зоны составляет 2 мг/м3[5].
Примечания
Ссылки
Нитроглицерин: получение в лаборатории
Нитроглицерин — одно из наиболее известных взрывчатых веществ, основа состава динамита. Он нашел широкое применение во многих областях промышленности благодаря своим характеристикам, однако до сих пор одна из главных проблем, связанных с ним — вопрос безопасности.
История
История нитроглицерина начинается с итальянского ученого-химика Асканьо Собреро. Он впервые синтезировал это вещество в 1846 году. Первоначально ему было дано название пироглицерина. Уже Собреро обнаружил его большую неустойчивость — нитроглицерин мог взрываться даже от слабых сотрясений или ударов.

Мощность взрыва нитроглицерина теоретически делала его перспективным реагентом в горнодобывающей и строительной промышленностях — он был гораздо эффективнее существовавших на то время видов взрывчатки. Однако упомянутая нестабильность создавала слишком большую угрозу при его хранении и транспортировке — поэтому нитроглицерин отложили в долгий ящик.
Дело чуть сдвинулось с места при появлении Альфреда Нобеля и его семьи — отец и сыновья наладили промышленное производство этого вещества в 1862 году, невзирая на все опасности, связанные с ним. Однако случилось то, что должно было случиться рано или поздно — на фабрике произошел взрыв, и младший брат Нобеля погиб. Отец после перенесенного горя отошел от дел, однако Альфред сумел продолжить производство. Для повышения безопасности он смешивал нитроглицерин с метанолом — смесь была более стабильной, однако очень пожароопасной. Это все еще не было окончательным решением.

Им стал динамит — нитроглицерин, поглощенный кизельгуром (осадочной породой). Взрывоопасность вещества уменьшилась на несколько порядков. Позже смесь совершенствовалась, кизельгур заменяли более эффективными стабилизаторами, однако суть оставалось той же — жидкость поглощалась и переставала взрываться от малейших сотрясений.
Физические и химические свойства

Нитроглицерин — это нитроэфир азотной кислоты и глицерина. В нормальных условиях это желтоватая, вязкая маслянистая жидкость. Нитроглицерин нерастворим в воде. Этим его свойством пользовался Нобель: чтобы после транспортировки подготовить нитроглицерин к применению и освободить его от метанола, он промывал смесь водой — метиловый спирт растворялся в ней и уходил, а нитроглицерин оставался. Это же свойство используют при получении нитроглицерина: водой продукт синтеза промывают от остатков реагентов.
Нитроглицерин гидролизуется (с образованием глицерина и азотной кислоты) при нагревании. Без нагревания идет щелочной гидролиз.
Взрывчатые свойства
Как уже было сказано, нитроглицерин крайне неустойчив. Однако здесь стоит сделать важное замечание: он восприимчив именно к механическому воздействию — взрывается от сотрясения или удара. Если просто поджечь его, жидкость, скорее всего, будет спокойно гореть без взрыва.

Стабилизация нитроглицерина. Динамит
Первым опытом по стабилизации нитроглицерина Нобеля был динамит — кизельгур полностью поглощал жидкость, и смесь была безопасной (до тех пор, конечно, пока ее не активируют в подрывной шашке). Причина, по которой используется именно кизельгур — капиллярный эффект. Наличие микротрубочек в этой породе обусловливает эффективное всасывание жидкости (нитроглицерина) и удержание ее там на долгое время.

Получение в лаборатории
Реакция получения нитроглицерина в лаборатории сейчас все та же, которой пользовался еще Собреро — этерификация в присутствии серной кислоты. Сначала берется смесь азотной и серной кислот. Кислоты необходимы концентрированные, с малым количеством воды. Далее к смеси малыми порциями при постоянном перемешивании постепенно добавляется глицерин. Температура должна поддерживаться низкая, так как в горячем растворе вместо этерификации (образования эфира) будет происходить окисление глицерина азотной кислотой.
Но так как реакция идет с выделением большого количества тепла, смесь необходимо постоянно охлаждать (обычно это делается с помощью льда). Как правило, она держится в районе 0 °С, превышение отметки в 25 °С может грозить взрывом. Контроль температуры осуществляется постоянно с помощью термометра.
Нитроглицерин тяжелее воды, однако легче минеральных (азотной и серной) кислот. Поэтому в реакционной смеси продукт будет лежать отдельным слоем на поверхности. После окончания реакции сосуд необходимо еще охладить, подождать, пока в верхнем слое не скопится максимальное количество нитроглицерина, а потом слить его в другую емкость с холодной водой. Затем идет интенсивная промывка в больших объемах воды. Это необходимо для того, чтобы как можно лучше очистить нитроглицерин от всех примесей. Это важно, потому что в комплекте с остатками непрореагировавших кислот взрывоопасность вещества увеличивается в несколько раз.
Промышленное получение
В промышленности уже давно довели до автоматизации процесс получения нитроглицерина. Система, которая используется в настоящее время, в основных своих аспектах была придумана еще в 1935 году Биацци (и так и называется — установка Биацци). Главные технические решения в ней — это сепараторы. Первичная смесь непромытого нитроглицерина сначала в сепараторе под действием центробежных сил разделяется на две фазы — ту, что с нитроглицерином, отбирают для дальнейшей промывки, а кислоты остаются в сепараторе.

Остальные этапы производства совпадают со стандартными. То есть, смешивание глицерина и нитрующей смеси в реакторе (производится с помощью специальных насосов, перемешивается турбинной мешалкой, охлаждение более мощное — с помощью фреона), несколько этапов промывки (водой и чуть подщелоченной водой), перед каждым из которых идет этап с сепаратором.
Установка Биацци достаточно безопасна и обладает достаточно высокой производительностью по сравнению с другими технологиями (однако обычно большое количество продукта теряется при промывке).
Домашние условия
К сожалению, хотя, скорее, к счастью, синтез нитроглицерина в домашних условиях связан со слишком большим количеством трудностей, преодоление которых в основном не стоит результата.
Единственный возможный способ синтеза в домашних условиях — получение нитроглицерина из глицерина (как и в лабораторном способе). И здесь основная проблема — серная и азотная кислоты. Продажа этих реактивов разрешена только определенным юридическим лицам и строго контролируется государством.
Возникает очевидное решение — синтезировать их самостоятельно. Жюль Верн в своем романе «Таинственный остров», рассказывая об эпизоде изготовления главными героями нитроглицерина, опустил конечный момент процесса, однако крайне подробно описал процесс получения серной и азотной кислот.
Действительно заинтересовавшиеся могут заглянуть в книгу (первая часть, глава семнадцатая), однако и тут загвоздка — необитаемый остров буквально изобиловал необходимыми реактивами, поэтому в распоряжении героев оказались серный колчедан, водоросли, много угля (для обжига), калийная селитра и так далее. Будет ли это у среднестатистического увлекающегося человека? Вряд ли. Поэтому домашний нитроглицерин в абсолютном большинстве случаев остается лишь мечтой.
Глицерин — Википедия
Глицери́н (от греч. γλυκερός — сладкий) — органическое соединение, простейший представитель трёхатомных спиртов с формулой C3H5(OH)3{\displaystyle {\ce {C3H5(OH)3}}}. Представляет собой вязкую прозрачную жидкость со сладким вкусом. Нетоксичен, в отличие например от простейших двухатомных спиртов.
Синонимы: глицерóл, пропантриол-1,2,3.
Бесцветная вязкая жидкость без запаха. Сладкий на вкус, отчего и получил своё название (греч. γλυκερός — сладкий). Имеет молярную массу 92,09 г/моль, относительную плотность d420{\displaystyle d_{4}^{20}} = 1,260, коэффициент преломления nD20{\displaystyle n_{D}^{20}} = 1,4740. Температура плавления составляет 17,9 °C, кипит при 290 °C, частично при этом разлагаясь. Гигроскопичен, поглощает воду из атмосферы в количестве до 40 % от собственной массы. С водой, метанолом, этанолом, ацетоном смешивается в любых пропорциях, но не растворим в эфире и хлороформе, хотя и способен растворяться в их смесях с этанолом[2].
При растворении глицерина в воде выделяется теплота и происходит контракция — уменьшение объёма раствора. Смеси глицерина с водой обладают температурой плавления значительно более низкой, чем каждое из веществ по отдельности, например, при массовом содержании глицерина в 66,7 % его смесь с водой будет замерзать при −46,5 °C[2].
Образует азеотропы с нафталином, его производными и рядом других веществ[2].
Химические свойства глицерина типичны для многоатомных спиртов.
Взаимодействие глицерина с галогеноводородами или галогенидами фосфора ведёт к образованию моно- и дигалогенгидринов.
Глицерин этерифицируется карбоновыми и минеральными кислородосодержащими кислотами с образованием соответствующих сложных эфиров. Так, с азотной кислотой глицерин образует тринитрат — нитроглицерин (получен в 1847 г. Асканио Собреро), использующийся в настоящее время в производстве бездымных порохов.
При дегидратации он образует токсичный акролеин:
- HOCh3CH(OH)−Ch3OH⟶h3C=CH−CHO+2h3O{\displaystyle {\ce {HOCh3CH(OH)-Ch3OH -> h3C=CH-CHO + 2h3O}}},
и окисляется до глицеринового альдегида Ch3OHCHOHCHO{\displaystyle {\ce {Ch3OHCHOHCHO}}}, дигидроксиацетона Ch3OHCOCh3OH{\displaystyle {\ce {Ch3OHCOCh3OH}}} или глицериновой кислоты Ch3OHCHOHCOOH{\displaystyle {\ce {Ch3OHCHOHCOOH}}}.
Сложные эфиры глицерина и высших карбоновых кислот — жиры являются важными метаболитами, существенное биологическое значение также имеют фосфолипиды — смешанные глицериды фосфорной и карбоновых кислот.
Глицерин впервые был получен в 1779 году Карлом Вильгельмом Шееле при омылении жиров в присутствии оксидов свинца[3]. Основную массу глицерина получают как побочный продукт при омылении жиров[4].
Большинство синтетических методов получения глицерина основано на использовании пропилена в качестве исходного продукта. Хлорированием пропилена при 450—500 °С получают аллилхлорид, при присоединении к последнему хлорноватистой кислоты образуются хлоргидрины, например, Ch3ClCHOHCh3Cl{\displaystyle {\ce {Ch3ClCHOHCh3Cl}}}, которые при омылении щёлочью превращаются в глицерин.
На превращениях аллилхлорида в глицерин через дихлоргидрин или аллиловый спирт основаны другие методы. Известен также метод получения глицерина окислением пропилена в акролеин; при пропускании смеси паров акролеина и изопропилового спирта через смешанный ZnO{\displaystyle {\ce {ZnO}}} — MgO{\displaystyle {{\ce {MgO}}}} катализатор образуется аллиловый спирт. Он при 190—270 °C в водном растворе перекиси водорода превращается в глицерин.
Глицерин можно получить также из продуктов гидролиза крахмала, древесной муки, гидрированием образовавшихся моносахаридов или гликолевым брожением сахаров. Также глицерин получается в качестве побочного продукта при производстве биотоплива.
Производные глицерина и их место в обмене веществ живых организмов[править | править код]
Глицериды[править | править код]
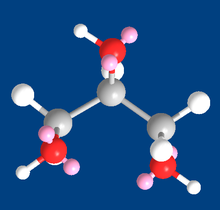 Глицерин (3D модель), показаны атомы и электронные пары при атомах кислорода (розовый цвет)
Глицерин (3D модель), показаны атомы и электронные пары при атомах кислорода (розовый цвет)Триглицериды являются производными глицерина и образуются при присоединении к нему высших жирных кислот. Триглицериды являются важными компонентами в процессе обмена веществ в живых организмах.
Жиры и масла гидрофобны и нерастворимы в воде, так как гидроксильные группы глицерина заменены малополярными остатками жирных кислот.
Область применения глицерина разнообразна: пищевая промышленность, табачное производство, электронные сигареты, медицинская промышленность, производство моющих и косметических средств, сельское хозяйство, текстильная, бумажная и кожевенная отрасли промышленности, производство пластмасс, лакокрасочная промышленность, электротехника и радиотехника (в качестве флюса при пайке).
Глицерин относится к группе стабилизаторов, обладающих свойствами сохранять и увеличивать степень вязкости и консистенции пищевых продуктов. Зарегистрирован как пищевая добавка Е422, и используется в качестве эмульгатора, при помощи которого смешиваются различные несмешиваемые смеси.
Поскольку глицерин хорошо поддается желированию и горит без запаха и чада, его используют для изготовления высококачественных прозрачных свечей и основы для жидкости, используемой в дым-машинах.
Также глицерин используется при изготовлении динамита[5].
В последние годы глицерин используется, наряду с пропиленгликолем, в качестве основного компонента для приготовления жидкости и картриджей для электронных сигарет.
Используется в криобиологии и крионике как основной компонент популярных проникающих криопротекторов для криоконсервирования анатомических препаратов, биологических тканей и организмов.

|
|
НИТРОГЛИЦЕРИН (глицеринтринитрат,
тринитрин) O2NOCH(CH2ONO2)2, мол.
м. 227,14; бесцв. маслянистая жидкость, склонная к переохлаждению; т. кип. 125°С/2
мм рт.ст., d1520 1,5951, d410
1,735; пD20 1,4732; DH0обр
367 кДж/моЛь; m 12,72 •10-30 Кл.м, e 19,25; ур-ние температурной
зависимости давления пара р(мм рт.ст.) = 2,4.1011
ехр (—8400/RT). Кристаллический нитроглицерин существует в двух модификациях — стабильной
ромбич. (т. пл. 13,5°С) и метастабильной триклин-ной (т. пл. 2,8 °С). Нитроглицерин хорошо раств. в ацетоне,
диэтиловом эфире, метаноле, этилацетате, уксусной к-те, бензоле, нитробензоле
и жидких нитроэфирах, ограниченно-в др. спиртах, плохо-в ССl4, бензине,
глицерине, воде (при 20°С-0,13%, 50°С-0,2%, 80 °С-0,35%). Хорошо
пластифицирует нек-рые сорта нитроцеллюлозы. По хим. св-вам нитроглицерин-типичный
представитель нитратов органических. Реагирует с протонными и апротонными
к-тами и основаниями; склонен к окислит.-восстановит. р-циям и гомолитич. распаду
с отщеплением NO2, к-рый может сопровождаться сильным самоускорением.
Медленно гидролизуется в воде, быстрей-в к-тах; легко омыляется щелочами. Характерная
р-ция на нитроглицерин-пурпурно-красное окрашивание при действии анилина и H2SO4;
при добавлении Н2О появляется зеленое окрашивание. Нитроглицерин-мощное бризантное ВВ.
Опасен в обращении; обладает высокой чувствительностью к удару и трению, ограниченно
стоек химически и термически (т. всп. 200 °С), его горение способно легко
переходить во взрыв. Скорость детонации 7650 м/с; может детонировать с малой
скоростью (1500-2000 м/с). Критич. диаметр детонации в стеклянной оболочке 2,1
мм. Теплота взрыва 6300 кДж/моль; объем газообразных продуктов взрыва 713 л/кг.
Жидкий нитроглицерин горит стационарно и турбулентно. Скорость горения в стационарном режиме
при давлении 0,1 МПа 1,4 мм/с; критич. диаметр
0,5 мм. Турбулизация повести горящей жидкости приводит к существованию области
давления (и диаметров заряда), в к-рой нитроглицерин не горит. При увеличении диаметра
заряда и давления нитроглицерин начинает гореть в турбулентном режиме с гораздо большими
скоростями. Получают нитроглицерин этерификацией
глицерина смесью H2SO4 и HNO3 состава 1:1.
Совр. пром. процессы его произ-ва непрерывны и высокопроизводительны. Нитрование
ведут в инжекторе, сепарацию продукта от отработанной к-ты и его послед. промывку-в
центрифуге. Такое проведение процесса наименее опасно из-за малой загруженности
аппаратуры. Простота процесса позволяет осуществить надежный дистанц. контроль
и автоматич. управление. Нитроглицерин обычно не хранят, а сразу перерабатывают в изделия. Нитроглицерин-компонент взрывчатых
составов и порохов, сосудорасширяющее лек. ср-во. В больших дозах ядовит; всасывается
через кожу, вызывает головную боль; ПДК 2 мг/м3. Впервые синтезирован А.
Собреро в 1846; техн. использование предложено А. Нобелем, организовавшим его
пром. произ-во в 60-70-х гг. 19 в. Лит.: АндреевК.К.,
Термическое разложение и горение взрывчатых веществ, 2 изд., М., 1966; Орлова
Е.Ю., Химия и технология бризантных и взрывчатых веществ, 3 изд., Л., 1981.
Б. А. Лурье. |
НИТРОГЛИЦЕРИН — это… Что такое НИТРОГЛИЦЕРИН?
- НИТРОГЛИЦЕРИН
- НИТРОГЛИЦЕРИН
- НИТРОГЛИЦЕРИ́Н, нитроглицерина, муж. (хим.). Жидкое маслянистое взрывчатое и лекарственное вещество, соединение смеси азотной и серной кислоты с глицерином. Препараты нитроглицерина применяются при болезнях сердца.
Толковый словарь Ушакова. Д.Н. Ушаков. 1935-1940.
.
- НИТРАТ
- НИТЧАТКА
Смотреть что такое «НИТРОГЛИЦЕРИН» в других словарях:
нитроглицерин — нитроглицерин … Орфографический словарь-справочник
НИТРОГЛИЦЕРИН — Действующее вещество ›› Нитроглицерин (Nitroglycerin) Латинское название Nitroglycerin АТХ: ›› C01DA02 Нитроглицерин Фармакологическая группа: Нитраты и нитратоподобные средства Нозологическая классификация (МКБ 10) ›› I20 Стенокардия [грудная… … Словарь медицинских препаратов
НИТРОГЛИЦЕРИН — Маслянистая жидкость, получаемая посредством обработки глицерина серною и азотною кислотами и действующая, как сильное взрывчатое вещество. Объяснение 25000 иностранных слов, вошедших в употребление в русский язык, с означением их корней.… … Словарь иностранных слов русского языка
НИТРОГЛИЦЕРИН — НИТРОГЛИЦЕРИН, маслянистая жидкость, применяемая в изготовлении взрывчатых веществ. Получают нитроглицерин в процессе реакции нитрирующей смеси (азотной и серной кислот) с глицерином. Брать в руки даже малые количества вещества слишком опасно,… … Научно-технический энциклопедический словарь
НИТРОГЛИЦЕРИН — (Nitroglycerine) одно из важнейших взрывчатых веществ, находящее много разнообразных применений. Н. служит основным материалом для нитроглицериновых бездымных порохов. Самойлов К. И. Морской словарь. М. Л.: Государственное Военно морское… … Морской словарь
НИТРОГЛИЦЕРИН — полный эфир глицерина и азотной кислоты. Слегка желтая густая жидкость. Температура замерзания 13,5 .С. Чувствителен к удару, трению, огню. Токсичен. Теплота взрыва 6,3 МДж/кг. Применяется в нитроглицериновых взрывчатых веществах и бездымных… … Большой Энциклопедический словарь
Нитроглицерин — глицеринтринитрат (a. nitroclycerin; н. Nitroglycerin; ф. nitroglycerine; и. nitroglicerina), высокочувствит. мощное жидкое BB, представляющее собой полный эфир глицерина и азотной кислоты. Впервые получен в Италии A. Собреро в 1847. H.… … Геологическая энциклопедия
НИТРОГЛИЦЕРИН — НИТРОГЛИЦЕРИН, а, муж. Органическое соединение маслянистая жидкость, получаемая действием азотной кислоты на глицерин, употр. в технике и медицине. | прил. нитроглицериновый, ая, ое. Толковый словарь Ожегова. С.И. Ожегов, Н.Ю. Шведова. 1949 1992 … Толковый словарь Ожегова
нитроглицерин — сущ., кол во синонимов: 12 • взрывчатка (232) • глицеринтринитрат (4) • лекарство … Словарь синонимов
НИТРОГЛИЦЕРИН — НИТРОГЛИЦЕРИН, Nitroglycerinum (синонимы: Glycerinum trinitricum, Trinitrin, Trinitroglycerinum, Glonoin, Angioneurosin), C3H5(O.N02)a, является полным азотнокислым эфиром глицерина и представляет собой прозрачную, бесцветную или слегка… … Большая медицинская энциклопедия
