АЖБП – алкогольная жировая болезнь печени
Алкогольная болезнь печени (АБП) — это комплекс патологических изменений в печени, развитие которых вызвано хроническим употреблением алкоголя в токсических дозах.
Около 30% всех диффузных поражений печеночной ткани связано именно с АБП1. Длительный
прием алкогольных напитков негативно отражается на всех органах и системах, в том числе
и печени. Дело в том, что этанол в клетках печени в процессе метаболизма превращается
в ацетальдегид, который и оказывает токсическое действие на клетки.9 Стоит
отметить, что у женщин в среднем отмечена более низкая активность фермента, обеспечивающего
образование ацетальдегида, в сравнении с мужчинами, чем объясняется более тяжелое течение АБП
среди женщин и развитие алкогольного повреждения печени в более короткий период времени и при
более низких дозах потребляемого алкоголя 10
10
Цирроз печени в России
В большинстве развитых стран АБП является одним из самых распространенных заболеваний, которое диагностируют у 10-25% мужчин и немного реже среди женщин2. Исследования ВОЗ (Всемирной организации здравоохранения) показали, что цирроз печени в России занимает шестое место среди всех причин смертности2.
АБП можно было бы назвать алкогольной жировой болезнью печени, что связано с развитием жировой дистрофии печени на первой стадии заболевания при систематическом употреблении этанола в высоких дозах.1 Такой феномен, накопление жира в клетках печени, происходит и при неалкогольной жировой болезни печени.
Причины, факторы риска
Основная причина развития АБП — злоупотребление алкоголем, однако прямой зависимости между дозами
регулярно употребляемых спиртных напитков и возникновением болезни, степенью ее прогрессирования
и прогнозом не установлено1,3. Основными факторами риска развития АБП являются:
Основными факторами риска развития АБП являются:
-
Ежедневный длительный прием алкоголя в токсических дозах: больше 30г этанола для
мужчин10 (это 75 г водки или 600 мл пива), а для женщин — 20 г
(примерно 200 мл вина) в сутки1. Допустимое к ежедневному потреблению
количество алкоголя, расценивающееся как «безопасная доза», разнится:
в европейских рекомендациях по диагностике и лечению АБП В любом случае алкоголь — фактор токсического повреждения, поэтому
следует осторожно относиться к употреблению алкогольных напитков даже в самых малых дозах.
В любом случае алкоголь — фактор токсического повреждения, поэтому
следует осторожно относиться к употреблению алкогольных напитков даже в самых малых дозах.
- Наследственность. Предрасположенность к развитию алкогольной болезни печени объясняется генетически обусловленными различиями в работе ферментных систем, отвечающих за нейтрализацию этанола 1.
- Этническая принадлежность. Недостаточная активность фермента, метаболизирующего этанол, наблюдается у 50% населения Азии.1
- Избыточный вес или ожирение. Является независимым фактором риска развития АБП.1
-
Алкогольная зависимость у лиц с вирусными гепатитами (особенно В и С) ассоциировано
с более выраженными патологическими изменениями в органе, а также с более высоким
уровнем смертности в сравнении с пациентами, не страдающими вирусными
гепатитами.
 1
1
Механизм развития АБП
Этанол в желудке и в печени окисляется до ацетальдегида, весьма реактогенного соединения, которое повреждает белки, нарушает их функции, что в свою препятствует нормальной функции клеток печени, стимулирует перекисное окисление липидов свободными радикалами.
При этом нарушается обмен жиров и отложение жировых капель в клетках печени. Токсическое действие ацетальдегида ведет также к повреждению мембран клеток и, в конечном счете, их гибели.1
Стадии и их симптомы
Клинические проявления АБП зависят от стадии заболевания, которые перетекают из одной в другую:
-
Алкогольный стеатоз (жировая дистрофия) — наиболее частая
форма, ее диагностируют у 50-90% пациентов, которые злоупотребляют алкоголем1.

Протекает обычно бессимптомно или с неспецифическими симптомами, такими как слабость, снижение аппетита, тяжесть и дискомфорт в животе, правом подреберье. Может развиваться длительно или, наоборот, стремительно в течение нескольких недель1. При инициации терапии на данной стадии и прекращении потребления алкоголя можно добиться полной регрессии стеатоза1,11. -
Алкогольный стеатогепатит — прогрессирующий
воспалительно-дистрофический процесс в печени, связанный с повреждением печени алкоголем.
Среди больных, госпитализированных с АБП, эта стадия заболевания диагностируется у 10-35%
пациентов.
К сожалению, алкогольный стеатогепатит может быть ассоциирован с высоким уровнем летальности
в первый месяц заболевания (до 50%).

В таких случаях его называют «алкогольным гепатитом тяжелого течения», и при этом состоянии врачи могут применять глюкокортикоиды.12 -
Алкогольный фиброз с переходом в цирроз
печени5 — формирование соединительной ткани на месте участков
некроза (гибели гепатоцитов).
Состояние пациентов до некоторых пор может оставаться удовлетворительным, но при декомпенсации заболевания могут наблюдаться желтуха, печеночная энцефалопатия, склонность к кровотечениям и отеки.
При осмотре пациента с циррозом врач может обратить внимание на так называемый алкогольный габитус,
или «facies alcoholica»: телеангиоэктазии, контрактура Дюпиетрена (характерно неразгибающиеся
пальцы руки), атрофия мышц плечевого пояса, увеличение лимфоузлов и слюнных желез. 12 Кроме
того, на данной стадии может параллельно развиваться алкогольная полинейропатия (чаще всего нарушения
ощущения и движения в конечностях), воспаление поджелудочной железы (панкреатит), поражение сердца
(кардиомиопатия).
12 Кроме
того, на данной стадии может параллельно развиваться алкогольная полинейропатия (чаще всего нарушения
ощущения и движения в конечностях), воспаление поджелудочной железы (панкреатит), поражение сердца
(кардиомиопатия).
Важно понимать, что алкоголь может напрямую (генотоксически)
новообразования в печени — гепатоцеллюлярной карциномы6.
Диагностика
Один из ключевых вопросов диагностики АБП — заподозрить алкоголь как причину патологии.
Естественно, пациенты не всегда готовы признать, что злоупотребляют алкогольными напитками. Разработаны
даже специальные опросники, которые помогают ненавязчиво прояснить отношения пациента с «зеленым
змием»6.
Результаты лабораторных исследований также помогают подтвердить диагноз8:
повышение числа лейкоцитов в периферической крови — лейкоцитоз
снижение уровня гемоглобина и эритроцитов — анемияповышение АСТ, АЛТ незначительные, соотношение АСТ/АЛТ обычно больше2,
уровень билирубина и показатели свертываемости крови (протромбиновое время) могут сообщить о тяжести заболевания.
Из инструментальных исследований наибольшее скрининговое значение для диагностики патологии печени
остается ультразвуковая диагностика (УЗИ). Комплексное УЗИ органов брюшной полости, включая печень
и желчный пузырь помогает исключить механическую желтуху, такде можно обнаружить стеатоз («жирную
печень»): равномерное увеличение органа, повышение эхогенности, диффузную гетерогенность, закругленные
края органа.
Доступны и такие методы визуализации как МРТ и КТ, однако, в силу стоимости, они применяются значительно реже. Биопсия печени дает наиболее полное представление о форме и стадии болезни, однако ее проведение связано с повышенным риском осложнений, этот метод имеет противопоказания, должен проводится с соблюдением ряда предосторожностей, поэтому используется еще реже.
Лечение, прогнозы
Лечение алкогольной болезни печени основано на следующих принципах7:
- Полный отказ от употребления алкоголя в любом виде.
- Коррекция питания и соблюдение диеты. Обязательно оценивается
текущее состояние — избыток или недостаток массы тела, и в зависимости
от этого разрабатывается рацион питания.

- При тяжелом гепатите могут быть использованы глюкокортикостероиды, которые по некоторым данным улучшали выживаемость, хотя последнее время рациональность их применения оспаривается7.
- При необходимости рассматривается необходимость трансплантации печени.
Здесь важно отметить, что согласно современным научным представлениям ничто, кроме отказа от алкоголя не продлевает жизнь при АБП. Нет волшебной пилюли, которая позволит продолжать «возлияния» без последствий. Нет уловки, рецепта или хитрости, которые позволят безнаказанно употреблять токсические вещества. Любые способы «почистить печень» — иллюзия для психологического спокойствия комфорта больного, его близких и родственников.
То есть прием любых лекарственных препаратов носит вспомогательный характер по отношению
к прекращению приема алкоголя. Тем не менее, действительно существуют средства, прием которых
направлен на поддержку больного в его комплексной борьбе с данной патологией. Например,
эссенциальные фосфолипиды, помогают защитить клетки печени от повреждающего действия свободных
радикалов, способствуют замедлению прогрессирования фиброза, помогают в нормализации обмена жиров
и углеводов при АБП7.
Тем не менее, действительно существуют средства, прием которых
направлен на поддержку больного в его комплексной борьбе с данной патологией. Например,
эссенциальные фосфолипиды, помогают защитить клетки печени от повреждающего действия свободных
радикалов, способствуют замедлению прогрессирования фиброза, помогают в нормализации обмена жиров
и углеводов при АБП7.
Однако, еще раз подчеркнем, любые препараты — дополнительный инструмент
в борьбе с данной патологией, главное — отказ от алкоголя. И отказ
значит полный отказ. Без компромиссов. Это действительно важно, ведь речь идет о продолжительности
и качестве жизни больного. Ведь прогноз зависит не только от стадии болезни
и ее тяжести. Конечно, стремительное развитие гепатита и формирование цирроза относятся
к неблагоприятным прогностическим признакам и снижают выживаемость.
В то же время своевременное лечение и отказ от злоупотребления алкоголем дают шанс
на выздоровление.
Алкогольная болезнь печени
Алкогольная болезнь печени — заболевание, которое возникает при длительном (более 10-12 лет) употреблении алкоголя, который обладает прямым гепатотоксическим действием.Среднесуточными дозами чистого этанола, приводящими к развитию болезни, являются: более 40-80г для мужчин; более 20г — для женщин. В 1 мл алкоголя содержится примерно 0,79 г этанола.
Алкогольная болезнь печени может проявляться симптомами жировой дистрофии печени (стеатоз), алкогольного гепатита и цирроза . Самой ранней и обратимой стадией повреждения печени вследствие злоупотребления алкоголем является стеатоз (возникает в 90-100% случаев).
Диагностика алкогольной болезни печени основана на признаках хронической алкогольной интоксикации (контрактура Дюпюитрена, пальмарная эритема, увеличение околоушных желез), результатах лабораторных тестов, данных визуализирующих методов обследования.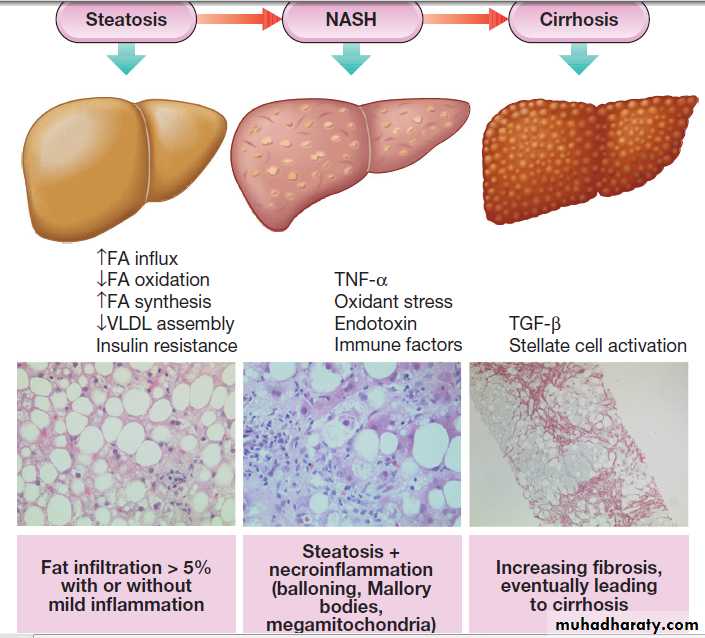 Проводится биопсия печени.
Проводится биопсия печени.
Лечение заключается в полном отказе от употребления алкоголя, назначении кортикостероидов, эссенциальных фосфолипидов. В терминальной стадии выполняется трансплантация печени.
Классификация алкогольной болезни печени
Стеатоз печени
Стеатоз печени вследствие злоупотребления алкоголем развивается у 90-100% пациентов. В южной Италии стеатоз диагностируется у 46,4% людей, злоупотребляющих алкоголем (более 60 г/сут) и у 95,5% страдающих ожирением.При отказе от употребления алкоголя патологические изменения в печени, характерные для стеатоза, нормализуются в течение 2-4 недель. Часто отмечается бессимптомное течение этой стадии.
При длительном злоупотреблении алкоголем возникают алкогольный гепатит и цирроз печени.
Алкогольный гепатит
Алкогольный гепатит — подострое воспаление ткани печени. Гистологической характеристикой этой стадии является центрилобулярная полиморфоядерная инфильтрация, гигантские митохондрии и тельца Мэллори.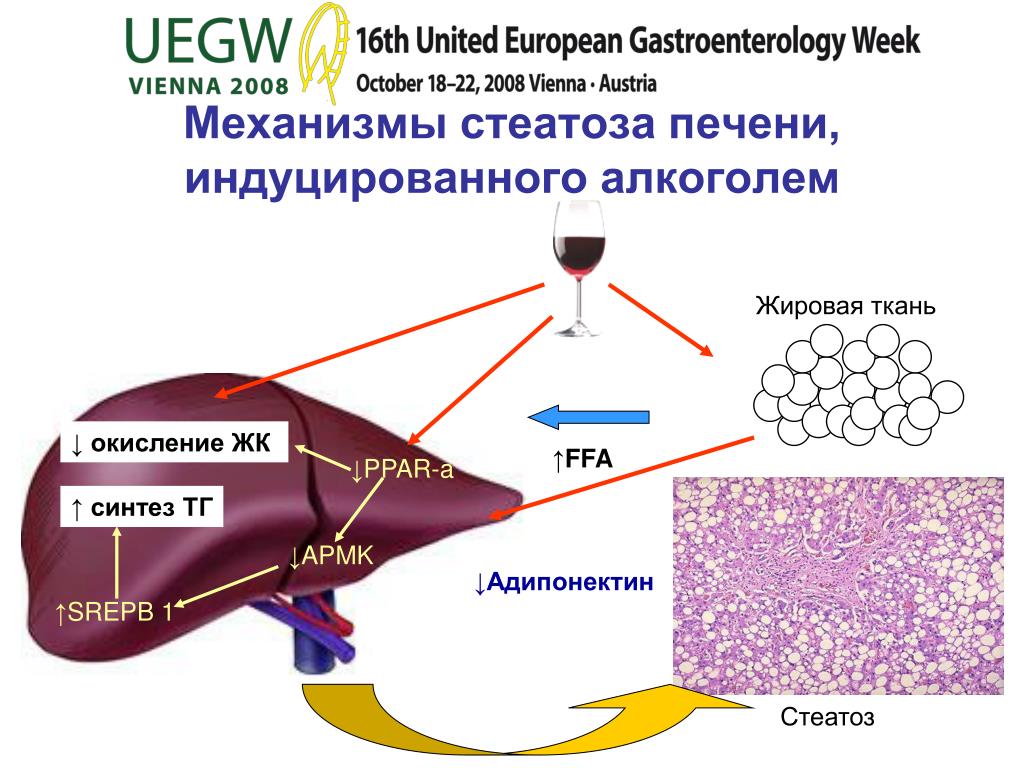 Появляется центрилобулярный и перисинусоидальный фиброз.
Появляется центрилобулярный и перисинусоидальный фиброз.Алкогольный гепатит сопровождается разрушением гепатоцитов, нарушением функции печени, формированием цирроза печени. У пациента появляется слабость, потеря веса, тошнота, рвота боль в правом подреберье, желтуха. Печень при осмотре увеличена и плотная.
Осложнениями алкогольного гепатита являются: кровотечения из варикозно-расширенных вен, печеночная энцефалопатия, коагулопатия, асцит , спонтанный бактериальный перитонит. Развитие осложнений свидетельствует о неблагоприятном прогнозе.
Цирроз печени
Конечной стадией алкогольной болезни печени является цирроз (развивается в 10-20% случаев), характеризующийся массивным фиброзом, очагами регенерации. У пациентов нарушается функция печени, развивается портальная гипертензия .Повышается риск развития гепатоцеллюлярной карциномы . В большинстве случаев причиной смерти пациентов являются осложнения цирроза печени: асцит , спонтанный бактериальный перитонит, гепаторенальный синдром, энцефалопатия и кровотечение из варикозно-расширенных вен.
Диагностика
Алкогольную болезнь печени можно заподозрить, если у пациента, длительно и систематически злоупотребляющего алкоголем (среднесуточными дозами чистого этанола, приводящими к развитию болезни, являются: более 40-80г для мужчин; более 20г — для женщин) появляются признаки поражения печени: снижение аппетита, дискомфорт и тупая боль в правом подреберье или эпигастральной области, тошнота, желтуха, гепатомегалия.Прогноз
Прогноз алкогольной болезни печени зависит от стадии алкогольной болезни печени и тяжести заболевания.При стеатозе прогноз благоприятный. При отказе от употребления алкоголя патологические изменения в печени, характерные для стеатоза, нормализуются в течение 2-4 недель.
При продолжении приема алкоголя заболевание прогрессирует. Факторами, способствующими ухудшению течения болезни, являются: инфицирование вирусами хронических гепатитов В и С, женский пол, ожирение.
При наличии гипербилирубинемии > 20 мг/дл (> 360 мкмоль/л), удлиненного протромбинового времени, появлении симптомов печеночной энцефалопатии, вероятность возникновения цирроза печени составляет 50%, а риск летального исхода — 20-50%.
При развитии цирроза печени 5-летних показателей выживаемости достигают только 50% пациентов.
Кроме того, при развитии цирроза печени повышается риск возникновения гепатоцеллюлярной карциномы .
Алкогольная болезнь печени, алкогольный гепатит
Что такое алкогольный гепатит?
Алкогольная болезнь печени (АБП) или алкокгольный гепатит – это повреждение печени, вызванное действием этанола на печеночные клетки. Болезнь развивается медленно (годами) и проходит следующие стадии: стеатоз, стеатогепатит, цирроз печени. Алкогольная болезнь печени встречается также часто, как и вирусные поражения печени (гепатит В и гепатит С) и приводит к циррозу печени примерно у 15-20% больных, хронически злоупотребляющих алкоголем. Как правило, это пожилые люди (старше 60 лет), однако в последнее время алкогольный цирроз стал одной из основных причин обращения к врачу-гепатологу, в возрастной группе от 45 до 65 лет.
Кто подвержен этому заболеванию?
Алкогольное поражение печени с исходом в цирроз происходит при употреблении от 40 до 80 г чистого этанола в день у мужчин и от 20 до 40 г у женщин. Развитие цирроза у мужчин наблюдается через 10 лет, а у женщин через 5 лет.Риск развития цирроза при АБП зависит не только от пола, но также от генетической предрасположенности и инфицирования вирусами гепатитов В и С. Неправильное питание (хроническое недоедание и недостаток витаминов А и Е) усугубляет токсическое действие алкоголя на печень. Употребление алкоголя вне приема пищи увеличивает в несколько раз риск развития АБП с исходом в цирроз.
Как проявляется АБП?
Клинические проявления АБП различны от отсутствия каких бы то ни было признаков заболевания (стеатоз), до тяжелых осложнений при сформировавшемся циррозе.
Алкогольный стеатоз печени выявляется в 60-100 % случаев у лиц, злоупотребляющих алкоголем. На этой стадии чаще всего наблюдается астения, нарушения пищеварения (тошнота), дискомфорт и болевой синдром в правом подреберье. Однако чаще алкогольный стеатоз печени протекает бессимптомно и обнаруживается случайно.
Однако чаще алкогольный стеатоз печени протекает бессимптомно и обнаруживается случайно.
Алкогольный стеатоз – это обратимая ситуация при условии прекращения приема алкоголя.
Формы АБП – острая и хроническая
Острый алкогольный гепатит, в отличие от хронического алкогольного гепатита, обычно протекает с выраженными симптомами и часто заканчивается летально. Наиболее характерно наличие тупой боли в правом подреберье, лихорадки, желтухи. Печень обычно увеличена, значительно повышены АЛТ,АСТ и ГГТ. При холестатической форме АБП основным клиническим проявлением является желтуха, невыносимый кожный зуд, болевой синдром, лихорадка, потемнение мочи и обесцвеченный кал. Хотя эта форма заболевания встречается редко (5-10 %), однако летальность ее составляет 50-60 %
Наиболее опасной является фульминантная форма (стремительное развитие патологических процессов), при которой прогрессирует декомпенсация и развитие геморрагичекого синдрома и почечной недостаточности.
Цирроз печени развивается примерно у 40 % с АБП. При продолжении приема спиртных напитков пятилетняя выживаемость не превышает 10 %.
Диагностика АБП
Для АБП характерны: увеличение околоушных желез, выпадение волос на теле, увеличение печени, снижение мышечной массы, энцефалопатия, полинейропатия, хронический панкреатит, и другие.
Среди лабораторных маркеров основными являются ГГТ, АСТ, АЛТ (АСТ>АЛТ), снижение уровня тромтоцитов в крови, повышение уровня трансферрина. На поздних стадиях цирроза нарушается белковосинтезирующая функция печени с увеличением уровня гамма-глобулинов и снижение альбумина.
Метод эластометрии (ФиброМакс, Фибротест) позволяет неинвазивно оценить степень выраженности фибротических изменений печени.
Лечение алкогольной болезни печени
Основой лечения является полный отказ от алкоголя, который эффективен на любой стадии заболевания.
Терапия основана на воздействии на все звенья патологического процесса. Наиболее часто применяют иммунные и антиоксидантные препараты. Доказано возможное применение глюкокортикостероидов при остром алкогольном гепатите с тяжелым течением (индекс Мэддрея>32).
Наиболее часто применяют иммунные и антиоксидантные препараты. Доказано возможное применение глюкокортикостероидов при остром алкогольном гепатите с тяжелым течением (индекс Мэддрея>32).
Для лечения алкогольного стеатоза применяют в качестве комплексной терапии следующие препараты: адеметионин (гептрал), урсодезоксихолевая кислота (урсосан), эссенциальные фосфолипиды (фосфоглив), силимарин.
Адеметионин и фосфолипиды могут применяться как внутривенно, так и в таблетках.
Урсодезоксихолевая кислота может быть эффективна и при холестатической форме АБП.
Принципы лечения алкогольного цирроза печени основаны на устранении его осложнений – портальной гипертензии, асцита, печеночной энцефалопатии, перитонита.
При варикозном расширении вен пищевода для снижения давления в системе воротной вены и профилактики кровотечения проводится их лигирование оперативным путем.
Для лечения асцита используют калийсберегающие мочегонные препараты. Доза подбирается индивидуально до достижения положительного результата.
Доза подбирается индивидуально до достижения положительного результата.
В ряде случаев рекомендовано внутривенное введение альбумина.
Лечение энцефалопатии предусматривает использование препаратов стимулирующих обмен аммиака, снижая таким образом его токсическое действие на ЦНС. К таким препаратам относится орнитин аспартат и лактулоза.
В случае тяжелого алкогольного гепатита или декомпенсированного цирроза печени рекомендуется трансплантация печени. Принципиальным условием для этого является полное прекращение приема алкоголя в течение как минимум 6 месяцев до операции.
Алкогольная болезнь печени
«Имеет смысл хотя бы раз в год давать организму передышку и хотя бы месяц не употреблять алкоголь, не есть жирного, жареного и сладкого, и что самое главное – проверять свою печень. Достаточно просто сделать УЗИ у профессионалов и оценить количество жира в печени и стадию фиброза в ней».
Главный врач «ГЦ Эксперт» Мехтиев С.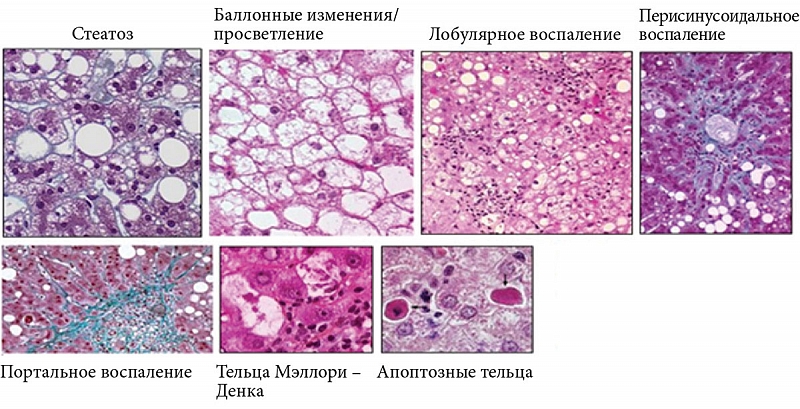 Н.
Н.
Безопасное количество потребляемого для человека алкоголя до сих пор вызывает массу дискуссий. По рекомендациям ВОЗ безопасным считается прием 21 единицы алкоголя в неделю для мужчин и 14 — для женщин. Единица или порция алкоголя равна 30 граммам 40% напитков (водка), 100 граммам напитков 9–11% (сухое вино) и 200 граммам напитков 3–5% (пиво). Однако еженедельное употребление даже допустимой дозы в течение 5 лет в 50% случаев приводит к развитию алкогольного цирроза печени. А при употреблении алкогольных коктейлей условный риск цирроза печени возрастает еще на 20%. В тех случаях, когда крепкие алкогольные напитки смешивают с пивом, риск повышается еще на 30%.
Цель лечения алкогольного гепатита состоит в предупреждении развития цирроза печени. Лечение индивидуальное и комплексное с учетом тяжести состояния пациента и риска развития осложнений. Главным условием является полный отказ от употребления алкоголя в течение 6 месяцев, для многих пациентов с алкогольной зависимостью это является серьезной психологической проблемой и может занять много времени. Поэтому в случае наличия хронического алкогольного гепатита врачи нашего центра стараются улучшить самочувствие и качество жизни пациента с помощью курса противовоспалительной, гепатопротекторной и дезинтоксикационной терапии, при желании пациента могут порекомендовать специалиста, который помогает избавится от алкогольной зависимости. По результатам обследования врач-гепатолог на консультации информирует пациента о течение его заболевания и дает дальнейшей прогноз с учетом отказа от алкоголя и без него.
Поэтому в случае наличия хронического алкогольного гепатита врачи нашего центра стараются улучшить самочувствие и качество жизни пациента с помощью курса противовоспалительной, гепатопротекторной и дезинтоксикационной терапии, при желании пациента могут порекомендовать специалиста, который помогает избавится от алкогольной зависимости. По результатам обследования врач-гепатолог на консультации информирует пациента о течение его заболевания и дает дальнейшей прогноз с учетом отказа от алкоголя и без него.
В нашем центре вы можете пройти полное обследование печени, включающее все необходимые лабораторные и инструментальные исследования, позволяющие определить стадию фиброза, а также получить развернутую консультацию врача-гепатолога.
Пациент в результате лечения получит
- Улучшение самочувствия и качества жизни.
- Снижение риска развития или прогрессирования цирроза.
Советы и рекомендации
Алкогольная болезнь печени может развиваться не только у людей, злоупотребляющих алкоголем и имеющих алкогольную зависимость. Поэтому если вы хорошо переносите и употребляете большие дозы алкоголя на протяжении многих лет, рекомендуем проверять состояние печени с помощью УЗИ хотя бы раз в год.
Поэтому если вы хорошо переносите и употребляете большие дозы алкоголя на протяжении многих лет, рекомендуем проверять состояние печени с помощью УЗИ хотя бы раз в год.
Лечебные рекомендации при жировом гепатозе на начальной стадии алкогольной болезни печени сводятся к отказу от употребления алкоголя, хотя бы в течение 1 месяца и снижению массы тела, при наличии ожирения.
Справочная информация
Алкогольная болезнь печени — это хроническое заболевание, к формированию которого приводит хроническое злоупотребление алкоголем. Алкоголь рассматривается во всем мире как один из основных факторов риска для развития угрожающих жизни заболеваний наряду с курением и высоким кровяных давлением, в том числе цирроза печени.
Алкогольная болезнь печени и алкоголизм – две болезни и одна проблема
А.А. САМСОНОВ1, д.м.н., профессор, Е.Ю. ПЛОТНИКОВА2, д.м.н., профессор, И.Н. НИКУШКИНА1, д.м.н., профессор, Е.А. ТАЛИЦКАЯ3, М.В. КРАСНОВА4, к.м.н., О.А. КРАСНОВ5, д.м.н., профессор
КРАСНОВА4, к.м.н., О.А. КРАСНОВ5, д.м.н., профессор1 Кафедра пропедевтики внутренних болезней и гастроэнтерологии МГМСУ им. А.И. Евдокимова
2 Кафедра подготовки врачей первичного звена здравоохранения, руководитель курса клинической гастроэнтерологии, ГБОУ ВПО «КемГМА» Минздрава России, г. Кемерово
3 Гастроэнтерологическое отделение МБЛПУ «Городская клиническая больница №1», г. Новокузнецк
4 Гастроэнтерологическое отделение Кузбасского областного гепатологического центра, МБУЗ «ГКБ №3 им. М.А. Подгорбунского», г. Кемерово
5 Кафедра госпитальной хирургии ГБОУ ВПО «КемГМА» Минздрава России, главный врач МБУЗ «ГКБ №3 им. М.А. Подгорбунского», г. Кемерово
Данная работа посвящена алкогольному поражению печени, которое развивается по типу стеатоза/стеатогепатита/фиброза с последующей трансформацией в цирроз печени. Описаны патогенетические механизмы алкогольного повреждения печени по типу стеатоза/стеатогепатита. В разделе лечения алкогольного стеатогепатита рассмотрены современные данные о применении препаратов с высоким уровнем доказательности и рекомендаций. Также в статье приводятся собственные исследования по качеству жизни и влиянию соматических жалоб у пациентов с разными вариантами жировой болезни печени.
В разделе лечения алкогольного стеатогепатита рассмотрены современные данные о применении препаратов с высоким уровнем доказательности и рекомендаций. Также в статье приводятся собственные исследования по качеству жизни и влиянию соматических жалоб у пациентов с разными вариантами жировой болезни печени.
Если вы знаете алкоголизм, то вы знаете всю медицину.
Перефразируя William Osler.
История показывает, что употребление алкогольных напитков, полученных путем брожения, и, как следствие, развитие патологии печени существует со времен неолита (около 10 тыс. лет до н.э.) [1] и является приоритетной причиной заболеваний печени во всем мире.
Болезни печени, связанные с употреблением алкоголя, протекают по трем клинико-морфологическим вариантам (стадиям): жировая дистрофия печени (стеатоз), алкогольный гепатит с фиброзом (стиеатогепатит) и цирроз печени. Стеатогепатит, развивающийся при регулярном приеме большого количества алкоголя, как правило, при условии обязательной абстиненции, обратим. Острый алкогольный гепатит, возникающий при алкогольных эксцессах, может протекать от бессимптомного «биохимического» расстройства, незаметного для больного, до молниеносной печеночной недостаточности и смерти. Цирроз печени в исходе стеатоза/стеатогепатита предусматривает патологическую трансформацию структуры нормальной печеночной паренхимы что приводит к клиническим проявлениям портальной гипертензии и печеночной недостаточности.
Острый алкогольный гепатит, возникающий при алкогольных эксцессах, может протекать от бессимптомного «биохимического» расстройства, незаметного для больного, до молниеносной печеночной недостаточности и смерти. Цирроз печени в исходе стеатоза/стеатогепатита предусматривает патологическую трансформацию структуры нормальной печеночной паренхимы что приводит к клиническим проявлениям портальной гипертензии и печеночной недостаточности.
Распространенность алкогольной болезни печени (АБП) зависит от многих факторов, включая генетические (склонность к злоупотреблению алкоголем, пол больного, этнический тип и др.) и фенотипические (например, доступность алкоголя, социально-экономическая доступность, традиции), и поэтому трудно определить, какие из них являются ведущими.
В целом риск заболеваний печени возрастает с увеличением количества и длительностью употребления алкоголя [2, 3]. При этом чрезмерное употребление алкоголя не является достаточным для возникновения алкогольной болезни печени.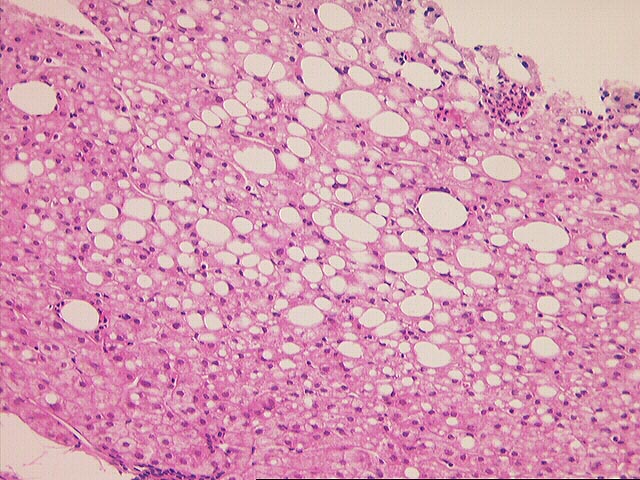 По данным Grant B.F. и соавт., только у 1 из 5 алкоголиков развивается алкогольный стеатогепатит, а у 1 из 4 развивается цирроз печени. Порог ежедневного употребления чистого этанола в 40 г может вызывать патологические изменения по типу алкогольного стеатогепатита, а прием более 80 г в день связано с увеличением степени тяжести алкогольного гепатита. Существует четкое дозозависимое соотношение между приемом алкоголя и частотой формирования алкогольного цирроза печени – это ежедневное употребление более 60 г чистого этанола у мужчин и 20 г у женщин [4]. По другим данным, жировая инфильтрация печени развивается примерно у 90% людей, которые ежедневно принимают больше чем 60 г чистого этанола, [5], но такой же морфологический субстрат, как жировая дистрофия печени может регистрироваться и у людей, не принимающих алкоголь [6]. Как уже было сказано, алкогольный стеатоз печени, обычно протекающий бессимптомно, может быть полностью обратим при отказе от алкоголя примерно через 4–6 недель [7].
По данным Grant B.F. и соавт., только у 1 из 5 алкоголиков развивается алкогольный стеатогепатит, а у 1 из 4 развивается цирроз печени. Порог ежедневного употребления чистого этанола в 40 г может вызывать патологические изменения по типу алкогольного стеатогепатита, а прием более 80 г в день связано с увеличением степени тяжести алкогольного гепатита. Существует четкое дозозависимое соотношение между приемом алкоголя и частотой формирования алкогольного цирроза печени – это ежедневное употребление более 60 г чистого этанола у мужчин и 20 г у женщин [4]. По другим данным, жировая инфильтрация печени развивается примерно у 90% людей, которые ежедневно принимают больше чем 60 г чистого этанола, [5], но такой же морфологический субстрат, как жировая дистрофия печени может регистрироваться и у людей, не принимающих алкоголь [6]. Как уже было сказано, алкогольный стеатоз печени, обычно протекающий бессимптомно, может быть полностью обратим при отказе от алкоголя примерно через 4–6 недель [7]. Вместе с тем некоторые исследования показали, что прогрессирование фиброза и исход в цирроз происходит у 5–15% пациентов, несмотря даже на полную абстиненцию [8, 9].
Вместе с тем некоторые исследования показали, что прогрессирование фиброза и исход в цирроз происходит у 5–15% пациентов, несмотря даже на полную абстиненцию [8, 9].
Проблема злоупотребления алкоголем очень актуальна в нашей стране. В литературе часто приводятся различные эпидемиологические данные по этому поводу, но все они только верхушка айсберга под названием «алкогольная болезнь печени». Как говорилось выше, алкоголизм у пациентов формируется раньше и чаще, чем АБП. Алкогольная зависимость – это сложная биохимическая «комбинация» превращения этанола в центральной нервной системе с выработкой в конечном этапе эндорфинов и дофамина, которые становятся «жизненно» необходимы пациентам с алкоголизмом. Эти люди в нашем обществе натыкаются часто на различные виды социального порицания, административного и уголовного наказаний, но в силу определенных особенностей заболевания не воспринимаются социумом как тяжелобольные.
Диагностика алкоголизма основывается на клиническом обследовании, специальных тестах (опросник CAGE [10]): тест на выявление постинтоксикационного алкогольного синдрома (ПАС), перечень физикальных признаков ХАИ – хронической алкогольной интоксикации («Сетка LeGo», 1976) в модификации О. Б. Жаркова, П.П. Огурцова, В.С. Моисеева и многих других.
Б. Жаркова, П.П. Огурцова, В.С. Моисеева и многих других.
Диагноз алкогольного гепатита также основан на тщательном сборе анамнеза, осмотре, клинических лабораторных и инструментальных исследованиях. Клинические проявления скудные: тяжесть в правом подреберье, вздутие живота, тошнота и диарея после употребления жирной пищи. Большинство больных жалобы не предъявляет. У большинства (более 70%) из них наблюдается гепатомегалия с гладкой поверхностью, выявляемой пальпаторно. Иктеричность и увеличение селезенки обнаруживаются редко. В лабораторных исследованиях характерно увеличение коэффициента де Ритиса – соотношение аспартатаминотрансферазы (AST) и аланинаминотрансферазы (ALT). Другие общие и неспецифические лабораторные отклонения включают анемию, лейкоцитоз, тромбоцитопению, гипоальбуминемию, гипергаммаглобулинемию, гипербилирубинемию, гипераммониемию и другие метаболические нарушения. Для установления диагноза иногда необходима биопсия печени. Наиболее характерные гистологические проявления алкогольной болезни печени: жировая дистрофия гепатоцитов, наличие телец Мэллори, нейтрофильная инфильтрация и перивенулярный фиброз [11].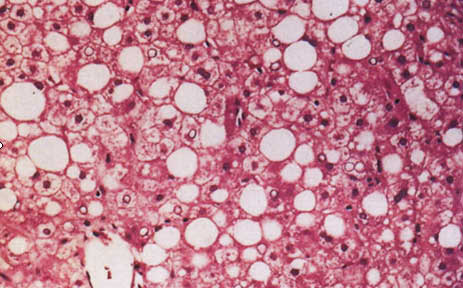 Диагноз алкогольной болезни печени основан на выявлении классических признаков и симптомов поражения печени у пациента со значительным употреблением алкоголя в анамнезе. Следует иметь в виду, что пациенты, как правило, занижают количество употребляемого алкоголя, но опрос членов семьи и близких друзей может обеспечить более точную оценку количества принимаего алкоголя. При этом клиническое подозрение на алкогольный гепатит может быть неточным у больных до 30% случаев [12].
Диагноз алкогольной болезни печени основан на выявлении классических признаков и симптомов поражения печени у пациента со значительным употреблением алкоголя в анамнезе. Следует иметь в виду, что пациенты, как правило, занижают количество употребляемого алкоголя, но опрос членов семьи и близких друзей может обеспечить более точную оценку количества принимаего алкоголя. При этом клиническое подозрение на алкогольный гепатит может быть неточным у больных до 30% случаев [12].
Мы провели сравнительный клинический анализ пациентов с алкогольным стеатогепатитом (АСГ) и неалкогольным стеатогепатитом (НАСГ), контрольную группу составили люди аналогичного возраста, не имеющие патологии печени. Различия между параметрами сравнения считались статистически различными при р ≤ 0,05. Исследование проводилось в соответствии с принципами Хельсинкской декларации Всемирной медицинской ассоциации (в редакции 2000 г. с разъяснениями, данными на генеральной ассамблее ВМА, Токио, 2004), с правилами Качественной клинической практики Международной конференции по гармонизации (ICH GCP), этическими принципами, изложенными в Директиве Европейского союза 2001/20/ЕС и требованиями национального российского законодательства. Протокол исследования одобрен комитетом по этике ГБОУ ВПО «КемГМА» Минздрава России; процедуры рассмотрения и одобрения исследования соответствовали требованиям национального законодательства. Каждый больной подписал Информированное согласие на участие в исследованиях.
Протокол исследования одобрен комитетом по этике ГБОУ ВПО «КемГМА» Минздрава России; процедуры рассмотрения и одобрения исследования соответствовали требованиям национального законодательства. Каждый больной подписал Информированное согласие на участие в исследованиях.
Диагноз был подтвержден клинически, лабораторно, инструментально, большинству пациентов выполнена биопсия печени. Между рядом клинических показателей были выявлены статистически значимые различия. В задачи исследования не входило выявлять у пациентов алкоголизм, консультации нарколога не были предусмотрены, но диагноз алкогольной болезни печени выставлялся на основании данных анамнеза со слов самих пациентов и их родственников, а также объективных клинических данных. Всем обследуемым предлагалось заполнить ряд тестов, в которые входили Ноттингемский профиль здоровья (Nottingham Health Profile) по оценке качества жизни пациентов [13], интенсивность субъективных недомоганий оценивалась с помощью Гиссенского опросника «влияния соматических жалоб», разработанного в психосоматической клинике Гиссенского университета [14].
К удивлению исследователей, самые лучшие показатели по исследованию качества жизни оказались у пациентов с АСГ, а результаты по Гиссенскому опроснику указывали на самый высокий «прессинг жалоб» в контрольной группе. Результаты исследований представлены в таблице 1.
Таблица 1. Результаты показателей качества жизни по NHP и по Гиссенскому опроснику «давления соматических жалоб»
|
Показатель |
АСГ |
НАСГ |
НАСГ |
Контрольная группа p | ||||||||
|
|
М |
±SD |
М |
±SD |
М |
±SD |
|
| ||||
|
КЖ-ЭНЕР |
5,60000 |
13,41702 |
32,16271 |
35,81925 |
10,40000 |
12,09617 |
0,0000004 |
| ||||
|
КЖ-БОЛЬ |
9,67305 |
15,70354 |
19,89525 |
28,36756 |
8,27633 |
12,68954 |
0,0124304 |
| ||||
|
КЖ-ЭМОЦ |
12,08085 |
14,95820 |
12,32085 |
14,18457 |
13,37567 |
13,88680 |
0,920190 |
| ||||
|
КЖ-СОН |
28,52695 |
33,31003 |
35,33644 |
28,70661 |
19,19500 |
26,54171 |
0,059933 |
| ||||
|
КЖ-СОЦ |
8,66542 |
13,13223 |
11,95441 |
18,88667 |
9,91533 |
17,41684 |
0,554153 |
| ||||
|
КЖ-ФИЗ |
7,53136 |
11,39543 |
15,10407 |
17,25977 |
11,66100 |
12,51378 |
0,0170905 |
| ||||
|
КЖ-ОБЩ |
71,9251 |
62,2467 |
125,8500 |
118,6458 |
75,4307 |
61,0578 |
0,0025104 |
| ||||
|
Г-И |
3,627119 |
2,778602 |
5,779661 |
3,939490 |
7,300000 |
2,878577 |
0,0000041 |
| ||||
|
Г-Ж |
5,237288 |
3,962492 |
6,016949 |
3,785141 |
4,366667 |
3,547542 |
0,149593 |
| ||||
|
Г-Р |
5,96610 |
4,820810 |
8,06780 |
5,429372 |
10,03333 |
5,536608 |
0,0021871 |
| ||||
|
Г-С |
2,576271 |
2,877999 |
4,508475 |
3,887969 |
4,633333 |
3,809999 |
0,0043312 |
| ||||
|
Г-ДЖ |
17,40678 |
12,20672 |
24,01695 |
15,44009 |
26,53333 |
12,66473 |
0,0044892 |
| ||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 Статистически значимые различия (р < 0,05) между всеми группами;
2 Статистически значимые различия (р < 0,05) между 1-й группой и 2–3 группами;
4 Статистически значимые различия (р < 0,05) между 2-й группой и 1, 3 группами;
5 Статистически значимые различия (р < 0,05) между 1-й группой и 2-й группой.
КЖ-ЭНЕР – энергичность, КЖ-БОЛЬ – болевые ощущения, КЖ-ЭМОЦ – эмоциональное состояние, КЖ-СОН – сон, КЖ-СОЦ – социальная изоляция, КЖ-ФИЗ – физическая активность, КЖ-ОБЩ – общая сумма баллов по NHP.
Г-И – «истощение», Г-Ж – «желудочные» жалобы, Г-Р – «ревматические» жалобы, Г-С – «сердечные» жалобы, Г-ДЖ – общее «давление» жалоб по Гиссенскому опроснику.
Данные исследования указывают на то, что пациенты с алкогольным стеатогепатитом вполне удовлетворительно чувствуют себя, несмотря даже на клинико-лабораторные изменения. Поэтому мы часто видим впервые этих пациентов уже на стадии тяжелых осложнений цирроза печени: кровотечения из варикозно-расширенных вен пищевода и желудка или прямой кишки, печеночной энцефалопатии и др.Системное воздействие алкоголя настолько коварно, что кроме тяжелого поражения печени пациенты не «замечают» симптомов поражения ЦНС, сердечно-сосудистой, выделительной, опорно-двигательной и других систем. Очередная доза этанолсодержащего напитка нивелирует все проявления алкоголизма – тяжелого системного заболевания, определяя хорошее настроение и самочувствие пациента. При этом болезнь прогрессирует, а поражение печени нарастает.
При этом болезнь прогрессирует, а поражение печени нарастает.
В целом проблема АБП, как и алкоголизма, давно вышла за рамки чисто медицинской, превратившись в социальную болезнь общества.
Чем же мы можем помочь этим пациентам на стадии алкогольного стеатогепатита?
Сегодня существуют различные методики, от психотерапевтических до медикаментозных и хирургических, по лечению алкоголизма и алкогольных поражений печени. Основой терапии алкогольной болезни печени является полное воздержание от алкоголя. Пациенты часто не могут достичь полного и прочного отказа от приема алкоголя без посторонней помощи, поэтому является целесообразным лечение, направленное на борьбу с химической зависимостью. Для этой цели с успехом применяются сегодня как дисульфирам [15], так и высокоэффективные налтрексон и акампросат (ацетимотаурин) [16–20]. Госпитализация показана пациентам с желтухой, энцефалопатией, асцитом, кровотечением, лихорадкой и другими грозными осложнениями. Почти все пациенты с алкогольным гепатитом имеют различные степени недоедания, но оценка тяжести трофологических расстройств остается проблемой, т. к. нет высокочувствительных и специфичных клинических или лабораторных параметров для этих больных. Также у этих пациентов часто выявляется дефицит по ряду витаминов и микроэлементов, включая витамины А, D, тиамин, фолиевую кислоту, пиридоксин, цинк и ряд других компонентов [21].
Степень недоедания у этих больных напрямую определяет краткосрочную (1 месяц) и долгосрочную (1 год) смертность. В течение 1 года с момента постановки диагноза алкогольного гепатита у пациентов с легкой степенью недоедания регистрируется 14%-ная смертность, по сравнению с 76%-ной смертностью у пациентов с тяжелой степенью недостаточности питания [22]. Энтеральное питание для таких пациентов предпочтительнее парентерального, а количество белка в рационе должно обеспечивать положительный баланс азота [23–25].
Применение кортикостероидов как специфическая терапия при алкогольном гепатите вызывает большой интерес у гепатологов всего мира. Три рандомизированных контролируемых исследования, изучающих применение кортикостероидов (преднизолон 40 мг/сут или его эквивалент метилпреднизолон 28 мг/сут в течение 28 дней) у пациентов с тяжелым острым алкогольным гепатитом, указывают на достоверное повышение непосредственной выживаемости таких больных [26, 27]. Результаты других рандомизированных контролируемых исследований противоречивы [28, 29]. Современные практические рекомендации поддерживают использование кортикостероидов у пациентов, у которых диагноз тяжелого алкогольного гепатита является бесспорным [30]. Однако эффективность кортикостероидов не была оценена у пациентов с почечной недостаточностью, активной инфекцией, панкреатитом, желудочно-кишечными кровотечениями и некоторыми другими тяжелыми осложнениями.
Нарушение регуляции цитокинов, включая фактор некроза опухоли (TNF) и некоторые другие, играет ключевую роль в патофизиологии алкогольного стеатогепатита. Наиболее изучен в группе антицитокиновых препаратов при АБП, пентоксифиллин, который является ингибитором синтеза TNF. Повышение уровня TNF было связано с более высокой смертностью от алкогольного гепатита. В ряде рандомизированных двойных слепых контролируемых исследований по применению пентоксифиллина при алкогольном гепатите регистрировалось значительное снижение указанного показателя [31, 32].
Алкогольный стеатогепатит, особенно острый, является наиболее распространенным показанием для трансплантации органа после хронических заболеваний печени в ряде стран Европы, Северной Америки и др. [33, 34]. В России на сегодняшний день выполняется очень малое количество таких операций. На «вооружении» отечественных гастроэнтерологов, терапевтов, реаниматологов, которые сталкиваются с необходимостью проведения эффективной терапии АБП, сегодня находятся препараты различных механизмов действия, которые объединены в группу «гепатопротекторов». К ним относятся в первую очередь адеметионин и урсодезоксихолевая кислота. Определенный эффект отмечен при использовании орнитин-аспартата, силимарина, липоевой кислоты и некоторых других средств.
Заключение
Как подчеркивается в самых последних международных руководствах, медицинские работники должны быть внимательны к признакам скрытого злоупотребления алкоголем [23]. Многие пациенты часто скрывают употребление алкоголя. Кроме того, не существует никаких клинических или лабораторных признаков, специфических для алкогольной болезни печени. Алкогольная зависимость пациента определяется по физической толерантности и симптомам абстиненции. Очень удобно использовать скрининговую анкету CAGE:
С – Испытывали ли Вы потребность напиться «до отключения»?
А – Возникает ли у Вас раздражение в ответ на намеки, касающиеся употребления алкоголя?
G – Появляется ли у Вас чувство вины за избыточное употребление алкоголя?
Е – Употребляете ли Вы алкоголь по утрам для устранения похмелья?
Данная анкета является предпочтительным инструментом скрининга алкогольной зависимости при более чем 2 положительных ответах (чувствительность 71% и специфичность 95%) [35].
При выявлении АБП необходимо применять все современные методы лечения, включая медикаментозные, чтобы максимально сохранить здоровье пациента, несмотря на нестандартное течение этого тяжелого заболевания и отношение самого больного к своему состоянию.
Литература
1. Patrick CH. Alcohol, Culture, and Society. Durham, NC: Duke University Press; 1952. — Р. 12-13.
2. Savolainen VT, Liesto K. Männikkö A, et al: Alcohol consumption and alcoholic liver disease: Evidence of a threshold level of effects of ethanol. Alcohol Clin Exp Res 1993;17(5):1112-1117.
3. Lelbach WK: Cirrhosis in the alcoholic and its relation to the volume of alcohol abuse. Ann NY Acad Sci 1975;252:85-105.
4. Grant BF, Dufour MC, Harford TC: Epidemiology of alcoholic liver disease. Semin Liver Dis 1988;8(1):12-25.
5. Crabb DW. Pathogenesis of alcoholic liver disease: newer mechanisms of injury. Keio J Med 1999;48:184-188.
6. Lieber CS, Jones DP, Decarli LM. Effects of prolonged ethanol intake: production of fatty liver despite adequate diets. J Clin Invest 1965;44: 1009-1021.
7. Mendenhall CL. Anabolic steroid therapy as an adjunct to diet in alcoholic hepatic steatosis. Am J Dig Dis 1968;13:783-791.
8. Leevy CM. Fatty liver: a study of 270 patients with biopsy proven fatty liver and review of the literature. Medicine (Baltimore) 1962;41:249-276.
9. Sorensen TI, Orholm M, Bentsen KD, Hoybye G, Eghoje K, Christoffersen P. Prospective evaluation of alcohol abuse and alcoholic liver injury in men as predictors of development of cirrhosis. Lancet 1984;2:241-244.
10. NIAAA. Eighth Report to the U.S. Congress on Alcohol and Health, 1994.
11. Maddrey WC: Alcoholic hepatitis: Clinicopathologic features and therapy. Semin Liv Dis 1998;8(1):91-102.
12. O’Shea RS, Dasarathy S, McCullough AJ: Alcoholic Liver Disease. Hepatology 2010;51(1):307-328.
13. Новик А.А., Ионова Т.И. Руководство по исследованию качества жизни в медицине. СПб.:Издательский дом «Нева», 2002. – 320с.
14. Голдынкина, Е.А. Гиссенский опросник давления соматических жалоб. / Е.А. Голдынкина, Г.Л. Исурина. // Методическое пособие. – СПб.: Психоневрологический институт им. В.М.Бехтерева. 1992 – 24с.
15. Pharmacotherapy for alcohol dependence. Summary, Evidence Report/Technology Assessment: Number 3, January 1999. Agency for Health Care Policy and Research. Rockville, MD.
16. Srisurapanont M, Jarusuraisin N. Opioid antagonists for alcohol dependence. Cochrane Database Syst Rev 2005;CD001867.
17. Palmer AJ, Neeser K, Weiss C, Brandt A, Comte S, Fox M. The longterm cost-effectiveness of improving alcohol abstinence with adjuvant acamprosate. Alcohol Alcohol 2000;35:478-492.
18. Mason BJ. Acamprosate in the treatment of alcohol dependence. Expert Opin Pharmacother 2005;6:2103-2115.
19. Anton RF, O’Malley SS, Ciraulo DA, Cisler RA, Couper D, Donovan DM, et al. Combined pharmacotherapies and behavioral interventions for alcohol dependence: the COMBINE study: a randomized controlled trial. JAMA 2006;295:2003-2017.
20. Addolorato G, Leggio L, Ferrulli A, Cardone S, Vonghia L, Mirijello A, et al. Effectiveness and safety of baclofen for maintenance of alcohol abstinence in alcohol-dependent patients with liver cirrhosis: randomised, double-blind controlled study. Lancet 2007;370:1915-1922.
21. Mezey E. Interaction between alcohol and nutrition in the pathogenesis of alcoholic liver disease. Semin Liver Dis 1991;11:340-348.
22. Mendenhall CL, Tosch T, Weesner RE, et al: VA cooperative study on alcoholic hepatitis II: Prognostic significance of protein-calorie malnutrition. Am J Clin Nutr 1986;43:213-218.
23. O’Shea RS, Dasarathy S, McCullough AJ: Alcoholic Liver Disease. Hepatology 2010;51(1):307-328.
24. Mendenhall CL, Tosch T, Weesner RE, et al: VA cooperative study on alcoholic hepatitis II: Prognostic significance of protein-calorie malnutrition. Am J Clin Nutr 1986;43:213-218.
25. Schenker S, Halff GA: Nutritional therapy in alcoholic liver disease. Semin Liver Dis 1993;13(2):196-209.
26. Carithers RL, Herlong HF, Diehl AM, et al: Methylprednisolone therapy in patients with severe alcoholic hepatitis. Ann Intern Med 1989;110:685-690.
27. Ramond MJ, Poynard T, Rueff B, et al: A randomized trial of prednisolone in patients with severe alcoholic hepatitis. N Engl J Med 1992;326:507-512.
28. Depew W, Boyer T, Omata M, et al: Double-blind controlled trial of prednisolone therapy in patients with severe acute alcoholic hepatitis and spontaneous encephalopathy. Gastroenterol 1980;78(3):524-529.
29. Theodossi A, Eddleston ALWF, Williams R: Controlled trial of methylprednisolone therapy in severe acute alcoholic hepatitis. Gut 1982; 23(1):75-79.
30. O’Shea RS, Dasarathy S, McCullough AJ: Alcoholic Liver Disease. Hepatology 2010;51(1):307-328.
31. Akriviadis E, Botla R, Briggs W, Han S, Reynolds T, Shakil O. Pentoxifylline improves short-term survival in severe acute alcoholic hepatitis: a double-blind, placebo-controlled trial. Gastroenterology 2000;119: 1637-1648.
32. Menon KV, Stadheim L, Kamath PS, Wiesner RH, Gores GJ, Peine CJ, et al. A pilot study of the safety and tolerability of etanercept in patients with alcoholic hepatitis. Am J Gastroenterol 2004;99:255-260.
33. Burra P, Lucey MR. Liver transplantation in alcoholic patients. Transpl Int 2005;18:491-498.
34. O’Grady JG. Liver transplantation alcohol related liver disease: (deliberately) stirring a hornet’s nest! Gut 2006;55:1529-1531.
35. Aertgeerts B. Buntinx F, Kester A: The value of the CAGE in screening for alcohol abuse and alcohol dependence in general clinical populations: a diagnostic meta-analysis. J Clin Epidemiol 2004;57:30-39.
Алкогольная болезнь печени — CMT-Kazan.ru
Этиловый спирт обладает прямым ядовитым воздействием на клетки печени. Поэтому регулярный приём алкоголя ведет к появлению функциональных и морфологических изменений в печени. Степень поражения печени при злоупотреблении алкоголем зависит от количества потребляемого алкоголя, времени, в течение которого печень подвергается воздействию этого ядовитого для нее вещества и индивидуальной восприимчивости к нему каждого конкретного человека.
Сопутствующая информация: кодирование от алкоголизма, лечебный плазмаферез, вывод из запоя
При хроническом потреблении алкоголя отмечаются три основных патологических изменения печени:
Фиброз : патологоческое изменение, связанное с чрезмерным или постоянным потреблением алкоголя. Фиброз печени часто сравнивают с прогрессирующим в печени рубцом. Фиброз печени представляет собой процесс рубцевания с накоплением фиброзной ткани с замещением паренхимы печени на рубцовую ткань, при этом последней стадией является цирроз.
Стеатоз : накопление жира в клетках печени вследствие превращения алкоголя в триглицериды. Степень стеатоза определяется в зависимости от количества клеток печени с цитоплазматическими включениями. Более распространенное название стеатоза — «жировая дистрофия печени».
АСГ(алкогольный стеатогепатит) — воспаление печени вследствие злоупотребления алкоголем. Активность стеатогепатита определяется выраженностью гепатоцеллюлярного некроза, полинуклеарной инфильтрацей, баллонизацей и наличим телец Мэллори. Алкогольный стеатогепатит часто сравнивают с ожогом.
Диагностика алкогольного поражения печени и прогноза развития болезни проводится с помощью неинвазивных биохимических тестов (альтернатива биопсии печени), эластометрии паренхимы печени, УЗИ.
В зависимости от стадии заболевания, степени активности патологического процесса мы подбираем объем лечебных мероприятий. В клинической практике мы используем только проверенные схемы лечения.
«Центр Медицинской Токсикологии» специализируется на диагностике и лечении токсических поражений печени. Записаться на приём к гепатологу вы можете по телефону (843) 258-77-92 с 8.00 до 20.00, ежедневно. Наш адрес: ул.Ноксинский спуск, дом 45.
Алкогольная болезнь печени — klinika64.ru
Действие алкоголя на людей имеет многофакторный характер, индивидуально и очень вариабельно. В большинстве случаев поражаются головной мозг, поджелудочная железа, реже сердце, почки. Однако при злоупотреблении спиртными напитками в центре событий находиться печень. Алкогольная болезнь печени проявляется тремя основными вариантами: жировой гепатоз или стеатоз печени, гепатит (острый и хронический стеатогепатит), цирроз печени. Эти формы являются стадиями алкогольной болезни, могут встречаться как изолированно, так и в сочетании друг с другом.
Жировой гепатоз относиться к наиболее часто встречаемой форме. Он обнаруживается более чем у половины пациентов, может протекать бессимптомно и диагностируется при случайном обследовании. Суть болезни заключается в накоплении жира в клетках печени в результате нарушения обмена веществ под действием алкоголя. При этом отмечается увеличения органа в размерах. Основная жалоба это боль, чувство тяжести и дискомфорта в правом подреберье. Печеночные ферменты (Аст и Алт) в норме. Диагноз подтверждает при ультразвуковом исследовании брюшной полости, которое выявляет гепатомегалию и стеатоз. При строгом воздержании от спиртного жировой гепатоз претерпевает обратное развитие в течение 4 недель. Если же злоупотребление алкоголем продолжается, то неизбежно наступает следующая стадия — алкогольный стеатогепатит. Алкогольный стеатогепатит сопровождается обязательным повышением печеночных ферментов (Аст, Алт), которые указывает на разрушение печени. На месте разрушенных клеток формируется фиброзная ткань, «рубцы», что, в конечном счете, ведет к цирротической трансформации. Острый алкогольный гепатит развивается при употреблении большого количества алкоголя, обычно после запоя, является серьезным и угрожающим жизни звеном алкогольной болезни печени. К сожалению, в большинстве случаев, особенно в первое время пациенту удается скрыть от врача факт злоупотребления и тем самым осложнить диагностику и отсрочить назначение необходимого лечения. Острый алкогольный гепатит протекает с желтухой, лихорадкой, выраженной слабостью. Отмечается значительное увеличение печени. За счет скопления жидкости в брюшной полости, увеличивается в объеме живот. Могут присутствовать отеки на ногах. Спонтанно возникают носовые кровотечения, появляются синяки. Зачастую больной эйфоричен или заторможен, неадекватен. Острый алкогольный гепатит требует немедленной госпитализации пациента. Лечение длительное, под тщательным медицинским наблюдением и может продолжаться до полугода. Несмотря на все прилагаемые усилия смертность в этой группе пациентов очень велика. Кроме того, даже после одного эпизода острого алкогольного гепатита у половины больных формируется цирроз печени, который, к сожалению, является не обратимым. Цирроз на стадии компенсации не имеет каких-либо внешних проявлений. С течением времени, при продолжающем возлиянии, наступает декомпенсация: снижается масса тела, появляется асцит, отеки, увеличивается в размерах селезенка. Уменьшается количество гемоглобина, лейкоцитов (белых клеток крови), тромбоцитов. Нарушается система свертываемости крови, снижается синтез белка. В пищеводе при эзофагогастродуоденоскопии выявляются ворикозно расширенные вены, кровотечение из которых является одной из основных причин смерти.
Своеобразие алкогольной болезни печени придают общие характерные признаки алкогольной интоксикации. Так, «Любительница абсента» Пабло Пикассо — пример глубоко пьющей женщины. Замечен и красный нос, и тусклый взгляд, и болезненная худоба, которая характерна для далеко зашедшей стадии алкоголизма. Признаки алкогольной интоксикации наблюдаются часто и хотя бы один из них, отмечается 90 % больных. Прежде всего, бросается в глаза внешний облик много пьющего человека. Типична гиперемия, иногда синюшность лица. По поводу чего можно вспомнить шутливые строки М. Булгакова о киевском князе Владимире, «прозванном за свою любовь к спиртным напиткам «Красным солнышком». Наблюдаются множественные сосудистые звездочки на лице и зоне декольте. Возможно увеличение слюнных желез (щеки хомячка), у мужчин увеличение грудных желез. Типичен тремор рук и кончика языка. У большинства, особенно после запоя, определяется артериальная гипертензия, которая, у 2/3 исчезает в течение недели воздержания от алкоголя.
Вовремя начатое лечение алкогольной болезни печени может привести к обратному развитию процесса вплоть до полного излечения и бесспорно самым эффективным способом лечения является полное, категоричное воздержания от дальнейшего приема этанола (абстиненция). Абстиненция делает более благоприятным течение любой стадии заболевания. Продолжение приема алкоголя относится к абсолютному противопоказанию к пересадке печени. Из лекарственных средств наиболее часто применяются S-аденозилметионин (гептрал) и урсодезоксихолиевая кислота. При тяжелой форме острого алкогольного гепатита показано назначение кортикостероидов или пентоксифиллина. Декомпенсация цирроза лечится по общим правилам основных осложнений этой стадии (терапия отечно-асцитического синдрома, портальной гипертензии, энцефалопатии).
Прогноз алкогольной болезни печени во многом зависит от того сможет ли больной преодолеть алкогольную зависимость, что в свою очередь зависит от поддержки семьи, финансовых возможностей и социально-экономического положения.
Алкогольный стеатоз в клетках печени
Abstract
Считалось, что вызванная алкоголем жировая дистрофия печени (стеатоз) является результатом чрезмерного образования восстанавливающих эквивалентов в результате метаболизма этанола, тем самым увеличивая накопление жира. Недавние открытия выявили более сложную картину, при которой окисление этанола все еще необходимо, но специфическая транскрипция, а также гуморальные факторы также играют важную роль. Участвующие факторы транскрипции включают белок 1, связывающий регуляторный элемент стерола (SREBP-1), который активируется для индукции генов, регулирующих биосинтез липидов.Напротив, потребление этанола вызывает общее подавление окисления липидов (жирных кислот), что является отражением инактивации рецептора-альфа, активируемого пролифератором пероксисом (PPAR-α), который регулирует гены, участвующие в окислении жирных кислот. Третий фактор транскрипции — это реакция раннего роста-1 (Egr-1), которая сильно индуцируется до начала стеатоза. Активность всех этих факторов регулируется основным регуляторным ферментом, AMP-киназой. Важные гуморальные факторы, включая адипонектин и фактор некроза опухоли-α (TNF-α), также регулируют стеатоз, вызванный алкоголем.На их уровень влияет потребление алкоголя и друг друга. В этом обзоре кратко описаны действия этих белков при ожирении печени, вызванном этанолом. Поскольку в настоящее время стеатоз рассматривается как значительный фактор риска прогрессирующей патологии печени, понимание молекулярных механизмов его этиологии имеет важное значение для разработки эффективных методов лечения.
Ключевые слова: Метаболизм этанола, Жировая печень, белок, связывающий регуляторный элемент стерола, Рецептор, активируемый пролифератором пероксисом, Ранний ростовой ответ-1, Токсичность жирных кислот, триглицериды, ацетальдегид, активные формы кислорода
ВВЕДЕНИЕ
Жировая печень (стеатоз) это самый ранний и наиболее частый ответ печени на умеренные или большие дозы (т.е. разгул) алкоголя, а также к хроническому употреблению этанола [1]. Стеатоз ранее считался относительно безвредным побочным эффектом чрезмерного употребления алкоголя. Однако недавние данные показывают, что ожирение печени, вызванное алкоголем, увеличивает восприимчивость печени к более серьезным патологиям, если употребление алкоголя продолжается. Лица с алкогольным стеатозом подвержены развитию алкогольного стеатогепатита (АСГ), фиброза печени, цирроза и даже гепатоцеллюлярной карциномы. Ожирение, которое может усиливать алкогольную жировую дистрофию печени, также считается дополнительным фактором риска алкогольного цирроза [2] и прогрессирующего заболевания печени у трезвенников [3].Последний чаще всего клинически проявляется как неалкогольный стеатогепатит (НАСГ). Причина (ы), почему у некоторых людей жировая дистрофия печени прогрессирует до более поздних стадий заболевания печени, не ясна. Современная концепция, принятая многими исследователями, — это гипотеза о двух ударах, согласно которой первый удар — это стеатоз. За этим следует второй «удар» в виде продукции цитокинов (например, TNF-α), митохондриальной дисфункции и / или окислительного стресса. Считается, что все три этих «попадания» являются основными причинами повреждения печени, вызванного алкоголем, и могут усугубить начальный стеатоз.Развивающаяся концепция, которая получает все большее распространение, заключается в том, что определенные накопленные жирные кислоты токсичны для печени, но их токсичность снижается за счет этерификации глицерином с образованием триацилглицеринов (триглицеридов). Таким образом, накопление липидов в печени, вызванное этанолом, а также накопление липидов из пищевых источников, вызвало новый интерес как краеугольный камень токсичности для печени, поскольку он может не только инициировать, но и усиливать прогрессирование алкогольной болезни печени. В этом обзоре будут обсуждаться как метаболические, так и молекулярные факторы, которые способствуют стеатозу, вызванному этанолом.Также будет рассмотрен возможный механизм (ы), с помощью которого повреждение печени инициируется для развития прогрессирующей патологии печени.
МЕТАБОЛИЗМ ЭТАНОЛА И ЖИРНАЯ ПЕЧЕНЬ
Печень является основным местом метаболизма этанола, поскольку гепатоциты экспрессируют основные ферменты метаболизма этанола, алкогольдегидрогеназу (АДГ) и цитохром P450 2E1 (CYP2E1) на более высоких уровнях, чем в любой другой ткани [4 -6]. ADH с константой Михаэлиса от 1 до 2 ммоль / л. катализирует окисление этанола, используя НАД в качестве кофермента в реакции, которая образует ацетальдегид и восстановленный НАД (т.е.е. NADH + ) в реакции (1) ниже. Было показано, что это и последующее окисление ацетальдегида до ацетата с образованием другого восстанавливающего эквивалента NADH + в реакции, катализируемой альдегиддегидрогеназой (ALDH) в реакции (2), приведенной ниже, вызывают значительные изменения окислительно-восстановительного потенциала клетки и обеспечивают большее наличие субстрата для синтеза жирных кислот.
Math
Повышенное образование восстановленного НАД также нарушает митохондриальное β-окисление жирных кислот, тем самым снижая скорость окисления липидов.Это метаболическое объяснение ожирения печени было преобладающей концепцией в течение ряда лет, но его было недостаточно для объяснения быстрого образования ожирения печени после острого введения этанола. Кроме того, степень изменения окислительно-восстановительного потенциала печени in vivo после хронического введения этанола грызунам была значительной, но довольно скромной. Таким образом, метаболическое объяснение вызванной алкоголем ожирения печени стало недостаточным для объяснения всех изменений липидов печени после употребления этанола.Более поздние открытия в передаче клеточных сигналов и характеристике специфических факторов транскрипции побудили к исследованиям специфических факторов, которые действуют в патофизиологии стеатоза, вызванного этанолом.
ОБНОВЛЕННЫЕ МЕХАНИЗМЫ ЭТАНОЛ-ИНДУЦИРОВАННОЙ ЖИРНОЙ ПЕЧЕНИ
Повышение синтеза липидов за счет потребления этанола
Синтез триглицеридов жирных кислот печени и фосфолипидов ускоряется после острого и хронического употребления этанола [7]. Усиленный липогенез является отражением более высокой экспрессии липогенных ферментов, включая синтазу жирных кислот, ацил-КоА-карбоксилазу (АСС), цитрат-лиазу АТФ (ACL), стеароил-КоА-десастуразу и яблочный фермент.[8,9]. Эти ферменты кодируются генами, регулируемыми фактором транскрипции, белком-1, связывающим регуляторный элемент стерола, или SREBP-1.
Активация SREBP-1 и повышенная экспрессия липогенных ферментов
За счет активации SREBP, члена семейства транскрипционных факторов, нацеленных на гены, кодирующие ферменты, участвующие в метаболизме холестерина, потребление этанола может сократить нормальный метаболизм липидов в печени, преобразовывая печень от сжигания липидов до органа, накапливающего липиды.Существует три изоформы SREBP: SREBP-1a, 1c и 2. SREBP 1a и 1c являются альтернативными формами белка, кодируемого одним и тем же экзоном. Формы 1c и 2 в основном участвуют в регуляции синтеза жирных кислот и холестерина соответственно. Все белки SREBP находятся в эндоплазматическом ретикулуме. Чтобы функционировать как фактор транскрипции, аминоконцевой домен SREBP протеолитически отщепляется от карбоксиконцевого домена в аппарате Гольджи, и фрагмент перемещается в ядро клетки.Это достигается протеолитическим расщеплением под действием двух протеаз; протеаза сайта 1 (S1P) и протеаза сайта 2 (S2P), обе расположены в аппарате Гольджи. SREBP первоначально перемещается из своего сайта в ER в Golgi с помощью белка, активирующего расщепление SREBP (SCAP). Активность SCAP чувствительна к уровням внутриклеточного холестерина и имеет в своей первичной структуре домен, чувствительный к холестерину. Когда уровни холестерина низкие, SCAP перемещает SREBP из ER в Golgi, где S1P расщепляет форму предшественника SREBP, производя связанный с мембраной промежуточный продукт.Промежуточный продукт затем расщепляется S2P для высвобождения активного домена фактора транскрипции из мембраны, что позволяет ему связываться со специфическими промоторными элементами на ДНК. В нормальных условиях, когда уровни внутриклеточного холестерина повышаются, активность SCAP подавляется, тем самым предотвращая транспорт и активацию SREBP с помощью S1P и S2P. С другой стороны, метаболизм этанола нарушает регуляторную петлю активации SBEBP и вызывает повышенное расщепление SREBP-1c, даже когда внутриклеточные уровни холестерина и / или жирных кислот высоки.Активный SREBP-1c экспериментально обнаруживается в ядерных фракциях как белок массой 65 кДа, происходящий от предшественника массой 125 кДа. Таким образом, SREBP-1c играет важную роль в развитии жировой дистрофии печени, вызванной этанолом. Ядерные фракции из печени грызунов, получавших этанол, или из культивированных клеток, способных к метаболизму этанола, имеют повышенные уровни активной формы SREBP-1c. О необходимости метаболизма этанола для индукции SREBP сообщалось с использованием культивируемых клеток, и есть значительные доказательства того, что активирующим фактором является ацетальдегид [10]. Механизм вызванной этанолом активации SREBP-1 также частично связан с ингибированием AMP-активированного белка. киназа (AMPK), более подробно описанная ниже.AMPK катализирует фосфорилирование целевых ферментов, некоторые из которых являются важными ферментами, ограничивающими скорость метаболизма липидов в печени. Ингибируя активность AMPK, этанол снимает подавление SREBP-1, вызывая его активацию и повышая его уровни в ядре.
Снижение окисления жирных кислот, вызванное этанолом: Регулирование альфа-рецептора, активируемого пролифератором пероксисом
Снижение окисления жирных кислот, вызванное этанолом: Регулирование альфа-рецептора, активируемого пролифератором пероксисом, является ядерным рецептором, который регулирует экспрессию генов, обладающих пероксисомой элементы ответа пролифератора в их промоторных областях.Несколько таких генов — это те, которые кодируют переносчики жирных кислот, включая картитин пальмитоилтрансферазу I, белки, участвующие в экспорте, такие как аполипопротеин B, микросомальный белок-переносчик триглицеридов, белок, связывающий жирные кислоты, и ацил-КоА-дегидрогеназу. PPAR-α взаимодействует с рецептором ретиноида X (RXR). Белковый комплекс активируется путем связывания с жирными кислотами, тем самым повышая экспрессию белков, участвующих в транспорте и окислении жирных кислот.
Введение этанола грызунам или воздействие этанола на культивируемые клетки, метаболизирующие этанол, вызывают общее подавление PPAR-α, что отражается в снижении связывания комплексом RXR-PPAR-α со специфической для PPAR-α промоторной последовательностью [11 ].Этот эффект этанола усиливается при воздействии на обработанные этанолом клеток гепатомы ингибитора альдегиддегидрогеназы, цианамида, и отменяется ингибитором алкогольдегидрогеназы, 4-метилпиразолом. Кроме того, RXR-PPAR-α, экстрагированный из клеток гепатомы, ранее подвергнутых воздействию этанола или ацетальдегида, плохо связывается с олигонуклеотидом, содержащим элементы ответа пролифератора пероксисомы, что указывает на то, что ацетальдегид ответственен за действие этанола. Возможно, что ацетальдегид, благодаря своей способности ковалентно связывать белки [12], может образовывать аддукты с транскрипционным комплексом PPAR-α, тем самым препятствуя его способности связывать промоторный элемент (ы).Это примечательно; однако эффект на уровне транскрипции не повсеместно подавляет все ферменты, регулируемые PPAR-α. Исследования in vivo показали, что устойчивый уровень мРНК, кодирующей ацил-КоА-дегидрогеназу со средней длиной цепи, снижается этанолом, но мРНК, кодирующие другие PPAR-α-чувствительные ферменты, в том числе упомянутые выше, подвергаются минимальному влиянию, не затрагиваются и белка, связывающего жирные кислоты, фактически индуцированного этанолом. Объяснение этому, как описано Юом и Краббом [13], заключается в том, что регулирование окисления жирных кислот контролируется не только активностью ферментов окисления жирных кислот.Существует дополнительная аллостерическая регуляция транспорта жирных кислот в митохондрии за счет внутримитохондриальных уровней малонил-КоА, который ингибирует карнитин-пальмитоилтрансферазу I (CPTI), тем самым предотвращая перенос производных жирных ацил-КоА в эту органеллу. При сопутствующей повышающей регуляции биосинтеза жирных кислот этанолом это важный шаг в понижающей регуляции окисления жирных кислот. Дополнительным естественным регуляторным фактором является гормон адипоцитов адипонектин.Хроническое введение этанола вызывает значительное снижение циркулирующего адипонектина, что связано с вызванным этанолом снижением окисления жирных кислот [14]. Восстановление адипонектина у животных, получавших этанол, обработкой рекомбинантной формой гормона восстанавливает окисление жирных кислот до нормального уровня. Более того, такое лечение снижает уровень TNF-α у этих животных, поскольку известно, что гормон и цитокин регулируют продукцию друг друга [13].
Также примечательно, что вызванное этанолом ингибирование окисления жирных кислот может быть обращено, что продемонстрировано экспериментами, в которых животных, получавших этанол, лечили совместно с агонистом PPAR-α, WY14, 643.Жирная печень у этих животных была заблокирована из-за индукции PPAR-α, который, в свою очередь, ускорял окисление жирных кислот, предотвращая, таким образом, ожирение печени, вызванное этанолом [15]. Эти результаты подчеркивают метаболическое значение окисления жирных кислот в устранении стеатоза и подчеркивают терапевтический потенциал этого агента и других агонистов PPAR-α в качестве дополнений к природному гормону адипонектину.
Аденозинмонофосфат-активированная протеинкиназа и алкогольная ожирение печени
Было показано, что метаболизм липидов в печени строго регулируется аденозинмонофосфат-активированной протеинкиназой (AMPK).Этот фермент, гетеротримерный белок, сам активируется AMP, а также фосфорилированием другой киназой, LKB-1. Повышенный уровень АМФ является индикатором низкого внутриклеточного энергетического заряда. Следовательно, когда AMP активирует AMPK, он подавляет энергетические пути, по-видимому, как средство сохранения энергии (АТФ). Такие пути использования АТФ обычно являются биосинтетическими и включают синтез липидов, РНК и белков. И наоборот, AMPK активирует катаболические пути производства АТФ, такие как окисление жирных кислот, цикл TCA и гликолиз.Лимитирующим ферментом в биосинтезе липидов является ацетил-КоА-карбоксилаза (АСС), активность которой подавляется посредством фосфорилирования с помощью AMPK [16]. АСС катализирует карбоксилирование ацетил-КоА до малонил-КоА. Последний является мощным ингибитором окисления липидов, и его снижение уровня потенцирует митохондриальный транспорт и окисление жирных кислот.
Когда этанол добавляется к культивируемым клеткам гепатомы, окисляющим этанол, он индуцирует транскрипцию промотора, регулируемого SREBP, и увеличивает уровни зрелой формы SREBP-1.Оба эти эффекта блокируются включением в культуральную среду 5-аминоимидазол-4-карбоксамид рибонуклеозида (AICAR) или метформина, обоих активаторов AMPK [17]. Кроме того, сверхэкспрессия AMPK в этих клетках блокирует индуцированное этанолом повышение активности промотора и белка SREBP. Воздействие этанола на клетки снижает активность AMPK. Исследования in vivo подтверждают эти выводы. Кормление мышей этанольной диетой значительно снижает активность печеночного AMPK, одновременно увеличивая активность ограничивающего скорость фермента, ACC [17].В то же время снижается окисление жирных кислот. Эти данные демонстрируют, что AMPK регулирует вызванную этанолом активацию SREBP-1 и развитие стеатоза. Они также демонстрируют терапевтическую ценность AICAR и метформина в предотвращении и / или обращении вспять ожирения печени, вызванного не только этанолом, но и диетической индукцией. Последнее было продемонстрировано на экспериментальных животных с дефицитом лептина, получавшими метформин [18]. Таким образом, центральная роль AMPK в регулировании этих активностей хорошо иллюстрируется влиянием этанола на формирование жировой ткани печени.
Роль Egr-1 в вызванном этанолом стеатозе
Другой фактор транскрипции, ранний ростовой ответ-1 (Egr-1), также, по-видимому, играет роль в вызванном этанолом стеатозе. Egr-1, также известный как фактор роста нервов 1-A (NGF1-A), является непосредственным ранним геном и фактором транскрипции, который регулирует гены, участвующие в реакции на клеточный стресс. Ранние исследования показали, что Egr-1 индуцируется в ответ на факторы роста [19,20]. Некоторые гены, относящиеся к повреждению печени, вызванному алкоголем, имеют промоторные области, которые связывают Egr-1.Среди этих генов есть те, которые кодируют фактор роста тромбоцитов (PDGF), трансформирующий фактор роста бета (TGF-β) и молекулу межклеточной адгезии-1 (ICAM-1) [21]. В частности, что касается ожирения печени, вызванного этанолом, Egr-1 также связывает ген, кодирующий фактор некроза опухоли альфа (TNF-α) [22]. Это последнее открытие заслуживает внимания, поскольку этот цитокин считается липогенным, вызывая активацию SREBP-1, тем самым усиливая биосинтез липидов [23]. Возможно, наиболее убедительным доказательством важности Egr-1 при стеатозе, вызванном этанолом, является сообщение McMullen et al [24], который показал, что, в отличие от мышей дикого типа, у которых развивается ожирение печени в ответ на хроническое введение этанола, что у Egr-1 нулевых мышей не обнаруживается ни стеатоза печени, ни повышенного уровня TNF-α после четырех недель хронического кормления этанолом.Эти рабочие также сообщили об увеличении выработки Egr-1 у мышей, получавших этанол и получавших липополисахарид (LPS), по сравнению с контрольными мышами, получавшими такое же лечение. Данные свидетельствуют о том, что отсутствие Egr-1 предотвращает ожирение печени, вызванное этанолом, и снижает чувствительность к LPS. Исследования Zhou et al [1] продемонстрировали, что через 90 минут после острой дозы этанола (6 г / кг массы тела) уровни TNF-α в печени повышаются в три раза, а затем уровни триглицеридов в печени. Хотя эти исследователи не измеряли Egr-1, они показали тесную связь между повышенными уровнями эндотоксина в плазме, окислительным стрессом и TNF-α у мышей, получавших этанол, предполагая, что эндотоксин, через окислительный стресс , стимулирует производство TNF. -α.Последнее может быть результатом усиленной транскрипции Egr-1.
Хотя Egr-1 синтезируется быстро, его уровни также регулируются через деградацию протеасомой [25]. Было высказано предположение, что ингибирование активности протеасом введением этанола играет особую роль в увеличении белка SREBP-1, который также является субстратом протеасомы [17]. Сходным образом уровни PPAR-α и RXR контролируются убиквитин-протеасомным путем [26,27]. Таким образом, слишком сильное ингибирование протеасом также может способствовать индуцированному этанолом повышению Egr-1.Недавние эксперименты в нашей лаборатории показали, что однократное введение этанола мышам дикого типа вызывает повышение как мРНК Egr-1, так и уровня белка в печени этих животных через один час после введения этанола. Эти повышения предшествуют вызванному этанолом повышению триглицеридов, обнаруживаемому через 3 часа. В культивируемых клетках гепатомы, которые метаболизируют этанол, сверхэкспрессия Egr-1 после трансфекции аденовирусным вектором экспрессии Egr-1 увеличивает накопление триглицеридов в этих клетках по сравнению с контрольными клетками.Кроме того, воздействие этанола на трансфицированные клетки вызывает дальнейшее повышение уровня Egr-1 с одновременным повышением клеточных триглицеридов (Donohue, неопубликовано). Эти данные предоставляют дополнительные доказательства важной роли Egr-1 в индуцированной этанолом жировой ткани печени и возможности того, что он может инициировать последующие события. Они также предполагают, что в культивируемых клетках может иметь место посттрансляционная регуляция Egr-1 через подавление активности протеасом, вызываемое этанолом . Хотя Egr-1 регулирует экспрессию TNF-α, он также связывается с промоторными областями других генов, включая тот, который кодирует трансформирующий фактор роста-β (TGF-β), который играет важную роль в фиброзе печени [28].Таким образом, Egr-1 может быть основным фактором не только при стеатозе, но и на более поздних стадиях вызванного алкоголем повреждения печени, как предположили Pritchard и Nagy [20].
Алкогольный стеатоз: Что такое настоящий токсин?
В предыдущих разделах были описаны молекулярные механизмы, с помощью которых потребление этанола нарушает метаболизм липидов в печени, что приводит к ожирению печени. Как указывалось ранее, развивающаяся концепция, которая получает все большее распространение, заключается в том, что определенные накопленные жирные кислоты токсичны для печени, но их токсичность ослабляется этерификацией глицерином с образованием триацилглицеринов (триглицеридов).По иронии судьбы, накопление триглицеридов является основным средством количественной оценки ожирения печени. Таким образом, вопрос о том, существует ли общая токсичность накопленных жирных кислот или что определенные жирные кислоты являются гепатотоксичными, важен для определения того, подвержены ли алкоголики риску более поздней стадии заболевания. В недавней работе Yamaguchi et al [30,31] использовался антисмысловой олигонуклеотид (ASO) для блокирования синтеза диацилглицерин-ацилтрансферазы (DAG), тем самым подавляя синтез триглицеридов. Блокада DAG, который катализирует заключительный этап синтеза триглицеридов, уменьшала стеатоз печени у этих животных, когда они получали диету с дефицитом метионина и холина для индукции НАСГ.Однако такое лечение с помощью ASO усугубляло повреждение печени, вызывая фиброз, несмотря на то, что уровни TNF-α были снижены, уровни адипонектина были увеличены, а чувствительность к инсулину улучшилась. Объяснение этих результатов заключается в том, что предотвращение синтеза триглицеридов увеличивает внутриклеточные уровни свободных жирных кислот в печени. Хотя конкретные жирные кислоты не были идентифицированы, тот факт, что усиленное перекисное окисление липидов произошло у животных с повреждением печени, предполагает, что накопление ненасыщенных жирных кислот, скорее всего, будет инкриминировано как вызывающее дальнейшее повреждение печени.Что касается стеатоза, вызванного этанолом, имеется значительный объем доказательств того, что ненасыщенные жирные кислоты из кукурузного масла или рыбьего жира вызывают большее повреждение печени, чем насыщенные жирные кислоты, когда любая из них употребляется в сочетании с алкоголем.
ЗАКЛЮЧЕНИЕ
Вышеупомянутый обзор суммировал как ранее, так и в настоящее время принятые модели жировой дистрофии печени, вызванной алкоголем. Таким образом, потребление этанола вызывает активацию SREBP-1, который индуцирует гены, участвующие в биосинтезе липидов.Напротив, потребление этанола подавляет фактор транскрипции PPAR-α, который регулирует ферменты, участвующие в окислении жирных кислот, и одновременно предотвращает импорт жирных кислот в митохондрии для окисления. Регулирование Egr-1 этанолом — менее хорошо изученная, но важная область исследования, так как его быстрая индукция может быть выше двух последних факторов или может осуществлять координированную регуляцию вместе с SREBP-1 и PPAR-α. Наконец, следует подчеркнуть, что в разделах этого обзора АСГ сравнивали с другими жировыми заболеваниями печени, включая НАСГ.Последнее использовалось просто как аналогичное заболевание, но не предполагалось, что эти два заболевания (ASH и NASH) — одно и то же. Очевидно, что необходимы дальнейшие исследования патофизиологии стеатоза, вызванного этанолом, но недавние исследования продемонстрировали значительный прогресс в отношении терапевтических мер. Эти последние открытия наверняка подтолкнут к дальнейшим действиям по предотвращению или уменьшению повреждения печени, вызванного злоупотреблением алкоголем.
Алкоголь-индуцированный стеатоз в клетках печени
Abstract
Алкоголь-индуцированный жировой гепатоз (стеатоз) считается результатом чрезмерного образования восстанавливающих эквивалентов в результате метаболизма этанола, тем самым увеличивая накопление жира.Недавние открытия выявили более сложную картину, при которой окисление этанола все еще необходимо, но специфическая транскрипция, а также гуморальные факторы также играют важную роль. Участвующие факторы транскрипции включают белок 1, связывающий регуляторный элемент стерола (SREBP-1), который активируется для индукции генов, регулирующих биосинтез липидов. Напротив, потребление этанола вызывает общее подавление окисления липидов (жирных кислот), что является отражением инактивации рецептора-альфа, активируемого пролифератором пероксисом (PPAR-α), который регулирует гены, участвующие в окислении жирных кислот.Третий фактор транскрипции — это реакция раннего роста-1 (Egr-1), которая сильно индуцируется до начала стеатоза. Активность всех этих факторов регулируется основным регуляторным ферментом, AMP-киназой. Важные гуморальные факторы, включая адипонектин и фактор некроза опухоли-α (TNF-α), также регулируют стеатоз, вызванный алкоголем. На их уровень влияет потребление алкоголя и друг друга. В этом обзоре кратко описаны действия этих белков при ожирении печени, вызванном этанолом.Поскольку в настоящее время стеатоз рассматривается как значительный фактор риска прогрессирующей патологии печени, понимание молекулярных механизмов его этиологии имеет важное значение для разработки эффективных методов лечения.
Ключевые слова: Метаболизм этанола, Жировая печень, белок, связывающий регуляторный элемент стерола, Рецептор, активируемый пролифератором пероксисом, Ранний ростовой ответ-1, Токсичность жирных кислот, триглицериды, ацетальдегид, активные формы кислорода
ВВЕДЕНИЕ
Жировая печень (стеатоз) это самый ранний и наиболее частый ответ печени на умеренные или большие дозы (т.е. разгул) алкоголя, а также к хроническому употреблению этанола [1]. Стеатоз ранее считался относительно безвредным побочным эффектом чрезмерного употребления алкоголя. Однако недавние данные показывают, что ожирение печени, вызванное алкоголем, увеличивает восприимчивость печени к более серьезным патологиям, если употребление алкоголя продолжается. Лица с алкогольным стеатозом подвержены развитию алкогольного стеатогепатита (АСГ), фиброза печени, цирроза и даже гепатоцеллюлярной карциномы. Ожирение, которое может усиливать алкогольную жировую дистрофию печени, также считается дополнительным фактором риска алкогольного цирроза [2] и прогрессирующего заболевания печени у трезвенников [3].Последний чаще всего клинически проявляется как неалкогольный стеатогепатит (НАСГ). Причина (ы), почему у некоторых людей жировая дистрофия печени прогрессирует до более поздних стадий заболевания печени, не ясна. Современная концепция, принятая многими исследователями, — это гипотеза о двух ударах, согласно которой первый удар — это стеатоз. За этим следует второй «удар» в виде продукции цитокинов (например, TNF-α), митохондриальной дисфункции и / или окислительного стресса. Считается, что все три этих «попадания» являются основными причинами повреждения печени, вызванного алкоголем, и могут усугубить начальный стеатоз.Развивающаяся концепция, которая получает все большее распространение, заключается в том, что определенные накопленные жирные кислоты токсичны для печени, но их токсичность снижается за счет этерификации глицерином с образованием триацилглицеринов (триглицеридов). Таким образом, накопление липидов в печени, вызванное этанолом, а также накопление липидов из пищевых источников, вызвало новый интерес как краеугольный камень токсичности для печени, поскольку он может не только инициировать, но и усиливать прогрессирование алкогольной болезни печени. В этом обзоре будут обсуждаться как метаболические, так и молекулярные факторы, которые способствуют стеатозу, вызванному этанолом.Также будет рассмотрен возможный механизм (ы), с помощью которого повреждение печени инициируется для развития прогрессирующей патологии печени.
МЕТАБОЛИЗМ ЭТАНОЛА И ЖИРНАЯ ПЕЧЕНЬ
Печень является основным местом метаболизма этанола, поскольку гепатоциты экспрессируют основные ферменты метаболизма этанола, алкогольдегидрогеназу (АДГ) и цитохром P450 2E1 (CYP2E1) на более высоких уровнях, чем в любой другой ткани [4 -6]. ADH с константой Михаэлиса от 1 до 2 ммоль / л. катализирует окисление этанола, используя НАД в качестве кофермента в реакции, которая образует ацетальдегид и восстановленный НАД (т.е.е. NADH + ) в реакции (1) ниже. Было показано, что это и последующее окисление ацетальдегида до ацетата с образованием другого восстанавливающего эквивалента NADH + в реакции, катализируемой альдегиддегидрогеназой (ALDH) в реакции (2), приведенной ниже, вызывают значительные изменения окислительно-восстановительного потенциала клетки и обеспечивают большее наличие субстрата для синтеза жирных кислот.
Math
Повышенное образование восстановленного НАД также нарушает митохондриальное β-окисление жирных кислот, тем самым снижая скорость окисления липидов.Это метаболическое объяснение ожирения печени было преобладающей концепцией в течение ряда лет, но его было недостаточно для объяснения быстрого образования ожирения печени после острого введения этанола. Кроме того, степень изменения окислительно-восстановительного потенциала печени in vivo после хронического введения этанола грызунам была значительной, но довольно скромной. Таким образом, метаболическое объяснение вызванной алкоголем ожирения печени стало недостаточным для объяснения всех изменений липидов печени после употребления этанола.Более поздние открытия в передаче клеточных сигналов и характеристике специфических факторов транскрипции побудили к исследованиям специфических факторов, которые действуют в патофизиологии стеатоза, вызванного этанолом.
ОБНОВЛЕННЫЕ МЕХАНИЗМЫ ЭТАНОЛ-ИНДУЦИРОВАННОЙ ЖИРНОЙ ПЕЧЕНИ
Повышение синтеза липидов за счет потребления этанола
Синтез триглицеридов жирных кислот печени и фосфолипидов ускоряется после острого и хронического употребления этанола [7]. Усиленный липогенез является отражением более высокой экспрессии липогенных ферментов, включая синтазу жирных кислот, ацил-КоА-карбоксилазу (АСС), цитрат-лиазу АТФ (ACL), стеароил-КоА-десастуразу и яблочный фермент.[8,9]. Эти ферменты кодируются генами, регулируемыми фактором транскрипции, белком-1, связывающим регуляторный элемент стерола, или SREBP-1.
Активация SREBP-1 и повышенная экспрессия липогенных ферментов
За счет активации SREBP, члена семейства транскрипционных факторов, нацеленных на гены, кодирующие ферменты, участвующие в метаболизме холестерина, потребление этанола может сократить нормальный метаболизм липидов в печени, преобразовывая печень от сжигания липидов до органа, накапливающего липиды.Существует три изоформы SREBP: SREBP-1a, 1c и 2. SREBP 1a и 1c являются альтернативными формами белка, кодируемого одним и тем же экзоном. Формы 1c и 2 в основном участвуют в регуляции синтеза жирных кислот и холестерина соответственно. Все белки SREBP находятся в эндоплазматическом ретикулуме. Чтобы функционировать как фактор транскрипции, аминоконцевой домен SREBP протеолитически отщепляется от карбоксиконцевого домена в аппарате Гольджи, и фрагмент перемещается в ядро клетки.Это достигается протеолитическим расщеплением под действием двух протеаз; протеаза сайта 1 (S1P) и протеаза сайта 2 (S2P), обе расположены в аппарате Гольджи. SREBP первоначально перемещается из своего сайта в ER в Golgi с помощью белка, активирующего расщепление SREBP (SCAP). Активность SCAP чувствительна к уровням внутриклеточного холестерина и имеет в своей первичной структуре домен, чувствительный к холестерину. Когда уровни холестерина низкие, SCAP перемещает SREBP из ER в Golgi, где S1P расщепляет форму предшественника SREBP, производя связанный с мембраной промежуточный продукт.Промежуточный продукт затем расщепляется S2P для высвобождения активного домена фактора транскрипции из мембраны, что позволяет ему связываться со специфическими промоторными элементами на ДНК. В нормальных условиях, когда уровни внутриклеточного холестерина повышаются, активность SCAP подавляется, тем самым предотвращая транспорт и активацию SREBP с помощью S1P и S2P. С другой стороны, метаболизм этанола нарушает регуляторную петлю активации SBEBP и вызывает повышенное расщепление SREBP-1c, даже когда внутриклеточные уровни холестерина и / или жирных кислот высоки.Активный SREBP-1c экспериментально обнаруживается в ядерных фракциях как белок массой 65 кДа, происходящий от предшественника массой 125 кДа. Таким образом, SREBP-1c играет важную роль в развитии жировой дистрофии печени, вызванной этанолом. Ядерные фракции из печени грызунов, получавших этанол, или из культивированных клеток, способных к метаболизму этанола, имеют повышенные уровни активной формы SREBP-1c. О необходимости метаболизма этанола для индукции SREBP сообщалось с использованием культивируемых клеток, и есть значительные доказательства того, что активирующим фактором является ацетальдегид [10]. Механизм вызванной этанолом активации SREBP-1 также частично связан с ингибированием AMP-активированного белка. киназа (AMPK), более подробно описанная ниже.AMPK катализирует фосфорилирование целевых ферментов, некоторые из которых являются важными ферментами, ограничивающими скорость метаболизма липидов в печени. Ингибируя активность AMPK, этанол снимает подавление SREBP-1, вызывая его активацию и повышая его уровни в ядре.
Снижение окисления жирных кислот, вызванное этанолом: Регулирование альфа-рецептора, активируемого пролифератором пероксисом
Снижение окисления жирных кислот, вызванное этанолом: Регулирование альфа-рецептора, активируемого пролифератором пероксисом, является ядерным рецептором, который регулирует экспрессию генов, обладающих пероксисомой элементы ответа пролифератора в их промоторных областях.Несколько таких генов — это те, которые кодируют переносчики жирных кислот, включая картитин пальмитоилтрансферазу I, белки, участвующие в экспорте, такие как аполипопротеин B, микросомальный белок-переносчик триглицеридов, белок, связывающий жирные кислоты, и ацил-КоА-дегидрогеназу. PPAR-α взаимодействует с рецептором ретиноида X (RXR). Белковый комплекс активируется путем связывания с жирными кислотами, тем самым повышая экспрессию белков, участвующих в транспорте и окислении жирных кислот.
Введение этанола грызунам или воздействие этанола на культивируемые клетки, метаболизирующие этанол, вызывают общее подавление PPAR-α, что отражается в снижении связывания комплексом RXR-PPAR-α со специфической для PPAR-α промоторной последовательностью [11 ].Этот эффект этанола усиливается при воздействии на обработанные этанолом клеток гепатомы ингибитора альдегиддегидрогеназы, цианамида, и отменяется ингибитором алкогольдегидрогеназы, 4-метилпиразолом. Кроме того, RXR-PPAR-α, экстрагированный из клеток гепатомы, ранее подвергнутых воздействию этанола или ацетальдегида, плохо связывается с олигонуклеотидом, содержащим элементы ответа пролифератора пероксисомы, что указывает на то, что ацетальдегид ответственен за действие этанола. Возможно, что ацетальдегид, благодаря своей способности ковалентно связывать белки [12], может образовывать аддукты с транскрипционным комплексом PPAR-α, тем самым препятствуя его способности связывать промоторный элемент (ы).Это примечательно; однако эффект на уровне транскрипции не повсеместно подавляет все ферменты, регулируемые PPAR-α. Исследования in vivo показали, что устойчивый уровень мРНК, кодирующей ацил-КоА-дегидрогеназу со средней длиной цепи, снижается этанолом, но мРНК, кодирующие другие PPAR-α-чувствительные ферменты, в том числе упомянутые выше, подвергаются минимальному влиянию, не затрагиваются и белка, связывающего жирные кислоты, фактически индуцированного этанолом. Объяснение этому, как описано Юом и Краббом [13], заключается в том, что регулирование окисления жирных кислот контролируется не только активностью ферментов окисления жирных кислот.Существует дополнительная аллостерическая регуляция транспорта жирных кислот в митохондрии за счет внутримитохондриальных уровней малонил-КоА, который ингибирует карнитин-пальмитоилтрансферазу I (CPTI), тем самым предотвращая перенос производных жирных ацил-КоА в эту органеллу. При сопутствующей повышающей регуляции биосинтеза жирных кислот этанолом это важный шаг в понижающей регуляции окисления жирных кислот. Дополнительным естественным регуляторным фактором является гормон адипоцитов адипонектин.Хроническое введение этанола вызывает значительное снижение циркулирующего адипонектина, что связано с вызванным этанолом снижением окисления жирных кислот [14]. Восстановление адипонектина у животных, получавших этанол, обработкой рекомбинантной формой гормона восстанавливает окисление жирных кислот до нормального уровня. Более того, такое лечение снижает уровень TNF-α у этих животных, поскольку известно, что гормон и цитокин регулируют продукцию друг друга [13].
Также примечательно, что вызванное этанолом ингибирование окисления жирных кислот может быть обращено, что продемонстрировано экспериментами, в которых животных, получавших этанол, лечили совместно с агонистом PPAR-α, WY14, 643.Жирная печень у этих животных была заблокирована из-за индукции PPAR-α, который, в свою очередь, ускорял окисление жирных кислот, предотвращая, таким образом, ожирение печени, вызванное этанолом [15]. Эти результаты подчеркивают метаболическое значение окисления жирных кислот в устранении стеатоза и подчеркивают терапевтический потенциал этого агента и других агонистов PPAR-α в качестве дополнений к природному гормону адипонектину.
Аденозинмонофосфат-активированная протеинкиназа и алкогольная ожирение печени
Было показано, что метаболизм липидов в печени строго регулируется аденозинмонофосфат-активированной протеинкиназой (AMPK).Этот фермент, гетеротримерный белок, сам активируется AMP, а также фосфорилированием другой киназой, LKB-1. Повышенный уровень АМФ является индикатором низкого внутриклеточного энергетического заряда. Следовательно, когда AMP активирует AMPK, он подавляет энергетические пути, по-видимому, как средство сохранения энергии (АТФ). Такие пути использования АТФ обычно являются биосинтетическими и включают синтез липидов, РНК и белков. И наоборот, AMPK активирует катаболические пути производства АТФ, такие как окисление жирных кислот, цикл TCA и гликолиз.Лимитирующим ферментом в биосинтезе липидов является ацетил-КоА-карбоксилаза (АСС), активность которой подавляется посредством фосфорилирования с помощью AMPK [16]. АСС катализирует карбоксилирование ацетил-КоА до малонил-КоА. Последний является мощным ингибитором окисления липидов, и его снижение уровня потенцирует митохондриальный транспорт и окисление жирных кислот.
Когда этанол добавляется к культивируемым клеткам гепатомы, окисляющим этанол, он индуцирует транскрипцию промотора, регулируемого SREBP, и увеличивает уровни зрелой формы SREBP-1.Оба эти эффекта блокируются включением в культуральную среду 5-аминоимидазол-4-карбоксамид рибонуклеозида (AICAR) или метформина, обоих активаторов AMPK [17]. Кроме того, сверхэкспрессия AMPK в этих клетках блокирует индуцированное этанолом повышение активности промотора и белка SREBP. Воздействие этанола на клетки снижает активность AMPK. Исследования in vivo подтверждают эти выводы. Кормление мышей этанольной диетой значительно снижает активность печеночного AMPK, одновременно увеличивая активность ограничивающего скорость фермента, ACC [17].В то же время снижается окисление жирных кислот. Эти данные демонстрируют, что AMPK регулирует вызванную этанолом активацию SREBP-1 и развитие стеатоза. Они также демонстрируют терапевтическую ценность AICAR и метформина в предотвращении и / или обращении вспять ожирения печени, вызванного не только этанолом, но и диетической индукцией. Последнее было продемонстрировано на экспериментальных животных с дефицитом лептина, получавшими метформин [18]. Таким образом, центральная роль AMPK в регулировании этих активностей хорошо иллюстрируется влиянием этанола на формирование жировой ткани печени.
Роль Egr-1 в вызванном этанолом стеатозе
Другой фактор транскрипции, ранний ростовой ответ-1 (Egr-1), также, по-видимому, играет роль в вызванном этанолом стеатозе. Egr-1, также известный как фактор роста нервов 1-A (NGF1-A), является непосредственным ранним геном и фактором транскрипции, который регулирует гены, участвующие в реакции на клеточный стресс. Ранние исследования показали, что Egr-1 индуцируется в ответ на факторы роста [19,20]. Некоторые гены, относящиеся к повреждению печени, вызванному алкоголем, имеют промоторные области, которые связывают Egr-1.Среди этих генов есть те, которые кодируют фактор роста тромбоцитов (PDGF), трансформирующий фактор роста бета (TGF-β) и молекулу межклеточной адгезии-1 (ICAM-1) [21]. В частности, что касается ожирения печени, вызванного этанолом, Egr-1 также связывает ген, кодирующий фактор некроза опухоли альфа (TNF-α) [22]. Это последнее открытие заслуживает внимания, поскольку этот цитокин считается липогенным, вызывая активацию SREBP-1, тем самым усиливая биосинтез липидов [23]. Возможно, наиболее убедительным доказательством важности Egr-1 при стеатозе, вызванном этанолом, является сообщение McMullen et al [24], который показал, что, в отличие от мышей дикого типа, у которых развивается ожирение печени в ответ на хроническое введение этанола, что у Egr-1 нулевых мышей не обнаруживается ни стеатоза печени, ни повышенного уровня TNF-α после четырех недель хронического кормления этанолом.Эти рабочие также сообщили об увеличении выработки Egr-1 у мышей, получавших этанол и получавших липополисахарид (LPS), по сравнению с контрольными мышами, получавшими такое же лечение. Данные свидетельствуют о том, что отсутствие Egr-1 предотвращает ожирение печени, вызванное этанолом, и снижает чувствительность к LPS. Исследования Zhou et al [1] продемонстрировали, что через 90 минут после острой дозы этанола (6 г / кг массы тела) уровни TNF-α в печени повышаются в три раза, а затем уровни триглицеридов в печени. Хотя эти исследователи не измеряли Egr-1, они показали тесную связь между повышенными уровнями эндотоксина в плазме, окислительным стрессом и TNF-α у мышей, получавших этанол, предполагая, что эндотоксин, через окислительный стресс , стимулирует производство TNF. -α.Последнее может быть результатом усиленной транскрипции Egr-1.
Хотя Egr-1 синтезируется быстро, его уровни также регулируются через деградацию протеасомой [25]. Было высказано предположение, что ингибирование активности протеасом введением этанола играет особую роль в увеличении белка SREBP-1, который также является субстратом протеасомы [17]. Сходным образом уровни PPAR-α и RXR контролируются убиквитин-протеасомным путем [26,27]. Таким образом, слишком сильное ингибирование протеасом также может способствовать индуцированному этанолом повышению Egr-1.Недавние эксперименты в нашей лаборатории показали, что однократное введение этанола мышам дикого типа вызывает повышение как мРНК Egr-1, так и уровня белка в печени этих животных через один час после введения этанола. Эти повышения предшествуют вызванному этанолом повышению триглицеридов, обнаруживаемому через 3 часа. В культивируемых клетках гепатомы, которые метаболизируют этанол, сверхэкспрессия Egr-1 после трансфекции аденовирусным вектором экспрессии Egr-1 увеличивает накопление триглицеридов в этих клетках по сравнению с контрольными клетками.Кроме того, воздействие этанола на трансфицированные клетки вызывает дальнейшее повышение уровня Egr-1 с одновременным повышением клеточных триглицеридов (Donohue, неопубликовано). Эти данные предоставляют дополнительные доказательства важной роли Egr-1 в индуцированной этанолом жировой ткани печени и возможности того, что он может инициировать последующие события. Они также предполагают, что в культивируемых клетках может иметь место посттрансляционная регуляция Egr-1 через подавление активности протеасом, вызываемое этанолом . Хотя Egr-1 регулирует экспрессию TNF-α, он также связывается с промоторными областями других генов, включая тот, который кодирует трансформирующий фактор роста-β (TGF-β), который играет важную роль в фиброзе печени [28].Таким образом, Egr-1 может быть основным фактором не только при стеатозе, но и на более поздних стадиях вызванного алкоголем повреждения печени, как предположили Pritchard и Nagy [20].
Алкогольный стеатоз: Что такое настоящий токсин?
В предыдущих разделах были описаны молекулярные механизмы, с помощью которых потребление этанола нарушает метаболизм липидов в печени, что приводит к ожирению печени. Как указывалось ранее, развивающаяся концепция, которая получает все большее распространение, заключается в том, что определенные накопленные жирные кислоты токсичны для печени, но их токсичность ослабляется этерификацией глицерином с образованием триацилглицеринов (триглицеридов).По иронии судьбы, накопление триглицеридов является основным средством количественной оценки ожирения печени. Таким образом, вопрос о том, существует ли общая токсичность накопленных жирных кислот или что определенные жирные кислоты являются гепатотоксичными, важен для определения того, подвержены ли алкоголики риску более поздней стадии заболевания. В недавней работе Yamaguchi et al [30,31] использовался антисмысловой олигонуклеотид (ASO) для блокирования синтеза диацилглицерин-ацилтрансферазы (DAG), тем самым подавляя синтез триглицеридов. Блокада DAG, который катализирует заключительный этап синтеза триглицеридов, уменьшала стеатоз печени у этих животных, когда они получали диету с дефицитом метионина и холина для индукции НАСГ.Однако такое лечение с помощью ASO усугубляло повреждение печени, вызывая фиброз, несмотря на то, что уровни TNF-α были снижены, уровни адипонектина были увеличены, а чувствительность к инсулину улучшилась. Объяснение этих результатов заключается в том, что предотвращение синтеза триглицеридов увеличивает внутриклеточные уровни свободных жирных кислот в печени. Хотя конкретные жирные кислоты не были идентифицированы, тот факт, что усиленное перекисное окисление липидов произошло у животных с повреждением печени, предполагает, что накопление ненасыщенных жирных кислот, скорее всего, будет инкриминировано как вызывающее дальнейшее повреждение печени.Что касается стеатоза, вызванного этанолом, имеется значительный объем доказательств того, что ненасыщенные жирные кислоты из кукурузного масла или рыбьего жира вызывают большее повреждение печени, чем насыщенные жирные кислоты, когда любая из них употребляется в сочетании с алкоголем.
ЗАКЛЮЧЕНИЕ
Вышеупомянутый обзор суммировал как ранее, так и в настоящее время принятые модели жировой дистрофии печени, вызванной алкоголем. Таким образом, потребление этанола вызывает активацию SREBP-1, который индуцирует гены, участвующие в биосинтезе липидов.Напротив, потребление этанола подавляет фактор транскрипции PPAR-α, который регулирует ферменты, участвующие в окислении жирных кислот, и одновременно предотвращает импорт жирных кислот в митохондрии для окисления. Регулирование Egr-1 этанолом — менее хорошо изученная, но важная область исследования, так как его быстрая индукция может быть выше двух последних факторов или может осуществлять координированную регуляцию вместе с SREBP-1 и PPAR-α. Наконец, следует подчеркнуть, что в разделах этого обзора АСГ сравнивали с другими жировыми заболеваниями печени, включая НАСГ.Последнее использовалось просто как аналогичное заболевание, но не предполагалось, что эти два заболевания (ASH и NASH) — одно и то же. Очевидно, что необходимы дальнейшие исследования патофизиологии стеатоза, вызванного этанолом, но недавние исследования продемонстрировали значительный прогресс в отношении терапевтических мер. Эти последние открытия наверняка подтолкнут к дальнейшим действиям по предотвращению или уменьшению повреждения печени, вызванного злоупотреблением алкоголем.
Алкогольная болезнь печени | Кливлендская клиника
ОпределениеОпределение
Catherine Frakes Vozzo, DO
Nicole Welch, MD
Carlos Romero-Marrero, MD
Kyrsten D.Фэрбенкс, MD
Опубликован: Июнь 2018
Срок действия: Июнь 2021
Существует 3 типа заболеваний печени, связанных с употреблением алкоголя: ожирение печени, алкогольный гепатит или цирроз (Таблица 1). Жировая болезнь печени возникает после острого употребления алкоголя и обычно обратима при воздержании. Считается, что ожирение печени не предрасполагает пациента к какой-либо хронической форме заболевания печени, если сохраняется воздержание или умеренность. Алкогольный гепатит — это острая форма вызванного алкоголем поражения печени, которое возникает при употреблении большого количества алкоголя в течение длительного периода.Алкогольный гепатит может варьироваться по степени тяжести от бессимптомного нарушения биохимии до печеночной недостаточности и смерти. Цирроз включает замену нормальной паренхимы печени обширными толстыми полосами фиброзной ткани и регенеративными узелками, что приводит к клиническим проявлениям портальной гипертензии и печеночной недостаточности.
Таблица 1. Типы алкогольных заболеваний печени
| Тип | Гистологическая специфичность в отношении алкогольной причины | Прогноз | Реверсивный |
| Жировая печень | № | Отлично | Есть |
| Гепатит алкогольный | № | Переменная | Переменная |
| Цирроз | № | Охраняемая | Обычно нет |
Эпидемиология и факторы риска
То, что известно об эпидемиологии заболеваний печени, изменилось благодаря лучшему пониманию неалкогольной жировой болезни печени и хронического вирусного гепатита.
Распространенность алкогольной болезни печени (ALD) трудно определить, поскольку на нее влияют многие факторы, включая генетические (например, склонность к злоупотреблению алкоголем, пол) и окружающую среду (например, доступность алкоголя, социальная приемлемость употребления алкоголя, сопутствующая гепатотоксичность). оскорбления) факторы. В Соединенных Штатах, по оценкам, 67,3% населения потребляет алкоголь, и 7,4% населения соответствует критериям злоупотребления алкоголем. Уровень употребления алкоголя широко варьируется во всем мире, самый высокий показатель — в США.С. и Европа. У мужчин вероятность развития АБК выше, чем у женщин, потому что мужчины потребляют больше алкоголя. Однако женщины более подвержены гепатотоксичности алкоголя и имеют в два раза больший относительный риск АБП и цирроза печени по сравнению с мужчинами. Повышенный индекс массы тела также является фактором риска развития ALD, а также неалкогольной жировой болезни печени.
Этническая принадлежность и генетика являются важными факторами, связанными с ALD. Смертность от цирроза выше у мужчин латиноамериканского происхождения, коренных американцев и коренных жителей Аляски по сравнению с белым населением.Генетические факторы, такие как наличие пататин-подобного домена фосфолипазы, содержащего ген 3 (PNPLA3) , по-видимому, связаны с более тяжелым фенотипом и плохим прогнозом.
В целом риск заболевания печени увеличивается с увеличением количества и продолжительности употребления алкоголя. Количество алкоголя в алкогольных напитках зависит от объема в зависимости от типа напитка (Таблица 2).
Таблица 2. Содержание алкоголя по видам алкогольных напитков
| Тип | Количество, унции | Спирт, граммы (г) |
| Пиво | 12 | 14 |
| Вино | 5 | 14 |
| Ликер (крепость 80) | 1.5 | 14 |
Хотя употребление алкоголя необходимо для ALD, чрезмерное употребление алкоголя не обязательно способствует развитию ALD. Среди лиц, злоупотребляющих алкоголем, только у каждого пятого развивается алкогольный гепатит, а у каждого четвертого — цирроз.
Жирная печень является универсальной находкой среди сильно пьющих, и до 40% лиц с умеренным потреблением алкоголя (10-80 мг / день) также демонстрируют жировые изменения в печени. Основываясь на серии аутопсий мужчин, пороговое суточное потребление алкоголя 40 г необходимо для возникновения патологических изменений алкогольного гепатита.Употребление более 80 г алкоголя в день связано с увеличением тяжести алкогольного гепатита, но не с общей распространенностью. Существует четкая дозозависимая связь между употреблением алкоголя и заболеваемостью алкогольным циррозом печени. Ежедневное употребление более 60 г алкоголя у мужчин и 20 г у женщин значительно увеличивает риск цирроза печени. Кроме того, ежедневное употребление алкоголя по сравнению с запоями более вредно.
ПатофизиологияПатофизиология
Печень и, в меньшей степени, желудочно-кишечный тракт, являются основными участками метаболизма алкоголя.Существует 2 основных пути метаболизма алкоголя в печени: алкогольдегидрогеназа и цитохром P450 (CYP) 2E1. Алкогольдегидрогеназа — это цитозольный фермент гепатоцитов, который превращает спирт в ацетальдегид. Впоследствии ацетальдегид метаболизируется в ацетат с помощью митохондриального фермента ацетальдегиддегидрогеназы. CYP 2E1 также превращает спирт в ацетальдегид.
Повреждение печени происходит несколькими взаимосвязанными путями. Алкогольдегидрогеназа и ацетальдегиддегидрогеназа вызывают восстановление никотинамидадениндинуклеотида (НАД) до НАДН (восстановленная форма НАД).Измененное соотношение НАД / НАДН способствует ожирению печени за счет ингибирования глюконеогенеза и окисления жирных кислот. CYP 2E1, который активируется при хроническом употреблении алкоголя, генерирует свободные радикалы за счет окисления никотинамидадениндинуклеотидфосфата (НАДФН) до НАДФ. Хроническое воздействие алкоголя также активирует макрофаги печени, которые затем продуцируют фактор некроза опухоли альфа (TNF-альфа). TNF-альфа побуждает митохондрии увеличивать производство активных форм кислорода. Окислительный стресс способствует некрозу и апоптозу гепатоцитов, что усиливается у алкоголиков с дефицитом антиоксидантов, таких как глутатион и витамин Е.Свободные радикалы инициируют перекисное окисление липидов, которое вызывает воспаление и фиброз. Воспаление также провоцируется ацетальдегидом, который, ковалентно связываясь с клеточными белками, образует антигенные аддукты.
Естественная историяЕстественная история
Спектр ALD может включать простой стеатоз печени, острый алкогольный гепатит и алкогольный цирроз.Возможно совпадение этих заболеваний.
Стеатоз печени
При воздержании от алкоголя морфологические изменения жировой ткани печени обычно возвращаются к норме. Хотя краткосрочный прогноз у пациентов с алкогольным стеатозом отличный, при более длительном наблюдении было обнаружено, что цирроз чаще развивается у лиц, злоупотребляющих алкоголем, с жировыми изменениями печени, чем у пациентов с нормальной гистологией печени. Клинические факторы риска, которые предсказывают прогрессирование фиброза, цирроза или обоих, включают тяжелый стеатоз, женский пол, продолжающееся чрезмерное употребление алкоголя, наличие мегамитохондрий, смешанный макровезикулярно-микровезикулярный стеатоз и перивенулярный фиброз по гистологии.
Гепатит алкогольный
Системымогут использоваться для оценки степени тяжести алкогольного гепатита и для руководства лечением. Оценка дискриминантной функции Мэддри (DF) более 32 или оценка модели терминальной стадии заболевания печени (MELD) более 21 указывает на тяжелый алкогольный гепатит и необходимость фармакологического лечения. Печеночная энцефалопатия и асцит чаще встречаются у пациентов, умерших от алкогольного гепатита, чем у выживших. Долгосрочная выживаемость у пациентов с алкогольным гепатитом, прекративших употребление алкоголя, значительно дольше, чем у пациентов, которые продолжают пить.Трехлетняя выживаемость приближается к 90% у трезвенников, тогда как у активно пьющих она составляет менее 70%. Продолжительность выживания в обеих группах значительно меньше, чем в популяции того же возраста.
Цирроз алкогольный
Цирроз исторически считался необратимым результатом тяжелого и длительного повреждения печени. Однако исследования с участием пациентов с заболеваниями печени от многих различных причин убедительно показали, что фиброз и цирроз могут иметь компонент обратимости.Для пациентов с декомпенсированным алкогольным циррозом печени, перенесших трансплантацию, выживаемость сопоставима с выживаемостью пациентов с другими причинами заболевания печени с 5-летней выживаемостью примерно 70%.
Признаки и симптомыПризнаки и симптомы
Как правило, у пациентов с ожирением печени симптомы отсутствуют или имеются неспецифические симптомы, не указывающие на острое заболевание печени.Поддерживающие признаки при физикальном осмотре включают увеличенную и гладкую, но редко болезненную печень. При отсутствии наложенного печеночного процесса стигматы хронических заболеваний печени, таких как ангиомы пауков, асцит или астериксис, скорее всего, отсутствуют.
Алкогольный гепатит — это синдром различной степени тяжести, поэтому симптомы его проявления могут быть разными. Симптомы могут быть неспецифическими и легкими и включать анорексию и потерю веса, боль и вздутие живота или тошноту и рвоту. Альтернативно, более серьезные и специфические симптомы могут включать энцефалопатию и печеночную недостаточность.Физические признаки включают гепатомегалию, желтуху, асцит, ангиомы пауков, лихорадку и энцефалопатию.
Установленный алкогольный цирроз может проявляться декомпенсацией без предшествующей истории ожирения печени или алкогольного гепатита. В качестве альтернативы алкогольный цирроз может быть диагностирован одновременно с острым алкогольным гепатитом. Симптомы и признаки алкогольного цирроза печени не помогают дифференцировать его от других причин цирроза. Пациенты могут иметь желтуху, зуд, отклонения от нормы лабораторных исследований (например, тромбоцитопению, гипоальбуминемию, коагулопатию) или осложнения портальной гипертензии, такие как кровотечение из варикозно расширенных вен, асцит или печеночная энцефалопатия.
ДиагностикаДиагностика
Рис. 1. Гистологические данные при алкогольной жировой болезни печени включают накопление жира в гепатоцитах.
Жировая печень обычно диагностируется у бессимптомного пациента, который проходит обследование на предмет аномальных функциональных проб печени; как правило, уровни аминотрансферазы менее чем в два раза превышают верхний предел нормы.Никакие лабораторные тесты не позволяют диагностировать ожирение печени. Характерные результаты ультразвукового исследования включают гиперэхогенную печень с гепатомегалией или без нее. Компьютерная томография (КТ) и магнитно-резонансная томография (МРТ) позволяют легко обнаружить цирроз печени. На МРТ при ALD могут присутствовать особенности, включая увеличенный размер хвостатой доли, более частую визуализацию правой вырезки печени и более крупные регенеративные узелки. Биопсия печени редко требуется для диагностики ожирения печени в соответствующих клинических условиях, но может быть полезна для исключения стеатогепатита или фиброза.
Типичные гистологические находки жировой ткани печени включают накопление жира в гепатоцитах, которое часто является макровезикулярным, но иногда и микровезикулярным (рис. 1). Чаще всего поражается центрилобулярная область ацинуса печени. Однако при тяжелом ожирении печени жир распределяется по ацинусу. Жирная печень неспецифична для употребления алкоголя; это связано с ожирением, инсулинорезистентностью, гиперлипидемией, недоеданием и различными лекарствами. Таким образом, связь ожирения печени с употреблением алкоголя требует подробного и точного анамнеза пациента.
Рис. 2. Воспаление и некроз центилобулярной области ацинуса печени.
Диагноз алкогольного гепатита также основывается на тщательном анамнезе, физическом осмотре и анализе лабораторных тестов. В недавнем консенсусном заявлении Консорциума по алкогольным гепатитам дано рабочее определение алкогольного гепатита, которое включает желтуху в течение 60 дней при интенсивном употреблении (> 50 г / день) алкоголя в течение минимум 6 месяцев, билирубин в сыворотке> 3 мг / дл Соотношение АСТ: АЛТ> 1.5 и никакой другой очевидной причины гепатита. В заявлении предлагалось классифицировать пациентов с алкогольным гепатитом как определенных, когда для установления диагноза использовалась биопсия печени, вероятно, когда клинические и лабораторные признаки присутствовали без потенциальных смешивающих проблем, и возможно, когда присутствовали смешанные проблемы. Другие общие и неспецифические лабораторные отклонения включают анемию и лейкоцитоз. В нашем центре, учитывая ограниченные возможности лечения, мы регулярно выполняли биопсию печени с помощью трансъюгулярного доступа для подтверждения диагноза.
Классические гистологические признаки алкогольного гепатита включают воспаление и некроз, которые наиболее выражены в центрилобулярной области ацинуса печени (рис. 2). Гепатоциты классически раздуваются, что вызывает сдавление синусоиды и обратимую портальную гипертензию. Инфильтрат воспалительных клеток, расположенный в основном в синусоидах и рядом с некротическими гепатоцитами, состоит из полиморфноядерных и мононуклеарных клеток. Помимо воспаления и некроза, у многих пациентов с алкогольным гепатитом наблюдается жировая инфильтрация и тельца Мэллори, которые представляют собой внутриклеточные перинуклеарные скопления промежуточных филаментов, которые являются эозинофильными при окрашивании гематоксилин-эозином.Ни жировая инфильтрация, ни тельца Мэллори не являются специфическими для алкогольного гепатита и не необходимы для диагностики.
Рисунок 3. Гистология алкогольного цирроза в конечной стадии.
Диагноз алкогольного цирроза печени основывается на обнаружении классических признаков и симптомов терминальной стадии заболевания печени у пациента со значительным употреблением алкоголя в анамнезе. Пациенты склонны занижать сведения о своем потреблении алкоголя, а беседы с членами семьи и близкими друзьями могут дать более точную оценку потребления алкоголя.
Пациенты могут иметь любые или все осложнения портальной гипертензии, включая асцит, кровотечение из варикозно расширенных вен и печеночную энцефалопатию. Гистология алкогольного цирроза в конечной стадии при отсутствии острого алкогольного гепатита напоминает гистологию поздней стадии заболевания печени, вызванной многими другими причинами, без каких-либо отчетливых патологических данных (рис. 3).
Общий клинический диагноз алкогольной болезни печени, основанный на сочетании физических данных, лабораторных показателей и клинической проницательности, является относительно точным (Таблица 3).Однако биопсия печени может быть оправдана в отдельных случаях, особенно когда диагноз ставится под сомнение. Клиническое подозрение на алкогольный гепатит может быть неточным у 30% пациентов. Помимо подтверждения диагноза, биопсия печени также полезна для исключения других непредвиденных причин заболевания печени, лучшего определения степени повреждения, прогнозирования и принятия терапевтических решений.
Таблица 3. Физикальное обследование и результаты лабораторных исследований при алкогольной болезни печени
| Физический осмотр | |
| Конституционный | |
| Кожа |
|
| Опорно-двигательный аппарат |
|
| Мочеполовая | |
| Живот |
|
| Неврологический |
|
| Результаты лабораторных исследований | |
| Синтетическая функция печени |
|
| Уровни ферментов печени |
|
| Гематологический |
|
| Метаболический |
|
Лечение
Основа терапии ALD — воздержание.Пациенты часто не могут добиться полного и длительного воздержания от алкоголя без посторонней помощи, и уместно направление в бригаду по лечению химической зависимости. Госпитализация показана для ускорения диагностической оценки пациентов с желтухой, энцефалопатией или асцитом неизвестной причины. Кроме того, следует госпитализировать пациентов с известной АБП, у которых наблюдается почечная недостаточность, лихорадка, недостаточное пероральное потребление для поддержания гидратации или быстрое ухудшение функции печени, что демонстрируется прогрессирующей энцефалопатией или коагулопатией.Пациентам с подозрением на алкогольный гепатит следует сделать посев крови, мочи и асцита для определения наличия бактериальных инфекций независимо от того, есть ли у них лихорадка. Наличие синдрома системного воспалительного ответа при поступлении связано с высоким риском синдрома полиорганной недостаточности, что связано с очень высокой смертностью.
Нутритивная поддержкаПоддерживающая терапия для всех пациентов включает адекватное питание. Почти все пациенты с алкогольным гепатитом в той или иной степени страдают от недоедания, но оценка серьезности недоедания остается сложной задачей из-за отсутствия чувствительных и конкретных клинических или лабораторных параметров.Диетолог играет важную роль в оценке степени недоедания и назначении пищевых добавок у истощенных пациентов-алкоголиков. Степень недоедания напрямую коррелирует с краткосрочной (1 месяц) и долгосрочной (1 год) смертностью. Через 1 год с момента постановки диагноза алкогольного гепатита у пациентов с легким недоеданием уровень смертности составляет 14%, по сравнению с 76% смертностью у пациентов с тяжелым недоеданием. Попытки исправить белково-калорийное недоедание с помощью дополнительного перорального или парентерального питания, или того и другого, дали неоднозначные результаты.В общем, энтеральное питание предпочтительнее парентерального, и для обеспечения положительного баланса азота необходимо давать белок. Аминокислоты с разветвленной цепью полезны в качестве добавки для поддержания положительного баланса азота у пациентов, которые не переносят чрезмерное потребление белка из-за развития энцефалопатии; однако стоимость ограничивает рутинное использование у всех пациентов с алкогольной недостаточностью. Пищевые добавки обычно связаны с улучшением результатов печеночных тестов, но лишь в редких случаях с улучшением показателей смертности.Краткое изложение рекомендаций по ежедневному кормлению пациентов с ALD см. В самых последних практических руководствах. Текущие рекомендации предлагают регулярную диету с содержанием белка от 1 до 1,5 г и от 30 до 40 ккал / кг массы тела для адекватного восстановления. Если пациент не может есть из-за анорексии или измененного психического статуса, следует рассмотреть возможность использования зонда для энтерального питания. Одно только парентеральное питание неадекватно.
ЛечениеИспользование кортикостероидов в качестве специфической терапии алкогольного гепатита вызвало большой интерес.Обоснованием этого подхода является возможная роль иммунной системы в инициировании и сохранении поражения печени. Было проведено более 20 рандомизированных контролируемых исследований с участием пациентов с тяжелым алкогольным гепатитом, получавших глюкокортикоиды. Некоторые испытания не продемонстрировали значительного преимущества глюкокортикоидов, в то время как другие продемонстрировали улучшение выживаемости. Мета-анализ 15 исследований, проведенный в 2008 г., пришел к выводу, что глюкокортикоиды не приносят пользы, за исключением, возможно, группы с DF> 32.Это было подтверждено метаанализом 5 крупнейших исследований 2011 года, который показал улучшение показателей смертности при лечении преднизолоном.
Пентоксифиллин, пероральный ингибитор фосфодиэстеразы, также является ингибитором синтеза TNF. Повышенные уровни TNF были связаны с более высокой смертностью от алкогольного гепатита. В рандомизированном двойном слепом контролируемом исследовании изучалось влияние лечения пентоксифиллином на краткосрочную выживаемость и прогрессирование гепаторенального синдрома у пациентов с тяжелым алкогольным гепатитом.Среди пациентов, получавших пентоксифиллин, 24% (12 из 49) умерли по сравнению с 52% (24 из 52) пациентов, получавших плацебо ( P = 0,037). Гепаторенальный синдром стал причиной смерти у 50% (6 из 12) пациентов, получавших пентоксифиллин, по сравнению с 92% (22 из 24) пациентов, получавших плацебо ( P = 0,009). Последующий метаанализ не показал положительных результатов.
Испытание стероидов или пентоксифиллина при алкогольном гепатите (STOPAH) — это рандомизированное контрольное испытание, опубликованное в 2015 году и крупнейшее на сегодняшний день испытание по лечению алкогольного гепатита.Это исследование включало 1092 пациента с алкогольным гепатитом и показало, что ни преднизолон, ни пентоксифиллин не снижают общую смертность через 28 дней. Преднизолон был связан с незначительным улучшением смертности через 28 дней, но без улучшения через 90 дней или 1 год. Метаанализ, включающий исследование STOPAH, показал доказательства среднего качества, что глюкокортикоиды сами по себе или в комбинации с PTX или антиоксидантом N-ацетилцистеином снижали 28-дневную, но не 90-дневную смертность у пациентов с алкогольным гепатитом.
Пациенты с DF ≥ 32 или MELD ≥ 21 должны рассматриваться для включения в клинические испытания, если таковые имеются. Если клинические испытания недоступны, целесообразно испытание лечения глюкокортикоидами. Шкала Лилля предназначена для определения того, следует ли пациентам, получавшим кортикостероиды, прекратить лечение через 1 неделю лечения из-за отсутствия ответа на лечение. Это хороший предиктор шестимесячной летальности, и у пациентов с показателем менее 0,45 прогноз считается хорошим, и лечение кортикостероидами следует продолжать.По последним данным, лечение пентоксифиллином не поддерживается.
Гранулоцитарный колониестимулирующий фактор был предложен в качестве агента для стимуляции регенерации печени у пациентов с алкогольным гепатитом путем стимулирования миграции стволовых клеток, полученных из костного мозга, в печень. Одноцентровое исследование из Индии показало улучшение выживаемости у пациентов, получавших гранулоцитарный колониестимулирующий фактор, через 90 дней. Однако его использование у пациентов с алкогольным гепатитом носит экспериментальный характер. Другие методы лечения алкогольного гепатита, которые были исследованы, но не оказались эффективными, включают пропилтиоурацил; инфликсимаб; инсулин и глюкагон; блокаторы кальциевых каналов; антиоксиданты, такие как витамин E, S-аденозил-L-метионин или силимарин, который является активным ингредиентом расторопши.
Трансплантация печениЛечение пациента с алкогольным циррозом печени отражает лечение пациентов с любым другим типом цирроза и включает профилактику и лечение асцита, спонтанного бактериального перитонита, кровотечения из варикозно расширенных вен, энцефалопатии, недостаточности питания и гепатоцеллюлярной карциномы. Как только развился запущенный цирроз печени с признаками декомпенсации (асцит, спонтанный бактериальный перитонит, печеночная энцефалопатия, кровотечение из варикозно расширенных вен), пациента следует направить в центр трансплантации.
Уже более десяти лет алкогольный цирроз является вторым ведущим показанием для трансплантации печени в США. Применимость трансплантации печени для пациентов с тяжелым алкогольным гепатитом является этически спорной, учитывая нехватку органов для трансплантации печени и примерно 20% трансплантации печени. смертность в листе ожидания. Большинству центров трансплантации требуется 6 месяцев трезвости, прежде чем их можно будет рассматривать для трансплантации. Это требование теоретически имеет двойное преимущество: прогнозирует долгосрочное воздержание и позволяет восстановить функцию печени после острого алкогольного гепатита.Это правило оказывается невыгодным для людей с тяжелым алкогольным гепатитом, потому что от 70% до 80% могут умереть в течение этого периода. Mathurin et al. Обнаружили, что ранняя трансплантация печени у пациентов с тяжелым алкогольным гепатитом по сравнению с теми, кому не была проведена трансплантация, имела более высокую 6-месячную выживаемость, и это преимущество выживаемости сохранялось в течение 2 лет наблюдения. Рецидивы после трансплантации возникают не чаще, чем у пациентов с алкогольным циррозом печени, не страдающих алкогольным гепатитом.
Таблица 4.Исследуемые методы лечения алкогольной болезни печени
| Лечение | Рекомендуется повседневное использование | Потенциальная выгода |
| Воздержание | Есть | Выживание |
| Нутриционная поддержка | Есть | Выживание, лаборатория |
| Кортикостероиды | Есть | Выживание |
| Пентоксифиллин | № | Выживаемость без почечной недостаточности |
| Пропилтиоурацил | № | № |
| Инфликсимаб | № | № |
| Колхицин | № | № |
| Инсулин, глюкагон | № | № |
| Блокатор кальциевых каналов | № | № |
| Витамин E | № | № |
| S-аденозил-L-метионин | № | № |
| Силимарин (расторопша) | № | № |
| Трансплантация печени | Рассмотрим (при декомпенсированном циррозе) | 5-летняя выживаемость ~ 70% |
Профилактика и скрининг
Как подчеркивается в последних национальных практических руководствах, медицинские работники должны внимательно следить за признаками скрытого злоупотребления алкоголем.18 Многие пациенты открыто не раскрывают точную историю употребления алкоголя. Кроме того, никакие результаты физикального обследования или лабораторные отклонения не являются специфическими для ALD. Поэтому всех пациентов следует обследовать на предмет злоупотребления алкоголем или зависимости. Злоупотребление определяется как вредное употребление алкоголя с развитием негативных последствий для здоровья или общества. Зависимость определяется физической терпимостью и симптомами отмены. Анкета CAGE (сокращение употребления алкоголя, раздражение из-за беспокойства других по поводу выпивки, чувство вины за выпивку, употребление алкоголя в качестве откровения по утрам) является предпочтительным инструментом скрининга, с более чем 2 положительными ответами, обеспечивающими чувствительность 71% и специфичность 95% для алкогольной зависимости.
ЗаключениеЗаключение
Клиницисты должны проверять всех пациентов на наличие вредных привычек употребления алкоголя. Всем пациентам с алкогольными заболеваниями печени следует воздерживаться от алкоголя. Для людей с тяжелым заболеванием (например, DF ≥32 или печеночной энцефалопатией или и тем и другим) и без противопоказаний к их применению следует рассмотреть стероиды.Трансплантацию печени следует рассматривать как вариант лечения пациентов с декомпенсированным циррозом, связанным с алкоголем, и тяжелым алкогольным гепатитом.
РезюмеСводка
- Все пациенты должны пройти скрининг на алкогольную болезнь печени.
- Воздержание — краеугольный камень лечения алкогольной болезни печени.
- Алкогольная болезнь печени — неоднородное заболевание.
- Для диагностики алкогольной болезни печени требуется подробный анамнез пациента с подтверждающими лабораторными и визуализирующими исследованиями.
- Биопсия печени может быть полезна для подтверждения диагноза, исключения других заболеваний и прогноза.
- Пациентов с тяжелым алкогольным гепатитом следует рассматривать для включения в клинические испытания.
- Лечение кортикостероидами может применяться у пациентов с DF> 32 или MELD> 21 без противопоказаний к глюкокортикоидам.
- Текущие данные не подтверждают необходимость лечения пентоксифиллином.
- Пациенты с алкогольным циррозом печени должны быть обследованы для трансплантации печени.
Рекомендуемая литература
- Чако К.Р., Рейнус Дж. Спектр алкогольной болезни печени. Clin Liver Dis 2016; 20 (3): 419–427.
- Trépo E, Romeo S, Zucman-Rossi J, Nahon P. PNPLA3 ген при заболеваниях печени. J Hepatol 2016; 65 (2): 399–412.
- Savolainen VT, Liesto K, Männikkö A, Penttilä A, Karhunen PJ. Употребление алкоголя и алкогольная болезнь печени: данные о пороговом уровне воздействия этанола. Alcohol Clin Exp Res 1993; 17 (5): 1112–1117.
- Lelbach WK. Цирроз у алкоголиков и его связь с объемом злоупотребления алкоголем. Ann N Y Acad Sci 1975; 252: 85–105.
- Grant BF, Dufour MC, Harford TC. Эпидемиология алкогольной болезни печени. Semin Liver Dis 1988; 8 (1): 12–25.
- Стюарт С., Джонс Д., Дэй С.П. Алкогольная болезнь печени: новый взгляд на механизмы и стратегии профилактики. Trends Mol Med 2001; 7 (9): 408–413.
- Zhou Z, Wang L, Song Z, Lambert JC, McClain CJ, Кан YJ. Критическое участие оксидантного стресса в острой индуцированной алкоголем продукции TNF-альфа в печени. Am J Pathol 2003; 163 (3): 1137–1146.
- Соренсен Т.И., Орхольм М., Бентсен К.Д., Хойбай Г., Эгойе К., Кристофферсен П. Проспективная оценка злоупотребления алкоголем и алкогольного поражения печени у мужчин как предикторов развития цирроза. Lancet 1984; 2 (8397): 241–244.
- Александр Дж. Ф., Лишнер М. В., Галамбос Дж. Т.. Естественное течение алкогольного гепатита. II. Долгосрочный прогноз. Am J Gastroenterol 1971; 56 (6): 515–525.
- Bonis PA, Friedman SL, Kaplan MM. Обратим ли фиброз печени? N Engl J Med 2001; 344 (6): 452–454.
- Романо Д. Р., Хименес С., Родригес Ф. и др. Ортотопическая трансплантация печени при алкогольном циррозе печени. Transplant Proc 1999; 31 (6): 2491–2493.
- Мэддри WC. Алкогольный гепатит: клинико-патологические особенности и терапия. Semin Liver Dis 1988; 8 (1): 91–102.
- Окадзаки Х., Ито К., Фудзита Т., Койке С., Такано К., Мацунага Н. Дискриминация алкоголиков от вирус-индуцированного цирроза на МРТ. AJR Am J Roentgenol 2000; 175 (6): 1677–1681.
- Baptista A, Bianchi L, de Groote J, et al; обзор международной группы. Алкогольная болезнь печени: морфологические проявления. Lancet 1981; 1 (8222): 707–711.
- Крабб Д.В., Баталлер Р., Чаласани Н.П. и др .; Консорциумы NIAAA по борьбе с алкогольным гепатитом. Стандартные определения и общие элементы данных для клинических испытаний у пациентов с алкогольным гепатитом: Рекомендация NIAAA Alcoholic Hepatitis Consortia. Гастроэнтерология 2016; 150 (4): 785–790.
- Митчелл М.С., Фридман Л.С., Макклейн С.Дж. Медицинское ведение тяжелого алкогольного гепатита: экспертная оценка комитета по обновлению клинической практики института AGA. Клин Гастроэнтерол Гепатол 2017; 15 (1): 5–12.
- Finlayson ND. Клинические особенности алкогольной болезни печени. Baillieres Clin Gastroenterol 1993; 7 (3): 627–640.
- O’Shea RS, Dasarathy S, McCullough AJ; Комитет по практическим рекомендациям Американской ассоциации по изучению заболеваний печени; Комитет по параметрам практики Американского колледжа гастроэнтерологии.Алкогольная болезнь печени. Гепатология 2010; 51: 307–328.
- Mendenhall CL, Tosch T., Weesner RE, et al. В.А. кооперативное исследование по алкогольному гепатиту. II: Прогностическое значение белково-калорийной недостаточности. Am J Clin Nutr 1986; 43 (2): 213–218.
- Schenker S, Halff GA. Лечебное питание при алкогольной болезни печени. Semin Liver Dis 1993; 13 (2): 196–209.
- Rambaldi A, Saconato HH, Christensen E, Thorlund K, Wetterslev J, Gluud C.Систематический обзор: глюкокортикостероиды при алкогольном гепатите — систематический обзор Кокрановской гепатобилиарной группы с метаанализами и последовательным анализом рандомизированных клинических испытаний. Aliment Pharmacol Ther 2008; 27 (12): 1167–1178.
- Mathurin P, O’Grady J, Carithers RL, et al. Кортикостероиды улучшают краткосрочную выживаемость у пациентов с тяжелым алкогольным гепатитом: метаанализ индивидуальных данных пациентов. кишки 2011 г .; 60 (2): 255–260.
- Hallé P, Paré P, Kaptein E, Kanel G, Redeker AG, Reynolds TB.Двойное слепое контролируемое исследование пропилтиоурацила у пациентов с тяжелым острым алкогольным гепатитом. Гастроэнтерология 1982; 82 (5 Pt 1): 925–931.
- Акривиадис Э., Ботла Р., Бриггс В., Хан С., Рейнольдс Т., Шакил О. Пентоксифиллин улучшает краткосрочную выживаемость при тяжелом остром алкогольном гепатите: двойное слепое плацебо-контролируемое исследование. Гастроэнтерология 2000; 119 (6): 1637–1648.
- Паркер Р., Армстронг М.Дж., Корбетт С., Роу И.А., Хулихан Д.Д. Систематический обзор: пентоксифиллин для лечения тяжелого алкогольного гепатита. Aliment Pharmacol Ther 2013; 37 (9): 845–854.
- Терсз М.Р., Ричардсон П., Эллисон М. и др .; STOPAH Trial. Преднизолон или пентоксифиллин при алкогольном гепатите. N Engl J Med 2015; 372 (17): 1619–1628.
- Singh S, Murad MH, Chandar AK, et al. Сравнительная эффективность фармакологических вмешательств при тяжелом алкогольном гепатите: систематический обзор и сетевой метаанализ. Гастроэнтерология 2015; 149 (4): 958–970.e12.
- Louvet A, Naveau S, Abdelnour M, et al.Модель Лилля: новый инструмент терапевтической стратегии у пациентов с тяжелым алкогольным гепатитом, получающих стероиды. Гепатология 2007; 45 (6): 1348–1354.
- Сингх В., Шарма А.К., Нарасимхан Р.Л., Бхалла А., Шарма Н., Шарма Р. Гранулоцитарный колониестимулирующий фактор при тяжелом алкогольном гепатите: рандомизированное пилотное исследование. Am J Gastroenterol 2014; 109 (9): 1417–1423.
- Rambaldi A, Gluud C. Мета-анализ пропилтиоурацила при алкогольной болезни печени — обзор Кокрановской гепатобилиарной группы. Liver 2001; 21 (6): 398–404.
- Naveau S, Chollet-Martin S, Dharancy S и др .; Группа фуа-алкогольных напитков Французской ассоциации фуа. Двойное слепое рандомизированное контролируемое исследование инфликсимаба, связанного с преднизолоном, при остром алкогольном гепатите. Гепатология 2004; 39 (5): 1390–1397.
- Bird G, Lau JY, Koskinas J, Wicks C, Williams R. Инфузия инсулина и глюкагона при остром алкогольном гепатите: проспективное рандомизированное контролируемое исследование. Гепатология 1991; 14 (6): 1097–1101.
- Bird GL, Prach AT, McMahon AD, Forrest JA, Mills PR, Danesh BJ. Рандомизированное контролируемое двойное слепое исследование антагониста кальциевых каналов амлодипина в лечении острого алкогольного гепатита. J Hepatol 1998; 28 (2): 194–198.
- Trinchet JC, Balkau B, Poupon RE и др. Лечение тяжелого алкогольного гепатита инфузией инсулина и глюкагона: многоцентровое последовательное исследование. Гепатология 1992; 15 (1): 76–81.
- Mezey E, Potter JJ, Rennie-Tankersley L, Caballeria J, Pares A. Рандомизированное плацебо-контролируемое испытание витамина E при алкогольном гепатите. J Hepatol 2004; 40 (1): 40–46.
- Rambaldi A, Gluud C. S-аденозил-L-метионин при алкогольных заболеваниях печени. Кокрановская база данных Syst Rev 2006; (2): CD002235.
- Rambaldi A, Jacobs BP, Iaquinto G, Gluud C. Расторопша пятнистая при алкогольных и / или гепатитах B или C заболеваниях печени — систематический Кокрановский обзор гепатобилиарной группы с метаанализами рандомизированных клинических испытаний. Am J Gastroenterol 2005; 100 (11): 2583–2591.
- Mathurin P, Moreno C, Samuel D, et al. Ранняя трансплантация печени при тяжелом алкогольном гепатите. N Engl J Med 2011; 365 (19): 1790–1800.
- Аддолорато Г., Баталлер Р., Бурра П. и др. Трансплантация печени при алкогольной болезни печени. Трансплантация 2016; 100 (5): 981–987.
- Aertgeerts B, Buntinx F, Kester A. Значение CAGE в скрининге злоупотребления алкоголем и алкогольной зависимости в общеклинических популяциях: диагностический метаанализ. J Clin Epidemiol 2004; 57 (1): 30–39.
Безалкогольный и алкогольный стеатогепатит (НАЖБП / AFLD)
Что такое жировая болезнь печени?
Жировая болезнь печени означает, что у вас есть лишний жир в печени. Вы могли слышать, как ваш врач назвал это стеатозом печени.
Сильное употребление алкоголя повышает вероятность его заболеть. Со временем чрезмерное употребление алкоголя приводит к накоплению жира в клетках печени. Это затрудняет работу печени.
Но ожирение печени можно получить, даже если не употреблять много алкоголя.
Неалкогольная жировая болезнь печени (НАЖБП)
Существует два различных типа неалкогольной жировой болезни печени:
Простая жировая болезнь печени: Это означает, что у вас жир в печени, но у вас может не быть воспаления в печени или повреждение клеток печени. Обычно это не ухудшается и не вызывает проблем с печенью. У большинства людей с НАЖБП просто ожирение печени.
Неалкогольный стеатогепатит (НАСГ): Это гораздо серьезнее, чем простая жировая дистрофия печени. НАСГ означает, что у вас воспаление печени. Воспаление и повреждение клеток печени, которые происходят при НАСГ, могут вызывать серьезные проблемы, такие как фиброз и цирроз, которые являются типами рубцевания печени, и рак печени. Около 20% людей с НАЖБП страдают НАСГ.
Алкогольная жировая болезнь печени (ALD)
Алкогольная жировая болезнь печени поддается профилактике. Обычно становится лучше, когда вы перестаете употреблять алкоголь.Если вы продолжаете пить, ALD может вызвать серьезные проблемы. К ним относятся:
- Увеличенная печень. Это не всегда вызывает симптомы, но вы можете испытывать боль или дискомфорт в верхней правой части живота.
- Алкогольный гепатит. Это опухоль печени, которая может вызывать жар, тошноту, рвоту, боль в животе и желтуху (желтоватость кожи и глаз).
- Алкогольный цирроз печени. Это скопление рубцовой ткани в печени. Он может вызывать те же симптомы, что и алкогольный гепатит плюс:
Обычно на первом месте стоит жировая болезнь печени, связанная с алкоголем.Затем болезнь может ухудшиться и перерасти в алкогольный гепатит. Со временем может перерасти в алкогольный цирроз печени.
Если вы много пьете, проконсультируйтесь с врачом. Это конфиденциально, и они могут помочь вам контролировать употребление алкоголя и сохранить ваше здоровье.
Симптомы жировой болезни печени
При БАП и НАЖБП симптомы обычно отсутствуют. У некоторых людей могут быть такие признаки, как усталость или боль в правой верхней части живота, где находится печень.
Если у вас НАСГ или цирроз, у вас могут быть такие симптомы, как:
- Вздутие живота
- Расширенные кровеносные сосуды под кожей
- Большая грудь у мужчин
- Красные ладони
- Кожа и глаза, которые кажутся желтоватыми из-за состояния, называемого желтухой
Причины и факторы риска
Причиной ALD является переизбыток алкоголя.У вас может быть еще больше шансов получить его, если вы много пьете и
- страдаете ожирением
- недоедаете
- У вас хронический вирусный гепатит, особенно гепатит C
- Имеют гены, которые повышают вероятность заражения
- Афроамериканец или латиноамериканец
- Возраст — чем вы старше, тем выше вероятность.
Причина, по которой у одних людей с НАЖБП просто ожирение печени, а у других НАСГ, неизвестна. Причиной могут быть гены.НАЖБП или НАСГ более вероятны, если:
Продолжение
Есть также несколько менее распространенных причин, по которым вы можете получить НАЖБП или НАСГ. К ним относятся:
Диагноз
Поскольку у большинства людей нет симптомов, эти состояния нелегко диагностировать.
Ваш врач может использовать разные методы, чтобы выяснить, есть ли у вас жировая болезнь печени. Ваш врач может использовать следующие данные для диагностики жировой болезни печени:
- История болезни. Ваш врач спросит вас об употреблении алкоголя.Эта информация может помочь вашему врачу определить, есть ли у вас ALD или NAFLD, поэтому будьте правдивы. Они также спросят о лекарствах, которые вы принимаете, о том, как вы питаетесь, и о других заболеваниях, которые могут у вас быть.
- Физический осмотр. Врач взвешивает вас и проверяет ваше тело на наличие признаков проблем с печенью, таких как увеличение печени или желтуха.
- Анализы крови . Они могут показать, есть ли у вас высокий уровень ферментов печени, таких как аланинаминотрансфераза (АЛТ) и аспартатаминотрансфераза (АСТ).Если это так, возможно, проблема с вашей печенью.
- Визуальные тесты . Вы можете пройти УЗИ, компьютерную томографию (КТ) или магнитно-резонансную томографию (МРТ). Эти тесты могут помочь определить, есть ли в вашей печени жир. Но они не могут сказать, есть ли у вас обычная жировая дистрофия печени или NASH
- Биопсия печени. Не всем с НАЖБП требуется биопсия печени. Ваш врач может порекомендовать его, если вы подвержены риску развития НАСГ или если другие тесты показывают, что у вас могут быть осложнения НАСГ, такие как цирроз.Врач берет образец ткани из вашей печени и отправляет его в лабораторию, чтобы проверить, есть ли у вас воспаление или повреждение печени. Это можно сделать в больнице или амбулаторном хирургическом центре. Перед процедурой вам дадут лекарство, которое поможет вам расслабиться или снять боль. Для биопсии врач обезболивает пораженный участок и с помощью специальной иглы берет небольшой кусочек ткани из печени. Биопсия печени — единственный способ для врачей диагностировать НАСГ.
Лечение жирной болезни печени
Лекарств, одобренных для лечения НАЖБП, не существует, хотя некоторые из них проходят клинические испытания.
Обычно первая линия лечения — похудение. Это помогает уменьшить жир, воспаление и рубцы в печени. Потеря от 3% до 5% веса тела может сократить количество жира в печени. Операция по снижению веса также возможна, если вам есть что терять.
Продолжение
Вам также необходимо бросить пить. Это единственный способ предотвратить ухудшение состояния печени. Возможно, вы даже сможете отменить некоторые уже нанесенные повреждения печени. Поговорите со своим врачом о том, как вам получить помощь.Вам может потребоваться программа детоксикации под медицинским наблюдением, чтобы безопасно бросить пить и справиться с симптомами отмены.
Если у вас есть осложнения из-за НАСГ, такие как цирроз или печеночная недостаточность, вам может потребоваться пересадка печени. В целом, люди с НАСГ, перенесшие трансплантацию печени, очень хорошо себя чувствуют.
Самопомощь при жировой болезни печени
Помочь могут изменения в образе жизни:
- Больше упражняйтесь. Старайтесь быть активными хотя бы 30 минут в день большую часть дней недели.Если вы пытаетесь похудеть, вы можете обнаружить, что это помогает больше заниматься спортом. Но если вы еще не занимаетесь спортом регулярно, сначала проконсультируйтесь с врачом и начинайте медленно.
- Будь добр к своей печени. Не делайте вещей, которые заставят его работать усерднее. Откажитесь от алкоголя. Принимайте лекарства и безрецептурные препараты только в соответствии с инструкциями. Поговорите со своим врачом, прежде чем пробовать какие-либо лечебные травы. Просто потому, что продукт натуральный, это не значит, что он безопасен.
- Понизьте уровень холестерина. Соблюдайте здоровую растительную диету, занимайтесь спортом и принимайте лекарства. Это позволит получить — и сохранить — уровень холестерина и триглицеридов на необходимом уровне.
- Управляйте диабетом. Проверьте уровень сахара в крови и принимайте лекарства в соответствии с предписаниями врача.
Осложнения жировой болезни печени
Основным осложнением всех этих состояний является цирроз или рубцевание печени. Когда ваша печень пытается остановить воспаление, связанное с этими состояниями, она создает области шрамов.По мере распространения воспаления растут и рубцы, и в конечном итоге ваша печень перестает выполнять свою работу. Это может привести к:
- Скопление жидкости в брюшной полости
- Набухшие вены в пищеводе, которые могут лопнуть и кровоточить
- Путаница и сонливость
- Рак печени
- Печеночная недостаточность
Можно ли предотвратить ожирение печени?
Для предотвращения ALD:
- Пейте в умеренных количествах: Это один напиток в день для женщин и мужчин старше 65 лет и до двух напитков для мужчин в возрасте 65 лет и младше.
- Защитите себя от гепатита C: Эта вирусная инфекция печени может повысить вероятность цирроза печени, если вы пьете.
- Проверьте, прежде чем смешивать лекарства и алкоголь: Спросите своего врача, можно ли употреблять алкоголь с рецептурными лекарствами, которые вы принимаете. Прочтите предупреждающую этикетку на лекарствах, отпускаемых без рецепта. Не пейте, если принимаете такие продукты, как парацетамол, который в сочетании с алкоголем может повредить печень.
Продолжение
При НАЖБП и НАСГ все сводится к тому, чтобы сделать лучший выбор:
- Ешьте здоровую пищу. Выберите растительную диету с большим количеством фруктов, овощей, цельного зерна и полезных жиров.
- Поддерживайте здоровый вес. Похудей, если нужно. Если у вас здоровый вес, старайтесь поддерживать его, выбирая здоровую диету и занимаясь спортом.
- Упражнение. Тренируйтесь большую часть дней в неделю. Если вы какое-то время не проявляли активности, сначала поговорите со своим врачом.
Болезнь печени, связанная с алкоголем — NHS
Алкогольная болезнь печени (ARLD) относится к повреждению печени, вызванному чрезмерным потреблением алкоголя.Существует несколько степеней тяжести и ряд сопутствующих симптомов.
Симптомы алкогольной болезни печени (ARLD)
ARLD обычно не вызывает никаких симптомов, пока печень не будет серьезно повреждена.
Когда это происходит, симптомы могут включать:
Это означает, что ARLD часто диагностируется во время тестов на другие состояния или на стадии серьезного поражения печени.
Если вы регулярно злоупотребляете алкоголем, сообщите об этом своему терапевту, чтобы он проверил, не повреждена ли ваша печень.
Информация:Консультации по коронавирусу
Получите консультацию о коронавирусе и заболеваниях печени в British Liver Trust
Алкоголь и печень
За исключением мозга, печень является самым сложным органом в организме.
В его функции входят:
- фильтрация токсинов из крови
- помощь в переваривании пищи
- регулирование уровня сахара и холестерина в крови
- помощь в борьбе с инфекциями и болезнями
Печень очень устойчива и способна к самовосстановлению.Каждый раз, когда ваша печень фильтрует алкоголь, некоторые клетки печени умирают.
В печени могут развиваться новые клетки, но длительное злоупотребление алкоголем (чрезмерное употребление алкоголя) в течение многих лет может снизить ее способность к регенерации. Это может привести к серьезному и необратимому повреждению печени.
ARLD очень распространен в Великобритании. Число людей с этим заболеванием увеличивалось за последние несколько десятилетий в результате увеличения уровня злоупотребления алкоголем.
Подробнее о причинах ARLD.
Этапы ARLD
Существует 3 основных этапа ARLD, хотя каждый этап часто перекрывается. Эти этапы объясняются ниже.
Алкогольная жировая болезнь печени
Употребление большого количества алкоголя даже в течение всего нескольких дней может привести к накоплению жиров в печени.
Это называется алкогольной жировой болезнью печени и является первой стадией ARLD.
Жировая болезнь печени редко вызывает какие-либо симптомы, но это важный предупреждающий признак того, что вы употребляете алкоголь в больших количествах.
Жировая болезнь печени обратима. Если вы перестанете употреблять алкоголь на 2 недели, ваша печень должна прийти в норму.
Алкогольный гепатит
Алкогольный гепатит, не связанный с инфекционным гепатитом, является потенциально серьезным заболеванием, которое может быть вызвано злоупотреблением алкоголем в течение длительного периода.
Когда это развивается, это может быть первый раз, когда человек осознает, что повреждает свою печень из-за алкоголя.
Реже алкогольный гепатит может возникнуть, если вы употребляете большое количество алкоголя за короткий период времени (запой).
Поражение печени, связанное с алкогольным гепатитом легкой степени, обычно обратимо, если вы навсегда бросите пить.
Однако тяжелый алкогольный гепатит является серьезным и опасным для жизни заболеванием.
Многие люди ежегодно умирают от этого заболевания в Великобритании, и некоторые люди узнают о поражении печени только тогда, когда их состояние достигает этой стадии.
Цирроз
Цирроз — это стадия ARLD, при которой печень имеет значительные рубцы. Даже на этом этапе явных симптомов может не быть.
Обычно это необратимо, но немедленное прекращение употребления алкоголя может предотвратить дальнейшие повреждения и значительно увеличить продолжительность жизни.
У человека с циррозом печени, вызванного алкоголем, который не бросает пить, вероятность прожить еще как минимум 5 лет составляет менее 50%.
Лечение алкогольной болезни печени (ARLD)
В настоящее время нет специального лечения для ARLD.Основное лечение — бросить пить, желательно на всю оставшуюся жизнь.
Это снижает риск дальнейшего повреждения печени и дает ей наилучшие шансы на выздоровление.
Если человек зависим от алкоголя, бросить пить может быть очень трудно.
Но поддержка, совет и лечение могут быть доступны через местные службы поддержки алкоголиков.
Пересадка печени может потребоваться в тяжелых случаях, когда печень перестала функционировать и не улучшается после прекращения употребления алкоголя.
Пересадка печени будет рассматриваться только в том случае, если у вас развились осложнения цирроза, несмотря на то, что вы бросили пить.
Все отделения по пересадке печени требуют, чтобы человек не употреблял алкоголь в ожидании трансплантации и до конца своей жизни.
Осложнения
Смертность, связанная с ARLD, значительно выросла за последние несколько десятилетий.
Злоупотребление алкоголем в настоящее время является одной из самых частых причин смерти в Великобритании, наряду с курением и высоким кровяным давлением.
Опасные для жизни осложнения ARLD включают:
- внутреннее (варикозное) кровотечение
- накопление токсинов в головном мозге (энцефалопатия)
- накопление жидкости в брюшной полости (асцит) с ассоциированной почечной недостаточностью
- рак печени
- повышенная уязвимость к заражению
Подробнее об осложнениях ARLD.
Профилактика заболеваний печени, связанных с алкоголем (ARLD)
Самый эффективный способ предотвратить ARLD — это прекратить употребление алкоголя или придерживаться рекомендуемых пределов:
- мужчинам и женщинам рекомендуется не пить регулярно более 14 единиц в неделю
- распределять потребление алкоголя более чем на 3 дня, если вы выпивать до 14 единиц в неделю
Единица алкоголя равна примерно половине пинты светлого пива нормальной крепости или мерке (25 мл) крепких спиртных напитков.
Даже если вы много лет пьете, сокращение или прекращение употребления алкоголя будет иметь важные краткосрочные и долгосрочные преимущества для вашей печени и общего состояния здоровья.
См. Наши страницы о алкоголе и алкоголе для получения дополнительной информации и советов.
Видео: болезнь печени
В этом видео консультант-гепатолог Марк Райт объясняет заболевание печени и объясняет, как отказ от алкоголя может помочь.
Последний раз просмотр СМИ: 3 июля 2018 г.
Срок сдачи обзора СМИ: 3 июля 2021 г.
Последняя проверка страницы: 10 августа 2018 г.
Срок следующего рассмотрения: 10 августа 2021 г.
Алкогольная жирная печень — обзор
1 Введение
Алкогольная и неалкогольная жировая болезнь печени (AFLD и NAFLD, соответственно) являются основными причинами заболеваемости и смертности в мире. При приеме алкоголя или безалкогольных веществ, таких как диета с высоким содержанием жиров (HFD) или безалкогольные напитки, содержащие кукурузный сироп с высоким содержанием фруктозы (HFCS), триглицериды накапливаются в гепатоцитах, что приводит к развитию ожирения печени (стеатоз печени), который является обратимым. условие.После непрерывного воздействия или приема этих веществ стеатоз печени может прогрессировать до воспалительного стеатогепатита, фиброза, цирроза и даже гепатоцеллюлярной карциномы. В целом прогрессирование доброкачественной жировой болезни печени до более тяжелой болезни печени напрямую коррелирует с количеством, частотой приема и продолжительностью факторов стресса (например, алкоголем или высоким содержанием жиров) (Zakhari & Li, 2007). Кроме того, известно, что существуют относительно большие индивидуальные различия в скорости выведения этанола, возможно, из-за генетических факторов и факторов окружающей среды (Li, Yin, Crabb, O’Connor, & Ramchandani, 2001).Кроме того, прогрессирование заболевания печени может усугубляться или облегчаться, особенно при наличии других сопутствующих факторов риска (Lieber, 2004a), таких как вирус гепатита B или C (Mueller, Millonig, & Seitz, 2009; Otani et al., 2005; Rigamonti et al., 2003; Szabo, Saha, & Bukong, 2015; Szabo et al., 2010; Zakhari, 2013), ВИЧ (Fan, Joshi, Koval, & Guidot, 2011; Persidsky et al., 2011), ожирение (Cederbaum, 2012a; Hart, Morrison, Batty, Mitchell, & Davey, 2010; Loomba et al., 2013, 2010), диабет (Hassan et al., 2002), курение (Kuper et al., 2000; Purohit, Rapaka, Kwon, & Song, 2013; Salaspuro & Salaspuro, 2004), клинически используемые наркотики (Boelsterli & Lee, 2014; McClain, Kromhout, Peterson, & Holtzman, 1980; Seeff, Cuccherini, Zimmerman, Adler, & Benjamin, 1986) или загрязнители окружающей среды, такие как бензол в бензине (Kalf, Post, & Snyder, 1987). Например, у людей, которые пьют более 60 г в день, выше вероятность развития фиброза, цирроза, гепатоцеллюлярной карциномы и, в конечном итоге, печеночной недостаточности (Lucey, Mathurin, & Morgan, 2009; Stickel & Seitz, 2010).Кроме того, одновременное употребление алкоголя и одного или двух из этих факторов риска значительно увеличивает тяжесть заболевания печени с повышением заболеваемости и смертности (Neuman et al., 2014). В этом обзоре мы кратко описываем механизмы различных типов заболеваний печени, вызванных алкоголем (этанолом), HFD или другими потенциально гепатотоксичными веществами, а также ферментами, участвующими в метаболизме алкоголя, способствующими заболеванию печени. Наконец, мы также описываем возможности трансляционных исследований в области профилактики или лечения различных форм заболеваний печени.
Алкогольная болезнь печени — AMBOSS
Последнее обновление: 3 ноября 2020 г.
Резюме
Алкогольная болезнь печени (ALD) относится к ряду прогрессирующих заболеваний печени, вызванных хроническим и чрезмерным употреблением алкоголя. Треть населения США употребляет алкоголь сверх рекомендованных уровней, что увеличивает риск развития АБК. Существует три стадии ALD, которые могут происходить, а могут и не происходить последовательно. Первая стадия обычно протекает бессимптомно и включает развитие (потенциально) обратимого алкогольного ожирения печени.Продолжительное употребление алкоголя приведет к алкогольному гепатиту, второй стадии, которая часто становится хронической. Клинические проявления на этой стадии включают желтуху, утомляемость и лихорадку. На третьей и последней стадии у пациента развивается алкогольный цирроз печени. Анамнез пациента, уровни трансаминаз и исследования изображений имеют решающее значение для диагностики и показывают различные модели повреждения печени. Неалкогольный стеатогепатит — это дифференциальный диагноз, который в настоящее время считается важной причиной цирроза печени.Лечение ALD требует полного прекращения употребления алкоголя.
Эпидемиология
- Вторая по частоте причина цирроза печени в США
- 28% населения США превышает рекомендуемые пределы употребления алкоголя.
- Распространенность злоупотребления алкоголем в течение жизни: 18%
- У ~ 10–20% алкоголиков развивается цирроз.
Каталожные номера: [1] [2] [3] [4]
Эпидемиологические данные относятся к США, если не указано иное.
Этиология
- Алкоголизм — очень важная причина хронических заболеваний печени.
- Значительное употребление алкоголя
- Мужчины:> 210 г чистого алкоголя в неделю
- Женщины:> 140 г чистого алкоголя в неделю
Справочные материалы: [1] [5]
Патофизиология
Клинические особенности
Стадии ALD могут перекрываться и не обязательно протекать последовательно.
Алкогольная жировая дистрофия печени (обратимая)
- В основном бессимптомная
- Некоторые пациенты сообщают о ощущении давления в верхней части живота.
- Гепатомегалия: мягкая консистенция
- Регресс после прекращения употребления алкоголя
- Острое обострение с риском печеночной недостаточности встречается редко.
Алкогольный гепатит (обратимый в легких случаях)
Цирроз, связанный с алкоголем (необратимый)
- Заключительная стадия ALD
- См. «Клинические особенности» цирроза печени.
Каталожные номера: [6] [7]
Диагностика
Злоупотребление алкоголем в анамнезе, которое коррелирует с типичными лабораторными и визуальными данными, является диагностикой алкогольной болезни печени.
Визуализирующие и лабораторные исследования в случае алкогольной жировой болезни печени покажут обратные изменения в течение месяца, если пациент воздерживается от алкоголя!
Чтобы помнить, что АСТ> АЛТ при алкогольном гепатите, подумайте о «Сделайте тост с алкоголем!
Каталожные номера: [9] [10]
Патология
- Алкогольная жирная печень
- Накопление липидных капель в гепатоцитах с постепенным некрозом единичных клеток внутри долек
- Алкогольный гепатит
- Цирроз, связанный с алкоголем
Алкогольная жировая дистрофия печени и алкогольный гепатит легкой степени могут быть обратимыми после прекращения приема алкоголя.Однако тяжелые формы алкогольного гепатита и цирроза не обратимы!
Каталожные номера: [11] [12] [13] [14] [15]
Дифференциальные диагнозы
Неалкогольная жировая болезнь печени (НАЖБП) и неалкогольный стеатогепатит (НАСГ)
НАСГ — это диагноз исключения! Другие причины хронического заболевания печени должны быть исключены лабораторными исследованиями и / или биопсией.
Различие между алкогольной и неалкогольной жировой болезнью печени можно провести только на основании анамнеза пациента!
АЛТ больше, чем АСТ (АСТ / АЛТ), если печень инфильтрирована липидами.
Каталожные номера: [16] [17]
Перечисленные здесь дифференциальные диагнозы не являются исчерпывающими.
Лечение
Ссылки: [7]
Осложнения
В основном характеризуются совокупностью клинических проявлений, вызванных снижением функции печени:
Другие поражения органов в результате хронического употребления алкоголя
Синдром Зиева
Мы перечисляем наиболее важные осложнения.Выбор не исчерпывающий.
Каталожные номера
- Wolf DC. Цирроз. В: Ананд Б.С., Цирроз . Нью-Йорк, штат Нью-Йорк: WebMD. http://emedicine.medscape.com/article/185856 . Обновлено: 8 января 2017 г. Дата обращения: 25 марта 2017 г.
- Мауриелло Л.М., Гёкбайрак Н.С., Ван Мартер Д.Ф., Пайва А.Л., Прочаска Ю.М. Интернет-ориентированное компьютерное вмешательство для пропаганды ответственного употребления алкоголя: результаты пилотного тестирования с участием работающих взрослых. Спиртное лакомство Q .2012; 30 (1): с.91-108. DOI: 10.1080 / 07347324.2012.635528. | Открыть в режиме чтения QxMD
- Хасин Д., Киз К. Эпидемиология алкогольных и наркотических расстройств . Springer Нью-Йорк ; 2010 г. : п. 23–49
- Матюрин П., Баталлер Р. Тенденции в лечении и бремени алкогольной болезни печени. Дж. Гепатол . 2015; 62 (1): стр.S38-S46. DOI: 10.1016 / j.jhep.2015.03.006. | Открыть в режиме чтения QxMD
- Флегель К., Макдональд Н., Хеберт ПК.Пьянство: слишком распространено и опасно. Кан Мед Ассо Дж. . 2011; 183 (4): с.411. DOI: 10.1503 / cmaj.110029. | Открыть в режиме чтения QxMD
- O’Shea RS, Dasarathy S, McCullough AJ et al. Алкогольная болезнь печени. Ам Дж. Гастроэнтерол . 2009; 105 (1): с.14-32. DOI: 10.1038 / ajg.2009.593. | Открыть в режиме чтения QxMD
- Heuman DM. Алкогольный гепатит. В: Ананд Б.С., Алкогольный гепатит .Нью-Йорк, штат Нью-Йорк: WebMD. http://emedicine.medscape.com/article/170539 . Обновлено: 30 декабря 2016 г. Проверено: 25 марта 2017 г.
- Роберт Т. Минс. Гематологические осложнения употребления алкоголя. В: Сообщение TW, под ред. Дата обновления . Уолтем, Массачусетс: UpToDate. https://www.uptodate.com/contents/matologic-complications-of-alcohol-use . Последнее обновление: 22 января 2020 г. Дата обращения: 17 августа 2020 г.
- Akunjee M, Akunjee N. Книга CSA: MRCGP Решение симптомов CSA: Клинические основы для экзамена MRCGP CSA .Клиническая подготовка ; 2014 г.
- Диффузный стеатоз печени. https://radiopaedia.org/articles/diffuse-hepatic-steatosis . Обновлено: 1 января 2017 г. Доступ: 25 марта 2017 г.
- Гольян Э.Ф. Rapid Review Pathology . Эльзевир Сондерс ; 2013
- Томмолино Э. Жирная печень. В: Anand BS, Fatty Liver . Нью-Йорк, штат Нью-Йорк: WebMD. http://emedicine.medscape.com/article/175472 . Обновлено: 25 января 2017 г. Дата обращения: 25 марта 2017 г.
- Сахуджа П. Патология алкогольной болезни печени, отличить ли ее от неалкогольного стеатогепатита ?. Мир Дж. Гастроэнтерол . 2014; 20 (44): с.16474–16479. DOI: 10.3748 / wjg.v20.i44.16474. | Открыть в режиме чтения QxMD
- Орман Е.С., Одена Г., Баталлер Р. Алкогольная болезнь печени: патогенез, управление и новые цели для терапии. J Гастроэнтерол Hepatol . 2013; 28 год (S1): с.77-84. DOI: 10.1111 / jgh.12030. | Открыть в режиме чтения QxMD
- Торруэллас С.

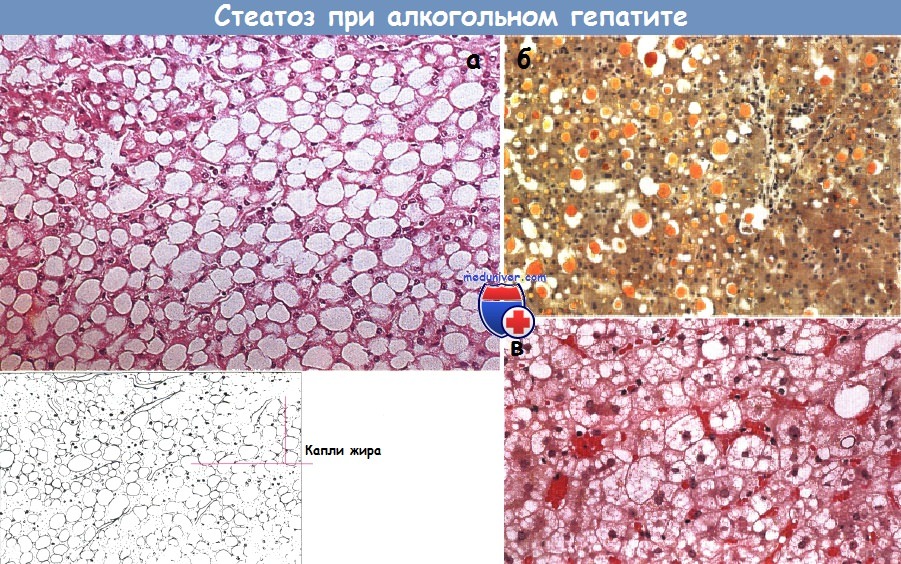 В любом случае алкоголь — фактор токсического повреждения, поэтому
следует осторожно относиться к употреблению алкогольных напитков даже в самых малых дозах.
В любом случае алкоголь — фактор токсического повреждения, поэтому
следует осторожно относиться к употреблению алкогольных напитков даже в самых малых дозах.
 1
1

