Синдром Дресслера (I24.1) > Справочник заболеваний MedElement > MedElement
Классически синдром развивается на 2–4-й неделе ИМ, однако эти сроки могут уменьшаться – «ранний СД» и увеличиваться до нескольких месяцев, «поздний СД». Иногда течение СД принимает агрессивный и затяжной характер, он может длиться месяцы и годы, протекать с ремиссиями и обострениями
Основные клинические проявления синдрома: лихорадка, перикардит, плеврит, пневмонит и поражение суставов. Одновременное поражение перикарда, плевры и легких при постинфарктном синдроме наблюдается не часто. Чаще перикардит сочетается с плевритом или с пневмонитом. В ряде случаев имеет место только перикардит или плеврит, либо пневмонит.
Лихорадка при СД не имеет какой-либо строгой закономерности. Как правило, она бывает субфебрильной, хотя в отдельных случаях может быть фебрильной или вообще отсутствовать .
Перикардит является обязательным элементом СД. Клинически он проявляется болью в перикардиальной зоне, которая может иррадиировать в шею, плечо, спину, брюшную полость. Боль может быть острой приступообразной (плевритическая) или давящей, сжимающей (ишемической). Она может усиливаться при дыхании, кашле, глотании и ослабевать в вертикальном положении или лежа на животе . Как правило, она длительная и исчезает или ослабевает после появления в полости перикарда воспалительного экссудата. Главный аускультативный признак перикардита – шум трения перикарда: в первый день болезни при внимательной аускультации он определяется у абсолютного большинства (до 85 %) больных. Шум лучше всего выслушивается у левого края грудины, при задержке дыхания и наклоне туловища пациента вперед. В классическом варианте он состоит из трех компонентов – предсердного (определяется в систолу) и желудочкового (систолического и диастолического). Как и боль, шум трения перикарда уменьшается или исчезает вовсе после появления в полости перикарда выпота, раздвигающего трущиеся листки перикарда . Обычно перикардит протекает нетяжело: уже через несколько дней боли стихают, а экссудат в полости перикарда почти никогда не накапливается в таком количестве, чтобы ухудшить кровообращение, хотя иногда могут появиться признаки тяжелой тампонады сердца . Иногда воспалительный процесс в перикарде при СД принимает затяжной рецидивирующий характер и заканчивается развитием констриктивного перикардита.
При применении антикоагулянтов на фоне СД возможно также развитие геморрагического перикардита, хотя подобное осложнение может быть и при отсутствии антикоагулянтной терапии .
Плеврит. Проявляется болью в боковых отделах грудной клетки, усиливающейся при дыхании, затруднением дыхания, шумом трения плевры, притуплением перкуторного звука. Он может быть сухим и экссудативным, односторонним и двусторонним. Нередко плеврит носит междолевой характер и не сопровождается типичными физикальными симптомами .
Пневмонит.
Поражение суставов. Для СД характерно появление так называемого «синдрома плеча»: болезненных ощущений в области плечелопаточных суставов, чаще слева, ограничение подвижности этих суставов. Вовлечение в процесс синовиальных оболочек нередко приводит к возникновению болей и в крупных суставах конечностей .
Другие проявления. Проявлением постинфарктного синдрома может быть сердечная недостаточность вследствие диастолической дисфункции, геморрагический васкулит и острый гломерулонефрит .
что это такое в кпрдиологии, симптомы и лечение
Кардиальные патологии имеют угрожающий характер не только сами по себе. Значительные риски возникают после кажущегося благополучия и полного излечения от заболевания.
Многие состояния описанного профиля способны привести к аутоиммунным процессам в организме. Такие явления относительно редки, по разным оценкам, вероятность наступления реакции составляет 3-10% не более.
Синдром Дресслера — это выраженный аутоимунный ответ на перенесенный некроз кардиомиоцитов (постинфарктный синдром). В результате разрушения клеточных структур наблюдается выброс большого количества особых белковых соединений, на которые и возникает иммунный ответ.
Это отсроченный результат перенесенного поражения сердечнососудистой системы. Становится итогом инфаркта, воспалительных заболеваний, прочих патологий.
Восстановление проводится в амбулаторных условиях. Осложнения грозные, но, к счастью, возникают не чаще, чем в 4% ситуаций.
Синдром крайне редко провоцирует летальный исход, описаны единичные случаи подобного итога. Тем не менее, качество жизни падает существенно. Болезнь склонна к хронизации и частым рецидивам.
Механизм развития патологии
Рассматриваемое явление гетерогенно по характеру. Что стоит знать о нем. В ходе воспаления, инфаркта и прочих явлений деструктивного рода обнаруживается отмирание клеток-кардиомиоцитов.
В кровь попадает большое количество белковых соединений. Иммунитет реагирует на них как на опасных вторженцев, вырабатывая особые антитела. Постепенно ответ вырывается из-под контроля и становится стереотипным.
Атаке собственного иммунитета подвергается все похожие белковые структуры клеточных оболочек. Это не только здоровые ткани сердца, но и ткани суставов, легочных структур и прочих анатомических образований.
Обычно синдром Дресслера развивается как итог обширного поражения сердца, в частности миокарда. Клинические варианты зависят от предрасположенности.
Также течение и риски усугубляются на фоне наличия в анамнезе сопутствующих аутоиммунных патологических процессов. Например, ревматоидного артрита, системной красной волчанки и прочих.
С большой вероятностью локализация синдрома будет соответствовать основному очагу. Одно состояние обуславливает другое.
Причины становления
Факторов развития относительно мало. Они всегда имеют строго кардиальное происхождение и связаны с поражением сердечных тканей.
Примерный перечень явлений:
Инфаркт миокарда
Самый распространенный патологический процесс. Лидирует в числе виновников начала описанного аутоиммунного состояния. Суть заключается в отмирании, некроза активных, функциональных тканей.

Чем больше площадь поражения, тем интенсивнее протекает заболевание. Это понятно, учитывая количество выходящих белковых соединений. Сила иммунного ответа соответствует положению вещей.
Развитие синдрома Дресслера не раннее, а отсроченное. Сразу заметить какие-либо изменения невозможно. Примерные сроки — 2-7 недель, плюс-минус.
Возникает заболевание остро, симптоматика появляется сразу и в полном объеме. Причем не обязательно, что признаки будут со стороны сердца. Под ударом суставы, легкие и прочие структуры.
Число случаев постинфарктного синдрома Дресслера, определяется как 95-97%.
Травмы грудной клетки
От ушибов до переломов, в том числе ребер и прочих. Не всегда происходит повреждение сердца, потому случаи рассматриваются в индивидуальном порядке.
При подозрении на вовлечение кардиальных структур проводится ЭКГ эхокардиография, по возможности такте магнитно-резонансное исследование. Обязательна консультация профильного специалиста.
Вероятность развития синдрома Дресслера на фоне полученной травмы минимальна. Если не считать случаев обширного поражения миокарда (такое возможно, например, при дорожно-транспортном происшествии с тяжелыми повреждениями и т.д.).
Радиочастотная абляция
Кардиохирургическая малоинвазивная операция. Назначается для устранения очагов патологического электрического возбуждения в миокарде.
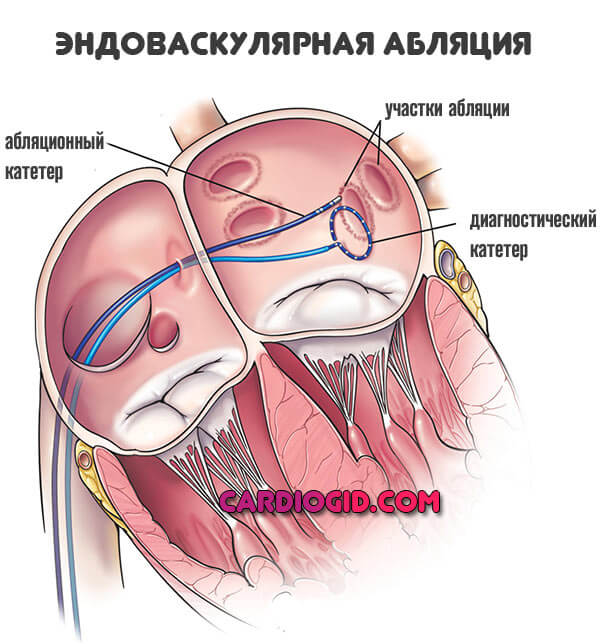
Проводится в крайних случаях, как методика восстановления нормального ритма. Осложнения всегда возможны, пациент об этом знать должен.
Вероятность описанного исхода незначительна, примерно 1-3% от общего числа ситуаций заканчивается синдромом Дресслера. Даже в подобном случае обычно все ограничивается единственным эпизодом за целую жизнь.
Проведенные операции иного рода
Любые. От протезирования до имплантации стимулятора, дефибриллятора и прочих. Каждое хирургическое вмешательство — это травматичный опыт для сердца. Потому избежать повреждения миоцитов невозможно.

Не всегда выброс специфических белков заканчивается столь плачевно, зависит от обширности повреждения.
Факторы риска
Основным виновником остается инфаркт. Возникает вопрос, почему в таком случае синдром Дресслера после инфаркта отмечается не у всех пациентов поголовно? Ведь согласно статистике, примерное количество пациентов с диагностированным аутоиммунным процессом составляет от 4 до 20% по разным оценкам. Дело в группе факторов повышенного риска.
Исследования показывают, что большая часть пациентов имела в анамнезе хотя бы один описанный момент:
- Гиперсенсибилизация организма. Обычно на фоне текущей аллергической реакции. Не важно как она проявляется: крапивницей, отеком Квинке, бронхиальной астмой или прочими явлениями.
- Аутоиммунные патологии. Ревматоидный артрит, тиреоидит Хашимото, васкулит, системная красна волчанка, псориаз. Значения не имеет. Любой фактор определяется как момент повышенного риска.
- Ослабленный иммунитет. На фоне часто переносимых инфекционно-воспалительных патологий и прочих состояний.
Все пациенты схожи в данных показателях. Половозрастных особенностей заболевание не имеет.
Симптоматика, в зависимости от локализации
Всего выделяют 6 патологических процессов, обусловленных описанным заболеванием. Примерный срок возникновения первых проявлений — 2-7 недель.
Возможно позднее начало состояния. Тогда клиническая картина развивается спустя почти год, но это относительно редкий вариант. О каких локализациях приходится говорить:
Сердечная
Представлена перикардитом. Речь идет о воспалении особой соединительнотканной сумке, в которой располагается мышечный орган. Она защищает его от смещения и поддерживает на одном месте.

Состояние сопровождается группой признаков:
- Интенсивные пульсирующие, давящие или жгучие боли в грудной клетке. Причем они не похожи на таковые при инфаркте, как говорят сами пациенты. Сила дискомфорта становится иной при перемене положения тела, после глубокого вдоха особенно.
- Подъем температуры. До уровня 38-39 градусов Цельсия. Это результат аутоиммунного поражения.
- Рост венозного давления, проявляется набуханием шейных сосудов. Падение артериального показателя (обычно незначительное, в пределах 10-20 мм ртутного столба от нормы).
Возможны аритмии на фоне скопление выпота в перикарде, это первый признак начинающейся тампонады. Грозное явление.
Кожная локализация
Представлена аутоиммунным дерматитом или крапивницей.
Симптомы:
- Интенсивный, мучительный зуд.
- Образование красноватой или яркой сыпи по всему телу или не отдельных участках, в зависимости от силы иммунного ответа.
- Формирование папул, то есть небольших пузырьков, заполненных серозным (прозрачным) экссудатом.
- Повышение местной температуры.
При этом связь между перенесенным инфарктом или травмой столь неочевидна, что на кардиогенный характер патологического процесса подумать трудно, требуется длительное обследование.
Возможно, речь идет о совпадении или ответе на прием лекарственных средств. Диагностика поставит точку в вопросе. Тем более, что картина крови на фоне аутоиммунного процесса достаточно специфична.
Брюшная локализация синдрома Дресслера
Определяется перитонитом, воспалением внутренней выстилки полости. Имеет яркую клиническую картину:
- Мучительные, интенсивные боли в животе. Сила дискомфорта становится ниже при нахождении правильного, удобного положения тела. Обычно лежа на боку с подогнутыми ногами.
- Понос или запор.
- Повышение температуры (до 39 градусов, бывает и меньше).
Специфические реакции также присутствуют. Специальные тесты дают возможность выявить перитонит.
При этом нужно срочно отграничить аутоиммунную форму от инфекционно-воспалительной. Вторая нередко выступает результатом запущенного аппендицита или же прочих патологий желудочно-кишечного тракта.
От итогов диагностики зависит терапевтическая тактика. При асептической форме, не связанной с проникновением бактерий требуется консервативное лечение.
Внимание:Характерная черта поражения, спровоцированного патогенными агентами — температура свыше 39 градусов.
Плевральная локализация
Воспаляется наружная оболочка легких. Проявления мало специфичны:
- Сухой непродуктивный кашель не протяжении нескольких дней.
- Боли в грудной клетке сзади, тупые, ноющие по своему характеру.
- Повышение температуры тела до 39 градусов Цельсия или ниже.
Легочная локализация
Альвеолит (также называется пневмонит, не стоит путать с похожим заболеванием). Имеет неинфекционную природу, но признаки примерно те же:
- Интенсивный дискомфорт при дыхании, невозможность набрать воздуха, неудовлетворенность процессом.
- Синюшность кожных покровов по причине недостаточного газообмена во всем организме.
- Слабость, сонливость.
- Кашель с незначительным количеством мокроты.
- Непереносимость даже минимальной физической активности.
Дифференциальная диагностика проводится пневмонией. Показано проведение спирографии, по возможности бронхоскопии или минимум рентгенографии грудной клетки или МРТ/КТ.
Суставная форма
Артрит. Обычно поражает крупные суставы: плечевые, коленные, бедренные, с одной или двух сторон сразу.
Признаки напоминают проявления ревматоидного воспаления:
- Сильные боли в месте вовлечения в патологический процесс.
- Нарушения двигательной активности.
- Ощущение скованности.
- Краснота, припухлость и отечность сустава.
- Невозможность осуществлять элементарные действия.
Осложнением выступает дополнительное поражение надкостницы. Наблюдается при длительном не леченом варианте.
Есть и некоторые общие симптомы:
- Стабильно высокая температура тела на уровне фебрилитета (но не выше 39 градусов Цельсия).
- Слабость, сонливость, недомогание.
- Воспаление слизистых оболочек. Половых органов, ротовой полости и других. Возможно в комплексе. Эта зацепка позволяет заподозрить описанный аутоиммунный процесс.
Синдром Дресслера в кардиологии вариативен: на сердечные формы приходится не более 15% всех зафиксированных ситуаций. Это парадоксально.
Восстановление проводится в стационарных или амбулаторных условиях.
Диагностика
Обследование под контролем кардиолога и группы профильных специалистов. Каких именно — определяет клиническая картина.
Примерная схема мероприятий:
- Устный опрос больного. Симптомы, описанные выше, красноречиво говорят о процессе.
- Сбор анамнеза. Как правило, в течение 2 месяцев, реже года наблюдалась травма грудной клетки или инфаркт, либо же миокардит. Еще хуже, если лечение не проводилось вообще.
- Измерение артериального давления, частоты сердечных сокращений.
- Электрокардиография, ЭХО-КГ.
Также МРТ грудной клетки. Это основные методы выявления синдрома Дресслера, локализованного в соединительнотканной сумке.
Дополнительно показаны:
- Анализ крови общий. На фоне нормального количества лейкоцитов и СОЭ (исключает острый инфекционный процесс) обнаруживается повышение уровня эозинофилов. Явное указание на аутоиммунное происхождение.
- Рентгенография грудной клетке, по мере надобности МРТ или КТ.
- Бронхоскопия. В крайних случаях.
- Оценка состояния сустава посредством УЗИ или пункции.
- Анализ мокроты.
- Ультразвуковое исследование брюшной полости.
Схема приблизительная. На деле позиций может потребоваться больше или же меньше. В любом случае, синдром Дресслера, учитывая его относительную редкость и неспецифичность симптоматики, представляет собой сложный вызов ведущему врачу.
Лечение
В основном консервативное. Предполагает прием медикаментов нескольких фармацевтических групп:
- Противовоспалительные нестероидного происхождения. Кеторолак, Ибупрофен, Найз и прочие. Для купирования процесса.
- Глюкокортикоиды. Для тех же целей, но при неэффективности первых. Дексаметазон или Преднизолон курсами. При резистентном течении показан прием определенными схемами на протяжении всей жизни пациента.
- Алкалоиды. Колхицин. Снимает воспаление, предотвращает распад тканей под влиянием иммунного фактора.
- Препараты для защиты желудочно-кишечного тракта. Омепразол и прочие.
При существенных сомнениях относительно происхождения допустимо применить антибиотики в качестве экспериментального метода. На фоне течения синдрома эффекта не будет.
Хирургическая терапия применяется крайне редко. Задача такого лечения — устранение осложнений, которые могут возникнуть. В основном речь о перикардите.
Проводится пункция, иссечение околосердечной сумки, прочие методики. Оценка состояния и выработка радикальной тактики ложится на плечи врача.

Постинфарктный синдром Дресслера лечится консервативными методами, хирургический способ показан в крайних случаях, на фоне развития потенциально фатальных процессов.
Возможные последствия
Вероятность становления осложнений минимальна.
Среди таковых:
- Тампонада сердца. Выход жидкости в перикард со сдавливанием самого мышечного органа.

- Гепатит. Воспаление печеночных структур. К циррозу приводит относительно редко, но рисковать не стоит.
- Васкулиты. Поражения сосудистых стенок. Итогом оказывается рубцевание, заращение просвета, образование тромбов и прочие моменты.

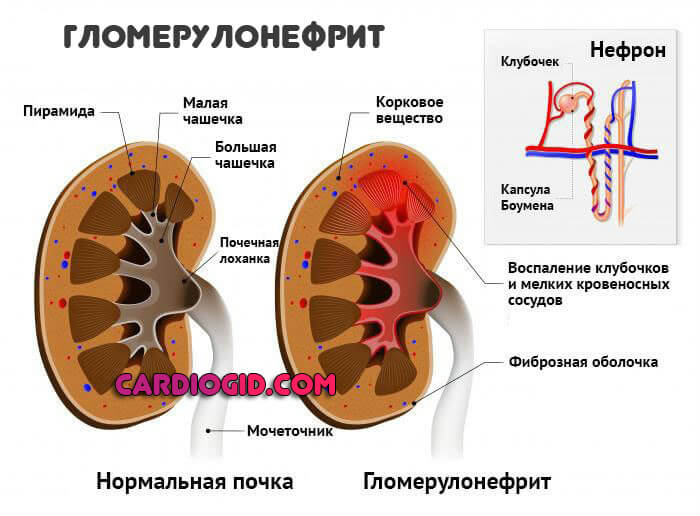
- Гломерулонефрит. Воспалительно-дегенеративное поражение почек аутоиммунного характера. Деструкция приводит к недостаточности, скорому летальному исходу.
Возможно развитие множественной, сочетанной формы синдрома Дресслера. Потенциально такой тип лечится намного хуже.
Прогноз
Определяется индивидуальными особенностями организма. По статистике выживаемость близится к 95-98%.
Смерть от описанного состояния — явление исключительно редкое. В литературе описаны единичные случаи. Это казуистика.
Основные причины летального исхода — сердечная недостаточность, остановка работы мышечного органа на фоне тампонады. Тем не менее, качество жизни при синдроме Дресслера падает в разы.
Прогноз в основном благоприятный. Сохранение трудовой активности маловероятно, способность обслуживать себя в быту существенно падает.
В заключение
Аутоиммунные последствия инфаркта и прочих поражений кардиальных структур встречаются нечасто. Но имеют тенденцию к ранней хронизации, резистентности (невосприимчивости) к лечению. Потому пациенту приходится мириться к новым условиям жизни.
При грамотной терапии продолжительность биологического существования неотличима от таковой без описанного синдрома. Прогноз хороший в любом случае. Но закрывать глаза на состояние нельзя.
Более того, оно может усугублять постинфарктный реабилитационный период, приводить к усложнению сердечной недостаточности и косвенному развитию летального исхода.
Синдром Дресслера (постинфарктный): развитие, формы, признаки, лечение
Автор: Солдатенков Илья Витальевич, врач-терапевт
Постинфарктный синдром Дресслера — аутоиммунная патология, осложняющая инфаркт миокарда и проявляющаяся симптомами воспаления перикарда, плевры и легких. Это особая реакция организма на собственные клетки, в результате которой поражаются внутренние органы, сосуды и суставы.
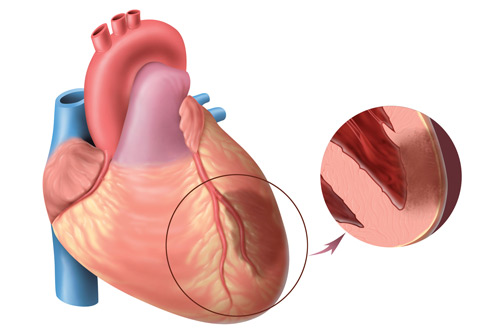
Инфаркт миокарда — гибель или некроз сердечной мышцы, часто заканчивающийся смертью больных. Тромбоз коронарных артерий приводит к нарушению кровоснабжения миокарда, развитию кислородного голодания и быстрой гибели мышечной ткани. Образуются зоны некроза, дающие начало воспалительному процессу. В пораженной области происходит отмирание тканей, из некротизированных участков выделяется в кровь большое количество токсичных продуктов распада.
Погибшие клетки миокарда воспринимаются организмом как чужеродные и вызывают в окружающих тканях реактивные изменения. Развивается асептическое воспаление соединительной ткани, имеющее длительное и тяжелое течение с частой сменой обострений и ремиссий.
Синдром Дресслера встречается довольно редко: патология регистрируется у 4 % больных с острой коронарной недостаточностью. Это связано широким использованием НПВС, распространением неинвазивных методов терапии сердечно-сосудистых заболеваний, сложной диагностикой патологии.
Формы
В кардиологии выделяют следующие формы патологии:
- Типичная или развернутая форма постинфарктного синдрома проявляется симптомами воспаления перикарда, плевры, легких, суставов. Выделяют смешанные варианты.
- Атипичная форма реализуется воспалением крупных суставов, аллергическим поражением кожи, развитием перитонита или бронхиальной астмы. Более редкие формы — пульмонит, периостит, перихондрит, синовит, васкулит, гломерулонефрит.
- Малосимптомная форма — стойкий субфебрилитет, артралгия, характерные изменения в составе крови.
По течению и времени развития синдром Дресслера подразделяется на:
- «Ранний СД» – возникающий сразу после инфаркта,
- «Поздний СД» – развивающийся спустя несколько месяцев после инфаркта.
Причины
Основные этиопатогенетические факторы синдрома Дресслера:
-

инфаркт миокарда
Инфаркт миокарда, а точнее его последствия являются основными этиологическими факторами заболевания. В результате некроза кардиомиоцитов в крови появляются специфические антитела к собственным клеткам организма. В наибольшей степени подвержены патологии серозные оболочки. В организме формируется гиперчувствительность к патологически измененному белку пораженных кардиомиоцитов. Собственные клетки организмом становятся аутоантигенами, которые взаимодействуют с антителами и образуют иммунные комплексы. Они фиксируются в различных органах и тканях, повреждая их. Развивается асептическое воспаление плевры, перикарда и суставов. В плевральной, перикардиальной и суставной полостях скапливается транссудат, возникает боль и нарушается функция органа.
- В более редких случаях причиной патологии становятся операции на сердце — комиссуротомия, кардиотомия.
- Тяжелые травмы сердца, ранения, контузии, удары в область сердца провоцируют развитие патологии.
- Вирусная инфекция – этиологический фактор патологии у лиц, в крови которых обнаруживают повышение титра противовирусных антител.
Группу риска составляют лица, страдающие полимиозитом, склеродермией, васкулитами, саркоидозом, спондилоартрозом.
Симптоматика
Синдром Дресслера проявляется интоксикацией, кардиалгией, полисерозитом. У больных появляется боль в груди, слабость, разбитость, недомогание, лихорадка, затем присоединяются симптомы гидроперикарда и гидроторакса.
Боль за грудиной имеет сжимающий или давящий характер, иррадиирует в левую руку, лопатку, плечо. Прием препаратов из группы нитратов обычно не приносит облегчения. При осмотре больных отмечают бледность кожи, гипергидроз, гипотонию, тахикардию. Аускультативно обнаруживаются глухие тоны и «ритм галопа». В таком состоянии больных следует немедленно госпитализировать.
Перикардит
Основным проявлением патологии является боль, интенсивность которой варьируется от умеренной до мучительной и приступообразной. Она ослабевают в положении стоя, а усиливается, когда пациент лежит на спине, глубоко дышит или кашляет. Боль бывает постоянной или возникающей периодически.
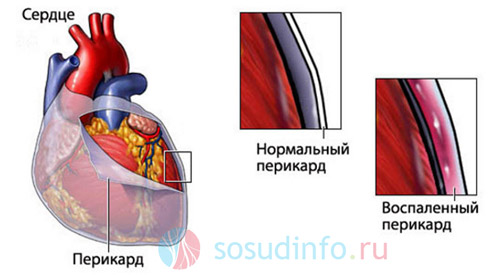
Кроме болевого синдрома для перикардита характерны следующие признаки:
- Шум трения перикарда, выслушиваемый у левого края грудины, особенно при наклоне туловища вперед. Он уменьшается после выделения жидкости в перикард и состоит из предсердного и желудочкового компонентов, возникающих в систолу и диастолу соответственно.
- Лихорадка — подъем температуры тела до субфебрильных значений. Интоксикационный синдром проявляется слабостью, недомоганием, ломотой в мышцах и суставах. Причиной лихорадки является активация пирогенов, выделяющихся в кровь при воспалении.
- Лейкоцитоз, эозинофилия и высокая СОЭ.
- Одышка, набухание яремных вен, гепатомегалия — признаки тяжелого течения патологии.
- Сердцебиение, сухой кашель, озноб, поверхностное и частое дыхание.
- Асцит.
- Отеки ног.
Перикардит – обязательный элемент синдрома Дресслера, имеющий нетяжелое течение. Спустя несколько дней интенсивность боли уменьшается, температура тела нормализуется, общее состояние больных улучшается.
Плеврит
Плеврит — воспалительное заболевание плевры, основные симптомы которого: боль в груди, затрудненное дыхание, кашель, шум трения плевры, лихорадка. Больные часто жалуются на ощущение царапанья внутри.
Формы плеврита:
- Сухой,
- Влажный,
- Односторонний,
- Двусторонний.
Он может протекать изолированно или сочетаться с перикардитом и прочими проявлениями патологии. Глубокое дыхание и кашель усиливают боль, которая проходит сама через пару дней.
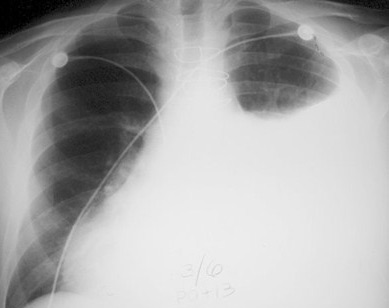
пример рентгена легких при синдроме Дресслера
Пневмонит
Пневмонит — аутоиммунное воспаление легочной ткани, проявляющееся загрудинной болью, одышкой, сухим или влажным кашлем с кровавой мокротой. При пневмоните очаги воспаления локализуются в нижних долях легких. Над этими перкуторно обнаруживается укороченный перкуторный звук, аускультативно — мелкопузырчатые влажные хрипы, в мокроте — кровь.
Среди наименее распространенных симптомов патологии выделяют поражения суставов, сосудов и внутренних органов. Артрит плечевого сустава аутоаллергической этиологии, проявляющийся всеми признаками воспаления: болью, ограничением подвижности, онемением, парестезией, гиперемией кожи. Межфаланговые суставы, а иногда и вся кисть отекает. Артрит протекает на фоне лихорадки.
Длительная ишемия миокарда приводит к развитию очаговой дистрофии и мелкоочаговому инфаркту. В этом случае первые симптомы патологии появляются поздно.
Диагностика
Диагноз синдрома Дресслера основывается на жалобах пациента, данных анамнеза жизни и болезни, осмотра, перкуссии и аускультации грудной клетки. Визуальный осмотр позволяет обнаружить у пациентов бледность или посинение кожи, обусловленное гипоксией тканей. Выбухают яремные вены и кожа между ребрами слева, что связано с повышенным давлением в грудной клетке. Чтобы уменьшить болевые ощущения, больные стараются «дышать животом». Перкуторно определяется расширение сердечной тупости, аускультативно — приглушение сердечных тонов.
К дополнительным методах исследования относятся клинический анализ крови, иммунограмма, ревмопробы, электрокардиография, фонокардиография, УЗИ сердца, рентгенография грудной клетки и плечевых суставов, компьютерная или магнитно-резонансная томография, пункция перикарда. Биопсия позволяет обнаружить воспалительные изменения в ткани перикарда. Для этого берут кусочек ткани и исследуют его под микроскопом.
- Компьютерная томография выявляет характерные изменения в сердечной сумке и оценивает состояние органов средостения. Результаты исследования представляют собой снимок на пленке, подробно описывающий структурные изменения и подтверждающий предполагаемый диагноз.Магнитно-резонансная томография позволяет обнаружить повреждения миокарда, точечные участки воспаления, спайки, экссудат. Пациенты, находясь в туннеле, по сигналу врача перестают дышать и двигаться.Эхокардиография – неопасная и неинвазивная методика, проводимая с помощью ультразвука. Она выявляет жидкость в сердечной сумке, утолщение листков перикарда, спайки между ними, новообразования.
Лабораторная диагностика включает: клинический анализ крови и мочи, микробиологические тесты, цитологический анализ, иммунологическое исследование.
Лечение
Больным рекомендуют вести здоровый образ жизни, употреблять в пищу много свежих овощей и фруктов, злаков, круп, растительных жиров. Необходимо отказаться от вредных привычек, выполнять дыхательную гимнастику и лечебную физкультуру.

Медикаментозное лечение патологии проводят в условиях стационара. Препараты, назначаемые больным:
- НПВС – «Диклофенак», «Индометацин», «Ибупрофен», «Аспирин». Они оказывают болеутоляющее и жаропонижающее действие.
- Глюкокортикостероиды – «Преднизолон», «Дексаметазон». Они оказывают выраженный и быстрый эффект в связи с аутоиммунным происхождением патологии, способствуют более быстрому и полному рассасыванию выпота. Гормонотерапию проводят длительно. Состояние больных улучшается уже на 2-3 день от начала лечения.
- Кардиотропные препараты – препараты, нормализующие обменные процессы в сердечной мышце: «Триметазидин», «Панангин», «Аспаркам».
- Бета-блокаторы – «Атенолол», «Бисопролол», «Конкор».
- Гиполипидемические препараты – «Пробуркол», «Фенофибрат», «Ловастатин».
- Ингибиторы АПФ – «Каптоприл», «Эналаприл», «Лизиноприл».
- Антикоагулянты – «Варфарин», «Клопидогрел», «Аспирин».
- Анальгетики для снятия выраженного болевого синдрома – «Кетонал», «Нурофен», «Найз».
Благодаря современным терапевтическим методам и высокому качеству лечения больных с инфарктом миокарда, в настоящее время значительно уменьшилось количество случаев синдрома Дресслера.
Видео: о синдроме Дресслера (eng)
Рекомендации читателям СосудИнфо дают профессиональные медики с высшим образованием и опытом профильной работы.
На ваш вопрос ответит один из ведущих авторов сайта.
На вопросы данного раздела в текущий момент отвечает: Сазыкина Оксана Юрьевна, кардиолог, терапевт
Поблагодарить специалиста за помощь или поддержать проект СосудИнфо можно произвольным платежом по ссылке.
Постинфарктный синдром — причины, симптомы, диагностика и лечение

Постинфарктный синдром – это перикардит аутоиммунного генеза, развивающийся спустя несколько недель после острого инфаркта миокарда. Данное осложнение характеризуется классической триадой симптомов: боль в груди, шум трения листков перикарда, легочные проявления (хрипы, кашель, одышка). Для верификации диагноза выполняется общеклинический анализ крови, ЭКГ, рентген грудной клетки, УЗИ перикарда и плевральной полости. Лечение включает в себя симптоматическую, противовоспалительную и кардиотропную терапию. При осложненном течении проводится плевроцентез, перикардиоцентез или перикардэктомия.
Общие сведения
В клинической терминологии постинфарктным синдромом (ПС), или синдромом Дресслера, называется аутоиммунное поражение околосердечной сумки. Это осложнение, обусловленное неадекватной реакцией иммунной системы на деструктивно измененные белки миокарда, в 1955 году описал американский кардиолог В. Дресслер. В его честь болезнь получила свое второе название. Кроме того, в медицинской литературе встречаются такие термины, как поздний перикардит, посткардиотомический, посттравматический перикардиальный синдром и постинфарктный полисерозит. В целом распространенность ПС в популяции составляет 3-4%. Однако по данным различных авторитетных источников, с учетом атипичных и малосимптомных форм осложнение развивается у 15-30% пациентов, перенесших обширный, осложненный или повторный инфаркт миокарда (ИМ).

Постинфарктный синдром
Причины постинфарктного синдрома
Первопричиной заболевания является ишемическое повреждение структурных волокон миокарда, повлекшее за собой гибель кардиомиоцитов. Чаще всего оно возникает при крупноочаговом осложненном инфаркте. В процессе разрушения некротизированных тканей в кровоток поступают денатурированные белки, на которые иммунная система реагирует, как на чужеродные. В результате развивается аутоиммунная реакция, являющаяся причиной возникновения постинфарктного синдрома.
Определенную значимость в формировании симптомокомплекса играют антигены крови, проникающей в околосердечную оболочку при нарушении целостности сердечной мышцы. Поэтому, помимо острого ИМ, пусковым механизмом развития заболевания может стать гемоперикард (кровоизлияние в перикардиальную полость), обусловленное травмами грудной клетки, ранениями сердца или неадекватными кардиохирургическими вмешательствами. Также в группу риска входят постинфарктные пациенты с аутоиммунными патологиями. Некоторые авторы считают, что причиной воспалительного процесса является вирусная инфекция. Однако единодушия по поводу данного вопроса у специалистов в области кардиологии до сих пор нет.
Патогенез
Постинфарктный синдром представляет собой аутоиммунный процесс, возникающий вследствие интенсификации выработки антител к кардиальным антигенам. Острое нарушение кровоснабжения миокарда и гибель клеток влечет за собой резорбцию участков некроза и выход денатурированных компонентов в кровь. Это приводит к формированию иммунного ответа с образованием аутоантител, направленных против белков, входящих в состав серозных оболочек органов-мишеней.
Специфические антитела к кардиомиоцитам, в большом количестве присутствующие в плазме крови постинфарктных больных, формируют иммунные комплексы с клетками собственных тканей. Свободно циркулируя в кровяном русле, они накапливаются в перикардиальной, висцеральной плевре и во внутренних слоях суставных сумок, провоцируя асептическое воспаление. В дополнение повышается уровень Т-ЦТЛ (цитотоксических лимфоцитов), разрушающих поврежденные клетки собственного организма. Таким образом, изменяется состояние и клеточного, и гуморального иммунитета, что подтверждает аутоиммунный генез симптомокомплекса.
Классификация
Постинфарктный синдром подразделяется на 3 основные формы. В пределах каждой из них имеется несколько вариантов, классификация которых основана на локализации воспалительного процесса.
- Типичная. Клинические проявления типичной (развернутой) формы ПС связаны с воспалением перикарда, висцеральной плевры и тканей легкого. Она включает одиночные и комбинированные варианты постинфарктного аутоиммунного повреждения соединительной ткани:
- перикардиальный — воспаляется висцеральный и париетальный листок околосердечной сумки;
- плевральный — мишенью аутоантител становится плевра, на первый план выходят признаки гидроторакса;
- пневмонический — обнаруживаются инфильтративные изменения в легких, приводящие к развитию пневмонита;
- перикардиально-плевральный — присутствуют признаки сенсибилизации тканей серозной оболочки перикарда и плевры;
- перикардиально-пневмоничекий – выявляется поражение околосердечной оболочки и ткани легкого;
- перикардиально-плеврально-пневмонический — воспаление с сердечной сумки переходит на плевральные и легочные структуры.
- Атипичная. Для этой формы свойственны варианты, связанные с поражением антителами тканей сосудов и суставов. Она сопровождается воспалением крупных суставных сочленений или кожными реакциями: «синдромом плеча», пекталгией, дерматитом, узловой эритемой.
- Стертая (малосимптомная). При стертой форме со слабо выраженными основными симптомами наблюдается упорная артралгия, лихорадочное состояние и изменение количественного и качественного состава белой крови. При диагностике стертых и атипичных форм нередко возникают определенные трудности, обуславливающие актуальность более углубленного изучения данной проблемы.
Симптомы постинфарктного синдрома
Классический постинфарктный синдром формируется через 2-4 недели после ИМ. Иногда сроки могут увеличиваться или уменьшаться. К наиболее характерным симптомам заболевания относят лихорадочное состояние, болевые ощущения и тяжесть в груди, одышку, кашель. Патологический процесс чаще всего начинается остро, повышением температуры тела до субфебрильных или фебрильных отметок. Появляется слабость, головокружение, тошнота, учащается пульс и дыхание. Иногда температурные показатели остаются в пределах нормы.
Обязательным компонентом симптомокомплекса является перикардит. Для него типичны различные по интенсивности болевые ощущения в области сердца, отдающие в середину живота, под мечевидный отросток, в шею, лопатки, плечи и обе руки. Боли могут быть острыми, приступообразными, или тупыми, сжимающими. При кашле и глотании появляется чувство сдавленности в груди, болезненность усиливается. В положении стоя или лежа на животе боль ослабевает. Нередко наблюдается одышка, сердцебиение, частое поверхностное дыхание.
У 85% постинфарктных пациентов с самого первого дня появляется характерный шум трения перикардиальных листков. Он обнаруживается при аускультации, независимо от дыхания и сердечного цикла. Через несколько суток боли стихают, а шум исчезает после появления выпота. Типичное проявление плеврита — колющая односторонняя боль в верхней части туловища. Она усиливается при глубоких вдохах и наклонах в здоровую сторону. Вынужденное положение на больном боку облегчает состояние. При пальпации обнаруживается крепитация.
Для пневмонита характерно ослабленное жесткое дыхание, мелкопузырчатые хрипы, одышка, сухой или влажный кашель. Реже развивается резистентная к антибиотикам нижнедолевая пневмония. Заболевание сопровождается слабостью, усиленным потоотделением и лихорадкой. В мокроте могут обнаруживаться кровяные примеси, что существенно усложняет диагностику. При атипичных формах постинфарктного симптомокомплекса нарушаются функции различных суставов: плечевых, кистевых, грудинно-реберных. Болезнь может протекать по типу моно- и полиартритов.
Осложнения
При отсутствии своевременной диагностики и профессиональной врачебной помощи постинфарктный синдром способен привести к развитию геморрагического или констриктивного перикардита (появлению кровянистого экссудата или сдавливанию сердечных тканей), а в запущенных случаях стать причиной тяжелой тампонады сердца. Для заболевания свойственно рецидивирующее течение с обострениями и ремиссиями, возникающими в промежутках от 1-2 недель до 2-х месяцев. Как правило, под влиянием лечения наблюдается ослабление симптомов, а при отсутствии терапевтической коррекции болезнь атакует с новой силой.
Диагностика
При постановке диагноза учитываются жалобы больного, характерные клинические проявления и результаты комплексного лабораторного и инструментального обследования. К наиболее ценным диагностическим параметрам, позволяющим дать заключение о состоянии пациента на момент исследования и на дальнейшую перспективу, относят:
- Клинические критерии. Объективными признаками, подтверждающими высокую вероятность формирования постинфарктного полисерозита, является перикардит и фебрильная лихорадка. Характерной считается боль за грудиной, иррадиирующая в межлопаточную область и распространяющаяся вдоль трапециевидной мышцы, сухой кашель, различная по степени выраженности одышка.
- Лабораторные исследования. В общем анализе крови возможен лейкоцитоз, эозинофилия, увеличение СОЭ. Чтобы дифференцировать синдром Дресслера от повторного ИМ, проводится исследование крови на сывороточные маркеры повреждения миокарда. Увеличение содержания глобулярных белков — тропонина I и тропонина Т — позволяет подтвердить факт гибели клеток, случившийся в промежутке 4-48 часов. Титр противокардиальных антител остается таким же, как и при неосложненном ИМ.
- ЭКГ. На повторных электрокардиограммах наблюдается отрицательная динамика. Наиболее характерный признак – однонаправленное смещение сегмента ST в большинстве отведений (с максимальным зубцом желудочкового комплекса). По мере накопления в перикардиальной полости экссудата амплитуда комплекса ORS может снижаться.
- Рентгенография грудной клетки. При плеврите обнаруживается утолщение междолевой плевры, при перикардите расширяется сердечная тень, при пневмоните выявляются ограниченные затемнения в легких, усиливается диффузный рисунок в прикорневых зонах. В отдельных случаях на снимке четко видна кардиомегалия, ограничение подвижности левого купола диафрагмы.
- УЗИ перикарда и плевральной полости. Производится оценка эхографической картины, визуализируется утолщение листков перикарда, выявляется наличие и определяется количество жидкости в перикардиальной и плевральной полостях.
В неясных диагностических случаях для дифференциации болей и выявления жидкости в полостях или инфильтратов в легочной ткани назначается МРТ сердца и легких. При наличии признаков тампонады для уточнения характера выпота, скопившегося в околосердечной сумке, проводится диагностический перикардиоцентез с последующим лабораторным исследованием полученного материала.
Лечение постинфарктного синдрома
Лечение проходит в условиях специализированного стационара. Главная роль в перечне лечебных мероприятий принадлежит медикаментозной терапии. Она преследует несколько целей, и предполагает применение фармакопрепаратов разнонаправленного механизма действия:
- Противовоспалительные. При отсутствии противопоказаний препаратами выбора являются НПВП, которые назначаются с учетом профиля безопасности. В случае резистентности к нестероидным средствам проводятся короткие курсы глюкокортикоидов. При тяжелом течении болезни, рефрактерном к противовоспалительной терапии нестероидными средствами и гормонами, применяются ЛС других групп (колхицин, метотрексат).
- Кардиотропные. Для устранения сердечных нарушений назначаются препараты, использующиеся при лечении ишемической болезни сердца: антиангинальные средства, бета-блокаторы, блокаторы кальциевых каналов, нитраты, сердечные гликозиды. При назначении учитывается основной механизм фармакологического действия, возможные побочные эффекты и кардиотоксичность.
Антикоагулянты в связи с высоким риском развития гемоперикарда не применяются. При необходимости их использования назначаются субтерапевтические дозировки. В каждом конкретном случае лечение ПС подбирается индивидуально. При выраженных болях показаны внутримышечные инъекции анальгетиков. При большом скоплении выпота выполняется плевроцентез или пункция перикардиальной полости. При сердечной тампонаде проводится хирургическая операция — перикардэктомия.
Прогноз и профилактика
Постинфарктный синдром не является опасным для жизни состоянием, и даже при самом тяжелом течении прогноз относительно благоприятный. Методы первичной профилактики, направленной на устранение причин ПС, еще не разработаны. Для снижения частоты суставных проявлений пациентам, перенесшим острый ИМ, рекомендуется ранняя активизация. При заболеваниях с рецидивирующим течением назначается противорецидивная терапия, призванная предотвратить повторные обострения патологического процесса.
Синдром Дресслера (постинфарктный синдром) — Симптомы и лечение. Журнал Медикал
 Причины сидрома
Причины сидрома
Симптомы
Диагностика
Лечение
Образ жизни, осложнения и прогноз
Инфаркт миокарда опасен не только тем, что вызывает значительное нарушение функций сердечно-сосудистой системы, но еще и тем, что может приводить к развитию осложнений. Одним из них является синдром Дресслера, или постинфарктный синдром.
Синдром Дресслера – это аутоиммунное поражение соединительной ткани в организме пациента, перенесшего обширный инфаркт миокарда. Проявляется лихорадкой, поражением перикарда, плевры, легочной ткани и суставных оболочек. Развивается в 4% всех случаев на 10 – 14 день от начала инфаркта. Опасность этого синдрома в том, что он может протекать длительно, с периодическими обострениями и ремиссиями, нарушая качество жизни и самочувствие пациента.
Выделяют следующие формы синдрома:
1. Типичная форма характеризуется различными сочетаниями повреждений соединительной ткани:
— перикардиальный вариант
— плевральный
— пневмонический
— перикардиально–пневмонический
— перикардиально–плевральный
— плевро–пневмонический
— перикардиально-плеврально-пневмонический
2. Атипичная форма проявляется кардио-плечевым, артритическим, кожным, перитонеальным вариантами.
3. Малосимптомная (стертая) форма проявляется субфебрильной лихорадкой, болями в суставах и изменениями в общем анализе крови.
Причины синдрома Дресслера
Основной причиной заболевания является повреждение и гибель (некроз) клеток сердечной мышцы при остром инфаркте миокарда, выход продуктов распада в кровь и аутосенсибилизация (повышенная иммунная чувствительность, направленная на собственные ткани) организма к денатурированному белку погибших клеток. Происходит агрессия иммунных клеток, ответственных за распознавание антигенов (чужеродных веществ), но в данном случае эта реакция направлена против молекул белка, располагающихся на клетках оболочек, выстилающих сердце, легкие и суставы — перикарда, плевры и синовиальных (суставных) оболочек. В результате имеет место перекрестная аутоиммунная реакция с собственными клетками, которые организм расценивает как чужеродные. Плевра, перикард и синовиальные оболочки воспаляются, но воспаление носит асептический характер, без бактерий и вирусов, и выделяют некоторое количество жидкости, которая скапливается между листками плевры и перикарда, а также в суставах, вызывая боль и нарушение функций.
Не только крупноочаговый или трансмуральный инфаркт миокарда может явиться причиной синдрома Дресслера, но и хирургические вмешательства на сердце. После реконструктивных операций на митральном клапане редко развивается посткомиссуротомный синдром, а после вмешательств на сердце с рассечением перикарда – посткардиотомный синдром. Эти варианты схожи с постинфарктным синдромом в плане причин, механизмов развития, клинических проявлений и лечения, поэтому обобщенно они все называются синдромом Дресслера.
Увеличивают риск развития данного осложнения имеющиеся у пациента системные аутоиммунные заболевания (системная красная волчанка, ревматоидный артрит и др), а также поздняя двигательная активизация пациента после инфаркта.
Симптомы синдрома Дресслера
Клинические проявления могут возникнуть во временном промежутке от двух недель до двух месяцев после острого инфаркта. Синдром Дресслера проявляется такими признаками:
— Общее недомогание и плохое самочувствие.
— Повышение температуры чаще происходит до субфебрильных цифр (не выше 39 0С), в межприступный период может быть стойкий субфебрилитет (37.3 – 38 0С).
— Перикардит – обязательный признак синдрома Дресслера. Проявляется болями в области сердца острого, давящего, сжимающего характера, усиливающимися на высоте вдоха и при кашле и исчезающими в положении лежа или сидя с наклоном вперед. Могут отдавать в шею, плечо и левую руку.
— Пневмонит (не следует путать с пневмонией — воспалительным бактериальным или вирусным поражением легких) развивается вследствие поражения интерстициальной ткани легких и проявляется разлитыми болями в грудной клетке с обеих сторон, одышкой при нагрузке и сухим кашлем, иногда с прожилками крови. При жалобах пациента на одышку, кашель и кровохарканье врач должен думать о другом грозном осложнении инфаркта – тромбоэмболии легочной артерии.
— Плеврит проявляется поверхностной болью в левой половине грудной клетки, больше сбоку и сзади и сухим кашлем. Боли и кашель самостоятельно исчезают в течение двух – четырех дней. Плеврит в сочетании с признаками перикардита, пневмонита и температурой позволяет достоверно предположить диагноз синдрома Дресслера.
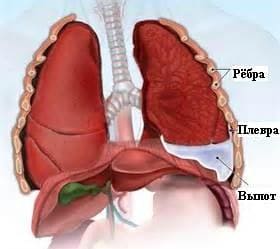
На рисунке изображен выпот в плевральной полости
— Синдром «грудь — плечо — рука» (кардиоплечевой синдром) в настоящее время развивается гораздо реже, чем раньше, что связывают с более ранней активизацией пациента после инфаркта. Проявляется болями в области левого плечевого сустава, нарушениями чувствительности в левой руке, чувством онемения и «ползания мурашек» в кисти, бледной, мраморной окраской кожи руки и кисти.
— Синдром передней грудной стенки обусловлен прогрессированием остеохондроза суставов в месте соединении грудины и ключицы, и, вероятнее всего, также связан с длительной неподвижностью пациента в остром периоде инфаркта. Проявляется болью и припухлостью в области грудины и ключицы слева.
— Кожные проявления: могут развиться высыпания на коже, напоминающие крапивницу, дерматит, экзему или эритему.
В большинстве случаев наблюдается хроническое течение синдрома с обострениями, которые длятся от нескольких дней до 3 – 4 недель, и ремиссиями продолжительностью несколько месяцев. Редко наблюдается однократная атака с полным выздоровлением.
Диагностика синдрома Дресслера
Диагноз может быть заподозрен на основании характерных жалоб пациента после перенесенного инфаркта в последние два месяца, а также на основании данных осмотра пациента – при аускультации грудной клетки выслушиваются шум трения перикарда и плевры, влажные хрипы в нижних отделах легких. Для уточнения диагноза могут быть назначены дополнительные методы исследования:
— Развернутый анализ крови – наблюдаются увеличение числа лейкоцитов (более 10 х 109/л), ускорение СОЭ (более 20 мм/час), увеличение количества эозинофилов (более 5% в лейкоцитарной формуле).
— Биохимический анализ крови, ревматологические пробы, иммунологические исследования. Определяется повышенный уровень С – реактивного белка, может быть повышен уровень МВ – фракции креатинфосфокиназы и тропонинов (маркеров острого инфаркта), но не всегда, что требует дифференциальной диагностики с повторным инфарктом миокарда.
— ЭКГ не выявляет каких – либо значимых отклонений, кроме признаков рубцующегося инфаркта.
— Эхокардиография выявляет утолщение листков перикарда, ограничение их подвижности, наличие жидкости (выпота) в перикардиальной полости. Определяются зоны сниженной сократимости миокарда (гипокинезия), свидетельствующая о перенесенном инфаркте.
— Рентгенография грудной клетки – определяются утолщение междолевой плевры при плеврите, может быть диффузное усиление легочного рисунка, линейные или очаговые затемнения в легочной ткани при пневмоните, увеличение тени сердца при перикардите.
— Рентгенография плечевых суставов может показать сужение суставной щели, уплотнение костных тканей и другие признаки имеющегося ранее остеоартроза.
— КТ или МРТ грудной клетки назначаются в диагностически неясных случаях для уточнения характера перикардита, плеврита и пневмонита.
Лечение синдрома Дресслера
Терапия синдрома, возникшего впервые в жизни, должна проводиться в стационаре. Последующие рецидивы могут лечиться амбулаторно при нетяжелом течении.
Из препаратов внутривенно и в таблетированных формах назначаются:
— преднизолон, дексаметазон и другие глюкокортикоидные гормоны в суточной дозе 30 – 40 мг. Улучшение состояния наблюдается уже на второй – третий день от начала лечения гормонами, но терапия должна быть долгой, в течение нескольких недель и месяцев, так как при отмене препаратов возможен новый рецидив. Необходима постепенная отмена преднизолона, со снижением дозировки на 5 мг в неделю до полной отмены препарата.
— нестероидные противовоспалительные средства (НПВС): диклофенак, индометацин, аспирин, нимесулид, дозировки определяются лечащим врачом.
— антибиотики неэффективны, но могут быть назначены при трудностях дифференциальной диагностики с инфекционным поражением легких, перикарда и суставов.
— кардиотропные препараты для терапии ИБС – аспирин, беттаблокаторы, гиполипидемические препараты (статины), ингибиторы АПФ и др.
— анальгин с димедролом внутримышечно при выраженном болевом синдроме.
Кроме медикаментозной терапии, в случаях выраженного выпотного плеврита и перикардита, когда в полостях скапливается значительное количество жидкости, могут быть показаны плевральная и перикардиальная пункции с удалением выпота.
Образ жизни с синдромом Дресслера
Пациенты с постинфарктным синдромом должны соблюдать здоровый образ жизни, который необходим для всех пациентов, перенесших острый инфаркт миокарда. Должны соблюдаться следующие несложные принципы:
— здоровое питание – большее употребление в пищу свежих овощей и фруктов, соков, морсов, злаковых продуктов и крупяных изделий, замена животных жиров на растительные. Следует ограничивать употребление жирных сортов мяса и птицы, исключить кофе, газированные напитки, жареные, острые, соленые, пряные блюда, а пищу готовить в отварном виде или на пару. Рекомендуется уменьшить количество потребляемой соли до 5 гр в сутки, а объем выпиваемой жидкости – до 1.5 литров в день;
— отказ от вредных привычек;
— ранняя активизация пациента в постели в остром периоде инфаркта и умеренная физическая активность в дальнейшем. Уже на вторые – третьи сутки при инфаркте показаны дыхательные упражнения и лечебная физкультура под контролем врача в положении лежа в постели (при строгом постельном режиме — движения кистями рук, упражнения на расслабление), а затем сидя и стоя (при палатном режиме) продолжительностью не более 5 – 10 минут. При дальнейшем санаторно – курортном лечении применяются дозированная ходьба, лечебная гимнастика и др.
Осложнения
Осложнения при постинфарктном синдроме практически не развиваются, хотя описаны единичные случаи тяжелого поражения почек с развитием гломерулонефрита, и поражения сосудов в виде геморрагического васкулита. Редко, при отсутствии лечения гормональными препаратами, возможен исход выпотного перикардита в слипчивый перикардит, который мешает расслаблению сердечной мышцы и способствует застою крови в большом круге кровообращения. Развивается рестриктивная (диастолическая) сердечная недостаточность.
Прогноз
Прогноз для жизни благоприятный.
Временная утрата трудоспособности (больничный лист) при осложненном синдромом Дресслера инфаркте миокарда определяется на срок 3 – 3.5 месяца, по показаниям возможно дольше.
Стойкая утрата трудоспособности (инвалидность) определяется частотой рецидивов, степенью нарушений сердечно – сосудистых функций, вызванных не только плевритом, перикардитом и поражением суставов, но и самим инфарктом миокарда. Как правило, непосредственно синдром Дресслера к инвалидизации не приводит.
Врач терапевт Сазыкина О.Ю.
Синдром Дресслера
Синдром, обусловленный аутосенсибилизацией к продуктам распада сердечной ткани и излившейся крови в перикард.
Развивается у 3-6% больных, чаще у больных, перенесших крупноочаговый инфаркт миокарда, осложнившийся эпистенокардитическим перикардитом.
Клиническая симптоматика возникает через 2-6 недель после начала инфаркта миокарда. Проявляется перикардитом, плевритом, пневмонитом. Реже встречаются миозит грудной мышцы, артрит плечевого сустава.
Длительность проявлений — от 3-4 дней до 4 недель.
При перикардите отмечается длительный болевой синдром, четко не связанный с нагрузками. Боль усиливается при глубоком вдохе, поворотах туловища. Значительного накопления жидкости в перикарде обычно нет. Выслушивается отчетливый шум трения перикарда, более выраженный слева от грудины в 3-5 межреберьях.
При пневмоните во время аускультации отмечают влажные хрипы, при рентгенологическом обследовании — различной выраженности затемнения. Пневмонит может сочетаться с накоплением жидкости в плевральной полости.
Миозиты грудной мышцы сопровождаются болями, определяющимися пальпаторно и усиливающимися при движении плечевого пояса.
На ЭКГ формируются подъемы сегмента ST в нескольких отведениях, увеличение отрицательной фазы T. Могут возникнуть трудности дифференциальной диагностики с рецидивом или повторным инфарктом миокарда. Для дифференциальной диагностики важны клинические данные и результаты лабораторного обследования.
Обычно выявляют лейкоцитоз, эозинофилию, повышение СОЭ, СРП, фибрина, сиаловых кислот, гамма-глобулинов.
Течение заболевания острое, затяжное или рецидивирующее. Обострения не зависят от характера течения и проявлений ИБС. По вариантам синдром Дресслера разделяют на типичный, атипичный и малосимптомный. Изредка синдром Дресслера протекает с проявлениями геморрагического васкулита (А.Я.Арипов и соавт., 1978), бронхиальной астмы, поражений почек, аутоиммунного гепатита (А.В.Сумароков, З.Г.Апросина, 1972), проктита, желудочно-кишечного кровотечения (А.Д.Хетагуров и др., 1987), перикардита с тампонадой сердца (А.И.Кирсанов и соавт., 1990).
Лечебные мероприятия заключаются в приеме преднизолона в дозе 15-20 мг в сутки. Меньшее значение имеют противовоспалительные и десенсибилизирующие средства.
Тромбоэндокардит
Поражение эндокарда при инфаркте миокарда приводит к образованию пристеночных тромбов.
Клиническими проявлениями этого осложнения являются длительный субфебрилитет, потливость, слабость, тахикардия, признаки сердечной недостаточности, лейкоцитоз, ускорение СОЭ. Характерны тромбоэмболии большого круга кровообращения.
Диагностика основывается на отчетливой клинической симптоматике и обнаружении пристеночных тромбов при эхокардиографическом обследовании. Могут проводиться исследования с радиоактивным фибриногеном, который откладывается в тромбах.
Лечебные мероприятия заключаются в назначении антикоагулянтов и дезагрегантов.
Тромбоэмболические осложнения
В настоящее время при использовании тромболитических препаратов и дезагрегантов тромбоэмболические осложнения встречаются у 2-6 % больных с инфарктом миокарда.
В механизмах их возникновения большое значение имеют повышение свертывающей активности крови, развитие ДВС синдрома; изменения сосудистой стенки в связи с атеросклерозом; застой крови, обусловленный шоком и сердечной недостаточностью; нарушение сердечной гемодинамики в связи с образованием аневризмы, дилатации миокарда, мерцательной аритмии; тромбоэндокардит; обострение тромбофлебитов малого таза, голеней. В развитии этих осложнений большое значение имеет длительная обездвиженность больного.
Наиболее часто отмечается тромбоэмболия легочной артерии. Диагностика ее сложна. Связано это с малой специфичностью симптоматики, трудностью отличия ее от проявлений инфаркта миокарда. У больных с ТЭЛА отмечается динамика ЭКГ, напоминающая задний инфаркт миокарда: Q III (SI-Q III), отрицательный T в III, aVF, V1-V4, высокий Р во II, III отведениях. Отличием являются: высокий R в III отведении, повышение «легочной» фракции ЛДГ3. Диагноз подтверждается динамикой рентгенологических изменений в легких.
Тромбоэмболии конечностей приводят к внезапной сильной боли, похолоданию ее, исчезновению пульса, появлению парестезии, исчезновению чувствительности, парезам.
Тромбоэмболия почечных артерий характеризуется различной выраженностью болей в области поясницы, слабостью, тошнотой, рвотой, повышением артериального давления, появлением эритроцитов в моче. Может быть олигурия, симптомы почечной недостаточности.
Тромбоэмболия мезентериальных артерий проявляется сильной, неопределенной болью в животе. Затем развивается парез кишечника и клиника динамической непроходимости. Может быть дегтеобразный стул. Часто развивается шок.
Тромбоэмболия мозговых сосудов. Клиническая картина характеризуется внезапной головной болью, развитием очаговой симптоматики. Могут быть различной выраженности общемозговые симптомы.
При всех тромбоэмболических осложнениях может возникать острая левожелудочковая недостаточность.
Синдром Дресслера в кардиологии: современная диагностика и лечение
Синдром Дресслера – редкое аутоиммунное заболевание, возникающее на фоне ранее перенесенного инфаркта миокарда. Первые симптомы патологии развиваются лишь спустя несколько недель или месяцев с момента формирования ишемических изменений в мышечной ткани сердца. Клинические признаки связаны с возникновением перикардита, воспаления серозных оболочек грудной полости и легких. Проявления включают в себя одышку, общую слабость, кашель и болевые ощущения. Лечение основано на применении гормональных средств, угнетающих иммунный ответ. Профилактика предполагает недопущение развития инфаркта миокарда, который является основным этиологическим фактором недуга.
Причины возникновения
Заболевание представляет собой аутоиммунный процесс. Это означает, что проблема формируется вследствие неадекватной работы защитных механизмов организма. Установлено, что возникновение синдрома Дресслера после инфаркта провоцируется следующим каскадом реакций:
- Ишемические процессы в миокарде приводят к изменению нормального строения мышечной ткани. При кислородном голодании клетки погибают, то есть образуется некроз.
- Постинфарктный синдром развивается в тех случаях, когда иммунная система неправильно реагирует на отмершие элементы кардиальных структур. В норме отдельные участки некроза окружены воспалением, однако патологические комплексы антиген-антитело не образуются.
- Возникновение болезни можно сравнить с аллергией. Организм отторгает погибшие клетки, то есть реагирует на содержащийся в тканях белок. Однако в случае с синдромом Дресслера иммунные комплексы образуются в ответ на повреждение собственных клеток организма. Их отложение приводит к усугублению воспаления, которое поражает не только мышечную ткань, но и перикард, а также серозные оболочки, легкие и даже суставы.
Самой частой причиной подобного аутоиммунного процесса является ишемическое повреждение миокарда. Именно поэтому синдром Дресслера называют постинфарктным. Однако другие факторы также способны провоцировать развитие недуга. Нарушение формируется как осложнение кардиологических операций, при травматических повреждениях сердца, а также при заражении некоторыми вирусными инфекциями.
Таким образом, для возникновения синдрома Дресслера требуется повреждающее воздействие тканей сердца, которое сопровождается развитием воспаления. А изменение нормального иммунного ответа на данный процесс и приводит к формированию характерной клинической картины.

На начальном этапе изучения заболевания Дресслер сделал предположение по поводу распространенности поражения. Он выдвинул гипотезу о том, что иммунологическое расстройство будет встречаться примерно у 3–4% пациентов, перенесших ранее инфаркт миокарда. Однако на сегодняшний день проблема диагностируется намного реже. Врачи связывают данную закономерность со значительным прогрессом в медицинской сфере. Важную роль при этом играет не только терапия самого синдрома Дресслера, но и помощь, оказываемая больным с острой ишемией сердца.
Современные методы борьбы с инфарктом, а также его ускоренная диагностика значительно снизили процент осложнений.
Риск пострадать от развития патологии иммунного ответа сохраняется у пациентов, страдающих одновременно несколькими расстройствами, а также у лиц, которые заражаются инфекционными патологиями в период реабилитации. Есть данные и о высокой вероятности возникновения синдрома Дресслера в постинфарктном состоянии у людей, которые ранее проходили длительную терапию «Преднизолоном» и другими кортикостероидами. Предположительно, больше шансов столкнуться с подобным осложнением и у пациентов с третьей группой крови и отрицательным резус-фактором.
Характерная симптоматика
В кардиологии описано несколько форм заболевания:
- Типичное течение синдрома Дресслера связано с развитием воспаления в полости сердечной сумки, легких и суставах. В патологический процесс вовлекается и плевра. Данный вид проблемы встречается чаще всего.
- Атипичная форма заболевания сопровождается поражением суставов, развитием кожных проявлений аллергии, а также возникновением у пациента астмы и перитонита. В ряде случаев симптомы синдрома Дресслера включают в себя воспаление почек, внутренней поверхности сосудов и надкостницы.
- В редких случаях клинические признаки патологии включают в себя гипертермию на фоне увеличения количества лейкоцитов в крови, а также повышение показателя СОЭ. При этом классические проявления недуга зачастую не регистрируются, что во многом затрудняет диагностику проблемы. Тогда говорят о малосимптомной форме заболевания.
Основные клинические признаки синдрома Дресслера, возникающие при типичном течении недуга, включают в себя:
- Развитие перикардита, происходящее вследствие скопления иммунных комплексов в сердечной сумке. На фоне данного процесса отмечается сильное воспаление, приводящее к выраженной боли. Кроме этого, регистрируются жалобы на одышку, а также видимое увеличение вен в области шеи. Зачастую перикардит сопровождают отеки конечностей и асцит. При отсутствии адекватной медицинской помощи велик риск развития тампонады сердца.
- Плеврит – второй характерный симптом синдрома Дресслера. Принято дифференцировать два типа патологии: сухой и влажный. В первом случае диагностируется характерный шум трения, который ощущается пациентами при дыхании. Поражаться могут как обе половины грудной клетки, так и только одна. Если между серозными листками скапливается экссудат, боли становятся менее интенсивными. Отмечается приглушенность сердечного толчка, синюшность покровов и значительное ухудшение самочувствия.
- Пневмонит при синдроме Дресслера встречается реже, чем плеврит или перикардит. Характерно поражение нижних отделов легких. У пациентов возникает сильный кашель, в результате чего происходит отхождение мокроты, зачастую с примесями крови. Во время аускультации дыхательной системы выслушиваются влажные хрипы.
В большинстве случаев отмечается сочетание сразу нескольких характерных симптомов. Именно это позволяет врачам заподозрить аутоиммунную патологию.

Необходимая диагностика
На развитие синдрома Дресслера указывает ранее перенесенный инфаркт миокарда, а также операции на сердце или его травматические повреждения. Для подтверждения наличия проблемы проводится осмотр пациента, аускультация и перкуссия грудной клетки, в ходе чего обнаруживаются характерные признаки болезни. Диагностировать образование экссудата в сердечной сумке и между серозными листками грудной полости можно при помощи рентгена.
На снимках визуализируются характерные затемнения, а также отмечаются признаки увеличения границ сердца. В ряде случаев с целью подтверждения недуга используется и компьютерная томография, которая дает более четкое изображение.
Диагностика синдрома Дресслера подразумевает проведение ЭХО. В ходе УЗИ обнаруживается характерное скопление жидкости, а также утолщение листков перикарда и развитие спаечных процессов. Для оценки характера экссудата осуществляется пункция с забором содержимого на анализ. С целью определения вовлеченности в процесс других внутренних органов используются лабораторные тесты.
Лечебные мероприятия
Несмотря на то что синдром Дресслера не относится к числу неотложных состояний, в отличие от инфаркта, он также требует оказания своевременной медицинской помощи. В большинстве случаев при заболевании проводится консервативная терапия с использованием различных групп препаратов. При отсутствии эффекта от подобных методов прибегают к применению хирургических техник. Рекомендации включают в себя также сбалансированное питание, отдых и отказ от вредных привычек.
Лекарственная терапия
Для борьбы с заболеванием используются следующие средства:
- Нестероидные противовоспалительные препараты назначаются при стабильном состоянии пациента. К данной группе относятся такие медикаменты, как «Ибупрофен» и «Диклофенак». Они способствуют уменьшению интенсивности клинических проявлений.
- Основу лечения синдрома Дресслера составляют глюкокортикоиды, такие как «Дексаметазон» и «Преднизолон». Эти соединения угнетают патологические защитные реакции, за счет чего прекращается формирование иммунных комплексов и наступает видимое улучшение самочувствия пациента. При рецидивировании проблемы гормональная терапия используется на протяжении всей жизни.
- Для поддержания работы сердечной мышцы назначаются препараты, содержащие такие элементы, как калий и магний. К числу подобных средств относятся «Панангин» и «Аспаркам».
- При наличии выраженного болевого синдрома оправдано использование сильнодействующих анальгетиков.
- С целью профилактики развития вторичной инфекции назначаются антибиотики, например, «Кларитромицин». Они применяются в комбинации со стероидами и препятствуют размножению патогенных бактерий.
Хирургическое вмешательство
При отсутствии эффекта от консервативной терапии применяются более радикальные методы:
- Перикардэктомия – процедура, заключающаяся в резекции сердечной сумки. Серозные листы удаляются полностью или частично. Такая операция используется с целью снятия давления с кардиальных структур.
- Пункция перикардиальной полости. Она выполняется как с диагностической, так и с лечебной целью. Откачивание экссудата из полости сердечной сумки приводит к значительному улучшению состояния пациента.
Прогноз при своевременном лечении благоприятный. Раннее обращение к врачу предотвращает развитие опасных для жизни осложнений.
Отзывы
Лидия, 45 лет, г. Ростов
У мамы после перенесенного инфаркта миокарда развился синдром Дресслера – редкая аутоиммунная проблема. Ее положили в больницу на капельницы, пришлось даже делать пункцию перикарда, чтобы откачать скопившуюся там жидкость. Выписали маму через две недели. Гормональные средства она принимала еще долго.
Сергей, 38 лет, г. Астрахань
Отец не так давно перенес инфаркт. Через месяц после приступа его снова госпитализировали. На этот раз с синдромом Дресслера – редким осложнением ишемии сердца. Папе назначили кортикостероиды и поддерживающие препараты, он пролежал под капельницами неделю. На фоне лечения состояние значительно улучшилось. Гормоны отец принимает до сих пор.
 Загрузка…
Загрузка…