ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ (РН) | Энциклопедия Кругосвет
ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ (РН). Одно из важнейших свойств водных растворов – их кислотность (или щелочность), которая определяется концентрацией ионов Н+ и ОН– (см. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ. ЭЛЕКТРОЛИТЫ). Концентрации этих ионов в водных растворах связаны простой зависимостью [H+][OH–] = Кw; (квадратными скобками принято обозначать концентрацию в единицах моль/л). Величина Kw называется ионным произведением воды и при данной температуре постоянна. Так, при 0оС она равна 0,11Ч10–14, при 20оС – 0,69Ч10–14, а при 100оС – 55,0Ч10–14. Чаще всего пользуются значением Kw при 25оС, которое равно 1,00Ч10–14. В абсолютно чистой воде, не содержащей даже растворенных газов, концентрации ионов Н+ и ОН– равны (раствор нейтрален). В других случаях эти концентрации не совпадают: в кислых растворах преобладают ионы Н
Из сказанного следует, что можно однозначно выразить кислотность раствора, указав концентрацию в нем только ионов водорода. Например, в чистой воде [H+] = 10–7 моль/л. На практике оперировать такими числами неудобно. Кроме того, концентрации ионов Н+ в растворах могут отличаться в сотни триллионов раз – примерно от 10 –15 моль/л (крепкие растворы щелочей) до 10 моль/л (концентрированная соляная кислота), что невозможно изобразить ни на каком графике. Поэтому давно договорились для концентрации ионов водорода в растворе указывать только показатель степени 10, взятый с обратным знаком; для этого концентрацию следует выразить в виде степени 10х, без множителя, например, 3,7Ч10–3 = 10–2,43. (При более точных расчетах, особенно в концентрированных растворах, вместо концентрации ионов используют их активности.) Этот показатель степени получил название водородного показателя, а сокращенно рН – от обозначения водорода и немецкого слова Potenz – математическая степень. Таким образом, по определению, рН = –lg[Н+]; эта величина может изменяться в небольших пределах – всего от –1 до 15 (а чаще – от 0 до 14). При этом изменению концентрации ионов Н+ в 10 раз соответствует изменение рН на одну единицу. Обозначение рН ввел в научный обиход в 1909 датский физикохимик и биохимик С.П.Л.Сёренсен, который занимался в то время изучением процессов, происходящих при сбраживании пивного солода, и их зависимостью от кислотности среды.
При комнатной температуре в нейтральных растворах рН = 7, в кислых растворах рН < 7, а в щелочных рН > 7. Приблизительно значение рН водного раствора можно определить с помощью индикаторов. Например, метиловый оранжевый при рН < 3,1 имеет красный цвет, а при рН > 4,4 – желтый; лакмус при рН < 6,1 красный, а при рН > 8 – синий и т.д. Более точно (до сотых долей) значение рН можно определить с помощью специальных приборов – рН-метров. Такие приборы измеряют электрический потенциал специального электрода, погруженного в раствор; этот потенциал зависит от концентрации ионов водорода в растворе, и его можно измерить с высокой точностью.
Интересно сравнить значения рН растворов различных кислот, оснований, солей (при концентрации 0,1 моль/л), а также некоторых смесей и природных объектов. Для малорастворимых соединений, отмеченных звездочкой, приведены рН насыщенных растворов.
Таблица 1. Водородные показатели для растворов | |
| Раствор | РН |
| HCl | 1,0 |
| H2SO4 | 1,2 |
| H2C2O4 | 1,3 |
| NaHSO4 | 1,4 |
| Н3РО4 | 1,5 |
| Желудочный сок | 1,6 |
| Винная кислота | 2,0 |
| 2,1 | |
| HNO2 | 2,2 |
| Лимонный сок | 2,3 |
| Молочная кислота | 2,4 |
| Салициловая кислота | 2,4 |
| Столовый уксус | 3,0 |
| Сок грейпфрута | 3,2 |
| СО2 | 3,7 |
| Яблочный сок | 3,8 |
| H2S | 4,1 |
| Моча | 4,8–7,5 |
| Черный кофе | 5,0 |
| Слюна | 7,4–8 |
| Молоко | 6,7 |
| Кровь | 7,35–7,45 |
| Желчь | 7,8–8,6 |
| Вода океанов | 7,9–8,4 |
| Fe(OH)2 | 9,5 |
| MgO | 10,0 |
| Mg(OH)2 | 10,5 |
| Na2CO3 | 11 |
| Ca(OH)2 | 11,5 |
| NaOH | 13,0 |
Таблица позволяет сделать ряд интересных наблюдений. Значения рН, например, сразу показывают сравнительную силу кислот и оснований. Хорошо видно также сильное изменение нейтральной среды в результате гидролиза солей, образованных слабыми кислотами и основаниями, а также при диссоциации кислых солей.
Природная вода всегда имеет кислую реакцию (рН < 7) из-за того, что в ней растворен углекислый газ; при его реакции с водой образуется кислота: СО2 + Н2О « Н+ + НСО32–. Если насытить воду углекислым газом при атмосферном давлении, рН полученной «газировки» будет равен 3,7; такую кислотность имеет примерно 0,0007%-ный раствор соляной кислоты – желудочный сок намного кислее! Но даже если повысить давление CO2 над раствором до 20 атм, значение pH не опускается ниже 3,3. Это значит, что газированную воду (в умеренных количествах, конечно) можно пить без вреда для здоровья, даже если она насыщена углекислым газом.
Определенные значения рН имеют исключительно большое значение для жизнедеятельности живых организмов. Биохимические процессы в них должны протекать при строго заданной кислотности. Биологические катализаторы – ферменты способны работать только в определенных пределах рН, а при выходе за эти пределы их активность может резко снижаться. Например, активность фермента пепсина, который катализирует гидролиз белков и способствует таким образом перевариванию белковой пищи в желудке, максимальна при значениях рН около 2. Поэтому для нормального пищеварения необходимо, чтобы желудочный сок имел довольно низкие значения рН: в норме 1,53–1,67. При язвенной болезни желудка рН понижается в среднем до 1,48, а при язве двенадцатиперстной кишки может доходить даже до 105. Точное значение рН желудочного сока определяют путем внутрижелудочного исследования (рН-зонд). Если у человека понижена кислотность, врач может назначить прием с пищей слабого раствора соляной кислоты, а при повышенной кислотности – принимать противокислотные средства, например, гидроксиды магния или алюминия. Интересно, что если выпить лимонный сок, кислотность желудочного сока… понизится! Действительно, раствор лимонной кислоты лишь разбавит более сильную соляную кислоту, содержащуюся в желудочном соке.
В клетках организма рН имеет значение около 7, во внеклеточной жидкости – 7,4. Нервные окончания, которые находятся вне клеток, очень чувствительны к изменению рН. При механических или термических повреждениях тканей стенки клеток разрушаются и их содержимое попадает на нервные окончания. В результате человек чувствует боль. Скандинавский исследователь Олаф Линдал проделал такой эксперимент: с помощью специального безыгольного инъектора человеку впрыскивали сквозь кожу очень тонкую струйку раствора, которая не повреждала клетки, но действовала на нервные окончания. Было показано, что боль вызывают именно катионы водорода, причем с уменьшением рН раствора боль усиливается. Аналогично непосредственно «действует на нервы» и раствор муравьиной кислоты, который жалящие насекомые или крапива впрыскивают под кожу. Разным значением рН тканей объясняется также, почему при некоторых воспалениях человек чувствует боль, а при некоторых – нет.
Интересно, что впрыскивание под кожу чистой воды дало особенно сильную боль. Объясняется это странное на первый взгляд явление так: клетки при контакте с чистой водой в результате осмотического давления разрываются и их содержимое воздействует на нервные окончания.
В очень узких пределах должно оставаться значение рН крови; даже небольшое ее подкисление (ацидоз) или защелачивание (алкалоз) может привести к гибели организма. Ацидоз наблюдается при таких заболеваниях как бронхит, недостаточность кровообращения, опухоли легких, пневмония, диабет, лихорадка, поражения почек и кишечника. Алколоз же наблюдается при гипервентиляции легких (или при вдыхании чистого кислорода), при анемии, отравлении СО, истерии, опухоли мозга, избыточном потреблении питьевой соды или щелочных минеральных вод, приеме диуретических лекарств. Интересно, что рН артериальной крови в норме должно быть в пределах 7,37–7,45, а венозной – 7,34–7,43. Различные микроорганизмы также весьма чувствительны к кислотности среды. Так, патогенные микробы быстро развиваются в слабощелочной среде, тогда как кислую среду они не выдерживают. Поэтому для консервирования (маринование, соление) продуктов используют, как правило, кислые растворы, добавляя в них уксус или пищевые кислоты. Большое значение имеет правильный подбор рН и для химико-технологических процессов.
Поддержать нужное значение рН, не дать ему заметно отклониться в ту или другую сторону при изменении условий возможно при использовании так называемых буферных (от англ. buff – смягчать толчки) растворов. Такие растворы часто представляют собой смесь слабой кислоты и ее соли или слабого основания и его соли. Подобные растворы «сопротивляются» в определенных пределах (которые называются емкостью буфера) попыткам изменить их рН. Например, если попытаться немного подкислить смесь уксусной кислоты и ацетата натрия, то ацетат-ионы свяжут избыточные ионы Н+ в малодиссоциированную уксусную кислоту, и рН раствора почти не изменится (ацетат-ионов в буферном растворе много, так как они образуются в результате полной диссоциации ацетата натрия). С другой стороны, если ввести в такой раствор немного щелочи, избыток ионов ОН– будет нейтрализован уксусной кислотой с сохранением значения рН. Аналогичным образом действуют и другие буферные растворы, причем каждый из них поддерживает определенное значение рН. Буферным действием обладают также растворы кислых солей фосфорной кислоты и слабых органических кислот – щавелевой, винной, лимонной, фталевой и др. Конкретное значение рН буферного раствора зависит от концентрации компонентов буфера. Так, ацетатный буфер позволяет поддерживать рН раствора в интервале 3,8–6,3; фосфатный (смесь КН2РО4 и Na2HPO4) – в интервале 4,8 – 7,0, боратный (смесь Na2B4O7 и NaOH) – в интервале 9,2–11 и т.д.
Многие природные жидкости обладают буферными свойствами. Примером может служить вода в океане, буферные свойства которой во многом обусловлены растворенным углекислым газом и гидрокарбонат-ионами НСО3–. Источником последних, помимо СО2, являются огромные количества карбоната кальция в виде раковин, меловых и известняковых отложений в океане. Интересно, что фотосинтетическая деятельность планктона – одного из основных поставщиков кислорода в атмосферу, приводит к повышению рН среды. Происходит это в соответствии с принципом Ле Шателье в результате смещения равновесия при поглощении растворенного углекислого газа: 2Н+ + СО32–« Н+ + НСО3–« Н2СО3« Н2О + СО2. Когда в ходе фотосинтеза CO2 + H2O + hv ® 1/n(CH2O)n + O2 из раствора удаляется СО2, равновесие смещается вправо и среда становится более щелочной. В клетках организма гидратация СО2 катализируется ферментом карбоангидразой.
Клеточная жидкость, кровь также являются примерами природных буферных растворов. Так, кровь содержит около 0,025 моль/л углекислого газа, причем его содержание у мужчин примерно на 5% выше, чем у женщин. Примерно такая же в крови концентрация гидрокарбонат-ионов (их тоже больше у мужчин).
При исследовании почвы рН является одной из наиболее важных характеристик. Разные почвы могут иметь рН от 4,5 до 10. По значению рН, в частности, можно судить о содержании в почве питательных веществ, а также о том, какие растения могут успешно расти на данной почве. Например, рост фасоли, салата, черной смородины затрудняется при рН почвы ниже 6,0; капусты – ниже 5,4; яблони – ниже 5,0; картофеля – ниже 4,9. Кислые почвы обычно менее богаты питательными веществами, поскольку хуже удерживают в себе катионы металлов, необходимые растениям. Например, попавшие в почву ионы водорода вытесняют из нее связанные ионы Са2+. А вытесненные из глинистых (алюмосиликатных) пород ионы алюминия в больших концентрациях токсичны для сельскохозяйственных культур.
Для раскисления кислых почв используют их известкование – внесение веществ, постепенно связывающих избыток кислоты. Таким веществом могут служить природные минералы – мел, известняк, доломит, а также известь, шлак с металлургических заводов. Количество внесенного раскислителя зависит от буферной емкости почвы. Например, для известкования глинистой почвы требуется больше раскисляющих веществ, чем для песчаной.
Большое значение имеют измерения рН дождевой воды, которая может оказаться довольно кислой из-за присутствия в ней серной и азотной кислот. Эти кислоты образуются в атмосфере из оксидов азота и серы (IV), которые выбрасываются с отходами многочисленных производств, транспорта, котельных и ТЭЦ. Известно, что кислотные дожди с низким значением рН (менее 5,6) губят растительность, живой мир водоемов. Поэтому постоянно ведется контроль рН дождевой воды.
Илья Леенсон
Кислотно-основные индикаторы — Википедия
Материал из Википедии — свободной энциклопедии
Кислотно-основные индикаторы (pH-индикаторы[1]) — органические соединения, способные изменять цвет в растворе при изменении кислотности (pH). Индикаторы широко используют в титровании в аналитической химии и биохимии. Их преимуществом является дешевизна, быстрота и наглядность исследования. Однако из-за субъективности определения цвета и невысокой точности индикаторы pH не всегда удобны; поэтому для точного измерения pH используют pH-метры с цифровой индикацией.
 Измерение pH с помощью индикаторной бумаги
Измерение pH с помощью индикаторной бумагиKs{\displaystyle K_{s}}:
Ks=c(Ind−)⋅c(h4O+)c(HInd).{\displaystyle K_{s}={c(Ind^{-})\cdot c(H_{3}O^{+}) \over c(HInd)}.}
Индикаторы обычно используют, добавляя несколько капель водного или спиртового раствора, либо немного порошка (например, смесь мурексида с хлоридом натрия) к пробе исследуемого раствора. Так, при титровании, в аликвоту исследуемого раствора добавляют индикатор, и наблюдают за изменениями цвета в точке эквивалентности.
Другой способ применения — использование полосок бумаги, пропитанных раствором индикатора или смеси индикаторов и высушенных (например, Универсальный индикатор). Такие полоски выпускают в самых разнообразных вариантах — с нанесенной на них цветной шкалой — эталоном цвета (в том числе для окрашенных или мутных сред), или с напечатанными числовыми значениями рН; для точного измерения в узких диапазонах рН, и для ориентировочного исследования растворов; в рулончиках, коробках и пеналах, или в виде отрывных книжечек.
Современные индикаторные полоски могут быть изготовлены с красителем — индикатором, привитым к целлюлозе или иному полимеру. Это делает их устойчивыми к вымыванию, вплоть до многократного использования.
Кислотно-основные индикаторы (водные растворы)[править | править код]
Интервалы перехода цвета индикаторов[править | править код]
На рисунке приведены ориентировочные данные о существовании разных цветных форм индикаторов в водных растворах.
Более точные сведения (несколько переходов, численное значение pH) см. в следующем разделе.
Таблица значений рН перехода наиболее распространённых индикаторов[править | править код]
Приведены распространённые в лабораторной практике кислотно-основные индикаторы в порядке возрастания значений pH[2], вызывающих изменение окраски [3]. Римские цифры в квадратных скобках отвечают номеру перехода окраски (для индикаторов с несколькими точками перехода).
| Индикатор и номер перехода | х[4] | Цвет более кислой формы | Интервал pH и номер перехода | Цвет более щелочной формы | ||
|---|---|---|---|---|---|---|
| Малахитовый зелёный | жёлтый | 0,1-2,0 [l] | сине-зелёный | |||
| Метиловый фиолетовый | жёлтый | 0,13–0,5 [I] | зелёный | |||
| Крезоловый красный [I] | красный | 0,2–1,8 [I] | жёлтый | |||
| Метиловый фиолетовый [II] | зелёный | 1,0–1,5 [II] | синий | |||
| Тимоловый синий [I] | к | красный | 1,2–2,8 [I] | жёлтый | ||
| Тропеолин 00 | o | красный | 1,3–3,2 | жёлтый | ||
| Метиловый фиолетовый [III] | синий | 2,0–3,0 [III] | фиолетовый | |||
| (Ди)метиловый жёлтый | o | красный | 3,0–4,0 | жёлтый | ||
| Бромфеноловый синий | к | жёлтый | 3,0–4,6 | сине-фиолетовый | ||
| Конго красный | синий | 3,0–5,2 | к | красный | ||
| Метиловый оранжевый | o | красный | 3,1–(4,0)4,4 | (оранжево-)жёлтый | ||
| Бромкрезоловый зелёный | к | жёлтый | 3,8–5,4 | синий | ||
| Бромкрезоловый синий | жёлтый | 3,8–5,4 | синий | |||
| Лакмоид | к | красный | 4,0–6,4 | синий | ||
| Метиловый красный | o | красный | 4,2(4,4)–6,2(6,3) | жёлтый | ||
| Хлорфеноловый красный | к | жёлтый | 5,0–6,6 | красный | ||
| Лакмус (азолитмин) | красный | 5,0–8,0 (4,5-8,3) | синий | |||
| Бромкрезоловый пурпурный | к | жёлтый | 5,2–6,8(6,7) | фиолетовый | ||
| Бромтимоловый синий | к | жёлтый | 6,0–7,6 | синий | ||
| Нейтральный красный | o | красный | 6,8–8,0 | янтарно-жёлтый | ||
| Феноловый красный | о | жёлтый | 6,8–(8,0)8,4 | ярко-красный | ||
| Крезоловый красный [II] | к | жёлтый | 7,0(7,2)–8,8 [II] | тёмно-красный | ||
| α-Нафтолфталеин | к | жёлто-розовый | 7,3–8,7 | синий | ||
| Тимоловый синий [II] | к | жёлтый | 8,0–9,6 [II] | синий | ||
| Фенолфталеин[5] [I] | к | бесцветный | 8,2–10,0 [I] | малиново-красный | ||
| Тимолфталеин | к | бесцветный | 9,3(9,4)–10,5(10,6) | синий | ||
| Ализариновый жёлтый ЖЖ | к | бледно-лимонно-жёлтый | 10,1–12,0 | коричнево-жёлтый | ||
| Нильский голубой | синий | 10,1–11,1 | красный | |||
| Диазофиолетовый | жёлтый | 10,1–12,0 | фиолетовый | |||
| Малахитовый зелёный | сине-зелёный | 11,6-13,6 [ll] | бесцветный | |||
| Индигокармин | синий | 11,6–14,0 | жёлтый | |||
| Epsilon Blue | оранжевый | 11,6–13,0 | тёмно-фиолетовый | |||
- ↑ Юлия Блинохватова, Валерия Вихрева, Тамара Клейменова, Ольга Марковцева. Химия неорганическая и аналитическая. — Litres, 2017. — С. 33. — 66 с. — ISBN 9785040190010.
- ↑ Величины в круглых скобках взяты из книги «Краткий справочник химика», сост. В.И.Перельман, М.-Л., „Химия“, 1964.
- ↑ Точное значение рН перехода для большинства индикаторов несколько зависит от ионной силы раствора (I). Так, значение рН перехода, определяемое при I=0,1 (напр., раствор хлоридов натрия или калия) отличается от точки перехода в растворе с I=0,5 или I=0,0025 на 0,15…0,25 единицы рН.
- ↑ *Столбец «х» — характер индикатора: к—кислота, о—основание.
- ↑ Фенолфталеин в сильно щелочной среде обесцвечивается. В среде концентрированной серной кислоты также он даёт красную окраску, обусловленую строением катиона фенолфталеина, хотя и не такую интенсивную. Эти малоизвестные факты могут привести к ошибкам при определении реакции среды.
Универсальный индикатор[править | править код]
 Универсальная индикаторная бумага
Универсальная индикаторная бумагаШироко применяются смеси индикаторов, позволяющие определить значение pH растворов в большом диапазоне концентраций (1-10; 0-12). Растворами таких смесей — «универсальных индикаторов» обычно пропитывают полоски «индикаторной бумаги», либо сам индикатор наносится на край специальных полимерных полосок («визуальные индикаторные тест-полоски»)[1], с помощью которых можно быстро (с точностью до единиц рН, или даже десятых долей рН) определить кислотность исследуемых водных растворов. Для более точного определения полученный при нанесении капли раствора цвет индикаторной бумаги немедленно сравнивают с эталонной цветовой шкалой.
Антоцианы и другие растительные пигменты способны менять цвет в зависимости от рН среды (клеточного сока). Антоцианы имеют преимущественно красный цвет в кислой среде и синий в щелочной. Сок из красной капусты или столовой свёклы нередко используют в качестве индикатора при начальном обучении химии.
- Бейтс Р., Определение рН. Теория и практика, пер. с англ., 2 изд., Л., 1972
Определение рН в почве (лабораторная работа)
Материалы и оборудование: весы технические; колбы на 100 мл; дистиллированная вода; 1 н раствор KCl; стаканчики на 50 мл; стандартные буферные растворы с рН от 1,68 до 9,22; иономер; вспомогательный хлорсеребряный электрод; стеклянный электрод, предварительно выдержанный в 0,1 н растворе НСl.
Содержание работы: определение реакции почв относится к числу наиболее распространенных анализов, как при теоретических, так и при прикладных исследованиях почв. Реакция почвенного раствора имеет большое значение для произрастания растений и жизнедеятельности микроорганизмов, может определять развитие и направление химических и биохимических процессов, то есть влиять на трансформацию минеральной и органической части почвы, растворение, миграцию соединений и т.д.
Реакция почвенного раствора определяется концентрацией водородных ионов, но эта концентрация часто бывает очень малой, поэтому для удобства, в практических целях используется обратный десятичный логарифм активности этих ионов (ан+), который условно обозначается символом рН.
рН = -lg ан+
Таким образом, рН — это обратный десятичный логарифм активности или концентрации ионов водорода в растворе.
Символ рН позволяет выразить активность водородных ионов (ан+) в кислой и в щелочной среде, то есть представить ан+ в пределах 100 – 10-14. С увеличением концентрации водородных ионов (подкисление раствора) активность ионов водорода так же повышается, значение рН понижается; при подщелачивании раствора происходит обратное.
Например, при активности ан+ равной 10-3, отрицательный логарифм 10-3=3 и рН=3; если ан+=10-9, то –lg 10-9=9 и рН=9. В зависимости от величины рН реакция почв может изменяться от сильнокислой до сильнощелочной (табл. 30).
Таблица 30.
Уровни кислотности и щелочности почв
РН н2о | Название реакции среды | рНКСl |
<5,0 | Очень сильнокислая | <4,0 |
5,1-5,5 | Сильнокислая | 4,1-4,5 |
5,6-6,0 | Среднекислая | 4,6-5,0 |
6,1-6,5 | Слабокислая | 5,1-5,5 |
6,6-7,3 | Нейтральная | 5,6-6,0 |
7,4-7,9 | Слабощелочная | >6,0 |
8,0-8,5 | Среднещелочная | |
8,6-9,0 | Сильнощелочная | |
>9,0 | Очень сильнощелочная |
Кислая реакция характерна для подзолистых и дерново-подзолистых почв. Серые лесные почвы имеют слабокислую реакцию. Повышение кислотности пахотных горизонтов почв, может выражаться морфологически, когда появляется белесоватая окраска, отсутствует вскипание от соляной кислоты. Кроме этого, в растительном покрове появляются такие сорняки как щавель, щучка, фиалка трехцветная и др.
Реакция черноземов близка к нейтральной, в карбонатных горизонтах и карбонатных черноземах переходит в слабощелочную. Каштановые почвы характеризуются большей частью слабощелочной реакцией. Наиболее благоприятной для роста и развития растений является слабокислая, нейтральная или слабощелочная реакция среды.
В ходе лабораторной работы определяется актуальная (рНН2О) и потенциальная обменная (рНKCl) кислотность.
Ход определения:
В две колбы на 100 мл отвешивается на технических весах по 10 г воздушно-сухой почвы, пропущенной через сито с отверстиями диаметром в 1 мм. В одну колбу приливается 25 мл свежей дистиллированной воды, во вторую — 25 мл 1н раствора KCl (колбы подписать).
Дистиллированная вода должна иметь нейтральную рН, а KCl около 5,6.
Содержимое колб тщательно перемешивают и встряхивают на ротаторе в течение 5 мин., далее приступают к измерению величины рН водной и солевой суспензии потенциометрическим методом.
Потенциометрическое определение рН состоит в измерении электродвижущей силы (э.д.с.) гальванического элемента, состоящего из вспомогательного электрода с известным потенциалом и индикаторного электрода, потенциал которого зависит от концентрации активных ионов водорода в испытуемом растворе. Индикаторный электрод работает обратимо по отношению к иону, концентрация которого определяется.
Когда оба электрода погружаются в раствор, между ними возникает э.д.с., величина которой зависит от концентрации ионов водорода в испытуемом растворе.
В качестве вспомогательного электрода обычно применяют насыщенный хлорсеребряный электрод. В качестве индикаторного электрода при измерении рН лучше использовать стеклянный, т.к. он применим в широком диапазоне рН растворов, прост в обращении и удобен в работе.
Перед работой иономер проверяют по одному из стандартных буферных растворов с известной рН. Если ошибка измерения величины рН по буферному раствору не превышает ±0,05рН, то можно сразу приступать к анализу испытуемых растворов. Если ошибка больше, то производят проверку и калибровку прибора по двум стандартным буферным растворам, например с рН 1,68 и 9,22. После калибровки иономера и успокоения стрелки прибора приступают к измерению рН испытуемых растворов.
Электроды погружаются в стаканчик с испытуемым раствором, ожидается успокоение стрелки прибора и производится отсчет по верхней шкале прибора. При этом сопоставляются показания на верхней шкале и положение переключателя «пределы измерения».
Измеряемая величина рН будет равна: начальное значение рН для данного диапазона измерений (берется нижний предел измерений) + показание верхней шкалы прибора.
Пример вычислений: если переключатель диапазона установлен на положении «2-5» и стрелка прибора на верхней шкале остановилась на значении 3,01, то измеряемая величина рН будет равна 2+3,01= 5,01. Теперь оценим полученный результат с помощью таблицы 30. Реакция среды – кислая.
Обсуждение результатов
Полученные данные по определению рН вносятся в сводную таблицу химического анализа почвы (табл. 22). Для более полной оценки вероятного отрицательного действия кислотности почв важно установить не только разные ее формы, но и соотношение между суммой обменных оснований S (см. п. 4.3) и всем количеством ионов водорода (и алюминия) в почвенном поглощающем комплексе (эта величина соответствует гидролитической кислотности – Нг). Эти показатели определяют расчетным путем.
Сумма S+Нr определяет величину обменной способности почвы, то есть это все обменные катионы, включая водород и алюминий. Эту величину обычно называют емкостью поглощения или емкостью катионного обмена почвы (ЕКО), которая выражается в мг-экв на 100 г почвы. Таким образом:
ЕКО = S+Hг
Отношение суммы обменных оснований к емкости катионного обмена, выраженное в процентах, называется степенью насыщенности почв основаниями (V, %):
V = [S:(S+Hг)]·100% = S:ЕКО ·100%
Пример вычисления. Предположим, что сумма обменных оснований, определенная по Каппену – Гильковицу, равна 3,8 мг-экв/100 г почвы, а величина гидролитической кислотности – 4,4 мг-экв/100 г почвы. Степень насыщенности почв основаниями будет равна:
V = [3,8:(3,8+4,4)]·100% = 3,8:8,2 ·100% = 46%
Степень насыщенности почв основаниями показывает, какую часть всей емкости поглощения занимают обменные основания. В почвах, не содержащих поглощенного водорода (каштановые, бурые, карбонатные черноземы, сероземы и др.), она равна 100%. В почве с гидролитической кислотностью степень насыщенности меньше 100%. Чем больше в почве поглощенного водорода, тем меньше насыщенность основаниями.
Степень насыщенности основаниями и рН – весьма важные характеристики почвы. Этими величинами пользуются при решении многих практических вопросов. Особенно большое значение придают им при обосновании таких мероприятий, как известкование и фосфоритование кислых почв. Например, по нуждаемости в извести в зависимости от степени насыщенности основаниями и рН кислые почвы делят на четыре группы (табл. 31):
Таблица 31.
Полёт (РН) — Википедия
Эту страницу предлагается переименовать. Пояснение причин и обсуждение — на странице Википедия:К переименованию/9 февраля 2017. Пожалуйста, основывайте свои аргументы на правилах именования статей. Не удаляйте шаблон до подведения итога обсуждения.Переименовать в предложенное название, снять этот шаблон. |
| РН 11А59 «Полёт» | |
|---|---|
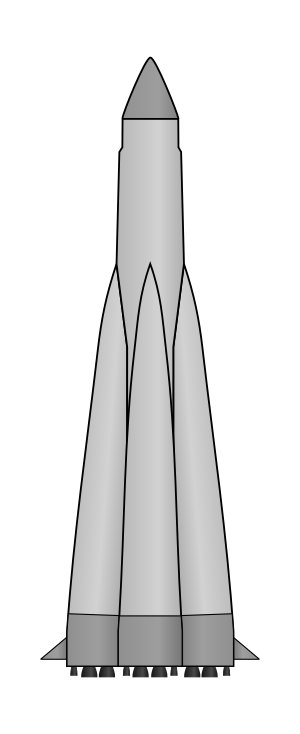 | |
| Общие сведения | |
| Страна |  СССР СССР |
| Семейство | Р-7А |
| Индекс | 11А59 |
| Назначение | ракета-носитель |
| Разработчик | ОКБ-1, ЦСКБ-Прогресс |
| Изготовитель | ЦСКБ-Прогресс |
| Основные характеристики | |
| Количество ступеней | 2 |
| Длина (с ГЧ) | 30 м[1] |
| Диаметр | 2,99 м[1] |
| Стартовая масса | 277 т[1] |
| Забрасываемый вес | 1,95 т |
| Вид топлива | Т1 + LOX |
| Полезная нагрузка | «И-2В» |
| История запусков | |
| Состояние | эксплуатация завершена |
| Места запуска | Байконур, площадка №31/6 |
| Число запусков | 2 |
| • успешных | 2 |
| Первый запуск | 1 ноября 1963 года[1] |
| Последний запуск | 12 апреля 1964 года[1] |
Полёт (индекс ГУКОС — 11А59) — советская двухступенчатая ракета-носитель лёгкого класса из семейства «Р-7». РН «Полёт» разрабатывалась и изготавливалась в куйбышевском филиале № 3 ОКБ-1 (ныне — ЦСКБ-Прогресс) под руководством Дмитрия Ильича Козлова и Сергея Павловича Королёва[2].
РН «Полёт» является модификацией ракеты-носителя «Р-7А» и была предназначена для вывода на круговую орбиту специальных маневрирующих ИСЗ — «Полёт-1» и «Полёт-2», разработки ОКБ-52 под руководством Владимира Николаевича Челомея
и была предназначена для вывода на круговую орбиту специальных маневрирующих ИСЗ — «Полёт-1» и «Полёт-2», разработки ОКБ-52 под руководством Владимира Николаевича Челомея [2][1].
[2][1].
Содержание
- 1 История создания
- 2 Особенности конструкции
- 3 Список всех запусков ракеты-носителя «Полёт»
- 4 См. также
- 5 Примечания
- 6 Литература
- 7 Ссылки
 | Этот раздел не завершён.Вы поможете проекту, исправив и дополнив его. |
Двухступенчатая РН 11А59 была разработана во исполнение Постановления ЦК КПСС и Совета Министров СССР № 258—110 от 16 марта 1961 года, филиалом № 3 ОКБ-1 (ныне — «ЦСКБ-Прогресс») на базе межконтинентальной баллистической ракеты (МБР) «Р-7А» (индекс ГУКОС — 8К74).
Испытательные работы по отработке процессов отделения объекта ИС (рабочее название аппаратов И-2В) от второй ступени ракеты-носителя 11А59 проводились на лётно-испытательной доводочной базе в Жуковском[3].
 | Этот раздел не завершён.Вы поможете проекту, исправив и дополнив его. |
Ракета-носитель 11А59 разрабатывалась на базе «Р-7А» путём создания принципиальной новой по конструкции и виду головной части. Принципиальным техническим нововведением был факт использования детонационного шнура вокруг корпуса для сброса головной части[3].
Список всех запусков ракеты-носителя «Полёт»[править | править код]
Ракетой-носителем 11А59 «Полёт» с космодрома Байконур в 1963 и 1964 гг. были запущены первые советские маневрирующие спутники «Полет-1» и «Полет-2», типа «И-2В», созданные в ОКБ-52 под руководством В. Н. Челомея.
| Список запусков ракеты-носителя «Полёт» [4] | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| № Запуска | Дата (UTC) | Полезная нагрузка | Тип КК | NSSDC ID | SCD | Стартовый комплекс | Результат | |||
| 1 | 1 ноября 1963 года |  Полёт-1 Полёт-1 | «И-1В» № 1 | 1963-043A | 00683 |  Байконур 31/6 Байконур 31/6 | Успех | |||
| 2 | 12 апреля 1964 года |  Полёт-2 Полёт-2 | «И-1В» № 2 | 1964-019A | 00784 |  Байконур 31/6 Байконур 31/6 | Успех | |||
- Союз (ракета-носитель)
- Р-7 (семейство ракет-носителей)
- ↑ 1 2 3 4 5 6 Encyclopedia Astronautica.
- ↑ 1 2 Самарские ступени «Семерки», 2011, с. 68.
- ↑ 1 2 Поляченко В. А. «На море и в космосе: Воспоминания», 2008, p. 88.
- ↑ Gunter’s space page.
- Кирилин А. Н., Ахметов Р. Н., Тюлевин С. В., Ткаченко С. И. Самарские ступени «Семерки». — Самара: Агни, 2011. — 256 с. — 2000 экз. — ISBN 978-5-89850-163-1.
- Кобелев В. Н., Милованов А. Г. Ракеты-носители: Учеб.пособие. — М.: ФГБОУ ВПО «МАТИ», 1993. — 165 с. — ISBN 5-230-21066-4.
- Поляченко В. А. На море и в космосе: Воспоминания. — СПб.: «МОРСАР АВ», 2008. — 192 с. + 32 с. вклейка с. — 1500 экз. — ISBN 5-93599-001-8. Архивная копия от 27 октября 2012 на Wayback Machine
- М. А. Первов. История развития отечественного ракетостроения. — М.: Издательский дом «Столичная энциклопедия», 2014. — 920 с. — 1200 экз. — ISBN 978-5-903989-22-5.
- Sputnik 11A59 (англ.). Encyclopedia Astronautica. Дата обращения 3 мая 2013. Архивировано 3 сентября 2013 года.
- R-7 Family (англ.). Gunter’s space page. Дата обращения 3 мая 2013. Архивировано 3 сентября 2013 года.
 | Это заготовка статьи о ракетной, ракетно-космической технике или космическом аппарате. Вы можете помочь проекту, дополнив её. |
Советская и российская ракетно-космическая техника | ||
|---|---|---|
| Эксплуатируемые РН |
|  |
| Разрабатываемые РН |
| |
| Выведенные из эксплуатации РН |
| |
| Разгонные блоки |
| |
| Многоразовые космические системы |
| |
Соляная кислота — Википедия
Соля́ная кислота́ (также хлороводоро́дная, хлористоводоро́дная кислота) — раствор хлороводорода (HCl{\displaystyle {\ce {HCl}}}) в воде, сильная одноосновная кислота. Бесцветная, прозрачная, едкая жидкость, «дымящаяся» на воздухе (техническая соляная кислота — желтоватого цвета из-за примесей железа, хлора и пр.). В концентрации около 0,5 % присутствует в желудке человека. Соли соляной кислоты называются хлоридами.
Впервые хлороводород получил алхимик Василий Валентин, нагрев гептагидрат сульфата железа с поваренной солью и назвав полученное вещество «духом соли» (лат. spiritus salis). Иоганн Глаубер в XVII в. получил соляную кислоту из поваренной соли и серной кислоты. В 1790 году британский химик Гемфри Дэви получил хлороводород из водорода и хлора, таким образом установив его состав. Возникновение промышленного производства соляной кислоты связано с технологией получения карбоната натрия: на первой стадии этого процесса поваренную соль вводили в реакцию с серной кислотой, в результате чего выделялся хлороводород. В 1863 году в Англии был принят закон «Alkali Act», согласно которому запрещалось выбрасывать этот хлороводород в воздух, а необходимо было пропускать его в воду. Это привело к развитию промышленного производства соляной кислоты. Дальнейшее развитие произошло благодаря промышленным методам получения гидроксида натрия и хлора путём электролиза растворов хлорида натрия[1].
Физические свойства соляной кислоты сильно зависят от концентрации растворённого хлороводорода:
| Конц. (вес), мас. % | Конц. (г/л), кг HCl/м³ | Плотность, кг/л | Молярность, M | Водородный показатель (pH) | Вязкость, мПа·с | Удельная теплоемкость, кДж/(кг·К) | Давление пара, Па | Т. кип., °C | Т. пл., °C |
| 10 % | 104,80 | 1,048 | 2,87 | −0,4578 | 1,16 | 3,47 | 0,527 | 103 | −18 |
| 20 % | 219,60 | 1,098 | 6,02 | −0,7796 | 1,37 | 2,99 | 27,3 | 108 | −59 |
| 30 % | 344,70 | 1,149 | 9,45 | −0,9754 | 1,70 | 2,60 | 1,410 | 90 | −52 |
| 32 % | 370,88 | 1,159 | 10,17 | −1,0073 | 1,80 | 2,55 | 3,130 | 84 | −43 |
| 34 % | 397,46 | 1,169 | 10,90 | −1,0374 | 1,90 | 2,50 | 6,733 | 71 | −36 |
| 36 % | 424,44 | 1,179 | 11,64 | −1,06595 | 1,99 | 2,46 | 14,100 | 61 | −30 |
| 38 % | 451,82 | 1,189 | 12,39 | −1,0931 | 2,10 | 2,43 | 28,000 | 48 | −26 |
При 20 °C, 1 атм (101 кПа)
При низкой температуре хлороводород с водой даёт кристаллогидраты составов HCl⋅h3O{\displaystyle {\ce {HCl.h3O}}} (т. пл. −15,4 °С), HCl⋅2h3O{\displaystyle {\ce {HCl.2h3O}}} (т. пл. −18 °С), HCl⋅3h3O{\displaystyle {\ce {HCl.3h3O}}} (т. пл. –25 °С), HCl⋅6h3O{\displaystyle {\ce {HCl.6h3O}}} (т. пл. −70 °С). При атмосферном давлении (101,3 кПа) хлороводород с водой образуют азеотропную смесь с т. кип. 108,6 °С и содержанием HCl{\displaystyle {\ce {HCl}}} 20,4 мас. %[2].
- 2Na+2HCl⟶2NaCl+h3↑{\displaystyle {\ce {2Na + 2HCl -> 2NaCl + h3 ^}}},
- Mg+2HCl⟶MgCl2+h3↑{\displaystyle {\ce {Mg + 2HCl -> MgCl2 + h3 ^}}},
- 2Al+6HCl⟶2AlCl3+3h3↑{\displaystyle {\ce {2Al + 6HCl -> 2AlCl3 + 3h3 ^}}}.
- Na2O+2HCl⟶2NaCl+h3O{\displaystyle {\ce {Na2O + 2HCl -> 2NaCl + h3O}}},
- MgO+2HCl⟶MgCl2+h3O{\displaystyle {\ce {MgO + 2HCl -> MgCl2 + h3O}}},
- Al2O3+6HCl⟶2AlCl3+3h3O{\displaystyle {\ce {Al2O3 + 6HCl -> 2AlCl3 + 3H_2O}}}.
- NaOH+HCl⟶NaCl+h3O{\displaystyle {\ce {NaOH + HCl -> NaCl + h3O}}},
- Ba(OH)2+2HCl⟶BaCl2+2h3O{\displaystyle {\ce {Ba(OH)2 + 2HCl -> BaCl2 + 2H_2O}}},
- Al(OH)3+3HCl⟶AlCl3+3h3O{\displaystyle {\ce {Al(OH)3 + 3HCl -> AlCl3 + 3H_2O}}}.
- Na2CO3+2HCl⟶2NaCl+h3O+CO2↑{\displaystyle {\ce {Na2CO3 + 2HCl -> 2NaCl + h3O + CO2 ^}}}.
- 2KMnO4+16HCl⟶5Cl2↑+2MnCl2+2KCl+8h3O{\displaystyle {\ce {2KMnO4 + 16HCl -> 5Cl_2 ^ + 2MnCl2 + 2KCl + 8h3O}}}.
 Соляная кислота (в стакане) взаимодействует с аммиаком
Соляная кислота (в стакане) взаимодействует с аммиаком- Nh4+HCl⟶Nh5Cl{\displaystyle {\ce {Nh4 + HCl -> Nh5Cl}}}.
- HCl+AgNO3⟶AgCl↓+HNO3{\displaystyle {\ce {HCl + AgNO3 -> AgCl v + HNO3}}}.
Соляную кислоту получают растворением газообразного хлороводорода в воде. Хлороводород получают сжиганием водорода в хлоре, полученная таким способом кислота называется синтетической. Также соляную кислоту получают из абгазов — побочных газов, образующихся при различных процессах, например, при хлорировании углеводородов. Хлороводород, содержащийся в этих газах, называется абгазным, а полученная таким образом кислота — абгазной. В последние десятилетия доля абгазной соляной кислоты в объёме производства постепенно увеличивается, вытесняя кислоту, полученную сжиганием водорода в хлоре. Но полученная методом сжигания водорода в хлоре соляная кислота содержит меньше примесей и применяется при необходимости высокой чистоты.
В лабораторных условиях используется разработанный ещё алхимиками способ, заключающийся в действии концентрированной серной кислоты на поваренную соль:
- NaCl +h3SO4→150 ∘CNaHSO4 +HCl{\displaystyle {\ce {NaCl\ +h3SO4->[150~^{\circ }{\text{C}}]NaHSO4\ +HCl}}}.
При температуре выше 550 °C и избытке поваренной соли возможно взаимодействие:
- 2NaCl +h3SO4→550 ∘CNa2SO4 +2HCl{\displaystyle {\ce {2NaCl\ +h3SO4->[550~^{\circ }{\text{C}}]Na2SO4\ +2HCl}}}.
Возможно получение путём гидролиза хлоридов магния, алюминия (нагревается гидратированная соль):
- MgCl2⋅6h3O→t, ∘CMgO +2HCl +5h3O{\displaystyle {\ce {MgCl2.6h3O->[t,~^{\circ }{\text{C}}]MgO\ +2HCl\ +5h3O}}},
- AlCl3⋅6h3O→t, ∘CAl(OH)3 +3HCl +3h3O{\displaystyle {\ce {AlCl3.6h3O->[t,~^{\circ }{\text{C}}]Al(OH)3\ +3HCl\ +3h3O}}}.
Эти реакции могут идти не до конца с образованием основных хлоридов (оксихлоридов) переменного состава, например:
- 2MgCl2+h3O⟶Mg2OCl2+2HCl{\displaystyle {\ce {2MgCl2 + h3O -> Mg2OCl2 + 2HCl}}}[5]
Хлороводород хорошо растворим в воде. Так, при 0 °C 1 объём воды может поглотить 507 объёмов HCl{\displaystyle {\ce {HCl}}}, что соответствует концентрации кислоты 45 %. Однако при комнатной температуре растворимость HCl{\displaystyle {\ce {HCl}}} ниже, поэтому на практике обычно используют 36-процентную соляную кислоту.
Промышленность[править | править код]
Медицина[править | править код]
- Естественная составная часть желудочного сока человека. В концентрации 0,3—0,5 %, обычно в смеси с ферментом пепсином, назначается внутрь при недостаточной кислотности.
 Высококонцентрированная соляная кислота — едкое вещество, при попадании на кожу вызывает сильные химические ожоги. Особенно опасно попадание в глаза. Для нейтрализации ожогов применяют раствор слабого основания, или соли слабой кислоты, обычно питьевой соды.
Высококонцентрированная соляная кислота — едкое вещество, при попадании на кожу вызывает сильные химические ожоги. Особенно опасно попадание в глаза. Для нейтрализации ожогов применяют раствор слабого основания, или соли слабой кислоты, обычно питьевой соды.
При открывании сосудов с концентрированной соляной кислотой пары хлороводорода, притягивая влагу воздуха, образуют туман, раздражающий глаза и дыхательные пути человека.
Реагируя с сильными окислителями (хлорной известью, диоксидом марганца, перманганатом калия) образует токсичный газообразный хлор.
В РФ оборот соляной кислоты концентрации 15 % и более — ограничен[6].
- Austin S., Glowacki A. Hydrochloric Acid (англ.) // Ullmann’s Encyclopedia of Industrial Chemistry. — Wiley, 2000. — DOI:10.1002/14356007.a13_283.
