причины, симптомы, цена лечения кардиосклероза в Москве
Одной из опасных форм проявления ишемической болезни сердца является кардиосклероз. Самостоятельно диагностировать его довольно сложно. Часто его можно определить, только сделав электрокардиограмму.
Кардиосклероз выражается в патологии сердечной мышцы (миокарда), в которой разрастается соединительная ткань. Она образует рубцы разной величины, замещающие собой отмирающие волокна миокарда, и вызывает деформацию сердечного клапана. Размер сердечной мышцы увеличивается, что постепенно приводит к гипертрофии сердца и уменьшению его сократительной способности.
Виды кардиосклероза
По морфологическому принципу различают следующие типы этого заболевания:
- очаговый;
- диффузный.
Диффузный тип характерен распространением соединительной ткани на весь миокард, а очаговый на отдельные участки мышцы, и он, чаще всего, является осложнением после перенесенного инфаркта или миокардита.
По этиологии или причинам, эта патология является следствием ряда заболеваний. Различают следующие виды:
- постинфарктный;
- атеросклеротический;
- миокардитический.
Постинфарктная форма обычно является результатом перенесенного инфаркта. На месте некротических повреждений образуются рубцы, что снижает сократительную способность сердечной мышцы.
При повторных инфарктах количество рубцовой ткани возрастает и возникает угроза хронической аневризмы (выпячивание стенки мышцы, ослабленной и растянутой соединительной тканью). Разрыв аневризмы приводит к летальному исходу. Поэтому пациенты должны быть под постоянным наблюдением врача в больнице, им также рекомендуется покой и психологический комфорт.
Атеросклеротическая форма, как правило, это результат атеросклероза крупных сосудов, а также ишемической болезни сердца. Процесс развития болезни длительный и возникает в результате гипоксии клеток, которые не получают необходимого количества кислорода из-за больных сосудов.
Миокардитическая форма развивается из-за воспаления в миокарде. Этим типом патологии чаще страдают молодые пациенты, имеющие в своем анамнезе хронические инфекции, аллергии. В этом случае поражается правый желудочек сердца, он увеличивается в объеме, кровоснабжение становится недостаточным.
Часто болезнь развивается бессимптомно. Постепенно, в результате склеротирования сосудов, начинаются нарушения сердечного ритма, может развиваться сердечная недостаточность.
Основными симптомами постинфарктной и атеросклеротической форм являются:
- усиленное сердцебиение;
- затрудненное дыхание;
- отеки;
- нарушения ритма сердцебиения.
Заболевание часто сопровождается артериальной гипертензией. Стадии обострения могут чередоваться с довольно длительными периодами ремиссии.
Не следует откладывать поход к врачу. Опытный кардиолог поставит правильный диагноз и распишет лечение с учетом тяжести состояния.Какие бы патологии ни вызывали кардиосклероз, (увеличение миокарда, наличие воспалительных процессов, сужение сосудов), его глубинные причины кроются в:
- отсутствии достаточных физических нагрузок;
- переедании;
- злоупотреблении алкоголем;
- стрессах;
- слишком больших физических нагрузках;
- курении.
Кардиосклероз — диагностика и лечение в медицинском центре «Андреевские больницы
Кардиосклероз – это заболевание сердца, при котором мышечная ткань замещается соединительной тканью. Из-за того, что соединительная ткань ригидна и не способна к сокращению снижается общая сократительная способность миокарда и все это приводит к развитию сердечной недостаточности.
Кардиосклероз делится на атеросклеротический, постинфарктный и постмиокардитический, последний из которых может быть очаговым или диффузным.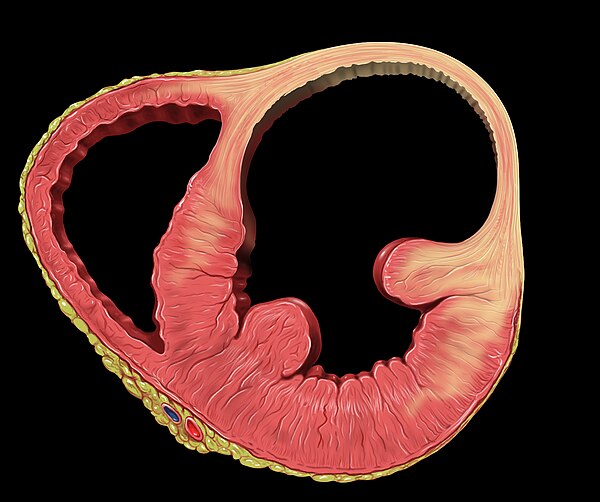
Причины кардиосклероза
Чаще всего кардиосклероз является следствием либо осложнением таких заболеваний, как миокардит, миокардиодистрофия, атеросклероз сосудов сердца, ревматизм.
Постинфарктный кардиосклероз образуется после формирования рубца на месте некроза ткани у больного, перенесшего инфаркт миокарда. Частой локализацией этого вида склероза является левый желудочек.
Кардиосклероз не зависит от возраста больного и возможен как у пожилых людей, так и у молодых.
Симптомы кардиосклероза
Если склеротический очаг затрагивает проводящую систему сердца, то он проявляется различного вида аритмиями и нарушениями проводимости. Больной ощущает перебои в сердце, учащение или, наоборот, урежение пульса, одышку, слабость.
Диффузный кардиосклероз более опасен в своем проявлении. Он приводит к недостаточности миокарда, застойным явлениям в легких, печени, увеличению размеров сердца. При декомпенсации появляется одышка даже в покое, отеки лодыжек, икр, кашель, учащенное сердцебиение. При обследовании обнаруживается жидкость в брюшной и плевральной полостях, а также в перикарде.
При декомпенсации появляется одышка даже в покое, отеки лодыжек, икр, кашель, учащенное сердцебиение. При обследовании обнаруживается жидкость в брюшной и плевральной полостях, а также в перикарде.
Диагностика кардиосклероза
Для постановки предварительного диагноза собирается анамнез: уточняется наличие заболеваний, которые приводят к возникновению склероза сердца.
Осмотр больного проводится врачом-кардиологом, записываются его жалобы.
Для подтверждения диагноза назначаются:
- Электрокардиограмма (ЭКГ), с помощью которой выявляются нарушения ритма, проводимости и так далее.
- Эхокардиография (ЭХОКГ), помогающая уточнить степень сократительной способности миокарда, определить размеры сердца, исследовать клапанный аппарат.
-
Магнитно-резонансная томография сердца (МРТ) (назначается в случае необходимости). Этим исследованием делают послойные «срезы» всего сердца для уточнения и детального рассмотрения очага поражения.

- Ангиография сердца. Позволяет определить утолщение стенок сосудов и артерий, сужение их просветов или полную закупорку.
Лечение кардиосклероза
Консервативное лечение сводится к симптоматической терапии, направленной на устранение симптомов заболевания и ликвидацию сердечной недостаточности. Назначаются препараты, улучшающие метаболизм в сердце, нормализующие ритм и проводимость, снимающие одышку, отеки.
Больному рекомендуется ограничить физические нагрузки.
Аневризма сердца(истончение стенки ЛЖ после перенесенного инфаркта миокарда) лечится только хирургическим путем, при необратимых нарушениях ритма обязательна операция по вживлению электрокардиостимулятора.
Профилактика кардиосклероза
Одним из основополагающих факторов является полноценное и правильное питание. Важно избегать стрессовых ситуаций и переохлаждений.
Профилактика предусматривает раннюю диагностику и качественное лечение атеросклероза, миокардитов, коронарной недостаточности, ишемии сосудов сердца и других сердечных патологий.
симптомы, виды и профилактика заболевания
Во многих санаториях Кавминвод и Беларуси проводится профилактика сердечно-сосудистых заболеваний, в которую входит назначение специальной диеты, щадящий режим и дозированные нагрузки. На протяжении всего курса пациент находится под наблюдением лечащего врача, что является важным фактором, улучшающим прогноз при заболеваниях сердца.
Что такое кардиосклероз
Кардиосклероз – это патологическое состояние, при котором клетки сердечной мышцы заменяются рубцовой тканью. Из-за того, что рубцовая ткань не участвует в сокращении сердца, миокард начинает работать с возрастающей нагрузкой. Сердечная мышца постепенно увеличивается в размерах, развивается гипертрофия левого желудочка, а потом и других отделов сердца. Со временем резервы гипертрофированного миокарда исчерпываются, это приводит к уменьшению сократительной способности сердца (оно не может нормально перекачивать кровь) и развитию недостаточности кровообращения, то есть сердечной недостаточности.
Симптоматика кардиосклероза
Клинические проявления кардиосклероза зависят от степени распространения соединительной ткани по отношению к здоровой ткани миокарда. Чем больше рубцов, тем более выражена сердечная недостаточность и ее внешние проявления: одышка, отеки, нарушения сердечного ритма (мерцательная аритмия и экстрасистолия).
Кардиосклеротические изменения хорошо проявляются на электрокардиографии, а также на эхокардиографии и результатах радионуклидного исследования миокарда.
Причины развития кардиосклероза
Кардиосклероз развивается вследствие инфаркта миокарда, атеросклероза, миокардита и различных миокардиодистрофий. Эти заболевания, в свою очередь, возникают чаще всего из-за неправильного образа жизни:
- переедание;
- курение;
- употребление алкоголя;
- гиподинамия (малоподвижный образ жизни) или, наоборот, чрезмерные физические нагрузки;
- постоянные эмоциональные стрессы.
Виды кардиосклероза
Существует три разновидности кардиосклероза:
- атеросклеротический;
- постинфарктный кардиосклероз;
- постмиокардитический кардиосклероз.

Атеросклеротическая форма развивается при ишемической болезни сердца. Процесс этот долгий, может развиваться годами. Мышечная ткань сердца заменяется соединительной (рубцовой) постепенно, вследствие постоянного кислородного голодания», т.е. плохого кровоснабжения миокарда.
Длительное время больной может не ощущать никаких симптомов из-за медленного развития болезни. Через какое-то время развивается сердечная недостаточность, которая проявляется плохой переносимостью физических нагрузок, одышкой, отеками и учащенным сердцебиением, аритмией.
Постинфарктный кардиосклероз развивается на месте некроза, образовавшегося после перенесенного острого инфаркта миокарда. Повторные инфаркты образуют рубцы в разных частях сердца, что значительно снижает сократительную способность миокарда. Распространенные инфаркты, затрагивающие все слои миокарда,могут привести к развитию аневризмы.
Аневризма – это выпячивание на сердечной мышце, своеобразный «мешок», который образуется при слабой мышечной стенке под действием высокого давления. Разрыв аневризмы приводит к смертельному исходу.
Разрыв аневризмы приводит к смертельному исходу.
Вот почему в период реабилитации после инфаркта миокарда, особенно обширного, необходим покой и отсутствие стрессов, чтобы процесс рубцевания прошел правильно, без образования аневризм.
Миокардитический кардиосклероз образуется вследствие различных заболеваний, вызывающих воспалительный ответ в миокарде, таких, как хронический тонзиллит, гнойные ангины, гайморит, кариес и т.д., а также воспалительных заболеваний миокарда (ревматизм, миокардиты). Может наблюдаться не только у взрослых людей, но также у детей и подростков.
По участкам поражения кардиосклероз подразделяется на:
- диффузный;
- очаговый.
При диффузном кардиосклерозе наблюдается равномерное распределение соединительной ткани по всей поверхности сердечной мышцы. Очаговый кардиосклероз характеризуется участками рубцовой ткани, образовавшейся, чаще всего, после инфаркта миокарда или миокардита.
Профилактика кардиосклероза
Для профилактики кардиосклероза, а также для прохождения курса реабилитации после перенесенного инфаркта миокарда, санаторно-курортные учреждения предлагают специальные оздоровительные программы, направленные на постепенное восстановление функций сердечной мышцы.
Важно помнить, что в санатории принимаются пациенты с неострой стадией заболевания, с заболеванием на стадии затухания или ремиссии.
При кардиосклерозе назначается щадящий режим с дозированными нагрузками, для того, чтобы рубцевание происходило правильно, без образования аневризм; а также специальная диета, в которой сведено к минимуму количество животных жиров, снижено количество поваренной соли и дозировано суточное потребление жидкости.
Процедуры, применяемые при кардиосклерозе:
Санатории, занимающиеся лечением заболеваний сердечно-сосудистой системы:
Профиль автора:
Заболевания кардиологического профиля
|
|
от операции C.
 Beck до операции V. Dor в модификации Л.А. Бокерии Главная
Beck до операции V. Dor в модификации Л.А. Бокерии ГлавнаяВидео Развитие концепции хирургического лечения постинфарктной аневризмы левого желудочка и межжелудочковой перегородки: от операции C. Beck до операции V. Dor в модификации Л.А. Бокерии
rassh/2014year_18sessia/h3/18/Lebedev.mp4
Лебедев Б. Ю., Иванов И. В.
НЦССХ им. А.Н. Бакулева;
Первые описания ПАЛЖС относятся к 18 веку (Hunter J., Galeati D.). В 1914 г. M. Sternberg выявил связь между аневризмами сердца и склерозом коронарных артерий. А первую попытку хирургического лечения ПАЛЖС предпринял в1944 г. C.S. Beck. К сожалению, она не увенчалась успехом, больной погиб. В 1954 г. Ф.Г. Углов предложил инвагинировать аневризматический мешок. В 1955 г. W. Likoff и Ch.Ph. Bailey выполнили первую успешную операцию при ПАЛЖС. Они резецировали аневризму с использованием специального зажима. В СССР аналогичную операцию предложил Б.В. Петровский. Он же разработал операцию пластики аневризмы лоскутом из диафрагмы. Все эти операции проводили без искусственного кровообращения (ИК), что не давало возможности полноценной коррекции геометрии ЛЖ и пластики межжелудочковой перегородки (МЖП). Это стало основной причиной того, что операции по поводу ПАЛЖС без ИК перестали интересовать хирургов и ушли в историю. В 1958 г. D.A. Cooly с коллегами успешно провели линейную пластику аневризмы левого желудочка с использованием ИК. Именно эта операция послужила основой для дальнейшего совершенствования хирургической техники лечения ПАЛЖС. В1980 г. D.A. Cooly предложил дополнять аневризмэктомию пластикой МЖП тефлоновой тканью для устранения парадоксальной пульсации перегородки. Для устранения дисфункции МЖП и, одновременно, желудочковых аритмий V. Dor в 1984 г. предложил ряд методик. Операция Дор I предусматривала устранение аритмогенных зон путем рассечением эндокарда на границе с аневризмой и прошиванием разреза нитью которая одновременно фиксировала и заплату, закрывавшею аневризму. Операция Дор II проводится аналогично, но без заплаты.
Все эти операции проводили без искусственного кровообращения (ИК), что не давало возможности полноценной коррекции геометрии ЛЖ и пластики межжелудочковой перегородки (МЖП). Это стало основной причиной того, что операции по поводу ПАЛЖС без ИК перестали интересовать хирургов и ушли в историю. В 1958 г. D.A. Cooly с коллегами успешно провели линейную пластику аневризмы левого желудочка с использованием ИК. Именно эта операция послужила основой для дальнейшего совершенствования хирургической техники лечения ПАЛЖС. В1980 г. D.A. Cooly предложил дополнять аневризмэктомию пластикой МЖП тефлоновой тканью для устранения парадоксальной пульсации перегородки. Для устранения дисфункции МЖП и, одновременно, желудочковых аритмий V. Dor в 1984 г. предложил ряд методик. Операция Дор I предусматривала устранение аритмогенных зон путем рассечением эндокарда на границе с аневризмой и прошиванием разреза нитью которая одновременно фиксировала и заплату, закрывавшею аневризму. Операция Дор II проводится аналогично, но без заплаты. Модификация Дор I предусматривает использования в качестве заплаты материал из фторлон-лавсана без рассечения эндокарда на границе рубца и здорового миокарда, а модификация Дор II подразумевает использования в качестве заплаты лоскута из фиброзного эндокарда. Нередко эти операции дополнялись реваскуляризацией миокарда. В 1990-х гг. процедуры Дора дополнили российские хирурги. В 1993 г. Л.А. Бокерия предложил комбинированную пластику ПАЛЖС, а в1994 г. Л.А Бокерия и Г.Г. Федоров разработали тактику хирургического лечения аневризм в зависимости от их локализаций и использование при переднеперегородочной и верхушечной аневризмах операцию Дора в модификации Бокерия. Таким образом, эволюция операций при постинфарктных аневризмах ЛЖС следовала по пути от закрытых методик к открытым, от пластики аневризм биологическими тканями к пластике синтетическими, от пластики без учета анатомии проводящей системы сердца к способам профилактики желудочковых аритмий, от операции Бека к операции Дора-Бокерия.
Модификация Дор I предусматривает использования в качестве заплаты материал из фторлон-лавсана без рассечения эндокарда на границе рубца и здорового миокарда, а модификация Дор II подразумевает использования в качестве заплаты лоскута из фиброзного эндокарда. Нередко эти операции дополнялись реваскуляризацией миокарда. В 1990-х гг. процедуры Дора дополнили российские хирурги. В 1993 г. Л.А. Бокерия предложил комбинированную пластику ПАЛЖС, а в1994 г. Л.А Бокерия и Г.Г. Федоров разработали тактику хирургического лечения аневризм в зависимости от их локализаций и использование при переднеперегородочной и верхушечной аневризмах операцию Дора в модификации Бокерия. Таким образом, эволюция операций при постинфарктных аневризмах ЛЖС следовала по пути от закрытых методик к открытым, от пластики аневризм биологическими тканями к пластике синтетическими, от пластики без учета анатомии проводящей системы сердца к способам профилактики желудочковых аритмий, от операции Бека к операции Дора-Бокерия.
КОМОРБИДНАЯ ПАТОЛОГИЯ ПРИ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА СРЕДИ ПАЦИЕНТОВ КАРДИОХИРУРГИЧЕСКИХ ЦЕНТРОВ ЧЕЛЯБИНСКА И КЕМЕРОВО | Эфрос
1. Cervera R., Bakaeen F., Cornwell L., Wang X.L., Coselli J.S., Surg. 2012;93(6):1950-1954.D0I:10.1016/j.athoracsur.2012.02.071 LeMaire S.A. et al. Impact of functional status on survival after
2. Weintraub W.S., Grau-Sepulveda M.V., Weiss J.M., O’Brien coronary artery bypass grafting in a veteran population. Ann. Thorac. S.M., Peterson E.D., Kolm P. et al. Comparative effectiveness of revascularization strategies.N Engl. J. 2012;366 (16): 1467-1476. D0I:10.1056/NEJMoa1110717
3. Sen B.B., Niemann B., Roth P., Aser R., Schonburg M., Boning A. Shortand long-term outcomes in octogenarians after coronary artery bypass surgery. Eur. J. Cardiothorac. Surg. 2012; 42 (5):102-107. D0I:10.1093/ejcts/ezs410
Eur. J. Cardiothorac. Surg. 2012; 42 (5):102-107. D0I:10.1093/ejcts/ezs410
4. Saxena A., Dinh D., Smith J.A., Shardey G., Reid C.M., Newcomb A.E. Sex differences in outcomes following isolated coronary artery bypass graft surgery in Australian patients: analysis of the Australasian Society of Cardiac and Thoracic Surgeons cardiac surgery database. Eur. J. Cardiothorac. Surg. 2012; 41(4):755-762. DOI: https://doi.org/10.1093/ejcts/ezr039
5. Перхов В.И., Киреев А.Б., Ахмедов Ш.Д. История, реальность и перспективы обеспечения населения РФ бесплатной высокотехнологической медицинской помощью. Сибирский медицинский журнал.2009; 24(1): 63-66. [Perkhov V.I., Kireev A.B., Akhmedov Sh.D. History, reality and perspectives of rendering free of charge hightechnology medical aid for the population of russian federation. The Siberian medical journal. 2009. 24(1): 63-66. (In Russ)].
2009. 24(1): 63-66. (In Russ)].
6. Nardi P., Pellegrino A., Scafuri A., Binaco I., Polisca P., Iorio F. etal. Long-term outcomes after surgical ventricular restoration and coronary artery bypass grafting in patients with postinfarction left ventricular anterior aneurysm. J. Cardiovasc. Med. (Hagerstown). 2010; 11 (2): 96-102.D0I:10.2459/JCM.0b013e32832f9fc1
7. Solodky A., Behar S., Boyko V., Battler A., Hasdai D. The outcome of coronary artery bypass grafting surgery among patients hospitalized with acute coronary syndrome: the Euro Heart Survey of acute coronary syndrome experience. Cardiology. 2005; 103: 44-47.
8. Fleisher LA. Preoperative assessment of the patient with cardiac disease undergoing noncardiac surgery. Anesthesiol. Clin. 2016; 34 (1):59-70. D0I: 10.1016/j.anclin.2015.10.006
D0I: 10.1016/j.anclin.2015.10.006
9. Самородская И.В., Никифорова M.A. Терминология и методы оценки влияния коморбидности на прогноз и исходы лечения. Бюллетень НЦССХ им. АН. Бакулева РАМН. 2013; 14 (4): 18-26. [Samorodskaya I.V., Nikiforova M.A. Terminology and methods of assessment of influence of comorbidity on prognosis and outcomes of treatment. Byulleten’ A.N.Bakoulev Scientific Center for Cardiovascular Surgery of the Russian Academy of Medical Sciences.2013; 14 (4): 18-26. (InRuss)].
10. Бокерия Л.А., Ступаков И.Н., Самородская И.В., Болотова Е.В. Распространенность сопутствующих заболеваний у больных ишемической болезнью сердца, нуждающихся в кардиохирургическом лечении. Бюллетень НЦССХ им. А.Н. Бакулева РАМН. 2009; 10 (3): 46. [Bokeriya L.A., Stupakov I.N., Samorodskaya I.V., Bolotova E.V. The prevalence of comorbidities in patients with coronary heart disease who require cardiac surgery treatment. Byulleten’ A.N. Bakoulev Scientific Center for Cardiovascular Surgery of the Russian Academy of Medical Sciences.2009; 10 (3): 46. (InRuss)].
Byulleten’ A.N. Bakoulev Scientific Center for Cardiovascular Surgery of the Russian Academy of Medical Sciences.2009; 10 (3): 46. (InRuss)].
11. Ахмедов Ш.Д., Мотрева А.П., Роговская Ю.В., Кошельская О.А., Шипулин В.М. Сравнительная клинико-морфологическая оценка результатов хирургического лечения ИБС у больных сахарным диабетом 2 типа и у пациентов без нарушений углеводного обмена. Сибирский медицинский журнал. 2007; 22(3): 3438. [Akhmedov Sh.D., Motreva A.P., RogovskayaYu.V., Koshel’skaya O.A., Shipulin V.M. Comparative clinical-morphological estimation of results of surgical treatment IHD in patients with diabetes of type 2 and in patients without infringements of a carbohydrate. The Siberian medical journal. 2007; 22(3): 34-38. (In Russ)].
12. Тарасов P.C., Иванов C.B., Казанцев A.H., Бурков H.H., Ануфриев А.И., Зинец М.Г. и др.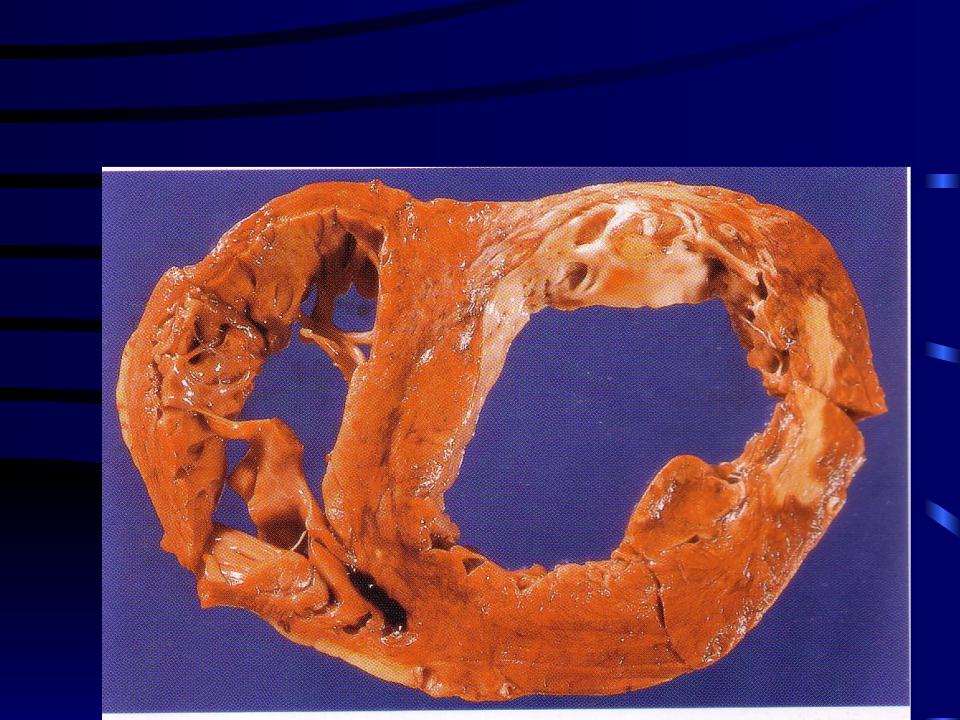 Госпитальные результаты различных стратегий хирургического лечения пациентов с сочетанным поражением коронарного русла и внутренних сонных артерий. Комплексные проблемы сердечно-сосудистых заболеваний. 2016; 4:15-24. D0I:10.17802/2306-1278-2016-4-15-24. [Tarasov R.S., Ivanov S.V., Kazantsev A.N., Burkov N.N., Anufriev A.I., Zinets M.G. et al. Hospital results of the different strategies of surgical treatment of patients with concomitant coronary disease and internal carotid arteries stenoses. Complex Issues of Cardiovascular Diseases. 2016; 4:15-24. D0I:10.17802/2306-1278-2016-4-15-24(In Russ)].
Госпитальные результаты различных стратегий хирургического лечения пациентов с сочетанным поражением коронарного русла и внутренних сонных артерий. Комплексные проблемы сердечно-сосудистых заболеваний. 2016; 4:15-24. D0I:10.17802/2306-1278-2016-4-15-24. [Tarasov R.S., Ivanov S.V., Kazantsev A.N., Burkov N.N., Anufriev A.I., Zinets M.G. et al. Hospital results of the different strategies of surgical treatment of patients with concomitant coronary disease and internal carotid arteries stenoses. Complex Issues of Cardiovascular Diseases. 2016; 4:15-24. D0I:10.17802/2306-1278-2016-4-15-24(In Russ)].
13. Никитин Ю.П., Воевода М.И., Симонова Г.И. Сахарный диабет и метаболический синдром в Сибири и на Дальнем Востоке. Вестник РАМН. 2012; 1:66-74. [Nikitin Yu.P., Voevoda M.I., Simonova G.I. Sakharnyy diabet i metabolicheskiy sindrom v Sibiri i na Dal’nem Vostoke. Vestnik RAMN. 2012; 1:66-74.(In Russ)].
14. Барбараш О.Л., Семенов В.Ю., Самородская И.В., Евсеева M.B., Рожков Н.А., Сумин А.Н. и др. Коморбидная патология у больных ишемической болезнью сердца при коронарном шунтировании: опыт двух кардиохирургических центров. Российский кардиологический журнал. 2017; (3):6-13. DOI: 10.15829/15604071-2017-3-6-13.[Barbarash0.L., Semenov V.Yu.,Samorodskaya I. V., Evseeva M.V., Rozhkov N.A., Sumin A.N. Comorbid conditions in patients with coronary artery disease undergoing coronary artery bypass grafting: dual center experience. RussJCardiol. 2017; (3):6-13. DOI: 10.15829/1560-4071-2017-3-6-13 (InRuss)].
Барбараш О.Л., Семенов В.Ю., Самородская И.В., Евсеева M.B., Рожков Н.А., Сумин А.Н. и др. Коморбидная патология у больных ишемической болезнью сердца при коронарном шунтировании: опыт двух кардиохирургических центров. Российский кардиологический журнал. 2017; (3):6-13. DOI: 10.15829/15604071-2017-3-6-13.[Barbarash0.L., Semenov V.Yu.,Samorodskaya I. V., Evseeva M.V., Rozhkov N.A., Sumin A.N. Comorbid conditions in patients with coronary artery disease undergoing coronary artery bypass grafting: dual center experience. RussJCardiol. 2017; (3):6-13. DOI: 10.15829/1560-4071-2017-3-6-13 (InRuss)].
15. Рекомендации по лечению стабильной ишемической болезни сердца. ESC 2013. Российский кардиологический журнал. 2014; 7(111): 7-79. [Recommendations on stable coronary artery disease treatment. ESC 2013. Russ J Cardiol. 2014; 7(111):7-79. (In Russ)].
16. DAgostino R.S., Jacobs J.P., Badhwar V., Paone G., Rankin J.S., Hanetal J.M. The Society of Thoracic Surgeons Adult Cardiac Surgery Database: 2016 Update on Outcomes and Quality. Ann Thorac Surg. 2016; 101: 24-32.DOI:10.1016/j.athoracsur.2015.11.032
DAgostino R.S., Jacobs J.P., Badhwar V., Paone G., Rankin J.S., Hanetal J.M. The Society of Thoracic Surgeons Adult Cardiac Surgery Database: 2016 Update on Outcomes and Quality. Ann Thorac Surg. 2016; 101: 24-32.DOI:10.1016/j.athoracsur.2015.11.032
17. Кочурова Л.В., Елисеев B.A. Множественность заболеваний у детей, проживающих в экологически неблагоприятных регионах Сибири. Экология человека. 2011; 11: 19-24. [Kochurova L.V., Eliseev V.A. Mnozhestvennost’ zabolevaniyudetey, prozhivayushchikh v ekologicheski neblagopriyatnykh regionakh Sibiri. Ekologiya cheloveka. 2011; 11: 19-24. (InRuss)].
18. Губанова В.Г., Беляева Ю.Н., Шеметова Г.Н. Коморбидный пациент: этапы формирования, факторы риска и тактика ведения. Современные проблемы науки и образования. 2015; 6:1-7. [ Gubanova V.G., BelyaevaYu.N., Shemetova G.N. Komorbidnyy patsient: etapy formirovaniya, factory riska i taktikavedeniya. Sovremennye problem nauki obrazovaniya. 2015; 6:1-7. (InRuss)].
Sovremennye problem nauki obrazovaniya. 2015; 6:1-7. (InRuss)].
19. Алекян Б.Г., Бузиашвили Ю.И., Голухова E.3., Бокерия О.Л., Никитина Т.Г., Петросян КВ и др. Непосредственные результаты чрескожных коронарных вмешательств у пациентов старше 80 лет с хронической ишемической болезнью сердца. Грудная и сердечно-сосудистая хирургия. 2014; 6:12-16. [Alekyan B. G., Buziashvili Yu.I., Golukhova E.Z., Bokeriya O.L., Nikitina T.G., Petrosyan K.V et al. Immediate results of percutaneous coronary interventions in patients older than 80 years with chronic ischemic heart disease. Thoracic and Cardiovascular Surgery. 2014; 6:12-16. (In Russ)].
EXPERIENCE OF THE PROCEDURE ADVANCED REAL-TIME AND SHEAR WAVES SPLEEN ELASTOGRAPHYIN MULTIDISCIPLINARY HOSPITAL | Kovalev
64 patients were examined to improve technique of shear wave and real-time elastography. There were 11 patients with hematologic diseases, 19 — with infectious diseases, 24 patients with gastroenterological pathology and 10 patients with cardiologic diseases, with primary results of spleen stiffness indicators. According to the results of the studies have been made conclusions about improvement the reproducibility and efficiency of research using advanced techniques. The sensitivity amounted to 93,1%, specificity — to 89,3% and precision — 91,3%, while by using the routine method these indices amounted to 68,2%, 91,4% and 79,4% accordingly.
There were 11 patients with hematologic diseases, 19 — with infectious diseases, 24 patients with gastroenterological pathology and 10 patients with cardiologic diseases, with primary results of spleen stiffness indicators. According to the results of the studies have been made conclusions about improvement the reproducibility and efficiency of research using advanced techniques. The sensitivity amounted to 93,1%, specificity — to 89,3% and precision — 91,3%, while by using the routine method these indices amounted to 68,2%, 91,4% and 79,4% accordingly.
Введение В последние годы активно разрабатывается новое направление в ультразвуковой диагно- стике — соноэластография (СЭГ) [1, 2, 4 — 7, 10, 11, 16]. В основе этой методики визуализации тканей лежит различие эластических свойств (упругости, жесткости и растяжимости) нор- мальных и патологически измененных тканей, визуальная оценка их деформации, реализован- ная в современных ультразвуковых диагности- ческих приборах [1, 2, 4 — 7, 10]. Благодаря методике компрессионной эластографии (КЭ) и эла- стографии сдвиговых волн (ЭСВ) используется технология, позволяющая оценивать эластич- ность тканей дистанционно. Причем, при прове- дении эластографии сдвиговых волн результаты исследования можно выразить и в цифровых показателях (КПа), в то время как при прове- дении компрессионной эластографии — в услов- ных единицах, отражающих разницу жесткости измеряемых участков очага/органа [1, 5 — 7, 10, 14, 17 — 20]. Цель исследования: оценить клинико- диагностические возможности усовершенство- ванной методики компрессионной эластографии и эластографии сдвиговых волн при исследова- нии селезенки в многопрофильном стационаре. Материалы и методы исследования За 2014 — 2015 годы на базе ОГБУЗ «Кли- ническая больница № 1» сотрудниками Про- блемной научно-исследовательской лаборато- рии ГБОУ ВПО Смоленского Государственного Медицинского Университета было обследовано 64 пациента, распределение больных по полу и возрасту представлены в таблице (табл.
Благодаря методике компрессионной эластографии (КЭ) и эла- стографии сдвиговых волн (ЭСВ) используется технология, позволяющая оценивать эластич- ность тканей дистанционно. Причем, при прове- дении эластографии сдвиговых волн результаты исследования можно выразить и в цифровых показателях (КПа), в то время как при прове- дении компрессионной эластографии — в услов- ных единицах, отражающих разницу жесткости измеряемых участков очага/органа [1, 5 — 7, 10, 14, 17 — 20]. Цель исследования: оценить клинико- диагностические возможности усовершенство- ванной методики компрессионной эластографии и эластографии сдвиговых волн при исследова- нии селезенки в многопрофильном стационаре. Материалы и методы исследования За 2014 — 2015 годы на базе ОГБУЗ «Кли- ническая больница № 1» сотрудниками Про- блемной научно-исследовательской лаборато- рии ГБОУ ВПО Смоленского Государственного Медицинского Университета было обследовано 64 пациента, распределение больных по полу и возрасту представлены в таблице (табл. 1). В первую группу пациентов входило 11 паци- ентов с заболеваниями систем крови (5 паци- ентов с диагнозом железодефицитная анемия тяжелой степени тяжести, на фоне хроничес- кого атрофического гастродуоденита, средней степени тяжести; 6 пациентов с диагнозом лим- фогранулематоз, 2 стадия, категория В). Вторая группа инфекционных больных — 19 (5 пациен- тов с диагнозом инфекционный мононуклеоз; 14 пациентов с диагнозом хронический вирус- ный гепатит В, из них 5 пациентов с гепатитом В в стадии обострения с умеренными нарушени- ями функции печени (повышение АЛТ и АСТ соответственно до 93±6,2 Ед/л и 97±5 Ед/л) и 9 пациентов с выраженными нарушениями функции печени (повышение АЛТ до 223±19, АСТ до 245±19 Ед/л, ЩФ до 777±25 Ед/л) и начальными проявлениями портальной гипер- тензии и эндоскопическими признаками вари- козно расширенных вен пищевода 2-3 степени). Третья группа больных гастроэнтерологичес- кого отделения — 24 (13 пациентов с диагно- зом цирроз печени смешанного генеза (алко- гольной и вирусной природы) с выраженными нарушениями функции печени (повышение АЛТ до 390±22, АСТ до 330±21 Ед/л, ЩФ до 899±25 Ед/л), класс B по Чайлд-Пью, порталь- ной гипертензией и расширением вен пищевода; 11 пациентов с диагнозом — острый алкогольный гепатит, тяжелая форма, отечно-асцитический вариант) и пациентов с кардиологическими заболеваниями — 10 (диагноз — ИБС.
1). В первую группу пациентов входило 11 паци- ентов с заболеваниями систем крови (5 паци- ентов с диагнозом железодефицитная анемия тяжелой степени тяжести, на фоне хроничес- кого атрофического гастродуоденита, средней степени тяжести; 6 пациентов с диагнозом лим- фогранулематоз, 2 стадия, категория В). Вторая группа инфекционных больных — 19 (5 пациен- тов с диагнозом инфекционный мононуклеоз; 14 пациентов с диагнозом хронический вирус- ный гепатит В, из них 5 пациентов с гепатитом В в стадии обострения с умеренными нарушени- ями функции печени (повышение АЛТ и АСТ соответственно до 93±6,2 Ед/л и 97±5 Ед/л) и 9 пациентов с выраженными нарушениями функции печени (повышение АЛТ до 223±19, АСТ до 245±19 Ед/л, ЩФ до 777±25 Ед/л) и начальными проявлениями портальной гипер- тензии и эндоскопическими признаками вари- козно расширенных вен пищевода 2-3 степени). Третья группа больных гастроэнтерологичес- кого отделения — 24 (13 пациентов с диагно- зом цирроз печени смешанного генеза (алко- гольной и вирусной природы) с выраженными нарушениями функции печени (повышение АЛТ до 390±22, АСТ до 330±21 Ед/л, ЩФ до 899±25 Ед/л), класс B по Чайлд-Пью, порталь- ной гипертензией и расширением вен пищевода; 11 пациентов с диагнозом — острый алкогольный гепатит, тяжелая форма, отечно-асцитический вариант) и пациентов с кардиологическими заболеваниями — 10 (диагноз — ИБС. Атероскле- ротический и постинфарктный коронарокардио- склероз. Артериальная гипертензия 3 степени, риск 4. Хроническая сердечная недостаточность 2 Б. Постоянная форма мерцательной аритмии). Исследование проводилось на аппаратах с возможностью применения эластографии сдви- говых волн и компрессионной эластографи конвексным датчиком (частотой 3,5 — 5 МГц) АНГИОДИН-Соно/П-Ультра НПФ БИОСС, (Россия) и Hitachi Preirus (Япония). С учетом отсутствия стандартизированных этапов эла- стографии сдвиговых волн и компрессионной эластографии селезенки в предыдущих иссле- дованиях [17], мы предложили усовершенство- ванную методику, основанную на четком, поэ- тапном применении СЭГ и КЭ. Первым (основ- ным) этапом нашего исследования было про- ведение эластографии сдвиговых волн и ком- прессионной эластографии в стандартном поло- жении пациента лежа на правом боку с запро- кинутой за голову левой рукой с положением ультразвукового датчика параллельно ребер- ной дуге (рис. 1а, б). Вторым (основным) эта- пом нашего исследования было проведение эла- стографии сдвиговых волн в стандартном поло- жении пациента лежа на правом боку с запроки- нутой за голову левой рукой с положением уль- тразвукового датчика перпендикулярно ребер- ной дуге с получением максимального размера селезенки в поперечнике, с выведением сосу- дов ворот селезенки (рис.
Атероскле- ротический и постинфарктный коронарокардио- склероз. Артериальная гипертензия 3 степени, риск 4. Хроническая сердечная недостаточность 2 Б. Постоянная форма мерцательной аритмии). Исследование проводилось на аппаратах с возможностью применения эластографии сдви- говых волн и компрессионной эластографи конвексным датчиком (частотой 3,5 — 5 МГц) АНГИОДИН-Соно/П-Ультра НПФ БИОСС, (Россия) и Hitachi Preirus (Япония). С учетом отсутствия стандартизированных этапов эла- стографии сдвиговых волн и компрессионной эластографии селезенки в предыдущих иссле- дованиях [17], мы предложили усовершенство- ванную методику, основанную на четком, поэ- тапном применении СЭГ и КЭ. Первым (основ- ным) этапом нашего исследования было про- ведение эластографии сдвиговых волн и ком- прессионной эластографии в стандартном поло- жении пациента лежа на правом боку с запро- кинутой за голову левой рукой с положением ультразвукового датчика параллельно ребер- ной дуге (рис. 1а, б). Вторым (основным) эта- пом нашего исследования было проведение эла- стографии сдвиговых волн в стандартном поло- жении пациента лежа на правом боку с запроки- нутой за голову левой рукой с положением уль- тразвукового датчика перпендикулярно ребер- ной дуге с получением максимального размера селезенки в поперечнике, с выведением сосу- дов ворот селезенки (рис. 2). Третьим этапом (дополнительный) было проведение эластогра- фии сдвиговых волн у пациента лежа на спине с запрокинутой за голову левой рукой, с воз- можностью ротировать датчик, как параллельно реберной дуге, так и перпендикулярно. Принци- пиальными требованиями всех этапов явилось Распределение групп пациентов по полу и возрасту Таблица 1 Группы Всего Мужчины Женщины Средний возраст Абс. % Абс. % Абс. % 1 группа пациенты с ЗК 11 17,2 7 10,9 4 6,25 43,42±4,54 2 группа пациенты ИБ 19 29,7 17 26,6 2 3,1 40,75±7,26 3 группа пациенты ГО 24 37,5 18 28,1 6 9,4 42,14±6,69 4 группа пациенты КО 10 15,6 6 9,4 4 6,25 46,60±8,35 Всего 64 100 48 75 16 25 43,23±6,71 Примечание: ЗК — заболевания крови, ИБ — инфекционные больные, ГО — пациенты гастроэнтерологического отделения, КО — пациенты кардиологического отделения. Рис. 2. Второй этап стандартизированной методики: зона измерения эластографии сдвиговых волн при положении пациента лежа на правом боку, где 1 — схематичная визуализация селезенки при таком положении тела и датчика, 2 — положение датчика: перпендикулярно ребрам, 3 — проекция расположения ребер, 4 — зоны исследования плотности селезенки — мультифокальность исследования,5 — проекция визуализации сосудов в воротах селезенки проведение ЭСВ в 7 различных точках селе- зенки, на расстоянии 4-5 мм от капсулы селе- зенки и от крупных сосудов (рис 3).
2). Третьим этапом (дополнительный) было проведение эластогра- фии сдвиговых волн у пациента лежа на спине с запрокинутой за голову левой рукой, с воз- можностью ротировать датчик, как параллельно реберной дуге, так и перпендикулярно. Принци- пиальными требованиями всех этапов явилось Распределение групп пациентов по полу и возрасту Таблица 1 Группы Всего Мужчины Женщины Средний возраст Абс. % Абс. % Абс. % 1 группа пациенты с ЗК 11 17,2 7 10,9 4 6,25 43,42±4,54 2 группа пациенты ИБ 19 29,7 17 26,6 2 3,1 40,75±7,26 3 группа пациенты ГО 24 37,5 18 28,1 6 9,4 42,14±6,69 4 группа пациенты КО 10 15,6 6 9,4 4 6,25 46,60±8,35 Всего 64 100 48 75 16 25 43,23±6,71 Примечание: ЗК — заболевания крови, ИБ — инфекционные больные, ГО — пациенты гастроэнтерологического отделения, КО — пациенты кардиологического отделения. Рис. 2. Второй этап стандартизированной методики: зона измерения эластографии сдвиговых волн при положении пациента лежа на правом боку, где 1 — схематичная визуализация селезенки при таком положении тела и датчика, 2 — положение датчика: перпендикулярно ребрам, 3 — проекция расположения ребер, 4 — зоны исследования плотности селезенки — мультифокальность исследования,5 — проекция визуализации сосудов в воротах селезенки проведение ЭСВ в 7 различных точках селе- зенки, на расстоянии 4-5 мм от капсулы селе- зенки и от крупных сосудов (рис 3). Проведение исследования на спине применялось в качестве уточняющего исследования, при недостаточной визуализации селезенки на первом и втором этапах или трудностях при эластографии сдви- говых волн (неустойчивая фиксация изображе- ния, смещение за счет дыхательных движений и др). Данный этап не проводится, если все точки измерения на 1-2 этапах устойчивы при эласто- графии, а также при компрессионной эластогра- фии, из-за трудностей выполнения и визуализа- ции селезенки и почки при данном положение пациента. По итогам проводился анализ вос- производимости методики (ложноотрицатель- ные (ЛО) и ложноположительные (ЛП) резуль- таты) [3]. Также было проведено распределение Рис. 3. Зоны исследования селезенки при эластографии сдвиговых волн, где 1 — капсула селезенки (10 мм), 2 — зона повышенного кровоснабжения селезенки зона Б, 3 — сосуды селезенки, — участки исследования эластографии,сдвиговых волн селезенки в зоне предпочтительной для измерения — зона В, — зона нежелательная для измерений (зоны А — 1/6 длинника селезенки) — зона А, — участки исследования эластографии сдвиговых волн в зоне Б.
Проведение исследования на спине применялось в качестве уточняющего исследования, при недостаточной визуализации селезенки на первом и втором этапах или трудностях при эластографии сдви- говых волн (неустойчивая фиксация изображе- ния, смещение за счет дыхательных движений и др). Данный этап не проводится, если все точки измерения на 1-2 этапах устойчивы при эласто- графии, а также при компрессионной эластогра- фии, из-за трудностей выполнения и визуализа- ции селезенки и почки при данном положение пациента. По итогам проводился анализ вос- производимости методики (ложноотрицатель- ные (ЛО) и ложноположительные (ЛП) резуль- таты) [3]. Также было проведено распределение Рис. 3. Зоны исследования селезенки при эластографии сдвиговых волн, где 1 — капсула селезенки (10 мм), 2 — зона повышенного кровоснабжения селезенки зона Б, 3 — сосуды селезенки, — участки исследования эластографии,сдвиговых волн селезенки в зоне предпочтительной для измерения — зона В, — зона нежелательная для измерений (зоны А — 1/6 длинника селезенки) — зона А, — участки исследования эластографии сдвиговых волн в зоне Б. полученных количественных результатов жест- кости паренхимы селезенки в зависимости от нозологичес-кой формы. Референтным методом являлось цитологическое исследование биоп- сийного материала, аутопсии, заключительный клинический диагноз. Результаты исследования При анализе разработанного нами алгоритма проведения ЭСВ и КЭ и стандартного обследова- ния была выявлена тесная взаимосвязь времени, затраченного на исследование, появления ЛО и ЛП результатов и, как следствие, воспроизводи- мости методики в зависимости от применяемого алгоритма исследования. На стандартное обсле- дование уходило от 15 до 20 мин, на ЛО прихо- дилось 17,4%, на ЛП 20,6%, воспроизводимость колебалась от 37% до 70%. При проведении раз- работанной нами методики было получено ЛО — 8,2%, ЛП — 10,8%, воспроизводимость 93%. Ана- лизируя полученные данные можно отметить, что используя разработанный нами алгоритм увеличивается время проведения исследования, это связано с тем, что увеличивается количество зон эластографии сдвиговых волн, что, в свою очередь, значительно уменьшает появление ЛП и ЛО результатов.
полученных количественных результатов жест- кости паренхимы селезенки в зависимости от нозологичес-кой формы. Референтным методом являлось цитологическое исследование биоп- сийного материала, аутопсии, заключительный клинический диагноз. Результаты исследования При анализе разработанного нами алгоритма проведения ЭСВ и КЭ и стандартного обследова- ния была выявлена тесная взаимосвязь времени, затраченного на исследование, появления ЛО и ЛП результатов и, как следствие, воспроизводи- мости методики в зависимости от применяемого алгоритма исследования. На стандартное обсле- дование уходило от 15 до 20 мин, на ЛО прихо- дилось 17,4%, на ЛП 20,6%, воспроизводимость колебалась от 37% до 70%. При проведении раз- работанной нами методики было получено ЛО — 8,2%, ЛП — 10,8%, воспроизводимость 93%. Ана- лизируя полученные данные можно отметить, что используя разработанный нами алгоритм увеличивается время проведения исследования, это связано с тем, что увеличивается количество зон эластографии сдвиговых волн, что, в свою очередь, значительно уменьшает появление ЛП и ЛО результатов. При анализе полученных количественных данных, для ЭСВ выраженных в КПа, для КЭ — коэффициенте разницы (КР) выраженном в у.е., были получены следующие результаты: у пациентов с диагнозом железоде- фицитная анемия тяжелой степени тяжести, на фоне хронического атрофического гастродуоде- нита, средней степени тяжести показатель жест- кости составил 8,7±1,6 КПа, коэффициент раз- Таблица 2 Сравнительные данные возможности рутинной и усовершенствованной методики Алгоритм исследования Время затра- ченное на исследование Появление ложно- отрицательных или ложноположительных результатов Воспроизводимость алгоритма Чувствительность(Ч), специфичность (С), точность (Т) Стандартная методика ЭСВ 15 -20 мин 38% =>ЛО — 17,4% ЛП — 20,6% 37 -70%* 68,2% 91,4% 79,3% Разработанная методика ЭСВ 30 — 40 мин 19% =>ЛО — 8,2% ЛП — 10,8% 93% 93,1% 89,3% 91,3% ницы (КР) составил 0,9±0,31 у.е.; у пациентов с диагнозом лимфогранулематоз 2 стадия, катего- рия В — 18,6±2,8 КПа, КР — 1,8±0,69 у.е.; у пациентов с диагнозом инфекционный мононуклеоз — 5,9±2,2 КПа, КР — 0,4±0,23 у.
При анализе полученных количественных данных, для ЭСВ выраженных в КПа, для КЭ — коэффициенте разницы (КР) выраженном в у.е., были получены следующие результаты: у пациентов с диагнозом железоде- фицитная анемия тяжелой степени тяжести, на фоне хронического атрофического гастродуоде- нита, средней степени тяжести показатель жест- кости составил 8,7±1,6 КПа, коэффициент раз- Таблица 2 Сравнительные данные возможности рутинной и усовершенствованной методики Алгоритм исследования Время затра- ченное на исследование Появление ложно- отрицательных или ложноположительных результатов Воспроизводимость алгоритма Чувствительность(Ч), специфичность (С), точность (Т) Стандартная методика ЭСВ 15 -20 мин 38% =>ЛО — 17,4% ЛП — 20,6% 37 -70%* 68,2% 91,4% 79,3% Разработанная методика ЭСВ 30 — 40 мин 19% =>ЛО — 8,2% ЛП — 10,8% 93% 93,1% 89,3% 91,3% ницы (КР) составил 0,9±0,31 у.е.; у пациентов с диагнозом лимфогранулематоз 2 стадия, катего- рия В — 18,6±2,8 КПа, КР — 1,8±0,69 у.е.; у пациентов с диагнозом инфекционный мононуклеоз — 5,9±2,2 КПа, КР — 0,4±0,23 у. е.; у пациентов с гепатитом В в стадии обострения с умеренными нарушениями функции печени — 10,2±3,7 КПа, КР — 1,5±0,59 у.е., у пациентов с гепатитом В и выраженными нарушениями функции печени, начальными проявлениями портальной гипер- тензии и умеренным узловатым расширением вен пищевода — 32,2±3,2 КПа, КР — 31±6,3 у.е.; у пациентов с диагнозом цирроз печени смешан- ного генеза (алкогольной и вирусной природы) с выраженными нарушениями функции печени, портальной гипертензией и расширением вен пищевода — 34,4±4,7 КПа, КР — 33±7,3 у.е., у пациентов с диагнозом острый алкогольный гепатит, тяжелая форма, отечно-асцитический вариант — 12,7±3,5 КПа, КР — 1,5±0,45 у.е. и у пациентов с диагнозом: ИБС. Атеросклеротиче- ский и постинфарктный коронарокардиоскле- роз. Артериальная гипертензия 3 степени, риск Хроническая сердечная недостаточность 2Б. Постоянная форма мерцательной аритмии — 8,3±2,8 КПа, КР — 0,7±0,33 у.е.. При сравнении полученных данных с референтным методом были получены следующие данные чувствительности, специфичности и точности, пред- ставленные в таблице 2. Выводы При проведении эластографии сдвиговых волн и компрессионной эластографии по разра- ботанной нами усовершенствованной методике выявляется уменьшение ЛО и ЛП результатов. Вместе с тем, в начале освоения методики повы- шается время на проведение исследования. Это говорит о том, что несмотря на простоту при- менения методики эластографии, необходимо мультифокальное исследование селезенки. В таком случае специалист избежит неинформа- тивных случаев обследования пациента. При применении усовершенствованной методики также качественно возрастает воспроизводи- мость данных эластографии. Эластография сдвиговых волн и компресси- онная эластография селезенки позволяет опре- делить жесткость, а следовательно и ее вовле- ченность в патологический процесс, что непо- средственно влияет на исход и прогноз заболе- вания. Получены пилотные результаты информа- тивности применения эластографии сдвиговых волн при различных заболеваниях: чувствитель- ность — 93,1%, специфичность — 89,3%, точность — 91,3%.
е.; у пациентов с гепатитом В в стадии обострения с умеренными нарушениями функции печени — 10,2±3,7 КПа, КР — 1,5±0,59 у.е., у пациентов с гепатитом В и выраженными нарушениями функции печени, начальными проявлениями портальной гипер- тензии и умеренным узловатым расширением вен пищевода — 32,2±3,2 КПа, КР — 31±6,3 у.е.; у пациентов с диагнозом цирроз печени смешан- ного генеза (алкогольной и вирусной природы) с выраженными нарушениями функции печени, портальной гипертензией и расширением вен пищевода — 34,4±4,7 КПа, КР — 33±7,3 у.е., у пациентов с диагнозом острый алкогольный гепатит, тяжелая форма, отечно-асцитический вариант — 12,7±3,5 КПа, КР — 1,5±0,45 у.е. и у пациентов с диагнозом: ИБС. Атеросклеротиче- ский и постинфарктный коронарокардиоскле- роз. Артериальная гипертензия 3 степени, риск Хроническая сердечная недостаточность 2Б. Постоянная форма мерцательной аритмии — 8,3±2,8 КПа, КР — 0,7±0,33 у.е.. При сравнении полученных данных с референтным методом были получены следующие данные чувствительности, специфичности и точности, пред- ставленные в таблице 2. Выводы При проведении эластографии сдвиговых волн и компрессионной эластографии по разра- ботанной нами усовершенствованной методике выявляется уменьшение ЛО и ЛП результатов. Вместе с тем, в начале освоения методики повы- шается время на проведение исследования. Это говорит о том, что несмотря на простоту при- менения методики эластографии, необходимо мультифокальное исследование селезенки. В таком случае специалист избежит неинформа- тивных случаев обследования пациента. При применении усовершенствованной методики также качественно возрастает воспроизводи- мость данных эластографии. Эластография сдвиговых волн и компресси- онная эластография селезенки позволяет опре- делить жесткость, а следовательно и ее вовле- ченность в патологический процесс, что непо- средственно влияет на исход и прогноз заболе- вания. Получены пилотные результаты информа- тивности применения эластографии сдвиговых волн при различных заболеваниях: чувствитель- ность — 93,1%, специфичность — 89,3%, точность — 91,3%.
- Борсуков А.В., Крюковский С.Б., Покусаева В.Н. с соавт. Эластография в клинической гепатологии (частные вопросы). Смоленск: Смоленская городская типография; 2011; 276 с.
- Буеверов А.О. Эластография — новый метод неинвазивной диагностики фиброза печени. Гепатологический форум. 2007. № 2. С. 14-18.
- Гланц С. Медико-биологическая статистика. Пер. с англ. М., Практика, 1998. 459 с.
- Зубарев А.В. Эластография — новый метод поиска рака различных локализаций / А.В. Зубарев, В.Е. Гажонова, Е.Н. Хохлова, и др. // Радиология — практика. 2008. № 6. C. 6-18.
- Митьков В.В. Оценка воспроизводимости результатов количественой ультразвуковой эластрографии / В.В. Митьков, С.А. Хуако, Э.Р. Ампилогова и др. // Ультразвуковая и функциональная диагностика. 2011. № 2. С. 120.
- Осипов Л.В. Технологии эластографии в ультразвуковой диагностике (обзор). Медицинский алфавит. Диагностическая радиология и онкотерапия. 2013; 3-4: 5-21.
- Bamber J., Cosgrove D., Dietrich C.F. et al. EFSUMB Guidelines and Recommendations on the Clinical Use of Ultrasound Elastography. Part 1: Basic Principles and Technology. Ultraschall in Med. 2013; 34: 169-184.
- R.H. Behler, T.C. Nichols, H. Zhu, et al. ARFI imaging for noninvasive material characterization of atherosclerossis. Part II: toward in vivo characterization / / Ultrasound Med Biol. 2009. Vol. 35. P. 278-295.
- Bercoff J. Supersonic shear imaging: a new technique for soft tissue elasticity napping. IEEE Trans / J. Bercoff, M. Tanter, M. Fink // Ultrason Ferroelectr Freq Control. 2004. Vol. 51, N 4. P. 396-409.
- Cosgrove D., Bamber J., Dietrich C.F., et al. EFSUMB Guidelines and Recommendations on the Clinical Use of Ultrasound Elastography. Part 2: Clin Appl. DOI http://dx.doi.org/10.1055/s-0033-1335375 Published on-line: 2013.
- Garra B.S. Imaging and estimation of tissue elasticity by ultrasound. Ultrasound Q. 2007. Vol. 23, N 4. P. 255-268.
- Giorgio A. Sonographic recongnition of intraparenchymal regenerating nodules using high-frequency transducers in patients with cirrhosis / A. Giorgio, G. Francia, G. de Stefano et al. // J. Ultrasound Med. 1991. Vol. 10, N 7. P. 355-59.
- M. Giovannini, B. Thomas, B. Erwan et al. Endoscopic ultrasound elastography for evaluation of lymph nodes and pancreatic masses: a multicenter study. World J Gastroenterol. 2009. Vol. 15, N 13. P. 1587-93.
- Goertz R.S. Measurement of liver elasticity with acoustic radiation force impulse (ARFI) technology: an alternative noninvasive method for staging liver fibrosis in viral hepatitis / R.S. Goertz, Y. Zopf, V. Jugl, et al. // Ultraschall Med. 2010. Vol. 31, N 2. P. 151-155.
- Gomez-Dominguez, E. Transient elastography: a valid alternative to biopsy in patients with chronic liver disease / E. Gomez-Dominguez, J. Mendoza, S. Rubio et al. // Aliment Pharmacol Ther. 2006. Vol. 24. P. 513-18.
- Greenleaf, J.F. Selected methods for imaging elastic properties of biological tissues. / J.F. Greenleaf, M. Fatemi, M. Insana // Ann Rev Bomed Eng. 2003. Vol. 5. P. 57-78.
- Leonardo R., Massimo A., et al. A New Sampling Method for Spleen Stiffness Measurement Based on Quantitative Acoustic Radiation Force Impulse Elastography for Noninvasive Assessment of Esophageal Varices in Newly Diagnosed HCV-Related Cirrhosis. Hindawi Publishing Corporation. BioMed Res Int Vol. 2014, Article ID 365982, 8 pgs.
- M. Lupsor, R. Badea, H. Stefanescu, et al. Performance of a New Elastographic Method (ARFI technology) Compared to Unidimensional Transient Elastography in the Noninvasive Assessment of Chronic Hepatitis C. Preliminary Resalts. J Gastrointest Liver Dis. 2009. Vol. 3. P. 303-10.
- Nightingale K. Shear-wave generation using acoustic radiation force: in vivo and ex vivo results / K. Nightingale, S. McAleavey, G. Trahey // Ultrasound Med Biol. 2003. Vol. 29, N 12. P. 1715-1723.
- M.L. Palmeri, K. Frinkley, L. Zhai, et al. Acoustic Radiation Force Impulse (ARFI) imagibg of the gastrointestinal tract.Ultrasonic Imaging. 2005. Vol. 27. P. 75-88.
Views
Abstract — 198
PDF (Russian) — 176
Cited-By
Article Metrics
PlumX
Постинфарктный кардиосклероз — Лечение сердечно-сосудистой системы Красная Пахра Московская область
Постинфарктный кардиосклероз — Лечение сердечно-сосудистой системы Красная Пахра Московская областьПорядок санаторно-курортного лечения постинфарктного кардиосклероза: замедление прогрессирования сердечной недостаточности, нарушение проводимости и сердечного ритма, профилактика разрастания соединительной ткани.
Вылечить болезнь невозможно, поэтому врачи все силы тратили на поддержание жизни и состояния пациента. Назначили диуретики, метаболические средства и бета-адреноблокаторы для профилактики аритмий. Назначен к периферическим статинам, бета-адреноблокаторам, антиагрегантам, диуретикам, антиаритмическим препаратам и т. Д.
Противопоказания
- Ишемическая болезнь сердца: стенокардия 111-1V функциональных классов нестабильной стенокардии.
- Недостаточность кровообращения выше 1 степени.
- Миокардит в активной стадии.
- Нарушения ритма сердца: атриовентрикулярная блокада 11-111 степени, часто более 5 ударов в минуту, пароксизмальная а-фибрилляция предсердий, наджелудочковая пароксизмальная тахикардия, желудочковая пароксизмальная тахикардия.
- Облитерирующий тромбангиит с тенденцией к генерализации, свежими изъязвлениями и гангреной.
- Тромбоэмболическая болезнь.
- Гипертоническая болезнь третьей степени.
Результаты лечения
В результате правильного лечения можно избежать развития сердечной недостаточности, опасных аритмий и продлить активное долголетие. После операции наблюдается улучшение функционирования жизнеспособного миокарда.Последствия отсутствия лечения
Инфаркт миокарда — заболевание, которое заставляет пациента регулярно следить за своим состоянием.Пропуски могут привести к необратимым последствиям — развитию аневризмы, угрожающих жизни аритмий, прогрессированию сердечной недостаточности и инвалидности.Инфаркт миокарда — форма ишемической болезни сердца, которая характеризуется частичным замещением сердечной мышечной ткани в исходе сердечного приступа. У человека одышка, утомляемость, отеки и нарушение сердечного ритма.
Лечение постинфарктного кардиосклероза в Марианских Лазнях, Чехия
Тип ишемической болезни сердца, при которой часть сердечной мышцы заменяется соединительной тканью.Пациенты с постинфарктным кардиосклерозом жалуются на прогрессирующую одышку, тахикардию, снижение выносливости при физических нагрузках, ортопноэ. На фоне сопутствующей артериальной гипертензии может развиться отек легких. При развитии недостаточности правого желудочка появляются отеки ног, гидроторакс, гидроперикард, акроцианоз, набухают вены на шее. Часто диагностируются мерцательная аритмия, блокада, желудочковые экстрасистолии. Пациенту необходимо ограничить физические и психоэмоциональные нагрузки, соблюдать диету, регулярно принимать ингибиторы АПФ, нитраты, бета-адреноблокаторы, антиагреганты, диуретики или препараты других групп, назначенные лечащим кардиологом.В сложных случаях показано хирургическое лечение, в том числе имплантация кардиостимулятора.
Лучшие спа-отели в Марианске-Лазне по качеству лечения
Спа Отель Вилла Валир
3 *От 71 € за 1 день полный пансион и лечение
10,0 /10Спа Отель Роял
4 *От 74 € за 1 день полный пансион и лечение
9,8 /10Спа Отель Мария Спа
4 *От 110 € за 1 день полный пансион и лечение
9,7 /10Спа Отель Ричард
4 *От 47 € за 1 день полный пансион и лечение
8,4 /10Спа Отель Звезда
4 *От 109 € за 1 день полный пансион и лечение
9,6 /10Спа Отель Империал
4 *От 105 € за 1 день полный пансион и лечение
9,5 /10 Показать все спа-отели в городе Марианске-ЛазнеПочинская Марина Александровна Руководитель службы поддержки
Консультация врача
Бесплатная помощь врача санатория
Если у вас возникли трудности с выбором санатория или спа-отеля, подходящего для лечения ваших заболеваний, воспользуйтесь бесплатной консультацией санаторно-курортного врача Елены Хорошевой.
Отправьте свой вопрос здесьЕлена Хорошева Главный врач sanatoriums.com
Постинфарктный кардиосклероз
Инфаркт миокарда — одно из самых тяжелых сердечно-сосудистых заболеваний.Часто осложняется различными патологиями, в том числе постинфарктным кардиосклерозом. Это заболевание считается достаточно тяжелым и требует соответствующего лечения.
Постинфарктный кардиосклероз (ПИКС) — сердечно-сосудистое заболевание, при котором кисты миокарда замещаются соединительной тканью. Чаще всего это связано с некрозом клеток, возникающим при длительной ишемии сердечной мышцы. В результате нарушается деятельность сердца, могут развиваться различные формы аритмии.
Заболевание включено в Международную классификацию болезней (МКБ-10) под кодом I25.1 и озаглавлено «Атеросклеротическое заболевание сердца. Коронарные артерии: атерома, атеросклероз, болезнь, склероз».
Для обследования больных с подозрением на постинфарктный кардиосклероз используются различные методы обследования (электрокардиография, УЗИ, ЧСС, рентген ОГК). После постановки точного диагноза назначается лечение, так как без этого грозит развитие сердечной недостаточности.
Что такое кардиосклероз?
Причины
Постинфарктный кардиосклероз вызывается одной основной причиной — смертью сердечных клеток, чаще всего вызываемой ишемической болезнью сердца. После этого некротизированные участки миокарда замещаются элементами соединительной ткани, из-за чего сердце начинает хуже сокращаться.
Рубцевание миокарда после сердечного приступа начинается сразу после приступа и заканчивается примерно через два-четыре месяца.
В редких случаях PICS развивается по двум другим причинам:
- Дистрофия миокарда — из-за нарушения обмена веществ в сердечной мышце развиваются необратимые процессы, приводящие к некрозу кардиомиоцитов. На их месте и образовались PICS.
- Травма органа — при физическом воздействии на миокард, которое чаще всего происходит при различных операциях и процедурах, на месте поражения развивается РИС со всеми вытекающими последствиями.
Две последние причины PICS обнаруживаются гораздо реже, чем основная.
Прогностические факторы для развития PICS:
- Курение
- Ожирение
- Частые напряжения
- Физическое перенапряжение
- Длительный гипертонус
- Наследственная предрасположенность
На фоне таких факторов риска заболевание развивается медленнее, но непрерывно, что в результате также может привести к сердечной недостаточности.
Клиника
Выраженность проявлений постинфарктного кардиосклероза в основном зависит от тяжести поражения миокарда. Чем глубже и больше рубцов образуется после инфаркта миокарда и лежащего в основе постинфарктного кардиосклероза, тем тяжелее клиническая картина. Также немаловажное значение имеет локализация РИС.
Симптомы ПИКС часто совпадают с признаками осложнений, развивающихся на фоне заболевания. В частности, можно определить следующие заболевания с характерными проявлениями:
- Сердечная недостаточность — будут отмечены отек, тяжелое дыхание и снижение физической активности.
Сердечная астма — проявляется ночной одышкой. Часто такие пациенты занимают положение ортопноэ (полусосущего), так как им становится хуже в положении лежа.
Самопроизвольная стенокардия также может быть следствием РИС, и в то же время сочетание пациента вызывает боль в сердце, особенно при эмоциональном или физическом напряжении.
Гидротакси — проявляется ощущением тяжести на стороне поражения. Кроме того, усиливается одышка.
Акроцианоз — характеризуется смещением отдаленных частей тела (носа, губ, пальцев) из-за нарушения кровообращения.
Развитие крупномасштабного постинфарктного кардиосклероза часто связано с тяжелой клинической картиной. Это связано с заменой большого участка миокарда соединительной тканью, не способной проводить электрические импульсы и сокращаться. Поэтому в данном случае чаще определяют следующие характеристики:
- Боль в области сердца
- Осложненное дыхание
- Нарушение ритма сердца
- Выражение слабости и утомляемости
- Ощущение тяжести в нижних конечностях от отека тканей
Осложнения
- Мерцательная аритмия
- Аневризма левого желудочка
- Разнообразные блокады: атриовентрикулярная, пучок Гиссы, ножки Пуркинье
- Различные тромбозы, тромбоэмболические проявления
- Пароксизмальная желудочковая тахикардия
- Экстра вагинальная астма
- Тампонада перикарда
- Синдром слабости синусового узла.
В особо тяжелых случаях может произойти разрыв аневризмы, в результате чего пациент умирает. Кроме того, осложнения снижают качество жизни пациента из-за прогрессирования определенных состояний:
- Запах усиливается
- Инвалидность и снижена физическая выносливость
- Часто беспокоящие нарушения сердечного ритма
- Может наблюдаться фибрилляция желудочков и предсердий
При формировании атеросклероза побочные эффекты могут влиять на не внетелесные части тела.В частности, часто определяют:
- Расстройства ощущений в конечностях, в основном поражающие голени и фаланги пальцев рук
- Синдром холодных конечностей
- Прогрессирующая атрофия мышц
Такие патологические нарушения могут поражать сосудистую систему головного мозга, глаз и другие органы / системы тела.
Видео Гипертония, ишемическая болезнь сердца, кардиосклероз
Диагностика
При подозрении на постинфарктный кардиосклероз врачу-кардиологу назначается ряд исследований:
- Анализ истории болезни пациента
- Осмотр пациента врачом
- Электрокардиография проведения
- Ультразвуковое исследование сердца
- Ритмокардиография, дополнительное неинвазивное электрофизиологическое исследование сердца, с помощью которого врач получает информацию о вариабельности ритма и кровотока
- Позитронно-эмиссионная томография (ПЭТ) сердца — это радионуклидное томографическое исследование, позволяющее обнаружить участки гипоперфузии (склерозирования) миокарда
- Коронарная ангиография — рентгеноконтрастное исследование коронарных артерий сердца для диагностики ишемической болезни сердца с использованием рентгеновских лучей и контрастных веществ
- Эхокардиография — один из методов ультразвукового исследования, направленный на изучение морфофункциональных изменений сердца и его клапанного аппарата.
- Рентгенография может помочь определить размер сердца.
- Стресс-тесты — позволяют диагностировать или исключить преходящую ишемию
- Холтеровское мониторирование — позволяет контролировать сердце пациента каждый день
- Вентрикулография — это более целенаправленное исследование, представляющее собой рентгеновский метод оценки клеток сердца, в которые вводится контрастное вещество. В этом случае изображение контрастируемых отделов сердца фиксируется на специальной пленке или другом регистрирующем устройстве.
Постинфарктный кардиосклероз на ЭКГ
Данный метод обследования пациентов с ПИКС направлен на анализ биоэлектрической активности волокон миокарда.Импульс, возникающий в синусовом узле, проходит по специальным волокнам. Параллельно с прохождением пульсового сигнала кардиомиоциты сокращаются.
Во время электрокардиографии направление движущегося импульса фиксируется с помощью специальных чувствительных электродов и регистрирующего устройства. В результате врач может получить клиническую картину работы отдельных структур сердца.
Сама процедура безболезненна и занимает немного времени. Принимая во внимание всю подготовку к этому исследованию, обычно это занимает от 10 до 15 минут.
При ФИКС на ЭКГ выявляются следующие нарушения:
- Изменения прочности на разрыв QRS, что указывает на аномалию желудочков.
- Отрезок S-T может располагаться ниже изолинии.
- Зубцы Т иногда опускаются ниже нормы, в том числе переход к отрицательным значениям.
- В тяжелых случаях определяется тремор или мерцательная аритмия.
- Наличие блокады свидетельствует о плохой проводимости сердца.
Лечение
Образованный постинфарктный кардиосклероз можно вылечить только оперативным путем. Медикаментозное лечение применяют только на стадии поражения сосудов атеросклерозом. В таких случаях еще можно с помощью специальных препаратов усилить обмен веществ и кровоснабжение сердца, что улучшит состояние пациента.
Лечебное действие основано на применении следующих групп препаратов:
- Метаболические вещества (рибоксин, кардиомагнол, милдронат, глицин, биотредин и др.))
- Фибраты (гевилон, нормолип, фенофибрат, гемфиброзил, регулятор и др.)
- Статины (апексстатин, овуакор, пивастатин, аторвастатин, кардиостимулятор, симвастатин, лобстер и др.)
- Ингибиторы АПФ (миоприл, миниприл, каптоприл, эналакор, оливин и др.)
- Кардиотоники (строфантин, ланоксин, диланацин и др.)
- Диуретики (лазикс, фуросемид, индап и др.)
Лечение медикаментами, как правило, проводится комплексно с учетом индивидуальных особенностей каждого пациента.
Оперативное лечение
Применяется в случае неэффективности лечебного воздействия. Из современных хирургических методов для улучшения состояния больных постинфарктным кардиосклерозом чаще всего используются:
- Расширение сосудов, в частности коронарных. Для этого применяют баллонную ангиопластику или стентирование, которые в некоторых случаях совмещают в одной процедуре.
- Шунтирование — Шунт создается для обхода суженной части артерии, для которой чаще всего используется часть бедренной вены.
Помимо вышеперечисленных методов лечения, применяется физиотерапия, например, электрофорез. Применяется местно, в области сердца, и при этом обязательно используются какие-либо препараты, чаще всего статины, которые благодаря такому методу лечения попадают прямо в места поражения.
Для укрепления организма рекомендуется пройти курс лечения на курорте, расположенном в горной местности. В нормальном состоянии пациенту могут быть назначены лечебные упражнения, способствующие повышению мышечного тонуса и нормализации артериального давления.
Прогноз
При постинфарктном кардиосклерозе прогнозируемое заключение основывается на тяжести течения и локализации патологического очага.
Значительное ухудшение качества жизни пациентов наблюдается при поражении левого желудочка, особенно если сердечный выброс снижен на 20%. Лекарства могут поддерживать состояние, но кардинальное улучшение может наступить только после трансплантации органа. В противном случае прогнозируется пятилетняя выживаемость.
Клинически неблагоприятный прогноз при большом количестве поражений соединительной ткани. Как известно, они не способны сокращаться или пульсировать, поэтому остальной миокард стремится выдержать интенсивную работу, но обычно через такое время у компенсации развивается сердечная недостаточность.
Развитие постинфарктного кардиосклероза — необратимый процесс, поэтому после его обнаружения следует проводить адекватное лечение под наблюдением квалифицированного специалиста.Только в этом случае возможно не только улучшение состояния, но и спасение жизни пациента.
Профилактика
Практика принципов здорового образа жизни — профилактика многих патологий, в том числе постинфарктного кардиосклероза. Это заболевание, как и любое другое сердечно-сосудистое заболевание, тесно связано с питанием и образом жизни человека, поэтому для предотвращения развития ПИКС необходимо выполнять несколько простых правил:
- Важно придерживаться здорового и сбалансированного питания.В частности, есть нужно дробно, но чаще примерно 5-6 раз в день. Следует выбирать продукты, богатые калием и магнием.
- Физическая активность должна быть регулярной, но не перегруженной.
- Большое значение имеет полноценный отдых и полноценный сон.
- Необходимо поддерживать эмоциональную устойчивость, для чего следует избегать стрессов.
- Полезные умеренные СПА-процедуры.
- Хорошее воздействие на организм оказывает лечебный массаж.
- Сохранять позитивный настрой стоит, несмотря ни на что.
Отдельно обращая внимание на питание, следует отметить:
- От кофе и алкоголя хорошо отказаться.
- Необходимо свести к минимуму употребление тонизирующих напитков (какао, черный чай)
- Соль нужно употреблять в ограниченном количестве
- Не используйте сильнорослый чеснок и лук
- Сорт рыбы должен быть нежирным.
Скопление газов в кишечнике также может плохо сказаться на состоянии человека, поэтому важно ограничить употребление фасоли, молока, свежей капусты всех сортов.Также при профилактике развития атеросклероза, приводящего к ПИКС, необходимо исключить из рациона легкие, печень и мозг животных. Вместо этого лучше есть зелень и фрукты.
4,83 ср. рейтинг ( 95 % баллов) — 6 голосов — голосов
Влияние коморбидной депрессии на приверженность к терапии рассеянного склероза
Цель .Изучите влияние коморбидной депрессии на приверженность модифицирующей болезнь терапии (DMT) при рассеянном склерозе (MS). Методы . Ретроспективная база данных использовалась для идентификации пациентов с рассеянным склерозом, получавших ДМТ. Пациенты с РС и коморбидной депрессией были сопоставлены только с пациентами с РС. Приверженность к ДМТ выражалась коэффициентом владения лекарствами (MPR), и для изучения связи между коморбидной депрессией и приверженностью к ДМТ использовались многомерные регрессии. Результатов .Пациенты с коморбидной депрессией имели MPR на 10 пунктов ниже () и с меньшей вероятностью достигли MPR не менее 80% (отношение шансов; 95% доверительный интервал (ДИ) 0,42–0,74), чем пациенты без депрессии. Хотя лечение антидепрессантами обычно не оказывало значительного влияния на вероятность достижения порогового значения MPR 80% (; 95% ДИ 0,50–3,48), соблюдение рекомендаций по терапии антидепрессантами было связано с улучшением приверженности к терапии ДМТ. Выводы . Пациенты с РС с коморбидной депрессией примерно вдвое реже придерживались ДМТ по сравнению с пациентами с РС без депрессии.Хотя лечение антидепрессантами в целом не улучшало вероятность приверженности, лечение антидепрессантами в течение как минимум 6 месяцев было связано с лучшей приверженностью к ДМТ.
1. Введение
Рассеянный склероз (РС) — наиболее частое неврологическое состояние, приводящее к инвалидности, у молодых людей и подростков в Соединенных Штатах [1]. Примерно 400 000 американцев страдают рассеянным склерозом, и каждую неделю это заболевание диагностируется примерно у 200 человек [2]. Хотя результаты существующих исследований бремени болезни, проведенных для РС в Соединенных Штатах, различаются в зависимости от используемых источников данных [3], все они сообщают о существенных экономических последствиях РС как для человека, так и для страны.Сообщается, что стоимость каждого рецидива рассеянного склероза составляет приблизительно 12 870 долларов США [4]. Средняя стоимость лечения рассеянного склероза для отдельного пациента ежегодно составляет от 12 879 долларов (2004 долларов) [5] до 34 000 долларов (1994 долларов) [6]. Эти цифры соответствуют национальным расходам от 5,2 миллиарда долларов (12 879 долларов на 400 000 американцев с диагнозом РС) [5] до 6,8 миллиардов долларов (на основе цифр распространенности, использованных авторами [6], ежегодно.
Хотя РС неизлечим, продукты питания и Было показано, что лекарственные препараты, одобренные Управлением по контролю за продуктами и лекарствами (FDA), модифицирующие болезнь (DMT) снижают частоту рецидивов и замедляют прогрессирование заболевания [7, 8].Однако лекарства могут работать, только если их принимать. Было показано, что несоблюдение режима приема лекарств связано с повышенной заболеваемостью пациентов, ухудшением качества жизни и увеличением финансовой нагрузки на медицинские учреждения [9]. Кроме того, исследования также показали, что приверженность лечению у пациентов с РС обычно неоптимальна [10–13].
Одним из факторов, который, как было показано, отрицательно влияет на приверженность пациентов с РС, является наличие коморбидной депрессии [10, 13]. Этот фактор может повлиять на большую часть населения РС, поскольку депрессия распространена среди людей с РС.Исследования показали, что до половины всех пациентов с РС [14, 15] имеют коморбидную депрессию, и что распространенность этой коморбидности в три раза превышает уровень большой депрессии и сопутствующей психической патологии в выборках на уровне сообщества и превышает частота депрессии среди пациентов с другими неврологическими расстройствами [16].
Учитывая потенциальное влияние депрессии на приверженность к лечению РС, а также относительно высокую распространенность этой сопутствующей патологии, этот анализ был разработан для количественной оценки влияния коморбидной депрессии и антидепрессивной терапии на приверженность к терапии, модифицирующей болезнь (ДМТ) при РС.Учитывая предыдущую литературу, в которой сообщается о связи между расстройствами настроения и приверженностью пациентам с РС [10], мы предположили, что диагноз коморбидной депрессии будет иметь негативное влияние на приверженность. Кроме того, мы исследовали влияние приема антидепрессантов на приверженность к лечению РС. При этом анализ количественно определяет связь между коморбидной депрессией, приемом антидепрессантов и приверженностью к терапии РС.
2. Материалы и методы
2.1. Данные
Базы данных MedStat MarketScan Commercial Claims and Encounters (CCAE) и Medicare (MDCR) предоставили данные для этого анализа, который был сосредоточен исключительно на данных с 1 января 2004 года по 25 марта 2009 года. Эти ретроспективные базы данных страховых требований включают данные о здравоохранении частного сектора от примерно 100 плательщиков и содержат данные о клиническом использовании, расходах и регистрации в стационарных, амбулаторных, рецептурных лекарствах и отпускных службах. Деидентифицированные базы данных полностью соответствуют Закону о переносимости и подотчетности медицинского страхования (HIPAA) и связывают оплаченные претензии и данные о встречах с подробной информацией о пациентах на разных сайтах и типах поставщиков с течением времени.
2.2. Образец
Для включения в исследование пациенты должны были получить по крайней мере один диагноз РС (код ICD-9-CM 340.xx) и терапию, изменяющую заболевание (DMT), с первой такой квитанцией в окно даты, обозначенное как индексная дата, и исходный полученный ДМТ, идентифицированный как лекарство, предназначенное для лечения (ITT). Пациенты были исключены, если у них была диагностирована беременность (код МКБ-9-CM 630.xx-676.xx, V22.2x или V22.3x) в течение периода времени от 6 месяцев до даты индекса (т.е., пре-период) через 12 месяцев после даты индекса (т. е. постпериод). Наконец, пациенты должны были иметь непрерывное страховое покрытие с начала до конца периода после окончания периода. По этим критериям была отобрана 11780 человек (рис. 1).
Учитывая вышеупомянутую когорту людей, группа затем была разделена на пациентов, у которых не было ни диагноза депрессии, ни приема антидепрессантов в предшествующий период (т. Е., Только РС) и тех, у кого была диагностирована коморбидная депрессия (т. Е. РС и депрессия). Чтобы быть идентифицированными как страдающие депрессией в течение 6 месяцев до начала периода, пациенты должны были получить 2 или более амбулаторных или 1 или более стационарных диагнозов депрессии (МКБ-9-CM 296.2x, 296.3x или 311.xx), или 1 или несколько диагнозов депрессии и 1 или несколько выписанных рецептов на антидепрессант. Для пациентов, которые не получали антидепрессант, требовалось установить один стационарный диагноз или два амбулаторных диагноза депрессии, чтобы гарантировать, что пациенту был поставлен диагноз депрессии, а не просто скрининг на депрессию.Кроме того, такой алгоритм обычно используется для идентификации диагнозов в ретроспективных базах данных [17, 18]. Было 4479 человек с диагнозом РС, у которых не было доказательств депрессии (только РС), и у 448 человек был диагностирован РС и коморбидная депрессия (РС и депрессия). Из 448 человек с РС и депрессией 379 человек получили по крайней мере один рецепт на антидепрессант.
Учитывая вышеупомянутую выборку пациентов, были обследованы три подгруппы пациентов.Одна группа состояла из сопоставимой группы пациентов с РС только с пациентами с РС и депрессией, где пациенты были сопоставлены 1: 1 без замены в зависимости от возраста, пола, региона проживания, года индексации и намерения лечить лекарствами. . Это сопоставление привело к успешному совпадению 97% и окончательной выборке из 876 человек: 436 человек с РС и депрессией и 436 человек только с РС. В дополнение к обследованию пациентов с РС и только пациентов с РС и депрессией, мы также исследовали приверженность лечению, сравнивая пациентов, у которых была диагностирована депрессия, но не принимавших антидепрессант (), с пациентами с диагнозом депрессия, которые действительно получали антидепрессант ().Эти две группы были сопоставлены 1: 1 без замены с использованием тех же факторов, которые использовались для сопоставления группы только РС и группы РС и депрессии. В результате была получена окончательная выборка из 76 человек: 38 человек с диагнозом депрессия и не принимавших антидепрессант, и 38 человек, у которых была диагностирована депрессия и которые выполнили хотя бы один рецепт на антидепрессант. Третья группа сравнивала пациентов, получавших антидепрессанты, на основании соблюдения лечебных рекомендаций по применению антидепрессантов [19].В частности, пациенты были разделены на группы после получения как минимум 6-месячного запаса антидепрессантов. Опять же, две когорты были сопоставлены 1: 1 без замены, с окончательной выборкой из 142 человек: 71 человек лечился в соответствии с рекомендациями, и 71 человек получал антидепрессанты менее 6 месяцев.
2.3. Измерение приверженности
Хотя приверженность обычно измеряет степень, в которой пациент действует в соответствии с предписанным интервалом и дозой режима дозирования [20], такая информация обычно не доступна в базе данных ретроспективных требований.Таким образом, приверженность «… операционализируется в ретроспективных оценках как количество выданных доз по отношению к периоду отпуска, часто называемое коэффициентом владения лекарством (MPR)» [20]. Эта переменная измеряется как процент дней, в течение которых лекарство ITT было доступно пациенту, на основе дат получения рецепта в течение 1-летнего периода после окончания периода лечения и является обычным показателем приверженности лечению при изучении ретроспективных данных [6, 21, 22]. В качестве теста на надежность результатов мы также рассмотрели альтернативный прокси для определения приверженности.В частности, для каждого пациента также была рассчитана переменная доля охваченных дней (PDC) [23]. PDC, как и MPR, является мерой процента дней, в течение которых человек получал свой препарат ITT в течение года после даты индексации. Однако, в отличие от MPR, PDC не допускает совпадения предписаний. В результате, PDC, в отличие от MPR, всегда будет иметь верхнюю границу 1. Результаты, представленные здесь, не чувствительны к этой альтернативной спецификации, и, следовательно, результаты, в которых PDC использовался в качестве зависимой переменной, не сообщались.Однако следует отметить, что ни MPR, ни PDC не могут измерить, принимал ли человек рецепт после того, как он был заполнен, выполнил ли человек рецепт, выписанный его врачом, или прекратил ли человек принимать лекарства ITT по рекомендации врача или вопреки ему. .
2.4. Статистический анализ
Описательная статистика сравнивалась между группами с использованием статистики хи-квадрат. Многомерные регрессии использовались для изучения влияния коморбидной депрессии, а также медикаментозного лечения депрессии на вероятность того, что пациент будет придерживаться своего MS ITT DMT.В частности, обычные регрессии наименьших квадратов использовались для изучения влияния депрессии на MPR, когда MPR измеряли как непрерывные переменные, в то время как логистические модели использовались для изучения связи депрессии с вероятностью достижения порогового значения MPR не менее 80% [ 24, 25].
В многомерных моделях была выдвинута гипотеза, что в дополнение к факторам, по которым группы были сопоставлены (возраст, пол, регион проживания, терапия ITT DMT и год даты индекса), другие характеристики пациента также могут влиять на приверженность.В частности, эти анализы также изучали связь между статусом страхования пациента, характеристиками лекарств ITT, общим состоянием здоровья пациента, уровнем инвалидности и приверженностью к ITT DMT. Характеристики лекарств ITT, которые были исследованы, включали сумму доплаты, за которую лицо несло ответственность, а также то, было ли лекарство ITT доставлено по почте. Была выдвинута гипотеза, что пациенты, которым требуется внести доплату за свои лекарства, могут быть менее привержены своему режиму лечения, в то время как доставка по почте может быть связана с простотой использования и, следовательно, может быть связана с улучшенной приверженностью.Общее состояние здоровья пациента оценивалось с помощью индекса коморбидности Чарлсона (CCI) [26, 27]. Эта мера, которая хорошо зарекомендовала себя как алгоритм прогнозирования больничной смертности и часто используется в ретроспективном анализе баз данных, состоит из средневзвешенного значения, основанного на получении диагностических кодов, связанных с 17 заболеваниями. Примеры состояний, включенных в CCI, включают заболевание почек, инфаркт миокарда, злокачественные новообразования, заболевания печени, цереброваскулярные заболевания, застойную сердечную недостаточность, деменцию и диабет [28].Наконец, уровень пациентки инвалидности проксированного наличия опорно-двигательного аппарат или медицинской инвалидность. Эти нарушения были подтверждены путем изучения наличия диагнозов вторичных состояний, связанных со слизисто-скелетными или медицинскими нарушениями, и предыдущие исследования показали, что эти косвенные признаки связаны как с наличием, так и с тяжестью инвалидности [29].
Все анализы проводились с использованием SAS версии 9.3. Значения ≤ 0,05 считались статистически значимыми.
3. Результаты и обсуждение
3.1. Результаты: описательная статистика
Как и ожидалось, во всех случаях группы были идентичны с точки зрения соответствующих переменных: возраст, пол, регион проживания, ITT DMT и год даты индекса. При сравнении группы только РС с пациентами с РС и депрессией (таблица 1) результаты показали, что пациенты с диагнозом коморбидной депрессии значительно реже получали страхование через страхование по месту обслуживания (13,30% против 22,71%;), но значительно. с большей вероятностью будут застрахованы через предпочтительную организацию-поставщик (51.83% против 43,81%; ) или иметь «другое» страхование (4,36% против 1,83%;). Кроме того, пациенты с коморбидной депрессией реже получали доплату, связанную с их рецептом на лечение по индексу ITT (77,98% против 84,86%;). Сравнение пациентов с рассеянным склерозом только с пациентами с рассеянным склерозом и депрессией выявило значительные различия как в общем состоянии здоровья, так и в функциональных ограничениях между двумя группами, при этом пациенты с коморбидной депрессией обычно имеют более слабое здоровье. Например, пациенты с диагнозом коморбидной депрессии с меньшей вероятностью имели 0 баллов по шкале Чарлсона (62.18% против 75,92%; ) и с большей вероятностью будет иметь балл по Чарлсону 1-2 (30,28% против 21,33%;) или 3 или более (7,57% против 2,75%;). Точно так же у пациентов с коморбидной депрессией значительно чаще диагностировалось скелетно-мышечное ограничение (60,09% против 41,51%;) или медицинское ограничение (48,17% против 31,42%;).
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||



 кл. (NYHA)
кл. (NYHA) к. (NYHA)
к. (NYHA)