Периоды реабилитации после инсульта | Прогнозы
Реабилитация после перенесенного инсульта дает возможность частично вернуть утраченные навыки, потому что независимо от состояния здоровья человек не хочет быть обузой для родных. Согласно статистическим данным реабилитация после инсульта дает положительный результат в 70%.
Врачи отметили, что у больных, перенесших ишемический инсульт, реабилитационная программа дает хорошие результаты, а отличие от поражений после геморрагического инсульта.
При оценивании эффективности проводимых мероприятий учитываются:
- объем поражения тканей головного мозга;
- степень тяжести остаточных явлений;
- время начала проведения лечения.
Из-за ишемии в области поражения нервные клетки головного мозга или сдавливания гематомой отмечается безвозвратное их отмирание. Между здоровыми и отмершими имеется пограничная зона – группа клеток, которые восстанавливаются при проведении медикаментозной терапии.
Продолжительность реабилитации различна и зависит от тяжести течения заболевания и индивидуальных особенностей организма человека, перенесшего инсульт от нескольких месяцев до 3 лет.
Начальный период
Продолжительность начального периода составляет 6 месяцев. В этот период основная медикаментозная терапия дополняется ноотропными препаратами, комплексами витаминов и успокоительными средствами. С момента восстановления сознания, кроме, растираний камфорным спиртом и частых переворачиваний проводится массирование грудной клетки и пассивные движения конечностями. На третьи сутки подключается дыхательная гимнастика.
К концу первой недели больному рекомендуется сидеть и совершать активные движения конечностями. Подобранные упражнения необходимо выполнять несколько раз в день, продолжительность занятий зависит от возможностей больного. Не стоит их делать через силу. Спустя еще несколько дней врач может разрешить передвигаться.
Через 2 недели врачи разрешают посещать занятия лечебной физкультурой в зале. Подобранный комплекс упражнений выполняется медленно и плавно, при этом больному помогает в этом тренер. Он показывает правильную технику выполнения упражнений, чтобы в дальнейшем делать их самостоятельно.
Курс лечения дополняется физиотерапией
- электрофорезом со средствами, содержащими йод;
- дарсонвализацией;
- электрофорезом воротниковой зоны с никотиновой кислотой;
- динамическими токами.
Физиотерапия необходима для уменьшения выраженности болевого синдрома, снятия напряженности мышечных волокон и расширения сосудов. Проведение мануальной терапии позволяет предотвратить атрофию мышц и восстановить чувствительность.
Поздний период
Он является продолжением начального периода и может длиться до 6 месяцев. Лучшим вариантом является продолжение восстановительной терапии в условиях специализированного лечебного учреждения.
Продолжаются занятия лечебной гимнастикой с введением новых упражнений и увеличением нагрузки физиотерапия – иглорефлексотерапия, грязелечение и бальнеотерапия. Это помогает улучшить двигательную активность, доставку питательных веществ к мышцам и расслабление центральной нервной системы.
При сохранении дефекта речи проводятся занятия с логопедом. В специализированном классе обучают заново самостоятельному обслуживанию в быту. Занятия направлены на повторное обучение держанию ложки и другим навыкам, которые до удара больной мог выполнять без труда.
Реабилитация необходима для устранения апатии и депрессивных состояний, приводит к появлению воли к жизни.
Длительная реабилитация
Продолжительность проведения реабилитационных мер не ограничивается по времени. Потому как из-за индивидуальных особенностей и степени поражения в среднем восстановление утраченных навыков происходит спустя 3 года. Этого времени хватает для адаптации больных к новым условиям жизни. А родным – для налаживания быта и решения вопросов об уходе.
Потому как из-за индивидуальных особенностей и степени поражения в среднем восстановление утраченных навыков происходит спустя 3 года. Этого времени хватает для адаптации больных к новым условиям жизни. А родным – для налаживания быта и решения вопросов об уходе.
При этом больные способны обучиться мелким бытовым движениям: наливать воду в чашку, поворачивать ключ в замке и прочее. Часть больных может получить новую специальность для работы на дому.
Противопоказания
Проведение реабилитации противопоказано в следующих случаях:
- нахождение больного в коме;
- резко выраженное агрессивное поведение, обусловленное нарушением психики;
- повторный инсульт в старческом возрасте;
- тяжелое течение сахарного диабета;
- судорожный синдром;
- туберкулез;
- злокачественное новообразование.
Вероятность полного восстановления после перенесенного инсульта невысока, но не стоит опускать руки. Точное следование врачебным рекомендациям позволит достигнуть более высоких результатов.
Точное следование врачебным рекомендациям позволит достигнуть более высоких результатов.
Реабилитация после ишемического инсульта
17.06.2019
Реабилитация после ишемического инсульта
Ишемический инсульт – это резкое нарушение кровообращения участка головного мозга по причине закупорки или сужения сосудов, в результате чего происходит гибель тканей мозга. По статистике более 80% всех зарегистрированных случаев инсульта приходится на ишемический тип. В среднем 85% пациентов, перенесших ишемический инсульт, становятся инвалидами. Примерно у половины из них в течение последующих 5 лет развивается повторный инсульт.На вопросы о реабилитации после ишемического инсульта отвечает Елена Николаевна Кузнецова – врач-невролог «Моей клинки». Елена Николаевна имеет опыт работы более 30 лет, обладает обширными знаниями в области диагностики и лечения заболеваний нервной системы и осложнений патологии опорно-двигательного аппарата. Проводит реабилитацию после травм, острых нарушений мозгового и спинного кровообращения по индивидуальной программе. В Клинике ведет прием взрослых и детей с 14 лет.
Проводит реабилитацию после травм, острых нарушений мозгового и спинного кровообращения по индивидуальной программе. В Клинике ведет прием взрослых и детей с 14 лет.
— Елена Николаевна, каковы причины ишемического инсульта?
— Чаще всего причиной служит атеросклероз и закупорка артерии головного мозга тромбом. Увеличивают риск ишемического инсульта болезни сердца и сахарный диабет. Курение, злоупотребление алкоголем, постоянные стрессы, малоподвижный образ жизни, ожирение также являются факторами риска. Влияние на вероятность возникновения ишемического инсульта может оказывать и наследственность. У некоторых людей этот фактор проявляется в повышенной свертываемости крови, в результате чего они больше подвержены риску образования тромбов.
Замечу, что сейчас среди всех факторов на первый план выходят стрессы и малоподвижный образ жизни. И, к сожалению, мы все чаще сталкиваемся с инсультами у молодых людей, так как они более подвержены влиянию этих факторов.
— Каковы последствия ишемического инсульта?
— Последствия зависят от обширности поражения головного мозга. Чаще встречаются нарушения речи и двигательного аппарата: парез, слабость, потеря мелкой моторики и мимики. У многих отмечается нарушение или полная потеря зрения, когнитивные нарушения, нарушения памяти и эмоционального состояния.
— Возможно ли полное восстановление после инсульта и возвращение пациента к привычной жизни?
— Полностью восстанавливаются после инсульта лишь 16% пациентов. Остальные 80-85% выживших остаются инвалидами, полностью или частично утратившими возможность вести полноценный образ жизни.
— С чем связан такой высокий процент инвалидизации? От чего зависит, попадет пациент в эти 16% или нет?
— При инсульте происходит отмирание участков мозга вследствие того, что к ним из-за закупорки сосудов не поступает кровь. Полное восстановление поврежденных тканей, как правило, невозможно. Иногда их функцию на себя берут другие отделы мозга, в этом случае можно говорить о возможности полноценного возвращения человека к нормальной жизни.
Сроки и вероятность восстановления после инсульта всегда зависят от множества факторов. В первую очередь – это объем и локализация пораженных клеток головного мозга. Чем меньше процент поражения тканей, тем выше вероятность полного восстановления. Важным фактором являются физиологические особенности конкретного пациента: его сопутствующие заболевания, возраст и др. На первом этапе реабилитации особое значение имеет психологическое состояние человека, его настрой на выздоровление.
Еще одним значимым фактором является своевременное начало комплексной и индивидуально подобранной реабилитации. При этом восстановительные мероприятия должны начинаться уже с первых дней после инсульта. Это позволяет не только увеличить шансы пациента на улучшение физических функций, но и вовлечь его в процесс реабилитации.
— Значение имеет и то, насколько быстро пациенту оказана медицинская помощь, верно?
— Безусловно. Чем раньше пациенту с инсультом будет оказана экстренная медицинская помощь, тем большее количество клеток головного мозга удастся сохранить.
— По каким признакам можно распознать ишемический инсульт?
— Для распознавания инсульта существует простой тест под названием «рука-лицо-речь». Три слова отражают движения, которые необходимо воспроизвести человеку: поднять руки, улыбнуться и произнести фразу. После инсульта человек не сможет удерживать обе руки в перпендикулярном телу положении, одна будет падать. При улыбке одна сторона лица заметно «провиснет», появится асимметрия. Речь будет нечеткой и невнятной.
— Как в этом случае действовать? Какие меры нужно предпринять, чтобы помочь человеку?
— Первый и главный шаг – вызвать скорую помощь. Не пытаться доставить пациента в больницу самостоятельно, а дождаться приезда врачей. Пока помощь в пути, нужно уложить человека в горизонтальное положение, приподняв его голову, и поддерживать с ним контакт. Нельзя давать пациенту есть или пить, так как при инсульте часто нарушается функция глотания.
— Что происходит с пациентом после поступления в лечебное учреждение? С чего начинается его реабилитация?
— Прежде всего, пациента обследуют, чтобы определить объем поражения мозга. Для этого проводятся компьютерная или магнитно-резонансная томография. После этого начинается медикаментозное лечение, направленное на улучшение кровообращения пораженного участка мозга, снятие отека, поддержание стабильной работы сердца и пр.
Далее начинается процесс непосредственной реабилитации, которая состоит из нескольких этапов. С первых дней поступления пациента в лечебное учреждение с ним работает целый ряд врачей и специалистов: невролог, реабилитолог, массажист и др. В этот период их главная задача – запустить процесс восстановления функций организма, чтобы человек в дальнейшем смог самостоятельно обслуживать себя.
На втором этапе целью реабилитации является восстановление речи, двигательных и когнитивных функций. Для этого назначается лечебная гимнастика, массаж, физиопроцедуры, а также проводится работа с психологом и логопедом.
Для этого назначается лечебная гимнастика, массаж, физиопроцедуры, а также проводится работа с психологом и логопедом.
Восстановление мелкой моторики и навыков самообслуживания является третьим этапом реабилитации, когда пациент начинает двигаться самостоятельно. Он может длиться от нескольких месяцев до нескольких лет, в зависимости от тяжести последствий, возникших в результате инсульта.
— Примерно у половины пациентов, перенесших инсульт, в течение последующих 5 лет развивается повторное нарушение кровообращения. Как этого избежать?
— Профилактика повторного инсульта должна быть направлена на коррекцию нарушений, которые стали причиной такого состояния. Во-первых, обязательный контроль артериального давления. Регулярный прием индивидуально подобранных лекарственных препаратов позволит в будущем избегать скачков и резкого падения давления.
Необходимо соблюдать особую диету. Сбалансированное питание позволяет держать в пределах нормы холестерин и глюкозу в крови, повышенный уровень которых увеличивает риск развития сахарного диабета и образования тромбов.
Очень важна физическая активность: занятия лечебной физкультурой, прогулки на свежем воздухе, плавание и др.
— Как опытный врач, чем можете «напугать» современных молодых людей, граждан трудоспособного возраста, чтобы они задумались о проблеме раннего инсульта?
— Еще совсем недавно ишемический инсульт диагностировался у людей старше 60 лет, что было связано с возрастными изменениями сосудов. Однако сегодня это заболевание значительно помолодело. Инсульты все чаще происходят у молодых пациентов, которым едва исполнилось 30 лет. В моей практике были пациенты от 18 лет, которые перенесли острое нарушение мозгового кровообращения. Необходимо понимать, что регулярные стрессы, переутомление, общее истощение, нездоровые привычки, малоподвижный образ жизни создают все условия для развития ишемического инсульта. Он всегда приходит неожиданно и «переворачивает» жизнь человека, значительно ухудшая не только ее качество, но и продолжительность. Поэтому крайне важно позаботиться о своем здоровье вовремя.
Врачи-неврологи «Моей Клиники» осуществляют лечение неврологических заболеваний амбулаторно, в собственном стационаре и на дому.
Записаться на прием к неврологу можно по телефону 8 (912) 493-03-03 или через электронные формы обратной связи на сайте.
Что нельзя делать после перенесенного инсульта
«КВ» решили выяснить, от каких привычек стоит отказаться после перенесенного острого нарушения мозгового кровообращения. Рассказывает нам об этом руководитель отделения неврологии РКБ, врач высшей категории, заслуженный врач Татарстана Марат Хайруллов.
— Несмотря на перенесенный инсульт, многие пациенты не перестают отказываться от сигарет и алкоголя. Может ли все это вызвать болезнь повторно?
— Алкоголь после инсульта запрещен минимум на год, в дальнейшем от него стоит отказаться или существенно снизить его потребление. Во-первых, пациент должен принимать определенные препараты, многие из которых просто несовместимы со спиртным. Во-вторых, алкоголь способствует развитию атеросклеротических изменений в стенках сосудов. Соответственно, значительно повышается риск повторных нарушений мозгового кровообращения.
Во-вторых, алкоголь способствует развитию атеросклеротических изменений в стенках сосудов. Соответственно, значительно повышается риск повторных нарушений мозгового кровообращения.
О курении после инсульта стоит забыть навсегда. Оно губительно действует на стенки сосудов, вызывает спазм сосудов, повышает склонность к образованию тромбов, значительно увеличивает риск развития атеросклероза. Стенки сосудов уплотняются, просвет артерий сужается, кровоток замедляется, возрастает риск кровоизлияния в мозг.
— Марат Абдулхаевич, что еще нельзя делать после перенесенного инсульта?
— Восстановление после такого мозгового удара требует долгого времени. Особенно осторожными необходимо быть в первый год. В число факторов, способных привести к повторному приступу, входят и высокие температуры. В частности, после инсульта нельзя загорать, находиться длительное время на солнце. Можно сидеть в бане, но нельзя париться и пребывать там долго. Банные процедуры для здорового человека полезны, однако после инсульта могут навредить. Это стресс для ослабленного организма. Возможен разрыв сосудов по причине нарушения кровотока.
Это стресс для ослабленного организма. Возможен разрыв сосудов по причине нарушения кровотока.
— А можно ли после болезни летать на самолете или водить автомобиль?
— Многое зависит от обширности поражения мозга, от того, насколько успешно прошел процесс восстановления утраченных после инсульта функций. Перелеты нелегко даются даже здоровым людям. Для тех, кто перенес инсульт, перепады давления на высоте, пониженное содержание кислорода в кабине, в частности, во время взлета, попадание в зоны турбулентности опасны. Каждый конкретный случай, летать или не летать, нужно обговаривать с лечащим врачом. Если он разрешит, значит, можно, запретит — нельзя, есть основания.
Что касается вождения автомобиля. Если острота зрения, скорость реакции, активность мыслительных процессов, ясность мышления, функции мышц сохранены (опять-таки обо всем этом должен судить доктор), пациент в состоянии быстро и адекватно оценивать ситуацию на дороге, то он может сесть за руль. Но это постоянный стресс, перевозбуждение для организма, что может привести к повышению артериального давления. А гипертония с течением времени становится причиной возникновения атеросклероза, инсультов.
А гипертония с течением времени становится причиной возникновения атеросклероза, инсультов.
— Каким должно быть питание после инсульта?
— Питание прежде всего должно быть сбалансированным и здоровым. Для восстановления после инсульта организму необходимы овощи, фрукты, зелень, морепродукты, натуральные приправы (тмин, кинза, базилик). В меню необходимо включить постные супы, каши, бобовые, кисломолочные продукты, орехи и сухофрукты в небольших количествах. Для улучшения восстановления пораженных участков головного мозга важно потреблять продукты с высоким содержанием магния — бананы, свеклу, шпинат. Кроме того, пищевые волокна помогают снизить концентрацию холестерина в крови — это пшеничные отруби, тыква, овсяная каша, кабачки. Одним из главных компонентов, необходимых для восстановления, является бутилированная вода. Ограничить себя следует в потреблении солений, яиц, кофе, сахара. Запрещены консервы, копчености, некоторые полуфабрикаты, сало, грибы, жирные сорта птицы, рыбы и мяса.
Линар Вафин, генеральный директор МИБС-Казань, кандидат медицинских наук:
— Инсульт, или острое нарушение мозгового кровообращения, является второй по частоте причиной смертности людей во всем мире. Ранняя диагностика и оказание своевременной помощи могут минимизировать последствия инсульта, помочь избежать инвалидности или летального исхода. Компьютерная (КТ) и магнитно-резонансная (МРТ) томографии являются золотым стандартом в диагностике патологических изменений в головном мозге. Диагностика инсульта в первую очередь состоит в том, чтобы с помощью компьютерной томографии (КТ) убедиться в наличии или отсутствии кровоизлияния в головной мозг. Если КТ показала, что инсульт не геморрагический, то врачи начинают соответствующее лечение. Одновременно с лечением могут выполняться и другие диагностические процедуры, например МРТ-исследование, которое позволяет выявить ишемический инсульт на ранней стадии (при наличии полного пакета программного обеспечения), оценить его тяжесть и узнать другие сведения, необходимые для того, чтобы все терапевтические усилия врача направить в соответствующее русло.
Значение ЛФК в курсе реабилитации – интенсивное восстановление после инсульта
Важная часть реабилитации в программе восстановления больных с ОМНК (острыми нарушениями мозгового кровообращения) – это двигательная реабилитация, по сути — идет системное восстановление после инсульта движением, лечебной физкультурой и занятиями на специальных тренажерах. Сейчас весь комплекс физических воздействий носит название «физическая терапия» (на организм воздействуют физические факторы). И ЛФК при этом является только одной из ее частей.
Виды и формат занятий ЛФК – как должны проходить упражнения для восстановления после инсульта?
Практикуемые в большинстве учреждений групповые занятия ЛФК в программах реабилитации пациентов с ОНМК (острыми нарушениями мозгового кровообращения) не эффективны для индивидуального развития и увеличения объема возможностей конкретного пациента. Они только поддерживают определенный уровень его активности. Однако для того, чтобы восстановление после инсульта важных утраченных функций шло успешно, нужны планомерные индивидуальные занятия. Поэтому все формы работы по данному направлению в реабилитационном центре носят характер только индивидуальных упражнений для восстановления после инсульта. Виды физической терапии и ЛФК как ее части – в данном случае являются инструментами, которые инструктор, методист или врач выбирает в зависимости от того, какую задачу он решает для конкретного пациента.
Поэтому все формы работы по данному направлению в реабилитационном центре носят характер только индивидуальных упражнений для восстановления после инсульта. Виды физической терапии и ЛФК как ее части – в данном случае являются инструментами, которые инструктор, методист или врач выбирает в зависимости от того, какую задачу он решает для конкретного пациента.
При реабилитации могут использоваться методики Бобат, PNF, Войта. Сейчас есть специализированные медицинские тренажеры для восстановления после инсульта, которые помогают эти же задачи решать более успешно. Например, подвесная система, которая позволяет нивелировать действие силы тяжести и заниматься с конкретной группой мышц. Для закрепления автоматических движений (например, ходьба) можно использовать систему Мотомед, которая обеспечивает необходимый объем движений, дозированную нагрузку и помогает повысить выносливость. Вносятся в программу реабилитации и специальные упражнения для восстановления после инсульта частично парализованных конечностей. Реабилитационный центр «Спутник в Комарово» оснащен новейшими тренажерами. Здесь врач может использовать для оптимизации процесса восстановления после инсульта любые современные методики и оборудование.
Реабилитационный центр «Спутник в Комарово» оснащен новейшими тренажерами. Здесь врач может использовать для оптимизации процесса восстановления после инсульта любые современные методики и оборудование.
Инсульт лечение и восстановление, показания и противопоказания
Противопоказаний для ЛФК у больных после инсульта практически нет. Даже самым тяжелым пациентам показана лечебная физкультура. Конечно, это будут занятия не на развитие выносливости, а на поддержание работоспособности и мобильности суставов, профилактика пролежней, пневмонии и т.д.
В такой ситуации выбирается вариант пассивных занятий, но это тоже лечебная физкультура, только со щадящей и дозированной нагрузкой. Для контроля нагрузки используются такие показатели, как пульс, давление, насыщение крови кислородом. Ориентируясь на них, можно понять, достаточна или избыточна нагрузка для конкретного пациента, и выбрать оптимальный режим занятий. Инсульт, лечение и восстановление после которого всецело зависит от интенсивности занятий ЛФК буквально с первых дней реабилитации – не окончательный диагноз. За пациента даже в самом тяжелом состоянии надо бороться. Восстановление функций после инсульта будет более полным, если интенсивнее и разнообразнее будут занятия со специалистами клиники реабилитации после инсульта.
За пациента даже в самом тяжелом состоянии надо бороться. Восстановление функций после инсульта будет более полным, если интенсивнее и разнообразнее будут занятия со специалистами клиники реабилитации после инсульта.
Задачи и длительность ЛФК в программах реабилитации
ЛФК помогает убрать слабость мышц, повысить выносливость, восстановить необходимый объем движений в тех конечностях, в которых на данный момент сформировалась слабость или спастическое повышение мышечного тонуса. И длительность курса ЛФК при решении таких задач является понятием условным. Один пациент поймет, как правильно пользоваться ослабленной кистью за пять-семь занятий, а другому надо восстанавливать весь двигательный стереотип, и на это могут уйти месяцы.
По рекомендациям Всемирной организации здравоохранения активные занятия со специалистами-реабилитолагами для таких больных должны продолжаться не менее полугода.
Преимущества реабилитационного центра «Спутник в Комарово» для больных, перенесших инсульт
В пансионате созданы условия для оптимального развития реабилитационного процесса: начиная от окружающей обстановки – тишина, чистый лесной воздух, отсутствие суеты не только внутри, но и вокруг пансионата – и заканчивая специалистами, у которых есть возможность неограниченное количество времени работать с каждым пациентом индивидуально.
Не менее важна и профессиональная диагностическая аппаратура, которая дает возможность скрупулезно контролировать состояние пациента и позволяет вовремя принимать решения при появлении негативных симптомов.
Имеют значение и условия проживания, и сбалансированное питание, и грамотный сестринский уход, который способствует закреплению тех навыков, что пациенты получают, занимаясь лечебной физкультурой.
Реабилитация и восстановление после инсульта
Справки по прямому телефону центра:
Восстановление после инсульта возможно! Многолетний опыт работы реабилитационного центра «Преодоление» доказал это и лег в основу создания эффективной программы лечения. Мы возвращаем пациентам способность двигаться, говорить, выполнять бытовые задачи, справляться эмоционально с последствиями заболевания.
Инсульт — скоротечное поражение головного мозга, способное в одночасье лишить человека возможности самообслуживания. Вследствие закупорки или разрыва сосудов:
- искажается или полностью теряется речь;
- ухудшается зрение;
- резко снижается двигательная функция, ослабевают мышцы, происходит полный или частичный паралич конечностей;
- нарушаются связи нервной системы;
- страдают внимание, память, способность воспринимать и усваивать новую информацию;
- развивается постинсультная депрессия.

Видео о центре «Преодоление» → Наша команда → Фотопрогулка по центру →
Повышенный уровень стресса, эмоциональное перенапряжение, отсутствие полноценного сна и отдыха сегодня стали причинами возникновения данного заболевания у молодых людей. Реабилитация после инсульта важна как для пожилых, так и для молодых пациентов, в том числе, подростков. Ключевым моментом скорейшего восстановления является оперативность обращения за помощью: каждый день промедления усложняет последующее лечение, продлевает его срок.
Ранняя медицинская, когнитивная, социальная, физическая реабилитация после инсульта в нашем реабилитационном центре в Москве исключает период развития депрессии, связанной с утратой привычных способностей, и позволяет эффективнее мотивировать пациента на выздоровление. Кроме того, быстрое включение в схему лечения не позволяет больному привыкнуть к использованию здоровых конечностей вместо парализованных после перенесенного инсульта.
Программа восстановления после инсульта
В центре реабилитации «Преодоление» проводится индивидуальная работа с каждым пациентом. Успех лечения зависит от того, насколько точно проанализированы проблемы, возникшие после перенесенного заболевания, поэтому особое внимание мы уделяем диагностике. В зависимости от индивидуальных особенностей пациента и возможных противопоказаний к тем или иным процедурам, мультидисциплинарная бригада центра проводит коррекцию базовой программы, дополняет ее, рекомендует оптимальные сроки для полного восстановления после инсульта.
На всех этапах реабилитации в программу включаются определенные средства диагностики здоровья и оценки состояния пациента.
|
Консультации специалистов:
|
Анализы:
|
Диагностика:
|
Методы реабилитации пациентов после ишемического и геморрагического инсульта, включенные в курс нашего центра::
- Кинезиотерапия индивидуальная — 20 процедур;
- Механотерапия индивидуальная — 10 процедур;
- Гидрокинезотерапия индивидуальная — 12 процедур;
- Массаж классический — 10 процедур;
- Физиотерапия — 20 процедур;
- Баланс тренинг — 10 процедур;
- Занятия с логопедом — 8 занятий;
- Занятия с нейропсихологом — 4 занятия;
- Эрготерапия — 8 процедур;
- Социальная адаптация — 8 процедур.

В центре «Преодоление» можно пройти платную реабилитацию после инсульта на современных тренажерах для восстановления двигательной функции, силы мышц и равновесия. У нас пациент получает лечение, которое невозможно осуществить в домашних условиях и все время терапии находится под наблюдением специалистов.
Сроки реабилитации
Восстановительный период должен составлять не менее 21 дня. Наша программа рассчитана на 30 дней, в течение которых пациент проходит интенсивную терапию, направленную на возвращение ему самостоятельности, возможности ясно выражать свои мысли, быть эмоционально устойчивым к восприятию сложностей, возникших в результате болезни. При срочном обращении за помощью в реабилитационный центр (в течение 20 суток после инсульта), больной имеет большой шанс на полное восстановление и возвращение к полноценной жизни.
В процессе лечения важен комплексный подход: нельзя работать только над восстановлением речи, движением руки или ноги, улучшением памяти. Мы следим за тем, чтобы во время терапии были задействованы все системы организма: только в этом случае можно гарантировать устойчивый результат применяемой схемы лечения. Комплексная работа по восстановлению после инсульта в реабилитационном центре Москвы направлена также на предупреждение рецидива болезни. Наша задача — вернуть пациенту утраченные функции движения, речи, восприятия и вместе с тем, вселить в него уверенность, что он может продолжать полноценную жизнь, несмотря на возникшие трудности.
Мы следим за тем, чтобы во время терапии были задействованы все системы организма: только в этом случае можно гарантировать устойчивый результат применяемой схемы лечения. Комплексная работа по восстановлению после инсульта в реабилитационном центре Москвы направлена также на предупреждение рецидива болезни. Наша задача — вернуть пациенту утраченные функции движения, речи, восприятия и вместе с тем, вселить в него уверенность, что он может продолжать полноценную жизнь, несмотря на возникшие трудности.
Где пройти реабилитацию после инсульта в Москве
В центре «Преодоление» пациентов встречают квалифицированные специалисты-реабилитологи. Здесь созданы все условия для эффективного и комфортного прохождения курса лечения. Индивидуальная работа позволяет обратить внимание на каждый нюанс в состоянии больного и сразу внести необходимые корректировки в программу, уменьшить или увеличить интенсивность терапии. Стоимость реабилитации после инсульта включает цены на все применяемые в программе процедуры, анализы и консультации. Бесплатная помощь, предоставляемая по полису в рамках ОМС, не всегда позволяет составить полноценную программу с применением всех возможностей центра. В этом случае по завершению терапии рекомендуется обратить внимание на динамику восстановления, достигнутые результаты и при необходимости продолжить реабилитацию.
Бесплатная помощь, предоставляемая по полису в рамках ОМС, не всегда позволяет составить полноценную программу с применением всех возможностей центра. В этом случае по завершению терапии рекомендуется обратить внимание на динамику восстановления, достигнутые результаты и при необходимости продолжить реабилитацию.
Не сомневайтесь и не ждите, пока последствия инсульта укоренятся! Обращайтесь за помощью сразу, как это станет возможным, подарив близкому человеку шанс на быстрое восстановление.
По всем вопросам звоните
Восстановление после инсульта
ПОКАЗАНИЯ ДЛЯ ПРОВЕДЕНИЯ РЕАБИЛИТАЦИИ ПОСЛЕ ИНСУЛЬТА
- нарушение двигательных функций
- координаторные нарушения
- речевые нарушения
РЕАБИЛИТАЦИЯ ПОСЛЕ ИНСУЛЬТА В РКМЦ
В нашем Центре мы обеспечиваем индивидуальное мультидисциплинарное сопровождение на каждом этапе реабилитации пациентов, перенесших нарушение кровообращение головного мозга.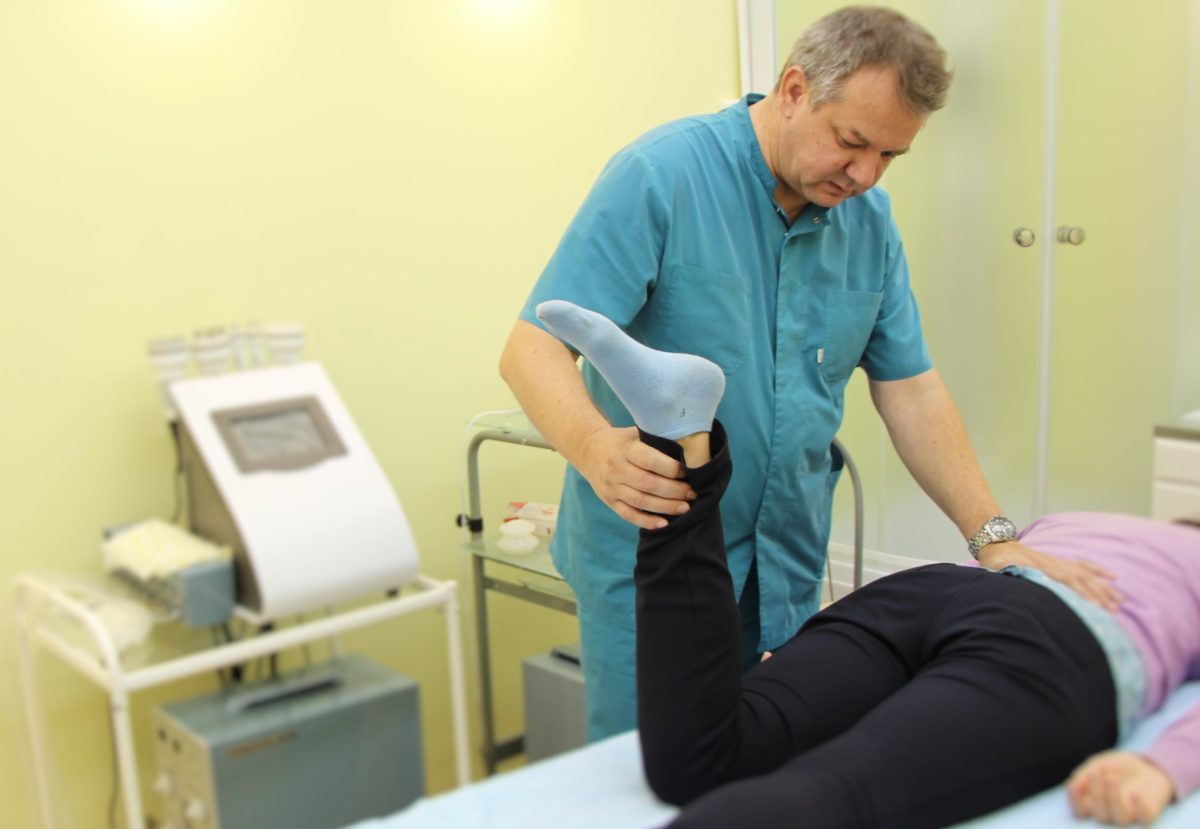 Неограниченные возможности для нейродвигательной реабилитации обеспечивают нам возможность начать процесс восстановления в максимально ранние сроки, начиная с отделения интенсивной терапии.
Неограниченные возможности для нейродвигательной реабилитации обеспечивают нам возможность начать процесс восстановления в максимально ранние сроки, начиная с отделения интенсивной терапии.
Инновационный стол-вертиклизатор Erigo Pro (Hocoma, Швейцария) с интегрированным роботизированным устройством и встроенной синхронизированной функцией электростимуляции мышц нижних конечностей обеспечивает поддержание нормальной жизнедеятельности организма лежачего больного. Возможность ранней вертикализации позволяет нормализовать кровообращение, предупредить возникновение пролежней, застойных явлений в легких и пневмоний, тромбоза вен нижних конечностей, мышечной спастики и контрактуры суставов.
Следующая задача — восстановление нарушенных функций и способностей. На каждом этапе восстановления с пациентом работают опытные специалисты по физической реабилитации.
На ранних этапах важно сохранить движения в суставах конечностей, предупредить развитие контрактур. С этой целью проводится пассивная гимнастика, которую сочетают с лечением положением, пассивной имитацией ходьбы, дыхательными упражнениями и массажем конечностей.
С этой целью проводится пассивная гимнастика, которую сочетают с лечением положением, пассивной имитацией ходьбы, дыхательными упражнениями и массажем конечностей.
В дальнейшем приступают к тренировке активных движений, обучению поддержания положения сидя.Устранение двигательных и координаторных нарушений проводится на новейшем оборудовании с применением технологий биологической обратной связи. Уникальные многофункциональные реабилитационные тренажеры Amadeo, Tymo, Pablo (Tyromotion GmbH, Австрия) для оценки и коррекции нарушений моторики верхних и нижних конечностей, туловища. Тренировки осуществляются при помощи интерактивных программ, что обеспечивает поддержание внимания, когнитивных функций и мотивации.
В восстановлении двигательных функций и бытовых навыков мы применяем также такие методы, как эрготерапия и зеркальная терапия.
Важной задачей после инсульта является восстановление навыков ходьбы. Пациенты поэтапно обучаются поддерживать положение стоя, восстанавливать правильную походку. Система с беговой дорожкой для обучения навыкам ходьбы с разгрузкой веса H/P/COSMOS Robowalk expander (HPCOSMOS, Германия) позволяет ускорить процесс восстановления двигательных функций.
Пациенты поэтапно обучаются поддерживать положение стоя, восстанавливать правильную походку. Система с беговой дорожкой для обучения навыкам ходьбы с разгрузкой веса H/P/COSMOS Robowalk expander (HPCOSMOS, Германия) позволяет ускорить процесс восстановления двигательных функций.
Дополнительным эффективным доступным нам методом в реабилитации является кинезиотейпирование. Коррекция мышечного тонуса с помощью эластичных, наклеиваемых на кожу, хлопковых лент способствует восстановлению функции пораженных конечностей.
Не менее важна психологическая и социальная адаптация пациентов, перенесших инсульт. Эту задачу решают опытные психологи, психотерапевты, логопед на каждом реабилитационном этапе.
На поздних сроках реабилитации проводится восстановительная гимнастика в воде. Бассейн в отделении реабилитации и физиотерапии оборудован специальным подъемником для комфорта и безопасности пациентов с ограниченными возможностями, а также водными тренажерами.
Также в поздние сроки восстановления применяется широкий спектр физиотерапевтического воздействия, бальнеолечения, массаж, рефлексотерапия.
ПРОТИВОПОКАЗАНИЯ
Тяжелое состояние пациента.
КАК ПРОЙТИ РЕАБИЛИТАЦИЮ ПОСЛЕ ИНСУЛЬТА В РКМЦ
С целью восстановительного лечения и реабилитации возможна госпитализация пациентов в неврологическое отделение нашего Центра. (Госпитализация осуществляется по согласованию с заведующей неврологическим отделением Чечик Натальей Михайловной).
Для этого нужно:
- Позвонить в Контакт-центр для записи на прием к заведующей неврологическим отделением
- Прийти на прием в назначенное время с имеющимися у вас медицинскими документами.
- В день госпитализации в регистратуре заключить договор на оказание платных услуг
- Оплатить счет в кассе РКМЦ или через ЕРИП
Что делать, если у вас инсульт? Невролог составил простую инструкцию, которая может вас спасти
За год в Беларуси инсульт случается более чем у 30 000 человек. Только 10% из них возвращаются к обычной жизни. Врач-невролог Сергей Марченко рассказывает, как определить инсульт и что нужно делать, пока еще не поздно.
Только 10% из них возвращаются к обычной жизни. Врач-невролог Сергей Марченко рассказывает, как определить инсульт и что нужно делать, пока еще не поздно.
Что такое вообще инсульт?
– Это острое нарушение кровообращения в головном мозге, которое всегда является вторичным заболеванием. У здоровых людей оно не возникает.
По механизму нарушения кровообращения инсульты разделяют на ишемические (около 85% всех инсультов) и геморрагические. В первом случае сосуд закупоривается тромбом (эмболом), во втором – сосуд разрывается. Деление инсультов по степени тяжести тоже есть, но даже нетяжелый инсульт – это смертельно опасное заболевание.
Симптомы у этих типов одни и те же?
Симптомы инсульта зависят от локализации в мозге, а не от того, какой именно это инсульт. Если нарушено кровообращение в центре речи, пострадает речь, в двигательном центре – нарушатся движения в руке и (или) ноге.
Как понять, что у человека инсульт?
Для выявления инсульта придуман очень простой тест, который рекомендуют все национальные и международные протоколы. Он называется «Лицо, рука, речь, время», и на его основании сотрудники бригады скорой помощи имеют право ставить диагноз «инсульт».
Он называется «Лицо, рука, речь, время», и на его основании сотрудники бригады скорой помощи имеют право ставить диагноз «инсульт».
Лицо: просят пациента улыбнуться или показать зубы. При инсульте происходит заметная асимметрия лица (угол рта с одной стороны «висит»).
Рука: просят пациента поднять и удерживать в течение 5 секунд обе руки на 90° в положении сидя и на 45° в положении лежа. При инсульте одна из рук опускается.
Речь: просят пациента сказать простую фразу. При инсульте у пациента не получается четко и правильно выговорить простую фразу, речь его неразборчива, невнятна.
При наличии хотя бы одного симптома, свидетельствующего о развитии инсульта, необходимо срочно вызвать «скорую» – чем раньше будет оказана помощь, тем больше шансов на восстановление.
Время: очень важно выяснить, когда случился инсульт. Нужно спросить у человека, когда он или окружающие впервые заметили эти нарушения. Если человек не может вспомнить, когда впервые заметил симптомы, мы спрашиваем его близких, когда те в последний раз видели его без них.
Если человек не может вспомнить, когда впервые заметил симптомы, мы спрашиваем его близких, когда те в последний раз видели его без них.
Есть понятие «терапевтическое окно» – время, когда можно попытаться полностью восстановить кровообращение. Оно относится к ишемическим типам инсультов, ведь, когда сосуд рвется, нужно не восстанавливать кровоток, а останавливать кровотечение и убирать гематому.
Длительность «терапевтического окна» – не больше 6 часов. Первые четыре с половиной часа закупорку сосуда можно вылечить и медикаментами (т.е. применив тромболизис), и эндоваскулярными способами (применив тромбэкстракцию) – то есть с помощью специальных устройств, которые проводят в артерии головного мозга и извлекают тромб механическим путем. В промежутке 4,5–6 часов возможно только эндоваскулярное лечение.
Успех лечения инсульта целиком и полностью зависит от времени обращения за медицинской помощью. К сожалению, если симптомы не очень ярко выражены, люди часто ждут, когда все само пройдет, а оно не проходит, и иногда становится только хуже.
А я могу по этому тесту определить инсульт у себя?
Конечно. Если вы понимаете, что с вами что-то не так, вы всегда можете улыбнуться себе в зеркало и посмотреть, насколько симметрична улыбка, оценить свою речь, попробовать удержать обе руки. Но все-таки чаще всего инсульты, конечно, диагностируют кому-то. Родственники видят, что с человеком что-то не то.
Когда случается инсульт, что в этот момент происходит с человеком? Он падает в обморок, резко ухудшается состояние?
Возможны все варианты. При закупорке крупного сосуда человек может и сознание потерять, потому что перестает снабжаться кислородом крупный участок мозга. Если сосуд маленький, симптомы могут быть малозаметными, но постепенно становятся более выраженными.
При инсульте должны быть все эти симптомы?
Нет. Симптомы могут быть и все вместе, и какой-то один из них: все зависит от того, насколько крупный сосуд и какая часть мозга пострадали. К тому же важно помнить еще такие нюансы: в тесте говорится только про руку, но слабость может быть и в ноге, у человека могут появиться расстройства координации.
К тому же важно помнить еще такие нюансы: в тесте говорится только про руку, но слабость может быть и в ноге, у человека могут появиться расстройства координации.
Главное: если у вас внезапно изменилось состояние, не ждите, а сразу обращайтесь за помощью! Это касается не только инсульта, в медицине очень многое зависит от времени: сложно успешно лечить хирургическую патологию, когда боль в животе длится неделю, а кардиологам – инфаркт миокарда при длительности болевого синдрома более 24 часов.
С чем можно перепутать инсульт?
С болезнями, которые вызывают такие же симптомы. Это может быть и опухоль, и травма, и инфекционное поражение мозга (энцефалит, менингит). Все эти болезни опасны, и их в любом случае нужно лечить, а не ждать, пока само пройдет.
Такие симптомы, скорее всего, сами не исчезнут. И даже если они пропадут, к врачу идти обязательно. Есть понятие «преходящее нарушение мозгового кровообращения» – когда неврологические симптомы возникают, но быстро проходят, потому что кровообращение восстанавливается самостоятельно в течение суток. Это тоже очень грозное состояние, предвестник полноценного инсульта.
Это тоже очень грозное состояние, предвестник полноценного инсульта.
А можно ли не заметить инсульт?
Можно. Мозг отвечает за все в нашем организме, но при этом имеет функционально незначимые зоны: если инсульт случится в одной из них, симптомы будут малозначительны либо и вовсе незаметны. Такой инсульт часто обнаруживают уже в виде застарелых изменений на томограммах головного мозга.
Как мне помочь человеку, у которого инсульт?
Вызвать скорую помощь – набрав 103. Уже после уложить его с приподнятым на 30–45 градусов корпусом, обеспечить проходимость дыхательных путей, освободив шею от одежды и очистив полость рта от рвотных масс и инородных предметов, в том числе съемных зубных протезов, в случае бессознательного состояния пациента его необходимо повернуть на бок для профилактики попадания в дыхательные пути слюны, рвоты.
Никакую другую помощь оказывать не стоит: не снижать давление, не давать лекарств. Лечение инсульта зависит от его типа, а установить его может только врач.
Лечение инсульта зависит от его типа, а установить его может только врач.
А что делать, если у меня инсульт с нарушениями речи, а рядом никого нет?
Если они незначительные, старайтесь сделать все, чтобы диспетчер скорой медицинской помощи понял, что вы хотите. Если не получается, попробуйте написать кому-нибудь из знакомых, попросите вызвать вам «скорую».
Что делать, если инсульт у человека случился вдали от города?
Все равно нужно вызывать скорую медицинскую помощь. У нас вся страна разделена на зоны обслуживания, за любым местом закреплена подстанция скорой помощи, откуда должна приехать бригада и оказать помощь.
Если это совсем глухомань и вы понимаете, что туда ехать будут очень долго, есть смысл погрузить человека в машину и доехать до ближайшего населенного пункта или больницы.
Сейчас в Беларуси идет активная работа по организации региональных сосудистых центров, которые предназначены для оказания помощи пациентам, находящимся примерно в 70-километровой зоне, где должны будут современными способами лечить и инсульты, и инфаркты.
Чем обычно заканчивается инсульт?
Смертью, инвалидностью или выздоровлением. Статистика исходов инсульта не меняется десятилетиями: 20–30% пациентов умирают в течение года, около 60% остаются инвалидами различных групп и только примерно 10% возвращаются к обычной жизни.
Если бы наши сограждане начали обращаться за помощью своевременно, меньше людей оставались бы инвалидами.
Около 60% пациентов с инсультами, к которым применяли тромболизис или тромбоэкстракцию, выписываются из больницы либо вообще без нарушений, либо с минимальными – это без учета реабилитационного периода. Именно поэтому я так радею за своевременное обращение к врачам: у нас есть все для лечения – знания, навыки и техника.
А какими именно бывают последствия инсульта?
Чаще всего последствия – это симптомы, от которых не удалось избавиться во время лечения и реабилитации. Они зависят от размера инсульта и его расположения. Сразу предсказать исход инсульта в большинстве случаев сложно.
А бывают ли последствия со стороны психики?
Конечно, они могут быть, и более того, они часто встречаются. Инсульт – это повреждение мозга, тут даже логические цепочки строить не надо. Например, люди с нарушением речи порой становятся напряженными и чрезмерно активными из-за того, что их не понимают, что они не могут высказать свою мысль. Увы, бывает, люди становятся и неадекватными.
От чего зависит восстановление?
Во-первых, от времени обращения пациента, от того, удалось ли нам восстановить кровоток до гибели большого участка мозга. Когда сосуд перекрывается тромбом (эмболом), участок мозга, который кровоснабжается только этим сосудом, в любом случае погибает (совсем без кислорода мозг живет всего 5-6 минут) – это «ядро инсульта». Окружающие «ядро» участки мозга, имеющие смежное кровоснабжения не только из пострадавшего сосуда, будут испытывать кислородное голодание. И если мы вовремя восстановим кровоток, то они вернутся в обычное состояние и эти участки мозга останутся здоровыми.
Во-вторых, от диаметра закупоренного сосуда: чем он больше, тем больше инсульт, тяжелее симптоматика и лечение.
В «терапевтическое окно» обращается только 30% заболевших, и половина – пациенты с кровоизлиянием в мозг, которых лечат совсем по-другому, к которым тромболизис неприменим. Из этих 30% за 2017 год тромболизис и (или) тромбоэкстракцию удалось применить всего лишь в 4,2% случаев, то есть у каждого восьмого. Остальные лечатся как обычно, к ним не применяют эти современные методы: приезжают они вовремя, но мы находим противопоказания. В таких случаях, увы, кровоток восстановить не получается: люди либо погибают, либо остаются инвалидами.
Что мне делать, чтобы полностью восстановиться?
Вовремя приехать в больницу, удачно пролечиться и активно реабилитироваться. В реабилитацию входят прием лекарств, лечебная физкультура по рекомендации специалиста, посещение логопеда и т.д. Кстати, эффективность восстановления очень повышает поддержка и помощь близких. Как именно вы можете помочь, вам скажет и покажет лечащий врач, главное – заниматься с болеющим.
Как именно вы можете помочь, вам скажет и покажет лечащий врач, главное – заниматься с болеющим.
После инсульта обязательно ли идти к психотерапевту?
Лечить нужно все, что нуждается в лечении, любое отклонение в состоянии здоровья. Если у человека после инсульта сформировались нарушения, которые не прошли, с ними не нужно свыкаться – это касается и психики.
Есть ли вероятность, что инсульт снова повторится?
К сожалению, у тех, кто перенес инсульт, риск возникновения еще одного увеличивается во много раз, особенно в первый год. Дальше риск уменьшается, но все равно остается высоким. По данным различных публикаций, повторный инсульт возникает у 30–50% пациентов.
Обязательно после лечения соблюдать меры вторичной профилактики инсульта – это прием лекарств, у многих на пожизненной основе, качественное изменение образа жизни, контроль болезни, которая привела к инсульту.
А что мне делать, чтобы инсульта и в первый раз не было?
Быть здоровым. Только, к сожалению, с годами это не получается, поэтому первичная профилактика – своевременное выявление хронических и других заболеваний, которые могут привести к инсульту. Для этого у нас в стране хорошо продумана система диспансеризации: для каждого возраста разработан план обследований, который позволяет исключить болезни, характерные для него. Это бесплатно и доступно, главное – дойти до поликлиники, выполнить назначенные обследования, завершить все осмотрами необходимых специалистов. Кроме инсульта существует много других опасных болезней, и их все нужно лечить.
Только, к сожалению, с годами это не получается, поэтому первичная профилактика – своевременное выявление хронических и других заболеваний, которые могут привести к инсульту. Для этого у нас в стране хорошо продумана система диспансеризации: для каждого возраста разработан план обследований, который позволяет исключить болезни, характерные для него. Это бесплатно и доступно, главное – дойти до поликлиники, выполнить назначенные обследования, завершить все осмотрами необходимых специалистов. Кроме инсульта существует много других опасных болезней, и их все нужно лечить.
Если нет проблем со здоровьем, нужно исключить курение, злоупотребление алкоголем, начать больше двигаться и правильно питаться.
Какие болезни вызывают инсульт?
Болезни, которые встречаются у подавляющего большинства пациентов с инсультом, – это артериальная гипертензия, атеросклероз сосудов головного мозга, нарушение ритма сердца, сахарный диабет. Курение, употребление алкоголя, лишний вес, малоподвижный образ жизни – все это будет способствовать инсульту.
А что чаще всего «запускает» инсульт?
Далеко не всегда можно сказать, из-за чего случился инсульт. Организм может долго приспосабливаться к изменениям, пока они не превышают лимит его возможностей. Атеросклеротическая бляшка может долго расти, но рано или поздно она перекрывает сосуд или, если она нестабильна, отрывается от стенки и перекрывает его.
Чаще всего «спусковым крючком» является скачок артериального давления.
Зависит ли инсульт от наследственности?
Если у бабушки был инсульт, не обязательно, что он будет и у вас. Но бывает наследственная предрасположенность к хроническим болезням, которые становятся причиной инсульта. Если гипертония есть у вашей мамы, скорее всего, она будет и у вас.
Зависит ли болезнь от возраста?
Инсульт случается преимущественно у людей пожилого возраста, тех, кто вышел на пенсию. Но в последние годы отмечается увеличение доли пациентов трудоспособного возраста, современные диагностические возможности позволяют чаще выявлять эту болезнь у молодых людей.
Абсолютные и относительные противопоказания к внутривенному введению rt-PA при остром ишемическом инсульте
Abstract
Большинство противопоказаний к внутривенному (внутривенному) введению рекомбинантного тканевого активатора плазминогена (rtPA) возникли в качестве критериев исключения в крупных испытаниях по инсульту. Они были получены на основе консенсуса экспертов в исследовании Национального института неврологических расстройств и инсульта (NINDS). Несмотря на то, что безопасность и эффективность внутривенного введения rtPA неоднократно подтверждались в крупных международных обсервационных исследованиях за последние 20 лет, большинство пациентов с острым ишемическим инсультом, к сожалению, все еще не получают тромболитического лечения.Некоторые из исходных критериев исключения оказались излишне ограничивающими в реальной клинической практике. Было высказано предположение, что применение ослабленных критериев исключения может увеличить скорость внутривенного тромболизиса до 20% с результатами, сопоставимыми с тромболизисом с более традиционными критериями. Мы рассматриваем абсолютные и относительные противопоказания к внутривенному введению rtPA при остром ишемическом инсульте, обсуждая основную причину и доказательства, подтверждающие эти критерии исключения.
Мы рассматриваем абсолютные и относительные противопоказания к внутривенному введению rtPA при остром ишемическом инсульте, обсуждая основную причину и доказательства, подтверждающие эти критерии исключения.
Ключевые слова: острый инсульт, тромболитическая терапия, тканевой активатор плазминогена, противопоказания
Абсолютные противопоказания
Острое внутричерепное кровоизлияние
Обнаружение внутричерепного кровоизлияния (ВЧК) при визуализации головного мозга является абсолютным противопоказанием для внутривенного введения рекомбинантных изображений головного мозга. тканевый активатор плазминогена (rtPA) при остром ишемическом инсульте в последних рекомендациях Американской кардиологической ассоциации (AHA) и на этикетке препарата Activase (alteplase, rtPA) (Genentech, Inc.). 1 Это включает внутрипаренхимальное кровоизлияние, субарахноидальное кровоизлияние, внутрижелудочковое кровоизлияние, эпидуральную гематому, субдуральную гематому или геморрагическую конверсию инфаркта. Нет опубликованных отчетов или исследований, оценивающих безопасность внутривенного введения rtPA в таких условиях, поскольку риски явно перевешивают любые потенциальные преимущества.
Нет опубликованных отчетов или исследований, оценивающих безопасность внутривенного введения rtPA в таких условиях, поскольку риски явно перевешивают любые потенциальные преимущества.
История ICH
Как в руководстве AHA, 2013 г., так и на этикетке препарата Activase (альтеплаза, rtPA) считается, что наличие ICH в анамнезе является абсолютным противопоказанием. 1 Имеется мало данных о рисках лизиса в этой популяции, и они, вероятно, значительно варьируются в зависимости от индивидуальных характеристик пациента. Несколько случаев опубликованы в крупных обзорах пациентов, получавших тромболизис «не по назначению». В одном обзоре с участием 499 пациентов у 3 в анамнезе был ВЧГ. 2 Ни у одного из этих пациентов не было симптоматического ICH (sICH) после тромболизиса. Двое из них достигли благоприятного функционального результата через 3 месяца. 2 В другом исследовании, в котором рассматривались 135 пациентов, которые лечились rtPA, несмотря на формальные противопоказания, у 3 пациентов в анамнезе имелась ВЧГ, а у одного из них была sICH. 3 Риск внутривенного введения rtPA у пациентов с вероятным ICH в анамнезе варьируется в зависимости от нескольких индивидуальных факторов, включая (1) время, прошедшее с момента ICH, (2) причину предшествующей ICH и было ли проведено окончательное лечение (например, клипирование или намотка аневризмы или артериовенозной мальформации [АВМ]), (3) хирургическая эвакуация гематомы и (4) объем остаточной энцефаломаляции. Мы думаем, что при некоторых обстоятельствах может быть разумным введение rtPA внутривенно, но соотношение пользы и риска следует оценивать на индивидуальной основе.
3 Риск внутривенного введения rtPA у пациентов с вероятным ICH в анамнезе варьируется в зависимости от нескольких индивидуальных факторов, включая (1) время, прошедшее с момента ICH, (2) причину предшествующей ICH и было ли проведено окончательное лечение (например, клипирование или намотка аневризмы или артериовенозной мальформации [АВМ]), (3) хирургическая эвакуация гематомы и (4) объем остаточной энцефаломаляции. Мы думаем, что при некоторых обстоятельствах может быть разумным введение rtPA внутривенно, но соотношение пользы и риска следует оценивать на индивидуальной основе.
Использование последовательностей, взвешенных по чувствительности, в магнитно-резонансной томографии (МРТ) увеличило обнаружение бессимптомных церебральных микрокровоизлияний. В исследованиях инсульта без тромболизиса количество микрокровоизлияний коррелирует с частотой ICH, 4 , но наличие известных микрокровоизлияний не является противопоказанием для внутривенного введения rtPA. Одно крупное многоцентровое исследование объединило анализ данных МРТ пациентов, получавших тромболизис внутривенно. 5 Всего 242 микрокровоизлияния было идентифицировано с помощью изображений, взвешенных по T2 *, у 86 (15%) из 570 пациентов.Доля пациентов с sICH была выше среди пациентов с микрокровоизлиянием (5,8%) по сравнению с пациентами без микрокровоизлияний (2,7%), но эта разница не была статистически значимой. 5 Принимая во внимание имеющиеся данные, нельзя отказывать пациентам в внутривенном введении rtPA из-за микрокровоизлияний, обнаруженных на МРТ.
Одно крупное многоцентровое исследование объединило анализ данных МРТ пациентов, получавших тромболизис внутривенно. 5 Всего 242 микрокровоизлияния было идентифицировано с помощью изображений, взвешенных по T2 *, у 86 (15%) из 570 пациентов.Доля пациентов с sICH была выше среди пациентов с микрокровоизлиянием (5,8%) по сравнению с пациентами без микрокровоизлияний (2,7%), но эта разница не была статистически значимой. 5 Принимая во внимание имеющиеся данные, нельзя отказывать пациентам в внутривенном введении rtPA из-за микрокровоизлияний, обнаруженных на МРТ.
Тяжелая неконтролируемая гипертензия
Неконтролируемая гипертензия до значений, превышающих систолическое давление 185 мм рт. 1 Вероятно, это получено из критерия исключения для исследований Национального института неврологических расстройств и инсульта (NINDS). 6 Взаимосвязь между артериальным давлением (АД), антигипертензивной терапией и клиническими исходами при остром инсульте сложна. В нескольких исследованиях артериальная гипертензия была связана с повышенным риском неблагоприятных исходов и ICH. 7–9 В регистре безопасного проведения лечения инсульта (SITS) более высокое систолическое АД (САД) после лизиса было независимо связано с худшими исходами и повышенным риском ICH. 7 Связь между САД и sICH была линейной, тогда как связь между САД и клиническим исходом была U-образной. В ретроспективном анализе исследования NINDS антигипертензивная терапия, назначенная с до тромболизиса , не была связана с различиями в результатах. Однако у пациентов с артериальной гипертензией, получавших антигипертензивные препараты после рандомизации , вероятность благоприятного исхода через 3 месяца была ниже. 10
В нескольких исследованиях артериальная гипертензия была связана с повышенным риском неблагоприятных исходов и ICH. 7–9 В регистре безопасного проведения лечения инсульта (SITS) более высокое систолическое АД (САД) после лизиса было независимо связано с худшими исходами и повышенным риском ICH. 7 Связь между САД и sICH была линейной, тогда как связь между САД и клиническим исходом была U-образной. В ретроспективном анализе исследования NINDS антигипертензивная терапия, назначенная с до тромболизиса , не была связана с различиями в результатах. Однако у пациентов с артериальной гипертензией, получавших антигипертензивные препараты после рандомизации , вероятность благоприятного исхода через 3 месяца была ниже. 10
Результаты других исследований показывают, что исходное АД не является независимым предиктором ВЧГ или неблагоприятных исходов. 11–13 В 1 исследовании с участием 351 пациента, получавшего rtPA, более высокое САД перед лечением было связано с худшими показателями реканализации, но САД не было независимо связано с исходом. 12 У пациентов, получавших rtPA из раннего опыта в районе Кливленда, не было существенной разницы в доле с тяжелой гипертензией между пациентами с sICH и без. 14 Тяжелая гипертензия не должна препятствовать лечению внутривенным введением rtPA пациентов с острым инсультом, при условии, что ее можно контролировать с помощью гипотензивных препаратов.Использование гипотензивных средств для достижения контроля АД у пациентов до rtPA представляется безопасным.
12 У пациентов, получавших rtPA из раннего опыта в районе Кливленда, не было существенной разницы в доле с тяжелой гипертензией между пациентами с sICH и без. 14 Тяжелая гипертензия не должна препятствовать лечению внутривенным введением rtPA пациентов с острым инсультом, при условии, что ее можно контролировать с помощью гипотензивных препаратов.Использование гипотензивных средств для достижения контроля АД у пациентов до rtPA представляется безопасным.
Серьезная травма головы или инсульт в предыдущие 3 месяца
Руководящие принципы AHA и этикетка препарата от 2013 года рассматривают значительную травму головы или инсульт в течение предшествующих 3 месяцев как критерии исключения для внутривенного введения rtPA при остром инсульте. 1 Посттравматический инфаркт головного мозга регистрируется у 2–10% пациентов с тяжелой травмой головы, но назначение тромболитиков этой группе населения вызывает беспокойство.Пациенты с травмами часто имеют коагулопатию. Системные травмы и переломы могут увеличить риск системных геморрагических осложнений. Ушибы головного мозга, переломы черепа, диффузное повреждение аксонов и травматический ICH могут увеличить риск ICH. В небольшом обзоре пациентов, получавших лечение с нарушением протокола, 1 пациент прошел лечение внутривенным тромболизисом через 3 недели после перенесенной тяжелой травмы головы и получил смертельный sICH. 15 Два крупных европейских ретроспективных исследования пациентов, получавших rtPA внутривенно не по назначению, включали очень небольшое количество пациентов с недавней травмой головы, но не сообщалось никаких подробностей, специфичных для этой популяции. 16,17 Хотя данные крайне ограничены, мы считаем этот критерий исключения разумным, поскольку риски в этой настройке, вероятно, чрезмерно высоки.
Системные травмы и переломы могут увеличить риск системных геморрагических осложнений. Ушибы головного мозга, переломы черепа, диффузное повреждение аксонов и травматический ICH могут увеличить риск ICH. В небольшом обзоре пациентов, получавших лечение с нарушением протокола, 1 пациент прошел лечение внутривенным тромболизисом через 3 недели после перенесенной тяжелой травмы головы и получил смертельный sICH. 15 Два крупных европейских ретроспективных исследования пациентов, получавших rtPA внутривенно не по назначению, включали очень небольшое количество пациентов с недавней травмой головы, но не сообщалось никаких подробностей, специфичных для этой популяции. 16,17 Хотя данные крайне ограничены, мы считаем этот критерий исключения разумным, поскольку риски в этой настройке, вероятно, чрезмерно высоки.
Предполагается, что пациенты с острым инсультом, недавно перенесшие ишемический инсульт в течение предыдущих 3 месяцев, подвержены более высокому риску ВЧГ при внутривенном введении rtPA. Эти пациенты были исключены из исторического исследования NINDs. 6 Эффективность и безопасность в таких ситуациях в значительной степени неизвестны и, вероятно, сильно различаются с учетом индивидуальных характеристик, таких как размер и механизм перенесенного инфаркта, возраст и тяжесть повторного инсульта.Редко сообщалось о случаях, когда пациенты получали rtPA внутривенно по поводу инсульта дважды в течение 3 месяцев. В одном отчете подробно описывается пациент, который успешно лечился второй дозой (уменьшенной до 50 мг) внутривенного введения rtPA через 90 часов после первой дозы после повторной окклюзии артерии. У этого пациента исход благоприятный. 18 При периоде полужизни в плазме α, составляющем приблизительно 5 минут, rtPA быстро выводится из кровотока при нормальных метаболических условиях. 18 Повторный внутривенный тромболизис может быть целесообразным в некоторых случаях, особенно при небольшом объеме перенесенного инфаркта, но риски неизвестны.
Эти пациенты были исключены из исторического исследования NINDs. 6 Эффективность и безопасность в таких ситуациях в значительной степени неизвестны и, вероятно, сильно различаются с учетом индивидуальных характеристик, таких как размер и механизм перенесенного инфаркта, возраст и тяжесть повторного инсульта.Редко сообщалось о случаях, когда пациенты получали rtPA внутривенно по поводу инсульта дважды в течение 3 месяцев. В одном отчете подробно описывается пациент, который успешно лечился второй дозой (уменьшенной до 50 мг) внутривенного введения rtPA через 90 часов после первой дозы после повторной окклюзии артерии. У этого пациента исход благоприятный. 18 При периоде полужизни в плазме α, составляющем приблизительно 5 минут, rtPA быстро выводится из кровотока при нормальных метаболических условиях. 18 Повторный внутривенный тромболизис может быть целесообразным в некоторых случаях, особенно при небольшом объеме перенесенного инфаркта, но риски неизвестны.
Тромбоцитопения и коагулопатия
Тромбоцитопения
Хотя нет необходимости ждать подсчета тромбоцитов перед внутривенным введением rtPA, если нет подозрения на тромбоцитопению, количество тромбоцитов <100000 / мм 3 является противопоказанием для внутривенного введения rtPA в соответствии с рекомендациями AHA и вкладышем по лекарствам. 1 Геморрагические осложнения у пациентов с тромбоцитопенией, получающих rtPA внутривенно, не оценивались ни в проспективном, ни в рандомизированном исследовании.Из 14 306 пациентов из нескольких исследований, только приблизительно 20 пациентов с тромбоцитами <100 000 мм 3 , получавших rtPA внутривенно по поводу инсульта, были описаны подробно. 2,3,19,20 Из них только у 1 пациента был зарегистрирован sICH, но чрезвычайно небольшое количество опубликованных случаев не позволяет сделать однозначных выводов о безопасности внутривенного тромболизиса в этом случае.
Коагулопатия
Точно так же мало данных об эффективности или безопасности внутривенного введения rtPA при остром инсульте в условиях аномальных тестов на коагуляцию. Риск всех типов кровотечений может повышаться при внутривенном введении rtPA, если пациенту вводят системную антикоагулянтную терапию. Наличие активного кровоточащего диатеза или коагулопатии является противопоказанием к внутривенному введению rtPA для лечения острого ишемического инсульта. 1 Подозрение на коагулопатию обычно связано с антикоагулянтной терапией. Другие потенциальные причины включают цирроз печени, терминальную стадию почечной недостаточности, гематологические злокачественные новообразования, дефицит витамина К, сепсис и синдром антифосфолипидных антител.Кардиологи обнаружили ранний успех многогранного подхода к лечению острой окклюзии коронарных артерий путем сочетания антикоагуляции с системным фибринолизом, хотя более высокие значения активированного частичного тромбопластинового времени (АЧТВ) (и более высокие дозы гепарина) были связаны с более высокими показателями ICH. 21 Данных о пациентах с инсультом с длительным АЧТВ, которые лечились внутривенным введением rtPA, немного. Всего в английской литературе описано около 162 пациентов, а о sICH — у 6 (3.7%) пациенты. 2,11,15,19,20 Как ни странно, в этом анализе была статистически значимая разница в шансах на благоприятный исход при внутривенном тромболизисе, который благоприятствовал пациентам с пролонгированным АЧТВ (отношение шансов [OR] 1,57, 95% доверительный интервал [ CI] 1.02–2.41). 20 Одним из самых крупных отдельных исследований с участием пациентов было проспективное исследование тромболизиса в клинической практике в 57 медицинских центрах США. 11 О специфическом aPTT во время внутривенного введения rtPA в этих исследованиях, как правило, не сообщалось. 19,11
Риск всех типов кровотечений может повышаться при внутривенном введении rtPA, если пациенту вводят системную антикоагулянтную терапию. Наличие активного кровоточащего диатеза или коагулопатии является противопоказанием к внутривенному введению rtPA для лечения острого ишемического инсульта. 1 Подозрение на коагулопатию обычно связано с антикоагулянтной терапией. Другие потенциальные причины включают цирроз печени, терминальную стадию почечной недостаточности, гематологические злокачественные новообразования, дефицит витамина К, сепсис и синдром антифосфолипидных антител.Кардиологи обнаружили ранний успех многогранного подхода к лечению острой окклюзии коронарных артерий путем сочетания антикоагуляции с системным фибринолизом, хотя более высокие значения активированного частичного тромбопластинового времени (АЧТВ) (и более высокие дозы гепарина) были связаны с более высокими показателями ICH. 21 Данных о пациентах с инсультом с длительным АЧТВ, которые лечились внутривенным введением rtPA, немного. Всего в английской литературе описано около 162 пациентов, а о sICH — у 6 (3.7%) пациенты. 2,11,15,19,20 Как ни странно, в этом анализе была статистически значимая разница в шансах на благоприятный исход при внутривенном тромболизисе, который благоприятствовал пациентам с пролонгированным АЧТВ (отношение шансов [OR] 1,57, 95% доверительный интервал [ CI] 1.02–2.41). 20 Одним из самых крупных отдельных исследований с участием пациентов было проспективное исследование тромболизиса в клинической практике в 57 медицинских центрах США. 11 О специфическом aPTT во время внутривенного введения rtPA в этих исследованиях, как правило, не сообщалось. 19,11
Согласно последним рекомендациям AHA, «текущее использование антикоагулянта с международным нормализационным коэффициентом (INR)> 1,7 или частичным тромбопластином (PT)> 15 секунд» является абсолютным противопоказанием к внутривенному лечению rtPA. 1 Приблизительно 115 пациентов с инсультом, леченным варфарином, с МНО> 1,7 на момент внутривенного тромболизиса, были зарегистрированы в английской литературе, главным образом из крупных регистров. 2,11,15,17,19,20,22,23 Из них sICH был зарегистрирован только у 1 пациента.Большинство исследований не предоставили информацию о частоте каких-либо ICH или функциональных исходов, поскольку эти пациенты изучались среди более крупных групп. Повышенное МНО может быть вызвано другими расстройствами, такими как заболевание печени или гематологические нарушения. В одном большом анализе 2755 тромболизированных пациентов, объединенных из испытаний, было 138 пациентов с МНО> 1,7 от любой причины и еще 14 с МНО> 1,7 из-за пероральной антикоагулянтной терапии. 20 У 138 пациентов с высоким МНО по причинам, не связанным с антикоагулянтами, шансы на более благоприятный исход для тромболизированных пациентов по сравнению с контрольной группой после поправки на возраст и исходный уровень NIHSS немного выше у пациентов с МНО> 1.7, но это различие не было статистически значимым (OR 1,21, 95% CI 0,82–1,78). Непонятно, почему наблюдается тенденция к повышению показателей благоприятного исхода у пациентов с пролонгированным МНО и АЧТВ. Предположительно, возможно, что это были очень хорошо отобранные пациенты с относительно низким риском геморрагической трансформации, и что дополнительный антикоагулянтный эффект фактически улучшил реканализацию.
Безопасность внутривенного введения rtPA у пациентов с инсультом, принимающих варфарин, у которых во время инсульта наблюдается субтерапевтическое МНО, оспаривается.Текущие руководящие принципы AHA / Американской ассоциации инсульта допускают внутривенное лечение rtPA для пациентов, получавших лечение в течение 3 часов с момента начала заболевания с МНО ≤1,7, 1 , в то время как европейская лицензия указывает, что это противопоказано, если пациент принимает пероральные антикоагулянты независимо от МНО. 24 Два относительно небольших многоцентровых регистра и несколько одноцентровых серий случаев показали широкий разброс показателей sICH (0–36%) у пациентов, принимавших варфарин с субтерапевтическим МНО во время тромболизиса. 2,25–31 В 2 метаанализах, самый крупный из которых включал 284 пациента, OR для sICH был увеличен для пациентов, принимавших варфарин (OR 2,6, 95% CI 1,1-5,9 и скорректированное OR 4,1 [1-16,1 ]), но оба этих анализа не были скорректированы с учетом потенциальных искажающих факторов. 30,32 Данные из 2 крупных регистров (Get-With-The-Guidelines и SITSr) показывают, что, хотя у пациентов, принимающих варфарин, действительно более высокие общие показатели sICH, чем у тех, кто не принимает варфарин, когда такие факторы, как тяжесть инсульта, пожилой возраст, и сопутствующие заболевания, лечение варфарином в условиях субтерапевтического МНО не увеличивает независимо риск sICH. 22,23
Низкомолекулярный гепарин
Низкомолекулярные гепарины (НМГ) действуют дольше и обладают большей биодоступностью, чем нефракционированный гепарин. Внутривенный тромболизис при инсульте противопоказан, если пациент принимает терапевтические дозы НМГ из-за предполагаемого высокого риска геморрагических осложнений. Сообщений о внутривенном тромболизисе у пациентов, принимающих НМГ, в литературе мало. Одно исследование включало 21 тромболизированного пациента, получавшего НМГ, 18 из которых получали дозу в течение предшествующих 24 часов. 25 Однако большинство из них принимали профилактические дозы, и только 5 из них были прописаны в терапевтических дозах. Внутричерепное кровоизлияние произошло у 8 (38%; у 3 были симптомы). Семь (33%) достигли благоприятного исхода и 6 (29%) умерли. По сравнению с пациентами, не принимавшими антикоагулянты, у тех, кто принимал НМГ, вероятность sICH была на 8,4 выше (95% ДИ 2,2–32,2), на 5,3 выше вероятность смерти (95% ДИ 1,8–15,5) и на 68% ниже вероятность независимости через 3 месяца. 25 Однако большинство из этих пациентов были госпитализированы во время инсульта, и у них могли быть сопутствующие заболевания, которые искажали ассоциации.О других случаях очень небольшого числа пациентов на НМГ, получавших тромболизис, сообщается как о частях более крупных исследований, в которых не было случаев ICH. 2 Наиболее разумно избегать внутривенного введения rtPA, если пациент получил терапевтическую дозу LMWH в течение предыдущих 24 часов.
Прямые ингибиторы тромбина
Дабигатран и аргатробан напрямую ингибируют тромбин, предотвращая образование фибрина из фибриногена. Привлекательность прямых ингибиторов тромбина по сравнению с традиционными антагонистами витамина К многофакторна: более предсказуемая фармакокинетика, отсутствие необходимости в рутинном лабораторном мониторинге, меньшее количество лекарств-взаимодействий и, возможно, повышение экономической эффективности. 33 Безопасность и эффективность внутривенного введения rtPA у пациентов, принимавших прямые ингибиторы тромбина, изучены недостаточно. Более того, если кровотечения все же возникают, стратегии лечения и отмены антикоагуляции остаются спорными.
Опубликованный опыт ограничен в основном описаниями случаев. 34–39 Сообщалось только об 1 ICH со смертельным исходом. Прямые ингибиторы тромбина также изучались в качестве адъюванта к rtPA внутривенно для лечения острого ишемического инсульта.В пилотном исследовании 65 пациентов с острым инсультом, получавших Аргатробан вместе с внутривенным введением rtPA, sICH произошел у 3 (4,6%) пациентов. 40 Из-за таких ограниченных данных о дабигатране и внутривенном введении rtPA безопасность и эффективность тромболизиса у пациентов, принимающих прямые ингибиторы тромбина, неизвестны. Хотя INR и pTT не являются достаточно надежными индикаторами антикоагулянтного эффекта дабигатрана, тромбиновое время (TT) чувствительно к наличию активности дабигатрана. 41 Основываясь на нашем текущем понимании фармакокинетики, внутривенное введение rtPA может считаться разумным в некоторых случаях, если у пациентов нормальные TT, aPTT и PT, но это должно стать предметом будущих исследований.
Ингибиторы фактора Ха
Клиницисты могут ожидать увеличения числа пациентов, получающих антикоагулянтную терапию пероральными ингибиторами фактора Ха апиксабаном или ривароксабаном. Было показано, что эти агенты превосходят (апиксабан) или не уступают (ривароксабан) варфарину в предотвращении вторичного инсульта, связанного с фибрилляцией предсердий, и уменьшения кровотечений. 42,43 Прямые ингибиторы фактора Ха могут продлевать ПВ и АЧТВ, но не с достаточной надежностью для точной оценки антикоагулянтных эффектов.В некоторых случаях может проводиться осторожное лечение в соответствии с периодом полувыведения лекарства, но до тех пор, пока не будет доступен надежный и быстрый метод измерения их антикоагулянтного эффекта, следует предполагать, что пациенты, принимающие эти лекарства, имеют более высокий риск, чем обычный. Учитывая, что было зарегистрировано так мало пациентов и что большая часть данных поступает из реестров или исследований, в которых вероятна систематическая ошибка, мы думаем, что эти пациенты не должны регулярно получать rtPA внутривенно, если они не являются частью научных исследований.
Тяжелая гипогликемия или гипергликемия
Измерение уровня глюкозы в крови является необходимым условием перед внутривенным введением rtPA. Основная причина этого состояния — исключение тяжелой гипогликемии, которая редко может имитировать симптомы инсульта. Еще реже тяжелая гипергликемия может вызвать очаговый неврологический дефицит. Предыдущие версии рекомендаций AHA по лечению острого инсульта указывали уровни глюкозы ниже 50 мг / дл (2,7 ммоль / л) и выше 400 мг / дл (22,2 ммоль / л) в качестве противопоказаний для тромболизиса, но в самом последнем издании гипогликемия указывается только как исключение. 1 Между тем, вкладыш в упаковке Управления по контролю за продуктами и лекарствами (FDA) для Activase (alteplase, rtPA) рекомендует «с особой тщательностью» диагностировать инсульт у пациентов с уровнем глюкозы <50 или> 400 мг / дл.
На практике опытные эксперты путают тяжелую гипогликемию с инсультом. Хотя очаговые нарушения (в частности, гемипарез) могут возникать, они обычно связаны с изменением сознания или судорогами. Пациенты также отличаются потливостью.Быстрое разрешение после введения декстрозы является диагностическим. Области ограниченной диффузии могут быть вызваны эпизодами гипогликемии, но обычно они двусторонние и наблюдаются у пациентов в коме. 44 Гипергликемия часто встречается у пациентов с острым инсультом и может быть тяжелой у пациентов с диабетом. Тем не менее, это исключительно причина очагового неврологического дефицита при отсутствии изменений в уровне настороженности.
Еще одна причина для измерения уровня глюкозы в крови заключается в том, что гипогликемия и гипергликемия могут усугубить ишемию головного мозга, а гипергликемия также связана с уменьшением шансов реканализации и повышенным риском ICH. 45–48 Стойкая гипергликемия, а не только исходная гипергликемия, может быть в большей степени связана с этими пагубными эффектами. 44 Хотя нет доказательств того, что экстренная коррекция гипергликемии может улучшить исходы при остром ишемическом инсульте или облегчить реканализацию, кажется разумным лечить гипергликемию (например, стремясь к уровню глюкозы <180-200 мг / дл), пока она вызывает строго следует избегать гипогликемии любой степени.
Безопасность тромболизиса у пациентов с тяжелой гипогликемией или гипогликемией изучена недостаточно.В большом анализе Virtual International Stroke Trials Registry (VISTA) только 9 пациентов с глюкозой <50 мг / дл (5 получали rtPA) и 23 - глюкозой> 400 мг / дл (6 получали rtPA) были идентифицированы среди Всего на учете 9613 пациентов. 20 В этих небольших подгруппах пациентов тромболизис не повлиял на исходы, и среди пролеченных не было случаев sICH.
Таким образом, нет убедительных доказательств, чтобы рассматривать нарушения уровня глюкозы в качестве противопоказаний для внутривенного введения rtPA.Целесообразно лечить rtPA пациентов с подозрением на инсульт и тяжелой гипергликемией. Мы также считаем целесообразным лечить пациентов с симптомами инсульта и тяжелой гипогликемией, состояние которых не улучшается сразу после инфузии декстрозы.
Ранние рентгенологические ишемические изменения
Признаки ранней ишемии на первичной компьютерной томографии (КТ) головы не являются абсолютным противопоказанием к внутривенному введению rtPA пациентам с инсультом, но это вызывает разногласия.В рекомендациях AHA от 2013 г. рекомендуется проводить внутривенный тромболизис, если эти изменения присутствуют, независимо от их степени. 1 Признаки ранней ишемии (потеря четкости определения базальных ганглиев, сглаживание борозды, очаговое набухание и масс-эффект, а также потеря четкости соединения серого и белого вещества) необходимо отличать от областей явной гипоплотности, указывающих на установлен инфаркт головного мозга. Целью тромболизиса является реперфузия ишемической, но жизнеспособной паренхимы головного мозга (полутень).Пациенты со значительным «несоответствием» между областью относительно небольшого центрального инфаркта и большей площадью окружающей полутени являются пациентами, которым может помочь rtPA, независимо от того, есть ли тонкие рентгенологические свидетельства ишемических изменений. Хотя сейчас доступны более новые методы визуализации — КТ и МРТ-сканирование перфузии — они более трудозатратны и требуют больше времени, чем неконтрастная КТ. Не было показано, что лечение под контролем перфузионной визуализации улучшает исходы у пациентов, получающих rtPA.Таким образом, мы не думаем, что визуализация перфузии должна выполняться в рутинной практике у пациентов до внутривенного тромболизиса. В нашей практике мы используем визуализацию перфузии у отдельных пациентов; например, для пациентов с симптомами с неясной датой начала, такими как «инсульты при пробуждении».
В отличие от едва различимых рентгенологических признаков ранней ишемии, явная гипоплотность на КТ отражает более тяжелое и необратимое повреждение головного мозга и увеличивает риск геморрагической трансформации. Если участки с пониженной плотностью охватывают более одной трети пораженного полушария головного мозга, внутривенный тромболизис противопоказан и не должен применяться. 1 Оценить степень ишемии по сравнению с инфарктом не всегда просто. Даже среди опытных нейрорадиологов и неврологов согласие между экспертами определить, затрагивает ли ишемия менее или более одной трети территории средней мозговой артерии (СМА), является лишь умеренным (κ. 4). 49 Результаты апостериорного анализа Европейского совместного исследования острого инсульта (ECASS) показали, что степень гипоаттенуации на КТ головы была предиктором ответа на тромболизис. 50 Пациенты с областями гипоаттенуации, поражающими менее или равной одной трети территории СМА, имели повышенные шансы на благоприятный исход (OR 3,43, 95% ДИ 1,61-7,33), тогда как пациенты с областями гипоаттенуации, охватывающими более одной трети на территории MCA наблюдалось нестатистически значимое снижение шансов на благоприятный исход (OR 0,41, 95% CI 0,06–2,70). Кроме того, что, вероятно, объясняет связь с клиническими исходами, повышался риск sICH. 50
Относительные противопоказания
Пожилой возраст
На вкладыше к препарату Activase (alteplase, rtPA) указан «пожилой возраст (например, старше 75 лет)» в качестве предупреждения о том, что риск внутривенного rtPA может возрасти. Пожилой возраст не считается противопоказанием или исключением в рекомендациях AHA. 1 Из пациентов, включенных в ранние клинические испытания внутривенного тромболизиса при инсульте, только около 0,5% были старше 80 лет. 51 Исследование NINDS специально не исключало пожилых пациентов, но средний возраст составлял 69 лет. 6 Верхний предел для включения в испытания ECASS составлял 80 лет. 52–54 Возраст является независимым фактором риска неблагоприятного исхода у пациентов с ишемическим инсультом, независимо от того, вводится ли rtPA внутривенно. Краткосрочная и долгосрочная смертность в два раза выше у пациентов старше 85 лет по сравнению с более молодыми пациентами. 55,56
Третье международное исследование инсульта (IST-3), международное рандомизированное контролируемое исследование, включало 1617 пациентов старше 80 лет. 57 Пациенты были рандомизированы в группу rtPA или плацебо в течение 6 часов после появления симптомов. Первичной конечной точкой была доля пациентов, выживших и независимых через 6 месяцев, которые существенно не различались между двумя группами (37% в группе rtPA и 35% в контрольной группе [ P = 0,181]). В анализе подгрупп существенная разница существовала в скорректированном эффекте лечения между пациентами старше 80 лет и пациентами моложе, что свидетельствует о большей пользе у очень пожилых пациентов.Кроме того, систематический обзор, в котором анализировались 7012 пациентов из 12 исследований, показал, что пациенты старше 80 лет выздоравливали так же, как и те, кто моложе, особенно когда лечение было начато раньше.
Другое исследование включало 3472 тромболизированных пациента старше 80 лет из Международного регистра тромболизиса инсульта и сравнивало их с контрольными пациентами из регистра нейропротективного лечения VISTA. 58 Распределение баллов по шкале mRS через 3 месяца было лучше у пациентов с тромболизацией как у очень пожилых, так и у более молодых пациентов.
Достаточно последовательное сообщение было получено из нескольких наблюдательных исследований: восьмидесятилетние и девяностолетние имеют более высокий уровень смертности и меньше шансов на достижение благоприятных результатов, чем пациенты <80, но схожие показатели sICH. 16,59–63 Более низкие показатели хороших результатов могут частично отражать многочисленные сопутствующие заболевания у пожилых пациентов, а также их пониженную способность восстанавливать функции через реабилитацию. В нескольких исследованиях подгруппы пожилых людей имели статистически значимо более высокие показатели застойной сердечной недостаточности, ишемической болезни сердца и гипертонии. 60,62,64,65
Таким образом, существующие данные не поддерживают исключение пациентов старше 80 лет из приема rtPA по поводу острого инсульта. Благоприятные исходы встречаются реже, а уровень смертности выше, но это также верно для нелеченных пациентов и может отражать рост сопутствующих заболеваний и меньший потенциал для реабилитации. Ставки sICH сопоставимы. Профиль безопасности rtPA у очень пожилых пациентов в большинстве исследований предполагает, что можно надлежащим образом отбирать пожилых пациентов для тромболизиса, и наилучшие имеющиеся данные показывают, что польза, получаемая от внутривенного введения rtPA, не уменьшается.
Легкие или улучшающиеся симптомы инсульта
Хотя легкие или быстро улучшающиеся неврологические расстройства часто указывались в качестве критерия относительного исключения для внутривенного тромболизиса, а этикетка FDA не рекомендует использование активазы (альтеплазы, rtPA) для незначительных симптомов инсульта. данные показывают, что от 20% до 30% пациентов с легкими или улучшающимися симптомами, когда рассматривается тромболизис, могут иметь значительную нетрудоспособность через 3 месяца. 66–68 Легкие инсульты в литературе часто определяются по шкале NIHSS ≤4.Однако это оперативное определение не всегда представляет собой незначительные недостатки для пациента. Например, тяжелый монопарез (даже потеря ловкости рук для человека в зависимости от его способности выполнять свою работу), дисбаланс походки, афазия или серьезный дефицит поля зрения — все это может изолированно отключать дефицит, и в этих случаях NIHSS будет ≤ 4. Кроме того, у некоторых пациентов с легкими симптомами может быть окклюзия проксимального внутричерепного сосуда, и они подвергаются большему риску неврологического ухудшения и стойкой инвалидности. 68,69 Пациенты с ранним улучшением дефицита могут также иметь больше шансов на последующее неврологическое снижение. 70
Текущие руководства AHA заявляют, что внутривенный тромболизис может рассматриваться у пациентов с легким инсультом и у пациентов с быстро улучшающимися симптомами (класс IIb, уровень доказательности C), и рекомендуют дальнейшие исследования для уточнения значения тромболизиса у этих пациентов. 1 Ограниченные данные свидетельствуют о том, что тромболизис безопасен и эффективен у пациентов с легким инсультом, в том числе результаты основополагающего исследования NINDS, в котором фактически участвовала меньшая часть пациентов с NIHSS ≤4. 71,72 Многоцентровое проспективное, рандомизированное и двойное слепое исследование PRISMS в настоящее время проводится для оценки того, улучшает ли внутривенное введение активазы (альтеплаза, rtPA) в течение 3 часов после появления симптомов исходы у пациентов с легким инсультом (определяется как NIHSS). ≤ 5).
До тех пор, пока не появятся дополнительные доказательства, мы считаем наиболее разумным решить, проводить ли тромболизис, исходя из значимости текущего дефицита (независимо от того, улучшается ли он) для конкретного человека.Если у пациента будут ограничения в жизни, если дефицит останется, мы выбираем лечение тромболизисом. Для пациентов с быстро улучшающимися симптомами, у которых тромболизис не считается необходимым, но у которых изначально был тяжелый дефицит, целесообразно рассмотреть возможность получения изображения сосудов, чтобы исключить окклюзию проксимальной артерии, пока пациент все еще находится в отделении неотложной помощи.
Тяжелый инсульт и кома
Первоначальная тяжесть дефицита является основным фактором, определяющим исход инсульта, независимо от того, проводился ли тромболизис.Тяжелые инсульты (по-разному определяемые как NIHSS> 20 или> 25) обычно вызваны обширными инфарктами, которые могут иметь более высокий риск геморрагической трансформации. Это отражено во вкладыше FDA для Activase (alteplase, rtPA), предупреждающем, что риск ICH выше у пациентов с тяжелым инсультом. Однако есть убедительные доказательства того, что внутривенный тромболизис полезен для пациентов с тяжелым инсультом, и на самом деле эти пациенты могут получить наибольшую пользу от лечения.
Анализ данных NINDS показал, что внутривенное введение rtPA было связано с улучшением результатов у пациентов с NIHSS> 20. 73 В небольшой подгруппе пациентов с NIHSS> 25 в IST-3 положительный эффект внутривенного тромболизиса усиливался, даже когда пациенты были включены в исследование в течение 6 часов после появления симптомов. 57 Аналогичным образом, при анализе 9613 пациентов в VISTA, у тех, у кого NIHSS> 22, были более высокие шансы на лучший функциональный результат. 20 Это неудивительно. Само собой разумеется, что пациенты с очень тяжелым дефицитом имеют гораздо меньше шансов восстановить хорошую функцию, если не произойдет своевременная реперфузия.
Хотя, вероятно, правда, что тяжелые инсульты действительно несут больший риск sICH, имеющиеся доказательства не являются окончательными. Не все исследования подтверждают повышенный риск кровотечения при тяжелом инсульте. 74 Тем не менее, реперфузионное повреждение является наиболее частым механизмом симптоматического кровотечения после тромболизиса, и у пациентов с большими участками ишемии более вероятно развитие этого типа повреждения, если тромболизис достигает реканализации. Тем не менее, вероятность благоприятного исхода увеличивается при использовании внутривенного введения rtPA после учета этого геморрагического риска.
Кома была противопоказанием для регистрации в NINDS. 6 Основанием для исключения коматозных пациентов было предотвращение включения возможных имитаторов инсульта. Хотя кома — очень редкое проявление инсульта, она может возникнуть у пациентов с окклюзией основной артерии, которым может быть полезен внутривенный тромболизис. 75 Следовательно, кома сама по себе не должна считаться противопоказанием для внутривенного введения rtPA и должна применяться при подозрении на окклюзию основной артерии.
Текущие рекомендации AHA 1 не упоминают тяжелые инсульты (или кому) как относительное противопоказание для внутривенного тромболизиса в течение 3 часов, но предостерегают от лечения пациентов с NIHSS> 25 более 3 часов, учитывая, что эти пациенты были исключены из ECASS -3 (ECASS-3 2009) и безопасность rtPA в расширенном временном окне для этих тяжелых инсультов не доказана. Мы полностью согласны с тем, что не должно быть порогового значения, выше которого не показан тромболизис, по крайней мере, в течение 3 часов с момента появления симптомов.
Недавняя серьезная операция
На вкладыше Activase (alteplase, rtPA) перечислены недавние серьезные операции (например, коронарное шунтирование, родоразрешение и биопсия органа) в качестве предупреждения, но не абсолютного противопоказания. В рекомендациях AHA это также считается относительным противопоказанием, 1 , но оно не указано в качестве противопоказания в Рекомендациях Европейской инициативы по борьбе с инсультом. 24 Произвольные определения терминов «недавний» и «крупный» могут быть проблематичными, а временные рамки, используемые в крупных исследованиях, различались.Например, в исследование NINDS были исключены пациенты, перенесшие серьезную операцию в течение предыдущих 14 дней, 6 , в то время как в исследование ECASS исключены пациенты, перенесшие серьезную операцию в течение предшествующих 3 месяцев. 52,54
Проблема внутривенного введения rtPA пациентам, которые недавно перенесли операцию, связана с риском кровотечения в хирургическом койке. Несмотря на то, что это очевидно обоснованное беспокойство, следует рассмотреть конкретный тип и место операции, а также способность контролировать возможные кровотечения, прежде чем отказываться от варианта внутривенного введения rtPA.Конечно, тяжесть инсульта также должна приниматься во внимание при оценке предполагаемых рисков и преимуществ тромболизиса в этих случаях.
Доказательств, прямо подтверждающих это противопоказание, мало. Есть несколько исследований пациентов, которым вводили rtPA не по инструкции по поводу острого инсульта, которые включали небольшие группы пациентов, перенесших недавнюю операцию. В одном из них 8 пациентов перенесли операцию в течение 3 месяцев. 2 В этой очень небольшой группе показатели sICH (1 из 8) и неблагоприятных исходов (3 из 8) не были чрезмерно высокими.Примечательно, что ни у одного из этих пациентов не было системного кровотечения, что якобы является причиной исключения этих пациентов из внутривенного лизиса.
В регистре инсульта, который включал 1104 пациентов с инсультом, леченным rtPA, 13 перенесли хирургическое вмешательство или травму в течение предшествующих 3 месяцев. У пациентов, перенесших недавнюю операцию, было 2 системных кровотечения — 1 после имплантации кардиостимулятора и 1 после перианальной операции. Обоим пациентам сделали переливание крови, но серьезных кровотечений не было. 16 Дополнительные случаи указывают на то, что кровотечение в месте недавней операции может потребовать инвазивных вмешательств — для достижения гемостаза или эвакуации гематомы — и переливания крови, но все же совместимо с благоприятным неврологическим восстановлением. Данные о тромболизисе у пациентов с острым инсультом немногочисленны, и, несомненно, существует некоторая предвзятость публикаций в отношении сообщения о случаях без серьезных осложнений. Каждого пациента необходимо оценивать индивидуально. Если риск системного кровотечения из-за внутривенного тромболизиса считается слишком высоким у послеоперационного пациента с острым ишемическим инсультом и подозрением на окклюзию крупных сосудов, эндоваскулярная терапия может быть разумным и даже потенциально более безопасным вариантом.
Артериальная пункция несжимаемого сосуда
Артериальная пункция несжимаемого сосуда в течение 7 дней до появления симптомов острого инсульта является предупреждением для вкладыша Activase (альтеплаза, rtPA) и является относительным противопоказанием к внутривенному введению rtPA в соответствии с рекомендациями AHA. 1 Этот сценарий встречается крайне редко и, скорее всего, имеет место у тяжелобольных пациентов, которым недавно была проведена катетеризация подключичной или внутренней яремной вены. Другие ситуации, в которых осуществляется доступ к несжимаемым венам, — это установка электродов для стимуляции или дефибрилляции, диализных катетеров, катетеров легочной артерии или транскатетерной установки сердечного клапана.Пациент, подвергающийся одной из этих процедур, может быть менее функциональным и более больным, чем общая популяция, в которой изучалась внутривенная rtPA, и соотношение рисков к потенциальной пользе в этой подгруппе также может существенно отличаться. Обычное клиническое наблюдение увеличения кровотечения у пациентов с антикоагулянтной терапией, которым установлены центральные венозные катетеры, и потенциальные последствия неконтролируемого и опасного для жизни кровотечения, вероятно, оправдывают этот критерий исключения, хотя в опубликованной литературе нет данных, поддерживающих или опровергающих эту рекомендацию.
Недавнее желудочно-кишечное или мочеполовое кровотечение
В рекомендациях AHA от 2013 г. желудочно-кишечное (ЖКТ) или мочевыводящее кровотечение в течение предыдущего 21 дня рассматривается как критерий относительного исключения для внутривенного введения rtPA при остром ишемическом инсульте. Активное внутреннее кровотечение — абсолютное противопоказание. «Недавнее» желудочно-кишечное или мочеполовое кровотечение считается предупреждением на этикетке препарата. Данные, относящиеся к эффективности и безопасности внутривенного введения rtPA при инсульте на фоне недавнего желудочно-кишечного кровотечения, чрезвычайно ограничены и, вероятно, подвержены ошибкам отбора и публикации.В 1 исследовании только 1 такой пациент (с гематурией) лечился внутривенным тромболизисом. Этот пациент не страдал sICH и имел mRS 1 через 90 дней. 2
Как и в случае большинства относительных противопоказаний, потенциальные риски и преимущества внутривенного тромболизиса у этой подгруппы пациентов, скорее всего, значительно варьируются в зависимости от нескольких факторов. Двадцать один день был выбран произвольно и в некоторых случаях может быть излишне осторожным. Факторы, которые следует учитывать, включают время, прошедшее с момента кровотечения, серьезность дефицита инсульта, причину и тяжесть кровотечения, а также то, какое лечение было предоставлено для предшествующего эпизода кровотечения.Пациенты с тяжелым инсультом, у которых были скрытые кровоизлияния в желудочно-кишечный тракт или мочеиспускательные органы, диффузные или мультифокальные поражения, подверженные кровотечению, могут быть более безопасными кандидатами для рассмотрения внутриартериальной терапии инсульта, поскольку риск системного внутривенного тромболизиса у этих пациентов может быть недопустимым.
Приступ в начале
Припадок в начале симптомов инсульта с постиктальными резидуальными неврологическими нарушениями в рекомендациях AHA считается относительным противопоказанием к внутривенному введению rtPA. 1 Основанием для исключения таких пациентов является то, что очаговый неврологический дефицит в этой ситуации более вероятен из-за имитации инсульта — постиктального паралича Тодда — а не острой церебральной ишемии.Однако эти сущности не исключают друг друга, поскольку приступы редко возникают в начале острого ишемического инсульта. 76 Примечательно, что риск sICH после тромболизиса имитаторов инсульта чрезвычайно низок. 77,78 Кроме того, исторические особенности изъятия в начале могут вводить в заблуждение.
Большинство данных о тромболизисе у пациентов с приступами в начале получено из ретроспективных обзоров проспективно собранных пациентов для регистров. В общей сложности почти 300 пациентов с приступом в начале получили в / в rtPA по поводу симптомов, подобных инсульту, описанных в английской литературе. 77–83 Из них sICH был зарегистрирован только у 2 пациентов, один из которых имел отдаленный анамнез хирургического удаления опухоли головного мозга. Согласно недавнему опросу, 91% неврологов, перенесших инсульт, рекомендовали бы внутривенное введение rtPA пациентам с приступами в начале появления симптомов. 84
Недавний инфаркт миокарда
Недавний острый инфаркт миокарда в анамнезе за 3 месяца до инсульта является относительным противопоказанием к внутривенному тромболизису согласно последним рекомендациям AHA, 1 , но не является противопоказанием в Европе. руководящие принципы 24 или согласно этикетке препарата.Это также не было критерием исключения в исследованиях NIND или ECASS. Основные опасения по поводу назначения rtPA этим пациентам: (1) возможность кровотечения миокарда, предрасполагающего к разрыву стенки миокарда, (2) перикардит после инфаркта миокарда, который может стать геморрагическим, и (3) возможные тромбы желудочков, которые могут эмболизироваться из-за лизиса. Разрыв стенки миокарда является редким осложнением инфаркта миокарда и становится еще реже, поскольку немедленное вмешательство стало стандартом при инфаркте миокарда с подъемом сегмента ST (ИМпST).Разрыв стенки происходит только после трансмурального инфаркта, и самый высокий риск — в течение 2–5 дней. Когда пациенты получают внутривенный лизис по показаниям на ИМ, нет большой разницы между частотой разрыва сердца среди тех, кто получает тромболизис (1-8%), и тех, кто не получает тромболизис (1-5%). 85
Данных о тромболизисе при инсульте при недавно перенесенном инфаркте миокарда очень мало, и большая часть того, что сообщается, представляет собой отчеты о клинических случаях, несомненно, подверженных предвзятости публикации.В отчетах о клинических случаях описаны 5 пожилых женщин, у которых после приема rtPA по поводу инсульта развился разрыв сердца и гемоперикард. Только у одной из них недавно был хорошо задокументированный ИМ — у 93-летней женщины с сопутствующим ИМпST. 86 У другого пациента была операция по аортокоронарному шунтированию 16 дней назад, а у другого была одышка за несколько дней до обращения с неспецифическими изменениями на электрокардиограмме. 87 Из 5, 4 закончились смертельным исходом. 86–88 Внезапная гипотензия, возникающая примерно через 30 минут — 2 часа после завершения rtPA, должна вызывать подозрение на это осложнение.
После инфаркта миокарда фиброз и рубцевание миокарда завершаются к шестой или седьмой неделе. На основании этого было предложено сократить время после инфаркта миокарда, которое считается противопоказанием для внутривенного тромболизиса, до 7 недель. 85 Тип инфаркта миокарда, помимо тяжести симптомов инсульта, также должен влиять на процесс принятия решений. Пациенты с ИМпST, особенно те, у которых не затрагивается передняя сердечная стенка, могут иметь более низкий риск этого осложнения, но достоверных данных для оценки рисков или направления лечения в этой подгруппе пациентов нет.
Структурные поражения центральной нервной системы
Наличие внутричерепного новообразования, АВМ или аневризмы является противопоказанием в соответствии с рекомендациями AHA и этикеткой препарата. Риски внутривенного введения rtPA пациентам с инсультом и внутричерепными новообразованиями малоизвестны. Опубликованная литература ограничена описаниями случаев, большинство из которых были «успешными». 16,89–91 Случаи с достаточной детализацией описаны в. Был опубликован только 1 пациент, у которого была ICH, пациент с мультиформной глиобластомой височной доли, которая не была известна и проявлялась как умеренный массовый эффект на исходной компьютерной томографии. 92 В дополнение к подробным отчетам о случаях, несколько других были включены в более крупные отчеты о пациентах, которые получали rtPA не по назначению по поводу инсульта. Например, внутривенный тромболизис без sICH был проведен еще 3 пациентам с менингиомами, 1 — с холестеатомой и 1 — с опухолью околоносовых органов. 16 Имеется также несколько сообщений о пациентах с внутричерепными новообразованиями (менингиомы и аденома гипофиза), которым проводили внутривенный тромболизис по поводу ИМпST или тромбоэмболии легочной артерии. 93–95 Примечательно, что, несмотря на более высокую дозу литиков и сопутствующую системную антикоагуляцию, у этих пациентов не было ICH. Следует снова признать возможность систематической ошибки публикации, но эти случаи показывают, что внутривенный тромболизис может быть безопасным для некоторых пациентов с внутричерепными новообразованиями, особенно если новообразование относительно небольшое и расположено вне оси.
Таблица 1.
Краткое описание пациентов с опухолями головного мозга, получавших ТРА.
| Возраст / пол | Показания к лизису | NIHSS | Расположение опухоли | Размер опухоли, см | Тип опухоли | ICH | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Neil | CPE | CP10 | 3.3 × 1,3 | Невринома слухового нерва | Нет | ||||||||||||||
| Нил | 74 / F | Инсульт | 13 | Парафальцин | н / д | Менингиома | Менингиома | Менингиома | Инсульт | 7 | Височная доля | «Очень маленький» | GBM | Нет | |||||
| Grimm | 80 / M | Ход | 9039 n / aGBM | sICH | |||||||||||||||
| Hsieh | 60 / F | Ход | 11 | Лобное основание черепа | 2.0 | Менингиома | Отсутствует | ||||||||||||
| Etgen | 72 / F | Инсульт | 12 | Фронтальный | 2,5 | Менингиома | — | Гипофиз | 1,8 × 1,5 | Аденома гипофиза | Нет | ||||||||
| Рубенштейн | 77 / F | ИМпST | — | н / д | 0.8 × 0,8 | Менингиома | Отсутствует | ||||||||||||
| Jaffe | 62 / F | ИМпST | — | CPA | 1,0 | Менингиома | 9039 | — | Височная доля | 2,5 | GBM | Нет |
О безопасности внутривенного тромболизиса у пациентов с неразорвавшимися внутричерепными аневризмами сообщалось в отчетах о клинических случаях или в ретроспективных сериях случаев ().Частота sICH статистически не различалась между пациентами с аневризмами (0–13%) и без них (1–10%), но объем выборки невелик. 96–98,100 В английской литературе не сообщалось о случаях разрыва аневризмы, вызванных внутривенным введением rtPA. Хотя необходимо учитывать вероятность смещения отбора и смещения публикации, эти серии предполагают, что в / в rtPA можно безопасно вводить пациентам с неразорвавшимися случайными внутричерепными аневризмами. Следует отметить отсутствие данных о риске ВЧГ у пациентов с большими или гигантскими аневризмами, что может быть связано с более высоким риском.
Таблица 2.
Сводная информация о частоте внутричерепных кровотечений у зарегистрированных пациентов с внутричерепными аневризмами, которым был проведен внутривенный тромболизис при инсульте.
| Пациенты с аневризмой, n | sICH аневризма, n (%) | sICH без аневризмы, n (%) | любая аневризма ICH, n (%) | любая ICH аневризма, n (%) | |
|---|---|---|---|---|---|
| 96 | 22 | 0 (0) | 10 (4.7) | 3 (13,6) | 41 (19,1) |
| 97 | 8 | 1 (12,5) | 6 (3,7) | нет данных | нет данных |
| 98 | 10 | 1 (10) | 1 (1,1) | 2 (20) | 9 (9,5) |
| 99 | 8 | 1 (12,5) | н / д | 3 (37,5) | 63 (33,9) |
Деменция
Деменция не была включена в список критериев исключения в большинстве крупных исследований тромболизиса и не упоминается как противопоказание для rtPA в текущих рекомендациях по острому инсульту.Тем не менее, в рутинной клинической практике часто возникает вопрос, является ли внутривенное введение rtPA безопасным и эффективным у пациентов с деменцией и острым ишемическим инсультом. Исходная деменция связана с более низким использованием rtPA, 99 , и это связано с восприятием того, что она повышает риск кровотечения и вряд ли принесет пользу. 101 Фактические данные, хотя и ограниченные, не подтверждают эти утверждения.
Неудивительно, что деменция связана с худшими исходами после инсульта 102,103 даже среди пациентов, которым проводят тромболизис. 103 Однако деменция сама по себе, по-видимому, не увеличивает риск смерти (при выписке, 30 дней или даже 1 год) или госпитализации и связана только с тенденцией к большей функциональной инвалидности, когда анализ соответствующим образом скорректирован с учетом кофакторов. . 103 Точно так же деменция не увеличивала значительно риск ВЧГ по сравнению с подобранной контрольной группой в 2 исследованиях, анализирующих большие группы пациентов. 99,104
Следовательно, представляется безопасным назначать тромболизис пациентам с острым инсультом и предшествующей деменцией.Еще предстоит выяснить, является ли тромболизис эффективным для улучшения функциональных результатов у этих пациентов. Таким образом, решение о назначении rtPA должно приниматься индивидуально в зависимости от предыдущего уровня функции и тяжести дефицита инсульта.
Абсолютные и относительные противопоказания к внутривенному введению rt-PA при остром ишемическом инсульте
Abstract
Большинство противопоказаний к внутривенному (IV) введению рекомбинантного тканевого активатора плазминогена (rtPA) возникли в качестве критериев исключения в крупных исследованиях инсульта.Они были получены на основе консенсуса экспертов в исследовании Национального института неврологических расстройств и инсульта (NINDS). Несмотря на то, что безопасность и эффективность внутривенного введения rtPA неоднократно подтверждались в крупных международных обсервационных исследованиях за последние 20 лет, большинство пациентов с острым ишемическим инсультом, к сожалению, все еще не получают тромболитического лечения. Некоторые из исходных критериев исключения оказались излишне ограничивающими в реальной клинической практике. Было высказано предположение, что применение ослабленных критериев исключения может увеличить скорость внутривенного тромболизиса до 20% с результатами, сопоставимыми с тромболизисом с более традиционными критериями.Мы рассматриваем абсолютные и относительные противопоказания к внутривенному введению rtPA при остром ишемическом инсульте, обсуждая основную причину и доказательства, подтверждающие эти критерии исключения.
Ключевые слова: острый инсульт, тромболитическая терапия, тканевой активатор плазминогена, противопоказания
Абсолютные противопоказания
Острое внутричерепное кровоизлияние
Обнаружение внутричерепного кровоизлияния (ВЧК) при визуализации головного мозга является абсолютным противопоказанием для внутривенного введения рекомбинантных изображений головного мозга. тканевый активатор плазминогена (rtPA) при остром ишемическом инсульте в последних рекомендациях Американской кардиологической ассоциации (AHA) и на этикетке препарата Activase (alteplase, rtPA) (Genentech, Inc.). 1 Это включает внутрипаренхимальное кровоизлияние, субарахноидальное кровоизлияние, внутрижелудочковое кровоизлияние, эпидуральную гематому, субдуральную гематому или геморрагическую конверсию инфаркта. Нет опубликованных отчетов или исследований, оценивающих безопасность внутривенного введения rtPA в таких условиях, поскольку риски явно перевешивают любые потенциальные преимущества.
История ICH
Как в руководстве AHA, 2013 г., так и на этикетке препарата Activase (альтеплаза, rtPA) считается, что наличие ICH в анамнезе является абсолютным противопоказанием. 1 Имеется мало данных о рисках лизиса в этой популяции, и они, вероятно, значительно варьируются в зависимости от индивидуальных характеристик пациента. Несколько случаев опубликованы в крупных обзорах пациентов, получавших тромболизис «не по назначению». В одном обзоре с участием 499 пациентов у 3 в анамнезе был ВЧГ. 2 Ни у одного из этих пациентов не было симптоматического ICH (sICH) после тромболизиса. Двое из них достигли благоприятного функционального результата через 3 месяца. 2 В другом исследовании, в котором рассматривались 135 пациентов, которые лечились rtPA, несмотря на формальные противопоказания, у 3 пациентов в анамнезе имелась ВЧГ, а у одного из них была sICH. 3 Риск внутривенного введения rtPA у пациентов с вероятным ICH в анамнезе варьируется в зависимости от нескольких индивидуальных факторов, включая (1) время, прошедшее с момента ICH, (2) причину предшествующей ICH и было ли проведено окончательное лечение (например, клипирование или намотка аневризмы или артериовенозной мальформации [АВМ]), (3) хирургическая эвакуация гематомы и (4) объем остаточной энцефаломаляции. Мы думаем, что при некоторых обстоятельствах может быть разумным введение rtPA внутривенно, но соотношение пользы и риска следует оценивать на индивидуальной основе.
Использование последовательностей, взвешенных по чувствительности, в магнитно-резонансной томографии (МРТ) увеличило обнаружение бессимптомных церебральных микрокровоизлияний. В исследованиях инсульта без тромболизиса количество микрокровоизлияний коррелирует с частотой ICH, 4 , но наличие известных микрокровоизлияний не является противопоказанием для внутривенного введения rtPA. Одно крупное многоцентровое исследование объединило анализ данных МРТ пациентов, получавших тромболизис внутривенно. 5 Всего 242 микрокровоизлияния было идентифицировано с помощью изображений, взвешенных по T2 *, у 86 (15%) из 570 пациентов.Доля пациентов с sICH была выше среди пациентов с микрокровоизлиянием (5,8%) по сравнению с пациентами без микрокровоизлияний (2,7%), но эта разница не была статистически значимой. 5 Принимая во внимание имеющиеся данные, нельзя отказывать пациентам в внутривенном введении rtPA из-за микрокровоизлияний, обнаруженных на МРТ.
Тяжелая неконтролируемая гипертензия
Неконтролируемая гипертензия до значений, превышающих систолическое давление 185 мм рт. 1 Вероятно, это получено из критерия исключения для исследований Национального института неврологических расстройств и инсульта (NINDS). 6 Взаимосвязь между артериальным давлением (АД), антигипертензивной терапией и клиническими исходами при остром инсульте сложна. В нескольких исследованиях артериальная гипертензия была связана с повышенным риском неблагоприятных исходов и ICH. 7–9 В регистре безопасного проведения лечения инсульта (SITS) более высокое систолическое АД (САД) после лизиса было независимо связано с худшими исходами и повышенным риском ICH. 7 Связь между САД и sICH была линейной, тогда как связь между САД и клиническим исходом была U-образной. В ретроспективном анализе исследования NINDS антигипертензивная терапия, назначенная с до тромболизиса , не была связана с различиями в результатах. Однако у пациентов с артериальной гипертензией, получавших антигипертензивные препараты после рандомизации , вероятность благоприятного исхода через 3 месяца была ниже. 10
Результаты других исследований показывают, что исходное АД не является независимым предиктором ВЧГ или неблагоприятных исходов. 11–13 В 1 исследовании с участием 351 пациента, получавшего rtPA, более высокое САД перед лечением было связано с худшими показателями реканализации, но САД не было независимо связано с исходом. 12 У пациентов, получавших rtPA из раннего опыта в районе Кливленда, не было существенной разницы в доле с тяжелой гипертензией между пациентами с sICH и без. 14 Тяжелая гипертензия не должна препятствовать лечению внутривенным введением rtPA пациентов с острым инсультом, при условии, что ее можно контролировать с помощью гипотензивных препаратов.Использование гипотензивных средств для достижения контроля АД у пациентов до rtPA представляется безопасным.
Серьезная травма головы или инсульт в предыдущие 3 месяца
Руководящие принципы AHA и этикетка препарата от 2013 года рассматривают значительную травму головы или инсульт в течение предшествующих 3 месяцев как критерии исключения для внутривенного введения rtPA при остром инсульте. 1 Посттравматический инфаркт головного мозга регистрируется у 2–10% пациентов с тяжелой травмой головы, но назначение тромболитиков этой группе населения вызывает беспокойство.Пациенты с травмами часто имеют коагулопатию. Системные травмы и переломы могут увеличить риск системных геморрагических осложнений. Ушибы головного мозга, переломы черепа, диффузное повреждение аксонов и травматический ICH могут увеличить риск ICH. В небольшом обзоре пациентов, получавших лечение с нарушением протокола, 1 пациент прошел лечение внутривенным тромболизисом через 3 недели после перенесенной тяжелой травмы головы и получил смертельный sICH. 15 Два крупных европейских ретроспективных исследования пациентов, получавших rtPA внутривенно не по назначению, включали очень небольшое количество пациентов с недавней травмой головы, но не сообщалось никаких подробностей, специфичных для этой популяции. 16,17 Хотя данные крайне ограничены, мы считаем этот критерий исключения разумным, поскольку риски в этой настройке, вероятно, чрезмерно высоки.
Предполагается, что пациенты с острым инсультом, недавно перенесшие ишемический инсульт в течение предыдущих 3 месяцев, подвержены более высокому риску ВЧГ при внутривенном введении rtPA. Эти пациенты были исключены из исторического исследования NINDs. 6 Эффективность и безопасность в таких ситуациях в значительной степени неизвестны и, вероятно, сильно различаются с учетом индивидуальных характеристик, таких как размер и механизм перенесенного инфаркта, возраст и тяжесть повторного инсульта.Редко сообщалось о случаях, когда пациенты получали rtPA внутривенно по поводу инсульта дважды в течение 3 месяцев. В одном отчете подробно описывается пациент, который успешно лечился второй дозой (уменьшенной до 50 мг) внутривенного введения rtPA через 90 часов после первой дозы после повторной окклюзии артерии. У этого пациента исход благоприятный. 18 При периоде полужизни в плазме α, составляющем приблизительно 5 минут, rtPA быстро выводится из кровотока при нормальных метаболических условиях. 18 Повторный внутривенный тромболизис может быть целесообразным в некоторых случаях, особенно при небольшом объеме перенесенного инфаркта, но риски неизвестны.
Тромбоцитопения и коагулопатия
Тромбоцитопения
Хотя нет необходимости ждать подсчета тромбоцитов перед внутривенным введением rtPA, если нет подозрения на тромбоцитопению, количество тромбоцитов <100000 / мм 3 является противопоказанием для внутривенного введения rtPA в соответствии с рекомендациями AHA и вкладышем по лекарствам. 1 Геморрагические осложнения у пациентов с тромбоцитопенией, получающих rtPA внутривенно, не оценивались ни в проспективном, ни в рандомизированном исследовании.Из 14 306 пациентов из нескольких исследований, только приблизительно 20 пациентов с тромбоцитами <100 000 мм 3 , получавших rtPA внутривенно по поводу инсульта, были описаны подробно. 2,3,19,20 Из них только у 1 пациента был зарегистрирован sICH, но чрезвычайно небольшое количество опубликованных случаев не позволяет сделать однозначных выводов о безопасности внутривенного тромболизиса в этом случае.
Коагулопатия
Точно так же мало данных об эффективности или безопасности внутривенного введения rtPA при остром инсульте в условиях аномальных тестов на коагуляцию.Риск всех типов кровотечений может повышаться при внутривенном введении rtPA, если пациенту вводят системную антикоагулянтную терапию. Наличие активного кровоточащего диатеза или коагулопатии является противопоказанием к внутривенному введению rtPA для лечения острого ишемического инсульта. 1 Подозрение на коагулопатию обычно связано с антикоагулянтной терапией. Другие потенциальные причины включают цирроз печени, терминальную стадию почечной недостаточности, гематологические злокачественные новообразования, дефицит витамина К, сепсис и синдром антифосфолипидных антител.Кардиологи обнаружили ранний успех многогранного подхода к лечению острой окклюзии коронарных артерий путем сочетания антикоагуляции с системным фибринолизом, хотя более высокие значения активированного частичного тромбопластинового времени (АЧТВ) (и более высокие дозы гепарина) были связаны с более высокими показателями ICH. 21 Данных о пациентах с инсультом с длительным АЧТВ, которые лечились внутривенным введением rtPA, немного. Всего в английской литературе описано около 162 пациентов, а о sICH — у 6 (3.7%) пациенты. 2,11,15,19,20 Как ни странно, в этом анализе была статистически значимая разница в шансах на благоприятный исход при внутривенном тромболизисе, который благоприятствовал пациентам с пролонгированным АЧТВ (отношение шансов [OR] 1,57, 95% доверительный интервал [ CI] 1.02–2.41). 20 Одним из самых крупных отдельных исследований с участием пациентов было проспективное исследование тромболизиса в клинической практике в 57 медицинских центрах США. 11 О специфическом aPTT во время внутривенного введения rtPA в этих исследованиях, как правило, не сообщалось. 19,11
Согласно последним рекомендациям AHA, «текущее использование антикоагулянта с международным нормализационным коэффициентом (INR)> 1,7 или частичным тромбопластином (PT)> 15 секунд» является абсолютным противопоказанием к внутривенному лечению rtPA. 1 Приблизительно 115 пациентов с инсультом, леченным варфарином, с МНО> 1,7 на момент внутривенного тромболизиса, были зарегистрированы в английской литературе, главным образом из крупных регистров. 2,11,15,17,19,20,22,23 Из них sICH был зарегистрирован только у 1 пациента.Большинство исследований не предоставили информацию о частоте каких-либо ICH или функциональных исходов, поскольку эти пациенты изучались среди более крупных групп. Повышенное МНО может быть вызвано другими расстройствами, такими как заболевание печени или гематологические нарушения. В одном большом анализе 2755 тромболизированных пациентов, объединенных из испытаний, было 138 пациентов с МНО> 1,7 от любой причины и еще 14 с МНО> 1,7 из-за пероральной антикоагулянтной терапии. 20 У 138 пациентов с высоким МНО по причинам, не связанным с антикоагулянтами, шансы на более благоприятный исход для тромболизированных пациентов по сравнению с контрольной группой после поправки на возраст и исходный уровень NIHSS немного выше у пациентов с МНО> 1.7, но это различие не было статистически значимым (OR 1,21, 95% CI 0,82–1,78). Непонятно, почему наблюдается тенденция к повышению показателей благоприятного исхода у пациентов с пролонгированным МНО и АЧТВ. Предположительно, возможно, что это были очень хорошо отобранные пациенты с относительно низким риском геморрагической трансформации, и что дополнительный антикоагулянтный эффект фактически улучшил реканализацию.
Безопасность внутривенного введения rtPA у пациентов с инсультом, принимающих варфарин, у которых во время инсульта наблюдается субтерапевтическое МНО, оспаривается.Текущие руководящие принципы AHA / Американской ассоциации инсульта допускают внутривенное лечение rtPA для пациентов, получавших лечение в течение 3 часов с момента начала заболевания с МНО ≤1,7, 1 , в то время как европейская лицензия указывает, что это противопоказано, если пациент принимает пероральные антикоагулянты независимо от МНО. 24 Два относительно небольших многоцентровых регистра и несколько одноцентровых серий случаев показали широкий разброс показателей sICH (0–36%) у пациентов, принимавших варфарин с субтерапевтическим МНО во время тромболизиса. 2,25–31 В 2 метаанализах, самый крупный из которых включал 284 пациента, OR для sICH был увеличен для пациентов, принимавших варфарин (OR 2,6, 95% CI 1,1-5,9 и скорректированное OR 4,1 [1-16,1 ]), но оба этих анализа не были скорректированы с учетом потенциальных искажающих факторов. 30,32 Данные из 2 крупных регистров (Get-With-The-Guidelines и SITSr) показывают, что, хотя у пациентов, принимающих варфарин, действительно более высокие общие показатели sICH, чем у тех, кто не принимает варфарин, когда такие факторы, как тяжесть инсульта, пожилой возраст, и сопутствующие заболевания, лечение варфарином в условиях субтерапевтического МНО не увеличивает независимо риск sICH. 22,23
Низкомолекулярный гепарин
Низкомолекулярные гепарины (НМГ) действуют дольше и обладают большей биодоступностью, чем нефракционированный гепарин. Внутривенный тромболизис при инсульте противопоказан, если пациент принимает терапевтические дозы НМГ из-за предполагаемого высокого риска геморрагических осложнений. Сообщений о внутривенном тромболизисе у пациентов, принимающих НМГ, в литературе мало. Одно исследование включало 21 тромболизированного пациента, получавшего НМГ, 18 из которых получали дозу в течение предшествующих 24 часов. 25 Однако большинство из них принимали профилактические дозы, и только 5 из них были прописаны в терапевтических дозах. Внутричерепное кровоизлияние произошло у 8 (38%; у 3 были симптомы). Семь (33%) достигли благоприятного исхода и 6 (29%) умерли. По сравнению с пациентами, не принимавшими антикоагулянты, у тех, кто принимал НМГ, вероятность sICH была на 8,4 выше (95% ДИ 2,2–32,2), на 5,3 выше вероятность смерти (95% ДИ 1,8–15,5) и на 68% ниже вероятность независимости через 3 месяца. 25 Однако большинство из этих пациентов были госпитализированы во время инсульта, и у них могли быть сопутствующие заболевания, которые искажали ассоциации.О других случаях очень небольшого числа пациентов на НМГ, получавших тромболизис, сообщается как о частях более крупных исследований, в которых не было случаев ICH. 2 Наиболее разумно избегать внутривенного введения rtPA, если пациент получил терапевтическую дозу LMWH в течение предыдущих 24 часов.
Прямые ингибиторы тромбина
Дабигатран и аргатробан напрямую ингибируют тромбин, предотвращая образование фибрина из фибриногена. Привлекательность прямых ингибиторов тромбина по сравнению с традиционными антагонистами витамина К многофакторна: более предсказуемая фармакокинетика, отсутствие необходимости в рутинном лабораторном мониторинге, меньшее количество лекарств-взаимодействий и, возможно, повышение экономической эффективности. 33 Безопасность и эффективность внутривенного введения rtPA у пациентов, принимавших прямые ингибиторы тромбина, изучены недостаточно. Более того, если кровотечения все же возникают, стратегии лечения и отмены антикоагуляции остаются спорными.
Опубликованный опыт ограничен в основном описаниями случаев. 34–39 Сообщалось только об 1 ICH со смертельным исходом. Прямые ингибиторы тромбина также изучались в качестве адъюванта к rtPA внутривенно для лечения острого ишемического инсульта.В пилотном исследовании 65 пациентов с острым инсультом, получавших Аргатробан вместе с внутривенным введением rtPA, sICH произошел у 3 (4,6%) пациентов. 40 Из-за таких ограниченных данных о дабигатране и внутривенном введении rtPA безопасность и эффективность тромболизиса у пациентов, принимающих прямые ингибиторы тромбина, неизвестны. Хотя INR и pTT не являются достаточно надежными индикаторами антикоагулянтного эффекта дабигатрана, тромбиновое время (TT) чувствительно к наличию активности дабигатрана. 41 Основываясь на нашем текущем понимании фармакокинетики, внутривенное введение rtPA может считаться разумным в некоторых случаях, если у пациентов нормальные TT, aPTT и PT, но это должно стать предметом будущих исследований.
Ингибиторы фактора Ха
Клиницисты могут ожидать увеличения числа пациентов, получающих антикоагулянтную терапию пероральными ингибиторами фактора Ха апиксабаном или ривароксабаном. Было показано, что эти агенты превосходят (апиксабан) или не уступают (ривароксабан) варфарину в предотвращении вторичного инсульта, связанного с фибрилляцией предсердий, и уменьшения кровотечений. 42,43 Прямые ингибиторы фактора Ха могут продлевать ПВ и АЧТВ, но не с достаточной надежностью для точной оценки антикоагулянтных эффектов.В некоторых случаях может проводиться осторожное лечение в соответствии с периодом полувыведения лекарства, но до тех пор, пока не будет доступен надежный и быстрый метод измерения их антикоагулянтного эффекта, следует предполагать, что пациенты, принимающие эти лекарства, имеют более высокий риск, чем обычный. Учитывая, что было зарегистрировано так мало пациентов и что большая часть данных поступает из реестров или исследований, в которых вероятна систематическая ошибка, мы думаем, что эти пациенты не должны регулярно получать rtPA внутривенно, если они не являются частью научных исследований.
Тяжелая гипогликемия или гипергликемия
Измерение уровня глюкозы в крови является необходимым условием перед внутривенным введением rtPA. Основная причина этого состояния — исключение тяжелой гипогликемии, которая редко может имитировать симптомы инсульта. Еще реже тяжелая гипергликемия может вызвать очаговый неврологический дефицит. Предыдущие версии рекомендаций AHA по лечению острого инсульта указывали уровни глюкозы ниже 50 мг / дл (2,7 ммоль / л) и выше 400 мг / дл (22,2 ммоль / л) в качестве противопоказаний для тромболизиса, но в самом последнем издании гипогликемия указывается только как исключение. 1 Между тем, вкладыш в упаковке Управления по контролю за продуктами и лекарствами (FDA) для Activase (alteplase, rtPA) рекомендует «с особой тщательностью» диагностировать инсульт у пациентов с уровнем глюкозы <50 или> 400 мг / дл.
На практике опытные эксперты путают тяжелую гипогликемию с инсультом. Хотя очаговые нарушения (в частности, гемипарез) могут возникать, они обычно связаны с изменением сознания или судорогами. Пациенты также отличаются потливостью.Быстрое разрешение после введения декстрозы является диагностическим. Области ограниченной диффузии могут быть вызваны эпизодами гипогликемии, но обычно они двусторонние и наблюдаются у пациентов в коме. 44 Гипергликемия часто встречается у пациентов с острым инсультом и может быть тяжелой у пациентов с диабетом. Тем не менее, это исключительно причина очагового неврологического дефицита при отсутствии изменений в уровне настороженности.
Еще одна причина для измерения уровня глюкозы в крови заключается в том, что гипогликемия и гипергликемия могут усугубить ишемию головного мозга, а гипергликемия также связана с уменьшением шансов реканализации и повышенным риском ICH. 45–48 Стойкая гипергликемия, а не только исходная гипергликемия, может быть в большей степени связана с этими пагубными эффектами. 44 Хотя нет доказательств того, что экстренная коррекция гипергликемии может улучшить исходы при остром ишемическом инсульте или облегчить реканализацию, кажется разумным лечить гипергликемию (например, стремясь к уровню глюкозы <180-200 мг / дл), пока она вызывает строго следует избегать гипогликемии любой степени.
Безопасность тромболизиса у пациентов с тяжелой гипогликемией или гипогликемией изучена недостаточно.В большом анализе Virtual International Stroke Trials Registry (VISTA) только 9 пациентов с глюкозой <50 мг / дл (5 получали rtPA) и 23 - глюкозой> 400 мг / дл (6 получали rtPA) были идентифицированы среди Всего на учете 9613 пациентов. 20 В этих небольших подгруппах пациентов тромболизис не повлиял на исходы, и среди пролеченных не было случаев sICH.
Таким образом, нет убедительных доказательств, чтобы рассматривать нарушения уровня глюкозы в качестве противопоказаний для внутривенного введения rtPA.Целесообразно лечить rtPA пациентов с подозрением на инсульт и тяжелой гипергликемией. Мы также считаем целесообразным лечить пациентов с симптомами инсульта и тяжелой гипогликемией, состояние которых не улучшается сразу после инфузии декстрозы.
Ранние рентгенологические ишемические изменения
Признаки ранней ишемии на первичной компьютерной томографии (КТ) головы не являются абсолютным противопоказанием к внутривенному введению rtPA пациентам с инсультом, но это вызывает разногласия.В рекомендациях AHA от 2013 г. рекомендуется проводить внутривенный тромболизис, если эти изменения присутствуют, независимо от их степени. 1 Признаки ранней ишемии (потеря четкости определения базальных ганглиев, сглаживание борозды, очаговое набухание и масс-эффект, а также потеря четкости соединения серого и белого вещества) необходимо отличать от областей явной гипоплотности, указывающих на установлен инфаркт головного мозга. Целью тромболизиса является реперфузия ишемической, но жизнеспособной паренхимы головного мозга (полутень).Пациенты со значительным «несоответствием» между областью относительно небольшого центрального инфаркта и большей площадью окружающей полутени являются пациентами, которым может помочь rtPA, независимо от того, есть ли тонкие рентгенологические свидетельства ишемических изменений. Хотя сейчас доступны более новые методы визуализации — КТ и МРТ-сканирование перфузии — они более трудозатратны и требуют больше времени, чем неконтрастная КТ. Не было показано, что лечение под контролем перфузионной визуализации улучшает исходы у пациентов, получающих rtPA.Таким образом, мы не думаем, что визуализация перфузии должна выполняться в рутинной практике у пациентов до внутривенного тромболизиса. В нашей практике мы используем визуализацию перфузии у отдельных пациентов; например, для пациентов с симптомами с неясной датой начала, такими как «инсульты при пробуждении».
В отличие от едва различимых рентгенологических признаков ранней ишемии, явная гипоплотность на КТ отражает более тяжелое и необратимое повреждение головного мозга и увеличивает риск геморрагической трансформации. Если участки с пониженной плотностью охватывают более одной трети пораженного полушария головного мозга, внутривенный тромболизис противопоказан и не должен применяться. 1 Оценить степень ишемии по сравнению с инфарктом не всегда просто. Даже среди опытных нейрорадиологов и неврологов согласие между экспертами определить, затрагивает ли ишемия менее или более одной трети территории средней мозговой артерии (СМА), является лишь умеренным (κ. 4). 49 Результаты апостериорного анализа Европейского совместного исследования острого инсульта (ECASS) показали, что степень гипоаттенуации на КТ головы была предиктором ответа на тромболизис. 50 Пациенты с областями гипоаттенуации, поражающими менее или равной одной трети территории СМА, имели повышенные шансы на благоприятный исход (OR 3,43, 95% ДИ 1,61-7,33), тогда как пациенты с областями гипоаттенуации, охватывающими более одной трети на территории MCA наблюдалось нестатистически значимое снижение шансов на благоприятный исход (OR 0,41, 95% CI 0,06–2,70). Кроме того, что, вероятно, объясняет связь с клиническими исходами, повышался риск sICH. 50
Относительные противопоказания
Пожилой возраст
На вкладыше к препарату Activase (alteplase, rtPA) указан «пожилой возраст (например, старше 75 лет)» в качестве предупреждения о том, что риск внутривенного rtPA может возрасти. Пожилой возраст не считается противопоказанием или исключением в рекомендациях AHA. 1 Из пациентов, включенных в ранние клинические испытания внутривенного тромболизиса при инсульте, только около 0,5% были старше 80 лет. 51 Исследование NINDS специально не исключало пожилых пациентов, но средний возраст составлял 69 лет. 6 Верхний предел для включения в испытания ECASS составлял 80 лет. 52–54 Возраст является независимым фактором риска неблагоприятного исхода у пациентов с ишемическим инсультом, независимо от того, вводится ли rtPA внутривенно. Краткосрочная и долгосрочная смертность в два раза выше у пациентов старше 85 лет по сравнению с более молодыми пациентами. 55,56
Третье международное исследование инсульта (IST-3), международное рандомизированное контролируемое исследование, включало 1617 пациентов старше 80 лет. 57 Пациенты были рандомизированы в группу rtPA или плацебо в течение 6 часов после появления симптомов. Первичной конечной точкой была доля пациентов, выживших и независимых через 6 месяцев, которые существенно не различались между двумя группами (37% в группе rtPA и 35% в контрольной группе [ P = 0,181]). В анализе подгрупп существенная разница существовала в скорректированном эффекте лечения между пациентами старше 80 лет и пациентами моложе, что свидетельствует о большей пользе у очень пожилых пациентов.Кроме того, систематический обзор, в котором анализировались 7012 пациентов из 12 исследований, показал, что пациенты старше 80 лет выздоравливали так же, как и те, кто моложе, особенно когда лечение было начато раньше.
Другое исследование включало 3472 тромболизированных пациента старше 80 лет из Международного регистра тромболизиса инсульта и сравнивало их с контрольными пациентами из регистра нейропротективного лечения VISTA. 58 Распределение баллов по шкале mRS через 3 месяца было лучше у пациентов с тромболизацией как у очень пожилых, так и у более молодых пациентов.
Достаточно последовательное сообщение было получено из нескольких наблюдательных исследований: восьмидесятилетние и девяностолетние имеют более высокий уровень смертности и меньше шансов на достижение благоприятных результатов, чем пациенты <80, но схожие показатели sICH. 16,59–63 Более низкие показатели хороших результатов могут частично отражать многочисленные сопутствующие заболевания у пожилых пациентов, а также их пониженную способность восстанавливать функции через реабилитацию. В нескольких исследованиях подгруппы пожилых людей имели статистически значимо более высокие показатели застойной сердечной недостаточности, ишемической болезни сердца и гипертонии. 60,62,64,65
Таким образом, существующие данные не поддерживают исключение пациентов старше 80 лет из приема rtPA по поводу острого инсульта. Благоприятные исходы встречаются реже, а уровень смертности выше, но это также верно для нелеченных пациентов и может отражать рост сопутствующих заболеваний и меньший потенциал для реабилитации. Ставки sICH сопоставимы. Профиль безопасности rtPA у очень пожилых пациентов в большинстве исследований предполагает, что можно надлежащим образом отбирать пожилых пациентов для тромболизиса, и наилучшие имеющиеся данные показывают, что польза, получаемая от внутривенного введения rtPA, не уменьшается.
Легкие или улучшающиеся симптомы инсульта
Хотя легкие или быстро улучшающиеся неврологические расстройства часто указывались в качестве критерия относительного исключения для внутривенного тромболизиса, а этикетка FDA не рекомендует использование активазы (альтеплазы, rtPA) для незначительных симптомов инсульта. данные показывают, что от 20% до 30% пациентов с легкими или улучшающимися симптомами, когда рассматривается тромболизис, могут иметь значительную нетрудоспособность через 3 месяца. 66–68 Легкие инсульты в литературе часто определяются по шкале NIHSS ≤4.Однако это оперативное определение не всегда представляет собой незначительные недостатки для пациента. Например, тяжелый монопарез (даже потеря ловкости рук для человека в зависимости от его способности выполнять свою работу), дисбаланс походки, афазия или серьезный дефицит поля зрения — все это может изолированно отключать дефицит, и в этих случаях NIHSS будет ≤ 4. Кроме того, у некоторых пациентов с легкими симптомами может быть окклюзия проксимального внутричерепного сосуда, и они подвергаются большему риску неврологического ухудшения и стойкой инвалидности. 68,69 Пациенты с ранним улучшением дефицита могут также иметь больше шансов на последующее неврологическое снижение. 70
Текущие руководства AHA заявляют, что внутривенный тромболизис может рассматриваться у пациентов с легким инсультом и у пациентов с быстро улучшающимися симптомами (класс IIb, уровень доказательности C), и рекомендуют дальнейшие исследования для уточнения значения тромболизиса у этих пациентов. 1 Ограниченные данные свидетельствуют о том, что тромболизис безопасен и эффективен у пациентов с легким инсультом, в том числе результаты основополагающего исследования NINDS, в котором фактически участвовала меньшая часть пациентов с NIHSS ≤4. 71,72 Многоцентровое проспективное, рандомизированное и двойное слепое исследование PRISMS в настоящее время проводится для оценки того, улучшает ли внутривенное введение активазы (альтеплаза, rtPA) в течение 3 часов после появления симптомов исходы у пациентов с легким инсультом (определяется как NIHSS). ≤ 5).
До тех пор, пока не появятся дополнительные доказательства, мы считаем наиболее разумным решить, проводить ли тромболизис, исходя из значимости текущего дефицита (независимо от того, улучшается ли он) для конкретного человека.Если у пациента будут ограничения в жизни, если дефицит останется, мы выбираем лечение тромболизисом. Для пациентов с быстро улучшающимися симптомами, у которых тромболизис не считается необходимым, но у которых изначально был тяжелый дефицит, целесообразно рассмотреть возможность получения изображения сосудов, чтобы исключить окклюзию проксимальной артерии, пока пациент все еще находится в отделении неотложной помощи.
Тяжелый инсульт и кома
Первоначальная тяжесть дефицита является основным фактором, определяющим исход инсульта, независимо от того, проводился ли тромболизис.Тяжелые инсульты (по-разному определяемые как NIHSS> 20 или> 25) обычно вызваны обширными инфарктами, которые могут иметь более высокий риск геморрагической трансформации. Это отражено во вкладыше FDA для Activase (alteplase, rtPA), предупреждающем, что риск ICH выше у пациентов с тяжелым инсультом. Однако есть убедительные доказательства того, что внутривенный тромболизис полезен для пациентов с тяжелым инсультом, и на самом деле эти пациенты могут получить наибольшую пользу от лечения.
Анализ данных NINDS показал, что внутривенное введение rtPA было связано с улучшением результатов у пациентов с NIHSS> 20. 73 В небольшой подгруппе пациентов с NIHSS> 25 в IST-3 положительный эффект внутривенного тромболизиса усиливался, даже когда пациенты были включены в исследование в течение 6 часов после появления симптомов. 57 Аналогичным образом, при анализе 9613 пациентов в VISTA, у тех, у кого NIHSS> 22, были более высокие шансы на лучший функциональный результат. 20 Это неудивительно. Само собой разумеется, что пациенты с очень тяжелым дефицитом имеют гораздо меньше шансов восстановить хорошую функцию, если не произойдет своевременная реперфузия.
Хотя, вероятно, правда, что тяжелые инсульты действительно несут больший риск sICH, имеющиеся доказательства не являются окончательными. Не все исследования подтверждают повышенный риск кровотечения при тяжелом инсульте. 74 Тем не менее, реперфузионное повреждение является наиболее частым механизмом симптоматического кровотечения после тромболизиса, и у пациентов с большими участками ишемии более вероятно развитие этого типа повреждения, если тромболизис достигает реканализации. Тем не менее, вероятность благоприятного исхода увеличивается при использовании внутривенного введения rtPA после учета этого геморрагического риска.
Кома была противопоказанием для регистрации в NINDS. 6 Основанием для исключения коматозных пациентов было предотвращение включения возможных имитаторов инсульта. Хотя кома — очень редкое проявление инсульта, она может возникнуть у пациентов с окклюзией основной артерии, которым может быть полезен внутривенный тромболизис. 75 Следовательно, кома сама по себе не должна считаться противопоказанием для внутривенного введения rtPA и должна применяться при подозрении на окклюзию основной артерии.
Текущие рекомендации AHA 1 не упоминают тяжелые инсульты (или кому) как относительное противопоказание для внутривенного тромболизиса в течение 3 часов, но предостерегают от лечения пациентов с NIHSS> 25 более 3 часов, учитывая, что эти пациенты были исключены из ECASS -3 (ECASS-3 2009) и безопасность rtPA в расширенном временном окне для этих тяжелых инсультов не доказана. Мы полностью согласны с тем, что не должно быть порогового значения, выше которого не показан тромболизис, по крайней мере, в течение 3 часов с момента появления симптомов.
Недавняя серьезная операция
На вкладыше Activase (alteplase, rtPA) перечислены недавние серьезные операции (например, коронарное шунтирование, родоразрешение и биопсия органа) в качестве предупреждения, но не абсолютного противопоказания. В рекомендациях AHA это также считается относительным противопоказанием, 1 , но оно не указано в качестве противопоказания в Рекомендациях Европейской инициативы по борьбе с инсультом. 24 Произвольные определения терминов «недавний» и «крупный» могут быть проблематичными, а временные рамки, используемые в крупных исследованиях, различались.Например, в исследование NINDS были исключены пациенты, перенесшие серьезную операцию в течение предыдущих 14 дней, 6 , в то время как в исследование ECASS исключены пациенты, перенесшие серьезную операцию в течение предшествующих 3 месяцев. 52,54
Проблема внутривенного введения rtPA пациентам, которые недавно перенесли операцию, связана с риском кровотечения в хирургическом койке. Несмотря на то, что это очевидно обоснованное беспокойство, следует рассмотреть конкретный тип и место операции, а также способность контролировать возможные кровотечения, прежде чем отказываться от варианта внутривенного введения rtPA.Конечно, тяжесть инсульта также должна приниматься во внимание при оценке предполагаемых рисков и преимуществ тромболизиса в этих случаях.
Доказательств, прямо подтверждающих это противопоказание, мало. Есть несколько исследований пациентов, которым вводили rtPA не по инструкции по поводу острого инсульта, которые включали небольшие группы пациентов, перенесших недавнюю операцию. В одном из них 8 пациентов перенесли операцию в течение 3 месяцев. 2 В этой очень небольшой группе показатели sICH (1 из 8) и неблагоприятных исходов (3 из 8) не были чрезмерно высокими.Примечательно, что ни у одного из этих пациентов не было системного кровотечения, что якобы является причиной исключения этих пациентов из внутривенного лизиса.
В регистре инсульта, который включал 1104 пациентов с инсультом, леченным rtPA, 13 перенесли хирургическое вмешательство или травму в течение предшествующих 3 месяцев. У пациентов, перенесших недавнюю операцию, было 2 системных кровотечения — 1 после имплантации кардиостимулятора и 1 после перианальной операции. Обоим пациентам сделали переливание крови, но серьезных кровотечений не было. 16 Дополнительные случаи указывают на то, что кровотечение в месте недавней операции может потребовать инвазивных вмешательств — для достижения гемостаза или эвакуации гематомы — и переливания крови, но все же совместимо с благоприятным неврологическим восстановлением. Данные о тромболизисе у пациентов с острым инсультом немногочисленны, и, несомненно, существует некоторая предвзятость публикаций в отношении сообщения о случаях без серьезных осложнений. Каждого пациента необходимо оценивать индивидуально. Если риск системного кровотечения из-за внутривенного тромболизиса считается слишком высоким у послеоперационного пациента с острым ишемическим инсультом и подозрением на окклюзию крупных сосудов, эндоваскулярная терапия может быть разумным и даже потенциально более безопасным вариантом.
Артериальная пункция несжимаемого сосуда
Артериальная пункция несжимаемого сосуда в течение 7 дней до появления симптомов острого инсульта является предупреждением для вкладыша Activase (альтеплаза, rtPA) и является относительным противопоказанием к внутривенному введению rtPA в соответствии с рекомендациями AHA. 1 Этот сценарий встречается крайне редко и, скорее всего, имеет место у тяжелобольных пациентов, которым недавно была проведена катетеризация подключичной или внутренней яремной вены. Другие ситуации, в которых осуществляется доступ к несжимаемым венам, — это установка электродов для стимуляции или дефибрилляции, диализных катетеров, катетеров легочной артерии или транскатетерной установки сердечного клапана.Пациент, подвергающийся одной из этих процедур, может быть менее функциональным и более больным, чем общая популяция, в которой изучалась внутривенная rtPA, и соотношение рисков к потенциальной пользе в этой подгруппе также может существенно отличаться. Обычное клиническое наблюдение увеличения кровотечения у пациентов с антикоагулянтной терапией, которым установлены центральные венозные катетеры, и потенциальные последствия неконтролируемого и опасного для жизни кровотечения, вероятно, оправдывают этот критерий исключения, хотя в опубликованной литературе нет данных, поддерживающих или опровергающих эту рекомендацию.
Недавнее желудочно-кишечное или мочеполовое кровотечение
В рекомендациях AHA от 2013 г. желудочно-кишечное (ЖКТ) или мочевыводящее кровотечение в течение предыдущего 21 дня рассматривается как критерий относительного исключения для внутривенного введения rtPA при остром ишемическом инсульте. Активное внутреннее кровотечение — абсолютное противопоказание. «Недавнее» желудочно-кишечное или мочеполовое кровотечение считается предупреждением на этикетке препарата. Данные, относящиеся к эффективности и безопасности внутривенного введения rtPA при инсульте на фоне недавнего желудочно-кишечного кровотечения, чрезвычайно ограничены и, вероятно, подвержены ошибкам отбора и публикации.В 1 исследовании только 1 такой пациент (с гематурией) лечился внутривенным тромболизисом. Этот пациент не страдал sICH и имел mRS 1 через 90 дней. 2
Как и в случае большинства относительных противопоказаний, потенциальные риски и преимущества внутривенного тромболизиса у этой подгруппы пациентов, скорее всего, значительно варьируются в зависимости от нескольких факторов. Двадцать один день был выбран произвольно и в некоторых случаях может быть излишне осторожным. Факторы, которые следует учитывать, включают время, прошедшее с момента кровотечения, серьезность дефицита инсульта, причину и тяжесть кровотечения, а также то, какое лечение было предоставлено для предшествующего эпизода кровотечения.Пациенты с тяжелым инсультом, у которых были скрытые кровоизлияния в желудочно-кишечный тракт или мочеиспускательные органы, диффузные или мультифокальные поражения, подверженные кровотечению, могут быть более безопасными кандидатами для рассмотрения внутриартериальной терапии инсульта, поскольку риск системного внутривенного тромболизиса у этих пациентов может быть недопустимым.
Приступ в начале
Припадок в начале симптомов инсульта с постиктальными резидуальными неврологическими нарушениями в рекомендациях AHA считается относительным противопоказанием к внутривенному введению rtPA. 1 Основанием для исключения таких пациентов является то, что очаговый неврологический дефицит в этой ситуации более вероятен из-за имитации инсульта — постиктального паралича Тодда — а не острой церебральной ишемии.Однако эти сущности не исключают друг друга, поскольку приступы редко возникают в начале острого ишемического инсульта. 76 Примечательно, что риск sICH после тромболизиса имитаторов инсульта чрезвычайно низок. 77,78 Кроме того, исторические особенности изъятия в начале могут вводить в заблуждение.
Большинство данных о тромболизисе у пациентов с приступами в начале получено из ретроспективных обзоров проспективно собранных пациентов для регистров. В общей сложности почти 300 пациентов с приступом в начале получили в / в rtPA по поводу симптомов, подобных инсульту, описанных в английской литературе. 77–83 Из них sICH был зарегистрирован только у 2 пациентов, один из которых имел отдаленный анамнез хирургического удаления опухоли головного мозга. Согласно недавнему опросу, 91% неврологов, перенесших инсульт, рекомендовали бы внутривенное введение rtPA пациентам с приступами в начале появления симптомов. 84
Недавний инфаркт миокарда
Недавний острый инфаркт миокарда в анамнезе за 3 месяца до инсульта является относительным противопоказанием к внутривенному тромболизису согласно последним рекомендациям AHA, 1 , но не является противопоказанием в Европе. руководящие принципы 24 или согласно этикетке препарата.Это также не было критерием исключения в исследованиях NIND или ECASS. Основные опасения по поводу назначения rtPA этим пациентам: (1) возможность кровотечения миокарда, предрасполагающего к разрыву стенки миокарда, (2) перикардит после инфаркта миокарда, который может стать геморрагическим, и (3) возможные тромбы желудочков, которые могут эмболизироваться из-за лизиса. Разрыв стенки миокарда является редким осложнением инфаркта миокарда и становится еще реже, поскольку немедленное вмешательство стало стандартом при инфаркте миокарда с подъемом сегмента ST (ИМпST).Разрыв стенки происходит только после трансмурального инфаркта, и самый высокий риск — в течение 2–5 дней. Когда пациенты получают внутривенный лизис по показаниям на ИМ, нет большой разницы между частотой разрыва сердца среди тех, кто получает тромболизис (1-8%), и тех, кто не получает тромболизис (1-5%). 85
Данных о тромболизисе при инсульте при недавно перенесенном инфаркте миокарда очень мало, и большая часть того, что сообщается, представляет собой отчеты о клинических случаях, несомненно, подверженных предвзятости публикации.В отчетах о клинических случаях описаны 5 пожилых женщин, у которых после приема rtPA по поводу инсульта развился разрыв сердца и гемоперикард. Только у одной из них недавно был хорошо задокументированный ИМ — у 93-летней женщины с сопутствующим ИМпST. 86 У другого пациента была операция по аортокоронарному шунтированию 16 дней назад, а у другого была одышка за несколько дней до обращения с неспецифическими изменениями на электрокардиограмме. 87 Из 5, 4 закончились смертельным исходом. 86–88 Внезапная гипотензия, возникающая примерно через 30 минут — 2 часа после завершения rtPA, должна вызывать подозрение на это осложнение.
После инфаркта миокарда фиброз и рубцевание миокарда завершаются к шестой или седьмой неделе. На основании этого было предложено сократить время после инфаркта миокарда, которое считается противопоказанием для внутривенного тромболизиса, до 7 недель. 85 Тип инфаркта миокарда, помимо тяжести симптомов инсульта, также должен влиять на процесс принятия решений. Пациенты с ИМпST, особенно те, у которых не затрагивается передняя сердечная стенка, могут иметь более низкий риск этого осложнения, но достоверных данных для оценки рисков или направления лечения в этой подгруппе пациентов нет.
Структурные поражения центральной нервной системы
Наличие внутричерепного новообразования, АВМ или аневризмы является противопоказанием в соответствии с рекомендациями AHA и этикеткой препарата. Риски внутривенного введения rtPA пациентам с инсультом и внутричерепными новообразованиями малоизвестны. Опубликованная литература ограничена описаниями случаев, большинство из которых были «успешными». 16,89–91 Случаи с достаточной детализацией описаны в. Был опубликован только 1 пациент, у которого была ICH, пациент с мультиформной глиобластомой височной доли, которая не была известна и проявлялась как умеренный массовый эффект на исходной компьютерной томографии. 92 В дополнение к подробным отчетам о случаях, несколько других были включены в более крупные отчеты о пациентах, которые получали rtPA не по назначению по поводу инсульта. Например, внутривенный тромболизис без sICH был проведен еще 3 пациентам с менингиомами, 1 — с холестеатомой и 1 — с опухолью околоносовых органов. 16 Имеется также несколько сообщений о пациентах с внутричерепными новообразованиями (менингиомы и аденома гипофиза), которым проводили внутривенный тромболизис по поводу ИМпST или тромбоэмболии легочной артерии. 93–95 Примечательно, что, несмотря на более высокую дозу литиков и сопутствующую системную антикоагуляцию, у этих пациентов не было ICH. Следует снова признать возможность систематической ошибки публикации, но эти случаи показывают, что внутривенный тромболизис может быть безопасным для некоторых пациентов с внутричерепными новообразованиями, особенно если новообразование относительно небольшое и расположено вне оси.
Таблица 1.
Краткое описание пациентов с опухолями головного мозга, получавших ТРА.
| Возраст / пол | Показания к лизису | NIHSS | Расположение опухоли | Размер опухоли, см | Тип опухоли | ICH | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Neil | CPE | CP10 | 3.3 × 1,3 | Невринома слухового нерва | Нет | ||||||||||||||
| Нил | 74 / F | Инсульт | 13 | Парафальцин | н / д | Менингиома | Менингиома | Менингиома | Инсульт | 7 | Височная доля | «Очень маленький» | GBM | Нет | |||||
| Grimm | 80 / M | Ход | 9039 n / aGBM | sICH | |||||||||||||||
| Hsieh | 60 / F | Ход | 11 | Лобное основание черепа | 2.0 | Менингиома | Отсутствует | ||||||||||||
| Etgen | 72 / F | Инсульт | 12 | Фронтальный | 2,5 | Менингиома | — | Гипофиз | 1,8 × 1,5 | Аденома гипофиза | Нет | ||||||||
| Рубенштейн | 77 / F | ИМпST | — | н / д | 0.8 × 0,8 | Менингиома | Отсутствует | ||||||||||||
| Jaffe | 62 / F | ИМпST | — | CPA | 1,0 | Менингиома | 9039 | — | Височная доля | 2,5 | GBM | Нет |
О безопасности внутривенного тромболизиса у пациентов с неразорвавшимися внутричерепными аневризмами сообщалось в отчетах о клинических случаях или в ретроспективных сериях случаев ().Частота sICH статистически не различалась между пациентами с аневризмами (0–13%) и без них (1–10%), но объем выборки невелик. 96–98,100 В английской литературе не сообщалось о случаях разрыва аневризмы, вызванных внутривенным введением rtPA. Хотя необходимо учитывать вероятность смещения отбора и смещения публикации, эти серии предполагают, что в / в rtPA можно безопасно вводить пациентам с неразорвавшимися случайными внутричерепными аневризмами. Следует отметить отсутствие данных о риске ВЧГ у пациентов с большими или гигантскими аневризмами, что может быть связано с более высоким риском.
Таблица 2.
Сводная информация о частоте внутричерепных кровотечений у зарегистрированных пациентов с внутричерепными аневризмами, которым был проведен внутривенный тромболизис при инсульте.
| Пациенты с аневризмой, n | sICH аневризма, n (%) | sICH без аневризмы, n (%) | любая аневризма ICH, n (%) | любая ICH аневризма, n (%) | |
|---|---|---|---|---|---|
| 96 | 22 | 0 (0) | 10 (4.7) | 3 (13,6) | 41 (19,1) |
| 97 | 8 | 1 (12,5) | 6 (3,7) | нет данных | нет данных |
| 98 | 10 | 1 (10) | 1 (1,1) | 2 (20) | 9 (9,5) |
| 99 | 8 | 1 (12,5) | н / д | 3 (37,5) | 63 (33,9) |
Деменция
Деменция не была включена в список критериев исключения в большинстве крупных исследований тромболизиса и не упоминается как противопоказание для rtPA в текущих рекомендациях по острому инсульту.Тем не менее, в рутинной клинической практике часто возникает вопрос, является ли внутривенное введение rtPA безопасным и эффективным у пациентов с деменцией и острым ишемическим инсультом. Исходная деменция связана с более низким использованием rtPA, 99 , и это связано с восприятием того, что она повышает риск кровотечения и вряд ли принесет пользу. 101 Фактические данные, хотя и ограниченные, не подтверждают эти утверждения.
Неудивительно, что деменция связана с худшими исходами после инсульта 102,103 даже среди пациентов, которым проводят тромболизис. 103 Однако деменция сама по себе, по-видимому, не увеличивает риск смерти (при выписке, 30 дней или даже 1 год) или госпитализации и связана только с тенденцией к большей функциональной инвалидности, когда анализ соответствующим образом скорректирован с учетом кофакторов. . 103 Точно так же деменция не увеличивала значительно риск ВЧГ по сравнению с подобранной контрольной группой в 2 исследованиях, анализирующих большие группы пациентов. 99,104
Следовательно, представляется безопасным назначать тромболизис пациентам с острым инсультом и предшествующей деменцией.Еще предстоит выяснить, является ли тромболизис эффективным для улучшения функциональных результатов у этих пациентов. Таким образом, решение о назначении rtPA должно приниматься индивидуально в зависимости от предыдущего уровня функции и тяжести дефицита инсульта.
Абсолютные и относительные противопоказания к внутривенному введению rt-PA при остром ишемическом инсульте
Abstract
Большинство противопоказаний к внутривенному (IV) введению рекомбинантного тканевого активатора плазминогена (rtPA) возникли в качестве критериев исключения в крупных исследованиях инсульта.Они были получены на основе консенсуса экспертов в исследовании Национального института неврологических расстройств и инсульта (NINDS). Несмотря на то, что безопасность и эффективность внутривенного введения rtPA неоднократно подтверждались в крупных международных обсервационных исследованиях за последние 20 лет, большинство пациентов с острым ишемическим инсультом, к сожалению, все еще не получают тромболитического лечения. Некоторые из исходных критериев исключения оказались излишне ограничивающими в реальной клинической практике. Было высказано предположение, что применение ослабленных критериев исключения может увеличить скорость внутривенного тромболизиса до 20% с результатами, сопоставимыми с тромболизисом с более традиционными критериями.Мы рассматриваем абсолютные и относительные противопоказания к внутривенному введению rtPA при остром ишемическом инсульте, обсуждая основную причину и доказательства, подтверждающие эти критерии исключения.
Ключевые слова: острый инсульт, тромболитическая терапия, тканевой активатор плазминогена, противопоказания
Абсолютные противопоказания
Острое внутричерепное кровоизлияние
Обнаружение внутричерепного кровоизлияния (ВЧК) при визуализации головного мозга является абсолютным противопоказанием для внутривенного введения рекомбинантных изображений головного мозга. тканевый активатор плазминогена (rtPA) при остром ишемическом инсульте в последних рекомендациях Американской кардиологической ассоциации (AHA) и на этикетке препарата Activase (alteplase, rtPA) (Genentech, Inc.). 1 Это включает внутрипаренхимальное кровоизлияние, субарахноидальное кровоизлияние, внутрижелудочковое кровоизлияние, эпидуральную гематому, субдуральную гематому или геморрагическую конверсию инфаркта. Нет опубликованных отчетов или исследований, оценивающих безопасность внутривенного введения rtPA в таких условиях, поскольку риски явно перевешивают любые потенциальные преимущества.
История ICH
Как в руководстве AHA, 2013 г., так и на этикетке препарата Activase (альтеплаза, rtPA) считается, что наличие ICH в анамнезе является абсолютным противопоказанием. 1 Имеется мало данных о рисках лизиса в этой популяции, и они, вероятно, значительно варьируются в зависимости от индивидуальных характеристик пациента. Несколько случаев опубликованы в крупных обзорах пациентов, получавших тромболизис «не по назначению». В одном обзоре с участием 499 пациентов у 3 в анамнезе был ВЧГ. 2 Ни у одного из этих пациентов не было симптоматического ICH (sICH) после тромболизиса. Двое из них достигли благоприятного функционального результата через 3 месяца. 2 В другом исследовании, в котором рассматривались 135 пациентов, которые лечились rtPA, несмотря на формальные противопоказания, у 3 пациентов в анамнезе имелась ВЧГ, а у одного из них была sICH. 3 Риск внутривенного введения rtPA у пациентов с вероятным ICH в анамнезе варьируется в зависимости от нескольких индивидуальных факторов, включая (1) время, прошедшее с момента ICH, (2) причину предшествующей ICH и было ли проведено окончательное лечение (например, клипирование или намотка аневризмы или артериовенозной мальформации [АВМ]), (3) хирургическая эвакуация гематомы и (4) объем остаточной энцефаломаляции. Мы думаем, что при некоторых обстоятельствах может быть разумным введение rtPA внутривенно, но соотношение пользы и риска следует оценивать на индивидуальной основе.
Использование последовательностей, взвешенных по чувствительности, в магнитно-резонансной томографии (МРТ) увеличило обнаружение бессимптомных церебральных микрокровоизлияний. В исследованиях инсульта без тромболизиса количество микрокровоизлияний коррелирует с частотой ICH, 4 , но наличие известных микрокровоизлияний не является противопоказанием для внутривенного введения rtPA. Одно крупное многоцентровое исследование объединило анализ данных МРТ пациентов, получавших тромболизис внутривенно. 5 Всего 242 микрокровоизлияния было идентифицировано с помощью изображений, взвешенных по T2 *, у 86 (15%) из 570 пациентов.Доля пациентов с sICH была выше среди пациентов с микрокровоизлиянием (5,8%) по сравнению с пациентами без микрокровоизлияний (2,7%), но эта разница не была статистически значимой. 5 Принимая во внимание имеющиеся данные, нельзя отказывать пациентам в внутривенном введении rtPA из-за микрокровоизлияний, обнаруженных на МРТ.
Тяжелая неконтролируемая гипертензия
Неконтролируемая гипертензия до значений, превышающих систолическое давление 185 мм рт. 1 Вероятно, это получено из критерия исключения для исследований Национального института неврологических расстройств и инсульта (NINDS). 6 Взаимосвязь между артериальным давлением (АД), антигипертензивной терапией и клиническими исходами при остром инсульте сложна. В нескольких исследованиях артериальная гипертензия была связана с повышенным риском неблагоприятных исходов и ICH. 7–9 В регистре безопасного проведения лечения инсульта (SITS) более высокое систолическое АД (САД) после лизиса было независимо связано с худшими исходами и повышенным риском ICH. 7 Связь между САД и sICH была линейной, тогда как связь между САД и клиническим исходом была U-образной. В ретроспективном анализе исследования NINDS антигипертензивная терапия, назначенная с до тромболизиса , не была связана с различиями в результатах. Однако у пациентов с артериальной гипертензией, получавших антигипертензивные препараты после рандомизации , вероятность благоприятного исхода через 3 месяца была ниже. 10
Результаты других исследований показывают, что исходное АД не является независимым предиктором ВЧГ или неблагоприятных исходов. 11–13 В 1 исследовании с участием 351 пациента, получавшего rtPA, более высокое САД перед лечением было связано с худшими показателями реканализации, но САД не было независимо связано с исходом. 12 У пациентов, получавших rtPA из раннего опыта в районе Кливленда, не было существенной разницы в доле с тяжелой гипертензией между пациентами с sICH и без. 14 Тяжелая гипертензия не должна препятствовать лечению внутривенным введением rtPA пациентов с острым инсультом, при условии, что ее можно контролировать с помощью гипотензивных препаратов.Использование гипотензивных средств для достижения контроля АД у пациентов до rtPA представляется безопасным.
Серьезная травма головы или инсульт в предыдущие 3 месяца
Руководящие принципы AHA и этикетка препарата от 2013 года рассматривают значительную травму головы или инсульт в течение предшествующих 3 месяцев как критерии исключения для внутривенного введения rtPA при остром инсульте. 1 Посттравматический инфаркт головного мозга регистрируется у 2–10% пациентов с тяжелой травмой головы, но назначение тромболитиков этой группе населения вызывает беспокойство.Пациенты с травмами часто имеют коагулопатию. Системные травмы и переломы могут увеличить риск системных геморрагических осложнений. Ушибы головного мозга, переломы черепа, диффузное повреждение аксонов и травматический ICH могут увеличить риск ICH. В небольшом обзоре пациентов, получавших лечение с нарушением протокола, 1 пациент прошел лечение внутривенным тромболизисом через 3 недели после перенесенной тяжелой травмы головы и получил смертельный sICH. 15 Два крупных европейских ретроспективных исследования пациентов, получавших rtPA внутривенно не по назначению, включали очень небольшое количество пациентов с недавней травмой головы, но не сообщалось никаких подробностей, специфичных для этой популяции. 16,17 Хотя данные крайне ограничены, мы считаем этот критерий исключения разумным, поскольку риски в этой настройке, вероятно, чрезмерно высоки.
Предполагается, что пациенты с острым инсультом, недавно перенесшие ишемический инсульт в течение предыдущих 3 месяцев, подвержены более высокому риску ВЧГ при внутривенном введении rtPA. Эти пациенты были исключены из исторического исследования NINDs. 6 Эффективность и безопасность в таких ситуациях в значительной степени неизвестны и, вероятно, сильно различаются с учетом индивидуальных характеристик, таких как размер и механизм перенесенного инфаркта, возраст и тяжесть повторного инсульта.Редко сообщалось о случаях, когда пациенты получали rtPA внутривенно по поводу инсульта дважды в течение 3 месяцев. В одном отчете подробно описывается пациент, который успешно лечился второй дозой (уменьшенной до 50 мг) внутривенного введения rtPA через 90 часов после первой дозы после повторной окклюзии артерии. У этого пациента исход благоприятный. 18 При периоде полужизни в плазме α, составляющем приблизительно 5 минут, rtPA быстро выводится из кровотока при нормальных метаболических условиях. 18 Повторный внутривенный тромболизис может быть целесообразным в некоторых случаях, особенно при небольшом объеме перенесенного инфаркта, но риски неизвестны.
Тромбоцитопения и коагулопатия
Тромбоцитопения
Хотя нет необходимости ждать подсчета тромбоцитов перед внутривенным введением rtPA, если нет подозрения на тромбоцитопению, количество тромбоцитов <100000 / мм 3 является противопоказанием для внутривенного введения rtPA в соответствии с рекомендациями AHA и вкладышем по лекарствам. 1 Геморрагические осложнения у пациентов с тромбоцитопенией, получающих rtPA внутривенно, не оценивались ни в проспективном, ни в рандомизированном исследовании.Из 14 306 пациентов из нескольких исследований, только приблизительно 20 пациентов с тромбоцитами <100 000 мм 3 , получавших rtPA внутривенно по поводу инсульта, были описаны подробно. 2,3,19,20 Из них только у 1 пациента был зарегистрирован sICH, но чрезвычайно небольшое количество опубликованных случаев не позволяет сделать однозначных выводов о безопасности внутривенного тромболизиса в этом случае.
Коагулопатия
Точно так же мало данных об эффективности или безопасности внутривенного введения rtPA при остром инсульте в условиях аномальных тестов на коагуляцию.Риск всех типов кровотечений может повышаться при внутривенном введении rtPA, если пациенту вводят системную антикоагулянтную терапию. Наличие активного кровоточащего диатеза или коагулопатии является противопоказанием к внутривенному введению rtPA для лечения острого ишемического инсульта. 1 Подозрение на коагулопатию обычно связано с антикоагулянтной терапией. Другие потенциальные причины включают цирроз печени, терминальную стадию почечной недостаточности, гематологические злокачественные новообразования, дефицит витамина К, сепсис и синдром антифосфолипидных антител.Кардиологи обнаружили ранний успех многогранного подхода к лечению острой окклюзии коронарных артерий путем сочетания антикоагуляции с системным фибринолизом, хотя более высокие значения активированного частичного тромбопластинового времени (АЧТВ) (и более высокие дозы гепарина) были связаны с более высокими показателями ICH. 21 Данных о пациентах с инсультом с длительным АЧТВ, которые лечились внутривенным введением rtPA, немного. Всего в английской литературе описано около 162 пациентов, а о sICH — у 6 (3.7%) пациенты. 2,11,15,19,20 Как ни странно, в этом анализе была статистически значимая разница в шансах на благоприятный исход при внутривенном тромболизисе, который благоприятствовал пациентам с пролонгированным АЧТВ (отношение шансов [OR] 1,57, 95% доверительный интервал [ CI] 1.02–2.41). 20 Одним из самых крупных отдельных исследований с участием пациентов было проспективное исследование тромболизиса в клинической практике в 57 медицинских центрах США. 11 О специфическом aPTT во время внутривенного введения rtPA в этих исследованиях, как правило, не сообщалось. 19,11
Согласно последним рекомендациям AHA, «текущее использование антикоагулянта с международным нормализационным коэффициентом (INR)> 1,7 или частичным тромбопластином (PT)> 15 секунд» является абсолютным противопоказанием к внутривенному лечению rtPA. 1 Приблизительно 115 пациентов с инсультом, леченным варфарином, с МНО> 1,7 на момент внутривенного тромболизиса, были зарегистрированы в английской литературе, главным образом из крупных регистров. 2,11,15,17,19,20,22,23 Из них sICH был зарегистрирован только у 1 пациента.Большинство исследований не предоставили информацию о частоте каких-либо ICH или функциональных исходов, поскольку эти пациенты изучались среди более крупных групп. Повышенное МНО может быть вызвано другими расстройствами, такими как заболевание печени или гематологические нарушения. В одном большом анализе 2755 тромболизированных пациентов, объединенных из испытаний, было 138 пациентов с МНО> 1,7 от любой причины и еще 14 с МНО> 1,7 из-за пероральной антикоагулянтной терапии. 20 У 138 пациентов с высоким МНО по причинам, не связанным с антикоагулянтами, шансы на более благоприятный исход для тромболизированных пациентов по сравнению с контрольной группой после поправки на возраст и исходный уровень NIHSS немного выше у пациентов с МНО> 1.7, но это различие не было статистически значимым (OR 1,21, 95% CI 0,82–1,78). Непонятно, почему наблюдается тенденция к повышению показателей благоприятного исхода у пациентов с пролонгированным МНО и АЧТВ. Предположительно, возможно, что это были очень хорошо отобранные пациенты с относительно низким риском геморрагической трансформации, и что дополнительный антикоагулянтный эффект фактически улучшил реканализацию.
Безопасность внутривенного введения rtPA у пациентов с инсультом, принимающих варфарин, у которых во время инсульта наблюдается субтерапевтическое МНО, оспаривается.Текущие руководящие принципы AHA / Американской ассоциации инсульта допускают внутривенное лечение rtPA для пациентов, получавших лечение в течение 3 часов с момента начала заболевания с МНО ≤1,7, 1 , в то время как европейская лицензия указывает, что это противопоказано, если пациент принимает пероральные антикоагулянты независимо от МНО. 24 Два относительно небольших многоцентровых регистра и несколько одноцентровых серий случаев показали широкий разброс показателей sICH (0–36%) у пациентов, принимавших варфарин с субтерапевтическим МНО во время тромболизиса. 2,25–31 В 2 метаанализах, самый крупный из которых включал 284 пациента, OR для sICH был увеличен для пациентов, принимавших варфарин (OR 2,6, 95% CI 1,1-5,9 и скорректированное OR 4,1 [1-16,1 ]), но оба этих анализа не были скорректированы с учетом потенциальных искажающих факторов. 30,32 Данные из 2 крупных регистров (Get-With-The-Guidelines и SITSr) показывают, что, хотя у пациентов, принимающих варфарин, действительно более высокие общие показатели sICH, чем у тех, кто не принимает варфарин, когда такие факторы, как тяжесть инсульта, пожилой возраст, и сопутствующие заболевания, лечение варфарином в условиях субтерапевтического МНО не увеличивает независимо риск sICH. 22,23
Низкомолекулярный гепарин
Низкомолекулярные гепарины (НМГ) действуют дольше и обладают большей биодоступностью, чем нефракционированный гепарин. Внутривенный тромболизис при инсульте противопоказан, если пациент принимает терапевтические дозы НМГ из-за предполагаемого высокого риска геморрагических осложнений. Сообщений о внутривенном тромболизисе у пациентов, принимающих НМГ, в литературе мало. Одно исследование включало 21 тромболизированного пациента, получавшего НМГ, 18 из которых получали дозу в течение предшествующих 24 часов. 25 Однако большинство из них принимали профилактические дозы, и только 5 из них были прописаны в терапевтических дозах. Внутричерепное кровоизлияние произошло у 8 (38%; у 3 были симптомы). Семь (33%) достигли благоприятного исхода и 6 (29%) умерли. По сравнению с пациентами, не принимавшими антикоагулянты, у тех, кто принимал НМГ, вероятность sICH была на 8,4 выше (95% ДИ 2,2–32,2), на 5,3 выше вероятность смерти (95% ДИ 1,8–15,5) и на 68% ниже вероятность независимости через 3 месяца. 25 Однако большинство из этих пациентов были госпитализированы во время инсульта, и у них могли быть сопутствующие заболевания, которые искажали ассоциации.О других случаях очень небольшого числа пациентов на НМГ, получавших тромболизис, сообщается как о частях более крупных исследований, в которых не было случаев ICH. 2 Наиболее разумно избегать внутривенного введения rtPA, если пациент получил терапевтическую дозу LMWH в течение предыдущих 24 часов.
Прямые ингибиторы тромбина
Дабигатран и аргатробан напрямую ингибируют тромбин, предотвращая образование фибрина из фибриногена. Привлекательность прямых ингибиторов тромбина по сравнению с традиционными антагонистами витамина К многофакторна: более предсказуемая фармакокинетика, отсутствие необходимости в рутинном лабораторном мониторинге, меньшее количество лекарств-взаимодействий и, возможно, повышение экономической эффективности. 33 Безопасность и эффективность внутривенного введения rtPA у пациентов, принимавших прямые ингибиторы тромбина, изучены недостаточно. Более того, если кровотечения все же возникают, стратегии лечения и отмены антикоагуляции остаются спорными.
Опубликованный опыт ограничен в основном описаниями случаев. 34–39 Сообщалось только об 1 ICH со смертельным исходом. Прямые ингибиторы тромбина также изучались в качестве адъюванта к rtPA внутривенно для лечения острого ишемического инсульта.В пилотном исследовании 65 пациентов с острым инсультом, получавших Аргатробан вместе с внутривенным введением rtPA, sICH произошел у 3 (4,6%) пациентов. 40 Из-за таких ограниченных данных о дабигатране и внутривенном введении rtPA безопасность и эффективность тромболизиса у пациентов, принимающих прямые ингибиторы тромбина, неизвестны. Хотя INR и pTT не являются достаточно надежными индикаторами антикоагулянтного эффекта дабигатрана, тромбиновое время (TT) чувствительно к наличию активности дабигатрана. 41 Основываясь на нашем текущем понимании фармакокинетики, внутривенное введение rtPA может считаться разумным в некоторых случаях, если у пациентов нормальные TT, aPTT и PT, но это должно стать предметом будущих исследований.
Ингибиторы фактора Ха
Клиницисты могут ожидать увеличения числа пациентов, получающих антикоагулянтную терапию пероральными ингибиторами фактора Ха апиксабаном или ривароксабаном. Было показано, что эти агенты превосходят (апиксабан) или не уступают (ривароксабан) варфарину в предотвращении вторичного инсульта, связанного с фибрилляцией предсердий, и уменьшения кровотечений. 42,43 Прямые ингибиторы фактора Ха могут продлевать ПВ и АЧТВ, но не с достаточной надежностью для точной оценки антикоагулянтных эффектов.В некоторых случаях может проводиться осторожное лечение в соответствии с периодом полувыведения лекарства, но до тех пор, пока не будет доступен надежный и быстрый метод измерения их антикоагулянтного эффекта, следует предполагать, что пациенты, принимающие эти лекарства, имеют более высокий риск, чем обычный. Учитывая, что было зарегистрировано так мало пациентов и что большая часть данных поступает из реестров или исследований, в которых вероятна систематическая ошибка, мы думаем, что эти пациенты не должны регулярно получать rtPA внутривенно, если они не являются частью научных исследований.
Тяжелая гипогликемия или гипергликемия
Измерение уровня глюкозы в крови является необходимым условием перед внутривенным введением rtPA. Основная причина этого состояния — исключение тяжелой гипогликемии, которая редко может имитировать симптомы инсульта. Еще реже тяжелая гипергликемия может вызвать очаговый неврологический дефицит. Предыдущие версии рекомендаций AHA по лечению острого инсульта указывали уровни глюкозы ниже 50 мг / дл (2,7 ммоль / л) и выше 400 мг / дл (22,2 ммоль / л) в качестве противопоказаний для тромболизиса, но в самом последнем издании гипогликемия указывается только как исключение. 1 Между тем, вкладыш в упаковке Управления по контролю за продуктами и лекарствами (FDA) для Activase (alteplase, rtPA) рекомендует «с особой тщательностью» диагностировать инсульт у пациентов с уровнем глюкозы <50 или> 400 мг / дл.
На практике опытные эксперты путают тяжелую гипогликемию с инсультом. Хотя очаговые нарушения (в частности, гемипарез) могут возникать, они обычно связаны с изменением сознания или судорогами. Пациенты также отличаются потливостью.Быстрое разрешение после введения декстрозы является диагностическим. Области ограниченной диффузии могут быть вызваны эпизодами гипогликемии, но обычно они двусторонние и наблюдаются у пациентов в коме. 44 Гипергликемия часто встречается у пациентов с острым инсультом и может быть тяжелой у пациентов с диабетом. Тем не менее, это исключительно причина очагового неврологического дефицита при отсутствии изменений в уровне настороженности.
Еще одна причина для измерения уровня глюкозы в крови заключается в том, что гипогликемия и гипергликемия могут усугубить ишемию головного мозга, а гипергликемия также связана с уменьшением шансов реканализации и повышенным риском ICH. 45–48 Стойкая гипергликемия, а не только исходная гипергликемия, может быть в большей степени связана с этими пагубными эффектами. 44 Хотя нет доказательств того, что экстренная коррекция гипергликемии может улучшить исходы при остром ишемическом инсульте или облегчить реканализацию, кажется разумным лечить гипергликемию (например, стремясь к уровню глюкозы <180-200 мг / дл), пока она вызывает строго следует избегать гипогликемии любой степени.
Безопасность тромболизиса у пациентов с тяжелой гипогликемией или гипогликемией изучена недостаточно.В большом анализе Virtual International Stroke Trials Registry (VISTA) только 9 пациентов с глюкозой <50 мг / дл (5 получали rtPA) и 23 - глюкозой> 400 мг / дл (6 получали rtPA) были идентифицированы среди Всего на учете 9613 пациентов. 20 В этих небольших подгруппах пациентов тромболизис не повлиял на исходы, и среди пролеченных не было случаев sICH.
Таким образом, нет убедительных доказательств, чтобы рассматривать нарушения уровня глюкозы в качестве противопоказаний для внутривенного введения rtPA.Целесообразно лечить rtPA пациентов с подозрением на инсульт и тяжелой гипергликемией. Мы также считаем целесообразным лечить пациентов с симптомами инсульта и тяжелой гипогликемией, состояние которых не улучшается сразу после инфузии декстрозы.
Ранние рентгенологические ишемические изменения
Признаки ранней ишемии на первичной компьютерной томографии (КТ) головы не являются абсолютным противопоказанием к внутривенному введению rtPA пациентам с инсультом, но это вызывает разногласия.В рекомендациях AHA от 2013 г. рекомендуется проводить внутривенный тромболизис, если эти изменения присутствуют, независимо от их степени. 1 Признаки ранней ишемии (потеря четкости определения базальных ганглиев, сглаживание борозды, очаговое набухание и масс-эффект, а также потеря четкости соединения серого и белого вещества) необходимо отличать от областей явной гипоплотности, указывающих на установлен инфаркт головного мозга. Целью тромболизиса является реперфузия ишемической, но жизнеспособной паренхимы головного мозга (полутень).Пациенты со значительным «несоответствием» между областью относительно небольшого центрального инфаркта и большей площадью окружающей полутени являются пациентами, которым может помочь rtPA, независимо от того, есть ли тонкие рентгенологические свидетельства ишемических изменений. Хотя сейчас доступны более новые методы визуализации — КТ и МРТ-сканирование перфузии — они более трудозатратны и требуют больше времени, чем неконтрастная КТ. Не было показано, что лечение под контролем перфузионной визуализации улучшает исходы у пациентов, получающих rtPA.Таким образом, мы не думаем, что визуализация перфузии должна выполняться в рутинной практике у пациентов до внутривенного тромболизиса. В нашей практике мы используем визуализацию перфузии у отдельных пациентов; например, для пациентов с симптомами с неясной датой начала, такими как «инсульты при пробуждении».
В отличие от едва различимых рентгенологических признаков ранней ишемии, явная гипоплотность на КТ отражает более тяжелое и необратимое повреждение головного мозга и увеличивает риск геморрагической трансформации. Если участки с пониженной плотностью охватывают более одной трети пораженного полушария головного мозга, внутривенный тромболизис противопоказан и не должен применяться. 1 Оценить степень ишемии по сравнению с инфарктом не всегда просто. Даже среди опытных нейрорадиологов и неврологов согласие между экспертами определить, затрагивает ли ишемия менее или более одной трети территории средней мозговой артерии (СМА), является лишь умеренным (κ. 4). 49 Результаты апостериорного анализа Европейского совместного исследования острого инсульта (ECASS) показали, что степень гипоаттенуации на КТ головы была предиктором ответа на тромболизис. 50 Пациенты с областями гипоаттенуации, поражающими менее или равной одной трети территории СМА, имели повышенные шансы на благоприятный исход (OR 3,43, 95% ДИ 1,61-7,33), тогда как пациенты с областями гипоаттенуации, охватывающими более одной трети на территории MCA наблюдалось нестатистически значимое снижение шансов на благоприятный исход (OR 0,41, 95% CI 0,06–2,70). Кроме того, что, вероятно, объясняет связь с клиническими исходами, повышался риск sICH. 50
Относительные противопоказания
Пожилой возраст
На вкладыше к препарату Activase (alteplase, rtPA) указан «пожилой возраст (например, старше 75 лет)» в качестве предупреждения о том, что риск внутривенного rtPA может возрасти. Пожилой возраст не считается противопоказанием или исключением в рекомендациях AHA. 1 Из пациентов, включенных в ранние клинические испытания внутривенного тромболизиса при инсульте, только около 0,5% были старше 80 лет. 51 Исследование NINDS специально не исключало пожилых пациентов, но средний возраст составлял 69 лет. 6 Верхний предел для включения в испытания ECASS составлял 80 лет. 52–54 Возраст является независимым фактором риска неблагоприятного исхода у пациентов с ишемическим инсультом, независимо от того, вводится ли rtPA внутривенно. Краткосрочная и долгосрочная смертность в два раза выше у пациентов старше 85 лет по сравнению с более молодыми пациентами. 55,56
Третье международное исследование инсульта (IST-3), международное рандомизированное контролируемое исследование, включало 1617 пациентов старше 80 лет. 57 Пациенты были рандомизированы в группу rtPA или плацебо в течение 6 часов после появления симптомов. Первичной конечной точкой была доля пациентов, выживших и независимых через 6 месяцев, которые существенно не различались между двумя группами (37% в группе rtPA и 35% в контрольной группе [ P = 0,181]). В анализе подгрупп существенная разница существовала в скорректированном эффекте лечения между пациентами старше 80 лет и пациентами моложе, что свидетельствует о большей пользе у очень пожилых пациентов.Кроме того, систематический обзор, в котором анализировались 7012 пациентов из 12 исследований, показал, что пациенты старше 80 лет выздоравливали так же, как и те, кто моложе, особенно когда лечение было начато раньше.
Другое исследование включало 3472 тромболизированных пациента старше 80 лет из Международного регистра тромболизиса инсульта и сравнивало их с контрольными пациентами из регистра нейропротективного лечения VISTA. 58 Распределение баллов по шкале mRS через 3 месяца было лучше у пациентов с тромболизацией как у очень пожилых, так и у более молодых пациентов.
Достаточно последовательное сообщение было получено из нескольких наблюдательных исследований: восьмидесятилетние и девяностолетние имеют более высокий уровень смертности и меньше шансов на достижение благоприятных результатов, чем пациенты <80, но схожие показатели sICH. 16,59–63 Более низкие показатели хороших результатов могут частично отражать многочисленные сопутствующие заболевания у пожилых пациентов, а также их пониженную способность восстанавливать функции через реабилитацию. В нескольких исследованиях подгруппы пожилых людей имели статистически значимо более высокие показатели застойной сердечной недостаточности, ишемической болезни сердца и гипертонии. 60,62,64,65
Таким образом, существующие данные не поддерживают исключение пациентов старше 80 лет из приема rtPA по поводу острого инсульта. Благоприятные исходы встречаются реже, а уровень смертности выше, но это также верно для нелеченных пациентов и может отражать рост сопутствующих заболеваний и меньший потенциал для реабилитации. Ставки sICH сопоставимы. Профиль безопасности rtPA у очень пожилых пациентов в большинстве исследований предполагает, что можно надлежащим образом отбирать пожилых пациентов для тромболизиса, и наилучшие имеющиеся данные показывают, что польза, получаемая от внутривенного введения rtPA, не уменьшается.
Легкие или улучшающиеся симптомы инсульта
Хотя легкие или быстро улучшающиеся неврологические расстройства часто указывались в качестве критерия относительного исключения для внутривенного тромболизиса, а этикетка FDA не рекомендует использование активазы (альтеплазы, rtPA) для незначительных симптомов инсульта. данные показывают, что от 20% до 30% пациентов с легкими или улучшающимися симптомами, когда рассматривается тромболизис, могут иметь значительную нетрудоспособность через 3 месяца. 66–68 Легкие инсульты в литературе часто определяются по шкале NIHSS ≤4.Однако это оперативное определение не всегда представляет собой незначительные недостатки для пациента. Например, тяжелый монопарез (даже потеря ловкости рук для человека в зависимости от его способности выполнять свою работу), дисбаланс походки, афазия или серьезный дефицит поля зрения — все это может изолированно отключать дефицит, и в этих случаях NIHSS будет ≤ 4. Кроме того, у некоторых пациентов с легкими симптомами может быть окклюзия проксимального внутричерепного сосуда, и они подвергаются большему риску неврологического ухудшения и стойкой инвалидности. 68,69 Пациенты с ранним улучшением дефицита могут также иметь больше шансов на последующее неврологическое снижение. 70
Текущие руководства AHA заявляют, что внутривенный тромболизис может рассматриваться у пациентов с легким инсультом и у пациентов с быстро улучшающимися симптомами (класс IIb, уровень доказательности C), и рекомендуют дальнейшие исследования для уточнения значения тромболизиса у этих пациентов. 1 Ограниченные данные свидетельствуют о том, что тромболизис безопасен и эффективен у пациентов с легким инсультом, в том числе результаты основополагающего исследования NINDS, в котором фактически участвовала меньшая часть пациентов с NIHSS ≤4. 71,72 Многоцентровое проспективное, рандомизированное и двойное слепое исследование PRISMS в настоящее время проводится для оценки того, улучшает ли внутривенное введение активазы (альтеплаза, rtPA) в течение 3 часов после появления симптомов исходы у пациентов с легким инсультом (определяется как NIHSS). ≤ 5).
До тех пор, пока не появятся дополнительные доказательства, мы считаем наиболее разумным решить, проводить ли тромболизис, исходя из значимости текущего дефицита (независимо от того, улучшается ли он) для конкретного человека.Если у пациента будут ограничения в жизни, если дефицит останется, мы выбираем лечение тромболизисом. Для пациентов с быстро улучшающимися симптомами, у которых тромболизис не считается необходимым, но у которых изначально был тяжелый дефицит, целесообразно рассмотреть возможность получения изображения сосудов, чтобы исключить окклюзию проксимальной артерии, пока пациент все еще находится в отделении неотложной помощи.
Тяжелый инсульт и кома
Первоначальная тяжесть дефицита является основным фактором, определяющим исход инсульта, независимо от того, проводился ли тромболизис.Тяжелые инсульты (по-разному определяемые как NIHSS> 20 или> 25) обычно вызваны обширными инфарктами, которые могут иметь более высокий риск геморрагической трансформации. Это отражено во вкладыше FDA для Activase (alteplase, rtPA), предупреждающем, что риск ICH выше у пациентов с тяжелым инсультом. Однако есть убедительные доказательства того, что внутривенный тромболизис полезен для пациентов с тяжелым инсультом, и на самом деле эти пациенты могут получить наибольшую пользу от лечения.
Анализ данных NINDS показал, что внутривенное введение rtPA было связано с улучшением результатов у пациентов с NIHSS> 20. 73 В небольшой подгруппе пациентов с NIHSS> 25 в IST-3 положительный эффект внутривенного тромболизиса усиливался, даже когда пациенты были включены в исследование в течение 6 часов после появления симптомов. 57 Аналогичным образом, при анализе 9613 пациентов в VISTA, у тех, у кого NIHSS> 22, были более высокие шансы на лучший функциональный результат. 20 Это неудивительно. Само собой разумеется, что пациенты с очень тяжелым дефицитом имеют гораздо меньше шансов восстановить хорошую функцию, если не произойдет своевременная реперфузия.
Хотя, вероятно, правда, что тяжелые инсульты действительно несут больший риск sICH, имеющиеся доказательства не являются окончательными. Не все исследования подтверждают повышенный риск кровотечения при тяжелом инсульте. 74 Тем не менее, реперфузионное повреждение является наиболее частым механизмом симптоматического кровотечения после тромболизиса, и у пациентов с большими участками ишемии более вероятно развитие этого типа повреждения, если тромболизис достигает реканализации. Тем не менее, вероятность благоприятного исхода увеличивается при использовании внутривенного введения rtPA после учета этого геморрагического риска.
Кома была противопоказанием для регистрации в NINDS. 6 Основанием для исключения коматозных пациентов было предотвращение включения возможных имитаторов инсульта. Хотя кома — очень редкое проявление инсульта, она может возникнуть у пациентов с окклюзией основной артерии, которым может быть полезен внутривенный тромболизис. 75 Следовательно, кома сама по себе не должна считаться противопоказанием для внутривенного введения rtPA и должна применяться при подозрении на окклюзию основной артерии.
Текущие рекомендации AHA 1 не упоминают тяжелые инсульты (или кому) как относительное противопоказание для внутривенного тромболизиса в течение 3 часов, но предостерегают от лечения пациентов с NIHSS> 25 более 3 часов, учитывая, что эти пациенты были исключены из ECASS -3 (ECASS-3 2009) и безопасность rtPA в расширенном временном окне для этих тяжелых инсультов не доказана. Мы полностью согласны с тем, что не должно быть порогового значения, выше которого не показан тромболизис, по крайней мере, в течение 3 часов с момента появления симптомов.
Недавняя серьезная операция
На вкладыше Activase (alteplase, rtPA) перечислены недавние серьезные операции (например, коронарное шунтирование, родоразрешение и биопсия органа) в качестве предупреждения, но не абсолютного противопоказания. В рекомендациях AHA это также считается относительным противопоказанием, 1 , но оно не указано в качестве противопоказания в Рекомендациях Европейской инициативы по борьбе с инсультом. 24 Произвольные определения терминов «недавний» и «крупный» могут быть проблематичными, а временные рамки, используемые в крупных исследованиях, различались.Например, в исследование NINDS были исключены пациенты, перенесшие серьезную операцию в течение предыдущих 14 дней, 6 , в то время как в исследование ECASS исключены пациенты, перенесшие серьезную операцию в течение предшествующих 3 месяцев. 52,54
Проблема внутривенного введения rtPA пациентам, которые недавно перенесли операцию, связана с риском кровотечения в хирургическом койке. Несмотря на то, что это очевидно обоснованное беспокойство, следует рассмотреть конкретный тип и место операции, а также способность контролировать возможные кровотечения, прежде чем отказываться от варианта внутривенного введения rtPA.Конечно, тяжесть инсульта также должна приниматься во внимание при оценке предполагаемых рисков и преимуществ тромболизиса в этих случаях.
Доказательств, прямо подтверждающих это противопоказание, мало. Есть несколько исследований пациентов, которым вводили rtPA не по инструкции по поводу острого инсульта, которые включали небольшие группы пациентов, перенесших недавнюю операцию. В одном из них 8 пациентов перенесли операцию в течение 3 месяцев. 2 В этой очень небольшой группе показатели sICH (1 из 8) и неблагоприятных исходов (3 из 8) не были чрезмерно высокими.Примечательно, что ни у одного из этих пациентов не было системного кровотечения, что якобы является причиной исключения этих пациентов из внутривенного лизиса.
В регистре инсульта, который включал 1104 пациентов с инсультом, леченным rtPA, 13 перенесли хирургическое вмешательство или травму в течение предшествующих 3 месяцев. У пациентов, перенесших недавнюю операцию, было 2 системных кровотечения — 1 после имплантации кардиостимулятора и 1 после перианальной операции. Обоим пациентам сделали переливание крови, но серьезных кровотечений не было. 16 Дополнительные случаи указывают на то, что кровотечение в месте недавней операции может потребовать инвазивных вмешательств — для достижения гемостаза или эвакуации гематомы — и переливания крови, но все же совместимо с благоприятным неврологическим восстановлением. Данные о тромболизисе у пациентов с острым инсультом немногочисленны, и, несомненно, существует некоторая предвзятость публикаций в отношении сообщения о случаях без серьезных осложнений. Каждого пациента необходимо оценивать индивидуально. Если риск системного кровотечения из-за внутривенного тромболизиса считается слишком высоким у послеоперационного пациента с острым ишемическим инсультом и подозрением на окклюзию крупных сосудов, эндоваскулярная терапия может быть разумным и даже потенциально более безопасным вариантом.
Артериальная пункция несжимаемого сосуда
Артериальная пункция несжимаемого сосуда в течение 7 дней до появления симптомов острого инсульта является предупреждением для вкладыша Activase (альтеплаза, rtPA) и является относительным противопоказанием к внутривенному введению rtPA в соответствии с рекомендациями AHA. 1 Этот сценарий встречается крайне редко и, скорее всего, имеет место у тяжелобольных пациентов, которым недавно была проведена катетеризация подключичной или внутренней яремной вены. Другие ситуации, в которых осуществляется доступ к несжимаемым венам, — это установка электродов для стимуляции или дефибрилляции, диализных катетеров, катетеров легочной артерии или транскатетерной установки сердечного клапана.Пациент, подвергающийся одной из этих процедур, может быть менее функциональным и более больным, чем общая популяция, в которой изучалась внутривенная rtPA, и соотношение рисков к потенциальной пользе в этой подгруппе также может существенно отличаться. Обычное клиническое наблюдение увеличения кровотечения у пациентов с антикоагулянтной терапией, которым установлены центральные венозные катетеры, и потенциальные последствия неконтролируемого и опасного для жизни кровотечения, вероятно, оправдывают этот критерий исключения, хотя в опубликованной литературе нет данных, поддерживающих или опровергающих эту рекомендацию.
Недавнее желудочно-кишечное или мочеполовое кровотечение
В рекомендациях AHA от 2013 г. желудочно-кишечное (ЖКТ) или мочевыводящее кровотечение в течение предыдущего 21 дня рассматривается как критерий относительного исключения для внутривенного введения rtPA при остром ишемическом инсульте. Активное внутреннее кровотечение — абсолютное противопоказание. «Недавнее» желудочно-кишечное или мочеполовое кровотечение считается предупреждением на этикетке препарата. Данные, относящиеся к эффективности и безопасности внутривенного введения rtPA при инсульте на фоне недавнего желудочно-кишечного кровотечения, чрезвычайно ограничены и, вероятно, подвержены ошибкам отбора и публикации.В 1 исследовании только 1 такой пациент (с гематурией) лечился внутривенным тромболизисом. Этот пациент не страдал sICH и имел mRS 1 через 90 дней. 2
Как и в случае большинства относительных противопоказаний, потенциальные риски и преимущества внутривенного тромболизиса у этой подгруппы пациентов, скорее всего, значительно варьируются в зависимости от нескольких факторов. Двадцать один день был выбран произвольно и в некоторых случаях может быть излишне осторожным. Факторы, которые следует учитывать, включают время, прошедшее с момента кровотечения, серьезность дефицита инсульта, причину и тяжесть кровотечения, а также то, какое лечение было предоставлено для предшествующего эпизода кровотечения.Пациенты с тяжелым инсультом, у которых были скрытые кровоизлияния в желудочно-кишечный тракт или мочеиспускательные органы, диффузные или мультифокальные поражения, подверженные кровотечению, могут быть более безопасными кандидатами для рассмотрения внутриартериальной терапии инсульта, поскольку риск системного внутривенного тромболизиса у этих пациентов может быть недопустимым.
Приступ в начале
Припадок в начале симптомов инсульта с постиктальными резидуальными неврологическими нарушениями в рекомендациях AHA считается относительным противопоказанием к внутривенному введению rtPA. 1 Основанием для исключения таких пациентов является то, что очаговый неврологический дефицит в этой ситуации более вероятен из-за имитации инсульта — постиктального паралича Тодда — а не острой церебральной ишемии.Однако эти сущности не исключают друг друга, поскольку приступы редко возникают в начале острого ишемического инсульта. 76 Примечательно, что риск sICH после тромболизиса имитаторов инсульта чрезвычайно низок. 77,78 Кроме того, исторические особенности изъятия в начале могут вводить в заблуждение.
Большинство данных о тромболизисе у пациентов с приступами в начале получено из ретроспективных обзоров проспективно собранных пациентов для регистров. В общей сложности почти 300 пациентов с приступом в начале получили в / в rtPA по поводу симптомов, подобных инсульту, описанных в английской литературе. 77–83 Из них sICH был зарегистрирован только у 2 пациентов, один из которых имел отдаленный анамнез хирургического удаления опухоли головного мозга. Согласно недавнему опросу, 91% неврологов, перенесших инсульт, рекомендовали бы внутривенное введение rtPA пациентам с приступами в начале появления симптомов. 84
Недавний инфаркт миокарда
Недавний острый инфаркт миокарда в анамнезе за 3 месяца до инсульта является относительным противопоказанием к внутривенному тромболизису согласно последним рекомендациям AHA, 1 , но не является противопоказанием в Европе. руководящие принципы 24 или согласно этикетке препарата.Это также не было критерием исключения в исследованиях NIND или ECASS. Основные опасения по поводу назначения rtPA этим пациентам: (1) возможность кровотечения миокарда, предрасполагающего к разрыву стенки миокарда, (2) перикардит после инфаркта миокарда, который может стать геморрагическим, и (3) возможные тромбы желудочков, которые могут эмболизироваться из-за лизиса. Разрыв стенки миокарда является редким осложнением инфаркта миокарда и становится еще реже, поскольку немедленное вмешательство стало стандартом при инфаркте миокарда с подъемом сегмента ST (ИМпST).Разрыв стенки происходит только после трансмурального инфаркта, и самый высокий риск — в течение 2–5 дней. Когда пациенты получают внутривенный лизис по показаниям на ИМ, нет большой разницы между частотой разрыва сердца среди тех, кто получает тромболизис (1-8%), и тех, кто не получает тромболизис (1-5%). 85
Данных о тромболизисе при инсульте при недавно перенесенном инфаркте миокарда очень мало, и большая часть того, что сообщается, представляет собой отчеты о клинических случаях, несомненно, подверженных предвзятости публикации.В отчетах о клинических случаях описаны 5 пожилых женщин, у которых после приема rtPA по поводу инсульта развился разрыв сердца и гемоперикард. Только у одной из них недавно был хорошо задокументированный ИМ — у 93-летней женщины с сопутствующим ИМпST. 86 У другого пациента была операция по аортокоронарному шунтированию 16 дней назад, а у другого была одышка за несколько дней до обращения с неспецифическими изменениями на электрокардиограмме. 87 Из 5, 4 закончились смертельным исходом. 86–88 Внезапная гипотензия, возникающая примерно через 30 минут — 2 часа после завершения rtPA, должна вызывать подозрение на это осложнение.
После инфаркта миокарда фиброз и рубцевание миокарда завершаются к шестой или седьмой неделе. На основании этого было предложено сократить время после инфаркта миокарда, которое считается противопоказанием для внутривенного тромболизиса, до 7 недель. 85 Тип инфаркта миокарда, помимо тяжести симптомов инсульта, также должен влиять на процесс принятия решений. Пациенты с ИМпST, особенно те, у которых не затрагивается передняя сердечная стенка, могут иметь более низкий риск этого осложнения, но достоверных данных для оценки рисков или направления лечения в этой подгруппе пациентов нет.
Структурные поражения центральной нервной системы
Наличие внутричерепного новообразования, АВМ или аневризмы является противопоказанием в соответствии с рекомендациями AHA и этикеткой препарата. Риски внутривенного введения rtPA пациентам с инсультом и внутричерепными новообразованиями малоизвестны. Опубликованная литература ограничена описаниями случаев, большинство из которых были «успешными». 16,89–91 Случаи с достаточной детализацией описаны в. Был опубликован только 1 пациент, у которого была ICH, пациент с мультиформной глиобластомой височной доли, которая не была известна и проявлялась как умеренный массовый эффект на исходной компьютерной томографии. 92 В дополнение к подробным отчетам о случаях, несколько других были включены в более крупные отчеты о пациентах, которые получали rtPA не по назначению по поводу инсульта. Например, внутривенный тромболизис без sICH был проведен еще 3 пациентам с менингиомами, 1 — с холестеатомой и 1 — с опухолью околоносовых органов. 16 Имеется также несколько сообщений о пациентах с внутричерепными новообразованиями (менингиомы и аденома гипофиза), которым проводили внутривенный тромболизис по поводу ИМпST или тромбоэмболии легочной артерии. 93–95 Примечательно, что, несмотря на более высокую дозу литиков и сопутствующую системную антикоагуляцию, у этих пациентов не было ICH. Следует снова признать возможность систематической ошибки публикации, но эти случаи показывают, что внутривенный тромболизис может быть безопасным для некоторых пациентов с внутричерепными новообразованиями, особенно если новообразование относительно небольшое и расположено вне оси.
Таблица 1.
Краткое описание пациентов с опухолями головного мозга, получавших ТРА.
| Возраст / пол | Показания к лизису | NIHSS | Расположение опухоли | Размер опухоли, см | Тип опухоли | ICH | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Neil | CPE | CP10 | 3.3 × 1,3 | Невринома слухового нерва | Нет | ||||||||||||||
| Нил | 74 / F | Инсульт | 13 | Парафальцин | н / д | Менингиома | Менингиома | Менингиома | Инсульт | 7 | Височная доля | «Очень маленький» | GBM | Нет | |||||
| Grimm | 80 / M | Ход | 9039 n / aGBM | sICH | |||||||||||||||
| Hsieh | 60 / F | Ход | 11 | Лобное основание черепа | 2.0 | Менингиома | Отсутствует | ||||||||||||
| Etgen | 72 / F | Инсульт | 12 | Фронтальный | 2,5 | Менингиома | — | Гипофиз | 1,8 × 1,5 | Аденома гипофиза | Нет | ||||||||
| Рубенштейн | 77 / F | ИМпST | — | н / д | 0.8 × 0,8 | Менингиома | Отсутствует | ||||||||||||
| Jaffe | 62 / F | ИМпST | — | CPA | 1,0 | Менингиома | 9039 | — | Височная доля | 2,5 | GBM | Нет |
О безопасности внутривенного тромболизиса у пациентов с неразорвавшимися внутричерепными аневризмами сообщалось в отчетах о клинических случаях или в ретроспективных сериях случаев ().Частота sICH статистически не различалась между пациентами с аневризмами (0–13%) и без них (1–10%), но объем выборки невелик. 96–98,100 В английской литературе не сообщалось о случаях разрыва аневризмы, вызванных внутривенным введением rtPA. Хотя необходимо учитывать вероятность смещения отбора и смещения публикации, эти серии предполагают, что в / в rtPA можно безопасно вводить пациентам с неразорвавшимися случайными внутричерепными аневризмами. Следует отметить отсутствие данных о риске ВЧГ у пациентов с большими или гигантскими аневризмами, что может быть связано с более высоким риском.
Таблица 2.
Сводная информация о частоте внутричерепных кровотечений у зарегистрированных пациентов с внутричерепными аневризмами, которым был проведен внутривенный тромболизис при инсульте.
| Пациенты с аневризмой, n | sICH аневризма, n (%) | sICH без аневризмы, n (%) | любая аневризма ICH, n (%) | любая ICH аневризма, n (%) | |
|---|---|---|---|---|---|
| 96 | 22 | 0 (0) | 10 (4.7) | 3 (13,6) | 41 (19,1) |
| 97 | 8 | 1 (12,5) | 6 (3,7) | нет данных | нет данных |
| 98 | 10 | 1 (10) | 1 (1,1) | 2 (20) | 9 (9,5) |
| 99 | 8 | 1 (12,5) | н / д | 3 (37,5) | 63 (33,9) |
Деменция
Деменция не была включена в список критериев исключения в большинстве крупных исследований тромболизиса и не упоминается как противопоказание для rtPA в текущих рекомендациях по острому инсульту.Тем не менее, в рутинной клинической практике часто возникает вопрос, является ли внутривенное введение rtPA безопасным и эффективным у пациентов с деменцией и острым ишемическим инсультом. Исходная деменция связана с более низким использованием rtPA, 99 , и это связано с восприятием того, что она повышает риск кровотечения и вряд ли принесет пользу. 101 Фактические данные, хотя и ограниченные, не подтверждают эти утверждения.
Неудивительно, что деменция связана с худшими исходами после инсульта 102,103 даже среди пациентов, которым проводят тромболизис. 103 Однако деменция сама по себе, по-видимому, не увеличивает риск смерти (при выписке, 30 дней или даже 1 год) или госпитализации и связана только с тенденцией к большей функциональной инвалидности, когда анализ соответствующим образом скорректирован с учетом кофакторов. . 103 Точно так же деменция не увеличивала значительно риск ВЧГ по сравнению с подобранной контрольной группой в 2 исследованиях, анализирующих большие группы пациентов. 99,104
Следовательно, представляется безопасным назначать тромболизис пациентам с острым инсультом и предшествующей деменцией.Еще предстоит выяснить, является ли тромболизис эффективным для улучшения функциональных результатов у этих пациентов. Таким образом, решение о назначении rtPA должно приниматься индивидуально в зависимости от предыдущего уровня функции и тяжести дефицита инсульта.
Абсолютные и относительные противопоказания к внутривенному введению rt-PA при остром ишемическом инсульте
Abstract
Большинство противопоказаний к внутривенному (IV) введению рекомбинантного тканевого активатора плазминогена (rtPA) возникли в качестве критериев исключения в крупных исследованиях инсульта.Они были получены на основе консенсуса экспертов в исследовании Национального института неврологических расстройств и инсульта (NINDS). Несмотря на то, что безопасность и эффективность внутривенного введения rtPA неоднократно подтверждались в крупных международных обсервационных исследованиях за последние 20 лет, большинство пациентов с острым ишемическим инсультом, к сожалению, все еще не получают тромболитического лечения. Некоторые из исходных критериев исключения оказались излишне ограничивающими в реальной клинической практике. Было высказано предположение, что применение ослабленных критериев исключения может увеличить скорость внутривенного тромболизиса до 20% с результатами, сопоставимыми с тромболизисом с более традиционными критериями.Мы рассматриваем абсолютные и относительные противопоказания к внутривенному введению rtPA при остром ишемическом инсульте, обсуждая основную причину и доказательства, подтверждающие эти критерии исключения.
Ключевые слова: острый инсульт, тромболитическая терапия, тканевой активатор плазминогена, противопоказания
Абсолютные противопоказания
Острое внутричерепное кровоизлияние
Обнаружение внутричерепного кровоизлияния (ВЧК) при визуализации головного мозга является абсолютным противопоказанием для внутривенного введения рекомбинантных изображений головного мозга. тканевый активатор плазминогена (rtPA) при остром ишемическом инсульте в последних рекомендациях Американской кардиологической ассоциации (AHA) и на этикетке препарата Activase (alteplase, rtPA) (Genentech, Inc.). 1 Это включает внутрипаренхимальное кровоизлияние, субарахноидальное кровоизлияние, внутрижелудочковое кровоизлияние, эпидуральную гематому, субдуральную гематому или геморрагическую конверсию инфаркта. Нет опубликованных отчетов или исследований, оценивающих безопасность внутривенного введения rtPA в таких условиях, поскольку риски явно перевешивают любые потенциальные преимущества.
История ICH
Как в руководстве AHA, 2013 г., так и на этикетке препарата Activase (альтеплаза, rtPA) считается, что наличие ICH в анамнезе является абсолютным противопоказанием. 1 Имеется мало данных о рисках лизиса в этой популяции, и они, вероятно, значительно варьируются в зависимости от индивидуальных характеристик пациента. Несколько случаев опубликованы в крупных обзорах пациентов, получавших тромболизис «не по назначению». В одном обзоре с участием 499 пациентов у 3 в анамнезе был ВЧГ. 2 Ни у одного из этих пациентов не было симптоматического ICH (sICH) после тромболизиса. Двое из них достигли благоприятного функционального результата через 3 месяца. 2 В другом исследовании, в котором рассматривались 135 пациентов, которые лечились rtPA, несмотря на формальные противопоказания, у 3 пациентов в анамнезе имелась ВЧГ, а у одного из них была sICH. 3 Риск внутривенного введения rtPA у пациентов с вероятным ICH в анамнезе варьируется в зависимости от нескольких индивидуальных факторов, включая (1) время, прошедшее с момента ICH, (2) причину предшествующей ICH и было ли проведено окончательное лечение (например, клипирование или намотка аневризмы или артериовенозной мальформации [АВМ]), (3) хирургическая эвакуация гематомы и (4) объем остаточной энцефаломаляции. Мы думаем, что при некоторых обстоятельствах может быть разумным введение rtPA внутривенно, но соотношение пользы и риска следует оценивать на индивидуальной основе.
Использование последовательностей, взвешенных по чувствительности, в магнитно-резонансной томографии (МРТ) увеличило обнаружение бессимптомных церебральных микрокровоизлияний. В исследованиях инсульта без тромболизиса количество микрокровоизлияний коррелирует с частотой ICH, 4 , но наличие известных микрокровоизлияний не является противопоказанием для внутривенного введения rtPA. Одно крупное многоцентровое исследование объединило анализ данных МРТ пациентов, получавших тромболизис внутривенно. 5 Всего 242 микрокровоизлияния было идентифицировано с помощью изображений, взвешенных по T2 *, у 86 (15%) из 570 пациентов.Доля пациентов с sICH была выше среди пациентов с микрокровоизлиянием (5,8%) по сравнению с пациентами без микрокровоизлияний (2,7%), но эта разница не была статистически значимой. 5 Принимая во внимание имеющиеся данные, нельзя отказывать пациентам в внутривенном введении rtPA из-за микрокровоизлияний, обнаруженных на МРТ.
Тяжелая неконтролируемая гипертензия
Неконтролируемая гипертензия до значений, превышающих систолическое давление 185 мм рт. 1 Вероятно, это получено из критерия исключения для исследований Национального института неврологических расстройств и инсульта (NINDS). 6 Взаимосвязь между артериальным давлением (АД), антигипертензивной терапией и клиническими исходами при остром инсульте сложна. В нескольких исследованиях артериальная гипертензия была связана с повышенным риском неблагоприятных исходов и ICH. 7–9 В регистре безопасного проведения лечения инсульта (SITS) более высокое систолическое АД (САД) после лизиса было независимо связано с худшими исходами и повышенным риском ICH. 7 Связь между САД и sICH была линейной, тогда как связь между САД и клиническим исходом была U-образной. В ретроспективном анализе исследования NINDS антигипертензивная терапия, назначенная с до тромболизиса , не была связана с различиями в результатах. Однако у пациентов с артериальной гипертензией, получавших антигипертензивные препараты после рандомизации , вероятность благоприятного исхода через 3 месяца была ниже. 10
Результаты других исследований показывают, что исходное АД не является независимым предиктором ВЧГ или неблагоприятных исходов. 11–13 В 1 исследовании с участием 351 пациента, получавшего rtPA, более высокое САД перед лечением было связано с худшими показателями реканализации, но САД не было независимо связано с исходом. 12 У пациентов, получавших rtPA из раннего опыта в районе Кливленда, не было существенной разницы в доле с тяжелой гипертензией между пациентами с sICH и без. 14 Тяжелая гипертензия не должна препятствовать лечению внутривенным введением rtPA пациентов с острым инсультом, при условии, что ее можно контролировать с помощью гипотензивных препаратов.Использование гипотензивных средств для достижения контроля АД у пациентов до rtPA представляется безопасным.
Серьезная травма головы или инсульт в предыдущие 3 месяца
Руководящие принципы AHA и этикетка препарата от 2013 года рассматривают значительную травму головы или инсульт в течение предшествующих 3 месяцев как критерии исключения для внутривенного введения rtPA при остром инсульте. 1 Посттравматический инфаркт головного мозга регистрируется у 2–10% пациентов с тяжелой травмой головы, но назначение тромболитиков этой группе населения вызывает беспокойство.Пациенты с травмами часто имеют коагулопатию. Системные травмы и переломы могут увеличить риск системных геморрагических осложнений. Ушибы головного мозга, переломы черепа, диффузное повреждение аксонов и травматический ICH могут увеличить риск ICH. В небольшом обзоре пациентов, получавших лечение с нарушением протокола, 1 пациент прошел лечение внутривенным тромболизисом через 3 недели после перенесенной тяжелой травмы головы и получил смертельный sICH. 15 Два крупных европейских ретроспективных исследования пациентов, получавших rtPA внутривенно не по назначению, включали очень небольшое количество пациентов с недавней травмой головы, но не сообщалось никаких подробностей, специфичных для этой популяции. 16,17 Хотя данные крайне ограничены, мы считаем этот критерий исключения разумным, поскольку риски в этой настройке, вероятно, чрезмерно высоки.
Предполагается, что пациенты с острым инсультом, недавно перенесшие ишемический инсульт в течение предыдущих 3 месяцев, подвержены более высокому риску ВЧГ при внутривенном введении rtPA. Эти пациенты были исключены из исторического исследования NINDs. 6 Эффективность и безопасность в таких ситуациях в значительной степени неизвестны и, вероятно, сильно различаются с учетом индивидуальных характеристик, таких как размер и механизм перенесенного инфаркта, возраст и тяжесть повторного инсульта.Редко сообщалось о случаях, когда пациенты получали rtPA внутривенно по поводу инсульта дважды в течение 3 месяцев. В одном отчете подробно описывается пациент, который успешно лечился второй дозой (уменьшенной до 50 мг) внутривенного введения rtPA через 90 часов после первой дозы после повторной окклюзии артерии. У этого пациента исход благоприятный. 18 При периоде полужизни в плазме α, составляющем приблизительно 5 минут, rtPA быстро выводится из кровотока при нормальных метаболических условиях. 18 Повторный внутривенный тромболизис может быть целесообразным в некоторых случаях, особенно при небольшом объеме перенесенного инфаркта, но риски неизвестны.
Тромбоцитопения и коагулопатия
Тромбоцитопения
Хотя нет необходимости ждать подсчета тромбоцитов перед внутривенным введением rtPA, если нет подозрения на тромбоцитопению, количество тромбоцитов <100000 / мм 3 является противопоказанием для внутривенного введения rtPA в соответствии с рекомендациями AHA и вкладышем по лекарствам. 1 Геморрагические осложнения у пациентов с тромбоцитопенией, получающих rtPA внутривенно, не оценивались ни в проспективном, ни в рандомизированном исследовании.Из 14 306 пациентов из нескольких исследований, только приблизительно 20 пациентов с тромбоцитами <100 000 мм 3 , получавших rtPA внутривенно по поводу инсульта, были описаны подробно. 2,3,19,20 Из них только у 1 пациента был зарегистрирован sICH, но чрезвычайно небольшое количество опубликованных случаев не позволяет сделать однозначных выводов о безопасности внутривенного тромболизиса в этом случае.
Коагулопатия
Точно так же мало данных об эффективности или безопасности внутривенного введения rtPA при остром инсульте в условиях аномальных тестов на коагуляцию.Риск всех типов кровотечений может повышаться при внутривенном введении rtPA, если пациенту вводят системную антикоагулянтную терапию. Наличие активного кровоточащего диатеза или коагулопатии является противопоказанием к внутривенному введению rtPA для лечения острого ишемического инсульта. 1 Подозрение на коагулопатию обычно связано с антикоагулянтной терапией. Другие потенциальные причины включают цирроз печени, терминальную стадию почечной недостаточности, гематологические злокачественные новообразования, дефицит витамина К, сепсис и синдром антифосфолипидных антител.Кардиологи обнаружили ранний успех многогранного подхода к лечению острой окклюзии коронарных артерий путем сочетания антикоагуляции с системным фибринолизом, хотя более высокие значения активированного частичного тромбопластинового времени (АЧТВ) (и более высокие дозы гепарина) были связаны с более высокими показателями ICH. 21 Данных о пациентах с инсультом с длительным АЧТВ, которые лечились внутривенным введением rtPA, немного. Всего в английской литературе описано около 162 пациентов, а о sICH — у 6 (3.7%) пациенты. 2,11,15,19,20 Как ни странно, в этом анализе была статистически значимая разница в шансах на благоприятный исход при внутривенном тромболизисе, который благоприятствовал пациентам с пролонгированным АЧТВ (отношение шансов [OR] 1,57, 95% доверительный интервал [ CI] 1.02–2.41). 20 Одним из самых крупных отдельных исследований с участием пациентов было проспективное исследование тромболизиса в клинической практике в 57 медицинских центрах США. 11 О специфическом aPTT во время внутривенного введения rtPA в этих исследованиях, как правило, не сообщалось. 19,11
Согласно последним рекомендациям AHA, «текущее использование антикоагулянта с международным нормализационным коэффициентом (INR)> 1,7 или частичным тромбопластином (PT)> 15 секунд» является абсолютным противопоказанием к внутривенному лечению rtPA. 1 Приблизительно 115 пациентов с инсультом, леченным варфарином, с МНО> 1,7 на момент внутривенного тромболизиса, были зарегистрированы в английской литературе, главным образом из крупных регистров. 2,11,15,17,19,20,22,23 Из них sICH был зарегистрирован только у 1 пациента.Большинство исследований не предоставили информацию о частоте каких-либо ICH или функциональных исходов, поскольку эти пациенты изучались среди более крупных групп. Повышенное МНО может быть вызвано другими расстройствами, такими как заболевание печени или гематологические нарушения. В одном большом анализе 2755 тромболизированных пациентов, объединенных из испытаний, было 138 пациентов с МНО> 1,7 от любой причины и еще 14 с МНО> 1,7 из-за пероральной антикоагулянтной терапии. 20 У 138 пациентов с высоким МНО по причинам, не связанным с антикоагулянтами, шансы на более благоприятный исход для тромболизированных пациентов по сравнению с контрольной группой после поправки на возраст и исходный уровень NIHSS немного выше у пациентов с МНО> 1.7, но это различие не было статистически значимым (OR 1,21, 95% CI 0,82–1,78). Непонятно, почему наблюдается тенденция к повышению показателей благоприятного исхода у пациентов с пролонгированным МНО и АЧТВ. Предположительно, возможно, что это были очень хорошо отобранные пациенты с относительно низким риском геморрагической трансформации, и что дополнительный антикоагулянтный эффект фактически улучшил реканализацию.
Безопасность внутривенного введения rtPA у пациентов с инсультом, принимающих варфарин, у которых во время инсульта наблюдается субтерапевтическое МНО, оспаривается.Текущие руководящие принципы AHA / Американской ассоциации инсульта допускают внутривенное лечение rtPA для пациентов, получавших лечение в течение 3 часов с момента начала заболевания с МНО ≤1,7, 1 , в то время как европейская лицензия указывает, что это противопоказано, если пациент принимает пероральные антикоагулянты независимо от МНО. 24 Два относительно небольших многоцентровых регистра и несколько одноцентровых серий случаев показали широкий разброс показателей sICH (0–36%) у пациентов, принимавших варфарин с субтерапевтическим МНО во время тромболизиса. 2,25–31 В 2 метаанализах, самый крупный из которых включал 284 пациента, OR для sICH был увеличен для пациентов, принимавших варфарин (OR 2,6, 95% CI 1,1-5,9 и скорректированное OR 4,1 [1-16,1 ]), но оба этих анализа не были скорректированы с учетом потенциальных искажающих факторов. 30,32 Данные из 2 крупных регистров (Get-With-The-Guidelines и SITSr) показывают, что, хотя у пациентов, принимающих варфарин, действительно более высокие общие показатели sICH, чем у тех, кто не принимает варфарин, когда такие факторы, как тяжесть инсульта, пожилой возраст, и сопутствующие заболевания, лечение варфарином в условиях субтерапевтического МНО не увеличивает независимо риск sICH. 22,23
Низкомолекулярный гепарин
Низкомолекулярные гепарины (НМГ) действуют дольше и обладают большей биодоступностью, чем нефракционированный гепарин. Внутривенный тромболизис при инсульте противопоказан, если пациент принимает терапевтические дозы НМГ из-за предполагаемого высокого риска геморрагических осложнений. Сообщений о внутривенном тромболизисе у пациентов, принимающих НМГ, в литературе мало. Одно исследование включало 21 тромболизированного пациента, получавшего НМГ, 18 из которых получали дозу в течение предшествующих 24 часов. 25 Однако большинство из них принимали профилактические дозы, и только 5 из них были прописаны в терапевтических дозах. Внутричерепное кровоизлияние произошло у 8 (38%; у 3 были симптомы). Семь (33%) достигли благоприятного исхода и 6 (29%) умерли. По сравнению с пациентами, не принимавшими антикоагулянты, у тех, кто принимал НМГ, вероятность sICH была на 8,4 выше (95% ДИ 2,2–32,2), на 5,3 выше вероятность смерти (95% ДИ 1,8–15,5) и на 68% ниже вероятность независимости через 3 месяца. 25 Однако большинство из этих пациентов были госпитализированы во время инсульта, и у них могли быть сопутствующие заболевания, которые искажали ассоциации.О других случаях очень небольшого числа пациентов на НМГ, получавших тромболизис, сообщается как о частях более крупных исследований, в которых не было случаев ICH. 2 Наиболее разумно избегать внутривенного введения rtPA, если пациент получил терапевтическую дозу LMWH в течение предыдущих 24 часов.
Прямые ингибиторы тромбина
Дабигатран и аргатробан напрямую ингибируют тромбин, предотвращая образование фибрина из фибриногена. Привлекательность прямых ингибиторов тромбина по сравнению с традиционными антагонистами витамина К многофакторна: более предсказуемая фармакокинетика, отсутствие необходимости в рутинном лабораторном мониторинге, меньшее количество лекарств-взаимодействий и, возможно, повышение экономической эффективности. 33 Безопасность и эффективность внутривенного введения rtPA у пациентов, принимавших прямые ингибиторы тромбина, изучены недостаточно. Более того, если кровотечения все же возникают, стратегии лечения и отмены антикоагуляции остаются спорными.
Опубликованный опыт ограничен в основном описаниями случаев. 34–39 Сообщалось только об 1 ICH со смертельным исходом. Прямые ингибиторы тромбина также изучались в качестве адъюванта к rtPA внутривенно для лечения острого ишемического инсульта.В пилотном исследовании 65 пациентов с острым инсультом, получавших Аргатробан вместе с внутривенным введением rtPA, sICH произошел у 3 (4,6%) пациентов. 40 Из-за таких ограниченных данных о дабигатране и внутривенном введении rtPA безопасность и эффективность тромболизиса у пациентов, принимающих прямые ингибиторы тромбина, неизвестны. Хотя INR и pTT не являются достаточно надежными индикаторами антикоагулянтного эффекта дабигатрана, тромбиновое время (TT) чувствительно к наличию активности дабигатрана. 41 Основываясь на нашем текущем понимании фармакокинетики, внутривенное введение rtPA может считаться разумным в некоторых случаях, если у пациентов нормальные TT, aPTT и PT, но это должно стать предметом будущих исследований.
Ингибиторы фактора Ха
Клиницисты могут ожидать увеличения числа пациентов, получающих антикоагулянтную терапию пероральными ингибиторами фактора Ха апиксабаном или ривароксабаном. Было показано, что эти агенты превосходят (апиксабан) или не уступают (ривароксабан) варфарину в предотвращении вторичного инсульта, связанного с фибрилляцией предсердий, и уменьшения кровотечений. 42,43 Прямые ингибиторы фактора Ха могут продлевать ПВ и АЧТВ, но не с достаточной надежностью для точной оценки антикоагулянтных эффектов.В некоторых случаях может проводиться осторожное лечение в соответствии с периодом полувыведения лекарства, но до тех пор, пока не будет доступен надежный и быстрый метод измерения их антикоагулянтного эффекта, следует предполагать, что пациенты, принимающие эти лекарства, имеют более высокий риск, чем обычный. Учитывая, что было зарегистрировано так мало пациентов и что большая часть данных поступает из реестров или исследований, в которых вероятна систематическая ошибка, мы думаем, что эти пациенты не должны регулярно получать rtPA внутривенно, если они не являются частью научных исследований.
Тяжелая гипогликемия или гипергликемия
Измерение уровня глюкозы в крови является необходимым условием перед внутривенным введением rtPA. Основная причина этого состояния — исключение тяжелой гипогликемии, которая редко может имитировать симптомы инсульта. Еще реже тяжелая гипергликемия может вызвать очаговый неврологический дефицит. Предыдущие версии рекомендаций AHA по лечению острого инсульта указывали уровни глюкозы ниже 50 мг / дл (2,7 ммоль / л) и выше 400 мг / дл (22,2 ммоль / л) в качестве противопоказаний для тромболизиса, но в самом последнем издании гипогликемия указывается только как исключение. 1 Между тем, вкладыш в упаковке Управления по контролю за продуктами и лекарствами (FDA) для Activase (alteplase, rtPA) рекомендует «с особой тщательностью» диагностировать инсульт у пациентов с уровнем глюкозы <50 или> 400 мг / дл.
На практике опытные эксперты путают тяжелую гипогликемию с инсультом. Хотя очаговые нарушения (в частности, гемипарез) могут возникать, они обычно связаны с изменением сознания или судорогами. Пациенты также отличаются потливостью.Быстрое разрешение после введения декстрозы является диагностическим. Области ограниченной диффузии могут быть вызваны эпизодами гипогликемии, но обычно они двусторонние и наблюдаются у пациентов в коме. 44 Гипергликемия часто встречается у пациентов с острым инсультом и может быть тяжелой у пациентов с диабетом. Тем не менее, это исключительно причина очагового неврологического дефицита при отсутствии изменений в уровне настороженности.
Еще одна причина для измерения уровня глюкозы в крови заключается в том, что гипогликемия и гипергликемия могут усугубить ишемию головного мозга, а гипергликемия также связана с уменьшением шансов реканализации и повышенным риском ICH. 45–48 Стойкая гипергликемия, а не только исходная гипергликемия, может быть в большей степени связана с этими пагубными эффектами. 44 Хотя нет доказательств того, что экстренная коррекция гипергликемии может улучшить исходы при остром ишемическом инсульте или облегчить реканализацию, кажется разумным лечить гипергликемию (например, стремясь к уровню глюкозы <180-200 мг / дл), пока она вызывает строго следует избегать гипогликемии любой степени.
Безопасность тромболизиса у пациентов с тяжелой гипогликемией или гипогликемией изучена недостаточно.В большом анализе Virtual International Stroke Trials Registry (VISTA) только 9 пациентов с глюкозой <50 мг / дл (5 получали rtPA) и 23 - глюкозой> 400 мг / дл (6 получали rtPA) были идентифицированы среди Всего на учете 9613 пациентов. 20 В этих небольших подгруппах пациентов тромболизис не повлиял на исходы, и среди пролеченных не было случаев sICH.
Таким образом, нет убедительных доказательств, чтобы рассматривать нарушения уровня глюкозы в качестве противопоказаний для внутривенного введения rtPA.Целесообразно лечить rtPA пациентов с подозрением на инсульт и тяжелой гипергликемией. Мы также считаем целесообразным лечить пациентов с симптомами инсульта и тяжелой гипогликемией, состояние которых не улучшается сразу после инфузии декстрозы.
Ранние рентгенологические ишемические изменения
Признаки ранней ишемии на первичной компьютерной томографии (КТ) головы не являются абсолютным противопоказанием к внутривенному введению rtPA пациентам с инсультом, но это вызывает разногласия.В рекомендациях AHA от 2013 г. рекомендуется проводить внутривенный тромболизис, если эти изменения присутствуют, независимо от их степени. 1 Признаки ранней ишемии (потеря четкости определения базальных ганглиев, сглаживание борозды, очаговое набухание и масс-эффект, а также потеря четкости соединения серого и белого вещества) необходимо отличать от областей явной гипоплотности, указывающих на установлен инфаркт головного мозга. Целью тромболизиса является реперфузия ишемической, но жизнеспособной паренхимы головного мозга (полутень).Пациенты со значительным «несоответствием» между областью относительно небольшого центрального инфаркта и большей площадью окружающей полутени являются пациентами, которым может помочь rtPA, независимо от того, есть ли тонкие рентгенологические свидетельства ишемических изменений. Хотя сейчас доступны более новые методы визуализации — КТ и МРТ-сканирование перфузии — они более трудозатратны и требуют больше времени, чем неконтрастная КТ. Не было показано, что лечение под контролем перфузионной визуализации улучшает исходы у пациентов, получающих rtPA.Таким образом, мы не думаем, что визуализация перфузии должна выполняться в рутинной практике у пациентов до внутривенного тромболизиса. В нашей практике мы используем визуализацию перфузии у отдельных пациентов; например, для пациентов с симптомами с неясной датой начала, такими как «инсульты при пробуждении».
В отличие от едва различимых рентгенологических признаков ранней ишемии, явная гипоплотность на КТ отражает более тяжелое и необратимое повреждение головного мозга и увеличивает риск геморрагической трансформации. Если участки с пониженной плотностью охватывают более одной трети пораженного полушария головного мозга, внутривенный тромболизис противопоказан и не должен применяться. 1 Оценить степень ишемии по сравнению с инфарктом не всегда просто. Даже среди опытных нейрорадиологов и неврологов согласие между экспертами определить, затрагивает ли ишемия менее или более одной трети территории средней мозговой артерии (СМА), является лишь умеренным (κ. 4). 49 Результаты апостериорного анализа Европейского совместного исследования острого инсульта (ECASS) показали, что степень гипоаттенуации на КТ головы была предиктором ответа на тромболизис. 50 Пациенты с областями гипоаттенуации, поражающими менее или равной одной трети территории СМА, имели повышенные шансы на благоприятный исход (OR 3,43, 95% ДИ 1,61-7,33), тогда как пациенты с областями гипоаттенуации, охватывающими более одной трети на территории MCA наблюдалось нестатистически значимое снижение шансов на благоприятный исход (OR 0,41, 95% CI 0,06–2,70). Кроме того, что, вероятно, объясняет связь с клиническими исходами, повышался риск sICH. 50
Относительные противопоказания
Пожилой возраст
На вкладыше к препарату Activase (alteplase, rtPA) указан «пожилой возраст (например, старше 75 лет)» в качестве предупреждения о том, что риск внутривенного rtPA может возрасти. Пожилой возраст не считается противопоказанием или исключением в рекомендациях AHA. 1 Из пациентов, включенных в ранние клинические испытания внутривенного тромболизиса при инсульте, только около 0,5% были старше 80 лет. 51 Исследование NINDS специально не исключало пожилых пациентов, но средний возраст составлял 69 лет. 6 Верхний предел для включения в испытания ECASS составлял 80 лет. 52–54 Возраст является независимым фактором риска неблагоприятного исхода у пациентов с ишемическим инсультом, независимо от того, вводится ли rtPA внутривенно. Краткосрочная и долгосрочная смертность в два раза выше у пациентов старше 85 лет по сравнению с более молодыми пациентами. 55,56
Третье международное исследование инсульта (IST-3), международное рандомизированное контролируемое исследование, включало 1617 пациентов старше 80 лет. 57 Пациенты были рандомизированы в группу rtPA или плацебо в течение 6 часов после появления симптомов. Первичной конечной точкой была доля пациентов, выживших и независимых через 6 месяцев, которые существенно не различались между двумя группами (37% в группе rtPA и 35% в контрольной группе [ P = 0,181]). В анализе подгрупп существенная разница существовала в скорректированном эффекте лечения между пациентами старше 80 лет и пациентами моложе, что свидетельствует о большей пользе у очень пожилых пациентов.Кроме того, систематический обзор, в котором анализировались 7012 пациентов из 12 исследований, показал, что пациенты старше 80 лет выздоравливали так же, как и те, кто моложе, особенно когда лечение было начато раньше.
Другое исследование включало 3472 тромболизированных пациента старше 80 лет из Международного регистра тромболизиса инсульта и сравнивало их с контрольными пациентами из регистра нейропротективного лечения VISTA. 58 Распределение баллов по шкале mRS через 3 месяца было лучше у пациентов с тромболизацией как у очень пожилых, так и у более молодых пациентов.
Достаточно последовательное сообщение было получено из нескольких наблюдательных исследований: восьмидесятилетние и девяностолетние имеют более высокий уровень смертности и меньше шансов на достижение благоприятных результатов, чем пациенты <80, но схожие показатели sICH. 16,59–63 Более низкие показатели хороших результатов могут частично отражать многочисленные сопутствующие заболевания у пожилых пациентов, а также их пониженную способность восстанавливать функции через реабилитацию. В нескольких исследованиях подгруппы пожилых людей имели статистически значимо более высокие показатели застойной сердечной недостаточности, ишемической болезни сердца и гипертонии. 60,62,64,65
Таким образом, существующие данные не поддерживают исключение пациентов старше 80 лет из приема rtPA по поводу острого инсульта. Благоприятные исходы встречаются реже, а уровень смертности выше, но это также верно для нелеченных пациентов и может отражать рост сопутствующих заболеваний и меньший потенциал для реабилитации. Ставки sICH сопоставимы. Профиль безопасности rtPA у очень пожилых пациентов в большинстве исследований предполагает, что можно надлежащим образом отбирать пожилых пациентов для тромболизиса, и наилучшие имеющиеся данные показывают, что польза, получаемая от внутривенного введения rtPA, не уменьшается.
Легкие или улучшающиеся симптомы инсульта
Хотя легкие или быстро улучшающиеся неврологические расстройства часто указывались в качестве критерия относительного исключения для внутривенного тромболизиса, а этикетка FDA не рекомендует использование активазы (альтеплазы, rtPA) для незначительных симптомов инсульта. данные показывают, что от 20% до 30% пациентов с легкими или улучшающимися симптомами, когда рассматривается тромболизис, могут иметь значительную нетрудоспособность через 3 месяца. 66–68 Легкие инсульты в литературе часто определяются по шкале NIHSS ≤4.Однако это оперативное определение не всегда представляет собой незначительные недостатки для пациента. Например, тяжелый монопарез (даже потеря ловкости рук для человека в зависимости от его способности выполнять свою работу), дисбаланс походки, афазия или серьезный дефицит поля зрения — все это может изолированно отключать дефицит, и в этих случаях NIHSS будет ≤ 4. Кроме того, у некоторых пациентов с легкими симптомами может быть окклюзия проксимального внутричерепного сосуда, и они подвергаются большему риску неврологического ухудшения и стойкой инвалидности. 68,69 Пациенты с ранним улучшением дефицита могут также иметь больше шансов на последующее неврологическое снижение. 70
Текущие руководства AHA заявляют, что внутривенный тромболизис может рассматриваться у пациентов с легким инсультом и у пациентов с быстро улучшающимися симптомами (класс IIb, уровень доказательности C), и рекомендуют дальнейшие исследования для уточнения значения тромболизиса у этих пациентов. 1 Ограниченные данные свидетельствуют о том, что тромболизис безопасен и эффективен у пациентов с легким инсультом, в том числе результаты основополагающего исследования NINDS, в котором фактически участвовала меньшая часть пациентов с NIHSS ≤4. 71,72 Многоцентровое проспективное, рандомизированное и двойное слепое исследование PRISMS в настоящее время проводится для оценки того, улучшает ли внутривенное введение активазы (альтеплаза, rtPA) в течение 3 часов после появления симптомов исходы у пациентов с легким инсультом (определяется как NIHSS). ≤ 5).
До тех пор, пока не появятся дополнительные доказательства, мы считаем наиболее разумным решить, проводить ли тромболизис, исходя из значимости текущего дефицита (независимо от того, улучшается ли он) для конкретного человека.Если у пациента будут ограничения в жизни, если дефицит останется, мы выбираем лечение тромболизисом. Для пациентов с быстро улучшающимися симптомами, у которых тромболизис не считается необходимым, но у которых изначально был тяжелый дефицит, целесообразно рассмотреть возможность получения изображения сосудов, чтобы исключить окклюзию проксимальной артерии, пока пациент все еще находится в отделении неотложной помощи.
Тяжелый инсульт и кома
Первоначальная тяжесть дефицита является основным фактором, определяющим исход инсульта, независимо от того, проводился ли тромболизис.Тяжелые инсульты (по-разному определяемые как NIHSS> 20 или> 25) обычно вызваны обширными инфарктами, которые могут иметь более высокий риск геморрагической трансформации. Это отражено во вкладыше FDA для Activase (alteplase, rtPA), предупреждающем, что риск ICH выше у пациентов с тяжелым инсультом. Однако есть убедительные доказательства того, что внутривенный тромболизис полезен для пациентов с тяжелым инсультом, и на самом деле эти пациенты могут получить наибольшую пользу от лечения.
Анализ данных NINDS показал, что внутривенное введение rtPA было связано с улучшением результатов у пациентов с NIHSS> 20. 73 В небольшой подгруппе пациентов с NIHSS> 25 в IST-3 положительный эффект внутривенного тромболизиса усиливался, даже когда пациенты были включены в исследование в течение 6 часов после появления симптомов. 57 Аналогичным образом, при анализе 9613 пациентов в VISTA, у тех, у кого NIHSS> 22, были более высокие шансы на лучший функциональный результат. 20 Это неудивительно. Само собой разумеется, что пациенты с очень тяжелым дефицитом имеют гораздо меньше шансов восстановить хорошую функцию, если не произойдет своевременная реперфузия.
Хотя, вероятно, правда, что тяжелые инсульты действительно несут больший риск sICH, имеющиеся доказательства не являются окончательными. Не все исследования подтверждают повышенный риск кровотечения при тяжелом инсульте. 74 Тем не менее, реперфузионное повреждение является наиболее частым механизмом симптоматического кровотечения после тромболизиса, и у пациентов с большими участками ишемии более вероятно развитие этого типа повреждения, если тромболизис достигает реканализации. Тем не менее, вероятность благоприятного исхода увеличивается при использовании внутривенного введения rtPA после учета этого геморрагического риска.
Кома была противопоказанием для регистрации в NINDS. 6 Основанием для исключения коматозных пациентов было предотвращение включения возможных имитаторов инсульта. Хотя кома — очень редкое проявление инсульта, она может возникнуть у пациентов с окклюзией основной артерии, которым может быть полезен внутривенный тромболизис. 75 Следовательно, кома сама по себе не должна считаться противопоказанием для внутривенного введения rtPA и должна применяться при подозрении на окклюзию основной артерии.
Текущие рекомендации AHA 1 не упоминают тяжелые инсульты (или кому) как относительное противопоказание для внутривенного тромболизиса в течение 3 часов, но предостерегают от лечения пациентов с NIHSS> 25 более 3 часов, учитывая, что эти пациенты были исключены из ECASS -3 (ECASS-3 2009) и безопасность rtPA в расширенном временном окне для этих тяжелых инсультов не доказана. Мы полностью согласны с тем, что не должно быть порогового значения, выше которого не показан тромболизис, по крайней мере, в течение 3 часов с момента появления симптомов.
Недавняя серьезная операция
На вкладыше Activase (alteplase, rtPA) перечислены недавние серьезные операции (например, коронарное шунтирование, родоразрешение и биопсия органа) в качестве предупреждения, но не абсолютного противопоказания. В рекомендациях AHA это также считается относительным противопоказанием, 1 , но оно не указано в качестве противопоказания в Рекомендациях Европейской инициативы по борьбе с инсультом. 24 Произвольные определения терминов «недавний» и «крупный» могут быть проблематичными, а временные рамки, используемые в крупных исследованиях, различались.Например, в исследование NINDS были исключены пациенты, перенесшие серьезную операцию в течение предыдущих 14 дней, 6 , в то время как в исследование ECASS исключены пациенты, перенесшие серьезную операцию в течение предшествующих 3 месяцев. 52,54
Проблема внутривенного введения rtPA пациентам, которые недавно перенесли операцию, связана с риском кровотечения в хирургическом койке. Несмотря на то, что это очевидно обоснованное беспокойство, следует рассмотреть конкретный тип и место операции, а также способность контролировать возможные кровотечения, прежде чем отказываться от варианта внутривенного введения rtPA.Конечно, тяжесть инсульта также должна приниматься во внимание при оценке предполагаемых рисков и преимуществ тромболизиса в этих случаях.
Доказательств, прямо подтверждающих это противопоказание, мало. Есть несколько исследований пациентов, которым вводили rtPA не по инструкции по поводу острого инсульта, которые включали небольшие группы пациентов, перенесших недавнюю операцию. В одном из них 8 пациентов перенесли операцию в течение 3 месяцев. 2 В этой очень небольшой группе показатели sICH (1 из 8) и неблагоприятных исходов (3 из 8) не были чрезмерно высокими.Примечательно, что ни у одного из этих пациентов не было системного кровотечения, что якобы является причиной исключения этих пациентов из внутривенного лизиса.
В регистре инсульта, который включал 1104 пациентов с инсультом, леченным rtPA, 13 перенесли хирургическое вмешательство или травму в течение предшествующих 3 месяцев. У пациентов, перенесших недавнюю операцию, было 2 системных кровотечения — 1 после имплантации кардиостимулятора и 1 после перианальной операции. Обоим пациентам сделали переливание крови, но серьезных кровотечений не было. 16 Дополнительные случаи указывают на то, что кровотечение в месте недавней операции может потребовать инвазивных вмешательств — для достижения гемостаза или эвакуации гематомы — и переливания крови, но все же совместимо с благоприятным неврологическим восстановлением. Данные о тромболизисе у пациентов с острым инсультом немногочисленны, и, несомненно, существует некоторая предвзятость публикаций в отношении сообщения о случаях без серьезных осложнений. Каждого пациента необходимо оценивать индивидуально. Если риск системного кровотечения из-за внутривенного тромболизиса считается слишком высоким у послеоперационного пациента с острым ишемическим инсультом и подозрением на окклюзию крупных сосудов, эндоваскулярная терапия может быть разумным и даже потенциально более безопасным вариантом.
Артериальная пункция несжимаемого сосуда
Артериальная пункция несжимаемого сосуда в течение 7 дней до появления симптомов острого инсульта является предупреждением для вкладыша Activase (альтеплаза, rtPA) и является относительным противопоказанием к внутривенному введению rtPA в соответствии с рекомендациями AHA. 1 Этот сценарий встречается крайне редко и, скорее всего, имеет место у тяжелобольных пациентов, которым недавно была проведена катетеризация подключичной или внутренней яремной вены. Другие ситуации, в которых осуществляется доступ к несжимаемым венам, — это установка электродов для стимуляции или дефибрилляции, диализных катетеров, катетеров легочной артерии или транскатетерной установки сердечного клапана.Пациент, подвергающийся одной из этих процедур, может быть менее функциональным и более больным, чем общая популяция, в которой изучалась внутривенная rtPA, и соотношение рисков к потенциальной пользе в этой подгруппе также может существенно отличаться. Обычное клиническое наблюдение увеличения кровотечения у пациентов с антикоагулянтной терапией, которым установлены центральные венозные катетеры, и потенциальные последствия неконтролируемого и опасного для жизни кровотечения, вероятно, оправдывают этот критерий исключения, хотя в опубликованной литературе нет данных, поддерживающих или опровергающих эту рекомендацию.
Недавнее желудочно-кишечное или мочеполовое кровотечение
В рекомендациях AHA от 2013 г. желудочно-кишечное (ЖКТ) или мочевыводящее кровотечение в течение предыдущего 21 дня рассматривается как критерий относительного исключения для внутривенного введения rtPA при остром ишемическом инсульте. Активное внутреннее кровотечение — абсолютное противопоказание. «Недавнее» желудочно-кишечное или мочеполовое кровотечение считается предупреждением на этикетке препарата. Данные, относящиеся к эффективности и безопасности внутривенного введения rtPA при инсульте на фоне недавнего желудочно-кишечного кровотечения, чрезвычайно ограничены и, вероятно, подвержены ошибкам отбора и публикации.В 1 исследовании только 1 такой пациент (с гематурией) лечился внутривенным тромболизисом. Этот пациент не страдал sICH и имел mRS 1 через 90 дней. 2
Как и в случае большинства относительных противопоказаний, потенциальные риски и преимущества внутривенного тромболизиса у этой подгруппы пациентов, скорее всего, значительно варьируются в зависимости от нескольких факторов. Двадцать один день был выбран произвольно и в некоторых случаях может быть излишне осторожным. Факторы, которые следует учитывать, включают время, прошедшее с момента кровотечения, серьезность дефицита инсульта, причину и тяжесть кровотечения, а также то, какое лечение было предоставлено для предшествующего эпизода кровотечения.Пациенты с тяжелым инсультом, у которых были скрытые кровоизлияния в желудочно-кишечный тракт или мочеиспускательные органы, диффузные или мультифокальные поражения, подверженные кровотечению, могут быть более безопасными кандидатами для рассмотрения внутриартериальной терапии инсульта, поскольку риск системного внутривенного тромболизиса у этих пациентов может быть недопустимым.
Приступ в начале
Припадок в начале симптомов инсульта с постиктальными резидуальными неврологическими нарушениями в рекомендациях AHA считается относительным противопоказанием к внутривенному введению rtPA. 1 Основанием для исключения таких пациентов является то, что очаговый неврологический дефицит в этой ситуации более вероятен из-за имитации инсульта — постиктального паралича Тодда — а не острой церебральной ишемии.Однако эти сущности не исключают друг друга, поскольку приступы редко возникают в начале острого ишемического инсульта. 76 Примечательно, что риск sICH после тромболизиса имитаторов инсульта чрезвычайно низок. 77,78 Кроме того, исторические особенности изъятия в начале могут вводить в заблуждение.
Большинство данных о тромболизисе у пациентов с приступами в начале получено из ретроспективных обзоров проспективно собранных пациентов для регистров. В общей сложности почти 300 пациентов с приступом в начале получили в / в rtPA по поводу симптомов, подобных инсульту, описанных в английской литературе. 77–83 Из них sICH был зарегистрирован только у 2 пациентов, один из которых имел отдаленный анамнез хирургического удаления опухоли головного мозга. Согласно недавнему опросу, 91% неврологов, перенесших инсульт, рекомендовали бы внутривенное введение rtPA пациентам с приступами в начале появления симптомов. 84
Недавний инфаркт миокарда
Недавний острый инфаркт миокарда в анамнезе за 3 месяца до инсульта является относительным противопоказанием к внутривенному тромболизису согласно последним рекомендациям AHA, 1 , но не является противопоказанием в Европе. руководящие принципы 24 или согласно этикетке препарата.Это также не было критерием исключения в исследованиях NIND или ECASS. Основные опасения по поводу назначения rtPA этим пациентам: (1) возможность кровотечения миокарда, предрасполагающего к разрыву стенки миокарда, (2) перикардит после инфаркта миокарда, который может стать геморрагическим, и (3) возможные тромбы желудочков, которые могут эмболизироваться из-за лизиса. Разрыв стенки миокарда является редким осложнением инфаркта миокарда и становится еще реже, поскольку немедленное вмешательство стало стандартом при инфаркте миокарда с подъемом сегмента ST (ИМпST).Разрыв стенки происходит только после трансмурального инфаркта, и самый высокий риск — в течение 2–5 дней. Когда пациенты получают внутривенный лизис по показаниям на ИМ, нет большой разницы между частотой разрыва сердца среди тех, кто получает тромболизис (1-8%), и тех, кто не получает тромболизис (1-5%). 85
Данных о тромболизисе при инсульте при недавно перенесенном инфаркте миокарда очень мало, и большая часть того, что сообщается, представляет собой отчеты о клинических случаях, несомненно, подверженных предвзятости публикации.В отчетах о клинических случаях описаны 5 пожилых женщин, у которых после приема rtPA по поводу инсульта развился разрыв сердца и гемоперикард. Только у одной из них недавно был хорошо задокументированный ИМ — у 93-летней женщины с сопутствующим ИМпST. 86 У другого пациента была операция по аортокоронарному шунтированию 16 дней назад, а у другого была одышка за несколько дней до обращения с неспецифическими изменениями на электрокардиограмме. 87 Из 5, 4 закончились смертельным исходом. 86–88 Внезапная гипотензия, возникающая примерно через 30 минут — 2 часа после завершения rtPA, должна вызывать подозрение на это осложнение.
После инфаркта миокарда фиброз и рубцевание миокарда завершаются к шестой или седьмой неделе. На основании этого было предложено сократить время после инфаркта миокарда, которое считается противопоказанием для внутривенного тромболизиса, до 7 недель. 85 Тип инфаркта миокарда, помимо тяжести симптомов инсульта, также должен влиять на процесс принятия решений. Пациенты с ИМпST, особенно те, у которых не затрагивается передняя сердечная стенка, могут иметь более низкий риск этого осложнения, но достоверных данных для оценки рисков или направления лечения в этой подгруппе пациентов нет.
Структурные поражения центральной нервной системы
Наличие внутричерепного новообразования, АВМ или аневризмы является противопоказанием в соответствии с рекомендациями AHA и этикеткой препарата. Риски внутривенного введения rtPA пациентам с инсультом и внутричерепными новообразованиями малоизвестны. Опубликованная литература ограничена описаниями случаев, большинство из которых были «успешными». 16,89–91 Случаи с достаточной детализацией описаны в. Был опубликован только 1 пациент, у которого была ICH, пациент с мультиформной глиобластомой височной доли, которая не была известна и проявлялась как умеренный массовый эффект на исходной компьютерной томографии. 92 В дополнение к подробным отчетам о случаях, несколько других были включены в более крупные отчеты о пациентах, которые получали rtPA не по назначению по поводу инсульта. Например, внутривенный тромболизис без sICH был проведен еще 3 пациентам с менингиомами, 1 — с холестеатомой и 1 — с опухолью околоносовых органов. 16 Имеется также несколько сообщений о пациентах с внутричерепными новообразованиями (менингиомы и аденома гипофиза), которым проводили внутривенный тромболизис по поводу ИМпST или тромбоэмболии легочной артерии. 93–95 Примечательно, что, несмотря на более высокую дозу литиков и сопутствующую системную антикоагуляцию, у этих пациентов не было ICH. Следует снова признать возможность систематической ошибки публикации, но эти случаи показывают, что внутривенный тромболизис может быть безопасным для некоторых пациентов с внутричерепными новообразованиями, особенно если новообразование относительно небольшое и расположено вне оси.
Таблица 1.
Краткое описание пациентов с опухолями головного мозга, получавших ТРА.
| Возраст / пол | Показания к лизису | NIHSS | Расположение опухоли | Размер опухоли, см | Тип опухоли | ICH | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Neil | CPE | CP10 | 3.3 × 1,3 | Невринома слухового нерва | Нет | ||||||||||||||
| Нил | 74 / F | Инсульт | 13 | Парафальцин | н / д | Менингиома | Менингиома | Менингиома | Инсульт | 7 | Височная доля | «Очень маленький» | GBM | Нет | |||||
| Grimm | 80 / M | Ход | 9039 n / aGBM | sICH | |||||||||||||||
| Hsieh | 60 / F | Ход | 11 | Лобное основание черепа | 2.0 | Менингиома | Отсутствует | ||||||||||||
| Etgen | 72 / F | Инсульт | 12 | Фронтальный | 2,5 | Менингиома | — | Гипофиз | 1,8 × 1,5 | Аденома гипофиза | Нет | ||||||||
| Рубенштейн | 77 / F | ИМпST | — | н / д | 0.8 × 0,8 | Менингиома | Отсутствует | ||||||||||||
| Jaffe | 62 / F | ИМпST | — | CPA | 1,0 | Менингиома | 9039 | — | Височная доля | 2,5 | GBM | Нет |
О безопасности внутривенного тромболизиса у пациентов с неразорвавшимися внутричерепными аневризмами сообщалось в отчетах о клинических случаях или в ретроспективных сериях случаев ().Частота sICH статистически не различалась между пациентами с аневризмами (0–13%) и без них (1–10%), но объем выборки невелик. 96–98,100 В английской литературе не сообщалось о случаях разрыва аневризмы, вызванных внутривенным введением rtPA. Хотя необходимо учитывать вероятность смещения отбора и смещения публикации, эти серии предполагают, что в / в rtPA можно безопасно вводить пациентам с неразорвавшимися случайными внутричерепными аневризмами. Следует отметить отсутствие данных о риске ВЧГ у пациентов с большими или гигантскими аневризмами, что может быть связано с более высоким риском.
Таблица 2.
Сводная информация о частоте внутричерепных кровотечений у зарегистрированных пациентов с внутричерепными аневризмами, которым был проведен внутривенный тромболизис при инсульте.
| Пациенты с аневризмой, n | sICH аневризма, n (%) | sICH без аневризмы, n (%) | любая аневризма ICH, n (%) | любая ICH аневризма, n (%) | |
|---|---|---|---|---|---|
| 96 | 22 | 0 (0) | 10 (4.7) | 3 (13,6) | 41 (19,1) |
| 97 | 8 | 1 (12,5) | 6 (3,7) | нет данных | нет данных |
| 98 | 10 | 1 (10) | 1 (1,1) | 2 (20) | 9 (9,5) |
| 99 | 8 | 1 (12,5) | н / д | 3 (37,5) | 63 (33,9) |
Деменция
Деменция не была включена в список критериев исключения в большинстве крупных исследований тромболизиса и не упоминается как противопоказание для rtPA в текущих рекомендациях по острому инсульту.Тем не менее, в рутинной клинической практике часто возникает вопрос, является ли внутривенное введение rtPA безопасным и эффективным у пациентов с деменцией и острым ишемическим инсультом. Исходная деменция связана с более низким использованием rtPA, 99 , и это связано с восприятием того, что она повышает риск кровотечения и вряд ли принесет пользу. 101 Фактические данные, хотя и ограниченные, не подтверждают эти утверждения.
Неудивительно, что деменция связана с худшими исходами после инсульта 102,103 даже среди пациентов, которым проводят тромболизис. 103 Однако деменция сама по себе, по-видимому, не увеличивает риск смерти (при выписке, 30 дней или даже 1 год) или госпитализации и связана только с тенденцией к большей функциональной инвалидности, когда анализ соответствующим образом скорректирован с учетом кофакторов. . 103 Точно так же деменция не увеличивала значительно риск ВЧГ по сравнению с подобранной контрольной группой в 2 исследованиях, анализирующих большие группы пациентов. 99,104
Следовательно, представляется безопасным назначать тромболизис пациентам с острым инсультом и предшествующей деменцией.Еще предстоит выяснить, является ли тромболизис эффективным для улучшения функциональных результатов у этих пациентов. Таким образом, решение о назначении rtPA должно приниматься индивидуально в зависимости от предыдущего уровня функции и тяжести дефицита инсульта.
Терапия TPA — StatPearls — Книжная полка NCBI
Непрерывное обучение
Альтеплаза (tPA) — мощное тромболитическое средство, используемое при лизисе острой тромбоэмболии. Показания к применению альтеплазы, одобренные FDA, включают тромбоэмболию легочной артерии, инфаркт миокарда с подъемом сегмента ST (ИМпST), ишемический инсульт при введении в течение 3 часов после появления симптомов и восстановление проходимости окклюзированных внутривенных (IV) катетеров.Есть также показания не по назначению. В этом упражнении излагаются показания, механизм действия, методы введения, важные побочные эффекты, противопоказания, токсичность и мониторинг терапии tPA с такими агентами, как альтеплаза, чтобы медицинские работники могли направлять терапию пациента там, где они показаны, как часть межпрофессиональной команды.
Цели:
Определить показания для начала терапии агентом tPA, таким как альтеплаза.
Ознакомьтесь с механизмом действия тканевых активаторов плазминогена, таких как альтеплаза.
Обобщите противопоказания и профиль нежелательных явлений препаратов tPA, таких как альтеплаза.
Опишите стратегии межпрофессиональной команды для улучшения координации помощи и коммуникации для правильного использования агентов tPA, таких как alteplase, для улучшения результатов лечения пациентов в различных сценариях, где это может быть эффективно.
Показания
Альтеплаза (tPA) — мощный тромболитический агент, используемый при лизисе острой тромбоэмболии.[1] [2] [3]
Утвержденные FDA показания для альтеплазы включают тромбоэмболию легочной артерии, инфаркт миокарда с подъемом сегмента ST (ИМпST), ишемический инсульт при введении в течение 3 часов после появления симптомов и восстановление проходимость окклюзионных внутривенных (IV) катетеров.
Общие показания не по назначению:
Лечение тромбоза глубоких вен (ТГВ) и тромбоза периферических артерий местным введением тромболитического агента при катетер-направленном тромболизисе
Ишемический инсульт при введении более 3 часов но не более 4.Через 5 часов после появления симптомов
Лечение тромбоза протезного клапана
Дополнительное лечение плеврального выпота или эмпиемы у детей.
Механизм действия
Алтеплаза действует в рамках эндогенного фибринолитического каскада, превращая плазминоген в плазмин путем гидролиза связи аргинин-валин в плазминогене. Затем активированный плазмин разрушает фибрин и фибриноген, что способствует растворению сгустка и восстановлению кровотока.[4] [5]
Введение
Дозирование и введение tPA зависят от показаний.
Показания, одобренные FDA
Легочная эмболия
Ишемический инсульт: Единственный анализ крови, который необходим перед использованием tPA, — это уровень глюкозы в крови. Если пациент принимает антикоагулянты, такие как кумадин, тогда только мы должны делать PT, PTT, INR и т. Д. Польза tPA во многом зависит от времени. Чем раньше пациент получит tPA; тем лучше результаты.
Максимальная рекомендуемая доза составляет 90 мг
Пациенты с нагрузкой менее или равной 100 кг с дозой 0,09 мг / кг (10% от дозы 0,9 мг / кг) в виде болюса внутривенно в течение 1 минуты с последующим введением 0,81 мг / кг. кг (90% дозы 0,9 мг / кг) в виде непрерывной инфузии в течение 60 минут.
Пациенты с нагрузкой более 100 кг вводят 9 мг (10% от 90 мг) в виде болюса внутривенно в течение 1 минуты, затем 81 мг (90% от 90 мг) в виде непрерывной инфузии в течение 60 минут.
ИМпST
Ввести в течение 30 минут после прибытия в больницу
Взрослым с массой тела более 67 кг вводят общую дозу 100 мг в виде 15 мг болюса внутривенно с последующей инфузией 50 мг внутривенно 30 минут, а затем вводится 35 мг внутривенно в течение следующих 60 минут
Взрослые с массой тела менее 67 кг получают болюс 15 мг внутривенно, затем 0.75 мг / кг внутривенно (не более 50 мг) вводится в течение 30 минут, а затем 0,5 мг / кг внутривенно (не более 35 мг) в течение следующих 60 минут
Окклюзия катетера внутривенно
Закапывание 2 мг альтеплазы в закупоренном просвете и выдержать 2 часа. Эту дозу можно повторить один раз, если первая попытка не увенчалась успехом, использование более 4 мг альтеплазы по этому показанию не было предметом исследований.
Показания не по назначению
Плевральные выпоты у детей
Катетер-направленная терапия
Тромбоз протезного клапана
Болезненная инъекция.В экстренных случаях целесообразно вводить tPA через внутрикостной доступ.
Побочные эффекты
Наиболее частые серьезные побочные эффекты, связанные с применением tPA, связаны с кровотечением. [6] [7] [8]
Кровотечение, связанное с терапией альтеплазой, можно разделить на две большие категории. Внутреннее кровотечение включает внутричерепное кровотечение (от 0,4% до 15,4%), забрюшинное кровотечение (менее 1%), желудочно-кишечное (ЖКТ) кровотечение (5%), мочеполовое кровотечение (4%) и респираторное кровотечение.Поверхностное или поверхностное кровотечение наблюдается в основном на пораженных или нарушенных участках, таких как венозные сокращения, артериальные проколы и места недавнего хирургического вмешательства. Менее серьезные спонтанные кровотечения включают экхимоз (1%), десневое кровотечение (менее 1%) и носовое кровотечение (менее 1%). В клинических исследованиях взрослых пациентов с острым ишемическим инсультом (n = 624) более высокая частота внутричерепных кровотечений, особенно симптоматических внутричерепных кровотечений, наблюдалась у пациентов, получавших альтеплазу, по сравнению с плацебо (общее внутричерепное кровотечение 15.4% против 6,4%, p <0,01; симптоматическое внутричерепное кровотечение 8% против 1,3%, p <0,01). Однако не наблюдалось увеличения частоты 90-дневной смертности или тяжелой инвалидности у пациентов, получавших альтеплазу. Исследования показывают, что частота внутричерепных кровотечений зависит от дозы, причем наибольший процент приходится на дозу 150 мг (1,3%) по сравнению с дозой 100 мг (0,4%). Частота нежелательных явлений, включая кровотечение, коррелирует с общим воздействием tPA.
Сердечные аритмии могут возникать при введении tPA для лечения ИМбпST и связаны с восстановлением тканевой перфузии, а не с воздействием лекарств.
Аллергические реакции, включая реакции анафилактического типа, возможны после воздействия tPA. Различные источники tPA имеют разный уровень антигенности. См. «Стрептокиназа» для дальнейшего обсуждения. Быстрое превращение плазминогена в плазмин сигнализирует о каскаде комплемента, ведущем к дегрануляции тучных клеток и последующей анафилактической реакции.
Противопоказания
Американская кардиологическая ассоциация опубликовала обновление 2016 г., в котором приведены критерии включения и исключения tPA для лечения ишемического инсульта.Следующий список включает самые последние абсолютные и относительные противопоказания к терапии, определенные AHA. 3
Гепарин, полученный в течение 48 часов, что привело к аномально повышенному АЧТВ выше верхнего предела нормы
Текущее использование муравья икоагулянт с МНО более 1.7 или PT более 15 секунд
Текущее использование прямых ингибиторов тромбина или прямых ингибиторов фактора Ха с повышенными чувствительными лабораторными тестами (например, АЧТВ, МНО, количество тромбоцитов, ЭСТ, ТТ или соответствующие анализы активности фактора Ха)
Концентрация глюкозы в крови менее 50 мг / дл (2,7 ммоль / л)
КТ демонстрирует многодолевой инфаркт (гипоплотность более одной трети полушария головного мозга)
Критерии относительного исключения
Недавний опыт предполагает что при некоторых обстоятельствах, при тщательном рассмотрении и взвешивании соотношения риска и пользы, пациенты могут получать фибринолитическую терапию, несмотря на одно или несколько относительных противопоказаний.Тщательно оцените риск внутривенного введения rtPA, если присутствует какое-либо из этих относительных противопоказаний:
Только незначительные или быстро улучшающиеся симптомы инсульта (исчезают автоматически)
Беременность
Судороги в начале с постиктальным остаточные неврологические нарушения
Серьезная операция или серьезная травма в течение предшествующих 14 дней
Недавнее кровотечение из желудочно-кишечного тракта или мочевыводящих путей (в течение предыдущих 21 дня)
Недавний острый инфаркт миокарда (в течение предшествующих 3 месяцев)
3 0 0 Мониторинг
Не существует рекомендаций по мониторингу терапевтических препаратов, касающихся эффективности терапии tPA.Если в случае катетерно-направленного лечения или повторного дозирования при тромбозе клапана проводится длительная терапия не по назначению, целесообразно серийное сканирование тромба. Профиль безопасности лучше всего контролировать по протромбиновому времени (PT), частичному тромбопластиновому времени (PTT), гемоглобину и гематокриту для оценки продолжающегося кровотечения. Следует отметить, что уровни фибриногена могут быть индикатором повышенного риска кровотечения при значениях менее 150 мг / дл.
Токсичность
Не существует агента прямого обратного действия для потенциально большого кровотечения, которое может возникнуть во время терапии tPA.Обычно используемые стратегии включают антифибринолитическую терапию, такую как транексамовая кислота или аминокапроновая кислота, хотя исследования конкретных дозировок отсутствуют. Если уровень фибриногена ниже 150 мг / дл, может быть дополнительная польза от свежезамороженной плазмы или криопреципитата. Криопреципитат следует использовать без промедления и внимательно следить за уровнем фибриногена.
Улучшение результатов команды здравоохранения
Больше нет никаких сомнений в эффективности тромболитических агентов для лечения некоторых заболеваний, но медсестры, фармацевты и радиологи должны полностью знать их показания и противопоказания.Чтобы эти агенты были эффективными, они не только требуют введения в течение определенного периода времени, но также необходимо убедиться, что у пациента нет состояния, которое противопоказано терапии. Кроме того, медсестра должна проинформировать пациента о процедуре, необходимости оставаться в постельном режиме в течение нескольких часов после процедуры и необходимости постоянно контролировать кровотечение. Кроме того, фармацевт должен быть знаком с новейшими антикоагулянтами и любыми возможными взаимодействиями с тромболитическими препаратами.Только благодаря тесному общению и постоянной бдительности между различными специалистами в области здравоохранения можно предотвратить серьезные осложнения, вызванные приемом этих препаратов. [2] [9] [Уровень V]
Результаты
Было проведено множество клинических испытаний для определения эффективности тромболитических средств у пациентов с острым инфарктом миокарда, тромбоэмболией легочной артерии, острой ишемией конечностей и эмболическим инсультом. При использовании для лечения острого инфаркта миокарда, эмболического инсульта и тромбоэмболии легочной артерии результаты от умеренных до хороших.Самым большим недостатком этой терапии является задержка прибытия пациента в отделение неотложной помощи или задержка постановки диагноза. Эти препараты спасли множество жизней, экономичны и сокращают время пребывания в больнице. [10] [11] [7] [Уровень II]
Вопросы повышения квалификации / повторения
Ссылки
- 1.
- Grossberg JA, Rebello LC, Haussen DC, Bouslama M, Bowen M, Barreira CM, Belagaje SR, Frankel MR, Nogueira RG. Помимо инсультов, связанных с окклюзией крупных сосудов: дистальная окклюзионная тромбэктомия.Инсульт. 2018 июл; 49 (7): 1662-1668. [PubMed: 29
5]
- 2.
- Бенуа Дж. Л., Хатри П., Адеойе О. М., Бродерик Дж. П., Макмаллан Дж. Т., Шейтц Дж. Ф., Вагал А. С., Экман М. Х. Догоспитальная сортировка пациентов с острым ишемическим инсультом в больницу, готовую к внутривенному введению tPA, и в больницу, готовую к эндоваскулярной терапии: анализ решения. Prehosp Emerg Care. 2018 ноябрь-декабрь; 22 (6): 722-733. [PubMed: 29847193]
- 3.
- Мак Грори Б., Яги С. Обновления в лечении инсульта. R I Med J (2013). 01 марта 2018; 101 (2): 30-33.[PubMed: 294
- 4.
- Имбаррато Дж., Бентли Дж., Гордхан А. Клинические результаты эндоваскулярной тромбэктомии у пациентов с тканевым активатором плазминогена по сравнению с пациентами с нетканевым активатором плазминогена в центрах первичной помощи при инсульте. J Neurosci Rural Pract. 2018 апрель-июнь; 9 (2): 240-244. [Бесплатная статья PMC: PMC5
1] [PubMed: 29725176] 93]- 5.
- Knecht T., Story J, Liu J, Davis W, Borlongan CV, Dela Peña IC. Подходы к дополнительной терапии ишемического инсульта: инновации для увеличения временного окна лечения.Int J Mol Sci. 2017 декабря 19; 18 (12) [Бесплатная статья PMC: PMC5751355] [PubMed: 2
- 6.
- Лю Х, Чжэн Х, Цао И, Пань И, Ван Д, Чжан Р, Ю С, Чжан Х, Ли С., Тонг Х, Лю К.Ф., Ван Й. Низкие и стандартные дозы внутривенного тканевого активатора плазминогена для острого ишемического инсульта: обновленный метаанализ. J Stroke Cerebrovasc Dis. 2018 Апрель; 27 (4): 988-997. [PubMed: 244]
- 7.
- Гиллиланд К., Шах Дж., Мартин Дж. Г., Миллер М. Дж.. Острая ишемия конечностей. Tech Vasc Interv Radiol.2017 декабрь; 20 (4): 274-280. [PubMed: 2
61]- 8.
- Вивьен Д. Можно ли улучшить преимущества лечения rtPA при инсульте? Rev Neurol (Париж). 2017 ноя; 173 (9): 566-571. [PubMed: 28797689]
- 9.
- Kepplinger J, Barlinn K, Deckert S, Scheibe M, Bodechtel U, Schmitt J. Безопасность и эффективность тромболизиса при телестроении: систематический обзор и метаанализ. Неврология. 2016 27 сентября; 87 (13): 1344-51. [PubMed: 27566746]
- 10.
- Аоки Дж., Судзуки К., Суда С., Окубо С., Мишина М., Нишияма Ю., Сакамото И., Кимура К.В сверхострой реканализационной терапии раннее прибытие в больницу улучшает исход у пациентов с окклюзией крупных артерий. Eur Neurol. 2018; 79 (5-6): 335-341. [PubMed: 29986341]
- 11.
- Man S, Zhao X, Uchino K, Hussain MS, Smith EE, Bhatt DL, Xian Y, Schwamm LH, Shah S, Khan Y, Fonarow GC. Сравнение лечения острого ишемического инсульта и результатов между центрами комплексного лечения инсульта и центрами первичного инсульта в США. Результаты Circ Cardiovasc Qual. 2018 июн; 11 (6): e004512.[Бесплатная статья PMC: PMC5978771] [PubMed: 29794035]
Терапия TPA — StatPearls — Книжная полка NCBI
Непрерывное обучение
Альтеплаза (tPA) — мощный тромболитический агент, используемый при лизисе острой тромбоэмболии. Показания к применению альтеплазы, одобренные FDA, включают тромбоэмболию легочной артерии, инфаркт миокарда с подъемом сегмента ST (ИМпST), ишемический инсульт при введении в течение 3 часов после появления симптомов и восстановление проходимости окклюзированных внутривенных (IV) катетеров.Есть также показания не по назначению. В этом упражнении излагаются показания, механизм действия, методы введения, важные побочные эффекты, противопоказания, токсичность и мониторинг терапии tPA с такими агентами, как альтеплаза, чтобы медицинские работники могли направлять терапию пациента там, где они показаны, как часть межпрофессиональной команды.
Цели:
Определить показания для начала терапии агентом tPA, таким как альтеплаза.
Ознакомьтесь с механизмом действия тканевых активаторов плазминогена, таких как альтеплаза.
Обобщите противопоказания и профиль нежелательных явлений препаратов tPA, таких как альтеплаза.
Опишите стратегии межпрофессиональной команды для улучшения координации помощи и коммуникации для правильного использования агентов tPA, таких как alteplase, для улучшения результатов лечения пациентов в различных сценариях, где это может быть эффективно.
Показания
Альтеплаза (tPA) — мощный тромболитический агент, используемый при лизисе острой тромбоэмболии.[1] [2] [3]
Утвержденные FDA показания для альтеплазы включают тромбоэмболию легочной артерии, инфаркт миокарда с подъемом сегмента ST (ИМпST), ишемический инсульт при введении в течение 3 часов после появления симптомов и восстановление проходимость окклюзионных внутривенных (IV) катетеров.
Общие показания не по назначению:
Лечение тромбоза глубоких вен (ТГВ) и тромбоза периферических артерий местным введением тромболитического агента при катетер-направленном тромболизисе
Ишемический инсульт при введении более 3 часов но не более 4.Через 5 часов после появления симптомов
Лечение тромбоза протезного клапана
Дополнительное лечение плеврального выпота или эмпиемы у детей.
Механизм действия
Алтеплаза действует в рамках эндогенного фибринолитического каскада, превращая плазминоген в плазмин путем гидролиза связи аргинин-валин в плазминогене. Затем активированный плазмин разрушает фибрин и фибриноген, что способствует растворению сгустка и восстановлению кровотока.[4] [5]
Введение
Дозирование и введение tPA зависят от показаний.
Показания, одобренные FDA
Легочная эмболия
Ишемический инсульт: Единственный анализ крови, который необходим перед использованием tPA, — это уровень глюкозы в крови. Если пациент принимает антикоагулянты, такие как кумадин, тогда только мы должны делать PT, PTT, INR и т. Д. Польза tPA во многом зависит от времени. Чем раньше пациент получит tPA; тем лучше результаты.
Максимальная рекомендуемая доза составляет 90 мг
Пациенты с нагрузкой менее или равной 100 кг с дозой 0,09 мг / кг (10% от дозы 0,9 мг / кг) в виде болюса внутривенно в течение 1 минуты с последующим введением 0,81 мг / кг. кг (90% дозы 0,9 мг / кг) в виде непрерывной инфузии в течение 60 минут.
Пациенты с нагрузкой более 100 кг вводят 9 мг (10% от 90 мг) в виде болюса внутривенно в течение 1 минуты, затем 81 мг (90% от 90 мг) в виде непрерывной инфузии в течение 60 минут.
ИМпST
Ввести в течение 30 минут после прибытия в больницу
Взрослым с массой тела более 67 кг вводят общую дозу 100 мг в виде 15 мг болюса внутривенно с последующей инфузией 50 мг внутривенно 30 минут, а затем вводится 35 мг внутривенно в течение следующих 60 минут
Взрослые с массой тела менее 67 кг получают болюс 15 мг внутривенно, затем 0.75 мг / кг внутривенно (не более 50 мг) вводится в течение 30 минут, а затем 0,5 мг / кг внутривенно (не более 35 мг) в течение следующих 60 минут
Окклюзия катетера внутривенно
Закапывание 2 мг альтеплазы в закупоренном просвете и выдержать 2 часа. Эту дозу можно повторить один раз, если первая попытка не увенчалась успехом, использование более 4 мг альтеплазы по этому показанию не было предметом исследований.
Показания не по назначению
Плевральные выпоты у детей
Катетер-направленная терапия
Тромбоз протезного клапана
Болезненная инъекция.В экстренных случаях целесообразно вводить tPA через внутрикостной доступ.
Побочные эффекты
Наиболее частые серьезные побочные эффекты, связанные с применением tPA, связаны с кровотечением. [6] [7] [8]
Кровотечение, связанное с терапией альтеплазой, можно разделить на две большие категории. Внутреннее кровотечение включает внутричерепное кровотечение (от 0,4% до 15,4%), забрюшинное кровотечение (менее 1%), желудочно-кишечное (ЖКТ) кровотечение (5%), мочеполовое кровотечение (4%) и респираторное кровотечение.Поверхностное или поверхностное кровотечение наблюдается в основном на пораженных или нарушенных участках, таких как венозные сокращения, артериальные проколы и места недавнего хирургического вмешательства. Менее серьезные спонтанные кровотечения включают экхимоз (1%), десневое кровотечение (менее 1%) и носовое кровотечение (менее 1%). В клинических исследованиях взрослых пациентов с острым ишемическим инсультом (n = 624) более высокая частота внутричерепных кровотечений, особенно симптоматических внутричерепных кровотечений, наблюдалась у пациентов, получавших альтеплазу, по сравнению с плацебо (общее внутричерепное кровотечение 15.4% против 6,4%, p <0,01; симптоматическое внутричерепное кровотечение 8% против 1,3%, p <0,01). Однако не наблюдалось увеличения частоты 90-дневной смертности или тяжелой инвалидности у пациентов, получавших альтеплазу. Исследования показывают, что частота внутричерепных кровотечений зависит от дозы, причем наибольший процент приходится на дозу 150 мг (1,3%) по сравнению с дозой 100 мг (0,4%). Частота нежелательных явлений, включая кровотечение, коррелирует с общим воздействием tPA.
Сердечные аритмии могут возникать при введении tPA для лечения ИМбпST и связаны с восстановлением тканевой перфузии, а не с воздействием лекарств.
Аллергические реакции, включая реакции анафилактического типа, возможны после воздействия tPA. Различные источники tPA имеют разный уровень антигенности. См. «Стрептокиназа» для дальнейшего обсуждения. Быстрое превращение плазминогена в плазмин сигнализирует о каскаде комплемента, ведущем к дегрануляции тучных клеток и последующей анафилактической реакции.
Противопоказания
Американская кардиологическая ассоциация опубликовала обновление 2016 г., в котором приведены критерии включения и исключения tPA для лечения ишемического инсульта.Следующий список включает самые последние абсолютные и относительные противопоказания к терапии, определенные AHA. 3
Гепарин, полученный в течение 48 часов, что привело к аномально повышенному АЧТВ выше верхнего предела нормы
Текущее использование муравья икоагулянт с МНО более 1.7 или PT более 15 секунд
Текущее использование прямых ингибиторов тромбина или прямых ингибиторов фактора Ха с повышенными чувствительными лабораторными тестами (например, АЧТВ, МНО, количество тромбоцитов, ЭСТ, ТТ или соответствующие анализы активности фактора Ха)
Концентрация глюкозы в крови менее 50 мг / дл (2,7 ммоль / л)
КТ демонстрирует многодолевой инфаркт (гипоплотность более одной трети полушария головного мозга)
Критерии относительного исключения
Недавний опыт предполагает что при некоторых обстоятельствах, при тщательном рассмотрении и взвешивании соотношения риска и пользы, пациенты могут получать фибринолитическую терапию, несмотря на одно или несколько относительных противопоказаний.Тщательно оцените риск внутривенного введения rtPA, если присутствует какое-либо из этих относительных противопоказаний:
Только незначительные или быстро улучшающиеся симптомы инсульта (исчезают автоматически)
Беременность
Судороги в начале с постиктальным остаточные неврологические нарушения
Серьезная операция или серьезная травма в течение предшествующих 14 дней
Недавнее кровотечение из желудочно-кишечного тракта или мочевыводящих путей (в течение предыдущих 21 дня)
Недавний острый инфаркт миокарда (в течение предшествующих 3 месяцев)
3 0 0 Мониторинг
Не существует рекомендаций по мониторингу терапевтических препаратов, касающихся эффективности терапии tPA.Если в случае катетерно-направленного лечения или повторного дозирования при тромбозе клапана проводится длительная терапия не по назначению, целесообразно серийное сканирование тромба. Профиль безопасности лучше всего контролировать по протромбиновому времени (PT), частичному тромбопластиновому времени (PTT), гемоглобину и гематокриту для оценки продолжающегося кровотечения. Следует отметить, что уровни фибриногена могут быть индикатором повышенного риска кровотечения при значениях менее 150 мг / дл.
Токсичность
Не существует агента прямого обратного действия для потенциально большого кровотечения, которое может возникнуть во время терапии tPA.Обычно используемые стратегии включают антифибринолитическую терапию, такую как транексамовая кислота или аминокапроновая кислота, хотя исследования конкретных дозировок отсутствуют. Если уровень фибриногена ниже 150 мг / дл, может быть дополнительная польза от свежезамороженной плазмы или криопреципитата. Криопреципитат следует использовать без промедления и внимательно следить за уровнем фибриногена.
Улучшение результатов команды здравоохранения
Больше нет никаких сомнений в эффективности тромболитических агентов для лечения некоторых заболеваний, но медсестры, фармацевты и радиологи должны полностью знать их показания и противопоказания.Чтобы эти агенты были эффективными, они не только требуют введения в течение определенного периода времени, но также необходимо убедиться, что у пациента нет состояния, которое противопоказано терапии. Кроме того, медсестра должна проинформировать пациента о процедуре, необходимости оставаться в постельном режиме в течение нескольких часов после процедуры и необходимости постоянно контролировать кровотечение. Кроме того, фармацевт должен быть знаком с новейшими антикоагулянтами и любыми возможными взаимодействиями с тромболитическими препаратами.Только благодаря тесному общению и постоянной бдительности между различными специалистами в области здравоохранения можно предотвратить серьезные осложнения, вызванные приемом этих препаратов. [2] [9] [Уровень V]
Результаты
Было проведено множество клинических испытаний для определения эффективности тромболитических средств у пациентов с острым инфарктом миокарда, тромбоэмболией легочной артерии, острой ишемией конечностей и эмболическим инсультом. При использовании для лечения острого инфаркта миокарда, эмболического инсульта и тромбоэмболии легочной артерии результаты от умеренных до хороших.Самым большим недостатком этой терапии является задержка прибытия пациента в отделение неотложной помощи или задержка постановки диагноза. Эти препараты спасли множество жизней, экономичны и сокращают время пребывания в больнице. [10] [11] [7] [Уровень II]
Вопросы повышения квалификации / повторения
Ссылки
- 1.
- Grossberg JA, Rebello LC, Haussen DC, Bouslama M, Bowen M, Barreira CM, Belagaje SR, Frankel MR, Nogueira RG. Помимо инсультов, связанных с окклюзией крупных сосудов: дистальная окклюзионная тромбэктомия.Инсульт. 2018 июл; 49 (7): 1662-1668. [PubMed: 29
5]
- 2.
- Бенуа Дж. Л., Хатри П., Адеойе О. М., Бродерик Дж. П., Макмаллан Дж. Т., Шейтц Дж. Ф., Вагал А. С., Экман М. Х. Догоспитальная сортировка пациентов с острым ишемическим инсультом в больницу, готовую к внутривенному введению tPA, и в больницу, готовую к эндоваскулярной терапии: анализ решения. Prehosp Emerg Care. 2018 ноябрь-декабрь; 22 (6): 722-733. [PubMed: 29847193]
- 3.
- Мак Грори Б., Яги С. Обновления в лечении инсульта. R I Med J (2013). 01 марта 2018; 101 (2): 30-33.[PubMed: 294
- 4.
- Имбаррато Дж., Бентли Дж., Гордхан А. Клинические результаты эндоваскулярной тромбэктомии у пациентов с тканевым активатором плазминогена по сравнению с пациентами с нетканевым активатором плазминогена в центрах первичной помощи при инсульте. J Neurosci Rural Pract. 2018 апрель-июнь; 9 (2): 240-244. [Бесплатная статья PMC: PMC5
1] [PubMed: 29725176] 93]- 5.
- Knecht T., Story J, Liu J, Davis W, Borlongan CV, Dela Peña IC. Подходы к дополнительной терапии ишемического инсульта: инновации для увеличения временного окна лечения.Int J Mol Sci. 2017 декабря 19; 18 (12) [Бесплатная статья PMC: PMC5751355] [PubMed: 2
- 6.
- Лю Х, Чжэн Х, Цао И, Пань И, Ван Д, Чжан Р, Ю С, Чжан Х, Ли С., Тонг Х, Лю К.Ф., Ван Й. Низкие и стандартные дозы внутривенного тканевого активатора плазминогена для острого ишемического инсульта: обновленный метаанализ. J Stroke Cerebrovasc Dis. 2018 Апрель; 27 (4): 988-997. [PubMed: 244]
- 7.
- Гиллиланд К., Шах Дж., Мартин Дж. Г., Миллер М. Дж.. Острая ишемия конечностей. Tech Vasc Interv Radiol.2017 декабрь; 20 (4): 274-280. [PubMed: 2
61]- 8.
- Вивьен Д. Можно ли улучшить преимущества лечения rtPA при инсульте? Rev Neurol (Париж). 2017 ноя; 173 (9): 566-571. [PubMed: 28797689]
- 9.
- Kepplinger J, Barlinn K, Deckert S, Scheibe M, Bodechtel U, Schmitt J. Безопасность и эффективность тромболизиса при телестроении: систематический обзор и метаанализ. Неврология. 2016 27 сентября; 87 (13): 1344-51. [PubMed: 27566746]
- 10.
- Аоки Дж., Судзуки К., Суда С., Окубо С., Мишина М., Нишияма Ю., Сакамото И., Кимура К.В сверхострой реканализационной терапии раннее прибытие в больницу улучшает исход у пациентов с окклюзией крупных артерий. Eur Neurol. 2018; 79 (5-6): 335-341. [PubMed: 29986341]
- 11.
- Man S, Zhao X, Uchino K, Hussain MS, Smith EE, Bhatt DL, Xian Y, Schwamm LH, Shah S, Khan Y, Fonarow GC. Сравнение лечения острого ишемического инсульта и результатов между центрами комплексного лечения инсульта и центрами первичного инсульта в США. Результаты Circ Cardiovasc Qual. 2018 июн; 11 (6): e004512.[Бесплатная статья PMC: PMC5978771] [PubMed: 29794035]
Терапия TPA — StatPearls — Книжная полка NCBI
Непрерывное обучение
Альтеплаза (tPA) — мощный тромболитический агент, используемый при лизисе острой тромбоэмболии. Показания к применению альтеплазы, одобренные FDA, включают тромбоэмболию легочной артерии, инфаркт миокарда с подъемом сегмента ST (ИМпST), ишемический инсульт при введении в течение 3 часов после появления симптомов и восстановление проходимости окклюзированных внутривенных (IV) катетеров.Есть также показания не по назначению. В этом упражнении излагаются показания, механизм действия, методы введения, важные побочные эффекты, противопоказания, токсичность и мониторинг терапии tPA с такими агентами, как альтеплаза, чтобы медицинские работники могли направлять терапию пациента там, где они показаны, как часть межпрофессиональной команды.
Цели:
Определить показания для начала терапии агентом tPA, таким как альтеплаза.
Ознакомьтесь с механизмом действия тканевых активаторов плазминогена, таких как альтеплаза.
Обобщите противопоказания и профиль нежелательных явлений препаратов tPA, таких как альтеплаза.
Опишите стратегии межпрофессиональной команды для улучшения координации помощи и коммуникации для правильного использования агентов tPA, таких как alteplase, для улучшения результатов лечения пациентов в различных сценариях, где это может быть эффективно.
Показания
Альтеплаза (tPA) — мощный тромболитический агент, используемый при лизисе острой тромбоэмболии.[1] [2] [3]
Утвержденные FDA показания для альтеплазы включают тромбоэмболию легочной артерии, инфаркт миокарда с подъемом сегмента ST (ИМпST), ишемический инсульт при введении в течение 3 часов после появления симптомов и восстановление проходимость окклюзионных внутривенных (IV) катетеров.
Общие показания не по назначению:
Лечение тромбоза глубоких вен (ТГВ) и тромбоза периферических артерий местным введением тромболитического агента при катетер-направленном тромболизисе
Ишемический инсульт при введении более 3 часов но не более 4.Через 5 часов после появления симптомов
Лечение тромбоза протезного клапана
Дополнительное лечение плеврального выпота или эмпиемы у детей.
Механизм действия
Алтеплаза действует в рамках эндогенного фибринолитического каскада, превращая плазминоген в плазмин путем гидролиза связи аргинин-валин в плазминогене. Затем активированный плазмин разрушает фибрин и фибриноген, что способствует растворению сгустка и восстановлению кровотока.[4] [5]
Введение
Дозирование и введение tPA зависят от показаний.
Показания, одобренные FDA
Легочная эмболия
Ишемический инсульт: Единственный анализ крови, который необходим перед использованием tPA, — это уровень глюкозы в крови. Если пациент принимает антикоагулянты, такие как кумадин, тогда только мы должны делать PT, PTT, INR и т. Д. Польза tPA во многом зависит от времени. Чем раньше пациент получит tPA; тем лучше результаты.
Максимальная рекомендуемая доза составляет 90 мг
Пациенты с нагрузкой менее или равной 100 кг с дозой 0,09 мг / кг (10% от дозы 0,9 мг / кг) в виде болюса внутривенно в течение 1 минуты с последующим введением 0,81 мг / кг. кг (90% дозы 0,9 мг / кг) в виде непрерывной инфузии в течение 60 минут.
Пациенты с нагрузкой более 100 кг вводят 9 мг (10% от 90 мг) в виде болюса внутривенно в течение 1 минуты, затем 81 мг (90% от 90 мг) в виде непрерывной инфузии в течение 60 минут.
ИМпST
Ввести в течение 30 минут после прибытия в больницу
Взрослым с массой тела более 67 кг вводят общую дозу 100 мг в виде 15 мг болюса внутривенно с последующей инфузией 50 мг внутривенно 30 минут, а затем вводится 35 мг внутривенно в течение следующих 60 минут
Взрослые с массой тела менее 67 кг получают болюс 15 мг внутривенно, затем 0.75 мг / кг внутривенно (не более 50 мг) вводится в течение 30 минут, а затем 0,5 мг / кг внутривенно (не более 35 мг) в течение следующих 60 минут
Окклюзия катетера внутривенно
Закапывание 2 мг альтеплазы в закупоренном просвете и выдержать 2 часа. Эту дозу можно повторить один раз, если первая попытка не увенчалась успехом, использование более 4 мг альтеплазы по этому показанию не было предметом исследований.
Показания не по назначению
Плевральные выпоты у детей
Катетер-направленная терапия
Тромбоз протезного клапана
Болезненная инъекция.В экстренных случаях целесообразно вводить tPA через внутрикостной доступ.
Побочные эффекты
Наиболее частые серьезные побочные эффекты, связанные с применением tPA, связаны с кровотечением. [6] [7] [8]
Кровотечение, связанное с терапией альтеплазой, можно разделить на две большие категории. Внутреннее кровотечение включает внутричерепное кровотечение (от 0,4% до 15,4%), забрюшинное кровотечение (менее 1%), желудочно-кишечное (ЖКТ) кровотечение (5%), мочеполовое кровотечение (4%) и респираторное кровотечение.Поверхностное или поверхностное кровотечение наблюдается в основном на пораженных или нарушенных участках, таких как венозные сокращения, артериальные проколы и места недавнего хирургического вмешательства. Менее серьезные спонтанные кровотечения включают экхимоз (1%), десневое кровотечение (менее 1%) и носовое кровотечение (менее 1%). В клинических исследованиях взрослых пациентов с острым ишемическим инсультом (n = 624) более высокая частота внутричерепных кровотечений, особенно симптоматических внутричерепных кровотечений, наблюдалась у пациентов, получавших альтеплазу, по сравнению с плацебо (общее внутричерепное кровотечение 15.4% против 6,4%, p <0,01; симптоматическое внутричерепное кровотечение 8% против 1,3%, p <0,01). Однако не наблюдалось увеличения частоты 90-дневной смертности или тяжелой инвалидности у пациентов, получавших альтеплазу. Исследования показывают, что частота внутричерепных кровотечений зависит от дозы, причем наибольший процент приходится на дозу 150 мг (1,3%) по сравнению с дозой 100 мг (0,4%). Частота нежелательных явлений, включая кровотечение, коррелирует с общим воздействием tPA.
Сердечные аритмии могут возникать при введении tPA для лечения ИМбпST и связаны с восстановлением тканевой перфузии, а не с воздействием лекарств.
Аллергические реакции, включая реакции анафилактического типа, возможны после воздействия tPA. Различные источники tPA имеют разный уровень антигенности. См. «Стрептокиназа» для дальнейшего обсуждения. Быстрое превращение плазминогена в плазмин сигнализирует о каскаде комплемента, ведущем к дегрануляции тучных клеток и последующей анафилактической реакции.
Противопоказания
Американская кардиологическая ассоциация опубликовала обновление 2016 г., в котором приведены критерии включения и исключения tPA для лечения ишемического инсульта.Следующий список включает самые последние абсолютные и относительные противопоказания к терапии, определенные AHA. 3
Гепарин, полученный в течение 48 часов, что привело к аномально повышенному АЧТВ выше верхнего предела нормы
Текущее использование муравья икоагулянт с МНО более 1.7 или PT более 15 секунд
Текущее использование прямых ингибиторов тромбина или прямых ингибиторов фактора Ха с повышенными чувствительными лабораторными тестами (например, АЧТВ, МНО, количество тромбоцитов, ЭСТ, ТТ или соответствующие анализы активности фактора Ха)
Концентрация глюкозы в крови менее 50 мг / дл (2,7 ммоль / л)
КТ демонстрирует многодолевой инфаркт (гипоплотность более одной трети полушария головного мозга)
Критерии относительного исключения
Недавний опыт предполагает что при некоторых обстоятельствах, при тщательном рассмотрении и взвешивании соотношения риска и пользы, пациенты могут получать фибринолитическую терапию, несмотря на одно или несколько относительных противопоказаний.Тщательно оцените риск внутривенного введения rtPA, если присутствует какое-либо из этих относительных противопоказаний:
Только незначительные или быстро улучшающиеся симптомы инсульта (исчезают автоматически)
Беременность
Судороги в начале с постиктальным остаточные неврологические нарушения
Серьезная операция или серьезная травма в течение предшествующих 14 дней
Недавнее кровотечение из желудочно-кишечного тракта или мочевыводящих путей (в течение предыдущих 21 дня)
Недавний острый инфаркт миокарда (в течение предшествующих 3 месяцев)
3 0 0 Мониторинг
Не существует рекомендаций по мониторингу терапевтических препаратов, касающихся эффективности терапии tPA.Если в случае катетерно-направленного лечения или повторного дозирования при тромбозе клапана проводится длительная терапия не по назначению, целесообразно серийное сканирование тромба. Профиль безопасности лучше всего контролировать по протромбиновому времени (PT), частичному тромбопластиновому времени (PTT), гемоглобину и гематокриту для оценки продолжающегося кровотечения. Следует отметить, что уровни фибриногена могут быть индикатором повышенного риска кровотечения при значениях менее 150 мг / дл.
Токсичность
Не существует агента прямого обратного действия для потенциально большого кровотечения, которое может возникнуть во время терапии tPA.Обычно используемые стратегии включают антифибринолитическую терапию, такую как транексамовая кислота или аминокапроновая кислота, хотя исследования конкретных дозировок отсутствуют. Если уровень фибриногена ниже 150 мг / дл, может быть дополнительная польза от свежезамороженной плазмы или криопреципитата. Криопреципитат следует использовать без промедления и внимательно следить за уровнем фибриногена.
Улучшение результатов команды здравоохранения
Больше нет никаких сомнений в эффективности тромболитических агентов для лечения некоторых заболеваний, но медсестры, фармацевты и радиологи должны полностью знать их показания и противопоказания.Чтобы эти агенты были эффективными, они не только требуют введения в течение определенного периода времени, но также необходимо убедиться, что у пациента нет состояния, которое противопоказано терапии. Кроме того, медсестра должна проинформировать пациента о процедуре, необходимости оставаться в постельном режиме в течение нескольких часов после процедуры и необходимости постоянно контролировать кровотечение. Кроме того, фармацевт должен быть знаком с новейшими антикоагулянтами и любыми возможными взаимодействиями с тромболитическими препаратами.Только благодаря тесному общению и постоянной бдительности между различными специалистами в области здравоохранения можно предотвратить серьезные осложнения, вызванные приемом этих препаратов. [2] [9] [Уровень V]
Результаты
Было проведено множество клинических испытаний для определения эффективности тромболитических средств у пациентов с острым инфарктом миокарда, тромбоэмболией легочной артерии, острой ишемией конечностей и эмболическим инсультом. При использовании для лечения острого инфаркта миокарда, эмболического инсульта и тромбоэмболии легочной артерии результаты от умеренных до хороших.Самым большим недостатком этой терапии является задержка прибытия пациента в отделение неотложной помощи или задержка постановки диагноза. Эти препараты спасли множество жизней, экономичны и сокращают время пребывания в больнице. [10] [11] [7] [Уровень II]
Вопросы повышения квалификации / повторения
Ссылки
- 1.
- Grossberg JA, Rebello LC, Haussen DC, Bouslama M, Bowen M, Barreira CM, Belagaje SR, Frankel MR, Nogueira RG. Помимо инсультов, связанных с окклюзией крупных сосудов: дистальная окклюзионная тромбэктомия.Инсульт. 2018 июл; 49 (7): 1662-1668. [PubMed: 29
5]
- 2.
- Бенуа Дж. Л., Хатри П., Адеойе О. М., Бродерик Дж. П., Макмаллан Дж. Т., Шейтц Дж. Ф., Вагал А. С., Экман М. Х. Догоспитальная сортировка пациентов с острым ишемическим инсультом в больницу, готовую к внутривенному введению tPA, и в больницу, готовую к эндоваскулярной терапии: анализ решения. Prehosp Emerg Care. 2018 ноябрь-декабрь; 22 (6): 722-733. [PubMed: 29847193]
- 3.
- Мак Грори Б., Яги С. Обновления в лечении инсульта. R I Med J (2013). 01 марта 2018; 101 (2): 30-33.[PubMed: 294
- 4.
- Имбаррато Дж., Бентли Дж., Гордхан А. Клинические результаты эндоваскулярной тромбэктомии у пациентов с тканевым активатором плазминогена по сравнению с пациентами с нетканевым активатором плазминогена в центрах первичной помощи при инсульте. J Neurosci Rural Pract. 2018 апрель-июнь; 9 (2): 240-244. [Бесплатная статья PMC: PMC5
1] [PubMed: 29725176] 93]- 5.
- Knecht T., Story J, Liu J, Davis W, Borlongan CV, Dela Peña IC. Подходы к дополнительной терапии ишемического инсульта: инновации для увеличения временного окна лечения.Int J Mol Sci. 2017 декабря 19; 18 (12) [Бесплатная статья PMC: PMC5751355] [PubMed: 2
- 6.
- Лю Х, Чжэн Х, Цао И, Пань И, Ван Д, Чжан Р, Ю С, Чжан Х, Ли С., Тонг Х, Лю К.Ф., Ван Й. Низкие и стандартные дозы внутривенного тканевого активатора плазминогена для острого ишемического инсульта: обновленный метаанализ. J Stroke Cerebrovasc Dis. 2018 Апрель; 27 (4): 988-997. [PubMed: 244]
- 7.
- Гиллиланд К., Шах Дж., Мартин Дж. Г., Миллер М. Дж.. Острая ишемия конечностей. Tech Vasc Interv Radiol.2017 декабрь; 20 (4): 274-280. [PubMed: 2
61]- 8.
- Вивьен Д. Можно ли улучшить преимущества лечения rtPA при инсульте? Rev Neurol (Париж). 2017 ноя; 173 (9): 566-571. [PubMed: 28797689]
- 9.
- Kepplinger J, Barlinn K, Deckert S, Scheibe M, Bodechtel U, Schmitt J. Безопасность и эффективность тромболизиса при телестроении: систематический обзор и метаанализ. Неврология. 2016 27 сентября; 87 (13): 1344-51. [PubMed: 27566746]
- 10.
- Аоки Дж., Судзуки К., Суда С., Окубо С., Мишина М., Нишияма Ю., Сакамото И., Кимура К.В сверхострой реканализационной терапии раннее прибытие в больницу улучшает исход у пациентов с окклюзией крупных артерий. Eur Neurol. 2018; 79 (5-6): 335-341. [PubMed: 29986341]
- 11.
- Man S, Zhao X, Uchino K, Hussain MS, Smith EE, Bhatt DL, Xian Y, Schwamm LH, Shah S, Khan Y, Fonarow GC.