Острый промиелоцитарный лейкоз – симптомы, лечение
Острый промиелоцитарный лейкоз (ОПЛ) – это относительно редкая разновидность острого миелоидного лейкоза (ОМЛ), для которой характерно аномальное накопление промиелоцитов. По сравнению с ОМЛ это довольно «молодая» патология (средний возраст больных – примерно 30–40 лет), а также одна из самых благоприятных и хорошо поддающихся лечению форм.
Механизм развития
Первым признаком острого промиелоцитарного лейкоза выступают кровоизлияния. Чаще всего это кровотечения, развивающиеся на местах травм, также это могут быть маточные, носовые кровотечения или кровоподтеки. Процесс сопровождается умеренной тромбоцитопенией.
Признаки кровоточивости постепенно нарастают. Позднее к ним присоединяются симптомы опухолевой интоксикации. Селезенка и печень увеличиваются редко, а лимфатические узлы практически не участвуют в патологическом процессе. Из-за этих признаков промиелоцитарный лейкоз считают «медленным» лейкозом.
В начале развития заболевания показатели красной крови нормальные или слегка пониженные, в половине случаев уровень гемоглобина отмечается выше 100 г/л. Число тромбоцитов и лейкоцитов снижено.
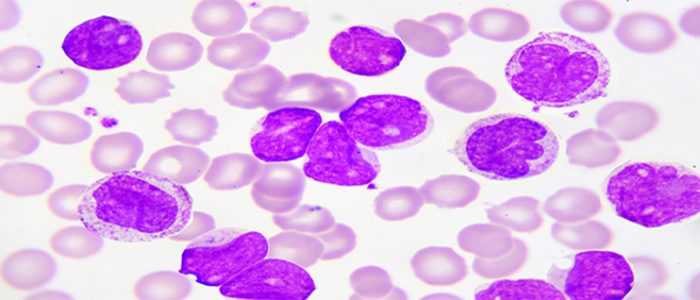
Для лабораторных показателей крови характерно разнообразие бластных клеток, причем большинство имеет цитоплазматические отростки, похожие на ложноножки. В 80% случаев лейкозные клетки имеют крупную зернистость, и тогда недуг классифицируют как макрогранулярный. В 20% случаев преобладают мелкозернистые клетки, и эту форму называют микрогранулярной. При ней лейкоцитоз в крови и выход в нее лейкозных клеток наблюдаются чаще.
Симптомы
Острый промиелоцитарный лейкоз протекает быстро. Основной признак – это кровотечения при минимальных повреждениях кожи, после чего образуются синяки и кровоизлияния, а при ослабленном иммунитете присоединяется инфекция. Пациенты часто имеют кровоточивость десен, носовые кровотечения, у женщин обильны менструальные выделения.
В связи с этим развивается анемия, усталость, слабость, затруднение легочного дыхания, лихорадка. Лейкопения приводит к снижению иммунитета. В анализах отмечается пониженное содержание лейкоцитов, тромбоцитов, эритроцитов, появляются аномальные бластные клетки (в 10–30% случаев). Развиваются нарушения свертываемости крови, в том числе ДВС-синдром (диссеминированное внутрисосудистое свертывание).
С началом цитостатической терапии симптомы ОПЛ отступают, температура может снизиться уже на следующий день, а также уменьшается кровоточивость. Но это еще не будет признаком восстановления кроветворения – лишь цитостатический эффект.
Диагностика
Для определения заболевания и исключения других форм острого миелоидного лейкоза проводится исследование тканей костного мозга и крови. При этом достоверным признаком острого промиелоцитарного лейкоза является большой процент нетипичных бластов в образцах.
Общий анализ крови покажет анемию и выраженную тромбоцитопению. Цитогенетическое исследование выявит транслокацию длинных плеч хромосом 17 и 15 либо 17 и 11. Также методом полимеразной цепной реакции проводится тестирование на гены PML/RARA или PLZF/RARA. Кроме того, на заболевание указывает избыточное наличие в бластных клетках периферической крови телец Ауэра.
Лечение
Лечение острого промиелоцитарного лейкоза требует участия специалистов различного профиля, а также качественной лабораторной и трансфузиологической службы. Если есть подозрение на ОПЛ, вначале проводится профилактика коагулопатии (введение свежезамороженной плазмы криопреципитата и концентрата тромбоцитов), что особенно важно при активном кровотечении или лабораторных признаках коагулопатии. При первых симптомах этой формы лейкоза проводится терапия ATRA, еще до подтверждения диагноза на цитогенетическом уровне. Кроме того, на четвертый день приема ATRA или сразу же (в зависимости от показаний) проводится химиотерапия.
После интенсивной фазы назначается поддерживающая терапия, которая включает комбинацию химиотерапии и ATRA. Курс длится 24 месяца. Если терапия ATRA неэффективна, плохо переносится пациентом либо наступает рецидив, рекомендуется прием триоксида мышьяка.
Прогноз
В настоящее время прогноз продолжительности жизни при этой форме лейкоза в 70% случаев составляет 12 лет без обострений. Раньше эта форма лейкоза считалась одной из тяжелейших и приводила к гибели пациента в течение суток. Но после изобретения препаратов, эффективных при данном недуге, она стала одной из наиболее излечимых злокачественных патологий.
В 80% случаев лечение вызывает улучшение, все чаще – стойкое. Без лечения продолжительность жизни больного острым промиелоцитарным лейкозом составляет несколько недель или дней.
Острый промиелоцитарный лейкоз | Фонд «Подари жизнь»
Суть болезни
Острый промиелоцитарный лейкоз (ОПЛ, ОМЛ М3, ОПМЛ) – вариант острого миелоидного лейкоза, который характеризуется аномальным накоплением одного из видов миелоидных клеток –
Частота встречаемости
ОПЛ составляет около 10% всех случаев острого миелоидного лейкоза. В отличие от многих других вариантов острого миелолейкоза, ОПЛ часто встречается не у пожилых, а у молодых взрослых: средний возраст больных в момент диагноза около 40 лет. Однако ОПЛ может встречаться в любом возрасте, включая детский.
Признаки и симптомы
Как и остальные виды острого лейкоза, ОПЛ обычно характеризуется проявлениями анемии (утомляемость, слабость, одышка) и тромбоцитопении, то есть недостатка тромбоцитов (повышенная кровоточивость, появление синяков и кровоподтеков). Недостаток нормальных лейкоцитов ведет к инфекциям. Кроме того, при ОПЛ может дополнительно наблюдаться кровоточивость, связанная с синдромом диссеминированного внутрисосудистого свертывания (ДВС). Это наиболее грозный симптом ОПЛ.
Как правило, ОПЛ характеризуется очень быстрым появлением и нарастанием симптомов.
Диагностика
ОПЛ диагностируется на основании морфологического и цитохимического анализа образца костного мозга. Диагностика обязательно включает в себя обнаружение характерной хромосомной транслокации t(15;17) (иногда других, существенно более редких транслокаций) в ходе стандартного цитогенетического или молекулярно-генетического (полимеразная цепная реакция) анализа.
Лечение
Лечение ОПЛ отличается от терапии других форм острого миелоидного лейкоза использованием специфического лекарства — ATRA (полностью транс-ретиноевая кислота, третиноин, весаноид), которое как бы «перепрограммирует» лейкемические промиелоциты на превращение в зрелые гранулоциты. Обычно ATRA используется в сочетании с химиопрепаратами группы антрациклинов (даунорубицин, идарубицин), может также применяться цитарабин. Проводится несколько курсов лечения: индукция, консолидация и поддерживающая терапия в течение 1-2 лет.
К сожалению, примерно у 15% больных использование ATRA вызывает серьезные осложнения (синдром ретиноевой кислоты): одышку, повышение температуры, боли в костях, отеки, прибавку в весе, печеночную и/или почечную недостаточность и другие симптомы. Для лечения этих осложнений используется дексаметазон.
При рецидиве болезни, неэффективности или плохой переносимости терапии ATRA для лечения ОПЛ может применяться триоксид мышьяка (трисенокс, асадин), который во многих случаях характеризуется высокой эффективностью в сочетании с умеренной токсичностью. Среди возможных побочных действий триоксида мышьяка – дифференцировочный синдром, аналогичный упомянутому выше синдрому ретиноевой кислоты; иногда – нарушение сердечного ритма.
В случае рецидива или недостаточной эффективности обычной терапии может применяться аутологичная или аллогенная трансплантация костного мозга.
Прогноз
Без лечения больные ОПЛ погибают в течение нескольких недель, иногда даже считанных дней. Ранее ОПЛ считался разновидностью лейкоза с очень плохим прогнозом. Однако при использовании современных протоколов терапии ОПЛ поддается излечению лучше, чем остальные варианты острого миелоидного лейкоза: стойкая ремиссия достигается у подавляющего большинства больных (более 70%, у молодых пациентов — до 90%). Поскольку столь заметное улучшение связано с открытием лекарств, эффективных против именно этой конкретной разновидности лейкоза, специалисты возлагают надежду на то, что и для других вариантов острого миелоидного лейкоза будут в свое время найдены подобные специфические препараты.Острый промиелоцитарный лейкоз — Википедия
Острый промиелоцитарный лейкоз (ОПМЛ, ОПЛ) — это особый подвид острого миелоидного лейкоза (ОМЛ), злокачественного опухолевого заболевания белых кровяных клеток, по Франко-Американо-Британской классификации (ФАБ) относящийся к подтипу М3.[1] При ОПЛ наблюдается аномальное накопление в костном мозгу и в крови незрелых гранулоцитов, так называемых промиелоцитов. Эта форма ОМЛ характеризуется типичной хромосомной транслокацией, вовлекающей ген рецептора ретиноевой кислоты типа альфа (
Симптомы
Симптомы ОПЛ в целом сходны с симптомами других форм ОМЛ. В частности, возможны следующие симптомы:[5]
Кровоточивость и кровотечения вследствие тромбоцитопении (пониженного содержания тромбоцитов в крови) может наблюдаться в следующих формах:
Острый промиелоцитарный лейкоз обычно характеризуется наличием реципрокной хромосомной транслокации между участком хромосомы 17, содержащим ген рецептора ретиноевой кислоты типа альфа, и участком хромосомы 15, содержащим ген так называемого белка острого промиелоцитарного лейкоза (PML). Эта транслокация приводит к образованию аномального онкогенного фузионного протеина PML-RARalpha. Эта транслокация обозначается как t(15;17)(q22;q21) и встречается в 95 % случаев ОПЛ. А ген рецептора RAR зависит от ретиноевой кислоты для регуляции транскрипции.[1]
Описаны при ПМЛ также 8 типов других редких хромосомных транслокаций, приводящих к формированию других аномальных фузионных онкопротеинов гена RARalpha с другими генами, в частности транслокация t(11;17), приводящая к слиянию гена RARalpha с геном так называемого «цинкового пальцеобразного белка промиелоцитарного лейкоза» (c геном
Слияние генов белков PML и RARA в результате транслокации t(15;17)(q22;q21) приводит к образованию аномального гибридного фузионного онкопротеина с изменёнными (необычными) внутриклеточными функциями. Этот аномальный онкопротеин с повышенным аффинитетом связывается с регуляторными участками внутриклеточной ДНК, блокируя транскрипцию важных генов, необходимых для процесса созревания и дифференцировки гранулоцитов. Он делает это при помощи усиленного взаимодействия молекул белка ядерного корепрессора (NCOR) и молекул гистон-деацетилазы (HDAC). Хотя хромосомная транслокация, включающая ген RARalpha, считается необходимой для инициации (начала) процесса лейкозогенеза, она сама по себе не достаточна для возникновения ПМЛ — требуется также приобретение этими клетками дополнительных мутаций.[1]
Мутация t(11;17), приводящая к образованию аномального фузионного онкопротеина RAR-α/PLZF приводит к развитию такого подтипа ОПЛ, который не чувствителен к стандартной терапии полностью транс-ретиноевой кислотой и/или триоксидом мышьяка и менее чувствителен, по сравнению с более частым вариантом RAR-α/PML, к стандартной химиотерапии ОМЛ, в частности к цитарабину и антрациклинам, таким, как даунорубицин, идарубицин, митоксантрон. Это приводит к худшему прогнозу в этой подгруппе пациентов.[1]
Диагностика
Острый промиелоцитарный лейкоз может быть отдифференцирован от других форм ОМЛ на основании патоморфологического исследования трепанобиоптата и аспирата костного мозга, а также крови, при котором может быть установлено, что бластные клетки по своему строению являются промиелоцитами. Дальнейшая диагностика требует цитогенетического исследования на характерные транслокации длинных плеч хромосом 17 и 15 или 17 и 11 — t(15,17) или t(11,17) и тестирования на наличие фузионных генов PML/RARA или PLZF/RARA, что может быть сделано при помощи полимеразной цепной реакции или флуоресцентной in situ гибридизации. Иногда могут встречаться скрытые транслокации, не обнаруживаемые при стандартном цитогенетическом исследовании. В подобных случаях полимеразная цепная реакция (ПЦР) критически необходима для подтверждения (верификации) диагноза.[1] Наличие в бластных клетках периферической крови большого количества телец Ауэра делает диагноз острого промиелоцитарного лейкоза очень вероятным, так как для бластных промиелоцитов очень характерно обилие телец Ауэра (по сравнению с более ранними бластными клетками типов M0, M1 и M2).
Лечение
Индукционное лечение
Полностью транс-ретиноевая кислотаОПЛ является уникальным среди острых миелоидных лейкозов по своей чувствительности к полностью транс-ретиноевой кислоте, кислой форме витамина А и к триоксиду мышьяка.[1] Лечение полностью транс-ретиноевой кислотой вызывает диссоциацию белкового комплекса RAR с белками NCOR (ядерным корепрессором) и HDACL (лиганд гистон-деацетилазы) и позволяет, напротив, связываться с рецептором RAR активаторам транскрипции и гистон-ацетилтрансферазам. Это, в свою очередь, позволяет запуститься процессу транскрипции нужных генов и процессу дифференцировки незрелых лейкозных промиелоцитов в зрелые гранулоциты. Таким образом, благодаря влиянию полностью транс-ретиноевой кислоты, «исправляется» аберрантная работа онкогенного транскрипционного фактора PML/RARalpha. При этом, в отличие от традиционной химиотерапии, полностью транс-ретиноевая кислота непосредственно не убивает злокачественные клетки. Вместо этого полностью транс-ретиноевая кислота вызывает их терминальную дифференцировку, после которой они подвергаются спонтанному апоптозу подобно здоровым гранулоцитам, у которых истёк отведённый им срок жизни (причём «в норме», до приобретения злокачественным клоном анти-апоптотических мутаций, апоптоз этих дифференцировавшихся под влиянием ATRA злокачественных клеток происходит гораздо быстрее, чем апоптоз здоровых гранулоцитов).[1] Полностью транс-ретиноевая кислота одна (в монотерапии) способна вызвать ремиссию при ОПЛ. Однако ремиссия, вызванная применением одной лишь ATRA, при ОПЛ, как правило, кратковременна в отсутствие одновременно проводимой «традиционной» химиотерапии и/или лечения триоксидом мышьяка, так как лейкозные клетки довольно быстро приобретают устойчивость к ATRA.[1] Начиная с 2013 года стандартом лечения ОПЛ является одновременное применение ATRA и триоксида мышьяка (плюс-минус традиционная химиотерапия).[7] До 2013 года стандартом лечения ОПЛ было одновременное применение ATRA и традиционной химиотерапии, основанной на применении антрациклинов (даунорубицин, доксорубицин, идарубицин или митоксантрон).
Ранее, до выявления того факта, что ОПЛ менее других разновидностей ОМЛ нуждается в традиционной химиотерапии и менее других разновидностей ОМЛ чувствителен к цитарабину, зато более других разновидностей чувствителен к антрациклинам, и что добавление цитарабина или других агентов не увеличивает процент полных ремиссий и общую выживаемость по сравнению с сочетанием «ATRA + антрациклин», зато более токсично, вместо схемы «ATRA + монотерапия антрациклином» часто применяли лечение «ATRA + та или иная схема традиционной противолейкозной химиотерапии» (например, ATRA + «7+3» или ATRA + ADE). Обе разновидности лечения (ATRA плюс триоксид мышьяка и ATRA плюс традиционная химиотерапия) приводят к примерно одинаковым результатам — около 90—95 % полных клинических и гематологических ремиссий. Но поскольку триоксид мышьяка менее токсичен и даёт меньше побочных эффектов, чем традиционная химиотерапия, и более специфичен в отношении клеток ОПЛ, то именно сочетание ATRA и триоксида мышьяка стало новым стандартом лечения ОПЛ.[4]
Лечение полностью транс-ретиноевой кислотой ассоциируется с уникальным побочным эффектом, ранее называвшимся «синдром ретиноевой кислоты» (более современное и корректное название «дифференциационный синдром» или «синдром дифференциации»)].[8] Дифференциационный синдром проявляется затруднением лёгочного дыхания (диспноэ), головной болью, лихорадкой (гипертермией), прибавкой массы тела, периферическими отеками, коагулопатией (кровоточивостью или тромбозами, ДВС-синдромом). Лечится дифференциационный синдром немедленным назначением глюкокортикоидов, например, преднизолона или дексаметазона, назначением гепарина для профилактики ДВС-синдрома и немедленным присоединением (или увеличением дозы) химиотерапии к уже проводящемуся лечению ATRA. При резко выраженном дифференциационном синдроме может потребоваться временная отмена или временное снижение дозы ATRA.[9] Этиологию дифференциационного синдрома связывают с массивным высвобождением цитокинов из массово дифференцирующихся и затем погибающих лейкозных промиелоцитов, что приводит к резкому повышению проницаемости капилляров (отеки, диспноэ и др.) и нарушениям в свертывающей системе крови.[9]
Моноклональное антитело гемтузумаб озогамицин (Милотарг) в комбинации с ATRA также было успешно использовано в лечении ОПЛ.[10] Однако оно было изъято с рынка США из-за подозрений в чрезмерной токсичности этого лекарства и отсутствии у него положительного влияния на общую и безрецидивную выживаемость больных с ОМЛ, отсутствии преимуществ перед традиционной химиотерапией. В Австралии, Канаде или Великобритании это лекарство никогда не продавалось.[10][11] Гемтузумаб озогамицин в комбинации с ATRA вызывал положительный ответ у приблизительно 84 % пациентов с ОПЛ, что сравнимо с цифрами, наблюдавшимися у пациентов, лечившихся традиционной комбинацией «ATRA плюс антрациклин».[10] Поскольку гемтузумаб озогамицин обладает меньшей кардиотоксичностью, чем антрациклины, такой вариант лечения мог бы быть более предпочтительным для пожилых больных с ОПЛ и больных с сопутствующими сердечно-сосудистыми заболеваниями.[10]
Консолидационное лечение
После достижения стойкой ремиссии стандартно рекомендуется 2 года поддерживающей терапии ATRA в сочетании с меркаптопурином и метотрексатом.[12] Значительный процент больных с ОПЛ рецидивирует без проведения поддерживающей терапии.[9] В европейском исследовании по ОПЛ, частота рецидивов в течение 2 лет среди тех, кто не получал поддерживающей химиотерапии, составляла 27 %, по сравнению с 11 % рецидивов у тех, которые поддерживающую химиотерапию получали.[13] Аналогично, в исследовании по ОПЛ, проведённом в США в 2000 году, общая 5-летняя выживаемость среди больных с ОПЛ, получавших поддерживающую терапию ATRA, составляла 61 %, по сравнению с 31 % среди тех, кто поддерживающую терапию ATRA не получал.[14]
Рецидив или рефрактерное заболевание
При рецидивах и рефрактерности ОПЛ в настоящее время изучается применение триоксида мышьяка. Были сообщения о достижении ремиссии при помощи монотерапии триоксидом мышьяка.[15] Исследования показали, что триоксид мышьяка вызывает реорганизацию ядерных телец и способствует деактивации и деградации мутантного PML-RAR онкопротеина.[16] Триоксид мышьяка также повышает активность каспазы, что вызывает апоптоз клеток.[17] Подобно ATRA, профилактическое применение триоксида мышьяка в поддерживающей терапии способно снизить риск рецидивов при ОПЛ, особенно у пациентов из группы высокого риска.[18] В Японии синтетический ретиноид, тамибаротен, лицензирован для применения при резистентном к ATRA ОПЛ.[19]
Помимо этого, при рецидивах и рефрактерности ОПЛ сохраняет своё значение и традиционная противолейкозная химиотерапия, в частности схемы «7+3», ADE, FLAG-подобные режимы и другие, а также высокодозная химиотерапия и аллогенная трансплантация гемопоэтических стволовых клеток.
Исследовательские агенты
Некоторые исследования показывают возможную потенциальную эффективность ингибиторов гистон-деацетилазы, таких, как вориностат или вальпроевая кислота, в лечении ОПЛ.[20][21][22]
Эпидемиология
Острый промиелоцитарный лейкоз представляет сравнительно редкую форму ОМЛ, всего около 10 — 12 % от всех случаев ОМЛ.[10] Средний возраст больных ОПЛ — приблизительно 30 — 40 лет,[23] что гораздо моложе, чем средний возраст больных с другими подтипами ОМЛ (70 лет). Частота ОПЛ выше среди пациентов латиноамериканского или южноевропейского происхождения.[24] ОПЛ может также возникнуть как вторичный лейкоз у больных, получавших лечение антрациклинами (например, доксорубицином, идарубицином, митоксантроном), алкилирующими агентами (например, циклофосфамидом) или ингибиторами топоизомеразы II (например, этопозидом), вследствие канцерогенности этих агентов. Большинство пациентов, получавших лечение этими агентами, у которых впоследствии развился ОПЛ, составляют больные с раком молочной железы в анамнезе.[25][26][27] У приблизительно 40 % пациентов с ОПЛ обнаруживаются, помимо t(15;17)(q22;q21), приводящей к появлению PML/RARalpha, дополнительные хромосомные аномалии в лейкозных клетках, такие, как трисомия 8-й хромосомы или изохромосома 17, но они, по-видимому, не оказывают существенного влияния на долгосрочный прогноз.[1]
Примечания
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 Kotiah, SD; Besa, EC. Sarkodee-Adoo, C; Talavera, F; Sacher, RA; McKenna, R; Besa, EC: Acute Promyelocytic Leukemia. Medscape Reference. WebMD (3 June 2013). Проверено 14 января 2014.
- ↑ Tallman MS, Altman JK (2008). «Curative strategies in acute promyelocytic leukemia». Hematology Am Soc Hematol Educ Program 2008: 391–9. DOI:10.1182/asheducation-2008.1.391. PMID 19074116.
- ↑ Hillestad, LK (November 1957). «Acute promyelocytic leukemia». Acta Med Scand. 159 (3): 189–94. DOI:10.1111/j.0954-6820.1957.tb00124.x. PMID 13508085.
- ↑ 1 2 Adès, L; Guerci, A; Raffoux, E; Sanz, M; Chevallier, P; Lapusan, S; Recher, C; Thomas, X; Rayon, C; Castaigne, S; Tournilhac, O; de Botton, S; Ifrah, N; Cahn JY; Solary E; Gardin, C; Fegeux, N; Bordessoule, D; Ferrant, A; Meyer-Monard, S; Vey, N; Dombret, H; Degos, L; Chevret, S; Fenaux, P; European APL Group (March 2010). «Very long-term outcome of acute promyelocytic leukemia after treatment with all-trans retinoic acid and chemotherapy: the European APL Group experience» (PDF). Blood 115 (9): 1690–1696. DOI:10.1182/blood-2009-07-233387. PMID 20018913.
- ↑ Kotiah, SD; Besa, EC. Sarkodee-Adoo, C; Talavera, F; Sacher, RA; McKenna, R; Besa, EC: Acute Promyelocytic Leukemia Clinical Presentation. Medscape Reference. WebMD (3 June 2013). Проверено 14 января 2014.
- ↑ Chen Z, Brand NJ, et al. (March 1993). «Fusion between a novel Krüppel-like zinc finger gene and the retinoic acid receptor-alpha locus due to a variant t(11;17) translocation associated with acute promyelocytic leukaemia». EMBO J 12 (3): 1161–7. PMID 8384553.
- ↑ Francesco Lo-Coco, M.D., et al. (July 2013). «Retinoic Acid and Arsenic Trioxide for Acute Promyelocytic Leukemia». New England Journal of Medicine 369 (2): 111–121. DOI:10.1056/NEJMoa1300874.
- ↑ Breccia, M; Latagliata, R; Carmosino, I; Cannella, L; Diverio, D; Guarini, A; De Propris, MS; Petti, MC; Avvisati, G; Cimino, G; Mandelli, F; Lo-Coco, F (December 2008). «Clinical and biological features of acute promyelocytic leukemia patients developing retinoic acid syndrome during induction treatment with all-trans retinoic acid and idarubicin». Haematologica 93 (12): 1918–20. DOI:10.3324/haematol.13510. PMID 18945746.
- ↑ 1 2 3 Kotiah, SD; Besa, EC. Sarkodee-Adoo, C; Talavera, F; Sacher, RA; McKenna, R; Besa, EC: Acute Promyelocytic Leukemia Treatment & Management. Medscape Reference. WebMD (3 June 2013). Проверено 14 января 2014.
- ↑ 1 2 3 4 5 Ravandi, F; Estey, EH; Appelbaum, FR; Lo-Coco, F; Schiffer, CA; Larson, RA; Burnett, AK; Kantarjian, HM (November 2012). «Gemtuzumab Ozogamicin: Time to Resurrect?» (PDF). Journal of Clinical Oncology 30 (32): 3921–3923. DOI:10.1200/JCO.2012.43.0132. PMID 22987091.
- ↑ Martindale: The Complete Drug Reference. — Pharmaceutical Press, 23 September 2011.
- ↑ Kotiah, SD. Anand, J; Braden, CD; Harris, JE: Acute Promyelocytic Leukema Treatment Protocols. Medscape Reference. WebMD (28 October 2013). Проверено 14 января 2014.
- ↑ Fenaux, P; Chastang, C; Chevret, S; Sanz, M; Dombret, H; Archimbaud, E; Fey, M; Rayon, C; Huguet, F; Sotto, JJ; Gardin, C; Makhoul, PC; Travade, P; Solary, E; Fegueux, N; Bordessoule, D; Miguel, JS; Link, H; Desablens, B; Stamatoullas, A; Deconinck, E; Maloisel, F; Castaigne, S; Preudhomme, C; Degos, L (August 1999). «A Randomized Comparison of All Transretinoic Acid (ATRA) Followed by Chemotherapy and ATRA Plus Chemotherapy and the Role of Maintenance Therapy in Newly Diagnosed Acute Promyelocytic Leukemia» (PDF). Blood 94 (4): 1192–1200. PMID 10438706.
- ↑ Tallman, MS; Andersen, JW; Schiffer, CA; Appelbaum, FR; Feusner, JH; Woods, WG; Ogden, A; Weinstein, H; Shepherd, L; Willman, C; Bloomfield, CD; Rowe, JM; Wiernik, PH (December 2002). «All-transretinoic acid in acute promyelocytic leukemia: long-term outcome and prognostic factor analysis from the North American Intergroup protocol» (PDF). Blood 100 (13): 4298–4302. DOI:10.1182/blood-2002-02-0632. PMID 12393590.
- ↑ Soignet SL, Maslak P, Wang ZG, et al. (November 1998). «Complete remission after treatment of acute promyelocytic leukemia with arsenic trioxide». N. Engl. J. Med. 339 (19): 1341–8. DOI:10.1056/NEJM199811053391901. PMID 9801394.
- ↑ Soignet,Complete Remission After Treatment of APL with Arsenic Trioxide 1998, 1346
- ↑ Soignet, 1998, 1347
- ↑ Arsenic Compound Improves Survival in Acute Promyelocytic Leukemia Patients . Sept 2007
- ↑ Miwako, I; Kagechika, H (August 2007). «Tamibarotene». Drugs Today (Barc) 43 (8): 563–568. DOI:10.1358/dot.2007.43.8.1072615. PMID 17925887.
- ↑ Martens, JH; Brinkman, AB; Simmer, F; Francoijs, KJ; Nebbioso, A; Ferrara, F; Altucci, L; Stunnenberg, HG (February 2010). «PML-RARa/RXR Alters the Epigenetic Landscape in Acute Promyelocytic Leukemia» (PDF). Cancer Cell 17 (2): 173–185. DOI:10.1016/j.ccr.2009.12.042. PMID 20159609.
- ↑ Leiva, M; Moretti, S; Soilihi, H; Pallavicini, I; Peres, L; Mercurio, C; Dal Zuffo, R; Minucci, S; de Thé, H (July 2012). «Valproic acid induces differentiation and transient tumor regression, but spares leukemia-initiating activity in mouse models of APL». Leukemia 26 (7): 1630–1637. DOI:10.1038/leu.2012.39. PMID 22333881.
- ↑ «Histone deacetylase inhibitors induce remission in transgenic models of therapy-resistant acute promyelocytic leukemia» (PDF). He, LZ; Tolentino, T; Grayson, P; Zhong, S; Warrell, RP Jr; Rifkind, RA; Marks, PA; Richon, VM; Pandolfi, PP 108 (9): 1321–1330. DOI:10.1172/JCI11537. PMID 11696577.
- ↑ Schiffer, CA; Stone, RM. Chapter 124: Acute Myeloid Leukemia in Adults // Holland-Frei Cancer Medicine / Bast, RC; Kufe, DW; Pollock, RE. — 5th. — Hamilton, ON : BC Decker, 2000.
- ↑ Douer, D; Santillana, S; Ramezani, L; Samanez, C; Slovak, ML; Lee, MS; Watkins, K; Williams, T; Vallejos, C (August 2003). «Acute promyelocytic leukaemia in patients originating in Latin America and is associated with an increased frequency of the bcr1 subtype of the PML/RARalpha fusion gene». British Journal of Haematology 122 (4): 563–70. DOI:10.1046/j.1365-2141.2003.04480.x. PMID 12899711.
- ↑ Ravandi, F (April 2011). «Therapy-related acute promyelocytic leukemia» (PDF). Haematologica 96 (4): 493–495. DOI:10.3324/haematol.2011.041970. PMID 21454880.
- ↑ Elliott, MA; Letendre, L; Tefferi, A; Hogan, WJ; Hook, C; Kaufmann, SH; Pruthi, RK; Pardanani, A; Begna, KH; Ashrani, AA; Wolanskyj, AP; Al-Kali, A; Litzow, MR (March 2012). «Therapy-related acute promyelocytic leukemia: observations relating to APL pathogenesis and therapy». European Journal of Haematology 88 (3): 237–243. DOI:10.1111/j.1600-0609.2011.01727.x. PMID 22023492.
- ↑ Rashidi, A; Fisher, SI (2013). «Therapy-related acute promyelocytic leukemia: a systematic review». Medical Oncology 30 (3): 625. DOI:10.1007/s12032-013-0625-5. PMID 23771799.
Ссылки
Острый промиелоцитарный лейкоз: прогноз, лечение
Некоторые заболевания крови чаще поражают детей. Острый промиелоцитарный лейкоз относится как раз к таковым и представляет собой рак белых кровяных телец. Механизм развития этой патологии заключается в чрезмерном образовании и накоплении в костном мозгу незрелых гранулоцитарных клеток. К заболеванию приводят генные и хромосомные аномалии. Течение болезни острое, с наличием характерной клинической симптоматики. Диагностируют ее по внешним признакам и данным лабораторных исследований. Лечение производится посредством введения трансретиноевой кислоты. Прогноз при этом типе заболевания относительно благоприятный.
Этиология патологии и факторы риска ее развития
Болезнь является генетически обусловленной. Главной ее причиной выступает дефект гена RAR, кодирующего рецепторы ретиноевой кислоты.
Заболевание белого ростка крови развивается вследствие таких причин:
- Генетические и хромосомные аномалии. Они характеризуются транслокациями участков хромосом, активациями патологических генов с запуском неконтролируемого размножения клеток-мутантов.
- Воздействие радиации. Обучение легко проникает через все ткани организма, попадая в костный мозг, где нарушает клеточное деление.
- Тератогенные факторы. Если на плод во время беременности воздействовали физические и химические агенты, это может привести к врожденным дефектом кроветворения.
- Использование гербицидов и инсектицидов. Употребление в пищу продуктов, в которых содержится остаточная концентрация этих химических веществ, также приводит к генным аномалиям.
Как распознать заболевание?
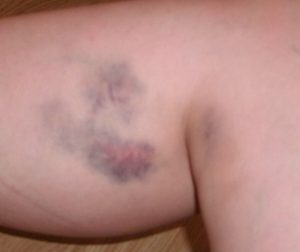 Одним из симптомов есть проявления синяков, которые возникают вследствие подкожного кровоизлияния.
Одним из симптомов есть проявления синяков, которые возникают вследствие подкожного кровоизлияния.Острый промиелоцитарный лейкоз дебютирует такой клинической симптоматикой:
- Астенизация организма. Ребенок или взрослый ощущают постоянную усталость, разбитость, головную боль и нежелание что-либо делать.
- Анемия. На фоне нарушения одного из участков кровяного ростка возникает малокровие.
- Одышка с нарушениями дыхательного ритма.
- Гипертермия. Температура чаще держится на субфебрильных цифрах, но может доходить до лихорадки.
- Кровоточивость десен.
- Самопроизвольное возникновение синяков. Они являются подкожными кровоизлияниями, возникающими вследствие тромбоцитопении — недостаточного количества свертывающих факторов крови.
- Склонность к инфекционным заболеваниям. Пациенты часто болеют вирусными и бактериальными инфекциями, сопровождающимися тяжелыми осложнениями.
Диагностика недуга
Лейкоз диагностируют по таким критериям:
- Лейкопения. Это низкое содержание в крови белых кровяных телец.
- Тромбоцитопения. Этим термином обозначают пониженное содержание тромбоцитов, обеспечивающих свертываемость крови.
- Эритропения. Общий анализ крови дает низкий показатель эритроцитов — клеток, переносящих тканям кислород.
- Периодический лейкоцитоз с наличием бластов. Это аномальное повышение концентрации лейкоцитов в период выброса патологических клеток из костного мозга.
- Коагулопатия. Этим термином обозначают нарушения свертывающих и противосвертывающих свойств крови.
- Наличие кровоизлияний при кожных и жгутовых пробах.
Методы лечения
 Метотрексат в комплексном медикаментозном лечении способствует уничтожению злокачественных клеток.
Метотрексат в комплексном медикаментозном лечении способствует уничтожению злокачественных клеток.Промиелоцитарный лейкоз лечится с помощью препаратов ретиноевой кислоты и мышьяка. Пациентов госпитализируют в онкологический стационар, где им дают также цитостатики — «Метотрексат» и «Митоксантрон». Все эти лекарства убивают злокачественные клетки, позволяя костному мозгу продуцировать нормальные. Применяют также медикаменты из группы антрациклинов. К ним относятся «Доксорубицин», «Даунорубицин» и «Идарубицин». Лечение производится по специальной схеме, с учетом чувствительности костномозговых структур. От трансретиноевой кислоты существует ряд побочных эффектов, объединяемых в синдром. Его составляющими являются головная боль, лихорадка, периферические отеки и синдром диссеминированного внутрисосудистого свертывания.
Вернуться к оглавлениюПрогноз при патологии
Продолжительность жизни при этом тяжелом заболевании крови составляет от 10 до 12 лет. Это достаточно длительный период, если сравнивать с другими болезнями кровяного ростка.
Патология прогрессирует в 70% случаев. Поэтому прогноз является относительно благоприятным с учетом положительного ответа пациента на лечебную тактику. Если у больного наблюдаются изменения в костном мозгу и периферической крови, это означает, что его шансы выжить повышаются. Прогноз улучшается также у тех пациентов, у которых заболевание дебютировало в более старшем возрасте. У малышей подобный диагноз практически всегда приводит к летальному исходу.
Острый промиелоцитарный лейкоз — Википедия. Что такое Острый промиелоцитарный лейкоз
Острый промиелоцитарный лейкоз (ОПМЛ, ОПЛ) — это особый подвид острого миелоидного лейкоза (ОМЛ), злокачественного опухолевого заболевания белых кровяных клеток, по Франко-Американо-Британской классификации (ФАБ) относящийся к подтипу М3.[1] При ОПЛ наблюдается аномальное накопление в костном мозгу и в крови незрелых гранулоцитов, так называемых промиелоцитов. Эта форма ОМЛ характеризуется типичной хромосомной транслокацией, вовлекающей ген рецептора ретиноевой кислоты типа альфа (RARα или RARA) и ген белка острого промиелоцитарного лейкоза (PML), что приводит к образованию аномального фузионного онкопротеина PML-RARalpha и к неконтролируемому размножению мутантных промиелоцитов. Эта форма ОМЛ также отличается уникальным ответом на лечение полностью транс-ретиноевой кислотой и триоксидом мышьяка. Острый промиелоцитарный лейкоз был впервые описан и охарактеризован в 1957 году[2][3]французскими и норвежскими врачами-онкогематологами. В то время ОПЛ считался сверхострым и фатальным заболеванием, одной из самых неблагоприятных форм ОМЛ.[1] В настоящее время ОПЛ с классической транслокацией, напротив, считается одной из самых благоприятных и хорошо излечимых форм острого миелоидного лейкоза, с 12-летней выживаемостью без прогрессирования приблизительно 70 %.[1][4]
Симптомы
Симптомы ОПЛ в целом сходны с симптомами других форм ОМЛ. В частности, возможны следующие симптомы:[5]
Кровоточивость и кровотечения вследствие тромбоцитопении (пониженного содержания тромбоцитов в крови) может наблюдаться в следующих формах:
Острый промиелоцитарный лейкоз обычно характеризуется наличием реципрокной хромосомной транслокации между участком хромосомы 17, содержащим ген рецептора ретиноевой кислоты типа альфа, и участком хромосомы 15, содержащим ген так называемого белка острого промиелоцитарного лейкоза (PML). Эта транслокация приводит к образованию аномального онкогенного фузионного протеина PML-RARalpha. Эта транслокация обозначается как t(15;17)(q22;q21) и встречается в 95 % случаев ОПЛ. А ген рецептора RAR зависит от ретиноевой кислоты для регуляции транскрипции.[1]
Описаны при ПМЛ также 8 типов других редких хромосомных транслокаций, приводящих к формированию других аномальных фузионных онкопротеинов гена RARalpha с другими генами, в частности транслокация t(11;17), приводящая к слиянию гена RARalpha с геном так называемого «цинкового пальцеобразного белка промиелоцитарного лейкоза» (c геном PLZF, известным также как ген ZBTB16)[6], с геном нуклеофосмина (NPM1), с геном, ассоциированным с ядерным матриксом (NUMA1), с геном фактора 5b сигнальной трансдукции и активации транскрипции (STAT5B), с геном регуляторной субъединицы 1α протеинкиназы А (PRKAR1A), с геном фактора, взаимодействующего с белками PAPOLA и CPSF1 (FIP1L1), с геном корепрессора BCL-6 или с геном олигонуклетид/олигосахарид-связывающей последовательности 2A (OBFC2A, также известный как NABP1). Некоторые из этих хромосомных аномалий также являются чувствительными к лечению полностью транс-ретиноевой кислотой, либо их чувствительность к лечению полностью транс-ретиноевой кислотой неизвестна вследствие большой редкости этих хромосомных перестроек. Известно, что формы ОПЛ с хромосомными перестройками, приводящими к образованию аномальных фузионных онкопротеинов STAT5B/RARA и PLZF/RARA, резистентен к лечению полностью транс-ретиноевой кислотой и поэтому имеют худший прогноз.[1]
Слияние генов белков PML и RARA в результате транслокации t(15;17)(q22;q21) приводит к образованию аномального гибридного фузионного онкопротеина с изменёнными (необычными) внутриклеточными функциями. Этот аномальный онкопротеин с повышенным аффинитетом связывается с регуляторными участками внутриклеточной ДНК, блокируя транскрипцию важных генов, необходимых для процесса созревания и дифференцировки гранулоцитов. Он делает это при помощи усиленного взаимодействия молекул белка ядерного корепрессора (NCOR) и молекул гистон-деацетилазы (HDAC). Хотя хромосомная транслокация, включающая ген RARalpha, считается необходимой для инициации (начала) процесса лейкозогенеза, она сама по себе не достаточна для возникновения ПМЛ — требуется также приобретение этими клетками дополнительных мутаций.[1]
Мутация t(11;17), приводящая к образованию аномального фузионного онкопротеина RAR-α/PLZF приводит к развитию такого подтипа ОПЛ, который не чувствителен к стандартной терапии полностью транс-ретиноевой кислотой и/или триоксидом мышьяка и менее чувствителен, по сравнению с более частым вариантом RAR-α/PML, к стандартной химиотерапии ОМЛ, в частности к цитарабину и антрациклинам, таким, как даунорубицин, идарубицин, митоксантрон. Это приводит к худшему прогнозу в этой подгруппе пациентов.[1]
Диагностика
Острый промиелоцитарный лейкоз может быть отдифференцирован от других форм ОМЛ на основании патоморфологического исследования трепанобиоптата и аспирата костного мозга, а также крови, при котором может быть установлено, что бластные клетки по своему строению являются промиелоцитами. Дальнейшая диагностика требует цитогенетического исследования на характерные транслокации длинных плеч хромосом 17 и 15 или 17 и 11 — t(15,17) или t(11,17) и тестирования на наличие фузионных генов PML/RARA или PLZF/RARA, что может быть сделано при помощи полимеразной цепной реакции или флуоресцентной in situ гибридизации. Иногда могут встречаться скрытые транслокации, не обнаруживаемые при стандартном цитогенетическом исследовании. В подобных случаях полимеразная цепная реакция (ПЦР) критически необходима для подтверждения (верификации) диагноза.[1] Наличие в бластных клетках периферической крови большого количества телец Ауэра делает диагноз острого промиелоцитарного лейкоза очень вероятным, так как для бластных промиелоцитов очень характерно обилие телец Ауэра (по сравнению с более ранними бластными клетками типов M0, M1 и M2).
Лечение
Индукционное лечение
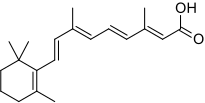 Полностью транс-ретиноевая кислота
Полностью транс-ретиноевая кислота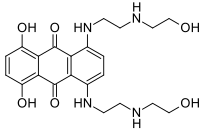
ОПЛ является уникальным среди острых миелоидных лейкозов по своей чувствительности к полностью транс-ретиноевой кислоте, кислой форме витамина А и к триоксиду мышьяка.[1] Лечение полностью транс-ретиноевой кислотой вызывает диссоциацию белкового комплекса RAR с белками NCOR (ядерным корепрессором) и HDACL (лиганд гистон-деацетилазы) и позволяет, напротив, связываться с рецептором RAR активаторам транскрипции и гистон-ацетилтрансферазам. Это, в свою очередь, позволяет запуститься процессу транскрипции нужных генов и процессу дифференцировки незрелых лейкозных промиелоцитов в зрелые гранулоциты. Таким образом, благодаря влиянию полностью транс-ретиноевой кислоты, «исправляется» аберрантная работа онкогенного транскрипционного фактора PML/RARalpha. При этом, в отличие от традиционной химиотерапии, полностью транс-ретиноевая кислота непосредственно не убивает злокачественные клетки. Вместо этого полностью транс-ретиноевая кислота вызывает их терминальную дифференцировку, после которой они подвергаются спонтанному апоптозу подобно здоровым гранулоцитам, у которых истёк отведённый им срок жизни (причём «в норме», до приобретения злокачественным клоном анти-апоптотических мутаций, апоптоз этих дифференцировавшихся под влиянием ATRA злокачественных клеток происходит гораздо быстрее, чем апоптоз здоровых гранулоцитов).[1] Полностью транс-ретиноевая кислота одна (в монотерапии) способна вызвать ремиссию при ОПЛ. Однако ремиссия, вызванная применением одной лишь ATRA, при ОПЛ, как правило, кратковременна в отсутствие одновременно проводимой «традиционной» химиотерапии и/или лечения триоксидом мышьяка, так как лейкозные клетки довольно быстро приобретают устойчивость к ATRA.[1] Начиная с 2013 года стандартом лечения ОПЛ является одновременное применение ATRA и триоксида мышьяка (плюс-минус традиционная химиотерапия).[7] До 2013 года стандартом лечения ОПЛ было одновременное применение ATRA и традиционной химиотерапии, основанной на применении антрациклинов (даунорубицин, доксорубицин, идарубицин или митоксантрон).
Ранее, до выявления того факта, что ОПЛ менее других разновидностей ОМЛ нуждается в традиционной химиотерапии и менее других разновидностей ОМЛ чувствителен к цитарабину, зато более других разновидностей чувствителен к антрациклинам, и что добавление цитарабина или других агентов не увеличивает процент полных ремиссий и общую выживаемость по сравнению с сочетанием «ATRA + антрациклин», зато более токсично, вместо схемы «ATRA + монотерапия антрациклином» часто применяли лечение «ATRA + та или иная схема традиционной противолейкозной химиотерапии» (например, ATRA + «7+3» или ATRA + ADE). Обе разновидности лечения (ATRA плюс триоксид мышьяка и ATRA плюс традиционная химиотерапия) приводят к примерно одинаковым результатам — около 90—95 % полных клинических и гематологических ремиссий. Но поскольку триоксид мышьяка менее токсичен и даёт меньше побочных эффектов, чем традиционная химиотерапия, и более специфичен в отношении клеток ОПЛ, то именно сочетание ATRA и триоксида мышьяка стало новым стандартом лечения ОПЛ.[4]
Лечение полностью транс-ретиноевой кислотой ассоциируется с уникальным побочным эффектом, ранее называвшимся «синдром ретиноевой кислоты» (более современное и корректное название «дифференциационный синдром» или «синдром дифференциации»)].[8] Дифференциационный синдром проявляется затруднением лёгочного дыхания (диспноэ), головной болью, лихорадкой (гипертермией), прибавкой массы тела, периферическими отеками, коагулопатией (кровоточивостью или тромбозами, ДВС-синдромом). Лечится дифференциационный синдром немедленным назначением глюкокортикоидов, например, преднизолона или дексаметазона, назначением гепарина для профилактики ДВС-синдрома и немедленным присоединением (или увеличением дозы) химиотерапии к уже проводящемуся лечению ATRA. При резко выраженном дифференциационном синдроме может потребоваться временная отмена или временное снижение дозы ATRA.[9] Этиологию дифференциационного синдрома связывают с массивным высвобождением цитокинов из массово дифференцирующихся и затем погибающих лейкозных промиелоцитов, что приводит к резкому повышению проницаемости капилляров (отеки, диспноэ и др.) и нарушениям в свертывающей системе крови.[9]
Моноклональное антитело гемтузумаб озогамицин (Милотарг) в комбинации с ATRA также было успешно использовано в лечении ОПЛ.[10] Однако оно было изъято с рынка США из-за подозрений в чрезмерной токсичности этого лекарства и отсутствии у него положительного влияния на общую и безрецидивную выживаемость больных с ОМЛ, отсутствии преимуществ перед традиционной химиотерапией. В Австралии, Канаде или Великобритании это лекарство никогда не продавалось.[10][11] Гемтузумаб озогамицин в комбинации с ATRA вызывал положительный ответ у приблизительно 84 % пациентов с ОПЛ, что сравнимо с цифрами, наблюдавшимися у пациентов, лечившихся традиционной комбинацией «ATRA плюс антрациклин».[10] Поскольку гемтузумаб озогамицин обладает меньшей кардиотоксичностью, чем антрациклины, такой вариант лечения мог бы быть более предпочтительным для пожилых больных с ОПЛ и больных с сопутствующими сердечно-сосудистыми заболеваниями.[10]
Консолидационное лечение
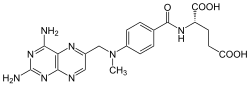
После достижения стойкой ремиссии стандартно рекомендуется 2 года поддерживающей терапии ATRA в сочетании с меркаптопурином и метотрексатом.[12] Значительный процент больных с ОПЛ рецидивирует без проведения поддерживающей терапии.[9] В европейском исследовании по ОПЛ, частота рецидивов в течение 2 лет среди тех, кто не получал поддерживающей химиотерапии, составляла 27 %, по сравнению с 11 % рецидивов у тех, которые поддерживающую химиотерапию получали.[13] Аналогично, в исследовании по ОПЛ, проведённом в США в 2000 году, общая 5-летняя выживаемость среди больных с ОПЛ, получавших поддерживающую терапию ATRA, составляла 61 %, по сравнению с 31 % среди тех, кто поддерживающую терапию ATRA не получал.[14]
Рецидив или рефрактерное заболевание
При рецидивах и рефрактерности ОПЛ в настоящее время изучается применение триоксида мышьяка. Были сообщения о достижении ремиссии при помощи монотерапии триоксидом мышьяка.[15] Исследования показали, что триоксид мышьяка вызывает реорганизацию ядерных телец и способствует деактивации и деградации мутантного PML-RAR онкопротеина.[16] Триоксид мышьяка также повышает активность каспазы, что вызывает апоптоз клеток.[17] Подобно ATRA, профилактическое применение триоксида мышьяка в поддерживающей терапии способно снизить риск рецидивов при ОПЛ, особенно у пациентов из группы высокого риска.[18] В Японии синтетический ретиноид, тамибаротен, лицензирован для применения при резистентном к ATRA ОПЛ.[19]
Помимо этого, при рецидивах и рефрактерности ОПЛ сохраняет своё значение и традиционная противолейкозная химиотерапия, в частности схемы «7+3», ADE, FLAG-подобные режимы и другие, а также высокодозная химиотерапия и аллогенная трансплантация гемопоэтических стволовых клеток.
Исследовательские агенты
Некоторые исследования показывают возможную потенциальную эффективность ингибиторов гистон-деацетилазы, таких, как вориностат или вальпроевая кислота, в лечении ОПЛ.[20][21][22]
Эпидемиология
Острый промиелоцитарный лейкоз представляет сравнительно редкую форму ОМЛ, всего около 10 — 12 % от всех случаев ОМЛ.[10] Средний возраст больных ОПЛ — приблизительно 30 — 40 лет,[23] что гораздо моложе, чем средний возраст больных с другими подтипами ОМЛ (70 лет). Частота ОПЛ выше среди пациентов латиноамериканского или южноевропейского происхождения.[24] ОПЛ может также возникнуть как вторичный лейкоз у больных, получавших лечение антрациклинами (например, доксорубицином, идарубицином, митоксантроном), алкилирующими агентами (например, циклофосфамидом) или ингибиторами топоизомеразы II (например, этопозидом), вследствие канцерогенности этих агентов. Большинство пациентов, получавших лечение этими агентами, у которых впоследствии развился ОПЛ, составляют больные с раком молочной железы в анамнезе.[25][26][27] У приблизительно 40 % пациентов с ОПЛ обнаруживаются, помимо t(15;17)(q22;q21), приводящей к появлению PML/RARalpha, дополнительные хромосомные аномалии в лейкозных клетках, такие, как трисомия 8-й хромосомы или изохромосома 17, но они, по-видимому, не оказывают существенного влияния на долгосрочный прогноз.[1]
Примечания
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 Kotiah, SD; Besa, EC. Sarkodee-Adoo, C; Talavera, F; Sacher, RA; McKenna, R; Besa, EC: Acute Promyelocytic Leukemia. Medscape Reference. WebMD (3 June 2013). Проверено 14 января 2014.
- ↑ Tallman MS, Altman JK (2008). “Curative strategies in acute promyelocytic leukemia”. Hematology Am Soc Hematol Educ Program. 2008: 391—9. DOI:10.1182/asheducation-2008.1.391. PMID 19074116.
- ↑ Hillestad, LK (November 1957). “Acute promyelocytic leukemia”. Acta Med Scand. 159 (3): 189—94. DOI:10.1111/j.0954-6820.1957.tb00124.x. PMID 13508085.
- ↑ 1 2 Adès, L; Guerci, A; Raffoux, E; Sanz, M; Chevallier, P; Lapusan, S; Recher, C; Thomas, X; Rayon, C; Castaigne, S; Tournilhac, O; de Botton, S; Ifrah, N; Cahn JY; Solary E; Gardin, C; Fegeux, N; Bordessoule, D; Ferrant, A; Meyer-Monard, S; Vey, N; Dombret, H; Degos, L; Chevret, S; Fenaux, P; European APL Group (March 2010). “Very long-term outcome of acute promyelocytic leukemia after treatment with all-trans retinoic acid and chemotherapy: the European APL Group experience” (PDF). Blood. 115 (9): 1690—1696. DOI:10.1182/blood-2009-07-233387. PMID 20018913.
- ↑ Kotiah, SD; Besa, EC. Sarkodee-Adoo, C; Talavera, F; Sacher, RA; McKenna, R; Besa, EC: Acute Promyelocytic Leukemia Clinical Presentation. Medscape Reference. WebMD (3 June 2013). Проверено 14 января 2014.
- ↑ Chen Z, Brand NJ; et al. (March 1993). “Fusion between a novel Krüppel-like zinc finger gene and the retinoic acid receptor-alpha locus due to a variant t(11;17) translocation associated with acute promyelocytic leukaemia”. EMBO J. 12 (3): 1161—7. PMC 413318. PMID 8384553.
- ↑ Francesco Lo-Coco, M.D.; et al. (July 2013). “Retinoic Acid and Arsenic Trioxide for Acute Promyelocytic Leukemia”. New England Journal of Medicine. 369 (2): 111—121. DOI:10.1056/NEJMoa1300874.
- ↑ Breccia, M; Latagliata, R; Carmosino, I; Cannella, L; Diverio, D; Guarini, A; De Propris, MS; Petti, MC; Avvisati, G; Cimino, G; Mandelli, F; Lo-Coco, F (December 2008). “Clinical and biological features of acute promyelocytic leukemia patients developing retinoic acid syndrome during induction treatment with all-trans retinoic acid and idarubicin”. Haematologica. 93 (12): 1918—20. DOI:10.3324/haematol.13510. PMID 18945746.
- ↑ 1 2 3 Kotiah, SD; Besa, EC. Sarkodee-Adoo, C; Talavera, F; Sacher, RA; McKenna, R; Besa, EC: Acute Promyelocytic Leukemia Treatment & Management. Medscape Reference. WebMD (3 June 2013). Проверено 14 января 2014.
- ↑ 1 2 3 4 5 Ravandi, F; Estey, EH; Appelbaum, FR; Lo-Coco, F; Schiffer, CA; Larson, RA; Burnett, AK; Kantarjian, HM (November 2012). “Gemtuzumab Ozogamicin: Time to Resurrect?” (PDF). Journal of Clinical Oncology. 30 (32): 3921—3923. DOI:10.1200/JCO.2012.43.0132. PMID 22987091.
- ↑ Martindale: The Complete Drug Reference. — Pharmaceutical Press, 23 September 2011.
- ↑ Kotiah, SD. Anand, J; Braden, CD; Harris, JE: Acute Promyelocytic Leukema Treatment Protocols. Medscape Reference. WebMD (28 October 2013). Проверено 14 января 2014.
- ↑ Fenaux, P; Chastang, C; Chevret, S; Sanz, M; Dombret, H; Archimbaud, E; Fey, M; Rayon, C; Huguet, F; Sotto, JJ; Gardin, C; Makhoul, PC; Travade, P; Solary, E; Fegueux, N; Bordessoule, D; Miguel, JS; Link, H; Desablens, B; Stamatoullas, A; Deconinck, E; Maloisel, F; Castaigne, S; Preudhomme, C; Degos, L (August 1999). “A Randomized Comparison of All Transretinoic Acid (ATRA) Followed by Chemotherapy and ATRA Plus Chemotherapy and the Role of Maintenance Therapy in Newly Diagnosed Acute Promyelocytic Leukemia” (PDF). Blood. 94 (4): 1192—1200. PMID 10438706.
- ↑ Tallman, MS; Andersen, JW; Schiffer, CA; Appelbaum, FR; Feusner, JH; Woods, WG; Ogden, A; Weinstein, H; Shepherd, L; Willman, C; Bloomfield, CD; Rowe, JM; Wiernik, PH (December 2002). “All-transretinoic acid in acute promyelocytic leukemia: long-term outcome and prognostic factor analysis from the North American Intergroup protocol” (PDF). Blood. 100 (13): 4298—4302. DOI:10.1182/blood-2002-02-0632. PMID 12393590.
- ↑ Soignet SL, Maslak P, Wang ZG; et al. (November 1998). “Complete remission after treatment of acute promyelocytic leukemia with arsenic trioxide”. N. Engl. J. Med. 339 (19): 1341—8. DOI:10.1056/NEJM199811053391901. PMID 9801394.
- ↑ Soignet,Complete Remission After Treatment of APL with Arsenic Trioxide 1998, 1346
- ↑ Soignet, 1998, 1347
- ↑ Arsenic Compound Improves Survival in Acute Promyelocytic Leukemia Patients . Sept 2007
- ↑ Miwako, I; Kagechika, H (August 2007). “Tamibarotene”. Drugs Today (Barc). 43 (8): 563—568. DOI:10.1358/dot.2007.43.8.1072615. PMID 17925887.
- ↑ Martens, JH; Brinkman, AB; Simmer, F; Francoijs, KJ; Nebbioso, A; Ferrara, F; Altucci, L; Stunnenberg, HG (February 2010). “PML-RARa/RXR Alters the Epigenetic Landscape in Acute Promyelocytic Leukemia” (PDF). Cancer Cell. 17 (2): 173—185. DOI:10.1016/j.ccr.2009.12.042. PMID 20159609. Архивировано из оригинала (PDF) 2013-03-15. Проверено 2014-09-16.
- ↑ Leiva, M; Moretti, S; Soilihi, H; Pallavicini, I; Peres, L; Mercurio, C; Dal Zuffo, R; Minucci, S; de Thé, H (July 2012). “Valproic acid induces differentiation and transient tumor regression, but spares leukemia-initiating activity in mouse models of APL”. Leukemia. 26 (7): 1630—1637. DOI:10.1038/leu.2012.39. PMID 22333881.
- ↑ “Histone deacetylase inhibitors induce remission in transgenic models of therapy-resistant acute promyelocytic leukemia” (PDF). He, LZ; Tolentino, T; Grayson, P; Zhong, S; Warrell, RP Jr; Rifkind, RA; Marks, PA; Richon, VM; Pandolfi, PP. 108 (9): 1321—1330. DOI:10.1172/JCI11537. PMC 209432. PMID 11696577.
- ↑ Schiffer, CA; Stone, RM. Chapter 124: Acute Myeloid Leukemia in Adults // Holland-Frei Cancer Medicine / Bast, RC; Kufe, DW; Pollock, RE. — 5th. — Hamilton, ON : BC Decker, 2000.
- ↑ Douer, D; Santillana, S; Ramezani, L; Samanez, C; Slovak, ML; Lee, MS; Watkins, K; Williams, T; Vallejos, C (August 2003). “Acute promyelocytic leukaemia in patients originating in Latin America and is associated with an increased frequency of the bcr1 subtype of the PML/RARalpha fusion gene”. British Journal of Haematology. 122 (4): 563—70. DOI:10.1046/j.1365-2141.2003.04480.x. PMID 12899711.
- ↑ Ravandi, F (April 2011). “Therapy-related acute promyelocytic leukemia” (PDF). Haematologica. 96 (4): 493—495. DOI:10.3324/haematol.2011.041970. PMC 3069223. PMID 21454880.
- ↑ Elliott, MA; Letendre, L; Tefferi, A; Hogan, WJ; Hook, C; Kaufmann, SH; Pruthi, RK; Pardanani, A; Begna, KH; Ashrani, AA; Wolanskyj, AP; Al-Kali, A; Litzow, MR (March 2012). “Therapy-related acute promyelocytic leukemia: observations relating to APL pathogenesis and therapy”. European Journal of Haematology. 88 (3): 237—243. DOI:10.1111/j.1600-0609.2011.01727.x. PMID 22023492.
- ↑ Rashidi, A; Fisher, SI (2013). “Therapy-related acute promyelocytic leukemia: a systematic review”. Medical Oncology. 30 (3): 625. DOI:10.1007/s12032-013-0625-5. PMID 23771799.
Ссылки
Острый промиелоцитарный лейкоз — Википедия
Острый промиелоцитарный лейкоз (ОПМЛ, ОПЛ) — это особый подвид острого миелоидного лейкоза (ОМЛ), злокачественного опухолевого заболевания белых кровяных клеток, по Франко-Американо-Британской классификации (ФАБ) относящийся к подтипу М3.[1] При ОПЛ наблюдается аномальное накопление в костном мозгу и в крови незрелых гранулоцитов, так называемых промиелоцитов. Эта форма ОМЛ характеризуется типичной хромосомной транслокацией, вовлекающей ген рецептора ретиноевой кислоты типа альфа (RARα или RARA) и ген белка острого промиелоцитарного лейкоза (PML), что приводит к образованию аномального фузионного онкопротеина PML-RARalpha и к неконтролируемому размножению мутантных промиелоцитов. Эта форма ОМЛ также отличается уникальным ответом на лечение полностью транс-ретиноевой кислотой и триоксидом мышьяка. Острый промиелоцитарный лейкоз был впервые описан и охарактеризован в 1957 году[2][3]французскими и норвежскими врачами-онкогематологами. В то время ОПЛ считался сверхострым и фатальным заболеванием, одной из самых неблагоприятных форм ОМЛ.[1] В настоящее время ОПЛ с классической транслокацией, напротив, считается одной из самых благоприятных и хорошо излечимых форм острого миелоидного лейкоза, с 12-летней выживаемостью без прогрессирования приблизительно 70 %.[1][4]
Симптомы
Симптомы ОПЛ в целом сходны с симптомами других форм ОМЛ. В частности, возможны следующие симптомы:[5]
Кровоточивость и кровотечения вследствие тромбоцитопении (пониженного содержания тромбоцитов в крови) может наблюдаться в следующих формах:
Видео по теме
Острый промиелоцитарный лейкоз обычно характеризуется наличием реципрокной хромосомной транслокации между участком хромосомы 17, содержащим ген рецептора ретиноевой кислоты типа альфа, и участком хромосомы 15, содержащим ген так называемого белка острого промиелоцитарного лейкоза (PML). Эта транслокация приводит к образованию аномального онкогенного фузионного протеина PML-RARalpha. Эта транслокация обозначается как t(15;17)(q22;q21) и встречается в 95 % случаев ОПЛ. А ген рецептора RAR зависит от ретиноевой кислоты для регуляции транскрипции.[1]
Описаны при ПМЛ также 8 типов других редких хромосомных транслокаций, приводящих к формированию других аномальных фузионных онкопротеинов гена RARalpha с другими генами, в частности транслокация t(11;17), приводящая к слиянию гена RARalpha с геном так называемого «цинкового пальцеобразного белка промиелоцитарного лейкоза» (c геном PLZF, известным также как ген ZBTB16)[6], с геном нуклеофосмина (NPM1), с геном, ассоциированным с ядерным матриксом (NUMA1), с геном фактора 5b сигнальной трансдукции и активации транскрипции (STAT5B), с геном регуляторной субъединицы 1α протеинкиназы А (PRKAR1A), с геном фактора, взаимодействующего с белками PAPOLA и CPSF1 (FIP1L1), с геном корепрессора BCL-6 или с геном олигонуклетид/олигосахарид-связывающей последовательности 2A (OBFC2A, также известный как NABP1). Некоторые из этих хромосомных аномалий также являются чувствительными к лечению полностью транс-ретиноевой кислотой, либо их чувствительность к лечению полностью транс-ретиноевой кислотой неизвестна вследствие большой редкости этих хромосомных перестроек. Известно, что формы ОПЛ с хромосомными перестройками, приводящими к образованию аномальных фузионных онкопротеинов STAT5B/RARA и PLZF/RARA, резистентен к лечению полностью транс-ретиноевой кислотой и поэтому имеют худший прогноз.[1]
Слияние генов белков PML и RARA в результате транслокации t(15;17)(q22;q21) приводит к образованию аномального гибридного фузионного онкопротеина с изменёнными (необычными) внутриклеточными функциями. Этот аномальный онкопротеин с повышенным аффинитетом связывается с регуляторными участками внутриклеточной ДНК, блокируя транскрипцию важных генов, необходимых для процесса созревания и дифференцировки гранулоцитов. Он делает это при помощи усиленного взаимодействия молекул белка ядерного корепрессора (NCOR) и молекул гистон-деацетилазы (HDAC). Хотя хромосомная транслокация, включающая ген RARalpha, считается необходимой для инициации (начала) процесса лейкозогенеза, она сама по себе не достаточна для возникновения ПМЛ — требуется также приобретение этими клетками дополнительных мутаций.[1]
Мутация t(11;17), приводящая к образованию аномального фузионного онкопротеина RAR-α/PLZF приводит к развитию такого подтипа ОПЛ, который не чувствителен к стандартной терапии полностью транс-ретиноевой кислотой и/или триоксидом мышьяка и менее чувствителен, по сравнению с более частым вариантом RAR-α/PML, к стандартной химиотерапии ОМЛ, в частности к цитарабину и антрациклинам, таким, как даунорубицин, идарубицин, митоксантрон. Это приводит к худшему прогнозу в этой подгруппе пациентов.[1]
Диагностика
Острый промиелоцитарный лейкоз может быть отдифференцирован от других форм ОМЛ на основании патоморфологического исследования трепанобиоптата и аспирата костного мозга, а также крови, при котором может быть установлено, что бластные клетки по своему строению являются промиелоцитами. Дальнейшая диагностика требует цитогенетического исследования на характерные транслокации длинных плеч хромосом 17 и 15 или 17 и 11 — t(15,17) или t(11,17) и тестирования на наличие фузионных генов PML/RARA или PLZF/RARA, что может быть сделано при помощи полимеразной цепной реакции или флуоресцентной in situ гибридизации. Иногда могут встречаться скрытые транслокации, не обнаруживаемые при стандартном цитогенетическом исследовании. В подобных случаях полимеразная цепная реакция (ПЦР) критически необходима для подтверждения (верификации) диагноза.[1] Наличие в бластных клетках периферической крови большого количества телец Ауэра делает диагноз острого промиелоцитарного лейкоза очень вероятным, так как для бластных промиелоцитов очень характерно обилие телец Ауэра (по сравнению с более ранними бластными клетками типов M0, M1 и M2).
Лечение
Индукционное лечение
 Полностью транс-ретиноевая кислота
Полностью транс-ретиноевая кислота

ОПЛ является уникальным среди острых миелоидных лейкозов по своей чувствительности к полностью транс-ретиноевой кислоте, кислой форме витамина А и к триоксиду мышьяка.[1] Лечение полностью транс-ретиноевой кислотой вызывает диссоциацию белкового комплекса RAR с белками NCOR (ядерным корепрессором) и HDACL (лиганд гистон-деацетилазы) и позволяет, напротив, связываться с рецептором RAR активаторам транскрипции и гистон-ацетилтрансферазам. Это, в свою очередь, позволяет запуститься процессу транскрипции нужных генов и процессу дифференцировки незрелых лейкозных промиелоцитов в зрелые гранулоциты. Таким образом, благодаря влиянию полностью транс-ретиноевой кислоты, «исправляется» аберрантная работа онкогенного транскрипционного фактора PML/RARalpha. При этом, в отличие от традиционной химиотерапии, полностью транс-ретиноевая кислота непосредственно не убивает злокачественные клетки. Вместо этого полностью транс-ретиноевая кислота вызывает их терминальную дифференцировку, после которой они подвергаются спонтанному апоптозу подобно здоровым гранулоцитам, у которых истёк отведённый им срок жизни (причём «в норме», до приобретения злокачественным клоном анти-апоптотических мутаций, апоптоз этих дифференцировавшихся под влиянием ATRA злокачественных клеток происходит гораздо быстрее, чем апоптоз здоровых гранулоцитов).[1] Полностью транс-ретиноевая кислота одна (в монотерапии) способна вызвать ремиссию при ОПЛ. Однако ремиссия, вызванная применением одной лишь ATRA, при ОПЛ, как правило, кратковременна в отсутствие одновременно проводимой «традиционной» химиотерапии и/или лечения триоксидом мышьяка, так как лейкозные клетки довольно быстро приобретают устойчивость к ATRA.[1] Начиная с 2013 года стандартом лечения ОПЛ является одновременное применение ATRA и триоксида мышьяка (плюс-минус традиционная химиотерапия).[7] До 2013 года стандартом лечения ОПЛ было одновременное применение ATRA и традиционной химиотерапии, основанной на применении антрациклинов (даунорубицин, доксорубицин, идарубицин или митоксантрон).
Ранее, до выявления того факта, что ОПЛ менее других разновидностей ОМЛ нуждается в традиционной химиотерапии и менее других разновидностей ОМЛ чувствителен к цитарабину, зато более других разновидностей чувствителен к антрациклинам, и что добавление цитарабина или других агентов не увеличивает процент полных ремиссий и общую выживаемость по сравнению с сочетанием «ATRA + антрациклин», зато более токсично, вместо схемы «ATRA + монотерапия антрациклином» часто применяли лечение «ATRA + та или иная схема традиционной противолейкозной химиотерапии» (например, ATRA + «7+3» или ATRA + ADE). Обе разновидности лечения (ATRA плюс триоксид мышьяка и ATRA плюс традиционная химиотерапия) приводят к примерно одинаковым результатам — около 90—95 % полных клинических и гематологических ремиссий. Но поскольку триоксид мышьяка менее токсичен и даёт меньше побочных эффектов, чем традиционная химиотерапия, и более специфичен в отношении клеток ОПЛ, то именно сочетание ATRA и триоксида мышьяка стало новым стандартом лечения ОПЛ.[4]
Лечение полностью транс-ретиноевой кислотой ассоциируется с уникальным побочным эффектом, ранее называвшимся «синдром ретиноевой кислоты» (более современное и корректное название «дифференциационный синдром» или «синдром дифференциации»)].[8] Дифференциационный синдром проявляется затруднением лёгочного дыхания (диспноэ), головной болью, лихорадкой (гипертермией), прибавкой массы тела, периферическими отеками, коагулопатией (кровоточивостью или тромбозами, ДВС-синдромом). Лечится дифференциационный синдром немедленным назначением глюкокортикоидов, например, преднизолона или дексаметазона, назначением гепарина для профилактики ДВС-синдрома и немедленным присоединением (или увеличением дозы) химиотерапии к уже проводящемуся лечению ATRA. При резко выраженном дифференциационном синдроме может потребоваться временная отмена или временное снижение дозы ATRA.[9] Этиологию дифференциационного синдрома связывают с массивным высвобождением цитокинов из массово дифференцирующихся и затем погибающих лейкозных промиелоцитов, что приводит к резкому повышению проницаемости капилляров (отеки, диспноэ и др.) и нарушениям в свертывающей системе крови.[9]
Моноклональное антитело гемтузумаб озогамицин (Милотарг) в комбинации с ATRA также было успешно использовано в лечении ОПЛ.[10] Однако оно было изъято с рынка США из-за подозрений в чрезмерной токсичности этого лекарства и отсутствии у него положительного влияния на общую и безрецидивную выживаемость больных с ОМЛ, отсутствии преимуществ перед традиционной химиотерапией. В Австралии, Канаде или Великобритании это лекарство никогда не продавалось.[10][11] Гемтузумаб озогамицин в комбинации с ATRA вызывал положительный ответ у приблизительно 84 % пациентов с ОПЛ, что сравнимо с цифрами, наблюдавшимися у пациентов, лечившихся традиционной комбинацией «ATRA плюс антрациклин».[10] Поскольку гемтузумаб озогамицин обладает меньшей кардиотоксичностью, чем антрациклины, такой вариант лечения мог бы быть более предпочтительным для пожилых больных с ОПЛ и больных с сопутствующими сердечно-сосудистыми заболеваниями.[10]
Консолидационное лечение
После достижения стойкой ремиссии стандартно рекомендуется 2 года поддерживающей терапии ATRA в сочетании с меркаптопурином и метотрексатом.[12] Значительный процент больных с ОПЛ рецидивирует без проведения поддерживающей терапии.[9] В европейском исследовании по ОПЛ, частота рецидивов в течение 2 лет среди тех, кто не получал поддерживающей химиотерапии, составляла 27 %, по сравнению с 11 % рецидивов у тех, которые поддерживающую химиотерапию получали.[13] Аналогично, в исследовании по ОПЛ, проведённом в США в 2000 году, общая 5-летняя выживаемость среди больных с ОПЛ, получавших поддерживающую терапию ATRA, составляла 61 %, по сравнению с 31 % среди тех, кто поддерживающую терапию ATRA не получал.[14]
Рецидив или рефрактерное заболевание
При рецидивах и рефрактерности ОПЛ в настоящее время изучается применение триоксида мышьяка. Были сообщения о достижении ремиссии при помощи монотерапии триоксидом мышьяка.[15] Исследования показали, что триоксид мышьяка вызывает реорганизацию ядерных телец и способствует деактивации и деградации мутантного PML-RAR онкопротеина.[16] Триоксид мышьяка также повышает активность каспазы, что вызывает апоптоз клеток.[17] Подобно ATRA, профилактическое применение триоксида мышьяка в поддерживающей терапии способно снизить риск рецидивов при ОПЛ, особенно у пациентов из группы высокого риска.[18] В Японии синтетический ретиноид, тамибаротен, лицензирован для применения при резистентном к ATRA ОПЛ.[19]
Помимо этого, при рецидивах и рефрактерности ОПЛ сохраняет своё значение и традиционная противолейкозная химиотерапия, в частности схемы «7+3», ADE, FLAG-подобные режимы и другие, а также высокодозная химиотерапия и аллогенная трансплантация гемопоэтических стволовых клеток.
Исследовательские агенты
Некоторые исследования показывают возможную потенциальную эффективность ингибиторов гистон-деацетилазы, таких, как вориностат или вальпроевая кислота, в лечении ОПЛ.[20][21][22]
Эпидемиология
Острый промиелоцитарный лейкоз представляет сравнительно редкую форму ОМЛ, всего около 10 — 12 % от всех случаев ОМЛ.[10] Средний возраст больных ОПЛ — приблизительно 30 — 40 лет,[23] что гораздо моложе, чем средний возраст больных с другими подтипами ОМЛ (70 лет). Частота ОПЛ выше среди пациентов латиноамериканского или южноевропейского происхождения.[24] ОПЛ может также возникнуть как вторичный лейкоз у больных, получавших лечение антрациклинами (например, доксорубицином, идарубицином, митоксантроном), алкилирующими агентами (например, циклофосфамидом) или ингибиторами топоизомеразы II (например, этопозидом), вследствие канцерогенности этих агентов. Большинство пациентов, получавших лечение этими агентами, у которых впоследствии развился ОПЛ, составляют больные с раком молочной железы в анамнезе.[25][26][27] У приблизительно 40 % пациентов с ОПЛ обнаруживаются, помимо t(15;17)(q22;q21), приводящей к появлению PML/RARalpha, дополнительные хромосомные аномалии в лейкозных клетках, такие, как трисомия 8-й хромосомы или изохромосома 17, но они, по-видимому, не оказывают существенного влияния на долгосрочный прогноз.[1]
Примечания
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 Kotiah, SD; Besa, EC. Sarkodee-Adoo, C; Talavera, F; Sacher, RA; McKenna, R; Besa, EC: Acute Promyelocytic Leukemia. Medscape Reference. WebMD (3 June 2013). Проверено 14 января 2014.
- ↑ Tallman MS, Altman JK (2008). «Curative strategies in acute promyelocytic leukemia». Hematology Am Soc Hematol Educ Program 2008: 391–9. DOI:10.1182/asheducation-2008.1.391. PMID 19074116.
- ↑ Hillestad, LK (November 1957). «Acute promyelocytic leukemia». Acta Med Scand. 159 (3): 189–94. DOI:10.1111/j.0954-6820.1957.tb00124.x. PMID 13508085.
- ↑ 1 2 Adès, L; Guerci, A; Raffoux, E; Sanz, M; Chevallier, P; Lapusan, S; Recher, C; Thomas, X; Rayon, C; Castaigne, S; Tournilhac, O; de Botton, S; Ifrah, N; Cahn JY; Solary E; Gardin, C; Fegeux, N; Bordessoule, D; Ferrant, A; Meyer-Monard, S; Vey, N; Dombret, H; Degos, L; Chevret, S; Fenaux, P; European APL Group (March 2010). «Very long-term outcome of acute promyelocytic leukemia after treatment with all-trans retinoic acid and chemotherapy: the European APL Group experience» (PDF). Blood 115 (9): 1690–1696. DOI:10.1182/blood-2009-07-233387. PMID 20018913.
- ↑ Kotiah, SD; Besa, EC. Sarkodee-Adoo, C; Talavera, F; Sacher, RA; McKenna, R; Besa, EC: Acute Promyelocytic Leukemia Clinical Presentation. Medscape Reference. WebMD (3 June 2013). Проверено 14 января 2014.
- ↑ Chen Z, Brand NJ, et al. (March 1993). «Fusion between a novel Krüppel-like zinc finger gene and the retinoic acid receptor-alpha locus due to a variant t(11;17) translocation associated with acute promyelocytic leukaemia». EMBO J 12 (3): 1161–7. PMID 8384553.
- ↑ Francesco Lo-Coco, M.D., et al. (July 2013). «Retinoic Acid and Arsenic Trioxide for Acute Promyelocytic Leukemia». New England Journal of Medicine 369 (2): 111–121. DOI:10.1056/NEJMoa1300874.
- ↑ Breccia, M; Latagliata, R; Carmosino, I; Cannella, L; Diverio, D; Guarini, A; De Propris, MS; Petti, MC; Avvisati, G; Cimino, G; Mandelli, F; Lo-Coco, F (December 2008). «Clinical and biological features of acute promyelocytic leukemia patients developing retinoic acid syndrome during induction treatment with all-trans retinoic acid and idarubicin». Haematologica 93 (12): 1918–20. DOI:10.3324/haematol.13510. PMID 18945746.
- ↑ 1 2 3 Kotiah, SD; Besa, EC. Sarkodee-Adoo, C; Talavera, F; Sacher, RA; McKenna, R; Besa, EC: Acute Promyelocytic Leukemia Treatment & Management. Medscape Reference. WebMD (3 June 2013). Проверено 14 января 2014.
- ↑ 1 2 3 4 5 Ravandi, F; Estey, EH; Appelbaum, FR; Lo-Coco, F; Schiffer, CA; Larson, RA; Burnett, AK; Kantarjian, HM (November 2012). «Gemtuzumab Ozogamicin: Time to Resurrect?» (PDF). Journal of Clinical Oncology 30 (32): 3921–3923. DOI:10.1200/JCO.2012.43.0132. PMID 22987091.
- ↑ Martindale: The Complete Drug Reference. — Pharmaceutical Press, 23 September 2011.
- ↑ Kotiah, SD. Anand, J; Braden, CD; Harris, JE: Acute Promyelocytic Leukema Treatment Protocols. Medscape Reference. WebMD (28 October 2013). Проверено 14 января 2014.
- ↑ Fenaux, P; Chastang, C; Chevret, S; Sanz, M; Dombret, H; Archimbaud, E; Fey, M; Rayon, C; Huguet, F; Sotto, JJ; Gardin, C; Makhoul, PC; Travade, P; Solary, E; Fegueux, N; Bordessoule, D; Miguel, JS; Link, H; Desablens, B; Stamatoullas, A; Deconinck, E; Maloisel, F; Castaigne, S; Preudhomme, C; Degos, L (August 1999). «A Randomized Comparison of All Transretinoic Acid (ATRA) Followed by Chemotherapy and ATRA Plus Chemotherapy and the Role of Maintenance Therapy in Newly Diagnosed Acute Promyelocytic Leukemia» (PDF). Blood 94 (4): 1192–1200. PMID 10438706.
- ↑ Tallman, MS; Andersen, JW; Schiffer, CA; Appelbaum, FR; Feusner, JH; Woods, WG; Ogden, A; Weinstein, H; Shepherd, L; Willman, C; Bloomfield, CD; Rowe, JM; Wiernik, PH (December 2002). «All-transretinoic acid in acute promyelocytic leukemia: long-term outcome and prognostic factor analysis from the North American Intergroup protocol» (PDF). Blood 100 (13): 4298–4302. DOI:10.1182/blood-2002-02-0632. PMID 12393590.
- ↑ Soignet SL, Maslak P, Wang ZG, et al. (November 1998). «Complete remission after treatment of acute promyelocytic leukemia with arsenic trioxide». N. Engl. J. Med. 339 (19): 1341–8. DOI:10.1056/NEJM199811053391901. PMID 9801394.
- ↑ Soignet,Complete Remission After Treatment of APL with Arsenic Trioxide 1998, 1346
- ↑ Soignet, 1998, 1347
- ↑ Arsenic Compound Improves Survival in Acute Promyelocytic Leukemia Patients . Sept 2007
- ↑ Miwako, I; Kagechika, H (August 2007). «Tamibarotene». Drugs Today (Barc) 43 (8): 563–568. DOI:10.1358/dot.2007.43.8.1072615. PMID 17925887.
- ↑ Martens, JH; Brinkman, AB; Simmer, F; Francoijs, KJ; Nebbioso, A; Ferrara, F; Altucci, L; Stunnenberg, HG (February 2010). «PML-RARa/RXR Alters the Epigenetic Landscape in Acute Promyelocytic Leukemia» (PDF). Cancer Cell 17 (2): 173–185. DOI:10.1016/j.ccr.2009.12.042. PMID 20159609.
- ↑ Leiva, M; Moretti, S; Soilihi, H; Pallavicini, I; Peres, L; Mercurio, C; Dal Zuffo, R; Minucci, S; de Thé, H (July 2012). «Valproic acid induces differentiation and transient tumor regression, but spares leukemia-initiating activity in mouse models of APL». Leukemia 26 (7): 1630–1637. DOI:10.1038/leu.2012.39. PMID 22333881.
- ↑ «Histone deacetylase inhibitors induce remission in transgenic models of therapy-resistant acute promyelocytic leukemia» (PDF). He, LZ; Tolentino, T; Grayson, P; Zhong, S; Warrell, RP Jr; Rifkind, RA; Marks, PA; Richon, VM; Pandolfi, PP 108 (9): 1321–1330. DOI:10.1172/JCI11537. PMID 11696577.
- ↑ Schiffer, CA; Stone, RM. Chapter 124: Acute Myeloid Leukemia in Adults // Holland-Frei Cancer Medicine / Bast, RC; Kufe, DW; Pollock, RE. — 5th. — Hamilton, ON : BC Decker, 2000.
- ↑ Douer, D; Santillana, S; Ramezani, L; Samanez, C; Slovak, ML; Lee, MS; Watkins, K; Williams, T; Vallejos, C (August 2003). «Acute promyelocytic leukaemia in patients originating in Latin America and is associated with an increased frequency of the bcr1 subtype of the PML/RARalpha fusion gene». British Journal of Haematology 122 (4): 563–70. DOI:10.1046/j.1365-2141.2003.04480.x. PMID 12899711.
- ↑ Ravandi, F (April 2011). «Therapy-related acute promyelocytic leukemia» (PDF). Haematologica 96 (4): 493–495. DOI:10.3324/haematol.2011.041970. PMID 21454880.
- ↑ Elliott, MA; Letendre, L; Tefferi, A; Hogan, WJ; Hook, C; Kaufmann, SH; Pruthi, RK; Pardanani, A; Begna, KH; Ashrani, AA; Wolanskyj, AP; Al-Kali, A; Litzow, MR (March 2012). «Therapy-related acute promyelocytic leukemia: observations relating to APL pathogenesis and therapy». European Journal of Haematology 88 (3): 237–243. DOI:10.1111/j.1600-0609.2011.01727.x. PMID 22023492.
- ↑ Rashidi, A; Fisher, SI (2013). «Therapy-related acute promyelocytic leukemia: a systematic review». Medical Oncology 30 (3): 625. DOI:10.1007/s12032-013-0625-5. PMID 23771799.
Ссылки
— ГБУ «КОКБ» Курганская областная клиническая больница — Официальный сайт
20 тысяч пациентов
ежегодно доверяют нам заботу о своем здоровье и проходят лечение в стационаре
10 тысяч операций
ежегодно выполняется в КОКБ, многие из которых уникальны
600 пациентов в день
обращаются в областную консультативную поликлинику, прием
проводится по 25 специальностям
1275 сотрудников
сегодня работает в КОКБ, в том числе 189 врачей и 558 средних медицинских работников
6
докторов
медицинских наук
18 кандидатов медицинских наук, 8 заслуженных врачей РФ трудятся сегодня к КОКБ
72% врачей
имеют высшую и первую категорию
6 корпусов
больничный городок состоит из 6 корпусов, хозяйственных служб
19
специализированных
отделений
в состав больницы входят 19 отделений на 520 коек
4
сертифицированные
лаборатории
Все виды анализов с использованием современного оборудования
1713
электронных
листков нетрудоспособности
выдано с начала 2018 года
7 врачей
ГБУ «КОКБ» в 2018 году удостоились награды «Лучший врач года»
24 врача
ГБУ «КОКБ» являются главными внештатными специалистами Департамента здравоохранения Курганской области
