Симптомы описторхоза у взрослых и детей. Диагностика, лечение
Летом часто обостряются заболевания желудочно-кишечного тракта. Одна из неприятных болезней – описторхоз. Её симптомы можно легко принять за гастрит. Но точный диагноз могут поставить только в медицинских центрах. Что такое описторхоз, как он себя проявляет и куда обращаться с первыми неприятными симптомами, рассказываем в этой статье.
Что такое описторхоз?
Трематодоз, вызванный плоскими червями. Возбудитель описторхоза, попадая в организм человека, концентрируется в печени и желчевыводящей системе. Паразит попадает в организм человека из плохо термически обработанных морепродуктов – сырой, вяленой, копченой рыбы или представителей семейства карповых.
Чем опасен описторхоз?
Возбудитель заболевания двуустка кошачья паразитирует в желчном пузыре и желчных протоках и пожирает слизистую оболочку органов. Постепенно ухудшается нормальный пищеварительный процесс. Возникает дисбактериоз, появляется аллергическая реакция непонятного происхождения, воспаляются ближайшие к желчному пузырю внутренние органы, формируются камни.
Если патология появляется во время беременности, паразит оказывает угнетающее действие на развитие плода, физическое и умственное развитие. Одно из самых страшных последствий – рак печени, желчного пузыря, поджелудочной железы.
Помимо органов желудочно-кишечного тракта, у больного страдают сердце и сосуды, обмен веществ, нервная система. Как следствие, может возникать вегетососудистая дистония, бессонница, нервозность, появляется тремор конечностей, снижается аппетит, изменяется менструальный цикл.
Первые симптомы описторхоза
Первые признаки появляются при снижении защитной функции иммунитета. На ранних стадиях пациент сталкивается с появлением общей слабости, усиливается потоотделение. Острая форма описторхоза проявляется следующим образом:
-
появление бессонницы и нервозности;
-
боль в правом подреберье;
-
болевые ощущения в спине и животе;
-
наличие астматического бронхита;
-
ощущение ломоты в теле и повышение температуры;
-
появление на коже аллергических высыпаний;
-
присутствие метеоризма, тошноты, рвоты, болей в животе, общего дискомфорта;
-
резкое снижение аппетита, слишком жидкая консистенция стула.

При обследовании организма врач может обнаружить увеличенную печень, повышенное количество эозинофилов в общем анализе крови.
Симптомы описторхоза у взрослых несколько отличаются от первых признаков детей. У маленьких непосед заболевание выражается в проявлении устойчивого аллергоза, интоксикации всего организма и иммунодепрессивном состоянии. Также может повышаться температура и держаться до 2-3 недель.
Симптомы у женщин проявляются наиболее ярко во время менструального цикла. Если в печени женщины есть паразит, то менструации становятся очень болезненными, а цикл становится нестабильным.
Как быстро проявляется патология?
Когда паразиты попадают в организм человека, начинают снижаться защитные функции иммунитета. После этого в течение 20 дней могут проявляться первые признаки. Человек испытывает общую слабость, недомогание, учащенное сердцебиение, повышение температуры тела, сильное потоотделение.
Примерно через 30 дней заболевание переходит в хроническую стадию и его симптомы становятся похожи на хронический холецистит, гастродуоденит, панкреатит, гепатит. Беспокоят приступы боли в правом подреберье, схожие с желчными коликами. Появляется нервозность, нарушения сна, хроническая усталость, частые аллергические высыпания на коже, дрожат руки, веки.
Период острого этапа заболевания – от нескольких дней до 3 месяцев, иногда дольше. К симптомам присоединяются признаки лёгочных заболеваний, увеличивается печень, могут выявиться эрозии и язвы слизистых оболочек и тканей желудка, двенадцатиперстной кишки во время проведения исследования.
Стадии острого описторхоза
Когда же речь идет об описторхозе острой формы, то ее разделяют на 4 класса.
-
Тифоподобное протекание – присутствуют симптомы панкреатита, желтухи и гепатита, увеличенная печень, есть гастрит, эозинофилы в крови до 90%.

-
Гепатохолангетический тип – панкреатит, ноющие боли в животе, поражается печень, нарушается функция поджелудочной железы.
-
Гастроэнтерологический – наличие энтероколита, язвы желудка, эрозивного гастрита, наблюдаются нарушения стула.
-
Поражение дыхательных путей – присутствие бронхита астматического типа, плеврита и пневмонии.
Как проводится диагностика заболевания?
Первое, что нужно сделать, если обнаружили у себя признаки описторхоза, — это не заниматься самолечением, а обратиться за консультацией гастроэнтеролога. Врач проведет визуальный осмотр, соберет анамнез и направит на анализы и дуоденальное зондирование. Это метод обследования пациента, который проводится при заболеваниях желчевыводящих путей и желчного пузыря для забора желчи на лабораторное исследование.
Другие виды диагностики:
-
общий анализ крови;
-
исследование внутренних органов с помощью УЗИ;
-
анализ кала на яйца глистов;
-
полимеразная цепная реакция (ПЦР).
После проведения диагностики, врач изучает результаты всех анализов и исследований, ставит пациенту точный диагноз. После постановки точного диагноза пациенту назначается лечение. Оно проходит под строгим наблюдением.
Лечение описторхоза
Лечение патологии должно проводиться независимо от стадии и вида описторхоза. Чем быстрее начато лечение, тем меньше вероятность того, что паразит нанесет сильные увечья вашему организму.
Для того, чтобы начать лечение, необходимо иметь свежие результаты общего анализа крови и мочи, биохимический анализ крови, ФГДС, УЗИ органов брюшной полости, для пациентов старше 40 лет также ЭКГ.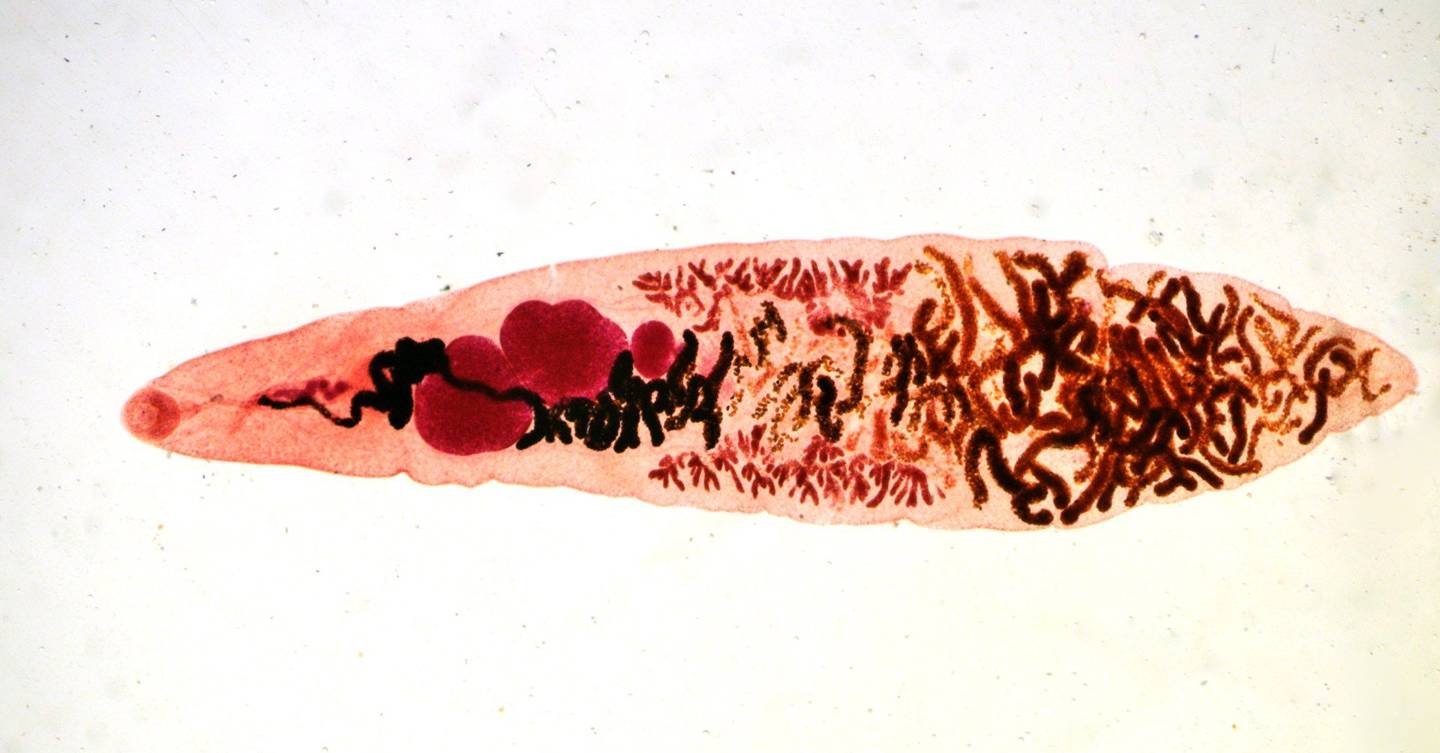
Использование медикаментозных препаратов снимает воспаление. Если есть аллергические реакции, интоксикация, то эту проблему устраняют за счет использования антигистаминных средств. Назначаются желчегонные препараты, которые принимаются в назначенные врачом сроки, прописывают антибиотики. Препараты чаще всего принимаются сроком до 14 дней. Для больного устанавливается специальная диета, которую он обязан соблюдать.
После курса лечения будет сделано контрольное дуоденальное зондирование, вы получите полное медицинское заключение и рекомендации врача, которых нужно придерживаться в течение всей жизни.
После проведения противопаразитарной терапии наступает период реабилитации. Он может длиться на протяжении 3-4 месяцев, основными его задачами являются:
-
восстановление нормальной работы органов пищеварительной системы;
-
полное избавление от мертвых гельминтов, которые остались в организме;
-
устранение последствий жизнедеятельности гельминтов в человеческом организме.
Лечение описторхоза в Красноярске
Диагностику и лечение паразитов можно пройти в частной медицинской клинике «Медюнион». В период пандемии мы оказываем все медицинские услуги согласно масочному режиму. Соблюдается дистанция между пациентами и работниками клиники, все рабочие поверхности обрабатываются каждый час. Наши пациенты могут воспользоваться масками и дезинфекторами для обработки рук.
Стоимость диагностики и лечения будет зависеть о проводимых процедур. Чтобы узнать больше информации, запишитесь на прием к гастроэнтерологу, который проведет осмотр, назначит анализы и лечение. Чтобы записаться, позвоните по телефону +7 391 202-95-54 или заполните онлайн-форму. Укажите необходимую вам процедуру и оставьте свои данные – наш специалист перезвонит вам и обсудит удобное время процедуры.
Кроме того, в клинике действует комплексная программа диагностики «Золотой стандарт». Она включает в себя все виды анализов, в том числе и на паразитов.
Ученые нашли точный способ выявления паразитов-сосальщиков | Статьи
Ученые разработали метод точной диагностики описторхоза — это заболевание, вызываемое плоскими червями класса сосальщиков. Паразит вредит организму интоксикацией, повреждает желчный пузырь и печень, закупоривает протоки, вызывая острые и хронические заболевания, которые чреваты серьезными осложнениями вплоть до гепатита и рака. Проблема масштабна: в северных регионах России, где развита культура сыроедения рыбы, распространенность этого заболевания достигает 40–50% населения. Уникальные наборы реагентов для точной диагностики описторхоза, разработанные в Сибирском государственном медицинском университете, на днях зарегистрированы Росздравнадзором.
Описторхоз — заболевание, вызываемое плоскими червями класса сосальщиков (описторхис). Паразиты длиной 8–18 мм, попадая в воду с фекалиями больного, начинают развиваться в пресноводных моллюсках, затем переходят ко второму промежуточному хозяину — рыбе семейства карповых. В рыбе описторхис обитает в подкожной клетчатке и мышцах, где проходит вторую стадию развития, становясь личинкой. Через 6 недель личинка уже способна заразить человека или животное. Через желудок и кишечник она попадает в желчный пузырь и желчные ходы печени и может жить и размножаться до двадцати лет. Паразит вредит организму интоксикацией, повреждает желчный пузырь и печень, закупоривает протоки, вызывая острые и хронические заболевания, которые чреваты серьезными осложнениями вплоть до гепатита и рака. Чем раньше начать лечение, тем быстрее можно убить сосальщика.
Наборы для точной диагностики описторхоза, разработанные в Сибирском государственном медицинском университете (СибГМУ), зарегистрированы Федеральной службой по надзору в сфере здравоохранения (Росздравнадзор). Новая диагностическая тест-система сможет применяться в медучреждениях по всей стране. Это позволит повысить точность исследований при выявлении этого опасного заболевания, следовательно, обеспечить своевременное лечение и ограничить распространение болезни.
Новая диагностическая тест-система сможет применяться в медучреждениях по всей стране. Это позволит повысить точность исследований при выявлении этого опасного заболевания, следовательно, обеспечить своевременное лечение и ограничить распространение болезни.
— Сибирь является мировым очагом описторхоза, — рассказала «Известиям» заместитель губернатора Томской области по научно-образовательному комплексу Людмила Огородова. — Opisthorchis felineus — вид описторхиса, который обитает только в пойме реки Оби и ее притоках, но, несмотря на ограниченный географический ареал распространения гельминта, его опасность для населения очень велика. Это связано с тем, что в северных регионах, где развита культура сыроедения рыбы, распространенность этого заболевания достигает 40–50% населения. Описторхоз может быть причиной развития рака печени, эти исследования мы проводим совместно с Окружным онкологическим центром Ханты-Мансийска.
Как сообщила «Известиям» ректор СибГМУ Ольга Кобякова, тест-система представляет собой набор реагентов для качественного суммарного выделения ДНК возбудителей описторхоза методом полимеразной цепной реакции (ПЦР) в режиме реального времени.
— Полимеразная цепная реакция — это молекулярно-генетический метод, который позволяет обнаружить ДНК описторхиса. Для диагностики пациенту необходимо сдать копрограмму, затем врач-лаборант работает с этим материалом для выделения ДНК. Визуально тест-система выглядит как коробочка с набором реагентов, — отметила Ольга Кобякова.
Необходимость в такой тест-системе есть не только в Томской области. Партнеры Томского консорциума по описторхозу из Таиланда, Швейцарии и Нидерландов уже выразили заинтересованность в ней.
Доктор медицинских наук, профессор РАН, директор Института медицинской паразитологии, тропических и трансмиссивных заболеваний им. Е.И. Марциновского Сеченовского университета, вуза — участника проекта 5-100, Александр Лукашев рассказал «Известиям», что проблема диагностики паразитарных заболеваний в настоящее время стоит очень остро.
— Часто это связано с биологией паразитов, которые за миллионы лет научились «прятаться» от иммунной системы хозяина, а заодно и от средств диагностики. Кроме того, многие паразитарные заболевания актуальны только для определенной местности и не очень интересны ведущим мировым компаниям, разрабатывающим средства диагностики. Эти проблемы характерны и для описторхоза. Уверен, что новый метод диагностики актуален не только для Сибири, но и для других регионов Российской Федерации, — отметил эксперт.
В структуре биогельминтозов на территории России на долю описторхоза приходится 74,4% заболеваемости. Наиболее неблагополучными являются Ханты-Мансийский и Ямало-Ненецкий автономные округа, Тюменская, Томская, Омская, Новосибирская области, Республика Алтай. В 2010 году было зарегистрировано 33 657 случаев заболевания описторхозом среди взрослых и 4571 — среди детей до 17 лет.
ЧИТАЙТЕ ТАКЖЕ
Профилактика описторхоза — Сургутская клиническая травматологическая больница
Профилактика описторхозаЗаражение человека и млекопитающих животных происходит при употреблении в пищу сырой, недостаточно термически обработанной и слабо просоленной рыбы с метацеркариями гельминта.
Поэтому в профилактике описторхоза большую роль играют навыки в кулинарной обработке рыбы. При недостаточной обработке личинки двуустки, находящиеся в рыбе, могут оставаться жизнеспособными. Поэтому заражение может произойти не только при случайном заглатывании мелких кусочков сырой рыбы, прилипшей к рукам, посуде и предметам домашнего обихода во время приготовления рыбных блюд, но и при употреблении в пищу недостаточно проваренной или прожаренной, слабо посоленной или слабо замороженной рыбы.
Возможность заражения описторхозом через хорошо проваренную рыбу и рыбу горячего копчения обычно исключается.
Безопасной также считается солёная рыба, если технологический процесс посола доведён до конца. При засолке мелкой (10-15 г) рыбы, когда она густо засыпается солью, личинки двуустки полностью погибают через 3-4 сутки, тогда как при засолке крупной (до 1 кг) — через 10 суток.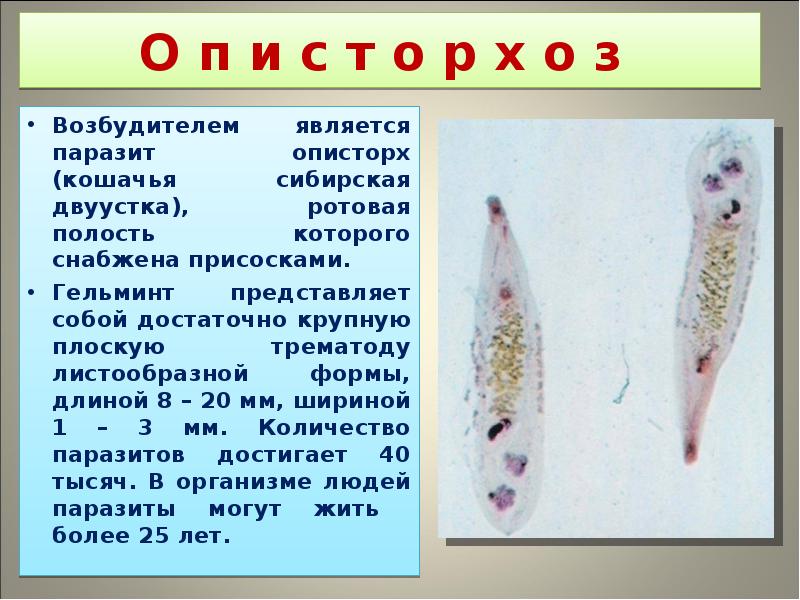
Холодное копчение не даёт гарантии полного обезвреживания, но гибель большинства метацеркариев наступает в процессе предварительного соления рыбы.
К замораживанию метацеркарии сравнительно стойки. При температуре -2°С гибель личинки в мелкой рыбе наступает лишь через 4-5 суток, а в крупной — через 2-3 недели. При температуре -23-25°С личинки гибнут через 72 часа, при температуре -30° С — через 6 часов.
При замораживании рыбы до — 40°С личинки погибают через 3 часа.
Немаловажную роль в заражении описторхозом играет употребление в пищу свежеприготовленной «строганины» (мороженой рыбы, нарезанной тонкими ломтиками), поскольку замораживание её при этом не бывает очень глубоким.
Речная рыба — вкусный и ценный продукт, к тому же для многих самый доступный. Однако отсутствие вакцинопрофилактики и лекарств, предупреждающих заражение, делает особенно важным знание правил кулинарной обработки рыбы из семейства карповых. Тем более что невооруженным глазом заметить личинку паразита в ней невозможно.
Вот основные правила обработки рыбы:
- Варить рыбу нужно 15-20 минут с момента закипания.
- Жарить рыбу необходимо 15-20 минут, порезав ее небольшими кусочками и распластав в достаточном количестве жира, лучше под крышкой.
- Рыбный пирог запекайте не менее часа в духовке.
- Для соления рыбы используйте 2 кг соли на 10 кг рыбы, посол проводите в течение двух и более недель.
- Вяление: 1-й способ — засолите рыбу выше указанным способом на две недели, а затем повесьте ее сушиться, 2-й способ — засолите рыбу на три дня и сушите ее три недели.
- Замораживание: 1-й способ — держите рыбу в морозильнике или на морозе при температуре — 28 градусов в течение 41 часа.
2-й способ — при температуре -35 градусов замораживайте рыбу 10 часов. - Нельзя употреблять малосоленую рыбу и строганину.
- Не забывайте, что при разделке рыбы и резке продуктов, употребляемых без обработки (овощи, хлеб и т.
 д.), следует использовать разные разделочные доски.
д.), следует использовать разные разделочные доски.
Описторхоз — БУ «Нижневартовская городская поликлиника»
Эпидемиология описторхоза
Источником инвазии являются зараженные описторхисами млекопитающие (домашние и дикие плотоядные, человек). Дикие плотоядные являются основным источником инвазии на большей части ареала, где человек не включен в циркуляцию возбудителя.
Основные факторы передачи: необеззараженная рыба только семейства карповых (вяленая, соленая, холодного копчения, строганина, сырая), содержащая жизнеспособных метацеркарий описторхиса. Заражение человека происходит при употреблении необеззараженной рыбы семейства карповых, содержащей жизнеспособных личинок описторхиса.
Естественная восприимчивость людей к заражению описторхисами высокая. Наибольшие показатели заболеваемости регистрируются в возрастной группе от 15 до 50 лет. Несколько чаще болеют мужчины. Заражение, как правило, происходит в летне-осенние месяцы. Часто наблюдаются повторные случаи заражения после излечения. Иммунитет нестойкий.
Описторхоз — пероральный биогельминтоз. Ареал возбудителя простирается от бассейна р. Енисей до западных границ Европы, но распространение заболевания у человека носит очаговый характер. Уровень пораженности населения описторхисами определяют социально-бытовые факторы: образ жизни (традиции, привычки), степень развития рыбного промысла, удельный вес рыбы в пищевом рационе, методы кулинарной обработки рыбы, санитарное состояние местности.
В связи с тем, что промежуточный и второй промежуточный хозяева обитают в водоемах, очаги описторхоза концентрируются вблизи рек. Крупнейший в мире очаг этого заболевания сформировался в Обь-Иртышском речном бассейне. Инвазированность сельского населения в нижнем течении р. Иртыш и среднем течении р. Обь достигает 90 — 95%, причем нередко инвазированны и дети дошкольного возраста.
Здесь регистрируются наиболее высокие показатели заболеваемости населения (до 1000 на 100 тыс.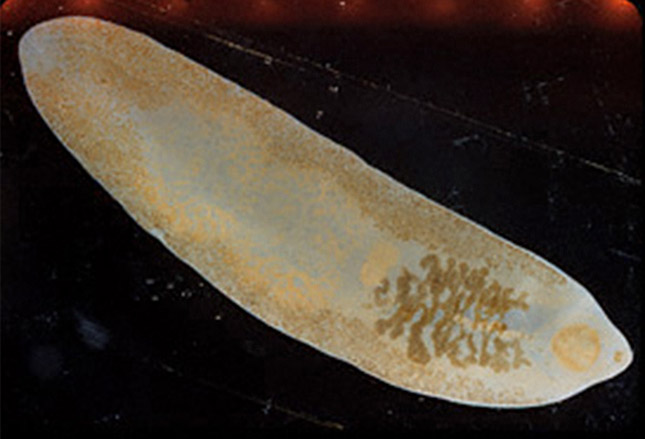 ). Причина такого исключительного значения данной территории в эпидемиологии описторхоза заключается в наличии чрезвычайно развитой речной поймы, обеспечивающей условия для циркуляции возбудителя болезни. Территории с приведенными выше количественными показателями пораженности населения относятся к гиперэндемичным.
). Причина такого исключительного значения данной территории в эпидемиологии описторхоза заключается в наличии чрезвычайно развитой речной поймы, обеспечивающей условия для циркуляции возбудителя болезни. Территории с приведенными выше количественными показателями пораженности населения относятся к гиперэндемичным.
Развитие Opisthorchis felineus происходит с тройной сменой хозяев: первого промежуточного (моллюски), второго промежуточного (рыбы) и окончательного (млекопитающие).
К числу окончательных хозяев паразита относятся человек, кошка, собака, свинья и более 25 видов диких млекопитающих, в рацион которых входит рыба (лисица, песец, соболь, хорек, выдра, норка, водяная полевка, ондатра и др.).
Из кишечника окончательных хозяев зрелые яйца описторхисов выделяются в окружающую среду. Яйца паразитов, попавшие в водоем, могут сохранять жизнеспособность 5 — 6 месяцев. В воде яйцо заглатывается моллюском рода Codiella или Opisthorchophorus. В кишечнике моллюска из яйца выходит мирацидий, проникает в полость тела и, претерпевая метаморфоз, превращается в половозрелую фазу развития — материнскую спороцисту. Размножаясь партеногенетическим путем (без оплодотворения), спороциста дает начало особям следующего, тоже партеногенетического поколения — редиям. В редиях 2-го поколения развиваются подвижные церкарии — личинки гермафродитного поколения. Время развития паразитов в моллюске в зависимости от температуры воды может составлять от 2 до 10 — 12 месяцев. Церкарии, покинув тело родительской особи, выходят из моллюска в воду и при помощи секрета особых желез прикрепляются к коже рыб семейства карповых (язь, елец, линь, плотва, лещ и др.). Затем они активно внедряются в подкожную клетчатку и мускулатуру, теряют хвост и спустя сутки инцистируются, превращаясь в метацеркарии, размеры которых составляют 0,21 — 0,33 x 0,17 — 0,25 мм. Через 6 недель метацеркарии становятся инвазионными, и содержащая их рыба может служить источником заражения окончательных хозяев.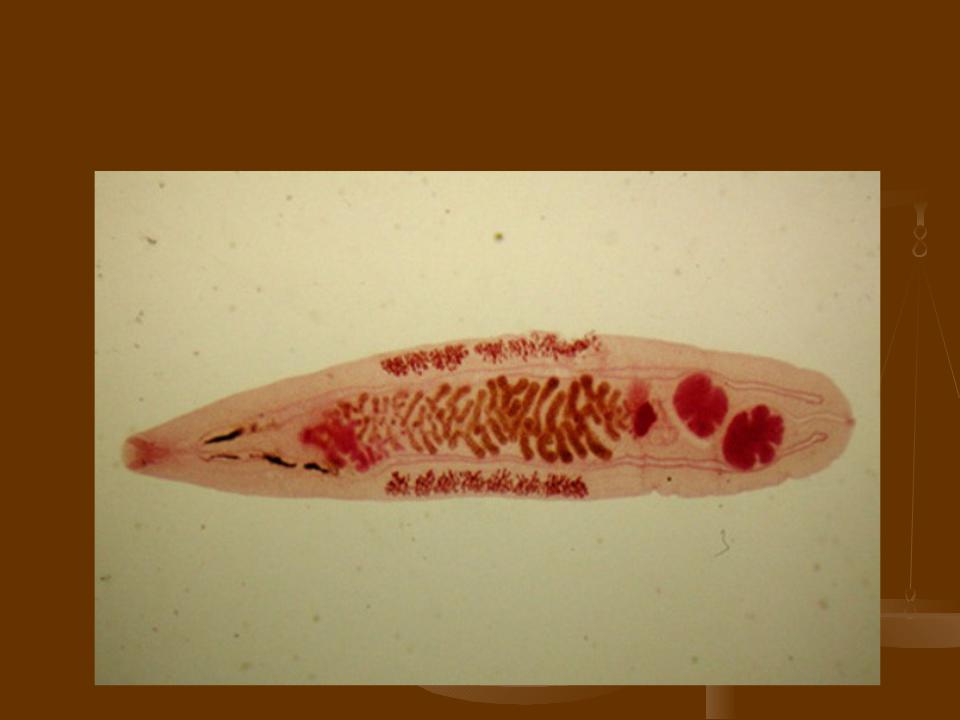 Метацеркарии в живой рыбе сохраняют свою жизнеспособность и инвазионность 5 — 8 лет. Весьма устойчивы они к воздействию низких температур. В замороженной рыбе личинки утрачивают жизнеспособность при -40 °C до 7 ч, при -35 °C до 14 ч, при -28 °C — 32 ч. Замораживание рыбы при более высокой температуре не гарантирует ее полного обеззараживания. Метацеркарии чувствительны к высоким температурам. После выделения из рыбы они погибают при 55 °C в течение 5 мин. При засолке, если доля соли в рыбе равна 14%, а плотность тузлука составляет 1,2, метацеркарии выживают в мелкой рыбе от 10 до 21 суток (в зависимости от вида рыбы), а в крупной, длиной свыше 25 см (язи, лещи, лини), — до 40 суток.
Метацеркарии в живой рыбе сохраняют свою жизнеспособность и инвазионность 5 — 8 лет. Весьма устойчивы они к воздействию низких температур. В замороженной рыбе личинки утрачивают жизнеспособность при -40 °C до 7 ч, при -35 °C до 14 ч, при -28 °C — 32 ч. Замораживание рыбы при более высокой температуре не гарантирует ее полного обеззараживания. Метацеркарии чувствительны к высоким температурам. После выделения из рыбы они погибают при 55 °C в течение 5 мин. При засолке, если доля соли в рыбе равна 14%, а плотность тузлука составляет 1,2, метацеркарии выживают в мелкой рыбе от 10 до 21 суток (в зависимости от вида рыбы), а в крупной, длиной свыше 25 см (язи, лещи, лини), — до 40 суток.
Высокая устойчивость метацеркарий к воздействию факторов окружающей среды требует соблюдения режимов обеззараживания материала и объектов внешней среды (поверхностей, лабораторной посуды и пр.) в испытательных лабораториях, проводящих исследование рыбы и готовой рыбной продукции на паразитарную чистоту.
В кишечнике дефинитивного хозяина под воздействием дуоденального сока личинки освобождаются от оболочек цист и по общему желчному протоку мигрируют в желчный пузырь и в желчные протоки печени. Иногда они могут попадать также в поджелудочную железу. Через 3 — 4 недели после заражения окончательных хозяев паразиты достигают половой зрелости и после оплодотворения начинают откладывать яйца. Выделяющиеся с фекалиями животных и человека зрелые яйца содержат личинку-мирацидий, не способную заразить дефинитивного хозяина без прохождения ее дальнейшего развития в промежуточном и дополнительном хозяине. Таким образом, выделения больного, а также загрязненные ими объекты внешней среды непосредственной эпидемической опасности для окружающих не представляют. Продолжительность жизни кошачьей двуустки может достигать 20 — 25 лет.
Санитарно-гигиенические мероприятия
Оценку состояния рыбохозяйственных водоемов по паразитологическим показателям проводят на территориях, где существует риск заражения описторхисами, 1 раз в 5 лет или по эпидемиологическим показаниям.
Места отлова, сроки и видовой состав рыб определяют управления Роспотребнадзора по субъектам Российской Федерации по плану-графику, согласованному с руководством рыбодобывающих организаций.
При оценке паразитологического состояния водоема в первую очередь исследуют виды рыб, наиболее подверженные заражению. Наилучшими индикаторами неблагополучия водоема в отношении инвазии личинками описторхиса являются язь, далее по убывающей — елец, линь, красноперка, плотва, лещ, голавль, синец, белоглазка, подуст, чехонь, жерех, пескарь, уклейка, густера, гольян, верховка, щиповка.
В аккредитованных испытательных лабораториях исследуют по 20 особей промыслового размера дополнительных хозяев описторхиса (рыб семейства карповые), распространенных на этой территории. При отрицательном результате число исследуемых экземпляров рыб доводится до 40. Если отрицательный результат подтверждается, водоем считается благополучным. Рыба, выловленная в таких водоемах, допускается на реализацию без ограничений.
При обнаружении в водоеме рыб, зараженных личинками описторхиса, всю рыбу данного вида и остальных видов, способных играть роль дополнительных хозяев описторхисов, а также рыбную продукцию подвергают обеззараживанию от личинок описторхисов перед реализацией.
Вся рыбопродукция из водоема допускается к сертификации и реализации только после ее обеззараживания.
При паразитологическом контроле сырья (свежей, охлажденной и мороженой рыбы) проводят микроскопическое исследование мышечных тканей и подкожной клетчатки рыбы на наличие метацеркарий описторхиса. Не допускается в реализацию и подлежит обеззараживанию сырье, в пробе которого обнаружена хотя бы одна жизнеспособная личинка описторхиса.
Проводят обязательный паразитологический контроль каждой партии готовой рыбной продукции холодного копчения, пресервов, соленой, пряной, маринованной (бочковой), вяленой рыбы. Готовая продукция не должна содержать жизнеспособных личинок описторхиса.
Рыбу язь для приготовления вяленой продукции холодного копчения допускают после замораживания.
Санитарно-паразитологический контроль рыбы и рыбной продукции на рынках обеспечивает руководитель рынка. Рыба, содержащая жизнеспособные личинки описторхиса, подлежит обеззараживанию.
Учитывая высокую устойчивость метацеркарий описторхисов к низким температурам, замораживание рыбы при более высокой температуре не гарантирует ее обеззараживания.
Обеззараживание рыбы от личинок описторхиса обеспечивается применением смешанного крепкого и среднего посола (плотность тузлука с первого дня посола 1,20 при температуре 1 — 2 °C) при достижении массовой доли соли в мясе рыбы 14%. При этом продолжительность посола должна быть:
а) пескаря, уклейки, гольяна, верховки — 10 суток;
б) плотвы, ельца, красноперки, голавля, синца, белоглазки, подуста, чехони, жереха, щиповки, мелких (до 25 см) язей, лещей, линей — 21 сутки;
в) крупных (свыше 25 см) язей, лещей, линей — 40 суток.
Допускается более слабый или менее длительный посол «условно годной» рыбы только после предварительного ее замораживания в режимах, указанных выше.
При невозможности обеспечить режимы замораживания, гарантирующие обеззараживание рыбной продукции, ее следует использовать для пищевых целей только после горячей термической обработки или стерилизации (консервы) в соответствии с действующими технологическими инструкциями.
Заморозка: в бытовом холодильнике личинки сохраняют жизнеспособность. При температуре -40 0— 7 часов, при — 35 0 — 14 часов, при -280 -32 часа.
При засолке рыбы необходимо применять 2кг соли на 10 кг рыбы. При этом продолжительность соления мелкой рыбы (до 25 см) — 14 суток; крупных (свыше 25 см) — 40 суток.
Вяление необходимо проводить с предварительным посолом в течение 2 недель из расчета 2 кг соли на 10 кг рыбы.
Варить рыбу следует порционными кусками не менее 20 минут с момента закипания, рыбные пельмени — не менее 20 минут с момента закипания.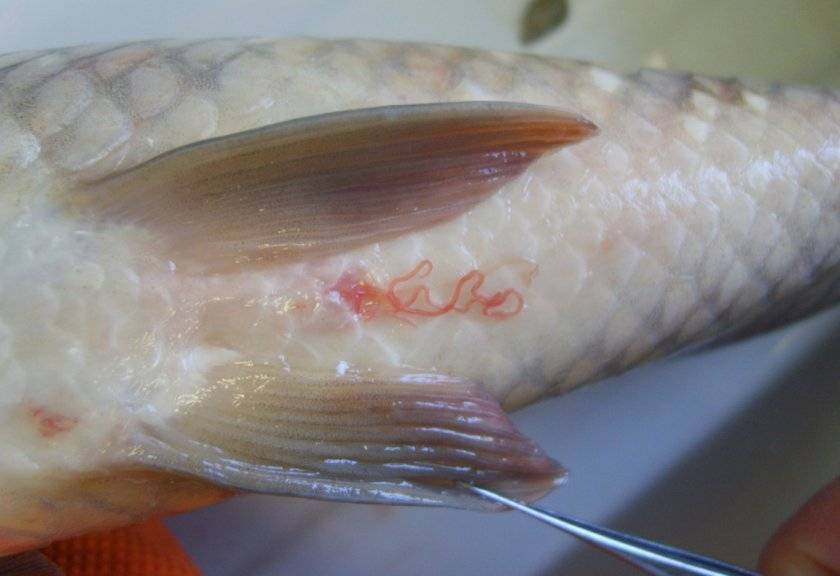 Рыбу (рыбные котлеты) необходимо жарить порционными кусками в жире 20 минут. Крупные куски рыбы весом до 100 г следует жарить в распластанном виде не менее 20 минут. Мелкую рыбу можно жарить целиком в течение 15—20 минут. Рыбные пироги необходимо выпекать 60 минут.
Рыбу (рыбные котлеты) необходимо жарить порционными кусками в жире 20 минут. Крупные куски рыбы весом до 100 г следует жарить в распластанном виде не менее 20 минут. Мелкую рыбу можно жарить целиком в течение 15—20 минут. Рыбные пироги необходимо выпекать 60 минут.
При холодном копчении рекомендуется предварительный посол в течение 2 недель (из расчета 2 кг соли на 10 кг рыбы).
Лечебно-профилактические мероприятия
Выявление инвазированных осуществляют лечебно-профилактические организации независимо от организационно-правовых форм и форм собственности, а также лица, занимающиеся частной медицинской практикой, при обращении и оказании медицинской помощи, а также при профилактических, плановых, предварительных при поступлении на работу и периодических обследованиях и осмотрах в установленном порядке.
Контрольные обследования.
Выявленные инвазированные берутся на учет в кабинетах инфекционных заболеваний или участковыми терапевтами (педиатрами) с заполнением контрольной карты диспансерного наблюдения. Контроль эффективности лечения проводят через 3 месяца после дегельминтизации. Критерии эффективности лечения — три отрицательных результата копроовоскопических исследований или однократного отрицательного результата дуоденального содержимого.
Моллюск — первый промежуточный хозяин Opisthorchis
Описторхоз, вызываемый трематодой Opisthorchis viverrini (англ.)русск., распространён в Юго-Восточной Азии на территории таких стран, как Таиланд, Лаос, Вьетнам и Камбоджа. Редкие случаи заболевания, связываемые с завозом заражённой рыбы, регистрируются в Европе и Северной Америке[6].
В структуре биогельминтозов на территории Российской Федерации на долю описторхоза приходится 74,4 % заболеваемости. Наиболее неблагополучными являются ХМАО-Югра и ЯНАО.
Возбудитель и заражение
Жизненный цикл трематод родаOpisthorchis
Возбудителями описторхоза являются печёночные сосальщики, в том числе Opisthorchis felineus (кошачья или сибирская двуустка), мелкий паразит ланцетовидной формы длиной 8—18 мм и шириной 1,2—2 мм.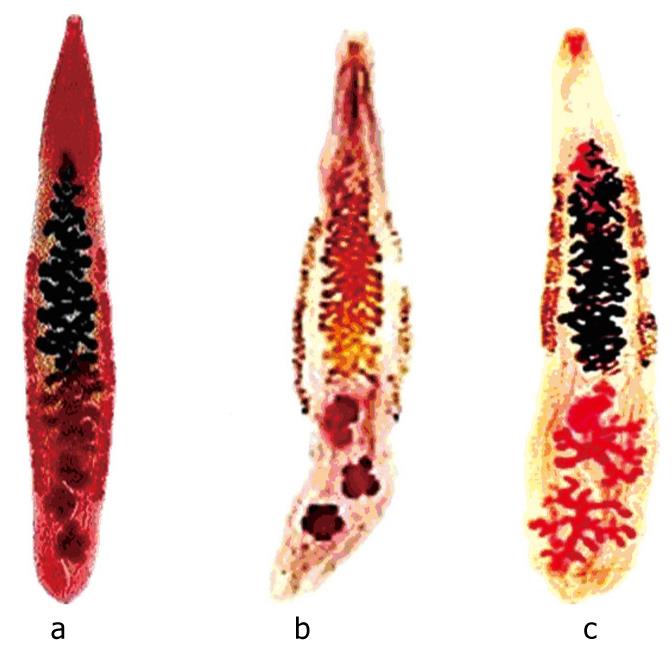 Развитие паразита происходит с участием двух промежуточных хозяев: моллюсков и карповых рыб. Конечными хозяевами являются человек и другие плотоядные животные.
Развитие паразита происходит с участием двух промежуточных хозяев: моллюсков и карповых рыб. Конечными хозяевами являются человек и другие плотоядные животные.
Первые промежуточные хозяева — пресноводные моллюски битинииды рода Codiella, обитающие в пересыхающих мелководных пойменных водоёмах. Их заражение происходит путём заглатывания яйца описторха, попадающих в водоем с фекалиями конечных хозяев, вместе с илом со дна водоёма. В теле моллюска паразит претерпевает метаморфоз. Эта стадия развития паразита длится в течение 2 месяцев. Образовавшиеся в результате церкарии покидают моллюска и активно внедряются в тело карповых рыб.
В теле рыбы паразит располагается в мышцах и подкожной клетчатке. Здесь он переходит к следующей стадии развития и превращается в метацеркарий, который лежит в округлой цисте серого цвета размером 0,17—0,21 мм. Личинка внутри очень подвижная. У освобождённого метацеркария (длина 0,44—1,36 мм, ширина 0,15—0,30 мм) хорошо видны две присоски и экскреторный пузырёк, заполненный чёрными гранулами. Через 6 недель после заражения рыбы паразит становится инвазионным, то есть способным заражать конечного хозяина. Из всех жизненных стадий описторхиса только метацеркарий способен приживаться и размножаться в организме человека и других хищных млекопитающих. Потенциальными носителями личинок описторхиса являются язь, елец, плотва, краснопёрка, лещ, голавль, синец, белоглазка,чехонь, жерех, линь, пескарь, уклея, гольян, верховка, шиповка. В бассейне Оби наибольшая заражённость отмечается у язя, чуть меньшая — у ельца и плотвы.
Конечные хозяева паразитов (человек, кошки, собаки, лисицы, песцы, хорьки и другие плотоядные животные) заражаются после поедания инвазированной рыбы. В желудке и начальном отделе тонкого кишечника конечного хозяина метацеркарии освобождаются от цист, после чего проникают через жёлчные протоки в жёлчный пузырь и жёлчные ходы печени. Здесь они через 10—12 дней достигают половой зрелости и начинают откладывать яйца. Яйца паразита, попавшие на почву, погибают в течение 8—10 дней, при попадании же в воду сохраняют жизнеспособность до года. В теле конечного хозяина паразит может обитать в течение 10—20 лет.
Яйца паразита, попавшие на почву, погибают в течение 8—10 дней, при попадании же в воду сохраняют жизнеспособность до года. В теле конечного хозяина паразит может обитать в течение 10—20 лет.
Личинка описторхиса
Клиника
Инкубационный период заболевания составляет от 2 до 4 недель. В клиническом течении различают две фазы: острую и хроническую.
Острая фаза чётко выявляется у впервые заболевших людей, недавно попавших в зону распространения описторхоза. При лёгком течении характерны такие признаки, как внезапное начало, температура до 38°С в течение 1—2 недель, жалобы на небольшую слабость и повышенную утомляемость. Среднетяжёлому течению присущи повышение температуры до 39°С и выше в течение 2—3 недель, высыпания на коже, боль в мышцах и суставах, у некоторых заболевших возникают рвота, диарея. При тяжёлом течении помимо высокой температуры тела, высыпаний, головной боли, заторможенности или возбуждения, бессонницы, отчетливо проявляются признаки, характерные для поражения внутренних органов. При поражении печени — желтуха различной интенсивности, боли в области печени, возможно увеличение лимфатических узлов. При поражении пищеварительного тракта — упорная приступообразная боль в правом подреберье, тошнота, рвота, вздутие живота, расстройства стула. У некоторых больных возможно возникновение кашля, болей в грудной клетке при дыхании.
Хронический описторхоз характерен для жителей эндемических районов и отличается большим разнообразием проявлений. Может протекать годами без выраженной острой стадии, возможно проявление клинических симптомов через 10—20 лет после заражения. Больные жалуются на чувство тяжести, распирания в надчревной области, снижение аппетита, рвоту, боль в правом подреберье. Постепенно формируется хронический гепатит. Хронический описторхоз может сопровождаться развитием цирроза печени и гепатоцеллюлярной карциномы.
Если паразиты локализуются в поджелудочной железе, то возникают боли опоясывающего характера с отдачей в левую половину грудной клетки, спину, левое плечо. Поражения нервной системы проявляются головной болью, головокружением, нарушением сна, эмоциональной неустойчивостью, депрессией, раздражительностью, частой сменой настроения и др. При хроническом описторхозе нередко возникают признаки поражения сердца: больные жалуются на боль или неприятные ощущения в области сердца, сердцебиение.
Поражения нервной системы проявляются головной болью, головокружением, нарушением сна, эмоциональной неустойчивостью, депрессией, раздражительностью, частой сменой настроения и др. При хроническом описторхозе нередко возникают признаки поражения сердца: больные жалуются на боль или неприятные ощущения в области сердца, сердцебиение.
При хроническом описторхозе часто выявляются нарушения желудочной секреции, признаки хронического гастрита, дуоденита,гастродуоденита, язвы желудка или двенадцатиперстной кишки. Симптоматика часто бывает не ярко выраженной. У отдельных больных хронический описторхоз может проявляться только симптомами холецистита, холангита, у других — преимущественно признаками недостаточности пищеварительных ферментов, у третьих — общетоксическими и аллергическими реакциями. Возможно также бессимптомное течение.
Лечение
Терапия описторхоза, как правило, является комплексной и включает наряду с применением специфических противогельминтных препаратов также более общие меры, направленные на восстановление нарушенной функции желудочно-кишечного тракта.
Лечение проводится препаратами только по указанию врача.
Большинство пациентов могут проходить лечение амбулаторно. Стационарное лечение рекомендуется больным с декомпенсацией функций органов, больным в острой стадии описторхоза. При острой стадии заболевания этиотропную терапию проводят после купирования приступов лихорадки, устранения интоксикации и аллергических проявлений. Для пациентов с хронической стадией рекомендуется проведение комплексной терапии, направленной на купирование острых состояний и достижение достаточной ремиссии сопутствующих заболеваний, после чего проводится специфическое лечение
Прогноз обычно благоприятный. Случаи летального исхода из-за развития печёночной недостаточности регистрируются крайне редко. Прогноз серьёзен при развитии гнойных процессов в жёлчевыделительной системе, жёлчных перитонитах и остром панкреатите.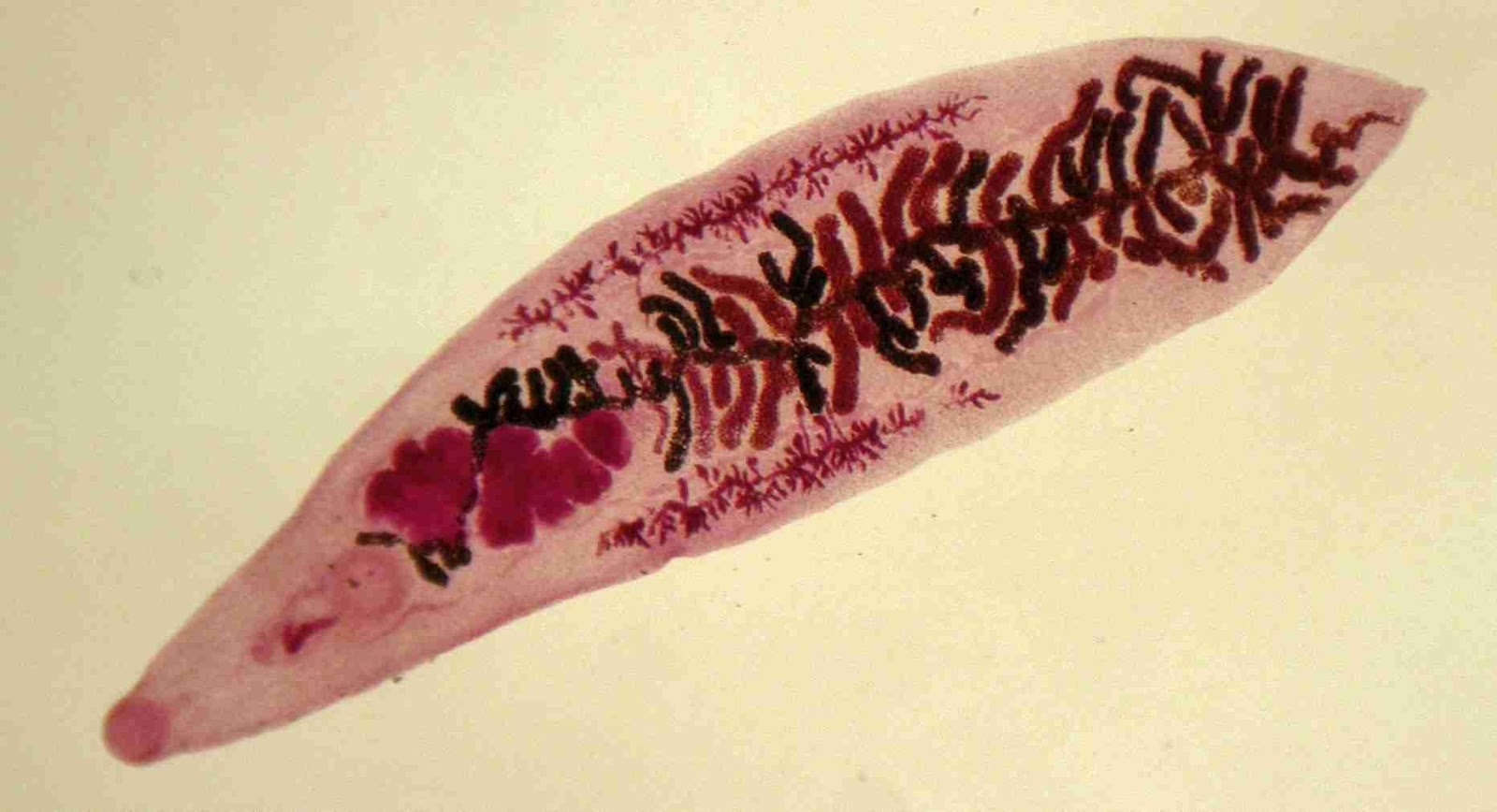
Переболевшие нуждаются в диспансерном наблюдении не менее 6 месяцев
Профилактика
В целях личной профилактики следует употреблять в пищу, только хорошо проваренную и прожаренную, тщательно просоленную рыбу. Избегать сырой, слабо проваренной или прожаренной, малосольной рыбы, строганины. Следует следить за тем, чтобы в водоёмы не попадали фекалии.
Для предотвращения дальнейшего распространения паразита не следует сбрасывать в водоёмы и на мусорные свалки отходы переработки рыбной продукции, а также скармливать животным без предварительного обеззараживания.
Подготовила:
Врач-эпидемиолог БУ «Нижневартовская городская поликлиника»
И.А. Егорова.
СанПиН 3.2.3215-14 «Профилактика паразитарных болезней на территории Российской Федерации
Количество просмотров: 4464
Трематодозы пищевого происхождения
Передача паразитов и бремя инвазий
Трематодозы пищевого происхождения являются зоонозами, и их возбудители могут передаваться человеку только после завершения сложного жизненного цикла, некоторые стадии которого протекают в организме промежуточного животного хозяина.
Первыми промежуточными хозяевами всех видов трематод являются пресноводные улитки. Второй хозяин бывает разным в зависимости от вида: в случае клонорхоза и описторхоза это пресноводные рыбы, а в случае парагонимоза — ракообразные. Заражение возбудителем парагонимоза может также происходить в результате употребления в пищу животных, питающихся ракообразными, например сырого мяса дикого кабана. В случае фасциолеза второй промежуточный хозяин не требуется, и заражение человека может происходить при употреблении содержащих личинки пресноводных растений. Окончательными хозяевами паразита всегда являются млекопитающие (см. таблицу 1).
Заражение человека происходит при употреблении в пищу инвазированного паразитом второго промежуточного хозяина или, в случае фасциолеза, – водной растительности, к которой прикрепляется личинка паразита.
Клонорхоз и описторхоз в основном распространены в Азии, где многие страны являются эндемичными по данным заболеваниям. В ряде гиперэндемичных сельских населенных пунктов Лаосской Народно-Демократической Республики зарегистрирован уровень пораженности населения O. viverrini на уровне свыше 80%. Парагонимоз встречается в Африке, Азии и Латинской Америке, иногда в районах, одновременно эндемичных по туберкулезу и трематодозам, что часто приводит к неправильной диагностике и лечению болезни и способствует неполной регистрации случаев. Фасциолез распространен повсеместно и является проблемой для значительного числа стран мира, из которых наиболее высокое бремя заболевания регистрируется в Латинской Америке и на Ближнем Востоке. Хотя случаи заболевания трематодозами пищевого происхождения отмечаются в более чем 70 странах мира, данные о их фактической распространенности весьма ограничены; особенно острый дефицит эпидемиологических данных существует в странах Африки.
Внутри стран передача инвазий часто происходит в границах определенных очагов и связана с привычками населения и особенностями местных экосистем. Риск заражения может повышаться при неудовлетворительном состоянии санитарных систем и несоблюдении гигиены питания, ограниченной доступности безопасной питьевой воды и определенных культурно обусловленных пищевых предпочтениях населения. Традиции совместного принятия пищи могут способствовать возникновению кластеров заражения в семьях или среди знакомых.
Истинные показатели бремени таких инвазий неясны, поскольку поражаемые ими группы населения зачастую мало о них знают и не всегда могут обращаться за медицинской помощью. В ходе расчетов, выполненных Справочной группой ВОЗ по эпидемиологии бремени болезней пищевого происхождения (2015 г.), было определено четыре вида передаваемых с пищей трематод, которые являются значимыми причинами инвалидности и, согласно оценкам, ежегодно вызывают в общей сложности 200 000 случаев болезни и более 7 000 случаев смерти, приводя к утрате более 2 миллионов лет жизни, скорректированных по инвалидности, во всем мире.
Трематодозы пищевого происхождения также наносят значительный экономический ущерб животноводству и рыбоводству в результате снижения продуктивности животных, а также введения ограничений на экспорт продукции и сокращения потребительского спроса.
Таблица 1. Эпидемиологические характеристики трематодозов пищевого происхождения
| Болезнь | Возбудитель | Приобретается при потреблении | Естественные окончательные хозяева | ||
| Клонорхоз | Clonorchis sinensis | рыбы | Собаки и другие питающиеся рыбой хищники | ||
| Описторхоз | Opisthorchis viverrini, O. felineus | рыбы | Кошки и другие питающиеся рыбой хищники | ||
| Фасциолез | Fasciola hepatica, F. gigantica | водных растений | Овцы, крупный рогатый скот и другие травоядные | ||
| Парагонимоз | Paragonimus spp. | ракообразных (крабов и раков) | Кошки, собаки и другие хищники, потребляющие в пищу ракообразных |
Симптомы
Бремя трематодозов пищевого происхождения для общественного здравоохранения выражается скорее в заболеваемости, нежели в смертности, при этом инвазии на ранних стадиях и в легкой форме часто остаются незамеченными. Хронические инвазии, как правило, сопровождаются тяжелой симптоматикой, затрагивающей конкретный орган, в котором локализуются взрослые особи гельминтов.
Легкая инвазия Opisthorchis spp и Clonorchis sinensis может протекать бессимптомно в острой фазе, однако при высокой паразитарной нагрузке вследствие обструкции желчных протоков гельминтами могут наблюдаться такие клинические проявления, как лихорадка и боль в верхнем правом отделе живота.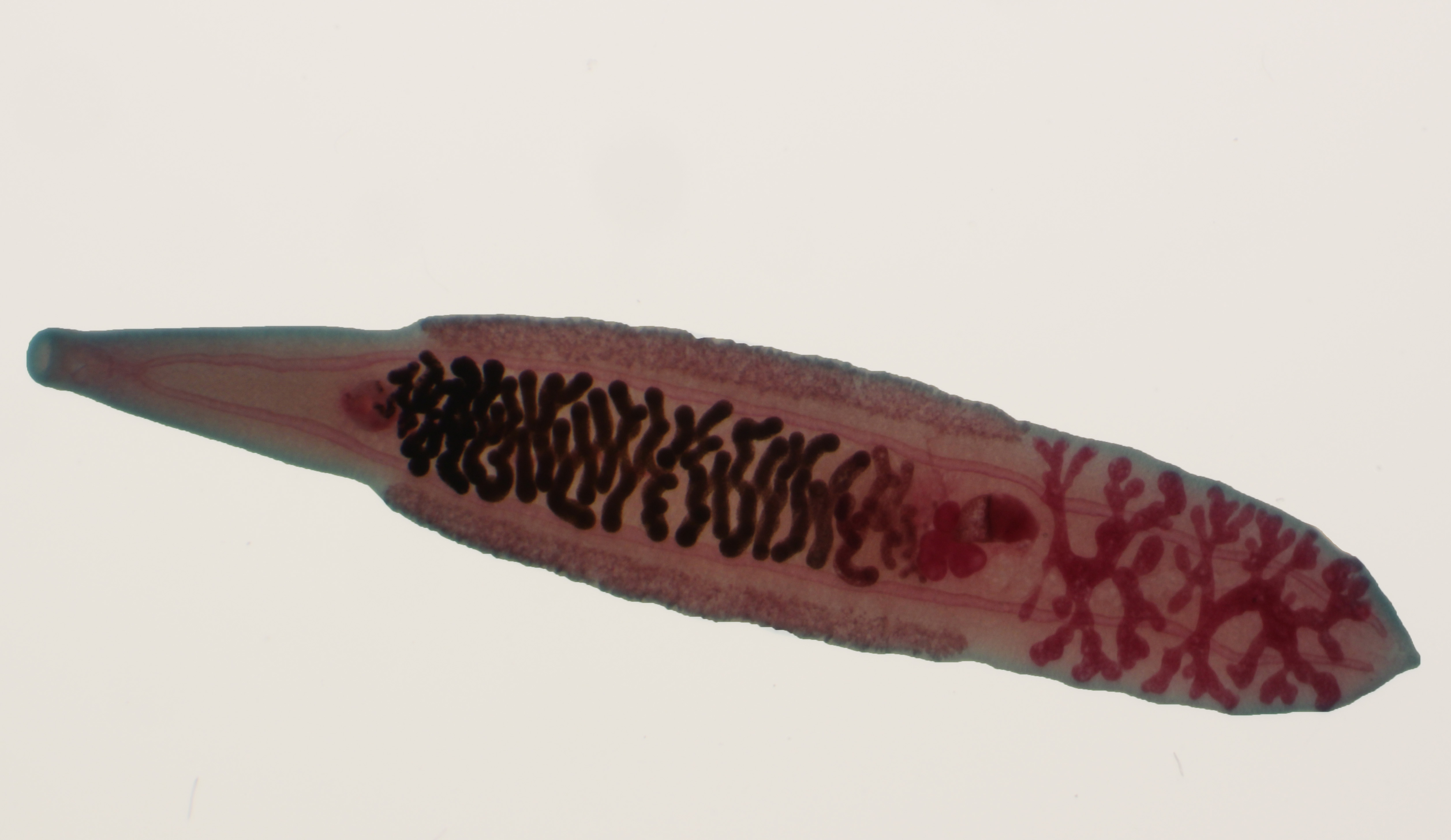 Наиболее тяжелой может быть хроническая инвазия O. viverrini и C. sinensis, вызванная растянутыми во времени эпизодами повторного заражения, когда хроническое воспаление приводит к фиброзу желчных протоков и повреждению сопредельной печеночной паренхимы. Эти патологические изменения могут привести к развитию холангиокарциномы – тяжелой и нередко смертельной форме рака желчных протоков. По этой причине как O. viverrini, так и C. sinensis признаны канцерогенами. Имеющихся данных о хронических инвазиях O. felineus недостаточно для того, чтобы данный паразит был отнесен к канцерогенам.
Наиболее тяжелой может быть хроническая инвазия O. viverrini и C. sinensis, вызванная растянутыми во времени эпизодами повторного заражения, когда хроническое воспаление приводит к фиброзу желчных протоков и повреждению сопредельной печеночной паренхимы. Эти патологические изменения могут привести к развитию холангиокарциномы – тяжелой и нередко смертельной форме рака желчных протоков. По этой причине как O. viverrini, так и C. sinensis признаны канцерогенами. Имеющихся данных о хронических инвазиях O. felineus недостаточно для того, чтобы данный паразит был отнесен к канцерогенам.
Фасциолез протекает в виде бессимптомного острого периода после попадания паразита в организм, за которым следуют острый период и хроническая фаза заболевания. Острый период заражения фасциолами начинается при разрушении молодыми сосальщиками ткани стенок кишечника и брюшины и их внедрении через оболочку печени в желчные протоки. Этот процесс сопровождается разрушением клеток печени и приводит к внутреннему кровотечению. Симптомы могут включать в себя лихорадку, тошноту, увеличение печени, крапивницу и острую боль в животе. Хроническая фаза заболевания начинается, когда гельминты проникают в желчные протоки, достигают половозрелости и начинают откладывать яйца. Яйца попадают сначала в желчь, затем в кишечник и с калом выделяются во внешнюю среду. Это может выражаться в виде таких симптомов, как периодическая боль, желтуха, анемия, панкреатит и желчекаменная болезнь. Вследствие хронического воспалительного поражения тканей хронические инвазии приводят к циррозу печени.
Парагонимоз на ранних стадиях может протекать бессимптомно. После проникновения паразита в легкие заболевание может сопровождаться выраженными клиническими проявлениями, в частности постоянным кашлем с выделением окрашенной кровью мокроты, болью в грудной клетке, одышкой и лихорадкой, которые могут приводить к таким осложнениям, как плевральный выпот и пневмоторакс. Симптомы и проявления заболевания можно спутать с туберкулезом, и это необходимо учитывать при отсутствии улучшений в процессе лечения больных с подозрением на туберкулез. Также довольно часто встречается эктопический парагонимоз, наиболее распространенной формой которого является церебральный парагонимоз. Его клиническими проявлениями могут быть головная боль, ухудшение зрения, эпилептические судороги и кровоизлияние в мозг.
Симптомы и проявления заболевания можно спутать с туберкулезом, и это необходимо учитывать при отсутствии улучшений в процессе лечения больных с подозрением на туберкулез. Также довольно часто встречается эктопический парагонимоз, наиболее распространенной формой которого является церебральный парагонимоз. Его клиническими проявлениями могут быть головная боль, ухудшение зрения, эпилептические судороги и кровоизлияние в мозг.
Диагностика
Случаи с подозрением на трематодоз пищевого происхождения выявляются на основании анализа клинической картины, оценки пищевого анамнеза на предмет факторов риска (употребление в пищу сырой рыбы, ракообразных, не прошедших термическую обработку водных растений), наличия эозионофилии и характерных изменений, видимых при выполнении ультразвукового исследования, компьютерной томографии (КТ) или магниторезонансной томографии (МРТ). Для подтверждения диагноза применяются различные диагностические методы.
- Паразитологические методы обнаружения яиц в образцах кала при подозрении на клонорхоз, описторхоз и фасциолез и прямое микроскопическое исследование мазков мокроты при подозрении на парагонимоз. Эти методы применяются чаще всего и характеризуются низкой чувствительностью при легкой паразитарной нагрузке, но при соответствующей квалификации лаборанта позволяют получить точный результат, хотя дифференциация морфологических особенностей яиц паразита при этом может быть затруднена. Исследование методом мазка по Като-Кац рекомендуется проводить дважды.
- Иммунологические методы для выявления паразит-специфических антител в образцах сыворотки или паразит-специфических антигенов с образцах сыворотки или кала. Данные методы нередко оказываются более чувствительными, однако выявление антител не позволяет различать текущие, недавно перенесенные или прошлые инвазии. Также возможны перекрестные реакции с антигенами других трематод.
- Такие молекулярные методы, как метод полимеразной цепной реакции, могут оказаться полезными и в настоящее время находятся на этапе экспериментальной разработки.

Лечение, профилактика и борьба
Борьба с трематодозами пищевого происхождения направлена на снижение риска заражения и уменьшение связанной с этим заболеваемости. При этом следует применять всеобъемлющий подход к вопросам здоровья, позволяющий учитывать взаимосвязи между здоровьем животных и человека и состоянием окружающей среды. Для сокращения интенсивности передачи и риска инвазий следует осуществлять комплекс мер, включающий информационно-разъяснительную и просветительскую работу среди населения по вопросам обеспечения безопасности пищевых продуктов, совершенствование санитарных систем и ведение санитарного и ветеринарного надзора.
В целях уменьшения заболеваемости ВОЗ рекомендует повышать доступность лечения с применением безопасных и эффективных противогельминтных средств.
- Лечение клонорхоза и описторхоза проводят празиквантелом дозами по 25 мг/кг три раза в день на протяжении двух – трех дней подряд либо однократной дозой 40 мг/кг.
- Лечение фасциолеза проводят однократной дозой триклабендазола 10 мг/кг. При отсутствии лечебного эффекта дозировку можно увеличить до 20 мг/кг в виде двух раздельных доз с интервалом 12–24 часа.
- Лечение парагонимоза может осуществляться триклабендазолом 20 мг/кг в виде двух раздельных доз по 10 мг/кг, назначаемых в один день, либо празиквантелом 25 мг/кг три раза в день на протяжении трех дней. Лечение триклабендазолом является предпочтительным в силу простоты данной схемы и, соответственно, более четкого соблюдения режима лечения.
В целях контроля за состоянием здоровья населения ВОЗ рекомендует проводить обследования населения на районном уровне и обеспечивать массовой химиопрофилактикой соответствующие группы населения в районах с большим количеством пораженных инвазиями лиц. Оказание индивидуальной помощи путем лечения пациентов с подтвержденной или подозреваемой инвазией является целесообразным в условиях меньшей концентрации случаев заболевания и доступности медицинских учреждений.
Добиться снижения распространенности инвазий можно исключительно методами профилактической химиотерапии. Такие факторы, как антисанитария и несоблюдение гигиены питания, наличие животных резервуаров паразитов и традиционные пищевые привычки населения, могут повышать показатели повторного заражения среди населения после лечения. При этом программы массовой химиопрофилактики должны осуществляться в рамках более широкого подхода к охране здоровья, предполагающего санитарное просвещение населения, ветеринарный и фитосанитарный надзор, обеспечение безопасности пищевых продуктов и совершенствования систем водоснабжения, санитарии и гигиены.
Рекомендуемые схемы лечения и стратегии обобщенно представлены в таблице 2.
Таблица 2. Рекомендуемые схемы лечения и стратегии
| Болезнь | Рекомендуемый препарат и дозировка | Рекомендуемая стратегия | |
| Клонорхоз и описторхоз | Ведение отдельных случаев | ||
| Празиквантел: 25 мг/кг три раза в день в течение 2-3 дней подряд | — Лечение всех подтвержденных случаев — В эндемичных районах: лечение всех подозрительных случаев | ||
| Превентивная химиотерапия | |||
| Празиквантел: 40 мг/кг однократно | В районах, сельских населенных пунктах или общинах, где имеются признаки возникновения кластеров случаев, – лечение всех жителей каждые 12 месяцев | ||
| Фасциолез | Ведение отдельных случаев | ||
| Триклабендазол: 10 мг/кг однократно (в случае отсутствия лечебного эффекта возможна двойная доза 20 мл/кг в два раздельных приема с интервалом 12–24 часа) | — Лечение всех подтвержденных случаев — В эндемичных районах: лечение всех подозрительных случаев | ||
| Превентивная химиотерапия | |||
| Триклабендазол: 10 мг/кг однократно | В районах, сельских населенных пунктах или общинах, где имеются признаки возникновения кластеров случаев, – лечение всех детей школьного возраста (5-14 лет) или всех жителей каждые 12 месяцев | ||
| Парагонимоз | Ведение отдельных случаев | ||
| Триклабендазол: — 2 х 10 мг/кг в течение одного дня или Празиквантел: — 25 мг/кг три раза в день в течение трех дней | — Лечение всех подтвержденных случаев — В эндемичных районах: лечение всех подозрительных случаев | ||
| Превентивная химиотерапия | |||
| Триклабендазол: 20 мг/кг однократно | В районах, сельских населенных пунктах или общинах, где имеются признаки возникновения кластеров случаев, – лечение всех жителей каждые 12 месяцев | ||
Лечение описторхоза в Одинцово
В организм человека личинки паразитов попадают вместе с сырой или недостаточно термически обработанной рыбой и длительно живут в нем (35-40 лет), нанося вред и отравляя организм продуктами своей жизнедеятельности. Против описторхов не вырабатывается иммунитет и возможно неоднократное заражение ими.
Против описторхов не вырабатывается иммунитет и возможно неоднократное заражение ими.
Описторхии в организме не размножаются. Количество их увеличивается каждый раз при приеме в пищу зараженной рыбы. Больной описторхозом не является заразным для других людей. Возбудитель описторхоза поражает обычно весь желудочно-кишечный тракт, но наиболее часто паразита находят в желчных ходах, желчном пузыре и протоках поджелудочной железы.
Организм хозяина вынужден постоянно обеспечивать паразита питательными веществами, удалять продукты его жизнедеятельности. С другой стороны паразит подавляет защитные реакции организма хозяина. Борьба человека с паразитом проявляется в виде клинических симптомов заболевания описторхозом.
Симптомы
Ведущим из них является развитие аллергических реакций, в виде крапивницы, которая появляется и исчезает независимо от каких либо причин, отека, вплоть до отека Квинке, холодовой аллергии. Описторхоз может быть основной причиной поллинозов, бронхиальной астмы, различных поражений кожи – проблемной кожи, псориаза, экземы. Больные обычно жалуются на боли в правом подреберье, тошноту, головные боли, боли в суставах и в мышцах, постоянную утомляемость, усталость. Описторхоз может быть основной причиной или поддерживать язвенную болезнь желудка и 12-перстной кишки, воспаления поджелудочной железы, дискинезии желчевыводящей системы, гипертонии, бесплодия, облысения, различных расстройств со стороны сердечнососудистой системы (аритмии, экстрасистолии и др.), нервной системы (неврозы, депрессии), эндокринной и что наиболее важно, иммунной систем. При наличии описторхоза, трудно или вообще не поддаются лечению различные хронические заболевания (трихомониаз, хламидиоз, простатит и др.) Однако необходимо отметить, что описторхоз может протекать до поры до времени, совершенно бессимптомно и сразу проявиться в виде цирроза и рака печени. Гельминты оказывают отрицательное влияние на течение беременности и родов, физическое и умственное развитие детей и на многое, многое другое.
Диагностика и лечение
Диагностика описторхоза проводится на основании клинических симптомов, результатов дуоденального зондирования и анализа кала на яйцеглист. Все другие методы являются косвенными и не могут с достоверностью констатировать наличие или отсутствие заболевания.
В настоящее время существуют множественные методы лечения описторхоза, которые делятся на общепринятые, традиционные и нетрадиционные, и все они содержат рациональные элементы воздействия на паразита. Для того чтобы обезопасить себя и членов своей семьи нужно соблюдать элементарные правила профилактики описторхоза. Основой эффективной профилактики является исключение из рациона не обеззараженной рыбы и рыбной продукции. Обеззараживание можно достигнуть благодаря тщательной термической обработке, замораживанию, копчению или солению.
Черви в печени. Чем опасен описторхоз? | ЗДОРОВЬЕ: Медицина | ЗДОРОВЬЕ
Блюда из речной рыбы традиционны для сибиряков: уха, пироги, жареные караси. Но малейшее несоблюдение правил термической обработки, и любимые лещ, сазан, елец, язь, чебак, плотва и карасики могут стать причиной описторхоза. При этом паразитарном заболевании, прежде всего, страдают печень и поджелудочная железа. Ежегодно взрослые и дети оказываются на больничной койке с острым течением недуга. Чем опасен описторхоз, в материале «АиФ – Тюмень».
Только Well Donе
Часто описторхоз маскируется под другие патологии, распознать его бывает непросто. В острой форме он маскируется под желтуху или аллергию, проявляется повышенным потоотделением, слабостью, суставными и мышечными болями, тошнотой и рвотой, головной болью, бронхитом, может протекать с высокой температурой. Это связано с реакцией организма на гельминтов. В хронической форме описторхоз дает о себе знать болями в животе, чаще всего в правом подреберье, аллергической сыпью, вялостью, недомоганием, беспричинной температурой, явления диспепсическими явлениями – расстройство стула, тяжесть в желудке. Установить точный диагноз помогает анализ на антитела либо на наличие яиц паразита.
Установить точный диагноз помогает анализ на антитела либо на наличие яиц паразита.
«Основной источник заражения – рыбы карповых пород, водящиеся в Обь-Иртышском бассейне, – рассказывает заведующая детским отделением Областной инфекционной больницы Галина Полушкина. – Особенно опасна строганина из этих рыб. Поскольку для некоторых коренных народов нашего региона употребление в пищу сырой рыбы – традиционно, для нас описторхоз – актуальная проблема».
«Поймать» паразитов можно и через плохо проваренную, недостаточно обжаренную, пропеченную, просоленную рыбу, а также через общую с другими продуктами разделочную доску, ножи. Карася, леща, язя и других представителей семейства карповых следует есть только после полного приготовления. Например, варить не менее 20 минут с момента закипания воды или бульона, жарить – только под закрытой крышкой небольшими кусочками по 20 минут каждую сторону, чтобы наверняка все приготовилось. Если рыба в пироге, то раньше часа выключать духовку не стоит. При солении рыбу нужно продержать в рассоле не менее двух недель.
«Поймать» паразитов можно и через плохо прожаренную или не до конца проваренную, пропеченную, вяленую рыбу. Фото: pixabay.com«Чаще всего заражение обусловлено употреблением в пищу плохо обработанной рыбы. Когда при приготовлении не выдерживается температурный режим, паразиты вместе с мясом рыбы попадают в человеческий организм и вызывают болезнь. Острая форма описторхоза чаще диагностируется у тех, кто недавно переехал в наш регион из другой местности. Дело в том, что местные жители уже сенсибилизированы, то есть «встречались» с паразитами, они есть в их организме, но никак не проявляются. Обнаруживают их, как правило, случайно, при очередном обследовании, когда требуется выполнить анализ на наличие яиц глистов», – говорит врач.
Анализы покажут
По словам Галины Евгеньевны, традиция давать маленьким детям пробовать сырую рыбу есть не только у коренных народов тюменского севера. В семьях местных рыбаков улов частенько идет на стол, бывает совсем малюток кормят рыбой – и сырой, и приготовленной. В практике врача были случаи, когда с описторхозом в больницу госпитализировались годовалые ребятишки. А самому маленькому пациенту было всего девять месяцев.
В семьях местных рыбаков улов частенько идет на стол, бывает совсем малюток кормят рыбой – и сырой, и приготовленной. В практике врача были случаи, когда с описторхозом в больницу госпитализировались годовалые ребятишки. А самому маленькому пациенту было всего девять месяцев.
Описторхоз может протекать и бессимптомно, такая форма чревата серьезными осложнениями – от токсического миокардита до рака печени.
Выявить паразитов поможет обычный анализ кала на яйца глист, правда, сдать его нужно три-четыре раза. Один анализ может не показать описторхоз. Любителям речной рыбы такое исследование желательно проводить каждые полгода, раз в год можно сдать анализ крови на антитела.
Обе формы описторхоза успешно лечатся, но есть одно условие: после излечения придется навсегда отказаться от рыб карповых пород, так как при повторном заражении течение болезни будет тяжелее в разы.
Описторхис — обзор | ScienceDirect Topics
Этиология:
Opisthorchis viverrini — это наиболее распространенный билиарный печеночный сосальщик у людей, наиболее тесно связанный с холангиокарциномой (вставка 20.3).
Эпидемиология: Opisthorchis видов и Clonorchis sinensis , иногда идентифицируемые как Opisthorchis sinensis , передаются человеку через употребление в пищу сырой рыбы, содержащей инфекционные метацеркарии (Таблица 20.4). По оценкам, 17 миллионов человек во всем мире инфицированы этими организмами; 9 миллионов — O. viverrini , 7 миллионов — C. sinensis и 1,5 миллиона — O. felineus . 47 Географическое распространение этих сосальщиков зависит от ареала промежуточных улиток и рыб-хозяев (рис. 20.10). O. viverrini является эндемиком Лаоса, Камбоджи и Таиланда. C. sinensis встречается в Китае, Тайване, Вьетнаме, Корее, Гонконге и Японии. O. felineus встречается в некоторых частях Азии, Восточной Европы и Сибири.
O. felineus встречается в некоторых частях Азии, Восточной Европы и Сибири.
В отличие от Ascaris и Trichuris , как распространенность, так и тяжесть инфекций билиарного печеночного сосальщика увеличиваются с возрастом. Традиционное приготовление пищи приводит к постоянному воздействию на всю жизнь. В Лаосе, Камбодже и некоторых частях северного Таиланда люди всех возрастов наслаждаются кои пла — смесью толченой сырой рыбы и специй. 47 В Китае, где многие дети ловят и едят сырую рыбу, возрастное распределение смещено в сторону детей. 36
Хотя подавляющее большинство инфицированных иммигрантов прибывает из Юго-Восточной Азии, случаи O. guayaquilensis и O. felineus были зарегистрированы у иммигрантов из Эквадора и бывшего Советского Союза, соответственно, в Соединенных Штатах. 47 В регионах Сибири популярным блюдом является замороженная рыба карповых, нарезанная тонкими ломтиками. 36
Инфекции билиарного печеночного двуустки являются хроническими и остаются проблемой для иммигрантов в течение многих лет после иммиграции. Было зарегистрировано, что C. sinensis вызывает панкреатит у человека через 24 года после выхода из эндемичной зоны. 48 Распространенность инфекций Opisthorchis составила 5% среди группы камбоджийских беженцев после 6 лет проживания в Канаде. 13 Выявление инфекций билиарного печеночного двуустки имеет бимодальное распределение по времени с момента иммиграции. В серии из 17 случаев примерно половина инфекций была диагностирована во время первичного обследования при прибытии в течение 3 месяцев после иммиграции.Четверть случаев заражения была диагностирована у иммигрантов, проживающих в США более 5 лет, из них 12% — через 10 лет. Некоторые из тех, кому поставили поздний диагноз, после эмиграции посетили свои страны происхождения, что указывает на возможность заражения инфекциями, связанными с поездками. 47
47
Описторхис — обзор | Темы ScienceDirect
5.4 Трематодные трематоды пищевого происхождения
Клинически важные пищевые трематоды включают печеночные двуустки Opisthorchis spp., Clonorchis sinensis , Fasciola spp. И легочная двуустка Paragonimus spp. (Sripa et al., 2010; Waikagul, 2015). Наиболее распространенными трематодами с тяжелыми клиническими осложнениями являются мелкие пищевые печеночные двуустки Opisthorchis viverrini и Clonorchis sinensis . Эти два вида имеют сложный жизненный цикл, и окончательные окончательные хозяева, включая людей, собак и кошек, заражаются после употребления в пищу сырой или неправильно приготовленной рыбы, содержащей инфекционные метацеркарии.Заражение Fasciola spp. возникает в результате проглатывания метацеркарий, обнаруженных на загрязненных водных растениях, таких как кресс-салат, и заражения Paragonimus spp. возникает после употребления в пищу неправильно приготовленных пресноводных крабов и других ракообразных, которые выступают в качестве промежуточных хозяев (Sripa et al., 2010). Opisthorchis spp., C. sinensis и Paragonimus spp. являются паразитами исключительно пищевого происхождения, и хотя Fasciola spp. потенциально передаются через воду, подавляющее большинство случаев передаются через пищу (Torgerson et al., 2014).
Жизненный цикл трематод пищевого происхождения сложен, и передача ограничена территориями, где сосуществуют первый и второй промежуточные хозяева и где пищевые привычки позволяют передавать инфекции людям (Keizer and Utzinger, 2005). Географическое распространение трематод пищевого происхождения разнообразно, и их пространственно-очаговая встречаемость представляет методологические проблемы при оценке заболеваемости и бремени болезней (Furst et al., 2012). В 2005 году во всем мире трематодой пищевого происхождения было инфицировано около 56 миллионов человек (Furst et al. , 2012), и, по оценкам, 750 миллионов человек подвергались риску заражения (Keizer and Utzinger, 2009; Sripa et al., 2010). Из числа инфицированных около 8 миллионов случаев с тяжелыми последствиями ежегодно приводили к более чем 7000 смертельных исходов. C. sinensis и O. viverrini вызывают наиболее тяжелое заболевание, и инфекция может привести к холангиокарциноме, изнурительному раку желчного протока (Sripa et al., 2007). Потенциал Opisthorchis felineus вызывать рак желчных протоков в настоящее время является предметом обсуждения, но эта инфекция действительно приводит к тяжелым заболеваниям в эндемичных регионах Центральной Азии и Восточной Европы (Furst et al., 2012; Хотез, Алибек, 2011).
, 2012), и, по оценкам, 750 миллионов человек подвергались риску заражения (Keizer and Utzinger, 2009; Sripa et al., 2010). Из числа инфицированных около 8 миллионов случаев с тяжелыми последствиями ежегодно приводили к более чем 7000 смертельных исходов. C. sinensis и O. viverrini вызывают наиболее тяжелое заболевание, и инфекция может привести к холангиокарциноме, изнурительному раку желчного протока (Sripa et al., 2007). Потенциал Opisthorchis felineus вызывать рак желчных протоков в настоящее время является предметом обсуждения, но эта инфекция действительно приводит к тяжелым заболеваниям в эндемичных регионах Центральной Азии и Восточной Европы (Furst et al., 2012; Хотез, Алибек, 2011).
Глобальное бремя трематод пищевого происхождения в 2005 г. оценивалось в 665 000 DALY, при этом подавляющее большинство бремени несли люди, проживающие в пространственно очаговых районах эндемичности (Furst et al., 2012). Только в Китае (включая Гонконг и Макао) было потеряно более 440 000 DALY, в основном из-за клонорхоза (231 547 DALY) и парагонимоза (188 439 DALY). Бремя описторхоза, вызываемого O. viverrini , ограничивается в основном эндемичными регионами Таиланда и Лаоса в Юго-Восточной Азии, в результате чего потеряно 74 070 DALY.Расчетное бремя описторхоза, вызванного O. felineus в Центральной Азии и Восточной Европе, было относительно небольшим по сравнению с предполагаемыми потерями 297 DALY. Глобальное бремя фасциолоза в основном несут Боливия, Эквадор и Перу в Латинской Америке (потеряно 17 318 DALY), а также Египет и Иран в Северной Африке и на Ближнем Востоке (потеря 17 275 DALYS) (Furst et al., 2012).
Оценки заболеваемости трематодами пищевого происхождения консервативны и, скорее всего, занижают истинную заболеваемость (Furst et al., 2012). Напротив, исследование ГББ 2010 оценило глобальное бремя трематодозов пищевого происхождения примерно в 1,9 миллиона потерянных DALY или 27 потерянных DALY на 100 000 населения (Murray et al. , 2012b). В исследовании Furst et al. (2012) использовались DW 0,099 для тяжелого парагонимоза; 0,100 — церебральный парагонимоз; 0,104 — тяжелый клонорхоз, тяжелый описторхоз и тяжелый фасциолоаз; и 0,116 для тяжелой кишечной инфекции. В то время как исследование ГББ 2010 использовало DW для умеренной абдоминально-тазовой болезни 0.123 для всех условий (Murray et al., 2012a; Salomon et al., 2012). Однако важно то, что Furst et al. (2012) приписывают смерть опистохиозу и клонорхозу, а исследование ГББ 2010 — нет (Lozano et al., 2012), несмотря на убедительные доказательства обратного (Hotez et al., 2014). Различия в методологии и весе болезней могут служить причиной различных оценок, но очевидно, что трематодозы пищевого происхождения вызывают существенное снижение качества жизни во всем мире. Кроме того, очаговый характер возникновения означает, что оценка бремени болезней была бы значительной в эндемичных районах, если бы для расчета потерянных DALY на 100 000 человеко-лет использовались более мелкие географические единицы.
, 2012b). В исследовании Furst et al. (2012) использовались DW 0,099 для тяжелого парагонимоза; 0,100 — церебральный парагонимоз; 0,104 — тяжелый клонорхоз, тяжелый описторхоз и тяжелый фасциолоаз; и 0,116 для тяжелой кишечной инфекции. В то время как исследование ГББ 2010 использовало DW для умеренной абдоминально-тазовой болезни 0.123 для всех условий (Murray et al., 2012a; Salomon et al., 2012). Однако важно то, что Furst et al. (2012) приписывают смерть опистохиозу и клонорхозу, а исследование ГББ 2010 — нет (Lozano et al., 2012), несмотря на убедительные доказательства обратного (Hotez et al., 2014). Различия в методологии и весе болезней могут служить причиной различных оценок, но очевидно, что трематодозы пищевого происхождения вызывают существенное снижение качества жизни во всем мире. Кроме того, очаговый характер возникновения означает, что оценка бремени болезней была бы значительной в эндемичных районах, если бы для расчета потерянных DALY на 100 000 человеко-лет использовались более мелкие географические единицы.
Обновленные молекулярно-филогенетические данные по Opisthorchis spp. (Trematoda: Opisthorchioidea) от уток во Вьетнаме | Паразиты и векторы
Opisthorchis sp. Образцы BD2013, собранные с поляВзрослые особи и яйца Opisthorchis sp. BD2013 были собраны у естественно инфицированных домашних уток ( Anas platyrhynchos ), происходящих из 4 населенных пунктов (округа Фу Кат, Фу Ми, Ан Ньон и Туй Фуок) в провинции Бинь Динь Центрального Вьетнама [6, 20] (Таблица 1).Каждый взрослый червь, неокрашенный или окрашенный уксусным кармином, был морфологически идентифицирован с помощью световой микроскопии [5]. До трех взрослых червей из каждой местности индивидуально фиксировали в 70% этаноле, а одного или двух червей из каждой местности отдельно подвергали экстракции геномной ДНК и молекулярному анализу.
Таблица 1 Список полевых образцов, использованных в этом исследовании, их географическое место сбора в провинции Биньдинь и их хозяева Рыбы (укрывающие метацеркарии) и улитки (сбрасывающие церкарии) были собраны в озере Митхо в низинах провинции Биньдинь [20].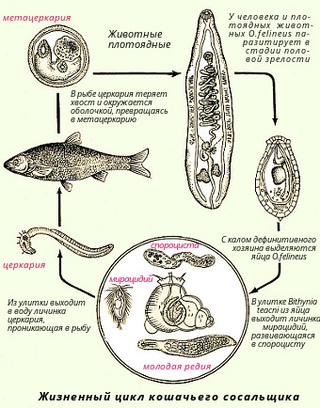 Зараженные рыбы были идентифицированы как Puntius brevis , Esomus metallicus , Rasbora aurotaenia , а улитка — как Bithynia funiculata [20] (Таблица 1). Для молекулярного анализа метацеркарии и церкарии по отдельности фиксировали в буфере RNAlater ™ (Qiagen, Texas, USA) при 4 ° C. Отдельных паразитов от каждого промежуточного хозяина и каждой местности использовали для экстракции ДНК и молекулярного исследования.
Зараженные рыбы были идентифицированы как Puntius brevis , Esomus metallicus , Rasbora aurotaenia , а улитка — как Bithynia funiculata [20] (Таблица 1). Для молекулярного анализа метацеркарии и церкарии по отдельности фиксировали в буфере RNAlater ™ (Qiagen, Texas, USA) при 4 ° C. Отдельных паразитов от каждого промежуточного хозяина и каждой местности использовали для экстракции ДНК и молекулярного исследования.
Яйца были индивидуально собраны из желчного пузыря естественно инфицированных уток путем десятикратного промывания и центрифугирования желчи в физиологическом растворе (0.9% NaCl), затем трижды в фосфатно-солевом буфере (PBS) перед хранением при -20 ° C до использования (Таблица 1).
Экстракция геномной ДНК и праймеры
Полную геномную ДНК экстрагировали из отдельных взрослых особей, метацеркарий, церкарий или объединенных яиц (примерно 2000–3000 яиц) с использованием набора для очистки геномной ДНК GeneJET ™ (Thermo Fisher Scientific Inc., Массачусетс, США) в соответствии с инструкциями производителя. Небольшая модификация, примененная для яиц, заключалась в увеличении периода инкубации на 3–4 часа после ферментативного лизиса.Геномную ДНК элюировали 50 мкл буфера для элюции, входящего в набор, и хранили при -20 ° C. Концентрацию ДНК оценивали с использованием спектрофотометра GBC UV / visible 911A (GBC Scientific Equipment Pty. Ltd., Braeside, Australia) и разбавляли до рабочей концентрации 50 нг / мкл (около 10 нг / мкл для ДНК из яиц). 2–3 мкл этой геномной ДНК использовали в качестве матрицы в ПЦР объемом 50 мкл.
Праймеры, используемые как для амплификации, так и для секвенирования митохондриальных и ядерных рибосомных генов, перечислены в таблице 2.Пара праймеров OACOBF / OACO1R амплифицировала примерно 7,8 т.п.н. мтДНК. На основе последовательности, полученной из этого ампликона, были сконструированы три пары праймеров, специфичных для отдельных генов, кодирующих целевой белок. Пары праймеров OACOBF / OACOBR, OAND1F / OAND1R, OACO1F / OACO1R амплифицировали полные гены cob , nad 1 и cox 1 соответственно. Пары праймеров U18SF / U18SR были использованы для получения основных фрагментов рибосомных 18S и U28SF / U28SR для 28S соответственно [12]. Дополнительные внутренние праймеры были разработаны и использованы по мере необходимости (таблица 2).
Пары праймеров U18SF / U18SR были использованы для получения основных фрагментов рибосомных 18S и U28SF / U28SR для 28S соответственно [12]. Дополнительные внутренние праймеры были разработаны и использованы по мере необходимости (таблица 2).
Амплификация митохондриальных и рибосомных генов
Геномная область mt размером 7,8 т.п.н.
Длинные реакции ПЦР готовили с использованием 25 мкл Fusion High-Fidelity PCR Master Mix (2 ×) (Thermo Fisher Scientific Inc., Уолтем, Массачусетс, США) и 2 мкл каждого праймера (10 пмоль / мкл), 2 мкл ДНК-матрицы взрослого образца (50 нг / мкл), 2 мкл ДМСО (диметилсульфоксид) и 17 мкл H 2 O до конечного объема 50 мкл.Все ПЦР проводили в термоциклере MJ PTC-100 с инициированием при 98 ° C в течение 30 с, за которыми следовали 35 циклов, состоящих из денатурации в течение 10 с при 98 ° C, отжига при 56 ° C в течение 30 с, удлинения при 72 ° C. C в течение 6 мин.
Индивидуальные гены mt и рибосомальной ДНК
ПЦР-реакции по 50 мкл были приготовлены с использованием 25 мкл DreamTaq PCR Master Mix (2 ×) (Thermo Fisher Scientific Inc., Уолтем, Массачусетс, США), 2 мкл каждого праймера (10 пмоль / мкл), 2 мкл ДНК-матрицы (50 нг / мкл для взрослых; 50 нг / мкл для метацеркарий; 10–20 нг / мкл для церкарий и яиц), 2 мкл ДМСО (диметилсульфоксид) и 17 мкл H 2 О.Все ПЦР проводили в термоциклере MJ PTC-100 с инициированием при 94 ° C в течение 5 мин, за которыми следовали 35 циклов, состоящих из денатурации в течение 30 с при 94 ° C, отжига при 56 ° C в течение 30 с, удлинения при 72 ° C. C в течение 3 мин.
Секвенирование и анализ последовательностей
продуктов ПЦР были получены как минимум из двух отдельных образцов для каждой матрицы (т. Е. Взрослых особей, метацеркарий, церкарий и яиц), происходящих из разных географических мест.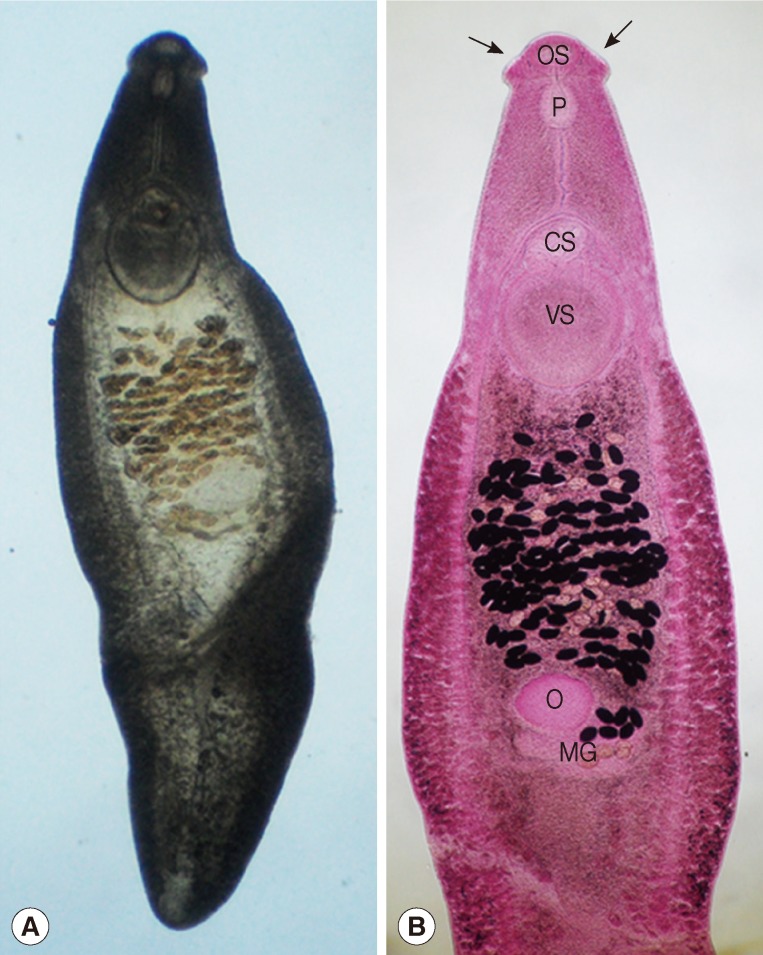 Продукты ПЦР (по 10 мкл каждого) исследовали на 1% агарозном геле, окрашивали бромидом этидия и визуализировали в УФ-свете (Wealtec, Meadowvale Way Sparks, США).
Продукты ПЦР (по 10 мкл каждого) исследовали на 1% агарозном геле, окрашивали бромидом этидия и визуализировали в УФ-свете (Wealtec, Meadowvale Way Sparks, США).
Все очищенные или экстрагированные из геля ампликоны подвергали прямому секвенированию с помощью автоматических секвенаторов с использованием амплификации / фланкирования и внутренних праймеров (таблица 2) путем обхода праймеров в обоих направлениях (Macrogen Inc., Сеул, Южная Корея). Последовательности (по две из каждого образца) были выровнены, чтобы получить окончательную последовательность для характеристики. Все последовательности Opisthorchis sp. BD2013 были идентичны, независимо от стадии жизненного цикла или местонахождения.
Конкатенированные нуклеотидные и аминокислотные последовательности трех генов, кодирующих белок, i.е., cob + nad 1 + cox 1, были использованы для вывода парных генетических дистанций между 10 описторхидами (таблица 3). Эти изоляты включали Opisthorchis sp. BD2013 и эталонные последовательности из Лаоса (JF739555), Вьетнама (MF287777 – MF287779) и Таиланда (MF287780 – MF287782). Генетические дистанции были выведены путем попарного анализа с использованием программы MEGA6.0, а количество замен оснований на сайт было рассчитано наиболее упрощенным методом (нескорректированное p-расстояние) [21].
Таблица 3 Сводные данные для полных митохондриальных геномов видов, обеспечивающих цитохром b ( cob ), субъединицу 1 никотинамиддегидрогеназы ( nad 1) и цитохром c субъединицу 1 оксидазы ( cox 1), используемые в филогенетический анализ, включающий Opisthorchis sp. BD2013 у уток во ВьетнамеФилогенетический анализ
Получение последовательностей ДНК
Филогенетический анализ с использованием трех митохондриальных белков, кодирующих ( cob , nad 1, cox 1) и двух ядерных рибосомных генов (18S и 28S рДНК), был проведен для изучения таксономическое размещение Opisthorchis sp. BD2013 от уток в надсемействе Opisthorchioidea. Использовали последовательности видов / изолятов трематод Opisthorchiidae, Heterophyidae, Fasciolidae и Schistosomatidae (в качестве внешней группы). Сводные данные по видам / изолятам, в основном из доступных полных митохондриальных геномов, представлены в таблице 3. Номера доступа для целевых и контрольных последовательностей 18S и 28S рДНК перечислены в таблице 4. Для Opisthorchis sp. BD2013, мы решили использовать только две последовательности взрослых особей и по одной из метацеркарий, церкарий и яиц для филогенетических анализов.
BD2013 от уток в надсемействе Opisthorchioidea. Использовали последовательности видов / изолятов трематод Opisthorchiidae, Heterophyidae, Fasciolidae и Schistosomatidae (в качестве внешней группы). Сводные данные по видам / изолятам, в основном из доступных полных митохондриальных геномов, представлены в таблице 3. Номера доступа для целевых и контрольных последовательностей 18S и 28S рДНК перечислены в таблице 4. Для Opisthorchis sp. BD2013, мы решили использовать только две последовательности взрослых особей и по одной из метацеркарий, церкарий и яиц для филогенетических анализов.
Конкатенированные нуклеотидные последовательности генов, кодирующих белок mt ( cob , nad 1, cox 1) взрослых особей, метацеркарий, церкарий и яиц Opisthorchis sp. BD2013, а также из дополнительных таксонов (доступных в GenBank; см. Таблицу 3) были импортированы в GENEDOC 2.7 (доступно на http://iubio.bio.indiana.edu/soft/molbio/ibmpc/genedoc-readme.html) и выровнено для филогенетического анализа. Кроме того, последовательности описторхиидов были транслированы (с использованием генетического кода митохондрий иглокожих / плоских червей: таблица трансляции 9 в GenBank), и выведенные аминокислотные последовательности выровнены для попарного анализа генетических расстояний.
ДНК-последовательностей генов 18S рРНК и 28S рРНК (перечисленных в Таблице 4) выравнивали отдельно с помощью GENEDOC 2.7. Последовательности были обрезаны с обоих концов до самой короткой длины репрезентативных последовательностей.Для 18S рДНК в этом исследовании окончательное выравнивание было длиной 2005 нуклеотидов (нт), из которых 87 нт положений были обрезаны на 5′-конце и 114 нуклеотидов на 3′-конце, оставив 1804 символа для анализа. Для 28S рДНК окончательное выравнивание составило 1449 нуклеотидов, из которых 122 нуклеотида были обрезаны на 5′-конце и 123 нуклеотида на 3′-конце, оставив 1202 символа для анализа. Затем две последовательности были объединены, как указано в таблице 4, предпочтительно из одних и тех же штаммов / изолятов. Конкатенированные последовательности рДНК 18S + 28S, представляющие виды / изоляты, были импортированы в GENEDOC 2.7, а филогенетический анализ и построение дерева были выполнены с помощью MEGA6.0 [21].
Для 28S рДНК окончательное выравнивание составило 1449 нуклеотидов, из которых 122 нуклеотида были обрезаны на 5′-конце и 123 нуклеотида на 3′-конце, оставив 1202 символа для анализа. Затем две последовательности были объединены, как указано в таблице 4, предпочтительно из одних и тех же штаммов / изолятов. Конкатенированные последовательности рДНК 18S + 28S, представляющие виды / изоляты, были импортированы в GENEDOC 2.7, а филогенетический анализ и построение дерева были выполнены с помощью MEGA6.0 [21].
Филогенетическая реконструкция
Выравнивания конкатенированных нуклеотидов ( cob , cox 1, nad 1) и 18S + 28S последовательностей, соответственно, были обрезаны до длины самой короткой последовательности и импортированы в MEGA 6.06. программное обеспечение [21]. В каждом случае проводился анализ максимального правдоподобия (ML). Для последовательностей ДНК мы использовали общую обратимую во времени модель эволюции с гамма-распределенной гетерогенностью по скорости и долей инвариантных сайтов (GTR + Γ + I).MEGA присвоила этой модели лучший результат по байесовскому информационному критерию. Для аминокислотных последовательностей использовали модель Джонса-Тейлора-Торнтона (JTT) с однородными скоростями и метод обмена ближайшего соседа (NNI). Достоверность каждого узла оценивалась с помощью 1000 повторных выборок бутстрапов [21].
Паспорта безопасности патогенов: инфекционные вещества — Opisthorchis spp.
РАЗДЕЛ I — ИНФЕКЦИОННЫЙ АГЕНТ
НАИМЕНОВАНИЕ: Opisthorchis spp.
СИНОНИМ ИЛИ ПЕРЕКРЕСТНАЯ ССЫЛКА: Описторхоз, клонорхоз, Opisthorchis felineus , Opisthorchis viverrini , болезнь печени кошки-двуустки, pa-ярд бай-май найтуб Сноска 1 Footnote 1 Footnote 1 Footnote 1 Footnote 1 ХАРАКТЕРИСТИКИ: Opisthorchis spp. ПАТОГЕННОСТЬ / ТОКСИЧНОСТЬ: Существует консенсус в отношении того, что биологические и патологические характеристики Opisthorchis и Clonorchis являются одними и теми же патогенами низкой степени злокачественности для желчевыводящих путей. Большинство случаев заражения Opisthorchis (около 80%) — это легкие инфекции. Footnote 1 Footnote 2 .Легкая инфекция, классифицируемая по показателю менее 1000 яиц / г кала, обычно протекает бессимптомно, за исключением эозинофилии. Footnote 2 . На этой стадии не наблюдается заметного нарушения функции печени. Footnote 2 . Тяжелая инфекция классифицируется как 10 000–30 000 яиц / г фекалий Footnote 2 . Клинические проявления тяжелой инфекции включают диарею, запор, боль в животе, анорексию, несварение желудка, желудочно-кишечное кровотечение, усталость, умеренную лихорадку, желтуху, увеличенный или нефункциональный желчный пузырь, холецистит, холангит, абсцесс печени и камни в желчном пузыре Footnote 2 Сноска 3 Сноска 7 . ЭПИДЕМИОЛОГИЯ: О.viverrini — эндемик в Таиланде, Лаосе и Камбодже. O. felineus встречается в Северной Европе и Азии. Footnote 2 . Заражение чаще встречается с сентября по февраль. В эндемичных районах уровень инфицирования может достигать 90% у людей и 97% у рыб. Footnote 5 . Инфекция редко встречается у детей до 5 лет. Распространенность описторхоза выше в районах с плохим или антисанитарным состоянием. Footnote 9 Footnote 10 . HOST RANGE : Люди, улитки, рыбы, кошки, собаки, рептилии, земноводные и рыбоядные животные Сноска 4 Сноска 11-13 ИНФЕКЦИОННАЯ ДОЗА: Возможно всего 1-2 метацеркарии Сноска 8 . РЕЖИМ ПЕРЕДАЧИ: Opisthorchis spp. передаются при попадании в организм сырой или недоваренной рыбы, содержащей метацеркарии. Footnote 3 . ПЕРИОД ИНКУБАЦИИ: Метацеркарии достигают желчных протоков через несколько часов после проглатывания Footnote 7 . Opisthorchis spp. требуется около 4 недель для созревания взрослых червей и производства яиц. КОММУНИКАЦИЯ: Не передается напрямую от человека к человеку. ВОДОХРАНИТЕЛЬ: Карповые рыбы, собаки, кошки, свиньи, крысы, кролики, рыбоядные млекопитающие Сноска 2 Сноска 12 Сноска 13 . ЗООНОЗ: Да, инфекция может передаваться от окончательных хозяев, включая домашних кошек и собак Сноска 2 Сноска 12 . ВЕКТОРЫ: Улитки Сноска 3 . ЛЕКАРСТВЕННАЯ УСТОЙЧИВОСТЬ: Чувствительность к однократной дозе празиквантела и многодозовой альбендазолу Сноска 2 Сноска 14 Сноска 15 . УСТОЙЧИВОСТЬ К ДЕЗИНФЕКЦИОННЫМ СРЕДСТВАМ: Чувствительность к 0,7% сульфату аммония Сноска 7 . ФИЗИЧЕСКАЯ НЕАКТИВАЦИЯ: Цисты чувствительны к глубокому замораживанию при -30oC в течение 32 часов. Footnote 2 . Все стадии Opisthorchis spp. чувствительны к нагреванию до 56 ° C в течение 30 минут Footnote 16 . ВЫЖИВАНИЕ ВНЕ ХОЗЯЙСТВА: Церкарии остаются заразными в пресной воде около 20 часов. Сноска 17 . НАБЛЮДЕНИЕ: Описторхоз диагностируется так же, как и при клорнорхозе. Наблюдать за симптомами, подтверждать инфекцию путем выявления яиц в кале или дуоденального сока под микроскопом (уже, чем яиц Clonorchis ) Footnote 2 Footnote 14 . ELISA также можно использовать для обнаружения антигена O. viverrini Footnote 2 . Инфекцию можно подтвердить с помощью ПЦР. Сноска 5 Сноска 18 . Примечание. Не все методы диагностики доступны во всех странах. ПЕРВАЯ ПОМОЩЬ / ЛЕЧЕНИЕ: Празиквантел следует назначить Сноска 2 Сноска 14 . Если это не переносится, можно использовать альбендазол в качестве альтернативы. Footnote 14 . ИММУНИЗАЦИЯ: Нет ПРОФИЛАКТИКА: Нет ИНФЕКЦИИ, ПОЛУЧЕННЫЕ В ЛАБОРАТОРИИ: По состоянию на 2010 г. ИСТОЧНИК / ОБРАЗЦЫ: Аспираты фекалий, печени и селезенки Сноска 3 Сноска 5 ОСНОВНАЯ ОПАСНОСТЬ: Проглатывание инфекционных агентов. ОСОБЫЕ ОПАСНОСТИ: Животные, инфицированные Opisthorchis spp. представляют собой потенциальную опасность. КЛАССИФИКАЦИЯ ГРУПП РИСКА: Группа риска 2. ТРЕБОВАНИЯ К СРЕДЕ : Помещения, оборудование и операционные методы уровня 2 для работы с инфекционными или потенциально инфекционными материалами, животными или культурами. ЗАЩИТНАЯ ОДЕЖДА : Лабораторный халат. Перчатки при неизбежном прямом контакте кожи с инфицированными материалами или животными. При наличии известного или потенциального риска воздействия брызг необходимо использовать средства защиты глаз. Footnote 19 . ДРУГИЕ МЕРЫ ПРЕДОСТОРОЖНОСТИ : Все процедуры, которые могут привести к образованию аэрозолей, или связаны с высокими концентрациями или большими объемами, должны проводиться в шкафу биологической безопасности ( BSC ). Использование игл, шприцев и других острых предметов должно быть строго ограничено.Дополнительные меры предосторожности следует учитывать при работе с животными или крупномасштабной деятельности. Footnote 19 . РАЗЛИВЫ: Дайте аэрозолям осесть и, надев защитную одежду, аккуратно накройте разлив бумажными полотенцами и нанесите соответствующее дезинфицирующее средство, начиная с периметра и двигаясь к центру. Перед очисткой дайте достаточно времени для контакта. УТИЛИЗАЦИЯ: Обеззараживайте все отходы, которые содержат инфекционные организмы или контактировали с ними, перед их утилизацией в автоклаве, химической дезинфекции, гамма-облучением или сжиганием. ХРАНЕНИЕ: Возбудитель инфекции следует хранить в герметичных контейнерах с соответствующей маркировкой. НОРМАТИВНАЯ ИНФОРМАЦИЯ: Импорт, транспортировка и использование патогенных микроорганизмов в Канаде регулируется многими регулирующими органами, включая Агентство общественного здравоохранения Канады, Министерство здравоохранения Канады, Канадское агентство по инспекции пищевых продуктов, Министерство окружающей среды Канады и Министерство транспорта Канады. Пользователи несут ответственность за соблюдение всех соответствующих законов, постановлений, руководств и стандартов. ОБНОВЛЕНО: ноябрь 2011 ПОДГОТОВЛЕНО: Управление по регулированию патогенов, Агентство общественного здравоохранения Канады Хотя информация, мнения и рекомендации, содержащиеся в этом Паспорте безопасности патогенов, собраны из источников, которые считаются надежными, мы не несем ответственности за точность, достаточность или надежность, а также за любые убытки или травмы, возникшие в результате использования информации. Часто обнаруживаются новые опасности, и эта информация может быть не полностью актуальной. Авторские права © Агентство общественного здравоохранения Канады, 2011 г. Канада По всей Юго-Восточной Азии наблюдается поразительно высокая заболеваемость холангиокарциномой (CCA — печеночный рак эпителия желчных протоков), особенно среди людей из сельских районов Лаоса и Северо-Восточного Таиланда, инфицированных печеночной двуусткой, Opisthorchis viverrini , одним из всего три канцерогенных эукариотических возбудителя.Более распространенные канцерогенные микробы, такие как Helicobacter pylori , вызывают рак менее чем у 1% инфицированных людей, в то время как у одной шестой людей с описторхозом разовьется CCA. У вас есть доступ к этой статье , возможно, трудно сделать вывод из этих отчетов о случаях, и наши результаты остаются информативными. Хотя трудно доказать четкую взаимосвязь между паразитом и конкретным раком у человека, в этом систематическом обзоре были обнаружены некоторые косвенные доказательства новых паразитов, которые могут быть связаны с канцерогенезом , которые заслуживают дальнейшего исследования . между раком и паразитарными инфекциями подчеркивает потенциальное клиническое влияние этой связи . У нашего исследования есть ограничения. В литературе имеется не более нескольких популяционных исследований , которые могли бы укрепить связь между раком и паразитами (временная связь — ), а также силу связи. Например, исключенная статья представляла собой исследование случай-контроль, в котором было обнаружено 24% из пациентов с раком желудочно-кишечного тракта (ЖКТ) с серологическим положительным результатом на Strongyloides, тогда как только 4,5% пациентов с — не имели GI. рак ранее подвергался воздействию Strongyloides. 42 Исключение было основано на единичном результате распространенности Strongyloides без доказательств наличия паразита в раке tis- sue. Другое исследование методом случай-контроль показало, что распространенность инфекции Strongyloides у пациентов с раком желчных путей составляла 18,4% по сравнению с отрицательным контролем, 7,5% (p50,03). 43 Основное место обитания Strongyloides обычно находится в двенадцатиперстной кишке , а не в желчных путях (биологическая достоверность), поэтому исследование было исключено из окончательного анализа.Можно ли задать вопрос о том, может ли отчет о случае обнаружения паразита в раке ткани обязательно соответствовать причинно-следственной связи. Тем не менее, мы выбрали эти случаи для дальнейшего анализа , учитывая тот факт, что рак содержал паразита, свидетельство опухоли, связанной с паразитом, и отсутствие явных факторов, связанных с раком, кроме самого паразита. . Последовательность и повторение текущих результатов необходимы в будущих исследованиях.Статьи, в которых предполагалась потенциальная роль паразита в опухоли или раке, не были включены , что сводит эти низкокачественные обсервационные исследования к , искажая наши результаты. Поскольку мы пытались быть более инклюзивными, чем исключающими, при выборе паразитов, наше исследование также может нести риск систематической ошибки отбора. В исследованиях отсутствовала зависимость «доза-ответ» . Другими словами, более высокая интенсивность инфекции может привести к более высокой интенсивности повреждения тканей (т.е.e., Fasciola hepatica и цирроз печени у крупного рогатого скота), но интенсивность инфекции не была указана в исследованиях, которые обнаружили связь между раком и паразитами. 44 В заключение, этот систематический обзор пролил свет на текущие знания о связи паразитарных инфекций (кроме Schistosoma, Opisthorchis и Clonorchis) и рака для матери. В этом обзоре выявлено несколько канцерогенных механизмов .Связь между паразитами и раком должна быть подтверждена в будущих экспериментальных и популяционных исследованиях . Список литературы 1. ВОЗ. Доступно по адресу: http://www.who.int/ mediacentre / factheets / fs366 / en /. (Проверено , 14 августа 2015 г.) 2. Мюррей С.Дж., Барбер Р.М., Форман К.Дж. и др. Dis- лет жизни с поправкой на способности (DALY) для 291 заболевания и случаев легкости и травм в 21 регионе, 1990-2010 гг .: систематический анализ глобального бремени болезней легкости Исследование 2010.Ланцет 2012; 380: 2197–223. 3. Хотез П.Дж., Альварадо М., Баса ~ без М.Г. и др. Исследование глобального бремени болезней , 2010 г .: интерпретация и последствия для забытых тропических болезней . PLoS Negl Trop Dis 2014; 8: e2865. 4. Honeycutt J, Hammam O, Hsieh MH. Schisto- soma haematobium, индуцированная яйцеклеткой urothe- лиальные аномалии, зависящие от p53, модулируются полом хозяина. Exp Parasitol 2015; 158: 55–60.http://dx.doi.org/10.1016/j.exppara.2015. 07.002. 5. Sripa B., Brindley PJ, Mulvenna J, et al. канцерогенное заболевание печени Opisthorchis viverrini– множественные пути к раку. Тенденции Parasitol 2012; 28: 395–407 6. Weitzman MD, Weitzman JB. Какого возраста плотина — ? Воздействие патогенов на пути, которые поддерживают целостность генома хозяина. Cell Host Microbe 2014; 15: 283–94. 7. Охниши С., Ма Н, Танан Р. и др.Повреждение ДНК в канцерогенезе, связанном с воспалением, и раковые стволовые клетки цер. Oxid Med Cell Longev 2013; 2013: 387014 8. Либерати А., Альтман Д.Г., Тецлафф Дж. И др. PRISMA Group: Заявление PRISMA для системы отчетности тематических обзоров и метаанализов исследований, которые оценивают медицинские вмешательства: объяснение и уточнение. PLoS Med 2009; 6: e1000100. 9. Бахрами С., Эсмаилзаде С., Орян А.Роль оксидативного стресса в одновременном возникновении Fasciola gigantica и лейомиомы у крупного рогатого скота. Вет Паразитол 2014; 203: 43–50. 10. Сео А.Н., Гу Ю.К., Чунг Д.И. и др. Коморбидный аденокарцинома желудка и желудка и двенадцатиперстной кишки Strongyloides stercoralis инфекция: отчет о клиническом случае. Korean J Parasitol 2015; 53: 95–9. 11. Tomaino C, Catalano C, Tiba M, et al. Первый отчет о случаях колоректального рака, ассоциированного с хроническим стронгилоидным стеркоральным колитом, и последующие комплексные управленческие решения .Gas- троэнтерология 2015; 148: S575 12. Hayes KS, Cliffe LJ, Potten CS, et al. Инфекция Trichuris muris связана с обострением опухолей кишечника. Immunology 2013; 140: 102 13. Андраде Р., Дантас А., Пиментел Л. и др. Platyno- холангиокарциномы, индуцированные somum fastosum, у кошек. Ветеринарный паразитол 2012; 190: 277–80. 14. Абду А.Г., Харба Н.М., Афи А.Ф. и др. Оценка инфекции Cryptosporidium parvum у иммунокомпетентных и иммунокомпетентных мышей и ее роль в запуске кишечной дисплазии. Int J Infect Dis 2013; 17: e593–600. 15. Certad G, Ngouanesavanh T, Guyot K, et al. Cryptosporidium parvum, потенциальная причина аденокарциномы колик. Infect Agent Cancer 2007; 2:22. 16. Twu O, Dess ı D, Vu A, et al. Trichomonas vagi- nalis, гомолог ингибитора миграции макрофагов , индуцирует рост клеток простаты, инвазивность и воспалительные реакции. Proc Natl Acad Sci USA 2014; 111: 8179–84 17.Шен Д.Ф., Херборт С.П., Туайон Н. и др. Обнаружение ДНК Toxoplasma gondii в первичной внутриглазной B-клеточной лимфоме. Мод Pathol 2001; 14: 995–9. 18. Эррера Л.А., Родру Игез У., Гебхарт Э. и др. Повышенная частота транслокаций хромо- сомов 7, 11 и 14 в лимфоцитах пациентов с нейроцистицеркозом. Mutagenesis 2001; 16: 495– 7. 19. Rainey JJ, Mwanda WO, Wairiumu P, et al.Spa- Исходное распространение лимфомы Беркитта в Кении и связь с риском малярии. Trop Med Int Health 2007; 12: 936–43. 20. Торгбор С., Авуах П., Дейч К. и др. Мультифакторная роль для малярии P. falciparum в патогенезе эндемичной лимфомы Беркитта . PLoS Pathog 2014; 10: e1004170. 21. Aka P, Vila MC, Jariwala A, et al. Эндемическая Bur- лимфома котенка связана с силой и разнообразием малярии Plasmodium falciparum стадийно-специфическим ответом антител к антигену.Кровь 2013; 122: 629–35. 22. Турхан Н., Эсендагли Г., Озкаяр О. и др. Co- наличие инфекции Echinococcus granulosus и метастазов рака в печени коррелирует с сниженным иммунным ответом Th2. Parasite Immu- № 2015; 37: 16–22. 23. Marsolier J, Perichon M, DeBarry JD, Villoutreix BO, Chluba J, Lopez T., Garrido C, Zhou XZ, Lu KP, Fritsch L, Ait-Si-Ali S, Mhadhbi M, Medjkane S, Weitzman JB.Паразиты Theileria секретируют изомеразу пролил для поддержания трансформации лейкоцитов хозяина. Природа 2015; 520: 378–82. 24. Medjkane S, Perichon M, Marsolier J, et al. Thei- leria вызывает окислительный стресс и HIF1aactiva- , которые необходимы для трансформации лейкоцитов хозяина . Онкоген 2014; 33: 1809–17 Инфекционные причины рака 6 Канцерогенез, связанный с паразитами Int. J. Рак: 00, 00–00 (2016) V C2016 UICC Этот сайт использует файлы cookie для повышения производительности.Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт. Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины: является родом трематодных печеночных двуусток, принадлежащих к семейству Opisthorchiidae Footnote 3 . Взрослые особи имеют длину 5-10 мм, ширину 0,8-1,9 мм и проживают в желчном пузыре, желчных протоках и (реже) протоках поджелудочной железы своего окончательного млекопитающего-хозяина Footnote 2 Footnote 4 Footnote 5 .Яйца поедаются первым промежуточным хозяином (улитками). Первым промежуточным хозяином служат несколько видов рода брюхоногих моллюсков Bithynia . Внутри улиток из яиц выделяются мирацидии, которые развиваются на стадиях спороцист, редий и церкарий в течение 6-8 недель Footnote 3 Footnote 6 . Церкарии высвобождаются и проникают в пресноводных рыб (второй промежуточный хозяин), проникая в их мышцы в виде метацеркарий. Окончательные хозяева заражаются при поедании недоваренной или сырой рыбы с метацеркариями.После созревания взрослые особи выпускают яйца, которые хозяин сбрасывает с фекалиями. Яйца желто-коричневые, овальные, размером примерно 27 на 16 мкм. Footnote 5 Footnote 7 .
является родом трематодных печеночных двуусток, принадлежащих к семейству Opisthorchiidae Footnote 3 . Взрослые особи имеют длину 5-10 мм, ширину 0,8-1,9 мм и проживают в желчном пузыре, желчных протоках и (реже) протоках поджелудочной железы своего окончательного млекопитающего-хозяина Footnote 2 Footnote 4 Footnote 5 .Яйца поедаются первым промежуточным хозяином (улитками). Первым промежуточным хозяином служат несколько видов рода брюхоногих моллюсков Bithynia . Внутри улиток из яиц выделяются мирацидии, которые развиваются на стадиях спороцист, редий и церкарий в течение 6-8 недель Footnote 3 Footnote 6 . Церкарии высвобождаются и проникают в пресноводных рыб (второй промежуточный хозяин), проникая в их мышцы в виде метацеркарий. Окончательные хозяева заражаются при поедании недоваренной или сырой рыбы с метацеркариями.После созревания взрослые особи выпускают яйца, которые хозяин сбрасывает с фекалиями. Яйца желто-коричневые, овальные, размером примерно 27 на 16 мкм. Footnote 5 Footnote 7 . РАЗДЕЛ II — ИДЕНТИФИКАЦИЯ ОПАСНОСТИ
 Клинические проявления нелеченой хронической инфекции включают отек ног, асцит, умеренный цирроз печени, гепатомегалию, гиперплазию и воспаление билиарного эпителия. Footnote 2 . Холангиокарцинома тесно связана с инфекцией O. viverrini и имеет высокий уровень смертности. Footnote 2 . Обычно он развивается через 30-40 лет после первоначального заражения, и его жертвы обычно умирают в течение 3-6 месяцев. Footnote 2 Footnote 8 .
Клинические проявления нелеченой хронической инфекции включают отек ног, асцит, умеренный цирроз печени, гепатомегалию, гиперплазию и воспаление билиарного эпителия. Footnote 2 . Холангиокарцинома тесно связана с инфекцией O. viverrini и имеет высокий уровень смертности. Footnote 2 . Обычно он развивается через 30-40 лет после первоначального заражения, и его жертвы обычно умирают в течение 3-6 месяцев. Footnote 2 Footnote 8 . РАЗДЕЛ III — РАСПРОСТРАНЕНИЕ

РАЗДЕЛ IV — УСТОЙЧИВОСТЬ И ЖЕСТКОСТЬ
РАЗДЕЛ V — ПЕРВАЯ ПОМОЩЬ / МЕДИЦИНСКАЯ
РАЗДЕЛ VI — ЛАБОРАТОРНЫЕ ОПАСНОСТИ
 не зарегистрированы.
не зарегистрированы. РАЗДЕЛ VII —
КОНТРОЛЬ ВОЗДЕЙСТВИЯ / ЛИЧНАЯ ЗАЩИТА РАЗДЕЛ VIII — ОБРАЩЕНИЕ С
И ХРАНЕНИЕ 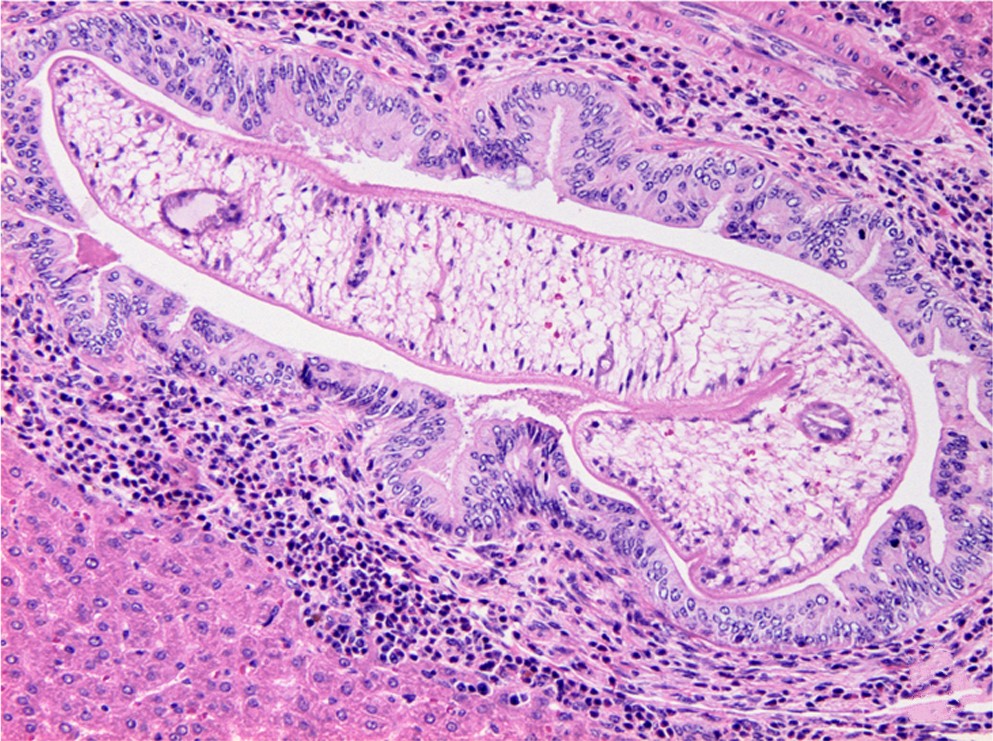
РАЗДЕЛ IX —
НОРМАТИВНАЯ И ДРУГАЯ ИНФОРМАЦИЯ ССЫЛКИ
Инфекция, вызываемая канцерогенным печеночным двуустком человека, Opisthorchis viverrini
 Механизмы, с помощью которых O. viverrini вызывает рак, являются многофакторными, включая механическое раздражение от действий и движений сосальщиков, иммунопатологию, диетические нитрозамины и секрецию паразитарных белков, которые способствуют возникновению опухолевой среды.Геномные и протеомные исследования секретома печеночной двуустки ускорили открытие белков паразитов с известной / потенциальной ролью в патогенезе и онкогенезе, создав основу для понимания и, в конечном итоге, предотвращения заболеваемости и смертности, приписываемых этому высококанцерогенному паразиту.
Механизмы, с помощью которых O. viverrini вызывает рак, являются многофакторными, включая механическое раздражение от действий и движений сосальщиков, иммунопатологию, диетические нитрозамины и секрецию паразитарных белков, которые способствуют возникновению опухолевой среды.Геномные и протеомные исследования секретома печеночной двуустки ускорили открытие белков паразитов с известной / потенциальной ролью в патогенезе и онкогенезе, создав основу для понимания и, в конечном итоге, предотвращения заболеваемости и смертности, приписываемых этому высококанцерогенному паразиту. (PDF) Канцерогенез, связанный с паразитами, отличными от Schistosoma, Opisthorchis и Clonorchis: систематический обзор
 Более того, отсутствие крупных популяционных исследований
Более того, отсутствие крупных популяционных исследований Произошла ошибка при настройке вашего пользовательского файла cookie
Произошла ошибка при настройке вашего пользовательского файла cookie Настройка вашего браузера для приема файлов cookie

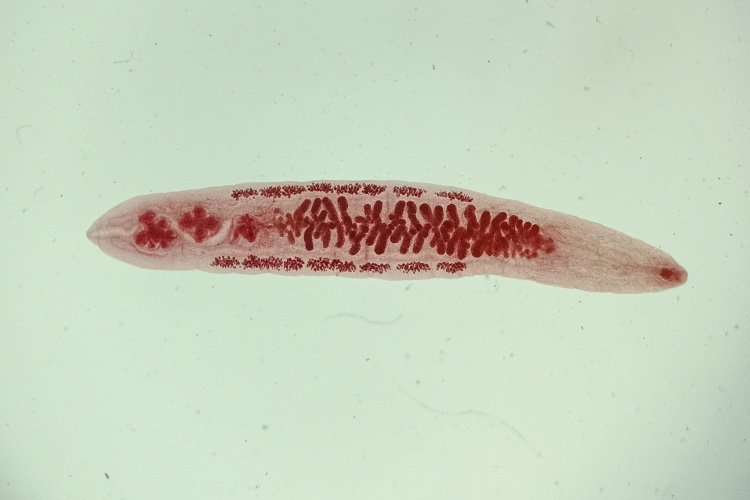

 д.), следует использовать разные разделочные доски.
д.), следует использовать разные разделочные доски.