Нефротический синдром — Википедия
Нефротический синдром — состояние, характеризующееся генерализованными отеками, массивной протеинурией (выше 50 мг*кг/сут или выше 3,5 г/сутки), гипопротеинемией и гипоальбуминемией (менее 20 г/л), гиперлипидемией (холестерин выше 6,5 ммоль/л). Термин предложен Е. М. Тареевым в 1923 году.
Характерен для поражения клубочкового аппарата почек.
Классификация
Гистологическая классификация
|
|
|
|
|
|
|
| Нефротический синдром |
|
|
|
|
| ||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ||||||||||||||||||||||||
|
|
| Болезнь минимальных изменений |
|
| Фокальный сегментарный гломерулосклероз |
|
| Мембранозная нефропатия |
|
| Мембранопролиферативный гломерулонефрит | |||||||||||||||||||||||||||||
Диагностика
Диагностика основывается на выявленных изменениях в анализах крови и мочи (протеинурия, гиперлипидемия, гипопротеинемия), на клинических данных. Клиника МИНС(НС с минимальными изменениями) развертывается постепенно, причём преобладают экстраренальные симптомы, особенно отечный: появляются нарастающие отеки, вначале век, лица, поясничной области (в дальнейшем могут достигать степени анасарки — распространённый отёк подкожной клетчатки), половых органов, асцит, гидроторакс, реже — гидроперикард. Характерна значительная гепатомегалия вследствие дистрофии печени. Кожа становится бледной («перламутровая» бледность) при отсутствии анемии, сухой, появляются признаки гиповитаминозов А, С, В1, В2, дистрофические изменения. Могут наблюдаться ломкость и потускнение волос, на коже — трещины, из которых вытекает жидкость, striae distensae. Ребёнок вялый, плохо ест, развивается одышка, тахикардия, систолический шум на верхушке («гипопротеинемическая кардиопатия»).
Тяжёлым осложнением у больных анасаркой, то есть выраженной гипопротеинемией, может быть гиповолемический шок, которому предшествуют анорексия, рвота, резкие боли в животе. В наблюдениях Н. Д. Савенковой и А. В. Папаяна (1997) абдоминальный болевой синдром развивается у 23,5 % детей с гипоальбуминемией менее 15 г/л, а мигрирующие рожеподобные эритемы у 33,3 %, тромботические эпизоды у 12,5 %, ОПН у 3,3 % детей с той же выраженностью гипоальбуминемии, тогда как нефротический гиповолемический шок отмечен лишь при уровне белка в сыворотке менее 10 г/л (у 5 %). По мере схождения отеков становится все заметнее уменьшение массы скелетных мышц.
Артериальное кровяное давление обычно нормальное, лишь у до10% детей может быть кратковременная артериальная гипертензия. Уровень альбумина в сыворотке крови у таких детей менее 10 г/л.
Содержание общего белка в плазме (сыворотке) крови снижено иногда до 40 г/л.
Особенно резко снижена концентрация альбуминов и g-глобулина, тогда как уровень a2-глобулинов повышен, то есть наблюдается резкая диспротеинемия. Сыворотка крови имеет молочный цвет, в ней находят высокий уровень липидов, холестерина, фибриногена. Уровень азотистых шлаков крови, как правило, нормальный, а содержание калия и натрия снижено. СОЭ резко увеличена (до 50-70 мм/час).
Ренальная симптоматика — олигурия с высокой относительной плотностью (1,026-1,030) мочи и выраженная протеинурия. При исследовании клубочковой фильтрации по эндогенному креатинину получают нормальные и даже повышенные показатели, но это ложное впечатление. Если учесть степень протеинурии, то клубочковая фильтрация при МИНС всегда снижена.
Клиническая картина, течение и исход НС, осложнившего диффузный гломерулонефрит, отличаются от клиники МИНС.
Мочевой синдром при МИНС слагается из следующих симптомов:
1. протеинурия,
2. олигурия с высокой относительной плотностью мочи,
3. цилиндрурия.
Протеинурия при МИНС, как правило, селективная, то есть в моче находят белки плазмы крови с молекулярной массой менее 85 000 (альбумин и его полимеры, преальбумины, сидерофилин, гаптоглобин, трансферрин, a1- и b-глобулины, a1- и a2-гликопротеины и др.). В большинстве случаев у детей с селективной протеинурией прогноз лучше, и они чувствительны к терапии глюкокортикоидами. В генезе протеинурии имеет значение и нарушение реабсорбции белка в почечных канальцах. Неселективная протеинурия, когда в моче есть много крупномолекулярных белков, как правило, следствие фибропластического процесса, склероза, то есть для МИНС нехарактерна. Напомним, что у здорового ребёнка старше 4 лет в суточной моче может быть до 100—150 мг белка.
Олигурия связана с гиповолемией, гиперальдостеронизмом, поражением канальцев. Из-за протеинурии относительная плотность мочи увеличена, достигает 1,040. Высока активность в крови больных и АДГ.
Иногда при НС отмечается массивная лейкоцитурия, обусловленная иммунопатологическим процессом в почках. Лейкоцитурия чаще кратковременная и не связана с бактериальной инфекцией, то есть пиелонефритом. Частота выявления лейкоцитурий и эритроцитурий при МИНС по данным разных авторов не превышает 10 %.
При большом количестве белка в моче он может свернуться ещё в канальцах, принимая их форму; на этот слепок наслаивается жироперерожденный почечный эпителий — так образуются гиалиновые, зернистые и восковые цилиндры.
Отеки. Массивная и длительная альбуминурия у больного с НС в конце концов неизбежно вызывает гипопротеинемию, так как потери белка превышают интенсивность его синтеза. Гипопротеинемия ведёт к нарушению старлингова равновесия между гидродинамическим, фильтрационным и коллоидно-осмотическим давлением. Это приводит к преобладанию оттока жидкости из артериального русла над притоком. Отеки начинают появляться, когда уровень альбумина снижается ниже 27 г/л плазмы и развиваются всегда, если гипоальбуминемия достигает 18 г/л.
В патогенезе отеков важную роль играет и вторичный гиперальдостеронизм, типичный для НС. В результате его в организме задерживается натрий, а следовательно, и вода, хотя в крови имеется гипонатриемия.
Гипопротеинемия. Основной причиной гипопротеинемии у больных с НС являются большие потери альбуминов с мочой и перемещение их в ткани. Кроме того, имеют значение повышенный катаболизм альбуминов, нарушение белоксинтезирующей функции печени. Уменьшение содержания g-глобулинов в крови больных прежде всего с нарушением их синтеза. Гипоальбуминемия и гиповолемия, дефицит антикоагулянтов — антитромбина III и протеинов С и S, гиперфибриногенемия, гиперлипидемия создают угрозу для тромботических нарушений у больных МИНС.
Гиперлипидемия. Некоторые авторы связывают увеличение уровня липопротеинов низкой и очень низкой плотности, холестерина и липидов (свободные жирные кислоты, триглицериды, фосфолипиды и др.) при НС с нарушением функции печени, другие объясняют это явление понижением функции щитовидной железы. В связи с тем, что внутривенное введение раствора альбумина препятствует нарастанию гиперхолестеринемии, предполагают, что увеличение уровня холестерина в крови происходит компенсаторно вследствие уменьшения содержания альбуминов. Поскольку липидемию в эксперименте можно получить после перевязки мочеточников, высказывают мысль о том, что гиперхолестеринемия и липидемия при МИНС имеют почечное происхождение и зависят от повреждения интермедиарного обмена в ферментной системе канальцев. В генезе гиперлипидемии имеет значение также низкий уровень в крови лецитин-холестеринацетилтрансферазы, в больших количествах выделяющейся с мочой, и низкая активность липопротеидлипазы. При МИНС обычно диагностируют IIа и IIб типы гиперлипидемий.
Нарушения фосфорно-кальциевого обмена (гипокальциемия, остеопороз, остеомаляция) обусловлены нарушением функции почек, а также метаболизма витамина D.
Нарушения обмена железа и микроэлементов с низкими уровнями в крови как железа, так и цинка, меди, кобальта определяют в значительной степени склонность таких больных к анемиям, трофическим расстройствам кожи, задержке роста, а возможно — иммунодефицитам.
Вязкость крови при МИНС повышена за счёт гиперлипидемии, повышенной адгезивности тромбоцитов. В то же время уровни факторов свертывания крови (прокоагулянтов) и антисвертывания (антитромбин III, протеины С и S) снижены, что и объясняет сравнительно низкую частоту декомпенсированного ДВС-синдрома при МИНС.
Инфекции — прежде одно из очень частых осложнений МИНС. Особенно часто были перитониты, которые в большинстве случаев вызывались пневмококками, но в 25-50 % случаев — кишечной палочкой.
Диагноз
Характерная клинико-лабораторная картина МИНС в подавляющем большинстве случаев (90-95 %) у детей 2-7 лет позволяет поставить диагноз без биопсии почек. Хороший и быстрый ответ на терапию глюкокортикоидами подтверждает диагноз. В то же время, целесообразно у любого ребёнка с НС определить уровень IgE, выяснить наличие хронических персистирующих вирусных инфекций (гепатит B, цитомегалия, герпес-вирусные инфекции и др.), так как положительные результаты существенно дополняют и модифицируют терапию. О рецидивирующем течении НС свидетельствуют 2 рецидива в год, а о часто рецидивирующем — 3 и более рецидивов в год. Ремиссию констатируют при отсутствии протеинурии или её значении менее 4 мг/м2 в час и достижении уровня альбумина сыворотки 35 г/л. Биопсия показана детям с НС в возрасте до года и старше 12 лет, ибо у них очень мала частота МИНС.
Дифференциальная диагностика
Прежде всего Нефротический синдром необходимо дифференцировать от гломерулонефрита, СКВ, амилоидоза почек, интерстициального нефрита, тромбоза печеночных вен.
Лечение
- Диета — при нарушении функции почек ограничение приема жидкости, бессолевая, оптимальное по возрасту количество белка
- Инфузионная терапия (альбумин, реополиглюкин и др)
- Диуретики
мочегонные средства играют большую роль в лечении заболевания почек, однако при бесконтрольном и длительном их применении могут наступить резкая потеря натрия и снижение объема циркулирующей крови, гипокалиемия и метаболический ацидоз. Форсированный диурез с помощью больших доз диуретиков, как и ультрафильтрация, в условиях резкой гипоальбуминемии или выраженной почечной недостаточности может осложниться трудноуправляемым гиповолемическим шоком или дальнейшим снижением клубочковой фильтрации. Поэтому лечение диуретиками рекомендуется проводить максимально кратковременно и возобновлять только в случаях заметного снижения диуреза и нарастания отеков.
Для лечения нефротических отеков обычно применяют фуросемид — 20 — 400 мг внутрь, 20 — 1200 мг внутривенно), который оказывает достаточно мощное и быстрое, хотя и кратковременное, действие. Подобно фуросемиду действует и этакриновая кислота (50 — 200 мг/сут). Слабее действует гипотиазид, диуретический эффект которого наблюдается через 1 — 2 ч после приема 25 — 100 мг препарата. Важную роль в борьбе с отеками играют калийсберегающие диуретики — триамтерен, амилорид, особенно спиронолактоны (альдактон, верошпирон). Верошпирон применяют в дозе от 25 до 200—300 мг в сутки, Он наиболее эффектииен в сочетании с тиазидовыми диуретиками, фуросемидом. Отеки — при нефротическом синдроме, обусловленном амилоидозом, отличаются большой резистентностью к мочегонным средствам.
- Гепарин
- Антибактериальная терапия
- Кортикостероиды
Глюкокортикоиды (ГК) — преднизолон (ПЗ) (медопред, преднизол, преднизолон) и метилпреднизолон (МП) (метипред, солу-медрол) — являются первыми препаратами выбора при иммуносупрессивном лечении ГН. ГК влияют на перераспределение иммунокомпетентных и воспалительных клеток, препятствуя их поступлению в очаг воспаления, подавляют их чувствительность к медиаторам воспаления, угнетают секрецию таких провоспалительных цитокинов, как ФНО-α, ИЛ-1, ИЛ-2, ИЛ-6. ГК запускают процессы глюконеогенеза, способствуя включению антител в углеводный обмен и тем самым снижая их количество, тонизируют капиллярную стенку и снижают гиперемию за счёт активации и набухания перицитов. Введение больших доз ГК в виде «пульсов» МП угнетает образование ДНК-антител, приостанавливает образование иммунных комплексов, уменьшает их массу и способствует выходу из субэндотелиальных слоёв гломерулярной базельной мембраны, повышает клубочковую фильтрацию и почечный кровоток. ГК назначаются детям во всех случаях впервые возникшего НС, при рецидивах гормоночувствительного НС (как правило, НСМИ), при прогрессирующем течении ГН, в сочетании с другими иммунодепрессантами и пр.
На практике применяются три режима ГК терапии.
Постоянный пероральный прием ПЗ в дозе 1-2 мг/кг в 2-4 приема с учетом суточной активности коры надпочечников (максимальные дозы препарата в утренние часы с последующим снижением, последний прием не позднее 16.00) назначается в начале лечения для достижения ремиссии.
Альтернирующий (альтернативный) режим приема ПЗ используется при переходе на поддерживающую терапию. Заключается в приеме суточной дозы ПЗ через день, что позволяет при сохранении клинического эффекта значительно снизить побочные явления: острые — бессонницу, эйфорию, психоз, повышение аппетита; хронические — отеки, ожирение, миопатию, стрии, атрофию кожи, гирсутизм, aкне, остеопороз, катаракту, повышение АД, стероидный диабет; адреналовый криз — острую надпочечниковую недостаточность при резкой отмене препарата. Также существует вариант альтернирующего режима с приемом ПЗ ежедневно в течение 3 дней, затем 3-4 дня перерыва. По эффективности оба режима альтернирующего приема ПЗ примерно одинаковы.
Пульс-терапия МП используется для достижения очень высоких концентраций ГК в плазме. Заключается во внутривенном капельном введении в течение 20-40 мин около 30 мг/кг МП (не более 1 г на пульс) один раз в 48 ч. Количество введений, а также разовая и суммарная доза определяются выбранной схемой терапии данной патологии.
Побочные эффекты глюкокортикоидов могут быть следующими: бессонница, эйфория, психоз, повышение аппетита, отеки, ожирение, миопатия, стрии, атрофия кожи, гирсутизм, акне, остеопороз, катаракта, повышение АД, стероидный диабет, адреналовый криз (острая надпочечниковая недостаточность при резкой отмене препарата)
Цитостатические (цитотоксические) препараты (ЦС). Алкилирующие агенты: циклофосфамид (циклофосфан, цитоксан) и хлорамбуцил (хлорбутин, лейкеран) — нарушают деление клеток за счёт связывания с нуклеиновыми кислотами ядерной ДНК. Поступают в организм в неактивном состоянии, активизируются в печени. Действуют неизбирательно на все делящиеся клетки (неселективные иммуносупрессанты).
Циклофосфамид назначается внутрь или в виде «пульсов». Внутрь препарат назначается из расчёта 2,0-2,5 мг/кг/сут на 8-12 нед при лечении гормонозависимого или часторецидивирующего НС на фоне постепенного снижения дозы альтернирующего режима ПЗ, а также при гормонорезистентности.
Пульс-терапия циклофосфамидом проводится на фоне альтернирующего курса ПЗ при гормонозависимом и гормонорезистентном НС из расчёта 12-17 мг/кг внутривенно капельно. Количество «пульсов» и временной интервал между ними зависят от выбранной схемы терапии. Другой вариант — «пульс» 1 раз в месяц в течение 6-12 мес, в кумулятивной дозе не выше 250 мг/кг.
Хлорамбуцил принимается per os в дозе 0,15-0,2 мг/кг/сут в течение 8-10 нед для лечения гормонозависимого и часторецидивирующего НС, реже при гормонорезистентном НС, на фоне альтернирующего курса ПЗ с постепенным снижением.
Антиметаболиты — азатиоприн и метотрексат — в настоящее время при лечении ГН используются редко. Из побочных действий цитостатиков возможны: при применении циклофосфана — тошнота, рвота, лейкопения, геморрагический цистит, недостаточность гонад; хлорбутина — лёгочный фиброз, дерматит, судороги, гепатопатия, лейкопения.
Ссылки
Нефротический синдром — это… Что такое Нефротический синдром?
Нефротический синдром — состояние, характеризующееся генерализованными отеками, массивной протеинурией (выше 50 мг*кг/сут или выше 3,5 г/сутки), гипопротеинемией и гипоальбуминемией (менее 20 г/л), гиперлипидемией (холестерин выше 6,5 ммоль/л). Термин предложен Е.М. Тареевым в 1923 году.
Нефротический синдром (НС) — клинико-лабораторный симптомокомплекс, клинически характеризующийся периферическими или генерализованными отеками вплоть до асцита и анасарки, а лабораторно — протеинурией более 3,5 г/сут или более 50 мг/кг/сут, гипопротеинемией, гипоальбуминемией (ниже 20 г/л), диспротеинемией, гиперлипидемией и липидурией.
Классификация
Клинические формы НС
Первичный НС
1. Врожденный и инфантильный:
- врожденный “финского типа” с микрокистозом и “французского” типа с диффузными мезангиальными изменениями;
- НС с минимальными изменениями;
- НС с мезангиопролиферативными изменениями или с фокально-сегментарным гломерулосклерозом (ФСГС).
2. НС при первичном гломерулонефрите:
- НС с минимальными изменениями;
- НC с мембранозными или ФСГС, мембранозно-пролиферативными, мезангиопролиферативными, экстракапиллярными, с полулуниями, фибропластическими (склерозирующими) изменениями.
Вторичный НС
- Врожденный и инфантильный НС, ассоциативный с эндокринопатиями, кистозной гипоплазией легких и микрогирией, порэнцефалией, тромбозом почечных вен, внутриутробными инфекциями (сифилис, токсоплазмоз, цитомегалия, гепатит В, ВИЧ-инфекция и др.).
- НС при почечном дизэмбриогенезе, рефлюкс-нефропатии.
- НС при наследственных и хромосомных заболеваниях.
- НС при системных васкулитах и диффузных заболеваниях соединительной ткани, ревматизме, ревматоидном артрите.
- НС при острых и хронических инфекционных заболеваниях (гепатите В, энтеровирусных, герпес-вирусных, ВИЧ-инфекциях, сифилисе, туберкулёзе, дифтерии, инфекционном эндокардите), протозоозах (лейшманиоз, малярия), гельминтозах (аскаридоз, трихинеллез, описторхоз, эхинококкоз).
- НС при первичном, вторичном, наследственном амилоидозе.
- НС при саркоидозе, злокачественных опухолях (опухоль Вильмса), лейкозах, лимфосаркоме, лимфогранулематозе.
- НС при эндокринных заболеваниях (сахарный диабет, аутоиммунный тиреоидит), псориазе.
- НС при гемоглобинопатиях.
- НС при тромбозе почечных вен и гемолитико-уремическом синдроме.
- НС при укусах змей, пчел, ос, а также НС при введении вакцин и лекарственном поражении почек.
Стадии активности НС
- активная,
- неактивная — клинико-лабораторная ремиссия (полная или частичная, на или без поддерживающей терапии).
Тяжесть НС
- средней тяжести — гипоальбуминемия до 20 г/л;
- тяжелая — гипоальбуминемия ниже 20 г/л;
- крайне тяжелая — гипоальбуминемия ниже 10 г/л;
Вариант ответа на глюкокортикоидную терапию
- гормоночувствительный НС;
- гормонозависимый НС;
- гормонорезистентный НС.
Течение НС
- острое с исходом в ремиссию без последующих рецидивов;
- хроническое рецидивирующее, персистирующее, прогрессирующее;
- быстро прогрессирующее — подострое, злокачественное.
Функция почек
- сохранена — ПН0;
- нарушение функции почек в остром периоде;
Осложнения НС
- нефротический гиповолемический криз (шок, абдоминальный болевой синдром, рожеподобные эритемы), почечная эклампсия, тромбозы артериальные и венозные, ОПН, ХПН, вирусная, бактериальная, микотическая инфекции;
- осложнения, обусловленные проводимой терапией глюкокортикоидами, цитостатиками, антикоагулянтами, антиагрегантами; нестероидными противовоспалительными и 4-аминохинолинового ряда препаратами.
Гистологическая классификация
|
|
|
|
|
|
|
| Нефротический синдром |
|
|
|
|
| ||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||||||||||||||||||||||
|
|
| Болезнь минимальных изменений |
|
| Фокальный сегментарный гломерулосклероз |
|
| Мембранозная нефропатия |
|
| Мембранопролиферативный гломерулонефрит | |||||||||||||||||||||||||||||
Диагностика
Диагностика основывается на выявленных изменениях в анализах крови и мочи (протеинурия, гиперлипидемия, гипопротеинемия), на клинических данных. Клиника МИНС развертывается постепенно, причем преобладают экстраренальные симптомы, особенно отечный: появляются нарастающие отеки, вначале век, лица , поясничной области (в дальнейшем могут достигать степени анасарки — распространенный отек подкожной клетчатки), половых органов, асцит, гидроторакс, реже — гидроперикард. Характерна значительная гепатомегалия вследствие дистрофии печени. Кожа становится бледной (“перламутровая” бледность) при отсутствии анемии, сухой, появляются признаки гиповитаминозов А, С, В1, В2, дистрофические изменения. Могут наблюдаться ломкость и потускнение волос, на коже — трещины, из которых вытекает жидкость, striae distensae. Ребенок вялый, плохо ест, развивается одышка, тахикардия, систолический шум на верхушке (“гипопротеинемическая кардиопатия”).
Тяжелым осложнением у больных анасаркой, т. е. выраженной гипопротеинемией, может быть гиповолемический шок, которому предшествуют анорексия, рвота, резкие боли в животе. В наблюдениях Н. Д. Савенковой и А. В. Папаяна (1997) абдоминальный болевой синдром развивается у 23,5 % детей с гипоальбуминемией менее 15 г/л, а мигрирующие рожеподобные эритемы у 33,3 %, тромботические эпизоды у 12,5 %, ОПН у 3,3% детей с той же выраженностью гипоальбуминемии, тогда как нефротический гиповолемический шок отмечен лишь при уровне белка в сыворотке менее 10 г/л (у 5%). По мере схождения отеков становится все заметнее уменьшение массы скелетных мышц.
Артериальное кровяное давление обычно нормальное, лишь у до10% детей может быть кратковременная артериальная гипертензия. Уровень альбумина в сыворотке крови у таких детей менее 10 г/л.
Содержание общего белка в плазме (сыворотке) крови снижено иногда до 40 г/л.
Особенно резко снижена концентрация альбуминов и g-глобулина, тогда как уровень a2-глобулинов повышен, т. е. наблюдается резкая диспротеинемия. Сыворотка крови имеет молочный цвет, в ней находят высокий уровень липидов, холестерина, фибриногена. Уровень азотистых шлаков крови, как правило, нормальный, а содержание калия и натрия снижено. СОЭ резко увеличена (до 50–70 мм/час).
Ренальная симптоматика — олигурия с высокой относительной плотностью (1,026–1,030) мочи и выраженная протеинурия. При исследовании клубочковой фильтрации по эндогенному креатинину получают нормальные и даже повышенные показатели, но это ложное впечатление. Если учесть степень протеинурии, то клубочковая фильтрация при МИНС всегда снижена.
Клиническая картина, течение и исход НС, осложнившего диффузный гломерулонефрит, отличаются от клиники МИНС.
Мочевой синдром при МИНС слагается из следующих симптомов:
1. протеинурия,
2. олигурия с высокой относительной плотностью мочи,
3. цилиндрурия.
Протеинурия при МИНС, как правило, селективная, т. е. в моче находят белки плазмы крови с молекулярной массой менее 85 000 (альбумин и его полимеры, преальбумины, сидерофилин, гаптоглобин, трансферрин, a1- и b-глобулины, a1- и a2-гликопротеины и др.). В большинстве случаев у детей с селективной протеинурией прогноз лучше, и они чувствительны к терапии глюкокортикоидами. В генезе протеинурии имеет значение и нарушение реабсорбции белка в почечных канальцах. Неселективная протеинурия, когда в моче есть много крупномолекулярных белков, как правило, следствие фибропластического процесса, склероза, т. е. для МИНС нехарактерна. Напомним, что у здорового ребенка старше 4 лет в суточной моче может быть до 100–150 мг белка.
Олигурия связана с гиповолемией, гиперальдостеронизмом, поражением канальцев. Из-за протеинурии относительная плотность мочи увеличена, достигает 1,040. Высока активность в крови больных и АДГ.
Иногда при НС отмечается массивная лейкоцитурия, обусловленная иммунопатологическим процессом в почках. Лейкоцитурия чаще кратковременная и не связана с бактериальной инфекцией, т. е. пиелонефритом. Частота выявления лейкоцитурий и эритроцитурий при МИНС по данным разных авторов не превышает 10%.
При большом количестве белка в моче он может свернуться еще в канальцах, принимая их форму; на этот слепок наслаивается жироперерожденный почечный эпителий — так образуются гиалиновые, зернистые и восковые цилиндры.
Отеки. Массивная и длительная альбуминурия у больного с НС в конце концов неизбежно вызывает гипопротеинемию, так как потери белка превышают интенсивность его синтеза. Гипопротеинемия ведет к нарушению старлингова равновесия между гидродинамическим, фильтрационным и коллоидно-осмотическим давлением. Это приводит к преобладанию оттока жидкости из артериального русла над притоком. Отеки начинают появляться, когда уровень альбумина снижается ниже 27 г/л плазмы и развиваются всегда, если гипоальбуминемия достигает 18 г/л.
В патогенезе отеков важную роль играет и вторичный гиперальдостеронизм, типичный для НС. В результате его в организме задерживается натрий, а следовательно, и вода, хотя в крови имеется гипонатриемия.
Гипопротеинемия. Основной причиной гипопротеинемии у больных с НС являются большие потери альбуминов с мочой и перемещение их в ткани. Кроме того, имеют значение повышенный катаболизм альбуминов, нарушение белоксинтезирующей функции печени. Уменьшение содержания g-глобулинов в крови больных прежде всего с нарушением их синтеза. Гипоальбуминемия и гиповолемия, дефицит антикоагулянтов — антитромбина III и протеинов С и S, гиперфибриногенемия, гиперлипидемия создают угрозу для тромботических нарушений у больных МИНС.
Гиперлипидемия. Некоторые авторы связывают увеличение уровня липопротеинов низкой и очень низкой плотности, холестерина и липидов (свободные жирные кислоты, триглицериды, фосфолипиды и др.) при НС с нарушением функции печени, другие объясняют это явление понижением функции щитовидной железы. В связи с тем, что внутривенное введение раствора альбумина препятствует нарастанию гиперхолестеринемии, предполагают, что увеличение уровня холестерина в крови происходит компенсаторно вследствие уменьшения содержания альбуминов. Поскольку липидемию в эксперименте можно получить после перевязки мочеточников, высказывают мысль о том, что гиперхолестеринемия и липидемия при МИНС имеют почечное происхождение и зависят от повреждения интермедиарного обмена в ферментной системе канальцев. В генезе гиперлипидемии имеет значение также низкий уровень в крови лецитин-холестеринацетилтрансферазы, в больших количествах выделяющейся с мочой, и низкая активность липопротеидлипазы. При МИНС обычно диагностируют IIа и IIб типы гиперлипидемий.
Нарушения фосфорно-кальциевого обмена (гипокальциемия, остеопороз, остеомаляция) обусловлены нарушением функции почек, а также метаболизма витамина D.
Нарушения обмена железа и микроэлементов с низкими уровнями в крови как железа, так и цинка, меди, кобальта определяют в значительной степени склонность таких больных к анемиям, трофическим расстройствам кожи, задержке роста, а возможно — иммунодефицитам.
Вязкость крови при МИНС повышена за счет гиперлипидемии, повышенной адгезивности тромбоцитов. В то же время уровни факторов свертывания крови (прокоагулянтов) и антисвертывания (антитромбин III, протеины С и S) снижены, что и объясняет сравнительно низкую частоту декомпенсированного ДВС-синдрома при МИНС.
Инфекции — прежде одно из очень частых осложнений МИНС. Особенно часто были перитониты, которые в большинстве случаев вызывались пневмококками, но в 25–50% случаев — кишечной палочкой.
Диагноз
Характерная клинико-лабораторная картина МИНС в подавляющем большинстве случаев (90–95%) у детей 2–7 лет позволяет поставить диагноз без биопсии почек. Хороший и быстрый ответ на терапию глюкокортикоидами подтверждает диагноз. В то же время, целесообразно у любого ребенка с НС определить уровень IgE, выяснить наличие хронических персистирующих вирусных инфекций (гепатит В, цитомегалия, герпес-вирусные инфекции и др.), так как положительные результаты существенно дополняют и модифицируют терапию. О рецидивирующем течении НС свидетельствуют 2 рецидива в год, а о часто рецидивирующем — 3 и более рецидивов в год. Ремиссию констатируют при отсутствии протеинурии или ее значении менее 4 мг/м2 в час и достижении уровня альбумина сыворотки 35 г/л. Биопсия показана детям с НС в возрасте до года и старше 12 лет, ибо у них очень мала частота МИНС.
Дифференциальная диагностика
Прежде всего Нефротический синдром необходимо дифференцировать от гломерулонефрита, СКВ, амилоидоза почек, интерстициального нефрита, тромбоза печеночных вен.
Лечение
- Диета — при нарушении функции почек ограничение приема жидкости, бессолевая, оптимальное по возрасту количество белка
- Инфузионная терапия (альбумин, реополиглюкин и др)
- Диуретики
мочегонные средства играют большую роль в лечении заболевания почек, однако при бесконтрольном и длительном их применении могут наступить резкая потеря натрия и снижение объема циркулирующей крови, гипокалиемия и метаболический ацидоз. Форсированный диурез с помощью больших доз диуретиков, как и ультрафильтрация, в условиях резкой гипоальбуминемии или выраженной почечной недостаточности может осложниться трудноуправляемым гиповолемическим шоком или дальнейшим снижением клубочковой фильтрации. Поэтому лечение диуретиками рекомендуется проводить максимально кратковременно и возобновлять только в случаях заметного снижения диуреза и нарастания отеков.
Для лечения нефротических отеков обычно применяют фуросемид – 20 – 400 мг внутрь, 20 – 1200 мг внутривенно), который оказывает достаточно мощное и быстрое, хотя и кратковременное, действие. Подобно фуросемиду действует и этакриновая кислота (50 – 200 мг/сут). Слабее действует гипотиазид, диуретический эффект которого наблюдается через 1 – 2 ч после приема 25 – 100 мг препарата. Важную роль в борьбе с отеками играют калийсберегающие диуретики – триамтерен, амилорид, особенно спиронолактоны (альдактон, верошпирон). Верошпирон применяют в дозе от 25 до 200 – 300 мг в сутки, Он наиболее эффектииен в сочетании с тиазидовыми диуретиками, фуросемидом. Отеки – при нефротическом синдроме, обусловленном амилоидозом, отличаются большой резистентностью к мочегонным средствам.
- Гепарин
- Антибактериальная терапия
- Кортикостероиды
Глюкокортикоиды (ГК) — преднизолон (ПЗ) (медопред, преднизол, преднизолон) и метилпреднизолон (МП) (метипред, солу-медрол) — являются первыми препаратами выбора при иммуносупрессивном лечении ГН. ГК влияют на перераспределение иммунокомпетентных и воспалительных клеток, препятствуя их поступлению в очаг воспаления, подавляют их чувствительность к медиаторам воспаления, угнетают секрецию таких провоспалительных цитокинов, как ФНО-α, ИЛ-1, ИЛ-2, ИЛ-6. ГК запускают процессы глюконеогенеза, способствуя включению антител в углеводный обмен и тем самым снижая их количество, тонизируют капиллярную стенку и снижают гиперемию за счет активации и набухания перицитов. Введение больших доз ГК в виде «пульсов» МП угнетает образование ДНК-антител, приостанавливает образование иммунных комплексов, уменьшает их массу и способствует выходу из субэндотелиальных слоев гломерулярной базельной мембраны, повышает клубочковую фильтрацию и почечный кровоток. ГК назначаются детям во всех случаях впервые возникшего НС, при рецидивах гормоночувствительного НС (как правило, НСМИ), при прогрессирующем течении ГН, в сочетании с другими иммунодепрессантами и пр.
На практике применяются три режима ГК терапии.
Постоянный пероральный прием ПЗ в дозе 1–2 мг/кг в 2–4 приема с учетом суточной активности коры надпочечников (максимальные дозы препарата в утренние часы с последующим снижением, последний прием не позднее 16.00) назначается в начале лечения для достижения ремиссии.
Альтернирующий (альтернативный) режим приема ПЗ используется при переходе на поддерживающую терапию. Заключается в приеме суточной дозы ПЗ через день, что позволяет при сохранении клинического эффекта значительно снизить побочные явления: острые — бессонницу, эйфорию, психоз, повышение аппетита; хронические — отеки, ожирение, миопатию, стрии, атрофию кожи, гирсутизм, aкне, остеопороз, катаракту, повышение АД, стероидный диабет; адреналовый криз — острую надпочечниковую недостаточность при резкой отмене препарата. Также существует вариант альтернирующего режима с приемом ПЗ ежедневно в течение 3 дней, затем 3–4 дня перерыва. По эффективности оба режима альтернирующего приема ПЗ примерно одинаковы.
Пульс-терапия МП используется для достижения очень высоких концентраций ГК в плазме. Заключается во внутривенном капельном введении в течение 20–40 мин около 30 мг/кг МП (не более 1 г на пульс) один раз в 48 ч. Количество введений, а также разовая и суммарная доза определяются выбранной схемой терапии данной патологии.
Побочные эффекты глюкокортикоидов могут быть следующими: бессонница, эйфория, психоз, повышение аппетита, отеки, ожирение, миопатия, стрии, атрофия кожи, гирсутизм, акне, остеопороз, катаракта, повышение АД, стероидный диабет, адреналовый криз (острая надпочечниковая недостаточность при резкой отмене препарата)
Цитостатические (цитотоксические) препараты (ЦС). Алкилирующие агенты: циклофосфамид (циклофосфан, цитоксан) и хлорамбуцил (хлорбутин, лейкеран) — нарушают деление клеток за счет связывания с нуклеиновыми кислотами ядерной ДНК. Поступают в организм в неактивном состоянии, активизируются в печени. Действуют неизбирательно на все делящиеся клетки (неселективные иммуносупрессанты).
Циклофосфамид назначается внутрь или в виде «пульсов». Внутрь препарат назначается из расчета 2,0–2,5 мг/кг/сут на 8–12 нед при лечении гормонозависимого или часторецидивирующего НС на фоне постепенного снижения дозы альтернирующего режима ПЗ, а также при гормонорезистентности.
Пульс-терапия циклофосфамидом проводится на фоне альтернирующего курса ПЗ при гормонозависимом и гормонорезистентном НС из расчета 12–17 мг/кг внутривенно капельно. Количество «пульсов» и временной интервал между ними зависят от выбранной схемы терапии. Другой вариант — «пульс» 1 раз в месяц в течение 6–12 мес, в кумулятивной дозе не выше 250 мг/кг.
Хлорамбуцил принимается per os в дозе 0,15–0,2 мг/кг/сут в течение 8–10 нед для лечения гормонозависимого и часторецидивирующего НС, реже при гормонорезистентном НС, на фоне альтернирующего курса ПЗ с постепенным снижением.
Антиметаболиты — азатиоприн и метотрексат — в настоящее время при лечении ГН используются редко. Из побочных действий цитостатиков возможны: при применении циклофосфана — тошнота, рвота, лейкопения, геморрагический цистит, недостаточность гонад; хлорбутина — легочный фиброз, дерматит, судороги, гепатопатия, лейкопения.
Ссылки
Синдром нефротический – что это такое, причины, диагностика и лечение
Синдром нефротический – это целый комплекс состояний, которые в разной степени интенсивности проявляются у пациентов при нефрозе (патологиях почек). Основным проявлением считается протеинурия, при которой в моче присутствует большое количество белка ввиду нарушения обмена данного вещества. Также пациенты страдают от отеков.
Специалисты отмечают, что данное состояние развивается при наличии различных системных, урологических или инфекционных патологий. В современном мире этот термин заменен понятием нефроз, что используется также во Всемирной Организации Здравоохранения. Нефротический синдром – это состояние, встречающееся у людей в возрасте 30-40 лет, и в редких случаях у детей.
Общие сведения
Люди, не имеющие специального медицинского образования, нередко взаимозаменяют или путают нефротический синдром и нефритический. Однако эти понятия имеют определенные отличия. В первом случае подразумевается нарушение, а именно снижение, фильтрации почечных клубочков.
Состояние сопровождается яркой гематурией, протеинурией, а также в организме задерживается жидкость и соли. При нефритическом синдроме происходит развитие воспалительного процесса в почках. Сам по себе нефроз является комплексом патологических состояний этих органов.

Особенности патогенеза синдрома. Источник: ppt-online.org
Главной отличительной особенностью во втором случае является то, что в урине отсутствует примесь крови, но при этом имеются выраженные отеки. Также стоит отметить, что данные синдромы – это не диагноз, а лишь представление нескольких симптомов патологии.
Разбираясь с таким понятием как нефротический синдром, что это такое и каким бывает, нужно сказать, что он может являться первичным (врожденное или приобретенное поражение почек), а также вторичным, когда заболевание, ранее пролеченное, дало рецидив и развилось повторно.
Причины
В зависимости от того, на каком фоне возник нефротический синдром, лечение однозначно будет отличаться. При первичном типе основными провоцирующими факторами считаются: генетическая предрасположенность, мембранозная нефропатия, пиелонефрит, гломерулонефрит, первичный амилоидоз, гипернефрома и прочее.
Также в медицинской практике были зарегистрированы случаи возникновения рассматриваемого состояния после приема некоторых лекарственных препаратов, в результате отравления организма химическими веществами или аллергий. В тех ситуациях, когда медик не может точно назвать причин развития патологии, диагностируют идиопатическую форму, что бывает у детей от 1,5 до 5 лет.
Острый нефротический синдром с определенной частотностью выявляется у людей, которые склонны к аллергиям или же имеют аутоиммунные заболевания. Это обусловлено тем, что в крови человека формируются специфические клетки, которые создают определенный симбиоз между вирусами, бактериями и ДНК, антигенами.

Осложненное заболевание. Источник: ppt-online.org
В результате такой реакции начинает развиваться процесс воспалительного характера, негативно воздействующий на капилляры почечных клубочков. Уровень их проницаемости увеличивается, совместно с абсорбцией белка. Протеин проникает в мочу, при исследовании которой диагностируется выраженная протеинурия.
Патогенез нефротического синдрома, который не связан с аутоиммунными процессами, в настоящее время все еще находится на стадии изучения.
Симптоматика
Изучая такое состояние как нефротический синдром, что это такое и как проявляется, необходимо еще раз сказать – причин возникновения патологии очень много, но совместно с этим симптоматика практически всегда одинакова. В зависимости от характера течения провоцирующего заболевания, синдром может развиваться как длительное, так и короткое время.
Симптомы нефротический синдром имеет следующие:
- Выраженная отечность;
- Развитие анемии;
- Общее ухудшение состояния;
- Нарушения в процессе мочеиспускания.
Если сдать урину на лабораторное исследование, то в ней будет определяться показатель белка в диапазоне 3,5-5 г/сутки, при этом практически все протеины, а именно 90%, являются альбуминами. Если организм теряет вещество в значительной степени, то в составе сыворотки биологической жидкости его показатель не превышает 60 г/л.
Нефротический синдром острый проявляется отечностью, которая возникает в результате чрезмерного скопления жидкости в организме. Изначально данный симптом проявляется на лице, после чего распространяется на конечности и область поясничного отдела спины. На этом фоне у пациента может развиться асцит, гидроторакс, гидроперикард и анасарка.

Гидроперикард выступает в качестве тяжелого осложнения. Источник: present5.com
Главное отличие нефротического синдрома от нефритического – это протеинурия. Вне зависимости от состояния у человека могут начать появляться осложнения в виде общей слабости, понижения активности, утраты аппетита, чувства жажды, головной боли и одышки, судорог, расстройств желудочно-кишечного тракта.
Нефротический синдром причины возникновения имеет различные. Если своевременно не провести правильное лечение, то может произойти присоединение инфекции после приема иммуносуспрессивных лекарственных средств, случится отек мозга или нефротический криз, отек миокарда, тромбоз сосудов и стремительный атеросклероз.
Диагностика
Чтобы диагностировать нефрит синдром, необходимо провести лабораторные исследования. Если пациент считает, что у него имеются определенные проблемы в работе почек, то ему рекомендуется посетить уролога или нефролога. Изначально специалист выполнит визуальный осмотр, а также произведет сбор анамнеза.
Благодаря этим данным можно будет определить наличие или отсутствие возможных провоцирующих факторов, например, генетическая предрасположенность. Что касается визуального осмотра, то главный признак – это наличие отеков, побледневших кожных покровов, увеличенной печени.
В обязательном порядке назначается сдача общего и биохимического анализа крови и исследование мочи. Если прогрессирует воспалительный процесс, то по результатам будет определено увеличенное СОЭ, повышенная концентрация лейкоцитов, совместно с этим уровень гемоглобина снижен. Что касается крови, то в ней понижен альбумин, прослеживается гипопротеинемия, высокое содержание холестерина.
Нефроз почки подтверждается высоким уровнем плотности урины, повышением количества лейкоцитов, наличием цилиндров. При рассмотрении осадка имеются кристаллы, нейтральные липиды, большое содержание белка. Важно оценить и степень поражения почек. Для этого выполняют ЭКГ, ультразвуковой скрининг, допплерографию сосудов и сцинтиграфию почек.
Иногда может потребоваться уточнить первичный диагноз. В этом случае назначаются более информативные и узкоспециализированные исследования. Зачастую пациентам проводят биопсию почек, ангиографию или иммунологические исследования. Лишь после всего этого врач может точно сказать, что у пациента нефротический или нефритический синдром.
Лечение
В обязательном порядке весь терапевтический процесс должен контролировать опытный медицинский работник, в частности нефролог или уролог. Не исключено, что пациенту потребуется консультация ревматолога или эндокринолога. В зависимости от первопричины развития заболевания подход к лечению будет отличаться, но обязательно он комплексный.
При подозрении на нефротический синдром пациента обязательно госпитализируют. Это необходимо для того, чтобы определить истинный провоцирующий фактор, наличие различных осложнений, а также развитие анасарки. Больной должен соблюдать постельный режим, диету, придерживаться норм питья и принимать таблетки.
В зависимости от того, какие симптомы при нефротическом синдроме преобладают, врачи назначают лекарственные препараты различных фармакологических групп. В комплекс входят гормональные медикаменты, цитостатики, диуретики, антибиотики, а также иммунодепрессанты. Обязателен прием кортикостероидов для остановки прогрессирования воспалительного процесса, профилактики аллергии.

Пациентам обязательно назначается комплексная медикаментозная терапия. Источник: medistoriya.ru
Если диагностирован нефроз почки, тогда показан прием Преднизолона и Триамцинолона. В зависимости от характера течения патологии, а также индивидуальных особенностей организма пациента, продолжительность терапии определяется индивидуально. В среднем курс составляет от 6 до 20 недель.
Когда выполняется прием препаратов гормональной группы, с определенной периодичностью необходимо сдавать кровь и урину на исследование. Благодаря этому можно контролировать появление негативных реакций. В комплекс медикаментозной терапии вводят витамин D и кальций, чтобы не нарушался состав костной массы.
Цитостатические медикаменты работают таким образом, что прекращается деление и размножение патогенных клеток. Однако их назначение оправдано лишь в ситуации, когда у больного отмечается устойчивость к кортикостероидам, либо же имеются противопоказания к приему препаратов этой группы.
Чаще всего назначают такие цитостатики как Фуросемид и Индапамид. Если заболевание имеет аутоиммунную причину, тогда показаны иммунодепрессанты, например, Циклоспорин, Таклоримус или Азатиоприн. В ситуации, когда нефротический синдром сопровождается присоединением инфекции, необходим прием антибактериальных лекарственных средств.
Нередко у пациентов развивается артериальная гипертензия. Для ее устранения в комплекс терапии вводят ингибиторы АПФ, блокаторы ионов кальция и ангиотензинных рецепторов (Каптоприл, Амлодипин, Лозартан). Если имеется интоксикация организма или нарушен процесс кровообращения, назначают Альбумин и Реополиглюкан.
Диета
Особое внимание следует уделять правильному питанию при диагностированном нефротическом синдроме. Чтобы стабилизировать процесс обмена веществ, восстановить мочеиспускание, устранить отеки, рекомендуется диета стола №7. В сутки по правилам человек должен получать от 2700 до 3100 кКал.
Пища в организм должна поступать малыми порциями, но часто, поэтому кушать стоит 5-6 раз в течение суток. Категорически не допускается употреблять жареные блюда. Продукты следует варить, готовить на пару или запекать. Количество потребляемой соли сводится до 2-4 грамм в день, а лучше полностью ее исключить.

Во время терапии важно придерживаться правил диетического питания. Источник: mirfitness.info
Поскольку во время болезни человек теряет много протеина, пища должна быть белковой, из расчета 2 грамма вещества на каждый килограмм массы тела. При наличии в составе медикаментозной терапии диуретиков, рацион должен содержать продукты, обогащенные кальцием. В случае с большой концентрацией липидов в составе урины, из рациона убираются животные жиры (максимум 80 грамм в сутки). Углеводная порция продуктов не должна превышать 450 грамм.
В тех ситуациях когда у пациента сильно отекают верхние и нижние конечности, а также другие части тела, необходимо снизить суточное потребление жидкости. Рассчитывается это исходя из объема суточного диуреза, а количество выпитой воды должно быть больше на 30 мл.
Рассмотренное состояние считается комплексом симптомов, при этом оно диагностируется на фоне различных заболеваний. Чтобы получить благоприятный прогноз на выздоровление, необходимо своевременно диагностировать заболевание и провести правильное, полноценное лечение.
О патологии (видео)
Дата обновления: 17.09.2018, дата следующего обновления: 17.09.2021
Хронический нефритический синдром
Хронический нефритический синдром сопровождает заболевания разной этиологии, характеризующиеся диффузным склерозом клубочков почек и приводящие к ХПН. Клинически хронический нефритический синдром проявляется протеинурией, цилиндрурией, гематурией и артериальной гипертензией. Хронический нефритический синдром обычно развивается на фоне очагового или сегментарного склероза почки, мембранозного или мембранозно – пролиферативного гломерулонефрита.
При этом синдроме происходит увеличение внеклеточного материала (мезангиального матрикса, базальной мембраны клубочков, спавшихся капиллярных петель), а также отложение иммуноглобулинов в почечных клубочках. Поражение интерстиция почек характеризуется атрофией канальцев и выраженными склеротическими изменениями.
Хронический нефритический синдром развивается постепенно и может быть выявлен случайно при медицинском осмотре. Часто у больных субъективные жалобы в начале развития синдрома отсутствуют. При обследовании выявляют рецидивирующие эпизоды протеинурии и гематурии. В более тяжелых случаях могут быть выявлены признаки уремии – тошнота, рвота, одышка, кожный зуд, повышенная утомляемость. В более позднем периоде присоединяются отеки, артериальная гипертензия и азотемия.
В общем анализе мочи у больных выявляются протеинурия, гематурия, эритроцитарные и гиалиновые цилиндры. В крови отмечается повышение уровня азота, мочевины и креатинина, анемия, признаки метаболического ацидоза, гиперфосфатемия и другие признаки ХПН. Диагноз подтверждают биопсией почки.
Лечение в основном симптоматическое. Используются диета с ограничением натрия, антигипертензивные препараты. Проводится профилактика и лечение ХПН.
Отечный синдром
Патогенез почечных отеков сложен и складывается из ряда патофизиологических механизмов. Ведущая роль в их образовании принадлежит гипопротеинемии, гипоальбуминемии и диспротеинемии. Однако одними этими факторами патогенез почечных отеков не ограничивается. Вслед за снижением количества белка в крови последовательно включаются и другие механизмы: снижение онкотического давления сыворотки крови, уменьшение объема циркулирующей крови, нарушение сосудистой проницаемости в сторону ее повышения для воды и белков (за счет активации фермента гиалуронидазы, гипокальцемии, гистаминемии, деполимеризации мукополисахаридов межклеточного вещества тканей). Большое значение имеет уменьшение объема циркулирующей крови. Это приводит к возбуждению рецепторов сосудистой стенки и включению компенсаторных механизмов поддержания внутрисосудистого объема с их сложной гормональной регуляцией, в частности, усиленной выработкой в коре надпочечников альдостерона. Развивающийся вторичный альдостеронизм приводит к задержке в организме больных натрия, хлоридов и воды. Это ведет к увеличению секреции антидиуретического гормона, который усугубляет задержку воды за счет усиления ее канальцевой реабсорбции (схема 2).
Множественность патогенетических механизмов делает почечные отеки стойкими и распространенными. Они могут развиваться постепенно или же бурно, за одну ночь, достигать степени анасарки. Заметные вначале в области век, лица, поясничной области и половых органов, отеки при прогрессировании почечной патологии распространяются на всю подкожно-жировую клетчатку, растягивая кожу до образования дистензионных стрий. На этой стадии у большинства больных образуются транссудаты в серозных полостях: одно- и
Схема 2
Нефритический (острый нефритический) синдром
Симптомокомплекс «острого нефритического синдрома» (ОНС) характеризуется:
Гематурией (макро, микрогематурией)
Протеинурией (умеренной)
Отеками (чаще умеренными)
Артериальной гипертензией
Быстрым снижением скорости клубочковой фильтрации и азотемией
Наряду с полным клинико-лабораторным комплексом у некоторых больных могут быть только отдельные его признаки, например небольшие отеки под глазами и мочевой синдром. Отеки и гипертензия могут быть невыраженными и кратковременными признаками болезни. Причинами ОНС являются инфекции (острый постстрептококковый ГН, другие постинфекционные ГН). Необходимо дифференцировать с системными заболеваниями (СКВ, системные васкулиты, синдром Гудпасчера и др)
(табл. 3).
Таблица 3. Причины нефритического синдрома
Первичные ГН |
|
Системные заболевания | |
Острый тубулоинтерстициальный нефрит |
Патогенез главных симптомов – отека и гипертензии, связано с активацией ренин-ангиотензин-альдостероновой системы и задержкой соли и воды (рис.3).
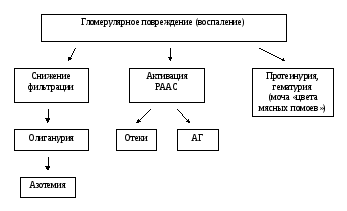
Рисунок 3. Патогенез нефритического синдрома.
На фоне имеющегося хронического гломерулонефрита поражение клубочков прогрессирует медленно с постепенным нарастанием протеинурии, гематурии, артериальной гипертензии и снижением функции почек (хроническая болезнь почек 1-5 ст).
Быстропрогрессируюший ГН (БПГН) – форма заболевания клубочков, при котором отмечается быстро нарастающая почечная недостаточность с олигурией в сочетании с протеинурией и гематурией, обычно без признаков нефротического синдрома. Морфологическим эквивалентом БПГН является экстракапиллярный ГН («полулуния» в клубочках в >50 % клубочков).
У детей и молодых взрослых наиболее частой причиной нефритического синдрома является постстрептококковый или постинфекционный ГН. При хроническом течении чаще всего выявляется IgA нефропатия. IgA нефропатия, начавшись как ОНС, может длительно протекать у детей и молодых гематурией и протеинурией. Но через длительное время (10 и более лет) на первый план выступает артериальная гипертензия и снижение функций почек вплоть до терминальной почечной недостаточности (ХБП 5 ст). Заболевание часто встречается в Казахстане и других странах Азии.
Осложнения острого нефритического синдрома – эклампсия и острая сердечная недостаточность, развивающиеся вследствие быстро нарастающей гипертензии и задержки натрия и воды. Наряду с преходящей азотемией, на фоне олиганурии может развиться тяжелая ОПН, требующая гемодиализного лечения.
Практически важно отличить острый нефритический синдром от БПГН с полулуниями (нужна биопсия почки), поскольку объем терапевтических мероприятий и прогноз при этих состояниях различен.
