Синдром Морганьи — Стюарта — Мореля — Википедия
Материал из Википедии — свободной энциклопедии
Синдром Морганьи — Стюарта — Мореля (метаболическая краниопатия) — состояние, связанное с широким спектром эндокринных проблем, включая сахарный и несахарный диабеты и гиперпаратиреоз[1]. Другие признаки и симптомы включают головную боль, головокружение, избыточное оволосение по мужскому типу, проблемы с менструацией, галакторею, ожирение, депрессию и эпилептические припадки[1][2]. Утолщение внутренней поверхности лобной части черепа является, как правило, начальной стадией заболевания, известного как hyperostosis frontalis interna (англ.)[1][3].
Синдром впервые был описан в 1765 году итальянским патологоанатомом Джованни Баттиста Морганьи[3] и позднее, в 1928 году, английским неврологом Дугласом Стюартом.[4] Швейцарский врач Фердинанд Морель (польск.)русск. (1888—1957) в 1930 году к клинической картине добавил нарушения менструального цикла и импотенцию
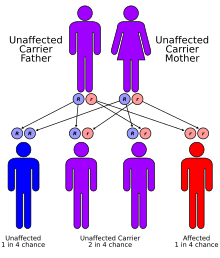
Этиология заболевания до конца не изучена, но оно связано с гипертрофией коры надпочечников в связи с гиперсекрецией адренокортикотропного гормона, влияние которой и обусловливает вторичные симптомы. Похожие симптомы были отмечены у женщин с повышенным пролактином на фоне гиперостоза лобной кости в 43 % случаев[7]. Ряд исследований показал аутосомно-доминантное наследование заболевания[8][9]. Заболевание характерно в основном для женщин.
Диагноз ставят на основе жалоб и клинической картины; также используют гистологические методы исследования. На рентгенограмме визуализируется утолщение лобной кости. Синдром Морганьи — Стюарта — Мореля дифференцируют в первую очередь от болезни Иценко — Кушинга и адипозогенитальной дистрофии.
Лечение симптоматическое. В редких случаях может быть хирургически удалена разросшаяся внутренняя часть лобной кости.
- ↑ 1 2 3 Nallegowda M., Singh U., Khanna M., Yadav S.L., Choudhary A.R., Thakar A. Morgagni Stewart Morel syndrome—additional features (англ.) // Neurology India (англ.)русск. : journal. — 2005. — March (vol. 53, no. 1). — P. 117—119. — DOI:10.4103/0028-3886.15078. — PMID 15805672.
- ↑ Psychiatria. Podręcznik dla studentów medycyny / Bilikiewicz A. — 3. — Warszawa: Lekarskie PZWL, 2006. — P. 150. — ISBN 83-200-3388-8.
- ↑ 1 2 She R., Szakacs J. Hyperostosis frontalis interna: case report and review of literature (англ.) // Annals of Clinical and Laboratory Science (англ.)русск. : journal. — 2004. — Vol. 34, no. 2. — P. 206—208. — PMID 15228235.
- ↑ Stewart RM. Localized cranial hyperostosis in insane (англ.) // Journal of Neurology and Psychopathology. — 1928. — Iss. 8. — No. 321.
- ↑ Morel F. L’hyperostose frontale interne. Syndrome de l’hyperostose frontale interne avec adipose et troubles cérébraux.. — Париж, 1930.
- ↑ Henschen F. Morgagni’s syndrome (англ.). — Jena, 1937.
- ↑ Hyperostosis frontalis, galactorrhoea/hyperprolactinaemia, and Morgagni-Stewart-Morel syndrome // The Lancet. — Elsevier, 1983-02-26. — Т. 1, вып. 8322. — С. 474. — PMID 6131191.
- ↑ Koller M.F., Papassotiropoulos A., Henke K., Behrends B., Noda S., Kratzer A., Hock C., Hofmann M. Evidence of a genetic basis of Morgagni-Stewart-Morel syndrome. A case report of identical twins (англ.) // Neuro-degenerative diseases : journal. — 2005. — Vol. 2. — P. 56—60. — DOI:10.1159/000089284. — PMID 16909048.
- ↑ Knies P.T., Le Fever H.E. Metabolic craniopathy: hyperostosis frontalis interna. (англ.) // Annals of Internal Medicine (англ.)русск. : journal. — 1941. — No. 14. — P. 1858—1892.
Мультисистемная атрофия — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 22 октября 2017; проверки требуют 6 правок. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 22 октября 2017; проверки требуют 6 правок.Мультисистемная атрофия — дегенеративное[1]неврологическое заболевание. Оно связано с дегенерацией нервных клеток определённых участков мозга. Эта клеточная дегенерация вызывает проблемы с движением, балансом и другими вегетативными функциями тела, такими как контроль за мочеиспусканием или регуляцией кровяного давления. Причины этого синдрома неизвестны и не было выявлено никаких конкретных факторов риска.[2] Около 55% случаев заболевания приходится на мужчин от 50-и до 60-и лет.[3]
Общая распространённость мультисистемной атрофии оценивается в 4,6 случаев на 100 000 человек.[4][5] Данное заболевание встречается чаще у мужчин, чем у женщин, и исследования показывают здесь соотношение в пределах от 1,4:1[6] с увеличением до 1,9:1.[7]
Мультисистемная атрофия характеризуется сочетанием следующих признаков, которые могут присутствовать в любой комбинации:[7][8]
При преобладании вегетативной недостаточности иногда используется термин синдром Шая — Дрейджера, хотя он официально уже не существует из-за изменений в терминологии.[9][10][11][12]
Также может существовать вариант с особенностями мультисистемной атрофии и деменцией с тельцами Леви.[13]
Первичные признаки[править | править код]
Наиболее распространённым первым признаком мультисистемной атрофии является появление «акинетически-ригидного синдрома» (то есть замедленность первоначальных движений, напоминающее болезнь Паркинсона), выявляется в 62% первичного осмотра. Другие общие признаки заболевания включают в себя проблемы с балансом (мозжечковая атаксия), выявляется в 22% на первичном осмотре, а затем мочеполовые проблемы (9%). Для мужчин первым признаком может служить эректильная дисфункция (неспособность достичь и поддерживать эрекцию). И мужчины, и женщины с данной болезнью часто испытывают проблемы с мочевым пузырём или неспособность к мочеиспусканию (недержание мочи). Примерно 1 из 5 больных мультисистемной атрофией страдают от падений в первый год проявления их заболевания. [3]
Симптомы прогрессирующего заболевания[править | править код]
У прогрессирующего заболевания преобладают три группы признаков. Это следующие:
- паркинсонизм (медленные, неловкие движения, письмо становится мелким и паучьеобразным)
- дисфункция мозжечка (затруднённость координации движений и баланса)
- вегетативная дисфункция (нарушение автоматических функций тела), включает:
Могут быть и другие симптомы, такие как двоение в глазах.[15]
Некоторые пациенты (в одном исследовании — 20%) в результате мультисистемной атрофии испытывают значительные когнитивные нарушения.[16]
Возможная связь была обнаружена с геном (Src гомология, содержащая 2 домена), превращающим 2 протеина, расположенных в дистальной 350-кб сублетомерной области 19-й хромосомы (19p13.3).[17]
Испанский терапевт Карлос Кристос, умерший с этим заболеванием в 2008 году, явился объектом документального фильма «Las Alas de la Vida» («Крылья жизни») о борьбе со своей болезнью. Хроники «Sophie’s Search for a Cure» также рассказывают о борьбе женщины с мультисистемной атрофией.
В 7ой серии («If I should fall from grace») 8ого сезона «Скорой помощи» (Emergency Room), у бабушки доктора Картера диагностируют это заболевание.
- ↑ Медицинский словарь Вебстера (англ.) (Проверено 25 мая 2012)
- ↑ National Study Seeks Cause of Baffling, Fatal Disorder Called Multiple System Atrophy (неопр.) (недоступная ссылка). UCSD Health Sciences Communications Healthbeat (5 декабря 2003). Дата обращения 1 июля 2008. Архивировано 22 сентября 2012 года.
- ↑ 1 2 Bensimon G., Ludolph A., Agid Y., Vidailhet M., Payan C., Leigh P.N. Riluzole treatment, survival and diagnostic criteria in Parkinson plus disorders: The NNIPPS Study (англ.) // Brain (англ.)русск. : journal. — Oxford University Press, 2008. — Vol. 132, no. Pt 1. — P. 156—171. — DOI:10.1093/brain/awn291. — PMID 19029129.
- ↑ Prevalence of rare diseases : Bibliographic data (неопр.) (PDF). Orphanet (ноябрь 2008). Дата обращения 24 мая 2012. Архивировано 22 сентября 2012 года. (Проверено 25 мая 2012)
- ↑ Bower J., Maraganore D., McDonnell S., Rocca W. Incidence of progressive supranuclear palsy and multiple system atrophy in Olmsted County, Minnesota, 1976 to 1990 (англ.) // Neurology (англ.)русск. : journal. — Wolters Kluwer (англ.)русск., 1997. — Vol. 49, no. 5. — P. 1284—1288. — PMID 9371909.
- ↑ Wenning G.K., Colosimo C., Geser F., Poewe W. Multiple system atrophy (англ.) // The Lancet. — Elsevier, 2004. — February (vol. 3, no. 2). — P. 93—103. — DOI:10.1016/S1474-4422(03)00662-8. — PMID 14747001.
Wenning G.K., Colosimo C., Geser F., Poewe W. Erratum (англ.) // The Lancet. — Elsevier, 2004. — March (vol. 3, no. 3). — P. 137. — DOI:10.1016/S1474-4422(04)00695-7. - ↑ 1 2 Swan L., Dupont J. Multiple system atrophy (англ.) // Physical Therapy (англ.)русск.. — 1999. — May (vol. 79, no. 5). — P. 488—494. — PMID 10331752.
- ↑ Burn D.J., Jaros E. Multiple system atrophy: cellular and molecular pathology (англ.) // Journal of Clinical Pathology (англ.)русск. : journal. — 2001. — December (vol. 54, no. 6). — P. 419—426. — PMID 11724918.
- ↑ Jellinger K.A. More frequent Lewy bodies but less frequent Alzheimer-type lesions in multiple system atrophy as compared to age-matched control brains (англ.) // Acta Neuropathologica (англ.)русск. : journal. — 2007. — Vol. 114, no. 3. — P. 299—303. — DOI:10.1007/s00401-007-0227-4. — PMID 17476513.
- ↑ The Consensus Committee of the American Autonomic Society and the American Academy of Neurology. Consensus statement on the definition of orthostatic hypotension, pure autonomic failure, and multiple system atrophy (англ.) // Neurology (англ.)русск. : journal. — Wolters Kluwer (англ.)русск., 1996. — Vol. 46, no. 5. — P. 1470. — PMID 8628505.
- ↑ Синдром Шая — Дрейджера на сайте «Who Named It?» (Кто назвал это?) (англ.) (Проверено 25 мая 2012)
- ↑ Shy G.M., Drager G.A. A neurological syndrome associated with orthostatic hypotension: a clinical-pathologic study (англ.) // JAMA Neurology (англ.)русск. : journal. — 1960. — Vol. 2. — P. 511—527. — PMID 14446364.
- ↑ Sikorska B., Papierz W., Preusser M., Liberski P.P., Budka H. Synucleinopathy with features of both multiple system atrophy and dementia with Lewy bodies (англ.) // Neuropathology and Applied Neurobiology (англ.)русск. : journal. — 2007. — Vol. 33, no. 1. — P. 126—129. — DOI:10.1111/j.1365-2990.2006.00817.x. — PMID 17239015.
- ↑ Gilman S., Koeppe R.A., Chervin R.D., et al. REM sleep behavior disorder is related to striatal monoaminergic deficit in MSA (англ.) // Neurology (англ.)русск. : journal. — Wolters Kluwer (англ.)русск., 2003. — July (vol. 61, no. 1). — P. 29—34. — PMID 12847152.
- ↑ NINDS NIH MSA with Orthostatic Hypotension (неопр.) (недоступная ссылка). Дата обращения 25 мая 2012. Архивировано 14 мая 2012 года.
- ↑ Brown R.G., Lacomblez L., Landwehrmeyer B.G., Bak T., Uttner I., Dubois B., Agid Y., Ludolph A., Bensimon G., Payan C., Leigh NP; for the NNIPPS Study Group. Cognitive impairment in patients with multiple system atrophy and progressive supranuclear palsy (англ.) // Brain (англ.)русск. : journal. — Oxford University Press, 2010. — August (vol. 133, no. Pt 8). — P. 2382—2393. — DOI:10.1093/brain/awq158. — PMID 20576697.
- ↑ Sasaki H., Emi M., Iijima H., et al. Copy number loss of (src homology 2 domain containing)-transforming protein 2 (SHC2) gene: discordant loss in monozygotic twins and frequent loss in patients with multiple system atrophy (англ.) // Molecular Brain (англ.)русск. : journal. — 2011. — Vol. 4. — P. 24. — DOI:10.1186/1756-6606-4-24. — PMID 21658278.
Синдром высокого мака — Википедия
Синдром высокого мака (англ. tall poppy syndrome) — термин, использующийся для описания социального феномена, выражающегося в неприязни и нападках на людей, которые выделяются из толпы благодаря своим редким талантам или выдающимся успехам. Схож с такими понятиями, как зависть, обида или ревность к чужому успеху. Термин широко используется во многих англоговорящих странах.
 Tarquinius Superbus Лоуренса Альма-Тадема, картина изображает царя при получении Лорел; маки на переднем плане относятся к аллегории «высокий мак»
Tarquinius Superbus Лоуренса Альма-Тадема, картина изображает царя при получении Лорел; маки на переднем плане относятся к аллегории «высокий мак»Концепция берёт своё начало в геродотовской «Истории» (книга 5, 92ф), аристотелевской «Политике» (1284a), а также в ливиевой «Истории Рима», Книге I.
 | Периандр послал глашатая к Фрасибулу спросить совета, как ему, установив самый надежный государственный строй, лучше всего управлять городом. Фрасибул же отправился с прибывшим от Периандра глашатаем за город и привел его на ниву. Проходя вместе с ним по полю, Фрасибул снова и снова переспрашивал о причине прибытия его из Коринфа. При этом тиран, видя возвышающиеся над другими колосья, все время обрывал их. Обрывая же колосья, он выбрасывал их, пока не уничтожил таким образом самую красивую и густую часть нивы. Так вот, проведя глашатая через поле и не дав никакого ответа, тиран отпустил его. По возвращении же глашатая в Коринф Периандр полюбопытствовал узнать ответ Фрасибула. А глашатай объявил, что не привез никакого ответа и удивляется, как это Периандр мог послать его за советом к такому безумному человеку, который опустошает собственную землю. Затем он рассказал, что видел у Фрасибула. Периандр же понял поступок Фрасибула, сообразив, что тот ему советует умертвить выдающихся граждан. Тогда-то тиран начал проявлять величайшую жестокость к своим гражданам. Всех уцелевших от казней и изгнаний Кипсела теперь прикончил Периандр.Геродот, «История», Книга 5, 92-f |  |
Аристотель использует рассказ Геродота в Политике, (1284a) с поменявшимися ролями, ссылаясь на совет Периандра Фрасибулу через глашатая. Вестник сообщает, что в ответ на его просьбу Периандр оторвал верхушку у мака, что Фрасибул понял так — «надо избавиться от именитых граждан».
Ещё одна ссылка на историю с маками есть у Ливия о тиране Рима Тарквинии Гордом. К тому приходит посланник от его сына Секста Тарквиния с вопросом, что делать дальше в Габии после завоевания там полноты власти. Вместо устного ответа посланнику Тарквиний идёт в свой огород, берёт палку и одним движением взмахивает ей в огороде, тем самым отре́зав головки самых высоких маков. Посланник, уставший ждать ответа, возвращается в Габию и рассказывает Сексту, что видел. Секст осознаёт, что отец хочет, чтобы он предал смерти всех выдающихся людей Габии, что Секст Тарквиний впоследствии и делает[1].
Фраза использовалась ещё в 1864 в связи со скандалом по поводу возведения в рыцарство[2]:
Сложнее найти обоснование для такой регалии как Орден подвязки. Но в таком случае он приобретает значение залога — потому что его всегда дают или людям исключительным, или же тем, чьё социальное положение достаточно сильно, чтобы вызывать опасения у нынешнего министра. Это своего рода публичное признание того, что вы являетесь высоким маком. И, поскольку в наши дни голову уже нельзя отрезать, то стоит вас купить.
Оригинальный текст (англ.)
It is more difficult to find a similar recommendation for such a dignity as the Order of the Garter. But then it derives a collateral value from the fact that it is always given either to people of singular distinction, or else to men whose social position is sufficient to make them formidable to the Minister of the day. It is a kind of public proclamation that you are a tall poppy and that, as in these days your head cannot be struck off, it is worth while to buy you.
Фраза была снова использована в 1904 году на дебатах в Парламенте Австралии[3]:
Сенатор О’Киф: Он посчитал нужным назначить Верховного Комиссара.
Сэр Уильям Зил: Ещё один высокий мак.
Сенатор О’Киф: Некоторые высокие маки были нужны.
Оригинальный текст (англ.)
Senator. O’Keefe– He regarded the appointment of a High Commissioner as necessary.Sir William Zeal– Another tall poppy.
Senator. O’Keefe– Some tall poppies were necessary.»
В 1930 году The Townsville Daily Bulletin писал[4]:
Несомненно, одним из зол Правительства в Австралии и Великобритании является вопиющая зарплата руководства: от высокого мака с 3 000 фунтов в год к рабочему с его 260 фунтами.
Оригинальный текст (англ.)
Unquestionably one of the evils of Government in Australia and Britain is the appalling cost of administration, from the tall poppy at £3,000 per annum to the toiler at £260.
Фраза стала более популярной в 1931 году — после того как премьер-министр Нового Южного Уэльса Джек Ланг[en] описал свою эгалитарную политику как «отрезание голов высоких маков». «Мистер Ланг присмирил высоких маков — тех, кого мог достать»[5]. «Высокие маки партии затаскали имя мистера Ланга по дебатам, чтобы размыть проблему»[6].
Фраза возродилась в 1984 году после публикации бестселлера Сьюзан Митчелл (Susan Mitchell) под названием «Высокие маки» (Tall Poppies). В книге она брала интервью у девяти успешных австралиек[7].
По поводу австралийского определения Питер Хартчет[en] из Sydney Morning Herald писал: «(Австралийские) граждане знают, что у некоторых из них больше власти и денег, чем у остальных… Но, согласно негласному национальному этическому коду, ни одному австралийцу не разрешено допускать мысль, что он или она лучше любого другого австралийца. Как это соблюдается? Незамедлительной корректировкой с помощью уравнивающих насмешек. У этого есть название — «синдром высокого мака». Самые высокие цветы в поле будут подрезаны по размеру остальных. Иногда это неправильно понимают… Австралийцев коробит вовсе не чужой успех — униженность, которую создают все те, кто набирает высоту»[8][9].
До того как стать премьер-министром, Маргарет Тэтчер объяснила свою философию американской аудитории — «пусть ваши маки растут в высоту», хотя сообщалось, что она добавила себе под нос: «если они, конечно, не работники профсоюза»[10].
Цитата была использована в США в политических целях, и любое утверждение о том, что Соединённое Королевство несёт в себе культуру синдрома высокого мака (в смысле крабового менталитета, как Австралия и Новая Зеландия[11]), оспаривалось[12].
Вера в силу данного культурного и социального феномена, а также в его отрицательную направленность, продиктована политикой. Синдром высокого мака имеет прямое отношение к тому, что некоторые консерваторы, либералы и либертарианцы называют «политикой зависти».
Некоторые комментаторы утверждают, что синдром высокого мака — это универсальный феномен, который является более распространённым в отдельных культурах. Понятия janteloven, или «закон Янте», в Скандинавии, и «я знал вашего отца» в Шотландии, очень похожи. Подобные явления существуют в Нидерландах (где оно называется maaiveldcultuur). В США, Бенджамин Франклин Фэйрлес, президент Американской сталелитейной корпорации (1950), раскритиковал такое поведение, заявив: «Вы не можете усилить одно за счет ослабления другого; и нельзя добавить роста гному, отрезав ногу великана».[13]
Престиж нулевой суммы[править | править код]
Некоторые социологи, в частности Макс Вебер, считают, что в определённых социальных группах приобретение престижа и власти — это игра с нулевой суммой, и эта ситуация может оправдывать неприязнь к «высоким макам».[14] В таких группах строго ограничены престиж, количество внимания, власти и материальных ресурсов, которые члены могут дать друг другу или разделить между собой. Статус — это относительная величина, поэтому для поднятия статуса одного другой человек должен упасть. Человек, у которого больше престижа, является препятствием для другого человека к получению престижа. И человек, который вдруг поднимается над остальными, становится откровенной угрозой для статуса других. Унижение или саботаж популярного члена группы понизит его статус, таким образом сделав агрессора возможной заменой в групповой иерархии.
Этот паттерн с нулевой суммой может быть найден в малых группах, характеризуемых фиксированной иерархией, и где практически нет прихода новых членов в группу. Примеры включают бедные американские общины и некоторые уличные банды.[15][16] Схожей концепцией является менталитет краба, в котором успешные члены бедной общины рассматриваются в качестве ущерба репутации других членов сообщества. Образ взят из наблюдения, что краб лезущий наверх из ведра (или, в других версиях, бочки) тянется вниз своими собратьями.
Недавнее исследование, проведённые в Университете Уаикато в Новой Зеландии, показывает, что культура синдрома высокого мака может привести к снижению средней производительности до 20 % для организации, а также объясняет, почему кибертравлю можно считать современным продолжением физического убийства времён царя Тарквиния[11].
- ↑ Livius, Titus. The Earliest Legends: 1.54 // The History of Rome, Vol. I (неопр.). — University of Virginia Library: Electronic Text Center.
- ↑ Empire (Sydney, NSW : 1850–1875, newspaper), 8 December 1864, p.5.
- ↑ The Examiner (Launceston, Tasmania), 10 March 1904, p.6.
- ↑ The Townsville Daily Bulletin, 8 October 1930, p.6.
- ↑ Canberra Times, 26 July 1934, p.1.
- ↑ Sydney Morning Herald, 12 August 1935, p.9.
- ↑ Mitchell, Susan. Tall poppies nine successful Australian women talk to Susan Mitchell (англ.). — Ringwood, Victoria, Australia Penguin Books, 1984. — ISBN 0140072101.
- ↑ Peter Hartcher (англ.). Sydney Morning Herald. Дата обращения 30 ноября 2017.
- ↑ Lack A. Poppy. — Reaktion Books, 2016. — С. 224. — ISBN 9781780237008.
- ↑ Comfort, Nicholas. Brewer’s Politics (неопр.). — Cassell, 1993. — С. 599. — ISBN 0-304-34085-5.
- ↑ 1 2 Spacey, S. Crab Mentality, Cyberbullying and ‘Name and Shame’ Rankings (англ.) // In Press : journal. — Waikato University, 2015.
- ↑ Spacey, S. (15 November 2015), Are you «Begging to be Cyberbullied» on LinkedIn?, <https://www.linkedin.com/pulse/you-begging-cyberbullied-your-linkedin-profile-simon-spacey>. Проверено 15 ноября 2015.
- ↑ 142. Benjamin Franklin Fairless (1890–1962). // Respectfully Quoted: A Dictionary of Quotations (англ.). — 1989.
- ↑ Ethics of Interpersonal Relationships (неопр.). — Karnac Books Ltd, 2009. — С. 346. — ISBN 978-1-85575-605-2.
- ↑ Relation of Threatened Egotism to Violence and Aggression: The Dark Side of High Self-Esteem (англ.) // Psychological Review (англ.)русск. : journal. — American Psychological Association; republished at Emotionalcompetency.com, 1996. — Vol. 103. — P. 5—33. — DOI:10.1037/0033-295x.103.1.5. — PMID 8650299.
- ↑ Baumeister, Roy (1997), Evil: Inside Human Violence and Cruelty, с. 167
Синдром Макла — Уэльса — Википедия
Синдром Макла — Уэльса (MWS) (иначе холодовой аутовоспалительный синдром) — это мутация в гене CIAS1 с развитием холодового аутовоспалительного синдрома. Является редким аутовоспалительным заболеванием наследственного характера (к 1998 году было описано не более 100 случаев[2]). Преимущественно этническая распространённость — народы Северной Европы. Тип наследования — аутосомно-доминантный. Генетическая основа — мутация гена CIAS1, расположенного на длинном плече 1-й хромосомы (1q44) и кодирующего белка криопирина (пурин-подобный белок преимущественно экспрессирующийся в лейкоцитах периферической крови)[3]. Данный белок является основной образуемого в клетке супрамолекулярного комплекса, называемого инфламмасомой, выполняющего функцию превращения pro-IL-1β (одного из основных провоспалительных цитокинов) в активную форму, а также принимающего участие в выполнении программы апоптоза. Холодовой аутовоспалительный синдром тесно связан с двумя другими синдромами: семейной холодовой крапивницы и мультисистемным воспалительным заболеванием неонатального возраста — фактически, все связаны с мутациями гена. В целом Синдром Макла — Уэльса относится к группе криопирин-связанных периодических синдромов (англ.)русск. (CAPS)[4].
Мутация в гене CIAS1 приводит к увеличению активности белка криопирин. Этот белок отвечает за реакцию организма на повреждение или инфекцию. В это время химическое вещество интерлейкин 1β вырабатывают иммунные клетки макрофаги. Это химическое вещество взаимодействует с рецептором на поверхности других клеток иммунной системы, они дают симптомы воспаления, такие как лихорадка, артрит и недомогание. Во время болезни, повышение активности криопирина приводит к увеличению интерлейкина 1β. Это приводит к воспалению во всём теле с соответствующими симптомами[5].
Первые симптомы появляются после переохлаждения и переутомления через 1,5 — 2 часа: сыпь, жар (лихорадка). В основном симптомы идут в такой последовательности:
- Периодическая уртикарная сыпь
- Жар (лихорадка)
- Отёк суставов
- Конъюнктивит
- Лейкоцитоз
- Потеря слуха (из-за атрофии слухового нерва)
- Амилоидоз почек
Обычно смерть наступает из-за амилоидоза почек или остановки сердца.
Впервые болезнь была описана в 1962 году британскими исследователями Томасом Джеймсом Маклом (англ. Thomas James Muckle) и Майклом Верноном Уэльсом (англ. Michael Vernon Wells)[6].
Макл и Уэльс описали семью из Дербишира, в которой крапивница, прогрессирующая перцептивная глухота и амилоидоз почек были объединены в преимущественно наследственный синдром. Новооткрытым заболеванием были затронуты пять поколений семьи. Вскрытие двух пациентов показало отсутствие Кортиева органа, атрофию улиткового нерва и амилоидную инфильтрацию почек. В 1969 году американский невролог Джозеф Ти. Блек (англ. Joseph T. Black) описал пораженных болезнью лиц в трех поколениях одной семьи и отметил боли в конечностях (артралгия), как один из симптомов[7].
Ревматолог Бертело и соавторы в 1994 году исследовали четыре поколения семьи, в которой у семи членов проявились различные признаки синдрома, связанные с биполярным афтозом (щечной и генитальной молочницей) в пяти случаях и цистинурию в одном, двое других родственников страдали от ихтиоза. Никаких признаков амилоидоза обнаружено не было[8].
В 1996 году исследователи сообщили о трех поколениях семьи, в которой три сестры страдали интермиттирующей (эпизодической) крапивницей, полиартралгией и периодическими болями в животе. У все троих наблюдавшихся диагностирована микрогематурия, но никаких доказательств амилоидоза почек. Микроскопическая гематурия была установлена также у их матери и дочери одной из них. Ни один из пациентов не имел признаков глухоты[9].
Гербиг с соавторами в 1998 году описали[10] 21-летняя женщину и её отца, страдавших от Синдрома Макла — Уэльса, у наблюдаемых задокументированы повышенные сывороточные уровни ИЛ-6 во время вспышки крапивницы. Симптомы и высокий уровень ИЛ-6 показали циркадный паттерн у дочери. Её крапивница преимущественно локализовалась на туловище и конечностях, была незудящая, и, казалось, следовала «внутренним часам» начинаясь после полудня, достигая кульминации к позднему вечеру, и затем исчезая в течение ночи. Все это часто сопровождалось лихорадкой, ознобами, спазмом кожных мышц, общим недомоганием и болями в конечностях, симптомы, как правило, чаще всего фиксировались по понедельникам. Утром не было абсолютно никаких симптомов. Пациент не может определенно выделить факторы приводящие к этому за исключением усталости и перегрева вызванного солнечной погодой. В возрасте 7 лет аудиограмма показала умеренную нейросенсорную тугоухость, но родители отказались от дальнейших исследований, поскольку отец, страдавший от аналогичных симптомов и показывавший постоянно повышенную скорость оседания эритроцитов, напротив чувствовал себя совершенно здоровым.
Исследовательская группа Гербига также заявила, что только около 100 случаев синдрома совмещающего симптомы крапивницы глухоты и амилоидоза были зарегистрированы после описания синдрома Маклом и Уэльсом в 1962 году у 9 членов семьи из Дербишира. Они предположили, что некоторые из спорадических случаев, в частности вероятно, были смешаны с другими расстройствами, к примеру, синдромом CINCA (хронический детский кожно-артикулярно-неврологический синдром)[11]. Они также указали на спорадический случай, описанный Линке и соавторами[12] в 1983 году в качестве вероятного примера к выдвинутой Маклом и Уэльсом конечной симптоматике синдрома[10].
Либерман и соавторы описали гистологические особенности поражения кожи в спорадическом случае синдрома Макла — Уэльса. Так пациент, 54-летний мужчина, имел бессимптомные, затухающие очаги высыпаний начиная с возраста 2 месяцев, часто сопровождавшиеся ознобом, артралгией и на поздних стадиях — болями в нижних конечностях. Его детство было осложнено стойкими лимфаденопатией, гепатоспленомегалией, отеком диска зрительного нерва, анемией, «подагрическими» артритами и увеличением скорости оседания эритроцитов без видимой причины. В возрасте 19 лет перцептивная тугоухость привела к необходимости ношения двухсторонних слуховых аппаратов, кроме того был прописан курс антибиотиков против почечной инфекции. В период с 20 до 40 лет у него было несколько эпизодов культуро-отрицательного эозинофильного менингита с комой или судорогами. Установлено, что это была частичная реакция на кортикостероиды, и следовательно, исследователи предположили васкулит центральной нервной системы. Мозговая биопсия показала хронический менингит с васкулярной астроглиальной реакцией без васкулита. В период с 30 до 50 лет он страдал рецидивными болями в животе, обильным поносом и нефротическим синдромом, требующим перитонеального диализа. Ректальная и почечная биопсии показали амилоидные отложения. В возрасте 50 лет ему была сделана двухсторонняя трансплантация роговицы по причине ленточной кератопатии (кальцификации роговицы). В возрасте 54 лет, несмотря на противовоспалительную терапию, в том числе преднизолоном, азатиоприном и циклоспорином, его состояние постепенно ухудшилось, и он умер во время гипотензивного эпизода. Семейный анамнез был отрицательным для того что бы сделать вывод о соответствии симптомам синдрома Макла — Уэльса. Диагноз синдром Макла — Уэльса был поставлен лишь незадолго до смерти пациента[13].
В клинической практике отмечаются приступы лихорадки, сопровождающиеся артралгией, уртикарной сыпью (без зуда), явлениями конъюнктивита, реже — микрогематурия, лимфаденопатия, гепатоспленомегалия, боли в животе. Иногда встречаются другие симптомы, характерные для родственных синдромов CAPS: реакция на холод, неврологические проявления (галлюцинации). У больных выявляют положительный тест ревматических розеток, увеличение содержания IgG и IgA, повышение СОЭ, лейкоцитоз. При лабораторном исследовании во время приступа определяется повышение С-реактивного белка, лейкоцитоз. Прогноз определяется глухотой, развивающейся вследствие атрофии слухового нерва, симптомами прогрессирующего мультиорганного амилоидоза АА типа.
В 14 серии 7 сезона телесериала «Доктор Хаус» с этим синдромом обратился пациент.
- ↑ Monarch Disease Ontology release 2018-06-29sonu — 2018-06-29 — 2018.
- ↑ Gerbig, A. W., Dahinden, C. A., Mullis, P., Hunziker, T. Circadian elevation of IL-6 levels in Muckle-Wells syndrome: a disorder of the neuro-immune axis? // Quarterly Journal of Medicine. — 91: 489—492, 1998. — PMID 9797932
- ↑ Cuisset, L., Drenth, J. P. H., Berthelot, J.-M., Meyrier, A., Vaudour, G., Watts, R. A., Scott, D. G. I., Nicholls, A., Pavek, S., Vasseur, C., Beckmann, J. S., Delpech, M., Grateau, G. Genetic linkage of the Muckle-Wells syndrome to chromosome 1q44. // American Journal of Human Genetics. — 65: 1054—1059, 1999. — PMID 10486324
- ↑ Hoffman, H. M., Mueller, J. L., Broide, D. H., Wanderer, A. A., Kolodner, R. D. Mutation of a new gene encoding a putative pyrin-like protein causes familial cold autoinflammatory syndrome and Muckle-Wells syndrome. // Nature Genetics. — 29: 301—305, 2001. — PMID 11687797
- ↑ Mariathasan S, Weiss DS, Newton K, McBride J, O’Rourke K, Roose-Girma M, Lee WP, Weinrauch Y, Monack DM, Dixit VM. Cryopyrin activates the inflammasome in response to toxins and ATP. // Nature. — 440 (7081): 228-32. (9 March 2006). — PMID 16407890
- ↑ Muckle, T. J., Wells, M. Urticaria, deafness and amyloidosis: a new heredo-familial syndrome. // Quarterly Journal of Medicine. — 31: 235—248, 1962. — PMID 14476827
- ↑ Black, J. T. Amyloidosis, deafness, urticaria and limb pains: a hereditary syndrome. // Annals of Internal Medicine. — 70: 989—994, 1969. — PMID 5769632
- ↑ Berthelot, J.-M., Maugars, Y., Robillard, N., Pascal, O., Stalder, J.-F., David, A., Prost, A. Autosomal dominant Muckle-Wells syndrome associated with cystinuria, ichthyosis, and aphthosis in a four-generation family. // American Journal of Medical Genetics. — 53: 72-74, 1994. — PMID 7802040
- ↑ Throssell, D., Feehally, J., Trembath, R., Walls, J. Urticaria, arthralgia, and nephropathy without amyloidosis: another variant of the Muckle-Wells syndrome? // Clinical Genetics. — 49: 130—133, 1996. — PMID 8737977
- ↑ 1 2 Gerbig, A. W., Dahinden, C. A., Mullis, P., Hunziker, T. Circadian elevation of IL-6 levels in Muckle-Wells syndrome: a disorder of the neuro-immune axis? // Quarterly Journal of Medicine. — 1998 Jul;91(7): 489—492. — PMID 9797932
- ↑ Prieur, A. M., Griscelli, C., Lampert, F., Truckenbrodt, H., Guggenheim, M. A., Lovell, D. J., Pelkonnen, P., Chevrant-Breton, J., Ansell, B. M. A chronic, infantile, neurological, cutaneous and articular (CINCA) syndrome: a specific entity analysed in 30 patients. // Scandinavian Journal of Rheumatology — Supplement. — 66: 57-68, 1987. — PMID 3482735
- ↑ Linke, R. P., Heilmann, K. L., Nathrath, W. B. J., Eulitz, M. Identification of amyloid A protein in a sporadic Muckle-Wells syndrome: N-terminal amino acid sequence after isolation from formalin-fixed tissue. //Laboratory Investigation. — 48: 698—704, 1983. — PMID 6406764
- ↑ Lieberman, A., Grossman, M. E., Silvers, D. N. Muckle-Wells syndrome: case report and review of cutaneous pathology. // Journal of the American Academy of Dermatology. — 39: 290—291, 1998. — PMID 9704852
- ↑ Rynne M, MacLean C, Bybee A, McDermott MF, Emery P. Hearing improvement in a patient with variant Muckle‐Wells syndrome in response to interleukin 1 receptor antagonism. // Annals of the rheumatic diseases. — 2006 April; 65(4): 533-4. — PMC 1798106. — PMID 16531551
Синдром Альстрёма — Википедия
Синдро́м Альстрёма (англ. Alström syndrome) — генетическая патология человека, относящаяся к группе цилиопатий. Характеризуется пигментной дегенерацией сетчатки, ожирением, прогрессирующей нейросенсорной глухотой, дилятационной кардиомиопатией, сахарным диабетом и нефропатией. Впервые описан в 1959 году шведским психиатром Карлом-Генри Альстрёмом (англ.)русск..
Описано около 300 случаев синдрома Альстрёма. Частота синдрома Альстрёма наивысшая во французской популяции и среди некоторых других географических и этнических изолятов.
Единственный ген, известный на сегодня, связанный с синдромом Альстрёма — это ALMS1. Молекулярным методом мутация подтверждается у 20—45 % пациентов. Ген картирован 2рр.13.
Характерна значительная вариабельность клинической картины даже среди сиблингов. Дети при рождении имеют нормальную массу тела, но на протяжении 1-го года жизни появляется ожирение. Индекс массы тела — больше 95 центилей. Для детей с синдромом Альстрёма характерен быстрый темп роста до пубертатного периода и опережение костного возраста. Раннее закрытие зон роста обусловливает низкий конечный рост (< 5 перцентиля) у 85 % пациентов. Формируется сколиоз или кифоз.
Практически с первых месяцев жизни наблюдаются нистагм, фотодисфория, ретинит, снижение центрального и периферического зрения[1]. Применение электроретинографии позволяет обнаружить прогрессирующее ухудшение функции палочек и колбочек. Также диагностируется пигментная дегенерация сетчатки. Возможно развитие полной слепоты уже в детском возрасте, умственное развитие не страдает[1].
Осмотр глазного дна в первые года может не выявить патологии, либо может выявить бледный диск зрительного нерва и сужение сосудов сетчатки. Позднее появляются прогрессирующая дистрофия нейроэпителия с атрофией и пигментной инфильтрацией внутренних пластов сетчатки, которые к 7-летнему возрасту могут привести к слепоте, катаракте.
Нейросенсорная глухота в первом десятилетии у 70 % больных прогрессирует от умеренной до тяжелой (40—70 дБ). От 10 до 30 лет наблюдается значительное снижение слуха.
Дилятационная кардиомиопатия с манифестацией в детском или подростковом периоде наблюдается более чем у 60 % случаев. На некоторых этапах жизни приводит к возникновению сердечной недостаточности и смерти. Обычно клиника дилятационной кардиомиопатии, и её результата — сердечной недостаточности зависит от возраста их проявления. Около 80 % больных переносят дилятационную кардиомиопатию в молодом возрасте. Из них 10 % имеют рецидивы, которые прогрессируют в более позднем возрасте.
Синдром инсулинорезистентности диагностируют при наличии следующих критериев (не менее чем 3 из 4):
Часто с инсулинорезистентностью связан чёрный акантоз (acanthosis nigricans).
Задержка умственного развития описана у некоторых пациентов, хотя как правило не достигает глубокой степени. Эти дети имеют трудности в обучении, восприятии и речевом развитии, задержку формирования моторных навыков.
Сахарный диабет — это результат инсулинорезистентности. Как правило это диабет 2 типа.
Гипогонадотропный гипогонадизм, гирсутизм у девочек, поликистоз яичников, в более позднем возрасте эндометриоз. Наружные половые органы сформированы правильно. Но все пациенты с синдромом Альстрёма нефертильны.
Урологические/почечные нарушения встречаются у 50 % пациентов, характеризуются отсутствием координации деятельности мочевого пузыря: недержанием мочи, большими интервалами между мочеиспусканиями.
Печёночные дисфункции — в крови увеличиваются трансаминазы, чаще наблюдается жировая дистрофия, фиброз.
В некоторых случаях развивается резистентный к АДГ несахарный диабет, у мужчин — гипогонадотропный гипогонадизм (при биопсии яичек обнаруживают аплазию герминативных клеток, склероз семенных канальцев)[1].
Диагноз синдрома Альстрёма в значительной мере базируется на наличии кардинальных клинических признаков, которые могут проявиться на протяжении всей жизни:
Лабораторные данные: гиперурикемия, гипертриглицеридемия и аминоацидурия[1].
Проводят с синдромом Барде — Бидля. Главное отличие — в дебюте заболевания. Синдром Альстрёма начинается около 2-х лет, а синдром Барде — Бидля — около 8 летнего возраста. Но также есть и иные отличия. Также проводят дифдиагностику с вродженным амаврозом Лебера (LCA), ранней дилатационной кардиомиопатией, наследственными митохондриальными болезнями.
Специфического лечения нет. При фотодисфории — использование цветных линз, при ожирении — лечебное питание по общепринятым методикам, регулярные физические нагрузки, при нейросенсорной глухоте — хирургическая коррекция у пациентов с экссудативным отитом, цифровые слуховые аппараты, при дилятационной кардиомиопатии — ингибиторы АПФ, мочегонные, при развитии сердечной недостаточности — сердечные гликозиды, адреноблокаторы, при сахарном диабете — лечение по принятой схеме, при гипертриглицеридемии — высокие дозы статинов, никотиновая кислота, и другая симптоматическая терапия.
- ↑ 1 2 3 4 5 Симптомы и синдромы в эндокринологии / Под ред. Ю. И. Караченцева. — 1-е изд. — Х.: ООО «С.А.М.», Харьков, 2006. — С. 24. — 227 с. — (Справочное пособие). — 1000 экз. — ISBN 978-966-8591-14-3.
МОРГАНЬИ СИНДРОМ — Большая Медицинская Энциклопедия
МОРГАНЬИ СИНДРОМ (G. В. Morgagni, итал. врач и анатом, 1682 — 1771; син.: гиперостотический эндокраниоз Морганьи, метаболическая краниопатия, синдром Стюарта — Мореля, синдром Мура — Карра, синдром Морганьи — Стюарта — Мореля, эндокраниоз, синдром внутреннего лобного гиперостоза) — клинический синдром, характеризующийся наличием гиперостоза внутренней пластинки лобной кости и нарушениями в системе гипоталамус — гипофиз — эндокринные железы. Первое описание дано в 1761 г. Дж. Морганьи. В 1937 г. Хеншен (D. Henshen) охарактеризовал патогенез и основные клин, симптомы синдрома и назвал его синдромом Морганьи. М. с. наблюдается чаще у женщин в детородном возрасте; среди больных с неопухолевыми заболеваниями гипоталамо-гипофизарной области он составляет по данным разных ученых от 7 до 50%.
Этиология и патогенез
Большинство исследователей связывают проявление всех симптомов М. с. с нарушениями в системе гипоталамус — гипофиз — эндокринные железы. Тонзиллогенная интоксикация, острые инфекционные болезни, инфицированные роды и аборты, реже — черепно-мозговая травма могут быть провоцирующими факторами, к-рые вызывают изменения в системе гипоталамус — гипофиз — эндокринные железы. Внутренний лобный гиперостоз рассматривается как местный процесс, сопровождающийся отложением солей кальция в тканях; патогенез его неясен.
Клиническая картина
Основные клин, симптомы при М.С.— гиперостоз внутренней пластинки лобной кости, ожирение (по гипоталамическому типу с равномерным отложением жира) и гирсутизм (см.)— составляют классическую триаду Морганьи; одновременно могут наблюдаться расстройства: эмоционально-психические (эмоциональная неустойчивость, снижение памяти, расстройство сна, повышенная утомляемость), вегетативные и неврологические (булимия, полидипсия, птоз, нарушения конвергенции глаз, головные боли, головокружение, потливость, трофические изменения кожи и слизистых оболочек половых органов, повышение АД, иногда эпилептиформные припадки) и нейроэндокринные (нарушения углеводного обмена, овариально-менструальной функции по типу опсо- и аменореи, бесплодие). Обмен кальция и фосфора при этом не нарушен. Центральный механизм нарушения функции яичников подтверждается наличием изменений соотношения уровня экскреции гонадотропинов — фолликулостимулирующего гормона (ФСГ) и лютеинизирующего гормона (ЛГ) гипофиза. При опсоменорее (см. Менструальный цикл) уровень экскреции ФСГ и ЛГ снижен, но отмечены циклические колебания этого уровня. При длительной аменорее экскреция как ФСГ, так и ЛГ резко снижена и отсутствуют выраженные колебания в количественной экскреции гонадотропинов.
Для выявления функц, состояния мозга при М. с. используется электроэнцефалография (см.), при этом у нек-рых больных на ЭЭГ в отведениях от лобных и прецентральных отделов головного мозга преобладает отчетливо выраженная тэта-активность с частотой 5—7 колебаний в 1 секунду; реакция депрессии основного ритма на непрерывный свет ослаблена. У других больных имеются выраженные явления раздражения с преобладанием частой активности во всех отведениях от коры головного мозга. У часта больных отклонения обнаруживаются только под воздействием функц, нагрузок. Установлена определенная зависимость между симптомами заболевания и данными ЭЭГ. При булимии (см.), полидипсии (см.), трофических изменениях кожи и слизистых оболочек, эмоционально-психических расстройствах, головной боли на ЭЭГ обнаруживают нарушения в диэнцефальной области. При стволовых нарушениях — умеренный птоз (см.), нарушение конвергенции глаз (см.) — и головных болях на ЭЭГ преобладают изменения в ретикулярной формации среднего мозга. При сочетании перечисленных симптомов с повышением АД и нарушением углеводного обмена на ЭЭГ имеются нарушения в мезо- и диэнцефальных структурах.
Выраженность клин. картины, как правило, не связана с возрастом и длительностью заболевания, а зависит от функц, активности гипофиза.
Диагноз
 Рентгенограмма черепа (боковая проекция) больного с синдромом Морганьи: резкое утолщение лобной кости (указано стрелкой) за счет гиперостоза внутренней пластинки.
Рентгенограмма черепа (боковая проекция) больного с синдромом Морганьи: резкое утолщение лобной кости (указано стрелкой) за счет гиперостоза внутренней пластинки.Диагноз устанавливают на основании клин, картины и данных ЭЭГ. Для уточнения диагноза необходимо рентгенол, исследование, т. к. гиперостоз внутренней пластинки лобной кости (рис.), являющийся обязательным признаком этого синдрома, может быть выявлен только при краниографии (см.). О локализации и протяженности изменений судят по снимкам черепа в боковой проекции. Как правило, дополнительные костные разрастания в виде отдельных узлов или разлитого характера располагаются в средней и нижней третях чешуи лобной кости, изредка — и в теменных костях. По сравнению с неизмененными участками кость может быть утолщена в 2—3 раза. Этим изменениям могут сопутствовать различной формы и размеров очаги обызвествления твердой мозговой оболочки в зоне, примыкающей к внутренней поверхности лобной кости.
При длительном течении заболевания и резко выраженном гиперостозе лобной кости из-за уменьшения объема черепа на краниограммах могут быть обнаружены признаки повышения внутричерепного давления (усиление пальцевых вдавлений, углубление борозд синусов и др.).
Дифференциальный диагноз проводят с адипозо-генитальной дистрофией (см.), болезнью Иценко — Кушинга (см. Иценко — Кушинга болезнь), алиментарным ожирением (см.).
Лечение
Лечение заключается в проведении рассасывающей и дегидратационной терапии (см.), к-рая устраняет или смягчает симптомы гипоталамо-гипофизарной патологии. При нарушениях овариально-менструального цикла и бесплодии назначают гонадотропины — ФСГ и ЛГ. Дозы подбирают индивидуально под контролем тестов функц, диагностики (в среднем по 75—150 ЕД ФСГ в течение 7—10 дней до появления признаков овуляции, а затем по 3000 ЕД ЛГ в течение 3 дней). Можно применять кломифен-цитрат.
Прогноз для жизни благоприятный. В результате лечения снижается вес тела, уменьшаются головные боли, головокружения, восстанавливаются менструации и может наступить беременность.
Профилактика заключается в предупреждении инфекционных болезней, интоксикаций, ожирения.
Библиография: Бухман А. И. Рентгенодиагностика в эндокринологии, с. 89, М., 1974; Латаш Л. П. Гипоталамус, приспособительная активность и электроэнцефалограмма, М., 1968; Макарченко А. Ф. и др. Физиология и патология переходного периода женщины, Киев, 1967; Супрун А. В. и Каган И. Е. Рентгенологическая картина костей черепа у женщин с патологическим климаксом и нарушением регуляции внутриглазного давления, Офтальм, журн., № 5, с. 353, 1975; Calame А. Le syndrome de Morgagni, Morel, P., 1951; H e n s с h enD. Morgagni’s Syndrom, Jena, 1937, bibliogr.; Moore S h. Hyperostosis cranii, Springfield, 1955; Morgagni G. B. De sedibus et causis morborum per anatomen indagatis libri quinque, v. 1—2, Venetiis, 1761; S i 1 i n — ii o v a-M £ 1 k o v a E. a B 1 a z e k O. Endokraniosa, Praha, 1958.
3. Л. Леменева; Ю. Г. Елашов (рент.).
Синдром Маклеода — причины, симптомы, диагностика и лечение

Синдром Маклеода — это хроническая патология с прогрессирующей гипоплазией и снижением плотности одного легкого или его доли, редукцией артериол, облитерацией мелких бронхов и буллезным изменением альвеол. Течение синдрома Маклеода сопровождается нарастающей экспираторной одышкой, устойчивым кашлем с непостоянной скудной мокротой, диффузными болями в груди, асимметрией грудной клетки, дыхательной недостаточностью. Диагностика синдрома Маклеода включает рентгенографию и КТ легких, бронхографию, сцинтиграфию легких, исследование ФВД. Для устранения патологического симптомокомплекса выполняется лобэктомия или пневмонэктомия.
Общие сведения
Синдром Маклеода (синдром Свайра-Джеймса, синдром Януса, «сверхпрозрачное» легкое, односторонняя легочная эмфизема) — клинико-рентгенологический синдром, сопровождающийся уменьшением и прогрессирующими эмфизематозными изменениями доли или легкого целиком, поражением легочных артериол и бронхиол. В 1953 г. синдром был описан Swyer и James; в 1954 г. британский пульмонолог Macleod подробно нарисовал патогенез заболевания, а французский рентгенолог Janus представил рентгенологические признаки аномалии. Синдром Маклеода считается относительно редкой патологией (на 1966 г. было известно о 100 случаях заболевания), более часто выявляется у пациентов мужского пола. По комплексу проявлений синдром Маклеода входит в группу хронических обструктивных болезней легких (ХОБЛ). Изучение данной патологии находится в области интересов пульмонологии.

Синдром Маклеода
Причины
К формированию синдрома Маклеода приводят неоднократно перенесенные в раннем детстве (в первые 8 лет жизни) бронхолегочные заболевания, рецидивирующие тяжелые бронхиты и пневмонии, осложняющиеся постинфекционным облитерирующим бронхиолитом. Наиболее опасными в плане исхода в синдром Маклеода являются бронхиолиты, вызываемые РСВ, ЦМВ, аденовирусом, вирусом гриппа, парагриппа, микоплазмой, легионеллой, пневмоцистой. Наслоившаяся при этом вторичная инфекция провоцирует развитие бронхоэктазов.
Постинфекционные бронхиолиты в раннем детском возрасте протекают на фоне интенсивного развития альвеол из зародышевых терминальных и респираторных бронхиол, что способствует нарушению формирования паренхимы легких.
Патогенез
При синдроме Маклеода гистологически определяется повреждение бронхиолярных стенок, включающее гипертрофию желез, некробиоз слизистого эпителия, разрастание грануляций и подслизистого слоя с образованием микрополипов, а также перибронхиальный фиброз; разрывы альвеолярных перегородок, утолщение стенок ветвей легочной артерии и редукцию капиллярной сети. Иногда может иметь место картина панацинарной эмфиземы с отдельными субплевральными буллами, обструкцией артериол, расширением мелких бронхов с гипоплазией их стенок. Сохранить воздушность легкому помогает коллатеральная вентиляция через неповрежденные респираторные пути и поступление воздуха через поры Кона.
В большинстве случаев эмфизематозный процесс локализуется в левом легком; может охватывать весь орган или преимущественно поражать одну долю. Деформированное легкое практически не функционирует, резко уменьшается в объеме, теряет эластические свойства. Возникающее при этом смещение средостения приводит к значительному нарушению легочной циркуляции и вентиляции в здоровом легком, обеспечивающем основной газообмен.
Классификация
По этиопатогенетическим критериям различают циркуляционную, вентиляционную и циркуляционно-вентиляционную формы синдрома Маклеода.
- Циркуляционная форма обусловлена наличием односторонней сосудистой аномалии легких. Это может быть врожденное отсутствие (агенезия/аплазия) одной легочной артерии с компенсацией легочного кровообращения за счет системного кровообращения бронхов. Возможна также приобретенная патология легочной артерии вследствие ее острой эмболии и ишемии, постоперационного тромбоза, а также внешней компрессии сосуда внутригрудными лимфоузлами при туберкулезе.
- Вентиляционная форма синдрома Маклеода обусловлена наличием врожденных пороков развития респираторных отделов бронхиального дерева (гигантской обширной эмфиземы с бронхомаляцией, врожденных бронхоэктазий с дисгенезией дыхательных путей) или приобретенной бронхолегочной патологии (вторичной обструктивной эмфиземы в результате неполной закупорки крупного бронха опухолью или инородным телом; постинфекционной или компенсаторной эмфиземы; прогрессивной легочной дистрофии с деструкцией).
Развитие циркуляционно-вентиляционной формы синдрома Маклеода вызвано гипоплазией одной из легочных артерий. Это состояние наблюдается редко, имеет обычно длительное скрытое течение.
Симптомы
Синдром Маклеода может манифестировать в любом возрасте, обычно проявляется в юношеском периоде и у взрослых. Для врожденной гигантской обширной эмфиземы типичен ранний дебют синдрома Маклеода (в период новорожденности и до 4-5 лет), при врожденных бронхоэктазиях клиническое начало обычно приходится на возраст 8-12 лет.
Заболевание протекает в хронической форме. Может иметь место бессимптомное или слабовыраженное течение. Проявления синдрома Маклеода неспецифичны, сходны с симптомами бронхита и БЭБ. Без видимых причин появляется экспираторная одышка, которая постепенно прогрессирует. Часто наблюдается устойчивый кашель с непостоянной скудной мокротой и диффузные боли в груди, заметна асимметрия грудной клетки. Выделение обильной мокроты гнойного характера указывает на вторичное инфицирование. Могут отмечаться периодические (связанные с ОРВИ) фебрильные эпизоды с усилением бронхиальных явлений и обструкции.
При врожденной артериовенозной мальформации и туберкулезе синдром Маклеода может сопровождаться кровохарканьем, приступами пароксизмального кашля, истерической одышкой с резко учащенным дыханием, риском асфиксии. Синдром Маклеода осложняется дыхательной недостаточностью, бронхиальной обструкцией различной выраженности, развитием бронхиальной астмы и декомпенсированного легочного сердца.
Диагностика
Диагностика синдрома Маклеода включает сбор анамнеза, осмотр, рентгенографию и КТ легких, бронхографию, радиоизотопное сканирование, исследование внешнего дыхания. В анамнезе больных синдромом Маклеода присутствуют частые случаи тяжелых бронхолегочных заболеваний. Визуально отмечается деформация грудной клетки с уменьшением объема на стороне поражения, перкуторно — смещение средостения в противоположную сторону, коробочный оттенок звука; аускультативно – асимметричное дыхание с ослаблением в области пораженного легкого, сухие рассеянные хрипы, кратковременные крепитирующие шумы, удлинение выдоха.
При проведении рентгенографии легких заметно выраженное одностороннее увеличение прозрачности («сверхпрозрачность») ткани легких и обедненный легочный рисунок с зонами, лишенными его целиком (крупные буллы). Точной идентификации тонкостенных буллезных формирований при синдроме Маклеода помогает инспираторная и экспираторная КТ легких. Исследование на выдохе показывает усиление выраженности изменений на этих участках — симптом «воздушной ловушки». Тень средостения на высоте вдоха отклоняется в сторону здорового легкого.
Бронхографически в эмфизематозном легком определяются признаки сужения периферических бронхов, свидетельствующие о деформирующем бронхите. Данные ангиопульмонографии указывают на одностороннее уменьшение диаметра ствола и ветвей легочной артерии, увеличение углов их расхождения, аплазию капиллярной сети.
Сцинтиграфия легких выявляет отсутствие абсорбции радиоизотопа пораженным легким. Исследование ФВД определяет специфические эмфизематозные изменения (увеличение OEЛ, уменьшение ЖЕЛ), признаки бронхиальной обструкции, дыхательной недостаточности по экспираторному типу. Дифференциальную диагностику синдрома Маклеода проводят с простой гипоплазией или эмфиземой легкого, бронхиальной астмой, ХОБЛ, осложненными спонтанным пневмотораксом.
Лечение синдрома Маклеода
Лечение определяется степенью клинических проявлений и темпами прогрессирования патологии. Для купирования дыхательной недостаточности и ассоциированных заболеваний показана госпитализация и симптоматическая терапия. При наслоении респираторных гнойно-воспалительных процессов используются антибиотики. Дополнительно проводятся кислородотерапия, ЛФК.
Оперативное вмешательство выполняется в случае резкого нарушения эмфизематозным легким газообменной функции здорового легкого или частых инфекционных осложнениях. Объем резекции сводится к лобэктомии или пневмонэктомии. Прогноз синдрома Маклеода определяется частотой бронхолегочных инфекций и уровнем развития дыхательной недостаточности, обычно считается неопределенным или неблагоприятным.
