Перипортальная кардиомиопатия > Клинические протоколы МЗ РК
Каптоприл (начальная доза 6.25-12.5 мг 3 раза в сутки, целевая доза 25-50 мг 3 раза в день)
Эналаприл (начальная доза 1.25-2.5 мг 2 раза в день, целевая доза 10 мг 2 раза в день)
Рамиприл (начальная доза 1.25-2.5 мг 2 раза в день, целевая доза 5мг 2 раза в день)
Лизиноприл (начальная доза 2.5-5 мгежедневно, целевая доза 25-40 мг ежедневно)
БРА (при непереносимости ИАПФ)
Кандесартан (начальная доза 2 мг ежедневно, целевая доза 32 мгежедневно)
Валсартан (начальная доза 40 мгдважды в день, целевая доза 160 мг дважды в день)
Возможно назначение нитратов или гидралазина, если женщина не переносит ИАПФ и БРА
Петлевые диуретики
Фуросемид внутривенно или перорально, доза должна рассматриваться на основе СКФ: СКФ>60 мл/минна 1.73 м2:
фуросемид 20-40 мг каждые 12-24
СКФ<60 мл/минна 1.73 м2:
фуросемид 20-80 мг каждые 12-24
Вазодилататоры
Гидралазин (начальнаядоза37.5мг 3 или 4 раза в день, целевая доза 40 мг 3 раза в день)
Изосорбидадинитрат (начальная доза 20 мг 3 раза в день, целевая доза 40 мг 3 раза в день)
Антагонисты альдостерона
Верошпирон (начальная доза 12.5 мг ежедневно, целевая доза 25-50 мг в день)
Эплеренон (начальная доза 12.5 мгежедневно, целевая доза 25-50 мг ежедневно)
Бета-блокаторы
Карведилол (начальная доза 3.125 мг дважды в день, целевая доза 25 мг дважды в день)
Метопролол замедленного высвобождения (начальная доза 0.125 мгвдень, целевая доза 0.25 мгвдень)
Блокаторы пролактина
Бромкриптин 2.5 мг дважды в день 2 недели, затем 4 недели по 2.5 мг 1 раз в день
Варфарин при ФВ<35%
Начальная доза варфарина 2,5 мг в сутки, в течение первых 5-7 дней контроль МНО ежедневно или через день, после стабилизации МНО (2,0-3,0) контроль 2 раза в неделю, затем 1 раз в неделю, затем 1 раз в месяц. При необходимости дозу повышают на 1/4 или 1/2 таблетки в сутки. Полное антикоагулянтное действие варфарина проявляется на 3-5 сутки, в связи с чем его назначают на фоне лечения гепаринами. НФГ или НМГ применяют до тех пор, пока не будет достигнуто целевое МНО (2,0-3,0).
Ведение больных с декомпенсированной ППКМП
Дыхательные пути
Интубировать сразу же при синдроме дистресса для предупреждения осложнений, связанных с дыхательными путями позднее при лечении.Дыхание
Обеспечить кислородотерапию.
Поддерживать непрерывную пульсоксиметрию мониторированием SaO2.
Измерять газы артериальной крови каждые 4-6 ч до тех пор, пока дыхание не стабилизируется
Кровообращение
Начать мониторинг сердца и артериального давления.
Установить артериальный катетер для точного измерения артериального давления и взятия проб крови.
Обеспечить центральный венозный доступ для мониторинга центрального венозного давления.
Фармакотерапия острой сердечной недостаточности при ППКМП
Петлевые диуретики внутривенно (с осторожностью у женщин в предродовом периоде)
Фуросемид внутривенно или перорально, доза должна рассматриваться на основе СКФ>60 мл/мин на 1.73 м2:
фуросемид 20-40 мг каждые 12-24
СКФ<60 мл/минна 1.73 м2:
фуросемид 20-80 мг каждые 12-24
При выраженной объемной перегрузке обсудить инфузию фуросемида или изолированную ультрафильтрацию
Вазодилататоры
Нитроглицерин инфузионно 5-10 мг/мин, титровать по клиническому состоянию и АД Нитропруссид 0.1-5 мкг/кгв минуту, использовать с осторожностью у женщин в предродовом периоде
Положительные инотропные средства
Милринон 0.125-0.5 мкг/кг в минуту
Добутамин 2.5-10 мкг/кг в минуту
Избегать бета-блокаторов в острой фазе, так как могут снизить перфузию
Не фракционированный гепарин изолированно или совместно с варфарином
Обсудить эндомиокардиальную биопсию, если не исключается вирусный миокардит, в таком случае рассмотреть иммунносупрессивную терапию (азатиаприн, кортикостероиды)
Следует приложить все усилия для разработки перорального режим применения лекарств, которое может поддерживать симптоматическое улучшение и уменьшать риск последующего ухудшения клинического состояния.
На рисунке 2 представлен алгоритм ведения беременной с тяжелым течением ППКМП.
Рисунок 2
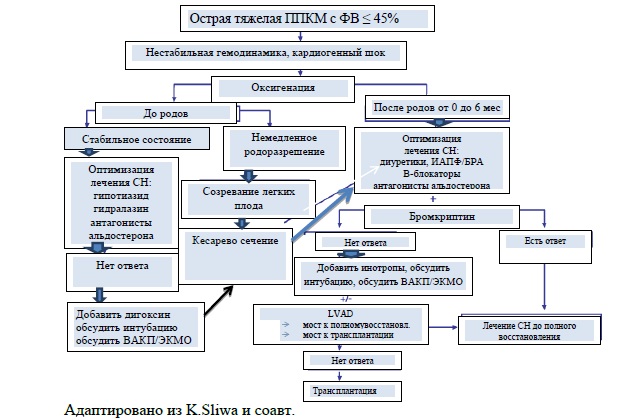
Медикаментозное лечение, оказываемое на амбулаторном этапе
Перечень основных лекарственных средств:
Наименование | Ед.изм. | Кол-во | Обоснование | Класс** Уровень** |
| Каптоприл 25 мг, 50 мг Эналаприл 5мг,10мг,20 мг Лизиноприл 2,5 м, 5мг, 10 мг, 20 мг Рамиприл 1,25 мг, 2,5 мг, 5 мг | Табл. Табл. Табл. | 14 14 14 | Кардиопротекция, патогенетическое лечение СН | IC |
| Карведилол 6,25 мг, 12,5 мг. 25 мг Метопрололсукцинат 25 мг, 50 мг, 100 мг | Табл. Табл. | 28 30 | Кардиопротекция, патогенетическое лечение СН | IC |
| Спиронолактон 25 мг, 100 мг | Табл. | 20 | 1.Кардиопротекция, патогенетическое лечение СН в дозе нейрогуморального модулятора (12.5-50 мг) 2.Как диуретик (100-300 мг) в дополнение к основным диуретикам (петлевые+ тиазидные) при рефрактерных симптомах задержки жидкости | IC |
| Фуросемид 40 мг | Амп. | 10 | Для устранения симптомов задержки жидкости | IC |
| Фуросемид 40 мг | Табл. | 20 | ||
| Торасемид 5мг, 10 мг | Табл. | 20 | ||
| Гидрохлоротиазид 50 мг. 100 мг | Табл. | 02 |
Перечень дополнительных лекарственных средств:
Наименование | Ед.изм. | Кол-во | Обоснование | Суточная доза | Класс Уровень |
| Блокаторы рецептора ангиотензинаII (Кандесартан, Валсартан 40мг, 80 мг, Лозартан (только в послеродовом периоде) | Табл. | 14 | Кардиопротекция, патогенетическое лечение СН | 40-160 мг | IC |
| Нитроглицерин аэрозоль | флак. | 1 | ППКМП, осложненные острой левожелудочковой недостаточностью | ||
| Дигоксин 0,25 мг | Табл. | 14 | Пациентам с синусовым ритмом с ФВ ≤ 45%, которые не толерантны к ББ, на фоне приема основных препаратов ИАПФ/БРА), АА | 0,25 мг | |
| Препараты калия (панангин, хлорид калия 4%-10 мл) | амп. | 10 | При гипокалиемии | ||
| Калия-магния аспарагинат | флак. | 5 | При гипокалиемии | ||
| Амиодарон 150 мг (3 мл) в амп. | амп. | 10 | Купирование нарушений ритма | 150-900 мг | |
| Амиодарон200 мг в табл. | Табл. | 20 | Лечение и профилактика нарушений ритма | 100-600 мг | |
| Атропин 0,1%, амп. | амп. | 5 | брадиаритмии | ||
| Ацетилсалициловая кислота (500 мг). 75 мг, 100 мг, 150мг | Табл. | 5 | Профилактика тромбозов при низком риске ТЭО | 75-100 | |
| Пероральные антикоагулянты (варфарин 2,5 мг) | Табл. | Профилактика тромбозов при высоком риске ТЭО | 2.5 и более | ||
| ИПП (омепразол 20 мг, пантапразол 20 мг и др.) | Кап. | 28 | Гастропротекция при назначении антикоагулянтной или антиагрегантной терапии по показаниям | 20 мг | |
| Бромокриптин 1,25-5 мг в сутки | таб | 30 | Восстановление функций сократимости миокарда | 1,25-5 | |
| Каберголин 0,25-1,0 -2 раза в неделю | таб | Восстановление функций сократимости миокарда | 0,25-1,0 -2 раза в неделю |
Медикаментозное лечение оказываемое на стационарном уровне
Перечень основных лекарственных средств
Наименование | Ед. изм. | Кол-во | Обоснование | Класс Уровень |
| Ингибиторы АПФ Каптоприл 25 мг, 50 мг Эналаприл 5мг,10мг,20 мг Лизиноприл 2,5 м, 5мг, 10 мг, 20 мг Рамиприл 1,25 мг, 2,5 мг, 5 мг | Табл. Табл. Табл. | 14 14 14 | Кардиопротекция, патогенетическое лечение СН | IC |
| Бета-адреноблокаторы Карведилол 6,25 мг, 12,5 мг. 25 мг Метопролол сукцинат 25 мг, 50 мг, 100 мг | Табл. Табл. | 28 30 | Кардиопротекция, патогенетическое лечение СН | IC |
| Спиронолактон 25 мг, 100 мг | Табл. | 20 | 1.Кардиопротекция, патогенетическое лечение СН в дозе нейрогуморального модулятора (12.5-50 мг) | IC |
| 2. Как диуретик (100-300 мг) в дополнение к основным диуретикам (петлевые+ тиазидные) при рефрактерных симптомах задержки жидкости | ||||
| Фуросемид 40 мг | Амп. | 10 | Для устранения симптомов задержки жидкости | IC |
| Фуросемид 40 мг | Табл. | 20 | Для устранения симптомов задержки жидкости | |
| Торасемид 5мг, 10 мг | Табл. | 20 | Для устранения симптомов задержки жидкости | |
| Гидрохлоротиазид 50 мг. 100 мг | Табл. | 20 | Для устранения симптомов задержки жидкости |
Перечень дополнительных лекарственных средств
Наименование | Ед.изм. | Кол-во | Обоснование | Класс Уровень |
| Блокаторы рецептора ангиотензинаII (Кандесартан, Валсартан 40мг, 80 мг, Лосартан | Табл. | 14 | Кардиопротекция, патогенетическое лечение СН | IC |
| Добутамин20 мл 250мг. | флак. | 5 | Гемодинамическая поддержка при ППКМП, осложненных ОСН | |
| Левосимендан 12,5 мг | флак. | 4 | Гемодинамическая поддержка при ППКМП, осложненных ОСН | |
| Норадреналин 0,2% 1,0 мл. | амп. | 4 | Гемодинамическая поддержка при ППКМП, осложненных ОСН | |
| Нитроглицерин 0,1% 10 мл. | флак. | 4 | ППКМП, осложненные острой левожелудочковой недостаточностью | |
| Нитроглицерин аэрозоль | флак. | 1 | ППКМП, осложненные острой левожелудочковой недостаточностью | |
| Гидралазин 1,0 мл 0,01; 0,025 | Амп. Таб. | Рефрактерная СН | ||
| Нитропруссид 0,05 | Амп. | Рефрактерная СН | ||
| Милринон 0,1%-10,0 | Амп. | Рефрактерная СН | ||
| Дигоксин 1,0 мл | Амп. | 3 | При ППКМП, осложненных ОСН только в минимальных дозах – при обязательном мониторинге ритма. | |
| Дигоксин 0,25 мг | табл. | 14 | Могут рассматриваться у пациентов с синусовым ритмом с ФВ ≤ 45%, которые нетолерантнык ББ, на фоне приема основных препаратов ИАПФ/БРА), АА | |
| Препараты калия (панангин, хлорид калия 4%-10 мл) | амп. | 10 | При гипокалиемии | |
| Калия-магния аспарагинат | флак | 5 | При гипокалиемии | |
| Амиодарон 150 мг (3 мл) в амп. | амп. | 10 | Купирование нарушений ритма | |
| Амиодарон200 мг в табл. | Табл. | 20 | Лечение и профилактика нарушений ритма | |
| Атропин 0,1%, амп. | амп. | 5 | Брадиаритмии | |
| Ацетилсалициловая кислота (500 мг). 75 мг, 100 мг, 150мг | Табл. | 5 | Профилактика тромбозов при низком риске ТЭО | |
| Прямые антикоагулянты (нефракционированный гепарин-, низкомолекулярные гепарины-надропарин, эноксапарин- по 16 шприцов) | амп. | 1 | Профилактика тромбозов при высоком риске ТЭО | |
| Фондапаринукс 2,5 мг | амп. | 14 | Профилактика тромбозов при высоком риске ТЭО | |
| Пероральные антикоагулянты (варфарин 2,5 мг) | таб. | Профилактика тромбозов при высоком риске ТЭО | ||
| ИПП (омепразол 20 мг, пантапразол 20 мг и др.) | Кап. | 28 | Гастропротекция при назначении антикоагулянтной или антиагрегантной терапии по показаниям | |
| Бромокриптин 1,25-5 мг в сутки | таб. | 30 | Восстановление функции сократимости миокарда | |
| Каберголин 0,25-1,0 -2 раза в неделю | таб. | Восстановление функции сократимости миокарда |
Медикаментозное лечение оказываемое на этапе скорой неотложной помощи
Наименование | Ед.изм. | Кол-во | Обоснование | Класс Уровень |
| Ингибиторы АПФ Каптоприл 25 мг, 50 мг Эналаприл | Табл. ампулы | 14 | Симптомы ОЛЖН | IC |
| Добутамин20 мл 250мг. | флак. | 5 | Гемодинамическая поддержка при ППКМП, осложненных ОСН | |
| Норадреналин 0,2% 1,0 мл. | амп. | 4 | Гемодинамическая поддержка при ППКМП, осложненных ОСН | |
| Нитроглицерин 0,1% 10 мл. | флак. | 4 | ППКМП, осложненные острой левожелудочковой недостаточностью | |
| Нитроглицерин аэрозоль | флак. | 1 | ППКМП, осложненные острой левожелудочковой недостаточностью | |
| Дигоксин 1,0 мл | амп. | 3 | При ППКМП, осложненных ОСН только в минимальных дозах , при обязательном мониторинге ритма. | |
| Амиодарон 150 мг (3 мл) в амп. | амп. | 10 | Купирование нарушений ритма | |
| Атропин 0,1%, амп. | амп. | 5 | Брадиаритмии | |
| Фуросемид 40 мг | амп. | 10 | Для устранения симптомов задержки жидкости |
Другие методы лечения ППКМП: не применяются
Хирургическое вмешательство:
Если нет клинического улучшения от медикаментозной терапии:
− Обсудить проведение сердечной МРТ
− Произвести эндомиокардиальную биопсию для определения вирусного миокардита (если ранее не проводилась)
− Мероприятия по механической поддержке левого желудочка:
− Внутриаортальная баллонная контрпульсация
− Устройство для поддержки левого желудочка (LVAD)
− Экстракорпоральная мембранная оксигенация
− Сердечная трансплантацияХирургическое вмешательство, оказываемое в амбулаторных условиях: отсутствует.
Хирургическое вмешательство, оказываемое в стационарных условиях:
Внутриаортальная баллонная контрпульсация (ВАКП) – при неэффективности медикаментозной терапии.
Экстракорпоральная мембранная оксигенация (ЭКМО) — при рефрактерной сердечной недостаточности, не купируемом отеке легких с гипоксемией, в качестве моста к установке устройств поддержки левого желудочка у больных с рефрактерным кардиогенным шоком, несмотря на использование внутриаортального устройства и полной инотропной поддержки;
Желудочковые устройства для поддержки работы сердца (LVAD по показаниям (см. протокол по ХСН). Имплантация желудочкового assist устройства (LVAD) может быть рассмотрена перед включением пациента для трансплантации сердца, и должна рассматриваться как спасительная мера в ситуации, угрожающей жизни («мост к трансплантации»). Однако, тромбофилические осложнения, связанные с их использованием, остаются высокими, особенно при ППКМП, в связи с тем, что ППКМП является протромботическим состоянием. Размер устройства также остается сдерживающим фактором, так как не все типы устройств можно имплантировать женщинам с небольшой площадью поверхности тела. После клинического улучшения состояния больной и восстановления функции сердца, возможна попытка отключения от устройства.
Сердечная ресинхронизационная терапия и имплантация кардиовертера-дефибриллятора (СРТ и КВД) по показаниям (см. протокол по ХСН). Пациентам с симптоматической желудочковой аритмией должна быть рассмотрена имплантация кардиовертера/ дефибриллятора. Следует рассмотреть необходимость имплантации КВД с СРТ при ХСН III-IVФКNYHA и ширине комплекса QRS≥120 мс, если спустя 6 месяцев после манифестации ППКМП, несмотря на адекватную медикаментозную терапию, у пациентки сохраняется тяжелая дисфункция ЛЖ (ФВ менее 35%).
Трансплантация сердца.
Если пациентка зависит от инотропных средств или внутриаортальной контрпульсации, несмотря на оптимальную медицинскую терапию, или имплантацию механических устройств поддержки сердечной деятельности, должна рассматриваться сердечная т
Перипартальная кардиомиопатия — причины, симптомы, диагностика и лечение

Перипартальная кардиомиопатия – это редкое жизнеугрожающее заболевание сердца, возникающее во время беременности или в течение нескольких месяцев после родов. Клинически болезнь проявляется классическими симптомами застойной сердечной недостаточности: затруднением дыхания при физической нагрузке или ходьбе, учащенным сердцебиением, отеками на ногах. Отличительная особенность ХСН при перипартальной КМП – быстрое нарастание. Диагноз ставится на основании жалоб, анамнестических данных, лабораторно и инструментально подтвержденной сердечной недостаточности. Лечение проводится по общим принципам терапии ХСН с добавлением агонистов дофаминовых рецепторов.
Общие сведения
Перипартальная кардиомиопатия (перипартальная болезнь, кардиомиопатия Мидоуса) в подавляющем большинстве случаев развивается после родов (в течение 5-6 месяцев), реже – во II или III триместре беременности. Заболевание впервые было описано французским врачом Ц. Рицше в 1849 году. Средняя распространенность составляет 1 случай на 10 000 родов. Перипартальная КМП чаще возникает у лиц негроидной расы, поэтому в африканских странах ее встречаемость намного выше (1:100).

Перипартальная кардиомиопатия
Причины
Несмотря на многочисленные исследования, точный этиологический фактор патологии не установлен. Предполагается роль вирусов, вызывающих миокардит (вируса Коксаки А и В, Эпштейн-Барра), и аутоантител к белкам сердечной мышцы. Перипартальная КМП более часто наблюдается у ближайших родственников, что свидетельствует о генетической предрасположенности. Существуют факторы, увеличивающие вероятность развития ПКМП:
Патогенез
Неизвестный фактор стимулирует оксидативный стресс, который, в свою очередь, активирует в кардиомиоцитах катепсин D – белок, расщепляющий гормон пролактин на фрагменты. Один из них, 16кДа фрагмент, обладает кардиотоксическим эффектом, вызывает вазоконстрикцию, дисфункцию и запрограммированную гибель клеток миокарда, подавляет пролиферацию эндотелиальных клеток сосудов.
Все это приводит к расширению полостей сердца, ухудшению насосной функции миокарда правого и левого желудочка. Патоморфологические изменения при перипартальной кардиомиопатии неспецифичны и схожи с таковыми при миокардитах. Выявляется диффузная дегенерация, очаги миоцитолиза, некроза, фиброза, умеренная гипертрофия волокон миокарда.
Симптомы перипартальной кардиомиопатии
Временной промежуток возникновения признаков заболевания – от конца II триместра беременности до 6 месяца после родов. Наиболее часто клиническая картина начинает разворачиваться в течение первого месяца после рождения ребенка. Трудность распознавания ПКМП заключается в том, что ее ранние симптомы имитируют физиологические изменения при беременности.
К таким признакам можно отнести повышенную утомляемость, ухудшение переносимости физических нагрузок, небольшое затруднение дыхания, усиливающееся в лежачем положении (ортопноэ). Из-за быстрого прогрессирования ХСН симптомы усугубляются. Одышка присутствует даже в покое. Появляются ноющие боли в области сердца, головокружение, отеки на стопах и голенях, учащенное сердцебиение. Начинают беспокоить тянущие боли в правом подреберье из-за увеличения размеров печени.
Осложнения
Перипартальная кардиомиопатия является тяжелым состоянием с большим количеством осложнений, в том числе фатальных. При быстропрогрессирующем течении возможно развитие острой сердечной недостаточности с отеком легких или кардиогенным шоком. Резкая дилатация камер сердца способствует возникновению жизнеугрожающих нарушений ритма сердца.
Из-за вихревого движения крови в расширенных полостях сердца легко образуются тромбы, поэтому у больных ПКМП существует высокий риск кардиоэмболического инсульта и ТЭЛА. Ухудшение систолической функции миокарда неблагоприятно сказывается на плацентарном кровообращении, что приводит к внутриутробной гипоксии плода, задержке развития или антенатальной гибели.
Диагностика
Чаще всего больных курируют врачи-кардиологи. Беременные пациентки с перипартальной кардиомиопатией находятся под совместным наблюдением кардиолога и акушера-гинеколога. При физикальном осмотре обращают внимание на набухание шейных вен, усиливающееся при надавливании на печень (гепатоюгулярный рефлюкс), влажные хрипы в легких, глухость тонов сердца. ПКМП дифференцируют с приобретенными пороками сердца, дилатационной кардиомиопатией, миокардитами и пр.
Поскольку преобладающее число случаев ПКМП приходится на послеродовый период, большое значение имеет уточнение факта беременности у пациентки с быстропрогрессирующей ХСН. Отсутствие каких-либо кардиологических заболеваний (ИБС, пороки сердца) до начала гестации свидетельствует в пользу ПКМП. Для уточнения диагноза проводится дополнительное обследование, включающее:
- Лабораторные исследования. В крови обнаруживается повышение фрагмента пролактина 16кДа и маркера сердечной недостаточности – мозгового натрийуретического пептида (NT-proBNP).
- ЭКГ. На электрокардиограмме отмечаются признаки гипертрофии левого и правого желудочков, различные нарушения ритма: фибрилляция предсердий, желудочковая экстрасистолия, блокада левой ножки пучка Гиса.
- Эхо-КГ. Эхокардиография считается основным методом исследования. Выявляется расширение всех камер сердца, особенно левого желудочка, выраженное снижение фракции выброса (45-50%), относительная атриовентрикулярная недостаточность. Иногда встречаются пристеночные тромбы, умеренный перикардиальный выпот.
- МРТ сердца. Магнитно-резонансная томография позволяет провести детальную оценку структуры миокарда. Назначается при неоднозначных результатах Эхо-КГ.
- Рентгенография ОГК. На рентгенограмме органов отмечается расширение тени сердца, усиление сосудистого рисунка за счет венозного полнокровия сосудов малого круга кровообращения.
Лечение перипартальной кардиомиопатии
Консервативная терапия
После подтверждения диагноза больных обязательно госпитализируют в кардиологический стационар. При тяжелой недостаточности кровообращения показан перевод в отделение реанимации и интенсивной терапии для проведения внутриаортальной балонной контрпульсации. Несмотря на быстропрогрессирующее течение, почти у половины пациенток наблюдается спонтанное выздоровление.
Немедикаментозное лечение включает ограничение приема жидкости до 2 литров в сутки и поваренной соли до 3-4 граммов в сутки. При назначении лекарственной терапии беременным необходимо учитывать потенциальный нежелательный эффект некоторых медикаментов на плод. Рекомендованы:
- Агонисты дофаминовых рецепторов. Препараты действуют на главное патогенетическое звено ПКМП. Подавляя выработку пролактина, они снижают образование его кардиотоксического фрагмента (16кДа). У беременных применяется бромокриптин, после родов возможен перевод на каберголин или хинаголид.
- Ингибиторы АПФ. Основные лекарственные средства, замедляющие прогрессирование сердечной недостаточности.
- Бета-адреноблокаторы. Назначаются как альтернатива ингибиторам АПФ беременным женщинам, а также при наличии тахиаритмий.
- Вазодилататоры. Сосудорасширяющие медикаменты используются для снятия вазоспазма при систолическом давлении более 110 мм рт. ст.
- Диуретики. С целью уменьшения застойных явлений в легких и выведения жидкости применяются тиазидные и петлевые мочегонные препараты.
- Сердечные гликозиды. Для поддержания адекватного сердечного выброса при артериальной гипотензии показаны дигоксин, левосимендан.
- Антикоагулянты. Так как дилатация сердечных полостей сопровождается высоким риском тромбообразования, пациенткам рекомендован прием антикоагулянтов (варфарина, ривароксабана). Беременным разрешен только гепарин.
Хирургическое лечение
При выраженной ХСН (фракция выброса левого желудочка достигает менее 40%), развившейся у беременных, требуется прерывание беременности путем кесарева сечения. Крайне тяжелая, резистентная к консервативной терапии перипартальная кардиомиопатия служит показанием к трансплантации сердца. При устойчивых тахиаритмиях, сопровождающихся грубыми гемодинамическими нарушениями (критическое падение артериального давления), прибегают к имплантации кардиовертера-дефибриллятора.
Прогноз и профилактика
Перипартальная кардиомиопатия – жизнеугрожающее состояние с высоким процентом летальности. В зависимости от своевременности диагностирования и начала грамотной терапии частота летальных исходов составляет от 7 до 56%. Основными причинами смерти выступают нарушения ритма и проводимости сердца, тромбоэмболические осложнения, недостаточность кровообращения.
Полное восстановление насосной функции сердечной мышцы после лечения наблюдается в 50-65% случаев. У 30-50%, перенесших перипартальную КМП, при повторной беременности происходит рецидив заболевания, поэтому им рекомендуется применение различных методов контрацепции. Эффективных методов профилактики не существует.
причины, симптомы, лечение и диагностика
Перипартальная кардиомиопатия — это одна из разновидностей патологий сердечно-сосудистой системы, которая развивается у женщин в последнем триместре беременности либо в течение первых 5 месяцев после родов. Она определяется характерным комплексом симптомов, которые включают признаки сердечной недостаточности и нарушением работы левого желудочка. Определяющая особенность заболевания состоит в том, что ранее у пациенток отсутствуют любые нарушения сердечной деятельности. Такой вид кардиомиопатии очень редкий (в среднем — 1 случай на 1300 рожениц), но опасный, поскольку может приводить к летальному исходу.
Определение и механизм развития
Перипартальная кардиомиопатия — это идиопатическая патология, то есть определить точную причину ее развития невозможно. Точный диагноз можно поставить при обнаружении дисфункции левого желудочка, что проявляется комплексом характерных симптомов. Дилатация (расширение) желудочка диагностируется не в каждом случае, но этот признак также учитывается при обследовании. К основным критериям, которые отличают перипартальную кардиомиопатию от остальных разновидностей нарушения сердечной деятельности, можно отнести:
- яркое обострение симптомов в последний месяц беременности либо в первые месяцы после родов;
- отсутствие видимых причин, которые могли бы спровоцировать развитие сердечной недостаточности;
- отсутствие подобных патологий в анамнезе роженицы, в том числе в первые триместры беременности.
Первая теория, которая объясняет механизм развития перипартальной кардиомиопатии, — это С-реактивный белок. Он содержится в плазме крови и участвует в воспалительных реакциях, а у пациенток с подобным диагнозом регистрируется его стойкое повышение. Эта особенность объясняет повышенную частоту распространения болезни у жителей Африки — у чернокожих женщин средний уровень этого белка находится на более высоком уровне. Так, одной из первопричин кардиомиопатии можно считать воспалительные реакции, которые возникают на фоне повышения активности С-реактивного белка и затрагивают миокард.
Еще одно объяснение этому виду кардиомиопатии — аутоиммунные реакции. Они возникают при нарушении работы иммунной системы, когда защитные клетки воспринимают нормальные белки организма как чужеродные и запускают цикл воспалительных реакций. Кроме того, выявлен повышенный риск заболевания при многоплодной беременности. Два этих фактора взаимосвязаны — в крови женщин при многоплодной беременности определяется повышенное содержание аутоантител.
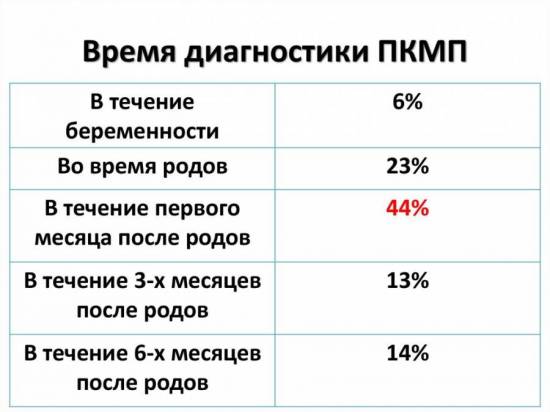
Первый месяц после родов считается наиболее опасным — именно в этот период зарегистрировано наибольшее количество случаев перипартальнной кардиомиопатии
В последнее время к числу возможных механизмов развития перипартальной кардиомиопатии добавляют оксидантный стресс. Антиоксиданты — это вещества, которые нейтрализуют действие свободных радикалов. Последними называются соединения, которые образуются клетками тела либо поступают в организм человека извне, а в больших количествах провоцируют разрушение и преждевременную гибель клеточных элементов. Полноценность работы систем антиоксидантной защиты обеспечивает утилизацию излишних свободных радикалов и защиту клеток от их пагубного воздействия. Однако чрезмерное их количество может становиться причиной опасных последствий, в том числе заболеваний миокарда. В случае перипартальной кардиомиопатии это объясняется повышением активности фермента катепсина D. Он отделяет от пролактина важный фрагмент, который способен подавлять ангиогенез — процесс формирования кровеносных сосудов. Его действие связывают с развитием сосудистых спазмов и преждевременной гибелью клеток.
СПРАВКА! Точные данные о частоте возникновения перипатральной кардиомиопатии отсутствуют. Этот показатель зависит в том числе от национальности и региона проживания пациенток — в Латинской Америке и Африке зарегистрирована максимальная частота случаев этого заболевания.
Причины
Причину перипартальной кардиомиопатии установить невозможно. Все современные исследования основаны на результатах обследований женщин разных возрастов и национальностей, сравнительной характеристике и статистике. Факторами риска, которые могут вызывать различные нарушения сердечной деятельности, в том числе патологии левого желудочка, считаются:
- возраст — патология чаще регистрируется у женщин старше 30 лет;
- многоплодная беременность либо большое количество родов;
- состояние преэклампсии;
- гестационная артериальная гипертензия — повышение артериального давления;
- влияние вредных привычек, наркотическая и другие виды зависимости.
Некоторые специалисты включают в этот список инфекционные заболевания и действие вирусов. Также исследовалось значение генетической предрасположенности, но подобной зависимости не было установлено. Основными факторами считаются различные биохимические процессы, которые развиваются при беременности, и нарушение ответа организма на подобные реакции.
Симптомы
Окончательный диагноз ставится на основании инструментальных и лабораторных методов обследования. При перипартальной кардиомиопатии определяется характерный комплекс симптомов, которые позволяют предположить именно эту патологию и дифференцировать ее от нарушений с подобными клиническими проявлениями.
- Одышка — первый симптом, который можно определить самостоятельно. Она усиливается после незначительных нагрузок, а также в лежачем положении. Кроме того, может присутствовать отек легких, выслушиваться влажные хрипы. В дополнение могут возникать жалобы на болезненные ощущения в области сердца.
- ЭКГ — один из основных критериев оценки состояния пациенток. Исследование указывает на развитие сердечной недостаточности, в большинстве случаев — на гипертрофию левого желудочка. Кроме того, могут выявляться различные нарушения сердечного ритма и предсердно-желудочковая блокада.
- ЭхоКГ — один из наиболее информативных методов диагностики. Этот способ используется для определения соотношения отделов сердца, обнаружения тромбов и других патологий. У большинства пациенток обнаруживается расширение левого желудочка и снижение фракции выброса жидкости (менее половины нормального показателя).
- МРТ — методика, которая позволяет точно визуализировать состояние миокарда и особенно информативна при дифференциальной диагностике. Исследование с использованием гадолиния применяется, чтобы отличить перипартальную кардиомиопатию от воспалительного процесса, но рекомендуется к применению уже после родов.
- Лабораторные исследования — анализ крови не менее важен, чем инструментальные методики. У пациенток определяется повышение активности С-реактивного белка, а также натрийуретического пептида В. Последний играет роль в механизмах гипертрофии и растяжения левого желудочка, но может выявляться и при других типах кардиомиопатии.
ВАЖНО! Клиническая картина при перипартальной кардиомиопатии может отличаться. Основные ее критерии, при которых важно провести полное обследование, — это одышка, боли за грудиной, отеки конечностей и другие симптомы.
Методы диагностики
Определение кардиомиопатии на современном этапе не вызывает сложностей. Для этого применяются инструментальные (ЭКГ, ЭхоКГ, МРТ) и лабораторные (анализ крови) методики, а также осмотр и сбор анамнеза. Сложность состоит в дифференциальной диагностике от других видов нарушения сердечной деятельности, среди которых выделяют миокардит, дилатационную кардиомиопатию, пороки сердца, инфаркт миокарда и тромбоэмболию легочной артерии. Определяющим фактором для постановки диагноза является снижение фракции выброса левого желудочка без видимой причины, характерным является его гипертрофия либо расширение.
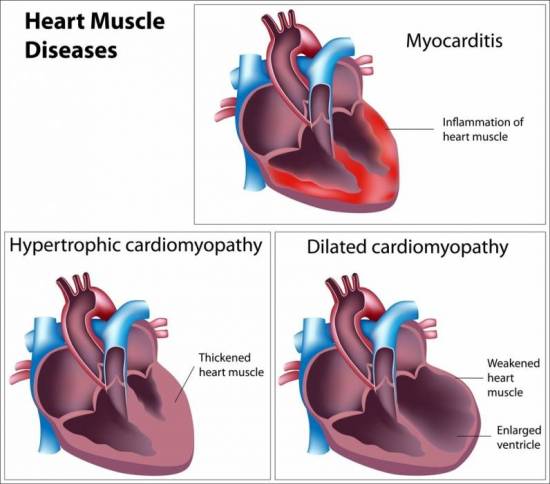
Основная цель диагностики — отличить перипартальную от других видов кардиомиопатий, воспалительных процессов и органических поражений миокарда
Лечение
Медикаментозная терапия перипартальной кардиомиопатии основана на снятии отечности, восстановлении нормального кровообращения, нормализации работы сердца и профилактику осложнений. Лечение назначается с учетом срока беременности и стадии сердечной патологии. Выделяют несколько принципов, каждый из которых направлен на устранение разных нарушений:
- для устранения отека легких — диуретики (фуросемид), нитроглицерин, инотропные препараты;
- при кардиогенном шоке — кислородная терапия, применение инотропных веществ (добутамин, левосимедан)
- для лечения хронической сердечной недостаточности — нитроглицерин, ингибиторы АПФ (после родов), гепарин (для профилактики появления тромбов), адреноблокаторы;
- бромокриптин — новый метод лечения, который позволяет снизить уровень оксидантного стресса и предотвратить опасные последствия.
Перипартальная кардиомиопатия — это редкая патология, но врачи продолжают исследования механизмов ее развития и наиболее безопасных методов лечения. Терапия успешна при своевременном обращении за медицинской помощью и проводится консервативными (медикаментозными) способами.
Перипартальная (послеродовая) кардиомиопатия — Likar.Info

Что такое перипартальная кардиомиопатия, какие клинические проявления заболевания? Какие методы используются для лечения?
 Перипартальная кардиомиопатия (ПКМП) относится к достаточно редким заболеваниям, однако ассоциируется со значительной материнской смертностью. ПКМП — опасное для жизни заболевание неизвестной этиологии, которое развивается у ранее здоровых женщин в перипартальный период и характеризуется развитием систолической дисфункции левого желудочка (ЛЖ) и симптоматической сердечной недостаточности (СН) в течение последнего месяца беременности или 5 мес после родов.
Перипартальная кардиомиопатия (ПКМП) относится к достаточно редким заболеваниям, однако ассоциируется со значительной материнской смертностью. ПКМП — опасное для жизни заболевание неизвестной этиологии, которое развивается у ранее здоровых женщин в перипартальный период и характеризуется развитием систолической дисфункции левого желудочка (ЛЖ) и симптоматической сердечной недостаточности (СН) в течение последнего месяца беременности или 5 мес после родов.
Согласно определению Европейского общества кардиологов, ПКМП — форма дилатационной кардиомиопатии (ДКМП), для которой характерно развитие признаков СН в течение последнего
месяца беременности или первых 5 мес после родов. ПКМП встречается относительно редко. Заболеваемость ПКМП колеблется от 1 случая на 1300 до 1 случая на 15 тыс. женщин, родивших живых детей [68] (в среднем — 1 случай на 2289 рожениц).
К факторам риска развития ПКМП относят:
- возраст. ПКМП может развиваться у женщин любого возраста, однако наиболее высокую заболеваемость наблюдают у беременных старше 30 лет;
- количество беременностей и родов. Многорожавших женщин относят к группе риска ПКМП;
- многоплодную беременность;
- гестационную АГ. Согласно данным литературы, частота гестационной артериальной гипертензии (АГ) у больных с ПКМП колеблется от 8–10% [14] до 43%;
- преэклампсию, которую диагностируют у 22% у больных ПКМП;
- этническое представительство;
- генетическую предрасположенность;
- токолитическую терапию;
- употребление кокаина.
Механизмы поражения кардиомиоцитов при ПКМП до конца неясны. Их повреждение может развиваться вследствие вирусной инфекции, генетических нарушений и токсемии с участием аутоиммунных механизмов. Существуют доказательства этиологической роли вирусных миокардитов в развитии ДКМП как в эксперименте на животных, так и у людей.
Рассматривается роль в патогенезе ПКМП пролактина, релаксина, образования иммунных комплексов, сердечной NO-синтетазы, незрелых дендритных клеток, сердечного дистрофина, толлподобных рецепторов (от англ. toll-like receptors), дефицита селена, повышающего чувствительность миокарда к повреждающим воздействиям и активации оксидантного стресса.
Клинические проявления ПКМП
Клинические проявления ПКМП обусловлены развитием систолической дисфункции ЛЖ и сходны с таковыми при идиопатической ДКМП.
Такие симптомы, как одышка, головокружение, отеки нижних конечностей могут наблюдаться и при нормально протекающей беременности. Одышку при беременности связывают с гипервентиляцией, вызванной прогестероном, а также давлением растущей матки на диафрагму. Периферические отеки имеют примерно две трети здоровых беременных. Однако при внезапном появлении отеков и других симптомов СН необходимо исключать ПКМП.
Клинические проявления ПКМП, кроме симптомов застойной СН, могут включать нарушения ритма сердца и тромбоэмболические осложнения. Во время беременности риск тромбоэмболических осложнений возрастает из-за высокой концентрации II, VII, VIII, X факторов свертывания крови и фибриногена, а также может быть связан с дилатацией полостей сердца, систолической дисфункцией и наличием фибрилляции предсердий. Повышенный риск их возникновения может сохраняться до 6 нед после родов.
Описаны также случаи бессимптомного течения этого заболевания. Диагноз ПКМП является диагнозом исключения.
Критериями ПКМП являются:
- развитие СН у беременных в течение последнего месяца беременности или 5 мес после родов;
- отсутствие сердечно-сосудистых заболеваний в анамнезе до последнего месяца беременности;
- отсутствие другой причины для развития СН;
- эхокардиографические признаки систолической дисфункции ЛЖ (ФВ ЛЖ <45%).
Медикаментозное лечение ПКМП во время беременности
При медикаментозном лечении ПКМП во время беременности могут быть использованы β-адреноблокаторы, нитраты, гидралазин, дигоксин. По мнению экспертов, применение диуретиков у беременных нежелательно в связи с тем, что они ухудшают маточно-плацентарный кровоток, но
в случае необходимости их назначения следует отдавать предпочтение тиазидным или петлевым (фуросемид) диуретикам.
Ингибиторы ангиотензинпревращающего фермента (АПФ), антагонисты рецепторов ангиотензина ІІ и варфарин таким больным противопоказаны вследствие их потенциального тератогенного действия. Отрицательное воздействие ингибиторов АПФ и антагонистов рецепторов ангиотензина ІІ на плод связывают с развитием фетальной гипотензии, пороков развития и задержкой внутриутробного развития плода, дисплазией почек, анурией, олигогидрамнионом и высоким риском смертиноворожденного. Ранее считали, что отрицательное воздействие ингибиторов АПФ на плод начинается только со ІІ триместра беременности, однако недавнее исследование показало их тератогенное действие и в І триместре. В случае фибрилляции предсердий при ПКМП эффективен дигоксин. Назначение антиаритмических препаратов 3-го (амиодарон, рибоксин) и 4-го (верапамил) классов следует избегать из-за побочного действия на плод. При их применении возможно развитие фетального гипотиреоза, брадикардии, нарушений проводимости сердца и гипотензии у плода, существует риск преждевременных родов.
При лечении ПКМП в послеродовой период возможно применение всех рекомендованных Европейским обществом кардиологов для лечения острой и хронической СН медикаментозных средств: диуретиков, ингибиторов АПФ, антагонистов рецепторов ангиотензина ІІ, спиронолактона, дигоксина и β-адреноблокаторов.
Пациенты с ПКМП и низкой ФВ ЛЖ (<35%) имеют высокий риск развития тромбоэмболических осложнений и при развитии последних должны получать антикоагулянтную терапию. Во время беременности можно применять нефракциониро ванный или низкомолекулярный гепарин. Варфарин не рекомендован для лечения беременных, так как он оказывает тератогенное действие, вызывая назальную гипоплазию и хондродисплазию, атрофию зрительного нерва, катаракту с полной или частичной слепотой, задержку умственного и физического развития, микроцефалию при применении в І триместре беременности, способствует развитию спонтанных мозговых кровотечений у плода при использовании во ІІ и ІІІ триместрах беременности. Согласно рекомендациям Американского колледжа кардиологии и Американской ассоциации сердца по
лечению больных с пороками клапанов сердца, варфарин является ≪сравнительно безопасным≫ в течение ІІ и ІІІ триместров беременности, но должен быть отменен (с переходом на гепарин) за несколько недель до родов.
Эффективность и безопасность иммуносупрессивной терапии при ПКМП сегодня не доказаны, что требует проведения крупных рандомизированных исследований. Вероятно, она может быть целесообразной при верифицированном миокардите. Однако при назначении иммуносупрессивной терапии необходимо исключить миокардит вирусного генеза, так как такое лечение может способствовать активации репликации вируса с последующим ухудшением функционального состояния миокарда.
Кардиомиопатии у детейЭту группу сердечных заболеваний объединяет отсутствие убедительных данных о причинах поражения мышцы сердца.
Перспективным в терапии больных с ПКМП может быть применение внутривенного иммуноглобулина, назначение u1091 {которого способствует повышению ФВ ЛЖ, а также приводит к значительному снижению уровней цитокинов и уменьшению выраженности оксидантного стресса. В экспериментальной модели ПКМП у мышей было обнаружено повышение активности сердечного катепсина Д, который может способствовать образованию проапоптической формы пролактина с молекулярной массой 16 кД [52]. Поэтому препараты, которые препятствуют секреции пролактина (бромокриптин), могут быть эффективными в лечении больных с ПКМП. Однако эти подходы также требуют изучения в контролируемых исследованиях.
В настоящее время оценивается эффективность и безопасность при лечении больных с ПКМП cтатинов, моноклональных антител, бета-интерферона, иммуноадсорбции, терапевтического афереза и кардиомиопластики.
Прогноз при ПКМП более благоприятный, чем при идиопатической ДКМП. Пятилетняя выживаемость больных ПКМП составляет 94%, ниже у больных со стойкими симптомами СН на протяжении 6 мес и более. Согласно результатам исследований, проведенных K. Sliwa et al. [91], восстановление функционального состояния сердца обычно происходит в течение 6 мес, однако может длиться и дольше. Нормализацию функционального состояния ЛЖ отмечают у 51–54% больных, но среди женщин негроидной расы — реже, только в 23% случаев. Восстановление параметров систолической функции ЛЖ сердца чаще наблюдают у пациенток с ФВ ЛЖ не ниже 27–30% или конечно-систолическим размером ЛЖ, не превышающим 5,5 см.
Ранняя диагностика, своевременное и адекватное лечение застойной СН, антикоагулянтная терапия и профилактика внезапной смерти улучшают прогноз при этом заболевании. Повторные беременности повышают риск рецидива ПКМП даже у женщин с восстановившимися параметрами систолической функции ЛЖ.
Литература
1. Каминский, В.В. Токолитическая терапия: новые возможности/В.В. Каминский. С.И. Жук//Жіночийлікар. – 2008. – № 6. – C. 3.
2. Amos A.M., Jaber W.A., Russell S.D. Improved outcomes in peripartum cardiomyopathy with contemporary//Am. Heart J. – 2006. – Vol. 152. – P. 509–513.
3. Andrade S.E., Raebel M.A., Brown J. et al. Outpatient use of cardiovascular drugs during pregnancy//Pharmacoepidemiol. Drug Saf. – 2008. – Vol. 17. – P. 240–247.
4. Ansari A.A., Fett J.D., Carraway R.E. et al. Autoimmune mechanisms as the basis forhuman peripartum cardiomyopathy//Clin. Rev. Allergy Immunol. – 2002. – Vol. 23. –P. 301–324.
5. Benlolo S., Lefoll C., Katchatouryan V. et al. Successful Use of Levosimendan in a Patient with Peripartum Cardiomyopathy//Anesth. Analg. – 2004. – Vol. 98. – P. 822–824.
6. Boldrini L., Faviana P., Pistolesi F. et al. Alterations of Fas (APO-1/CD 95) gene and its relationship with p53 in non small cell lung cancer//Oncogene. – 2001. – Vol. 20. – P. 6632–6637.
7. Bonow R.O., Carabello B.A., Chatterjee K. et al. 2006 Writing Committee Members, American College of Cardiology/American Heart Association Task Force. 2008 Focused update incorporated into the ACC/AHA 2006 guidelines for the management of patients with valvular heart disease: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to Revise the 1998 Guidelines for the Management of Patients With Valvular Heart Disease): endorsed by the Society
of Cardiovascular Anesthesiologists, Society for Cardiovascular Angiography and Interventions, and Society of Thoracic Surgeons// Circulation. – 2008. – Vol. 118. – P. e523–e661. 8. Bosch T. Therapeutic apheresis—state of the art in the year 2005//Ther. Apher. Dial. – 2005. – Vol. 9. – P. 459–468.
9. Bozkurt B., Villaneuva F.S., Holubkov R. et al. Intravenous immune globulin in the therapy of peripartum cardiomyopathy//J. Am. Coll. Cardiol. – 1999. – Vol. 34. – P. 177–180.
10. Briggs G.G. Drug effects on the fetus and breast-fed infant//Clin. Obstet. Gynecol. –2002. – Vol. 45. – P. 6–21.
11. Brown M.A., Mackenzie C., Dunsmuir W. et al. Can we predict recurrence of preeclampsia or gestational hypertension?//BJOG. – 2007. – Vol. 114. – P. 984–993.
12. Bultmann B.D., Klingel K., Nabauer M. et al. High prevalence of viral genomes and inflammation in peripartum cardiomyopathy//Am. J. Obstet. Gynecol. – 2005. –
Vol. 193. – P. 363–365.
13. Chapa J.B., Heiberger H.B., Weinert L. et al. Prognostic value of echocardiography in peripartum cardiomyopathy//Obstet. Gynecol. – 2005. – Vol. 105. – P. 1303–1308.
14. Chari R.S., Frangieh A.Y., Sibai B.M. et al. Hypertension during pregnancy: diagnosis, pathophysiology and management. In: Elkayam U., Gleicher N. eds. Cardiac Problems in Pregnancy. 3rd ed. New York, NY: Wiley-Liss. – 1998. – P. 257–273.
15. Cho S., Atwood J.E. Peripheral edema//Am. J. Med. – 2002. – Vol. 113. – P. 580–586.
16. Clark N.P., Delate T., Witt D.M. et al. A descriptive evaluation of unfractionated heparin use during pregnancy//J. Thromb. Thrombolysis – 2008, epub March 8.
17. Cooper W.O., Hernandez-Diaz S., Arbogast P.G. et al. Major congenital malformations after first-trimester exposure to ACE inhibitors//N. Engl. J. Med. – 2006. – Vol. 354. – P. 2443–2451.
Перипартальная кардиомиопатия
ПКМП (от лат. partus — роды) — систолическая дисфункция ЛЖ, характеризующаяся следующими дополнительными критериями:
- возникновение симптомов за 1 мес до родов или в течение первых 5 мес после них;
- отсутствие заболевания сердца в анамнезе;
- отсутствие любых других причин, обусловливающих возникновение патологических изменений сердца.
Таким образом, указанные критерии исключают заболевания сердца, которые могут манифестировать в условиях гемодинамического стресса во время нормальной беременности.
Распространенность и этиология
Истинная заболеваемость не установлена, хотя, по данным литературы, она составляет от одного случая на 3 тыс. беременностей до одного случая на 10 тыс. беременностей. Эти показатели, возможно, занижены, так как невыраженные формы ПКМП, вероятно, остаются нераспознанными в связи с часто развивающейся в последнем триместре беременности одышкой при физической нагрузке и отеками нижних конечностей.
Этиология ПКМП до сих пор остается неизвестной (табл. 1). Анализ результатов биопсии показал, что почти в 62% случаев присутствуют признаки воспаления, т.е. миокардита. Тем не менее связь между существованием миокардита и развитием ПКМП не доказана. В качестве возможных факторов, предрасполагающих к развитию ПКМП, рассматривают плохое питание, проживание в определенных географических районах и низкую концентрацию селена в крови.
С другой стороны, ПКМП регистрируют и у тех женщин, которые питаются полноценно. Ранее было высказано предположение о роли вирусной инфекции, но в этом случае сложно объяснить рецидив заболевания при последующих беременностях. Вызывает определенный интерес теория о возможном участии патологического иммунного ответа, возникающего при беременности и играющего определенную роль в патогенезе развития эклампсии. Описаны случаи семейного возникновения ПКМП. Наиболее вероятное объяснение развития этого заболевания — предложение рассматривать ПКМП как вариант семейной формы ДКМП, протекающей субклинически и манифестирующей при беременности. В пользу этой теории свидетельствуют многочисленные факты, требующие, тем не менее, дальнейшей проспективной оценки.
Таблица 1
Факторы риска развития перипартальной кардиомиопатии
|
Источники: De Beus E., van Mook W.N., Ramsay G. et al. Peripartum cardiomyopathy: a condition intensivists should be aware // Intensive Care Med. — 2003. — Vol. 29. — P. 167-174 и James P.R. A review of peripartum cardiomyopathy // Int. J. Clin. Pract. — 2004. — Vol. 58. — P. 363-365.
Клиническая картина
У больных ПКМП обычно присутствуют такие признаки ЛЖ-СН, как ортопноэ и пароксизмальная ночная одышка. Также обнаруживают повторные мономорфные ЖТ и системные тромбоэмболии.
Данные физикального обследования достаточно сложно интерпретировать, что связано с тем, что III тон и шум систолического изгнания выслушивают при аускультации у более чем 90% здоровых беременных.
Кроме того, небольшое отклонение влево оси комплекса QRS на ЭКГ во время беременности считают нормой.
При ПКМП часто отмечают неспецифические изменения сегмента ST, а также наджелудочковую или желудочковую ЭС. Основным методом диагностики заболевания считают 2D-ЭхоКГ, при проведении которой необходимо оценивать систолическую функцию ЛЖ. Некоторые авторы рекомендуют следующие ЭхоКГ-критерии: ФВ ЛЖ менее 45% и (или) фракция укорочения менее 30% в сочетании с КДР ЛЖ 2,7 см/м2 площади поверхности тела. Также обнаруживают дилатацию камер сердца (особенно через 1 мес после родов).
Лечение
При ПКМП назначают стандартное лечение СН. При кардиогенном шоке применяют баллонную аортальную контрпульсацию. Больных с ПКМП при отсутствии тяжелых симптомов заболевания можно наблюдать амбулаторно. Назначение иАПФ и антагонистов ангиотензиновых рецепторов после I триместра беременности противопоказано в связи с возможным неблагоприятным воздействием на плод (маловодие и его последствия, деформация конечностей, нарушение окостенения черепных костей, гипоплазия легких) и новорожденного (артериальная гипотензия и ХПН). Тем не менее есть данные об эффективности иАПФ с коротким периодом полувыведения, применяемых в малых дозах в качестве «терапии отчаяния» в небольших группах беременных с тяжелой устойчивой артериальной гипертензией. Ранее была проведена оценка количества околоплодных вод на фоне лечения иАПФ (в процессе подбора дозы).
Со стороны плода или новорожденного не было зарегистрировано никаких осложнений. У матерей отмечено улучшение гемодинамики и успешное течение беременности.
При многоцентровом исследовании клинического течения ПКМП 6% перинатологов сообщили об использовании иАПФ во время беременности. При тяжелой рефрактерной СН перед назначением иАПФ необходимо оценить потенциальный риск для плода и предполагаемую пользу для матери и проводить лечение таким образом, чтобы, по возможности, обеспечить положительный эффект как для матери, так и для ребенка.
Для беременности характерно физиологическое повышение свертываемости крови. Риск возникновения тромбоэмболии еще более усиливается при соблюдении постельного режима, приеме диуретиков, а также на фоне нарушения сократительной функции желудочков. Во время беременности рекомендовано назначение профилактических доз низкомолекулярного гепарина. Варфарин можно применять только после родоразрешения.
Прогноз
Данные об отдаленном прогнозе крайне вариабельны. У многих пациентов регресс симптомов сопровождается полным или частичным восстановлением функции ЛЖ. У больных с терминальной стадией СН прогноз сомнителен. При ретроспективной оценке данных исследования, в котором участвовали 42 больных ПКМП, а срок наблюдения составлял около восьми лет, летальный исход был зарегистрирован в 7% случаев. Примерно такому же числу больных была выполнена трансплантация сердца. В 43% случаев отмечена нормализация функции ЛЖ.
Результаты ранее проведенных клинических исследований демонстрировали менее благоприятные клинические исходы, а смертность достигала 56%. В результате ухудшения насосной функции сердца может наступить летальный исход. Также возможно развитие системных тромбоэмболий и желудочковых тахиаритмий. Прогностические факторы, ассоциированные с высоким риском неблагоприятного исхода, в настоящее время неизвестны. Тем не менее рекомендована комбинированная стратегия ранней диагностики заболевания и тактика агрессивного медикаментозного лечения.
Консультирование пациентов с ПКМП при планировании беременности представляет серьезную проблему, что связано с возможностью рецидива СН. Высказано предположение, что субклиническая желудочковая дисфункция сохраняется у многих больных, и гемодинамическая нагрузка при следующей беременности может спровоцировать декомпенсацию заболевания. Провоцирующим фактором может быть и обострение заболеваний, связанных с беременностью. При обследовании женщин с ПКМП и повторными беременностями обнаружено:
- развитие дисфункции ЛЖ и ухудшение клинического состояния матери;
- повышение частоты возникновения осложнений у женщин с неполным восстановлением функции желудочков до 50%.
Описаны случаи материнской смертности. В этой подгруппе также зарегистрировано увеличение частоты выкидышей и рождения недоношенных детей.
Женщины, у которых функция желудочков нормализовалась, имеют низкий риск летального исхода. В 20% случаев диагностируют клинически выраженную СН, которая в дальнейшем может привести к стойкому ухудшению функции ЛЖ. Именно поэтому необходимо регулярное обследование таких пациентов.
Дальнейшие перспективы
Болезни миокарда представлены широким спектром наследственных и приобретенных заболеваний сердечной мышцы. Термин «кардиомиопатия» долгое время использовался для описания первичных форм поражения миокарда неизвестной этиологии. Тем не менее в последние несколько лет стало очевидным, что большинство первичных форм представлены наследственными заболеваниями, возникающими в результате мутаций генов, ответственных за синтез саркомерных белков в случае ГКМП и за белки цитоскелета в случае ДКМП.
Вторичные формы представлены ГКМП- или ДКМП-подобными КМП, и также, как правило, имеют наследственный характер (например, амилоидоз, гемохроматоз, болезни накопления гликогена, болезнь Фабри). Истинные вторичные формы заболеваний миокарда, такие как ишемическая, алкогольная или гипертоническая КМП, также генетически детерминированы и могут имитировать сердечный фенотип ГКМП или ДКМП. Таким образом, большинство заболеваний миокарда представлены наследственными заболеваниями.
Otto M. Hess, William McKenna и Heinz-Peter Schultheiss
Болезни миокарда
Опубликовал Константин Моканов
симптомы, особенности диагностики и лечения у беременных

Кардиомиопатии (КМП) – группа заболеваний, каждое из которых проявляется поражением сердечной мышцы и нарушением ее функции с развитием сердечной недостаточности. Общим для всех КМП является неустановленная причина болезни.
Выделяют следующие разновидности КМП:
- дилатационная;
- гипертрофическая;
- рестриктивная.
У беременных женщин описана также особая форма КМП – перипартальная.
Дилатационная кардиомиопатия

Дилатационная КМП – распространенное поражение сердечной мышцы, сопровождающееся расширением (дилатацией) всех полостей сердца. В результате резко снижается сократительная способность миокарда, то есть сердце начинает слабо сокращаться и плохо перекачивать кровь. Уменьшается сердечный выброс – количество крови, изгоняемой из полости левого желудочка при каждом его сокращении. Развивается застойная сердечная недостаточность.
Дилатационная КМП – неоднородная группа заболеваний. Она может быть врожденной или приобретенной. Этот вид встречается у 60% всех больных с КМП. Причину болезни установить часто невозможно. Считается, что одним из вариантов является скрытое течение миокардита, вызванного вирусами гриппа, Коксаки и другими. Определенное значение имеет алкоголизм, сахарный диабет, другие состояния, протекающие с нарушением обмена веществ внутри клеток.
Беременность ухудшает симптоматику дилатационной КМП и вызывает развитие осложнений этого заболевания. Обычно при диагностированном заболевании, даже при нормальном самочувствии, женщине рекомендуют воздержаться от наступления беременности. Риск ухудшения состояния во время беременности или после родов очень высок. Ответственность за принятие такого решения остается за женщиной.
Если беременность все же наступила, тактика определяется показателями сократимости сердца, которые определяются с помощью эхокардиографии (ЭхоКГ). Самым важным является показатель фракции выброса: отношение выбрасываемой во время сокращения сердца крови к объему левого желудочка. Чем ниже фракция выброса, тем слабее сокращается сердце. При уровне этого показателя менее 40% рекомендуется наблюдение и лечение в специализированном роддоме. Если фракция выброса ниже 20%, рекомендуется прерывание беременности, потому что ее сохранение опасно для жизни женщины.
Лечение включает следующие группы препаратов:
- мочегонные (тиазидные и петлевые диуретики), которые выводят излишки жидкости из организма и тем самым уменьшают нагрузку на сердце;
- сердечные гликозиды, которые усиливают сократимость миокарда и повышают эффективность работы сердца;
- кардиоселективные бета-адреноблокаторы, замедляющие пульс и влияющие на течение сердечной недостаточности;
- антиаритмические препараты при появлении тяжелых нарушений сердечного ритма;
- низкомолекулярные гепарины или антагонисты витамина К у женщин с нарушениями ритма сердца для предупреждения тромбоэмболических осложнений.
Гипертрофическая кардиомиопатия
Гипертрофическая КМП считается заболеванием с неизвестной причиной. Однако в настоящее время выделено более 50 генов, мутации которых вызывают нарушение строения белка в клетках миокарда. Появление таких генетических изменений приводит к развитию этого заболевания. Наследуются эти мутации по аутосомно-доминантному типу. Это означает, что у больного родителя с очень высокой вероятностью будет больной ребенок.
Среди всего населения гипертрофическая КМП наблюдается у 2 – 5 человек из 10000. У четверти больных развивается обструктивная гипертрофическая КМП, у остальных – необструктивная ее форма. Проявления болезни зависят прежде всего от диастолической дисфункции сердца, то есть от нарушения его способности расслабляться. Основные симптомы включают одышку, головокружения и обмороки, боли в сердце в результате ишемии миокарда и нарушения сердечного ритма (экстрасистолия, пароксизмальная наджелудочковая тахикардия, различные блокады).
При планировании беременности женщинам с обморочными состояниями или тяжелыми аритмиями необходимо решить вопрос о хирургической операции по поводу гипертрофической КМП.
У большинства женщин беременность не оказывает неблагоприятного влияния на кровообращение. Основная опасность заключается в развитии тяжелых нарушений сердечного ритма.
При легком течении болезни пациентку раз в месяц должен осматривать кардиолог. Госпитализируется она в сроки, обычные для всех беременных с сердечно-сосудистыми заболеваниями. Роды проходят через естественные родовые пути.
Если выносящий тракт левого желудочка сужен умеренно, осуществляют индивидуальное наблюдение. Сроки госпитализации обычные, при необходимости чаще. Роды могут быть естественными, но с исключением потуг.
При тяжелой обструкции (сужении) выносящего тракта и градиенте давления 50 мм рт. ст. и выше беременность противопоказана. Если женщина настаивает на сохранении беременности, проводится госпитализация практически на все время вынашивания ребенка. Родоразрешение происходит с помощью операции кесарева сечения. При этом эпидуральная анестезия должна выполняться с большой осторожностью из-за риска расширения сосудов и резкого падения артериального давления.
Для медикаментозного лечения аритмий чаще всего назначают бета-адреноблокаторы или верапамил. Довольно часто приходится прибегать к хирургическому лечению: удалению части межжелудочковой перегородки, препятствующей нормальному току крови. В результате во многих случаях развивается полная атриовентрикулярная блокада, требующая установки электрокардиостимулятора.
Рестриктивная кардиомиопатия
Название болезни происходит от латинского слова, означающего ограничение. Эта болезнь проявляется значительным нарушением диастолической функции миокарда. Это значит, что сердце плохо расслабляется, стенки не растягиваются, объем желудочков в диастолу не увеличивается, и насосная функция резко ограничивается. Развивается сердечная недостаточность.
Клетки миокарда в таких условиях гибнут и замещаются соединительной тканью. Поражаются и сердечные клапаны. Развиваются тяжелые нарушения сердечного ритма.
Рестриктивная КМП – редкое состояние. Чаще всего она возникает как осложнение других заболеваний – амилоидоза, гемохроматоза, эндомиокардиального фиброза, эозинофильного эндомиокардита Леффлера. Вероятно развитие этой болезни под действием ионизирующей радиации, а также интоксикаций, в частности, антрациклинами.
Рестриктивная КМП – противопоказание для вынашивания беременности.
Перипартальная кардиомиопатия
 Этот вид кардиомиопатии возникает во время беременности, может иметь тяжелое течение и угрожать жизни женщины. Обычно при правильном лечении состояние таких больных нормализуется через некоторое время после родов.
Этот вид кардиомиопатии возникает во время беременности, может иметь тяжелое течение и угрожать жизни женщины. Обычно при правильном лечении состояние таких больных нормализуется через некоторое время после родов.Перипартальная КМП – состояние, специфическое для беременности. Оно возникает у одной женщины из 3000 – 4000 беременных, имеет тяжелое течение и неблагоприятный прогноз.
Факторы риска:
- многоплодная беременность;
- многократные беременности в анамнезе;
- наследственная предрасположенность;
- курение;
- сахарный диабет;
- артериальная гипертензия;
- несбалансированное питание;
- беременность в подростковом или позднем возрасте;
- длительный прием агонистов бета-2-адренорецепторов (например, по поводу бронхиальной астмы).
Точные причины и механизм развития заболевания неизвестны. Предполагается, что в его развитии участвуют инфекция, воспаление или аутоиммунное поражение.
Клинические перипартальная КМП проявляется в конце беременности или в первые месяцы после родов. Ее симптомы связаны с систолической дисфункцией миокарда, то есть со снижением его сократимости. При этом развивается сердечная недостаточность, включающая одышку, отеки, слабость, нарушения ритма и другие проявления. Такое заболевание нужно подозревать у всех женщин, которые плохо восстанавливаются после родов.
Большую опасность представляет острая сердечная недостаточность, например, отек легких, и жизнеугрожающие желудочковые аритмии. Встречаются случаи внезапной смерти у таких пациенток.
Диагностируется перипартальная КМП путем исключения других причин сердечной недостаточности. Для ее лечения используют кардиоселективные бета-адреноблокаторы, гидралазин, нитраты. После родов можно применять ингибиторы ангиотензинпревращающего фермента. Во время грудного вскармливания не противопоказаны эналаприл, каптоприл, беназеприл.
Фуросемид и гипотиазид применяют при застое крови в малом круге кровообращения, поскольку они способны ухудшать маточно-плацентарный кровоток. В послеродовом периоде возможно использование антагонистов альдостерона. Для поддержки работы сердца назначают допамин.
Если медикаментозные способы не могут обеспечить насосную функцию сердца, применяются вспомогательные методы, в частности, интрааортальная баллонная контрпульсация и искусственный левый желудочек.
У большинства пациенток работа сердца нормализуется в течение нескольких месяцев после родов. Если этого не произошло, устанавливают кардиовертер-дефибриллятор. Это устройство помогает сердцу работать в нормальном ритме и восстанавливает его деятельность при развитии тяжелых аритмий. В некоторых случаях рассматривают показания к пересадке сердца.
Если выраженных нарушений кровообращения нет, роды предпочтительнее вести через естественные родовые пути, используя эпидуральную анестезию. Неотложную операцию кесарева сечения проводят на любом сроке при нестабильных показателях кровообращения и тяжелой сердечной недостаточности.
После родов часто рекомендуют подавление лактации, поскольку этот процесс требует большой нагрузки на сердце.
При повторной беременности риск рецидива перипартальной КМП составляет от 30 до 50%, поэтому снова беременеть женщине не рекомендуется.
ПЕРИПАРТАЛЬНАЯ КАРДИОМИОПАТИЯ (ОПЫТ ЛЕЧЕНИЯ) |
Возникновение без видимой причины кардиомегалии и застойной сердечной недостаточности после родов у ранее здоровых женщин было впервые описано Германом и Кингом в 1930 году. [1]
В период с 2008 года по 2014 год в кардиологическом отделении АКБ ФГБУЗ ЮОМЦ ФМБА России находились на лечении три молодые женщины, у которых в послеродовом периоде развилась сердечная недостаточность на фоне дилятации полостей сердца, что было расценено как проявление перипартальной (послеродовой) кардиомиопатии.
В настоящее время этот термин включает в себя тяжелую патологию, развившуюся в третьем триместре беременности или раннем послеродовом периоде, характеризующуюся неблагоприятным прогнозом с высокой частотой развития дилятационной кардиомиопатии или наступления смерти.
Для развернутой клинической картины данного заболевания характерны одышка, тахикардия, артериальная гипотония, повышенное давление в яремной вене, аускультативно признаки ритма «галопа», систолический шум вследствии относительной недостаточности атрио-вентрикулярных клапанов, гепатомегалия и отеки.
При обзоре литературы [2] установлено, что в настоящее время основными диагностическими критериями послеродовой кардиомиопатии являются
- развитие сердечной недостаточности в последние месяцы беременности или первые 5 месяцев после родов,
- отсутствие другой установленной причины кардиомегалии и сердечной недостаточности,
- отсутствие какой — либо болезни сердца до последнего месяца беременности,
- дисфункция левого желудочка по данным ЭХОКС,
- фракция выброса левого желудочка менее 45 % или фракция укорочения менее 30 %.
В нашем кардиологическом отделении послеродовая кардиомиопатия представлена следующими клиническими случаями.
- Больная З., 32 лет, чеченка по национальности, поступила с жалобами на выраженную одышку при незначительной физической нагрузке, усиливающуюся в положении лежа, сухой кашель в ночное время, учащенное сердцебиение, тяжесть в правом подреберье.
Заболела через 3 месяца после преждевременных пятых родов. Со слов больной страдала тяжелым токсикозом (отеки, повышенное артериальное давление), после родов было кровотечение, ручное отделение последа.
При поступлении состояние больной тяжелое, передвигалась с трудом из-за выраженной инспираторной одышки, отмечались массивные отеки голеней и стоп, синусовая тахикардия 120 ударов в 1 минуту. В легких дыхание ослаблено в нижнебоковых отделах с обеих сторон, хрипы не выслушивались, верхушечный толчок определялся в 6 межреберье по передней подмышечной линии. Границы относительной тупости сердца расширены вправо на 1,5 см от края грудины и влево до передне-подмышечной линии. Тоны сердца приглушены. На легочной артерии и верхушке сердца выслушивался систолический шум, проводящийся в подмышечную область и под левую лопатку. АД – 140/90 мм.рт.ст. Печень увеличена на 12 см из-под реберной дуги, болезненная.
При инструментальном обследовании выявлены следующие изменения: ЭКГ – синусовая тахикардия 112-113-108 уд в 1 мин. Гипертрофия левого предсердия и левого желудочка. Нарушение внутрижелудочковой проводимости.
ЭХОКС – дилятация левого желудочка и левого предсердия. Снижение глобальной сократительной способности миокарда левого желудочка (фракция выброса 43%). Митральная регургитация III ст. Свободная жидкость в полости перикарда до 150 мл.
УЗИ органов брюшной полости и почек – гепатомегалия, расширенные печеночные вены, спленомегалия , на рентгенограмме органов грудной клетки –обогащение легочного рисунка за счет застойных изменений, в нижнелатеральных отделах облитерация синусов как следствие выпота в плевральную полость. Сердце шаровидной формы. Дуги сглажены. Справа вверху выбухающая верхняя полая вена как признак застоя в большом круге кровообращения.
Клинические и биохимические анализы крови, анализы мочи без патологических изменений, при консультации гинеколога заболеваний не выявлено.
Во время лечения в стационаре отмечалась склонность к артериальной гипотонии. На фоне проводимой терапии (препараты калия, дигоксин, лазикс, верошпирон, клексан, реополиглюкин, диротон) самочувствие и состояние больной значительно улучшились: уменьшилась одышка, купированы явления сердечной астмы, сократилась печень, исчезли отеки, нормализовалось АД. По данным контрольной ЭХОКС фракция выброса левого желудочка возросла до 52 %, исчезла свободная жидкость в перикарде, рентгенологически не определялась жидкость в плевральных полостях, уменьшились застойные изменения в легких. Учитывая связь заболевания с беременностью, быстрый эффект от проводимой терапии, нормальные показатели крови выставлен диагноз перипартальной кардиомиопатии. Больная выписана с рекомендациями приема конкора 2,5 мг/сутки, кардиомагнила, диротона 2,5 мг на ночь, диувера 10 мг утром, дигоксина 0,25 мг ½ таб. в сутки. Известно, что в настоящее время больная жива, ведет активный образ жизни.
- Больная И., 28 лет, казашка по национальности, поступила с жалобами на одышку при незначительной физической нагрузке, разговоре, сердцебиение, слабость, тошноту, рвоту. Заболела через 4 месяца после вторых родов, когда появились одышка при ходьбе, слабость, тошнота и рвота. Лечилась по месту жительства по поводу ревматического порока, так как появились шумы при аускультации сердца.
При осмотре выявлены пастозность голеней и стоп, расширение левой граница сердца до передней подмышечной линии, увеличение печени на 2 см из-под реберной дуги.
При обследовании на ЭКГ – синусовая тахикардия до 100 ударов в минуту. Гипертрофия левого предсердия и левого желудочка с изменениями в миокарде переднебоковой стенки. Единичная желудочковая экстрасистола.
При ЭХОКС – дилятация всех полостей сердца. Умеренная легочная гипертензия (систолическое давление 51 мм.рт.ст.), митральная регургитация IV ст. Снижение глобальной сократительной способности левого желудочка (фракция изгнания — 41% ).
Рентгенологически выявлено обогащение легочного рисунка в прикорневой зоне и расширение сердечно-сосудистой тени в поперечнике за счет левых отделов.
При исследовании крови воспалительных изменений не обнаружено. Получала лазикс, верошпирон, эгилок, берлиприл, препараты калия.
После проведенного лечения самочувствие улучшилось, одышка уменьшилась, стала активнее. По данным ЭХОКС фракция изгнания увеличилась до 48%, размер полости левого желудочка уменьшился с 7,5 см до 7,0 см.
Однако через 2,5 месяца больная вновь поступила с теми же жалобами, что при первичной госпитализации. При обследовании выявлена существенная отрицательная динамика: на ЭКГ данные за гипертрофию обоих предсердий и желудочков, появилось нарушение сердечного ритма по типу желудочковой и наджелудочковой бигимении, по данным ЭХОКС фракция выброса уменьшилась с 48% до 32%, увеличились размеры полостей обоих желудочков, левого предсердия. Появился выпот в плевральных полостях. Показатели крови оставались в пределах нормы, в том числе острофазовые показатели. На фоне терапии в соответствии со стандартами лечения ХСН уменьшилась одышка, исчезли отеки. Выписана с клиническим улучшением. Дальнейшая судьба больной неизвестна.
- Больная К., 33 лет, по национальности кореянка, ранее ничем не болевшая, через месяц после вторых родов стада отмечать одышку при незначительной физической нагрузке, приступы сердечной астмы в ночное время, сердцебиение, отёки голеней и стоп, тяжесть в правом подреберье, в связи с чем обратилась за медицинской помощью.
При осмотре ослабленное дыхание в нижних отделах лёгких, тахикардия, ритм сердечной деятельности правильный, склонность к гипотонии, расширение левой границы сердца, увеличенная на 4 см болезненная печень.
Рентгенологически — обогащение лёгочного рисунка, расширенная в поперечнике сердечно-сосудистая тень.
При обследовании на ЭКГ – синусовая тахикардия 103 уд в 1 мин. Изменение реполяризации в миокарде передне-перегородочной, боковой стенок.
ЭХОКС – дилятация левого желудочка. Снижение глобальной сократительной способности миокарда левого желудочка. Фракция выброса — 41%. Митральная регургитация II ст.
Клинические и биохимические анализы крови без особенностей. Проведено лечение — конкор 5 мг, хартил 2,5 мг, диувер 10 мг. Выписана с улучшением. В настоящее время чувствует себя удовлетворительно, жалоб не предъявляет, пульс 80 уд в 1 мин. По данным ЭКГ – вариант нормы, ЭХОКС – камеры сердца не расширены, фракция выброса — 64%.
Таким образом, у всех представленных женщин были повторные роды, сердечная недостаточность развилась в первые 5 месяцев после родов, сопровождалась дилатацией полостей сердца, снижением фракции выброса левого желудочка менее 45%, нормальными показателями клинического и биохимического исследования крови, быстрым положительным эффектом от лечения ХСН в 2-х случаях и, наоборот, прогрессированием кардиомегалии и сердечной недостаточности в одном, что позволило нам объединить эти случаи под диагнозом перипартальной кардиомиопатии.
Этиология данного заболевания в настоящее время остается неясной.
Основными предполагаемыми причинами считаются послеродовая гипертония, недостаточное и несбалансированное питание, низкое содержание селена, избыточное употребление соли и воды, миокардит, аутоиммунные реакции на повреждение миоцитов вирусами. Не исключают определенную роль клеток спермы и факта иммунизации при предыдущих беременностях, обсуждается гормональный статус при беременности, генетическая предрасположенность, нарушение адаптации к гемодинамическим изменениям, возникающим при беременности и пр.
Клиника перипартальной кардиомиопатии появляется вскоре после родов. Типичные ее проявления – задержка жидкости вплоть до анасарки, аритмии в виде рецидивирующих суправентрикулярных и желудочковых тахиаритмий, реже фибрилляции предсердий и желудочков, блокада левой ножки пучка Гиса, инфарктноподобные изменения с регистрацией в грудных отведениях комплекса QS. При ЭХОКС могут выявляться тромбы в одном или обоих желудочках.
Так как сроки формирования перипартальной кардиомиопатии не ясны, считается целесообразным проведение ЭХОКС у женщин с симптомами одышки и отечным синдромом на последних месяцах беременности или раннем послеродовом периоде. При установлении диагноза проводится традиционное лечение ХСН (петлевые диуретики, спиронолактон, ингибиторы АПФ, блокаторы рецепторов ангиотензина II, в-адреноблокаторы).
Летальность при данной патологии по разным авторам колеблется от 15 до 85%. Основные причины смерти – прогрессирующая сердечная недостаточность, тромбоэмболия, фибрилляция желудочков. Основным фактором, определяющим прогноз, является скорость восстановления функции левого желудочка. У женщин с благоприятным исходом заболевания последующая беременность в большинстве случаев приводит к развитию дисфункции левого желудочка, поэтому повторная беременность для данного контингента женщин нежелательна.
Используемая литература:
- Амосова Е.Н. Кардиомиопатии, 1999 год.
- Барбараш О.Л., Артымук Н.В., Барбараш Н.А. Дилатационная кардиомиопатия в акушерской практике — Проблемы женского здоровья № 1, том 3, 2008 год.
ПЕРИПАРТАЛЬНАЯ КАРДИОМИОПАТИЯ (ОПЫТ ЛЕЧЕНИЯ)
Written by: Лясковец Елена Юрьевна, Недорезова Наталия Станиславовна, Касаткина Наталья Сергеевна, Чекова Оксана Александровна
Published by: БАСАРАНОВИЧ ЕКАТЕРИНА
Date Published: 02/24/2017
Edition: ЕВРАЗИЙСКИЙ СОЮЗ УЧЕНЫХ_25.07.15_07(16)
Available in: Ebook
