Дефект межжелудочковой перегородки
Дефект межжелудочковой перегородки (ДМЖП) — это сброс на уровне межжелудочковой перегородки, которого в норме быть не должно и из-за которого нарушается функция сердца и всей системы кровообращения. Дефект встречается примерно у 5% новорожденных из 1000 — это второй по частоте врожденный порок сердца..
ДМЖП образуется вследствие нарушения эмбрионального развития.
Межжелудочковая перегородка преимущественно состоит из мышечной ткани, а верхняя часть значительно меньшая часть — из фиброзной ткани, ее называют мембранозной перегородкой. При этом мышечные дефекты перегородки составляют лишь до 20% всех случаев, а остальные относятся к перимембранозным. При дефекте межжедкдочковой перегородки появляются жалобы на одышку, плохую прибавку в весе, повышенную утомляемость, плохой аппетит.
Большие дефекты МЖП становятся причиной опасной сердечной недостаточности. Если дефект не диагностировали в младенчестве, то к трем годам у ребенка могут появиться жалобы боль в груди, носовые кровотечения и потери сознания.
Симптомы заболевания и диагностика
Симптомы ДМЖП зависят от размера дефекта. Небольшой дефект может не проявлять себя и не влиять на рост и развитие ребенка. При большом размере дефекта появляются симптомы сердечной недостаточности: одышка, плохая прибавка в весе, повышенная утомляемость и т.п. Без лечения может развиться серьезное осложнение — синдром Эйзенменгера. При дефектах межжелудочковой перегородки во время аускультации выслушивается грубый шум в сердце.
Для диагностики заболевания применяется рентгенография органов грудной клетки — она показывает увеличение сердца и легочного сосудистого рисунка. Также может быть назначена электрокардиограмма, которая показывает гипертрофию желудочков. Но нужно отметить, что при небольших дефектах эти исследования не всегда показательны, показатели могут быть в норме. Ключевой метод исследования при ДМЖП — эхокардиография. Она дает исчерпывающие анатомические и гемодинамические данные и позволяет установить диагноз.
Величину дефекта определяют в сравнении с диаметром аорты. Дефекты подразделяют на большие, средние и малые. При маленьких дефектах никаких симптомов заболевания не проявляется. Большие дефекты требуют операции.
Лечение
ДМЖП встречается как самостоятельное заболевание и в составе других пороков сердца.
Единственный метод лечения данной патологии — хирургический. Раньше оперативное лечение заключалось только в пластике ДМЖП в условиях искусственного кровообращения, доступ — рассечение грудины. Сегодня при благоприятной анатомии возможно лечение эндоваскулярным методом (через бедренные сосуды) или трансвентрикулярным методом (через маленький разрез, на работающем сердце).
Изолированный дефект межжелудочковой перегородки (ДМЖП)
Дефект межжелудочковой перегородки — самый частый врожденный порок сердца. Дефект, т. е. отверстие в перегородке, разъединяющей правый и левый желудочки, бывает единственным нарушением нормального развития сердца, и тогда говорят об изолированном дефекте или частью другого, более сложного порока, например, тетрады Фалло. В этом разделе мы будем обсуждать только изолированные дефекты.
е. отверстие в перегородке, разъединяющей правый и левый желудочки, бывает единственным нарушением нормального развития сердца, и тогда говорят об изолированном дефекте или частью другого, более сложного порока, например, тетрады Фалло. В этом разделе мы будем обсуждать только изолированные дефекты.
Межжелудочковая перегородка — это мощная мышечная преграда, образующая внутренние стенки как правого, так и левого желудочка, и в каждом — составляющая примерно 1/3 их общей площади. Она так же участвует в процессе сокращения и расслабления сердца при каждом цикле, как и остальные части желудочковых стенок. У плода она образуется из трех составных частей. На 4-5-ой неделе беременности все эти составные части должны точно сопоставиться и соединиться друг с другом, как в конструкторе Лего. Если же этого, по каким-то причинам, не происходит, в перегородке остается отверстие, или дефект. Вскоре после рождения и установления нормального кровотока в обоих кругах кровообращения, возникает значительная разница в давлении между левым и правым желудочками. И тогда кровь из левого желудочка начинает нагнетаться одновременно и в аорту, т.е. туда, куда и следует, и через дефект — в правый желудочек, где ее быть не должно. Т.е. при каждой систоле происходит сброс слева — направо. В такой ситуации правый желудочек вынужден работать с увеличенной нагрузкой, чтобы перекачать этот лишний объем, да к тому же, уже окисленной крови, снова в легкие и в левые отделы.
И тогда кровь из левого желудочка начинает нагнетаться одновременно и в аорту, т.е. туда, куда и следует, и через дефект — в правый желудочек, где ее быть не должно. Т.е. при каждой систоле происходит сброс слева — направо. В такой ситуации правый желудочек вынужден работать с увеличенной нагрузкой, чтобы перекачать этот лишний объем, да к тому же, уже окисленной крови, снова в легкие и в левые отделы.
Величина сброса зависит от размера и положения дефекта: он может быть небольшим и почти не сказываться на работе сердца, а может быть огромным, диаметром с устье аорты.
Типы дефектов межжелудочковой перегородки
Несколько слов о типах дефектов. Они могут быть «типичными», т.е. наиболее часто встречающимися, и занимать участок верхней части перегородки. Они могут быть мышечными, т.е. располагаться ближе к верхушке, и, наконец, высокими, под клапанами легочной артерии, единичными или множественными (т.е. больше одного).
Рассмотрим наиболее частый и «хороший» вариант.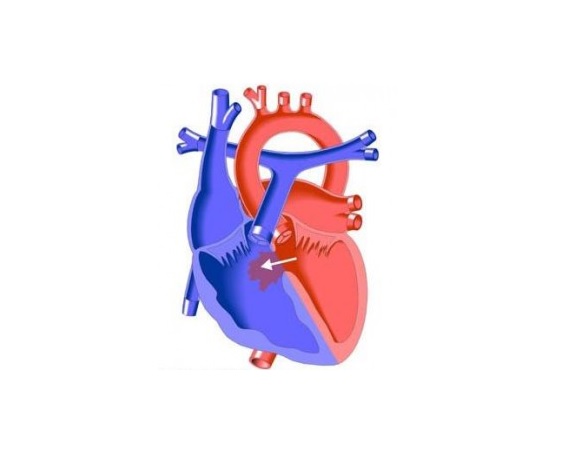 Ребенок родился нормального веса, доношенным и, конечно, очень красивым. Но вам уже в роддоме сказали, что у него есть «шум в сердце». Если там или где-то рядом есть аппарат для эхокардиографии и детский кардиолог — надо обязательно сделать исследование, чтобы понять, из-за чего этот шум, важно ли это, или — нет, скажется ли это в последующем. Но вот предположим, что на УЗИ дефект увидели, и диагноз поставлен. Ребенок, однако, выглядит нормально, хорошо ест и прибавляет в весе, ничем не болеет и, собственно, кроме шума в сердце, ни вас, ни его ничего не расстраивает. Запомните: чем громче шум, тем меньше дефект. Это ситуация, к которой замечательно подходит название известной пьесы В.Шекспира «Много шума из ничего». Сброс, который дает этот шум, можно иногда даже прощупать, если положить ладонь на левую сторону грудной клетки ребенка. Но для того, чтобы успокоиться, надо убедиться, что шум обязан только небольшому дефекту межжелудочковой перегородки и ничему другому. А для этого надо, чтобы вас наблюдал детский кардиолог, и каждые три месяца производили снятие электрокардиограммы и УЗИ.
Ребенок родился нормального веса, доношенным и, конечно, очень красивым. Но вам уже в роддоме сказали, что у него есть «шум в сердце». Если там или где-то рядом есть аппарат для эхокардиографии и детский кардиолог — надо обязательно сделать исследование, чтобы понять, из-за чего этот шум, важно ли это, или — нет, скажется ли это в последующем. Но вот предположим, что на УЗИ дефект увидели, и диагноз поставлен. Ребенок, однако, выглядит нормально, хорошо ест и прибавляет в весе, ничем не болеет и, собственно, кроме шума в сердце, ни вас, ни его ничего не расстраивает. Запомните: чем громче шум, тем меньше дефект. Это ситуация, к которой замечательно подходит название известной пьесы В.Шекспира «Много шума из ничего». Сброс, который дает этот шум, можно иногда даже прощупать, если положить ладонь на левую сторону грудной клетки ребенка. Но для того, чтобы успокоиться, надо убедиться, что шум обязан только небольшому дефекту межжелудочковой перегородки и ничему другому. А для этого надо, чтобы вас наблюдал детский кардиолог, и каждые три месяца производили снятие электрокардиограммы и УЗИ.
В большинстве случаев, примерно в 65-75%, такие дефекты закрываются сами, спонтанно, и, если не появились дополнительные симптомы, можно спокойно ждать 4-5 и даже более лет. Но, если ребенок достиг школьного возраста, оставаясь бессимптомным, то вам, тем не менее, могут операцию предложить. Дело в том, что при заболевании ребенка какой-либо детской инфекцией или даже при простом удалении испорченного зуба при наличии дефекта межжелудочковой перегородки возможно развитие эндокардита, т.е. воспалительного процесса внутренней оболочки сердечных камер. И, хотя такая вероятность очень мала — всего 1-2% случаев, она существует. В таком случае дефект закрывают скорее из профилактических, чем клинических соображений и никто не доказал, что этого не нужно делать.
Однако, прежде чем дать согласие на операцию, в таком случае, пожалуйста, не обижая никого, постарайтесь узнать, какой опыт имеется в том лечебном учреждении, куда вы обратились, какие там результаты операций, какова степень риска.
Поскольку состояние ребенка практически нормальное, а риск любого вмешательства всегда есть, то надо спокойно взвесить все. Нет, мы далеки от того, чтобы призвать вас отказаться от операции. Мы только хотим посоветовать быть очень обстоятельными, ведь никто никогда письменных гарантий вам не даст: операция есть операция, даже если ее производят в рентгенохирургическом кабинете (как вам, скорее всего, и предложат) и осложнения всегда возможны, а вы подпишете документ, подтверждающий ваше согласие. И окончательное решение — это ваша ответственность. И еще — никогда не внушайте такому ребенку, что у него — больное сердце. Не ограждайте его от доступных ему физических нагрузок, не делайте из него «инвалида». Излишнее «оберегание» и запреты могут привести к самым неблагоприятным последствиям в формировании его характера.
Но это — отдельная тема, и она касается не только ДМЖП.
Большие дефекты — это уже другая история, гораздо более опасная. Сразу после первого вздоха ребенка поток крови из левого желудочка делится на два — в аорту и в дефект, и они равны по объему! В тяжелой ситуации оказывается не только сердце, но и сосуды легких: правые отделы и сосуды легких переполняются возросшим объемом лишней крови, поступающей через дефект.
 А потом давление в правом желудочке может оказаться выше, чем в левом и тогда начинается так называемый «обратный сброс», или венозная кровь будет через дефект поступать в артериальную систему — в большой круг. Больной «синеет». Мы нарисовали эту картину, чтобы было понятно, что такой порок, как дефект межжелудочковой перегородки, который очень просто и безопасно закрыть на ранних стадиях, становится пороком, при котором закрытие теряет свой смысл, и оперировать уже поздно. Речь тут идет, напомним, только о больших дефектах или о тех случаях, когда отверстий в перегородке — несколько. К счастью, это бывает значительно реже, чем в большинстве случаев.
А потом давление в правом желудочке может оказаться выше, чем в левом и тогда начинается так называемый «обратный сброс», или венозная кровь будет через дефект поступать в артериальную систему — в большой круг. Больной «синеет». Мы нарисовали эту картину, чтобы было понятно, что такой порок, как дефект межжелудочковой перегородки, который очень просто и безопасно закрыть на ранних стадиях, становится пороком, при котором закрытие теряет свой смысл, и оперировать уже поздно. Речь тут идет, напомним, только о больших дефектах или о тех случаях, когда отверстий в перегородке — несколько. К счастью, это бывает значительно реже, чем в большинстве случаев.На что же надо обращать внимание, чтобы вовремя избежать такого развития событий?
Все сказанное выше относится только к дефектам межжелудочковой перегородки, протекающим абсолютно без жалоб, у вполне здоровых (в остальном) детей без каких-либо других признаков недостаточности сердца. На что при этом пороке надо обращать внимание?
Главный показатель периода новорожденности — прибавка веса. Предположим, грудной ребенок ест плохо, и поэтому мало прибавляет в весе. Аппетит у него нормальный, но из-за одышки ему трудно сосать, а ведь пока это его главная и довольно тяжелая работа. Он много плачет, потому что никогда не может насытиться. У детей постарше на этом фоне случаются частые простуды, которые становятся длительными и могут переходить в воспаление легких. Так может продолжаться несколько месяцев, и, если причина — ДМЖП, такой ребенок должен быть под постоянным наблюдением кардиолога, а если явления не проходят, вероятно, он будет получать сердечные препараты в виде дигоксина или наперестянки — старый добрый препарат, улучшающий работу сердца, а может быть, даже легкие мочегонные средства. У него сейчас — признаки сердечной недостаточности, с которой можно бороться консервативно. Но только пока.
Предположим, грудной ребенок ест плохо, и поэтому мало прибавляет в весе. Аппетит у него нормальный, но из-за одышки ему трудно сосать, а ведь пока это его главная и довольно тяжелая работа. Он много плачет, потому что никогда не может насытиться. У детей постарше на этом фоне случаются частые простуды, которые становятся длительными и могут переходить в воспаление легких. Так может продолжаться несколько месяцев, и, если причина — ДМЖП, такой ребенок должен быть под постоянным наблюдением кардиолога, а если явления не проходят, вероятно, он будет получать сердечные препараты в виде дигоксина или наперестянки — старый добрый препарат, улучшающий работу сердца, а может быть, даже легкие мочегонные средства. У него сейчас — признаки сердечной недостаточности, с которой можно бороться консервативно. Но только пока.
Когда же надо закрывать такой большой дефект?
На фоне лекарственной терапии симптомы могут пройти или значительно уменьшиться. Но если ничего не меняется, если размеры сердца увеличиваются и размеры дефекта на УЗИ остаются прежними – надо обращаться к хирургам.
В первые несколько месяцев жизни дефекты межжелудочковой перегородки, даже большие, могут уменьшиться или закрыться самостоятельно. Если ребенку лучше не становится — ждать нельзя, поскольку ситуация может перейти в ту, которую мы описали вначале, и оперировать будет уже поздно.
Самые лучшие результаты хирургии бывают после устранения больших ДМЖП в возрасте до двух-двух с половиной лет, когда у ребенка есть признаки сердечной недостаточности. Тогда еще все процессы обратимы. Сердце быстро понимает, что ему теперь намного легче, чем раньше. Оно быстро уменьшается в размерах и кровоток в обоих кругах нормализуется.
После операции ребенок практически здоров и нет никаких оснований причислять его к группе так называемых «инвалидов детства», как это иногда делают в лечебных учреждениях. Он может все, и быстро забудет о том, что с ним было, и кроме рубца на груди, ему об этом ничего не будет напоминать.
Итак, вам предлагают операцию, которая теперь уже необходима и абсолютно показана. Только она излечит ребенка и уберет от вас постоянное чувство угрозы его жизни. Оперирующий хирург расскажет вам, о чем идет речь в вашем случае, и что он собирается делать. Технические трудности (например, необходимость закрытия не одного, а нескольких дефектов) могут сделать операцию более сложной и продолжительной. При необычной, редкой ситуации хирург обязательно все вам объяснит, а ваша задача — попытаться понять все, что вам скажут, задать нужные вопросы и успокоиться.
Только она излечит ребенка и уберет от вас постоянное чувство угрозы его жизни. Оперирующий хирург расскажет вам, о чем идет речь в вашем случае, и что он собирается делать. Технические трудности (например, необходимость закрытия не одного, а нескольких дефектов) могут сделать операцию более сложной и продолжительной. При необычной, редкой ситуации хирург обязательно все вам объяснит, а ваша задача — попытаться понять все, что вам скажут, задать нужные вопросы и успокоиться.
Операция устранения дефекта межжелудочковой перегородки относится к открытым, поскольку нужно вскрыть полости сердца, и поэтому она делается с применением искусственного кровообращения.
Дефекты межжелудочковой перегородки закрывают ушиванием отверстия (т.е. просто накладывают несколько швов) или, чаще всего, с помощью заплатки из синтетического (или специальным образом обработанного биологического) материала, который быстро покрывается собственной тканью сердца.
Сейчас применяют и рентгенохирургические методы закрытия дефектов, но это не всегда возможно, зависит от анатомической локализации дефекта, да и квалификации рентгенохирурга тоже.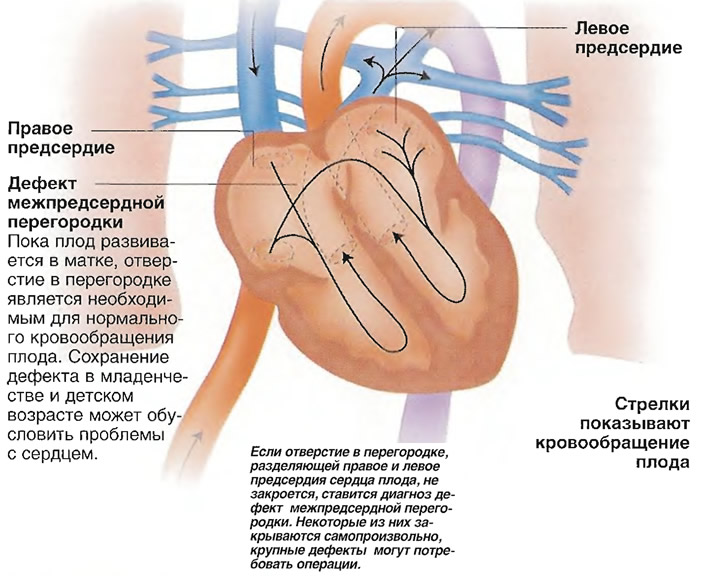 Традиционная операция по поводу дефектов межжелудочковой перегородки — одна из самых частых и отработанных в хирургии врожденных пороков сердца, а результаты ее — отличные. Так что при наличии показаний сомневаться вам не надо.
Традиционная операция по поводу дефектов межжелудочковой перегородки — одна из самых частых и отработанных в хирургии врожденных пороков сердца, а результаты ее — отличные. Так что при наличии показаний сомневаться вам не надо.
Радикальную операцию можно сделать не всегда. При очень большом дефекте у ребенка слишком малого веса, истощенного, с признаками сердечной недостаточности, которая не поддается консервативному лечению, сам фактор большой операции с искусственным кровообращением может быть опасным, особенно, когда речь идет о детях первых месяцев жизни. И тогда есть выход: разбить хирургическое лечение на два этапа – вначале помочь сердцу улучшить его состояние, а затем уже окончательно закрыть дефект.
Можно уменьшить сброс из левого желудочка в правый путем увеличения сопротивления выбросу из правого желудочка. Этим мы достигнем, снижения давления в системе легочной артерии, во-первых, ниже искусственно созданного препятствия кровотоку, выравним давление в правом и левом желудочках выше него (препятствия) и, в результате, и уменьшается объем самого сброса. А достигается это просто: на легочную артерию выше ее клапанов накладывают манжетку, которая сузит артерию примерно в ½ просвета.
А достигается это просто: на легочную артерию выше ее клапанов накладывают манжетку, которая сузит артерию примерно в ½ просвета.
Препятствие кровотоку, созданное искусственно, дает нам желаемый гемодинамический результат. Вторую операцию делается через несколько месяцев, не больше. Ни в коме случае нельзя ждать несколько лет, хотя состояние ребенка может и не внушать уже никаких опасений.
Однако послеоперационный период после операции суживания легочной артерии очень непростой, дети тяжело переносят это вспомогательное вмешательство, и именно поэтому сейчас мы стремимся к одномоментной радикальной коррекции порока. Даже тяжелые дети быстрее выходят из состояния сердечной недостаточности после радикальной коррекции порока, все угрожающие жизни симптомы постепенно исчезают.
Операция сужения легочной артерии — «вспомогательная». Она должна быть на вооружении там, где нет условий для безопасного проведения и выхаживания деток радикальной коррекции.
Заключительный этап лечения состоит из удаления этой манжеты и закрытия дефекта. Она делается уже в условиях искусственного кровообращения и не сопряжена с большим риском, особенно когда между ней и первым этапом прошел относительно небольшой срок.
Подведем итог. ДМЖП — частый врожденный порок, который может сопровождаться ранним появлением сердечной недостаточности, а в дальнейшем развитием необратимой легочной гипертензии.
Хирургическое лечение является единственным методом и позволяет полностью устранить порок и его последствия. Оно должно быть своевременным, а сама операция – безопасной. Операция может быть элективной или неотложной, но почти никогда экстренной. В некоторых случаях ее можно разделить на два этапа с промежутком в 6-12 месяцев. Появление у ребенка признаков «обратного сброса» при изолированном ДМЖП – признак упущенного времени. И при всех современных методах обследования такое осложнение никак и ничем не может быть оправдано, а часть вины ляжет и на вас, так как вы тоже не замечали или не хотели замечать того, что момент был упущен.
Врач поставил Вашему ребенку диагноз
Если вашему ребенку поставили диагноз врожденный порок сердца, не стоит опускать руки, нужно узнать все способы поддержания здоровья таких детей, а также причины развития данного заболевания, пройти необходимое обследование, чтобы врач назначил соответствующее лечение.Сердце человека состоит из четырех камер: правое предсердие (ПП) и правый желудочек (ПЖ), левое предсердие (ЛП) и левый желудочек (ЛЖ). Правые и левые отделы сердца между собой никак не сообщаются. В этом нет необходимости, так как они обеспечивают движение крови каждый по своему кругу. Левые отделы сердца отвечают за движение крови по большому кругу кровообращения. Из левого предсердия через левый желудочек в аорту (Ао) поступает артериальная кровь, богатая кислородом. Из аорты по многочисленным артериям, а потом и по капиллярам она разносится по всему организму, доставляя клеткам кислород. В свою очередь, «отработанная» организмом венозная кровь собирается в мелкие вены, которые сливаются в более крупные венозные сосуды – верхнюю и нижнюю полые вены (ВПВ и НПВ).
 Конечная точка путешествия венозной крови – правое предсердие. Оттуда через правый желудочек кровь попадает в легочную артерию (ЛА). Малый круг кровообращения проходит через легкие, где венозная кровь обогащается кислородом и вновь становится артериальной. Отток обновленной крови осуществляется по легочным венам (ЛВ), впадающим, в свою очередь, в левое предсердие.
Конечная точка путешествия венозной крови – правое предсердие. Оттуда через правый желудочек кровь попадает в легочную артерию (ЛА). Малый круг кровообращения проходит через легкие, где венозная кровь обогащается кислородом и вновь становится артериальной. Отток обновленной крови осуществляется по легочным венам (ЛВ), впадающим, в свою очередь, в левое предсердие.Особенности кровообращения у плода и новорожденного
Находясь в утробе матери, плод не дышит самостоятельно и его легкие не функционируют. Кровообращение осуществляется через плаценту. Насыщенная кислородом кровь матери поступает к плоду через пуповину: в венозный проток, откуда через систему сосудов в правое предсердие. У плода между правым и левым предсердием имеется отверстие – овальное окно. Через него кровь попадает в левое предсердие, затем в левый желудочек, аорту – и ко всем органам плода. Малый круг кровообращения отключен. В легкие плода кровь поступает через артериальный проток – соединение между аортой и легочной артерией. Венозный проток, овальное окно и артериальный проток имеются только у плода. Они называются «фетальными сообщениями».
Когда ребенок рождается и пуповину перевязывают, схема кровообращения радикально изменяется. С первым вдохом ребенка его легкие расправляются, давление в сосудах легких снижается, кровь притекает в легкие. Малый круг кровообращения начинает функционировать. Фетальные сообщения больше не нужны ребенку и постепенно закрываются (венозный проток – в течение первого месяца, артериальный проток и овальное окно – через два-три месяца). В некоторых случаях своевременного закрытия не происходит, тогда у ребенка диагностируют врожденный порок сердца (ВПС).
Иногда при развитии плода возникает аномалия и ребенок рождается с анатомически измененными структурами сердца, что также считается врожденным пороком сердца. Из 1000 детей с врожденными пороками рождается 8-10, и эта цифра увеличивается в последние годы (развитие и совершенствование диагностики позволяет врачам чаще и точнее распознавать пороки сердца, в том числе, когда ребенок еще в утробе матери).
Венозный проток, овальное окно и артериальный проток имеются только у плода. Они называются «фетальными сообщениями».
Когда ребенок рождается и пуповину перевязывают, схема кровообращения радикально изменяется. С первым вдохом ребенка его легкие расправляются, давление в сосудах легких снижается, кровь притекает в легкие. Малый круг кровообращения начинает функционировать. Фетальные сообщения больше не нужны ребенку и постепенно закрываются (венозный проток – в течение первого месяца, артериальный проток и овальное окно – через два-три месяца). В некоторых случаях своевременного закрытия не происходит, тогда у ребенка диагностируют врожденный порок сердца (ВПС).
Иногда при развитии плода возникает аномалия и ребенок рождается с анатомически измененными структурами сердца, что также считается врожденным пороком сердца. Из 1000 детей с врожденными пороками рождается 8-10, и эта цифра увеличивается в последние годы (развитие и совершенствование диагностики позволяет врачам чаще и точнее распознавать пороки сердца, в том числе, когда ребенок еще в утробе матери).
«Синие» и «бледные» пороки сердца
Аномалии могут быть очень разнообразными, наиболее часто встречающиеся имеют названия и объединяются в группы. Например, пороки разделяют на «синие» (при которых кожные покровы ребенка синюшные, «цианотичные») и «бледные» (кожные покровы бледные). Для жизни и развития ребенка более опасны «синие» пороки, при которых насыщение крови кислородом очень низкое. К «синим» порокам относятся Тетрада Фалло, транспозиция магистральных сосудов, атрезия легочной артерии. К «бледным» порокам относятся дефекты перегородок – межпредсердной, межжелудочковой. В некоторых случаях порок может частично компенсироваться за счет открытого артериального протока (в норме он закрывается, как только легкие ребенка расправляются с первым криком). Также у ребенка может недоразвиться клапан сердца – сформируется клапанный порок (наиболее часто, аортальный клапан или клапан легочной артерии).
Причины развития врожденного порока сердца
У плода формирование структур сердца происходит в первом триместре, на 2-8 неделе беременности. В этот период развиваются пороки, которые являются следствием наследственных генетических причин или воздействия неблагоприятных внешних факторов (например, инфекция или отравления). Иногда у ребенка имеется несколько пороков развития, в том числе и порок сердца. Риск рождения ребенка с врожденным пороком сердца очень высок, если:
— ранее у женщины были выкидыши или мертворожденные
— возраст женщины более 35 лет
— женщина во время беременности принимает алкоголь, психоактивные вещества (наркотики), курит
— в семье женщины есть история рождения детей с пороками или мертворождения
— женщина живет в экологически неблагоприятной местности (радиация, отравляющие вещества)
или работает на экологически неблагоприятном производстве
— во время беременности (особенно первые 2 месяца) женщина перенесла инфекционные, вирусные заболевания
— женщина принимала во время беременности лекарственные препараты
с тератогенным эффектом (приводящие к развитию уродств у плода) или
эндокринные препараты для сохранения беременности (гормоны).
Можно ли поставить диагноз ВПС у плода?
Возможность выявить у плода врожденный порок сердца существует, хотя ее нельзя назвать абсолютно информативной. Это зависит от многих причин, основные их которых — наличие высококлассной аппаратуры и квалифицированного специалиста, имеющего опыт перинатальной диагностики. Диагностика возможна начиная с 14-й недели беременности. Если при обследовании у плода выявляется аномалия развития, родителям сообщают о тяжести патологических изменений, возможностях лечения и о том, насколько будет ребенок жизнеспособен. Женщина может принять решение о прерывании беременности. Если есть надежда на успешные роды и лечение, женщина наблюдается у специалиста, роды принимают в специализированном роддоме (чаще всего женщине предлагают кесарево сечение).
Врожденный порок сердца у новорожденных
При рождении ребенка или в первые дни его жизни врачи могут заподозрить врожденный порок сердца.
На чем они основывают свои предположения?
— Шум в сердце. В первые несколько дней жизни ребенка шум в сердце нельзя расценивать как достоверный симптом врожденного порока сердца. Такого ребенка наблюдают, при сохранении шумов более 4-5 суток – обследуют. Само появление сердечного шума объясняется нарушением тока крови через сосуды и полости сердца (например, при наличии аномальных сужений, отверстий, резкой смены направления кровотока).
— синюшность кожных покровов (цианоз). В норме артериальная кровь богата кислородом и придает коже розовую окраску. Когда к артериальной крови примешивается бедная кислородом венозная кровь (в норме не происходит), кожа приобретает синюшный оттенок. В зависимости от типа порока цианоз может быть разной степени выраженности. Однако, врачам приходится уточнять причины цианоза, так как он может быть симптомом болезней органов дыхания и центральной нервной системы.
— проявления сердечной недостаточности. Сердце перекачивает кровь, работая как насос. Когда снижается насосная способность сердца, кровь начинает застаиваться в венозном русле, питание органов артериальной кровью снижается. Учащаются сердечные сокращения и дыхание, появляется увеличение печени и отечность, быстрая утомляемость и одышка. К сожалению, эти признаки очень трудно распознать у новорожденных. Высокая частота сердечных сокращений и дыхания наблюдается у маленьких детей в нормальном состоянии. Только при значительных отклонениях можно с достаточной уверенностью говорить о развитии у малыша сердечной недостаточности. Часто следствием развития сердечной недостаточности является спазм периферических сосудов, что проявляется похолоданием конечностей и кончика носа, их побледнением. Эти признаки помогают косвенно судить о недостаточности сердца.
— нарушения электрической функции сердца (сердечного ритма и проводимости), проявляющиеся аритмиями и, иногда, потерей сознания. Врач может услышать неровное сердцебиение при аускультации (выслушивании фонендоскопом) или увидеть на записи электрокардиограммы.
Как сами родители могут заподозрить у ребенка врожденный порок сердца?
Если порок сердца приводит к серьезным нарушениям гемодинамики (кровотока), как правило, его диагностируют уже в роддоме. При отсутствии выраженных проявлений ребенка могут выписать домой. Родители могут заметить, что малыш вялый, плохо сосет и часто срыгивает, во время кормления и при крике — синеет. Может проявиться выраженная тахикардия (частота сердечных сокращений выше 150 ударов в минуту). В этом случае нужно обязательно сообщить о жалобах педиатру и пройти специальные обследования.
Подтверждение диагноза врожденного порока сердца
В настоящее время наиболее доступным, простым, безболезненным для ребенка и высокоинформативным методом диагностики пороков сердца является эхокардиография. Во время исследования с помощью ультразвукового датчика врач видит толщину стенок, размеры камер сердца, состояние клапанной системы и расположение крупных сосудов. Допплеровский датчик позволяет увидеть направления кровотока и измерить его скорость. Во время исследования можно выполнить снимки, подтверждающие заключение специалиста. Также ребенку обязательно запишут электрокардиограмму. При необходимости более точного исследования (как правило, для определения тактики хирургического лечения порока) врач порекомендует зондирование сердца. Это инвазивная методика, для выполнения которой ребенок госпитализируется в стационар. Зондирование проводится врачем-рентгенхирургом в рентгеноперационной, в присутствии врача-анестезиолога, под внутривенным наркозом. Через прокол в вене или артерии специальные катетеры вводятся в сердце и магистральные сосуды, позволяя точно измерить давление в полостях сердца, аорте, легочной артерии. Введение специального рентген-контрастного препарата позволяет получить точное изображение внутреннего строения сердца и крупных сосудов (см. рисунок).
Диагноз – не приговор. Лечение ВПС (врожденного порока сердца)
Современная медицина позволяет не только своевременно диагностировать, но и лечить врожденные пороки сердца. Лечением ВПС занимаются кардиохирурги. При выявлении порока, сопровождающегося серьезным нарушением гемодинамики, влияющего на развитие ребенка и угрожающего жизни малыша, операция проводиться как можно раньше, иногда в первые дни жизни ребенка. При пороках, которые не влияют значительно на рост и развитие ребенка, операция может проводиться позже. Выбор сроков операции определяется хирургом. Если ребенку рекомендовали хирургическое вмешательство и его не удалось выполнить своевременно (часто из-за отказа родителей, непонимания серьезности проблемы), у ребенка может начаться патологическое изменение гемодинамики, приводящее к развитию и прогрессированию сердечной недостаточности. На определенном этапе изменения становятся необратимыми, операция уже не поможет.
Отнеситесь внимательно к советам и рекомендациям врачей, не лишайте своего ребенка возможности расти и развиваться, не быть инвалидом на всю жизнь!
Операция при врожденных пороках сердца
Многие годы операции при врожденных пороках сердца выполнялись только на открытом сердце, с использованием аппарата искусственного кровообращения (АИК), который берет на себя функции сердца во время его остановки. Сегодня при некоторых пороках такой операции существует альтернатива – устранение дефекта структур сердца с помощью системы AMPLATZER. Такие операции значительно безопаснее, не требуют раскрытия грудной клетки, не отличаясь по эффективности от «большой» хирургии. Если операция выполнена своевременно и успешно, ребенок полноценно развивается и растет, и часто – навсегда забывает о существовании порока. После операции обязательным является наблюдение педиатра, контрольные эхокардиографические исследования. Дети с врожденными пороками сердца часто болеют простудными заболеваниями из-за снижения иммунитета, поэтому в послеоперационном периоде проводится общеукрепляющее лечение и ограничиваются физические нагрузки. В дальнейшем у многих детей эти ограничения снимают и даже разрешают посещать спортивные секции.
Если Вы считаете, что у Вашего ребенка есть проблемы с сердцем, то Вы можете пройти эхокардиографическое исследование и обратиться за консультацией к детскому кардиологу.
Статья была опубликована сотрудниками нашего Центра ранее на «Сибирском медицинском портале».
не приговор» | Алмагуль Каратекенова: «Порок сердца
В преддверии Дня защиты детей о том, как сохранить здоровым детское сердце мы побеседовали с детским кардиологом ГУЗ «ОККД», главным внештатным специалистом Минздрава Саратовской области по специальности «Детская кардиология» Алмагуль Сагындыковной Каратекеновой. Доктор ответила на самые частые, но не теряющие актуальности вопросы о проблемах детских сердечно-сосудистых заболеваний. Предлагаем вашему вниманию ответы на них и призываем прислушаться к советам эксперта.
Самые частые заболевания сердца у детей, с которыми приходится сталкиваться?
Основные заболевания, с которыми обращаются к нам в кардиодиспансер – это врожденные пороки сердца и нарушения ритма. Самыми частыми пороками сердца являются дефект межжелудочковой перегородки, дефект межпредсердной перегородки и тетрада Фалло.
В каком возрасте уже можно определить наличие патологии?
Что касается врождённых пороков сердца, то их врачи могут предположить еще на этапе внутриутробного развития плода, начиная с 10-12 недель беременности. Поэтому будущим мамам так важно вовремя проходить все положенные УЗИ-скрининги плода. Если к моменту рождения у ребенка установлен врожденный порок сердца, требующий хирургической коррекции, то женщине рекомендуется родоразрешение вблизи федеральных кардиоцентров, чтобы быстро оказать ребёнку помощь. Есть и такие пороки сердца, которые не требуют хирургического лечения вообще, ребенок будет находиться под наблюдением врачей и получать необходимое консервативное лечение.
То есть врожденный порок сердца – не приговор?
Нет, не приговор! Современные методы лечения в большинстве случаев позволяют выполнить радикальную коррекцию врожденного порока сердца. Когда радикальная коррекция порока невозможна выполняют так называемую гемодинамическую коррекцию. Всю необходимую помощь можно получить на базе федеральных кардиоцентров совершено бесплатно, для этого необходимо оформить квоту по месту жительства. Главное для родителей быть информированными и следить за ситуацией вместе с кардиологом и кардиохирургом. В прошлом году в нашей области родилось 20 147 детей, из них у 349 детей был установлен диагноз врожденного порока сердца. Однако только у 44 детей это потребовало хирургического лечения. Это говорит о том, что очень низкий процент детей требует хирургического лечения даже при наличии врожденного порока сердца.
Вы упомянули второе по частоте заболевание сердца у детей – нарушение ритма? В чем его особенность и как распознать?
Жалобы при нарушениях ритма не специфичные, часто маме сложно понять, что они связаны именно с нарушениями в работе сердца. Поэтому нельзя игнорировать быструю утомляемость ребенка, жалобы на дискомфорт в области грудной клетки, чувство страха, иногда это и обморочные состояния. Всем детям важно проходить по месту жительства ЭКГ и, при необходимости, получать консультацию кардиолога. Обязательно ЭКГ-скрининг проводится в 1 месяц, затем в 1 год, и далее в 3, 7, 10 и 14 лет. Очень часто ребёнок при нарушении ритма вообще не предъявляет никаких жалоб, поэтому ЭКГ нам поможет вовремя распознать проблему.
Нарушения ритма – опасная патология?
Хотелось бы обратить внимание родителей, что есть так называемые жизнеугрожающие аритмии (желудочковая тахикардия, например), которые возникают внезапно и требуют экстренных действий. Поэтому мой совет родителям научиться оказывать первую помощь – непрямой массаж сердца, сердечно-легочную реанимацию, которая до приезда врачей может помочь спасти ребенку жизнь. Первую помощь может оказать любой находящийся рядом с пострадавшим человек, это необязательно медработник. Еще раз призываю – не игнорируйте жалобы ребенка и вовремя проходите плановые медосмотры в поликлинике! Такие простые действия могут предотвратить неприятные последствия.
Приведите пример, когда плановый скрининг помог спасти детскую жизнь?
В моей практике был случай, когда новорожденному ребенку пренатально патологии выявлено не было, в роддоме не было выполнено УЗИ сердца, т.к. он сразу после рождения попал в детскую инфекционную больницу. А в возрасте 1 месяца на плановом осмотре мы диагностировали ему врожденный порок сердца — коарктацию аорты, который требует экстренного хирургического лечения. На следующий день ребёнок был госпитализирован в Федеральный центр сердечно-сосудистой хирургии в городе Пенза, где был успешно прооперирован.
На что обратить внимание у новорожденных детей, что должно насторожить родителей?
Во-первых, это низкая прибавка в весе, необычный цвет кожных покровов (цианоз, бледность, мраморность), отеки и одышка в покое и при физической нагрузке. Для новорожденного ребёнка физическая нагрузка — это кормление. Если ему требуются перерывы в сосании, при этом он не прибавляет в весе – это повод обратиться к детскому кардиологу.
Подростки — это группа риска? На что надо обратить внимание?
В подростковом возрасте на первое место среди распространенных заболеваний выходит артериальная гипертензия. К нам на прием приходят дети с повышенным давлением, избыточной массой тела, высоким уровнем холестерина и сахара крови. И это уже прямое следствие нездорового образа жизни.
Как сберечь детское сердце? Ваш совет родителям.
Как я уже сказала, необходимо соблюдать все рекомендации врачей уже на этапе беременности. Если выявляются проблемы, то быть на связи с доктором. Во всех остальных случаях, как бы банально это не звучало, надо стараться вести здоровый образ жизни: рационально питаться, высыпаться, избегать гиподинамии, вести активный образ жизни и подавать пример ребенку. Пожалуйста, не ограничивайте физическую активность детей без каких-либо на то причин. Как показывает практика, наши родители ответственно относятся к здоровью детей. Но после 18 лет многие наши пациенты исчезают из поле зрения врачей, что приводит к печальным последствиям.
В ваших силах привить ребенку заботу о собственном здоровье и полезные привычки! Что касается квалифицированной медицинской помощи, то она абсолютно доступна в Саратовской области, в нашем кардиодиспансере, мы всегда на связи. Еще хочу посоветовать родителям информационный ресурс на базе сайта Ассоциации Детских кардиологов России, где также можно найти интересующую их информацию.
Беседовала Елена Симонцева
Попасть на прием к детскому кардиологу и кардиохирургу в ОККД можно по направлению из поликлиники, записавшись по телефону контакт-центра +7(8452) 65-99-61.
Лечение дефекта межжелудочковой перегородки в клиниках Германии
Выезд на лечение в Германию сейчас возможен!
Оформляем срочные медицинские визы для въезда в Германию!
Обращайтесь, мы знаем все про доступные авиарейсы по всему миру!
Дефект межжелудочковой перегородки (ДМЖП) – наиболее часто встречающийся врожденный порок сердца. Он характеризуется наличием одного или нескольких отверстий, расположенных между левым и правым желудочками. ДМЖП – это самый частый врожденный порок сердца, составляющий 30-35% от их общего числа.
На портале Booking Health представлены 73 немецких клиник по лечению дефекта межжелудочковой перегородки
Показать все клиники
Диагностика дефекта межжелудочковой перегородки
Основные методы диагностики ДМЖП – это ЭКГ (электрокардиография) и ЭхоКГ (эхокардиография, УЗИ сердца).
- ЭКГ. Позволяет заподозрить у ребенка дефект межжелудочковой перегородки на основании обнаружения признаков гипертрофии (увеличения) левого желудочка. При длительном течении заболевания может также гипертрофироваться правый желудочек. При незначительном дефекте межжелудочковой перегородки ЭКГ может не выявить никаких изменений.
- ЭхоКГ. Ультразвуковое исследование с допплерографией позволяет не только визуализировать ДМЖП и выявить его локализацию, но также определить давление в левом и правом желудочках. При помощи УЗИ врач имеет возможность обнаружить и другие пороки сердца, которые могут развиваться параллельно с дефектом межжелудочковой перегородки.
- МРТ. Уточняющий метод. Применяется, если имеются подозрения на ДМЖП, однако это заболевание не удалось повредить при помощи ЭхоКГ.
- Рентгенография грудной клетки. Вспомогательный метод. Позволяет выявить косвенные признаки ДМЖП: кардиомегалию (увеличение сердца) и усиление легочного рисунка.
Рекомендуемые клиники для диагностики дефекта межжелудочковой перегородки в Германии:
Показать все программы диагностики
Лечение дефекта межжелудочковой перегородки
Хирургические методы являются основными в лечении дефекта межжелудочковой перегородки. Тактика ведения пациентов с ДМЖП:
- Дети с легочной гипертензией (давление в легочной артерии выше 50% от системного) и симптомами хронической сердечной недостаточности, которая не поддается медикаментозной терапии – операция проводится в течение ближайшего времени, в возрасте до 3 месяцев.
- Дети с симптомами сердечной недостаточности и легочной гипертензией, состояние которых можно улучшить путем медикаментозного лечения – хирургическое лечение проводится позже, в возрасте до 6 месяцев.
- Дети с небольшим ДМЖП (давление в легочной артерии менее 50% от системного), которые испытывают симптомы хронической сердечной недостаточности – применяется консервативное лечение до 5 лет. Затем, если дефект не закрылся сам по себе (такое происходит в 30-50% случаев), выполняют операцию.
- Дети с небольшим ДМЖП, без симптомов хронической сердечной недостаточности – консервативное лечение не назначается, но в возрасте 5 лет нужно сделать операцию и устранить дефект.
Консервативная терапия (диуретики, сердечные гликозиды) назначается для симптоматического лечения сердечной недостаточности до проведения операции, либо пожизненно, если хирургическое лечение противопоказано.
У детей, которые отстают в физическом развитии в первый год жизни, применяются высококалорийные питательные смеси, позволяющие им стабильно набирать вес.
Хирургическое лечение выполняется различными методами, выбор которого определяется величиной и расположением дефекта, а также возможностями клиники.
- Пластическая реконструкция дефекта межжелудочковой перегородки. Хирургическое вмешательство, которое проводится с использованием аппарата искусственного кровообращения. Небольшие дефекты ушиваются. Для закрытия средних и крупных используются заплатки из синтетических материалов или собственного перикарда.
- Транскатетерная пластика ДМЖП. Эндоваскулярная операция. Проводится без искусственного кровообращения. Окклюдер, закрывающий дефект, вводится при помощи катетера через магистральные кровеносные сосуды.
Рекомендуемые клиники для лечения дефекта межжелудочковой перегородки в Германии
Университетская клиника Эссена
Устранение дефекта межжелудочковой перегородки методом пластической реконструкции2713help0
Устранение дефекта межжелудочковой перегородки методом транкатетерной минимально-инвазивной пластики0
Университетская клиника Дюссельдорф
Устранение дефекта межжелудочковой перегородки методом пластической реконструкции0
Устранение дефекта межжелудочковой перегородки методом транкатетерной минимально-инвазивной пластики0
Показать все программы лечения
Реабилитация при дефекте межжелудочковой перегородки
Кардиологическая реабилитация способствует улучшению качества жизни пациентов с заболеваниями сердца и кровеносных сосудов. Она повышает эффективность поддерживающего лечения хронических сердечно-сосудистых заболеваний, а также ускоряет восстановление после обострений. Особенно реабилитация важна для пациентов после кардиохирургических вмешательств.
Кардиологическая реабилитация ставит перед собой следующие цели:
- Восстановление нормальной функции сердечной мышцы
- Устранение симптомов (например, боли в груди, одышки и т.п.)
- Повышение трудоспособности и возможность вернуться к прежней профессиональной деятельности
- Повышение физической выносливости
- Профилактика обострений (в том числе, устранение факторов риска)
- Обучение пациента самоконтролю своего состояния, основным принципам самопомощи
- Улучшение психического состояния пациента, его способности «жить с болезнью»
Эффективная кардиологическая реабилитация проводится только в странах с развитой медицинской сферой. Это связано с доступностью инновационных медикаментов, соответствующего медицинского оборудования и специализирующихся в этой области докторов. В основе кардиологической реабилитации лежат такие методики:
- Медикаментозная поддержка для нормализации артериального давления, свертываемости крови, уровня холестерина
- Дозированные физические нагрузки под контролем инструктора, с постепенным повышением интенсивности
- Физиотерапия (дарсонвализация, электрофорез с лекарственными препаратами, электросон, магнитотерапия и лазерная терапия)
- Расслабляющие техники (массаж, ароматерапия, иглорефлексотерапия, психотерапия)
- Диетотерапия (контроль употребления соли, жидкости, специй и т.д.)
- Модификация образа жизни (отказ от курения, нормализация массы тела)
Кардиологическая реабилитация в Германии проходит под постоянным контролем кардиологов, терапевтов и специалистов по реабилитации. Программы рассчитаны на срок от 2 недель, но при необходимости могут продолжаться значительно дольше. В этой стране пациенту предоставляется качественный уход, проживание в комфортабельных номерах и индивидуально подобранное питание.
Программы реабилитации в Германии демонстрируют одни из самых лучших в мире результатов. Здесь успешно восстанавливает трудоспособность и отличное самочувствие большинство пациентов. Они остаются физически активными, возвращаются к полноценной социальной и семейной жизни.
Рекомендуемые клиники для прохождения кардиологической реабилитации в Германии:
Показать все программы реабилитации
Автор: Доктор Надежда Иванисова
Что входит в стоимость услуг
Стоимость лечения данного заболевания в Университетских клиниках Германии Вы можете узнать здесь. Оставьте заявку, и мы предоставим бесплатную консультацию врача и займемся организацией всего процесса лечения.
Сюда входит:
- Оформление приглашения на лечение для быстрого получения медицинской визы
- Запись на прием в удобное для Вас время
- Предварительная организация комплексного обследования и обсуждения плана лечения
- Предоставление трансфера из аэропота в клинику и обратно в аэропорт
- Предоставление услуг переводчика и личного медицинского координатора
- При необходимости – помощь в организации дальнейшего хирургического лечения
- Предоставление медицинской страховки от осложнений лечения с суммой покрытия 200 000 евро
- Подготовка и перевод медицинских выписок и рекомендаций из клиники
- Помощь в последующем общении с Вашим лечащим врачом, включая консультации по повторным рентгеновским снимкам через уникальную систему медицинского документооборота E-doc
Публикации в СМИ
Дефект межжелудочковой перегородки (ДМЖП) — ВПС с наличием сообщения между правым и левым желудочками.
Этиология • Врождённые пороки (изолированный ДМЖП, составная часть комбинированного ВПС, например тетрада Фалло, транспозиция магистральных сосудов, общий артериальный ствол, атрезия трёхстворчатого клапана и др.) • Существуют данные об аутосомно-доминантном и рецессивном типах наследования. В 3,3% случаев у прямых родственников больных с ДМЖП также обнаруживают этот порок • Разрыв межжелудочковой перегородки при травмах и ИМ.
Статистические данные • ДМЖП составляет 9–25% всех ВПС • Выявляют у 15,7% живорождённых детей с ВПС • Как осложнение трансмурального ИМ — 1–3% • 6% всех ДМЖП и 25% ДМЖП у грудных детей сопровождаются открытым артериальным протоком, 5% всех ДМЖП — коарктацией аорты, 2% врождённых ДМЖП — стенозом клапана аорты • В 1,7% случаев межжелудочковая перегородка отсутствует, и такое состояние характеризуют как единственный желудочек сердца • Соотношение мужского и женского пола — 1:1.
Патогенез. Степень функциональных нарушений зависит от величины сброса крови и общего лёгочного сосудистого сопротивления (ОЛСС). При сбросе слева направо и отношении лёгочного минутного объёма кровотока к системному (Qp/Qs) менее 1,5:1 лёгочный кровоток возрастает незначительно, и повышения ОЛСС не происходит. При больших ДМЖП (Qp/Qs более 2:1) значительно увеличиваются лёгочный кровоток и ОЛСС, и давления в правом и левом желудочках выравниваются. По мере увеличения ОЛСС возможно изменение направления сброса крови — он начинает происходить справа налево. Без лечения развиваются правожелудочковая и левожелудочковая недостаточность и необратимые изменения лёгочных сосудов (синдром Айзенменгера).
Варианты ДМЖП • Мембранозные ДМЖП (75%) располагаются в верхней части межжелудочковой перегородки, под клапаном аорты и септальной створкой трёхстворчатого клапана, часто закрываются самопроизвольно • Мышечные ДМЖП (10%) располагаются в мышечной части межжелудочковой перегородки, на значительном расстоянии от клапанов и проводящей системы, бывают множественными, фенестрированными и часто закрываются самопроизвольно • Надгребневые (ДМЖП выносящего тракта правого желудочка, 5%) располагаются выше наджелудочкового гребня, часто сопровождаются аортальной недостаточностью аортального клапана, самопроизвольно не закрываются • Открытый АВ-канал (10%) обнаруживают в задней части межжелудочковой перегородки, около места прикрепления колец митрального и трёхстворчатого клапанов, часто встречается при синдроме Дауна, сочетается с ДМПП типа ostium primum и пороками развития створок и хорд митрального и трёхстворчатого клапанов, самопроизвольно не закрывается • В зависимости от размера ДМЖП выделяют малые (болезнь Толочинова–Роже) и большие (более 1 см или половина диаметра устья аорты) дефекты.
Клиническая картина
• Жалобы: см. Дефект межпредсердной перегородки.
• Объективно • Бледность кожных покровов • Борозды Харрисона • Усиление верхушечного толчка, дрожание в области левого нижнего края грудины • Патологическое расщепление II тона в результате удлинения периода изгнания правого желудочка • Грубый пансистолический шум у левого нижнего края грудины • При надгребневых ДМЖП — диастолический шум аортальной недостаточности.
Инструментальная диагностика
• ЭКГ: признаки гипертрофии и перегрузки левых отделов, а при лёгочной гипертензии — и правых.
• Яремная флебография: высокоамплитудные волны A (сокращение предсердия при ригидном правом желудочке) и, иногда, волна V (трикуспидальная регургитация).
• ЭхоКГ •• Гипертрофия и дилатация левых отделов, а при лёгочной гипертензии — и правых •• Визуализация ДМЖП в допплеровском и В-режиме •• Диагностика сопутствующих аномалий (клапанных пороков, коарктация аорты и др.) •• Определяют систолическое давление в правом желудочке, степень сброса крови и Qp/Qs •• Взрослым проводят чреспищеводную ЭхоКГ.
• Рентгенография органов грудной клетки •• При небольших ДМЖП — нормальная рентгенологическая картина •• Выбухание дуги левого желудочка, усиление лёгочного сосудистого рисунка •• При лёгочной гипертензии — выбухание дуги лёгочной артерии, расширение и неструктурность корней лёгких с резким сужением дистальных ветвей и обеднением лёгочного сосудистого рисунка.
• Радионуклидная вентрикулография: см. Дефект межпредсердной перегородки.
• Катетеризация камер сердца •• Показана при подозрении на лёгочную гипертензию, перед операцией на открытом сердце и при противоречивых клинических данных •• Вычисляют Qp/Qs •• Проводят пробы с аминофиллином и ингаляцией кислорода для определения прогноза в отношении обратимости лёгочной гипертензии.
• Левая вентрикулография, коронарная ангиография: визуализация и количественная оценка сброса, диагностика ИБС при наличии симптомов или перед операцией.
Медикаментозное лечение. При бессимптомном течении и нормальном давлении в лёгочной артерии (даже при больших дефектах) возможно консервативное лечение до 3–5 лет жизни. При застое в малом круге кровообращения — периферические вазодилататоры (гидралазин или нитропруссид натрия), уменьшающие сброс слева направо. При правожелудочковой недостаточности — диуретики. До и в течение 6 мес после неосложнённой хирургической коррекции ДМЖП — профилактика инфекционного эндокардита.
Хирургическое лечение
Показания • При бессимптомном течении — если к 3–5 годам жизни не происходит самопроизвольного закрытия дефекта, хотя лучших результатов достигают при оперативном лечении в возрасте до 1 года • Сердечная недостаточность или лёгочная гипертензия у детей младшего возраста • У взрослых отношение Qp/Qs составляет 1,5 и более.
Противопоказания: см. Дефект межпредсердной перегородки.
Методы оперативного лечения. Паллиативное вмешательство — сужение лёгочного ствола манжетой, проводят при необходимости экстренной операции детям с массой тела менее 3 кг, при сопутствующих пороках сердца и малом опыте клиники по радикальной коррекции порока в раннем возрасте. При травматическом дефекте в области мембранозной части межпредсердной перегородки возможно ушивание дефекта. В остальных случаях проводят пластику дефекта заплатой из аутоперикарда или синтетических материалов. При постинфарктном ДМЖП проводят пластику дефекта с одномоментным коронарным шунтированием.
Специфические послеоперационные осложнения: инфекционный эндокардит, АВ-блокада, желудочковые аритмии, реканализация ДМЖП, недостаточность трёхстворчатого клапана.
Прогноз. У 80% пациентов с большими ДМЖП происходит спонтанное закрытие дефекта в течение 1 мес, у 90% — в возрасте до 8 лет, известны единичные случаи спонтанного закрытия ДМЖП в возрасте между 21 и 31 годами. При небольших дефектах продолжительность жизни существенно не меняется, но увеличивается риск инфекционного эндокардита (4%). При ДМЖП средних размеров сердечная недостаточность обычно развивается в детском возрасте, тяжёлую лёгочную гипертензию встречают редко. Большие ДМЖП без градиента давления между желудочками в 10% случаев приводят к развитию синдрома Айзенменгера, большинство таких больных умирают в детском или подростковом возрасте. Неотложное хирургическое вмешательство необходимо 35% детей в течение 3 мес после рождения, 45% — в течение 1 года. Материнская смертность во время беременности и родов при синдроме Айзенменгера превышает 50%. При постинфарктном ДМЖП через 1 год при отсутствии хирургического лечения выживают 7% больных. Госпитальная летальность после сужения лёгочной артерии — 7–9%, 5-летняя выживаемость — 80,7%, 10-летняя — 70,6%. Летальность при хирургическом лечении постинфарктных ДМЖП — 15–50%. Госпитальная летальность при закрытии изолированных врождённых ДМЖП с низким ОЛСС — 2,5%, с высоким ОЛСС — менее 5,6%.
Сокращения. Qp/Qs — отношение лёгочного минутного объёма кровотока к системному. ОЛСС — общее лёгочное сосудистое сопротивление.
МКБ-10 • Q21.0 ДМЖП
Дефект межпредсердной перегородки сердца: операция, лечение в СПб
Дефект межпредсердной перегородки – это отверстие в межпредсердной перегородке, через которое кровь поступает из левого в правое предсердие.
Дефекты по своему расположению и формированию подразделяются на первичные, вторичные дефекты межпредсердной перегородки и дефекты венозного синуса.
Дефекты могут иметь различную форму и размеры (вплоть до полного отсутствия перегородки и формирования единого предсердия), могут быть единичными и множественными, могут быть единственным пороком сердца, а могут входить в состав более сложных пороков сердца (открытый AV-канал, аномальный дренаж легочных вен и т.д.).
Причины дефекта межпредсердной перегородки
В основе формирования дефекта межпредсердной перегородки лежит нарушение развития первичной или вторичной перегородки в эмбриональном периоде.
- Первичный дефект располагается в нижней части межпредсердной перегородки рядом с фиброзными кольцами атриовентрикулярных клапанов (митрального и трехстворчатого), по сути его нижним краем является само фиброзное кольцо.
- Вторичный дефект располагается в центральной части межпредсердной перегородки, и все его края представлены самой перегородкой.
- Дефект венозного синуса – это дефект, локализующийся в верхней части межпредсердной перегородки. Данному пороку часто сопутствует аномальный дренаж лёгочных вен (часть лёгочных вен впадает не в левое предсердие, а в верхнюю полую вену).
Гемодинамика
Cмысл порока заключается в сбросе артериальной крови из большого круга кровообращения (левого предсердия) в малый круг кровообращения (правое предсердие), что приводит к перегрузке малого круга кровообращения избыточным объемом крови с поражением, в первую очередь, легких. Крайней формой поражения является формирование легочной гипертензии (высокого давления в сосудах легких). Легочная гипертензия при дефекте межпредсердной перегородки носит злокачественный характер, приводя к тяжелой сердечной недостаточности и гибели пациента.
Симптомы
Первые симптомы заболевания возникают в виде одышки при физической нагрузке, частых простуд, ощущения перебоев в работе сердца. При этом симптоматика разнообразная и зависит от локализации и размера дефекта, сочетания его с другими пороками сердца. Дефекты малого размера не имеют характерной клинической картины. Жалобы пациенты активно не предъявляют, физическая активность их не ограничена — порок обнаруживается случайно. При больших, гемодинамически значимых дефектах у пациентов появляются одышка, повышенная утомляемость, непереносимость физической нагрузки. После физических упражнений возможно возникновение кашля, сопровождающегося иногда кровохарканьем. Для таких пациентов характерны частые пневмонии, бронхиты.
Диагностика
- Осмотр пациента с аускультацией (выслушиванием) сердца выявляет шумы в сердце.
- ЭКГ выявляет гипертрофию миокарда правого желудочка, блокаду правой ножки пучка Гиса, аритмии разной степени тяжести, резкое отклонение электрической оси сердца влево.
- Рентгенография органов грудной клетки выявляет расширение ствола легочной артерии, увеличение сердца, усиление лёгочного рисунка.
- Трансторакальная эхокардиография позволяет не только визуализировать дефект межпредсердной перегородки и уточнить его характер (первичный, вторичный, дефект венозного синуса), но также оценить направление сброса крови через дефект и его гемодинамическую значимость (Qp/Qs).
- Чреспищеводная эхокардиография у взрослых позволяет получить детальную информацию о краях дефекта, что важно для выбора метода оперативного лечения.
- Зондирование камер сердца и атриография используется при недостаточной информации от вышеописанных методов исследования или как часть уже оперативного лечения.
Показания к операции на дефект межпредсердной перегородки
Принятие решения об оперативном лечении зависит от размера дефекта, его гемодинамических характеристик (объем и направление сброса крови через дефект), наличия и величины легочной гипертензии, возраста пациента, наличия сопутствующей патологии и т.д. Решение о целесообразности оперативного лечения принимается совместно лечащим кардиологом, кардиохирургом, врачами других специальностей (при необходимости).
Лечение дефекта межпредсердной перегородки
На данный момент существует два вида оперативного лечения:
- 1. Операция на открытом сердце в условиях искусственного кровообращения с ушиванием дефекта или его пластикой заплатой из перикарда.
- 2. Устранение дефекта межпредсердной перегородки с использованием специальных устройств (окклюдеров) в условиях рентгеноперационной через проколы артерий без стернотомии.
- Необходимо понимать, что не каждый дефект может быть устранен оперативным путем, существуют противопоказания к операции (дефекты малого диаметра, тяжелая легочная гипертензия, право-левый сброс через дефект), и не каждый дефект может быть устранен с использованием оккклюдеров (сочетание дефекта с аномальным дренажом легочных вен, первичные дефекты с отсутствующим нижним краем, дефекты большого размера, сочетание дефекта с другой
- патологией сердца являются показанием к открытой операции).
- Более подробно о конкретном случае заболевания, показаниях и противопоказаниях можно узнать в процессе консультации сердечно-сосудистого хирурга (на амбулаторном приеме).
Стоит ли мне беспокоиться, если УЗИ моего ребенка показывает порок сердца?
В честь Недели осведомленности о врожденных пороках сердца и Американский месяц сердца мы поговорили с врачом MultiCare по материнско-фетальной медицине и детским кардиологом из NorthWest Congenital Heart Care, одного из местных отделений детской кардиологии. MultiCare сотрудничает с нами о распространенных пороках сердца у младенцев и о том, почему важно их раннее выявление.
Для большинства будущих мам важные новости от УЗИ связаны с полом их ребенка. Но одна из самых важных задач для медицинской бригады — сердце ребенка.
По словам Тэмми Чао, доктора медицинских наук, регионального отделения материнско-фетальной медицины MultiCare, около 1 процента всех детей в Соединенных Штатах рождаются с той или иной формой порока сердца.
Примерно одной трети этих младенцев потребуется операция на сердце в течение первых недель или месяцев. А с помощью ультразвука большинство этих дефектов выявляются задолго до родов, что дает родителям и врачам драгоценное время для подготовки плана.
Если есть подозрение на порок сердца или у беременной женщины есть риск рождения ребенка с пороком сердца, детский кардиолог или фетальный кардиолог выполнит эхокардиограмму плода. С помощью этой подробной информации они могут определить серьезность проблемы в случае ее обнаружения, обучить будущих родителей и обсудить варианты лечения.
Иногда может потребоваться изменить план родов, чтобы в случае необходимости оказания неотложной помощи после родов все поставщики были осведомлены и готовы, — говорит Дженни Аллен, доктор медицины, из Северо-Западного отделения врожденного ухода за сердцем (NWCHC).
Стоит ли мне беспокоиться?Пациенты в первую очередь должны знать, что то, что ваш врач что-то обнаруживает на УЗИ, не означает, что ваш ребенок болен.
«Некоторые результаты ультразвукового исследования, такие как эхогенный внутрисердечный очаг (EIF), часто обнаруживаются при ультразвуковом исследовании», — говорит д-р Чао. «EIF — это яркое пятно в одной из камер сердца».
Хотя это требует некоторого расследования, это может быть ничто.
«Мы видим EIF у многих типичных здоровых младенцев, особенно в определенных этнических группах», — сказал д-р.- говорит Чао. «То, что мы видим, не означает, что есть порок сердца».
По ее словам, обнаружение серьезного порока сердца в утробе матери не обязательно опасно для жизни.
«Наиболее распространенные пороки сердца, которые мы наблюдаем, такие как дефекты межжелудочковой перегородки, не являются смертельными», — говорит д-р Чао. «Но около 25 процентов серьезных пороков сердца являются критическими».
Доктор Чао направляет женщин из акушерских клиник в девять округов западного Вашингтона.Некоторых из этих пациентов направляют в клинику материнско-фетальной медицины для рутинного ультразвукового обследования, а некоторых — из-за того, что при ультразвуковом исследовании, проведенном на месте у врача-акушера, была обнаружена аномалия.
«Каждой женщине через 20 недель проводится подробное ультразвуковое исследование», — говорит она. «Анатомическое обследование представляет собой обширный перечень контрольных вопросов, но мы уделяем много внимания сердцу, потому что это сложная структура».
Специалисты по ультразвуковой диагностике стараются получить четкие изображения сердца.
«Если изображения нечеткие или неполные с первой попытки, мы возвращаем пациента через пару недель, чтобы повторить попытку», — говорит д-р Чао. «Мы можем обнаружить большинство серьезных пороков сердца с помощью ультразвука».
Объясненные общие аномалии сердцаСамая распространенная врожденная аномалия сердца — это дефект межжелудочковой перегородки (ДМЖП), — говорит д-р Чао. ВСД — это отверстие между двумя нижними камерами сердца.
При обнаружении ДМЖП врачи внимательно изучают другие области сердца, а также другие органы, чтобы понять, является ли ДМЖП частью более крупного синдрома.Хорошая новость заключается в том, что многие случаи VSD закрываются сами по себе. Все, что нужно, — это следить, чтобы убедиться, что дефект закрывается. В других случаях требуется хирургическое вмешательство.
Педиатр / кардиолог плода может многое предсказать, насколько клинически важным может быть ДМЖП для ребенка после рождения, пока ребенок еще находится в утробе матери, и при необходимости продолжит осматривать ребенка после рождения со своими семьями, — говорит доктор Аллен.
«Мы позаботились о беременностях, связанных с различными пороками сердца плода, от дефектов межжелудочковой и предсердной перегородки (отверстие между верхними камерами сердца) до более серьезных состояний, таких как тетралогия Фалло, синдром гипоплазии левых отделов сердца, транспозиция большого артерии или артериального ствола », — говорит Чао.
Женщина, вынашивающая ребенка с пороком сердца, обнаруженным на УЗИ, направлена к детскому кардиологу. Иногда требуется только однократная эхокардиограмма. В других случаях кардиолог захочет увидеть серийные эхокардиограммы с последующими аналогичными исследованиями после родов.
Вместе с будущими семьями и специалистами по медицине матери и плода детский кардиолог составит план ухода за детьми с выявленными сердечными заболеваниями в пренатальном периоде и прояснит риски и преимущества вмешательства, если это необходимо, чтобы помочь семьям принимать информированные решения при уходе за детьми. их ребенок с болезнью сердца.
Часто детский кардиолог работает с семьями от беременности до взрослого, если требуется постоянный уход, говорит д-р Аллен из NWCHC.
Что вызывает врожденные пороки сердца?Подавляющее большинство врожденных пороков сердца развиваются спонтанно, то есть нет видимой причины и состояние не передается по наследству. Однако иногда плохо контролируемый материнский диабет может вызвать пороки сердца плода. Это можно увидеть у матерей, у которых до беременности был недиагностированный диабет.
Иногда порок сердца является лишь одним из аспектов более сложного генетического синдрома. Вот почему женщинам, у младенцев которых есть порок сердца, будет предложено генетическое консультирование в клинике MFM, и они могут рассмотреть возможность проведения дополнительных пренатальных тестов, таких как амниоцентез. Результаты могут успокоить обеспокоенных родителей или выявить генетический синдром, который может помочь родителям подготовиться к жизни после рождения ребенка.
«Результат для ребенка с пороком сердца обычно лучше, если нет связанного генетического синдрома и хромосомы в норме», — говорит Чао.
Некоторые пациенты считают, что единственное преимущество амниоцентеза — это возможность прервать беременность при обнаружении значительных отклонений, но доктор Чао говорит, что это не всегда так.
«Это может предложить пациентам душевное спокойствие, если не выявлено генетического синдрома или хромосомных проблем», — говорит она. «С другой стороны, если будет поставлен генетический диагноз, это может помочь пациентам выстроить ресурсы, такие как консультации узких специалистов или группы поддержки».
Синдром Дауна — одна из самых распространенных хромосомных проблем, связанных с врожденными пороками сердца.
Раннее обнаружение действительно помогаетВ редких случаях некоторые тяжелые врожденные пороки сердца неизлечимы.
«В нашей клинике есть службы психологической помощи семьям, чей ребенок может не выжить из-за серьезных пороков сердца», — говорит д-р Чао.
Конференция по комплексному уходу с участием представителей материнско-фетальной медицины, консультирования по вопросам горя, ведения пациентов, неонатологии, детской кардиологии, группы паллиативной помощи и членов семьи организуется во время беременности, чтобы план родов пациентки мог быть составлен заранее. Доставка.
План родов включает в себя такие вещи, как определение желаемого уровня медицинского вмешательства, сбор прядей волос ребенка, удержание ребенка как можно дольше, перерезание пуповины и другую эмоциональную поддержку.
«Это могут быть очень трудные случаи для всех, кто вовлечен», — говорит д-р Чао. «Наличие плана улучшает общение между командой и снижает стресс для семьи».
Некоторые формы врожденных пороков сердца являются тяжелыми, но при раннем и плановом вмешательстве новорожденные могут жить долгой и нормальной жизнью.По словам доктора Чао, несмотря на то, что внутриутробные операции по поводу пороков сердца остаются крайне редкими, раннее обнаружение может помочь улучшить результаты у детей с некоторыми серьезными дефектами.
После того, как диагностирован порок сердца плода, план родов может измениться, чтобы дать ребенку наилучшие шансы. Это может означать запланированные роды или тщательное наблюдение за беременностью.
При серьезных дефектах роды должны быть запланированы в учреждении, оборудованном для ухода за ребенком, включая возможное хирургическое или медицинское вмешательство.«Детский кардиолог поможет составить план родов и при необходимости организовать план вмешательства», — говорит д-р Аллен.
Хотя никто не ожидает узнать, что их беременность осложняется врожденным пороком сердца, новость об этом — обычное дело для будущих родителей. Будем надеяться, что с помощью узких специалистов семьи, столкнувшиеся с этой новостью, смогут узнать о болезни сердца своего ребенка и почувствовать поддержку в этом путешествии.
Подробнее о MultiCare Maternal-Fetal Medicine
Узнайте больше о NorthWest Congenital Heart Care
Врожденные пороки сердца — факты о дефекте межжелудочковой перегородки
Дефект межжелудочковой перегородки (произносится как желудочковый дефект межжелудочковой перегородки) (ДМЖП) — это врожденный порок сердца, при котором в стенке (перегородке) имеется отверстие, разделяющее две нижние камеры ( желудочки) сердца.Эта стенка также называется межжелудочковой перегородкой.
Что такое дефект межжелудочковой перегородки
Дефект межжелудочковой перегородки возникает во время беременности, если стенка, образующаяся между двумя желудочками, не развивается полностью, оставляя отверстие. Дефект межжелудочковой перегородки — это один из видов врожденного порока сердца. Врожденный означает наличие при рождении.
У ребенка без врожденного порока сердца правая сторона сердца перекачивает бедную кислородом кровь от сердца к легким, а левая сторона сердца перекачивает богатую кислородом кровь к остальным частям тела.
У младенцев с дефектом межжелудочковой перегородки кровь часто течет из левого желудочка через дефект межжелудочковой перегородки в правый желудочек и в легкие. Эта дополнительная кровь, закачиваемая в легкие, заставляет сердце и легкие работать тяжелее. Если со временем не устранить этот дефект, это может увеличить риск других осложнений, включая сердечную недостаточность, высокое кровяное давление в легких (так называемая легочная гипертензия), нерегулярные сердечные ритмы (так называемые аритмия) или инсульт.
Узнайте больше о том, как работает сердце »
Типы дефектов межжелудочковой перегородки
У младенца с дефектом межжелудочковой перегородки может быть одно или несколько отверстий в разных местах перегородки. У этих отверстий есть несколько названий. Некоторые общие места расположения и названия (см. Рисунок):
- Конвентрикулярный дефект межжелудочковой перегородки
В общем, это отверстие, в котором части межжелудочковой перегородки должны встречаться чуть ниже легочного и аортального клапана . - Перимембранозный дефект межжелудочковой перегородки
Это отверстие в верхней части межжелудочковой перегородки. - Дефект входной межжелудочковой перегородки
Это отверстие в перегородке рядом с местом, где кровь попадает в желудочки через трикуспидальный и митральный клапаны. Этот тип дефекта межжелудочковой перегородки также может быть частью другого порока сердца, называемого дефектом атриовентрикулярной перегородки (AVSD). - Мышечный дефект межжелудочковой перегородки
Это отверстие в нижней мышечной части межжелудочковой перегородки и является наиболее распространенным типом дефекта межжелудочковой перегородки.
Происшествие
В исследовании, проведенном в Атланте, Центры по контролю и профилактике заболеваний (CDC) подсчитали, что 42 из каждых 10 000 новорожденных имели дефект межжелудочковой перегородки. 1 Это означает, что ежегодно в США рождается около 16 800 детей с дефектом межжелудочковой перегородки. Другими словами, примерно 1 из 240 новорожденных в США ежегодно рождается с дефектом межжелудочковой перегородки.
Причины и факторы риска
Причины пороков сердца (таких как дефект межжелудочковой перегородки) у большинства младенцев неизвестны.У некоторых младенцев пороки сердца возникают из-за изменений в их генах или хромосомах . Считается, что пороки сердца также вызваны сочетанием генов и других факторов риска, таких как факторы, с которыми мать контактирует в окружающей среде, или то, что мать ест или пьет, или лекарства, которые она использует.
Подробнее о работе CDC по причинам и факторам риска »
Диагностика
Дефект межжелудочковой перегородки обычно диагностируется после рождения ребенка.
Размер дефекта межжелудочковой перегородки будет влиять на то, какие симптомы, если они есть, будут присутствовать, и услышит ли врач шум в сердце во время медицинского осмотра. Признаки дефекта межжелудочковой перегородки могут присутствовать при рождении или могут появиться только спустя много лет после рождения. Если отверстие маленькое, оно обычно закрывается само по себе, и у ребенка может не быть никаких признаков дефекта. Однако, если отверстие большое, у ребенка могут быть симптомы, в том числе:
- Одышка,
- Быстрое или тяжелое дыхание,
- Потоотделение,
- Усталость при кормлении, или
- Плохая прибавка в весе.
Во время медицинского осмотра врач может услышать отчетливый свистящий звук, называемый сердечным шумом. Если врач слышит шум в сердце или присутствуют другие признаки, он может запросить один или несколько тестов для подтверждения диагноза. Самый распространенный тест — это эхокардиограмма , которая представляет собой ультразвуковое исследование сердца , которое может показать проблемы со структурой сердца, показать, насколько велико отверстие, и показать, сколько крови течет через отверстие.
Процедуры
Лечение дефекта межжелудочковой перегородки зависит от размера отверстия и проблем, которые оно может вызвать.Многие дефекты межжелудочковой перегородки небольшие и закрываются сами по себе; если отверстие небольшое и не вызывает никаких симптомов, врач будет регулярно проверять ребенка, чтобы убедиться, что нет признаков сердечной недостаточности и что отверстие закрывается само. Если отверстие не закрывается само по себе или оно велико, могут потребоваться дальнейшие действия.
В зависимости от размера отверстия, симптомов и общего состояния здоровья ребенка врач может порекомендовать катетеризацию сердца или операцию на открытом сердце , чтобы закрыть отверстие и восстановить нормальный кровоток.После операции врач назначит регулярные контрольные визиты, чтобы убедиться, что дефект межжелудочковой перегородки остается закрытым. Большинство детей с закрытым дефектом межжелудочковой перегородки (самостоятельно или хирургическим путем) живут здоровой жизнью.
Лекарства
Некоторым детям потребуются лекарства, которые помогут укрепить сердечную мышцу, снизить кровяное давление и помочь организму избавиться от лишней жидкости.
Питание
Некоторые дети с дефектом межжелудочковой перегородки устают во время кормления и не едят достаточно, чтобы набрать вес.Чтобы обеспечить здоровую прибавку в весе младенцев, может быть прописана специальная высококалорийная смесь. Некоторые дети сильно устают во время кормления, и им может потребоваться кормление через зонд .
Список литературы
- Reller MD, Strickland MJ, Riehle-Colarusso T, Mahle W.T., Correa A. Распространенность врожденных пороков сердца в столичной Атланте, 1998-2005 гг. J Pediatr. 2008; 153: 807-13.
Изображения находятся в общественном достоянии и, следовательно, свободны от каких-либо ограничений авторских прав.В порядке любезности мы просим, чтобы поставщик контента (Центры по контролю и профилактике заболеваний, Национальный центр по врожденным дефектам и порокам развития) был указан и уведомлен о любом публичном или частном использовании этого изображения.
Изображения находятся в общественном достоянии и, следовательно, свободны от каких-либо ограничений авторских прав. В порядке любезности мы просим, чтобы поставщик контента (Центры по контролю и профилактике заболеваний, Национальный центр по врожденным дефектам и порокам развития) был указан и уведомлен о любом публичном или частном использовании этого изображения.
ссылок на ресурсы по другим врожденным порокам сердца
Многие организации стремятся больше узнать о врожденных пороках сердца и предоставить полезные ресурсы для семей и поставщиков медицинских услуг. Щелкните по ссылкам ниже, чтобы найти дополнительную информацию.
Ассоциация врожденных пороков сердца взрослыхexternal icon
Ассоциация врожденных пороков сердца взрослых — это национальная организация, предоставляющая услуги по обучению и поддержке взрослых с врожденными пороками сердца и их семей.Они ориентированы на долгосрочные потребности взрослых с врожденными пороками сердца и обеспечивают образование, информационно-пропагандистскую деятельность и защиту.
Американская педиатрическая академиявнешний значок
Американская академия педиатрии (AAP) — это организация, в которую входят 60 000 педиатров, занимающихся физическим, психическим и социальным здоровьем младенцев, детей, подростков и молодых людей. AAP предоставляет рекомендации и клинические руководства по ряду тем в педиатрической медицине, включая ответы на вопросы педиатров о скрининге пульсоксиметрии для выявления критических врожденных пороков сердца.
Американский колледж кардиологииexternal icon
Американский колледж кардиологии (ACC), некоммерческое медицинское общество, занимается улучшением качества жизни пациентов с сердечно-сосудистыми заболеваниями за счет постоянного улучшения качества, ориентированного на пациента ухода, инноваций в оплате и профессионализма. ACC обеспечивает профессиональное образование и управляет национальными регистрами для измерения и улучшения качества медицинской помощи.
Американская кардиологическая ассоциацияexternal icon
Американская кардиологическая ассоциация предлагает информацию о последствиях и рисках врожденных пороков сердца, а также о симптомах и лечении детей с врожденными пороками сердца.На этом веб-сайте также представлена информация о конкретных типах врожденных пороков сердца.
Фонд «Детское сердце «external icon
Фонд» Детское сердце «работает над изучением врожденных пороков сердца, финансируя исследования, направленные на диагностику, лечение и профилактику врожденных пороков сердца.
Консорциум общественного здравоохранения врожденных пороков сердцаxternal icon
CDC предоставляет техническую помощь Консорциуму общественного здравоохранения врожденных пороков сердца, уникальному сотрудничеству, которое объединяет семьи, экспертов и организации для решения проблемы врожденных пороков сердца посредством эпиднадзора, исследований, образования, укрепления здоровья и разработки политики .
Conquering CHDexternal icon
Conquering CHD миссия — «победить врожденный порок сердца». Они достигают этого за счет сотрудничества с пациентами, родителями, поставщиками медицинских услуг и партнерскими организациями для улучшения качества и результатов за счет обучения, поддержки, исследований и повышения осведомленности в отношении ИБС.
March of Dimesexternal icon
Марш Dimes — это национальная организация, цель которой — помочь детям родиться здоровыми. Их веб-сайт предлагает краткий обзор врожденных пороков сердца, дает описания некоторых конкретных дефектов и направляет читателей к дополнительным ресурсам.
Mended Little Heartsexternal icon
Mended Little Hearts является частью организации Mended Hearts и была основана в 2004 году. Они оказывают поддержку детям с врожденными пороками сердца и их семьям. Их веб-сайт предоставляет возможность семьям «самых маленьких сердечных больных» собраться вместе на собраниях групп поддержки и программах посещения.
Национальный институт сердца, легких и крови внешний значок
Национальный институт сердца, легких и крови предлагает обзор врожденных пороков сердца.Он включает информацию о том, как работает сердце, типах дефектов, причинах, признаках и симптомах, диагностике, лечении, проблемах, связанных с жизнью с врожденным пороком сердца, и клинических испытаниях.
Национальная сеть профилактики врожденных дефектов внешний значок
CDC поддерживает NBDPN и сотрудничает с ней. NBDPN — это группа из более чем 225 человек, работающих на национальном, региональном и местном уровнях, которые занимаются отслеживанием, исследованием и предотвращением врожденных дефектов. NBDPN служит форумом для обмена идеями об отслеживании и исследовании врожденных дефектов, а также для оказания технической поддержки государственным и местным программам.Основанная в 1997 году, NBDPN оценивает влияние врожденных дефектов на детей, семьи и систему здравоохранения. Сеть также определяет факторы риска врожденных дефектов. Эта информация может быть использована для разработки стратегий предотвращения врожденных дефектов и помощи семьям и их воспитателям в предотвращении других видов инвалидности у детей с врожденными дефектами.
Дефекты межпредсердной перегородки — NORD (Национальная организация по редким заболеваниям)
УЧЕБНИКИ
Beers MH, Berkow R., ред. Руководство Merck, 17-е изд. Станция Уайтхаус, Нью-Джерси: Исследовательские лаборатории Мерк; 1999: 2200.
Берков Р., изд. Руководство Merck — домашнее издание, 2-е изд. Станция Уайтхаус, Нью-Джерси: Исследовательские лаборатории Мерк; 2003: 1514-15.
Larson DE. изд. Книга здоровья семьи клиники Мэйо. Нью-Йорк, штат Нью-Йорк: Уильям Морроу и компания, Inc.; 1996: 52.
Каспер, Д.Л., Фаучи А.С., Лонго Д.Л. и др. Ред. Принципы внутренней медицины Харрисона. 16-е изд. Компании McGraw-Hill. Нью-Йорк, штат Нью-Йорк; 2005: 1385, 1392.
Фостер В., Александр Р.В., О’Рурк Р.А. и др. Ред. Сердце Херста. 11-е изд. Компании McGraw-Hill. Нью-Йорк, штат Нью-Йорк; 2004: 1797-1800.
ОБЗОР СТАТЕЙ
Латсон Л.А., Джонс Т.К., Якобсон Дж., Зан Э., Родс Дж.Ф. Анализ факторов, связанных с успешным транскатетером вторичных дефектов предсердий с использованием окклюдера Helex перегородки. Am Heart J. 2006; 151: 1129.e7-11.
Chatterjee T, Ritz A, Rehders TC, Ince H, Kisch S, Petzsch M, Nienaber CA. Чрескожное транскатетерное закрытие открытого овального отверстия.Минерва Кардиоангиол. 2006; 54: 31-39.
Nageh T, Meier B. Внутрисердечные устройства для профилактики инсульта. Ранее Cardiol. 2006; 9: 1-7.
Tobis MJ, Azarbal Z. Способствует ли открытое овальное отверстие криптогенному инсульту и мигрени. Tex Heart Inst J. 2005; 32: 362-65.
Kizer JR, Деверо, РБ. Клиническая практика. Открытое овальное отверстие у молодых людей с необъяснимым инсультом. N Engl J Med. 2005; 353: 2361-72.
Рейбрук Т., Мертенс Л. Физическая работоспособность и физическая активность при врожденном пороке сердца у взрослых.Eur J Cardiovasc Назад Rehabil. 2005; 12: 498-502.
Мур П. Врожденная катетеризация сердца под контролем МРТ и вмешательство: будущее? Катетер Cardiovasc Interv. 2005; 66: 1-8.
Моаке Л., Рамачотти С. Варианты лечения дефекта межпредсердной перегородки. Проблемы AACN Clin. 2005; 16: 252-66.
ИЗ ИНТЕРНЕТА
McKusick VA, Ed. Интернет-Менделирующее наследование в человеке (OMIM). Университет Джона Хопкинса. Дефект межпредсердной перегородки 1; ASD1. Номер записи; 108800: Дата последнего редактирования; 11.10.2004.
МакКусик В.А., Под ред. Интернет-Менделирующее наследование в человеке (OMIM). Университет Джона Хопкинса. Дефект межпредсердной перегородки 2; ASD2. Номер записи: 607941: Дата последнего редактирования; 23.06.2005.
Арнальдо Ф. Дефект межпредсердной перегородки. Медицинская энциклопедия. MedlinePlus. Дата обновления: 27.04.2004. 3 стр.
www.nlm.nih.gov/medlineplus/ency/article/000157.htm
Дефект межпредсердной перегородки. Американская Ассоциация Сердца. © 2006. 2 стр.
www.americanheart.org/presenter.jhtml?identifier=11065
Дефект межпредсердной перегородки (ДМПП).Сердечные аномалии / врожденные пороки сердца. Детский медицинский центр Цинциннати. Пересмотрено 10/04. 3 стр.
www.cincinnatichildrens.org/health/heart-encyclopedia/anomalies/asd.htm
Дефект межпредсердной перегородки. Национальный институт сердца, легких и крови. nd. 9pp.
www.nhlbi.nih.gov/health/dci/Diseases/asd/asd_all.html
10 фактов, которые ваш врач не скажет вам о врожденных пороках сердца
Каждый год в США рождается около 40 000 детей с врожденными пороками сердца (ВПС) чаще, чем любой другой тип врожденного порока, согласно U.S. Центры по контролю и профилактике заболеваний. Причина большинства пороков сердца неизвестна, но теперь, благодаря успеху современной дородовой помощи и кардиохирургии новорожденных, эти дети доживают до взрослой жизни больше, чем когда-либо прежде. Детская смертность, связанная с ИБС, снизилась почти на 60 процентов с 1987 по 2005 год, говорится в исследовании, опубликованном в Журнале Американского колледжа кардиологии.
Но многие люди, рожденные с врожденными пороками сердца, не осознают, насколько сильно их сердца продолжают отличаться от сердец других.ИБС — это проблема не только педиатрического здоровья.
Вот 10 фактов о врожденных пороках сердца у взрослых, о которых вы могли не слышать от врача.
1. Врожденные пороки сердца — не все одно и то же.
Для каждого из 100 детей, рожденных с врожденным пороком сердца — проблемой со структурой сердца — это состояние может быть уникальным. Это связано с тем, что существует более 40 известных типов врожденных пороков сердца, отмечает Фонд «Детское сердце», и даже больше уникальных.На протяжении всей жизни различия сохраняются.
«Нет двух взрослых пациентов с одинаковыми симптомами; каждый из них — свое собственное редкое заболевание », — объясняет 63-летняя Паула Миллер из Мемфиса, штат Теннесси, медсестра, рожденная с врожденным пороком сердца. Сейчас она работает менеджером по обслуживанию участников Ассоциации взрослых врожденных пороков сердца (ACHA), оказывая поддержку взрослым с пороками сердца.
Наиболее распространенным пороком сердца является атрезия и стеноз клапана легочной артерии, которые возникают, когда клапан сердца не открывается полностью, как показало национальное исследование U.С. Записи о рождении. Вторым по распространенности, по данным Национального института сердца, легких и крови, является сложный дефект, известный как тетралогия Фалло. У людей с этим заболеванием сердце имеет отверстие между желудочками и закупорку, где сердце обычно ведет к легким, среди других дефектов.
2. С врожденными пороками сердца живет больше взрослых, чем детей.
Вы можете даже не знать, что родились с врожденным пороком сердца, пока вам не поставят диагноз в зрелом возрасте.И, будучи взрослым с врожденным пороком сердца, временами вы можете чувствовать себя одиноким, но это не так. «За 49 лет я ни разу не встретил другого взрослого, живущего с ACHD, — говорит Миллер, — и я была медсестрой». По оценкам кардиологов, в настоящее время более 1 миллиона взрослых в США живут с врожденными пороками сердца, в то время как количество детей с ИБС составляет менее 1 миллиона. Цифры в США фактически основаны на показателях в Канаде, где системы общественного здравоохранения отслеживают пациентов на протяжении всей их жизни.
«В Соединенных Штатах у нас нет точных цифр, потому что нет системы наблюдения за взрослыми.Дети растут и теряются для последующего наблюдения », — говорит Миллер. Это должно измениться в ближайшее время, потому что Конгресс принял Закон о врожденном будущем сердца в 2010 году, закон, который обеспечивает финансирование для отслеживания CDC на протяжении всей жизни пациента. Но пока Миллер говорит: «Мы не знаем, кто самый старый человек, живущий с ACH. У нас нет возможности узнать ».
3. Операция по поводу врожденного порока сердца не является лекарством.
Если вы перенесли операцию на сердце в детстве, вам необходимо наблюдение как взрослый.«Врачи используют слово« фиксированный », но вы не фиксированы. Вы не излечились », — говорит Миллер, добавляя, что именно этот факт о ИБС удивил ее больше всего. По данным ACHA, взрослые с ИБС могут испытывать постоянные проблемы со здоровьем, такие как нарушение сердечного ритма, инсульт, сердечная недостаточность и даже преждевременная смерть от сердечно-сосудистых заболеваний, а также в три раза чаще госпитализации по сравнению с другими взрослыми.
Симптомы легко не заметить, потому что они неспецифичны. По словам Элизабет Э., вы можете чувствовать учащенное сердцебиение, испытывать трудности с упражнениями или испытывать повышенную утомляемость и одышку.Адамс, доктор медицины, врожденный кардиолог в Медицинском центре штата Пенсильвания в Херши, в Херши, штат Пенсильвания. Люди «могут захотеть зарыться головой в песок», — говорит доктор Адамс, вместо того, чтобы столкнуться с возможностью обострения проблемы с сердцем.
4. Если вы родились с врожденным пороком сердца, вашему взрослому сердцу требуется специализированная помощь.
Вы должны посещать кардиолога со специальной подготовкой по врожденным порокам сердца хотя бы один раз, согласно рекомендациям Американского колледжа кардиологов и Американской кардиологической ассоциации, а в случае более сложных пороков сердца — ежегодно.Но согласно ACHA, менее 10 процентов людей, рожденных с врожденными пороками сердца, действительно получают медицинскую помощь, в которой они нуждаются во взрослом возрасте. «Правильный врач — это не то же самое, что и общий кардиолог, который, возможно, имел всего шесть часов лекций по ИБС, не имея практического опыта», — говорит Миллер. В отличие от этого, будучи взрослым специалистом по врожденным порокам сердца, Адамс более года тренировался специально по вопросам врожденных пороков сердца у взрослых.
Эта область скоро станет новой специальностью, и первые экзамены совета запланированы на октябрь 2015 года Американским советом внутренней медицины.Беглый взгляд на карту клиник взрослых врожденных пороков сердца (ACHD) США, составленную Ассоциацией взрослых врожденных пороков сердца, показывает, что в некоторых регионах таких центров немного. Возможно, вам придется отправиться в путешествие, чтобы получить необходимое вам специализированное лечение. Миллер из Теннесси, у которого всего две клиники ACHD в штате. Она предлагает обратиться к местному врачу, а также использовать групповой подход, включающий взрослого специалиста по ИБС. «Найдите кого-нибудь, кто позволит вам отправить им записи, а затем поговорит с вашим местным врачом», — говорит она.
5. Жизнь с врожденным пороком сердца не избавляет вас от других серьезных заболеваний.
Как взрослый человек с ИБС, вы все еще подвержены другим условиям старения, — говорит Миллер, что удивляет и разочаровывает людей. «Вы думаете, что это то, что у вас есть, и больше ничего не получите. Но могут развиться остеопороз и болезни старения. Это все еще происходит, когда вы становитесь старше », — объясняет она.
Диагноз рака матки шокировал пожизненную сердечную пациентку Алиссу Баттерфасс, мать двоих маленьких детей.Баттерфасс родился с пороком сердца, который называется перестановкой большого сосуда. «У меня был порок сердца. Я закончил. Я была в безопасности, — написала Баттерфасс в своей личной истории, рассказанной в ACHA, — но я все еще не застрахована от рака ».
6. Визуализирующие обследования сердца у людей с врожденными пороками сердца выглядят иначе.
Из-за этого кардиологи, не прошедшие специализированную подготовку по врожденным порокам сердца, могут пропустить важные признаки болезни. Возможность может упасть прямо в тот самый момент, когда вам срочно понадобится замена сердечного клапана, например.Как отмечает Миллер: «Они привыкли смотреть на сердце с нормальной структурой. У нас напуганные сердца, и нам нужно особое отношение » Дефекты в структуре сердца могут быть отверстиями в сердце, отсутствующими сосудами, деформированными сердечными клапанами или различным сочетанием изменений в нормальном расположении сердца.
7. Как взрослому человеку с врожденным пороком сердца вам необходимо заниматься спортом.
«Когда я рос, мне никогда не разрешали заниматься спортом», — вспоминает Миллер. «Теперь они обнаружили, что упражнения чрезвычайно важны! Они побуждают людей ходить и двигаться.Миллер советует вместе с врачом найти безопасный и подходящий план упражнений. Американская кардиологическая ассоциация (AHA) отмечает, что большинству людей, рожденных с пороками сердца, не нужно ограничивать свою физическую активность.
8. С возрастом вам может понадобиться кардиостимулятор.
«Мне никогда не говорили, что мне может понадобиться кардиостимулятор», — говорит Миллер. «Но в 42 года мне поставили кардиостимулятор, когда у меня было двое маленьких детей». Под кожу имплантируется кардиостимулятор, который с помощью электрического импульса поддерживает регулярное биение камер сердца.Аномальная частота сердечных сокращений, называемая аритмией, может развиться у многих людей, живущих с врожденным пороком сердца. Тахикардия, очень частое сердцебиение, особенно распространено, отмечается в обзоре в Circulation. По опыту Миллера, у некоторых пациентов с ИБС фибрилляция предсердий развивается во взрослом возрасте.
«Вставить вывод от кардиостимулятора в сердце сложнее для многих взрослых пациентов с ИБС», — говорит Адамс. «Если у вас нет всех нужных связей в сердце, может быть сложнее продеть провода», — объясняет она.
9. Употребление алкоголя может быть опаснее для вас, если вы родились с врожденным пороком сердца.
«Употребление алкоголя может вызвать обезвоживание и усугубить аритмию», — говорит Миллер, у которого неконтролируемая фибрилляция предсердий — наиболее частое нарушение сердечного ритма. Помимо алкоголя, особенно опасны курение и стимуляторы, такие как кокаин, если вы живете с врожденным пороком сердца. По данным AHA, внутривенное введение препаратов подвергает ваше сердце еще большему риску.
10. Поиск сети поддержки может изменить жизнь.
«Наличие сети поддержки людей, которые понимали вас, изменило мою жизнь. Это зажгло во мне страсть », — говорит Миллер, который сейчас работает с ACHA. Дискуссионный форум в ACHA насчитывает 8 400 участников и продолжает расти, охватывая тысячи тем. А искренние послы ACHA готовы помочь пациентам и их семьям получить дополнительную личную поддержку на пути к здоровью. Сообщество Support Network в AHA также имеет онлайн-форум для родителей детей с врожденными пороками сердца.
Обзор дефекта межжелудочковой перегородки (VSD)
Сердце имеет четыре камеры: правую и левую верхнюю камеру, называемую предсердием, и правую и левую нижнюю камеру, называемую желудочком. Отверстие в стенке, разделяющее нижние камеры сердца (желудочки) и позволяющее крови проходить от левой стороны сердца к правой, называется дефектом межжелудочковой перегородки (VSD). Маленький VSD может не вызвать проблем, а многие маленькие VSD закрываются сами по себе. Средние или большие межжелудочковые перегородки могут нуждаться в хирургическом вмешательстве в раннем возрасте, чтобы предотвратить осложнения.ДМЖП, как известно, является одним из наиболее часто регистрируемых врожденных пороков сердца, с частотой от 0,1% до 0,4% всех живорождений и составляющим примерно от 20% до 30% всех врожденных пороков сердца.
Симптомы дефекта межжелудочковой перегородкиПризнаки и симптомы серьезных пороков сердца часто появляются в течение первых нескольких дней, недель или месяцев жизни ребенка. Симптомы ВСД у ребенка могут включать:
- Плохая прибавка в весе
- Учащенное дыхание или одышка.
- Усталость, повышенное потоотделение
- Одышка или шум в сердце слышны при прослушивании сердца с помощью стетоскопа.
Врач может не заметить признаков ДМЖП при рождении. Если дефект небольшой, симптомы могут проявиться только в детстве. Признаки и симптомы также различаются в зависимости от размера отверстия и других связанных с ним пороков сердца.
Врач может сначала заподозрить наличие порока сердца только во время регулярного осмотра, если он или она замечает шум во время прослушивания сердца ребенка с помощью стетоскопа.Иногда ДМЖП можно обнаружить даже при УЗИ плода еще до рождения ребенка. В других случаях ДМЖП не распознается, пока пациент не достигнет совершеннолетия.
Причины дефекта межжелудочковой перегородкиНет явной причины VSD. Считается, что генетика и факторы окружающей среды играют роль. ДМЖП могут возникать сами по себе или в сочетании с другими врожденными пороками сердца. ДМЖП возникает, когда мышечная стенка, разделяющая сердце на левую и правую стороны, не может полностью сформироваться между нижними камерами сердца во время внутриутробного развития.
Обычно правая сторона сердца перекачивает кровь в легкие для получения кислорода, а левая сторона перекачивает богатую кислородом кровь к остальному телу. VSD позволяет насыщенной кислородом крови смешиваться с дезоксигенированной кровью, заставляя сердце работать сильнее, чтобы обеспечить ткани организма достаточным количеством кислорода.
ДМЖП могут иметь несколько размеров и могут присутствовать в более чем нескольких местах стенки между желудочками одновременно.
Также возможно получить ДМЖП в зрелом возрасте, обычно после сердечного приступа или может даже возникнуть как осложнение некоторых сердечных вмешательств.
Факторы риска дефекта межжелудочковой перегородкиVSD может быть вызван семейной причиной или может возникать вместе с другими генетическими проблемами, такими как синдром Дауна.
Осложнения дефекта межжелудочковой перегородкиМаленький VSD редко может вызывать какие-либо проблемы. Сравнительно более крупные дефекты могут привести к легкой или даже опасной для жизни инвалидности. Лечение может предотвратить многие осложнения.
- Сердечная недостаточность : Из-за среднего или большого ДМЖП сердцу требуется работать больше, чем обычно, чтобы перекачивать достаточно крови в организм.В результате, если эти дефекты не лечить, может развиться сердечная недостаточность.
- Легочная гипертензия : Повышенный приток крови к легким из-за ДМЖП приводит к высокому кровяному давлению в легочных артериях с возможностью необратимого повреждения. Это состояние может привести к обратному кровотоку через отверстие, так называемому синдрому Эйзенменгера.
- Эндокардит : Редко.
- Другие проблемы с сердцем , включая нарушения сердечного ритма и клапанные проблемы.
В большинстве случаев невозможно предотвратить рождение ребенка с ДМЖП. Однако важно сделать все возможное, чтобы беременность была здоровой.
- Получите пренатальную помощь на раннем этапе, даже до наступления беременности : Поговорите со своим врачом о своем здоровье и обсудите любые изменения образа жизни, которые он может порекомендовать для здоровой беременности. Кроме того, убедитесь, что вы принимаете какие-либо лекарства.
- Соблюдайте сбалансированную диету : Включите витаминные добавки, содержащие фолиевую кислоту, и ограничьте потребление кофеина.
- Регулярно делайте физические упражнения : Поговорите с врачом, чтобы разработать план упражнений.
- Избегайте употребления веществ, которые являются известными факторами риска. : К ним относятся вредные вещества, такие как алкоголь, табак и запрещенные наркотики.
- Избегайте инфекций : Перед тем, как забеременеть, убедитесь, что у вас есть все необходимые прививки.Определенные типы инфекций могут быть вредными для развивающегося плода.
- Держите диабет под контролем : Если у кого-то диабет, проконсультируйтесь с врачом, чтобы убедиться, что он хорошо контролируется, прежде чем забеременеть.
VSD часто приводит к шуму в сердце, который ваш врач может заметить при обследовании с помощью стетоскопа. Если ваш врач испытывает такой шум в сердце, он / она может направить несколько анализов, в том числе:
- Эхокардиограмма : В этом тесте звуковые волны создают видеоизображение сердца.Врачи могут использовать этот тест для диагностики дефекта межжелудочковой перегородки и определения его размеров, локализации и степени тяжести. Его также можно использовать, чтобы узнать, есть ли другие проблемы с сердцем. Эхокардиографию также можно использовать для плода (эхокардиография плода).
- Электрокардиограмма (ЭКГ) : Этот тест регистрирует электрическую активность сердца через электроды, приклеенные к коже, и помогает диагностировать пороки сердца или проблемы с ритмом.
- Рентген грудной клетки : Рентгеновский снимок помогает врачу увидеть сердце и легкие.Это может помочь врачам увидеть, увеличено ли сердце и нет ли в легких лишней жидкости.
- Катетеризация сердца : В этом тесте тонкая гибкая трубка вводится в кровеносный сосуд в паху или руке и проводится через кровеносные сосуды в сердце. С помощью катетеризации сердца врачи могут диагностировать врожденные пороки сердца и определить функцию сердечных клапанов и камер.
- Пульсоксиметрия : Инструмент, с помощью которого небольшой зажим на кончике пальца измеряет количество кислорода, присутствующего в крови.
Маленькие ДМЖП могут не вызывать симптомов и не нуждаться в лечении. В некоторых случаях они могут закрываться сами по себе по мере роста вашего ребенка. Большие ДМЖП могут нуждаться в лечении или хирургическом вмешательстве.
- Процедура катетеризации : Закрытие межжелудочковой перегородки во время катетеризации не требует открытия грудной клетки. Вместо этого врач продевает тонкую трубку в кровеносный сосуд в области живота и направляет ее к сердцу.Затем врач использует сетку определенного размера, чтобы закрыть отверстие.
- Хирургическое лечение : Эта процедура обычно включает операцию на открытом сердце под общим наркозом. Для операции требуется вентилятор и разрез в груди. Врач закрывает отверстие пластырем или наложением швов.
- Гибридная процедура : Гибридная процедура использует комбинацию хирургических и катетерных методов. Доступ к сердцу обычно осуществляется через небольшой разрез, и процедура может выполняться без остановки сердца и с использованием вентилятора.Устройство закрывает ДМЖП через катетер, введенный через разрез.
Медицинское наблюдение
Кардиолог должен регулярно осматривать пациента. Если ДМЖП пациента небольшой или был закрыт в детстве и никаких других проблем не обнаружено, по возможности посещайте его ежегодно. .
Что понадобится пациенту в будущем?Лекарства могут потребоваться только в том случае, если у вашего пациента сердечная недостаточность (что очень редко) или если у пациента легочная гипертензия.При необходимости кардиолог может наблюдать за пациентом с помощью неинвазивных тестов. К ним относятся электрокардиограммы, тесты с физической нагрузкой и эхокардиограммы.
Ограничения деятельности
Большинству пациентов не нужно ограничивать свою активность. Однако, если у пациента легочная гипертензия, следует проконсультироваться с кардиологом, чтобы контролировать активность пациента.
Профилактика эндокардита
Неисправный дефект межжелудочковой перегородки не требует профилактики эндокардита в соответствии с рекомендациями современной Американской кардиологической ассоциации по лечению.После успешного закрытия ДМЖП профилактическое лечение необходимо только в течение шестимесячного периода заживления.
Беременность
Как только достигается закрытие дефекта межжелудочковой перегородки и не возникает нежелательной легочной гипертензии, риск беременности низкий. Если закрытие межжелудочковой перегородки не достигнуто, необходимо проконсультироваться с кардиологом.
Офис исследований Стартап, связанный с Калифорнийским университетом в Дэвисе, стремится улучшить обнаружение врожденных пороков сердца у новорожденных
28 апреля 2021 г.
Хизер Сифкес, доцент кафедры реанимации в детской больнице Калифорнийского университета в Дэвисе и основатель стартапа NeoPOSE, подписала письмо-соглашение об исключительных правах на коммерциализацию новой технологии, разработанной в Калифорнийском университете в Дэвисе, которая может улучшить обнаружение врожденных пороков сердца. у новорожденных.
По данным Центров по контролю за заболеваниями, около 7200 детей в США рождаются с критическим врожденным пороком сердца (ВПС) каждый год. Состояние опасно для жизни и мешает сердцу эффективно циркулировать кровь по всему телу.
Современный подход к скринингу этих дефектов использует пульсоксиметрию. Неинвазивный, безболезненный и недорогой тест измеряет насыщение крови кислородом как показатель того, насколько хорошо кислород доставляется к тканям через тело.Все штаты теперь требуют проверки. Сама Сифкес помогла принять закон в Орегоне, дав показания в поддержку экрана, пока закон рассматривался.
«Обязательство штатов было огромным шагом вперед в плане помощи в скрининге, но, к сожалению, примерно 15 процентов критических врожденных пороков сердца все еще остаются невыявленными», — сказал Сифкес. «И когда дело доходит до таких пороков сердца, сроки обнаружения имеют решающее значение».
Личный клинический опыт Зифкес укрепляет ее мотивацию продолжать улучшать обнаружение.Она вспоминает, в частности, один случай, когда двухнедельный ребенок пришел в отделение неотложной помощи очень больным.
«Было ясно, что у ребенка порок сердца, который не был обнаружен с помощью оксиметрического теста», — сказала она. «Поздний диагноз привел к неудачной смерти ребенка и зажег во мне огонь, чтобы изучить исследования, чтобы предотвратить повторение таких трагедий».
«Пульсовая оксиметрия хороша для выявления дефектов, которые вызывают плохую оксигенацию кровотока, например, когда прерывается путь от сердца к легким и обратно к сердцу», — сказала она.«Но условия, которые препятствуют кровотоку к телу, такие как коарктация аорты, выявляются только примерно в одной трети случаев с помощью скрининга насыщения кислородом». Коарктация аорты или сужение сосуда аорты — один из наиболее распространенных критических пороков сердца.
Чтобы восполнить пробел, Зифкес попытался усовершенствовать текущий инструмент скрининга, зная, что это может быть самый быстрый путь к клиническому признанию.
Пульсоксиметрию также можно использовать для количественной оценки кровотока, чтобы выявить отклонения, вызванные препятствиями на пути к телу, но изменчивость данных с течением времени делает это непрактичным для интерпретации и применения в клинических условиях.Как практикующий врач Сифкес знал, что данные необходимо будет обработать таким образом, чтобы они были ясными и применимыми.
Сифкес заручился помощью аспирантов и профессоров Чен-Ни Чуа и Сатьяна Лакшминрусимха для разработки алгоритма скрининга, который сочетает в себе неинвазивные измерения характеристик перфузии, оксигенации и формы волны.
В 2019 году команда получила награду Национального института здоровья детей и развития человека Юнис Кеннеди Шрайвер (NICHD) и грант Национального центра развития трансляционных наук (NCATS) на проведение клинического исследования в шести больницах.Цель состояла в том, чтобы разработать модель машинного обучения / искусственного интеллекта для определения значения перфузии (кровотока), которое может предсказать CCHD.
В 2020 году Siefkes получила внутреннее финансирование в виде гранта на подтверждение концепции от программы Venture Catalyst Data, Informatics and Application Launch (DIAL). Программа предоставляет гранты до 20 000 долларов США на продвижение исследований и инноваций с коммерческим потенциалом.
