Гемотрансфузия — это… Что такое Гемотрансфузия?
Гемотрансфузия (от др.-греч. αἷμα — кровь и от лат. trasfusio — переливание) — переливание крови, частный случай трансфузии, при которой переливаемой от донора к реципиенту биологической жидкостью является кровь или её компоненты. [1][2] Переливание цельной крови можно обозначить как трансплантацию, так как кровь является соединительной тканью.[источник не указан 50 дней]
Технология
Аппарат для переливания кровиПроизводится через вены (в острых случаях — через артерии) (также с использованием препаратов крови[3]) для замещения эритроцитов, лейкоцитов, белков плазмы крови, также для остановки восстановления объёма циркулирующей крови, её осмотического давления при потере крови (для этих целей могут использоваться также заменители крови).
Кроме потери крови показанием могут быть также аплазии кроветворения, ожоги, инфекции, отравления и другие.
Переливание может быть прямым и с предварительным сбором крови донора для хранения. Современный подход к переливанию крови состоит в компонентном переливании (плазма, эритроцитарная масса, лейкоцитарная масса, тромбоцитарная масса, отмытые эритроциты, тромбовзвесь, криопреципитат и другие более редкие компоненты).
При переливании непроверенной крови в кровь реципиента могут попадать возбудители болезней, имеющиеся у донора. В связи с этим в настоящее время широко используется метод карантинизации компонентов крови.
Кровь донора и реципиента должна быть совместима:
В ряде случаев при переливании учитывают наличие и других антигенов, например, Kell[4].
Кровь переливают строго по совпадению группы крови и резус фактора, лет 30 назад считалось, что первая группа крови с отрицательным резус-фактором является универсальной для всех групп, но с открытием агглютиногенов это мнение было признано неверным.
На данный момент «универсальной» крови нет, хотя есть равноценный кровезаменитель [5] — т. н. «голубая кровь.»[6][7] При переливании обязательно соблюдаются группа крови и резус-фактор.
История
- 1628 г. — Английский врач Уильям Гарвей делает открытие о кровообращении в человеческом организме. Почти сразу после этого была предпринята первая попытка переливания крови.
- 1665 г. — Проведены первые официально зарегистрированные переливания крови: английский врач Ричард Лоуэр (англ. Richard Lower) успешно спасает жизни больных собак, переливая им кровь других собак.
- 1667 г. — Жан-Батист Дени (фр. Jean-Baptiste Denis) во Франции и Ричард Лоуэр в Англии независимо друг от друга делают записи об удачных переливаниях крови от овцы человеку. Но в последующие десять лет переливания от животных к людям были запрещены законом из-за тяжёлых отрицательных реакций.
- 1795 г. — В США американский врач Филипп Синг Физик (англ. Philip Syng Physick) проводит первую трансфузию крови от человека к человеку, хотя информацию об этом нигде не публикует.
- 1818 г. — Джеймс Бланделл (англ. James Blundell), британский акушер, проводит первое удачное переливание человеческой крови пациентке с послеродовым кровотечением. Используя в качестве донора мужа пациентки, Бланделл взял у него почти четыре унции крови из руки и с помощью шприца перелил женщине. С 1825 по 1830 год Бланделл провел 10 трансфузий, пять из которых помогли пациентам. Бланделл опубликовал свои результаты, а также изобрёл первые удобные инструменты для взятия и переливания крови.
- 1832 г. — петербургский акушер Андрей Мартынович Вольф впервые в России успешно перелил роженице с акушерским кровотечением кровь её мужа и тем самым спас ей жизнь. Для переливания крови Вольф использовал методику, разработанную Бланделлом.
- 1900 г. — Карл Ландштейнер (нем. Karl Landsteiner), австрийский врач, открывает первые три группы крови — A, В и С. Группа С будет потом заменена на О. За свои открытия Ландштейнер получил в 1930 году Нобелевскую премию.
- 1902 г. — Коллеги Ландштейнера Альфред де Кастелло (итал. Alfred Decastello) и Адриано Стурли (итал. Adriano Sturli) добавляют к списку групп крови четвертую — AB.
- 1907 г. — Гектоэн (Hektoen) делает предположение о том, что безопасность трансфузий может быть усовершенствована, если кровь донора и реципиента проверять на совместимость, чтобы избежать осложнений. Рубен Оттенберг (англ. Reuben Ottenberg) в Нью-Йорке проводит первое переливание крови с использованием метода перекрёстной совместимости. Оттенберг также заметил, что группа крови передаётся по наследству по принципу Менделя и отметил «универсальную» пригодность крови первой группы.
- 1912 г. — Роджер Ли, врач общественной больницы Массачусетса, вместе с Полом Дадли Вайтом внедряют в лабораторные исследования так называемое «время свертывания крови Ли-Вайта». Ещё одно важнейшее открытие делает Ли, опытным путём доказывая, что кровь первой группы может быть перелита пациентам с любой группой, а пациентам с четвёртой группой крови подходит любая другая группа крови. Таким образом, введены понятия «универсальный донор» и «универсальный реципиент».
- 1914 г. — Изобретены и введены в действие антикоагулянты долговременного действия, позволившие консервировать донорскую кровь, и среди них цитрат натрия.
- 1915 г. — В госпитале Маунт Синай в Нью-Йорке, Ричард Левисон впервые использует цитрат для замены прямого переливания крови на непрямое. Несмотря на всю значимость этого изобретения, цитрат ввели в массовое использование только через 10 лет.
- 1916 г. — Фрэнсис Рус и Д. Р. Турнер впервые используют раствор цитрата натрия и глюкозы, позволяющий хранить кровь в течение нескольких дней после донации. Кровь начинают хранить в закрытых контейнерах. В ходе Первой мировой войны Великобритания использует мобильную станцию переливания крови (создателем считается Освальд Робертсон).
Кровяной допинг
Аутогемотрансфузия (переливание реципиенту его же собственной крови) достаточно распространена в спорте, несмотря на то, что МОК и ВАДА приравнивают её к применению допинга. Она ускоряет доставку кислорода к мышцам, тем самым увеличивая их производительность [8].
Видео
- Голубая кровь Документальный фильм о разработках кровезаменителя Группы профессора Ф. Ф. Белоярцева
Литература
- Монографии
- Справочник фельдшера/Под редакцией профессора А. Н. Шабанова. — М.:»Медицина», 1976 год
- Аграненко В. А. и Скачилова Н. Н. Гемотрансфузионные реакции и осложнения, М., 1986;
- Гаврилов О. К., Очерки истории развития и применения переливания крови, Л., 1968;
- Островский А. Г., Карашуров Е. С. .Переливание крови, препаратов крови и кровезаменителей: Учебное пособие. — Петрозаводск.:Изд-во ПетрГУ, 2000. — 136 с: ил.(Табл. 5. Ил. 37. Библиогр.:19 назв.)
- Петров И. Р., Бондина В. А., Сенчило Е. А., Плазмозамещающие растворы при лечении кровопотери и шока, Л., 1969;
- Репина М. А. Кровотечения в акушерской практике, М., 1986;
- Руководство по общей и клинической трансфузиологии, под ред. Б. В. Петровского, М., 1979;
- Руководство по переливанию крови и кровезаменителей, М.,1965
- Свирко Ю. С. «ПАТОФИЗИОЛОГИЧЕСКИЕ АСПЕКТЫ ПРИМЕНЕНИЯ КРОВЕСБЕРЕГАЮЩИХ МЕТОДИК У КАРДИОХИРУРГИЧЕСКИХ ПАЦИЕНТОВ С ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА»: Автореф. … д-ра мед. наук. — Томск, 2008. — 44 с.
- Серов В. Н. и Макацария А. Д. Тромботические и геморрагические осложнения в акушерстве, М., 1987;
- Справочник «Домашний Доктор» Глава IV. Хирургические болезниПереливание крови и кровезаменителей
- Справочник по кровезаменителям и препаратам крови, под ред. А. И. Бурназяна, М., 1969.
- Справочник по переливанию крови и кровезаменителей, под ред. О. К. Гаврилова,М., 1982.
- Тихонов В. И., Попов О. С., Шпилевой П. К. Кровотечение. Переливание крови: Учебно-методическое пособие. — Томск.:Изд-во ТГУ, 2005. — 148 с.
- Филатов А. Н., Чаплыгина 3. А., Депп М. Е., Белковые гидролизаты, [Л.], 1968
- Чернуха Е. А. и Комиссарова Л. М. Ведение больных с кровотечением во время и после операции кесарева сечения, Акуш. и гинек., № 10, с. 18,1986.
- Специализированные печатные издания
- Публицистика
- Евгения Рябцева, Александр Чубенко. Кровное дело // интернет-журнал «Коммерческая биотехнология» «Популярная механика» № 6, 2007
- Ольга Скрипник. Кровный интерес или Проблемы переливания донорской крови.
- Законодательство
Примечания
См. также
Переливание крови
Переливание крови (гемотрансфузия) — лечебный метод, заключающийся во введении в кровеносное русло больного (реципиента) цельной крови или ее компонентов, заготовленных от донора или от самого реципиента (аутогемотрансфузия), а также крови, излившейся в полости тела при травмах и операциях (реинфузия).
В лечебной практике наиболее широкое распространение имеет переливание эритроцитной массы (взвеси эритроцитов), свежезамороженной плазмы, концентрата тромбоцитов, лейкоцитной массы. Трансфузии эритроцитной массы показаны при различных анемических состояниях. Эритроцитная масса может применяться в комплексе с плазмозаменителями и препаратами плазмы. При переливании эритроцитной массы практически не бывает осложнений.
Трансфузии плазмы показаны при необходимости коррекции объема циркулирующей крови при массивных кровотечениях (особенно в акушерской практике), ожоговой болезни, гнойно-септических процессах, гемофилии и т. д. С целью максимального сохранения структуры плазменных белков и их биологической активности полученную после фракционирования плазму подвергают быстрому замораживанию при температуре -45°С). В то же время объем-замещающий эффект от введения плазмы непродолжителен и уступает действию альбумина и плазмозаменителей.
Переливание тромбоцитной массы показано при тромбоцитопенической кровоточивости. Лейкоцитную массу переливают больным при снижении способности к выработке собственных лейкоцитов. Наиболее распространенным методом переливания цельной крови или ее компонентов является внутривенное введение с помощью системы одноразового пользования с фильтром. Используются и другие пути введения крови и ее компонентов: внутриартериальный, внутриаортальный, внутрикостный.
Метод переливания цельной крови непосредственно от донора больному без стадии консервации крови называется прямым. Так как технологией этого метода не предусмотрено использование фильтров во время переливания, существенно повышается риск попадания в кровеносное русло реципиента мелких тромбов, неизбежно образующихся в системе для переливания, что чревато развитием тромбоэмболии мелких ветвей легочной артерии. Обменное переливание крови — частичное или полное удаление крови из кровеносного русла реципиента с одновременным замещением ее адекватным или превышающим объемом донорской крови — применяется для удаления различных ядов (при отравлениях, эндогенных интоксикациях), продуктов распада, гемолиза и антител (при гемолитической болезни новорожденных, гемотрансфузионном шоке, тяжелых токсикозах, острой почечной недостаточности). Лечебный плазмаферез является одной из основных трансфузиологических операций, при этом одновременно с изъятием плазмы проводится восполнение забираемого объема переливанием эритроцитов, свежезамороженной плазмы, реологических плазмозаменителей. Лечебное действие плазмафереза основано как на механическом удалении с плазмой токсических метаболитов, так и на возмещении недостающих жизненно важных компонентов внутренней среды организма, а также на деблокировании органов («очищение» печени, селезенки, почек).
 Правила
переливания крови
Правила
переливания крови
Правила переливания крови
Правила переливания крови
Показания к назначению переливания любой трансфузионной среды, а также ее дозировка и выбор метода трансфузии определяются лечащим врачом на основании клинических и лабораторных данных. Врач, производящий трансфузию, обязан независимо от проведенных ранее исследований и имеющихся записей лично провести следующие контрольные исследования: 1) определить групповую принадлежность крови реципиента по системе AB0 и сверить результат с данными истории болезни; 2) определить групповую принадлежность эритроцитов донора и сопоставить результат с данными на этикетке контейнера или бутылки; 3) провести пробы на совместимость в отношении групп крови донора и реципиента по системе AB0 и резус-фактору; 4) провести биологическую пробу.
Подбор крови и ее компонентов для переливания. Перед переливанием необходимо проведение следующих трансфузиологических мероприятий:
1) Получить предварительное добровольное согласие гражданина на переливание крови и ее компонентов. В случае если пациент находится в бессознательном состоянии, то необходимость трансфузии для спасения жизни пациента обосновывает показания врачей. Переливание крови детям проводят с письменного разрешения родителей.
2) Проверить группу крови пациента по системе АВ0, сверить полученный результат с данными истории болезни.
3) Перепроверить группу крови по системе АВ0 донорского контейнера с данными на этикетке контейнера.
4) Сравнить группу крови и резус-принадлежность, обозначенные на контейнере, с результатами исследования ранее внесенными в историю болезни и только что полученными.
5) Провести пробы на индивидуальную совместимость по системе АВО и резус эритроцитов доноров и сыворотки реципиента.
6) Уточнить у пациента фамилию, имя, отчество, год рождения и сверить их с указанными на титульном листе истории болезни. Данные должны совпадать и пациент должен их по возможности подтвердить (за исключением случаев, когда переливание проводят под наркозом или в бессознательном состоянии).
7) Провести биологическую пробу.
Визуально врач, осуществляющий трансфузию, проверяет герметичность упаковки, правильность паспортизации, оценивает качество трансфузионной среды. Определять годность гемотрансфузионной среды необходимо при достаточном освещении непосредственно на месте хранения, не допускается взбалтывание. Критериями годности для переливания являются: для цельной крови – прозрачность плазмы, равномерность верхнего слоя эритроцитов, наличие четкой границы между эритроцитами и плазмой, а для свежезамороженной плазмы – прозрачность при комнатной температуре. Запрещается переливание крови и ее компонентов, предварительно не обследованного на ВИЧ, гепатиты В и С, сифилис.
Проба на индивидуальную совместимость донора и реципиента по системе АВО.
На пластинку наносят 2-3 капли сыворотки реципиента и добавляют небольшое количество эритроцитов с таким расчетом, чтобы соотношение эритроцитов и сыворотки было 1:10 (для удобства рекомендуется сначала выпустить через иглу несколько капель эритроцитов из контейнера на край пластинки, затем оттуда стеклянной палочкой перенести маленькую каплю эритроцитов в сыворотку). Далее эритроциты перемешивают с сывороткой, пластинку слегка покачивают в течение 5 мин, наблюдая за ходом реакции. По истечении указанного времени в реагирующую смесь можно добавить 1-2 капли физиологического раствора для снятия возможной неспецифической агрегации эритроцитов. Учет результатов. Наличие агглютинации эритроцитов означает, что кровь донора несовместима с кровью реципиента и не должна быть ему перелита. Если по истечению 5 мин агглютинация эритроцитов отсутствует, то это означает, что кровь донора совместима с кровью реципиента по групповым агглютиногенам.
Непрямая проба Кумбса. В пробирку вносят 1 каплю (0,02 мл) осадка трижды отмытых эритроцитов донора, для чего выдавливают из пипетки небольшую каплю эритроцитов и касаются ею дна пробирки и добавляют 4 капли (0,2 мл) сыворотки реципиента. Содержимое пробирок перемешивают встряхиванием, после чего их помещают на 45 мин в термостат при температуре +37ºС. По истечению указанного времени эритроциты вновь трижды отмывают и готовят 5% взвесь в физиологическом растворе. Далее 1 каплю (0,05 мл) взвеси эритроцитов на фарфоровую пластинку, добавляют 1 каплю (0,05 мл) антиглобулиновой сыворотки, перемешивают стеклянной палочкой. Пластинку периодически покачивают в течении 5 минут. Учет результатов проводят невооруженным глазом или через лупу. Агглютинация эритроцитов свидетельствует о том, что кровь реципиента и донора несовместимы, отсутствие агглютинации является показателем совместимости крови донора и реципиента.
Для определения индивидуальной совместимости крови по системе Резус используется проба с применением 10% желатина и 33% полиглюкина.
Проба на совместимость с применением 10% желатина. В пробирку вносят одну небольшую каплю (0,02 мл) эритроцитов донора, для чего выдавливают из пипетки небольшую каплю эритроцитов и касаются ею дна пробирки. Добавляют 2 капли (0,1 мл) желатина и 2 капли (0,1 мл) сыворотки реципиента. Содержимое пробирок перемешивают встряхиванием, после чего их помещают в водяную баню на 15 минут или термостат на 30 мин при температуре +46-48ºС. По истечению указанного времени в пробирки добавляют 5-8 мл физиологического раствора и перемешивают содержимое путем 1-2 кратного переворачивания пробирок. Результат учитывают рассматривая пробирки на свет. Агглютинация эритроцитов свидетельствует о том, что кровь реципиента и донора не совместимы, отсутствие агрегации является показателем совместимости крови донора и реципиента.
Проба на совместимость с применение 33% полиглюкина. В пробирку вносят 2 капли (0,1 мл) сыворотки реципиента, 1 каплю (0,05 мл) эритроцитов донора и добавляют 1 каплю (0,1 мл) 33% полиглюкина. Пробирку наклоняют до горизонтального положения слегка потряхивая, затем медленно вращают таким образом, чтобы содержимое ее растеклось по стенкам тонким слоем. Такое растекание содержимого делает реакцию более выраженной. Контакт эритроцитов с сывороткой больного при вращении пробирки следует продолжать не менее 3 минут. Через 3-5 минут в пробирку добавляют 2-3 мл физиологического раствора и перемешивают содержимое путем 2-3 кратного перевертывание пробирки не взбалтывания. Учет результатов проводят невооруженным глазом или через лупу. Агглютинация эритроцитов свидетельствует о том, что кровь реципиента и донора несовместимы, отсутствие агглютинации является показателем совместимости крови донора и реципиента.
Биологическая проба. Перед применением контейнер с трансфузионной средой (эритроцитарная масса или взвесь, свежезамороженная плазма, цельная кровь) извлекают из холодильника и выдерживают при комнатной температуре в течение 30 мин, а в экстренных случаях согревают в водяной бане при температуре 37ºС под контролем термометра. Техника проведения пробы заключается в следующем: одновременно переливают 10 мл трансфузионной среды со скоростью 2-3 мл (40-60 капель в минуту), затем переливание прекращают и в течение 3 минут наблюдают за реципиентом, контролируя у него пульс, артериальное давление, общее состояние, цвет кожи, измеряют температуру тела. Такую процедуру повторяют еще дважды. Появление озноба, боли в пояснице, чувства жара, стеснения в груди, головной боли, тошноты или рвоты свидетельствует о биологической несовместимости, требует немедленного прекращения трансфузии и отказа от переливания данной трансфузионной среды. При переливании крови или ее компонентов у пациентов, находящихся под наркозом о реакции или начинающихся осложнениях судят по немотивированному усилению кровоточивости в операционной ране, снижению артериального давления, учащению пульса, изменению цвета мочи при катетеризации мочевого пузыря, а также по результатам пробы на выявление раннего гемолиза. В таких случаях переливание трансфузионной среды прекращают, хирург и анестезиолог совместно с трансфузиологом обязаны выяснить причину гемодинамических нарушений. Если их причиной явилась трансфузия, то данная среда не переливается, а лечение пациента проводится в зависимости от имеющихся клинических и лабораторных данных.
Гемотрансфузионные (посттрансфузионные) реакции и осложнения. У некоторых больных вскоре после П. к. отмечаются гемотрансфузионные реакции, не сопровождающиеся серьезными длительными нарушениями функции органов и систем и не представляющие непосредственной опасности для жизни больного. В зависимости от выраженности клинических проявлений различают гемотрансфузионные реакции трех степеней: легкие, средней тяжести и тяжелые. Легкие гемотрансфузионные реакции характеризуются повышением температуры тела в пределах 1°, болями в мышцах конечностей, головной болью, познабливанием и недомоганием. Эти явления кратковременны; обычно для их купирования не требуется каких-либо специальных лечебных мероприятий. Реакции средней тяжести проявляются повышением температуры тела на 1,5—2°, нарастающим ознобом, учащением пульса и дыхания, иногда крапивницей. При тяжелых реакциях температура тела повышается более чем на 2°, наблюдаются сильный озноб, цианоз губ, рвота, сильная головная боль, боль в пояснице и костях, одышка, крапивница и отек Квинке.
В зависимости от причины возникновения и клинического течения выделяют пирогенные, аллергические, анафилактические реакции. Они появляются через 20—30 мин после трансфузии (иногда во время нее) и продолжаются от нескольких минут до нескольких часов. Пирогенные реакции могут быть следствием внесения пирогенов вместе с консервированной кровью и эритроцитной массой в кровяное русло реципиента. Они проявляются общим недомоганием, лихорадкой, ознобом, головной болью; в ряде случаев возможны циркуляторные нарушения. Аллергические реакции возникают в результате сенсибилизации реципиента к антигенам плазменных белков, различным иммуноглобулинам, а также к антигенам лейкоцитов, тромбоцитов при переливании цельной крови, плазмы. Они проявляются лихорадкой, одышкой, удушьем, тошнотой, рвотой. Анафилактические реакции обусловлены изосенсибилизацией, чаще к иммуноглобулинам класса А. Основную роль в их патогенезе играет реакция антиген — антитело. Эти реакции сопровождаются выделением биологически активных веществ, вызывающих повреждение сосудистой стенки с образованием отека, спазм мышц бронхов и резкое снижение АД. Клинически они характеризуются острыми вазомоторными расстройствами.
Для лечения пирогенных реакций применяют жаропонижающие, десенсибилизирующие и симптоматические средства; для ликвидации аллергических реакций назначают антигистаминные и десенсибилизирующие средства (димедрол, супрастин, хлорид кальция, кортикостероиды), сердечно-сосудистые препараты, промедол. Лечение анафилактических реакций комплексное и включает методы реанимации (при показаниях), поскольку исход зависит от быстроты и эффективности экстренной помощи. Внутривенно медленно вводят 60—90 мг преднизолона или 16—32 мг дексаметазона в 20 мл 40% раствора глюкозы. При отсутствии эффекта в течение 15—20 мин введение глюкокортикоидов повторяют. При тяжелом коллапсе показана трансфузия реополиглюкина. В случае необходимости применяют сердечные гликозиды: вводят в вену медленно (в течение 5 мин) 0,5—1 мл 0,05% раствора строфантина или 1 мл 0,06% раствора коргликона в 20 мл 5, 20 или 40% раствора глюкозы или изотонического раствора хлорида натрия, а также антигистаминные средства (2—3 мл 1% раствора димедрола, 1—2 мл 2% раствора супрастина или 2 мл 2,5% раствора дипразина).
Профилактика гемотрансфузионных реакций включает строгое выполнение всех условий и требований, предъявляемых к заготовке и переливанию консервированной крови и ее компонентов; правильную подготовку и обработку систем и аппаратуры для трансфузий, применение систем для П. к. одноразового пользования; учет состояния реципиента до гемотрансфузии, характер его заболевания, индивидуальные особенности и реактивность организма, выявление повышенной чувствительности к вводимым белкам, сенсибилизацию беременностями, повторными трансфузиями с образованием антилейкоцитарных, антитромбоцитарных антител, антител к плазменным белкам и др.
Клинически осложнение, вызванное переливанием крови или эритроцитной массы, несовместимой по групповым факторам системы АВ0, проявляется гемотрансфузионным шоком, который возникает в момент трансфузии или чаще в ближайшее время после нее. Характерны кратковременное возбуждение больного, боли в груди, животе, пояснице. В дальнейшем отмечаются тахикардия, артериальная гипотензия, развивается картина массивного внутрисосудистого гемолиза (гемоглобинемия, гемоглобинурия, билирубинемия, желтуха) и острого нарушения функции почек и печени. Если шок развивается во время оперативного вмешательства, происходящего под наркозом, появляется выраженная кровоточивость.
Клинические проявления осложнений, вызванных переливанием крови или эритроцитной массы, несовместимой по резус-фактору, в большинстве случаев такие же, как и после переливания цельной крови или эритроцитной массы, несовместимой по групповым факторам АВ0, но они, как правило, возникают несколько позднее, протекают менее выражение.
При развитии гемотрансфузионного шока следует прежде всего немедленно прекратить П. к. и приступить к проведению интенсивной терапии. Основные лечебные мероприятия должны быть направлены на восстановление и поддержание функции жизненно важных органов, купирование геморрагического синдрома, предупреждение острой почечной недостаточности.
Для купирования нарушений гемодинамики и микроциркуляции необходимо вводить плазмозамещающие растворы реологического действия (реополиглюкин), гепарин, свежезамороженную плазму, 10—20% раствор сывороточного альбумина, изотонический раствор хлорида натрия или раствор Рингера — Локка. При проведении указанных мероприятий в пределах 2—6 ч после переливания несовместимой крови обычно удается вывести больных из состояния гемотрансфузионного шока и предупредить развитие острой почечной недостаточности.
Лечебные мероприятия осуществляют в следующем порядке. Производят инъекции сердечно-сосудистых (0,5—1 мл коргликона в 20 мл 40% раствора глюкозы), спазмолитических (2 мл 2% раствора папаверина), антигистаминных (2—3 мл 1% раствора димедрола, 1—2 мл 2% раствора супрастина или 2 мл 2,5% раствора дипразина) средств и кортикостероидных препаратов (внутривенно 50—150 мг преднизолона гемисукцината). При необходимости введение кортикостероидных препаратов повторяют, в последующие 2—3 дня их дозу постепенно снижают. Помимо этого, осуществляют вливание реополиглюкина (400—800 мл), гемодеза (400 мл), 10—20% раствора сывороточного альбумина (200—300 мл), щелочных растворов (200—250 мл 5% раствора гидрокарбоната натрия, лактосол), а также изотонического раствора хлорида натрия или раствора Рингера — Локка (1000 мл). Кроме того, вводят фуросемид (лазикс) внутривенно (80—100 мг), затем внутримышечно через 2—4 ч по 40 мг (фуросемид рекомендуется сочетать с 2,4% раствором эуфиллина, который вводят по 10 мл 2 раза через 1 ч, затем по 5 мл через 2 ч), маннит в виде 15% раствора внутривенно по 200 мл, через 2 ч — еще 200 мл. При отсутствии эффекта и развитии анурии дальнейшее введение маннита и лазикса прекращают, т.к. оно опасно ввиду угрозы развития гипергидратации внеклеточного пространства в результате гиперволемии, отека легких. Поэтому чрезвычайно важно раннее проведение гемодиализа (показания к нему возникают через 12 ч после зафиксированного ошибочного П. к. при отсутствии эффекта от проводимой интенсивной терапии).
Профилактика гемотрансфузионного шока основывается на тщательном выполнении врачом, переливающим кровь или эритроцитную массу, правил инструкции по П. к. Непосредственно перед П. к. или эритроцитной массы врач обязан: определить групповую принадлежность крови больного и сверить результат с записью в истории болезни и с обозначением группы крови на флаконе; определить групповую принадлежность крови донора, взятой из флакона, и сверить результат с записью на этом флаконе; провести пробы на совместимость по группам крови АВ0 и резус-фактору
что это такое, виды, показания и противопоказания, возможные осложнения переливания крови
Несмотря на огромный технологичный потенциал современной медицины применение гемотрансфузии все еще остается незаменимой процедурой.
Метод, предполагающий переливание крови, считается рискованным. Однако в отдельных ситуациях с его помощью можно спасти не только здоровье, но и жизнь человека.
Содержание материала:
Что такое гемотрансфузия
Гемотрансфузией называют медицинскую процедуру, в ходе которой реципиенту переливают кровь донора — напрямую или с использованием законсервированного материала.

Первые попытки переливания крови предприняты еще в XVII веке, когда было открыто кровообращение человека. Успех в этом направлении пришел к медикам гораздо позже — после того как ученые научились различать и определять группы крови.
Забор физиологической жидкости для длительного хранения осуществляется на станциях по переливанию крови или в других специализированных учреждениях.
Процедура сдачи донорской крови происходит добровольно. Полученный материал исследуют на наличие инфекций, затем стабилизируют и консервируют с помощью специальных добавок. Кроме того, донорская кровь служит источником для получения кровяных частиц — эритроцитов, тромбоцитов и плазмы.
В дальнейшем извлеченные компоненты используются для замещения недостающих частиц в крови пациента или на их основе производят лекарственные препараты, восстанавливающие и поддерживающие объем циркулирующего кровотока.
Найти биологическую жидкость с идеальной совместимостью параметров крайне сложно. Поэтому переливание цельной крови практикуется редко — только в случаях экстренной необходимости прямой гемотрансфузии.
Виды переливания крови
Процедура гемотрансфузии различается по методу выполнения и способу подачи крови. Выбор того или иного вида переливания определяется спецификой поставленных медиками задач и состоянием здоровья пациента.
Основные способы переливания крови:
- внутривенный — базовый, наиболее распространенный вид гемотрансфузии. Выполняется путем введения катетера в подключичную вену;
- внутриартериальный — применяется в исключительных случаях, например, при остановке сердца;
- внутрикостный — кровь вводят в подвздошную костную ткань или в скелетную часть грудины;
- внутрисердечный — гемотрансфузию в левый желудочек выполняют в тех случаях, когда нет возможности применить другие способы ввода биологической жидкости;
- внутриаортальный — применяется только в экстренных ситуациях.
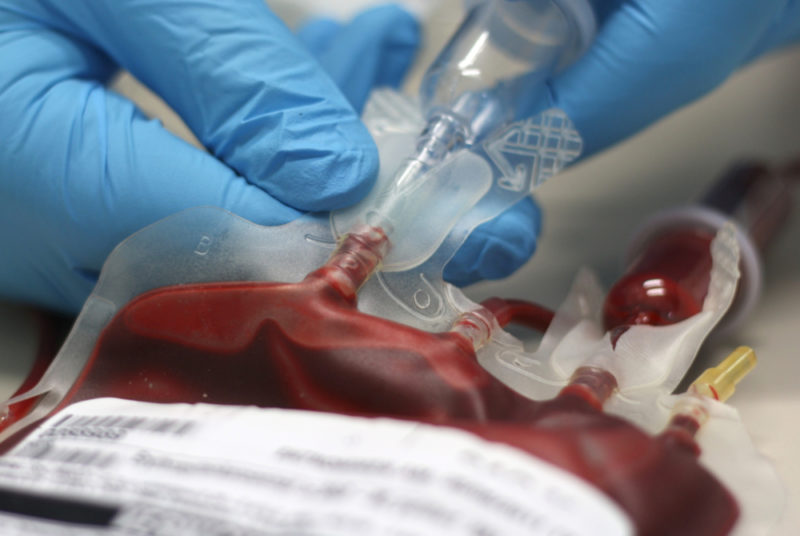
Прямое переливание крови предусматривает инфузию непосредственно из вены донора с применением специализированного медицинского оборудования, обеспечивающего непрерывную подачу биологической жидкости.
Непрямое переливание крови — процедура, в ходе которой используется законсервированный донорский материал.
Кроме того, существуют альтернативные виды гемотрансфузии:
- обменная, при которой у реципиента предварительно откачивают часть крови, а затем вводят донорский материал;
- аутогемотрансфузия — метод применения заранее законсервированной крови самого пациента;
- реинфузия — повторное использование крови, излитой и собранной в ходе оперативного вмешательства.
Скорость вливания биологической жидкости зависит от типа инфузии — капельной, струйной или струйно-капельной. Выбор параметров процедуры полностью находится в компетенции врача.
Биологическая проба на совместимость
Индивидуальные параметры крови у всех людей разные, даже если они близкие родственники. Исключение составляют только однояйцевые близнецы.

Поэтому чтобы избежать отторжения медики проверяют инфузионный материал на совместимость с кровью реципиента.
Как правило, биологическая проба на совместимость крови проходит в три этапа:
- пациенту струйно вливают 15 мл донорского материала;
- в течение трех минут контролируются показатели состояния реципиента — частота пульса, интенсивность дыхания, уровень артериального давления, возникновение отеков в области лица;
- при отсутствии побочных реакций процедуру повторяют еще два раза.
Если трехкратная проверка показала отсутствие осложнений, значит, вливаемая кровь совместима с биологическими параметрами пациента.
У пациентов, находящихся под наркозом, свидетельством совместимости крови считается стабильность параметров гемодинамики и общих показателей их состояния.
О наличии несовместимости свидетельствуют такие реакции, как: затрудненность дыхания, снижение давления, учащение сердцебиения, тяжесть в груди, нередко — боли в области поясницы.
Показания и подготовка к процедуре
По степени актуальности показания к гемотрансфузии разделяют на абсолютные и относительные. Абсолютным называют такое состояние больного, когда переливание крови расценивается как единственный способ его стабилизации и избежания смерти.
Применение гемотрансфузии особенно актуально при острых кровопотерях, травматическом шоке или обширных оперативных вмешательствах, вызвавших потерю большого количества крови.
К относительным показаниям относятся состояния, когда гемотрансфузия расценивается как вспомогательное, но не обязательное лечебное мероприятие.
В списке основных относительных показаний:
- анемии любой этиологии;
- воспалительные процессы, сопровождающиеся тяжелой формой интоксикации;
- нарушения свертываемости крови;
- авитаминоз, истощение организма вследствие голодания или хронической патологии;
- геморрагический диатез.
Инфузии донорской кровью позволяют заместить объем утраченной крови, восстановить газообменную функцию, усилить иммунный потенциал и обеспечить нормализацию свертывания.
Особенности подготовительного периода
Подготовка к переливанию крови призвана исключить развитие побочных реакций и осложнений, а также снизить сенсибилизацию организма.

Наиболее важным моментом подготовки к процедуре считается определение группы крови и резус-фактора пациента и донорского материала, сопоставление полученных данных.
Совместимой считается кровь одной групповой принадлежности и резус-фактора.
Кроме того, в обязанности врача входит полный сбор анамнеза пациента, а именно наличие:
- склонности к аллергии;
- хронических заболеваний;
- противопоказаний к гемотрансфузии;
- ранее перенесенных переливаний крови.
Если пациент женского пола, врач выясняет, были ли у нее роды и как они прошли. В отдельных случаях назначают дополнительное обследование на определение антител.
Кроме того, за несколько дней до процедуры пациенту рекомендуется ограничить употребление белковой пищи. А непосредственно в день переливания крови необходимо позаботиться, чтобы и кишечник, и мочевой пузырь не были заполнены.
Все перечисленные шаги подготовительного периода актуальны только при запланированном проведении гемотрансфузии.
При наличии абсолютных показаний необходимость подготовительных мероприятий к процедуре определяется врачом.
Техника переливания
Технические особенности переливания крови находятся в прямой зависимости от вида и метода выполнения гемотрансфузии.
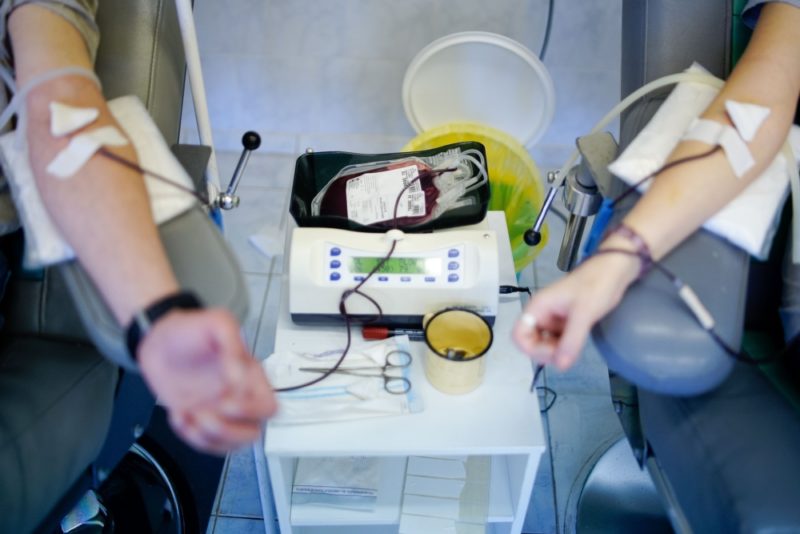
При прямой трансфузии используется только цельный биологический материал, не содержащий стабилизаторов, сохранивший все клеточные и белковые элементы, а также характеристики свертываемости.
Прямая трансфузия предполагает соединение донорской вены с веной реципиента посредством специального аппарата, устанавливаемого между донором и реципиентом.
После пункции вены пациенту вводят небольшое количество физиологического раствора. Затем выполняют пункцию вены донора и присоединяют к игле берущую часть аппаратной трубки. Ввод крови производится порциями по 25 мл. Стандартная скорость аппаратной гемотрансфузии составляет 75 мл крови в минуту.
Специфика выполнения непрямой трансфузии
При непрямой трансфузии используют специальное оборудование — систему, оснащенную короткой и длинной трубками (резиновой или пластиковой), иглами, фильтрами и капельницей с зажимом. Такие системы относятся к категории одноразовых и выпускаются в стерильной упаковке.
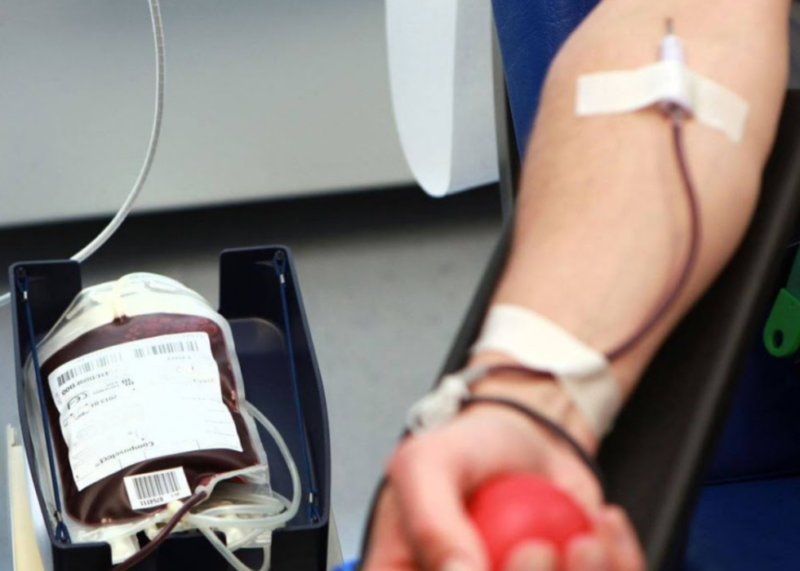
Одна из игл вводится во флакон с биологическим материалом, вторая — в вену пациента. Одно из беспрекословно выполняемых медиками правил — консервированную кровь переливают только из той емкости, в которой она упакована.
Скорость введения крови регулируют с помощью зажима, которым оснащена одна из резиновых трубок. Стандартная скорость трансфузии составляет 50 капель в минуту. Гемотрансфузию завершают, если во флаконе осталось 20 мл биологической жидкости. Иглу извлекают из вены пациента, а сверху накладывают повязку с антисептиком.
Оставшиеся 20 мл крови сохраняют в холодильнике. Если у пациента возникнут осложнения, этот материал будет исследован для определения причины побочной реакции.
Трансфузионные среды и препараты
Для выполнения гемотрансфузии используют цельную кровь, а также ее клеточные и неклеточные компоненты.

Донорская кровь для прямого переливания считается наиболее эффективной трансфузионной средой. Ее существенный недостаток — быстрая свертываемость, провоцирующая возникновение тромбоэмболии.
Консервированная кровь готовится на основе цельной с добавлением стабилизирующих и консервирующих компонентов — гидроцитрата натрия, глюкозы, фосфата. Применение цельной консервированной крови уместно при обширных кровопотерях.
Главный недостаток биоматериала — короткий срок хранения и постепенная потеря функциональных свойств уже через шесть часов после заготовки.
Клеточными компонентами называют частицы, извлеченные из цельной жидкости. На их основе создаются такие трансфузионные среды, как тромбоконцентрат, эритроцитарная масса или взвесь, гранулоциты, лейкоцитная масса.
К препаратам крови комплексного действия относят неклеточные компоненты — плазму, альбумин, сыворотку, протеин, иммуноглобулины, протромбиновый комплекс, криопреципитат, аутогемофильный глобулин, фибринолизин.
Гемотрансфузия новорожденному ребенку
Переливание крови новорожденным проводят при наличии таких же показаний, как и у взрослых людей.

Наиболее частым показанием к гемотрансфузии новорожденных считается гемолитическая желтуха. Для лечения патологии назначают введение эритроцитарной массы, отделенной от тромбоцитов и лейкоцитов.
Выбор дозировки выполняется врачом в индивидуальном порядке, с учетом особенностей организма новорожденного.
Возможные осложнения переливания крови
Процедура гемотрансфузии может стать причиной развития посттрансфузионных реакций или осложнений.

Реактивные проявления — тошнота, лихорадка, цианоз губ, повышение температуры, встречаются крайне редко и обычно не вызывают дисфункций внутренних органов.
Тогда как осложнения гемотрансфузии представляют угрозу для жизни пациента, поскольку способны вызвать серьезные нарушения работы жизненно важных органов:
- воздушная эмболия — проникновение пузырьков воздуха в вену;
- тромбоэмболия — закупорка артерий сгустками крови, которые образовались во время хранения биологической жидкости;
- гемотрансфузионный шок — результат несовместимости крови по группе или резус-фактору;
- гемолиз — острый или отсроченный. Сопровождается разрушением эритроцитов;
- цитратная или калиевая интоксикации — наблюдаются при избытке стабилизирующих биоматериал веществ;
- синдром массивной гемотрансфузии — возникает при избыточном вливании крови за короткий промежуток времени;
- вирусное или бактериальное заражение.
Появление трансфузионных осложнений свидетельствует о нарушении правил проведения процедуры или применении биоматериалов, несовместимых с кровью пациента.
Противопоказания к процедуре
Количество противопоказаний к проведению переливания крови значительно превышает список ситуаций, при которых эта процедура может быть полезной. Более того, если не учесть или игнорировать противопоказания к гемотрансфузии, процедура может стать причиной тяжелых нарушений здоровья.
Проводить переливание крови категорически запрещено пациентам, у которых диагностированы:
- острая недостаточность органов — сердца, печени, почек;
- туберкулез в активной форме;
- инфаркт миокарда;
- воспаления сердечных мышц;
- пороки сердца;
- тромбозы;
- патологии мозгового кровообращения.
Зачастую гемотрансфузия — это единственный шанс спасти пациенту жизнь. И главная задача медиков — максимально снизить риск появления осложнений и нежелательных реакций.
Обменное переливание крови — Википедия
Обме́нное перелива́ние кро́ви — синхронная инфузия донорской крови при заборе крови реципиента.
Обменное переливание крови подразумевает удаление крови из кровеносного русла пациента с одновременным замещением её на кровь донора. Объём переливаемой донорской крови равен или же превышает количество эксфузируемой крови.
Обменное переливание крови выполняют через две вены реципиента: через одну из крупных вен или артерий (для предупреждения свертывания крови при длительной процедуре) кровь реципиента эксфузируется, а через другую вливается донорская. При этом скорость обменного переливания крови — в диапазоне 50—100 мл/мин.
Создатель метода А. Богданов был убеждён, что когда идеология переживает свою социально-трудовую основу, то становится реакционной, превращаясь в «мертвеца, который хватает живого». Абсолютный марксизм по Богданову проникает в ряды борцов, подобно вампиру и превращает вчерашних активистов в неоврагов развития пролетарской мысли. Он писал[1]:
Наше отечество — страна молодого рабочего движения, не укрепившейся культуры, страна мучительно-изнуряющей борьбы — дала этому призраку едва ли не лучшие его жертвы: Г. Плеханова ещё недавно, В. Ильина теперь, не считая иных, менее крупных сил, но в своё время также полезных для общего дела. Товарищей, попавших во власть злого призрака, мы пожалеем и постараемся вылечить, хотя бы суровыми средствами, если нельзя иначе. А с вампиром поступим так, как со всякими вампирами поступать полагается: голову долой, и осиновый кол в сердце!
Врач посвятил себя Пролеткульту, а Ленин относился к пролеткультовцам настороженно — Пролеткульт был реформирован. Но врач пошёл дальше, теоретически обосновал обменное переливание крови, опираясь на тектологию («всеобщую организационную науку»).
Методика Александра Богданова[править | править код]
В конце 1925 году Сталин предложил медику создать Институт переливания крови. Для этих целей отведён особняк купца Игумнова на Большой Якиманке (в котором позднее размещена резиденция французскому посла).
Перед медиками на самом деле ставилась идеологическая задача — связать узами прямого (кровного) родства всё прогрессивное человечество. Врачи ограничились экспериментами и решением конкретных медицинских задач (среди исцеленных — сын самого Богданова). Но основатели тектологии не смирился с отказом от пролетарских идей. Была сформирована спецгруппа пациентов, в которую входила и Мария Ульянова. Богдановская методика операция в идеале требовала участия пожилых и юных партнёров: опытные партийцы передавали бы революционную кровь подрастающему поколению, связывая поколения «кровными узами».
Оперируя тектологическими приёмами, Богданов предложил способ одолеть старость. В этом суть метода «обменное переливание крови»[2]:
Есть все основания полагать, что молодая кровь, с её материалами, взятыми из молодых тканей, способна помочь стареющему организму в его борьбе по тем линиям, по которым он уже терпит поражения, то есть по которым он именно «стареется»; в какой мере помочь, это, конечно, может выяснить только опыт. Оптимальная пара при переливании крови — старик и юноша. С одной стороны, старик вместе с молодой кровью получит «иммунитеты» — способность противостоять разным заражениям». С другой стороны, молодой организм тоже не должен пострадать: молодость будет справляться и с материалом ослабленной, ухудшенной крови, кроме, разве, случаев заражения; притом и в более старой или, вообще, худшей крови должны находиться все же и такие элементы для развития, которых в этой лучшей не было.
Ревизия учения[править | править код]
Ветераны партии при обменном переливании крови выполняли миссию идейно-кровяного донорства и, в свою очередь, «причащались» массам. Большевики тем самым получали шанс на победу в борьбе со старостью. Идея магического вампиризма, преобразилась у Богданова в эзотерическую доктрину, предполагающую укоренение общества будущего в «физиологическом коллективизме», где индивиды соединены цепью «кровавых» взаимообменов.
Богданов умер от очередного (одиннадцатого) обменного переливания крови. На его похоронах Бухарин отметил, что медик «был коллективистом и по чувству, и по разуму одновременно. Даже его идеи о переливании крови покоились на необходимости своеобразного физиологического коллективизма, где отдельные сочеловеки смыкаются в общую физиологическую цепь и повышают тем жизнеспособность всех вместе и каждого в отдельности»[3].
В 1930-х годах идеи Богданова объявлены антиленинскими. Оказалось, что «теория т. н. физиологического коллективизма и теория борьбы со старостью являются методологически ошибочными, чуждыми марксизму установками»[источник не указан 2558 дней].
Тем не менее, с медицинской точки обменное переливание крови оказалось небесполезным[4][неавторитетный источник?]. В современной практике для обменного переливания используют консервированную кровь. Для полноценного замещения крови требуется 10—15 л донорской крови[5]. Обменное переливание крови применяется:
- для лечения гемолитической болезни новорожденных[6],
- при интоксикациях,
- гемотрансфузионном шоке,
- острой почечной недостаточности.
Эффект основан на механическом удалении токсических метаболитов и на возмещении недостающих жизненно важных компонентов внутренней среды организма. Помимо этого производится т. н. деблокирование внутренних органов реципиента.
Синдром массивной гемотрансфузии — причины, симптомы, диагностика и лечение
Синдром массивной гемотрансфузии – это комплекс осложнений, возникающий вследствие переливания большого объема донорской крови. Клинические проявления включают затруднение дыхания, мышечные судороги, замедление сердцебиения, а также повышенную кровоточивость. Диагноз выставляется на основании симптоматики, лабораторных показателей (снижение pH крови и концентрации ионизированного кальция, изменения в коагулограмме), инструментальных данных (электрокардиографии, рентгенографии, КТ). Лечение осуществляется с помощью внутривенного введения глюконата кальция, ингибиторов протеолиза, переливания плазмы, тромбоконцентрата и криопреципитата.
Общие сведения
Синдром массивной гемотрансфузии (СМГ, синдром массивного кровевозмещения) – осложнение, развивающееся при переливании больному в течение 24 часов крови, количество которой превышает 50% ОЦК (2,5-3,5 литров). По сути, синдром обусловлен перегрузкой сердечно-сосудистой системы, реакцией организма реципиента на растворы, использующиеся при консервировании крови, и метаболиты, образующиеся в результате несоблюдения правил техники хранения крови. Также возможны гемолитические реакции. Развитие СМГ не зависит от возраста и половой принадлежности больного. Патология тяжелее протекает у детей и пожилых. Точные статистические данные о частоте синдрома отсутствуют.
Синдром массивной гемотрансфузии
Причины
Основной причиной синдрома массивной гемотрансфузии являются переливания больших объемов крови, потребность в которых возникает при геморрагическом шоке. Подобные лечебные мероприятия показаны при обильных кровотечениях после полученной травмы, при тяжелых гематологических патологиях (гемолитический криз, выраженная тромбоцитопения), требующих постоянной гемотрансфузии, когда для спасения жизни пациента необходимо быстро восполнить ОЦК.
К развитию синдрома предрасполагает множество факторов. К ним относится прием некоторых лекарственных препаратов (антикоагулянтов, калийсберегающих диуретиков, ингибиторов АПФ), глубокий и продолжительный дефицит витамина Д, сопровождающийся гипокальциемией. Усугублению тяжести синдрома способствуют имеющиеся хронические заболевания – сердечная, почечная и печеночная недостаточность, сахарный диабет.
Патогенез
Спектр патологических реакций при данном синдроме широк и многогранен. Переливание большого количества крови в течение короткого времени перегружает сердечно-сосудистую систему (ССС), что ведет к повышению гидростатического давления в сосудах, особенно в сосудах легких, пропотеванию жидкой части крови (плазмы) в просвет альвеол. В донорской крови, которая хранилась слишком долго, эритроциты начинают разрушаться. Из них высвобождается калий.
В результате переливания «старой» крови, особенно в большом объеме, у реципиента развивается гиперкалиемия. Высокий уровень калия ухудшает процессы автоматизма и проводимости в сердечной мышце, что приводит к брадикардии, атриовентрикулярным блокадам и даже остановке сердца. Использующийся при заготовлении донорской крови в качестве антикоагулянта цитрат натрия (соль лимонной кислоты) связывает ионы кальция.
Низкая концентрация кальция в плазме повышает возбудимость скелетных мышц. Развивается судорожный синдром. Гипокальциемия путем изменения мембранного потенциала клеток миокарда удлиняет интервал Q-T, что увеличивает риск пароксизмальной желудочковой тахикардии (ПЖТ). Сильно изменяется кислотно-щелочное равновесие. Из-за образования бикарбонатов из цитрата КЩР сдвигается в сторону метаболического алкалоза. Алкалоз значительно ослабляет тонус сосудов, снижает сердечный выброс, тем самым приводя к артериальной гипотензии, шоку.
Алкалоз также усугубляет гипокальциемию. Значительно страдает и система гемостаза. С одной стороны, алкалоз вызывает агрегацию тромбоцитов, и как следствие, микротромбообразование и нарушение микроциркуляции. С другой стороны, консервированная кровь обеднена факторами свертывания. Возникает коагулопатия разведения и потребления. Гипокальциемия вносит дополнительный вклад в ухудшение способности крови к свертыванию.
Классификация
Существует несколько разновидностей и форм синдрома массивной гемотрансфузии, однако они развиваются не по отдельности, а совместно друг с другом. Зачастую у одного больного могут обнаруживаться все формы синдрома МГ. В клинической практике различают следующие виды патологии:
- Цитратная интоксикация. Содержащийся в консервированной крови цитрат натрия связывается с ионами кальция.
- Калиевая интоксикация. При слишком длительном хранении донорской крови эритроциты постепенно разрушаются, высвобождая большое количество калия.
- ДВС-синдром. Отмечается сочетание микротромбозов с геморрагическим синдромом вследствие сложных метаболических сдвигов при массивных переливаниях.
- Респираторный дистресс-синдром. Определяется повреждение легочной ткани как результат микротромбообразования, перегрузки сосудистого русла легочной артерии.
- Гипотермия. Использование замороженной крови ведет к снижению температуры тела пациента с замедлением всех обменных процессов организма.
Симптомы
Клиническая картина крайне разнообразна. Кожа приобретает бледно-синюшный оттенок. Больной испытывает признаки артериальной гипотонии – головокружение, шум в ушах, предобморочное состояние. Сердцебиение обычно замедленное, нерегулярное, возможны приступы тахикардии с неприятными ощущениями в области сердца. Объемная перегрузка ССС приводит к появлению влажного кашля, затруднению дыхания, особенно в лежачем положении, ощущению тяжести в правом подреберье и отекам на ногах. Характерны запоры вследствие атонии кишечника.
Наблюдается кровоточивость мест инъекций и установки катетеров, носовые, десневые кровотечения. Кожа покрывается геморрагическими элементами. Из-за гипокальциемии мышцы по всему телу начинают непроизвольно болезненно сокращаться. Наиболее сильно спазму подвержены икроножные, жевательные мышцы, мышцы сгибателей кисти. Для тяжелой гипокальциемии типичны такие симптомы как «руки акушера», «сардоническая улыбка».
Может возникнуть спазм коронарных артерий, вызывающий ишемию миокарда, о чем свидетельствует сжимающая или жгучая боль за грудиной. Дети более чувствительны к низкому содержанию кальция в крови, у них нередко встречается опистотонус – спина резко выгнута, голова запрокинута назад, ноги вытянуты, руки согнуты в локтях и запястьях. Иногда у больных с синдромом массивной гемотрансфузии развивается припадок как при эпилепсии.
Осложнения
Для СМГ типично большое количество неблагоприятных последствий. Наиболее частыми тяжелыми осложнениями считаются отек легких, массивные внутренние кровотечения (желудочно-кишечные, внутричерепные). Глубокие электролитные сдвиги становятся причиной жизнеугрожающих нарушений ритма сердца. Гипокальциемия нередко приводит к желудочковой тахикардии, переходящей в фибрилляцию желудочков, а гиперкалиемия – к полной атриовентрикулярной блокаде, асистолии (остановке сердца).
При гипокальциемии может наступить смерть от асфиксии вследствие ларингоспазма, перекрывающего просвет верхних дыхательных путей. Выраженный алкалоз вызывает резкое падение артериального давления (коллапс). Переливания крови от разных доноров неизбежно повышают вероятность несовместимости по различным антигенам, при которой возникает гемолиз, гемотрансфузионный шок, острая почечная недостаточность.
Диагностика
Ведение пациентов с СМГ осуществляют анестезиологи-реаниматологи, врачи-трансфузиологи. Обычно постановка диагноза не вызывает затруднений, однако необходимы дополнительные лабораторные и инструментальные обследования для подтверждения метаболических нарушений, а также с целью дифференциальной диагностики. Назначаются следующие диагностические методики:
- Анализы крови. В общем анализе крови обнаруживается низкий уровень эритроцитов, гемоглобина, тромбоцитов. В биохимическом анализе крови выявляется высокая концентрация калия, уменьшение содержания ионизированного кальция, в коагулограмме – признаки гипокоагуляции (удлинение протромбинового времени, гипофибриногенемия). Исследование КЩС показывает высокий pH.
- Инструментальные исследования. На электрокардиограмме отмечается брадикардия, удлиненный интервал QT, иногда ПЖТ, АВ-блокады. На рентгенограммах ОГК визуализируется усиление сосудистого рисунка, диффузные двусторонние затемнения по типу матового стекла. При подозрении на внутреннее кровотечение проводится ФЭГДС, КТ головного мозга, органов брюшной полости.
Дифференциальный диагноз СМГ осуществляется с геморрагическими диатезами (иммунной тромбоцитопенией, тромботической тромбоцитопенической пурпурой). Развитие отека легких при гемотрансфузии требует исключения TRALI-синдрома (острого посттрансфузионного повреждения легких иммунной природы). При возникновении выраженной гипокальциемии необходима дифференциальная диагностика со столбняком, эпилепсией.
Лечение синдрома массивной гемотрансфузии
Поскольку переливания крови обычно осуществляются в отделении реанимации и интенсивной терапии, лечение СМГ проходит там же. Терапия синдрома многокомпонентная, проводится в основном с помощью консервативных методов. Все нарушения достаточно легко поддаются коррекции. Первым и обязательным звеном патогенетической терапии является прекращение переливания цельной крови. Это позволяет предотвратить дальнейшее ухудшение состояния больного. Далее в зависимости от конкретной формы СМГ применяются следующие способы воздействия:
- Борьба с артериальной гипотензией и шоком. Чтобы поднять давление до нормальных цифр, назначают коллоидные плазмозамещающие растворы (сывороточный альбумин) и кристаллоидные растворы без содержания калия (физиологический раствор NaCl, «дисоль»). Для усиления сократительной способности миокарда и повышения тонуса сосудов эффективны допамин, норадреналин.
- Коррекция алкалоза и электролитных нарушений. Гиперкалиемию и гипокальциемию можно купировать внутривенным введением глюконата или хлорида кальция. Для снижения концентрации калия путем перемещения его в клетки вводят глюкозу с инсулином. При крайне высокой гиперкалиемии необходим срочный гемодиализ. Чтобы сместить pH к физиологическим значениям, используют ацетазоламид.
- Нормализация системы гемостаза. Для восстановления свертывающей функции крови применяют компоненты крови гемостатического действия, а именно тромботический концентрат, а также плазму и криопреципитат, содержащие факторы свертывания. С целью подавления фибринолитической активности крови назначают ингибиторы протеолитических ферментов (апротинин). Для улучшения микроциркуляции используют пентоксифиллин.
Профилактика и прогноз
СМГ является тяжелой патологией с большим числом опасных осложнений, однако при своевременной диагностике и адекватном лечении можно добиться быстрой нормализации состояния больного. Наиболее частыми причинами летального исхода являются отек легких, обильные кровотечения при ДВС-синдроме. Для первичной профилактики СМГ рекомендуется низкая скорость гемотрансфузии. С целью предупреждения гипотермии донорскую кровь необходимо полностью размораживать и подогревать до 36-37° С. Непосредственно перед гемотрансфузией обязательно нужно определять концентрацию калия и кальция.
Современные правила переливания крови
На основании правила Оттенберга и анализа системы резус-фактора возникло понятие «универсальный донор». К таким донорам относят людей, имеющих группу крови 0(I) Rh—. Такую кровь в небольшом количестве относительно безопасно можно перелить реципиенту с любой группой крови.
Современные достижения иммуногематологии и клиническая практика показали, что при переливании крови универсального донора реципиентам других групп возможен гемолиз эритроцитов реципиента не только за счёт естественных антител (при массивной гемотрансфузии), но и изоиммунными антителами анти-A (реже анти-B) донорской крови. Эти антитела образуются у универсальных доноров при иммунизации антигенами A и B во время беременности, вакцинации и т.д. Чаще всего при этом появляются изоиммунные антитела анти-A (их частота у универсальных доноров достигает 10-16%).
Переливание резус-отрицательной крови резус-положительному реципиенту может привести к образованию антител на слабые антигены системы резус (С и E).
В связи с этим в настоящее время необходимо переливать только одногруппную (по системе АВ0) и однорезусную кровь!
Только в исключительных случаях — при жизненных показаниях к гемотрансфузии и невозможности определить группу крови больного или при отсутствии одногруппной донорской крови — допустимо использование крови универсального донора (отмытые эритроциты 0(I) группы) в количестве до 500 мл. Детям переливание любой крови, кроме одногруппной, запрещено!
Переливание крови и её компонентов
Современная трансфузионная терапия, согласно определению выдающегося советского трансфузиолога и хирурга A.H. Филатова (1973), — раздельное или сочетанное применение крови, её компонентов и препаратов, а также кровезамещающих растворов.
Прежде чем приступить к переливанию крови и её компонентов, каждый врач должен помнить, что гемотрансфузию нельзя считать индифферентным вмешательством, иногда она представляет серьёзную опасность для состояния здоровья и даже жизни больного. Кровь — одна из тканей организма, поэтому переливание крови от одного индивидуума другому можно рассматривать как операцию трансплантации ткани.
Показания к гемотрансфузии
Для определения показаний к гемотрансфузии необходимо знать механизм влияния на организм пациента перелитой крови.
Механизм действия перелитой крови
Биологические эффекты гемотрансфузии обусловлены сложнейшими регуляторными механизмами. Перелитая кровь действует на элементы нервной рецепции, а также ферментные и гормональные системы обмена, изменяя его на всех уровнях: от молекулярного до органно-тканевого.
Перелитая кровь оказывает на организм реципиента следующие эффекты:
• заместительный;
• гемодинамический;
• иммунологический;
• гемостатический;
• стимулирующий.
Заместительный эффект
Заместительное действие заключается в возмещении утраченной организмом части крови. Введённые в организм эритроциты восстанавливают объём крови и её газотранспортную функцию. Лейкоциты повышают иммунные способности организма. Тромбоциты корригируют систему свёртывания крови.
Плазма и альбумин обладают гемодинамическим действием. Иммуноглобулины плазмы создают пассивный иммунитет. Факторы свёртывания крови и фибринолиза регулируют агрегатное состояние крови. Вводимые вместе с кровью питательные вещества (жиры, белки и углеводы) включаются в цепь биохимических реакций.
Эритроциты перелитой крови функционируют в сосудистом русле реципиента до 30 сут и более. Клетки белой крови покидают сосудистое русло вскоре после переливания, белки плазмы донорской крови циркулируют в сосудистом русле реципиента 18-36 дней.
Гемодинамический эффект
Переливание крови оказывает всестороннее воздействие на сердечно-сосудистую систему. У больных с острой кровопотерей и травматическим шоком оно приводит к стойкому увеличению ОЦК, увеличению венозного притока к правым отделам сердца, усилению работы сердца и повышению минутного объёма крови.
Улучшается микроциркуляция: расширяются артериолы и венулы, раскрывается сеть капилляров, в них ускоряется движение крови, сокращаются артериовенозные шунты, в результате чего редуцируется утечка крови из артериальной системы в венозную. Через 24- 48 ч после переливания крови у реципиента начинается усиленный приток тканевой лимфы в кровеносное русло, что также увеличивает ОЦК. Поэтому иногда после трансфузии прирост ОЦК превосходит объём перелитой крови.
Иммунологический эффект
Гемотрансфузия усиливает иммунологические свойства организма реципиента. За счёт введения гранулоцитов, макрофагов, лимфоцитов, компонентов комплемента, иммуноглобулинов, цитокинов, различные антибактериальных и антитоксических антител возрастает фагоцитарная активность лейкоцитов, активируется образование антител.
Особенно высоким иммунобиологическим действием обладают гипериммунные препараты плазмы, полученные от иммунизированных доноров, — антистафилококковая, антисинегнойная и противоожоговая плазма, иммуноглобулины направленного действия (антистафилококковый, противококлюшный, противостолбнячный иммуноглобулины и др.).
Гемостатический эффект
Переливание крови оказывает стимулирующее действие на систему гемостаза реципиента, вызывая умеренную гиперкоагуляцию, обусловленную увеличением тромбопластической и снижением антикоагулянтной активности крови. Переливание небольших доз (обычно 250 мл) тёплой крови или крови с малым сроком хранения (до 3 сут) оказывает гемостатическое действие благодаря активности вводимых с ней тромбоцитов и прокоагулянтов — факторов свёртывающей системы.
Особым гемостатическим действием обладают специальные виды плазмы (например, антигемофильная) и гемостатические препараты (фибриноген, криопреципитат, протромбиновый комплекс, тромбоцитарная масса и плазма, обогащённая тромбоцитами).
B то же время переливание массивных доз донорской крови в отдельных случаях может нарушить гемостатический баланс вплоть до развития синдрома диссеминированного внутрисосудистого свёртывания крови (ДBС-синдрома).
Стимулирующий эффект
После переливания крови в организме развиваются изменения, аналогичные стрессу. Происходит стимуляция гипоталамо-гипофизарно-адреналовой системы, что подтверждается увеличением содержания кортикостероидов в крови и моче реципиентов в посттрансфузионном периоде.
У реципиентов повышается основной обмен, увеличивается дыхательный коэффициент, усиливается газообмен.
Переливание крови оказывает стимулирующее действие на факторы естественного иммунитета: повышаются фагоцитарная активность гранулоцитов и образование антител в ответ на действие тех или иных антигенов.
«Переливание крови и ее компонентов»
Трансфузиология– наука о рациональном применении компонентов и препаратов крови с учетом особенностей течения заболевания и свойств используемой среды.
Трансфузия– лечебный метод, заключающийся во введении в кровеносное русло больного компонентов крови, заготовленных от донора или самого реципиента (аутодонорство).
Донор– человек, от которого переливают компоненты крови.
Реципиент– человек, которому переливают компоненты крови.
Иммунологические основы трансфузиологии
Обязательным требованием к гемотрансфузионной терапии является ее безопасность, прежде всего иммунологическая . Трансфузия компонентов крови является, по сути, пересадкой ткани, и возможна только после оценки совместимости крови донора и реципиента.
Классификация групп крови основана на наличии или отсутствии в плазменных и клеточных элементах крови групповых антигенов и антител. В настоящее время известно более 200 групповых антигенов крови, которые объединены в несколько групповых антигенных систем. Групповые антигены передаются по наследству, не меняются в течение жизни, их набор индивидуален у каждого человека.
Различают групповые антигенные системы эритроцитов, лейкоцитов, тромбоцитов и плазменных белков.
Групповые системы эритроцитов
Известно более 20 антигенных систем эритроцитов, из них для клинической практики наибольшее значение имеют системы АВО и резус. Совместимость по этим двум системам в обязательном порядке учитывается при каждой трансфузии.
Система АВО
Это первая эритроцитарная система антигенов, открыта в 1900г. венским ученым Карлом Ландштейнером. Он обнаружил и изучил три антигена. В 1907г. Ян Янский пришел к заключению о существовании четырех групп крови. С этого времени и по сей день определение групп крови по данной системе основывается на наличии в эритроцитах группоспецифических антигенов (О,А,В), а в сыворотке – антител анти-А(α) и анти-В (β).
Группоспецифические антигены (О,А,В) генетически обусловлены.
Антитела против антигенов системы АВО – изогемагглютинины, относящиеся к классу IgM. Способность к их выработке передается по наследству.
Различают четыре группы крови. Они имеют буквенно-цифровое обозначение:
— 43% в европейской популяции.
— 42% в европейской популяции.
— 11% в европейской популяции.
— 4% в европейской популяции.
Причина иммунологического конфликта в системе АВО – встреча одноименных агглютининов и агглютининогенов: А-α или В-β.
Групповая система резус
После антигенов АВО система антигенов резус имеет наибольшее значение в клинической практике. Присутствие антигена обозначается знаком «+», а его отсутствие – знаком «-». Резус-принадлежность эритроцитов определяется по наличию в фенотипе антигена Rh. Людей, в эритроцитах которых этот антиген присутствует, относят к резус-положительным, при его отсутствии – к резус-отрицательным. Частота резус-положительных лиц у европейцев – 85%.
Антитела против антигенов резус, в отличие от групповых антител, — иммунные, появляющиеся в результате изосенсибилизации. Их специфичность обусловливается антигенами. При переливании резус-положительных эритроцитов лицам с противорезусными антителами возникают посттрансфузионные реакции гемолитического типа. Это возникает в следующих случаях:
— при повторном переливании резус-положительной крови резус-отрицательному реципиенту. При первом переливании крови в организме человека образуются антирезусные антитела. При повторном переливании резус-положительной крови выработанные ранее антитела вызывают гемагглютинацию эритроцитов.
— во время беременности, если мать имеет резус-отрицательную кровь, а плод – резус-положительную. Агглютиногены резус-системы проникают через плацентарный барьер, где вырабатываются антирезусные антитела. Они проникают в организм плода, где и вызывают реакцию гемагглютинации. У плода развивается тяжелая гемолитическая анемия. Антирезусные антитела сохраняются всю жизнь, каждая следующая беременность более опасна.
