Анализы на Антитела к цитомегаловирусу (Cytomegalovirus), IgG, цены в лаборатории KDL
Антитела к цитомегаловирусу IgG вырабатываются при цитомегаловирусной инфекции и сохраняются длительное время, часто пожизненно, являясь маркерами перенесенной инфекции.
Цитомегаловирус (ЦМВ) – представитель семейства вирусов герпеса. Широко распространенная инфекция, 70-90% населения являются носителями ЦМВ и поэтому в их крови будут выявляться IgG даже при отсутствии клиники. При здоровом иммунитете цитомегаловирусная инфекция протекает без симптомов и человек не подозревает, что он инфицирован. Передаётся ЦМВ воздушно-капельным, половым путём, от матери к ребёнку в период беременности, возможна передача вируса при пересадке органов и тканей. Попав в организм, ЦМВ сохраняется пожизненно. При снижении иммунитета вирус может активизироваться.
Наибольшую опасность цитомегаловирусная инфекция представляет при выраженном иммунодефиците у пациента, также опасно первичное заражение женщины в период беременности.
В каких случаях обычно назначают исследование на определение уровня антител к цитомегаловирусу IgG?
- На этапе планирования беременности (цель — определить наличие или отсутствие защитных антител)
- Во время беременности
- При симптомах инфекционного мононуклеоза (ангина, увеличение периферических лимфоузлов) – одновременно исключается вирус Эпштейна-Барр
- При атипичном течении пневмонии, ОРЗ
- При увеличении печени и селезёнки (гепатоспленомегалия) или других признаки поражения печени, если исключены вирусные гепатиты
Что означают результаты теста?
Референсные значения:
- <6,0 — антитела не обнаружены
- >=6,0 — антитела обнаружены,
- 6,0 AE/ml — 15,0AE/ml — сомнительный результат.

Результат – <6,0 — антитела не обнаружены
- Отсутствие антител может свидетельствовать о том, что организм пациента не встречался ранее с ЦМВ- инфекцией
- Возможно в ранний период инфекции, когда ещё не успели выработаться IgG. При клинических подозрениях в этом случае рекомендовано определение IgM к цитомегаловирусу или выявление ДНК ЦМВ методом ПЦР.
Результат – >=6,0 — антитела обнаружены
- Обнаружены антитела к цитомегаловирусу. На основании только определения IgG невозможно достоверно определить давность инфицирования.
Результат 6,0 AE/ml — 15,0AE/ml — сомнительный результат.
- Рекомендуется исследование IgM-антител к ЦМВ и повторное исследование IgG-антител в динамике (например, через 2 недели). В случае текущей инфекции уровень антител через две недели вырастет.
Сроки выполнения теста.
1-2 дня.
Как подготовиться к анализу?
Кровь берётся утром натощак или в течение дня через 3 часа после необильного приёма пищи.
Сдать анализ на антитела IgG к цитомегаловирусу, ЦМВ
Метод определения Иммуноферментный анализ (ИФА).
Исследуемый материал Сыворотка крови
Доступен выезд на дом
Онлайн-регистрация Синонимы: Антитела класса G к цитомегаловирусу; АТ-ЦМВ-IgG.Anti-CMV-IgG; CMV Antibody, IgG.
Краткая характеристика определяемого аналита Антитела класса G к цитомегаловирусу (Anti-CMV-IgG)
В ответ на внедрение в организм цитомегаловируса (ЦМВ) развивается иммунная перестройка организма. Инкубационный период колеблется от 15 дней до 3 месяцев. При данной инфекции имеет место нестерильный иммунитет (то есть не наблюдается полной элиминации вируса). Иммунитет при цитомегаловирусной инфекции (ЦМВИ) нестойкий, медленный. Возможна реинфекция экзогенным вирусом или реактивация латентной инфекции. Вследствие длительного персистирования в организме вирус действует на все звенья иммунной системы больного. Защитная реакция организма проявляется, прежде всего, в виде образования специфических антител классов IgM и IgG к ЦМВ. Антитела класса IgG к цитомегаловирусу (CMV, ЦМВ) указывают на текущую или имевшую место в прошлом цитомегаловирусную инфекцию. Особенности инфекции. Цитомегаловирусная (ЦМВ) инфекция – это широко распространённое вирусное поражение организма, которое относится к так называемым оппортунистическим инфекциям, протекающим обычно латентно. Клинические проявления наблюдаются на фоне физиологических иммунодефицитных состояний (дети первых 3-5 лет жизни, беременные – чаще во 2 и 3 триместрах), а также у лиц с врождёнными или приобретёнными иммунодефицитами (ВИЧ-инфекция, применение иммунодепрессантов, онкогематологические заболевания, облучение, диабет и т.
При данной инфекции имеет место нестерильный иммунитет (то есть не наблюдается полной элиминации вируса). Иммунитет при цитомегаловирусной инфекции (ЦМВИ) нестойкий, медленный. Возможна реинфекция экзогенным вирусом или реактивация латентной инфекции. Вследствие длительного персистирования в организме вирус действует на все звенья иммунной системы больного. Защитная реакция организма проявляется, прежде всего, в виде образования специфических антител классов IgM и IgG к ЦМВ. Антитела класса IgG к цитомегаловирусу (CMV, ЦМВ) указывают на текущую или имевшую место в прошлом цитомегаловирусную инфекцию. Особенности инфекции. Цитомегаловирусная (ЦМВ) инфекция – это широко распространённое вирусное поражение организма, которое относится к так называемым оппортунистическим инфекциям, протекающим обычно латентно. Клинические проявления наблюдаются на фоне физиологических иммунодефицитных состояний (дети первых 3-5 лет жизни, беременные – чаще во 2 и 3 триместрах), а также у лиц с врождёнными или приобретёнными иммунодефицитами (ВИЧ-инфекция, применение иммунодепрессантов, онкогематологические заболевания, облучение, диабет и т.
Цитомегаловирус – вирус семейства герпес-вирусов. Так же, как и другие представители семейства, после инфицирования сохраняется в организме практически пожизненно. Устойчив во влажной среде. Группу риска составляют дети 5-6 лет, взрослые 16-30 лет, а также лица, практикующие анальный секс. Дети восприимчивы к передаче инфекции воздушно-капельным путём от родителей и других детей с латентными формами инфекции. Для взрослых более характерен половой путь передачи. Вирус содержится в сперме и других биологических жидкостях. Вертикальная передача инфекции (от матери к плоду) происходит трансплацентарно и в процессе родов. ЦМВ-инфекция характеризуется разнообразием клинических проявлений, но при полноценном иммунитете протекает клинически бессимптомно. В редких случаях развивается картина инфекционного мононуклеоза (около 10% всех случаев инфекционного мононуклеоза), клинически не отличимого от мононуклеоза, вызванного вирусом Эпштейн-Барра.
Репликация вируса происходит в тканях ретикуло-эндотелиальной системы, эпителии урогенитального тракта, печени, слизистой дыхательных путей и пищеварительного тракта. При снижении иммунитета после трансплантации органов, терапии иммуносупрессорами, ВИЧ-инфекции, а также у новорожденных, ЦМВ представляет серьезную угрозу, так как заболевание может затрагивать любой орган. Возможно развитие гепатита, пневмонии, эзофагита, гастрита, колита, ретинита, диффузной энцефалопатии, лихорадки, лейкопении. Заболевание может заканчиваться летально.
При снижении иммунитета после трансплантации органов, терапии иммуносупрессорами, ВИЧ-инфекции, а также у новорожденных, ЦМВ представляет серьезную угрозу, так как заболевание может затрагивать любой орган. Возможно развитие гепатита, пневмонии, эзофагита, гастрита, колита, ретинита, диффузной энцефалопатии, лихорадки, лейкопении. Заболевание может заканчиваться летально.
Цитомегаловирусная инфекция у беременных, обследование при беременности
При первичном инфицировании беременной цитомегаловирусом (в 35-50% случаев) или реактивации инфекции в период беременности (в 8-10% случаев) развивается внутриутробная инфекция. При развитии внутриутробной инфекции на сроке до 10 недель есть риск возникновения пороков развития, возможно самопроизвольное прерывание беременности. При инфицировании на 11-28 неделе возникают задержка внутриутробного развития, гипо- или дисплазии внутренних органов. Если инфицирование происходит на более позднем сроке, поражение может быть генерализованным, захватывать определённый орган (например, фетальный гепатит) или проявляться после рождения (гипертензионно-гидроцефальный синдром, нарушения слуха, интерстициальный пневмонит и т.
Особое значение лабораторная диагностика цитомегаловирусной инфекции имеет у следующих категорий обследуемых:
| Категория | Причины |
| Женщины, при подготовке к беременности | 1. Латентное течение заболевания Латентное течение заболевания
2. Сложность дифференциальной диагностики первичного инфицирования и рецидива инфекции при обследовании во время беременности 3. Тяжёлые последствия внутриутробной инфекции у новорожденных |
| Беременные женщины | Тяжёлые последствия внутриутробной инфекции у новорожденных |
| Иммунодефицитные состояния | Генерализованные формы |
Последовательное многократное определение уровня IgG-антител у новорожденных позволяет отличить врождённое заражение (постоянный уровень) от неонатального (нарастание титров). Если титр IgG антител при повторном (через две недели) анализе не увеличивается, то причин для тревоги нет, если титр IgG растёт, следует рассмотреть вопрос об аборте.
С какой целью определяют Антитела класса G к цитомегаловирусу (Anti-CMV-IgG)
Антитела класса IgG к цитомегаловирусу – специфические иммуноглобулины, вырабатываемые в организме человека в период выраженных клинических проявлений цитомегаловирусной инфекции и являющиеся серологическим маркером этого заболевания, а также перенесенной в прошлом цитомегаловирусной инфекции.
Важно! CMV-инфекция входит в группу TORCH-инфекций (название образовано начальными буквами в латинских наименованиях – Toxoplasma, Rubella, Cytomegalovirus, Herpes), считающихся потенциально опасными для развития ребёнка.
В идеальном случае проконсультироваться с врачом и пройти лабораторное обследование на TORCH-инфекции женщине нужно за 2-3 месяца до планируемой беременности, поскольку в этом случае будет возможность предпринять соответствующие лечебные или профилактические меры, а также при необходимости в будущем сравнить полученные результаты исследований до беременности с результатами обследований во время беременности.
Антитела к ЦМВ IgG (Anti-CMV IgG)
Антитела к ЦМВ IgG (Anti-CMV IgG)
Anti-CMV IgG (Анти-ЦМВ IgG) — Антитела класса IgG к цитомегаловирусу – специфические иммуноглобулины, вырабатывающиеся в организме человека в период выраженных клинических проявлений цитомегаловирусной инфекции и являющиеся серологическим маркером этого заболевания, а также перенесенной в прошлом цитомегаловирусной инфекции. Цитомегаловирус (ЦМВ) относится к семейству вирусов герпеса. Так же, как и другие представители этой группы, он может сохраняться у человека всю жизнь. У здоровых людей с нормальным иммунитетом первичная инфекция протекает без осложнений (и часто бессимптомно). Однако цитомегаловирус опасен при беременности (для ребёнка) и при иммунодефиците. Цитомегаловирусом можно заразиться через различные биологические жидкости: слюну, мочу, сперму, кровь. Кроме того, он передаётся от матери к ребёнку (во время беременности, родов или при кормлении).Если у женщины еще не было ЦМВ, значит, она входит в группу риска и ей следует уделять особое внимание профилактике ЦМВ. Для ребёнка опасна именно инфекция, которой мать заразилась первый раз во время беременности.
Цитомегаловирус (ЦМВ) относится к семейству вирусов герпеса. Так же, как и другие представители этой группы, он может сохраняться у человека всю жизнь. У здоровых людей с нормальным иммунитетом первичная инфекция протекает без осложнений (и часто бессимптомно). Однако цитомегаловирус опасен при беременности (для ребёнка) и при иммунодефиците. Цитомегаловирусом можно заразиться через различные биологические жидкости: слюну, мочу, сперму, кровь. Кроме того, он передаётся от матери к ребёнку (во время беременности, родов или при кормлении).Если у женщины еще не было ЦМВ, значит, она входит в группу риска и ей следует уделять особое внимание профилактике ЦМВ. Для ребёнка опасна именно инфекция, которой мать заразилась первый раз во время беременности.
При первичной инфекции у беременной женщины вирус часто попадает и в организм ребенка. Это еще не означает, что он заболеет. Как правило, заражение ЦМВ протекает бессимптомно. Однако примерно в 10 % случаев оно приводит к врождённым патологиям: микроцефалии, церебральной кальцификации, сыпи и увеличению селезёнки и печени. Это часто сопровождается снижением интеллекта и глухотой, возможен даже летальный исход. Кроме того, цитомегаловирус представляет опасность при ослаблении иммунной системы (например, из-за иммунодепрессантов или ВИЧ). При СПИДе ЦМВ протекает в тяжёлой форме и является частой причиной смерти больных. Выработка антител – это один из способов борьбы с вирусной инфекцией. Существует несколько классов антител (IgG, IgM, IgA и др.). Антитела класса G (IgG) присутствуют в крови в наибольшем количестве (по сравнению с другими типами иммуноглобули-нов). При первичной инфекции их уровень возрастает в первые недели после заражения и затем может оставаться высоким годами.
Это часто сопровождается снижением интеллекта и глухотой, возможен даже летальный исход. Кроме того, цитомегаловирус представляет опасность при ослаблении иммунной системы (например, из-за иммунодепрессантов или ВИЧ). При СПИДе ЦМВ протекает в тяжёлой форме и является частой причиной смерти больных. Выработка антител – это один из способов борьбы с вирусной инфекцией. Существует несколько классов антител (IgG, IgM, IgA и др.). Антитела класса G (IgG) присутствуют в крови в наибольшем количестве (по сравнению с другими типами иммуноглобули-нов). При первичной инфекции их уровень возрастает в первые недели после заражения и затем может оставаться высоким годами.
Подготовка к исследованию
Не курить в течение 30 минут до сдачи крови.
Показания к исследованию
Во время беременности (или при её планировании) – для оценки риска осложнений (проверочное исследование), при симптомах цитомегаловирусной инфекции, при нарушениях у плода по результатам УЗИ.
При симптомах цитомегаловирусной инфекции у людей с ослабленным иммунитетом.
При симптомах мононуклеоза (если тесты не выявили вирус Эпштейна – Барр).
Интерпретация
Референсные значения — отрицательно
Отрицательный результат при беременности
Женщина раньше не была инфицирована ЦМВ – есть риск приобрести первичную ЦМВ-инфекцию. Однако если с момента заражения прошло не больше 2-3 недель, то IgG могли еще не появиться. Чтобы исключить этот вариант, нужно сдать анализ повторно через 2 недели.
Положительный результат до беременности
Женщина уже была инфицирована ЦМВ в прошлом – риск осложнений минимален.
Положительный результат во время беременности
Нельзя сделать однозначный вывод. Возможно, ЦМВ попал в организм до беременности. Но не исключено, что женщина заразилась недавно, в начале беременности (за несколько недель до теста). Такой вариант представляет опасность для ребенка. Для точного диагноза нужны результаты других анализов.
Такой вариант представляет опасность для ребенка. Для точного диагноза нужны результаты других анализов.
При попытке установить возбудителя неизвестного заболевания единичный тест на IgG даёт мало информации. Нужно учитывать результаты всех анализов.
На результаты могут влиять
Иногда нужно узнать, заражён ли цитомегаловирусом сам новорождённый ребенок. Однако анализ на IgG в данном случае неинформативен. IgG могут проникать через плацентарный барьер, поэтому, если антитела есть у матери, то они же будут присутствовать и у ребенка.
Назначается в комплексе с
Cytomegalovirus, IgM
Cytomegalovirus, ДНК, ПЦР ( в плазме, мононуклеарах) качественный
Cytomegalovirus, ДНК, ПЦР ( в плазме, мононуклеарах) количественный
Авидность к ЦМВ
диагностика IgG к цитомегаловирусу (Антитела класса IgG к цитомегаловирусу (ЦМВ))
Антитела класса IgG к цитомегаловирусу — специфические иммуноглобулины, вырабатывающиеся в организме человека в период выраженных клинических проявлений цитомегаловирусной инфекции и являющиеся серологическим маркером этого заболевания, а также перенесенной в прошлом цитомегаловирусной инфекции.
Метод исследования
Иммуноферментный анализ.
Единицы измерения
МЕ/мл (международная единица на миллилитр).
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
- Не принимать пищу в течение 8-10 часов перед исследованием, можно пить чистую негазированную воду.
- Исключить физическое и эмоциональное перенапряжение за 24 часа до сдачи крови.
- Не курить в течение 3 часов до исследования.
Общая информация об исследовании
Цитомегаловирус (ЦМВ) относится к семейству вирусов герпеса. Так же, как и другие представители этой группы, он может сохраняться у человека всю жизнь. У здоровых людей с нормальным иммунитетом первичная инфекция протекает без осложнений (и часто бессимптомно). Однако цитомегаловирус опасен при беременности (для ребенка) и при иммунодефиците.
Цитомегаловирусом можно заразиться через различные биологические жидкости: слюну, мочу, сперму, кровь. Кроме того, он передается от матери к ребенку (во время беременности, родов или при кормлении).
Кроме того, он передается от матери к ребенку (во время беременности, родов или при кормлении).
Как правило, цитомегаловирусная инфекция протекает бессимптомно. Иногда заболевание напоминает инфекционный мононуклеоз: повышается температура, болит горло, увеличиваются лимфатические узлы. В дальнейшем вирус сохраняется внутри клеток в неактивном состоянии, но если организм окажется ослаблен, то он снова начнет размножаться.
Для женщины важно знать, была ли она заражена ЦМВ в прошлом, потому что именно это определяет, есть ли риск осложнений при беременности. Если раньше она уже была инфицирована, то риск минимален. Во время беременности может обостриться старая инфекция, однако такая форма обычно не вызывает тяжелых последствий.
Если у женщины еще не было ЦМВ, значит, она входит в группу риска и ей следует уделять особое внимание профилактике ЦМВ. Для ребенка опасна именно инфекция, которой мать заразилась первый раз во время беременности.
При первичной инфекции у беременной женщины вирус часто попадает и в организм ребенка. Это еще не означает, что он заболеет. Как правило, заражение ЦМВ протекает бессимптомно. Однако примерно в 10 % случаев оно приводит к врожденным патологиям: микроцефалии, церебральной кальцификации, сыпи и увеличению селезенки и печени. Это часто сопровождается снижением интеллекта и глухотой, возможен даже летальный исход.
Это еще не означает, что он заболеет. Как правило, заражение ЦМВ протекает бессимптомно. Однако примерно в 10 % случаев оно приводит к врожденным патологиям: микроцефалии, церебральной кальцификации, сыпи и увеличению селезенки и печени. Это часто сопровождается снижением интеллекта и глухотой, возможен даже летальный исход.
Выработка антител — это один из способов борьбы с вирусной инфекцией. Существует несколько классов антител (IgG, IgM, IgA и др.).
Антитела класса G (IgG) присутствуют в крови в наибольшем количестве (по сравнению с другими типами иммуноглобулинов). При первичной инфекции их уровень возрастает в первые недели после заражения и затем может оставаться высоким годами.
Кроме количества, часто определяется еще и авидность IgG — прочность, с которой антитело связывается с антигеном. Чем выше авидность, тем прочнее и быстрее антитела связывают вирусные белки. Когда человек впервые заражается ЦМВ, его антитела IgG обладают низкой авидностью, потом (через три месяца) она становится высокой. По авидности IgG судят о том, как давно произошло первоначальное заражение ЦМВ.
По авидности IgG судят о том, как давно произошло первоначальное заражение ЦМВ.
Для чего используется исследование?
- Чтобы установить, был ли человек в прошлом инфицирован ЦМВ.
- Для диагностики цитомегаловирусной инфекции.
- Чтобы установить возбудителя заболевания, которое похоже на цитомегаловирусную инфекцию.
Что означают результаты?
Референсные значения: 0 — 0,5 Ед/мл.
Отрицательный результат при беременности
- Женщина раньше не была инфицирована ЦМВ — есть риск приобрести первичную ЦМВ-инфекцию. Однако если с момента заражения прошло не больше 2-3 недель, то IgG могли еще не появиться. Чтобы исключить этот вариант, нужно сдать анализ повторно через 2 недели.
Положительный результат до беременности
- Женщина уже была инфицирована ЦМВ в прошлом – риск осложнений минимален.
Положительный результат во время беременности
- Нельзя сделать однозначный вывод.
 Возможно, ЦМВ попал в организм до беременности. Но не исключено, что женщина заразилась недавно, в начале беременности (за несколько недель до теста). Такой вариант представляет опасность для ребенка.
Возможно, ЦМВ попал в организм до беременности. Но не исключено, что женщина заразилась недавно, в начале беременности (за несколько недель до теста). Такой вариант представляет опасность для ребенка.
Вопрос: Евгений | 08 Июня, 2021
Как максимально ыстро делается тест пцр
Здравствуйте. При сдаче анализа до 15-00 часов срочное выполнение анализа возможно в течение 6 часов.
Вопрос: Анна | 07 Июня, 2021
Здравствуйте. Принимаете анализ на сахар из пальчика? (Капиллярная кровь)
Здравствуйте. При заборе крови из пальца проводим экспресс-метод определения уровня сахара. Более точные результаты дает венозный забор биоматериала.
Услуги центра ЭКО семейной клиники «Жемчужина» Челябинск
Цитомегаловирус IgM и IgG
Определение антител класса IgM и IgG к цитомегаловирусу в Челябинске – специфические иммуноглобулины, вырабатывающиеся в организме человека в остром периоде цитомегаловирусной инфекции и являющиеся ранним серологическим маркером этого заболевания.
Синонимы русские
Антитела класса IgM к цитомегаловирусу (ЦМВ).
Синонимы английские
Anti-CMV-IgM, CMV Antibody, IgM.
Метод исследования
Твердофазный хемилюминесцентный иммуноферментный анализ («сэндвич»-метод), ИФА исследование.
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
Не курить в течение 30 минут до сдачи крови.
Общая информация об исследовании
Цитомегаловирус (ЦМВ) относится к семейству вирусов герпеса. Так же, как и другие представители этой группы, он может сохраняться у человека всю жизнь. У здоровых людей с нормальным иммунитетом первичная инфекция протекает без осложнений (и часто бессимптомно). Однако цитомегаловирус опасен при беременности (для ребенка) и при иммунодефиците.
Цитомегаловирусом можно заразиться через различные биологические жидкости: слюну, мочу, сперму, кровь. Кроме того, он передается от матери к ребенку (во время беременности, родов или при кормлении).
Как правило, цитомегаловирусная инфекция протекает бессимптомно. Иногда заболевание напоминает инфекционный мононуклеоз: повышается температура, болит горло, увеличиваются лимфатические узлы. В дальнейшем вирус сохраняется внутри клеток в неактивном состоянии. Но если организм окажется ослаблен, то вирус снова начнет размножаться.
Для женщины важно знать, была ли она заражена ЦМВ в прошлом, потому что именно это определяет, есть ли риск осложнений при беременности. Если раньше она уже была инфицирована, то риск минимален. Во время беременности может возникнуть обострение старой инфекции, однако такая форма обычно не вызывает тяжелых последствий.
Если у женщины еще не было ЦМВ, значит, она входит в группу риска и ей следует уделять особое внимание профилактике цитомегаловирусной инфекции. Для ребенка опасна именно инфекция, которой мать заразилась первый раз во время беременности.
Для ребенка опасна именно инфекция, которой мать заразилась первый раз во время беременности.
При первичной инфекции у беременной женщины вирус часто попадает и в организм ребенка. Это еще не означает, что он заболеет. Как правило, заражение ЦМВ протекает бессимптомно. Однако примерно в 10 % случаев оно приводит к врожденным патологиям: микроцефалии, церебральной кальцификации, сыпи и увеличению селезенки и печени. Это часто сопровождается снижением интеллекта и глухотой, возможен даже летальный исход.
Таким образом, для будущей матери важно знать, была ли она в прошлом заражена ЦМВ. Если да, то риск осложнений из-за возможного ЦМВ становится незначительным. Если же нет – нужно проявлять особую осторожность во время беременности:
§ избегать незащищенного секса,
§ не контактировать со слюной другого человека (не целоваться, не использовать общую посуду, зубные щетки и пр.),
§ соблюдать правила гигиены при играх с детьми (мыть руки, если на них попадает слюна или моча),
§ сдавать анализ на ЦМВ при признаках общего недомогания.
Кроме того, цитомегаловирус представляет опасность при ослаблении иммунной системы (например, из-за иммунодепрессантов или ВИЧ). При СПИДе ЦМВ протекает в тяжелой форме и является частой причиной смерти больных.
Основные симптомы цитомегаловируса:
§ воспаление сетчатки (которое может приводить к слепоте),
§ колит (воспаление толстой кишки),
§ эзофагит (воспаление пищевода),
§ неврологические расстройства (энцефалит и др.).
Выработка антител – это один из способов борьбы с вирусной инфекцией. Существует несколько классов антител (IgG, IgM, IgA и др.), которые отличаются по своим функциям.
Иммуноглобулины M (IgM) обычно появляются в крови первыми (раньше, чем антитела других типов). Затем их количество постепенно уменьшается (этот процесс может длиться несколько месяцев). Если же произойдет обострение латентной инфекции, то уровень IgM вновь повысится.
Таким образом, IgM выявляются:
§ при первичной инфекции (в этом случае уровень IgM наиболее высокий),
§ при обострении болезни (а также при реинфекции, т. е. заражении новой формой вируса).
Для чего используется исследование?
Для диагностики острой цитомегаловирусной инфекции.
Когда назначается исследование?
§ При беременности.
§ При иммунодефиците (в частности, при ВИЧ-инфекции).
§ Когда у человека с нормальным иммунитетом есть симптомы мононуклеоза (если тесты не выявили вирус Эпштейна – Барр).
§ Если у новорожденных детей подозревают ЦМВ-инфекцию.
§ Во время беременности:
§ при симптомах заболевания,
§ если УЗИ выявило нарушения развития плода,
§ для скрининга.
ЦМВ-инфекция у беременных женщин часто протекает бессимптомно. Однако в некоторых случаях повышается температура, увеличиваются лимфоузлы, печень и/или селезенка.
Однако в некоторых случаях повышается температура, увеличиваются лимфоузлы, печень и/или селезенка.
При иммунодефиците симптомы ЦМВ-инфекции могут быть достаточно разнообразными: от общего недомогания до ретинита, колита, энцефалита и др.
§ Новорожденному анализ может быть назначен, если у ребенка:
§ желтуха, анемия,
§ увеличена селезенка и/или печень,
§ размер головы меньше нормального,
§ есть нарушения слуха или зрения,
§ есть неврологические расстройства (задержка умственного развития, конвульсии).
Что означают результаты на определение антител класса IgM?
Референсные значения
Результат: отрицательно.
Отрицательный результат
В данный момент нет текущей ЦМВ-инфекции. Если есть симптомы некоего заболевания, то они вызваны другим возбудителем. При этом ЦМВ может присутствовать в латентной форме. Правда, если заражение произошло совсем недавно (несколько дней назад), то антитела IgM, возможно, еще не успели появиться в крови.
При этом ЦМВ может присутствовать в латентной форме. Правда, если заражение произошло совсем недавно (несколько дней назад), то антитела IgM, возможно, еще не успели появиться в крови.
Положительный результат
Недавнее заражение (первичная инфекция). При первичной инфекции уровень IgM выше, чем при обострении.
После первичной инфекции IgM могут выявляться еще в течение нескольких месяцев.
Обострение латентной инфекции.
Важные замечания
Иногда нужно узнать, заражен ли новорожденный ребенок цитомегаловирусом. Для этого используют ПЦР и дополнительно определяют антитела. Если в крови ребенка выявляются IgM, значит, он действительно инфицирован ЦМВ.
Что такое реинфекция? В природе существует несколько разновидностей ЦМВ. Поэтому возможна ситуация, когда человек, уже инфицированный одним типом вируса, заражается еще и другим.
Что означают результаты?
Референсные значения: 0 — 0,5 Ед/мл.
Отрицательный результат при беременности
§ Женщина раньше не была инфицирована ЦМВ – есть риск приобрести первичную ЦМВ-инфекцию. Однако если с момента заражения прошло не больше 2-3 недель, то IgG могли еще не появиться. Чтобы исключить этот вариант, нужно сдать анализ повторно через 2 недели.
Положительный результат до беременности
§ Женщина уже была инфицирована ЦМВ в прошлом – риск осложнений минимален.
Положительный результат во время беременности
§ Нельзя сделать однозначный вывод. Возможно, ЦМВ попал в организм до беременности. Но не исключено, что женщина заразилась недавно, в начале беременности (за несколько недель до теста). Такой вариант представляет опасность для ребенка. Для точного диагноза нужны результаты других анализов (см. таблицу).
При попытке установить возбудителя неизвестного заболевания единичный тест на IgG дает мало информации. Нужно учитывать результаты всех анализов.
Нужно учитывать результаты всех анализов.
Результаты тестов в разных ситуациях
|
Первичная инфекция |
Обострение давней инфекции |
ЦМВ в латентном состоянии (человек был инфицирован в прошлом) |
Человек не заражен ЦМВ |
|
|
Результаты тестов |
IgG: первые 1-2 недели отсутствуют, потом их количество увеличивается. IgM: есть (высокий уровень). Авидность IgG: низкая. |
IgG: есть (количество увеличивается). IgM: есть (невысокий уровень). Авидность IgG: высокая. |
IgG: присутствуют на постоянном уровне. IgM: обычно нет. Авидность IgG: высокая.
|
IgG: нет. IgM: нет. |
Важные замечания
§ Иногда нужно узнать, заражен ли цитомегаловирусом сам новорожденный ребенок. Однако анализ на IgG в данном случае неинформативен. IgG могут проникать через плацентарный барьер, поэтому, если антитела есть у матери, то они же будут присутствовать и у ребенка.
§ Что такое реинфекция? В природе существует несколько разновидностей ЦМВ, так что возможна ситуация, когда человек, уже инфицированный одним типом вируса, заражается еще раз другим.
Анализ: Определение антител класса G (IgG) к цитомегаловирусу (Cytomegalovirus) в крови
Описание
Описание: Цитомегаловирусная инфекция (ЦМВИ) широко распространенная инфекционная болезнь человека. Носителями цитомегаловируса (ЦМВ) на слизистых верхних дыхательных путей, половых органов, в слюне, моче, сперме и других биологических жидкостях являются многие люди. В подавляющем большинстве случае ЦМВИ протекает в виде бессимптомного носительства или в виде самопроходящих симптомов ОРЗ, лимфоденита и др. Лабораторные исследования показывают наличие в крови антител к ЦМВИ у 80% обследуемых лиц старше 30 лет. Это значит, что они когда-то перенесли ЦМВИ. Опасность представляет первичная ЦМВИ для беременных женщин, т.к. может служить причиной внутриутробного поражения плода или инфицирования новорожденного. Особенно высока чувствительность плода к ЦМВИ на ранних стадиях развития (первые 3 месяца), т.к. в этом случае вероятность внутриутробного заражения достигает 50%. Клинические проявления ЦМВИ у новорожденных разнообразны: патология сердца, печени, пневмония. Задержка в росте, умственном развитии, микроцефалия и т.д. Серологическое исследование крови методом ИФА является в настоящее время наиболее распространенным анализом при данных инфекциях. Диагностическое значение при первичной герпетической инфекции имеет выявление IgM. Обнаружение IgG (при отсутствующих IgM) свидетельствует, как правило, о перенесенной в прошлом ЦМВИ или ее реактивации. Диагностических титров для IgG при герпетических инфекциях не существует, поэтому одним из методов, позволяющем дифференцировать стадии инфекции является четырехкратное нарастание титра IgG при исследовании парных образцов сывороток крови, взятых с интервалом 10-12 дней. В настоящее время разработан тест, который позволяет быстро и достоверно установить стадию инфекции — определение авидности IgG. Выявление в испытуемой сыворотке низкоавидных IgG указывает на свежую первичную инфекцию, высокоавидных антител — на персистирующую инфекцию (вне фазы реактивации).
Клинические проявления ЦМВИ у новорожденных разнообразны: патология сердца, печени, пневмония. Задержка в росте, умственном развитии, микроцефалия и т.д. Серологическое исследование крови методом ИФА является в настоящее время наиболее распространенным анализом при данных инфекциях. Диагностическое значение при первичной герпетической инфекции имеет выявление IgM. Обнаружение IgG (при отсутствующих IgM) свидетельствует, как правило, о перенесенной в прошлом ЦМВИ или ее реактивации. Диагностических титров для IgG при герпетических инфекциях не существует, поэтому одним из методов, позволяющем дифференцировать стадии инфекции является четырехкратное нарастание титра IgG при исследовании парных образцов сывороток крови, взятых с интервалом 10-12 дней. В настоящее время разработан тест, который позволяет быстро и достоверно установить стадию инфекции — определение авидности IgG. Выявление в испытуемой сыворотке низкоавидных IgG указывает на свежую первичную инфекцию, высокоавидных антител — на персистирующую инфекцию (вне фазы реактивации). Показатель индекса авидности в интервале «серой зоны» является промежуточным и указывает либо на позднюю стадию первичной инфекции, либо на возможность реактивации вируса. Сроки исполнения: До 3 дней. Подготовка к исследованию: Кровь сдается натощак (спустя 4-5 часов после приема пищи).
Показатель индекса авидности в интервале «серой зоны» является промежуточным и указывает либо на позднюю стадию первичной инфекции, либо на возможность реактивации вируса. Сроки исполнения: До 3 дней. Подготовка к исследованию: Кровь сдается натощак (спустя 4-5 часов после приема пищи).
Антитела IgG к Цитомегаловирусу (AT IgG CMV)
Срок выполнения, дней: 1-2
Код исследования: IA19
Цитомегаловирусная инфекция — антропонозная вирусная инфекционная болезнь. Цитомегаловирус относится к вирусу герпеса человека типа 5. Характеризуется преимущественно латентным течением у взрослых, а также генерализованной формой с поражением нервной системы и внутренних органов при внутриутробном заражении плода.
Антитела класса IgG выявляются в сыворотке крови через 2-4 недели после инфицирования цитомегаловирусом. Они являются показателями как текущей, так и перенесенной инфекции и могут обнаруживаться еще в течение нескольких лет после заболевания.
Они являются показателями как текущей, так и перенесенной инфекции и могут обнаруживаться еще в течение нескольких лет после заболевания.
Подготовка пациента: Сдача крови натощак.
Материал: Венозная кровь.
Стабильность пробы: не более 5 суток при температуре 2-8 °C при условии отсутствия микробной контаминации и не более 6 месяцев при температуре -20 °C. Замораживать только один раз.
Метод: ИФА.
Анализатор: Sinnowa ER-500.
Тест – система: Beckman Coulter (США).
Референсные значения (норма):
Отрицательный: <1.0;
Положительный: ≥1.0.
Основные показания к назначению анализа:
1. Подготовка к беременности;
2. Признаки внутриутробной инфекции, фето-плацентарная недостаточность;
3. Состояние иммуносупрессии при ВИЧ-инфекции, неопластических заболеваниях, приёме цитостатических препаратов и т. д.;
д.;
4. Клиническая картина инфекционного мононуклеоза в отсутствие инфекции, вызванной вирусом Эпштейна –Барра;
5. Гепато-спленомегалия неясной природы;
6. Лихорадка неясной этиологии;
7. Повышение уровня печёночных трансаминаз, гамма-ГТ, ЩФ в отсутствие маркёров вирусных гепатитов;
8. Атипичное течение пневмонии у детей;
9. Невынашивание беременности (замёршая беременность, привычные выкидыши).
Интерпретация результатов:
Положительный результат:
1. ЦМВ-инфекция;
2. Внутриутробная инфекция возможна, вероятность её возникновения неизвестна.
Отрицательный результат:
В сыворотке крови, взятой в начале острого периода ЦМВ-инфекции и к концу периода выздоровления, специфические антитела класса IgG и IgM могут отсутствовать. Поэтому отрицательный результат анализа не позволяет исключить инфекцию. Для уточнения диагноза необходимо не менее двух исследований крови.
Кинетика специфических иммуноглобулинов M, E, A и G при врожденной, первичной и вторичной цитомегаловирусной инфекции изучена с помощью иммуноферментного анализа с захватом антител
Иммуноферментный иммуноферментный анализ (ELISA) с захватом антител с использованием ядерного антигена цитомегаловируса, меченного ферментом (CMV), является надежным и легко выполняемым тестом, подходящим для рутинного использования. Однако, поскольку серологический ответ на ЦМВ-инфекцию может значительно различаться у разных пациентов, мы изучили кинетику ЦМВ-специфических иммуноглобулинов M (IgM), IgE, IgA и IgG в 352 сыворотках от 61 пациента с помощью ELISA с захватом антител. и тесты фиксации комплемента (CF).В группе мононуклеоза ЦМВ (n = 17) у большинства пациентов были антитела ко всем четырем классам иммуноглобулинов, но уровни антител быстро снижались, при этом половина пациентов имела погранично-положительную или отрицательную реакцию для всех классов, кроме IgG, через 2 месяца после появление симптомов. У двенадцати пациентов с первичной ЦМВ-инфекцией после трансплантации почек или костного мозга также развились все антитела класса иммуноглобулинов. Только у двух пациентов антитела IgM и IgE к CMV предшествовали сероконверсии антител CF, а у одного пациента эти антитела отставали на несколько месяцев.Большинство пациентов имели все классы антител против ЦМВ, кроме IgA, в течение года и более. Среди 10 пациентов, перенесших трансплантацию с вторичной ЦМВ-инфекцией, 50% имели длительные антитела IgM, и очень немногие имели антитела IgE или IgA, но все имели антитела IgG к ЦМВ. У 13 инфицированных младенцев специфический для ЦМВ серологический ответ также характеризовался длительными антителами IgM, IgE и IgG. У двух пациентов не выявлялись определяемые антитела IgM, и у одного из них также не обнаруживались антитела IgE. Ответ IgA у младенцев в целом отсутствовал; некоторые, однако, были погранично положительными.Из девяти пациентов с синдромом приобретенного иммунодефицита с ЦМВ-инфекцией, изученных в течение последнего года жизни, только у одного были антитела всех четырех классов, у остальных — только антитела против CF, и все, кроме одного, имели антитела класса IgG.
У двенадцати пациентов с первичной ЦМВ-инфекцией после трансплантации почек или костного мозга также развились все антитела класса иммуноглобулинов. Только у двух пациентов антитела IgM и IgE к CMV предшествовали сероконверсии антител CF, а у одного пациента эти антитела отставали на несколько месяцев.Большинство пациентов имели все классы антител против ЦМВ, кроме IgA, в течение года и более. Среди 10 пациентов, перенесших трансплантацию с вторичной ЦМВ-инфекцией, 50% имели длительные антитела IgM, и очень немногие имели антитела IgE или IgA, но все имели антитела IgG к ЦМВ. У 13 инфицированных младенцев специфический для ЦМВ серологический ответ также характеризовался длительными антителами IgM, IgE и IgG. У двух пациентов не выявлялись определяемые антитела IgM, и у одного из них также не обнаруживались антитела IgE. Ответ IgA у младенцев в целом отсутствовал; некоторые, однако, были погранично положительными.Из девяти пациентов с синдромом приобретенного иммунодефицита с ЦМВ-инфекцией, изученных в течение последнего года жизни, только у одного были антитела всех четырех классов, у остальных — только антитела против CF, и все, кроме одного, имели антитела класса IgG. Все исследованные сыворотки были также протестированы против контрольного антигена, продуцируемого из ядер неинфицированных клеток. Было обнаружено, что у некоторых пациентов вырабатывались антитела к ядерным антигенам параллельно с повышением уровня специфических антител. Неспецифические антитела встречались во всех четырех классах, но чаще всего они относились к классу IgM.Добавление немеченого контрольного антигена к конъюгатам не всегда было достаточным для прекращения этой неспецифической реакции.
Все исследованные сыворотки были также протестированы против контрольного антигена, продуцируемого из ядер неинфицированных клеток. Было обнаружено, что у некоторых пациентов вырабатывались антитела к ядерным антигенам параллельно с повышением уровня специфических антител. Неспецифические антитела встречались во всех четырех классах, но чаще всего они относились к классу IgM.Добавление немеченого контрольного антигена к конъюгатам не всегда было достаточным для прекращения этой неспецифической реакции.
антител подкласса IgG к ранним антигенам, индуцированным цитомегаловирусом человека (HCMV)
Браун В., Абрахам Р. (1989) Модифицированный диффузионный блоттинг для быстрого и эффективного переноса белка с помощью PhastSystem. Электрофорез 10: 249–253
Google Scholar
Brodt HR, Helm EB, Werner A, Joetten A, Bergmann L, Klüver A, Stille W (1986) Spontanverlauf der LAV / HTLV-III-Infektion. Dtsch Med Wochenschr 111: 1175–1180
Dtsch Med Wochenschr 111: 1175–1180
Google Scholar
Doerr HW, Rentschler M, Scheifler G (1987) Серологическое обнаружение активных инфекций, вызванных вирусами герпеса человека (CMV, EBV, HSV, VZV): диагностический потенциал антител, специфичных к классу IgA и подклассу IgG. Инфекция 15: 93–98
CAS PubMed Google Scholar
Фридман А.Д., Фурукава Т., Плоткин С.А. (1982) Обнаружение антител к раннему антигену цитомегаловируса у вакцинированных, здоровых добровольцев и кандидатов на трансплантацию почки.J Infect Dis 146: 255–259
Google Scholar
Фридман А.Д., Михельсон С., Плоткин С.А. (1982) Обнаружение антител к прераннему ядерному антигену и раннему раннему антигену у пациентов, иммунизированных цитмегаловирусной вакциной. Infect Immun 38: 1068–1072
Google Scholar
Gergely L, Chegledy J, Vaczi L (1981) Комплемент-связывающие антитела к человеческим цитомегаловирусу, индуцированным ранними ядерными антигенами при мононуклеозе. Med Microbiol Immunol 170: 99–108
Med Microbiol Immunol 170: 99–108
Google Scholar
Gerna G, Cereda PM, Cattaneo E, Achilli G, Revello G (1978) Иммуноглобулин G к вирус-специфическим ранним антигенам при врожденных, первичных и реактивированных цитомегаловирусных инфекциях человека. Infect Immun 22: 833–841
Google Scholar
Gilljam G, Wahren B (1989) Свойства подклассов IgG к цитомегаловирусу человека.J Virol методы 25: 139–152
Google Scholar
Griffiths PD, Buie KJ, Heath RB (1980) Сохранение высоких титров антител к ранним антигенам цитомегаловируса у беременных. Arch Virol 64: 303–309
Google Scholar
Hamann A, Braun W., Doerr HW (1991) Антитела против CMV-индуцированных «ранних» антигенов, обнаруженных с помощью иммуноблоттинга, не связаны исключительно с активной инфекцией. Res Virol 14 :: 33–37
Res Virol 14 :: 33–37
Google Scholar
Joassin L, Somze A, Reginster M (1989) Обнаружение с помощью иммуноферментного анализа специфических изотипов иммуноглобулина G при первичных и установленных цитомегаловирусных инфекциях. J Clin Microbiol 27: 139–144
Google Scholar
Keil GM, Fibi MR, Koszinowski UH (1985) Характеристика основных полипептидов немедленного раннего периода, кодируемых мышиным цитомегаловирусом.J Virol 54: 422–428
Google Scholar
Landini MP, Baldasarri B, Mirolo G, Ripalti A, La Placa M (1988) Реакционная способность структурных полипептидов цитомегаловируса с различными подклассами IgG, присутствующими в сыворотке крови человека. J Infect 16: 163–167
Google Scholar
Linde GA, Hammarström L, Persson MAA, Smith CIE, Sundqvist VA, Wahren B (1983) Вирус-специфическая активность антител различных подклассов иммуноглобулинов G и A при цитомегаловирусных инфекциях. Инфекция иммунной 42 237–244
Инфекция иммунной 42 237–244
Google Scholar
Матушке А., Генрих Б., Хельманн Р., Богнер Дж., Фюссл Х.С., Гебель Ф. Д. (1989) Zusammenstellung der gebräuchlichen Definitionen und Klassifikationssysteme bei HIV-Infektion. AIDS-Forschung 11: 587–594
Google Scholar
Middeldorp JM, Jongsma J, ter Haar A, Schirm J, The TH (1984) Выявление иммуноглобулиновых антител M и G против ранних и поздних антигенов цитомегаловируса с помощью иммуноферментного анализа.J Clin Microbiol 20: 763–771
Google Scholar
Musiani M, Landini MP, Feletti C, LaPlaca M (1978) Сывороточные антитела против «ранних» и «немедленных» антигенов, индуцированных цитомегаловирусом, и наличие вируса у реципиентов почечного трансплантата. Microbiologica 1 101–105
Google Scholar
Rodriquez GE, Adler SP (1990) Ответ подкласса иммуноглобулинов G на цитомегаловирус у серопозитивных пациентов после переливания крови. Переливание 30 528–531
Переливание 30 528–531
Google Scholar
The TH, Andersen HK, Spencer ES, Klein G (1977) Антитела против цитомегаловирусных ранних антигенов (CMV-EA) у реципиентов почечного аллотрансплантата с подавленным иммунитетом. Clin Exp Immunol 28: 502–505
Google Scholar
Варен Б., Линде А., Сундквист В.А., Люнгман П., Лённквист Б., Рингден О. (1984) IgG-подкласс-специфическая реактивность ЦМВ у реципиентов трансплантата костного мозга.Трансплантация 38: 479–483
Google Scholar
Титр антицитомегаловирусного иммуноглобулина M при врожденной инфекции в первом триместре беременности с первичной инфекцией: многоцентровое проспективное когортное исследование
Kenneson A, Cannon MJ. Обзор и метаанализ эпидемиологии врожденной цитомегаловирусной (ЦМВ) инфекции. Rev Med Virol 2007; 17 : 253–276.
Артикул Google Scholar
Fowler KB, Stagno S, Pass RF, Britt WJ, Boll TJ, Alford CA.Исход врожденной цитомегаловирусной инфекции в зависимости от статуса материнских антител. N Engl J Med 1992; 326 : 663–667.
CAS Статья Google Scholar
Адлер СП, Маршалл Б. Цитомегаловирусные инфекции. Pediatr Rev 2007; 28 : 92–100.
Артикул Google Scholar
Джонсон Дж. М., Андерсон БЛ.Цитомегаловирус: нужно ли проверять беременных на первичную инфекцию? Am J Perinatol 2013; 30 : 121–124.
Артикул Google Scholar
Ревелло М.Г., Герна Г. Диагностика и лечение цитомегаловирусной инфекции человека у матери, плода и новорожденного. Clin Microbiol Rev 2002; 15 : 680–715.
Артикул Google Scholar
Naessens A, Casteels A, Decatte L, Foulon W.Серологическая стратегия выявления новорожденных с риском врожденной цитомегаловирусной инфекции. J Pediatr 2005; 146 : 194–197.
Артикул Google Scholar
Канеко М., Самешима Х, Минемацу Т, Кусумото К., Ямаути А, Икеноуэ Т. Авидность материнского IgG, IgM и ультразвуковые аномалии: комбинированный метод выявления врожденной цитомегаловирусной инфекции с последствиями. J Perinatol 2013; 33 : 831–835.
CAS Статья Google Scholar
Munro SC, Hall B, Whybin LR, Leader L, Robertson P, Maine GT et al . Диагностика и скрининг цитомегаловирусной инфекции у беременных. J Clin Microbiol 2005; 43 : 4713–4718.
CAS Статья Google Scholar
Sonoyama A, Ebina Y, Morioka I, Tanimura K, Morizane M, Tairaku S et al . Низкая авидность IgG и аномалии развития плода на УЗИ позволяют прогнозировать врожденную цитомегаловирусную инфекцию. J Med Virol 2012; 84 : 1928–1933.
Низкая авидность IgG и аномалии развития плода на УЗИ позволяют прогнозировать врожденную цитомегаловирусную инфекцию. J Med Virol 2012; 84 : 1928–1933.
Артикул Google Scholar
Lagrou K, Bodeus M, Van Ranst M, Goubau P. Оценка авидности иммуноглобулина M (IgM), IgG и IgG к новому архитектору цитомегаловируса. J Clin Microbiol 2009; 47 : 1695–1699.
CAS Статья Google Scholar
Tagawa M, Minematsu T, Masuzaki H, Ishimaru T., Moriuchi H.Сероэпидемиологическое исследование цитомегаловирусной инфекции среди беременных в Нагасаки, Япония. Pediatr Int 2010; 52 : 459–462.
Артикул Google Scholar
Prince HE, Lape-Nixon M. Роль теста на авидность IgG к цитомегаловирусу (ЦМВ) в диагностике первичной ЦМВ-инфекции во время беременности. Clin Vaccine Immunol 2014; 21 : 1377–1384.
Clin Vaccine Immunol 2014; 21 : 1377–1384.
Артикул Google Scholar
Ламли С., Патель М., Гриффитс П.Д.Комбинация специфических антител IgM и антител IgG с низкой авидностью не всегда указывает на первичную инфекцию цитомегаловирусом. J Med Virol 2014; 86 : 834–837.
CAS Статья Google Scholar
Lazzarotto T, Guerra B, Gabrielli L, Lanari M, Landini MP. Обновленная информация о профилактике, диагностике и лечении цитомегаловирусной инфекции во время беременности. Clin Microbiol Infect 2011; 17 : 1285–1293.
CAS Статья Google Scholar
Танигучи К., Ватанабэ Н., Сато А., Джва С.К., Сузуки Т., Яманобе Й. и др. . Изменения распространенности цитомегаловируса среди беременных японских женщин — 10-летнее одноцентровое исследование. J Clin Virol 2014; 59 : 192–194.
J Clin Virol 2014; 59 : 192–194.
Артикул Google Scholar
Ямада Х., Моризане М., Танимура К., Мориока И., Эбина Ю., Мацуда Х. и др. .Испытание иммуноглобулиновой терапии плода при симптоматической врожденной цитомегаловирусной инфекции. J Репрод Иммунол 2012; 95 : 73–79.
CAS Google Scholar
Шигэми Д., Ямагути С., Оцука Т., Камои С., Такехшита Т. Распространенность антител IgG к цитомегаловирусу среди беременных женщин в Японии в 2009-2014 гг. Am J Infect Control 2015; 43 : 1218–1221.
CAS Статья Google Scholar
Эбина Ю., Минемацу Т., Сонояма А., Мориока И., Иноуэ Н., Тайраку С. и др. .Значение авидности IgG для прогнозирования врожденной цитомегаловирусной инфекции в проспективном когортном исследовании. J Perinat Med 2014; 42 : 755–759.
J Perinat Med 2014; 42 : 755–759.
CAS Статья Google Scholar
Нагамори Т., Кояно С., Иноуэ Н., Ямада Х., Осима М., Минемацу Т. и др. . Единичный штамм цитомегаловируса, связанный с потерей плода, а затем с врожденной инфекцией последующего ребенка, рожденного от той же матери. J Clin Virol 2010; 49 : 134–136.
Артикул Google Scholar
Блэкберн Н.К., Бесселаар Т.Г., Шоуб Б.Д., О’Коннелл К.Ф. Дифференциация первичной цитомегаловирусной инфекции от реактивации с помощью теста денатурации мочевины для измерения авидности антител. J Med Virol 1991; 33 : 6–9.
CAS Статья Google Scholar
Фатьма Б., Питер В.Р., Моника Л., Уильям Д.Р.Сравнение пяти иммуноанализов CMV IgM с авидностью IgG CMV для диагностики первичной инфекции CMV. Патология 2012; 44 : 381–383.
Патология 2012; 44 : 381–383.
Артикул Google Scholar
Prince HE, Leber AL. Валидация собственного теста на авидность цитомегаловирусного иммуноглобулина G (CMV IgG) и взаимосвязь авидности с уровнями CMV IgM. Clin Diagn Lab Immunol 2002; 9 : 824–827.
CAS PubMed PubMed Central Google Scholar
Revello MG, Lazzarotto T, Guerra B, Spinillo A, Ferrazzi E, Kustermann A et al .Рандомизированное исследование гипериммунного глобулина для предотвращения врожденного цитомегаловируса. N Engl J Med 2014; 370 : 1316–1326.
CAS Статья Google Scholar
Танимура К., Тайраку С., Эбина Ю., Мориока И., Нагамата С., Дегучи К. и др. . Прогнозирование врожденной цитомегаловирусной инфекции у беременных из группы высокого риска. Clin Infect Dis 2017; 64 : 159–165.
Clin Infect Dis 2017; 64 : 159–165.
CAS Статья Google Scholar
Иммунный глобулин цитомегаловируса человека: использование, взаимодействие, механизм действия
CytoGam (иммуноглобулин цитомегаловируса) содержит антитела IgG, представляющие антитела большого числа нормальных людей, которые внесли свой вклад в пулы плазмы, из которых был получен продукт.Глобулин содержит относительно высокую концентрацию антител, направленных против цитомегаловируса (CMV). В случае людей, которые могут подвергнуться воздействию ЦМВ, CytoGam может повысить уровень соответствующих антител до уровней, достаточных для предотвращения или снижения частоты серьезного заболевания ЦМВ. Метка .
ЦМВ — IGIV в основном состоит из иммуноглобулина G (IgG), в частности подклассов IgG1 и IgG3 . IgG1 и IgG3 играют важную роль в нейтрализации вирусов в дополнение к защите тканей и активации комплемента 3 .
Иммуноглобулины, такие как CMV-IGIV, препятствуют внеклеточным вирусам инфицировать их специфические клетки-мишени. Нейтрализация вирусов снижает способность вирусов распространяться из внеклеточной области во внутриклеточную. CMV-IGIV подавляет инфицирование клеток CMV из-за того, что вирус не может получить доступ к ключевым мишеням клеточной мембраны, или из-за вмешательства в непокрытие или проникновение. Цитогам подавляет эти процессы 3 .
Защита, производная от цитомегаловирусного иммуноглобулина (CMV-IGIV), имеет быстрое начало, сообщая соответствующие концентрации антител против CMV сразу после инфузии.Продолжительность действия CMV-IGIV составляет 1–3 месяца 3 .
IgG распространяется из плазмы в различные другие части тела 3 .
Цитомегаловирусный иммунный глобулин (CMV-IGIV) вводится внутривенным (IV) путем. CMV-IGIV в основном состоит из иммуноглобулина G (IgG), в частности подклассов IgG1 и IgG3 . Катаболизм иммуноглобулинов происходит в основном в плазме, однако печень также может играть роль Метка .
Катаболизм иммуноглобулинов происходит в основном в плазме, однако печень также может играть роль Метка .
Метаболизм IgG, по-видимому, является многокомпонентным процессом первого порядка. Более высокие концентрации IgG увеличивают скорость метаболизма и сокращают период полувыведения. Метаболизм IgG, вероятно, является многокомпонентным процессом первого порядка 3 .
IgG1 имеет период полураспада 23-25 дней, тогда как период полураспада IgG3 составляет всего 9 дней 3 .
CMV-IGIV производится из плазмы человека и, как и другие продукты из плазмы, несет возможность передачи вирусных агентов через кровь и, возможно, приона болезни Крейтцфельда-Якоба (CJD).Риск передачи распознанных вирусов, передающихся через кровь, считается низким из-за свойств инактивации и удаления вирусов в холодном этаноле по Кон-Онкли 4 .
Почечная недостаточность
Сообщалось о нарушении функции почек, острой почечной недостаточности (ARF), остром канальцевом некрозе (ATN), проксимальной канальцевой нефропатии, осмотическом нефрозе и смерти у пациентов, получавших IGIV. Увеличение азота мочевины в крови (АМК) и креатинина сыворотки произошло уже через 1-2 дня после лечения IGIV, и это прогрессировало до олигурии или анурии 7 .
Увеличение азота мочевины в крови (АМК) и креатинина сыворотки произошло уже через 1-2 дня после лечения IGIV, и это прогрессировало до олигурии или анурии 7 .
TRALI (травма легких, связанная с переливанием крови)
TRALI характеризуется тяжелым респираторным дистресс-синдромом, отеком легких, гипоксемией, нормальной функцией левого желудочка и лихорадкой. Обычно это происходит в течение 1-6 часов после переливания иммуноглобулина. Пациентам с TRALI следует проводить кислородную терапию в сочетании с респираторной поддержкой. Метка .
Гемолиз
Продукты иммуноглобулина для внутривенного введения (человека) (IGIV) могут содержать антитела группы крови, которые могут действовать как гемолизины и индуцировать покрытие красных кровяных телец иммуноглобулином in vivo, вызывая положительную прямую антиглобулиновую реакцию и, иногда, гемолиз.Гемолитическая анемия может развиться после терапии IGIV из-за повышенной секвестрации эритроцитов. Метка .
Метка .
* Тромботические события *
В группу риска входят пациенты с атеросклерозом в анамнезе, множественными сердечно-сосудистыми факторами риска, пожилым возрастом, нарушением сердечного выброса и / или известной или предполагаемой гипервязкостью. Возможные риски и преимущества IGIV следует сопоставить с рисками альтернативных методов лечения для всех пациентов, которым рассматривается возможность введения IGIV.Базовая оценка вязкости крови является важным фактором для пациентов с риском гипервязкости крови. Этикетка .
Синдром асептического менингита
Сообщалось, что синдром асептического менингита (AMS) нечасто возникает в связи с лечением иммуноглобулином внутривенно (человека) (IGIV). Синдром обычно начинается в течение от нескольких часов до 2 дней после лечения. Этот синдром характеризуется симптомами и признаками, включая сильную головную боль, ригидность затылочной кости, сонливость, лихорадку, светобоязнь, болезненные движения глаз, тошноту и рвоту. Метка .
Метка .
Исследования спинномозговой жидкости (ЦСЖ) часто дают положительные результаты с плеоцитозом до нескольких тысяч клеток на куб. Мм, преимущественно гранулоцитарного ряда, и повышенным уровнем белка до нескольких сотен мг / дл. Пациенты, испытывающие такие симптомы и признаки, должны пройти тщательное неврологическое обследование, включая исследования спинномозговой жидкости, чтобы исключить другие возможные причины менингита. Это состояние может возникать чаще при приеме высоких доз (2 г / кг или больше) IGIV.Прекращение лечения IGIV привело к ремиссии синдрома асептического менингита в течение нескольких дней без отдаленных последствий. Метка .
Цитомегаловирусный иммунный глобулин (CMV-IGIV) отнесен FDA к категории риска беременности C. Никаких хорошо контролируемых исследований у беременных женщин не проводилось, и неизвестно, может ли CMV-IGIV причинить вред женщинам или отрицательно повлиять на репродуктивную систему. По данным Консультативного комитета по практике иммунизации, введение иммуноглобулина беременным женщинам не представляет известного риска для плода. Метка .
Метка .
От производителя отсутствуют данные об использовании цитомегаловирусного иммуноглобулина (CMV-IGIV) при грудном вскармливании, и неизвестно, выделяется ли CMV-IGIV с грудным молоком. 3 .
Набор для ИФА IgG человека против цитомегаловируса (CMV) (ab108724)
Обзор
Название продукта
Набор для ELISA-анализа человеческих антител к цитомегаловирусу IgG (CMV)
Метод обнаружения
Колориметрический
точность
Интра-анализ Образец n Среднее SD CV% Поз.  Сыворотка
Сыворотка12 1,9% Между анализами Образец n Среднее SD CV% Поз.Сыворотка 4 6,2% Тип образца
Сыворотка, Геп плазма, Цит плазма
Тип анализа
Косвенный
Продолжительность анализа
Многоступенчатый стандартный анализ
Реактивность видов
Реагирует с: Человек
Обзор продукции
НаборAbcam’s anti-Cytomegalovirus (CMV) IgG Human in vitro ELISA (Enzyme-Linked Immunosorbent Assay) разработан для качественного измерения антител класса IgG против цитомегаловируса в сыворотке и плазме человека.

96-луночный планшет был предварительно покрыт антигенами цитомегаловируса для связывания родственных антител. В лунки добавляют контрольные или тестовые образцы и инкубируют. После промывания в лунки добавляют меченый пероксидазой хрена (HRP) конъюгат против человеческого IgG, который связывается с иммобилизованными антителами, специфичными к цитомегаловирусу. Затем TMB катализируется HRP с образованием продукта синего цвета, который меняется на желтый после добавления кислого стоп-раствора. Плотность желтой окраски прямо пропорциональна количеству образца IgG к цитомегаловирусу, захваченного в планшете.
Платформа
Микропланшет
Недвижимость
Инструкция по хранению
Хранить при + 4 ° C. См. Протоколы.
Компоненты Идентификатор 1 x 96 тестов Промывочный раствор 20X Колпачок белый 1 x 50 мл Защитная пленка 1 ед. 
Микропланшет с покрытием против антигенов цитомегаловируса (12 x 8 лунок) 1 ед. Цитомегаловирусный анти-IgG конъюгат HRP Кепка черная 1 x 20 мл Отсеченный контроль IgG к цитомегаловирусу Кепка зеленая 1 x 3 мл Цитомегаловирус IgG Отрицательный контроль Синяя кепка 1 x 2 мл Положительный контроль IgG к цитомегаловирусу Кепка красная 1 x 2 мл Разбавитель образца IgG Колпачок белый 1 x 100 мл Стоп-раствор красная кепка 1 x 15 мл Держатель ленты 1 шт. 
Раствор субстрата TMB Колпачок желтый 1 x 15 мл Направления исследований
Листы данных и документы
SDS скачать
Страна / регион Выберите страну / регион
Язык Выбор языка
Скачать брошюру
Список литературы (10)
ab108724 упоминается в 10 публикациях.
- Ciencewicki JM et al. Доноры плазмы на юго-западе США вносят положительный вклад в формирование разнообразного терапевтического профиля антител в иммуноглобулиновых продуктах.
 Sci Rep 10: 6850 (2020). PubMed: 32321978
Sci Rep 10: 6850 (2020). PubMed: 32321978 - Smith SL et al. Разнообразие NK-клеток периферической крови человека, идентифицированное секвенированием одноклеточной РНК. Blood Adv 4: 1388-1406 (2020). PubMed: 32271902
- Hameiri Bowen D et al. Цитомегаловирус-специфический иммуноглобулин G связан с хроническим заболеванием легких у детей и подростков из стран Африки к югу от Сахары с перинатальной ВИЧ-инфекцией. Clin Infect Dis Н / Д: Н / Д (2020). PubMed: 33242076
- Bowyer G et al. Снижение реакции на вакцину против Эболы у CMV + молодых людей связано с размножением CD57 + KLRG1 + Т-клеток. J Exp Med 217: Н / Д (2020). PubMed: 32413101
- Styles JN et al. Инфекции цитомегаловируса человека связаны с повышенными биомаркерами сосудистого поражения.
 Front Cell Infect Microbiol 10: 334 (2020). PubMed: 32733818
Front Cell Infect Microbiol 10: 334 (2020). PubMed: 32733818 - Саловин А и др. Энцефалит против рецепторов NMDA и неэнцефалитная инфекция HSV-1. Neurol Neuroimmunol Neuroinflamm 5: e458 (2018). PubMed: 29629396
- Przemska-Kosicka A et al. Синбиотик не влияет на возрастные изменения ответа естественных киллерных клеток на сезонную вакцинацию против гриппа: рандомизированное контролируемое исследование. Front Immunol 9: 591 (2018). PubMed: 29662493
- Enani S et al. Влияние старения и синбиотика на иммунный ответ на вакцинацию против сезонного гриппа; рандомизированное контролируемое исследование. Clin Nutr 37: 443-451 (2018). PubMed: 28215759
- Slawinski BL et al. Серопозитивный материнский цитомегаловирус и симптомы аутизма у детей.
 Am J Reprod Immunol 79: e12840 (2018). PubMed: 29520885
Am J Reprod Immunol 79: e12840 (2018). PubMed: 29520885 - Przemska-Kosicka A et al. Влияние синбиотика на реакцию на вакцинацию против сезонного гриппа сильно зависит от степени иммунного старения. Иммунное старение 13: 6 (2016). PubMed: 26985232
Отзывы клиентов и вопросы и ответы
1 — 6 из 6 Обзоры или вопросы и ответы
Просмотров: 10Просмотров: 50Просмотров: 100Сортировать по: Наивысшим голосам Сортировать по: Наименьшим голосам Сортировать по: Новым Первым Сортировать: Старым Первым
Количественное определение человеческого IgG к CMV в образцах плазмы с EDTA (свежезамороженных и хранящихся при -80 ° C) тестировали с использованием набора ab108724 ELISA. В информации, предоставленной с набором, говорилось, что ранее тестировались только образцы сыворотки и цитратной плазмы. Мы хотели проверить, позволяет ли набор точное количественное определение человеческих IgG анти-CMV в плазме EDTA.
В информации, предоставленной с набором, говорилось, что ранее тестировались только образцы сыворотки и цитратной плазмы. Мы хотели проверить, позволяет ли набор точное количественное определение человеческих IgG анти-CMV в плазме EDTA.
Образцы плазмы разбавляли 1: 100 разбавителем для образцов, поставляемым с набором (в соответствии с инструкциями производителя), и анализировали в двух экземплярах. Дублирующие лунки для положительного контроля, отсечки и отрицательного контроля, а также бланк были включены в соответствии с предоставленным протоколом.Все шаги выполнялись в соответствии с инструкциями, прилагаемыми к набору ELISA.
Абсорбцию (оптическую плотность, OD) определяли с помощью планшет-ридера, установленного на 450 нм с эталонной длиной волны 650 нм. Поглощение холостых лунок усредняли и вычитали из всех остальных лунок. Значения абсорбции были преобразованы в стандартные единицы в соответствии с инструкциями производителя (пороговое значение = 10 положительных единиц> 11 отрицательных единиц Набор четко различал IgG анти-CMV положительные и отрицательные образцы и позволял количественно определять эти антитела в образцах плазмы с ЭДТА (см. Рисунок). ).
Рисунок). ).
Протокол, прилагаемый к набору, был ясным и простым в использовании и содержал всю информацию, необходимую для проведения анализа.
Сообщество пользователей Abcam
Проверенный клиент
Опубликовано 04 сен 2019
Спасибо за ваше письмо.Прошу прощения за задержку с ответом на ваше письмо.
К сожалению, мы не продаем антигены для этих наборов отдельно.
Читать далее Спасибо за ваше письмо.
Я определил для вас следующие продукты;
ab108776
ab108778
ab108767
у нас нет набора IgM против краснухи
ab108724
ab108725
ab108737
ab108738
ab108739
ab10873 ab этот комплект.Пожалуйста, дайте мне знать, если вы не получите от нас известий в течение 24 часов после этого письма.
Надеюсь, эта информация будет полезной. Если вам потребуется дополнительная информация, пожалуйста, свяжитесь со мной.
Читать далееСпасибо за ваш запрос.
Я рад подтвердить, что чашки с ab108724 покрыты антигенами штамма CMV AD-169.
Надеюсь, эта информация окажется полезной. Пожалуйста, не стесняйтесь обращаться к ним снова, если у вас возникнут какие-либо вопросы.
A1: CMV ELISA, ab108724, является качественным и поэтому не имеет известного предела обнаружения.Чувствительность анализа определяется как вероятность положительного результата анализа в присутствии определенного аналита. Чувствительность анализа для этого набора составляет 98%. A2: Граничный контроль используется для определения порога оптической плотности, при котором образцы считаются положительными или отрицательными. Подробную информацию об этом расчете см. Во вставке продукта. A3: Элементы управления в этом наборе поставляются в жидкой форме, готовой к использованию.
Читать далее Спасибо за терпение. Лаборатория, разработавшая ИФА, прислала следующую информацию. Если он не полностью отвечает на ваши вопросы, свяжитесь со мной. CMV IgG ELISA — качественный тест. Поэтому у нас нет данных о пределе обнаружения или пике. Тепловая инактивация образцов не рекомендуется, так как это отрицательно влияет на результаты теста. Перекрестной реактивности с антителами против HSV1-2, кори, эпидемического паротита или VZV не наблюдалось. Специфичность диагностики определяется как вероятность отрицательного результата анализа в отсутствие определенного аналита.Для этого это 97,5%. Диагностическая чувствительность определяется как вероятность положительного результата анализа в присутствии определенного аналита. Чувствительность этого анализа 98%. Вмешательства в гемолитические, липемические или желтушные сыворотки не наблюдаются до концентраций гемоглобина 10 мг / мл, триглицеридов 5 мг / мл и билирубина 0,2 мг / мл.
Лаборатория, разработавшая ИФА, прислала следующую информацию. Если он не полностью отвечает на ваши вопросы, свяжитесь со мной. CMV IgG ELISA — качественный тест. Поэтому у нас нет данных о пределе обнаружения или пике. Тепловая инактивация образцов не рекомендуется, так как это отрицательно влияет на результаты теста. Перекрестной реактивности с антителами против HSV1-2, кори, эпидемического паротита или VZV не наблюдалось. Специфичность диагностики определяется как вероятность отрицательного результата анализа в отсутствие определенного аналита.Для этого это 97,5%. Диагностическая чувствительность определяется как вероятность положительного результата анализа в присутствии определенного аналита. Чувствительность этого анализа 98%. Вмешательства в гемолитические, липемические или желтушные сыворотки не наблюдаются до концентраций гемоглобина 10 мг / мл, триглицеридов 5 мг / мл и билирубина 0,2 мг / мл.
цитомегаловирусов при беременности | GLOWM
ВВЕДЕНИЕ
Цитомегаловирус (ЦМВ), член группы вирусов герпеса, является наиболее частой причиной врожденной вирусной инфекции 1 , 2 и наиболее частой инфекционной причиной задержки развития и нейросенсорной тугоухости в США. 3 Во всем мире 1% всех живорожденных младенцев инфицированы ЦМВ. ЦМВ распространен повсеместно, высоко видоспецифичен и, как и другие члены его семейства, заражает почти всех людей в какой-то момент их жизни. 4 Возраст приобретения варьируется в зависимости от географических и социально-экономических факторов, что приводит к большим различиям в распространенности среди групп.
3 Во всем мире 1% всех живорожденных младенцев инфицированы ЦМВ. ЦМВ распространен повсеместно, высоко видоспецифичен и, как и другие члены его семейства, заражает почти всех людей в какой-то момент их жизни. 4 Возраст приобретения варьируется в зависимости от географических и социально-экономических факторов, что приводит к большим различиям в распространенности среди групп.
Естественная история инфекции ЦМВ сложна и характеризуется латентным периодом в течение всей жизни, перемежающимся эпизодами рецидива инфекции после первичной инфекции.После первичной инфекции выделение вируса из нескольких разных участков может сохраняться от недель до лет, прежде чем вирус станет латентным. Эпизоды рецидивирующей инфекции с возобновлением выделения часто представляют собой реактивацию латентного вируса, но также могут быть вызваны повторным заражением антигенно другим штаммом ЦМВ. Независимо от стадии инфекции, большинство эпизодов ЦМВ-инфекции протекает бессимптомно и не представляет значительной угрозы для здоровья иммунокомпентентных хозяев. Однако инфицирование матери во время беременности может вызвать серьезные и необратимые последствия для плода.Несмотря на потенциально разрушительный характер врожденной инфекции, эффективного лечения не существует.
Однако инфицирование матери во время беременности может вызвать серьезные и необратимые последствия для плода.Несмотря на потенциально разрушительный характер врожденной инфекции, эффективного лечения не существует.
МИКРОБИОЛОГИЯ
Цитомегаловирус — самый крупный представитель семейства вирусов герпеса, которое также включает простой герпес типов 1 и 2, вирус Эпштейна-Барра (ВЭБ) и ветряную оспу. Его геном состоит из 240 килобаз двухцепочечной ДНК, кодирующей более 100 белков. 5 Вирус состоит из ядра длиной 64 нм, окруженного икосаэдрическим капсидом размером 110 нм, состоящим из 162 капсомеров.Неплотно нанесенная липидная бислойная оболочка окружает плохо выраженную оболочку, которая, в свою очередь, окружает вирусный капсид. Зрелая вирусная частица с оболочкой имеет диаметр примерно 200 нм. 6 Существует множество антигенно разнообразных штаммов вируса, но перекрестная реактивность является обычным явлением. Геномные исследования с использованием переваривания эндонуклеазами рестрикции показали, что средняя гомология между штаммами составляет 80%; однако известны тысячи различных штаммов. 7 Скрытый ЦМВ был обнаружен в моноцитах, легких, селезенке, почках, секреторных железах, 8 и шейке матки. 9
7 Скрытый ЦМВ был обнаружен в моноцитах, легких, селезенке, почках, секреторных железах, 8 и шейке матки. 9
Трехфазный цикл репликации ЦМВ, ограниченный клетками человека, характеризуется немедленной-ранней, ранней и поздней фазами. 10 Подобно другим вирусам герпеса, каскадный синтез мРНК и белков, коррелированный с тремя фазами цикла (названными α, β, γ, соответственно), тесно контролирует временную экспрессию вирусного генома. 7 , 11 Цикл репликации относительно длинный и требует приблизительно 96 часов для высвобождения потомства вируса из клеток, инфицированных in vitro. Репликация вирусной ДНК происходит в ядре инфицированной клетки, а оболочка приобретается путем прорастания через ядерную мембрану в цитоплазматическую вакуоль. 12
Цитопатология ЦМВ характеризуется увеличением и округлением клеток, базофильным внутриядерным включением и эозинофильным парануклеарным включением, которое часто придает инфицированным клеткам характерный вид «совиного глаза». 12 В дополнение к продуктивной инфекции, которая приводит к высвобождению активных вирусных частиц, ЦМВ может вызвать латентную инфекцию, при которой вирусная ДНК сохраняется в организме хозяина без активной репликации.
12 В дополнение к продуктивной инфекции, которая приводит к высвобождению активных вирусных частиц, ЦМВ может вызвать латентную инфекцию, при которой вирусная ДНК сохраняется в организме хозяина без активной репликации.
Рост вируса в культуре ткани может быть трудным и требует много времени. Фибробласты человека — единственные клетки, в которых CMV надежно растет in vitro, несмотря на тропизм вируса к эпителиальным клеткам in vivo. 2 Характерный цитопатический эффект развивается в течение нескольких часов или недель после инокуляции в зависимости от количества ЦМВ, присутствующего в образце. 13
ИММУНОЛОГИЯ
Контроль репликации CMV хозяином включает как неспецифические, так и специфические защитные механизмы.Индукция естественных клеток-киллеров и индукция интерферона сразу после инфекции ЦМВ, по-видимому, являются наиболее важными аспектами неспецифической защиты хозяина от вируса. Наиболее важные аспекты специфической иммунной защиты против ЦМВ являются клеточными, поскольку функционирующие Т-лимфоциты необходимы для контроля латентного вируса. 14 Гуморальные иммунные ответы на ЦМВ, по-видимому, не являются важной защитой от инфекции. Например, плод может быть инфицирован внутриутробной передачей ЦМВ у женщины, у которой до зачатия присутствовали антитела, а новорожденный может быть инфицирован ЦМВ в грудном молоке, несмотря на наличие пассивно приобретенных материнских антител.Следовательно, наличие антител не следует рассматривать как показатель иммунитета, а скорее как маркер предшествующей инфекции ЦМВ. Хотя специфические антитела не могут предотвратить инфекцию ЦМВ, они, похоже, уменьшают ее патогенность. 7
14 Гуморальные иммунные ответы на ЦМВ, по-видимому, не являются важной защитой от инфекции. Например, плод может быть инфицирован внутриутробной передачей ЦМВ у женщины, у которой до зачатия присутствовали антитела, а новорожденный может быть инфицирован ЦМВ в грудном молоке, несмотря на наличие пассивно приобретенных материнских антител.Следовательно, наличие антител не следует рассматривать как показатель иммунитета, а скорее как маркер предшествующей инфекции ЦМВ. Хотя специфические антитела не могут предотвратить инфекцию ЦМВ, они, похоже, уменьшают ее патогенность. 7
ПЕРЕДАЧА
Сохранение большого резервуара ЦМВ в человеческих популяциях в отсутствие каких-либо известных нечеловеческих переносчиков представляет собой чрезвычайно успешную форму паразитизма. Этот успех объясняется длительным постоянным выделением вируса после первичной инфекции, множеством мест выделения вируса, периодической реактивацией и выделением вируса, а также относительно вялотекущим течением инфекции, что позволяет иммунокомпетентному хозяину бесконечно жить с вирусом. Прямая или косвенная горизонтальная передача происходит в основном при контакте со слюной, мочой, цервикальными или вагинальными выделениями, спермой, грудным молоком или кровью. 15 , 16 , 17
Прямая или косвенная горизонтальная передача происходит в основном при контакте со слюной, мочой, цервикальными или вагинальными выделениями, спермой, грудным молоком или кровью. 15 , 16 , 17
Для передачи вируса обычно требуется тесный или интимный контакт между людьми. Соответственно, передача ЦМВ половым путем, грудное вскармливание и уход за детьми в дневное время были причастны к распространению ЦМВ. Серопозитивность выше среди лиц, имеющих несколько половых партнеров и имеющих в анамнезе заболевания, передающиеся половым путем. 18 Грудное вскармливание — потенциальный источник передачи новорожденному, поскольку серопозитивные женщины могут секретировать вирус с грудным молоком. 19 Детские сады способствуют распространению ЦМВ, способствуя тесному контакту с детьми, многие из которых выделяют вирус. 20 , 21 , 22 В частности, дети раннего возраста являются ключевым источником инфекции. Адлер и соавторы 23 обнаружили, что от 20% до 40% детей ясельного возраста, посещающих детские сады, выделяют цитомегаловирус.Горизонтальная передача ЦМВ от ребенка к ребенку происходит путем передачи вируса через слюну на руки и игрушки. 24 , 25
Адлер и соавторы 23 обнаружили, что от 20% до 40% детей ясельного возраста, посещающих детские сады, выделяют цитомегаловирус.Горизонтальная передача ЦМВ от ребенка к ребенку происходит путем передачи вируса через слюну на руки и игрушки. 24 , 25
Перинатальная передача ЦМВ происходит через несколько механизмов. Трансплацентарный перенос вируса внутриутробно и воздействие на плод ЦМВ, секретируемого во влагалище во время прохождения через родовые пути во время родов, являются основными способами вертикальной передачи. В послеродовой период инфекция может передаваться через грудное молоко или при прямом контакте человека с человеком. 26 В отличие от in utero (врожденная) инфекция, перинатальная инфекция (во время родов или в послеродовом периоде) не наносит серьезного вреда развитию новорожденного, за исключением младенцев с массой тела менее 1500 г. 27
ЭПИДЕМИОЛОГИЯ
Распространенность антител к ЦМВ увеличивается с возрастом, но модели приобретения широко варьируются среди населения в зависимости от географических и социально-экономических факторов. В целом распространенность ЦМВ-инфекции выше в развивающихся странах и среди стран с низким социально-экономическим статусом.В Соединенных Штатах от 40% до 60% детей с низким социально-экономическим статусом инфицированы к возрасту 5 лет, а к возрасту 20-25 лет от 80% до 100% заразились этой инфекцией. 28 Для сравнения, только от 40% до 60% взрослых из среднего высшего класса являются серопозитивными по отношению к ЦМВ. 29 Инфекция постоянно передается на протяжении всей жизни, так что к возрасту от 60 до 70 лет большинство людей становятся серопозитивными по ЦМВ независимо от социально-экономического статуса. 28
В целом распространенность ЦМВ-инфекции выше в развивающихся странах и среди стран с низким социально-экономическим статусом.В Соединенных Штатах от 40% до 60% детей с низким социально-экономическим статусом инфицированы к возрасту 5 лет, а к возрасту 20-25 лет от 80% до 100% заразились этой инфекцией. 28 Для сравнения, только от 40% до 60% взрослых из среднего высшего класса являются серопозитивными по отношению к ЦМВ. 29 Инфекция постоянно передается на протяжении всей жизни, так что к возрасту от 60 до 70 лет большинство людей становятся серопозитивными по ЦМВ независимо от социально-экономического статуса. 28
Процент серологически восприимчивых женщин репродуктивного возраста также варьируется в зависимости от географии и социально-экономического статуса, с более низкими показателями восприимчивости в Швеции и более высокими показателями в Соединенном Королевстве и Соединенных Штатах.В среднем уровни восприимчивости колеблются от 28% до 48% среди населения развитых стран со средним уровнем дохода. 30 , 31 , 32 , 33 , 34 Серопозитивность матери также коррелировала с множественной беременностью, старшим возрастом, первой беременностью до 15 лет и большим общим числом сексуальных партнеров. 18 Проспективные исследования женщин в Соединенных Штатах показывают, что частота приобретения ЦМВ у женщин детородного возраста со средним и высоким социально-экономическим статусом составляет примерно 2% в год по сравнению с 6% среди женщин с низким социально-экономическим положением. 35 Поскольку самый высокий уровень сероконверсии происходит в возрасте от 15 до 35 лет и значительная часть репродуктивного населения подвержена этому заболеванию, вероятность того, что первичная инфекция совпадает с беременностью, относительно высока. 36
30 , 31 , 32 , 33 , 34 Серопозитивность матери также коррелировала с множественной беременностью, старшим возрастом, первой беременностью до 15 лет и большим общим числом сексуальных партнеров. 18 Проспективные исследования женщин в Соединенных Штатах показывают, что частота приобретения ЦМВ у женщин детородного возраста со средним и высоким социально-экономическим статусом составляет примерно 2% в год по сравнению с 6% среди женщин с низким социально-экономическим положением. 35 Поскольку самый высокий уровень сероконверсии происходит в возрасте от 15 до 35 лет и значительная часть репродуктивного населения подвержена этому заболеванию, вероятность того, что первичная инфекция совпадает с беременностью, относительно высока. 36
Исследования приобретения ЦМВ во время беременности в таких разных регионах, как Техас, Алабама, Великобритания и Швеция, дали аналогичные показатели от 0,7% до 3,7% для пренатальной первичной инфекции среди восприимчивых женщин.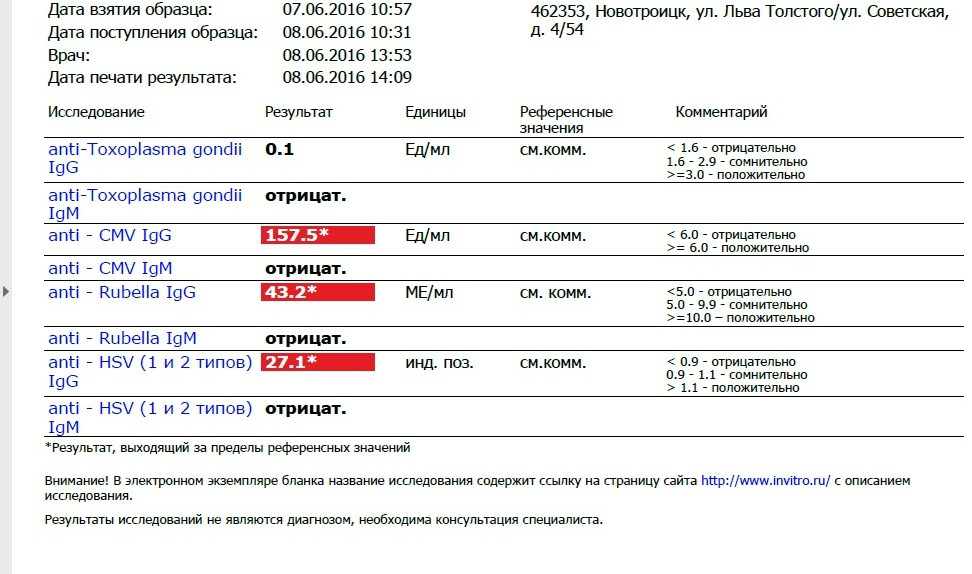 29 Факторы риска сероконверсии во время беременности включают молодой материнский возраст, наличие маленьких детей дома, 37 наличие дома детей в возрасте от 12 до 18 лет, 29 и представители небелой расы. 38
29 Факторы риска сероконверсии во время беременности включают молодой материнский возраст, наличие маленьких детей дома, 37 наличие дома детей в возрасте от 12 до 18 лет, 29 и представители небелой расы. 38
Особую озабоченность вызывает риск для серонегативных матерей, имеющих детей в дневных стационарах, а также для серонегативных работников дневных стационаров, которые забеременели, поскольку в детских учреждениях были зарегистрированы высокие уровни передачи ЦМВ. 39 Исследования показали, что родители детей, находящихся в дневном уходе, более склонны к сероконверсии, чем родители, чьи дети не находятся в дневном уходе. 23 , 40 Адлер и его коллеги 41 обнаружили, что 30% матерей малышей, инфицированных в дневных учреждениях, заразились сами в течение 1 года по сравнению с только 3% матерей неинфицированных малышей.Следовательно, наличие детей младше 3 лет с ЦМВ-инфекциями, приобретенными в дневном стационаре, является важным фактором риска материнского заражения ЦМВ. Работники дневного ухода также подвергаются повышенному риску заражения ЦМВ. Адлер и его коллеги 42 сообщили о ежегодном уровне сероконверсии в 11% для работников дневного ухода по сравнению с 2,2% для сотрудников больниц, соответствующих возрасту, расе и семейному положению. Для женщин, работающих с детьми младше 3 лет, риск первичного инфицирования увеличивается до 30% в год. 39
Работники дневного ухода также подвергаются повышенному риску заражения ЦМВ. Адлер и его коллеги 42 сообщили о ежегодном уровне сероконверсии в 11% для работников дневного ухода по сравнению с 2,2% для сотрудников больниц, соответствующих возрасту, расе и семейному положению. Для женщин, работающих с детьми младше 3 лет, риск первичного инфицирования увеличивается до 30% в год. 39
Больничные работники, контактирующие с новорожденными, детьми или пациентами с ослабленным иммунитетом, также могут подвергаться повышенному риску первичной ЦМВ-инфекции. Хотя несколько исследований выявили тенденции к более высокому уровню сероконверсии среди медицинских работников, контактирующих с пациентами из группы высокого риска, четкой взаимосвязи не установлено. Yeager 43 задокументировал уровень сероконверсии 4,1% и 7,7% в год для неонатальных медсестер и педиатрических медсестер, соответственно, по сравнению с 0% для сотрудников вне больниц.Точно так же Фридман и его коллеги 44 обнаружили, что уровень сероконверсии среди персонала педиатрической больницы выше среди сотрудников, контактировавших с пациентом, по сравнению с теми, кто не контактировал с пациентом. Однако в двух других когортных исследованиях не удалось выявить существенно различающихся показателей сероконверсии среди неонатальных медсестер, других медицинских работников и беременных женщин в сообществе. 45 , 46 Учитывая совокупность данных, педиатрический уход или уход за трансплантологами не обязательно следует рассматривать как профессиональный риск ЦМВ-инфекции.
Однако в двух других когортных исследованиях не удалось выявить существенно различающихся показателей сероконверсии среди неонатальных медсестер, других медицинских работников и беременных женщин в сообществе. 45 , 46 Учитывая совокупность данных, педиатрический уход или уход за трансплантологами не обязательно следует рассматривать как профессиональный риск ЦМВ-инфекции.
Частота и тяжесть инфекции плода варьируется в зависимости от того, перенесла ли мать первичную или рецидивирующую инфекцию ЦМВ во время беременности. На рисунке 1 представлена блок-схема, которая подчеркивает более высокую частоту атак, более высокий уровень симптоматической врожденной инфекции и худший прогноз врожденной инфекции у младенцев, подвергшихся первичной инфекции, по сравнению с рецидивирующей материнской инфекцией. Приблизительно от 1% до 4% серонегативных беременных женщин заражаются первичной ЦМВ-инфекцией во время беременности. 29 Частота инфицирования плода после первичной материнской инфекции составляет от 30% до 50%. 33 , 35 При рождении у 10% этих врожденно инфицированных младенцев проявляются признаки инклюзии ЦМВ (CID). Остальные 90% этих врожденно инфицированных младенцев не имеют симптомов при рождении; однако даже от 10% до 15% тех, у кого нет симптомов при рождении, имеют долгосрочные последствия. 3 , 47
33 , 35 При рождении у 10% этих врожденно инфицированных младенцев проявляются признаки инклюзии ЦМВ (CID). Остальные 90% этих врожденно инфицированных младенцев не имеют симптомов при рождении; однако даже от 10% до 15% тех, у кого нет симптомов при рождении, имеют долгосрочные последствия. 3 , 47
Рис. 1. Эпидемиология цитомегаловирусной инфекции.* Относится к статусу при рождении. СЭС, социально-экономический статус. |
Напротив, рецидивирующая материнская инфекция во время беременности, встречающаяся с частотой от 1% до 14% среди серопозитивных женщин, встречается чаще, чем материнская первичная инфекция во время беременности. Однако, в отличие от первичной материнской инфекции, только от 0,2% до 2% рецидивирующих инфекций вызывают врожденную инфекцию, и неонатальные последствия этих врожденных инфекций имеют тенденцию быть менее серьезными. Более 99% младенцев, врожденно инфицированных после рецидива материнской болезни, не имеют симптомов при рождении.Бессимптомные новорожденные могут по-прежнему испытывать долгосрочные последствия, но с меньшей частотой (от 5% до 10%), чем новорожденные, инфицированные врожденно во время первичной материнской инфекции. 3
Более 99% младенцев, врожденно инфицированных после рецидива материнской болезни, не имеют симптомов при рождении.Бессимптомные новорожденные могут по-прежнему испытывать долгосрочные последствия, но с меньшей частотой (от 5% до 10%), чем новорожденные, инфицированные врожденно во время первичной материнской инфекции. 3
МАТЕРИНСКАЯ ИНФЕКЦИЯ
Симптомы и признаки
Для большинства иммунокомпенсированных взрослых первичная или рецидивирующая инфекция ЦМВ протекает бессимптомно и проходит самостоятельно. Люди с симптомами могут иметь заболевание, похожее на мононуклеоз, подобное тому, которое вызывается ВЭБ. Болезнь длится от нескольких дней до недель и характеризуется лихорадкой, сильной усталостью, миалгией, легким фарингитом, кашлем, тошнотой, диареей и головной болью.Повышение температуры тела до 39–40 ° C не является редкостью и может длиться более 2 недель. Усталость и недомогание могут сохраняться в течение 4 недель и дольше. 12 При физикальном обследовании выявляется шейная или генерализованная лимфаденопатия. Редко может развиться гепатомегалия, спленомегалия или сыпь. Желтуха встречается редко. Ферменты печени слегка повышены у 90% пациентов с мононуклеозом ЦМВ и могут оставаться ненормальными в течение нескольких месяцев. Во время беременности лабораторные отклонения, указывающие на острую инфекцию, включают лимфопению или лимфоцитоз, связанные с атипичными лимфоцитами, и тромбоцитопению. 26
Редко может развиться гепатомегалия, спленомегалия или сыпь. Желтуха встречается редко. Ферменты печени слегка повышены у 90% пациентов с мононуклеозом ЦМВ и могут оставаться ненормальными в течение нескольких месяцев. Во время беременности лабораторные отклонения, указывающие на острую инфекцию, включают лимфопению или лимфоцитоз, связанные с атипичными лимфоцитами, и тромбоцитопению. 26
Дифференциальный диагноз мононуклеоза ЦМВ включает мононуклеоз ВЭБ, инфекцию, вызванную вирусом первичного иммунодефицита человека, и инфекцию токсоплазмоза. ЦМВ-гепатит необходимо дифференцировать от гепатита, вызываемого вирусом гепатита А, В или С. Мононуклеоз, вызванный ЦМВ, с меньшей вероятностью вызывает тяжелый фарингит, тонзиллит или значительную спленомегалию, и он не производит гетерофильных антител по сравнению с мононуклеозом, индуцированным ВЭБ. 48
Лабораторная диагностика
Преимущества и ограничения лабораторных тестов, используемых для диагностики ЦМВ, представлены в таблице 1. Лабораторные исследования являются полезным дополнением к клиническим данным, но, к сожалению, не позволяют однозначно отличить первичную инфекцию от рецидивирующей. Лабораторная диагностика ЦМВ-инфекции основана на серологических доказательствах инфекции и прямой идентификации ЦМВ. Различение первичного ЦМВ от рецидивирующего основано на материнских CMV-специфических серологических исследованиях, поскольку выделение вируса из мочи, горла или генитальных выделений может происходить как при первичном, так и при рецидивирующем заболевании. Определение роли ЦМВ в клинических условиях сложно, потому что многие взрослые люди, у которых в анамнезе не было симптоматических заболеваний, являются серопозитивными по ЦМВ-иммуноглобулину G (IgG), а периодическое выделение ЦМВ может происходить в течение многих лет после первичной инфекции и не иметь никакого отношения к болезни. .Ни наличие антител IgG, ни выделение вируса не определяют недавнюю инфекцию. Таким образом, для постановки точного диагноза необходима комбинация лабораторных тестов, интерпретируемых в клиническом контексте.
Лабораторные исследования являются полезным дополнением к клиническим данным, но, к сожалению, не позволяют однозначно отличить первичную инфекцию от рецидивирующей. Лабораторная диагностика ЦМВ-инфекции основана на серологических доказательствах инфекции и прямой идентификации ЦМВ. Различение первичного ЦМВ от рецидивирующего основано на материнских CMV-специфических серологических исследованиях, поскольку выделение вируса из мочи, горла или генитальных выделений может происходить как при первичном, так и при рецидивирующем заболевании. Определение роли ЦМВ в клинических условиях сложно, потому что многие взрослые люди, у которых в анамнезе не было симптоматических заболеваний, являются серопозитивными по ЦМВ-иммуноглобулину G (IgG), а периодическое выделение ЦМВ может происходить в течение многих лет после первичной инфекции и не иметь никакого отношения к болезни. .Ни наличие антител IgG, ни выделение вируса не определяют недавнюю инфекцию. Таким образом, для постановки точного диагноза необходима комбинация лабораторных тестов, интерпретируемых в клиническом контексте.
ТАБЛИЦА 1. Тесты, используемые для выявления инфекции ЦМВ *
Тест | Образцы | |||||||
Обнаружение антигена | ||||||||
Вирусная культура | 0002 Результаты анализа мочи | Моча | ||||||
Кровь | Вирус для дальнейшего изучения | |||||||
023 | 3 | 03 | Амниотическая жидкость | |||||
Прямая иммунофлуоресценция | Моча | Требуется быстрое обнаружение вируса (48 ч. | ||||||
Кровь | ||||||||
Амниотическая жидкость | 62902 | Быстрое обнаружение вируса | Дорого | |||||
Кровь | Количественное определение вирусной нагрузки 26 0 | из-за ложного заражения | ||||||
CSF | Типирование штамма вируса | |||||||
Амниотическая жидкость | ||||||||
IgG | Сыворотка | Демонстрация предыдущей инфекции | Требуется 2–50002 Сероконверсия | Демонстрация недавней инфекции путем сероконверсии | ||||
IgM | Сыворотка | острая инфекция | 3 острая инфекция | 3 или до 2 лет после острой инфекции | ||||
Редкая перекрестная реактивность с EBV | ||||||||
6 Фиксация | Демонстрация возрастающего титра | Как указано выше для серологии | ||||||
ЦМВ, цитомегаловирус; ЦСЖ, спинномозговая жидкость; IgG, иммуноглобулин G; IgM, иммуноглобулин M; EBV, вирус Эпштейна-Барра
(адаптировано из Rawlinson WD: Diagnosis of human cytomegalovirus инфекция и болезнь.Патология 31: 110, 1999.)
Ранее повышение титра анти-ЦМВ-антител за счет фиксации комплемента использовалось для диагностики первичной ЦМВ-инфекции. Однако более эффективный и точный иммуноферментный анализ (ELISA) заменил тест связывания комплемента. Серологический диагноз основывается на идентификации образцов иммуноглобулина M (IgM) и IgG, соответствующих первичной инфекции. Присутствие IgM, первоначального ответа антител на инфекцию, свидетельствует о первичной инфекции, но его следует интерпретировать с осторожностью, поскольку IgM к ЦМВ могут быть обнаружены в течение 2 лет у 5% людей после первичного инфицирования.Реинфекция и реактивация вируса связаны с положительным IgM и / или повышением титра связывающих комплемент антител примерно в 30% случаев. Иногда биологические ложноположительные результаты могут возникать из-за перекрестной реактивности с антителами, связанными с ВЭБ или аутоиммунными заболеваниями. 49 В среднем обнаружение CMV-специфических антител IgM с помощью ELISA имеет чувствительность только 75% для первичной инфекции. Это оставляет 25% женщин с первичной ЦМВ без определяемых уровней IgM и ложноотрицательного результата. 50
Демонстрация сероконверсии антител IgG или четырехкратного увеличения титра антител CMV-IgG в образцах, собранных с интервалом от 2 до 4 недель и протестированных одновременно, часто считается золотым стандартом для диагностики первичной инфекции CMV, но, как и определения IgM , не всегда точен. В некоторых случаях повышение титра антител может быть отложено до 4 недель с момента острого заболевания. 51
Тесты на авидность могут использоваться в качестве дополнения к ИФА. Антитела IgG с низкой авидностью вырабатываются на ранней стадии инфекции и могут использоваться в качестве еще одного маркера недавней первичной инфекции.Соответствие между антителами IgG хозяина и целевыми антигенами улучшается по мере того, как хозяин реагирует на патоген. Эта характеристика использовалась для определения возраста острой инфекции с использованием индекса авидности (AI). 52 AI менее 30% с большой вероятностью указывает на недавнюю первичную инфекцию (менее 3 месяцев). ИИ от 30% до 50%, возможно, связан с недавней инфекцией, а ИИ более 50% несовместим с недавней первичной инфекцией. 53 Тесты авидности обычно используются в качестве дополнения к ELISA, потому что они технически сложнее выполнять и трудоемки. 54
Диагностика рецидивирующей ЦМВ-инфекции зависит от выделения вируса из мочи, слюны или шейки матки, а не от серологических методов, поскольку уровни антител обычно не меняются у иммунокомпентентного хозяина. Прямое обнаружение вируса осуществляется путем культивирования вируса, амплификации нуклеиновой кислоты, прямого флуоресцентного теста на антитела и, в редких случаях, путем обнаружения антигена pp65 в крови. 49
Посев вирусов можно проводить на моче, лейкоцитной пленке периферических клеток, образцах бронхоальвеолярного лаважа, носоглоточных аспиратах, промываниях горла, сперме, цервикальном и вагинальном секрете, кале, слезах, околоплодных водах и грудном молоке.Образцы для культивирования следует инокулировать в клетки как можно скорее после сбора, предпочтительно в течение 4 часов. Образцы, взятые в нерабочее время, или образцы, отправленные в другие лаборатории для культивирования, можно хранить при 4 ° C до 1 недели, но при этом урожайность будет снижена. Через 10–14 дней после инокуляции в инфицированных клетках наблюдается цитопатический эффект, хотя для получения отрицательного результата требуется инкубация от 21 до 28 дней. К сожалению, вирусный посев — сложный, дорогой и трудоемкий процесс, требующий до 4 недель для получения окончательных результатов.Продолжительность времени, необходимого для диагностики посевом, может повлиять на принятие клинического решения, особенно в случае беременности.
Прямое определение флуоресцентных антител обеспечивает более быстрое обнаружение ЦМВ. Этот метод основан на ограниченной культуре вируса, но вирусные антигены могут быть обнаружены на поверхности клеток в течение 48 часов. 55 Вирус центрифугируют на монослоях клеточных культур, хранящихся в небольших пузырьках-оболочках под покровными стеклами, и инкубируют в течение 24-48 часов.Добавляют пул моноклональных антител к немедленным ранним и ранним антигенам и вторичное антитело, конъюгированное с флуоресцеином, и очаги инфекции идентифицируют с помощью флуоресцентного микроскопа. 56 По сравнению с вирусной культурой этот метод имеет чувствительность от 80% до 90% и специфичность от 95% до 100%.
Амплификация нуклеиновых кислот с помощью полимеразной цепной реакции (ПЦР) — новейший и наиболее многообещающий быстрый метод обнаружения вирусов. Для этого метода требуются специфические праймеры, комплементарные последовательностям ДНК по обе стороны от целевого сегмента ДНК ЦМВ.Одна копия гена может быть увеличена до 1 миллиона раз. 57 ПЦР имеет чувствительность от 80% до 100% по сравнению с культурой; однако такая высокая чувствительность может привести к ложноположительным результатам, основанным на усилении посторонних вирусных контаминантов или дефектных неинфекционных вирусных частиц. ПЦР также может использоваться для количественного определения уровня вируса. 49
Таким образом, первичную и рецидивирующую ЦМВ-инфекцию можно отличить только с помощью серологических исследований. Сероконверсия CMV-специфических антител IgG с отрицательных на положительные является признаком первичной инфекции, но, к сожалению, образцы для предварительной инфекции редко доступны в рутинной клинической практике.Антитела IgG к CMV могут указывать на перенесенную или текущую инфекцию, и один высокий титр не помогает определить разницу. Повышение титра от низкого до очень высокого в двух образцах сыворотки, полученных с интервалом в 2–3 недели, свидетельствует о недавней первичной инфекции, но не является диагностическим, поскольку рецидивирующая инфекция также может повысить титр антител. Присутствие антител CMV-IgM предполагает недавнюю первичную инфекцию CMV, 58 , но, опять же, результаты следует интерпретировать с осторожностью, поскольку антитела IgM могут сохраняться от 10 до 12 недель или дольше после первичной инфекции. 59
ВРОЖДЕННАЯ ИНФЕКЦИЯ
Врожденная ЦМВ-инфекция происходит гематогенным путем в плаценту с последующим инфицированием плаценты и последующим инфицированием плода. Передача может произойти в любое время во время беременности. Влияние срока беременности на момент заражения матери ЦМВ-инфекцией не так очевидно, как в случае других врожденных инфекций. Однако наихудшие последствия для плода были связаны с инфекцией в первом триместре, 26 , 48 , а клинически значимые нарушения чаще связаны с первичной инфекцией до 27 недель беременности. 35 Младенцы, рожденные от матерей, инфицированных на ранних сроках беременности, также с большей вероятностью будут маленькими для гестационного возраста и будут иметь микроцефалию и внутричерепные кальцификации, тогда как дети, рожденные от матерей, инфицированных на более поздних сроках беременности, с большей вероятностью будут иметь гепатит, пневмонию, пурпуру и тяжелая тромбоцитопения. 60 Как отмечалось ранее, первичная материнская инфекция с большей вероятностью приведет к внутриутробной передаче, чем к повторной инфекции.
Пренатальная диагностика
Несмотря на частое возникновение первичной материнской ЦМВ-инфекции и значительный риск осложнений для потомков инфицированных матерей, рутинный пренатальный скрининг матери не поддерживается, поскольку недоступен надежный и простой метод диагностики внутриутробной инфекции плода.К сожалению, пациенты часто должны принимать решения относительно ведения беременности, основываясь только на эмпирических цифрах риска.
Поскольку большинство первичных и рецидивирующих инфекций протекают бессимптомно, диагноз ЦМВ-инфекции во время беременности часто упускается. Подозрение на материнскую инфекцию должно быть подтверждено соответствующими серологическими тестами, поскольку определение первичной или рецидивирующей инфекции имеет решающее значение для прогнозирования неонатального прогноза. Сероконверсию или повышение титров IgG или IgM часто бывает трудно показать, так как большинство женщин не знают своего серологического статуса по ЦМВ до беременности.Парные образцы, взятые с интервалом от 1 до 4 недель, могут показывать возрастающие титры, но время, необходимое для этого диагностического теста, не позволяет быстро принять клиническое решение. Тест на авидность IgG может помочь в диагностике первичного ЦМВ, но эти тесты обычно доступны только в исследовательских лабораториях.
Прямой диагноз инфекции плода затруднен, и нет единого мнения относительно золотого стандарта диагностики. Клиническая оценка лежит в основе точного диагноза. Объединение материнских симптомов, результатов физикального обследования и серологических исследований вместе с результатами посева околоплодных вод и / или результатов ПЦР, определения IgM плода и результатов УЗИ составляет основу пренатальной диагностики.К сожалению, окончательный диагноз плода зачастую можно поставить только при вскрытии или родах.
ИЗОЛЯЦИЯ ЦИТОМЕГАЛОВИРУСА ИЗ АМНИОТИЧЕСКОЙ ЖИДКОСТИ.
Первый пренатальный диагноз ЦМВ-инфекции у плода был поставлен в 1971 году путем выделения вируса из околоплодных вод. 61 Поскольку эпителий почечных канальцев является основным местом репликации вируса, инфицированный плод предположительно выделяет ЦМВ в околоплодные воды с мочой плода. 62 Исследования документально подтвердили полезность посева околоплодных вод для выявления инфекции плода, и многие считают, что посев околоплодных вод является оптимальным местом для постановки пренатального диагноза врожденной инфекции. 63 , 64 Тестирование околоплодных вод после 20 недель беременности рекомендуется для уменьшения количества ложноотрицательных результатов посева. Чувствительность посева ЦМВ из околоплодных вод составляет от 80% до 100%, 64 , 65 , 66 , а специфичность близка к 100%. 65 В последнее время ПЦР околоплодных вод была добавлена в качестве быстрого средства обнаружения, но результаты следует интерпретировать с осторожностью из-за возможных ложноположительных результатов.
ХОРИОНСКАЯ ВИЛЛУС ОТБОР ПРОБ.
В качестве варианта диагностики врожденного ЦМВ в первом триместре был предложен забор проб ворсин хориона (CVS). Диагностика ЦМВ-инфекции плода в первом триместре позволит более раннее и безопасное прерывание беременности по желанию пациентки. Поскольку вирус, по-видимому, первоначально заражает плаценту с последующей амплификацией и передачей к плоду, 67 плацентарная ткань теоретически является потенциальным источником для выявления инфекции плода.Однако существуют ограниченные данные о чувствительности и специфичности посева или ПЦР плацентарной ткани или того и другого. Hogge et al. 68 выполнили CVS на четырех из шести беременностей, осложненных первичной материнской ЦМВ-инфекцией. У всех четырех были отрицательные результаты ПЦР, которые были подтверждены при рождении с отрицательными посевами мочи новорожденных. Прежде чем регулярно использовать CVS для диагностики ЦМВ-инфекции в первом триместре, необходимы дополнительные исследования.
КОРДОЦЕНТЕЗ ДЛЯ СЕРОЛОГИИ ПЛОДА.
Иммунная система плода способна к последовательному ответу на определенные антигенные стимулы к 22 неделе беременности, и оценка сыворотки плода на специфические для организма IgM использовалась для диагностики некоторых врожденных инфекций.Однако производство специфических IgM, по-видимому, связано с заражающим организмом. Например, хотя большинство плодов с врожденной инфекцией краснухи продуцируют специфические IgM через 22 недели, 69 только 15% плодов с врожденным токсоплазмозом продуцируют специфические IgM между 24 и 29 неделями. 70 Линч и соавторы 71 обнаружили, что, хотя общие уровни IgM были повышены у инфицированных плодов, взятых на 21 и 23 недели беременности, CMV-специфические IgM присутствовали только у одного из пяти протестированных плодов.Это контрастирует с распространенностью от 50% до 95% среди инфицированных новорожденных 72 и, вероятно, свидетельствует о незрелости иммунной системы плода в этом гестационном возрасте.
Несмотря на вариабельность продукции IgM плода, определение CMV-специфических IgM с помощью ELISA можно попытаться провести на крови плода, полученной с помощью кордоцентеза. Для повышения чувствительности этого анализа и исключения ложноположительных результатов из-за ревматоидного фактора сыворотки должны быть предварительно абсорбированы модифицированным препаратом стафилококкового протеина А. 50 Несколько исследований, проведенных по диагностической полезности фетальных CMV-специфических IgM, дали разные результаты. Hogge и соавторы 68 выполнили кордоцентез вместе с амниоцентезом трем беременным женщинам с первичной материнской ЦМВ-инфекцией. По сравнению с неонатальной культурой все три результата кордоцентеза были неверными с двумя ложноотрицательными и одним ложноположительным на сроке от 22,5 до 25 недель. Напротив, Hohlfeld и соавторы 64 сообщили только о двух ложноотрицательных результатах и ни о каких ложноположительных результатах у 16 обследованных пациентов.Примечательно, что в обеих сериях диагноз был точно поставлен с помощью амниоцентеза, а определение IgM плода не добавило дополнительной информации. Истинная чувствительность и специфичность определения IgM плода неизвестны, но в небольших сериях чувствительность составляла от 69% до 75%. 65 , 73 На основании этих результатов очевидно, что только IgM плода нельзя использовать для исключения или подтверждения врожденной ЦМВ-инфекции.
Хотя определение IgM плода может не добавить полезной диагностической информации, кровь плода, полученная при кордоцентезе, может дать прогностическую информацию, если ее отправить для оценки гематологических и печеночных параметров.Крайняя тромбоцитопения, анемия или повышенные результаты тестов функции печени, зарегистрированные в крови плода, предполагают более тяжелое заболевание; однако остается неизвестным, как эти параметры соотносятся с детскими недостатками. 64
УЗИ.
Часто подозрение на врожденную ЦМВ-инфекцию возникает из-за отклонений от нормы при обычном акушерском УЗИ. Расширение желудочков, микроцефалия, кальцификаты головного мозга и водянка считаются подозрительными на цитомегаловирусную инфекцию. Эта информация получена из серии случаев, в которых оценивались плоды матерей с задокументированной первичной ЦМВ или плоды с отклонениями от нормы при рутинном ультразвуковом обследовании, которые привели к обследованию на врожденную инфекцию.Результаты ультразвукового исследования, связанные с инфекцией ЦМВ, разнообразны и могут со временем меняться у конкретного плода. Например, может исчезнуть асцит, перикардиальный или плевральный выпот; однако это не обязательно означает улучшение прогноза. 62 , 71 Любой плод с признаками необъяснимой водянки должен быть обследован на наличие ЦМВ. 71 Нарушения, такие как расширение желудочков, маловодие, 71 выпот в перикард, 62 водянка и асцит, подтвержденные ультразвуком, были связаны с более тяжелыми синдромами. 64
ОГРАНИЧЕНИЯ ПРЕНАТАЛЬНОЙ ДИАГНОСТИКИ.
Хотя посев околоплодных вод чувствителен, его использование в качестве единственного метода диагностики проблематично. ПЦР, применяемая к образцам околоплодных вод, дополнительно увеличивает чувствительность анализа околоплодных вод и обеспечивает более быструю диагностику. Однако из-за сообщений о ложноотрицательных результатах посева околоплодных вод и ложноположительных результатах ПЦР околоплодных вод сочетание амниоцентеза и взятия пробы крови плода может обеспечить оптимальные средства для диагностики инфекции ЦМВ у плода.
Кордоцентез также обеспечивает анализ крови плода для определения прогноза плода. Гематологические признаки системной инфекции связаны с худшим прогнозом. 74 Аналогичным образом отклонения на УЗИ предполагают плохой прогноз; однако несколько случаев в литературе указывают на то, что системная ЦМВ плода не всегда приводит к тяжелой инвалидности новорожденного. 63 , 75 , 76 Таким образом, консультирование матери относительно возможного плохого прогноза для ее младенца должно быть оформлено соответствующим образом.Дальнейшие исследования необходимы для определения показателей плода, позволяющих прогнозировать тяжелую инвалидность.
Диагностика врожденной инфекции у новорожденных
При рождении у большинства детей, инфицированных ЦМВ, симптомы отсутствуют, и только около 10% имеют признаки ВИД. Клинические признаки CID наиболее часто включают гепатоспленомегалию, микроцефалию, желтуху и петехии. Гепатоспленомегалия вызывается экстрамедуллярным кроветворением и легким гепатитом, который обычно связан с повышенным уровнем ферментов печени и прямой и непрямой гипербилирубинемией.Петехии являются результатом тромбоцитопении и обычно проходят в течение нескольких недель или месяцев. К другим менее частым проявлениям относятся пурпура, пневмония, хориоретинит, церебральные кальцификации, гемолитическая анемия и паховые грыжи у мужчин. 13
Поскольку признаки и симптомы симптоматической ЦМВ-инфекции у новорожденных очень часто совпадают с таковыми при других неонатальных заболеваниях, для окончательного диагноза требуется лабораторное тестирование. Выделение вируса от младенцев в течение первых 3 недель жизни считается доказательством врожденной инфекции и наиболее чувствительным методом диагностики.Обычным местом выделения является моча, но вирус также был выделен из спинномозговой жидкости, слюны, лейкоцитарной пленки и образцов биопсии или ткани аутопсии. 77
Прогноз
Частота и тяжесть последствий у врожденно инфицированных младенцев связаны с наличием или отсутствием симптомов при рождении и стадией (первичной или рецидивирующей) материнской ЦМВ-инфекции во время беременности.
СИМПТОМАТИЧЕСКАЯ И АСИМПТОМАТИЧЕСКАЯ ИНФЕКЦИЯ ПРИ РОЖДЕНИИ.
В таблице 2 представлена частота осложнений у младенцев с симптомами по сравнению с младенцами без симптомов при рождении. Прогноз неблагоприятный для младенцев с CID при рождении. Более чем у 90% младенцев с симптомами наблюдаются серьезные последствия, такие как смерть (5,8%), хориоретинит (20,4%), нейросенсорная потеря слуха (58%) и умственная отсталость (55%). Boppana и соавторы, 78 , основанные на данных, полученных от 106 новорожденных с симптоматической врожденной ЦМВ-инфекцией, подтвердили мультисистемный характер заболевания и связанные с ним заболеваемость и смертность.Клинические и лабораторные отклонения указывали на поражение гептобилиарной, кроветворной и центральной нервной систем у большинства младенцев, обследованных в первый месяц жизни. Более двух третей этих младенцев имели по крайней мере один неонатальный признак заболевания центральной нервной системы (, например, микроцефалия, летаргия / гипотония, плохое сосание, судороги). Было обнаружено, что эти признаки коррелируют с умственной отсталостью у детей школьного возраста. 74
ТАБЛИЦА 2. Последствия у детей после врожденной ЦМВ-инфекции в зависимости от симптомов при рождении * и типа материнской инфекции †
Sequela | Симптоматика% (No.) | Асимптоматическая% (кол-во) | Первичная% (кол-во) | Рецидивирующая% (кол-во) | |
58,0 (58/100) | 7,4 (22/299) | 15,0 (18/120) | 5,0 (3/56) | ||
905 Двусторонняя потеря слуха | 370.0 (37/100) | 2,7 (8/299) | 8,0 (10/120) | 0 (0/56) | |
Порог речи 60 дБ † | 27,0 (27/100) | 1,7 (5/299) | 8,0 (9/120) | 0 (0/56) | |
Хориоретинит | 20,411759 / 93) | 2,5 (7/281) | 13.0 (9/68) | 0 (0/32) | |
IQ <70 | 55,0 (33/60) | 3,7 (6/159) | 6,0 (7/112) | 2,0 (1,54) | |
Микроцефалия, судороги или паралич | 51,9 (54/104) | 6,02,7 (9/330) | 0 (8/125) | 2,0 (1/64) | |
Микроцефалия | 37.5 (39/104) | 1,8 (6/330) | 5,0 (6/125) | 2,0 (1/64) | |
Изъятия | 230002 23 / 104) | 0,9 (3/330) | 5,0 (6/125) | 0 (0/64) | |
Парез / паралич | 104) | 0 (0/330) | 1.0 (1/125) | 0 (0/64) | |
Смерть§ | 5.8 (6/104) | 0,3 (1/330) | 2,0 (3/125) | 0 (0/64) |
IQ, коэффициент интеллекта.
* Данные Stagno S, Whitley RJ: Герпесвирусные инфекции у новорожденных и детей: цитомегаловирус и вирус простого герпеса. В Holmes KK (ed): Заболевания, передаваемые половым путем, p 1197, McGraw Hill, 1999.
† Данные из Fowler KB, Stagno S, Pass RF et al: Исход врожденной цитомегаловирусной инфекции в зависимости от статуса материнских антител.N Engl J Med 326: 665, 1992.
‡ Для ушей с лучшим слухом.
§После периода новорожденности.
Смертность среди младенцев с наиболее тяжелыми заболеваниями может достигать 30%. Смерть в течение первого месяца жизни обычно вызвана заболеванием полиорганной системы, которое вызывает тяжелую печеночную дисфункцию, диссеминированное внутрисосудистое свертывание крови и вторичные инфекции. Среди младенцев, изученных Боппаной и соавторами, 78 12% умерли в течение первых 6 недель жизни. Смерть, наступающая за пределами этого периода, но в течение 1 года жизни, обычно вызывается прогрессирующей печеночной недостаточностью и задержкой развития.Смерть после 1 года жизни обычно наступает из-за недоедания и инфекции среди людей с инфекцией центральной нервной системы и неврологической инвалидностью. 79
Напротив, прогноз относительно хороший для врожденно инфицированных младенцев, у которых при рождении нет симптомов. Только от 5% до 15% детей с бессимптомной врожденной инфекцией имеют долгосрочные последствия, которые становятся очевидными в течение первых 2 лет жизни. Нейросенсорная тугоухость — наиболее частое осложнение у этих младенцев, встречающееся примерно в 7 раз.5% инфицированных младенцев не имеют симптомов при рождении. 80 , 81 , 82 , 83 , 84 Почти в половине случаев поражение является двусторонним и достаточно серьезным, чтобы нарушить вербальное общение и обучение. Другие неврологические осложнения, такие как умственная отсталость, микроцефалия, судороги и паралич, тем не менее встречаются примерно у 2–3% врожденно инфицированных младенцев, у которых при рождении не было симптомов. 85
Таким образом, вероятность того, что младенцы, пережившие симптоматическую врожденную ЦМВ-инфекцию, будут иметь нормальное интеллектуальное развитие и слух, мала. 1 Напротив, прогноз для инфицированных младенцев, у которых нет симптомов при рождении, хороший.
ПЕРВИЧНАЯ И РЕАКЦИОННАЯ МАТЕРИНСКАЯ ИНФЕКЦИЯ.
Большинство младенцев с зарегистрированными последствиями родились от матерей с первичной инфекцией во время беременности. 51 Врожденные ЦМВ-инфекции у детей женщин с иммунитетом, приобретенным до беременности, с меньшей вероятностью будут иметь симптомы при рождении, чем инфекции, возникшие в результате первичной инфекции. 33 , 35
У этих детей также меньше вероятность тяжелых осложнений (см. Рис. 1). Fowler и соавторы 51 сравнили исходы 125 ЦМВ-инфицированных младенцев, рожденных от матерей, заразившихся первичной ЦМВ-инфекцией во время беременности, с 64 ЦМВ-инфицированными младенцами, рожденными от матерей с рецидивирующим заболеванием. Результаты, представленные в таблице 2, показывают, что существующие материнские антитела к ЦМВ защищают плод и уменьшают тяжесть последствий врожденной ЦМВ-инфекции.Дети, инфицированные после первичной материнской инфекции, с большей вероятностью имели функционально важную нейросенсорную тугоухость и имели более высокий коэффициент интеллекта менее 70, чем дети, инфицированные после рецидивирующей материнской инфекции. Дети в первичной группе также были более подвержены серьезным повреждениям, о чем свидетельствует преобладание множественных осложнений (6%) в этой группе по сравнению с таковой в повторной группе (0%).
ВЕДЕНИЕ МАТЕРИНСКИХ / ВРОЖДЕННЫХ ИНФЕКЦИЙ
Консультации
Консультирование женщины с первичной ЦМВ-инфекцией во время беременности является сложной задачей, а рациональный пренатальный протокол оценки состояния плода затруднен из-за капризов диагностических тестов и отсутствия последовательного прогноза для плода. .Рекомендуется подход, основанный на оценке риска. Априори риск тяжелого поражения младенца после первичной ЦМВ-инфекции у матери составляет от 3% до 6%, исходя из 40% вероятности врожденной инфекции, 10-15% вероятности появления у ребенка симптомов при рождении и 90%. % вероятность осложнений у новорожденных с симптомами, как показано на Рисунке 1.
Если диагностическое обследование подтверждает врожденную инфекцию, риск серьезного неврологического повреждения у младенца увеличивается примерно до 10%. И наоборот, у остальных 90% младенцев прогноз отличный.Таким образом, для 60–70% женщин с первичной ЦМВ во время беременности пренатальное тестирование плода дает обнадеживающий отрицательный результат и предотвращает ненужное прерывание беременности. У остальных 30-40% женщин результат будет положительным. In utero прогнозировать, что 10% этих плодов будут серьезно поражены, проблематично. Следует обсудить серийное ультразвуковое обследование и, возможно, кордоцентез на 22 неделе для оценки гематологических или печеночных аномалий у плода в качестве прогностических показателей.Некоторые из этих женщин предпочтут прерывание, не дожидаясь дополнительной информации, предоставленной ультразвуком или кордоцентезом. 68 Если кордоцентез показывает тяжелую тромбоцитопению, следует рассмотреть возможность переливания тромбоцитов наряду с серийным забором крови плода для подтверждения разрешения проблемы. Если тромбоцитопения плода сохраняется, способ родоразрешения может быть изменен. 75
Значение инфекции плода при отсутствии ультразвуковых признаков и аномальных лабораторных показателей остается неясным, но, учитывая высокий процент бессимптомных врожденных ЦМВ-инфекций при рождении, разумно разрешить эти беременности продолжаться под серийным ультразвуковым мониторингом.При рождении все инфицированные младенцы должны проходить тщательное наблюдение, включая серийную оценку слуха и психомоторного развития в течение нескольких лет. 64
Лечение
Не существует известного лечения ЦМВ-инфекции во время беременности. Два антиретровирусных препарата, ганцикловир и фоскарнет, доступны для лечения тяжелых угрожающих жизни или зрению ЦМВ-инфекций у пациентов с ослабленным иммунитетом. Системное лечение ганцикловиром не дало значительного клинического эффекта у врожденно инфицированных младенцев и связано со значительной токсичностью. 86 , 87 , 88 Изменчивый характер врожденного ЦМВ и необратимые повреждения, которые происходят в пренатальном периоде, затрудняют испытания послеродового лечения. Контролируемое клиническое испытание ганцикловира для лечения врожденного ЦМВ продолжается. 79
Вакцина
Младенцы, рожденные от женщин с первичной ЦМВ-инфекцией во время беременности, более склонны к серьезным заболеваниям при рождении, двусторонней потере слуха и умственной отсталости, чем младенцы, рожденные от женщин с рецидивирующей ЦМВ-инфекцией во время беременности . 51 В отличие от первичной ЦМВ-инфекции, лишь небольшой процент женщин с рецидивирующей инфекцией передают ЦМВ своим младенцам, и эти младенцы редко испытывают тяжелые последствия. 33 , 51 Таким образом, вакцинация восприимчивых женщин для предотвращения первичной ЦМВ-инфекции во время беременности может обеспечить защиту от повреждений, вызванных врожденной ЦМВ-инфекцией. 89
Две живые аттенуированные вакцины (штаммы AD-169 и Towne) прошли испытания на эффективность на иммунных и неиммунных здоровых хозяевах и реципиентах почечного трансплантата. 90 , 91 , 92 Среди пациентов с трансплантатом почки, иммунизированных вакциной штамма Таун, заболеваемость, связанная с первичной инфекцией ЦМВ, была снижена, но инфекция не была предотвращена. 93 Более важно, однако, что вирус вакцины не реактивировался у хозяев с ослабленным иммунитетом. Вакцина для предотвращения первичной инфекции среди беременных женщин в идеале не должна вызывать латентный период или повторно активироваться во время беременности. Из-за этого теоретического потенциала использования живых аттенуированных вакцин во время беременности обычно не рекомендуется.
Хотя исследования живого аттенуированного вируса должны продолжаться, более безопасный подход включает субъединичную вакцину, которая вызывает образование антител к белку оболочки вируса. Гилкопротеин gB — это самый распространенный белковый комплекс вирусной оболочки, экспрессирующийся на поверхности инфицированных клеток. Нейтрализующие антитела присутствуют вскоре после заражения и сохраняются во время фазы выздоровления. 94 Ранние испытания на людях в настоящее время продолжаются. 79
Профилактика
В отсутствие подходящей вакцины единственная доступная в настоящее время мера предотвращения ЦМВ-инфекции — это избегать заражения.ЦМВ не очень заразен, и горизонтальная передача требует тесного контакта с инфицированными выделениями или иногда с фомитами. Основными источниками воздействия на женщин детородного возраста являются половые контакты и дети, выделяющие вирус. Исследования поведенческих вмешательств, направленные на улучшение гигиены среди женщин с маленькими детьми, не смогли выявить статистически значимых различий в показателях сероконверсии среди небеременных женщин. Тем не менее, из 14 беременных женщин, прошедших обучение, ни у одной сероконверсии за 9-месячный период наблюдения не было.Это говорит о том, что обучение основным мерам гигиены может снизить вероятность заражения первичной инфекцией среди беременных женщин с маленькими детьми дома. 95 Беременным женщинам также следует рекомендовать избегать тесного контакта с людьми, которые могут выделять ЦМВ, например, взрослыми с симптомами, соответствующими мононуклеозу, и детьми ясельного возраста, посещающими групповые дневные стационары.
Пренатальный скрининг на антитела против ЦМВ остается спорным. Некоторые исследователи рекомендуют обследовать женщин детородного возраста для определения статуса антител.Затем серонегативные женщины могут принять меры предосторожности, чтобы избежать инфекции ЦМВ, например, избегать половых контактов с людьми, которые могут выделять ЦМВ, осторожно мыть руки после контакта с детскими выделениями и избегать использования общей посуды. 95 , 96 , 97 Однако эта рекомендация может оказаться нерентабельной, поскольку эффективность профилактического консультирования окончательно не доказана. 98 В качестве альтернативы всем беременным женщинам можно рекомендовать основные правила гигиены без тестирования на статус антител к ЦМВ.
В настоящее время рутинный скрининг на ЦМВ во время беременности для выявления тех, кто заразился первичной инфекцией во время беременности, не рекомендуется из-за низкой (от 1% до 2%) частоты первичной инфекции ЦМВ во время беременности и относительно низкой (40%) вероятности того, что возникает врожденная инфекция. Кроме того, инвазивный и неопределенный характер тестирования плода, отсутствие окончательных прогностических показателей и отсутствие эффективной противовирусной терапии делают рутинное серологическое тестирование во время беременности ограниченным.
ПОДТВЕРЖДЕНИЕ
Эта работа была поддержана в соответствии с соглашением о сотрудничестве Центров по контролю за заболеваниями через Ассоциацию преподавателей профилактической медицины.
Какие лекарства из класса иммуноглобулина используются для лечения цитомегаловируса (ЦМВ)?
Чжан Л.Дж., Ханфф П., Резерфорд К., Черчилль У.Х., Крампакер С.С. Обнаружение ДНК, РНК и антител цитомегаловируса человека в крови нормального донора. J Заразить Dis . 1995 апр.171 (4): 1002-6. [Медлайн].
Collier AC, Meyers JD, Corey L, Murphy VL, Roberts PL, Handsfield HH. Цитомегаловирусная инфекция у мужчин-гомосексуалистов. Отношение к сексуальной практике, антитела к вирусу иммунодефицита человека и клеточный иммунитет. Am J Med . 1987, 23 марта. 82 (3 Спецификации): 593-601. [Медлайн].
Guinan ME, Thomas PA, Pinsky PF, Goodrich JT, Selik RM, Jaffe HW. Гетеросексуальные и гомосексуальные пациенты с синдромом приобретенного иммунодефицита.Сравнение данных наблюдения, интервью и лабораторных данных. Энн Интерн Мед. . 1984 Февраль 100 (2): 213-8. [Медлайн].
Hodson EM, Jones CA, Webster AC, Strippoli GF, Barclay PG, Kable K. Противовирусные препараты для предотвращения цитомегаловирусной болезни и ранней смерти у реципиентов трансплантации твердых органов: систематический обзор рандомизированных контролируемых испытаний. Ланцет . 2005 18-24 июня. 365 (9477): 2105-15. [Медлайн].
Staras SA, Dollard SC, Radford KW, Flanders WD, Pass RF, Cannon MJ.Распространенность цитомегаловирусной инфекции в США, 1988–1994 гг. Clin Infect Dis . 2006 г. 1. 43 (9): 1143-51. [Медлайн].
Bate SL, Dollard SC, Cannon MJ. Распространенность цитомегаловируса по серологии в Соединенных Штатах: национальные обследования здоровья и питания, 1988-2004 гг. Clin Infect Dis . 1 июня 2010 г. 50 (11): 1439-47. [Медлайн].
Ljungman P, Griffiths P, Paya C. Определения цитомегаловирусной инфекции и болезни у реципиентов трансплантата. Clin Infect Dis . 2002 15 апреля. 34 (8): 1094-7. [Медлайн].
Cunha BA. Цитомегаловирусная пневмония: внебольничная пневмония у иммунокомпетентных хозяев. Инфекция Dis Clin North Am . 2010 марта, 24 (1): 147-58. [Медлайн].
Дейтон Дж. Р., Проф Сабин Калифорния, Джонсон Массачусетс, Эмери В.К., Уилсон П., Гриффитс, Полицейский. Важность цитомегаловирусной виремии в риске прогрессирования заболевания и смерти у ВИЧ-инфицированных пациентов, получающих высокоактивную антиретровирусную терапию. Ланцет . 2004, 26 июня, 363 (9427): 2116-21. [Медлайн].
Stagno S, Pass RF, Cloud G, Britt WJ, Henderson RE, Walton PD. Первичная цитомегаловирусная инфекция при беременности. Заболеваемость, передача плоду и клинический исход. JAMA . 1986, 10 октября. 256 (14): 1904-8. [Медлайн].
Stagno S. Cytomegalovirus. Ремингтон Дж. С., Кляйн Дж. Инфекционные болезни плода и новорожденного . Филадельфия: У. Б. Сондерс; 2001 г.389-424.
Arora N, Novak Z, Fowler KB, Boppana SB, Ross SA. Цитомегаловирусная вирурия и ДНКемия у здоровых серопозитивных женщин. J Заразить Dis . 2010 15 декабря. 202 (12): 1800-3. [Медлайн]. [Полный текст].
Уолтер Э.А., Гринберг П.Д., Гилберт М. Восстановление клеточного иммунитета против цитомегаловируса у реципиентов аллогенного костного мозга путем переноса клонов Т-клеток от донора. N Engl J Med . 1995 19 окт.333 (16): 1038-44. [Медлайн].
Бонковский Х.Л., Ли Р.В., Клацкин Г. Острый гранулематозный гепатит. Возникновение цитомегаловирусного мононуклеоза. JAMA . 1975, 22 сентября. 233 (12): 1284-8. [Медлайн].
Meiselman MS, Cello JP, Margaretten W. Цитомегаловирусный колит. Отчет о клинических, эндоскопических и патологических данных у двух пациентов с синдромом приобретенного иммунодефицита. Гастроэнтерология . 1985, январь, 88 (1, 1): 171-5.[Медлайн].
Орликовский Д., Порчер Р., Сивадон-Тарди В. и др. Синдром Гийена-Барре после первичной цитомегаловирусной инфекции: проспективное когортное исследование. Clin Infect Dis . 2011 Апрель 52 (7): 837-44. [Медлайн].
Джабс Д.А., Ван Натта М.Л., Кемпен Дж. Х., Рид Паван П., Лим Дж. И., Мерфи Р. Л. и др. Характеристика больных цитомегаловирусным ретинитом в эпоху высокоактивной антиретровирусной терапии. Ам Дж. Офтальмол .2002, январь 133 (1): 48-61. [Медлайн].
Karavellas MP, Plummer DJ, Macdonald JC, Torriani FJ, Shufelt CL, Azen SP. Заболеваемость витритом восстановления иммунитета у пациентов с цитомегаловирусным ретинитом после успешного проведения высокоактивной антиретровирусной терапии. J Заразить Dis . 1999, март 179 (3): 697-700. [Медлайн].
Wohl DA, Kendall MA, Owens S, Holland G, Nokta M, Spector SA. Безопасность прекращения поддерживающей терапии цитомегаловирусного (ЦМВ) ретинита и частота иммунного увеита после мощной антиретровирусной терапии. Клинические испытания ВИЧ . 2005 май-июнь. 6 (3): 136-46. [Медлайн].
Райт М.Э., Сузман Д.Л., Чаки К.Г., Мазур Х., Полис М.А., Робинсон MR. Обширная неоваскуляризация сетчатки как поздняя находка у инфицированных вирусом иммунодефицита людей с увеитом иммунного восстановления. Clin Infect Dis . 2003 15 апреля. 36 (8): 1063-6. [Медлайн].
Ричардсон В.П., Колвин РБ, Чизмен Ш. Гломерулопатия, связанная с цитомегаловирусной виремией в почечных аллотрансплантатах. N Engl J Med . 1981, 9 июля. 305 (2): 57-63. [Медлайн].
Torok-Storb B, Boeckh M, Hoy C. Ассоциация конкретных генотипов цитомегаловируса со смертью от миелосупрессии после трансплантации костного мозга. Кровь . 1997 Сентябрь 1. 90 (5): 2097-102. [Медлайн].
Мануэль О., Асберг А., Панг Х, Роллаг Х, Эмери В. К., Прейксайтис Дж. Влияние генетических полиморфизмов гликопротеина В цитомегаловируса на исходы у реципиентов трансплантата солидных органов с цитомегаловирусной болезнью. Clin Infect Dis . 2009 15 октября. 49 (8): 1160-6. [Медлайн].
Ивасенко Дж. М., Ховард Дж., Арбакл С. и др. Цитомегаловирусная инфекция человека часто выявляется у мертворожденных и связана с тромботической васкулопатией плода. J Заразить Dis . 2011 Июнь 203 (11): 1526-33. [Медлайн].
Klemola E, Von Essen R, Henle G, Henle W. Заболевание, подобное инфекционному мононуклеозу, с отрицательным тестом на агглютинацию гетерофилов. Клинические особенности в отношении антител к вирусу Эпштейна-Барра и цитомегаловирусу. J Заразить Dis . 1970 Июнь 121 (6): 608-14. [Медлайн].
Коэн Дж. И., Кори Г. Р.. Цитомегаловирусная инфекция у нормального хозяина. Медицина (Балтимор) . 1985 марта 64 (2): 100-14. [Медлайн].
Horwitz CA, Henle W., Henle G. Клиническая и лабораторная оценка мононуклеоза, вызванного цитомегаловирусом, у ранее здоровых людей. Отчет о 82 случаях. Медицина (Балтимор) . 1986 марта 65 (2): 124-34. [Медлайн].
Klemola E, Stenström R, von Essen R. Пневмония как клиническое проявление цитомегаловирусной инфекции у ранее здоровых взрослых. Scand J Infect Dis . 1972. 4 (1): 7-10. [Медлайн].
Jaber S, Chanques G, Borry J, Souche B, Verdier R, Perrigault PF. Цитомегаловирусная инфекция у тяжелобольных: сопутствующие факторы и последствия. Сундук . 2005 Январь 127 (1): 233-41. [Медлайн].
von Müller L, Klemm A, Weiss M, et al.Активная цитомегаловирусная инфекция у больных септическим шоком. Emerg Infect Dis . 2006 12 октября (10): 1517-22. [Медлайн]. [Полный текст].
Kalil AC, Флореску Д.Ф. Распространенность и смертность, связанные с цитомегаловирусной инфекцией, у пациентов с иммуносупрессией в отделении интенсивной терапии. Crit Care Med . 2009 37 августа (8): 2350-8. [Медлайн].
Cook CH, Yenchar JK, Kraner TO, Davies EA, Ferguson RM. Вирусы семейства оккультных герпесов могут повышать смертность тяжелобольных хирургических пациентов. Am J Surg . 1998 Октябрь 176 (4): 357-60. [Медлайн].
De Vlieger G, Meersseman W, Lagrou K, et al. Серостатус и исходы цитомегаловируса у тяжелобольных пациентов без иммунодефицита. Crit Care Med . 2012 января 40 (1): 36-42. [Медлайн].
Kim JM, Kim SJ, Joh JW и др. Опасна ли цитомегаловирусная инфекция у серопозитивных реципиентов по цитомегаловирусу после трансплантации печени ?. Трансплантация печени .2011 г., 17 (4): 446-55. [Медлайн].
Рубин Р.Х. Косвенное влияние цитомегаловирусной инфекции на исход трансплантации органов. JAMA . 1989 г., 23-30 июня. 261 (24): 3607-9. [Медлайн].
Фишман Ю.А., Рубин Р.Х. Инфекция у реципиентов трансплантата. N Engl J Med . 1998 11 июня. 338 (24): 1741-51. [Медлайн].
Снидман ДР. Инфекция при трансплантации солидных органов. Transpl Infect Dis .1999 Март 1 (1): 21-8. [Медлайн].
Johanssson I, Mårtensson G, Andersson R. Цитомегаловирус и отдаленные результаты после трансплантации легкого в Гетеборге, Швеция. Scand J Infect Dis . 2010. 42 (2): 129-36. [Медлайн].
Reed EC, Bowden RA, Dandliker PS. Лечение цитомегаловирусной пневмонии ганцикловиром и внутривенным цитомегаловирусным иммуноглобулином у пациентов с трансплантатами костного мозга. Энн Интерн Мед. .15 ноября 1988 г. 109 (10): 783-8. [Медлайн].
Eid AJ, Arthurs SK, Deziel PJ, Wilhelm MP, Razonable RR. Клинические предикторы рецидива после лечения первичной цитомегаловирусной болезни желудочно-кишечного тракта у реципиентов трансплантата солидных органов. Трансплантат Am J . 2010 января, 10 (1): 157-61. [Медлайн].
Дитрих Д.Т., Рахмин М. Цитомегаловирусный колит при СПИДе: презентация у 44 пациентов и обзор литературы. Синдр иммунодефицита J Acquir .1991. 4 Прил. 1: С29-35. [Медлайн].
McCutchan JA. Цитомегаловирусные инфекции нервной системы у больных СПИДом. Clin Infect Dis . 1995 г., 20 (4): 747-54. [Медлайн].
Shanahan A, Malani PN, Kaul DR. Рецидивирующая цитомегаловирусная инфекция у реципиентов солидных трансплантатов. Transpl Infect Dis . 2009 Декабрь 11 (6): 513-8. [Медлайн].
Моноклональное антитело к непосредственному раннему антигену против цитомегаловируса (CMV), неконъюгированное, клон 3G9.2 от CHEMICON. www.chemicon.com. Доступно на http://www.bio-medicine.org/biology-products/Anti-Cytomegalovirus—28CMV-29-Immediate-Early-Antigen-Monoclonal-Antibody—Unconjugated—Clone-3G9-2-from-CHEMICON -2132-1 /. Доступ: 17 марта 2010 г.
Мартин-Давила П., Фортун Дж., Гутьеррес С., Марти-Бельда П., Канделас А., Хонрубия А. и др. Анализ количественного ПЦР-анализа на ЦМВ-инфекцию у реципиентов трансплантата печени: цель поиска оптимального порогового значения. Дж. Клин Вирол .2005 июн. 33 (2): 138-44. [Медлайн].
Aitken C, Barrett-Muir W, Millar C, Templeton K, Thomas J, Sheridan F. Использование молекулярных анализов в диагностике и мониторинге цитомегаловирусной болезни после трансплантации почки. Дж. Клин Микробиол . 1999 Сентябрь 37 (9): 2804-7. [Медлайн]. [Полный текст].
Gerna G, Zipeto D, Parea M, Revello MG, Silini E, Percivalle E. Мониторинг цитомегаловирусных инфекций человека и лечение ганцикловиром у реципиентов трансплантата сердца путем определения виремии, антигенемии и ДНКемии. J Заразить Dis . 1991 Сентябрь 164 (3): 488-98. [Медлайн].
Tanabe K, Tokumoto T., Ishikawa N, Koyama I., Takahashi K, Fuchinoue S. Сравнительное исследование анализа антигенемии цитомегаловируса (CMV), полимеразной цепной реакции, серологических исследований и анализа пробирки в оболочке для ранней диагностики и мониторинга инфекции CMV после трансплантация почек. Трансплантация . 1997 Dec 27. 64 (12): 1721-5. [Медлайн].
Боппана С.Б., Росс С.А., Шимамура М., Палмер А.Л., Ахмед А., Майклс М.Г. и др.Полимеразно-цепная реакция слюны для скрининга на цитомегаловирус у новорожденных. N Engl J Med . 2 июня 2011 г. 364 (22): 2111-8. [Медлайн]. [Полный текст].
Sanghavi SK, Abu-Elmagd K, Keightley MC, St George K, Lewandowski K, Boes SS. Связь цитомегаловирусной нагрузки, оцененной с помощью ПЦР в реальном времени, с антигенемией pp65 у реципиентов трансплантата. Дж. Клин Вирол . 2008 г., 42 (4): 335-42. [Медлайн].
Джабс Д.А., Мартин Б.К., Форман М.С., Рикс МО.Цитомегаловирусная (ЦМВ) нагрузка ДНК в крови, прогрессирование ЦМВ ретинита и возникновение резистентного ЦМВ у пациентов с ЦМВ ретинитом. J Заразить Dis . 2005 15 августа. 192 (4): 640-9. [Медлайн].
Рош Молекулярная диагностика. Тест COBAS AMPLICOR CMV MONITOR. Доступно по адресу http://molecular.roche.com/assays/Pages/COBASAMPLICORCMVMONITORTest.aspx. Доступ: 10 июля 2012 г.
Рош Молекулярная диагностика. Тест COBAS AmpliPrep / COBAS TaqMan CMV.Доступно по адресу http://molecular.roche.com/assays/Pages/COBASAmpliPrepCOBASTaqManCMVTest.aspx. Доступ: 10 июля 2012 г.
Smith TF, Espy MJ, Mandrekar J, Jones MF, Cockerill FR, Patel R. Количественная полимеразная цепная реакция в реальном времени для оценки ДНКемии, вызванной цитомегаловирусом, вирусом Эпштейна-Барра и вирусом BK у реципиентов трансплантата твердых органов. Clin Infect Dis . 2007 15 октября. 45 (8): 1056-61. [Медлайн].
Дрю В.Л. Тестирование на устойчивость к цитомегаловирусу: подводные камни и проблемы для клинициста. Clin Infect Dis . 2010 мар. 1. 50 (5): 733-6. [Медлайн].
Дрю В.Л., Майнер Р., Салех Э. Тестирование чувствительности цитомегаловируса к противовирусным препаратам: критерии определения устойчивости к противовирусным препаратам. Клин Диагн Вирол . 1993 августа, 1 (3): 179-85. [Медлайн].
Lischka P, Hewlett G, Wunberg T., Baumeister J, Paulsen D, Goldner T, et al. Активность нового антицитомегаловирусного соединения AIC246 in vitro и in vivo. Противомикробные агенты Chemother .2010 марта 54 (3): 1290-7. [Медлайн].
Melendez DP, Razonable RR. Летермовир и ингибиторы комплекса терминаз: новый многообещающий класс исследуемых противовирусных препаратов против цитомегаловируса человека. Устойчивость к лекарствам от инфекций . 2015 5 августа, 8: 269-77. [Медлайн].
Bodro M, Sabé N, Lladó L, et al. Профилактика по сравнению с превентивной терапией цитомегаловирусной болезни у реципиентов трансплантата печени с высоким риском. Трансплантация печени .2012 сентября 18 (9): 1093-9. [Медлайн].
Witzke O, Hauser IA, Bartels M, Wolf G, Wolters H, Nitschke M. Профилактика валганцикловиром по сравнению с превентивной терапией у реципиентов почечного аллотрансплантата с положительной реакцией на цитомегаловирус: результаты одного года рандомизированного клинического исследования. Трансплантация . 2012 15 января. 93 (1): 61-8. [Медлайн].
Фишман Дж. А., Эмери В., Фриман Р., Паскуаль М., Ростаинг Л., Шлитт Х. Дж. Цитомегаловирус при трансплантации — бросая вызов статус-кво. Клиническая трансплантация . 2007 март-апрель. 21 (2): 149-58. [Медлайн].
Legendre C, Pascual M. Улучшение исходов для реципиентов солидных трансплантатов, подверженных риску цитомегаловирусной инфекции: болезнь с поздним началом и косвенные последствия. Clin Infect Dis . 2008 г. 1. 46 (5): 732-40. [Медлайн].
Авторы не указаны. Валганцикловир: новый препарат. ЦМВ-ретинит: более простое пероральное лечение. Прескрир Инт . 2003 Август.12 (66): 133-5. [Медлайн].
Caldés A, Gil-Vernet S, Armendariz Y, Colom H, Pou L, Niubó J, et al. Последовательное лечение цитомегаловирусной инфекции или заболевания коротким курсом внутривенного введения ганцикловира с последующим пероральным приемом валганцикловира: эффективность, безопасность и фармакокинетика. Transpl Infect Dis . 9 декабря 2009 г. [Medline].
Dieterich DT, Chachoua A, Lafleur F. Лечение ганцикловиром желудочно-кишечных инфекций, вызванных цитомегаловирусом, у пациентов со СПИДом. Ред. Заразить Dis . 1988 июль-август. 10 Приложение 3: S532-7. [Медлайн].
Kalil AC, Mindru C, Florescu DF. Эффективность валганцикловира 900 мг по сравнению с 450 мг для профилактики цитомегаловируса при трансплантации: метаанализ прямого и непрямого сравнения лечения. Clin Infect Dis . 2011 Февраль 52 (3): 313-21. [Медлайн].
Эйвери РК. Валганцикловир в низких дозах для профилактики цитомегаловируса при трансплантации органов: меньше действительно больше ?. Clin Infect Dis . 2011 Февраль 52 (3): 322-4. [Медлайн].
Цитомегаловирус. Трансплантат Am J . 4 ноября 2004 г., Дополнение 10: 51-8. [Медлайн].
Паудис Н., Мехметай А., Дзанацци М., Москарелли Л., Пиперно Р., Ди Мария Л. Превентивная терапия для профилактики цитомегаловирусной болезни у реципиентов почечного трансплантата: наш предварительный опыт. Протокол трансплантологии . 2009 Май. 41 (4): 1204-6. [Медлайн].
Бокх М., Гули Т.А., Майерсон Д.Раннее лечение цитомегаловируса pp65 под контролем антигенемии ганцикловиром по сравнению с ганцикловиром при приживлении после аллогенной трансплантации костного мозга: рандомизированное двойное слепое исследование. Кровь . 1996 15 ноября. 88 (10): 4063-71. [Медлайн].
Marty FM, Ljungman P, Chemaly RF, Maertens J, Dadwal SS, Duarte RF, et al. Летермовир Профилактика цитомегаловируса при трансплантации гемопоэтических клеток. N Engl J Med . 2017 6 декабря [Medline]. [Полный текст].
Avery RK, Marty FM, Strasfeld L, Lee I, Arrieta A, Chou S.Пероральный марибавир для лечения рефрактерных или резистентных цитомегаловирусных инфекций у реципиентов трансплантата. Transpl Infect Dis . 2010 декабря 12 (6): 489-96. [Медлайн].
Marty FM, Ljungman P, Papanicolaou GA, Winston DJ, Chemaly RF, Strasfeld L. Профилактика цитомегаловирусом у реципиентов аллогенных стволовых клеток: фаза 3, двойное слепое, плацебо-контролируемое, рандомизированное исследование . Ланцет Infect Dis .2011 г., 11 (4): 284-92. [Медлайн].
Trofe J, Pote L, Wade E, Blumberg E, Bloom RD. Марибавир: новый противовирусный агент с активностью против цитомегаловируса. Энн Фармакотер . 2008 г., 42 (10): 1447-57. [Медлайн].
Джон Г.Т., Маниваннан Дж., Чанди С., Питер С., Джейкоб С.К. Терапия лефлуномидом цитомегаловирусной болезни у реципиентов почечного аллотрансплантата. Трансплантация . 2004 15 мая. 77 (9): 1460-1. [Медлайн].
John GT, Manivannan J, Chandy S, Peter S, Fleming DH, Chandy SJ и др.Проспективная оценка терапии лефлуномидом цитомегаловирусной болезни у реципиентов почечного трансплантата. Протокол трансплантологии . 2005 декабрь 37 (10): 4303-5. [Медлайн].
Леви М.Э., Мандава Н., Чан Л.К., Вайнберг А., Олсон Дж.Л. Лечение цитомегаловирусного ретинита с множественной лекарственной устойчивостью с помощью системного введения лефлуномида. Transpl Infect Dis . 2006 марта 8 (1): 38-43. [Медлайн].
Battiwalla M, Paplham P, Almyroudis NG, McCarthy A, Abdelhalim A, Elefante A.Неспособность лефлуномида контролировать рецидивирующую цитомегаловирусную инфекцию при почечной недостаточности после трансплантации аллогенных стволовых клеток. Transpl Infect Dis . 2007 марта 9 (1): 28-32. [Медлайн].
Valantine HA, Luikart H, Doyle R, Theodore J, Hunt S, Oyer P. Влияние цитомегаловирусного гипериммунного глобулина на исход после кардиоторакальной трансплантации: сравнительное исследование комбинированной профилактики с применением гипериммунного глобулина CMV плюс ганцикловир в сравнении с ганцикловиром. Трансплантация . 2001 27 ноября. 72 (10): 1647-52. [Медлайн].
Go V, Поллард РБ. Цитомегаловирусная вакцина для трансплантации: мы ближе ?. J Заразить Dis . 15 июня 2008 г. 197 (12): 1631-3. [Медлайн].
Schleiss MR. Вакцина против цитомегаловируса укрощает тролля трансплантологов. Ланцет . 2011, 9 апреля. 377 (9773): 1216-8. [Медлайн].
Pass RF, Zhang C, Evans A, Simpson T, Andrews W., Huang ML, et al.Вакцинная профилактика материнской цитомегаловирусной инфекции. N Engl J Med . 2009 19 марта. 360 (12): 1191-9. [Медлайн]. [Полный текст].
Цена NB, Причард М.Н. Прогресс в разработке новых методов лечения герпесвирусных инфекций. Curr Opin Virol . 2011 декабрь 1 (6): 548-54. [Медлайн].
Торрес-Мадриз G, Boucher HW. Хозяева с ослабленным иммунитетом: перспективы лечения и профилактики цитомегаловирусной болезни у реципиентов солидных трансплантатов. Clin Infect Dis . 2008 г. 1. 47 (5): 702-11. [Медлайн].
Wolf DG, Shimoni A, Resnick IB, Stamminger T., Neumann AU, Chou S. Кинетика цитомегаловируса человека после введения артесуната после трансплантации гемопоэтических стволовых клеток. Противовирусный Res . 2011 Июнь 90 (3): 183-6. [Медлайн].
Шапира М.Ю., Резник И.Б., Чоу С. и др. Артесунат как мощное противовирусное средство у пациента с поздней лекарственно-устойчивой цитомегаловирусной инфекцией после трансплантации гемопоэтических стволовых клеток. Clin Infect Dis . 2008 г. 1. 46 (9): 1455-7. [Медлайн].
Каул Д.Р., Стулбен С., Кобер Э., Охо Т., Сандаски Э., Лишка П. Первый отчет об успешном лечении цитомегаловирусной болезни с множественной лекарственной устойчивостью с помощью нового анти-ЦМВ-соединения AIC246. Трансплантат Am J . 2011 Май. 11 (5): 1079-84. [Медлайн].
Александр Б.Т., Хладник Л.М., Огюстен К.М., Касабар Э., Маккиннон П.С., Райхли Р.М. Использование цитомегаловирусного внутривенного иммуноглобулина для дополнительного лечения цитомегаловируса у реципиентов трансплантата гемопоэтических стволовых клеток. Фармакотерапия . 30 июня 2010 г. (6): 554-61. [Медлайн].
Анджела М. Калиендо, MD, PhD. Тестирование вирусной нагрузки на цитомегаловирус у реципиентов солидных трансплантатов. Доступно по адресу http://www.uptodate.com/online/content/topic.do?topicKey=viral_in/21207&selectedTitle=6%7E150&source=search_result#h3. Доступ: 11 июля 2013 г.
Эйвери Р.К., Болвелл Б.Дж., Йен-Либерман Б. и др. Использование лефлуномида у реципиента аллогенного трансплантата костного мозга с резистентной цитомегаловирусной инфекцией. Пересадка костного мозга . 2004 Декабрь 34 (12): 1071-5. [Медлайн].
Эйвери Р.К., Моссад С.Б., Поджио Э., Лард М., Будев М., Болвелл Б. Полезность лефлуномида в лечении сложных цитомегаловирусных синдромов. Трансплантация . 27 августа 2010 г. 90 (4): 419-26. [Медлайн].
Bueno J, Ramil C, Green M. Текущие стратегии управления для профилактики и лечения цитомегаловирусной инфекции у педиатрических реципиентов трансплантата. Детские лекарства . 2002. 4 (5): 279-90. [Медлайн].
Cesaro S, Zhou X, Manzardo C, Buonfrate D, Cusinato R, Tridello G. Цидофовир для реактивации цитомегаловируса у педиатрических пациентов после трансплантации гемопоэтических стволовых клеток. Дж. Клин Вирол . 2005 Октябрь 34 (2): 129-32. [Медлайн].
Cunha BA, Gouzhva O, Nausheen S. Тяжелая внебольничная пневмония (ВП), вызванная цитомегаловирусом (ЦМВ), провоцирующая обострение системной красной волчанки (СКВ). Сердце легкое . 2009 май-июнь. 38 (3): 249-52. [Медлайн].
Cunha BA, Pherez F, Walls N. Тяжелая внебольничная пневмония (ВП), вызванная цитомегаловирусом (CMV), у хозяина без иммунодефицита. Сердце легкое . 2009 май-июнь. 38 (3): 243-8. [Медлайн].
Kling J. Цидофовир перспективен в отношении устойчивого цитомегаловируса. Доступно на http://www.medscape.com/viewarticle/811494. Доступ: 7 октября 2013 г.
Schleiss MR.VCL-CB01, инъекционная двухвалентная плазмидная ДНК-вакцина для потенциальной защиты от заболевания и инфекции ЦМВ. Curr Opin Mol Ther . 2009 Октябрь 11 (5): 572-8. [Медлайн].
Thorne JE, Jabs DA, Kempen JH, Holbrook JT, Nichols C, Meinert CL. Причины снижения остроты зрения у больных СПИДом и цитомегаловирусным ретинитом в эпоху высокоактивной антиретровирусной терапии. Офтальмология . 2006 август 113 (8): 1441-5. [Медлайн].
Wloch MK, Smith LR, Boutsaboualoy S, Reyes L, Han C, Kehler J.Безопасность и иммуногенность вакцины на основе бивалентной ДНК цитомегаловируса у здоровых взрослых людей. J Заразить Dis . 15 июня 2008 г., 197 (12): 1634-42. [Медлайн].


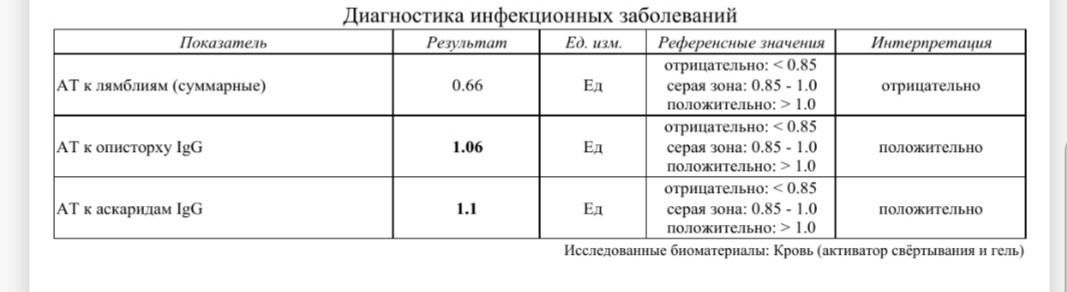 Возможно, ЦМВ попал в организм до беременности. Но не исключено, что женщина заразилась недавно, в начале беременности (за несколько недель до теста). Такой вариант представляет опасность для ребенка.
Возможно, ЦМВ попал в организм до беременности. Но не исключено, что женщина заразилась недавно, в начале беременности (за несколько недель до теста). Такой вариант представляет опасность для ребенка.
 Сыворотка
Сыворотка


 Sci Rep 10: 6850 (2020). PubMed: 32321978
Sci Rep 10: 6850 (2020). PubMed: 32321978 Front Cell Infect Microbiol 10: 334 (2020). PubMed: 32733818
Front Cell Infect Microbiol 10: 334 (2020). PubMed: 32733818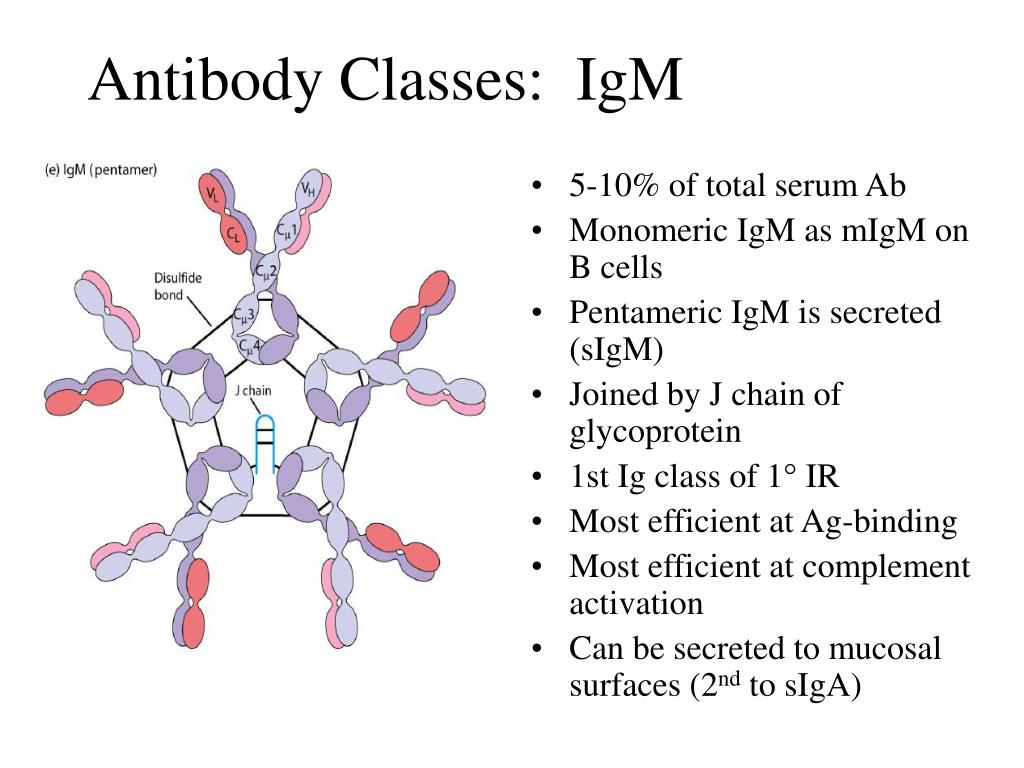 Am J Reprod Immunol 79: e12840 (2018). PubMed: 29520885
Am J Reprod Immunol 79: e12840 (2018). PubMed: 29520885