Ангиоспазм › Болезни › ДокторПитер.ру
Ангиоспазм (angiospasmus; греч. angeion сосуд + spasmos судорога, спазм) — преходящее патологическое сужение просвета артерий вследствие избыточного интенсивного и продолжительного сокращения мышц сосудистой стенки. Ангиоспазм — один из вариантов острой сосудистой дистонии (сосудистого криза). Следствием ангиоспазма является ишемия ткани в бассейне спазмированной артерии.
Признаки
Клиническая картина ангиоспазма зависит от его локализации и состоит главным образом в проявлениях нарушенной функции ишемизированной ткани (например, в мышечных органах — боль в зоне ишемии с иррадиацией по соответствующему сегменту соматической иннервации).
Течение ангиоспазма наиболее изучено при его локализации в сосудах конечностей. Кратковременный ангиоспазм пальцевой артерии при болезни и синдроме Рейно вызывает резкое побледнение и похолодание пальца с нарушением болевой и тактильной чувствительности — от локальных парестезий до анестезии.
Коронарный ангиоспазм проявляется стенокардией Принцметала — тяжелыми приступами болей за грудиной, возникающими в покое, часто в положении больного лежа, в период ночного сна. Во время приступа выявляются характерные изменения ЭКГ, иногда признаки острой очаговой дистрофии миокарда.
Во время приступа выявляются характерные изменения ЭКГ, иногда признаки острой очаговой дистрофии миокарда.
Церебральный ангиоспазм наблюдается часто при атеросклерозе сосудов головного мозга и лежит в основе патогенеза ишемического варианта церебрального криза у больных гипертонической болезнью. Отличительными симптомами этого варианта от других острых церебральных ангиодистоний являются очаговые неврологические нарушения, характерные для зоны ишемии головного мозга, соответствующей бассейну спазмированной артерии. У больных атеросклерозом головного мозга такие нарушения могут быть обусловлены не ангиоспазмом, а механизмами так называемой цереброваскулярной недостаточности — снижением кровотока в зоне расположения атеросклеротической бляшки при падении АД (например, ортостатическом), расстройствах сердечной деятельности. Наличие последних, регистрация сниженного АД, в том числе при ортостатических пробах, помогает дифференциальному диагнозу.
Ангиоспазм в органах брюшной полости не имеет специфических клинических проявлений. Спазм сосудов брыжейки проявляется брюшной жабой.
Спазм сосудов брыжейки проявляется брюшной жабой.
Описание
Термин «ангиоспазм» не следует применять для обозначения физиологической вазоконстрикции и тем более — физиологического повышения тонуса артерий без сужения просвета. Не имеет научного обоснования и распространившаяся в середине 20 в. тенденция связывать именно с ангиоспазмом проявления местных расстройств циркуляции, если их природа не установлена. На практике это приводит к гипердиагностике и не всегда оправданному назначению больному спазмолитических средств.
Ангиоспазмы могут наблюдаться в различных сосудистых регионах, обычно при заболеваниях, сопровождающихся поражением сосудов и их нервного аппарата (атеросклероз, васкулиты, аневризмы и др.) или нарушением нейрогуморальной регуляции сосудистого тонуса (гипертоническая болезнь, гипоталамический синдром, патологический климакс, неврозы и др.). Отмечена этиологическая роль курения, интоксикаций свинцом, сероуглеродом, а в развитии ангиоспазма в конечностях — обморожений и повторных охлаждений. Ангиоспазм нередко определяет клиническую динамику органических сосудистых заболеваний (атеросклероза, тромбозов, эмболий и др.), осложняя их течение. Продолжительный ангиоспазм в головном мозге (церебральный ангиоспазм.), в сердце (коронарный ангиоспазм), в сетчатке глаза может стать причиной серьезных расстройств кровообращения в этих органах вплоть до развития инсульта, инфаркта миокарда, нарушений зрения.
Ангиоспазм нередко определяет клиническую динамику органических сосудистых заболеваний (атеросклероза, тромбозов, эмболий и др.), осложняя их течение. Продолжительный ангиоспазм в головном мозге (церебральный ангиоспазм.), в сердце (коронарный ангиоспазм), в сетчатке глаза может стать причиной серьезных расстройств кровообращения в этих органах вплоть до развития инсульта, инфаркта миокарда, нарушений зрения.
Патогенез ангиоспазма изучен недостаточно, для артерий разных сосудистых регионов он не идентичен, но общим для механизма развития любого ангиоспазма является расстройство функции мембран гладкомышечных клеток сосуда, состоящее в нарушении обменного транспорта через мембраны ионов кальция, натрия, калия, что нарушает нормальное чередование фаз мышечного сокращения и расслабления. Ускоренная и усиленная деполяризация мембран, повышенный приток в клетки свободных ионов кальция способствуют развитию интенсивного мышечного сокращения, а задержка процессов реполяризации мембран (в норме предшествующей расслаблению мышцы) обусловливает длительное пребывание артериальной стенки в сокращенном состоянии. К таким нарушениям могут привести расстройства иннервации сосудистых стенок, дисбаланс в продукции и разрушении гуморальных регуляторов сосудистого тонуса, а также повышенная чувствительность рецепторов сосудистой стенки к нормальным вазоконстрикторным влияниям, что нередко обусловлено локальными изменениями ее метаболизма в зонах воспаления, рубцов, повреждения тромбом и др. Известно, например, что церебральный ангиоспазм часто наблюдается вблизи расположения атеросклеротической бляшки, аневризмы, субарахноидальнего кровоизлияния; коронарный ангиоспазм часто возникает в зоне тромбоза коронарной артерии.
К таким нарушениям могут привести расстройства иннервации сосудистых стенок, дисбаланс в продукции и разрушении гуморальных регуляторов сосудистого тонуса, а также повышенная чувствительность рецепторов сосудистой стенки к нормальным вазоконстрикторным влияниям, что нередко обусловлено локальными изменениями ее метаболизма в зонах воспаления, рубцов, повреждения тромбом и др. Известно, например, что церебральный ангиоспазм часто наблюдается вблизи расположения атеросклеротической бляшки, аневризмы, субарахноидальнего кровоизлияния; коронарный ангиоспазм часто возникает в зоне тромбоза коронарной артерии.
Возможность нейрогенного ангиоспазма, который наблюдается в артериях конечностей и, вероятно, может развиваться в артериях брюшной полости, не подтверждена пока для артерий головного мозга. Роль гиперсимпатикотонии в происхождении коронарного ангиоспазма также остается гипотетической. Коронарный ангиоспазм не возникает во время физической нагрузки (т.е. при активации симпатической нервной системы), не снимается, как правило, a-адреноблокаторами, а в эксперименте вызывается норадреналином лишь при определенных условиях (например, при одновременном применении b-адреноблокаторов) Имеется больше оснований предполагать патогенетическую роль активации вагусных влияний, так как коронарный ангиоспазм у человека обычно возникает в условиях покоя и показана возможность его провокации метахолином.
Диагностика
Диагноз ангиоспазм ставится на основании динамики симптомов, характерных для острого развития преходящей ишемии (стенокардия, брюшная жаба). Для периферического ангиоспазма характерны бледность кожи, местное снижение ее температуры.
Дифференциальный диагноз ангиоспазма и ишемии органической природы затруднен, особенно в тех случаях, когда ангиоспазм развивается на фоне обструктивных ангиопатий. В качестве дифференциального теста исследуют динамику кровотока под влиянием тепловых раздражителей (для ангиоспазма в конечностях) и фармакологических агентов. При смешанном генезе ишемии доля участия в нем ангиоспазма определяется по степени прироста кровотока в ответ на сосудорасширяющее воздействие. В условиях клиники для диагностики ангиоспазма различной локализации используют плетизмографию, реографию, локальную термометрию.
При смешанном генезе ишемии доля участия в нем ангиоспазма определяется по степени прироста кровотока в ответ на сосудорасширяющее воздействие. В условиях клиники для диагностики ангиоспазма различной локализации используют плетизмографию, реографию, локальную термометрию.
Лечение
Лечение и профилактика совпадают частично с лечением и профилактикой основных заболеваний, которым сопутствуют ангиоспазм. Исключается курение табака. Проводится санация очагов хронической инфекции. При ангиоспазме на фоне повышенного АД необходимо применение гипотензивных средств.
Непосредственное купирование ангиоспазма имеет свои особенности при отдельных его формах, например при гипертонических кризах, синдроме Рейно, стенокардии. Во многих случаях эффективны вазоактивные антагонисты кальция. Лекарства подбирают индивидуально с учетом регионарных различий в реакции сосудов.
При периферическом ангиоспазме нередко помогают растирание и согревание больной конечности, новокаиновая блокада в зоне корешков соответствующих сегментов.
Хирургические методы лечения — симпатэктомия и алкоголизация симпатических нервов показаны в основном при ангиоспазмах на фоне органических ангиопатий.
© Медицинская энциклопедия РАМН
Ангиоспазм — это… Что такое Ангиоспазм?
преходящее патологическое сужение просвета артерий вследствие избыточного интенсивного и продолжительного сокращения мышц сосудистой стенки. А. — один из вариантов острой сосудистой дистонии (сосудистого криза). Следствием А. является ишемия ткани в бассейне спазмированной артерии. Термин «ангиоспазм» не следует применять для обозначения физиологической вазоконстрикции и тем более — физиологического повышения тонуса артерий без сужения просвета. Не имеет научного обоснования и распространившаяся в середине 20 в. тенденция связывать именно с А. проявления местных расстройств циркуляции, если их природа не установлена. На практике это приводит к гипердиагностике и не всегда оправданному назначению больному спазмолитических средств.
 является расстройство функции мембран гладкомышечных клеток сосуда, состоящее в нарушении обменного транспорта через мембраны ионов кальция, натрия, калия, что нарушает нормальное чередование фаз мышечного сокращения и расслабления. Ускоренная и усиленная деполяризация мембран, повышенный приток в клетки свободных ионов кальция способствуют развитию интенсивного мышечною сокращения, а задержка процессов реполяризации мембран (в норме предшествующей расслаблению мышцы) обусловливает длительное пребывание артериальной стенки в сокращенном состоянии. К таким нарушениям могут привести расстройства иннервации сосудистых стенок, дисбаланс в продукции и разрушении гуморальных регуляторов сосудистого тонуса, а также повышенная чувствительность рецепторов сосудистой стенки к нормальным вазоконстрикторным влияниям, что нередко обусловлено локальными изменениями ее метаболизма в зонах воспаления, рубцов, повреждения тромбом и др. Известно, например, что церебральный А. часто наблюдается вблизи расположения атеросклеротической бляшки, аневризмы, субарахноидальнего кровоизлияния; коронарный А.
является расстройство функции мембран гладкомышечных клеток сосуда, состоящее в нарушении обменного транспорта через мембраны ионов кальция, натрия, калия, что нарушает нормальное чередование фаз мышечного сокращения и расслабления. Ускоренная и усиленная деполяризация мембран, повышенный приток в клетки свободных ионов кальция способствуют развитию интенсивного мышечною сокращения, а задержка процессов реполяризации мембран (в норме предшествующей расслаблению мышцы) обусловливает длительное пребывание артериальной стенки в сокращенном состоянии. К таким нарушениям могут привести расстройства иннервации сосудистых стенок, дисбаланс в продукции и разрушении гуморальных регуляторов сосудистого тонуса, а также повышенная чувствительность рецепторов сосудистой стенки к нормальным вазоконстрикторным влияниям, что нередко обусловлено локальными изменениями ее метаболизма в зонах воспаления, рубцов, повреждения тромбом и др. Известно, например, что церебральный А. часто наблюдается вблизи расположения атеросклеротической бляшки, аневризмы, субарахноидальнего кровоизлияния; коронарный А. часто возникает в зоне тромбоза коронарной артерии.
Возможность нейрогенного А., который наблюдается в артериях конечностей и, вероятно, может развиваться в артериях брюшной полости, не подтверждена пока для артерий головного мозга. Роль гиперсимпатикотонии в происхождении коронарного А. также остается гипотетической. Коронарный А. не возникает во время физической нагрузки (т.е. при активации симпатической нервной системы), не снимается, как правило, α-адреноблокаторами, а в эксперименте вызывается норадреналином лишь при определенных условиях (например, при одновременном применении β-адреноблокаторов) Имеется больше оснований предполагать патогенетическую роль активации вагусных влияний, т.к. коронарный А. у человека обычно возникает в условиях покоя и показана возможность его провокации метахолином. Большое значение может иметь нарушение функции эндотелия коронарных артерий, регулирующей локальный баланс гуморальных вазодилатирующих (простациклин) и вазоконстрикторных (серотонин, ПГ2α, тромбоксан А2) субстанций.
часто возникает в зоне тромбоза коронарной артерии.
Возможность нейрогенного А., который наблюдается в артериях конечностей и, вероятно, может развиваться в артериях брюшной полости, не подтверждена пока для артерий головного мозга. Роль гиперсимпатикотонии в происхождении коронарного А. также остается гипотетической. Коронарный А. не возникает во время физической нагрузки (т.е. при активации симпатической нервной системы), не снимается, как правило, α-адреноблокаторами, а в эксперименте вызывается норадреналином лишь при определенных условиях (например, при одновременном применении β-адреноблокаторов) Имеется больше оснований предполагать патогенетическую роль активации вагусных влияний, т.к. коронарный А. у человека обычно возникает в условиях покоя и показана возможность его провокации метахолином. Большое значение может иметь нарушение функции эндотелия коронарных артерий, регулирующей локальный баланс гуморальных вазодилатирующих (простациклин) и вазоконстрикторных (серотонин, ПГ2α, тромбоксан А2) субстанций. Тромбоксан А2 относится к наиболее сильным вазоконстрикторам, и локальное повышение его продукции (как и недостаточный синтез простациклина) может быть причиной коронароспазма. Клиническая картина А. зависит от его локализации и состоит главным образом в проявлениях нарушенной функции ишемизированной ткани (например, в мышечных органах — боль в зоне ишемии с иррадиацией по соответствующему сегменту соматической иннервации).
Течение А. наиболее изучено при его локализации в сосудах конечностей. Кратковременный А. пальцевой артерии при болезни и синдроме Рейно (см. Рейно синдром) вызывает резкое побледнение и похолодание пальца с нарушением болевой и тактильной чувствительности — от локальных парестезий до анестезии. Такая совокупность симптомов характеризуется как «мертвый палец» (digitus mortuus). Аналогичные признаки развиваются на всей конечности при спазме магистральных артерий обычно сопутствующем органическому их поражению. Симптом алебастровой (как у статуи) бледности ноги в таких случаях обозначается как «нога командора».
Тромбоксан А2 относится к наиболее сильным вазоконстрикторам, и локальное повышение его продукции (как и недостаточный синтез простациклина) может быть причиной коронароспазма. Клиническая картина А. зависит от его локализации и состоит главным образом в проявлениях нарушенной функции ишемизированной ткани (например, в мышечных органах — боль в зоне ишемии с иррадиацией по соответствующему сегменту соматической иннервации).
Течение А. наиболее изучено при его локализации в сосудах конечностей. Кратковременный А. пальцевой артерии при болезни и синдроме Рейно (см. Рейно синдром) вызывает резкое побледнение и похолодание пальца с нарушением болевой и тактильной чувствительности — от локальных парестезий до анестезии. Такая совокупность симптомов характеризуется как «мертвый палец» (digitus mortuus). Аналогичные признаки развиваются на всей конечности при спазме магистральных артерий обычно сопутствующем органическому их поражению. Симптом алебастровой (как у статуи) бледности ноги в таких случаях обозначается как «нога командора». В случае затянувшегося А. конечностей появляется дистальный цианоз, иногда равномерный, иногда в виде цианотичной сетки, создающей впечатление мраморной кожи. Появление цианоза обусловлено парезом венул в зоне ишемии. При digitus mor tuus цианоз обычно отсутствует, но он часто бывает при ишемии больших участков конечностей. Вслед за цианозом развивается некоторая отечность ткани, обусловленная повышением проницаемости для белков капилляров (вследствие гипоксии мембран). На следующем этапе развиваются некробиотические процессы и тем скорее, чем больше разрыв между потребностью ткани в кислороде и величиной притока крови.
Коронарный А. проявляется стенокардией Принцметала — тяжелыми приступами болей за грудиной, возникающими в покое, часто в положении больного лежа, в период ночного сна. Во время приступа выявляются характерные изменения ЭКГ (см. Стенокардия), иногда признаки острой очаговой дистрофии миокарда.
Церебральный А. наблюдается часто при атеросклерозе сосудов головного мозга и лежит в основе патогенеза ишемического варианта церебрального криза у больных гипертонической болезнью.
В случае затянувшегося А. конечностей появляется дистальный цианоз, иногда равномерный, иногда в виде цианотичной сетки, создающей впечатление мраморной кожи. Появление цианоза обусловлено парезом венул в зоне ишемии. При digitus mor tuus цианоз обычно отсутствует, но он часто бывает при ишемии больших участков конечностей. Вслед за цианозом развивается некоторая отечность ткани, обусловленная повышением проницаемости для белков капилляров (вследствие гипоксии мембран). На следующем этапе развиваются некробиотические процессы и тем скорее, чем больше разрыв между потребностью ткани в кислороде и величиной притока крови.
Коронарный А. проявляется стенокардией Принцметала — тяжелыми приступами болей за грудиной, возникающими в покое, часто в положении больного лежа, в период ночного сна. Во время приступа выявляются характерные изменения ЭКГ (см. Стенокардия), иногда признаки острой очаговой дистрофии миокарда.
Церебральный А. наблюдается часто при атеросклерозе сосудов головного мозга и лежит в основе патогенеза ишемического варианта церебрального криза у больных гипертонической болезнью.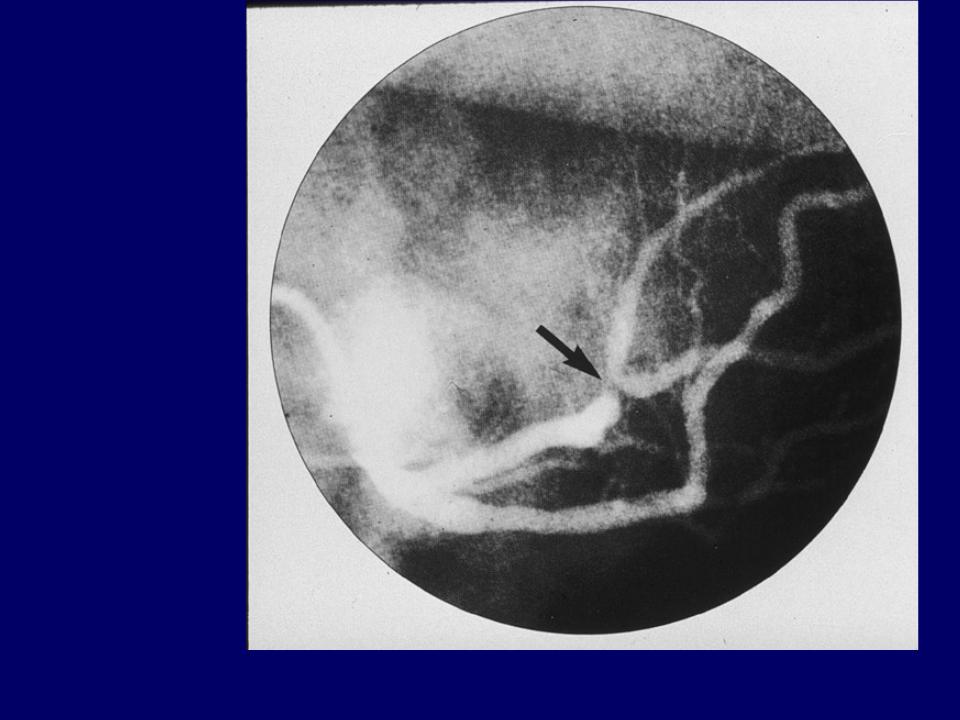 Отличительными симптомами этого варианта от других острых церебральных ангиодистоний являются очаговые неврологические нарушения, характерные для зоны ишемии головного мозга, соответствующей бассейну спазмированной артерии (см. Гипертонические кризы). У больных атеросклерозом головного мозга такие нарушения могут быть обусловлены не А., а механизмами так называемой цереброваскулярной недостаточности — снижением кровотока в зоне расположения атеросклеротической бляшки при падении АД (например, ортостатическом), расстройствах сердечной деятельности. Наличие последних, регистрация сниженного АД, в т.ч. при ортостатических пробах, помогает дифференциальному диагнозу.
Ангиоспазм в органах брюшной полости не имеет специфических клинических проявлений. Спазм сосудов брыжейки проявляется брюшной жабой (Брюшная жаба). Диагноз А. ставится на основании динамики симптомов, характерных для острого развития преходящей ишемии (стенокардия, брюшная жаба). Для периферического А.
Отличительными симптомами этого варианта от других острых церебральных ангиодистоний являются очаговые неврологические нарушения, характерные для зоны ишемии головного мозга, соответствующей бассейну спазмированной артерии (см. Гипертонические кризы). У больных атеросклерозом головного мозга такие нарушения могут быть обусловлены не А., а механизмами так называемой цереброваскулярной недостаточности — снижением кровотока в зоне расположения атеросклеротической бляшки при падении АД (например, ортостатическом), расстройствах сердечной деятельности. Наличие последних, регистрация сниженного АД, в т.ч. при ортостатических пробах, помогает дифференциальному диагнозу.
Ангиоспазм в органах брюшной полости не имеет специфических клинических проявлений. Спазм сосудов брыжейки проявляется брюшной жабой (Брюшная жаба). Диагноз А. ставится на основании динамики симптомов, характерных для острого развития преходящей ишемии (стенокардия, брюшная жаба). Для периферического А. характерны бледность кожи, местное снижение ее температуры.
Дифференциальный диагноз А. и ишемии органической природы затруднен, особенно в тех случаях, когда А. развивается на фоне обструктивных ангиопатий. В качестве дифференциального теста исследуют динамику кровотока под влиянием тепловых раздражителей (для А. в конечностях) и фармакологических агентов. При смешанном генезе ишемии доля участия в нем А. определяется по степени прироста кровотока в ответ на сосудорасширяющее воздействие. В условиях клиники для диагностики А. различной локализации используют плетизмографию (Плетизмография), реографию (Реография), локальную термометрию. Лечение и профилактика совпадают частично с лечением и профилактикой основных заболеваний, которым сопутствуют А. Исключается курение табака. Проводится санация очагов хронической инфекции. При А. на фоне повышенного АД необходимо применение гипотензивных средств.
Непосредственное купирование А. имеет свои особенности при отдельных его формах, например при гипертонических кризах, синдроме Рейно, стенокардии.
характерны бледность кожи, местное снижение ее температуры.
Дифференциальный диагноз А. и ишемии органической природы затруднен, особенно в тех случаях, когда А. развивается на фоне обструктивных ангиопатий. В качестве дифференциального теста исследуют динамику кровотока под влиянием тепловых раздражителей (для А. в конечностях) и фармакологических агентов. При смешанном генезе ишемии доля участия в нем А. определяется по степени прироста кровотока в ответ на сосудорасширяющее воздействие. В условиях клиники для диагностики А. различной локализации используют плетизмографию (Плетизмография), реографию (Реография), локальную термометрию. Лечение и профилактика совпадают частично с лечением и профилактикой основных заболеваний, которым сопутствуют А. Исключается курение табака. Проводится санация очагов хронической инфекции. При А. на фоне повышенного АД необходимо применение гипотензивных средств.
Непосредственное купирование А. имеет свои особенности при отдельных его формах, например при гипертонических кризах, синдроме Рейно, стенокардии..jpg) Во многих случаях эффективны вазоактивные антагонисты кальция — фенигидин (нифедипин, адалат, коринфар). Лекарства подбирают индивидуально с учетом регионарных различий в реакции сосудов. Нитриты, например, наиболее эффективны при коронарном А., но они, как правило, отрицательно влияют на кровоток в мозговых артериях. При церебральном А. эффективными при внутривенном введении могут быть винкимин, но-шпа, папаверин, эуфиллин.
При периферическом А. нередко помогают растирание и согревание больной конечности, новокаиновая блокада в зоне корешков соответствующих сегментов; внутриартериальное введение 10 мл 0,25% раствора новокаина или 3 мл 2% раствора но-шпы.
Во многих случаях эффективны вазоактивные антагонисты кальция — фенигидин (нифедипин, адалат, коринфар). Лекарства подбирают индивидуально с учетом регионарных различий в реакции сосудов. Нитриты, например, наиболее эффективны при коронарном А., но они, как правило, отрицательно влияют на кровоток в мозговых артериях. При церебральном А. эффективными при внутривенном введении могут быть винкимин, но-шпа, папаверин, эуфиллин.
При периферическом А. нередко помогают растирание и согревание больной конечности, новокаиновая блокада в зоне корешков соответствующих сегментов; внутриартериальное введение 10 мл 0,25% раствора новокаина или 3 мл 2% раствора но-шпы.Спазм сосудов (ангиоспазм) – симптомы и лечение
Разновидности ангиоспазма классифицируют по их локализации:
- в конечностях;
- в магистральных артериях;
-
в головном мозге.

Отдельный вариант патологии — ангиоспазм коронарных сосудов.
Причины спазма сосудов
Спазм кровеносных сосудов происходит при наличии нескольких факторов, влияющих на развитие этого недуга:
- Курение. Вредная привычка провоцирует сужение сосудов, в связи с чем к спазму может привести другой негативный фактор, к примеру, обычная простуда.
- Злоупотребление алкоголем.
- Неправильный режим сна и бодрствования.
- Физические и умственные перегрузки.
- Чрезмерное употребление кофе и чая.
- Интоксикация ядовитыми веществами, содержащими сероуглеродистые соединения и свинец.
- Воспаление кровеносных сосудов.
-
Нарушения нервной регуляции.

К последней причине относится целая группа факторов внутреннего и внешнего характера (неврозы, сбои в работе эндокринной системы и пр.).
Симптомы спазма сосудов
Если причиной ангиоспазма стало сужение капилляров, внешнее проявление будет заметно невооруженным глазом: пораженный участок тела приобретает алебастровый (белый) оттенок. Так, для болезни Рейно характерен так называемый синдром белых пальцев. Он связан с обескровливанием фаланг. Пальцы при этом теряют чувствительность. Другой симптом — сетчатое ливедо. При ангиоспазме на коже бедер и лодыжек возникают участки с характерным синеватым оттенком. Иногда симптом дополняется сетчатым рисунком. Кожа пораженного участка при этом холодеет и бледнеет. Ангиоспазм может привести к отеку и последующему некрозу тканей.
Если происходит сужение сосудов магистральной артерии, характерный симптом — так называемая нога командора. Проявление схоже с болезнью Рейно, но затрагивает всю нижнюю конечность. Нога холодеет, ее кожа приобретает беловатый оттенок. При продолжительном ангиоспазме возможно посинение конечности, возникает ее неполный паралич.
Нога холодеет, ее кожа приобретает беловатый оттенок. При продолжительном ангиоспазме возможно посинение конечности, возникает ее неполный паралич.
Коронарный спазм схож по своим симптомам со стенокардией. Чувствуется приступообразная боль за грудиной, которая не ослабевает, даже если тело в состоянии покоя.
Церебральный ангиоспазм возникает при атеросклерозе сосудов головного мозга. Но причиной симптома может стать не только эта патология. Ангиоспазм также возможен при поражении различных участков головного мозга.
Как определить спазм сосудов
Проявления ангиоспазма похожи на ишемические, особенно если заболевание развивается на форе обструктивной ангиопатии. Чтобы установить полную клиническую картину на основе симптомов пациента, необходимо провести ряд исследований. Под действием тепловых раздражителей и фармакологических агентов анализируется динамика кровотока. С помощью этих исследований обнаруживаются участки с ангиоспазмом.![]() Также применяются плетизмография, реография, локальное измерение температуры.
Также применяются плетизмография, реография, локальное измерение температуры.
Лечение спазма сосудов
Терапия, которая назначается для купирования или профилактики ангиоспазма, зачастую совпадает с лечением того заболевания, которое вызывает симптом. Если пациент курит или употребляет спиртное, ему в обязательном порядке следует отказаться от этих вредных привычек. При обнаружении очагов хронической инфекции происходит их санация. Если вместе с ангиоспазмом у пациента диагностируется повышенное артериальное давление, назначается прием гипотензивных препаратов.
В некоторых случаях применяются препараты, которые содержат вазоактивные блокаторы кальциевых каналов. Выбор лекарства должен учитывать индивидуальные особенности организма.
Периферический спазм требует дополнительной терапии, которая включает растирание и согревание больных конечностей, а также новокаиновую блокаду. В некоторых случаях требуется оперативное вмешательство — резекция симпатического нервного ствола, алкоголизация симпатических нервов.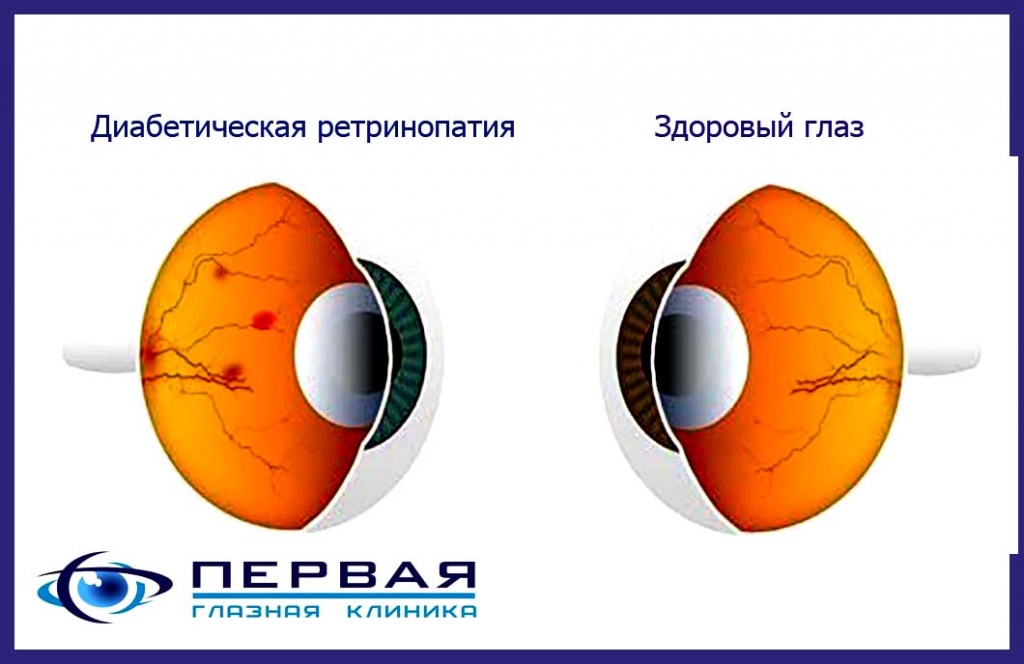
Чем опасен ангиоспазм сетчатки глаза
Ангиоспазм сетчатки — это экстренное состояние в офтальмологии, которое характеризуется нарушением обменных процессов в клетках по причине прекращения кровотока. Как любая неотложная форма болезни ангиоспазм нуждается в оперативном вмешательстве специалиста.
Наблюдение за людьми, перенесшими это состояние, позволяет сделать следующие выводы:
• нарушения работы сердечно-сосудистой системы – одна из причин возникновения ангиоспазма, об этом свидетельствуют 91,2% случаев;
• в частности атеросклероз и артериальная гипертензия приводят к ангиоспазму сетчатки, 60% случаев доказывают эту связь;
• в 25-30% случаях не удается определить, на фоне чего возник ангиоспазм;
• это экстренное состояние возникает, как правило, у людей после 40 лет;
• число заболевших мужчин в два раза больше, чем женщин.
Каковы причины этого состояния?
До конца причины нарушения кровообращения сетчатки не выяснены. В детском возрасте сокращение среднего слоя кровеносных сосудов происходит из-за особенности развития периферической нервной системы. У взрослого человека среди причин заболевания можно выделить следующие:
В детском возрасте сокращение среднего слоя кровеносных сосудов происходит из-за особенности развития периферической нервной системы. У взрослого человека среди причин заболевания можно выделить следующие:
1. Гипертоническая болезнь приводит к резкому рефлекторному сокращению сосудов, это касается и области глаза.
2. Сахарный диабет. Данная болезнь вызывает диабетическую ретинопатию. Последнее состояние сопровождается эпизодами ангиоспазма.
3. Атеросклероз ведет к повышению артериального давления и нарушению пропускания крови через сосудистую систему органов и тканей.
4. Вредные привычки. Злоупотребление курением и алкоголем может привести к ангиоспазму сетчатки, так как никотин и этиловый спирт – это вещества, которые ведут к сужению сосудов, нарушая кровоснабжение сетчатки глаза.
5. Интоксикация часто наблюдается у лиц, длительно пребывающих во вредных для здоровья условиях. В частности соединения сероуглерода и свинца повышают напряжение сосудистой стенки, из-за чего меняется диаметр просвета сосудов, приводя к нарушению кровотока.
Механизм зарождения болезни можно описать следующим образом: повышенная концентрация ионов кальция и снижение ионов калия и натрия приводят к изменению гладкомышечного слоя. В результате чего просвет сосудов сужается, замедляя кровоток. Длительная интоксикация приводит к тому, что тонус симпатической нервной системы повышается, это приводит к ангиоспазму. Наблюдения за инсулинозависимыми больными свидетельствуют о повышении у них степени жесткости стенок сосудов. Данный факт также приводит к ангиоспазму сетчатки.
Симптомы
Для ангиоспазма сетчатки свойственно поражение обоих глаз, в редких случаях – только одного. Характерными жалобами пациентов являются затуманивание зрения и появление мерцающих точек перед глазами. Если ангиоспазм носит кратковременный характер, симптомы проходят. Такой спазм также может сопровождаться искажением восприятия зрения подобно мета- и фотоморфопсий. Некоторые больные жалуются на дискомфорт в области глазницы пораженного органа зрения. В течение спазма пациента может преследовать головная боль и головокружение, пульсация в висках. После приступа общее состояние приходит в норму, зрительная функция восстанавливается. Если возникший ангиоспазм носит продолжительный характер, последствием может стать необратимая потеря остроты зрения.
В течение спазма пациента может преследовать головная боль и головокружение, пульсация в висках. После приступа общее состояние приходит в норму, зрительная функция восстанавливается. Если возникший ангиоспазм носит продолжительный характер, последствием может стать необратимая потеря остроты зрения.
Осложнения
Продолжительный спазм может привести не только к уменьшению остроты зрения, но и к полной его потере. Частота приступов является причиной выраженного дискомфорта и нарушению трудоспособности вследствие того, что у больных отсутствует способность предвидеть период развития следующего фрагмента. Прогрессирующая форма заболевания влечет за собой повышение внутриглазного давления. С течением времени у пациента проявляется вторичная офтальмогпиртензия, развивается глазная мигрень. Быстропроходящие приступы переносятся без осложнений.
Диагностика
Болезнь диагностируется исходя из данных анамнеза и проведенного осмотра, в некоторых случаях прибегают к дополнительным методам постановки диагноза. В течение ангиоспазма присутствуют такие явления как переполнение сосудов кровью и отечность конъюнктивы, после окончания приступа изменения передней области глаз отсутствуют при визуальном осмотре.
В течение ангиоспазма присутствуют такие явления как переполнение сосудов кровью и отечность конъюнктивы, после окончания приступа изменения передней области глаз отсутствуют при визуальном осмотре.
При диагностировании ангиоспазма сетчатой оболочки используются следующие методики:
— Офтальмоскопия. Видна резко суженная центральная артерия и ее ответвления малого диаметра при осмотре. Венозные артерии наполнены кровью. Наблюдается отечность зрительного нерва и его бледно-розовый цвет.
— Бесконтактная тонометрия. Диагностика этим методом основана на присутствии повышенного внутриглазного давления во время ангиоспазма. После исчезновения симптомов показатель нормализуется. Если данное явления не наблюдается, необходимо обратиться к электронной тонографии глаза.
— Антиография сетчатой оболочки. Дает возможность рассмотреть динамику в сетчаточных сосудах с помощью анализа циркуляции флуоресцеина. При заболевании гематоретинальный барьер не пропускает контраст.
— Оптическая когерентная томография сетчатой оболочки. Сканирование выявляет резкое увеличение желтого пятна (макулы). Фовеальная ямка выровнена, реакция сетчатки снижена. Кривая имеет нетипичный прямой вид.
Сканирование выявляет резкое увеличение желтого пятна (макулы). Фовеальная ямка выровнена, реакция сетчатки снижена. Кривая имеет нетипичный прямой вид.
Лечение
Этиотропное лечение не разработано. Патогенетическая терапия направлена на расширение спазмированных сосудов для восстановления ретинального кровотока в зоне ишемии. Крайне важно вовремя купировать симптоматику ангиоспазма, т. к. продолжительное нарушение микроциркуляции влечет за собой полную или частичную потерю зрения. По этой причине сразу же после осмотра глазного дна назначаются инфузии плазмозаменителей и спазмолитиков . Следующий этап лечения – выполнение электрофореза с сосудорасширяющими средствами (дротаверин) и периферическими вазодилататорами (бендазол).
Для того, чтоб снизить внутриглазное давление, используются салуретики и ингибиторы карбоангидразы. Если отсутствует эффект, в ретробульбарное пространство устанавливают ирригационную систему. Показаны инстилляции растворов блокаторов бета-адренорецепторов (тимолол, пилокарпина гидрохлорид). Если сопутствует повышение системного артериального давления, лекарственные препараты вводят внутримышечно. Для того, чтоб стимулировать регенерацию рецепторного аппарата, используются пептидные биорегуляторы. Если патология протекает тяжело, дополнительно показано ретробульбарное введение М-холинолитиков (атропина).
Если сопутствует повышение системного артериального давления, лекарственные препараты вводят внутримышечно. Для того, чтоб стимулировать регенерацию рецепторного аппарата, используются пептидные биорегуляторы. Если патология протекает тяжело, дополнительно показано ретробульбарное введение М-холинолитиков (атропина).
Прогноз и профилактические меры
На прогноз при ангиоспазме влияет характер приступа. Непродолжительное сужение мелких веток ЦАС глазного яблока проходит бесследно. Неблагоприятными в плане прогностики считаются вазоспастические реакции продолжительностью от 15 минут, когда наступают необратимые изменения со стороны сетчатки. Специфические профилактические меры на сегодняшний день не известны. Неспецифическая профилактика заключается в контроле артериального давления и уровня глюкозы крови, приеме статинов при атеросклерозе, применении средств индивидуальной защиты при работе с ядохимикатами в условиях производства.
Приходите на диагностику по адресу: Алматы, улица Толе би, 95а (угол улицы Байтурсынова).
Телефон: +7 (775) 007 01 00; +7 (727) 279 54 36
Instagram eyeinst_kz
Сайт eyeinst.kz
Ангиоспазм сетчатки
Ангиоспазм сетчатки — это экстренное состояние в офтальмологии, которое характеризуется нарушением обменных процессов в клетках по причине прекращения кровотока. Как любая неотложная форма болезни ангиоспазм нуждается в оперативном вмешательстве специалиста. Наблюдение за людьми, перенесшими это состояние, позволяет сделать следующие выводы:
- нарушения работы сердечно-сосудистой системы – одна из причин возникновения ангиоспазма, об этом свидетельствуют 91,2% случаев;
- в частности атеросклероз и артериальная гипертензия приводят к ангиоспазму сетчатки, 60% случаев доказывают эту связь;
- в 25-30% случаях не удается определить, на фоне чего возник ангиоспазм;
- это экстренное состояние возникает, как правило, у людей после 40 лет;
- число заболевших мужчин в два раза больше, чем женщин.

Каковы причины этого состояния?
До конца причины нарушения кровообращения сетчатки не выяснены. В детском возрасте сокращение среднего слоя кровеносных сосудов происходит из-за особенности развития периферической нервной системы. У взрослого человека среди причин заболевания можно выделить следующие:
- Гипертоническая болезнь приводит к резкому рефлекторному сокращению сосудов, это касается и области глаза.
- Сахарный диабет. Данная болезнь вызывает диабетическую ретинопатию. Последнее состояние сопровождается эпизодами ангиоспазма.
- Атеросклероз ведет к повышению артериального давления и нарушению пропускания крови через сосудистую систему органов и тканей.
- Вредные привычки. Злоупотребление курением и алкоголем может привести к ангиоспазму сетчатки, так как никотин и этиловый спирт – это вещества, которые ведут к сужению сосудов, нарушая кровоснабжение сетчатки глаза.
- Интоксикация часто наблюдается у лиц, длительно пребывающих во вредных для здоровья условиях.
 В частности соединения сероуглерода и свинца повышают напряжение сосудистой стенки, из-за чего меняется диаметр просвета сосудов, приводя к нарушению кровотока.
В частности соединения сероуглерода и свинца повышают напряжение сосудистой стенки, из-за чего меняется диаметр просвета сосудов, приводя к нарушению кровотока.
Механизм зарождения болезни можно описать следующим образом: повышенная концентрация ионов кальция и снижение ионов калия и натрия приводят к изменению гладкомышечного слоя. В результате чего просвет сосудов сужается, замедляя кровоток. Длительная интоксикация приводит к тому, что тонус симпатической нервной системы повышается, это приводит к ангиоспазму. Наблюдения за инсулинозависимыми больными свидетельствуют о повышении у них степени жесткости стенок сосудов. Данный факт также приводит к ангиоспазму сетчатки.
Симптомы
Для ангиоспазма сетчатки свойственно поражение обоих глаз, в редких случаях – только одного. Характерными жалобами пациентов являются затуманивание зрения и появление мерцающих точек перед глазами. Если ангиоспазм носит кратковременный характер, симптомы проходят. Такой спазм также может сопровождаться искажением восприятия зрения подобно мета- и фотоморфопсий. Некоторые больные жалуются на дискомфорт в области глазницы пораженного органа зрения. В течение спазма пациента может преследовать головная боль и головокружение, пульсация в висках. После приступа общее состояние приходит в норму, зрительная функция восстанавливается. Если возникший ангиоспазм носит продолжительный характер, последствием может стать необратимая потеря остроты зрения.
Такой спазм также может сопровождаться искажением восприятия зрения подобно мета- и фотоморфопсий. Некоторые больные жалуются на дискомфорт в области глазницы пораженного органа зрения. В течение спазма пациента может преследовать головная боль и головокружение, пульсация в висках. После приступа общее состояние приходит в норму, зрительная функция восстанавливается. Если возникший ангиоспазм носит продолжительный характер, последствием может стать необратимая потеря остроты зрения.
Осложнения
Продолжительный спазм может привести не только к уменьшению остроты зрения, но и к полной его потере. Частота приступов является причиной выраженного дискомфорта и нарушению трудоспособности вследствие того, что у больных отсутствует способность предвидеть период развития следующего фрагмента. Прогрессирующая форма заболевания влечет за собой повышение внутриглазного давления. С течением времени у пациента проявляется вторичная офтальмогпиртензия, развивается глазная мигрень.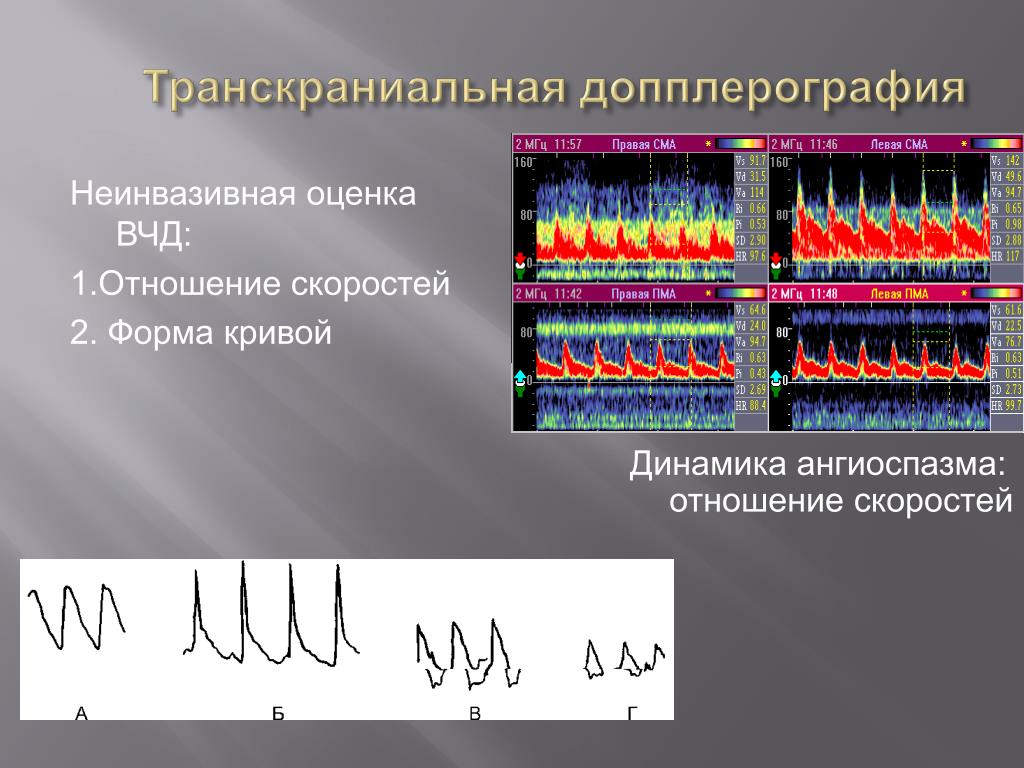 Быстропроходящие приступы переносятся без осложнений.
Быстропроходящие приступы переносятся без осложнений.
Диагностика
Болезнь диагностируется исходя из данных анамнеза и проведенного осмотра, в некоторых случаях прибегают к дополнительным методам постановки диагноза. В течение ангиоспазма присутствуют такие явления как переполнение сосудов кровью и отечность конъюнктивы, после окончания приступа изменения передней области глаз отсутствуют при визуальном осмотре.
При диагностировании ангиоспазма сетчатой оболочки используются следующие методики:
— Офтальмоскопия. Видна резко суженная центральная артерия и ее ответвления малого диаметра при осмотре. Венозные артерии наполнены кровью. Наблюдается отечность зрительного нерва и его бледно-розовый цвет.
— Бесконтактная тонометрия. Диагностика этим методом основана на присутствии повышенного внутриглазного давления во время ангиоспазма. После исчезновения симптомов показатель нормализуется. Если данное явления не наблюдается, необходимо обратиться к электронной тонографии глаза.
— Антиография сетчатой оболочки. Дает возможность рассмотреть динамику в сетчаточных сосудах с помощью анализа циркуляции флуоресцеина. При заболевании гематоретинальный барьер не пропускает контраст.
— Оптическая когерентная томография сетчатой оболочки. Сканирование выявляет резкое увеличение желтого пятна (макулы). Фовеальная ямка выровнена, реакция сетчатки снижена. Кривая имеет нетипичный прямой вид.
Лечение
Этиотропное лечение не разработано. Патогенетическая терапия направлена на расширение спазмированных сосудов для восстановления ретинального кровотока в зоне ишемии. Крайне важно вовремя купировать симптоматику ангиоспазма, т. к. продолжительное нарушение микроциркуляции влечет за собой полную или частичную потерю зрения. По этой причине сразу же после осмотра глазного дна назначаются инфузии плазмозаменителей и спазмолитиков . Следующий этап лечения – выполнение электрофореза с сосудорасширяющими средствами (дротаверин) и периферическими вазодилататорами (бендазол).
Для того, чтоб снизить внутриглазное давление, используются салуретики и ингибиторы карбоангидразы. Если отсутствует эффект, в ретробульбарное пространство устанавливают ирригационную систему. Показаны инстилляции растворов блокаторов бета-адренорецепторов (тимолол, пилокарпина гидрохлорид). Если сопутствует повышение системного артериального давления, лекарственные препараты вводят внутримышечно. Для того, чтоб стимулировать регенерацию рецепторного аппарата, используются пептидные биорегуляторы. Если патология протекает тяжело, дополнительно показано ретробульбарное введение М-холинолитиков (атропина).
Прогноз и профилактические меры
На прогноз при ангиоспазме влияет характер приступа. Непродолжительное сужение мелких веток ЦАС глазного яблока проходит бесследно. Неблагоприятными в плане прогностики считаются вазоспастические реакции продолжительностью от 15 минут, когда наступают необратимые изменения со стороны сетчатки. Специфические профилактические меры на сегодняшний день не известны. Неспецифическая профилактика заключается в контроле артериального давления и уровня глюкозы крови, приеме статинов при атеросклерозе, применении средств индивидуальной защиты при работе с ядохимикатами в условиях производства.
Неспецифическая профилактика заключается в контроле артериального давления и уровня глюкозы крови, приеме статинов при атеросклерозе, применении средств индивидуальной защиты при работе с ядохимикатами в условиях производства.
Советы специалистов, как сохранить здоровье сосудов в холодное время года
В последнее время мы все чаще сталкиваемся с погодными капризами: температура резко опускается, то через пару дней резко растет в сторону «плюса». Такие температурные колебания могут негативно отразиться на сосудистой системе. Евгений Ермолаев, заведующий отделением сосудистой и эндоваскулярной хирургии Запорожской областной больницы, рассказал о влиянии погодных условий на сосудистую систему и дал рекомендации, как избежать осложнений.
Как температура, особенно пониженная, влияет на сосуды?
Первое звено сосудистой системы, которое реагирует на погоду – это кожные покровы. На кожу природой возложена задача отвечать за терморегуляцию организма путем спазма и расширения сосудов. Например, в жаркую погоду сосуды расширяются, чтобы не допустить перегрева, в холодное время – сужаются, чтобы сохранить тепло.
Например, в жаркую погоду сосуды расширяются, чтобы не допустить перегрева, в холодное время – сужаются, чтобы сохранить тепло.
Непокрытая одеждой кожа (кисти рук, лицо, уши) реагирует в первую очередь Ангиоспазм, то есть сужение сосудов, при выходе на холод – это нормальная реакция организма. Однако у некоторых людей склонность к сужению сосудов повышенная. У них в ответ на температурную провокацию возникает ангиоспастический синдром, то есть затянувшийся спазм сосудов. Эти люди быстрее реагируют на прохладный воздух, у них сильно холодеют руки, вплоть до изменения цвета и появления онемения, они долго не могут согреться после прогулки на улице.
Ангиоспастический синдром однозначно вызывает дискомфорт. Однако есть еще более серьезные последствия, которые он может спровоцировать. Например, если у пациента уже есть проблемы с кровоснабжением в артериях нижних конечностей, то специфическая реакция на холод может вызвать даже трофические процессы! Конечно, это довольно редкие случаи, но тем не менее это показатель, к каким серьезным осложнениям может привести незначительная на первый взгляд особенность организма.
Эту реакцию, как и любую другую, можно тренировать и воспитывать. Укрепить сосуды поможет закалка, только закаляться нужно начинать с умом – последовательно и медленно, чтобы не нанести еще больше вреда. Также сосудистые хирурги ЗОКБ рекомендуют находится на холоде дозировано, не переохлаждаться, одеваться по сезону, носить теплые варежки, шарфы, носки.
Если вышеперечисленные симптомы вам знакомы – специалисты советуют пройти обследование. Получить информацию о состоянии кровотока можно с помощью капилляроскопии кистей и/или стоп, УЗИ сосудов верхних и/или нижних конечностей. Результатов этих двух исследований достаточно, чтобы выявить патологию и назначить ее лечение.
Ежегодно в отделении сосудистой и эндоваскулярной хирургии Запорожской областной больницы проходят стационарное лечение более тысячи жителей Запорожской области и других регионов Украины. Это пациенты с заболеваниями магистральных артерий (сужение, закупорка, аневризма аорты, патологии сонных артерий и др. ) и заболеваниями магистральных вен (варикозное расширение вен нижних конечностей, тромбоз глубоких вен нижних конечностей).
) и заболеваниями магистральных вен (варикозное расширение вен нижних конечностей, тромбоз глубоких вен нижних конечностей).
На какие симптомы нужно обратить внимание?
Развитие некоторых заболеваний сосудов сложно пропустить. Это ангиоспастический синдром, варикозная болезнь нижних конечностей, которые заметны визуально («звездочки» и венозная сетка при варикозе, изменение цвета кожи при ангиоспастическом синдроме). Но есть симптомы, которые редко связывают с заболеваниями сосудов.
Например, кратковременная потеря зрения на один глаз, онемение или нарушение движений в руке или ноге (рука на несколько минут повисла как плеть) могут свидетельствовать о закупорке сонных артерий. Это серьезная проблема, которая может спровоцировать инсульт головного мозга. По неприятным ощущениям или боли в икроножной мышце после ходьбы на небольшую дистанцию можно заподозрить заболевания артерий нижних конечностей. В тяжелых случаях эта болезнь может привести даже к гангрене и ампутации конечности, поэтому чтобы не допустить осложнений нужно обязательно пройти диагностику и начать лечение.
Как следить за здоровьем сосудов?
Сосудистые хирурги рекомендуют пациентам старше 45 лет регулярно следить за уровнем холестерина и глюкозы крови, контролировать артериальное давление. Если близкие родственники перенесли инфаркт или инсульт, болели сахарным диабетом – скрининг нужно проходить раз в 3 месяца. Этих обследований достаточно, чтобы вовремя заподозрить неполадки сосудистой системы и принять меры.
Если вам необходима консультация узкого специалиста – сосудистого хирурга, вы можете обратиться в консультативную поликлинику ЗОКБ (направление не обязательно). После приема специалист даст вам рекомендации, при необходимости – назначит дополнительные обследования или направит на стационарное лечение.
Церебральный ангиоспазм у пострадавших с тяжелой черепно-мозговой травмой Текст научной статьи по специальности «Клиническая медицина»
ОБЗОР
© КОЛЛЕКТИВ АВТОРОВ, 2015 УДК 617. 51-001.4-06:616.831-005.4
51-001.4-06:616.831-005.4
ЦЕРЕБРАЛЬНЫЙ АНГИОСПАЗМ У ПОСТРАДАВШИХ С ТЯЖЕЛОЙ ЧЕРЕПНО-МОЗГОВОЙ ТРАВМОЙ
Карпунин А.Ю.1, Петриков С.С.2, КрыловВ.В.2
‘МЗ РФ Государственное бюджетное учреждение Рязанской области «Областная клиническая больница», 390039, Рязань; 2НИИ скорой помощи им. Н.В. Склифосовского, Москва
Церебральный ангиоспазм (ЦА) является одним из факторов вторичного повреждения головного мозга у пострадавших с черепно-мозговой травмой (ЧМТ), увеличивающим риск неблагоприятного исхода заболевания. Частота развития ЦА находится в диапазоне от 18 до 70% и зависит не только от факторов, связанных с самим пациентом, но и от применяемых методов и критериев диагностики. Наряду с цифровой субтракционной ангиографией, являющейся «золотым стандартом» в диагностике ЦА, транскраниальная допплерография остается единственным прикроватным методом выявления и мониторинга ЦА со значимой чувствительностью и специфичностью./cerebrovascular-accident-502865123-575ada3c5f9b58f22ea68c7c.jpg) Однако количество эффективных лечебных опций ограничено, а методы, применяемые для лечения пациентов с аневризматическим суба-рахноидальным кровоизлиянием, имеют смешанные результаты при использовании у пострадавших с тяжелой ЧМТ, осложнившейся развитием ЦА. В настоящее время небольшое количество клинических данных ограничивает число рекомендаций по диагностике и интенсивной терапии ЦА у пострадавших с тяжелой ЧМТ, что, безусловно, требует проведения проспективных исследований, для формирования ориентированной на пациента лечебной программы.
Однако количество эффективных лечебных опций ограничено, а методы, применяемые для лечения пациентов с аневризматическим суба-рахноидальным кровоизлиянием, имеют смешанные результаты при использовании у пострадавших с тяжелой ЧМТ, осложнившейся развитием ЦА. В настоящее время небольшое количество клинических данных ограничивает число рекомендаций по диагностике и интенсивной терапии ЦА у пострадавших с тяжелой ЧМТ, что, безусловно, требует проведения проспективных исследований, для формирования ориентированной на пациента лечебной программы.
Ключевые слова: церебральный ангиоспазм; черепно-мозговая травма.
Для цитирования: Неврологический журнал. 2015; 20(1): 42-48.
Karpunin A.Yu., 2Petrikov S.S., 2Krylov V.V.
CEREBRAL VASOSPASM IN PATIENTS WITH SEVERE TRAUMATIC BRAIN INJURY
‘Regional Hospital of the Ministry of Health of Russian Federation, 390039, Ryazan, Russian Federation
2N. V. Sklifosovsky Federal Research Institute of Emergency Medicine, Moscow, Russian Federation
V. Sklifosovsky Federal Research Institute of Emergency Medicine, Moscow, Russian Federation
Cerebral vasospasm (CV) is one of the factors of secondary brain lesion in patients with brain injury (BI) that increases the risk of unfavorable outcomes of the disease. The incidence of CV varies from 18 to 70% and depends not only on the patients but also on the methods and criteria of diagnosis. Like digital subtraction angiography is a gold standard in CV diagnosis, the transcranial doppler ultrasonography is the only bed-side test with high sensitivity and specificity for revealing CV. The spectrum of effective treatment options is limited and methods used in treatment of patient with aneurismal subarachnoid hemorrhage are not matched to patients suffered from severe brain injury complicated by CV because of unclear outcomes. Nowadays there are limited clinical data for drawing up guidelines for diagnosis and management of CV in patients with severe BI. This fact urges prospective researches for elaborating management programs for such patients.
This fact urges prospective researches for elaborating management programs for such patients.
Key words: cerebral vasospasm; brain injury
Citation: Nevrologicheskiy zhurnal. 2015; 20(1): 42-48.
Черепно-мозговая травма (ЧМТ) является основной причиной смерти и инвалидизации лиц трудоспособного возраста [1, 2]. Частота ЧМТ колеблется от 180 до 220 на 100 000 населения в год, заболеваемость увеличивается ежегодно на 2%, а тяжелые
Сведения об авторах:
Карпунин Андрей Юрьевич (Karpunin Andrey Yuryevich) — зав. отд-нием реанимации и интенсивной терапии ГБУ РО «ОКБ», e-mail: [email protected], 390039, г. Рязань, ул. Интернациональная, дом 3а; Петриков Сергей Сергеевич (Petrikov Sergey Sergeyevich) — д-р мед.наук, проф., зам. директора, рук. регионального сосудистого центра НИИ СП им. Н.В. Склифосовского e-mail: [email protected]; Крылов Владимир Викторович (Krylov Vladimir Viktorovich) — акад. РАН, д-р мед. наук, проф., зав. каф. нейрохирургии и нейрореанимации Московского государственного медико-стоматологического университета, рук. отд-ния неотложной нейрохирургии НИИ скорой помощи им. Н.В. Склифосовского
формы встречаются более чем у 40% пострадавших. Летальность при всех формах ЧМТ составляет 7%, а при тяжелой варьирует от 28-32% до 65-81% [3]. Ежегодно в Российской Федерации ЧМТ получают около 600 тыс. человек, 50 тыс. из них погибают, еще 50 тыс. становятся инвалидами [3]. В США от ЧМТ ежегодно погибают около 53 тыс. человек [4, 5].
Патогенез ЧМТ инициируется непосредственным приложением первичных повреждающих факторов, разных по силе, биомеханике, длительности воздействия на кости черепа, мозговые оболочки, мозговую ткань, сосуды мозга, ликворную систему и вызывающих различные по тяжести морфофунк-циональные изменения [1, 6-8]. Однако, помимо первичных факторов повреждения, серьезную роль в патогенезе ЧМТ играют вторичные механизмы поражения мозга, которые приводят к формированию нейропатологических синдромов острой церебраль-
ной недостаточности [9]. К факторам вторичного повреждения относят патологические изменения гомеостаза, способные вызвать нарушения перфузии пораженных участков головного мозга и зоны пенумбры. Посттравматические нарушения кровообращения головного мозга приводят к возникновению ишемических очагов или увеличению уже существующих, вызывают расширение зон травматического некроза, а также затрудняют поступление лекарственных препаратов к месту патологических изменений [2]. У 45-80% умерших в результате травматического повреждения головного мозга при па-тологоанатомическом исследовании выявляют признаки микроциркуляторных расстройств и ишемии головного мозга [1, 5, 9].
Современная доктрина интенсивной терапии тяжелой ЧМТ основана на концепции профилактики и лечения вторичных повреждений головного мозга. (2006) определил ангиоспазм как «отсроченное сужение крупных артерий основания мозга после субарахноидаль-ного кровоизлияния (САК), часто ассоциированное с уменьшением перфузии в области, кровоснабжаемой пострадавшей артерией» [5]. В зависимости от степени выраженности и распространенности, ЦА может сопровождаться развитием ишемии мозга, которая при стойком нарушении церебрального кровотока способна приводить к формированию инфарктов мозга [1, 2, 4, 14].
В патогенезе ЦА выделяют два основных этапа. Сначала возникает преходящий спазм артерий в ответ на САК, а затем развивается стойкое сужение просвета артерий, обусловленное воздействием сгустка крови и продуктов его распада на сосудистую стенку. Развитие ЦА сопровождается фиброзом сосудистой стенки, возникающим в результате увеличения количества коллагена, и качественных изменений его структуры [15]. Ю.А. Медведев и со-авт. (1998) отметили стадийность патоморфологиче-ских изменений артериальных сосудов у пациентов после разрыва артериальных аневризм с прижизненно диагностированным ЦА. Авторы выявили массивную десквамацию эндотелия, с нарушенной меж- и внутриклеточной организацией эндотелио-цитов и клеточную эмболизацию ими дистальных отделов артериального русла, и определили эти изменения как поверхностный, асептический эксуда-тивно-некротический эндоартериит [16]. Некоторые авторы отмечают, что часть изменений при сосудистом спазме может быть связана с воспалительной реакцией в ответ на САК [15].
Следует отметить, что несмотря на то что посттравматический вазоспазм может существенно вли-
ять на прогноз тяжелой ЧМТ, в доступной нам литературе практически отсутствуют исследования, посвященные диагностике и лечению этого серьезного осложнения.
Частота и сроки развития ЦА
Посттравматический ангиоспазм (ПТА) впервые описан Б. Со1итпе11а и соавт. в 1963 г. Н. БгешёепГеК и И. Зипёсхот в 1963 г. при проведении ангиографии также выявляли ПТА у 10-15% пострадавших с тяжелой ЧМТ [17]. В дальнейших исследованиях частота ПТА колебалась от 18,6 до 50% [18]. Так, по данным И.К. Когёе81аш и соавт., полученным при исследовании у пострадавших с проникающей ЧМТ, частота ЦА составила 42,4% [19]. А.С. Болюх и соавт. наблюдали ПТА у 28,2% больных с ЧМТ [4]. В. Иотпег и со-авт. выявили ЦА у 28-41% пострадавших с тяжелой ЧМТ [17]. М. Наёаш и соавт. наблюдали увеличение частоты ПТА от 43 до 58% при травматическом САК, по сравнению с пациентами с ЧМТ без признаков травматического САК [20]. По данным большинства исследователей, ПТА развивается через 12 ч — 5 дней после травмы и продолжается от 12 ч до 30 сут [1, 9]. Некоторые авторы считают, что генерализованный ПТА развивается уже через 12-48 ч после травмы, начинаясь с бассейна задних мозговых артерий, достигает пика на 5-13-е сутки и продолжается 2-3 нед [18]. В. Аттташоиг и соавт. отметили, что у пострадавших с ЧМТ ангиоспазм развивался на 3-5-е сутки после травмы [5]. М. ОеЛе1 и соавт. определяли сроки развития церебрального вазоспазма у 299 пациентов с ЧМТ методом транскраниальной ультразвуковой допплерографии (ТКДГ). Авторы выявили, что у 50% пострадавших пик развития ПТА пришелся на 3-и сутки после травмы [18]. В ряде клинических исследований и руководств определены паттерны магистрального мозгового кровотока и их зависимость от тяжести ЧМТ, вида травматического повреждения головного мозга, а также влияние на исход заболевания. Частота ангиоспазма после травматического САК достигает 70%, а у 17-40% пациентов с ПТА развивается отсроченный неврологический дефицит, связанный с формированием инфарктов головного мозга [17]. Так Л.Я. Кравец и соавт. при исследовании церебрального кровотока у пациентов с ЧМТ выделили 3 типа нарушений мозгового кровотока: затрудненную перфузию (гипоперфузию), ангиоспазм, гиперперфузию. У большинства пациентов нарушения имели нестойкий характер [21]. Некоторые исследователи считают, что фаза гипоперфузии характеризует первые сутки после ЧМТ, гиперперфузии возникает на 2-3-и сутки, а ангиоспазм развивается на 4-15-е сутки. Большинство авторов отмечают, что сочетание затрудненной перфузии и ангиоспазма является фактором риска развития ишемических повреждений головного мозга и неблагоприятного прогноза заболевания [1, 14, 19, 22].
Факторы риска развития ЦА
Определение влияния различных факторов на развитие ПТА является крайне сложной задачей в
связи с многообразием клинических форм тяжелой ЧМТ и вызываемых ею интра- и экстрацеребральных нарушений. Количество исследований, посвященных поиску факторов риска ЦА у пострадавших с тяжелой ЧМТ, невелико.
Многие авторы указывают на причинно-следственную связь между наличием крови в субарахно-идальном пространстве и развитием вазоконстрик-торного ответа, выраженность которого напрямую зависит от количества излившейся крови [15, 21-24]. Так, в исследованиях Национального института Здоровья (США) и Европейского консорциума по ЧМТ отмечено, что наличие САК, определяемого при компьютерной томографии головного мозга, является независимым прогностическим фактором неблагоприятного исхода тяжелой ЧМТ [8]. C.M. Fisher и соавт. выявили корреляцию между анатомической формой САК и развитием симптомного ЦА у больных с нетравматическим САК. В данном исследовании авторы показали влияние анатомической формы САК после разрыва артериальной аневризмы на частоту развития симптомного ЦА [25]. В дальнейшем J. Claassen и соавт. выявили взаимосвязь развития ЦА не только с количеством излившейся крови, но и ее расположением в ликворных пространствах головного мозга, и определили наличие крови в боковых желудочках головного мозга, как наиболее неблагоприятную анатомическую форму САК при разрыве церебральных аневризм [5]. A. Chieregato и со-авт. установили корреляционную взаимосвязь между анатомической формой травматического САК и прогрессированием поражения травмированного головного мозга по данным компьютерной томографии. Так, у 36 пациентов с тяжелой ЧМТ частота неблагоприятных исходов нарастала с увеличением выраженности САК по шкале С.М. Fisher и в группах с 3-й и 4-й формами кровоизлияния составила 64 и 100% соответственно. Преимущественно ба-зальная локализация сгустков крови также повышала риск неблагоприятного исхода заболевания [25]. По данным Д.В. Свистова и соавт., констриктив-но-стенотическая артериопатия (КСА) достоверно чаще развивалась у пострадавших с тяжелой ЧМТ, сопровождавшейся массивным базальным САК (3-я и 4-я форма кровоизлияния по шкале С.М. Fisher) [23]. В работах Т. Machi и соавт., Н. Okado и соавт., М.И. Mayberg и соавт. определена важная роль ок-сигемоглобина и продуктов его распада в развитии церебральной вазоконстрикции у пациентов с САК вследствие разрыва церебральных аневризм [4, 8, 18]. K. Shahlaie и соавт. определили гипертермию при поступлении в стационар как один из факторов риска развития ПТА у пострадавших с тяжелой ЧМТ [19]. Некоторые авторы выявили значительную роль диффузных повреждений головного мозга в развитии ПТА [14, 23]. Так, Д.В. Свистов и соавт. показали увеличение частоты констриктивно-стенотической артериопатии у пострадавших со множественными внутричерепными повреждениями: эпи-, субдураль-ными и внутримозговыми гематомами, очагами уши-ба-размозжения головного мозга [23].
Ряд исследователей, отмечая связь ПТА с наличием эпидуральных и субдуральных гематом, не обнаружили корреляции между развитием ЦА и наличием САК [19]. Так А.С. Болюх и соавт. отметили увеличение частоты ЦА при преимущественно ба-зальной локализации ушибов головного мозга. ПТА был отмечен у 88,2% пострадавших с базальным расположением ушибов головного мозга и у 11,8% больных с конвекситальными очагами ушиба [22]. N.A. Martin и соавт. обнаружили взаимосвязь между развитием спазма средней мозговой артерии и наличием кровоизлияний в ликворных пространствах: внутри-желудочковом, субарахноидальном, субдуральном. Авторы наблюдали ПТА у 14-25% пациентов с кровоизлиянием в области одного, 65-78% — двух и 100% — трех ликворных пространств соответственно [5]. Посттравматический ангиоспазм может развиваться в области, отдаленной от очага повреждения или кровоизлияния. Описаны клинические наблюдения развития выраженного ангиоспазма на стороне, кон-тралатеральной основному повреждению [17]. Важно отметить, что в ряде случаев ПТА развивается при отсутствии внутричерепного кровоизлияния [9]. А.Ю. Зубков и соавт. регистрировали ангиоспазм у 29,6% пациентов с тяжелой ЧМТ без признаков САК. Авторы обнаружили корреляцию между развитием ЦА и наличием эпидуральных и субдуральных гематом, и не обнаружили какой либо связи частоты ЦА с паренхиматозными, внутрижелудочковыми или суба-рахноидалными кровоизлияниями [9]. N.A. Martin и соавт. также наблюдали ПТА у пациентов, у которых отсутствовали признаки субарахноидального или внутримозгового кровоизлияния на компьютерных томограммах головного мозга [19].
Некоторые авторы связывают ПТА с механическими причинами и повреждением эндотелия сосудов, которое сопровождается уменьшением количества потенциальных вазодилататоров (простаци-клин, оксид азота и его дериваты) и каскадным увеличением уровня вазоконстрикторных агентов (ка-техоламины, эндотелин-1, ангиотензин, продукты распада фибрина и гемоглобина, простагландины, тромбоксан и другие). Такие повреждения позволяют внутрисосудистым вазоактивным агентам и лейкоцитам достигать гладкомышечных клеток медии, вызывая в них функциональные и структурные нарушения, приводящие к развитию констриктивно-стенотической артериопатии [1, 16, 19]. Установлено негативное влияние артериальной гипертензии, повышения внутричерепного давления и кровоизлияния в субарахноидальное пространство на трансэн-дотелиальную проницаемость, изменения которой приводят к выраженным нарушениям гематоэнце-фалического барьера и развитию диффузного отека головного мозга [5, 16].
Следует отметить, что количество исследований, посвященных изучению факторов риска развития ЦА у пострадавших с тяжелой ЧМТ, крайне невелико, а имеющиеся данные не позволяют выделить наиболее важные патологические изменения, приводящие к возникновению спазма.
Диагностика ЦА
Ранняя диагностика ангиоспазма является актуальным вопросом интенсивной терапии пострадавших с тяжелой ЧМТ [14, 26]. В доступной нам литературе практически отсутствуют работы по диагностике ЦА у пострадавших с тяжелой ЧМТ. Диагностический поиск необходимо начинать через 24-48 ч с момента травмы и проводить его у всех пациентов с тяжелой ЧМТ и высоким риском развития ПТА [22]. Полиморфизм неврологических нарушений при тяжелой ЧМТ и нахождение пациента в коматозном состоянии затрудняют диагностику ЦА по клиническим симптомам [15].
В настоящее время для диагностики ПТА используют: церебральную ангиографию (ЦАГ), КТ-ангиографию, магнитно-резонансную ангиографию и ТКДГ.
ЦАГ, или цифровая субтракционная ангиография, — метод рентгеноконтрастного исследования сосудов головного мозга, который позволяет определить наличие нарушений кровотока по сосудам мозга, тонус и калибр сосудов, пути шунтирования и компенсаторного перетока, при необходимости одномоментно провести эндоваскулярное лечение локального ангиоспазма методами баллонной или химической ангиопластики и оценить его результаты [5, 15]. В настоящее время ЦАГ является «золотым стандартом» диагностики ангиоспазма [5]. Чувствительность ЦАГ в диагностике ЦА у пострадавших с ЧМТ не определена, а у больных с нетравматическим САК составляет 97-98%. Диагностическим критерием ангиографического ангиоспазма является сужение просвета артериального сосуда — на 25% (легкий), 25-50% (умеренный) и более 50% (тяжелый). Основными недостатками метода являются нагрузка контрастным веществом и невозможность проведения частых повторных исследований.
КТ-ангиография (КТА) — метод нейровизуали-зации, который отчасти лишен рисков, связанных с ЦАГ. Метод основан на технике спиральной КТ с использованием контрастного усиления йодсодержа-щим препаратом. Безусловными преимуществами КТА перед ЦАГ являются меньшая инвазивность, возможность 3Б-визуализации и многоугольной интерпретации полученных данных. По данным G.B. Anderson и соавт., КТА может заменить ЦАГ в диагностике ЦА у пациентов с нетравматическим САК, так как чувствительность метода составляет 85-98% [27]. Y. Otawara и соавт. определили, что чувствительность и специфичность КТА в обнаружении ЦА после аСАК составляет 64 и 96% соответственно [8].
Магнитно-резонансная ангиография (МРА) -метод неинвазивного исследования сосудов головного мозга, позволяющий оценить как анатомическую структуру церебральной сосудистой сети, так и функциональные характеристики кровотока. МРА — это отображение текущей в сосудах крови, создающей контраст со стационарными тканями. МРА-импульсные последовательности позволяют получить изображения, чувствительные к разным скоростям и направлениями потоков, турбулентности, разме-
рам сосудов [1]. Чувствительность МР-ангиографии в выявлении ЦА у пострадавших с тяжелой ЧМТ не определена, а у больных с нетравматическим САК достигает 92%. Существуют данные о наибольшей чувствительности МРА в диагностике спазма передней и средней мозговой артерий [27].
Транскраниальная допплерография (ТКДГ) является единственным неинвазивным методом диагностики ЦА [28]. ТКДГ — универсальный метод, который может быть выполнен у постели больного и доступен в большинстве медицинских центров [29]. Метод основан на феномене изменения частоты ультразвуковой волны при отражении от движущихся форменных элементов крови [29]. ТКДГ позволяет измерять линейные скорости кровотока (ЛСК), определять направление кровотока, оценивать состояние ауторегуляции мозгового кровотока, резерв церебро-васкулярной реактивности [26, 30]. Допплерографи-ческая оценка ЦА основана на прямой зависимости ЛСК от объемного кровотока и обратной от диаметра просвета сосуда. Метод был предложен и впервые исследован на добровольцах и у пациентов с САК вследствие разрыва церебральных аневризм И. АазМ и соавт. На основании последующих многочисленных исследований значение средней ЛСК по средней мозговой артерии, по данным ТКДГ, стало общепринятым критерием диагностики наличия и выраженности ЦА. Динамика изменения этого показателя является признаком развития ЦА и возможного отсроченного ишемического повреждения головного мозга [20]. Так, Л.Т. Хамидова и соавт. выявили различные паттерны изменения ЛСК у больных с разрывами церебральных аневризм с различными неврологическими исходами [28]. Для дифференциальной диагностики ЦА от возможной гиперемии головного мозга К.Б. Lindegaard и соавт. предложили вычислять полушарный индекс кровотока (индекс Линдегаарда). Индекс Линдегаарда представляет собой отношение средней скорости кровотока в средней мозговой артерии к средней скорости кровотока в экстракраниальном сегменте внутренней сонной артерии (в норме до 3,0) [30]. Диагностическими критериями ЦА по данным ТКДГ считают увеличение средней ЛСК по средней мозговой артерии до 120 см/с и более и индекса Линдегаарда до 3 и более [1, 28, 29]. При ЛСК 120-200 см/с ЦА считают умеренным, более 200 см/с — выраженным [1, 9]. Необходимо отметить, что на сосудистое сопротивление интракраниальных сосудов определенное влияние оказывает внутричерепное давление, и это находит свое отражение на характеристиках допплерограммы в виде снижения диастолической скорости кровотока и повышения пульсационного индекса (ПИ). Так М. На881ег и соавт. показали, что уровень диастолической ЛСК зависит от уровня периферического сопротивления кровотоку. Низкое сосудистое сопротивление характеризуется высокой диастолической скоростью кровотока (ЛСКд), тогда как низкая ЛСКд указывает на высокое периферическое сопротивление [28]. Преимуществами ТКДГ перед другими методами оценки мозгового кровотока являются простота и доступность метода,
неинвазивность, возможность многократных обследований, длительного мониторинга и прикроватного обследования больного [29, 31]. К недостаткам метода можно отнести невозможность измерения объемных скоростей кровотока и высокую «оператор-зависимость» (например, измеренная скорость кровотока может отличаться при изменении угла наклона датчика) [19]. По данным M.A. Sloan и соавт., чувствительность ТКДГ в диагностике ангиографически выявленного ангиоспазма при аСАК составляет 67% [5]. M. Wintermark и соавт. определили, что чувствительность и специфичность ТКДГ в сравнении с ЦАГ у пациентов с нетравматическим САК составляет 71,5 и 89,7% соответственно [9]. Определенным преимуществом перед ТКДГ обладает транскраниальное дуплексное сканирование (ТКДС) интракраниальных артерий. Метод позволяет исследовать не только скоростные и спектральные характеристики сосудов, но и структуры головного мозга, а также производить коррекцию угла сканирования при измерении ЛСК, что, безусловно, влияет на точность получаемых результатов. F. Proust и соавт. при проведении сравнительного исследования ТКДГ и ТКДС в диагностике ангиоспазма у 30 пациентов с САК показали, что чувствительность ТКДС была выше, чем у ТКДГ (100 и 83% соответственно), а специфичность существенно не различалась [5].
Влияние ЦА на исходы тяжелой ЧМТ
Оценка влияния ЦА на исходы тяжелой ЧМТ крайне проблематична в связи с гетерогенностью этиопатогенетических факторов, формирующих клиническую картину заболевания и необходимостью прижизненной дифференциальной диагностики причин, вызывающих те или иные повреждения головного мозга. Y.A. Zurynski и соавт. показали, что развитие ЦА сопровождалось увеличением количества неблагоприятных исходов у пострадавших с тяжелой ЧМТ с 40 до 87% [17]. М. Hadani и соавт. выявили, что у пострадавших с ЧМТ повышение ЛСК по основной артерии до 90 см/с и более сопровождается увеличением вероятности летального исхода до 33%, а вероятности вегетативного состояния — до 42% по сравнению с пациентами, у которых наблюдали повышение ЛСК до 75 см/с. [20]. J.F. Soustiel и соавт. определили, что у пациентов с травматическим САК и выраженным спазмом базилярной артерии вероятность стойкого неврологического дефицита или смерти составила 85,3% [8]. А.С. Болюх и соавт. при обследовании пострадавших с ЧМТ отметили увеличение частоты неблагоприятных исходов заболевания при развитии ЦА на 34,1% [22]. По данным Д.В. Свистова и соавт., в группе пациентов с КСА неблагоприятные исходы ЧМТ были отмечены в 3,8 раза чаще, чем у пациентов, у которых КСА не развилась [23].
Тактика лечения ЦА у пострадавших с тяжелой ЧМТ
Несмотря на то что многие исследователи определяют развитие ЦА как один из важнейших факто-
ров риска летального исхода у пострадавших с тяжелой ЧМТ, в доступной нам литературе практически отсутствуют исследования, посвященные подходам к лечению данного грозного осложнения. Одним из вариантов лечения ПТВ является ЗН-терапия (ги-перволемия, гипертензия, гемодилюция) [8, 13]. Однако некоторые авторы показали, что рутинное применение гиперволемии и гипертензии сопровождалось ухудшением исходов при тяжелой ЧМТ [13].
В настоящее время наибольшей доказательной базой подкреплено использование для лечения ЦА блокаторов кальциевых каналов, основным из которых является нимодипин [27]. По данным мета-анализов, использование пероральных форм нимоди-пина при лечение ЦА при САК вследствие разрыва церебральных аневризм приводило к улучшению неврологических исходов заболевания, но не влияло на частоту развития ЦА [13]. В большом Европейском исследовании, в которое были включены 852 пациента с травматическим САК, была оценена клиническая эффективность нимодипина в лечении пострадавших с ЧМТ. Авторы отметили, что применение парентеральной формы препарата в течение 7 сут после травмы сопровождалось увеличением количества выздоровевших с хорошим неврологическим исходом [17]. Аналогичные результаты были получены G.D. Murray и соавт., которые дополнили описанную схему, последующим 2-недельным пе-роральным приемом нимодипина. Исследователи показали, что использование нимодипина сопровождалось снижением неблагоприятных исходов тяжелой ЧМТ с 46 до 25%. ЦА в контрольной группе развился у 37% пациентов, а в группе пациентов, которым вводили нимодипин, — у 21%. Появление очаговых ишемических изменений головного мозга диагностировали у 22% пациентов контрольной группы и только у 7% пациентов, которым назначали нимодипин [13]. Основным ограничением использования нимодипина у пострадавших с тяжелой ЧМТ является развитие артериальной гипотензии [8].
Существуют данные об использовании статинов, антагонистов эндотелина-1, неглюкокортикоидно-го аминостероида — тирилазада и сульфата магния у больных с САК вследствие разрыва церебральных аневризм для профилактики и лечения ЦА. Однако мы не обнаружили исследований, посвященных оценке эффективности этих препаратов у пострадавших с тяжелой ЧМТ.
Эндоваскулярные методы лечения симптомного ЦА используют как у пациентов с САК вследствие разрыва церебральных аневризм, так и у пострадавших с ПТА. Описаны стратегии эффективного лечения ЦА внутриартериальным введением вазо-активных препаратов (папаверин, нимодипин) и эндоваскулярной баллонной ангиопластикой [5, 8]. Впервые баллонная ангиопластика была применена Ю.Н. Зубковым и соавт. для лечения вазоспазма после САК вследствие разрыва церебральных аневризм [9]. Сутью метода является механическое расширение спазмированных проксимальных сосудов головного мозга, способствующее увеличению моз-
гового кровотока в дистальных отделах сосудистого русла при сохраненном церебральном перфузион-ном давлении. Эндоваскулярное лечение диффузного ангиоспазма, локализованного преимущественно в дистальных артериях, предпочтительно методом химической ангиопластики и при суперселективном введении препаратов максимально лишено побочных эффектов в виде повышения внутричерепного давления, судорог и угнетения стволовых рефлексов [5]. Фактором, ограничивающим широкое использование химической вазодилатации, является короткая продолжительность действия используемых препаратов. В связи с этим некоторые авторы использовали продленные инфузии препаратов. Так, А.В. Кондратьев показал положительные результаты в лечении ПТА у пострадавших с тяжелой ЧМТ методом длительной внутриартериальной инфузии сосудорасширяющих препаратов. По данным ТКДГ, интенсивность ангиоспазма в опытной группе снизилась на 39,3% [32].
Лечение церебрального вазоспазма как одного из основных факторов вторичного ишемическо-го повреждения мозга при тяжелой ЧМТ является сложной мультидисциплинарной и малоизученной проблемой. Неоднозначные, порой противоречивые результаты рандомизированных исследований по оценке эффективности тех или иных методов лечения по всей видимости связаны с многообразием этиологических факторов и сложностью патогенетических синдромов, определяющих течение тяжелой ЧМТ.
Заключение
Таким образом, ЦА является грозным осложнением тяжелой ЧМТ и фактором риска неблагоприятного исхода заболевания. Однако при анализе литературы обращает на себя внимание небольшое количество работ, посвященных профилактике и лечению этого осложнения у пострадавших с тяжелой ЧМТ. До конца не определены частота и сроки развития ЦА, а также факторы, способствующие его возникновению. До настоящего времени отсутствуют четкие протоколы диагностики и лечения посттравматического ангиоспазма. Все это свидетельствует о необходимости проведения дальнейших исследований ЦА при тяжелой ЧМТ.
ЛИТЕРАТУРА
1. Коновалов А.Н., ред. Клиническое руководство по черепно-мозговой травме. М.: Антидор; 1998; т. 1-3.
2. Лебедев В.В. Крылов В.В. Неотложная нейрохирургия: Руководство для врачей. М.: Медицина; 2000.
3. Потапов А.А., Крылов В.В., Лихтерман Л.Б. и др. Современные рекомендации по диагностике и лечению тяжелой черепно-мозговой травмы. Вопросы нейрохирургии им. Н.Н. Бурденко. 2006; 1: 3-8.
4. Bouma G.J., Muizelaar J.P., Choi S.C. et al. Cerebral circulation and metabolism after severe traumatic brain injury: the elusive role of ischemia. J. Neurosurg. 1991; 75(5): 685-93.
5. Greenberg M.S. Handbook of Neurosurgery. 6th ed. New York: Thieme New York; 2006.
6. Кондратьев А.Н., Крылов В.В., Парфенов А.Л. и др. Клю-
чевые вопросы патофизиологии центральной нервной системы. В кн: Гельфанд Б.Р., Салтанов А.И., ред. Интенсивная терапия: национальное руководство. М.: ГЭОТАР-Медиа; 2009; т. 2.
7. Петриков С.С., Солодов А.А., Титова Ю.В., Гусейнова Х.Т., Крылов В.В., Хамидова Л.Т. Внутричерепное давление, церебральная перфузия и метаболизм в остром периоде внутричерепного кровоизлияния. Вопросы нейрохирургии им. Н.Н. Бурденко. 2009; 1: 11-7.
8. Haddad S.H., Arabi Y.M. Critical care management of severe traumatic brain injury in adults. Scand. J. Trauma, Resusc. Emerg. Med. 2012; 12: 2-15.
9. Zubkov A.Y., Pilkington A.S., Bernanke D.H., ParentA.D., Zhang J. Posttraumatic cerebral vasospasm: clinical and morphological presentations. J. Neurotrauma. 1999; 16: 763-70.
10. Белкин А.А., Зислин Б.Д., Аврамченко А.А. и др. Синдром церебральной недостаточности как концепция нейрореани-матологии. Анестезиология и реаниматология. 2008; 2: 4-8.
11. Щеголев А.В. Дифференцированный подход при формировании стратегии и тактики интенсивной терапии пострадавшим с тяжелой черепно-мозговой травмой: Дисс. … д-ра мед. наук. СПб.; 2009.
12. Scarabino Т., Salvolini U., Jinkin J.R. Emergency neuroradiology. Berlin; Heidelberg: springer; 2006.
13. Macdonald R. L. Management of cerebral vasospasm. Neurosurg. Rev. DOI 10.1007/s10143-005-0013-5.
14. Берснев В.П., Зубков А.Ю. Общая характеристика посттравматического вазоспазма. В кн.: Повреждения мозга (мини-мально-инвазивныеспособы диагностики и лечения): материалы 5-гомеждународного симпозиума. СПб.; 1999; 23-5.
15. Крылов В.В., Гусев С.А., Титова Г.П., Гусев A.C. Сосудистый спазм при субарахноидальном кровоизлиянии. М.: Медицина; 2000.
16. Медведев Ю.А., Зубков Ю.Н., Закарявичус Ж. Постгеморрагическая констриктивно-стенотическая артериопатия, как составная часть церебрального ангиоспазма. Нейрохирургия. 1998; 1: 22-7.
17. Shahlaie K., Boggan J.E., Latchaw R.E, Cheng J., Muizelaar J.P. Posttraumatic vasospasm detected by continuous brain tissue oxygen monitoring: Treatment with intraarterial verapamil and balloon angioplasty. Neurocrit. Care. 2009; 10: 61-9.
18. Oertel M., Boscardin W.J., Obrist W.D. et al. Posttraumatic vasospasm: the epidemiology, severity, and time course of an underestimated phenomenon: a prospective study performed in 299 patients. J. Neurosurg. 2005; 103: 812-24.
19. Shahlaie K. et al. Risk factors for posttraumatic vasospasm J. Neurosurg. 2011; 115: 602-11.
20. Hadani M., Bruk B., Ram Z., Knoller N., Bass A. Transiently increased basilar artery flow velocity following severe head injury: a time course transcranial Doppler study. J. Neurotrauma. 1997; 14: 629-36.
21. Кравец Л. Я., Зубов А. А., Трофимов А. О. Осложнения травматического субарахноидального кровоизлияния. В кн.: Материалы III Съезда нейрохирургов России. СПб.; 2002; 90-1.
22. Болюх А.С., Педаченко Е.Т. Церебральный вазоспазм при травматических внутричерепных кровоизлияниях. В кн.: Материалы III Съезда нейрохирургов России. СПб.; 2002: 13-4.
23. Свистов Д.В., Савчук А.Н. Допплерографическая картина сосудистого спазма при травматическом субарахноидальном кровоизлиянии. Регионарное кровообращение и микроциркуляция. 2003; 2 (10): 39-44.
24. Macdonald R.L., Weir B.K. A review of hemoglobin and the pathogenesis of cerebral vasospasm. Stroke. 1991; 22: 971-82.
25. Fisher C.M., Kistler J.P., Davids J.M. Relation of cerebral vasospasm to subarachnoid haemorrhage visualized by computerized tomographic scanning. Neurosurgery. 1980; 6: 1-9.
26. Крылов В.В., Петриков С.С., Белкин А.А. Лекции по нейро-реанимации. М.: Медицина; 2009.
27. Connolly E.S. Jr, Rabinstein A.A., Carhuapoma J.R., Derdeyn C.P., Dion J., Higashida R.T Guidelines for the management of aneurysmal subarachnoid hemorrhage. Stroke. 2012; 43: 171137.
28. Куксова Н.С., Хамидова Л.Т., Трофимова Е.Ю. Оценка функционального состояния головного мозга при нетравматическом субарахноидальном кровоизлиянии. Часть I. Сосудистый спазм, ишемия мозга и электрическая активность. Нейрохирургия. 2011; 3: 34-42.
29. Белкин А. А., Алашеев А.М., Инюшкин С.Н. Транскраниальная допплерография в интенсивной терапии. Екатеринбург: Издательство Клинического института мозга СУНЦ РАМН; 2004.
30. Lindegaard K.F., Nornes H., Bakke S.J. et al. Cerebral vasospasm diagnosis by mean of angiography and blood velocity measurements. Acta Neurochir. 1989; 100 (1-2): 12-24.
31. Петриков С.С., Крылов В.В. Нейромониторинг у больных с внутричерепными кровоизлияниями. Часть 2. Оценка мозгового кровотока и нейрофизиологический мониторинг. Нейрохирургия. 2010; 5: 5-10.
32. Кондратьев А.В. Церебральная гемодинамика при тяжелых изолированных и сочетанных черепно-мозговых травмах и ее коррекция длительной артериальной инфузией: Дисс.. кан. мед. наук. Хабаровск; 2006.
REFERENCES
1. Konovalov A.N., ed. Clinical Guidelines аor Traumatic Brain Injury. 1st ed. Moscow: Antidor; 1998; vol. 1-3. (in Russian)
2. Lebedev V.V. Krylov V.V. Emergency Neurosurgery: Guide for Physicians. Moscow: Meditsina; 2000. (in Russian)
3. Potapov A.A., Krylov V. V., Likhterman L.B. et al. Current recommendations for the diagnosis and treatment of severe traumatic brain injury. Voprosy neyrokhirurgii im. N.N. Burdenko. 2006; 1: 3-8. (in Russian)
4. Bouma G.J., Muizelaar J.P., Choi S.C. et al. Cerebral circulation and metabolism after severe traumatic brain injury: the elusive role of ischemia. J. Neurosurg. 1991; 75(5): 685-93.
5. Greenberg M.S. Handbook of Neurosurgery. 6th ed. New York: Thieme New York; 2006.
6. Kondrat’ev A.N., Krylov V.V., Parfenov A.L. e al. Key issues of the pathophysiology of the central nervous system. In: Gel’fand B.R. Saltanov A.I., eds. Intensive Care: National Guedlines. []. Moscow: GEOTAR-Media; 2009; vol. 2. (in Russian)
7. Petrikov S.S., Solodov A.A., Titova Yu.V., Guseynova Kh.T., Krylov V.V., Khamidova L.T. Intracranial pressure, cerebral perfusion and metabolism in acute intracerebral hemorrhage. Vo -prosy neyrokhirurgii im. N.N. Burdenko. 2009; 1: 11-7. (in Russian)
8. Haddad S.H., Arabi Y.M. Critical care management of severe traumatic brain injury in adults. Scand. J. Trauma, Resusc. Emerg. Med. 2012; 12: 2-15.
9. Zubkov A.Y., Pilkington A.S., Bernanke D.H., Parent A.D., Zhang J. Posttraumatic cerebral vasospasm: clinical and morphological presentations. J. Neurotrauma. 1999; 16: 763-70.
10. Belkin A.A., Zislin B.D., Avramchenko A.A. et al. A syndrome of cerebral insufficiency as a concept neurocritical care. Anes-teziologiya i reanimatologiya. 2008; 2: 4-8. (in Russian)
11. Shchegolev A.V. Differentiated Approach in Shaping the Strategy and Tactics of Intensive Care Affected with Severe Traumatic Brain Injury: Diss. St. Petersburg; 2009. (in Russian)
12. Scarabino T., Salvolini U., Jinkin J.R. Emergency neuroradiology. Berlin; Heidelberg: Springer; 2006.
13. Macdonald R. L. Management of cerebral vasospasm. Neuro-
surg. Rev. DOI 10.1007/s10143-005-0013-5.
14. Bersnev V.P., Zubkov A.Yu. General characteristics of post-traumatic vasospasm. In: Brain Damage (Minimally-Invasive Methods of Diagnosis and Treatment). St. Petersburg; 1999: 23-5. (in Russian)
15. Krylov V.V., Gusev S.A., Titova G.P., Gusev A.C. Vasospasm in Subarachnoid Hhemorrhage. Moscow: Meditsina; 2000. (in Russian)
16. Medvedev Yu.A., Zubkov Yu.N., Zakaryavichus Zh. Postgemor-rhagic constrictive-stenotic arteriopathy, as part of cerebral vasospasm. Neyrokhirurgiya. 1998; 1: 22-7. (in Russian)
17. Shahlaie K., Boggan J.E., Latchaw R.E, Cheng J., Muizelaar J.P. Posttraumatic vasospasm detected by continuous brain tissue oxygen monitoring: treatment with intraarterial verapamil and balloon angioplasty. Neurocrit. Care. 2009; 10: 61-9.
18. Oertel M., Boscardin W.J., Obrist W.D. et al. Posttraumatic va-sospasm: the epidemiology, severity, and time course of an underestimated phenomenon: a prospective study performed in 299 patients. J. Neurosurg. 2005; 103: 812-24.
19. Shahlaie K. et al. Risk factors for posttraumatic vasospasm J. Neurosurg. 2011; 115: 602-11.
20. Hadani M., Bruk B., Ram Z., Knoller N., Bass A. Transiently increased basilar artery flow velocity following severe head injury: a time course transcranial Doppler study. J. Neurotrauma. 1997; 14: 629-36.
21. Kravets L. Ya., Zubov A. A., Trofimov A. O. Complications of traumatic subarachnoid hemorrhage. In: Proceedings of the 3rd International Symposium. Neurosurgerons. St. Petersburg; 2002; 90-1. (in Russian)
22. Bolyukh A.S., Pedachenko E.T. Cerebral vasospasm in traumatic intracranial hemorrhages. In: Proceedings of the 3rd International Symposium. Neurosurgerons. St. Petersburg; 2002; 13-4. (in Russian)
23. Svistov D.V., Savchuk A.N. Dopplerographic picture of vaso-spasm in traumatic subarachnoid hemorrhage. Regionarnoye krovoobrashchenie i mikrotsirkulyatsiya. 2003; 2 (10): 39-44. (in Russian)
24. Macdonald R.L., Weir B.K. A review of hemoglobin and the pathogenesis of cerebral vasospasm. Stroke. 1991; 22: 971-82.
25. Fisher C.M., Kistler J.P., Davids J.M. Relation of cerebral vaso-spasm to subarachnoid haemorrhage visualized by computerized tomographic scanning. Neurosurgery. 1980; 6: 1-9.
26. Krylov V.V., Petrikov S.S., Belkin A.A. Lectures on Neurocritical Care. []. Moscow: Meditsina; 2009. (in Russian)
27. Connolly E.S. Jr, Rabinstein A.A., Carhuapoma J.R., Derdeyn C.P., Dion J., Higashida R.T Guidelines for the management of aneurysmal subarachnoid hemorrhage. Stroke. 2012; 43: 1711-37.
28. Kuksova N.S., Khamidova L.T., Trofimova E.Yu. Evaluation of the functional state of the brain in nontraumatic subarachnoid hemorrhage. Part I. vasospasm, cerebral ischemia and electrical activity. Neyrokhirurgiya. 2011; 3: 34-42. (in Russian)
29. Belkin A. A., Alasheev A.M., Inyushkin S.N. Transcranial Doppler in the Intensive Care Unit. Ekaterinburg: Izdatel’stvo Klin-icheskogo instituta mozga, SUNTs RAMN; 2004. (in Russian)
30. Lindegaard K.F., Nornes H., Bakke S.J. et al. Cerebral vasospasm diagnosis by mean of angiography and blood velocity measurements. Acta Neurochir. 1989; 100 (1-2): 12-24.
31. Petrikov S.S., Krylov V.V. Neuromonitoring in patients with intracranial hemorrhages. Part 2. Evaluation of cerebral blood flow and neurophysiological monitoring. Neyrokhirurgiya. 2010; 5: 5-10. (in Russian)
32. Kondrat’ev A.V. Cerebral Hemodynamics in Severe Isolated and Combined Traumatic Brain Injury and its Long-Term Correction of Arterial Infusion: Diss. Khabarovsk.; 2006. (in Russian)
Влияние спазма сосудов на результаты микрохирургического лечения аневризм сосудов головного мозга в остром периоде разрыва
1. Крылов В.В., редактор. [Микрохирургия аневризм головного мозга]. Москва: 2011. Русский.
2. Крылов В.В., Калинкин А.А., Петриков С.С. Патогенез церебрального ангиоспазма и ишемии головного мозга у пациентов с нетравматическим субарахноидальным кровоизлиянием из-за разрыва аневризмы головного мозга. Неврологический журнал. 2014; 19 (5): 4-12.Русский. https://www.elibrary.ru/item.asp?id=22024290
3. Рейхерт Л.И., Остапчук Е.С., Скорикова В.Г. [Спазм сосудов головного мозга и его влияние на исходы у пациентов с субарахноидальным кровоизлиянием в аневризму]. Медицинская наука и образование Урала. 2014; 15: 2 (78): 64-68. Русский. https://www.elibrary.ru/item.asp?id=22580623
4. Миллер Б.А., Туран Н., Чау М., Прадилла Г. Воспаление, спазм сосудов и повреждение головного мозга после субарахноидального кровоизлияния. Biomed Res Int.2014; 2014: 384342. [CrossRef] [PubMed] [PubMed Central]
5. Будохоски К.П., Гилфойл М., Хельми А., Хуусконен Т., Чосника М., Кироллос Р., Менон Д.К., Пикард Д.Д., Киркпатрик П.Дж. Патофизиология и лечение отсроченной ишемии головного мозга после субарахноидального кровоизлияния. J Neurol Neurosurg Psychiatry. 2014 декабрь; 85 (12): 1343-53. [CrossRef] [PubMed]
6. Флинн Л., Эндрюс П. Успехи в понимании отсроченной церебральной ишемии после аневризматического субарахноидального кровоизлияния.F1000Res. 2015 2 ноября; 4: F1000 Faculty Rev-1200. [CrossRef] [PubMed] [PubMed Central]
7. Козлов С.Ю., Родионов С.В., Руднев М.А. Факторы прогноза хирургического лечения аневризм артерий головного мозга. Вестник новых медицинских технологий. 2012; 19 (2): 153-7. Русский. https://elibrary.ru/item.asp?id=17878921
8. Литвак С.О. Индивидуализация микрохирургической тактики при клипировании аневризм артерий головного мозга. Эндоваскулярная нейрорадиология. 2018 27 декабря; 24 (2): 52-68.Украинец. [CrossRef]
9. Штайнер Т., Джувела С., Унтерберг А., Юнг С., Форстинг М., Ринкель Г.; Европейская организация по инсульту. Рекомендации Европейской организации по инсульту по лечению внутричерепных аневризм и субарахноидального кровоизлияния. Cerebrovasc Dis. 2013; 35 (2): 93-112. [CrossRef] [PubMed]
10. Крылов В.В., Дашьян В.Г., Шатохин Т.А., Шарифуллин Ф.А., Солодов А.А., Природов А.В., Левченко О.В., Токарев А.С., Хамидова Л.Т., Куксова Н.С., Айрапетян А.А., Калинкин А.А.[Сроки открытого хирургического лечения пациентов с массивным базальным субарахноидальным кровоизлиянием (Фишер 3) из-за разрыва аневризмы головного мозга]. Российский журнал нейрохирургии. 2015 (3): 11-7. Русский. https://www.therjn.com/jour/article/view/193/194
11. Дхар Р., Скалфани М.Т., Блэкберн С., Зазулия А.Р., Видин Т., Дирингер М. Взаимосвязь между ангиографическим вазоспазмом и регионарной гипоперфузией при аневризматическом субарахноидальном кровоизлиянии. Инсульт. 2012 Июль; 43 (7): 1788-94. [CrossRef] [PubMed] [PubMed Central]
12.Макдональд Р.Л. Отсроченное неврологическое ухудшение после субарахноидального кровоизлияния. Nat Rev Neurol. 2014 Янв; 10 (1): 44-58. [CrossRef] [PubMed]
13. Форман Б. Патофизиология отсроченной ишемии головного мозга. J Clin Neurophysiol. 2016 июн; 33 (3): 174-82. [CrossRef] [PubMed]
14. Фишер С.М., Кистлер Дж. П., Дэвис Дж. М.. Связь церебрального вазоспазма с субарахноидальным кровоизлиянием, визуализированная компьютерным томографическим сканированием. Нейрохирургия. 1980 Янв; 6 (1): 1-9.[CrossRef] [PubMed]
15. Малинова В., Долатовски К., Шрамм П., Мерер О., Роде В., Мильке Д. Ранняя КТ-перфузия всего мозга для выявления пациентов с риском отсроченной церебральной ишемии после субарахноидального кровоизлияния. J Neurosurg. 2016 июл; 125 (1): 128-36. [CrossRef] [PubMed]
16. Алаббас Ф., Хадия К., Аль-Джехани Х., Аль-Кахтани С.Ю. Гипонатриемия как предиктор симптоматического вазоспазма при аневризматическом субарахноидальном кровоизлиянии. Междисциплинарная нейрохирургия.2020 июл 28: 100843. [CrossRef]
17. Крылов В.В., Гусев С.А., Титова Г.П., Гусев А.С. [Спазм сосудов после субарахноидального кровоизлияния. Клинический атлас. Москва: Макцентр. 2000. Русский. https://elibrary.ru/item.asp?id=25499951
18. Кумар G, Шахрипур РБ, Харриган MR. Спазм сосудов при транскраниальной допплерографии является прогностическим признаком отсроченной церебральной ишемии при аневризматическом субарахноидальном кровоизлиянии: систематический обзор и метаанализ. J Neurosurg. 2016 Май; 124 (5): 1257-64.[CrossRef] [PubMed]
19. Цимейко О.А., Мороз В.В. Вазоспазм при субарахноидальном кровоизлиянии после разрыва артериальной аневризмы: этиология, патогенез (Обзор литературы). Украинский нейрохирургический журнал. 2002; (2): 22-8. Украинец. http://theunj.org/article/view/91808
20. Чеканова О.В., Скрябин В.В. Оптимизация клинико-инструментальной диагностики церебрального ангиоспазма при аневризматическом субарахноидальном кровотечении. Сибирский медицинский журнал (Томск).2008; 23 (4-2): 71-5. Русский. https://elibrary.ru/item.asp?id=13043534
Спазм коронарной артерии: повод для беспокойства?
Что такое спазм коронарной артерии?
Ответ от Рекхи Манкад, доктор медициныСпазм коронарной артерии — это временное сжатие (сжатие) мышц стенки одной из артерий, по которой кровь поступает в ваше сердце. Спазм может уменьшить или полностью заблокировать приток крови к части сердца.
Если спазм длится достаточно долго, у вас может быть боль в груди (стенокардия) и даже сердечный приступ (инфаркт миокарда).В отличие от типичной стенокардии, которая обычно возникает при физической активности, спазмы коронарных артерий часто возникают в состоянии покоя, обычно между полуночью и ранним утром.
Другие названия спазмов коронарных артерий: стенокардия Принцметала, вазоспастическая стенокардия или вариантная стенокардия.
Многие люди со спазмами коронарных артерий не имеют общих факторов риска сердечных заболеваний, таких как высокий уровень холестерина и высокое кровяное давление. Но они часто курят. Вы можете снизить риск спазмов коронарных артерий, бросив курить.
Спазмы коронарных артерий могут быть вызваны:
- Употребление табака
- Воздействие холода
- Экстремальный эмоциональный стресс
- Употребление запрещенных стимуляторов, таких как амфетамины и кокаин
Лечение спазмов коронарных артерий может включать в себя такие лекарства, как:
- Нитраты, которые используются для предотвращения спазмов и быстрого облегчения боли в груди по мере ее возникновения
- Блокаторы кальциевых каналов, расслабляющие артерии и уменьшающие спазм
- Статины, которые не только снижают уровень холестерина, но и предотвращают спазмы
Если спазмы коронарных артерий приводят к опасно учащенному сердцебиению (желудочковая аритмия), ваш врач может порекомендовать имплантируемый кардиовертер-дефибриллятор (ИКД).ИКД использует электрические импульсы для восстановления нормального сердцебиения и предотвращения внезапной сердечной смерти.
Если у вас возникла внезапная боль в груди, немедленно позвоните в службу 911 или скорую медицинскую помощь.
9 января 2019 г. Показать ссылки- Picard F, et al. Вазоспастическая стенокардия: обзор современной литературы. Архив сердечно-сосудистых заболеваний. В прессе. Доступ 25 сентября 2018 г.
- Bonow RO, et al., Eds. Острые коронарные синдромы без подъема сегмента ST. В: Болезнь сердца Браунвальда: Учебник сердечно-сосудистой медицины.11-е изд. Филадельфия, Пенсильвания: Сондерс Эльзевьер; 2019. https://www.clinicalkey.com. Доступ 25 сентября 2018 г.
- Пинто Д.С. и др. Вазоспастическая ангина. https://www.uptodate.com/contents/search. По состоянию на 6 сентября 2018 г.
- Манкад Р. (заключение эксперта). Клиника Мэйо, Рочестер, Миннесота, 5 октября 2018 г.
.
EPOS ™ — C-0528
Спазм сосудов является наиболее частым и серьезным осложнением нетравматического субарахноидального кровоизлияния (САК) и составляет 23% случаев инвалидности и смертности, связанных с САК (2,3).Повторное кровотечение из артериальной аневризмы — еще один повод для определения неблагоприятных исходов лечения, которые встречаются в 17,3% случаев (2). Есть несколько известных факторов риска сосудистого спазма и повторного разрыва аневризмы. полученные при изучении болезни, оценка интенсивности и степени кровотечения, анатомические особенности аневризмы (ее …
Мы использовали компьютерное моделирование для определения изменений гемодинамических параметров при аневризме, возникающий вследствие ангиоспазма афферентных сосудов на примере модели церебральной аневризмы, созданной с использованием компьютерного дизайна, а также на двух примерах моделей базилярной аневризмы и передней коммуникативной аневризмы по данным компьютерной томографической ангиографии (КТА).Мы исследовали влияние изменения скорости кровотока и формы профилей кровотока на напряжение сдвига поверхности стенки, особенно при …
Результаты моделирования гемодинамических характеристик для модели пиковой пульсовой волны без ангиоспазма и с локальным спазмом афферентного сосуда, полученные на компьютерных моделях, показаны на рисунках 2-3. Мы видим, что увеличение кривизны афферентного сосуда приводит к увеличению площади попадания крови в аневризму.При локальном спазме афферентного сосуда скорость кровотока значительно увеличивалась в спазмированной части сосудов и, вследствие этого, в аневризме. При неизмененной аневризме скорость потока афферентных сосудов составляла ~ 0,1 …
Математическое моделирование позволяет определять, понимание и визуальное представление процессов, происходящих при кровотоке по сосудам и в аневризме, а также их изменений из-за ангиоспазма.Создание математических моделей гемодинамических изменений в условиях ангиоспазма позволит понять и прогнозировать характер осложнений, которые могут возникнуть в остром периоде кровотечения (например, повторный разрыв аневризмы), что имеет большое значение для выбора хирургической стратегии.
Елена В. Григорьева, Доктор медицины, Кандидат наук, Отделение радиологии, Научно-исследовательский институт скорой помощи имени Н.В. Склифосовского, Москва, Россия, [email protected] Владимир В. Крылов, Доктор медицины, Кандидат наук, Заведующий отделением нейрохирургии, НИИ скорой помощи имени Н.В. Склифосовского, Профессор, Академик РАМН, Москва, Россия, [email protected] Александр В. Природов, Доктор медицины, Кандидат наук, Заместитель заведующего отделением нейрохирургии НИИ скорой помощи им. Н.В. Склифосовского, Москва, Россия, [email protected] Андрей В. Гаврилов, к.м.н., Заведующий лабораторией Д.Институт …
1. Цебрал Дж. Р., Кастро М. А., Берджесс Дж. Э., Перголицци Р., Putman C.M. Характеристика церебральной аневризмы для оценки риска разрыва с использованием индивидуальных моделей компьютерной гемодинамики // Am. Дж. Neurorad. — 2005. — Т. 26. — П. 2550–2559 2.Касселл Н.Ф., Торнер Дж. К., Хейли Э. Младший, Джейн Дж. А., Адамс Х.П., Kongable G.L. Международное совместное исследование сроков хирургического вмешательства при аневризме.Часть 1: Общие результаты управления .// J Neurosurg. — 1990 г. — Том 73. — П. 18–36 3.Касселл Н.Ф., Торнер Дж. К., Джейн Дж. А., Хейли Э. Младший, Адамс Х.П .: Международный …
биологических префиксов и суффиксов: angio-
Приставка ( angio- ) происходит от греческого angeion, означающего сосуд. Эта часть слова используется при обозначении сосуда, сосуда, оболочки или контейнера.
слов, начинающихся с: (angio-)
Следующие термины разделены в алфавитном порядке с использованием первой (а при необходимости второй и третьей) буквы после слова «ангио» в качестве ориентира.
Ангиобласты к ангионевротическому отеку
Ангиобласт (ангиобласт): Ангиобласт — это эмбриональная клетка, которая развивается в клетки крови и эндотелий кровеносных сосудов. Они берут начало в костном мозге и мигрируют в области, где необходимо формирование кровеносных сосудов.
Ангиобластома (ангиобластома): Эти опухоли состоят из ангиобластов, которые развиваются в мозговых оболочках головного и спинного мозга.
Ангиокардит (angio-card-itis): Ангиокардит — это заболевание, характеризующееся воспалением сердца и кровеносных сосудов.
Ангиокарп (ангиокарп): Это термин для растения, плоды которого частично или полностью покрыты оболочкой или шелухой. Это разновидность семенников или покрытосеменных растений.
Ангионевротический отек (ангионевротический отек): Это состояние, также известное как гигантская крапивница, характеризуется отеком глубоких слоев кожи, в которых находятся кровеносные и лимфатические сосуды. Это вызвано накоплением жидкости в тканях организма и обычно возникает в результате аллергической реакции.Наиболее распространены отеки глаз, губ, рук и ног. Аллергены, которые могут вызвать ангионевротический отек, включают пыльцу, укусы насекомых, лекарства и определенные виды пищи.
Ангиогенез в ангиоиммунобластные клетки
Ангиогенез (angio-genesis): Образование и развитие новых кровеносных сосудов называется ангиогенезом. Новые сосуды образуются по мере роста и миграции клеток, выстилающих кровеносные сосуды или эндотелий. Ангиогенез важен для восстановления и роста кровеносных сосудов.Этот процесс также играет роль в развитии и распространении опухолей, которые зависят от кровоснабжения, обеспечивающего необходимый кислород и питательные вещества.
Ангиограмма (ангиограмма): Это медицинский рентгеновский снимок кровеносных и лимфатических сосудов, который обычно проводится для исследования кровотока в артериях и венах. Это обследование обычно используется для выявления закупорки или сужения сердечных артерий.
Ангиография (ангиография): После инъекции рентгеноконтрастного вещества проведено рентгенологическое исследование сосудов.
Ангиоиммунобластный (ангио-иммуно-бластный): Этот термин относится к вещам, которые характеризуются иммунобластами лимфатических узлов или относятся к ним.
От ангиокинеза до ангиопатии
Ангиокинез (ангиокинез): Также называемый вазодвиганием, ангиокинез — это спонтанное движение или изменение тонуса кровеносного сосуда. Это вызвано изменениями гладкой мускулатуры при ее расширении и сокращении.
Ангиология (ангиология): Исследование кровеносных и лимфатических сосудов называется ангиологией.Эта область исследований сосредоточена на заболеваниях сердечно-сосудистой системы, а также на профилактике и лечении сосудистых и лимфатических заболеваний.
Ангиолиз (ангиолизис): Ангиолиз относится к разрушению или растворению кровеносных сосудов, которое наблюдается у новорожденных после перевязки пуповины.
Ангиома (angi-oma): Ангиома — это доброкачественная опухоль, состоящая в основном из кровеносных и лимфатических сосудов. Они могут возникать на любом участке тела и включать различные типы, такие как ангиомы паука и вишни.
Ангиомиогенез (ангио-миогенез): Это медицинский термин, обозначающий регенерацию ткани сердца (миокарда).
Ангиопатия (ангиопатия): Этот термин относится к любому типу заболевания кровеносных или лимфатических сосудов. Церебральная амилоидная ангиопатия — это тип ангиопатии, характеризующийся накоплением белковых отложений в кровеносных сосудах головного мозга, что может вызвать кровотечение и инсульт. Ангиопатия, вызванная высоким уровнем глюкозы в крови, известна как диабетическая ангиопатия.
Ангиопластика ангиоспазма
Ангиопластика (ангиопластика): Это медицинская процедура, используемая для расширения суженных кровеносных сосудов. Катетер с наконечником баллона вставляется в закупоренную артерию, и баллон надувается, чтобы расширить суженное пространство и улучшить кровоток.
Ангиорафия (ангиорафия): Это хирургический термин, относящийся к наложению швов на сосуде, обычно кровеносном сосуде.
Ангиорексис (angio — rrhexis): Этот термин относится к разрыву сосуда, особенно кровеносного сосуда.
Ангиосаркома (анги-саркома): Этот редкий злокачественный рак возникает в эндотелии кровеносных сосудов. Ангиосаркома может возникнуть в любом месте тела, но обычно возникает в тканях кожи, груди, селезенки и печени.
Ангиосклероз (ангиосклероз): Упрочнение стенок кровеносных сосудов называется ангиосклерозом. Затвердевшие артерии ограничивают приток крови к тканям тела. Это состояние также известно как атеросклероз.
Ангиоскоп (ангиоскоп): Ангиоскоп — это особый тип микроскопа или эндоскопа, используемый для исследования внутренней части капиллярных сосудов.Это ценный инструмент для диагностики сосудистых проблем.
Ангиоспазм (ангиоспазм 🙂 Это серьезное заболевание характеризуется внезапными спазмами кровеносных сосудов из-за высокого кровяного давления. Спазм сосудов может привести к частичному закрытию участка артерии или временному нарушению кровотока к органам или тканям.
покрытосеменных на ангиотензин
Покрытосеменные (ангиоспермия): Покрытосеменные, также называемые цветковыми растениями, являются растениями, производящими семена.Для них характерны семяпочки (яйца), заключенные в яичник. При оплодотворении семяпочки развиваются в семена.
Ангиостеноз (ангиостеноз): Этот термин относится к сужению сосуда, обычно кровеносного сосуда.
Ангиостимулятор (ангиостимулятор): Ангиостимулятор означает стимуляцию и рост кровеносных сосудов.
Ангиотензин (ангиотензин): Этот нейромедиатор заставляет кровеносные сосуды сужаться.Вещества ангиотензина помогают контролировать кровяное давление, сужая кровеносные сосуды и уменьшая кровоток.
Отделение нейрохирургии — Найдите врача
Обзор
С момента основания нашего отделения мы практикуем командную медицину. Мы используем самое современное диагностическое и операционное оборудование, включая компьютерную томографию и магнитно-резонансную томографию, различные обследования по физиологии мозга и ядерную медицину, операционные микроскопы, операционную систему навигации, эндоскопию головного мозга и хирургические лазеры. Мы без проблем работаем вместе с Центром неотложной помощи и работаем по системе дежурства в нерабочее время, чтобы работать быстро и эффективно.
Болезни и экспертиза
Заболевания, пролеченные в отделении нейрохирургии
| 1. Опухоль головного мозга | 2. Заболевание сосудов головного мозга | 3. Травма головы |
|---|---|---|
| Глиобластома Менингиома Акустическая шваннома Аденома гипофиза Краниофарингиома Метастаз в головной мозг Внутрижелудочковая опухоль | Субарахноидальное кровоизлияние Церебральное кровоизлияние Церебральный инфаркт Преходящая ишемическая атака Стеноз сонной артерии Болезнь Моямоя Артериовенозная мальформация Дуральная артериовенозная фистула Синтезирующая фистула Разрушение дуральной артерии | Перелом черепа Эпидуральная гематома Субдуральная гематома Травматическая внутримозговая гематома Травматическая эпилепсия Цереброспинальная утечка Оторея / ринорея |
| 4.Заболевания позвоночника | 5. Врожденная болезнь | 6. Функциональное заболевание |
| Грыжа шейного отдела позвоночника Стеноз шейного отдела позвоночного канала (OPLL) Оссификация желтой связки Опухоль позвоночника Травма позвоночника Миеломенингоцеле | Гидроцефалия Мальформация Киари Арахноидальная киста Спинальный дисрафизм, миеломенингоцеле Синдром привязанного спинного мозга Краниосиностоз | Гемифациальный спазм Невралгия тройничного нерва Идиопатическая гидроцефалия нормального давления (iNPH) Болезнь Паркинсона Неустранимая боль |
Оборудование
Диагностическое оборудование: КТ, МРТ, различные обследования физиологии мозга, сканирование в ядерной медицине и церебральная ангиография (DSA)
1.Оперативный микроскоп Olympus OME-9000 (флуоресцентный операционный микроскоп ICG ・ 5-ALA)
2. Нейрохирургическая эндоскопическая система Olympus EndoArm
3. Нейрохирургический нейро-навигатор
4. Периоперационный нейроэлектрофизиологический мониторинг
Группа нейроэлектрофизиологического мониторинга, состоящая из профессиональных инженеров центральной физиологической лаборатории, проводит периоперационные обследования. С этого момента краниотомия опухоли головного мозга возле области речи будет проводиться под нейроэлектрофизиологическим мониторингом с учетом операции в состоянии бодрствования.
Группа нейроэлектрофизиологического мониторинга, состоящая из профессиональных инженеров центральной физиологической лаборатории, проводит периоперационные обследования. С этого момента краниотомия опухоли головного мозга возле области речи будет проводиться под нейроэлектрофизиологическим мониторингом с учетом операции в состоянии бодрствования.
5. Оборудование для транскраниальной допплеровской ультразвуковой диагностики GADELIUS (TCD)
Лечение ангиоспазма в основном проводится; скорость мозгового кровотока измеряется в период цереброваскулярного спазма после субарахноидального кровоизлияния.
Результаты
| Количество операций | FY 2011 | 2012 финансовый год |
|---|---|---|
| Краниотомия опухоли головного мозга | 17 | 26 |
| Клипирование для краниотомии | 19 | 20 |
| Удаление гематомы головного мозга | 32 | 20 |
| Удаление артериовенозной мальформации | 7 | |
| Краниопластика | 4 | |
| Удаление опухоли кости | 2 | |
| Трансназальная хирургия | 2 | |
| Непрямой анастомоз | 1 | |
| Спондилодез шейного отдела позвоночника | 8 | 3 |
| Ламинэктомия / ламинопластика | 3 | |
| Шунт спинномозговой жидкости | 11 | 19 |
| Хирургия аневризмы | 34 | 18 |
| Эмболизация | 13 | |
| Стентирование сонной артерии | 6 | |
| Тромболизис / тромбэктомия | 2 | |
| Прочие | 163 | 72 |
Вверх
% PDF-1.4 % 1 0 объект >>> эндобдж 2 0 obj > поток uuid: 207fa698-e776-4535-839e-9083aeae077bxmp.did: 4977A1595A8FE511882FC421E23B5B75adobe: docid: indd: bcf2ca23-9776-11de-88e9-fb16433481ecproof: pdf3CB01133481ecproof: pdf3CB0115128DB0113DB0115128DC: сохранено 6.0 /
Спазм коронарной артерии: что это такое и варианты лечения
Недостаточно диагностированное состояние, называемое спазмом коронарной артерии, также известное как вариантная стенокардия или стенокардия Принцметала, вызывает боль в груди у многих людей.Профессор Колин Берри объясняет состояние старшей кардиологической медсестре Эмили МакГрат.
Что такое спазм коронарной артерии?
Это стеснение в груди или боль, вызванная сужением сердечной артерии. Также может быть боль в руке или челюсти.
Эти симптомы могут возникать спонтанно или из-за холода, физических упражнений или стресса.
Эти симптомы могут возникать спонтанно или из-за холода, физических упражнений или стресса. В некоторых случаях они могут быть связаны с менструальным циклом.В отличие от стенокардии, вызванной жировыми бляшками, блокирующими артерии, ведущие к сердцу, она вызвана спазмом мышечного слоя в стенке кровеносного сосуда, что приводит к временной закупорке артерии.
У некоторых пациентов наблюдается и спазм коронарной артерии, и микрососудистая стенокардия (проблемы с мельчайшими артериями, кровоснабжающими сердце) или даже закупорка, вызванная жировыми бляшками.
Это то же самое, что стенокардия Принцметала или вазоспастическая стенокардия?
Да, это также называется вазоспастической стенокардией, и исторически она была известна как стенокардия Принцметала или вариантная стенокардия.
Как диагностируется спазм коронарной артерии?
Ангиограмма используется для получения рентгеновского изображения сердечных артерий, в то время как врач вводит дозу химического вещества, называемого ацетилхолином, которое должно вызвать расслабление кровеносных сосудов. Если кровеносный сосуд вместо этого сужается (спазм сосудов), мы можем диагностировать спазм коронарной артерии.
Что вызывает спазм коронарной артерии?
В организме есть химические вещества, вызывающие сужение кровеносных сосудов, и другие химические вещества, вызывающие расслабление кровеносных сосудов.Стресс может вызвать сужение коронарных артерий, если слишком много сжимающих химикатов и недостаточно расслабляющих. Спазм может быть связан с участками воспаления в стенке кровеносного сосуда.
Какие варианты лечения спазма коронарной артерии?
Лечится блокаторами кальциевых каналов, такими как верапамил или дилтиазем. Эти препараты работают, останавливая всасывание кальция в мышечных клетках кровеносных сосудов, что расслабляет кровеносные сосуды.Ингибиторы АПФ и статины также могут помочь здоровью кровеносных сосудов.
Каковы перспективы этих пациентов?
У некоторых это проходит само по себе. Для других это сохраняется в течение многих лет. В некоторых случаях спазм сосудов может вызвать не только стенокардию, но и сердечный приступ — серьезное и опасное для жизни событие.
У кого возникает спазм коронарной артерии?
Женщины и мужчины могут быть затронуты в равной степени. Заболевание может возникнуть в любом возрасте, но особенно у людей старше 50 лет.
Какая доступна поддержка?
В настоящее время эта группа пациентов пользуется очень слабой поддержкой.Многим ставят неправильный диагноз, они месяцами сталкиваются с повторяющейся болью в груди, и им могут сказать, что больше нет никакой помощи. Эти пациенты могут чувствовать себя лишенными поддержки и не осознавать, что у многих людей такая же проблема. Существует группа в Facebook для людей со спазмом коронарной артерии, или вы можете связаться с другими участниками сообщества BHF HealthUnlocked.
Насколько распространен спазм коронарной артерии?
Мы недавно провели исследование коронарной микрососудистой стенокардии (CorMicA), финансируемое BHF. Исследование показало, что у половины пациентов, получивших коронарную ангиограмму, сердечные артерии не закупорены.
У четырех из пяти пациентов со стенокардией без закупорки сердечной артерии был спазм коронарной артерии или микрососудистая стенокардия, или и то, и другое. Из них примерно у 17% спазм коронарной артерии возникает сам по себе.
Исследование показало, что у половины пациентов, получивших коронарную ангиограмму, сердечные артерии не закупорены.
Еще у 20% он сочетается с микрососудистой стенокардией. Таким образом, по крайней мере, каждый третий пациент со стенокардией, но без закупорки, имеет спазм коронарной артерии.(У других пациентов наблюдается микрососудистая стенокардия без спазма коронарной артерии.)
Также возможно сделать компьютерную томографию, которая показывает, что коронарные артерии чистые. Однако компьютерная томография не может показать, есть ли проблемы с мелкими сосудами или вазоспазм. Нормальный результат компьютерной томографии может дать ложную уверенность. Это означает, что они могут получить не лучшее лечение.
Наше исследование CorMicA было первым, которое показало, что регулярное тестирование этих состояний уточняет диагноз и означает, что может быть назначено наилучшее индивидуальное лечение.Это приводит к улучшению стенокардии и качества жизни.
.



 В частности соединения сероуглерода и свинца повышают напряжение сосудистой стенки, из-за чего меняется диаметр просвета сосудов, приводя к нарушению кровотока.
В частности соединения сероуглерода и свинца повышают напряжение сосудистой стенки, из-за чего меняется диаметр просвета сосудов, приводя к нарушению кровотока.