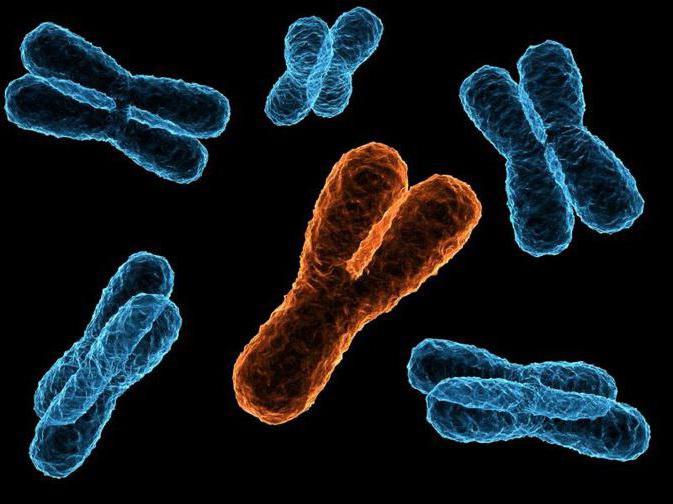
Болезнь Рандю-Ослера: диагностика и лечение
Болезнь Рандю-Ослера – это появление кровотечений из небольших капилляров (артериол или венул). Характерно, что данный процесс имеет не воспалительный характер. Чаще всего проявляется заболевание в виде сосудистых сеток (или звездочек). Но поражение сосудов возникает не только на поверхности кожного покрова. Также симптомы могут проявляться на слизистых оболочках других органов (бронхов, носа, рта, мочевого пузыря).
Болезнь Рандю-Ослера: клиника
Впервые данное заболевание описал выходец из Франции – Луи Мари Рандю. Полную же картину болезни предоставил английский специалист Уильям Ослер. Информацию дополнили и наблюдения Фредерика Вебера. Установлено, что данное заболевание передается по наследству. Ребенку достаточно унаследовать дефектный ген родителя. Страдают данным синдромом одинаково как мальчики, так и девочки. За развитие его отвечают следующие гены: первый отвечает за эндоглин, контролирует выработку гликопротеина. Второй относится к категории трансформирующих факторов роста. При их мутации сосуды теряют эластичность, наблюдаются дефекты их соединений, отклонения от нормы в строении эндотелиальных клеток. Стоит отметить, что болезнь Рандю-Ослера (диссеминированный гемангиоматоз) – состояние довольно редкое, а природа его происхождения не всегда понятна. Показатели распространенности болезни таковы: ею страдает 1 человек на 5000.

Первые симптомы развития болезни
Как правило, до 6 лет симптоматика заболевания не проявляется (несмотря на то что болезнь Рандю-Ослера передается по наследству). По достижении определенного возраста (6-10 лет) появляются первые признаки. На коже или слизистых других органов можно заметить появление ангиом (то есть опухолей сосудов). В результате дефектов капилляров и сосудов могут образовываться красные (или с оттенком синего) пятна, которые кровоточат. Болезнь Рандю-Ослера-Вебера характеризуется и низкими показателями свертываемости крови. В результате этого возможны кровотечения (даже как следствие микротравмы). Порой единственным симптомом, который может указать на наличие заболевания, являются носовые кровотечения. Также у девочек могут быть обильные менструации. Из-за частых кровотечений развивается малокровие, уровень гемоглобина падает.
Стадии заболевания
Болезнь Рандю-Ослера-Вебера имеет несколько стадий. Для каждой из них характерны определенные симптомы. На ранней стадии поражения сосудов небольшие, имеют вид мелких пятен. Промежуточная степень характеризуется наличием сосудистых звездочек, «паучков». Узловатая форма – это появление красных (круглых или овальных) узелков, которые выступают над поверхностью на несколько миллиметров. Диаметр они имеют от 5 до 7 миллиметров. При надавливании данные образования становятся бледными (все типы). Потом же они наполняются кровью.
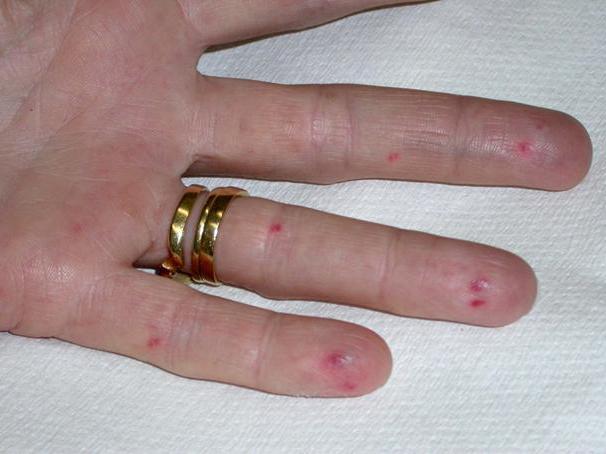
Классификация форм болезни
Как уже упоминалось, может носить наследственный характер болезнь Рандю-Ослера (фото проявлений недуга можно увидеть в этой статье), которая передается от родителей. Если таким синдромом страдают и папа, и мама, то у ребенка заболевание будет протекать в более тяжелой форме. Также существуют и спорадические случаи, которые возникают из-за мутации. В зависимости от места поражения специалисты выделяют назальный тип (кровотечения из носа), глоточный, кожный (могут кровоточить определенные участки кожи). Висцеральная форма характеризуется кровотечениями из внутренних органов. Также может наблюдаться и смешанный тип, при котором поражаются как кожные покровы, так и внутренние органы.

Болезнь Рандю-Ослера (шифр МКБ-10): факторы риска при диагнозе
Прежде всего, главным фактором опасности является наследственность. Также болезнь могут спровоцировать медицинские препараты, которые принимает беременная женщина в первые три месяца. Небезопасны и инфекционные заболевания, перенесенные в данный период. Спровоцировать кровотечение могут следующие моменты: трение одежды о поврежденные участки, высокое давление, несбалансированное питание. Отсутствие в пище необходимых микроэлементов, которые способны укрепить сосуды, – вот одна из причин их слабости. Особенно это касается сторонников вегетарианства.

Методы диагностики
Формулировка клинического диагноза при болезни Рандю-Ослера базируется на осмотре физического состояния больного. Как правило, на лице, голове, слизистых можно увидеть телеангиэктазии. Это образования красного цвета, которые выступают над поверхностью кожного покрова. Располагаться такие дефекты могут и на внутренних органах. Необходим общий анализ крови, который может указать на наличие анемии. Биохимический анализ дает возможность распознать сопутствующие инфекции и болезни. Также производится анализ мочи. Если в ней будут обнаружены эритроциты, то можно говорить о том, что развивается кровотечение почек, мочевыводящих путей. Специалист проводит ряд тестов. Проба щипка дает возможность судить о подкожных кровоизлияниях. Для проведения теста кожу под ключицей сдавливают на некоторое время. Подобную информацию дает и проба жгута (он накладывается на область предплечья на несколько минут). Если существует подозрения на болезнь Рандю-Ослера, диагностика не обходится без проведения тестов на скорость свертываемости крови, длительность кровотечения (пробивается палец). Полости тела осматриваются с помощью эндоскопа. Если наружные симптомы отсутствуют, то проводится компьютерная томография. Данный метод позволяет увидеть любые нарушения во внутренних органах.
Лечение заболевания
Болезнь Рандю-Ослера лечение предусматривает следующее. Во-первых, это консервативная терапия. Суть ее заключается в применении ингибиторов для орошения поверхности, что кровоточит. Данные медикаменты препятствуют рассасыванию сгустка крови и останавливают таким образом кровотечение. Как показывает практика, другие лекарственные средства малоэффективны. Нередко требуется оперативное вмешательство. В ходе его проведения удаляется поврежденная часть сосуда. Ее может заменить протез (если это необходимо). При носовых кровотечениях неплохой результат дает криокоагуляция. Используя жидкий азот, замораживается участок сосуда. Менее эффективным является использование лазера для прижигания. В некоторых случаях необходима гормональная терапия.
В тех случаях, когда болезнь Рандю-Ослера вызывает большие кровопотери, необходимо использование донорской крови. Дефицит компонентов, отвечающих за свертывание, восполняет переливание плазмы (свежезамороженной). Такая терапия используется при состояниях, которые угрожают жизни человека. Также в подобных случаях может понадобиться переливание донорских тромбоцитов. В случаях если пациент имеет тяжелую форму анемии (очень низкий уровень гемоглобина) или наступила анемическая кома (утрата сознания из-за нехватки кислорода для головного мозга), проводится переливание эритроцитов из крови донора. Зачастую их освобождают от белков, находящихся на поверхности.
Возможные осложнения недуга
Болезнь Рандю-Ослера, патогенез ее развития и отсутствие эффективного лечения может привести к целому ряду негативных моментов. Во-первых, развивается анемия. Значительные кровопотери способны привести к анемической коме. Человек при этом находится без сознания и никак не реагирует на внешние раздражители. Возможно также и наступление паралича. Данное заболевание может привести к слепоте (при кровотечениях в области сетчатки). Состояние внутренних органов значительно ухудшается. Опасным побочным эффектом болезни может стать кровоизлияние в головной мозг. Однако вовремя выявленное заболевание и грамотная терапия позволяют спасти здоровье и жизнь пациенту.
Профилактические мероприятия
Первичные меры профилактики необходимы еще до обнаружения проблемы. Семьи, в которых у одного или нескольких членов диагностирована болезнь Рандю-Ослера, должны проводить консультации с генетиком. Бывают случаи, когда дается рекомендация воздержаться от зачатия ребенка. Также стоит позаботиться о защитных силах организма. Хорошее действие окажут регулярные прогулки на улице, закаливание организма. Правильное питание со сбалансированным рационом также необходимо.

Вторичная профилактика заключается в регулярных осмотрах у специалистов. Ее целью является раннее выявление болезни. Если синдром уже диагностирован, то лечение должно быть своевременным и полноценным. При необходимости оперативного вмешательства пациент в обязательном порядке должен проконсультироваться с гематологом. Это позволит обезопасить человека от возникновения осложнений при операции (больших кровотечений). Каждый пациент и его близкие должны получить информацию о том, как оказывать доврачебную помощь при кровотечениях (как внутренних, так и наружных). Рекомендуется делать переливание донорских компонентов крови только в случаях крайней необходимости.
Болезнь Ослера – Рандю: причины, симптомы, диагностика, лечение
Среди генетических нарушений в работе сосудистой системы выделяется болезнь Ослера – Рандю. Как проявляется это заболевание? Чем оно опасно? Можно ли минимизировать проявления и осложнения? Подробности – далее в статье.
Что это такое
Патология нередко характеризуется под разными терминами. Все ее проявления связаны со стойким расширением сосудов наследственного характера или их кровоточивостью.
Это заболевание проявляется в деформации капилляров и множественной телеангиэктазии. Поражения располагаются на коже, слизистых оболочках, внутренних органах.
Причины
Причины возникновения синдрома Рандю-Ослера являются предметом жарких споров в медицинских кругах. Исследовательские данные ученых говорят о том, что у пациентов есть нарушение структуры трансмембранного белка эндотелиоцитов – эндоглина или киназы-1. Но это не является приобретенной формой дисплазии сосудистых оболочек.

Данное заболевание является следствием нарушений в период эмбрионального развития плода. После рождения, в лишенных нормальных защитных оболочек сосудах формируются аневризмы. Они, в свою очередь, легко поддаются разрушению, и приводит к кровотечению.
Провоцируется болезнь в результате частого продолжительного стояния на ногах в неудобной позе или такой же обуви. Избыточный вес, несоблюдения режима, малая активность и халатное отношение к своему здоровью способствуют ее возникновению.
Но главным фактором все же являются наследственные причины.
Симптомы
Сосудистые звездочки на теле обычно проявляются с сеткой капилляров. Возникновение патологии на ногах обусловлено варикозным расширением вен или гормональным сбоем.
Помимо сосудистой сетки возникают мелкие язвочки на коже. При внутренних кровотечениях отмечается бледность кожных покровов, слабость, испарина, озноб.

Начальные симптомы болезни Ослера характеризуются зудом и покалыванием в воспаленных местах. Быстрая утомляемость, стресс и гормональный сбой являются маскирующими факторами нарушения.
Как развивается
Так как заболевание происходит из-за генетической предрасположенности его можно диагностировать с ранних лет жизни ребенка. Вероятные внутриутробные отклонения у малыша можно заметить по состоянию матери во время беременности.
Патология встречается крайне редко, меньше, чем у 0.1% населения. Болезнь характеризуется следующими факторами:
- гипохромной анемией;
- стойким расширением мелких сосудов;
- венозными и капиллярными сетками на теле;
- синдромом Луи-Бара.
Большинство первичных симптомов обусловлено эмбриональным нарушением роста плода в третьем семестре. Оно влечет за собой хроническое и генетически передаваемое заболевание.

Чем опасно
Первое видимое проявление нарушения в том, что на теле возникают разного рода неприятные кровянистые язвочки. Чаще всего встречаются они на губах, но человек зачастую обуславливает это психологическим фактором их покусывания.
Самый опасное в этой патологии то, что она обычно проявляется в виде незначительных и нехарактерных симптомов. При неправильном диагнозе или отсутствии соответствующей терапии заболевание переходит в хроническую фазу.
Болезнь вызывает гематомы, внутренние и внешние кровотечения, и считается неизлечимой.
Нестерпимый зуд, вызываемый патологией, провоцирует повреждение мелких сосудов возле первичного очага.
Среди факторов о которых стоит беспокоится выделяют следующие:

- нарушение мозгового кровообращения;
- вегетососудистая дистония в прогрессирующей форме;
- наследственная кровяная телеангиэктазия;
- нарушения аутосомного типа;
- артериальная и венозная деформация;
- аневризма сосудов органов;
- новообразования, которые невозможно удалить хирургическим или другим путем;
- ЖКТ – кровотечения;
- нарушение нормальной работы органов и центральной нервной системы.
Чтобы не допускать прогрессирования, стоит внимательно относится к проявляемой симптоматике и своевременно применять терапевтические меры.
Диагностика
Данная патология быстро проникает во все ткани, органы и сосудистую систему. В основном диагностика проводится по принципу наличия внешних проявлений.

Если для полноценной диагностики внешних причин недостаточно проводятся эндоскопические обследования. В ходе процедуры устанавливается наличие внутренних кровотечений и уровень общей потери жидкости пациента.
Обязательным является прохождение ультразвуковое дуплексное сканирование. Этот метод позволяет узнать направление и скорость движения кровотока в сосудах. Только после такой манипуляции врач имеет право назначить лечение.
Лечение
Во время болезни Рандю Ослера лечение применяется в виде гемостатической терапии, с помощью 5% тромбина. Это способствует предотвращению кровотечений.
Криотерапия назначается реже, но ее эффективность выше гемостатической. В тяжелых случаях показано хирургическое вмешательство.
Прижигание сосудов, иссечение ангиом и пластика перегородок сосудов используются в случае визуально определяемых дефектов.
При развитии анемии используются препараты с повышенным содержанием железа.

Профилактические меры
Соблюдение здорового образа жизни не только поможет избежать или замедлить развитие патологии, но также укрепит иммунитет.
Больным с патологиями наследственного характера необходимо держать под контролем свое самочувствие. Им следует избегать поражения любых слизистых оболочек, чтобы не провоцировать появление болезни. Правильное питание и физическая активность помогут отсрочить обострение.
Несмотря на то, что болезнь считается неизлечимой, ее можно держать под контролем. Соблюдение рекомендаций врача способствует облегчению протекания острой фазы и уменьшает шанс рецидивов.
Современные аспекты терапии наследственной геморрагической телеангиоэктазии (болезни Рандю-Ослера).
Несмотря на определенные успехи в познании наследственной геморрагической телеангиэктазии (болезни Рандю-Ослера), особенно в области генетики, исследований висцеральных сосудистых мальформаций, вопросы лечения этого страдания остаются нерешенными. В настоящей работе приводится обзор работ, посвященных терапии болезни Рандю-Ослера, с учетом исследований последний лет; и представлены перспективные направления в решении этой проблемы.
Ливандовский Ю. А., Земсков Е. В. Современные данные о лечении наследственной геморрагической телеангиэктазии. Врач скорой помощи №12 // 2010.
Болезнь Рандю-Ослера (наследственная геморрагическая телеангиэктазия, НГТ) известна более века. Она проявляется сосудистыми изменениями типа телеангиэктазий слизистых оболочек и кожных покровов, а также висцеральными мальформациями печени, лёгких, головного мозга и других органов. Вторым важным клиническим признаком болезни служат геморрагии из телеангиэктазий носа, желудочно-кишечного тракта и т. д.. Третьим — наследственная природа болезни, которая сопряжена с аутосомно-доминантным типом наследования. Если в семье болен один из родителей, то теоретически у каждого ребёнка имеется 50% вероятность быть больным.
В последние десятилетия достигнуты несомненные успехи в молекулярной генетике, которые позволили выделить 4 типа болезни Рандю-Ослера. Многочисленные научные исследования подтвердили генетическую неоднородность заболевания. [1-3] Показано,что мутации эндоглин-корригирующего гена, расположенного на 9 хромосоме, (9q 34.1) связаны с НГТ I типа . [4-6] Второй вариант (НГТ II) вызван мутацией гена ALK 1(activin-receptor like kinase 1), который располагается на хромосоме 12, вблизи от центромеры (12q11-q19).[7-10] При этих типах НГТ мутация приводит к болезни путём гаплотической недостаточности. Доказано и существование третьего варианта (НГТ III) [11], связанного с геном, расположенным на хромосоме 5. Четвёртый вариант (НГТ IV) c проявлениями ювенильного полипоза, объясняют мутацией в гене SMAD4. [12-14]
В диагностике НГТ играют роль прежде всего, клинические признаки, а генетические исследования дополняют наши познания об этом заболевании. В последнее время появились данные, говорящие о том, что для выявления НГТ у потенциальных больных могут быть использованы и биологические показатели. Так уменьшение уровня ангиопоэтина 2 и растворимого эндоглина в крови свидетельствует в пользу данной патологии. [15]
Общие подходы лечения данного заболевания представлены в таблице 1.
Основные направления в терапии болезни Рандю-Ослера Таблица 1 .
| Клинические манифестации |
Направления терапии |
| Носовые кровотечения |
1. обычная временная тампонада носа с использованием гемостатических средств; 3. эстроген-прогестероновые препараты, тамоксифен; 4. лазерная локальная фотокоагуляция; 5. эмболизация кровоточащих сосудов; 6. операция резекции слизистой носа с последующей пластикой; 7. гипербарическая оксигенация |
| Желудочно-кишечные кровотечения |
1. эстроген-прогестероновые препараты |
| Сосудистые мальформации печени |
1. транскатетерная эмболизация сосудов |
| Артериовенозная мальформация лёгких |
1. транскатетерная эмболизация сосудов |
| Церебральные мальформации |
1. транскатетерная эмболизация сосудов 2. стереотаксическая радиотерапия |
| Постгеморрагическая анемия |
1. пероральная и парентеральная железотерапия |
Рецидивирующие носовые кровотечения обычно являются доминирующим признаком в клинической картине заболевания. Они значительно снижают качество жизни пациентов и служат причиной поиска эффективных подходов профилактики и лечения. Острые обильные носовые кровотечения могут привести к смерти. [16]
Широко применяются традиционные методы воздействия (местные гемостатические средства, тампонада носа гемостатической губкой и др. ). При значительных кровотечениях назначают этамзилат (дицинон) внутрь или внутривенно. Для борьбы с кровотечениями широко используют антифибринолитические препараты (местно, внутрь и парентерально) [17], учитывая, в частности, и факт повышения фибринолитической активности в местах телеангиэктазий.[18]
Чрескожная эмболизационная терапия остаётся методом выбора при тяжёлых массивных кровотечениях и даёт значительное улучшение качества жизни пациента как в отношении тяжести, частоты, так и продолжительности носовых кровотечений на протяжении первого месяца и года после эмболизации. Но данный метод хорош, когда выполняется опытными руками, так как сама манипуляция может стать причиной многих серьёзных осложнений. [22-24] Ещё один способ лечения жизнеугрожающих носовых кровотечений у больных НГТ такой, как дермопластика слизистой перегородки носа, так же является эффективным методом остановки кровотечений, который с одной стороны улучшает качество жизни пациента в отношении рецидивирования носовых кровотечений [25], а с другой -может приводить к различным осложнениям (появление запаха из носа, образование корок, снижение обоняния, утяжеление синусовой инфекции), ухудшающим самочувствие пациента.[26]
Было опубликовано много работ, посвящённых гормональной терапии НГТ эстрогенами [27-30], но результаты оказались неоднозначными.
Видимо, в настоящее время нецелесообразно проводить локальные термо и химио каутеризации, которые способны вызвать повреждение носовых структур.
Показано, что у больных НГТ имеется высокий уровень фактора роста эндотелия сосудов (VEGF), который может быть напрямую связан с развитием телеангиэктазий. В связи с этим, появились экспериментальные исследования применения ингибитора эндотелиального фактора роста бевацузимаба (авастатина) в виде назального спрея с целью урежения частоты носовых кровотечений. [31] В литературе есть данные о совместном использовании интраназального подслизистого введения бевацизумаба и лазерного прижигания. Результаты этого комбинированного метода лечения выявили преимущества перед назначением одного бевацузимаба. Отмечено значительнoе уменьшение степени и частоты носовых кровопотерь и снижение потребности в гемотрансфузиях, повышение работоспособности пациентов с НГТ. [32]
Прошло около девяти лет с того момента, когда впервые были описаны гемостатические эффекты тамоксифена, назначенного в качестве химиотерапии больной с раком молочной железы I стадии и НГТ.[33] И сравнительно недавно было проведено первое клиническое исследование, посвящённое влиянию антиэстрогенновой терапии тамоксифеном на выраженность носовых кровотечений при НГТ. Так у 25 пациентов, рандомизированных на две группы, был продемонстрирован положительный эффект тамоксифена в дозе 20 мг/сут в отношении частоты и тяжести носовых кровотечений. [34]
В эксперименте на культуре эндотелиальных клеток было показано повышение экспрессии белков генами ENG и ALK-1 под воздействием ралоксифена, являющегося селективным стимулятором эстрогеновых рецепторов. В связи с этим возникло предложение использовать данный препарат для лечения, к примеру, носовых кровотечений у женщин, страдающих остеопорозом, в постменопаузе.[35]
Интересные результаты были получены голландскими учёными, проводившими исследования влияния N-ацетилхолина (АЦХ) на выраженность эпистаксиса и качество жизни больных НГТ . Оказывается, АЦХ, обладая антиоксидантными свойствами, способен снижать частоту, тяжесть и продолжительность носовых кровотечений. При этом максимальный положительный эффект АЦХ наблюдался у лиц мужского пола и у носителей мутации в гене ENG, в то время как у представительниц прекрасного пола и у носителей дефекта в гене ALK-1 значительного улучшения состояния выявлено не было. [36]
В этом году группой французских учёных была впервые установлена возможность применения для лечения сосудистых дисплазий при НГТ печально известного седативного средства талидомида. В опытах на мышах, гетерозиготных по мутантному гену ENG, было показано, что лечение талидомидом способно стимулировать выработку тромбоцитарного фактора роста-В (PDGF-B) эндотелиоцитами и активировать созревание сосудистой стенки за счёт размножения интрамуральных клеток (перицитов). Прижизненное исследование назального эпителия у небольшой группы пациентов с НГТ также выявило эффективность талидомида в отношении носовых кровотечений, частота и выраженность которых значительно снизилась на фоне стабилизации сосудистой стенки и повышения уровня гемоглобина. Таким образом, как заявляют авторы работы, талидомид может стать новой стратегией лечения НГТ.[37]
При введении больных с НГТ не стоит, видимо, забывать и старых методов лечения, в частности, гипероксибаротерапию, при осуществлении которой отмечено уменьшение объёма и частоты носовых кровотечений или их прекращение более чем у половины больных. [38]
С целью профилактики носовых кровотечений следует исключить приём алкогольных напитков, включая пиво, острых блюд, уксуса, пряностей, которые, как показывают клинические наблюдения, могут провоцировать геморрагии. Не рекомендуется назначать лекарственные препараты, нарушающие функциональные свойства тромбоцитов (нестероидные противовоспалительные средства и др.), а также антикоагулянты, фибринолитики, способные ухудшить течение геморрагического диатеза.
Наружные кожные кровоточащие телеангиэктазии, которые представляют косметическую проблему, требуют локальной лазеротерапии или применения криовоздействия. [39]
При выраженных желудочно-кишечных кровотечениях с гемостатической целью применяют комбинацию низких доз эстрогена и прогестерона [40,41], механизм воздействия которых мало изучен, однако, у больных наблюдается меньшая потребность в гемотрансфузиях.
Лёгочные артериовенозные мальформации (АВМ) могут быть обнаружены почти у 30% больных с НГТ. Многие годы классическим методом лечения лёгочных сосудистых аномалий была резекция части или доли лёгкого. Но в последние десятилетия методом выбора является транскатетерная эмболизация питающих сосудов с помощью спиралей или отдельных надувных баллонов. [43-46] За последние годы число таких операций возросло, и в литературе можно встретить данные об успешном применении данной методики у детей [47], в том числе новорождённых, [48] и у женщин с различным сроком беременности [49, 50]. Также есть сообщения о проведении двум пациентам с НГТ экстренной эндоваскулярной эмболизации с отсроченным плевроцентезом по поводу спонтанного гемоторакса, развившегося в результате разрыва лёгочной АВМ. [51] Показано,что эмболотерапия питающей артерии с диаметром больше или равным 3 мм увеличивает продолжительность жизни и улучшает качество жизни больных.
Поражения печени при разбираемом заболевании могут иметь многие причины, важнейшими из которых являются сосудистые мальформации, телеангиэктазии, аневризмы, артериовенозные шунты.
Шунт из печёночной артерии в воротную вену вызывает портальную гипертензию, способствующую развитию желудочно-кишечных кровотечений, асцита. Вследствие сосудистых аномалий печени, хронической ишемии ткани этого органа возможна картина «псевдоцирроза».
Спиральная компьютерная томография выявляет у ¾ больных те или иные васкулярные аномалии в печени, у половины больных — артериопортальные шунты.
Имеется много сообщений [52-54] об успешной реализации метода эмболизации аномальных сосудов печени, но у части больных эта процедура способна вызывать развитие осложнений — некроз печёночной ткани.
Для больных НГТ с тяжёлым поражением печени единственным эффективным методом лечения на сегодняшний день является ортотопическая трансплантация печени (ОТП). [55-57]. Показаниями к трансплантации печени у больных с данной патологией могут служить следующие обстоятельства: сердечная недостаточность в связи с сосудистыми изменениями печени, билиарный некроз, ведущий к печёночной недостаточности, выраженная портальная гипертензия и т. д.
Трансплантация печени устраняет возможность развития гепатобилиарного сепсиса и предупреждает развитие сердечно-лёгочной недостаточности, значительно улучшая качество жизни пациентов.
Согласно результатам наблюдения за пациентами, перенёсшими ОТП, долгосрочная выживаемость составляет 75% (9 пациентов из 12 оперированных), при этом у выживших после трансплантации печени наблюдалось повышение качества жизни как за счёт урежения частоты носовых кровотечений, так и вследствие расширения режима физических нагрузок.[58].
В литературе встречаются единичные сообщения об успешном применении антагониста рецепторов фактора роста эндотелия бевацузимаба у больных с псевдоциррозом Ослера. Так на примере 47-летней пациентки с НГТ, с поражением печени по типу сосудистой мальформации, кахексией, холестазом, портальной гипертензией и асцитом, 12-недельный курс бевацузимаба в дозе 5мг/кг способствовал разрешению холестаза, уменьшению сердечной недостаточности и асцита, а также нормализации нутриативного статуса и, самое главное, исключения больной из списка очереди на ОТП. Как заявляют авторы статьи, применение бевацузимаба может потенциально снизить потребность в трансплантации печени у данной группы больных. [59]
Если у больных отсутствуют признаки портальной гипертензии, печёночной недостаточности, нет грубых сосудистых изменений, то специальной активной терапии им не требуется.
Сосудистые мальформации головного мозга выявляются, прежде всего, с помощью магнитно-резонансного исследования у 5-10% пациентов с НГТ. Они способны вызывать различные клинические симптомы (головную боль, эпилептические приступы, картину ишемических атак, редко — кровоизлияния).
При церебральных мальформациях могут потребоваться нейрохирургические подходы или стереотаксическая артериовенозная эмболотерапия. [60]
Вопрос о хирургическом вмешательстве при бессимптомных церебральных мальформациях, обнаруженных при магнитно-резонансном исследовании, остаётся дискутабельным.
В заключение, следует отметить, что данное заболевание, протекающее с ангиоматозным типом кровоточивости, обычно не является прямым противопоказанием для проведения экстренных и плановых оперативных вмешательств (аппендэктомии, холецистэктомии и др.)
Таким образом, приведённые в настоящей работе данные о современной тактике терапии различных проявлений наследственной геморрагической телеангиэктазии позволяют надеяться на то, что в ближайшем будущем появятся новые подходы в решении сложных вопросов этого сосудистого страдания.
Резюме
В статье представлен обзор современных взглядов на лечение относительно редкого сосудистого заболевания — наследственной геморрагической телеангиэктазии. Подчёркиваются успехи в понимании генетических основ данного страдания.
Список используемой литературы:
1. Marchuk D. A. The molecular genetics of hereditary hemorrhagic telangiectasia. Chest 1997, VIII, №6 (Suppl), 793-823.
2. Abdalla S. A., Cymerman U., Rushlow D. et. al. Novel mutations and polymorphisms in genes occusing hereditary hemorrhagic telangiectasia. Ilum. Mutat. 2005, V. 25, №3, S 320-1.
3. Kjeldson A. D., Muller T. R., Brusgaard K. et al. Clinical symptoms according to genotype amongst patients with hereditary hemorrhagic telangiectasia. I. Intern. Med. 2005, V. 258, P. 349-355.
4. Mc Allister K. A., Grogg K. M., Johnson D. W. et. al. Endoglin? a TGE-beta binding protein of endotelial cells, is the gene for hereditary hemorrhagic telangiectasia type I. Nat. Genet., 1994, V. 8 №4 P. 345-51.
5. Shovlin C. L., Hughes J. M. B., Fuddenham E. G. D. et. al. A gene for hereditary hemorrhagic telangiectasia maps to chromosone 9q 3. Nat. Genet., 1994, №6, P. 205-9.
6. Bayrak-Foydemir P., McDonald I., Markewit B. et. al. Genotype-phenotype correlation in hereditary hemorrhagic telangiectasia: mutations and manifestations. Am. I. Med. Genet. A. 2006, V. 140 P. 463-470.
7. Vincent P., Flauchu H., Hazan I. et.a l. A third locus for hereditary hemorrhagic telangiectasia maps to chromosome 12q. Hum. Molec. Genet., 1995, №4, P. 945-949.
8. Johnson D. W., Berg J. N., Baldwin M. A. et. al. Mutations in the activin receptor-like kinase 1 gene in hereditary hemorrhagic telangiectasia type 2. Nat. Genet. 1996, V. 13, P. 189-195.
9. Berg J. N., Gallione C. J., Stenzel T. T. et. al. The activin receptor-like kinase 1 gene: genomic structure and mutations in hereditary hemorrhagic telangiectasia type 2. Am. J. Ilum. Genet. 1997, V. 61 №1, P. 60-7.
10. Berg J., Porteus M., Reinhardt G. et. al. Hereditary hemorrhagic telangiectasia: a questionnaire the different phenotypes caused by endoglin and ALK1 mutations. J. Med. Genet. 2005, V. 40, P. 585-590.
11. Cole S. G., Begbie M. E., Wallace G. M. F. et. al. A new locus for hereditary hemorrhagic telangiectasia (HHT 3) maps to chromosome 5. J. Med. Genet. 2005, V. 42, P. 577-582.
12. Gallione C. J., Repetto G. M., Legins E. et. al. A combined syndrome of juvenile polyposis and hereditary hemorrhagic telangiectasia assosiated with mutations MADh5 (SMAD4). Lancet. 2004, V. 363, P. 852-859.
13. Gillespie J. S. J., McIvor R. A. Hereditary hemorrhagic telangiectasia in association with generalised juvinale polyposis. The Ulster Medical J. 2001, V. 70, №2б P. 145-48.
14. Gallione C., Aylsworth A.S., Beis J. et.al. Overlapping spectra of SMAD4 mutations in juvenile polyposis (JP) and JP-HHT syndrome. Am J Med Genet A. 2010 Feb;V. 52, №2, P. 333-339.
15. Ojeda-Fernandez L., Barrios L., Rodriguez-Barbero A. et.al. Reduced plasma levels of Ang-2 and sEng as novel biomarkers in hereditary hemorrhagic telangiectasia (HHT).Clin Chim Acta. 2010 Apr 2; V. 411№7-8, P. 494-499.
16. Siquier F. A propos d’une epistaxis morteel. Dresse Med.,1954, V. 62, №77, P. 1594.
17. Saba H. J., Morelli G. A, Logrono L. A. Brief report: treatment of bleeding in hereditary hemorrhagic telangiectasia with aminocapronic acid. N. Engl. J. Med. 1994, V. 330, № 25, P. 1789-90.
18. Kwen H. C., Silverman N. Fibrinolytic activity in lessions of hemorrhagic telangiectesia. Arch. Dermatol. 1973, V. 107, №4, P. 571-573.
19. Lenz H., Eichler J. Endonasale chirurgische Тechnik mit dem Argonlaser. Laryng. Rhinol. Otol. 1984, V. 63, P. 534-540.
20. Vickery C. L., Kuhn F. A. Using the KTP (532 laser) to control epistaxis in patients with hereditary hemorrhagic telangiectasia. South. Med. J. 1996, V. 89, P. 78-80.
21. Qeisthoff H. W., Fiorella M. L., Fiorella R. Treatment of recurrent epistaxis in HHT. Curr. Pharm. Des. 2006, V. 12, P. 1237-42.
22. Elden I., Montanera W., Ferbrugge K. et. al. Angiographic embolisation for the treatment of epistaxis: a review of 108 cases. Otolaryngol. Head. Neck. Surg. 1994 V. 111, P. 44-50.
23. Braak S.J., de Witt C.A., Disch F.J. et.al. Percutaneous embolisation on hereditary hemorrhagic telangiectasia patients with severe epistaxis.Rhinology. 2009 Jun;47(2):166-71.
24. Ernest J., Polácková V.K., Charvát F. [Ophthalmic complications after the embolisation of the internal carotid artery—a case report] Cesk Slov Oftalmol. 2008 Sep;64(5):202-6.
25. Saunders W. H. Septal dermoplasty for hereditary telangiectasia and other conditions. Otolaryngol. Clin. North. Am., 1973, №6, P. 745-755.
26. Levine C.G., Ross D.A., Henderson K.J. et.al. Long-term complications of septal dermoplasty in patients with hereditary hemorrhagic telangiectasia.Otolaryngol Head Neck Surg. 2008 Jun;138(6):721-4.
27. Koch H. J., Escher G. C., Levis J. S. Hormonal management of hereditary hemorrhagic telangiectasia. JAMA, 1952, V. 149, P. 1376-1380.
28. Harrison D. F. Familial hemorrhagic telangiectasia – 20 cases treated with systemic estrogen. Quart. J. Med. 1964, V. 33, P. 25-38.
29. Vase P. Estrogen treatment of hemorrhagic telangiectasia. Laryngoscope. 1982, V. 92, P. 314-20.
30. Jamenson J. J., Cave D. R. Hormonal and antihormonal therapy for epistaxis in hereditary hemorrhagic telangiectasia. Laryngoscope. 2004. V. 114, P. 705-709.
31. Davidson T.M., Olitsky S.E., Wei J.L. Hereditary hemorrhagic telangiectasia/avastin.Laryngoscope. 2010 Feb;120(2):432-5.
32. Simonds J., Miller F., Mandel J. et.al. The effect of bevacizumab (Avastin) treatment on epistaxis in hereditary hemorrhagic telangiectasia. Laryngoscope. 2009 May;119(5):988-92.
33. Zacharski L.R., Dunbar S.D., Newsom W.A. et.al. Hemostatic effects of tamoxifen in hereditary hemorrhagic telangiectasia.Thromb Haemost. 2001 Feb;85(2):371-2.
34. Yaniv E., Preis M., Hadar T. et. al. Antiestrogen therapy for hereditary hemorrhagic telangiectasia: a double-blind placebo-controlled clinical trial. Laryngoscope. 2009 Feb;119(2):284-8.
35. Albiсana V., Bernabeu-Herrero M.E., Zarrabeitia R. et.al. Estrogen therapy for hereditary haemorrhagic telangiectasia (HHT): Effects of raloxifene, on Endoglin and ALK1 expression in endothelial cells. Thromb Haemost. 2010 Mar 1;103(3):525-34.
36. de Gussem E.M., Snijder R.J., Disch F.J. et.al. The effect of N-acetylcysteine on epistaxis and quality of life in patients with HHT: a pilot study. Rhinology. 2009 Mar;47(1):85-8.
37. Lebrin F., Srun S., Raymond K.et.al. Thalidomide stimulates vessel maturation and reduces epistaxis in individuals with hereditary hemorrhagic telangiectasia. Nat Med. 2010 Apr;16(4):420-8.
38. Теплюк Т. Б. Наследственная геморрагическая телеангиэктазия (болезнь Рандю-Ослера): лёгочная гемодинамика и лечение геморрагического синдрома. Дисс. канд. мед. наук. М. 1986.
39. Сельдин М. А., Ливандовский Ю. А., Рудня П. Г. О носовых кровотечениях при болезни Рандю-Ослера. Гигиена, физиология на железнодорожном транспорте. 1974. №48, С. 20-22.
40. van Cutsen E., Rutgeerts P., Vantrappen G. Treatment of bleeding gastrointenstinal vascular malformations with estrogen-progesterone. Lancet. 1990. V. 336. P. 953-5.
41. van Cutsen E. Estrogen-progesterone, a new therapy of bleeding gastrointenstinal vascular malformations. Acta Gastroenterologica Belgica 1993. V. 56, №1, P. 2-10.
42. Sargeant J. R., Loizoi L. A., Rampton D. et. al. Laser ablation of upper gastrointenstinal vascular ectagies: long-term results. Gast. 1993. V. 34, P. 470-5.
43. White R. J., Lynch-Nyhan A., Ferry P. et. al. Pulmonary arteriovenous malformations: techniques and long-time outcome of embolotherapy. Radiology. 1988, V. 169, P. 663-669.
44. Haitjema T. J., Overtoom T. T., Westermann C. J. et. al. Embolisation of pulmonary arteriovenous malformations: results and fallow in 32 patients. Thorax, 1995, V. 50, P. 719-723.
45. Dutton J. A., Jackson J. E., Hughes J. M. et. al. Pulmonary arteriovenous malformations: results of treatment with coil embolisation in 53 patients. Am. J. Roentgenol. 1995, V. 165, P. 1119-25.
46. Cotton V., Dupuis-Girod S., Lesca G. et. al. Pulmonary vascular manifestations of hereditary hemorrhagic telangiectasia (Rendu-Osler disease). Respiration 2007, V. 74, P. 361-378.
47. Faughnan M.E., Thabet A., Mei-Zahav M. et.al. Pulmonary arteriovenous malformations in children: outcomes of transcatheter embolotherapy. J Pediatr. 2004 Dec;145(6):826-31.
48. Ruf B., Eicken A., Schreiber C. et.al. Clinical improvement after banding of a pulmonary branch artery in a symptomatic patient with Osler-Rendu-Weber syndrome. Pediatr Cardiol. 2010 Jan;31(1):136-7.
49. Gammon R.B., Miksa A.K., Keller F. S. Osler-Weber-Rendu disease and pulmonary arteriovenous fistulas: deterloration and embolotherapy during prednancy. Chest 1990 98: 1522-24.
50. Gershon A.S., Faughman M.E., Chon K.S. et.al. Transcatheter embolotherapy of maternal pulmonary arteriovenous malformations during pregnancy. Chest 2001;119:470-77.
51. Berg A.M., Amirbekian S., Mojibian H. et.al. Hemothorax due to rupture of pulmonary arteriovenous malformation: an interventional emergency. Chest. 2010 Mar;137(3):705-7.
52. Alison D. J., Jordan H., Hennessy O. Therapeutic embolisation of the hepatic artery: a review of 75 procedures. Lancet. 1985, 1, 595-598.
53. Roman C. F., Cha S. D., Jincarvito J. et. al. Transcatheter embolisation of hepatic arteriovenous fistula in Osler-Weber-Rendu disease — a case report. Angiology. 1987, V. 38, P. 484-488.
54. Stock L., Raat H., Caerts B. et. al. Transcatheter embolisation of hepatic arteriovenous fistulas in Rendu-Osler-Weber disease: a case review of the literature. European Radiology 1999, V. 9. P. 1434-1437.
55. Odorico J. S., Hakim M. N., Becker V. T. et. al. Liver transplantation as definative therapy for comlications after arteriae embolisations hepatic manifestations of hereditary hemorrhagic telangiectasia. Liver Transplantation Surgery 1998, № 4, P. 483-490.
56. Boillot O., Bianco J. Liver transplantation resolves the hyperdynamic circulation in hereditary hemorrhagic telangiectasia with hepatic involment. Gastroenterology 1999, V. 166, P. 187-92.
57. Hillert C., Broering D. C., Gundlach M. et. al. Hepatic involment in hereditary hemorrhagic telangiectasia: an unusual indication for liver transplantation. Liver Transplantation. 2001, V. 7, №3, P. 266-268.
58. Dupuis-Girod S., Chesnais A.L., Ginon I. et.al. Long-term outcome of patients with hereditary hemorrhagic telangiectasia and severe hepatic involvement after orthotopic liver transplantation: a single-center study. Liver Transpl. 2010 Mar;16(3):340-7.
59. Mitchell A., Adams L.A., MacQuillan G. et.al. Bevacizumab reverses need for liver transplantation in hereditary hemorrhagic telangiectasia. Liver Transpl. 2008 Feb;14(2):210-3.
60. Haitjema T., Westermann C. J., Overtoon T. T. et. al. Hereditary hemorrhagic telangiectasia (Osler-Weber-Rendu disease): new insights in pathogenesis, complication and treatment. Arch. Int. Med. 1996, V. 156, P. 714-719.
Статья добавлена 20 февраля 2015 г.
Болезнь Рандю-Ослера, причины возникновения, формы и стадии, симптомы, диагностика и терапия, прогноз
Появление красных пятен на лице различной формы не всегда обусловлено кожными патологиями. Причиной могут быть серьезные нарушения в организме, среди которых болезнь Рандю-Ослера.
Этиология синдрома Рандю-Ослера-Вебера
 Изучение первопричины синдрома Рандю-Ослера-Вебера продолжается до сих пор. Исследуя причину данной патологии, большинство ученых заключают, что нарушение обусловлено генетическим фактором. Вследствие аномального развития сосудистый эндотелий становится ослабленным, удлиняется и разрастается.
Изучение первопричины синдрома Рандю-Ослера-Вебера продолжается до сих пор. Исследуя причину данной патологии, большинство ученых заключают, что нарушение обусловлено генетическим фактором. Вследствие аномального развития сосудистый эндотелий становится ослабленным, удлиняется и разрастается.
Патология развивается на фоне видоизменения нескольких генов, активизирующих восстановление тканей и формообразование сосудов. У здорового человека сосудистые стенки состоят из внутреннего, среднего и внешнего слоев. При синдроме Рандю-Ослера структурное строение эндотелия нарушается. В результате отсутствия мышечных и эластичных волокон в микрососудах происходят такие изменения:
- ломкость и уменьшение эластичности сосудистой стенки;
- неустойчивость к растяжениям;
- образование разрывов, вызывающих кровотечения;
- ухудшение свертываемости крови.
Повышение кровоточивости обусловлено отсутствием эластичных и мышечных волокон в сосудах. Вследствие этого легкие повреждения заканчиваются геморрагиями. По мнению специалистов, патологический процесс начинается еще в период внутриутробного развития. Это может происходить на фоне приема лекарств или перенесенных женщиной инфекций во время беременности.
Формы и стадии недуга
Форма патологии определяется локализацией пораженных участков, поэтому болезнь подразделяют на такие виды:
- Назальная.
- Глоточная.
- Кожная.
- Висцеральная (внутренняя).
- Смешанная.
Последняя форма имеет смешанный характер, так как затрагивает одновременно внутренние органы и кожные покровы.
В практике у детей патологические процессы заметны на открытых участках тела. У взрослых людей кровоизлияния часто обнаруживают во внутренних органах.
Исходя из размеров кожных высыпаний, определяют стадию недуга:
Стадия недуга | Характеристика |
Начальная | Появление мелких пятен. |
Промежуточная | Формирование телеангиэктазий (сосудистых звездочек). |
Поздняя | Образование красных узелков, выступающих над поверхностью кожи. |
Клиническая картина геморрагической телеангиэктазии
Поскольку у болезни Рандю-Ослера генетическое происхождение, клинические признаки появляются еще в детском возрасте, начиная с 5 лет.
Проявление недуга включает в себя такие симптомы:
- частые кровотечения;
- затрудненное дыхание;
- формирование сосудистой сетки или пятнышек;
- кровоточащие сосудистые опухоли;
- наличие крови в моче, мокроте, кале;
- анемия.
Подобные признаки наблюдаются на губах и щеках, мочках ушей, крыльях носа, голове и слизистых оболочках рта. Со временем поражаются и другие участки тела. У взрослых телеангиэктазии гораздо больше и кровоточивость их сильнее.
Патология выдает себя рецидивирующими кровотечениями. В большинстве случаев они открываются во внутренних органах: печени, ЖКТ и дыхательных путях. Вследствие частых геморрагий снижается уровень гемоглобина. Это приводит к появлению сопутствующей симптоматике:
- Головокружения.
- Бледность кожных покровов.
- Предобморочное состояние.
- Быстрая утомляемость.
- Потемнение в глазах.
- Одышка.
- Шум в ушах.
- Учащение сердцебиения.
К перечисленным симптомам могут присоединяться и другие, в зависимости от пораженных участков. В дальнейшем патология приводит к нарушению в работе мочевыводящих путей, печени, сердца и головного мозга.
На первых этапах болезни наблюдаются носовые кровотечения. Постепенно геморрагии появляются из легких, почек, ЖКТ.
Кожа и слизистые оболочки
Геморрагии кожи и слизистых оболочек появляются сразу после кровотечений из носа.
Симптомы охватывают следующие участки тела:
- голова;
- верхние конечности;
- область лица: мочки ушей, веки, щеки, губы;
- наружная и внутренняя часть пазух носа;
- полость рта: десна, поверхность языка.
В большинстве случаев наблюдается кровоточивость из носа. Характер проявления данного симптома у каждого пациента индивидуален.
Сосудистые звездочки имеют разный оттенок: от красного вплоть до фиолетового. Характерная особенность телеангиэктазий – при надавливании они бледнеют, а позже снова наполняются кровью и восстанавливают цвет.
Головной мозг
Поражение головного мозга на фоне данного синдрома носит множественный характер.
При этом клиническая картина включает в себя следующее:
- Судорожные явления.
- Нарушение зрительной и слуховой функции.
- Приступы мигрени.
- Потеря чувствительности в некоторых участках тела.
- Кровоизлияние в головной мозг.
Подобные кровоизлияния очень опасны, так как могут провоцировать развитие эпилепсии и абсцесса головного мозга.
ЖКТ и печень
 Патология проявляется структурным изменением сосудов, расположенных на слизистых оболочках органов.
Патология проявляется структурным изменением сосудов, расположенных на слизистых оболочках органов.
При локализации синдрома в ЖКТ и печени внутренние кровотечения выдают себя такими симптомами:
- упадок сил;
- удушье;
- обмороки;
- головокружения;
- отечность брюшной полости;
- эпизоды рвоты с примесью крови;
- желтушный оттенок кожи;
- боль в правом подреберье.
О внутренних кровотечениях могут свидетельствовать примеси крови в урине, каловых массах и мокроте.
Легкие
Наиболее часто у пациентов структурное изменение сосудов обнаруживается в легких.
Это выражается в следующем:
- Ощущение нехватки воздуха.
- Изменение цвета лица: от красного до синюшного.
- Гиперемия конъюнктивы.
- Кровохарканье.
Подобные признаки появляются вследствие недостаточного объема кислорода в тканях и органах. Патология может сопровождаться легочной гипертензией с отеками конечностей, а иногда – с острыми болями в сердце.
Протекание беременности на фоне синдрома Рандю-Ослера
Женщины, вынашивающие ребенка с подобным диагнозом, находятся в группе риска. Поэтому беременность нужно планировать заранее. Ведь на фоне гормональных изменений повышается вероятность осложнений, особенно на втором и третьем триместре.
Беременные женщины с подобным диагнозом наблюдаются у гинеколога и гематолога. В ситуациях, когда недуг затрагивает другие органы, требуется консультация специалистов более узкого профиля. Как правило, серьезных осложнений во время родов нет. Ввиду гормональных изменений, случаи геморрагий крайне редки.
Диагностика геморрагической телеангиэктазии
Вначале врач осматривает пациента и оценивает его физическое состояние. Затем на основании имеющихся жалоб рекомендуется проведение диагностических мероприятий. Чтобы клиническая картина стала яснее, используются инструментальные и лабораторные методы выявления заболевания.
Эндоскопия
Необходимость в обследовании с помощи эндоскопа возникает при обнаружении внутренних кровотечений.
Используются такие методы:
- Бронхоскопия (исследование дыхательных путей).
- Фиброгастродуоденоскопия (для пищевода).
- Лапароскопия (для брюшной полости).
- Ларингоскопия (определяет состояние верхних дыхательных путей).
- Колоноскопия (проверка толстого кишечника).
Метод диагностики подбирается в зависимости от места локализации недуга.
Рентген и томография
У больных с церебральными нарушениями диагностика проводится с помощью лучевых исследований. Подобные процедуры облегчают дифференцирования патологий. Для этого проводят такие мероприятия:
- компьютерная томография;
- рентгенография;
- МРТ.
Подобные методики позволяют выявить нарушения в системе дыхания и поражения головного мозга.
Лабораторные анализы
Учитывая геморрагический характер проявления недуга, лабораторные процедуры направлены на изучение крови.
Исследуются такие гемопоказатели:
- Свертываемость.
- Уровень гемоглобина и эритроцитов.
- Исследование на железодефицит.
Помимо этого, с помощью цистоскопии выявляют наличие крови в урине, сдают анализы для определения генотипа.
Лечение и прогноз синдрома Рандю-Ослера-Вебера
Учитывая генетические причины, нет специфических методов терапии синдрома Рандю-Ослера. Поэтому больные нуждаются в пожизненном лечении, поддерживающем состояние здоровья.
В данном случае лечебный курс направлен, чтобы вызвать следующий эффект:
- купирование геморрагий;
- восполнение потерянного объема крови;
- ликвидация появившихся телеангиэктазий.
Достижение такого эффекта возможно благодаря применению лекарственных препаратов. При осложнении болезни используется переливание крови и хирургическое вмешательство.
В лечении синдрома Рандю-Ослера наиболее часто используются такие группы медикаментов:
- Дерматотропные: Бепантен, Пантенол.
- Витамины: Аевит, Квадевит, Декамевит.
- Гормональные: Эстрадиол.
- Гемостатики: Викасол, Дицинон.
- Ингибиторы фибринолиза: аминокапроновая кислота.
- Противоанемические: Мальтофер, Феррум Лек.
Если патология проявляется частыми геморрагиями и тяжелым поражением внутренних органов, медикаментозная терапия малоэффективна. В подобных случаях телеангиэктазии устраняются хирургическим путем.
При этом используются такие методы:
- химическая деструкция;
- лазерная абляция;
- криодеструкция;
- термокоагуляция (прижигание электротоком).
Принцип действия перечисленных процедур направлен на устранение поврежденного сосуда и перевязывание капилляров, снабжающих его кровью.
Исход патологии зависит от выраженности клинических признаков и характера поражения сосудистых стенок. Выявление заболевания на ранних этапах повышает шансы на устранение негативной симптоматики. Пациенты, соблюдающие все врачебные рекомендации, значительно улучшили состояние своего здоровья.
Неблагоприятный исход наблюдается у больных с церебральными проявлениями патологии. В таких случаях болезнь прогрессирует, провоцируя развитие эпилептических приступов, инсульта или абсцесса головного мозга.
Чем опасна болезнь
 Пациенты с болезнью Рандю-Ослера часто сталкиваются с осложнениями при неэффективности терапии.
Пациенты с болезнью Рандю-Ослера часто сталкиваются с осложнениями при неэффективности терапии.
Среди опасных последствий могут быть такие:
- Патологии миокарда.
- Кома, вызванная тяжелой анемией.
- Легочная гипертензия.
- Острая закупорка легочной артерии.
- Разрастание тканей печени.
- Геморрагический инсульт.
- Наступление паралича.
Вследствие массивных кровопотерь состояние больных ухудшается. Иногда это приводит к летальному исходу.
Геморрагическая телеангиэктазия влечет за собой тяжелые и опасные проявления. Своевременное оказание медицинской помощи поможет избежать негативных последствий и сохранить жизнь.
Синдром Рандю-Ослера:
Заметили ошибку? Выделите ее и нажмите Ctrl+Enter, чтобы сообщить нам.
причины, симптомы, диагностика и лечение. Наследственные болезни :: SYL.ru
В медицине такое явление, при котором мелкие капилляры и другие сосуды расширяются и находятся в таком состоянии без воспалительного процесса, называют телеангиэктазией. Болезнь Рандю-Ослера является частным случаем данной патологии. На коже она проявляется в виде мелкой сетки, пятен красного цвета. Такой недуг приносит, скорее, эстетические неудобства носителю, но на физическом состоянии никак не сказывается.
Причины болезни
В чем же состоят основные причины заболевания? Телеангиэктазия, по общепринятому мнению, имеет истоки в отклонениях от нормальной работы сердечно-сосудистой системы. Но данное утверждение верно лишь частично, поскольку причиной становится нарушение гормонального фона. Некоторые другие недуги тоже могут дать начало телеангиэктазии.
При болезни Рандю-Ослера кровь выделяется из мелких сосудов – артериол и венул. Болезнь поражает не только кожу, но и слизистые бронхов, носоглотки, мочевого пузыря и других внутренних органов.
На сегодняшний день данное отклонение фиксируется в 1 случае из 50 000, но может встречаться чаще. Заболевание имеет врожденный характер, относится к группе наследственной телеангиэктазии.
Болезнь Рандю-Вебера-Ослера проявляется при скоплениях очагов на коже и слизистых участках. Патогенез на данный момент не до конца изучен и понятен. Существует мнение о том, что отклонения от нормы в развитии мезенхимы дает предпосылки к возникновению болезни. Этот участок системы характерен отсутствием мышечной ткани у сегментов стенок кровеносных сосудов. Стенка здесь состоит из эндотелия, она окружена рыхлыми структурами.
Это состояние становится причиной истончения капилляров и венул. А те сосуды, которые формируют телеангиэктазий, при различных процессах расширяются, что приводит к анастомозированию с артериолами. Это происходит с участием капиллярных сегментов. Легко диагностируются артериально-венулярные анастомозы.
Проводимые обследования позволяют определить разрыхление соединительных тканей со скоплением гистиоцитов и лейкоцитов в острых зонах. У больных также присутствует недоразвитие потовыделяющих желез, сосков дермы, фиксируется низкое количество формирующихся волосяных луковиц.
При болезни Рандю-Ослера наблюдаются обильные и частые кровотечения, они происходят на фоне хрупкости сосудов. При данном недуге происходит нарушение системы выработки тромбоцитов, действия фибринолиза. Но такие явления бывают редко.
Факторы риска
Иногда у больного не выявляют наследственных признаков. В таком случае выделяют факторы, способствующие развитию болезни:
— малоподвижный образ жизни;
— курение;
— частое посещение солярия либо длительное пребывание на солнце.
Все эти факторы могут приводить к потере эластичности сосудов, а значит, способствовать появлению телеангиэктазий.
История описания болезни
Первое описание недуга, называемого также «диссеминированный гемангиоматоз», дал французский врач Луи Мари Рандю. Позднее более подробно его рассмотрел англичанин Уильям Ослер, также дополнил сведения Фредерик Вебер. Заболевание не имеет гендерных предпочтений, им могут страдать и девочки, и мальчики. Передают недуг два гена: отвечающий за наличие эндолгина, который обеспечивает выработку гликопротеина; и из категории, несущей сведения о факторах роста. Если эти гены видоизменяются, то сосуды перестают быть эластичными. Чаще всего описываемая проблема относится к категории «Наследственные болезни».
Симптоматика
Обычно никаких симптомов не наблюдается до достижения 6 лет, а иногда и до 10. Первыми признаками становятся ангиомы – опухоли сосудов. Из-за нарушения состояния капилляров и сосудов появляются красные с синим оттенком пятна, они кровоточат. При этом у больного присутствует низкая свертываемость крови. На этом фоне могут быть кровотечения при травмировании. У некоторых заболевших кроме кровотечений из носа нет других симптомов. У девочек на болезнь могут указать обильные менструальные выделения. А после частых кровотечений появляется малокровие, снижение гемоглобина.
Стадии болезни
На первой стадии, когда аномалии сосудов выражены незначительно, появляются мелкие пятна. На промежуточной возникают сосудистые звездочки. При узловатой стадии появляются красные выступы на поверхности кожи диаметром несколько миллиметров. Если надавить на них, то они бледнеют, потом наполняются кровью.
К взрослению у больных на кожном покрове появляются сгустки крови диаметром от булавочной головки до горошины. Они могут располагаться на губах, ушах, щеках, подбородке, груди, руках. Бывает кровавая рвота, стул. Печень и селезенка увеличиваются.
Если установлено, что ребенку болезнь Рандю-Ослера передалась от родителей, то форма ее будет более тяжкой. Различают несколько видов недуга в зависимости от локализации: назальный, глоточный, кожный. Бывает и смешанный тип, при котором поражены и кожа, и слизистая внутренних органов.
Что усиливает симптомы?
Проявление болезни усиливают:
— высокое артериальное давление;
— неправильное питание;
— нехватка микроэлементов, повышающих эластичность и прочность сосудов.
Есть мнение, что данные факторы при вегетарианстве способны привести к более тяжелому течению болезни.
Проявлениям недуга способствуют все виды воспалений и различные травмы. Потому больные должны избегать экстремальных физических нагрузок, приема алкоголя и т. п.
Диагностирование
Как обнаруживается болезнь Рандю-Ослера? Диагностика состоит в следующем. Пациент сдает общий анализ крови, при котором можно выявить анемию. Анализ на биохимию покажет, есть ли инфекции и другие болезни. Также у пациента берется анализ мочи. Если он проинформирует о наличии эритроцитов, возникнет вероятность проблем с почками и мочевыводящей системой. Берется и проба щипком, чтобы понять, насколько сильны подкожные кровоизлияния. Делается проба кожи под ключицей, когда ее сжимают.
При постановке диагноза производят тест на скорость свертываемости крови. После прокола отчитывают время истекания крови. Все полости тела осматривают с эндоскопом, при необходимости проводят компьютерную томографию.
Есть случаи, когда болезнь начинается с мозжечковой атаксии. Этот процесс пока не изучен. При приобретенных формах недуга врачи делают вывод о действии гормона эстрогена, так как он отвечает за эластичность сосудов. Вот так выявляется болезнь Рандю-Ослера.
Лечение
В качестве консервативной терапии для обработки участков с кровотечением применяются ингибиторы. Они помогают удалить сгустки крови, потому что разжижают ее. Иногда требуется проведение операции для удаления поврежденного участка сосуда. Если локализация в носу, то проводят криокоагуляцию, при которой жидким азотом замораживают сосуд. Редко используются гормоны.
Когда кровопотери достигают больших объемов, прибегают к помощи доноров. Недостаток элементов, обеспечивающих свертывание, восполняется при переливании плазмы. Это применяется лишь в крайних случаях при угрозе летального исхода. Иногда переливают донорские тромбоциты, если имеет место тяжелая анемия либо анемическая кома и утрата сознания вследствие недостатка кислорода для питания мозга.
У пациентов всегда при себе имеется раствор 5-8% аминокапроновой кислоты, который хранится в холодильнике. Этим средством орошается либо слизистая носа, либо доступные участки поражения.
Если болезнь Рандю-Ослера не подвергается лечению, то при развитии приводит к таким последствиям, как тяжелая анемия, анемическая кома. Иногда наступает паралич. Известны случаи слепоты при запущенной стадии на сетчатке глаз. Самым опасным может стать кровоизлияние в мозг.
Профилактика заболевания
До того как диагноз поставлен, тем семьям, в которых данная болезнь переносилась кем-либо, рекомендуется пройти консультацию генетика. Иногда родителям дают совет воздержаться от самостоятельного зачатия.
При выявленной болезни необходимо акцентировать внимание на иммунной системе. Помогают улучшить общее состояние и избежать тяжелых последствий при таком диагнозе, как болезнь Рандю-Ослера-Вебера:
— прогулки на свежем воздухе;
— закаливание;
— сбалансированное питание;
— регулярные осмотры у врача.
Все, кто находится рядом с больным, должны быть ознакомлены с правилами оказания первой доврачебной помощи.
Наследственные болезни
На сегодняшний день за редким исключением генетика может предсказать развитие многих болезней при исследовании генотипа человека. Недуги, которые передаются от родителей детям, вызваны хромосомными или генными дефектами. Значит, возникают проблемы в передаче наследственной информации.
Не все врожденные заболевания могут наследоваться. Иногда на плод воздействует некий фактор, приводящий к тому или иному заболеванию вне зависимости от генов родителей: химикаты, вредные лекарства, облучение. Некоторые из наследуемых недугов выявляются по прошествии двух-трех, а то и десяти лет после рождения.
Существует несколько типов наследственных заболеваний:
— генетические при повреждениях структуры ДНК;
— хромосомные при ненормальном числе хромосом;
— с генетической предрасположенностью могут быть гипертония, диабет, шизофрения.
По МКБ 10 болезнь Рандю-Ослера относится к последней категории.
Что изучает генетика?
Генетика сегодня изучает внешнюю среду и те признаки, которые передает ген. Методы исследования этой науки выявляют особенности наследования различных признаков. Имеет место изучение близнецов для установления влияния внешней среды на болезни. На основе различий между испытуемыми выявляются факторы, воздействующиена патологии. В науке используется метод сравнения структур хромосом здорового и больного человека. Изучается метаболизм. Также исследуется иммунитет и папиллярные узлы на руках и ногах — узоры, которые изменяются при жизни человека и свидетельствуют о мутациях в генах и хромосомах.
Иногда родители могут не страдать от заболевания, а лишь передавать его своим детям. Это явление называется пенетрантностью. Если проблема, например, болезнь Рандю-Ослера, наследуется по доминантному типу, то она передается из поколения в поколение при том, что страдать от нее может лишь один из родителей. Такими недугами являются сращение пальцев рук, увеличение их числа, дрожание рук и слабоумие при хорее Гентингтона.
При наследовании по рецессивному типу ген болезни может не проявляться. От нее могут страдать не самые близкие родственники. Но если случаются кровные браки, то скрытое носительство может стать явным.
Некоторые рецессивные заболевания наследуются в зависимости от пола. Обычно это гены, связанные с Х-хромосомой. Среди таких недугов — гемофилия, дальтонизм, врожденная слепота, глухота.
Итак, мы рассмотрели, что такое геморрагическая телеангиэктазия (болезнь Рандю-Ослера), а также ознакомились с некоторыми особенностями генетики как науки.
Болезнь Рандю-Ослера-Вебера: лечение и симптомы
О болезни наследственная геморрагическая телеангиэктазия (болезнь Рандю-Ослера-Вебера) в средствах массовой информации появилось множество сообщений после 1994 г. Именно в это время были опубликованы результаты нескольких масштабных исследований, во время которых были изучены причины, механизмы развития болезни, клиническая картина и варианты её лечения.
По данным исследований до 1994 года болезнь Рандю-Ослера-Вебера (подробное лечение и симптомы рассмотрим в статье) встречается с частотой 1 случай на 50 000 населения, по результатам 1994 г – 1 случай на 16 500. Скорее всего, причиной такого расхождения является возможность использования нового оборудования в подтверждении болезни.
Факт! В настоящее время считается, что количество больных этим заболеванием увеличивается. Но важно отметить, что это не количество больных увеличивается, а количество зарегистрированных случаев болезни Рандю-Ослера. Сейчас в клиниках первого и второго уровня медицинской помощи есть большое количество современной техники, которая помогает предположить и подтвердить правильный диагноз.
Симптомы болезни Рандю-Ослера
Заболевание Рандю-Ослера – это наследственная патология, которая передаётся от родителя ребёнку. Хромосомный дефект нарушает гистологическое строение стенки кровеносных сосудов, что вызывает их ломкость и повышает риск кровотечения.
Синонимы болезни Рандю-Ослера:
- Геморрагический ангиоматоз.
- Геморрагический диатез сосудистого генеза.
- Врождённая геморрагическая телеангиэктазия.
- Заболевание Рандю-Ослера-Вебера.
- Синдром Ослера.
- Диссеминированный гемангиоматоз.
Болезнь передаётся как аутосомно-доминантное заболевание. Этот тип наследственности подчиняется законам генетики Менделя и означает, что если один из родителей болен, патология в 50% случаев передастся и проявиться у его детей. В остальных случаях дети будут здоровы. Если болеют оба родителя, заболевание проявиться во всех случаях.
В руководстве «Диагностика болезней внутренних органов» А.Н. Окороков посвящает данному заболеванию целую главу. В ней говорится об исследованиях, которые были проведены для изучения не только причины, но и клинической картины болезни. Согласно результатам исследования 1994 г McDonald и Shovlin установили, что генетический дефект, который приводит к заболеванию, лежит в 9-ой хромосоме в локусе OWR1 (9q33-34). А вот Chovlin в 1997 г проводил ещё одно исследование, результаты которого показали, что дефект лежит ещё и в области 12-ой хромосомы 12q (локус OWR2), соответствующий рецепторамTGF-β.
Гистологическое обоснование наследственной телеангиэктазии
В норме сосудистая стенка состоит из слоёв:
- Эндотелиальный.
- Эластический.
- Мышечный.
- Фиброзный.
В каждом виде сосуда выраженность отдельно взятого слоя разная. Например, в артериальных сосудах, которые выдерживают большое кровяное давление мышечный и эластический слой наиболее выражены. Вены представлены в равной степени фиброзным, эластическим и мышечным слоями. Артериола имеет только мышечный слой, а венула фиброзный. Капилляр является самым незащищённым сосудом нашего организма, ведь он имеет только эндотелий.
В основе формирования заболевания лежит несостоятельность мышечного и эластического слоя всех кровеносных сосудов организма. Сосуды состоят практически из одного эндотелия и окружены рыхлой соединительной тканью. Именно в местах анастомозов между венулами и капиллярами появляются самые слабые участки, которые расширяются под давлением крови.

Слабость стенки сосуда приводит к появлению:
- Телеангиэктазия – стойкое расширение мелких сосудов, которое не имеет воспалительную природу.
- Артериовенозные шунты – прямое сообщение вен и артерий без включения более мелких сосудов. Такая патология приводит к нарушению трофики тканей в участке, который кровоснабжается за счёт этих сосудов.
- Аневризма – стойкое мешковидное расширение сосуда в одном месте.
[neutral title=””]Интересно знать! Аневризма бывает ложная и истинная. Истинная представляет под собой расширение всех слоёв сосуда, а ложная (пульсирующая) – это разрушение стенки сосуда, при котором не нарушается целостность его внешнего слоя. Это приводит к скоплению крови в просвете между средним и наружным слоем, что иногда выглядит как истинная аневризма.[/neutral]
Именно формирование телеангиэктазии в месте перехода капилляра в венулу и является характерным признаком болезни. Обычно ещё развивается патология и эндотелиального слоя сосуда, что сопровождается накоплением лейкоцитов и гистиоцитов вокруг сосудов. Также нарушается образование сосочков кожи и потовых желёз и волосяных фолликулов.
Повышенный риск кровотечений у больных Рандю-Ослером вызван ломкостью сосудов, но в 1998г учёными Endo, Mamiyaи Niitsu было замечено нарушение образования тромбоцитов. Так как процент таких больных был слишком мал, этот факт не стали вносить в диагностический критерий болезни, но сбрасывать его со счетов не стали.
Клиническая картина болезни Рандю-Ослера-Вебера
 Внешние признаки заболевания Вебера зачастую возникают в раннем школьном возрасте и проявляются в несколько этапов:
Внешние признаки заболевания Вебера зачастую возникают в раннем школьном возрасте и проявляются в несколько этапов:
- Начальный – на теле небольшое количество мелких пятен невоспалительного характера, которые имеют неправильную форму.
- Промежуточный – пятна постепенно увеличиваются и начинают принимать паукообразную форму.
- Узловой – диаметр расширения сосудов достигает 5-7 мм и выступает над уровнем кожных покровов.
В зависимости от расположения сосудистой звёздочки её цвет может варьироваться от алого до тёмно-синего.
Диагностический факт! Диагностическим критерием дефекта кожи является его исчезновение при надавливании на него. Этот метод хорошо известен как «диаскопия». Суть метода в распознании сосудистого или воспалительного характера пятна на коже. Обычным прозрачным стеклом на пятно надавливают. Если оно исчезло, значит, дефект сосудистого характера, если нет – воспалительного. При болезни Рандю-Ослера на коже возникают дефекты сосудистого характера, которые исчезают при надавливании.
Самым опасным клиническим признаком заболевания «Наследственная геморрагическая телеангиэктазия» является кровотечение. Оно может быть различно локализации и сопровождаться:
- Кровоподтёками на коже.
- Кровоизлияниями в глазном яблоке.
- Небольшим количеством свежей крови в кале.
- Кровью при чистке зубов.
- Кровотечением из носа.
- Кровью в мокроте при кашле или чихании.
- Алой кровью в рвотных массах.
Из-за потери хоть и небольшого количества крови, но постоянно, человек начинает чувствовать общие признаки болезни:
- Усталость.
- Сонливость.
- Головокружение и обмороки.
- Шум в ушах и «звёздочки» перед глазами.
- Учащение сердцебиения и одышка.
- Симптомы стенокардии.
Вышеперечисленные общие симптомы имеют обоснование:
- Нарушается трофика тканей, что приводит к гипоксии и голоданию клеток.
- Недостаток кислорода приводит к ускорению кровообращения.
- Патология сосудов сердца вызывает признаки кислородного голодания клеток сердечных клеток, что вызывает симптомы стенокардии.
Диагностические критерии заболевания
Симптомы, которые могут свидетельствовать о наличии болезни Рандю-Ослера:
- Частые носовые кровотечения – 90%.
- Воспалительные заболевания лёгких– 5-30%. В расширенных артерио-венозных анастомозах нижних отделах лёгких происходит застой крови, это приводит к застою в малом круге кровообращения и развитию воспалительных процессов. Это проявляется как одышка, цианоз, кровохарканье. Хроническая гипоксемия приводит к ответному повышению количества эритроцитов(гипоксемический эритроцитоз), что проявляется как сгущение крови.
- Желудочно- кишечные кровотечения в 20% случаев проявляют себя в возрасте 40-50 лет. Чаще это кровотечение из желудка, но в 10% случаев кровоточит толстая кишка, что может быть ошибочно расценено как геморрой, рак или полипоз.
- Нарушения работы головного и спинного мозга непосредственно связаны с сосудистой патологией, которая иногда купируется хирургическим путём.
- Цирроз печени возникает в 1-2%. Его причиной становиться именно нарушение трофики органа, но такое заключение является больше предположением, так как больные зачастую принимают большое количество медикаментов и исключить токсический медикаментозный гепатит нельзя.

Зачастую диагноз выставляется после длительного и мучительного лечения симптомов заболевания различными способами. Только благодаря подробному сбору анамнеза заболевания и жизни, тщательному осмотру тела пациента можно предположить наличие болезни Рандю-Ослера-Вебера. Для подтверждения предположительного диагноза необходимо сделать лабораторные и инструментальные методы диагностики.
Результаты лабораторных исследований:
- Клинический анализ крови – анемияили вторичный эритроцитоз на фоне снижения сатурации кислорода в крови,тромбоцитопения (редко).
- Биохимический анализ крови – недостаточность железа (вторичная железодефицитная анемия), нарушение электролитного состава крови.
- Пробы на свёртываемость крови – время свёртывания крови повышено (редко).
- Общий анализ мочи – эритроциты в моче (при наличии кровотечения в мочеполовой системе).

Результаты инструментальных методов исследования:
- ЭФГДС – признаки расширения сосудов слизистой оболочки верхнего отдела пищеварительной системы (ротовая полость, пищевод, желудок, ДПК).
- Колоноскопия – телеангиэктазии на слизистой толстого кишечника.
- Бронхоскопия – аневризмы и сосудистые звёздочки на слизистой оболочке дыхательных путей (применяется редко).
Иногда делают цистоскопию (осмотр мочевыделительных путей) и диагностические лапароскопические операции, но эти методы слишком травмаопасны, поэтому для подтверждения заболевания с целью не провоцировать возникновение кровотечения данные методы не применяются или применяются, но крайне редко.
Оптимальным методом осмотра сосудов внутренних органов является КТ или МРТ с контрастом, который позволяет визуализировать все аномальные сосудистые сплетения в организме.
Способы лечения болезни Рандю-Ослера
В настоящее время в мире существует 2 вида лечения любого заболевания:
- Патогенетическое лечение – способ борьбы непосредственно с синдромами проявления болезни.
- Этиологическое лечение – способ борьбы с главной причиной заболевания.
Так как причина заболевания кроется в генетическом коде каждой клетки человеческого организма, в практической медицине эффективным оказывается только патогенетическое лечение. Оно состоит из нескольких пунктов:
- Профилактика кровотечений.
- Поддержание кислотно-основного и электролитного состояния организма.
- Хирургическое иссечение больших дефектов сосудов.
- При необходимости укрепление стенки крупных сосудов (аорты).
- Купирование острых состояний: кровотечение, одышка, приступ стенокардии, головокружение, потеря сознания.

Особенности лечения больных синдромом Ослера
Лечение носовых кровотечений лучше не осуществлять с помощью тугих тампонад носовых ходов, так как это приводит к травме мелких сосудов и только усугубляет положение.
При кровотечении из мелких сосудов применение местных кровоостанавливающих средств является малоэффективным (Тромбин, Лебетокс).
Лучшим кровоостанавливающим средством является 5-8% Аминокапроновая кислота, которая при орошении слизистой и кожи действует быстро и длительно. После остановки кровотечения необходимо применить местные заживляющие препараты (Пантенол) для заживления раны.
Профилактика кровотечений состоит из:
- Ограничений в занятии травмоопасными видами спорта и досуга.
- Поддержание кровяного давления на нормальном уровне (110/70 – 120/80 мм.рт.ст.).
- Предупреждение воспалительных процессов в организме.
- Приём витаминов и микроэлементов в необходимом количестве.
- Ограничение стрессовых ситуаций.
- Ограничение и строгий контроль приёма препаратов разжижающих кровь (антикоагулянты).

В зависимости от тяжести течения болезни назначают лекарственные средства:
- Глюкокортикоиды (Преднизолон 4-8 мг в сутки) как противовоспалительное средство.
- Антиоксиданты для укрепления сосудов и вывода продуктов обмена (Аскорутин, Витамин Е).
- Препараты железа (Ферумлек) для лечения железодефицитной анемии.
- Приём большого количества воды для восполнения жидкости (Ессентуки, Регидрон).
В наше время этиологическое лечение наследственной геморрагической телеангиоэктазией невозможно, но есть шанс с помощью новейших технологий и разработок можно найти эффективный способ. Благодаря современным методикам коррекции ДНК в клетке в настоящее время можно предотвратить развитие заболевание у плода на ранних сроках внутриутробного развития или до момента зачатия.
На данный момент вложено большое количество денежных средств на изучение и разработку эффективных вариантов генотерапии заболевания. В любом случае генотерапия наследственной геморрагической телеангиэктазии это единственный шаг в будущее без этого смертельного заболевания, причиной которого стала ошибка ДНК половых клеток. Весь мир надеется, что человечество скоро узнает, чем лечить болезнь Рандю-Ослера.
Болезнь Рандю-Ослера. Причины, симптомы и лечение!
1.Общие сведения
К перечисленным в заголовке синонимическим диагнозам можно добавить еще несколько названий, часто употребляемых для обозначения данного заболевания, например, синдром Ослера, болезнь Рандю-Ослера-Вебера, геморрагическая телеангиэктазия и т.п.). Все они указывают на наиболее распространенный вид наследственной патологии сосудов: суть ее заключается в мелкоочаговом аномальном растяжении и истончении капиллярных стенок, что приводит к образованию множественных телеангиэктазий (сосудистых «звездочек», точек, «сеточек» и т.д.) с тенденцией к кровоточивости.
Эпидемиологическая картина характеризуется крайней неравномерностью и территориальной зависимостью. Так, болезнь Рандю-Ослера обнаруживается у каждого двухсотого из жителей Нидерландских Антильских островов, тогда как в других регионах земного шара частота встречаемости может не превышать 1:100 000.
2.Причины
На сегодняшний день в отношении патогенеза остаются вопросы. Согласно наиболее аргументированной и общепринятой точке зрения, характерная клиническая картина возникает вследствие аномального, неправильного строения тканей, из которых на этапе внутриутробного развития формируются стенки микрососудов: в них практически нет эластичных мышечных волокон, а оболочкой эндотелиальной стенки служит соединительная ткань. При таком составе сосудистая стенка отличается хрупкостью, уязвимостью и неустойчивостью к растяжениям, она легко образует аневризмы и разрывы, – что и приводит к кровотечениям.

Посетите нашу страницу
Сердечно-сосудистая хирургия
3.Симптомы и диагностика
Несмотря на то, что заболевание обусловлено генетически, проявляться оно начинает, как правило, лишь после 6-8 лет жизни. Первые видимые телеангиэктатические очаги обычно локализуются на губах, деснах, крыльях носа, щеках, мочках ушей. С годами телеангиэктазий становится больше, они появляются на новых участках и, кроме того, меняется их морфология: от маленьких красных точек к «паутинкам» и заметно выступающим ярко-красным узелкам. С возрастом усугубляется также геморрагическая тенденция.
Типичным и одним из первых симптомов болезни Рандю-Ослера являются носовые кровотечения. Их интенсивность в различных случаях варьирует: от сравнительно коротких и скудных до упорных и очень продолжительных. В истории медицины зафиксированы случаи смерти от кровопотери при геморрагической телеангиэктазии.
По мере прогрессирования сосудисто-стеночной несостоятельности телеангиэктатические очаги могут образовываться не только на слизистых и коже, но и на внутренних органах (головной мозг, ЖКТ, легкие, почки и т.д.). Соответственно, даже мелкие аневризмы или кровотечения в этом случае становятся очень опасными: высок риск развития тяжелой анемии и фатальной сердечнососудистой недостаточности.
Диагностика базируется на изучении анамнеза болезни (одним из ключевых признаков являются частые упорные кровотечения) и семейного анамнеза (наследственный фактор), а также на выявлении характерных телеангиэктазий. Как правило, на коже или слизистых оболочках они визуализируются уже при осмотре и не оставляют сомнений, однако вероятность латентных внутренних кровотечений создает показания к назначению эндоскопических исследований. Обязательно назначаются также общеклинический анализ крови и коагулограмма.

О нашей клинике
м. Чистые пруды
Страница Мединтерком!
4.Лечение
Первоочередными задачами являются предотвращение опасных геморрагий и купирование анемии, – в ряде случаев с этой целью назначают переливания крови. Длительное время терапевтическим стандартом при болезни Рандю-Ослера считалась тампонада носа, однако в настоящее время все больше специалистов отказываются от этого метода, находя в нем массу недостатков при малой эффективности. Сегодня в числе лечебных средств применяется орошение раствором аминокапроновой кислоты, различные методики коагуляции (крио-, электро-, лазерная) и искусственной эмболизации наиболее проблемных артерий. Наличие крупных аневризм зачастую вынуждает прибегать к хирургическому их устранению.
Пациентам с наследственной геморрагической телеангиэктазией приходится соблюдать особую диету и соблюдать все меры предосторожности, чтобы избегать травмирования кровоточивых и потенциально опасных очагов.