Этапы и принципы лечения острых лейкозов
Начало химиотерапии (XT) острых лейкозов (ОЛ) относится к 1946 г., когда проводилось лечение уретаном.Позже в лечебную практику были введены метотрексат, глюкокортикоиды, циклофосфан, 6-Меркаптопурин (1953 г.), винкристин (1960 г.), цитозар (1966 г.). Применение полихимиотерапии (ПХТ) в терапии ОЛ относится к началу 70-х годов ХХ-го века.
Основными целями лечения острых лейкозов является эрадикация лейкозного клона, восстановление нормального кроветворения и в результате этого — достижение длительной безрецидивной ремиссии или выздоровления больных.
Вследствие применения противоопухолевых препаратов развивается глубокая аплазия костного мозга (КМ). В период аплазии возникает т.н. состояние клональной конкуренции, когда пролиферативное преимущество получают клетки нормального кроветворного клона, которые и репопулируют КМ, восстанавливая здоровое поликлональное кроветворение.
В своем развитии острые лейкозы проходят несколько стадий:
— первый острый период (развернутая стадия, атака 1),
— полная ремиссия (клинико-гематологическая, цитогенетическая, молекулярная; первая, вторая и т.д.),
— выздоровление — наличие полной ремиссии более 5 лет,
— рецидив (первый, второй, и т.д.) — необходимо указывать локализацию рецидива: (костномозговой, экстрамедуллярный; нейролейкемия, поражение яичек, селезенки), даже при отсутствии изменений в анализах периферической крови и/или миелограмме,
— терминальная стадия.
Лечение острых лейкозов — многоэтапный и многокомпонентный процесс.
Но при всех ОЛ существует несколько основных этапов терапии:
— индукция ремиссии — максимально быстрое и существенное сокращение опухолевой массы и достижение полной ремиссии;
— консолидация ремиссии — закрепление достигнутого противоопухолевого эффекта; задачей этого периода является дальнейшее уменьшение числа остающихся после индукции ремиссии лейкемических клеток;
— поддерживающая терапия — продолжение цитостатического воздействия в малых дозах на возможно остающийся опухолевой клон; следует отметить, что при проведении некоторых программ интенсивной консолидационной терапии поддерживающая терапия не предусматривается;
— профилактика нейролейкемии — проводится при остром лимфобластном, монобластном, миеломонобластном, промиелоцитарном (на фоне терапии ATRA) лейкозах, а также при всех формах острого миелоидного лейкоза (ОМЛ) с исходным уровнем лейкоцитов выше 30,0х109/л; при уровне лейкоцитов менее 1,0х109/л и тромбоцитов менее первая люмбальная пункция проводится после первого курса индукции ремиссии при нормализации показателей периферической крови.
Вторым основополагающим принципом лечения ОЛ является необходимость проведения полноценной вспомогательной терапии, которая подразделяется на два направления — профилактику осложнений и их лечение.
К основным профилактическим методам относятся:
— обеспечение сосудистого доступа,
— профилактика синдрома массивного лизиса опухоли,
— профилактика геморрагических осложнений с помощью заместительных трансфузий тромбоцитов при их уровне менее 20,0х109/л,
— профилактика флебита, если не используется центральный венозный катетер,
— профилактика анемического синдрома — заместительные трансфузии эритромассы. В отсутствие признаков кислородной недостаточности при уровне гемоглобина 75-80 г/л не требуется трансфузии эритроцитов
— профилактика электролитных нарушений,
— профилактика коагуляционных нарушений (свежезамороженная плазма (СЗП), гепарин при гиперкоагуляции, ингибиторы протеолиза),
— профилактика инфекционных осложнений (селективная деконтаминация, обработка полости рта и т.д).
Практически у 80-90% больных ОЛ в период индукции ремиссии возникают те или иные инфекционные осложнения. Главный принцип лечения всех инфекций — эмпирическая поэтапная антибиотикотерапия с дальнейшим изменением спектра используемых антибиотиков в соответствии с результатами тестов. Модифицированный алгоритм лечения больных ОЛ в периоде глубокой цитопении (рис. 3).

Рис. 3. Алгоритм лечения фебрильной нейтропении
Поскольку целью терапии ОЛ является полная эрадикация лейкозного клона, для оценки эффективности терапии вводится понятие ремиссии острых лейкозов.
Различают несколько типов ремиссии, причем значение имеет только наличие полной ремиссии:
— клинико-гематологическая ремиссия: при нормо- или умеренно-клеточном костном мозге количество бластов в нем менее 5% при нормальном соотношении других ростков кроветворения; в периферической крови уровень гемоглобина (Hb) выше 100 г/л, количество тромбоцитов более 100,0х10
— цитогенетическая ремиссия: в идеале у больных должен отсутствовать лейкозный клон, т.е. не должны обнаруживаться кроветворные клетки с патологически измененным геномом, которые существовали в дебюте заболевания;
Однако при ОЛ в момент достижения полной клинико-гематологической ремиссии могут существовать три типа кроветворения:
а) восстановление нормального кроветворения,
б) сосуществование нормального и лейкемического (клонального) кроветворения, что соответствует понятию минимальной остаточной болезни, при которой рецидив неизбежен,
в) кроветворение восстанавливается в рамках лейкемического клона — ПХТ убирает лейкемический быстро прогрессирующий клон (фактически убирает субклоны) и позволяет предлейкемическому клону дифференцироваться до морфологически нормальных кроветворных клеток;
— молекулярная ремиссия: у больного ОЛ не определяются молекулярные маркеры — например, белки, синтезируемые химерными генами в результате транслокаций, которые характеризовали лейкемические клетки больного в дебюте заболевания.
Программа терапии любого варианта острых лейкозов по протоколам проводится с обязательным учетом факторов риска, причем эти факторы различны для острого лимфобластного лейкоза (ОЛЛ) и ОМЛ.
При ОЛЛ выделяют следующие группы риска:
1. Группа стандартного риска:
— вариант общего острого лимфобластного лейкоза (CD10+),
— возраст 15-35 лет,
— уровень лейкоцитов периферической крови менее 30,0х109/л,
— достижение ремиссии на 4-й неделе полихимиотерапии,
— отсутствие в бластах филадельфийской (Ph) хромосомы и химерного гена BCR/ABL с отсутствием продукции фузионного белка р190 или р185 кДа.
2. Группа высокого риска:
— ранний пре-В- или зрелый В-клеточный ОЛЛ,
— возраст 36-50 лет или менее 2 лет,
— уровень лейкоцитов периферической крови более 30,0х109/л,
— достижение ремиссии позже 4-й недели ПХТ,
— уровень лактатдегирогеназы (ЛДГ) более 1000 Ед/л,
— мужской пол,
— наличие Т-клеточного острого лимфобластного лейкоза (у больных детского возраста).
При ОМЛ выделяют следующие факторы риска:
— неадекватная ПХТ в начале лечения,
— возраст больного старше 60 лет,
— уровень лейкоцитов периферической крови более 30,0х109/л,
— уровень ЛДГ более 700 Ед/л,
— наличие миелодисплазии трех ростков кроветворения в момент установления диагноза ОМЛ,
— высокие показатели креатинина,
— тяжелый геморрагический синдром в дебюте ОМЛ,
— наличие очага инфекции до начала полихимиотерапии,
— нейролейкемия в дебюте заболевания,
Кроме того, прогностически неблагоприятными факторами при ОМЛ являются наличие хромосомных аберраций — трисомия 8, моносомия 5,7, делеции Хр5,7, t (10; 11). Наличие t (8; 21), t (15; 17), inv 16 позволяет отнести данных больных при отсутствии других факторов риска к группе с благоприятным прогнозом.
Следует отметить, что, если у пациента с кариотипом лейкозных клеток, отнесенного к неблагоприятному прогностическому варианту, ремиссия сохраняется в течение года, то признак теряет свое прогностическое значение. Поэтому наличие неблагоприятных прогностических факторов требует проведения более интенсивной терапии.
Ниже приводятся наиболее распространенные и эффективные протоколы ПХТ острых лейкозов. Дозы препаратов приводятся из расчета на один квадратный метр (м ) поверхности тела. Интервалы между курсами полихимиотерапии составляют 28 дней (от первого дня предыдущего цикла).
Программы полихимиотерапии острый миелобластный/миелоидный лейкоз «7+3»
Индукция ремиссии:цитозин-арабинозид — 100 мг/м в/венно 2 раза в сутки, 1-7 дни, даунорубицин (рубомицин) — 45 (60) мг/м в/венно 1 раз в сутки, 1-3 дни или митоксатрон — 10 мг/м в\венно 1 раз в сутки, 1-3 дни, или идарубицин — 12 мг/м в/венно 1 раз в сутки, 1-3 дни.
Проводится два курса индукции ремиссии, затем — два курса консолидационной терапии этими же препаратами в тех же дозах. При условии достижения полной ремиссии (по всем трем вариантам) начинаются курсы поддерживающей ротационной терапии, которые проводятся последовательно ежемесячно в течение трех лет:
«5 + 2»
Цитозин-арабинозид — 100 мг/м2 в/венно 2 раза в сутки, 1-5 дни, или подкожно по 50 мг/м2 4 раза в сутки, 1-5 дни. Даунорубицин (рубомицин) — 45 мг/м в/венно 1 раз в сутки, 1-2 дни.
«5 + ЦФ»
Цитозин-арабинозид — 100 мг/м2 в/венно 2 раза в сутки, 1-5 дни, или подкожно по 50 мг/м2 4 раза в сутки, 1-5 дни. Циклофосфан — 650 мг/м2 в/венно, 1 день.
«5 + 6-МП»
Цитозин-арабинозид — 100 мг/м2 в/венно 2 раза в сутки, 1-5 дни, или подкожно по 50 мг/м2 4 раза в сутки, 1-5 дни. 6-Меркаптопурин — 60 мг/м2 внутрь 2 раза в сутки, 1-5 дни, или 6-Тиогуанин — 50 мг/м2 внутрь 2 раза в сутки, 1-5 дни.
«5 + VCR + PRED»
Цитозин-арабинозид — 100 мг/м2 в/венно 2 раза в сутки, 1-5 дни, винкристин 1,4 мг/м2 в/венно, 1 день, преднизолон 60 мг/м внутрь ежедневно, 1-5 дни.
«7 + 3 + VP — 16»
Стандартная схема «7+3» дополняется введением этопозида в/венно в дозе 120 мг/м2 1 раз в сутки, 17-21 дни. Поддерживающая терапия проводится по схеме, приведенной выше. Следует отметить, что добавление вепезида в схему «7+3» статистически достоверно не отражается на 5-летней безрецидивной выживаемости больных.
Протокол CALGB
Индукция ремиссии:«7+3» — 1 курс.
Консолидация: HD-ARA-C — 4 курса:
цитозин-арабинозид — 3 г/м2 2 раза в сутки в/венно, 1, 3, 5, 7 дни.
«5+2» — 4 курса.
Далее поддерживающая терапия не проводится.
Протокол FLAG-Ida
Флюдарабин — 30 мг/м2, 30-минутная инфузия, 1-5 дни, цитарабин — 2 г/м2, 4-часовая инфузия через 4 часа после флюдарабина, 1-5 дни, идарубицин — 10 мг/м2 в сутки в/венно, 1-3 дни.За день до введения флюдарабина начинают введение гранулоцитарного колониестимулирующего фактора (Г-КСФ) в дозе 300 мкг/м ежедневно до дня восстановления показателей периферической крови.
Дальнейшая терапия может включать либо проведение аналогичного курса, либо выполнение другого курса по схеме:
идарубицин — 10 мг/м2 в/венно, 1-2 дни, цитарабин — 2 г/м2 в/венно, 1-2 дни.
При наличии резистентности протокол дополняется введением гентузумаба озогамина (GO) в дозе 9 мг/м в 8-й день цикла (протокол FLAG-I +GO).
Все пациенты с указанными формами ОМЛ, у которых достигнута ремиссия, должны рассматриваться как потенциальные кандидаты на выполнение трансплантации костного мозга (аллогенной или аутологичной).
«TAD — 9»Цитозин-арабинозид — 100 мг/м2 круглосуточно в/венно, 1-2 дни, цитозин-арабинозид — 100 мг/м2 в/венно 2 раза в сутки, 3-9 дни, даунорубицин — 60 мг/м2 в/венно 1 раз в сутки, 3-5 дни, 6-Тиогуанин — 100 мг/м2 внутрь 2 раза в сутки, 3-9 дни.
Обычно применяемая схема лечения по протоколу TAD-9 -программа двойной индукции. Второй индукционный курс каждому пациенту проводят на 21 день от начала терапии независимо от глубины цитопении и результатов первого курса. В последние годы программа была интенсифицирована, и второй курс TAD-9 был заменен программой НАМ.
Протокол НАМ
Цитозин-арабинозид — 3 г/м2 в/венно 2 раза в сутки, 1-3 дни, митоксантрон — 10 мг/м2 в/венно 1 раз в сутки, 3-5 дни.Российской исследовательской группой по изучению ОЛ рекомендуется следующий протокол терапии ОМЛ:
В качестве индукции ремиссии проводится 1 курс «7+3», далее, независимо от того, достигнута ремиссия или нет, проводятся 2 курса НАМ-терапии и два курса терапии цитозин-арабинозидом в высоких дозах (HiDAC) — цитарабин 3 г/м2 в/венно 2 раза в сутки 1, 3, 5, 7 дни, проводимые через две недели после восстановления показателей периферической крови. В дальнейшем поддерживающая терапия не проводится.
Перед курсом индукции ремиссии у больных с гиперлейкоцитозом (особенно выше 100,0х109/л) необходимо проведение предфазы циторедукционной терапии, рассчитанной на снижение числа лейкоцитов периферической крови приблизительно до 50,0х109/л.
Это позволяет уменьшить раннюю летальность больных вследствие предупреждения развития у них синдрома массивного лизиса опухоли (предупреждение легочного дистресс-синдрома, блокады функции почек). Терапию в предфазе проводят обычно гидроксимочевиной в дозе 60-100 мг на 1 кг веса в сутки на фоне гидратационной терапии (до 3 л/м2 в сутки) и приема аллопуринола (600-1200 мг/сутки) с целью профилактики блокады почечных канальцев солями мочевой кислоты.
При необходимости проводится форсированный диурез. Возможно проведение лейкоцитафереза на фоне приема гидроксимочевины. Данный подход может быть полезен при наличии симптомов лейкостаза в плане уменьшения объема циркулирующих опухолевых клеток.
Интралюмбальные пункции при ОМЛ проводятся в следующем режиме. Первая — до первого курса индукции; вторая/третья — перед следующими курсами индукции/консолидации; четвертая/пятая — перед третьим/шестым курсом ротационной терапии, все последующие — один раз в три месяца в течение одного года. Возможно более компактное проведение профилактических пункций: 4 пункции (по 2 в неделю) перед вторым курсом индукции/консолидации, затем — перед каждым вторым курсом поддерживающей терапии.
Применение ростовых факторов было связано с необходимостью сокращения сроков периода миелотоксического агранулоцитоза. Однако в больших рандомизированных исследованиях не выявлено статистически значимых отличий в отношении процента ремиссий, их продолжительности, частоте инфекционных осложнений и длительности антибиотикотерапии.
Более того, имеются данные о четкой тенденции к увеличению частоты рецидивов у больных, которым Г-КСФ вводился в период индукции ремиссии. Поэтому в рутинной практике можно не рекомендовать назначение Г-КСФ при лечении ОМЛ. Но если речь идет о высокодозных программах, то показано его применение в дозе 5 мкг/кг/сутки либо сразу после завершения курса индукции ремиссии, либо с первого дня развития агранулоцитоза.
Программы полихимиотерапии ОЛЛ
В лечении В-клеточных ОЛЛ взрослых применяется протокол CALGB 8811 (терапия без учета иммунофенотипа бластных клеток и групп риска — полная клинико-гематологическая ремиссия в 82%, 3-летняя безрецидивная выживаемость — в 41% случаев. Протокол практически идентичен применяемому в РБ протоколу Минск-98. Для лечения больных Т-клеточным ОЛЛ применяются другие протоколы ПХТ.Схема протокола CALGB 8811
Курс 1-й: индукция ремиссии (4 недели):циклофосфан — 1200 мг/м в/венно, 1-й день (800 мг/м2 для больных старше 60 лет), винкристин — 2 мг в/венно 1, 8, 15, 22 дни, даунорубицин — 45 мг/м в/венно, 1-3 дни (30 мг/м2 для больных старше 60 лет), преднизолон — 60 мг/м2 внутрь, 1-21 дни (1-7 дни для больных старше 60 лет), L-аспарагиназа — 6000 Ед/м2 подкожно, 1, 8, 11, 15, 18, 22 дни.
Курс 2-й: ранняя интенсификация: проводится два курса (8 недель):
метотрексат интратекально — 15 мг, 1-й день, циклофосфан — 1000 мг/м2 в/венно, 1-й день, 6-Меркаптопурин — 60 мг/м2 внутрь, 1-14 дни, цитарабин — 75 мг/м2 подкожно, 1-4, 8-11 дни, винкристин — 2 мг в/венно, 15, 22 дни, L-аспарагиназа — 6000 Ед/м подкожно, 15, 18, 22, 25 дни.
Курс 3-й: профилактика нейролейкемии и межкурсовая поддерживающая терапия (12 недель):
краниальное облучение — 2400 рад, 1-12 дни, метотрексат интратекально — 15 мг, 1, 8, 15, 22, 29 дни, 6-Меркаптопурин — 60 мг/м внутрь, 1-70 дни, метотрексат — 20 мг/м2 внутрь, 36, 43, 50, 57, 64 дни.
Курс 4-й: поздняя интенсификация (8 недель):
доксорубицин — 30 мг/м2 в/венно, 1, 8, 15 дни, винкристин — 2 мг в/венно, 1,8,15 дни, дексаметазон — 10 мг/м2 внутрь, 1-14 дни, циклофосфан — 1000 мг/м2 в/венно, 29-й день, 6-Тиогуанин — 60 мг/м2 внутрь, 29-12 дни, ццитарабин — 75 мг/м2 подкожно, 29-32, 36-39 дни.
Курс 5-й: длительная поддерживающая терапия (до 24 мес. от дня установления диагноза):
винкристин — 2 мг в/венно, 1-й день каждого 4-недельного цикла, преднизолон — 60 мг/м2 внутрь, 1-5 дни каждого 4-недельного цикла, 6-Меркаптопурин — 60 мг/м2 внутрь, 1-28 дни, метотрексат — 20 мг/м2 внутрь, 1, 8, 15, 22 дни.
В настоящее время для лечения ОЛЛ у взрослых рекомендуется следующий протокол:
Индукция ремиссии, фаза 1 (1-4 недели): даунорубицин — 60 мг/м2 в/венно, 1, 8, 15, 22 дни, винкристин — 1,4 мг/м2 в/венно, 1, 8, 15, 22 дни, дексаметазон — 10 мг/м2 внутрь, 1-5, 11-14 дни, ПЭГ-аспарагиназа — 2000 ед/м2 в/венно 2, 16 дни, метотрексат — 12,5 мг интратекально 14 день.
Фаза 2 (5-8 недели), при достижении уровня лейкоцитов 3,0х109/л:
циклофосфан — 650 мг/м2 в/венно 1, 15, 29 дни, цитарабин — 75 мг/м2 в/венно 6-9, 13-16, 20- 3, 27-30, 6-меркаптопурин — 60 мг/м2 внутрь 1-30 дни, метотрексат — 12,5 мг интратекально 1, 8, 15, 22 дни.
Интенсификация/таофилактика нейролейкемии: метотрексат — 3 г/м2 в/венно 1, 8 дни, ПЭГ-аспарагиназа — 2000 ед/м2 в/венно 2-й день. Постремиссионная терапия заключается в проведении поддерживающей терапии метотрексатом и 6-меркаптопурином в течение 24 месяцев с момента установления диагноза.
У пациентов с наличием ФНП решается вопрос об алло-ТГСК.
Для терапии рецидивов и рефрактерных форм ОЛЛ ГНЦ РАМН рекомендуется протокол РАЦОП. Протокол может быть использован в качестве консолидации у больных из группы риска.
Протокол RACOP/D-2005
Предфаза:преднизолон — 60 мг/м2 внутрь 1-7 дни или дексаметазон — 10 мг/м2 внутрь 1-7 дни.
Индукция ремиссии:
даунорубицин — 45 мг/м2 в/венно, 1-3 дни, цитарабин — 100 мг/м2 в/венно 2 раза в сутки, 1-7 дни, циклофосфамид — 400 мг/м2 в/венно 1 раз в сутки, 1-7 дни, винкристин — 2 мг в/венно, 1, 7 дни, преднизолон — 60 мг/м2 внутрь, 1-7 дни.
Профилактика нейролейкемии:
В период I фазы индукции ремиссии выполняется шесть ин-тратекальных пункций с введением метотрексата, цитарабина и преднизолона в стандартных дозах.
Терапия консолидации:
После проведения двух полнодозных курсов проводят один идентичный курс, но с дозой циклофосфана 200 мг/м и одним введением винкристина.
Терапия поддержания ремиссии по схеме чередования курсов 5-дневного RACOP — COAP — COMP с интервалом в один месяц в течение 3 лет от момента начала терапии.
В период поддерживающей терапии интратекальные пункции выполняются один раз в три месяца в течение всего периода лечения. Облучение головы в дозе 24 Гр выполняется только как этап лечения нейролейкемии.
5-дневный RACOP:
даунорубицин — 45 мг/м2 в/венно, 1-2 дни, цитарабин -100 мг/м2 в/венно 2 раза в сутки, 1-5 дни, циклофосфамид — 200 мг/м2 1 раз в сутки, 1-5 дни, винкристин — 2 мг в/венно, 1-й день, преднизолон — 60 мг/м2 внутрь, 1-5 дни.
COAP:
циклофосфан — 400 мг/м2 в/венно 1 раз в 1-й день, винкристин — 2 мг в/венно в 1-й день, цитарабин — 60 мг/м2 в/венно 2 раза в сутки, 1-5 дни, преднизолон — 40 мг/м2 внутрь, 1-5 дни.
СОМР:
циклофосфан — 1000 мг/м2 в/венно в 1-й день, винкристин — 2 мг в/венно в 1-й день, метотрексат — 12,5 мг/м2 в/мышечно или внутрь 1 раз в сутки, 3-4 дни, преднизолон — 100 мг внутрь, 1-5 дни.
Терапия острого лимфобластного лейкоза взрослых по протоколу MRC UCALL XII/ECOG E2993
Индукция ремиссии, фаза 1; 1-4 недели. даунорубицин — 60 мг/м2 в/венно 1, 8, 15, 22 дни винкристин — 1,4 мг/м2 в/венно 1, 8, 15, 22 дни, L-аспарагиназа — 10000 Ед в/венно или в/мышечно 17-28 дни,преднизолон — 60 мг/м2 внутрь 1-28 дни метотрексат -12,5 мг интратекально, 15 день. фаза 2; 5-8 недели.
Циклофосфамид — 650 мг/м2 в/венно 1, 15, 22 дни, цитарабин — 75 мг/м2 в/венно 1-1, 8-11, 15-18, 22-25 дни, 6-меркаптопурин — 60 мг/м2 внутрь, 1-28 дни, метотрексат — 12,5 мг интратекально, 1, 8, 15, 22 дни. Диагностическая люмбальная пункция выполнялась у всех пациентов.
Если нейролейкемия выявлялась в начале заболевания, метотрексат вводился интратекально или в цистерну Омайя каждую неделю до санации спинномозговой жидкости (в 1-й фазе). Дополнительно во время 2-й фазы проводилось облучение головного мозга в суммарной очаговой дозе (СОД) 24 Гр и спинного мозга в СОД 12 Гр, при этом метотрексат во 2-й фазе не вводился.
Терапия интенсификации:
• метотрексат — 3 г/м2 в/вено, 1, 8, 22 дни,
• L-аспарагиназа — 10000 Ед в/венно, 2, 9, 23 дни + стандартная доза лейковорина.
Консолидационный предтрасплантационный режим перед алло- или ауто-трансплантации гемопоэтических стволовых клеток (ТГСК) включал тотальное облучение тела в СОД 13,2 Гр (дважды в день по 2,2 Гр шесть раз) в дни 6-1 до трансплантации, дополненный введением этопозида в дозе 60 мг/кг в/венно в 3 день.
У пациентов, не подлежащих алло- или ауто-ТГСК, если нейролейкемии не было в дебюте заболевания, проводилась профилактика нейролейкемии:
• цитарабин — 50 мг в/вено, в 1-й день недели, всего 4 раза,
• краниальное облучение в СОД 24 Гр, цитарабин — 50 мг и/текально в таком же режиме спустя 3 месяца, всего 4 раза.
Терапия консолидации проводилась на фоне поддерживающей терапии.
1-й цикл: цитарабин — 75 мг/м2 в/венно 1-5 дни, этопозид — 100 мг/м2 в/венно 1-5 дни, винкристин — 1,4 мг/м2 в/венно 1, 8, 15, 22 дни, дексаметазон — 10 мг/м2 внутрь 1-28 дни.
2-й цикл: (начинается через 4 недели после 1-го цикла): цитарабин — 75 мг/м2 в/венно 1-5 дни, этопозид — 100 мг/м2 в/венно 1-5 дни.
3-й цикл: (начинается через 4 недели после 2-го цикла): даунорубицин — 25 мг/м2 в/венно 1, 8, 15, 22 дни, циклофосфамид — 650 мг/м в/венно в 29 день, цитарабин — 75 мг/м2 в/венно 31-34, 38-й дни, тиогуанин — 60 мг/м2 внутрь 29-12 дни.
4-й цикл идентичен 2-му циклу и начинается через 8 недель после окончания 3-го цикла.
Поддерживающая терапия (проводится в течение 2,5 лет после начала терапии интенсификации):
винкристин — 1,4 мг/м2 в/венно каждые 3 месяца, преднизолон — 60 мг/м2 внутрь 5 дней каждые 3 месяца, 6-меркаптопурин — 75 мг/м2 внутрь ежедневно постоянно, метотрексат — 20 мг/м2 внутрь или в/венно 1 раз в неделю. ФНП являлись: возраст старше 35 лет, отсутствие клинико-гематологической ремиссии на 4-й неделе или лейкоцитоз выше 30,0х109/л для В-ОЛЛ и выше 100,0×10% для Т-ОЛЛ, наличие Ph+ хромосомы.
Отдельно следует остановиться на программе лечения острого промиелоцитарного лейкоза (ОПЛ).
В связи с включением в схему терапии ОПЛ полностью трансретиноевой кислоты (all-trans retinoic acid — ATRA) клинико-гематологическая и цитогенетическая ремиссии констатируются уже после индукционного курса почти у 100% больных ОПЛ, однако молекулярно-генетическая ремиссия (отсутствие транскрипта PML/RARA-promyelocytic leukemia/retinoic acid receptor alpha) отмечена после второго курса постремиссионной терапии. Поэтому центральное место в оценке эффективности противолейкемической терапии занял мониторинг молекулярного рецидива.
В настоящее время общепринятыми являются следующие протоколы терапии ОПМ.
Протокол ОПЛ-2003
Индукция ремиссии:ATRA (весаноид) в дозе 25 мг/м2 в два приема в день по установлению диагноза до достижения полной ремиссии (не более 90 дней).
Курс «7+3» терапии в полных дозах с третьего дня приема ATRA с разовой дозой даунорубицина 60 мг/м2.
Постремиссионная консолидация: в течение трех месяцев проводится три курса терапии по схеме «7+3» с разовой дозой даунорубицина 45 мг/м2.
Интенсификация (один курс после восстановления показателей анализов крови):
ATRA — 25 мг/м2 в два приема в день — 1-14 дни,
цитарабин — 1 г/м2 2 раза в сутки в/венно — 3-6 дни,
даунорубицин — 30 мг/м2 в сутки в/венно — 1-3 дни.
Поддерживающая терапия постоянно в течение двух лет:
6-Меркаптопурин — 90 мг/м2 в сутки внутрь, метотрексат — 15 мг/м внутрь 1 раз в неделю.
Поздняя интенсификация: ATRA 25 мг/м2 в сутки в течение 15 дней каждые три месяца на фоне поддерживающей терапии.
Протокол PETHEMA
Индукция ремиссии:ATRA 45 мг/м2 в два приема в день до достижения полной ремисии (максимум в течение 90 дней).
Для пациентов моложе 20 лет доза уменьшена до 25 мг/м2, Идарубицин 12 мг/м в день в/венно в 2, 4, 6, 8 дни.
У пациентов старше 70 лет идарубицин в 8-й день не вводился.
Постремиссионная консолидация:
В течение трех месяцев проводятся следующие курсы монохимиотерапии:
1) идарубицин — 5 мг/м2 в день в/венно 1-4 дня, (1-й месяц),
2) митоксантрон — 10 мг/м2 в день в/венно 1-5 дней, (2-й месяц),
3) идарубицин — 12 мг/м2 в/венно 1-й день, (3-й месяц).
В группе пациентов промежуточного и высокого риска ежемесячно в сочетании с курсом монохимиотерапии проводился прием ATRA в дозе 45 мг/м2 1-15 дня.
Поддерживающая терапия (проводится в течение двух лет): 6-Меркаптопурин — 50 мг/м2 внутрь ежедневно, метотрексат — 15 мг/м2 внутримышечно 1 раз в неделю, ATRA 45 мг/м2 внутрь в два приема 1-15 дни каждого третьего месяца на фоне поддерживающей терапии.
Гематологическая ремиссия констатируется при нормализации гемограммы и содержания атипичных промиелоцитов в миелограмме менее 5%; молекулярная ремиссия — при наличии критериев гематологической ремиссии и отсутствии транскрипта PML/RARA в КМ.
Гематологическим рецидивом считается появление любого количества атипичных промиелоцитов в периферической крови или более 20% в миелограмме, или более 5% атипичных промиелоцитов в миелограмме при молекулярно-биологическом подтверждении наличия транскрипта PML/RARA в костного мозга на основании данных полимеразной цепной реакции (ПЦР).
Вторым препаратом в лечении ОПЛ, показавшим свою активность как в лечении первичных больных, так и при рецидивах, является триоксид мышьяка (Трисенокс), позволяющий получить полные ремиссии у 70-90% больных. Препарат не обладает цитостатическим действием, но способствует дифференцировке атипичных промиелоцитов до зрелых форм.
Триоксид мышьяка назначают в дозе 0,15 мг/кг в сутки в виде 1-2-часовой инфузии, лечение проводится до достижения ремиссии, но не более 50 дней. При получении ремиссии проводится консолидация: введение препарата в той же дозе по 5 дней в неделю на протяжении 5 недель. Безрецидивная выживаемость значительно выше при проведении повторных курсов терапии в сочетании триоксида мышьяка и цитостатических препаратов.
При наличии факторов риска рекомендуется аллотрансплантация гемопоэтических стволовых клеток в первой ремиссии.
А.Т. Фиясь
Опубликовал Константин Моканов
Острый лейкоз – лечение и прогноз
Лечение
Целью терапии является максимально полное уничтожение (эрадикация) лейкозного клона, восстановление нормального кроветворения, достижение длительной ремиссии или выздоровление. Для всех лейкозов существует три обязательных этапа лечения: индукция, консолидация, поддерживающая терапия и профилактика нейролейкемии.
Индукция проводится с момента установления диагноза и направлена на максимально быстрое уничтожение основной массы опухолевых клеток. Цель этапа консолидации — уничтожение оставшихся наиболее резистентных лейкозных клеток и предотвращение рецидива.
Лечение острых миелобластных лейкозов
Лечение острых миелобластных лейкозов (за исключением промиелоцитарного) начинается химиотерапией цитарабином и атрациклинами. Цитарабин является антиметаболическим препаратом, препятствующим синтезу ДНК. Противоопухолевые антибиотики из группы атрациклинов (даунорубицин, даунозом, идарубицин, дексорубицин и др.) приводят к разрыву цепей ДНК.
Наиболее часто для индукции используется программа «7+3»: цитарабин 100—200 мг/м2 в/в непрерывно в течение 7 сут, даунорубицин 45 мг/м2/сут в/в струйно в течение 3 сут.
Эффективность лечения может быть повышена при замене даунорубицина на идарубицин, который вводят в/в струйно в дозе 12–13 мг/м2 в первые 3 дня лечения.
Если полная ремиссия не достигнута в течение 14 и более суток, проводят второй курс индукционной химиотерапии по схеме «5+2» в тех же дозах цитостатиков, что и по схеме «7+3», но цитарабин вводят в течение 5 суток, а атрациклин — в первые 2 дня курса. Большая эффективность повторного курса может быть достигнута при лечении по схеме с высокими дозами цитарабина (3 г/м2 в течение 1 ч каждые 12 ч, всего 12 раз в зависимости от возраста — больным старше 50 лет дозу снижают до 1,5 г/м2) и идарубицина в дозе 12 мг/м2/сут в течение 3 сут. Лечение по схеме «7+3» позволяет получить полную ремиссию у 65 — 70% больных острым миелоидным лейкозом. После второго курса индукционной терапии полная ремиссия достигается у 75 — 80% больных.
При индукционной терапии миелоидных лейкозов по схеме «7+3» возможно применение этопозида — ингибитора ДНК-топоизомеразы II-фермента. Схема «7+3» с этопозидом увеличивает продолжительность безрецидивного периода, но на выживаемость не влияет.
Одновременно с индукционной химиотерапией проводят симптоматическую терапию, направленную на борьбу с осложнениями. При развитии агранулоцитоза необходимо переливание тромбоцитарной массы с целью поддержания уровня тромбоцитов выше 20000 мкл-1. Показаниями для переливания тромбоцитарной массы являются кровотечения и ДВС-синдром. При снижении гемоглобина ниже 8,5 г% показано переливание эритроцитарной массы, предварительно облученной для профилактики реакции «трансплантат против хозяина», через лейкоцитарные фильтры для предупреждения аллоиммунизации и пирогенной реакции.
При аплазии костного мозга, осложнившей химиотерапию, возможно развитие инфекции — основной причины смертельных исходов. Лихорадка в этот период является показанием для начала эмпирического лечения антибиотиками широкого спектра действия (пенициллином, ванкомицином, цефалоспоринами третьего поколенья) и противогрибковыми препаратами. После получения результатов посева крови проводят коррекцию лечения.
В настоящее время начато применения рекомбинантных ростовых кроветворных факторов, повышающих чувствительность опухолевых клеток к цитостатикам. Используют препараты Г-КСФ и ГМ-КСФ, которые увеличивают выживаемость и частоту полных ремиссий в результате уменьшения смертельных инфекционных осложнений. С целью стимуляции созревания и дифференцировки мегакариоцитов используют тромбопоэтин, уменьшающий продолжительность тромбоцитопении.
Индукционная химиотерапия может привести к массивному распаду опухоли, сопровождающемуся образованием большого количества солей мочевой кислоты, вызывающих блокаду почечных канальцев. Профилактика этого осложнения проводится гипергидратацией (3 л/м2) и аллопурином (600 — 800 мг/сут).
Лечение острого промиелоцитарного лейкоза
Лечение острого промиелоцитарного лейкоза проводят третиноином (ретиновой кислотой) при условии наличия транслокации t(15,17). Третиноин индуцирует дифференцировку и тормозит пролиферацию промиелоцитов, не обладая цитолитическим действием, приводит к начальному созреванию промиелоцитов, происходящих из лейкемического клона. В результате происходит перезаселение костного мозга и периферической крови нормальными поликлоновыми гемопоэтическими клетками и достижение полной ремиссии.
В первые три недели лечения третиноином возможны различные осложнения, в том числе «синдром ретиноевой кислоты», который проявляется лихорадкой, одышкой, болями в груди, нарастающей гипоксией и очагами затемнения в легких. Интенсивная терапия, глюкокортикоиды, ингаляция кислорода обычно уменьшают проявления синдрома. Для профилактики развития синдрома ретиноевой кислоты больным, имеющим высокий исходный уровень лейкоцитов (больше 10000 мкл-1), следует проводить полнодозную химиотерпию.
Преимущество третиноина перед стандартной схемой «7+3» доказано в контролируемых многоцентровых исследованиях. Большинство больных, леченых третиноином, имели значительную полную ремиссию. Но большое значение для прогноза рецидивов имеет проявление минимальной остаточной болезни. Отсутствие транскриптов химерного гена PML-RARA — признак длительного безрецидивного периода, но их наличие предсказывает рецидив. В этих случаях лечение необходимо продолжить.
Лечение острых лимфобластных лейкозов
Химиотерапия острого лимфобластного лейкоза в настоящее время достигла значительных успехов, особенно у детей. Бластные клетки при остром лимфобластном лейкозе более чувствительны к химиотерапии, чем бластные клетки при остром миелобластном лейкозе. Индукция проводится препаратами, позволяющими элиминировать бластные клетки при щадящем воздействии на костный мозг.
Наиболее часто применяют комбинацию винкристина (2 мг внутрь в 1-й, 8-й, 11-й, 15-й, 18-й, 22-й дни), преднизолона (60 мг/м2 внутрь ежедневно), L-аспарагиназы (6000 IU/м2 п/к в 1-й, 8-й, 11-й, 15-й, 18-й, 22-й дни). При четырехнедельной индукции используют дополнительно циклофосфан (1200 мг/м2 в/в в 1-й день) и даунорубицин (45 мг/м2 в/в в первые 3 дня). В качестве закрепляющей терапии применяют 6-меркаптопурин и метотрексат. Многим больным требуется профилактическое лечение нейролейкемии).
Химиотерапия дает хорошие результаты, особенно у детей до 15 лет. Полная ремиссия (обычно более 2 лет) может быть достигнута у 80% взрослых, но стойкая ремиссия наблюдается только у 15 — 20% больных. После первого рецидива основное значение приобретает трансплантация костного мозга. Лучевую терапию применяют для профилактики позднего рецидива. Облучают ЦНС и иногда гонады, наиболее опасные в отношении развития рецидивов.
На этапе консолидации проводят курс химиотерапии аналогично индукционному или курс с использованием высоких доз цитарабина в комбинации с метоксантроном или даунорубицином. Более эффективно проведение трех курсов высокодозного цитарабина.
Поддерживающая терапия включает ежемесячные программы «5+2»: цитарабин 100 мг/м2 в/в 2 раза в день и даунорубицин 45 мг/м2 в/в 1 раз в день.
Для консолидации используют алло- или аутотрансплантацию костного мозга. Аллотрансплантация проводится при отсутствии следующих противопоказаний: почечной, дыхательной и сердечно-сосудистой недостаточности. Донорами костного мозга обычно служат родные братья и сестры, совместимые с реципиентом по HLA. Трансплантацию костного мозга проводят во время полной первой ремиссии. Установлено, что после аллотрансплантации костного мозга рецидивы возникают несколько реже, но выживаемость практически не отличается от выживаемости после химиотерапии.
При аутотрансплантации больной получает собственные стволовые клетки, выделенные из крови и замороженные в первые дни восстановления костного мозга после высокодозовой химиотерапии или неочищенного костного мозга, загрязненного опухолевыми клетками. Ремиссия в течение 4-х лет наблюдается у 48% больных после аутотрансплантации костного мозга.
Трансплантация костного мозга может привести к тяжелым осложнениям: реакции «трансплантат против хозяина» (РТПХ), инфекции и вено-окклюзивной болезни. Главное осложнение — РТПХ — развивается вследствие пересадки Т-лимфоцитов, вызывающих иммунную реакцию против собственных антигенов.
РТПХ может развиться в течение 20–100 дней после трансплантации (острая реакция) лимфоцитов и через 6–12 мес (отсроченная реакция). Клинические проявления — дерматит, поражения желудочно-кишечного тракта (диарея) и печени (аутоиммунный гастрит).
При лечении синдрома «трансплантат против хозяина» используют высокие дозы метилпреднизолона. Препаратом второго ряда является антимоцитарный иммуноглобулин. Возможно назначение комбинации преднизолона, циклоспорина и малых доз азатиоприна в течение 1,5 — 2 мес.
Профилактика и лечение нейролейкемии
Профилактика и лечение нейролейкемии проводится при миеломонобластном, монобластном, промиелоцитарном лейкозах, а также в тех случаях, когда исходный лейкоцитоз превышает 30х109/л. У больных лимфобластными лейкозами она осуществляется при всех формах.
Профилактика нейролейкемии проводится в течение всех этапов лечения острого лейкоза. В периоде индукции эндолюмбально вводится 12,5 мг/м2 метотрексата 5 раз с интервалом 3 — 4 дня. В дальнейшем производится регулярное (1 раз в 3 месяца) введение метотрексата (12,5 мг/м2) и цитозара (25 мг) в течение всего времени терапии. В случаях непереносимости или возникновения церебральных осложнений при лечении указанными препаратами применяется курс облучения головы в суммарной дозе 24 ГР за 15—18 сеансов.
Лечение нейролейкемии проводится эндолюмбальным введением метотрексата (12,5 мг/м2) и цитозара (25 мг), доза которого в последующие пункции с интервалом 2 — 3 дня постепенно повышается до 30 мг. При проявлениях резистентности к данному лечению применяется краниальное облучение в суммарной дозе 24 ГР за 15 — 18 сеансов. Эффективность профилактики и лечения нейролейкемии оценивается по уровню бластного цитоза в спинномозговой жидкости в течение 1 года терапии.
Диспансеризация
В период полной клинико-гематологической ремиссии больной находится под регулярным наблюдением гематолога и врача общей практики. Исследование периферической крови (с гемограммой) производится 2 раза в месяц. Исследование миелограммы (стернального пунктата) осуществляется 1 раз в месяц на первом году ремиссии. Санаторно-курортное лечение противопоказано.
Прогноз
Ведущее значение в благоприятном исходе имеет достижение полной клинико-гематологической ремиссии. Достижение ремиссии зависит от различных факторов. Один из важнейших — возраст больного на момент постановки диагноза. Прогноз лучше у детей в возрасте от 2 до 6 лет, хуже у больных возрастной группы от 7 до 55 лет, у пожилых (после 55 лет) прогноз неблагоприятный.
Вторым независимым прогностическим фактором являются хромосомные абберации. Благоприятный прогноз у больных с транслокацией t(8;21) и инверсией inv(16), менее благоприятный прогноз у больных с транслокацией t(16) и у больных, не имеющих хромосомных аббераций.
Определенное негативное влияние на прогноз имеют наличие исходной трехростковой дисплазии кроветворения с анемией, лейкопенией или тромбоцитопенией, существовавшей более 1 мес, выраженный геморрагический синдром, тяжелые инфекционные осложнения. Меньшее значение имеют активность ферментов (ЛДГ) сыворотки крови и выраженный лейкоцитоз (или абсолютное число бластных клеток в крови).
Наиболее значимое влияние на прогноз могут оказывать нарушения стратегии и тактики химиотерапии: неправильный выбор программы лечения, несоблюдение доз цитостатиков, интервалов между курсами, плохое качество вспомогательной терапии и т.д. Это приводит к формированию резистентного лейкозного клона, что делает дальнейшую терапию малоперспективной.
| Губка гемостатическая |
| Азацитидин (Azacitidine) |
| Аллопуринол (Allopurinol) |
| Амброксол (Ambroxol) |
| Амикацин (Amikacin) |
| Аминокапроновая кислота (Aminocaproic acid) |
| Амлодипин (Amlodipine) |
| Амфотерицин B (Amphotericin B) |
| Анидулафунгин (Anidulafungin) |
| Антиингибиторный коагулянтный комплекс (Antiingibitorny coagulant complex) |
| Ацикловир (Acyclovir) |
| Бупивакаин (Bupivacaine) |
| Ванкомицин (Vancomycin) |
| Вориконазол (Voriconazole) |
| Ганцикловир (Ganciclovir) |
| Гентамицин (Gentamicin) |
| Гепарин (Heparin) |
| Гидроксикарбамид (Hydroxycarbamide) |
| Даунорубицин (Daunorubicin) |
| Дексаметазон (Dexamethasone) |
| Децитабин (Decitabine) |
| Дротаверин (Drotaverinum) |
| Идарубицин (Idarubicin) |
| Имипенем (Imipenem) |
| Иммуноглобулин человека нормальный (IgG+IgA+IgM) (Immunoglobulin human normal (IgG+IgA+IgM)) |
| Итраконазол (Itraconazole) |
| Каптоприл (Captopril) |
| Каспофунгин (Caspofungin) |
| Колистиметат натрия (Colistimethate sodium) |
| Концентрат тромбоцитов (КТ) |
| Лактулоза (Lactulose) |
| Левофлоксацин (Levofloxacin) |
| Лидокаин (Lidocaine) |
| Лизиноприл (Lisinopril) |
| Линезолид (Linezolid) |
| Меркаптопурин (Mercaptopurine) |
| Меропенем (Meropenem) |
| Метотрексат (Methotrexate) |
| Метронидазол (Metronidazole) |
| Микафунгин (Micafungin) |
| Митоксантрон (Mitoxantrone) |
| Надропарин (Nadroparin) |
| Омепразол (Omeprazole) |
| Ондансетрон (Ondansetron) |
| Офлоксацин (Ofloxacin) |
| Пиперациллин (Piperacillin) |
| Плазма свежезамороженная |
| Повидон (Povidone) |
| Позаконазол (Posaconazole) |
| Прокаин (Procaine) |
| Спиронолактон (Spironolactone) |
| Сульбактам (Sulbactam) |
| Сульфаметоксазол (Sulphamethoxazole) |
| Тобрамицин (Tobramycin) |
| Торасемид (Torasemide) |
| Трамадол (Tramadol) |
| Триметоприм (Trimethoprim) |
| Фамотидин (Famotidine) |
| Филграстим (Filgrastim) |
| Флударабин (Fludarabine) |
| Флуконазол (Fluconazole) |
| Фолиевая кислота (Folic acid) |
| Фуросемид (Furosemide) |
| Хлоргексидин (Chlorhexidine) |
| Цефепим (Cefepime) |
| Цефоперазон (Cefoperazone) |
| Цефтазидим (Ceftazidime) |
| Циклофосфамид (Cyclophosphamide) |
| Ципрофлоксацин (Ciprofloxacin) |
| Цитарабин (Cytarabine) |
| Эноксапарин натрия (Enoxaparin sodium) |
| Эритроцитарная масса |
| Эртапенем (Ertapenem) |
Паллиативная помощь при остром лейкозе у взрослых, лечение острого лейкоза

Лейкозы — это большая группа заболеваний, при которой происходит поражение системы кроветворения (гемопоэза). Чтобы лучше понять, что происходит с организмом при лейкозе, сначала нужно понимать, как организована система гемопоэза.
Клетки крови образуются из полипотентных (которые дают начало нескольким типам клеток) гемопоэтических (кровеобразующих) стволовых клеток (ГСК). Они проходят несколько стадий развития и в конце концов достигают зрелого состояния, при котором уже способны выполнять свои функциональные обязанности. Пока клетки незрелые, они не выходят в кровоток, а располагаются в органах кроветворения, главным образом в костном мозге, где и проходят свою дифференцировку и «обучение».
ГСК может пойти развиваться по двум направлениям:
- Миелопоэтическому, при котором образуются миелоидные клетки. Они названы так из-за того, что основную дифференцировку проходят в костном мозге (myelos — мозг, отсюда и название). В эту группу входят эритроциты, гранулоциты (нейтрофилы, базофилы и эозинофилы), моноциты и тромбоциты.
- Лимфопоэтическому, при котором образуются лимфоидные клетки. В процессе развития, они помимо костного мозга проходят дифференцировку в лимфатических узлах, селезенке и тимусе.
Итак, ГСК в процессе развития проходит несколько стадий:
- Стволовая клетка (СК) — она может пойти по любому пути развития в зависимости от потребностей организма.
- Частично детерминированная СК — на этой стадии она уже определилась, в каком направлении будет развиваться, миелоидном или лимфоидном.
- Унипотентная стволовая клетка — здесь уже начинают закладываться признаки дифференцировки внутри своего направления. Например, миелоидные клетки могут пойти в направлении эритропоэза, тромбопоэза или гранулопоэза, а лимфоидные клетки дифференцируются в направлении предшественников Т- и В-лимфоцитов.
- Бласты — это уже определившиеся клетки, в которых можно определить характерные для каждого типа клеток признаки, например, набор ферментов и рецепторов.
- Незрелые клетки, например, промиелоциты, пролимфоциты и др. Они способны выполнять какие-то функции, но не в полной мере. Тем не менее, при особой потребности организм использует и их ресурсы, выпуская их в общий кровоток.
- Зрелые клетки — они уже полноценные «бойцы».
В зависимости от того, на каком этапе развития происходит сбой, выделяют острые и хронические лейкозы. При острых лейкозах сбой происходит на уровне незрелых клеток — бластов. Поэтому их еще называют бластными лейкозами. Они имеют агрессивное течение, поскольку опухолевые клетки не могут выполнять свои функции, что без лечения быстро приводит к гибели больного. При хронических лейкозах сбой дифференцировки происходит уже на стадии зрелых клеток, поэтому они имеют более доброкачественное течение.
В зависимости от того, какой росток кроветворения поврежден, выделяют следующие виды острых лейкозов:
- Острый миелобластный лейкоз — опухоль из миелоидного ростка кроветворения. Более характерен для пожилых людей, но может встречаться и у молодых пациентов.
- Острый промиелоцитарный лейкоз — это особый тип миелобластного лейкоза, при котором сбой происходит на уровне незрелых гранулоцитов — промиелобластов. Раньше это была фатальная форма лейкоза, при которой пациенты погибали в течение нескольких недель после постановки диагноза. Но сейчас, при появлении трансретиноевой кислоты, лечение этой формы патологии достигло колоссальных успехов.
- Острый монобластный лейкоз — поражается моноцитарная линии кроветворения.
- Эритромиелоз — поражается красный росток кроветворения — эритроцитарный.
- Острый мегакариобластный лейкоз — очень редкая форма миелоцитарного лейкоза. При нем происходит поражение тромбоцитарного ростка.
- Острый лимфобластный лейкоз — это форма лимфопоэтичекого лейкоза. При нем поражается лимфоцитарный росток кроветворения. Заболевание в больше мере характерно для детского возраста.
Запись на консультацию круглосуточно
Причины возникновения острого лейкоза
Лейкозы возникают из-за мутации ГСК. При этом разные мутации проявляются на разных этапах гемопоэза. Следует сказать, что одного факта наличия мутации недостаточно. Вообще генетические поломки в клетках, в том числе и гемопоэтических, возникают регулярно, но существуют механизмы, которые либо уничтожают такие клетки, либо блокируют ее дальнейшее развитие. Чтобы развился лейкоз, нужны особые обстоятельства:
- Повторные мутации в уже мутировавшей ГСК.
- Ослабление иммунной защиты, при которой мутировавшая клетка остается нераспознанной и начинает активно размножаться. Такие промахи иммунитета могут возникнуть как в период внутриутробного развития, так и в процессе жизни взрослого человека.
Таким образом, к факторам риска развития острого лейкоза относят следующие:
- Наследственная предрасположенность.
- Вторичные и первичные иммунодефициты.
- Воздействие ионизирующего излучения — рентген, лучевая терапия и др.
- Некоторые химикаты.
- Некоторые лекарственные препараты, например, цитостатики, которые применяются для лечения злокачественных новообразований.
- Вирусы. В частности, доказана этиологическая роль вируса Эпштейна-Барр.
Методы лечения острых лейкозов
Лечение острых лейкозов проводится в соответствии с утвержденными протоколами и проходит в несколько стадий. Целью лечения является достижение стойкой полной ремиссии. В среднем, полный курс лечения занимает около 2-х лет. При развитии осложнений этот срок может увеличиваться.

Для подбора оптимальной схемы терапии, необходимо знать вид острого лейкоза, его молекулярно-генетический профиль и группу риска для пациента. При стандартной группе риска, лечение проводится в соответствии со следующей схемой:
- Индукция ремиссии — это самый сложный этап, который предполагает назначение многокомпонентных химиотерапевтических схем, чтобы уничтожить как можно больше лейкозных клеток. При этом организм испытывает мощное токсическое действие. С одной стороны, его оказывают химиотерапевтические препараты, а с другой — продукты распада опухолевых клеток. В этот период пациент должен находиться под круглосуточным наблюдением врачей, поэтому требуется госпитализация в стационар.
- Консолидация ремиссии. Индукционная терапия, какой бы мощной она не была, не может полностью уничтожить опухолевые клетки, поскольку часть из них находится в «спящем» состоянии и активируется через некоторое время. Чтобы уничтожить и их, проводится консолидация ремиссии. Для этого могут использоваться те же препараты, что и на первом этапе или другие схемы химиотерапии. Это зависит от вида лейкоза.
- Реиндукция ремиссии. По сути этот этап представляет собой повторение индукционного этапа — интенсивные курсы химиотерапии с высокими дозами цитостатиков. Цель этого этапа уничтожить оставшиеся злокачественные клетки, которые на момент лечения могли находиться в неактивном состоянии. Этот этап длится от нескольких недель до нескольких месяцев.
- Поддерживающая терапия. Это заключительный этап. Его цель — уничтожение оставшихся опухолевых клеток. С этой целью длительное время назначаются низкие дозы цитостатиков, которые уничтожат клетки, оставшиеся после курса лечения. Этот этап проходит амбулаторно, и, если состояние здоровья пациента позволяет, он может работать или получать образование.
В ряде случаев при неблагоприятном прогнозе или возникновении рецидива, обычных курсов химиотерапии бывает недостаточно. В связи с этим, используются дополнительные методы лечения.
Профилактика нейролейкоза — поражение головного и спинного мозга лейкозными клетками. С этой целью в спинномозговой канал вводят цитостатики и проводят лучевую терапию на область головного мозга.
Трансплантация гемопоэтических стволовых клеток. В ряде случае пациентам требуется проведение высокодозной полихимиотерапии. Ее назначают для преодоления опухолевой резистентности, при возникновении многократных рецидивов и др. Такое лечение очень мощное и позволяет уничтожить даже устойчивые опухолевые клетки. Однако такая терапия опустошает костный мозг (фабрику кровяных клеток), и он не может в быстрые сроки полноценно восстановить кроветворение. Чтобы преодолеть это состояние, производят трансплантацию гемопоэтических стволовых клеток. Их могут взять у пациента после этапа индукции или консолидации ремиссии. В этом случает трансплантация называется аутологичной. Если стволовые клетки берутся от донора, это называется аллогенной трансплантацией. В этом случае пациент получает иммунитет другого, здорового человека. Иммунные клетки будут атаковать оставшиеся опухолевые клетки, оказывая дополнительный лечебный эффект. Недостатком аллогенной трансплантации является риск развития реакции трансплантат против хозяина, когда иммунные клетки начинают атаковать организм реципиента, приводя к развитию различных осложнений.
Запись на консультацию круглосуточно
Последствия (ремиссия и рецидив)
Еще несколько десятилетий назад острые лейкозы приводили к смерти пациента в течение 2-3 месяцев после постановки диагноза. На сегодняшний день ситуация кардинально изменилась благодаря появлению новых препаратов для лечения.
На данный момент в клинике острых лейкозов выделяют следующие стадии:
- Первая атака — в этот период происходит активное размножение опухолевых клеток в костном мозге и выход их в кровь. Именно на данном этапе происходит постановка диагноза. Симптомы заболевания будут определяться тем, какой кроветворный росток поражен. Как правило, это упорные инфекции, анемии, общая слабость, увеличение лимфатических узлов и др.
- Период ремиссии. Если острый лейкоз ответил на химиотерапию, опухолевые клетки уничтожаются, и кроветворение восстанавливается. Количество бластов в костном мозге приходит в норму и не превышает 5% от общего количества клеток. Выделяют несколько видов ремиссии, в зависимости от того, насколько полно подавлен опухолевый клон. В настоящее время целью лечения является достижение полной ремиссии в течение 5 лет. По истечении этого срока, пациент считается полностью здоровым.
- Рецидив. У некоторых пациентов возникает рецидив, при котором опять увеличивается количество бластов. Они опять выходят в кровоток и могут образовывать внекостномозговые очаги инфильтрации. Рецидивов может быть несколько, и с каждым разом их все сложнее ввести в ремиссию. Тем не менее, у многих пациентов удается добиться полной пятилетней ремиссии, даже после нескольких рецидивов.
- Терминальная стадия. О ней говорят, когда все используемые методы лечения острых лейкозов теряют свою эффективность и сдерживать опухолевый рост уже невозможно. Происходит полное угнетение кроветворной системы организма.
Паллиативная помощь
Для терапии острого лейкоза имеется большое количество методов лечения. Это может быть химиотерапия, таргетная терапия, иммунотерапия. Все эти методы могут привести к ремиссии даже после многократных рецидивов. Поэтому как таковая, паллиативная терапия назначается редко и, как правило, у возрастных пациентов, которые не могут перенести тяжелое лечение.
В этом случае используется химиотерапия, медикаментозная терапия и лучевая терапия.
Химиотерапия
Химиотерапия при паллиативном лечении проводится не с целью достижения ремиссии, а для удержания опухолевого клона от стремительного размножения. На этом этапе могут применяться стандартные цитостатические препараты в меньших дозировках, иммунотерапия, таргетная терапия и другие методы противоопухолевого лечения.

Лучевая терапия
Лучевая терапия может применяться для облегчения болевого синдрома при сильном поражении костей, а также при наличии внекостномозговых очагов.
Сопроводительная медикаментозная терапия
Устранение болевого синдрома
Для помощи пациентам с болевым синдромом применяют различные обезболивающие препараты, начиная от нестероидных противовоспалительных препаратов (тот же ибупрофен) и заканчивая легкими и/или тяжелыми наркотическими средствами. Уменьшить выраженность болевого синдрома помогает и лучевая терапия.
Профилактика инфекций
На терминальных стадиях у больных серьезно нарушено кроветворение, и, как следствие, нет полноценной защиты от всех видов инфекций — бактериальной, грибковой, вирусной, что может привести к гибели пациента. Инфекционные осложнения являются одной из ведущих причин смерти при терминальных стадиях лейкозов.
Для предотвращения заражения, рекомендуется тщательно соблюдать принципы гигиены — уход за полостью рта, антисептическая обработка рук как самого больного, так и ухаживающего персонала, назначение профилактических антибактериальных и противогрибковых препаратов.
Трансфузионная поддержка
При сильном угнетении кроветворения, развивается тяжелая анемия и тромбоцитопения. Для купирования этих состояний могут применяться трансфузии эритроцитарной и тромбоцитарной массы.
Тромбоцитарные трансфузии
Раньше тромбомассу переливали при снижении количества тромбоцитов ниже 20*109/л. Но потом появились рекомендации, согласно которым тромбоцитарные трансфузии проводят при падении уровня тромбоцитов ниже 10*109/л. При более высоких цифрах назначение тромбомассы не приводит к снижению риска развития кровотечения.
При появлении признаков геморрагического синдрома, тромбоцитарную трансфузию начинают немедленно и при необходимости увеличивают ее объем. Признаки геморрагического синдрома:
- Наличие петехиальных высыпаний, особенно в полости рта и других слизистых.
- Повышение температуры при отсутствии очагов инфекции.
- Наличие кровотечения.
- Возникновение инфекции.
Трансфузии эритроцит-содержащих сред
У терминальных больных желательно поддерживать целевой уровень гемоглобина не ниже 80 г/л. Особое внимание уделяется пациентам с тромбоцитопениями. При развитии тяжелых анемий показано переливание эритромассы до достижения целевого уровня.
В настоящее время во всем мире принят принцип — если больного нельзя вылечить, это не значит, что ему нельзя помочь!
Запись на консультацию круглосуточно
Ремиссия при лейкозе: как добиться?
Раковые заболевания крови всегда протекают достаточно сложно, имеют серьезные последствия и тяжело поддаются лечению. Существует такой период, как ремиссия при лейкозе, которому характерно отсутствие клинической картины и симптоматики заболевания. Считать ремиссию окончанием болезни нельзя, но сам факт ее начала – хороший шанс к выздоровлению.
Лейкоз и его опасность
Лейкоз – это злокачественная болезнь кроветворной системы, которая характеризуется неконтролируемым размножением лейкоцитов и накоплением его незрелых форм в костном мозге и крови. Когда он прогрессирует, у человека развивается огромное количество заболеваний, симптомами которых является высокая кровоточивость, внутренние кровоизлияния, слабая иммунная система и различные осложнения инфекционной природы.
Выделяют такие группы лейкоза:
- Спонтанный – природа появления которого не известна до сегодняшнего дня.
- Лучевой – появившийся вследствие воздействия ионизирующих излучений.
- Лейкоз, причиной появления которого является воздействие каких-либо химических веществ.
- Лейкоз, появляющийся после перенесенных человеком вирусных и инфекционных заболеваний.
Все эти группы принято подразделять на два главных вида заболевания: острый и хронический лейкоз. Различие их в том, что острому лейкозу характерна опухолевая трансформация малодифференцированных или недифференцированных клеток крови, а хроническому – зреющих элементов клеток, при которой сохраняется их специализация.
Острый лейкоз очень быстро развивается, поэтому человеку с таким диагнозом нельзя затягивать с лечением, чтобы заболевание не привело к смерти спустя несколько недель или месяцев. Люди с хроническим лейкозом живут без какой-либо терапии несколько месяцев и даже лет. Опасность в том, что хронические лейкозы могут перерастать в неподвластную терапии острую форму.
Можно ли добиться ремиссии при лейкозе и как это сделать?
Комплексное лечение, которое проводится в наши дни, в основном гарантирует увеличение продолжительности жизни человека, полную или частичную ремиссию.
По данным проведенных исследований, большая часть людей с лейкозом, которые достаточно долго живут с острыми гемобластозами – дети. Предполагают, что поддерживающая терапия убирает лейкозные клетки, которые остались, и, скорее всего, не позволяет стать активными скрытым злокачественным элементам.
Что входит в поддерживающую терапию во время ремиссии лейкоза?
Какую применять поддерживающую терапию во время ремиссии до сих пор очень обсуждаемый и спорный вопрос. У врачей, которые проводят данную терапию во всех странах мира, на сегодняшний момент не существует однозначного мнения. Большинство специалистов в период ремиссии применяют антиметаболиты, блокирующие биосинтез нуклеиновых кислот и приостанавливающие клеточное деление. Другие специалисты считают правильным использование гормональных средств – глюкокортикостероидов.
Практика показывает, что комбинируя разные антилейкемические медикаменты получается достигнуть лучшего результата у больных острым лейкозом намного чаще, чем применяя монохимиотерапию (какой-либо один препарат). Детям предпочтительным способом терапии лейкоза считается использование метотрексата и 6-меркаптопурина.
Когда у пациента началась ремиссия острого лейкоза, поддерживающая терапия на протяжении всего этапа способствует значительному увеличению ее длительности и улучшению уровня его жизни. Были даже случаи, когда больным с острой формой лейкоза удавалось достигать ремиссии до пятнадцати лет. Чем длительнее будет первая ремиссия, тем длительнее будут и повторные.
Стационарная терапия больных лейкозом, прошедших курсовое лечение до начала ремиссии, считается немаловажным этапом, который определяет дальнейшие прогнозы их жизни. При поддерживающей терапии людям рекомендовано ограничивать себя в активной физической деятельности, обеспечивать организму полноценный сон и отдых, употреблять пищу с достаточным содержанием белка, витаминов и ограничить жиры. В ежедневный список продуктов необходимо включить много фруктов, овощей, ягод и зелень.
Сколько длиться ремиссия при лейкозе?
У людей с острым лейкозом в 95% и больше наблюдается полная ремиссия. У 70-80% пациентов болезнь не проявляет себя около 5 лет, поэтому их считают вылечившимися. Когда возникает рецидив заболевания в основном удается добиться еще одной полной ремиссии. Такие пациенты – претенденты на пересадку костного мозга с гарантией длительного периода жизни в 35-65% случаев.
У заболевших острым миелобластным лейкозом, прошедших эффективное лечение с применением разработанных схем химиотерапии в 75% наблюдается полная ремиссия, остальные пациенты умирают (продолжительность ремиссии может длиться до 18 месяцев). Молодым пациентам, достигнув первую полную ремиссию, разрешено делать пересадку костного мозга. У половины таких больных, подвергнувшихся пересадке, наблюдается длительный период ремиссии лейкоза.
Длительность жизни людей с хроническим лейкозом иногда достигает двадцати лет.

Критерии ремиссии острого лейкоза
Существуют такие критерии, по которым проводится оценка эффективности терапии лейкоза, применяемой для достижения ремиссии:
1) Костный мозг:
- Содержание бластных клеток и лимфоцитов в сумме не превышает двадцати процентов.
- Увеличивается количество клеток нормального кровообразования (от 30 процентов) с параллельным снижением количества бластных клеток.
2) Периферическая кровь:
- Отсутствие бластных клеток, показатель гемоглобина более 110 г/л, гранулоциты – больше 1,5*(10*9)/л, тромбоциты – больше 100*(10*9)/л. Данные показатели неизменны в течение месяца.
- Становится лучше периферическая кровь, благодаря снижению количество бластных клеток, гемоглобин от 90 г/л. Показатели не меняются в течение месяца.
3) Физикальные данные:
- Нет признаков лейкозного поражения печени, селезенки, лимфоузлов.
- Размеры органов, пораженных лейкозом, уменьшаются в два раза.
- Без изменений.
4) Клиническая картина:
- Отсутствие симптоматики заболевания.
- Симптоматика присутствует, но при активном спаде.
Факторы, способные спровоцировать рецидив
Рецидив лейкоза – это возвращение всех клинических и гематологических симптомов болезни. Но обострениям заболевания характерны некоторые особенности, в сравнении с первичной стадией лейкоза. Наблюдение за больными позволяет определить приближение рецидива заранее. Когда у пациента наблюдается ремиссия, при скором рецидиве меняется миелограмма и результаты анализа периферической крови. Также, отмечают характерное поражение нервной системы, легких, кожи и косной системы. Далее клиническая картина становится схожей с первичной стадией лейкоза, но все особенности заболевания при этом выражены не так ярко.
Люди, страдающие иммунодефицитом, имеющие наследственные хромосомные патологии и предрасположенность к лейкозу, должны ответственно проходить все профилактические осмотры.
Предрасположенность к острому лейкозу провоцируют ионизирующее излучение и влияние химических веществ, поэтому чтобы избежать рецидива необходимо на сколько это возможно ограничить контакт с этими опасными факторами.
Если человеку поставили диагноз “лейкоз”, своевременно начатое лечение поможет значительно продлить его жизнь и улучшить самочувствие. Также необходимо помнить, что ремиссия при лейкозе не гарантирует полного излечения от болезни, поэтому необходимо проводить поддерживающую терапию и регулярно посещать врача, который сможет предупредить появление рецидива и вовремя оказать необходимую помощь.
Диагностика лейкоза: все основные методы
Лейкоз – онкологический процесс, нарушающий работу кроветворной системы, при котором деформируются и видоизменяются клетки крови. Количество незрелых лимфоцитов беспорядочно увеличивается. Продуцируемые атипичные клетки распространяются по кровотоку и провоцируют рост метастазов в любых органах тела. Накапливаясь в костном мозге, они постепенно заменяют здоровые клетки. Нарушается баланс лейкоцитов, тромбоцитов и эритроцитов. Для выявления диагноза используют комплексный подход. Проблемой занимаются онкогематологи.
Заболевание, при котором нарушен кроветворный процесс, делится на ряд видов. Лейкозы возникают из определённых клеток и формируют новообразования.
- Лимфобластная лейкемия протекает в острой форме. Кровь наполняют повреждённые лейкоциты. Рак лимфобластного типа чаще встречается у детей младшего возраста. Главный симптом заболевания – частые инфекционные болезни с высыпаниями на кожных покровах. При этом ребёнок вялый, отказывается от еды, возникают частые кровотечения, образуются кровоподтеки на теле. При подтверждении диагноза начинается незамедлительное лечение, способное побороть злокачественный процесс.
- Лимфобластный лейкоз имеет хронический характер. Развивается медленно, без ярко выраженных симптомов. Обычно диагностируется у взрослых старше 60 лет. Преимущественно у представителей сильного пола.
- При лейкозе миелобластного типа наблюдается острое течение болезни. Незрелые миелоидные клетки обнаруживаются в крови и костном мозге. Болезнь поражает взрослое население. Характерны симптомы инфекционных заболеваний разного генеза.
- Миелолейкоз выступает в качестве подтверждения диагноза. Хроническая патология медленно развивается и обычно обнаруживается при диагностике других заболеваний.
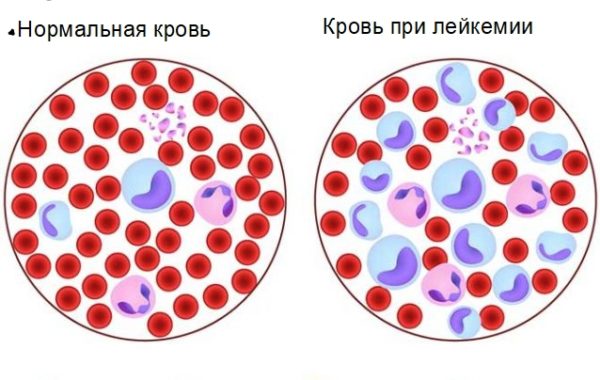

Хроническую стадию разделяют на 2 вида:
- Доброкачественный лейкоз диагностируется при наличии одного клона атипичной клетки.
- Для злокачественной формы характерно наличие вторичных клонов. Болезнь стремительно развивается с бесконтрольным делением бластов.
Причины возникновения болезни
Главная причина – аномальные процессы в кроветворящих органах, в частности в костном мозге. Развиваются на фоне аутоиммунных заболеваний, генетических нарушений на стадии формирования плода и под действием различных внешних факторов:
- Плохая экологическая обстановка;
- Вредные привычки;
- Вирусные поражения организма;
- Контакт с радиационным и ультрафиолетовым излучением.
Группа риска состоит из пожилых людей, больных с иммунодефицитом и хроническими воспалительными процессами в организме.
Методы лабораторной диагностики
Лейкемия признана опасным злокачественным заболеванием, требующим особого лечения. Из-за отсутствия ярких симптомов на первых стадиях болезни люди путают лейкозы с доброкачественными процессами. К примеру, частые простудные заболевания начинают пугать больного только после длительного времени развития болезни, усиления симптомов и при отсутствии положительной реакции на терапевтическое лечение. Если терапевт отмечает нарушения, свойственные болезням костного мозга, пациент направляется на консультацию и дальнейшее лечение к онкологу.


Лабораторные исследования назначают в начале определения проблемы. При результатах, отклоненных от нормы, наблюдается увеличение несозревших клеток. Их количество превышает 30%, эритроцитарные ростки занимают больше 50%. В костном мозге отмечаются атипичные промиелоциты.
Для диагностики уровня лейкоцитов, эритроцитов и тромбоцитов исследуют клинический анализ крови. Повышенный уровень лейкоцитов и снижение количества других клеток позволяют распознать рак на ранней стадии. При исследовании периферической крови обнаруживается нейтро- и тромбоцитопения, лимфоцитоз, азурофильные гранулы, нормохромная анемия и зрелые бласты с отсутствующим промежуточным созреванием.
- Для лейкоза характерно значительное снижение уровня гемоглобина. При этом больной исключает менструальные, обильные носовые кровотечения, потерю крови при хирургическом вмешательстве в ближайшее время. При онкологии гемоглобин падает в 2 раза. Показатель снижается при острой форме болезни.
- Отмечается снижение ретикулоцитов.
- Лимфоцитарная формула представлена серьёзными нарушениями. В зависимости от стадии рака, уровень лимфоцитов снижается и повышается.
- Врачи обращают внимание на скорость оседания эритроцитов (СОЭ). При онкологии она значительно увеличена.
- В формуле крови отсутствуют базофилы и эозинофилы.
- Если в крови отсутствуют переходные клетки, а формула представлена только большим количеством молодых и малым количеством зрелых форм, обнаруживается лейкемический провал.


Лейкоциты в крови человека
Совокупность нескольких признаков требует консультации гематолога. Если изменён один показатель в формуле крови, развитие онкологического процесса сводится к нулю.
Биохимия крови выявляет состояние и работоспособность внутренних органов под влиянием онкологического процесса.
При подозрении на лейкоз острой или хронической формы диагностика расширяется:
- Важно диагностировать степень злокачественности рака. Дифференциальная особенность клетки говорит о её природе и агрессивности. Эти особенности можно выявить с помощью гистологического исследования биоматериала.
- Костный мозг подвергается пункции с помощью иглы, введенной в полость кости. Обычно для биопсии выбирается грудная клетка. Исследование показывает наличие острого или хронического процесса. По анализу можно определить цитогенетический и морфологический вид болезни. С помощью данной процедуры выполняется проверка реакции пораженной клетки на химиопрепарат.
- Миеломограмма обнаруживает соотношение атипичных клеток с нормальными. Обследование показывает степень пораженности организма. У здорового человека бластные клетки не должны превышать 5%. Исследуемый материал представлен образцом костного мозга. Во время процедуры обнаруживаются лимфоцитоз и природа атипичных клеток. Отсутствуют мегакариоциты. Этот способ признан наиболее точным для постановки диагноза.
- Цитохимическая лабораторная диагностика основана на определении специфических ферментов. Метод незаменим при определении острых форм заболевания и прогнозировании их течения.
- Для диагностики острого лимфо- и миелобластного лейкоза проводят иммунофенотипирование. Тактика лечения этих видов лейкоза различна, поэтому важно уточнить диагноз.
- Необходимо исследовать ликвор (спинномозговую жидкость) для выявления повышенного количества клеток (цитоза).

Забор спинномозговой жидкости
Инструментальные исследования
Диагностика лейкоза включает ряд инструментальных методов. Они не уступают по информативности лабораторным. Чтобы провериться на рак крови, пациент проходит следующие исследования:
- При помощи компьютерной томографии выявляются повреждения сосудов и метастазы в лимфатических узлах. Метод используется для масштабной диагностики организма путём послойного сканирования.
- Рентгенография грудной клетки назначается при характерных симптомах повреждения лёгких: регулярном кашле, отделении мокроты с включениями крови, боли в груди.
- Если онкологический процесс поразил головной мозг, рекомендовано проведение магнитно-резонансной томографии. Для болезни характерны симптомы: ухудшение зрения, онемение конечностей, нарушения памяти и сознания, головокружения и обмороки.
- Для выявления отклонений в работе сердечной мышцы проводят электрокардиограмму и эхокардиограмму.
- Диф диагностика основана на исключении возможных патологий с такими же симптомами, как при лейкозе. Исследование проводится с помощью компьютерных программ. Лейкемия схожа по симптоматике со следующими заболеваниями:


- Мононуклеоз инфекционного генеза провоцирует увеличение селезёнки. Увеличивается температура тела. В крови присутствуют недоразвитые лимфоциты. Эти же показатели встречаются при ангине и желтухе.
- ВИЧ не является онкологической болезнью, но тоже снижает иммунитет до 0. Человек страдает от частых инфекционных заболеваний. Наблюдается лимфаденопатия. Специальный анализ крови исключает вариант развития рака.
- При поражении человека токсичными веществами развивается апластическая анемия. Клетки костного мозга заменяются жировой тканью. Развивается панцитопения.
- Снижение количества всех клеток крови происходит после операций на органах желудочно-кишечного тракта.
Современные методы исследования распознают рак на каждом этапе развития. Для благоприятного исхода необходимо обращаться за медицинской помощью при любых нарушениях здоровья. Система кроветворения выполняет жизненно важную функцию, позволяющую людям противостоять болезнетворным бактериям.
Результаты исследований предоставляют возможность подобрать индивидуальное эффективное лечение. Обычно с раком крови борется химиотерапия. Для определённой разновидности лейкоза онкологи используют различные медикаменты.
При отдельных патологических процессах применяют трансплантацию костного мозга. Кроветворный процесс перезапускается, и пациент входит в стойкую ремиссию.
